Область техники, к которой относится изобретение
Изобретение относится к фармацевтическим препаратам, а именно к новым со-кристаллам Теофиллина с Меглюмином или Трометамином, пригодными для фармацевтических препаратов.
Уровень техники
Теофиллин, как и Меглюмин с Трометамином являются действенными лекарственными веществами-субстанциями. Теофиллин в разных формах применяется медицине при застойных явлениях, как диуретические и кардиатонические средства, а также для улучшения мозгового кровообращения [1, 2].

Меглюмин способствует утилизации глюкозы и жирных кислот клетками, активирует ферментативные процессы цикла Кребса, нормализует газовый состав крови и кислотно-основное состояние. Восстанавливает энергетический потенциал клеток и снижает образование свободных радикалов. Оказывает положительный эффект на аэробные процессы в клетке. После внутривенного введения быстро утилизируется и не куммулирует в организме. По фармакологической классификации относится к дезинтоксикационным, антиоксидантным, антигипоксическим веществам.
Трометамин (Трисамин) [3] - 2-Амино-2-(гидроксиметил)-1,3-пропандиол, номер химического соединения в реестре информационной службы “Реферативного химического журнала” США (CAS) - 77-86-1, фармакологическая группа - 11.6.1, применяется в качестве средства для внутривенного введения в 3,66% растворах с целью коррекции кислотно-щелочного состава (КЩС) крови при ацидозах различной этиологии [8, 9]. Также, как и меглюмин обладает выраженными свойствами обычно характерными для органических аминов.
Основным препаратом для лечения бронхоспазматического синдрома является «Эуфиллин», международное название «Аминофиллин» [3], основным фармакологически действующим веществом которого является Теофиллин [1]. Последний используется также и как самостоятельный API в форме порошков для приема внутрь и в форме ректальных свечей. Чаще Теофиллин применяется в составе сложных лекарственных композиций в таблетках (Тео-Астхалин, Теофедрин-Н) и в составе пролонгированных форм (Теопэк, Теобиолонг, Теодур и др.) [4].
Основным недостатком субстанции «Теофиллина», ограничивающим её применение для купирования приступов бронхиальной астмы и ангиоспазмов, является её низкая природная растворимость в воде (1:180 при 20°С) и невозможность вследствие этого применять его в ингаляционных и, особенно, в инъекционных формах.
«Эуфиллин» (Аминофиллин*) - это водорастворимая форма теофиллина, содержащая в качестве растворяющей добавки этилендиамин [4] в количестве от 13,5 до 15,0% по массе кроме основного действующего вещества - теофиллина. Эуфиллин применяется в форме таблеток, но чаще - в растворах для инъекций, в том числе для внутривенных инфузий, а также в лекарственных формах для ингаляций.
К основным недостаткам водорастворимой формы теофиллина - субстанции «Аминофиллин» можно отнести следующие:
1. Небольшая широта терапевтического действия. Так называемый терапевтический индекс или «терапевтическое окно» слишком узкие, из-за чего вероятность возникновения нежелательных побочных эффектов слишком высокая, что и подтверждается, в том числе и печальной статистикой его использования. Последнее, скорее всего, связано с присутствием в составе эуфиллина водорастворяющей добавки - этилендиамина.
Этилендиамин (1,2-диаминоэтана) широко используется в органическом синтезе, в текстильной промышленности для обработки тканей, а также в качестве отвердителей эпоксидных смол [5]. По параметрам токсикометрии промышленных ядов этилендиамин отнесен к третьему классу опасности. Обладает раздражающим, гепатотоксическим и нефротоксическим действием, как и большинство аминов, угнетает кроветворение. ПДК воздуха рабочей зоны оценивается величиной 2 мг/м3, a DL50 (крыса) - 300 мг на 1 кг веса животного [6, 7].
2. Нестабильность Аминофиллина. Этилендиамин, как один из исходных составляющих вещества-субстанции «Аминофиллин», благодаря своим основным свойствам образует водорастворимый солеподобный комплекс с теофиллином, который в свою очередь представляет собой очень слабую органическую кислоту (рКа 8,8). В силу общеизвестных химических закономерностей образующаяся субстанция «Аминофиллин» характеризуется повышенной нестабильностью к гидролизу как в отношении влаги воздуха, так и, особенно, в растворах. Ситуация усугубляется летучестью этилендиамина. В конечном счете все это приводит к снижению качества-субстанции «Аминофиллин» по параметру «растворимость». При производстве и хранении в контакте с открытым воздухом субстанция «Аминофиллин» по указанным выше причинам также активно вступает в химическую реакцию с углекислотой воздуха (pKa-1 6,35), вследствие чего качество такой субстанции по параметру «растворимость» также может заметно ухудшиться, что создает проблемы при приготовлении инъекционных растворов на основе «Аминофиллина» как исходного вещества. Кроме этого, как и большинство аминов и особенно диаминов, этилендиамин подвержен окислительному воздействию кислорода воздуха, активизируемому влиянием света, особенно его ультрафиолетовой частью, что негативно сказывается на качестве конечного продукта «Аминофиллин» и требует соответствующей защиты его при хранении и использовании.
3. Неудовлетворительная технологичность производства. По своему агрегатному состоянию при нормальных условиях этилендиамин представляет собой маслообразную едкую летучую жидкость. При производстве препарата «Аминофиллин» для инъекций в качестве исходного сырьевого продукта требуется свежеперегнанный этилендиамин, срок годности которого ограничивается 7 сутками [4], что создает значительные неудобства. Кроме этого, определенные технологические (взрыво- и пожароопасность), а также санитарно-гигиенические проблемы возникают, когда в производстве приходится иметь дело с летучими едкими жидкими компонентами, как, например, в случае производства субстанции «Аминофиллин» - этилендиамином, вызывающим повышенную коррозию оборудования, порчу спецодежды, раздражение органов дыхания, слизистых и кожных покровов персонала.
4. Несмотря на то, что (Аминофиллин) квалифицируется как индивидуальное вещество-субстанция, на самом деле - это композитный продукт непостоянного состава, из-за чего в некотором смысле затруднены процедуры стандартизации данного объекта, перманентно изменяющим свой состав по мере его хранения и использования вследствие летучести одного из составляющих компонентов.
Известна со-кристаллическая форма теофиллина с дифлунисалом или диклофенаком (патент на изобретение РФ №2542100) которая, как указывается, имеет преимущества в улучшенной растворимости в сравнении с такими же характеристиками, известными для исходных составляющих Дифлунисала и Диклофенака в 1,5 и 1,6 раза соответственно. Что касается растворимости Теофиллина, то на этот счет в документе ничего не говорится, но если принять указанные выше величины в качестве прибавки растворимости и для Теофиллина (что логично), то это совсем недостаточно, чтобы решать терапевтические задачи, связанные с купированием ангиоспазмов или бронхоспазмов.
Известна «Усовершенствованная водорастворимая форма Теофиллина» (патент на изобретение РФ № 2240797). Данный вариант принимается за прототип.
Основным недостатком указанного предложения (пат. РФ № 2240797) является то, что оно сформулировано не в качестве нового индивидуального вещества с четко определенными идентификационными признаками, что упрощало бы формулирование для данного объекта спецификации и облегчало бы саму процедуру стандартизации его, а представлено в форме алгоритма его получения, что менее предпочтительно в отличие, например, от предлагаемых новых со-кристаллов в настоящей заявке.
Растворимость прототипа и одного из заявляемых нами новых со-кристаллов, например, со-кристалла Теофиллина с Меглюмином, определены нами в сравнительном варианте прямыми измерениями в соответствии с методикой общей фармакопейной статьи «Растворимость» ГФ XIV.ОФС.1.2.1000.15 в части «определение растворимости для веществ с неизвестной растворимостью». По результатам этого эксперимента новый со-кристалл Меглюмина с Теофиллином отнесен нами к категории «легко растворим в воде». Это означает, что для растворения 1 г этого вещества требуется от 1 до 10 мл воды при 20°С, в то время как объект, принятый нами за прототип по такой же методике может быть отнесен только к категории «растворим», то есть растворимость прототипа более чем на порядок ниже растворимости предлагаемого нового со-кристалла Теофиллина с Меглюмином.
Важными критериями эффективности препарата являются фармакокинетические показатели и физико-химические свойства различных структурных модификаций таких, например, как аморфная форма, соль, со-кристалл, полиморфные модификации. Они имеют различные физические и химические свойства, что сказывается на фармацевтических параметрах активного вещества, таких как стабильность при хранении, сжимаемость и другие. Определяющими факторами биодоступности являются растворимость и кинетические показатели растворения. Низкая растворимость лекарственного соединения в биологических жидкостях часто приводит к низкой эффективности лекарственного препарата. Поэтому увеличение уровня растворимости и скорости растворения препарата является актуальной технической задачей.
Известно большое количество способов повышающих растворимость веществ, применяемых в фармацевтическом производстве: возможно тонкое измельчение, которое значительно увеличивает площадь поверхности растворяемого соединения [Chaumeil J. С. Micronisation: a method of improving the Bioavailability of poorly soluble drugs // Methods Find. Exp. Clin. Pharmcol. - 1998 - 20(3) - P. 211-215]. В некоторых случаях приемлемо использование солей с улучшенной растворимостью [Agharkar S., Lindenbaum S., Higuchi T. Enhancement of solubility of drug salts by hydrophilic counter-ions: properties of organic salts of an anti-malarial drug // J. Pharm. Sci. - 1976-65(5) - P.747-749]; Также известен способ растворения лекарственных соединений в сложных и мицеллярных растворителях [Amin K., Dannenfelser R.-M., Zielinski J., Wang B. Lyophilization of polyethylene glycol mixtures // J. Pharm. Sci. - 2004 - 93(9) - P. 2244-2249], [Torchillin V.Р. Micellar nanocarriers: pharmaceutical perspectives // Pharm. Res. - 2007 - 24(1) - P. 1-16].
Однако у всех приведенных выше способов есть определенные недостатки. Тонкое измельчение вещества не увеличивает равновесную растворимость из-за возрастания Ван-дер-ваальсовых взаимодействий и электростатического притяжения между мелкими частицами.
Обычно в фармацевтике используются в основном слабо ионизированные и нейтральные молекулы, а соли, несмотря на их в большинстве случаев хорошую растворимость обладают, как правило, плохой биодоступностью, так как для трансмембранного их переноса требуются специальные механизмы. Наглядным примером в этом отношении может быть морская вода, компоненты которой, как известно, являются хорошо растворимыми солями. При заглатывании даже ощутимых количеств такой воды самое большое, что может быть в этой связи - это бурные события, которые будут происходить в просвете желудка и кишечника, могущие вызвать рвоту или диарею. Что же касается просвета кровеносных сосудов, то ионно-солевой баланс здесь практически не изменится, несмотря на довольно бурные события в просвете кишечника.
Использование сложных и мицеллярных растворителей предполагает приемлемую растворимость и совместимость молекул лекарственного соединения с растворителем, что не всегда достижимо.
Известно также, что повысить растворимость можно путем получения со-кристальной формы activity pharmaceutical ingredient (API) с компонентом, способствующим увеличению растворения. Со-кристаллы - это супрамолекулярные системы, где одним из составляющих является плохо растворимый, чаще всего это молекула лекарственного соединения (API), а вторым компонентом (ко-формером) выступает молекула хорошо растворимого соединения.
Раскрытие изобретения
Задачей предлагаемого изобретения является получение со-кристаллических форм Теофиллина с Меглюмином или Трометамином, характеризующимися высоким уровнем растворимости. Указанное свидетельствует о пригодности предлагаемых со-кристальных форм Теофиллина с Меглюмином или Трометамином для использования в фармацевтической промышленности.
Это достигается получением со-кристаллических форм Теофиллина с Меглюмином, Теофиллина с Трометамином, где молярное соотношение со-кристаллических систем в обоих случаях составляет 1:1, имеющих свойства, приведенные в таб. 1.
Осуществление изобретения
Заявленное изобретение позволяет получить преимущество, заключающееся в повышении растворимости Теофиллина, который в индивидуальном состоянии относится по этому показателю к ограничено растворимым в воде веществам (1:180 при 20°С), в то время как заявленные со-кристаллы Теофиллина с Меглюмином, а также Теофиллина с Трометамином относятся к категории хорошо растворимых в воде веществ, то есть при 20° в одном миллилитре воды можно растворить от 100 до 1000 мг, что в 10 раз выше, чем прототип и, что примерно в 50 раз более растворим по сравнению с показателями растворимости Теофиллина в чистом виде. Сравнивая по этому показателю с Эуфиллином заявляемые со-кристаллы более чем в 10 раза лучше растворимы. Кроме этого, использование заявляемых со-кристаллов в качестве средств купирования ангио и бронх спазмов позволит избежать опасных для жизни побочных явлений, характерных для Аминофиллина, которые, скорее всего, связаны с водорастворяющей добавкой - этилендиамином, входящего в его состав.
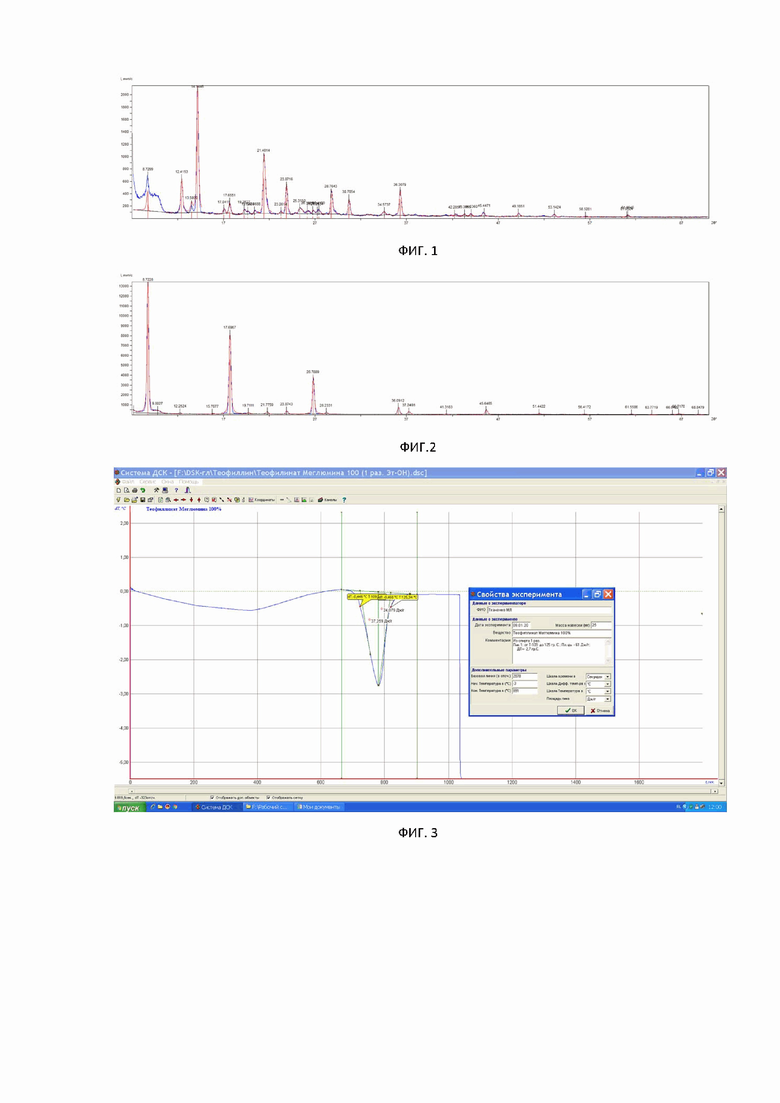
Фиг. 1. Типичный профиль XPRD со-кристаллов Теофиллина с Меглюмином.
Фиг. 2. Типичный профиль XPRD со-кристалла Теофиллина с Трометамином.
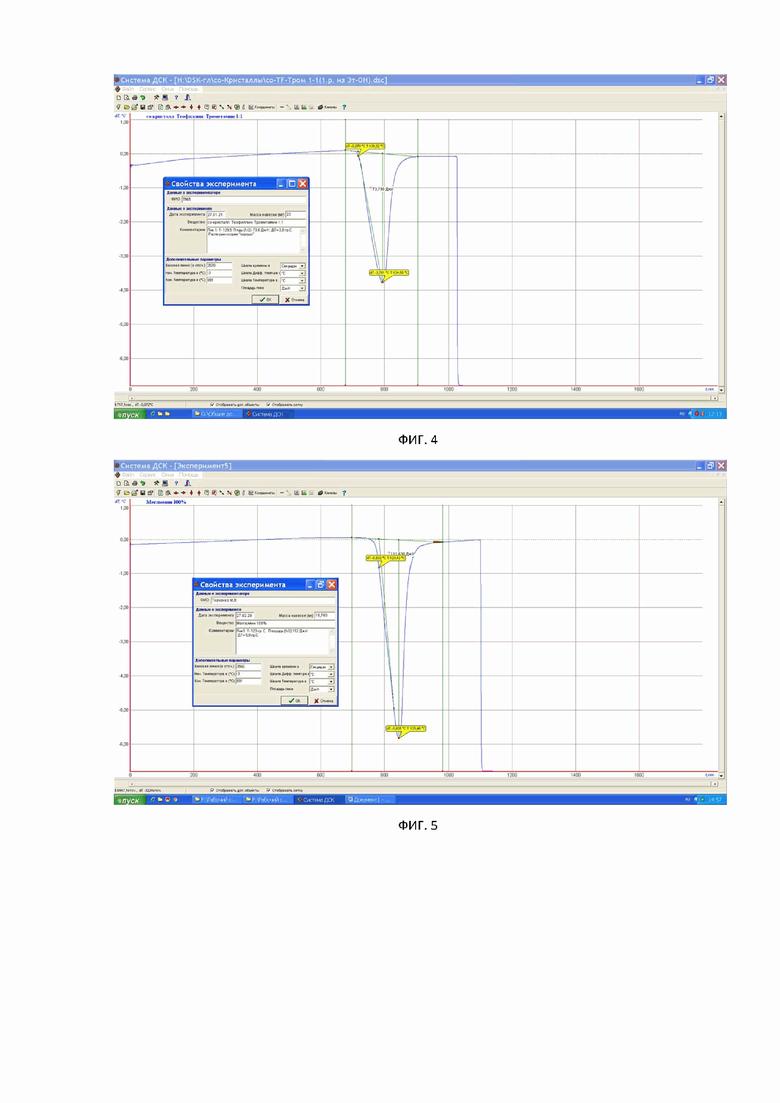
Фиг. 3. ДСК-термограмма со-кристаллической формы Теофиллина с Меглюмином.
Фиг. 4. ДСК-термограмма со-кристаллической формы Теофиллина с Трометамином.
Фиг. 5. ДСК-термограмма Меглюмина в чистом виде.
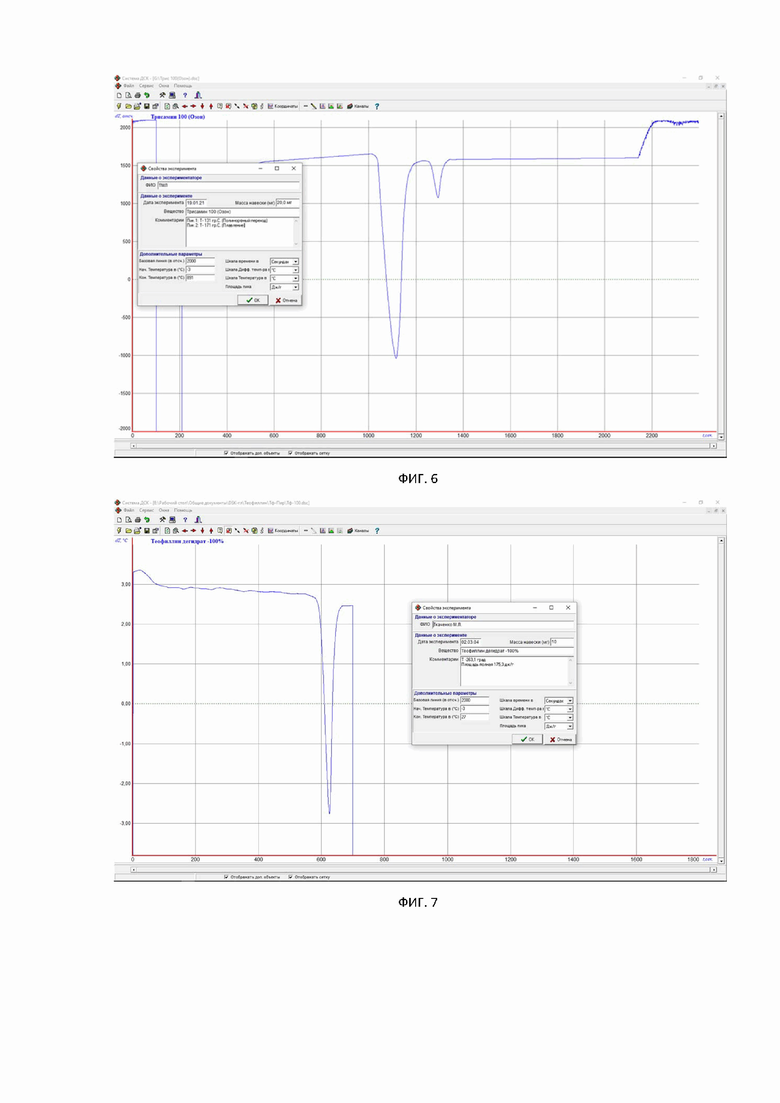
Фиг. 6. ДСК-термограмма Трометамина в чистом виде.
Фиг. 7. ДСК-термограмма Теофиллина дегидрата в чистом виде.
Заявленные новые со-кристаллы Теофиллина - твердые кристаллические стабильные индивидуальные вещества мелко игольчатой структуры в виде белого цвета порошка, не распадаются, не подвержены воздействию влаги и удобные для приготовления стабильных фармацевтических препаратов. Заявленные со-кристаллы Теофиллина могут быть использованы для производства жидких лекарственных форм для парентерального в том числе подкожного, внутримышечного и в растворах для ингаляционного использования.
Структура заявленных со-кристаллов доказана двумя методами, в совокупности достаточными для утверждения о полученных новых соединениях:
- дифракция в рентгеновских лучах поликристалла (XPRD)
- дифференциальная сканирующая калориметрия (DSC).
рентгеновского излучения на порошке
C7H8N4O2*C7H17NO5
Mr 180.16 +195.2= 375,4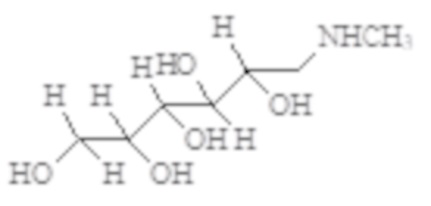
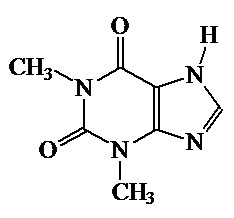 *
*
Белый кристаллический порошок, хорошо растворим в воде, умеренно в спирте.
Из этанола
C7H8N4O2* C4H11NO3
Mr 180,16+121.13=301,3 *
*
На фиг. 1 и 2 представлены типичные профили XPRD со-кристаллов Теофиллина с Меглюмином, Теофиллина с Трометамином в соответствии с предлагаемым изобретением.
На фиг. 3, 4, 5, 6, 7 представлены типичные термограммы DSC Теофиллина с Меглюмином, Теофиллина с Трометамином, Меглюмина Трометамина и Теофиллина дегидрата в чистом виде соответственно.
Сведения, подтверждающие возможность воспроизведения изобретения
Для получения заявляемых со-кристаллов использовали следующие вещества: Теофиллин - фирма производитель Шандонг Ксинхуа Фармасьютикал Ко. Лтд CAS 58-55-9 и CAS-83-67-0 соответственно, чистота 99%.
Меглюмин. Код CAS 6284-40-8. Оригинальное название продукта: Meglumine, low in endotoxins suitable for use as active pharmaceutical ingredient EMPROVE® api Ph Eur, JP, USP. Фирма производитель Molekula Limited Darnington, United Kingdom, чистота> 99%.
Трометамин (Tris). Код CAS-77-86-1. Оригинальное название продукта: suitable for use asexipient EMPROVE® exp Ph Eur, BP, JPC, USP Фирма производитель - Merck KGaA, чистота 99,9%.
Спирт метиловый ГОСТ 6995-77 «МЕТАНОЛ ХЧ» марка АКВА М - 012011 Производство реагентов Карла Фишера.
Новые со-кристаллы Теофиллина с Меглюмином или с Трометамином в существенной степени характеризуется результатами рентгеноструктурного анализа, показанными на фиг. 1, 2, а также в существенной степени описывается данными термограммы DSC, представленными на фиг. 3, 4.
Дополнительными преимуществами предлагаемых со-кристаллов являются принадлежность обоих составляющих в каждой из предлагаемых со-кристальных форм Теофиллина с Меглюмином (1:1), Теофиллина с Трометамином (1:1) к препаратам, использующимися в медицинской практике. Все в качестве действенных лекарственных средств. Меглюмин и Трометамин - хорошо растворимые в воде вещества. Теофиллин - ограниченно растворим (1:180 при 20°С). Предлагаемые со-кристальные формы Теофиллина с Меглюмином или Трометамином привлекательны тем, что будет представлять в себе принцип «два в одном», так сказать «drag and drag co-crystalline», обладающими только им присущими свойствами, отсутствующими у исходных веществ, такими как значительно улучшенная растворимость в пересчете на Теофиллин (до 1 г в 3,5 мл при 20°С), что более чем в 50 раз превышает растворимость теофиллина в чистом виде и в 10 раз выше растворимости прототипа, улучшенная биодоступность, термическая стабильность, улучшенные механические свойства и др.
Получить заявляемые со-кристаллы можно используя метод механохимической активации, что подтверждается приведенным примером.
Смесь 3,060 г (0,02 моль) Теофиллина с 3,904 г Меглюмина (0,02 моль) или 2,422 г Трометамина (0,02 моль) помещают в планетарную фарфоровую шаровую мельницу с рабочим объёмом 2000 см3. Туда же помещают 45 фарфоровых шаров диаметром 20 мм и 50 мл метанола. Запускают процесс механохимической активации по 1 часу с перерывом 5 минут. Полученную суспензию с помощью пластикового совка вместе с шарами осторожно перемещают на сетчатую воронку. Далее смывают метанольную суспензию с шаров и с внутренней рабочей поверхности шаровой мельницы небольшими порциями метанола. Объединённые смывы переносят в сосуд, в котором далее проводят процедуру очистки целевых продуктов перекристаллизацией из метанола с 5 г активированного угля, руководствуясь правилами общей лабораторной практики. Нагретый до кипения метанольный раствор (суспензию) фильтруют через бумажный фильтр, используя воронку Бюхнера под небольшим разряжением (водоструйный насос) в колбу Бунзена. Прозрачный горячий раствор из колбы Бунзена переносят в стеклянный стакан, который оставляют в пространстве вытяжного шкафа для кристаллизации целевых продуктов. При стоянии при комнатной температуре в пространстве вытяжного шкафа из горячего прозрачного бесцветного метанольного раствора по мере его остывания и естественного частичного испарения выпадает осадок в форме крупных игл соответствующего со-кристалла Теофиллина с Меглюмином или Трометамином, что подтверждено данными DSC, данными XPRD. Полученный профиль XPRD конечных продуктов в существенной степени соответствует тому, что показан на Фиг. 1, 2. Полученная термограмма DSC конечных продуктов в существенной степени соответствует тому, что показана на Фиг. 3,4.
Литература
1. Государственная фармакопея 14-е изд., том III., ФС.2.1.0053.18. сс. 4859-4862.
2. Государственная фармакопея 14-е изд., том III., ФС.2.1.0184.18, сс. 4863-4866.
3. Регистр лекарственных средств России. (Машковский изд. 15, сс. 686 (?)
4. Государственная фармакопея 14-е изд., том III., ФС 2.1.0053.18. сс. 3296-3300.
4. “Этилендиамин”. - ФС 42-3035-94.
5. Краткая химическая энциклопедия. - М., Т. 5, 1967, с. 1034-1035.
6. Измеров Н.Ф., Саноцкий И.В., Сидоров К.К. - Параметры токсикометрии промышленных ядов при однократном введении (справочник). - М.: Медицина, 1977, с. 190.
7. Троп Ф.С., Белобрагина С.В., Клюшина Л.В. и др. - В кн.: Промышленная токсикология и клиника профессиональных заболеваний химической этиологии. М.: Медицина, 1962, с. 78-79.
9. Регистр лекарственных средств России. - Вып. 9, М., ООО “РЛС-2002”, 2002, с. 862.
| название | год | авторы | номер документа |
|---|---|---|---|
| СО-КРИСТАЛЛИЧЕСКИЕ ФОРМЫ ТЕОБРОМИНА | 2022 |
|
RU2805751C2 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА ТЕОФИЛЛИНА С ДИФЛУНИСАЛОМ ИЛИ ДИКЛОФЕНАКОМ | 2013 |
|
RU2542100C1 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА НИФЛУМОВОЙ КИСЛОТЫ С ИЗОНИКОТИНАМИДОМ ИЛИ КОФЕИНОМ | 2013 |
|
RU2536484C1 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА 2-ГИДРОКСИБЕНЗАМИДА С САЛИЦИЛОВОЙ КИСЛОТОЙ | 2013 |
|
RU2539350C1 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА 2-ГИДРОКСИБЕНЗАМИДА С 4-АМИНОБЕНЗОЙНОЙ КИСЛОТОЙ | 2012 |
|
RU2497804C1 |
| УСОВЕРШЕНСТВОВАННАЯ ВОДОРАСТВОРИМАЯ ФОРМА ТЕОФИЛЛИНА | 2003 |
|
RU2240797C1 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА БИКАЛУТАМИДА | 2012 |
|
RU2510392C1 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА ФЕНБУФЕНА | 2012 |
|
RU2521572C1 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА ДИФЛУНИСАЛА | 2016 |
|
RU2617849C1 |
| КРИСТАЛЛЫ АЛКИНИЛСОДЕРЖАЩЕГО СОЕДИНЕНИЯ, ЕГО СОЛИ И СОЛЬВАТА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПУТИ ПРИМЕНЕНИЯ | 2021 |
|
RU2829609C1 |
Изобретение относится к способу получения со-кристаллических форм теофиллина с меглюмином и теофиллина с трометамином, где молярное соотношение в обоих случаях составляет 1:1, имеющих пики при 2θ (°) 8.6242, 9.5762, 12.1283, 15.6695, 16.9912, 17.6101, 19.1877, 19.6151, 21.6372, 23.7941, 24.7405, 25.8296, 26.7299, 8.1627, 29.0237, 33.1000, 34.2944 и пики при 2θ (°) 12.4715, 13.9308, 14.1418, 14.2572, 18.0419, 19.8859, 20.0612, 21.4605, 22.3185, 23.9172, 25.1470, 25.3925, 28.7318 по данным измерения дифракции рентгеновского излучения поликристалла соответственно, методом механохимической активации. Смесь теофиллина с меглюмином или теофиллина с трометамином помещают в планетарную фарфоровую шаровую мельницу и подвергают механическому воздействию в присутствии метанола, затем проводят очистку целевых продуктов перекристаллизацией из метанола путем адсорбции примесей активированным углём, горячего фильтрования и охлаждения полученного раствора. Технический результат – получение сокристаллических форм теофиллина с меглюмином или трометамином, характеризующихся высоким уровнем растворимости. 7 ил., 1 табл.
Способ получения со-кристаллических форм теофиллина с меглюмином и теофиллина с трометамином, где молярное соотношение в обоих случаях составляет 1:1, имеющих пики при 2θ (°) 8.6242, 9.5762, 12.1283, 15.6695, 16.9912, 17.6101, 19.1877, 19.6151, 21.6372, 23.7941, 24.7405, 25.8296, 26.7299, 8.1627, 29.0237, 33.1000, 34.2944 и пики при 2θ (°) 12.4715, 13.9308, 14.1418, 14.2572, 18.0419, 19.8859, 20.0612, 21.4605, 22.3185, 23.9172, 25.1470, 25.3925, 28.7318 по данным измерения дифракции рентгеновского излучения поликристалла соответственно, методом механохимической активации, заключающийся в том, что смесь теофиллина с меглюмином или теофиллина с трометамином помещают в планетарную фарфоровую шаровую мельницу и подвергают механическому воздействию в присутствии метанола, затем проводят очистку целевых продуктов перекристаллизацией из метанола путем адсорбции примесей активированным углём, горячего фильтрования и охлаждения полученного раствора.
| УСОВЕРШЕНСТВОВАННАЯ ВОДОРАСТВОРИМАЯ ФОРМА ТЕОФИЛЛИНА | 2003 |
|
RU2240797C1 |
| Энциклопедия лекарств, 2008 (16), Ежегодный сборник, Москва, "РЛС-2008", 2007, стр.584 | |||
| Richard J.Bastin et al.: "Salt selection and Optimisation Procedures for Pharmaceutical New Chemical Entities", ORGANIC PROCESS RESEARCH & DEVELOPMENT, 2000, vol.4, p.427-435 | |||
| ПИПЕРАЗИНОВЫЕ ПРОЛЕКАРСТВА И ЗАМЕЩЕННЫЕ ПИПЕРИДИНОВЫЕ ПРОТИВОВИРУСНЫЕ АГЕНТЫ | 2005 |
|
RU2374256C2 |
| Ranjit Thakuria et al.: " | |||
Авторы
Даты
2023-10-23—Публикация
2022-03-01—Подача