Изобретение относится к фармацевтическим препаратам, а именно к новому сокристаллу бикалутамида, пригодному для фармацевтических препаратов.
Уровень техники
N-[4-циано-3-(трифторметил)фенил]-3-[(4-фторфенил)сульфонил]-2-гидрокси-2-метилпропанамид, именуемый также бикалутамидом,
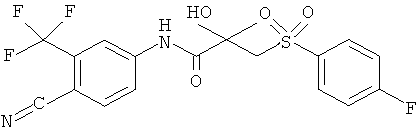
является известным фармацевтическим ингредиентом (API), использующимся в качестве нестероидного анти-андрогенного препарата при лечении рака предстательной железы [Furr B.J. The development of Casodex (bicalutamide): preclinical studies // Eur. Urol. - 1996 - 29(2) - P.83-95; Furr B.J., Tucker H. The preclinical development of bicalutamide: pharmacodynamics and mechanism of action // Urology - 1996 - 47(1 A) - P. 13-25; Waller A.S., Sharrard R.M., Berthon P., Maitland N.J. Androgen receptor localisation and turnover in human prostate epithelium treated with the antiandrogen, casodex // J. Mol. Endocrinol. - 2000 - 24 (3) - Р.339-351].
Бикалутамид (Casodex®) является антагонистом андрогенов, который блокирует действие этих гормонов, а именно тестостерона, в организме, препятствуя его связыванию с клеточными рецепторами. В определенных тканях андрогены контролируют рост и деление как нормальных, так и раковых клеток. Бикалутамид используется в лечении тестостеронзависимого рака простаты. За счет блокады рост-стимулирующей активности тестостерона в раковых клетках лечение бикалутамидом может вызывать уменьшение размера опухоли или задержку ее роста.
Бикалутамид применяют для лечения метастазирующего рака простаты в сочетании с другими препаратами - аналогами рилизинг-фактора лютеинизирующего гормона (LHRH), такими как гозерелин и леупролид.
Бикалутамид принимают в форме таблеток обычно раз в день параллельно с лечением LHRH.
Хотя и весьма редко, но в процессе лечения бикалутамидом возникает риск развития гепатотоксичности. Пациентам с имеющейся патологией печени данное лечение должно назначаться с осторожностью и на всем протяжении лечения необходимо периодически проводить биохимические анализы крови для контроля функции печени.
Терапевтическая активность бикалутамида была описана в клинической литературе, например [Chen J., Kim J., Dalton J.T. Discovery and therapeutic promise of selective androgen receptor modulators // Mol. Interv.-2005 - 5(3) - P.173-188; Schellhammer P.F., Sharifi R., Block N.L., Soloway M.S., Vernier P.M., Patterson A.L., Sarosdy M.F., Vogelzang N.J., Schellenger J.J., Kolvenbag G.J. Clinical benefits of bicalutamide compared with flutamide in combined androgen blockade for patients with advanced prostatic carcinoma: final report of a double-blind, randomized, multicenter trial. Casodex Combination Study Group // Urology - 1997 - 50(3) - Р.330-336]. Но не менее важным критерием эффективности препарата являются фармакокинетические показатели, физико-химические свойства различных структурных модификаций. Например, аморфная форма, соль, сокристалл, полиморфные модификации, имеют различные физические и химические свойства, что сказывается на фармацевтических параметрах API, таких как стабильность при хранении, сжимаемость и другие. Определяющими факторами биодоступности являются растворимость и кинетические показатели растворения. Низкая растворимость лекарственного соединения в биологических жидкостях приводит к низкой эффективности лекарственного препарата. Поэтому увеличение уровня растворимости и скорости растворения препарата является актуальной технической задачей.
Задачей повышения растворимости занимаются уже давно, поэтому в настоящий момент известно большое количество методов, решающих эту проблему:
• тонкое измельчение для создания большей площади поверхности растворяемого соединения [Chaumeil J. С.Micronisation: a method of improving the Bioavailability of poorly soluble drugs // Methods Find. Exp.Clin. Pharmcol. - 1998 - 20(3) - P.211-215];
• использование солей исследуемых объектов с улучшенной растворимостью [Agharkar S., Lindenbaum S., Higuchi Т. Enhancement of solubility of drug salts by hydrophilic counter-ions: properties of organic salts of an anti-malarial drug // J. Pharm. Sci. - 1976 - 65(5) - P. 747-749];
• растворение в сложных [Amin К., Dannenfelser R.-M., Zielinski J., Wang В. Lyophilization of polyethylene glycol mixtures // J. Pharm. Sci. - 2004 - 93(9) - P.2244-2249] и мицеллярных растворителях [Torchillin V.P. Micellar nanocarriers: pharmaceutical perspectives // Pharm. Res. - 2007 -24(1) - P. 1-16];
• образование супрамолекулярных комплексов с циклодекстринами [Rajewski R. A., Stella V. J. Pharmaceutical applications of cyclodextrins. 2. In vivo drug delivery // J. Pharm. Sci. - 1996 - 85(11) - P. 1142-1169];
• использование фосфолипидных везикул, наполненных липофильными соединениями [Humberstone A. J., Charman W. N. Lipid-based vehicles for the oral delivery of poorly soluble drugs // Adv. Drug Deliv. Rev. - 1997 - 25(1) - P. 103-128].
Однако известные способы нельзя характеризовать как универсальные методы. Так, несмотря на то, что тонкое измельчение вещества увеличивает скорость растворения лекарственного средства, однако оно не увеличивает равновесную растворимость вещества. Причина данной проблемы кроется в том, что возрастание ван-дер-ваальсовых взаимодействий и электростатического притяжения между мелкими частицами ведут к уменьшению эффективной площади растворения и, таким образом, ограничивают предел биологической активности.
Повышение растворимости путем получения солей неприемлемо, так как в фармацевтике используются в основном слабо ионизируемые и нейтральные молекулы, а соли в данный класс соединений не входят.
Использование сложных и мицеллярных растворителей предполагает приемлемую растворимость и совместимость молекул лекарственного соединения с растворителем, что не всегда достижимо.
Повышение растворимости путем образования комплексов с циклодекстринами, а также использование фосфолипидных везикул применимо для лекарственных соединений пролонгированного действия, однако, не редко требуются лекарства быстрого действия, например, нестероидные противовоспалительные средства.
Растворимость и скорость растворения бикалутамида в воде чрезвычайно низкая (<5 мг/л), поэтому вопрос повышения растворимости пытались решить ранее различными методами:
• создание твердых дисперсий с поливинипирролидоном [F. Ren, Q. Jing, Y. Tang, Y. Shen, J. Chen, F. Gao and J. Cui. Characteristics of Bicalutamide Solid Dispersions and Improvement of the Dissolution. Drug Development and Industrial Pharmacy, 32, 2006, p.967-972], с полиэтиленоксидом [O.A. Abu-Diak, D.S. Jones, G.P. Andrews. Understanding the Performance of Melt-Extruded Poly(ethylene oxide)-Bicalutamide Solid Dispersions: Characterisation of Microstructural Properties Using Thermal, Spectroscopic and Drug Release Methods. Journal of Pharmaceutical Sciences, 101(1), 2012, p.200-213];
• получение наноразмерных частиц бикалутамида [Y. Le, H. Ji, J.-F. Chen, Z. Shen, J. Yun, M. Pu. Nanosized bicalutamide and its molecular structure in solvents. International Journal of Pharmaceutics, 370 (2009), 175-180];
• получение различных нанодисперсий с бикалутамидом [С.Li, С.Li, Y. Le, J.-F. Chen, Formation of bicalutamide nanodispersion for dissolution rate enhancement. International Journal of Pharmaceutics, 404(2011), 257-263];
• получение микрокристаллов бикалутамида посредством жидких антирастворителей [Т. АН Мeer, К.P. Sawant, P.D. Amin. Liquid antisolvent precipitation process for solubility modulation of bicalutamide. Acta Pharm. 61, (2011), p.435-445]
• и др.
Несмотря на то, что в дисперсии с поливинипирролидоном растворимость бикалутамида возрастает, использование данной методики не приветствуется, потому что поливинипирролидон является вредной пищевой добавкой. Различные микро- и нанодисперсий несколько повышают растворимость, однако являются не стабильными.
Известно также, что повысить растворимость можно путем образования сокристальной формы API с компонентом, способствующим увеличению растворения. Сокристаллы - это супрамолекулярные системы, где одним из компонентов является плохо растворимый API, т.е. молекула лекарственного соединения, а вторым компонентом (коформером) выступает молекула хорошо растворимого соединения, которая лучше усваивается организмом и участвует в ферментативных процессах. [Lara-Ochoa F. and Espinosa-Perez G. Cocrystals definitions // Supramolecular Chemistry. - 2007 - 19(8) - P. 553-557].
Сокристаллы, использующиеся в фармацевтической индустрии, привлекательны тем, что дают возможность получения новых кристаллических форм API со специальными свойствами, такими как, улучшенная растворимость, термическая стабильность, улучшенные механические свойства и др. Более того, благодаря возможности подбора коформера для сокристалла, можно провести, так сказать, «точную настройку» физических свойств сокристалла.
До сих пор не известны технические решения повышения скорости и уровня растворимости именно бикалутамида методом получения его сокристаллической формы.
Сущность изобретения
Техническая задача изобретения состояла в поиске сокристаллической формы бикалутамида, имеющей более высокие скорость и уровень растворимости и пригодной для использования в фармацевтической промышленности.
Сущность изобретения состоит в следующем.
1. Сокристаллическая форма бикалутамида с 2-гидроксибензамидом.
2. Сокристаллическая форма по п.1, где молярное соотношение бикалутамида с 2-гидроксибензамидом составляет 1:1.
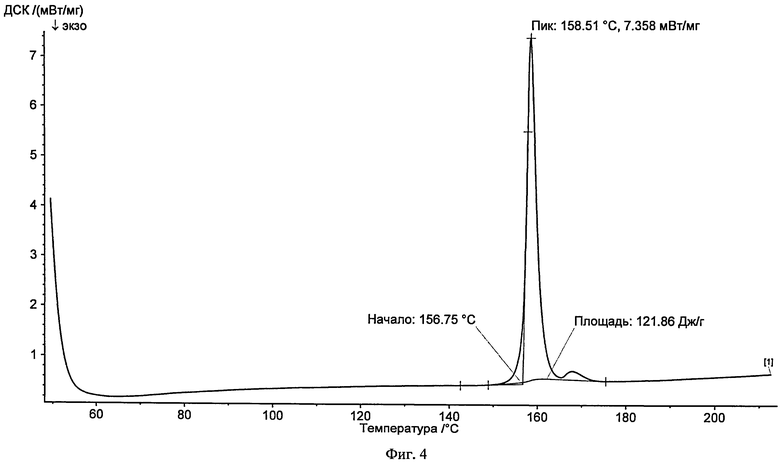
3. Сокристаллическая форма по п.1, имеющая эндотермический пик от 156 до 160°С, по данным измерений при помощи дифференциальной сканирующей калориметрии (анализа DSC).
4. Сокристаллическая форма по п.1, имеющая пики при 2θ(°) 3.16, 4.94, 5.66, 26.1 по данным измерения дифракции рентгеновского излучения монокристалла.
5. Сокристаллическая форма по п.1, имеющая эндотермический пик от 156 до 160°С, по данным измерений при помощи дифференциальной сканирующей калориметрии (анализа DSC) и пики при 2θ(°) 3.16, 4.94, 5.66, 26.1 по данным измерения дифракции рентгеновского излучения монокристалла.
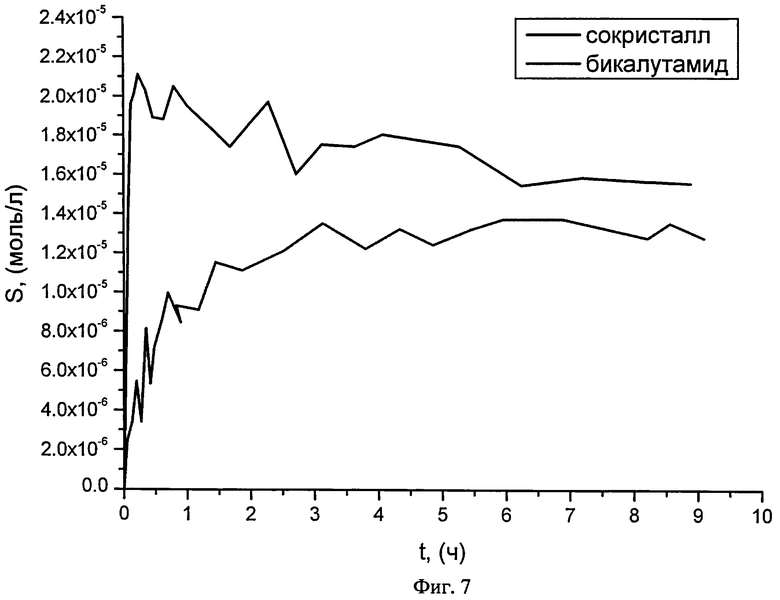
Заявленное изобретение позволяет получить следующее преимущество - повышение растворимости в воде в 2 раза по сравнению с показателями растворимости бикалутамида в чистом виде за первые 2 часа процесса растворения. Это важно, поскольку при наличии воспалительных процессов в организме человека, необходимо эффективное действие лекарственного средства именно в начальный период времени, что и обеспечивается сокристальной формой.
Дальнейшая оценка кинетики растворения показывает на любом временном промежутке растворимость сокристальной формы бикалутамида выше, чем соединения в чистом виде. Повышенная равновесная растворимость бикалутамида в сокристальной форме позволяет повысить эффективность пролонгированного действия лекарственного средства.
Данные по растворимости были получены для водного раствора при комнатной температуре на установке для измерения растворимости твердых соединений методом изотермического насыщения. Пробы отбирали в точках примерно 0.07, 0.12, 0.17, 0.25, 0.35, 0.5, 0.63, 0.8, 1, 1.4, 1.7, 2.3, 2.7, 3.1, 3.6, 4, 5.3, 6.2, 7.2, 8.2, 8.9, 23, 24 часа и анализировали при помощи спектрофотометра VARIAN CARY 50 в ультрафиолетовой области спектра, рабочий диапазон длин волн λ = 190÷400 нм.
Заявленный новый сокристалл - твердое кристаллическое стабильное вещество, не распадается, не подвержено воздействию влаги и удобен для приготовления стабильных фармацевтических препаратов. Заявленный сокристалл бикалутамида может использоваться для производства средства для лечения тестостеронзависимого рака простаты. Кроме того, за счет присутствия 2-гидроксибензамида полученный сокристалл обладает возможностью профилактики лихорадочного синдрома у больных раком простаты (простудные и инфекционные заболевания); болевого синдрома слабой и средней интенсивности: артралгия, миалгия, невралгия, мигрень и головная боль.
Структура заявленного сокристалла доказана тремя методами, в совокупности достаточными для утверждения об образовании нового соединения:
• дифракция в рентгеновских лучах поликристалла
• дифракция в рентгеновских лучах монокристалла
• дифференциальная сканирующая калориметрия (DSC).
На фиг.1 представлен типичный профиль XPRD сокристалла бикалутамид:2-гидроксибензамид (1:1) в соответствии с одним из вариантов изобретения.
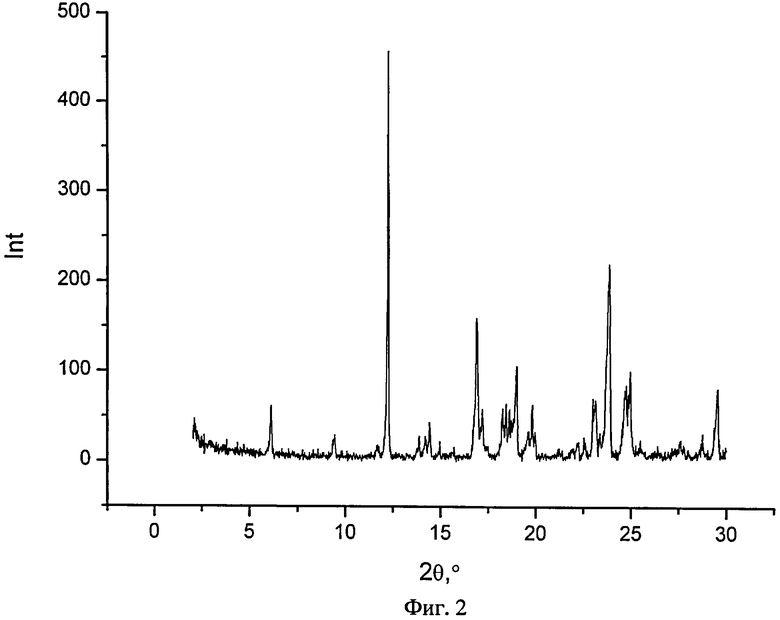
На фиг.2 представлен типичный профиль XPRD бикалутамида в чистом виде.
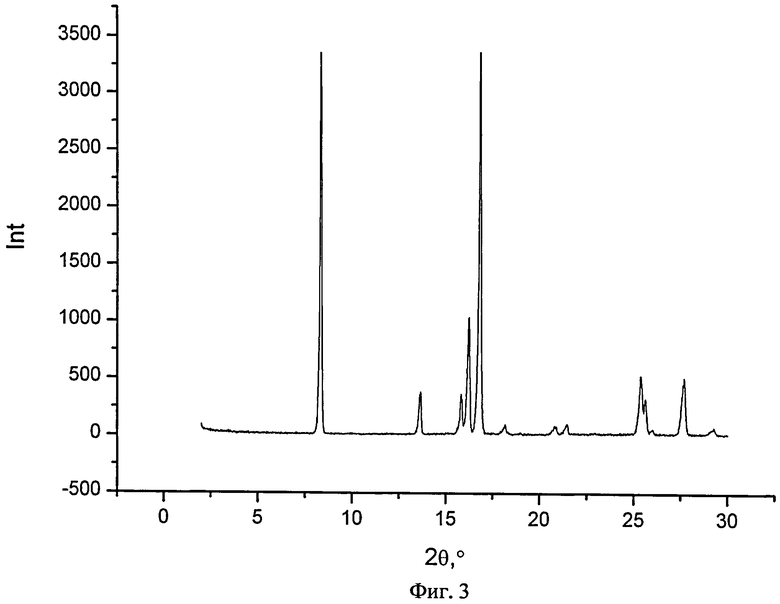
На фиг.3 представлен типичный профиль XPRD 2-гидроксибензамида в чистом виде.
На фиг.4 представлена типичная термограмма DSC сокристалла бикалутамид: 2-гидроксибензамид (1:1) в соответствии с одним из вариантов изобретения.
На фиг.5 представлена типичная термограмма DSC бикалутамида в чистом виде.
На фиг.6 представлена типичная термограмма DSC 2-гидроксибензамида в чистом виде.
На фиг.7 представлены данные по растворимости для сокристалла бикалутамид: 2-гидроксибензамид (1:1) и бикалутамида в чистом виде.
Сведения, подтверждающие возможность воспроизведения. изобретения
Для получения заявленного сокристалла использовали следующие вещества:
- бикалутамид - фирма производитель «Sigma-Aldrich», CAS 90357-06-5, чистота≥98%;
- 2-гидроксибензамид - фирма производитель «Sigma-Aldrich», lot S65911, CAS 65-45-2, чистота 99%;
- этанол - Спирт марки «Люкс» ГОСТ Р51652-2000 2001-07-01 «Спирт этиловый рективикованный из пищевого сырья. ТУ».
Новый сокристалл бикалутамида в существенной степени характеризуется результатами рентгеноструктурного анализа, показанными на фиг.1, 2, 3, и в существенной степени описывается данными термограммы DSC, представленными на фиг.4, 5, 6. Получить заявленный сокристалл можно и в твердой фазе и в растворе.
Пример 1
Смесь 86 мг (0,2 ммоль) бикалутамида и 27,4 мг (0,2 ммоль) 2-гидроксибензамида помещают в агатовые ячейки для перемола в планетарной микромельнице. В ячейку помещают 10 агатовых шариков диаметром 3 мм. Процесс перемолки на скорости 600 об/мин продолжают дважды по полчаса с перерывом 5 минут. Оставшийся порошок представляет собой сокристалл бикалутамид:2-гидроксибензамид (1:1), что было подтверждено данными XPRD и DSC. Полученный профиль XPRD конечного продукта в существенной степени соответствовал тому, что показан на Фиг.1. Полученная термограмма DSC конечного продукта в существенной степени соответствовала тому, что показана на Фиг.4.
Пример 2
Смесь 86 мг (0,2 ммоль) бикалутамида и 27,4 мг (0,2 ммоль) 2-гидроксибензамида растворяют в 2 мл этанола до полного растворения. Полученный прозрачный раствор оставляют в вытяжном шкафу до полного испарения растворителя. Оставшийся порошок представляет собой сокристалл бикалутамид:2-гидроксибензамид (1:1), что подтверждено данными DSC, термограмма, которой полностью совпадает с термограммой DSC конечного продукта, полученного по Примеру 1.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА 2-ГИДРОКСИБЕНЗАМИДА С 4-АМИНОБЕНЗОЙНОЙ КИСЛОТОЙ | 2012 |
|
RU2497804C1 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА 2-ГИДРОКСИБЕНЗАМИДА С САЛИЦИЛОВОЙ КИСЛОТОЙ | 2013 |
|
RU2539350C1 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА ФЕНБУФЕНА | 2012 |
|
RU2521572C1 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА НИФЛУМОВОЙ КИСЛОТЫ С ИЗОНИКОТИНАМИДОМ ИЛИ КОФЕИНОМ | 2013 |
|
RU2536484C1 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА ТЕОФИЛЛИНА С ДИФЛУНИСАЛОМ ИЛИ ДИКЛОФЕНАКОМ | 2013 |
|
RU2542100C1 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА ДИФЛУНИСАЛА | 2016 |
|
RU2617849C1 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА ИЗОНИАЗИДА | 2016 |
|
RU2630957C1 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА 1-[(5-ПАРА-МЕТИЛ-МЕТА-ХЛОР-ФЕНИЛАМИНО)-1,2,4-ТИАДИАЗОЛ-3-ИЛ]-ПРОПАН-2-ОЛА | 2019 |
|
RU2721335C1 |
| СО-КРИСТАЛЛИЧЕСКИЕ ФОРМЫ ТЕОФИЛЛИНА | 2022 |
|
RU2805752C2 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА 1-[5-(4-ХЛОРФЕНИЛАМИНО)-1,2,4-ТИАДИАЗОЛ-3-ИЛ]-ПРОПАН-2-ОЛА | 2018 |
|
RU2712443C1 |



Изобретение относится к сокристаллической форме бикалутамида с 2-гидроксибензамидом с молярным соотношением 1:1. Сокристаллическая форма имеет: эндотермический пик от 156 до 160°С по данным измерений при помощи дифференциальной сканирующей калориметрии (анализа DSC), пики при 2θ(°) 3.16, 4.94, 5.66, 26.1 по данным измерения дифракции рентгеновского излучения монокристалла. Технический результат: получена новая сокристаллическая форма бикалутамида с повышенной скоростью и уровнем растворимости, которая может найти применение в качестве фармацевтического препарата для лечения рака простаты. 4 з.п. ф-лы, 7 ил., 2 пр.
1. Сокристаллическая форма бикалутамида с 2-гидроксибензамидом.
2. Сокристаллическая форма по п.1, где молярное соотношение бикалутамида с 2-гидроксибензамидом составляет 1:1.
3. Сокристаллическая форма по п.1, имеющая эндотермический пик от 156 до 160°С, по данным измерений при помощи дифференциальной сканирующей калориметрии (анализа DSC).
4. Сокристаллическая форма по п.1, имеющая пики при 2θ(°) 3.16, 4.94, 5.66, 26.1 по данным измерения дифракции рентгеновского излучения монокристалла.
5. Сокристаллическая форма по п.1, имеющая эндотермический пик от 156 до 160°С, по данным измерений при помощи дифференциальной сканирующей калориметрии (анализа DSC) и пики при 2θ(°) 3.16, 4.94, 5.66, 26.1 по данным измерения дифракции рентгеновского излучения монокристалла.
| Ленточный тормоз двухстороннего действия | 1952 |
|
SU100172A1 |
| WO 2005089511 A1, 29.09.2005 | |||
| T | |||
| ALI MEER et al, Acta Pharm., vol.61, 2011, p.p.435-445 | |||
| ДИАФРАГМЕННЫЙ НАСОС | 1926 |
|
SU7101A1 |
Авторы
Даты
2014-03-27—Публикация
2012-12-21—Подача