Область техники
Настоящее изобретение относится к терапевтическому средству или профилактическому средству для нейропатической боли.
Предшествующий уровень техники
Под нейропатической болью (также обозначаемой как нейрогенная боль) подразумевают боль, вызванную нарушением или заболеванием периферической или центральной соматосенсорной нервной системы и приводящую к прямому повреждению, компрессии или т.п. нервной ткани без какого-либо болевого раздражения ноцицептора.
В качестве терапевтического лекарственного средства для нейропатической боли применяют противосудорожные средства, антидепрессанты и анксиолитические средства, а также противоэпилептические средства, включая прегабалин и габапентин, которые являются лигандами α2δ кальциевых каналов (непатентный документ 1). Из них прегабалин является всеобщим стандартным терапевтическим лекарственным средством для нейропатической боли, но также известно, что введение прегабалина часто вызывает побочные эффекты, такие как головокружение, сонливость, атаксия, слабость и т.п., в основе которых, как полагают, лежит ингибирующее действие на центральную нервную систему (непатентный документ 2).
Для уменьшения дозы прегабалина или габапентина в последние годы исследуют комбинированное использование этих лигандов α2δ кальциевых каналов с различными лекарственными средствами, и опубликовано, что можно получать синергическое анальгезирующее действие при комбинированном применении, например, лиганда α2δ кальциевых каналов с ингибитором фосфодиэстеразы типа 5 силденафилом, тадалафилом или варденафилом (патентный документ 1) или с другими лекарственными средствами (патентные документы 2-10 и непатентные документы 8-12), или при комбинированном применении габапентина с неопиоидным аналгетиком ацетаминофеном (непатентный документ 3) или нитро-парацетамолом (непатентный документ 4), или с опиоидным аналгетиком оксикодоном (непатентный документ 5) или морфином (непатентный документ 13), или с производным витамина B1 бенфотиамином (непатентный документ 6) или витамином B12 цианокобаламином (непатентный документ 6). Кроме того, также опубликовано, что синергическое анальгезирующее действие можно получать при комбинированном применении 3 лекарственных средств: габапентина, донепезила (ингибитора холинэстеразы) и дулоксетина (ингибитора обратного захвата серотонина и норадреналина) (непатентный документ 7).
Известный уровень техники и документы
Патентные документы
Патентный документ 1: WO 04/016259
Патентный документ 2: WO 10/025931
Патентный документ 3: WO 09/021058
Патентный документ 4: WO 08/079727
Патентный документ 5: WO 08/079720
Патентный документ 6: WO 07/090661
Патентный документ 7: WO 05/102390
Патентный документ 8: WO 05/025675
Патентный документ 9: WO 01/024792
Патентный документ 10: WO 01/013904
Патентный документ 11: WO 10/050577
Непатентные документы
Непатентный документ 1: Dooley et al., Trends Pharmacol. Sci., 2007, vol. 28, p. 75
Непатентный документ 2: Zaccara et al., Seizure, 2008, vol. 17, p. 405
Непатентный документ 3: Hama et al., Neuropharmacology, 2010, vol. 58, p. 758
Непатентный документ 4: Curros-Criado et al., Br. J. Pharmacol., 2009, vol. 158, p. 601
Непатентный документ 5: Hanna et al., Eur. J. Pain, 2008, vol. 12, p. 804
Непатентный документ 6: Mixcoatl-Zecuatl et al., Methods Find. Exp. Clin. Pharmacol., 2008, vol. 30, p. 431
Непатентный документ 7: Hayashida et al., Eur. J. Pharmacol., 2008, vol. 598, p. 21
Непатентный документ 8: Tomic et al., Eur. J. Pharmacol., 2010, vol. 628, p. 75
Непатентный документ 9: Park et al., J. Korean Med. Sci., 2008, vol. 23, p. 678
Непатентный документ 10: Imai et al., Eur. J. Pharmacol., 2008, vol. 588, p. 244
Непатентный документ 11: Codd et al., Pain, 2008, vol. 134, p. 254
Непатентный документ 12: Hayashida et al., Anesthesiology, 2007, vol. 106, p. 1213
Непатентный документ 13: De la O-Arciniega et al., Pharmacol. Biochem. Behav., 2009, vol. 92, p. 457
Сущность изобретения
Задачи, подлежащие решению посредством изобретения
Однако в настоящее время при комбинированном лечении лигандом α2δ кальциевых каналов из-за того, что такое лечение предназначено снижать побочные эффекты лиганда α2δ кальциевых каналов per se, наблюдают случаи, когда анальгезирующее действие является недостаточным вследствие уменьшения дозы лиганда α2δ кальциевых каналов, и случаи, когда возникают новые побочные эффекты вследствие увеличения дозы лекарственного средства, применяемого при комбинированном лечении. Например, опубликовано, что при комбинированном применении габапентина и морфина возникают нарушения моторной координации при дозе, достаточной для получения синергического анальгезирующего действия (непатентный документ 13). Таким образом, предполагают, что даже в случае применения любого другого лекарственного средства в комбинированном лечении трудно избежать возникновения побочных эффектов на центральную нервную систему при получении синергического анальгезирующего действия.
Таким образом, задача настоящего изобретения состоит в получении терапевтического средства или профилактического средства для нейропатической боли, посредством которого получают усиленное синергическое анальгезирующее действие при дозе, при которой лиганд α2δ кальциевых каналов не оказывает каких-либо побочных эффектов, а также при которой средство не оказывает каких-либо новых побочных эффектов на центральную нервную систему.
Средства решения задач
Авторы настоящего изобретения провели тщательное исследования с целью решения описанных выше проблем и установили, что при применении лиганда α2δ кальциевых каналов в комбинации с производным циклогексана, которое проявляет превосходное анальгезирующее действие при нейропатической боли, анальгезирующее действие при нейропатической боли является синергически усиленным без обострения побочных эффектов лиганда α2δ кальциевых каналов на центральную нервную систему.
Таким образом, настоящее изобретение относится к терапевтическому средству или профилактическому средству для нейропатической боли, где указанное средство содержит в качестве активных ингредиентов производное циклогексана, представленное формулой (I) ниже:
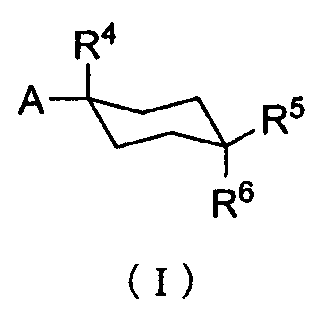
где A представляет собой заместитель, представленный формулой (IIa) или (IIb):

каждый R1 и R2 независимо представляет собой атом водорода, атом хлора, C1-C3 галогеналкильную группу, C1-C4 алкильную группу или C1-C4 алкоксигруппу; R3 представляет собой атом водорода или атом хлора; R4 представляет собой атом фтора, гидроксиметильную группу или гидроксильную группу; каждый R5 и R6 независимо представляет собой атом водорода, атом фтора, C1-C3 галогеналкильную группу, карбоксильную группу, метоксикарбонильную группу, этоксикарбонильную группу, C1-C4 алкоксигруппу, гидроксильную группу или C2-C5 алкилкарбонилоксигруппу или необязательно вместе образуют оксогруппу; каждый R7 и R8 независимо представляет собой атом водорода или атом фтора; Y представляет собой атом кислорода или атом серы и Z представляет собой атом азота или метиновую группу,
или его фармацевтически приемлемую соль, или его пролекарство; и лиганд α2δ кальциевых каналов.
Предпочтительно в описанном выше производном циклогексана или его фармацевтически приемлемой соли, или его пролекарстве каждый R1 и R2 независимо представляет собой трифторметильную группу, метильную группу или метоксигруппу; R3 представляет собой атом водорода; R4 представляет собой гидроксиметильную группу или гидроксильную группу и каждый R5 и R6 независимо представляет собой атом водорода, атом фтора, трифторметильную группу, карбоксильную группу, метоксигруппу, гидроксильную группу или ацетилоксигруппу (или R5 и R6 необязательно могут вместе образовывать оксогруппу).
Указанный выше лиганд α2δ кальциевых каналов предпочтительно представляет собой прегабалин или габапентин, более предпочтительно прегабалин.
Эффекты изобретения
Терапевтическое средство или профилактическое средство для нейропатической боли по настоящему изобретению может синергически усиливать анальгезирующее действие лиганда α2δ кальциевых каналов при сниженной дозе лиганда α2δ кальциевых каналов и существенно сокращать частоту побочных эффектов со стороны центральной нервной системы.
Краткое описание чертежей
На фиг.1 показан эффект комбинированного применения соединения 3 и прегабалина на модели частичного лигирования седалищного нерва (Зельтцера) на мышах (изменения через 1 час, 2 часа и 3 часа после перорального введения).
На фиг.2-A показан эффект комбинированного применения соединения 3 и прегабалина на модели частичного лигирования седалищного нерва (Зельтцера) на мышах (через 1 час после перорального введения).
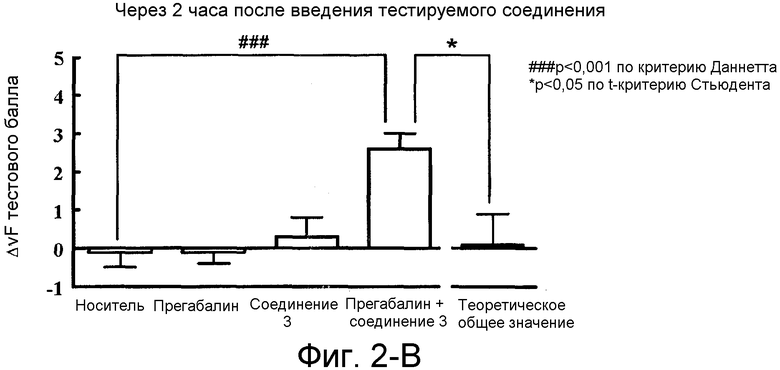
На фиг.2-B показан эффект комбинированного применения соединения 3 и прегабалина на модели частичного лигирования седалищного нерва (Зельтцера) на мышах (через 2 часа после перорального введения).
На фиг.3 показан эффект комбинированного применения соединения 3 и прегабалина в тесте "беличье колесо" на мышах (от 0,5 до 1,5 часов после перорального введения).
На фиг.4 показан эффект введения одного прегабалина на модели частичного лигирования седалищного нерва (Зельтцера) на мышах (через 1 час после перорального введения).
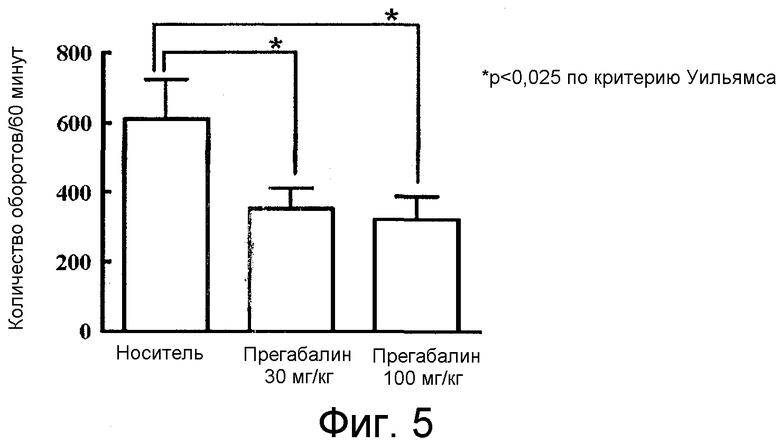
На фиг.5 показан эффект введения одного прегабалина в тесте "беличье колесо" на мышах (от 0,5 до 1,5 часов после перорального введения).
Способ осуществления изобретения
Терапевтическое средство или профилактическое средство для нейропатической боли по настоящему изобретению характеризуется тем, что содержит в качестве активных ингредиентов производное циклогексана, представленное ниже формулой (I), или его фармацевтически приемлемую соль, или его пролекарство; и лиганд α2δ кальциевых каналов.

где A представляет собой заместитель, представленный формулой (IIa) или (IIb):
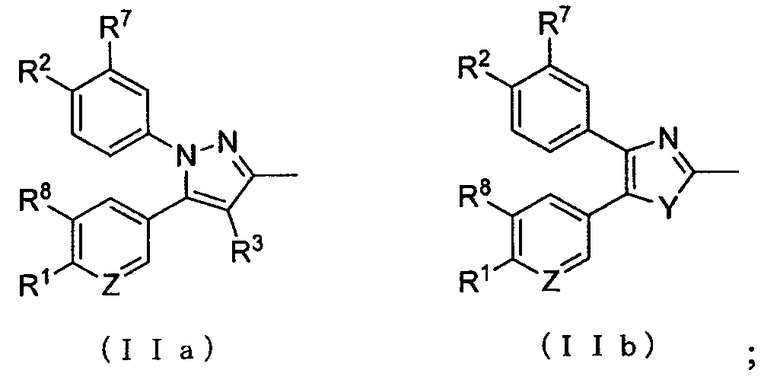
каждый R1 и R2 независимо представляет собой атом водорода, атом хлора, C1-C3 галогеналкильную группу, C1-C4 алкильную группу или C1-C4 алкоксигруппу; R3 представляет собой атом водорода или атом хлора; R4 представляет собой атом фтора, гидроксиметильную группу или гидроксильную группу; каждый R5 и R6 независимо представляет собой атом водорода, атом фтора, C1-C3 галогеналкильную группу, карбоксильную группу, метоксикарбонильную группу, этоксикарбонильную группу, C1-C4 алкоксигруппу, гидроксильную группу или C2-C5 алкилкарбонилоксигруппу или R5 и R6 могут вместе образовывать оксогруппу; каждый R7 и R8 независимо представляет собой атом водорода или атом фтора; Y представляет собой атом кислорода или атом серы и Z представляет собой атом азота или метиновую группу.
Термин "C1-C4 алкильная группа" обозначает неразветвленную, разветвленную или циклическую алкильную группу, содержащую от 1 до 4 атомов углерода, и примеры такой группы включают метильную группу, этильную группу, н-пропильную группу, изопропильную группу, циклопропильную группу, циклопропилметильную группу, н-бутильную группу, втор-бутильную группу и трет-бутильную группу.
Термин "C1-C4 алкоксигруппа" обозначает неразветвленную, разветвленную или циклическую алкилоксигруппу, содержащую от 1 до 4 атомов углерода, и примеры такой группы включают метоксигруппу, этоксигруппу, н-пропилоксигруппу, изопропилоксигруппу, циклопропилоксигруппу, н-бутоксигруппу, втор-бутоксигруппу и трет-бутоксигруппу.
Термин "C1-C3 галогеналкильная группа" обозначает неразветвленную алкильную группу, содержащую от 1 до 3 атомов углерода, где часть или все атомы водорода в группе замещены атомом(ами) галогена (под атомом галогена подразумевают атом фтора, атом хлора, атом брома или атом йода), и примеры такой группы включают монохлорметильную группу, монофторметильную группу, дифторметильную группу, трифторметильную группу, трихлорметильную группу и пентафторэтильную группу.
Примеры "C2-C5 алкилкарбонилоксигруппы" включают ацетилоксигруппу, этаноилоксигруппу, пропаноилоксигруппу, изопропаноилоксигруппу, бутаноилоксигруппу, изобутаноилоксигруппу и пивалоилоксигруппу.
В формуле (I) A предпочтительно представлен формулой (IIa), Y предпочтительно представляет собой атом кислорода и Z предпочтительно представляет собой метиновую группу.
R1 предпочтительно представляет собой атом водорода, атом хлора, трифторметильную группу, метильную группу, этильную группу, н-пропильную группу, изопропильную группу, метоксигруппу, этоксигруппу, н-пропилоксигруппу или изопропилоксигруппу, более предпочтительно трифторметильную группу, метильную группу или метоксигруппу и еще более предпочтительно метильную группу.
R2 предпочтительно представляет собой атом водорода, атом хлора, трифторметильную группу, метильную группу, этильную группу, н-пропильную группу, изопропильную группу, метоксигруппу, этоксигруппу, н-пропилоксигруппу или изопропилоксигруппу и более предпочтительно метоксигруппу.
R3 предпочтительно представляет собой атом водорода и R4 предпочтительно представляет собой гидроксиметильную группу или гидроксильную группу и более предпочтительно гидроксильную группу.
R5 предпочтительно представляет собой атом водорода, атом фтора, трифторметильную группу, карбоксильную группу, метоксигруппу, этоксигруппу, н-пропилоксигруппу, изопропилоксигруппу, гидроксильную группу, ацетилоксигруппу, пропаноилоксигруппу, бутаноилоксигруппу или изобутаноилоксигруппу, более предпочтительно атом водорода, гидроксильную группу или карбоксильную группу и еще более предпочтительно гидроксильную группу.
R6 предпочтительно представляет атом водорода, атом фтора, трифторметильную группу, карбоксильную группу, метоксигруппу, этоксигруппу, н-пропилоксигруппу, изопропилоксигруппу, гидроксильную группу, ацетилоксигруппу, пропаноилоксигруппу, бутаноилоксигруппу или изобутаноилоксигруппу, более предпочтительно атом водорода или гидроксильную группу и еще более предпочтительно атом водорода. R5 и R6 могут вместе образовывать оксогруппу.
Каждый R7 и R8 предпочтительно представляет собой атом водорода.
Из циклогексановых производных, представленных формулой (I), или их фармацевтически приемлемых солей, или пролекарств на их основе (далее в настоящем документе обозначаемые как соединение (I)) предпочтительные конкретные примеры представлены в таблице 1, но настоящее изобретение не ограничено ими.
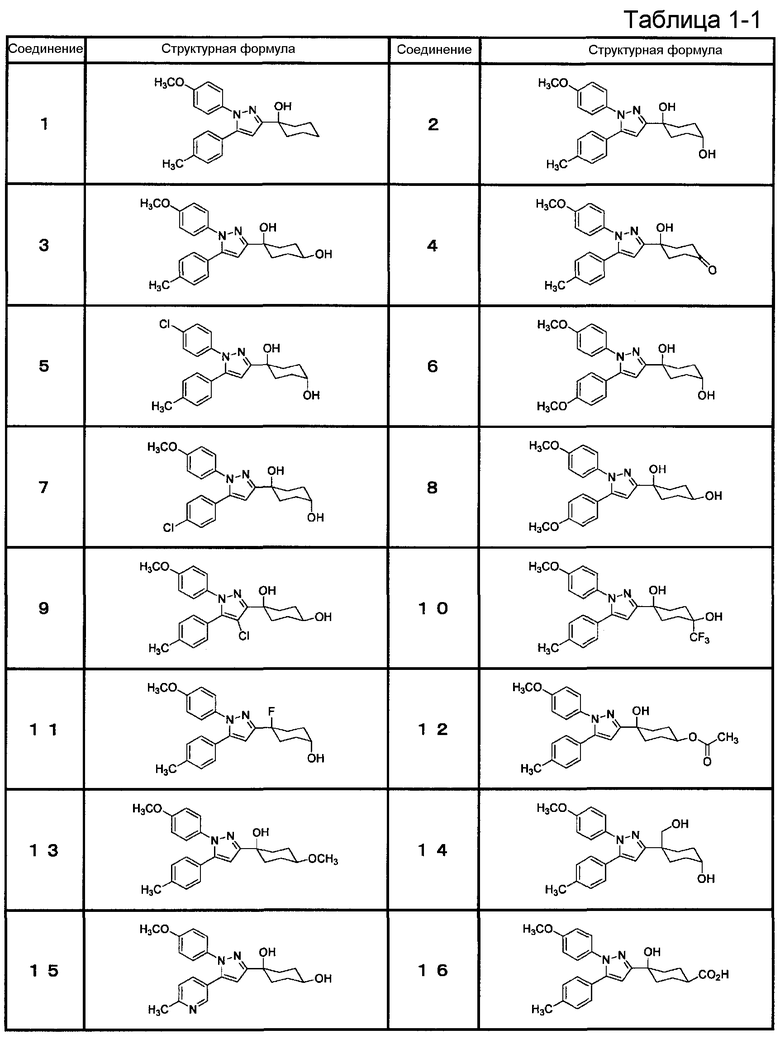
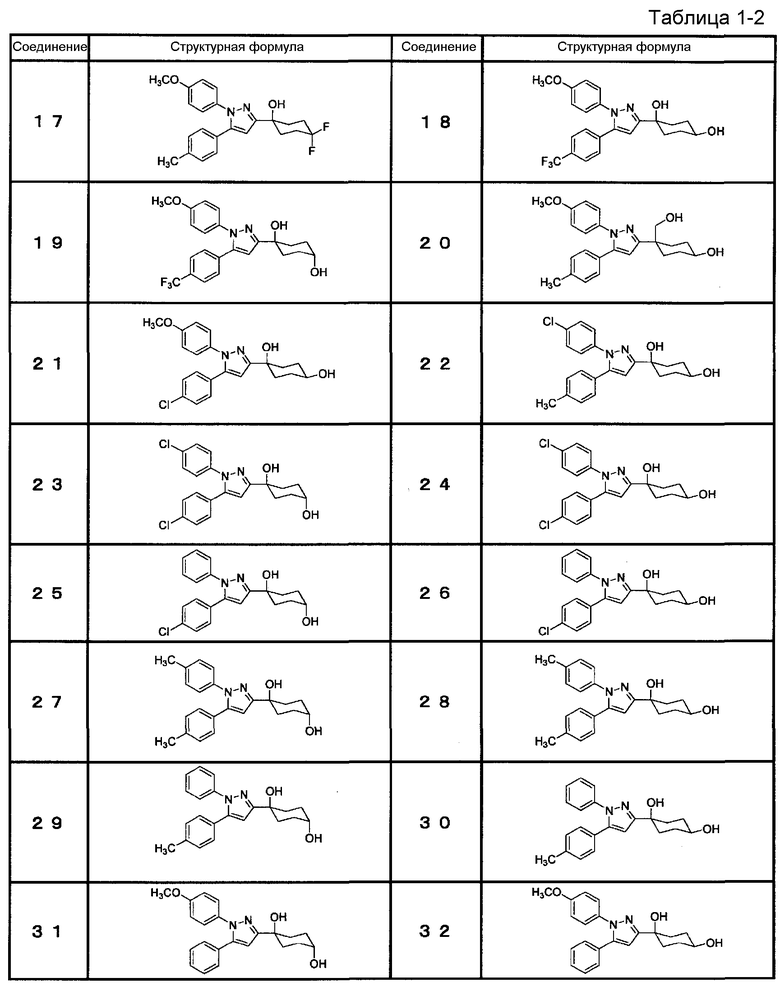
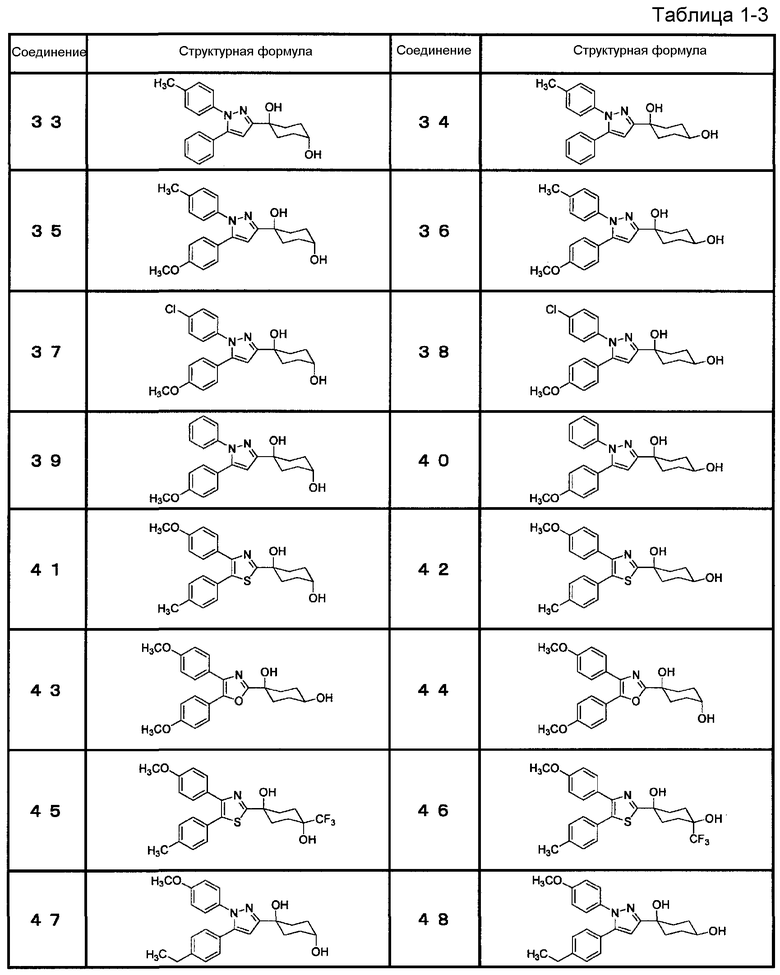
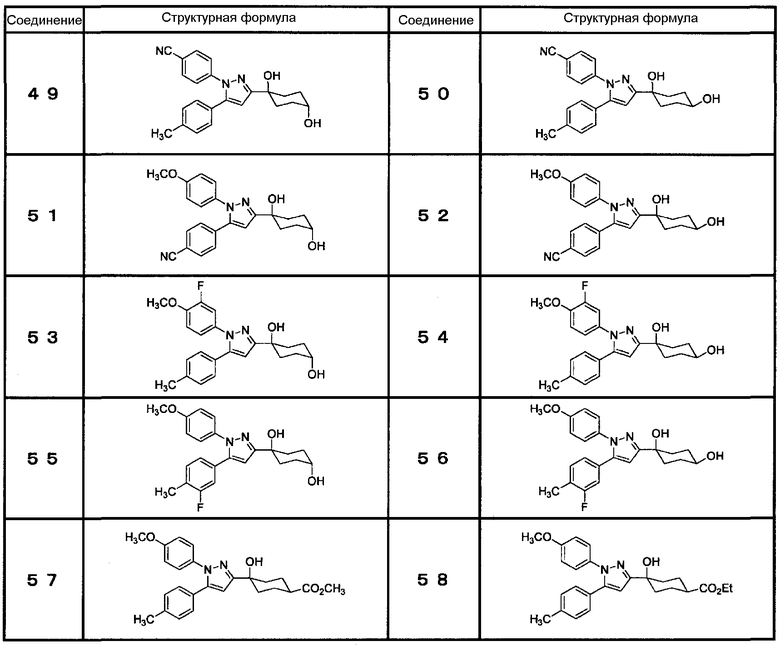

Соединение (I) включает все энантиомеры и их смеси, в случае если соединение (I) содержит асимметричный углерод(ы).
Соединение (I) включает все стереоизомеры и их смеси, в случае если соединение (I) содержит стереоизомер(ы).
Примеры лиганда α2δ кальциевых каналов для применения в комбинации с соединением (I) в настоящем изобретении включают прегабалин (S-(+)-4-амино-3-(2-метилпропил)бутановую кислоту или (S)-3-(аминометил)-5-(метилгексановую кислоту)) и габапентин (1-(аминометил)-циклогексануксусную кислоту или 2-[1-(аминометил)циклогексан]уксусную кислоту) и их фармацевтически приемлемые соли, и их пролекарства. Прегабалин или габапентин является предпочтительным, и прегабалин является более предпочтительным.
Примеры "фармацевтически приемлемой соли" включают соли неорганических кислот, такие как соль соляной кислоты, соль серной кислоты, соль фосфорной кислоты и соль бромистоводородной кислоты; соли органических кислот, такие как соль щавелевой кислоты, соль малоновой кислоты, соль лимонной кислоты, соль фумаровой кислоты, соль молочной кислоты, соль яблочной кислоты, соль янтарной кислоты, соль винной кислоты, соль уксусной кислоты, соль трифторуксусной кислоты, соль малеиновой кислоты, соль глюконовой кислоты, соль бензойной кислоты, соль аскорбиновой кислоты, соль метансульфоновой кислоты, соль п-толуолсульфоновой кислоты и соль коричной кислоты; соли неорганических оснований, такие как натриевая соль, калиевая соль, кальциевая соль, магниевая соль и аммонийная соль; и соли органических оснований, такие как метиламиновая соль, диэтиламиновая соль, триметиламиновая соль, триэтиламиновая соль, пиридиновая соль, триэтаноламиновая соль, этилендиаминовая соль и гуанидиновая соль. Дополнительно соединение (I) может образовывать гидрат или сольват, и в настоящее изобретение также включены кристаллические полиморфы.
Соединение (I) можно синтезировать, например, способом, как описано в опубликованном документе (WO 10/050577).
Лиганд α2δ кальциевых каналов можно синтезировать, например, способом, как описано в опубликованном документе (JP 51-88940 A, JP 7-508288 A или JP 2004-536873 A).
Терапевтическое средство или профилактическое средство для нейропатической боли, включающие в качестве активных ингредиентов соединение (I) и лиганд α2δ кальциевых каналов, также проявляют превосходное анальгезирующее действие при введении млекопитающему, отличному от человека. Примеры отличного от человека млекопитающего включают мышь, крысу, хомяка, кролика, кошку, собаку, крупный рогатый скот, овцу и обезьяну.
Примеры "нейропатической боли" включают раковую боль, герпетическую боль, постгерпетическую невралгию, связанную со СПИДом невралгию, невралгию тройничного нерва и нейропатическую боль при диабете.
Что касается способа введения терапевтического средства или профилактического средства для нейропатической боли, содержащего в качестве активных ингредиентов соединение (I) и лиганд α2δ кальциевых каналов, смесь обоих ингредиентов, т.е. комбинированное лекарственное средство из обоих ингредиентов, то его можно вводить перорально или парентерально в том виде, в котором оно предоставлено, или после дополнительной комбинации его с носителем, который является фармацевтически приемлемым. Альтернативно, соединение (I) и лиганд α2δ кальциевых каналов можно получать индивидуально в виде отдельных лекарственных средств, а не в виде комбинированного лекарственного средства, а затем их можно вводить в одно и то же время в том виде, в котором они предоставлены, или после дополнительной комбинации каждого из них с носителем, который является фармацевтически приемлемым. Кроме того, индивидуальные отдельные лекарственные средства также можно вводить так, что одно из отдельных лекарственных средств вводят после другого через соответствующий период времени. В этих случаях нет необходимости, чтобы лекарственные формы и способы введения индивидуальных отдельных лекарственных средств являлись одинаковыми, и они могут отличаться друг от друга. "Соответствующий период времени", как указано выше, можно подтверждать клинически или путем экспериментов на животных.
Примеры лекарственной формы, в случае, если соединение (I) и лиганд α2δ кальциевых каналов вводят перорально в виде индивидуальных отдельных лекарственных средств или в виде комбинированного лекарственного средства, включают таблетки (включая покрытые сахаром таблетки и таблетки с пленочным покрытием), пилюли, гранулы, порошки, капсулы (включая мягкие капсулы и микрокапсулы), сиропы, эмульсии и суспензии, и примеры лекарственной формы, в случае, если их вводят парентерально, включают инъекционные растворы, пропитывающие средства, капли и суппозитории. Кроме того, также эффективна комбинация активного ингредиента(ов) с соответствующей основой (например, полимером масляной кислоты, полимером гликолевой кислоты, сополимером масляной кислоты-гликолевой кислоты, смесью полимера масляной кислоты и полимера гликолевой кислоты, сложным полиглицериновым эфиром жирной кислоты или т.п.) для получения препарата(ов) с длительным высвобождением.
Получение отдельных лекарственных средств или комбинированного лекарственного средства соединения (I) и лиганда α2δ кальциевых каналов в указанной выше лекарственной форме можно проводить известным способом, который широко применяют в области составления фармацевтических средств. В этом случае лекарственные средства можно получать так, что по мере необходимости в них содержатся эксципиент, связывающее средство, смазывающее средство, дезинтегрирующее средство, подсластитель, поверхностно-активное вещество, суспендирующее средство, эмульгатор и/или т.п., которые широко используют в области составления фармацевтических средств.
Отдельные лекарственные средства или комбинированное лекарственное средство соединения (I) и лиганда α2δ кальциевых каналов можно получать в форме таблеток так, что в них содержатся эксципиент, связывающее средство, дезинтегрирующее средство, смазывающее средство и/или т.п.; или в форме пилюль или гранул так, что в них содержатся эксципиент, связывающее средство, дезинтегрирующее средство и/или т.п. Кроме того, отдельные лекарственные средства или комбинированное лекарственное средство можно получать в форме порошков или капсул так, что в них содержится эксципиент и/или т.п.; в форме сиропов так, что в них содержится подсластитель и/или т.п.; или в форме эмульсий или суспензий так, что в них содержатся поверхностно-активное вещество, суспендирующее средство, эмульгатор и/или т.п.
Примеры указанного выше эксципиента включают лактозу, глюкозу, крахмал, сахарозу, микрокристаллическую целлюлозу, солодку в виде порошка, маннит, бикарбонат натрия, фосфат кальция и сульфат кальция.
Примеры указанного выше связывающего средства включают крахмальный клейстер, раствор гуммиарабика, раствор желатина, раствор трагаканта, раствор карбоксиметилцеллюлозы, раствор альгината натрия и глицерин.
Примеры указанного выше дезинтегрирующего средства включают крахмал и карбонат кальция.
Примеры указанного выше смазывающего средства включают стеарат магния, стеариновую кислоту, стеарат кальция и очищенный тальк.
Примеры указанного выше подсластителя включают глюкозу, фруктозу, инвертированный сахар, сорбит, ксилит, глицерин и простой сироп.
Примеры указанного выше поверхностно-активного вещества включают лаурилсульфат натрия, полисорбат 80, сложный сорбитановый эфир одноосновной жирной кислоты и полиоксил 40 стеарат.
Примеры указанного выше суспендирующего средства включают гуммиарабик, альгинат натрия, карбоксиметилцеллюлозу натрия, метилцеллюлозу и бентонит.
Примеры указанного выше эмульгатора включают гуммиарабик, трагакант, желатин и полисорбат 80.
Кроме того, при получении отдельных лекарственных средств или комбинированного лекарственного средства соединения (I) и лиганда α2δ кальциевых каналов в указанной выше лекарственной форме могут быть добавлены краситель, консервант, ароматическое вещество, модификатор, стабилизатор, загуститель и/или т.п., которые широко используют в области составления фармацевтических средств.
Суточная доза препарата, содержащего лиганд α2δ кальциевых каналов, изменяется в зависимости от состояний и массы тела пациента, типа ингибитора, способа введения и/или т.п. Например, в случае, если перорально вводят габапентин, предпочтительно, чтобы введение проводили в количестве от 10 до 3600 мг на взрослого (с массой тела приблизительно 60 кг) один раз или раздельно до трех раз, и в случае, если перорально вводят прегабалин, предпочтительно, чтобы введение проводили в количестве от 5 до 600 мг на взрослого (с массой тела приблизительно 60 кг) один раз или раздельно до трех раз. В отношении суточной дозы препарата, содержащего соединение (I), например, в случае, если препарат вводят перорально, предпочтительно, чтобы введение проводили в количестве от 1 до 1000 мг на взрослого (с массой тела приблизительно 60 кг) один раз или раздельно до трех раз, и в случае, если препарат вводят парентерально, если препарат представляет собой инъекционный раствор, предпочтительно, чтобы введение проводили в количестве от 0,01 до 100 мг на 1 кг массы тела посредством внутривенной инъекции.
Примеры
Настоящее изобретение описано более конкретно посредством примера изобретения. Однако настоящее изобретение не ограничено приведенным ниже примером.
Пример 1. Комбинированное действие соединения (I) и лиганда α2δ кальциевых каналов на модели нейропатической боли на мышах
Для оценки использовали от 7 до 8 самцов мышей ICR в возрасте 5 недель для одной экспериментальной группы. Модели нейропатической боли на мышах проводили способом Зельтцера (Seltzer et al., Pain, 1990, vol. 43, p.205, Malmberg et al., Pain, 1998, vol. 76, p.215). Таким образом, седалищный нерв в области бедра правой задней конечности каждой мыши анестезировали и под микроскопом трижды туго перевязывали седалищный нерв шелковой нитью 8-0 (NATSUME SEISAKUSHO) так, что при перевязывании защемляли только половину толщины нерва.
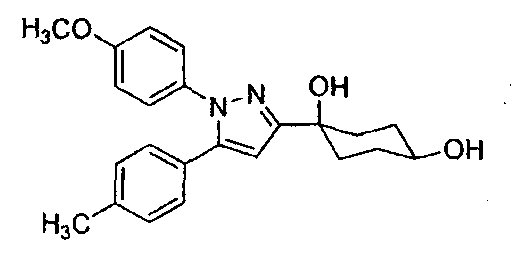
В качестве тестируемого соединения выбирали 1-(1-(4-метоксифенил)-5-(п-толил)-1H-пиразол-3-ил)циклогексан-цис-1,4-диол (далее в настоящем документе обозначаемое как соединение 3), которое представлено следующей ниже формулой и входит в состав соединения (I).
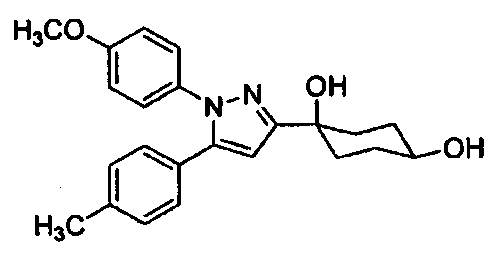
В качестве лиганда α2δ кальциевых каналов выбирали прегабалин.
Мышей в моделях нейропатической боли разделяли на 4 группы: группу, обрабатываемую носителем (носитель на фиг.1 и фиг.2), группу, обрабатываемую 3 мг/кг одного прегабалина (прегабалин на фиг.1 и фиг.2), группу, обрабатываемую 0,3 мг/кг одного соединения 3 (соединение 3 на фиг.1 и фиг.2) и группу, одновременно обрабатываемую 3 мг/кг прегабалина и 0,3 мг/кг соединения 3 (прегабалин + соединение 3 на фиг.1 и фиг.2).
Через семь суток после описанного выше перевязывания седалищного нерва мышам каждой группы вводили носитель, вводили суспензию одного прегабалина (3 мг/кг), вводили суспензию одного соединения 3 (0,3 мг/кг) или вводили (комбинированное введение) смешанную суспензию прегабалина и соединения 3 (3 мг/кг и 0,3 мг/кг, соответственно) с использованием 0,5% метилцеллюлозы в качестве носителя.
Оценку нейропатической боли (далее в настоящем документе "тест фон Фрея") проводили, как описано ниже. Мышей в моделях нейропатической боли по меньшей мере в течение 1 часа выдерживали в акриловой клетке для измерения (NATSUME SEISAKUSHO), расположенной на проволочной сетке. Затем с помощью нити (North Coast Medical. Inc.), оказывающей давление 0,16 г, мышей подвергали механическому тактильному раздражению, 3 раза прикладывая нить к поверхности подошвы обеих задних лап каждый раз в течение 3 секунд в интервалом в 3 секунды. Реакцию отдергивания, наблюдаемую при каждом механическом тактильном раздражении, оценивали в баллах (0 - нет реакции, 1 - проявляют слабую и/или небольшую реакцию отдергивания в ответ на раздражение, 2 - проявляют быструю реакцию отдергивания без вздрагивания (быстрое и продолжительное потряхивание лапами) или облизывания (облизывание лап) в ответ на раздражение, 3 - проявляют быструю реакцию отдергивания со вздрагиванием и/или лизанием) и полученную сумму баллов в трех повторениях использовали как общий балл.
Через семь суток после перевязывания седалищного нерва проводили тест фон Фрея до введения тестируемого соединения, через 1 час после введения, через 2 часа после введения и через 3 часа после введения. В качестве показателя анальгезирующего действия использовали разницу общего балла до и после введения тестируемого соединения (далее в настоящем документе "ΔvF тестового балла"), которую рассчитывали для каждого момента времени после введения тестируемого соединения от общего балла, полученного до введения тестируемого соединения.
Теоретическое общее значение, которое являлось теоретической ΔvF тестового балла, рассчитанной на основе предположения, что комбинированное применение соединения 3 и прегабалина проявляет не более чем дополнительное анальгезирующее действие, рассчитывали на основании ΔvF тестовых баллов, полученных при введении одного соединения 3 или прегабалина. Таким образом, отдельные ΔvF тестовых баллов мышей в группе, обработанной одним прегабалином, и мышей в группе, обработанной одним соединением 3, сортировали в возрастающем порядке, соответственно, и добавляли ΔvF тестовых баллов двух групп в тот же ряд, таким образом, получая теоретическое общее значение.
Результаты оценки представлены на фиг.1, фиг.2-A и фиг.2-B. На фигурах на вертикальной оси показана ΔvF тестового балла в тесте фон Фрея, и более высокий балл указывает на более сильное анальгезирующее действие. По горизонтальной оси на фиг.1 показано время после введения тестируемого соединения и на фиг.2 представлено, как обрабатывали каждую группу.
Статистическое сравнение группы, обработанной носителем, и группами, обработанными лекарственными средствами, в каждый момент времени проводили с использованием критерия Даннета после того, как находили достоверные зависимости между группами посредством анализа two-way ANOVA (с уровнем значимости менее 5%). Символ # на фигурах указывает значимое отличие (###p<0,001) от группы, обработанной носителем. Статистическое сравнение группы, одновременно обработанной 3 мг/кг прегабалина и 0,3 мг/кг соединения 3 (прегабалин + соединение 3 на фиг.2), и теоретического общего значения проводили с использованием t-критерия Стьюдента, после того как находили равными дисперсии с использованием критерия Фишера (с уровнем значимости менее 5%). Символ * на фигурах указывает значимое отличие (*p<0,05, **p<0,01) от теоретического общего значения.
В группе, обработанной 3 мг/кг одного прегабалина (прегабалин на фиг.1 и фиг.2), анальгезирующее действие не наблюдали в какие-либо моменты времени через 1 час, 2 часа и 3 часа после введения. Также в группе, обработанной 0,3 мг/кг одного соединения 3 (соединение 3 на фиг.1 и фиг.2), анальгезирующее действие не наблюдали в какие-либо моменты времени через 1 час, 2 часа и 3 часа после введения.
С другой стороны, в группе комбинированной обработки (прегабалин + соединение 3 на фиг.1 и фиг.2) статистически значимое сильное анальгезирующее действие наблюдали через 1 час и 2 часа после введения по сравнению с группой, обработанной носителем (носитель на фиг.1 и фиг.2). Кроме того, найдено статистически значимое отличие между теоретическим общим значением (теоретическое общее значение на фиг.2) и группой комбинированной обработки (прегабалин + соединение 3 на фиг.2) на моменты времени 1 час и 2 часа после введения. Эти результаты ясно указывают, что соединение (I) и лиганд α2δ кальциевых каналов синергически усиливают анальгезирующее действие друг друга при комбинированном использовании.
Пример 2. Комбинированное действие соединения (I) и лиганда α2δ кальциевых каналов в тесте "беличье колесо" на мышах
Для оценки использовали 8 самцов мышей ddY в возрасте 5 недель для одной экспериментальной группы. Тестируемое соединение, группирование мышей, используемый носитель и способ введения являлись такими же, как в примере 1.
Мышей помещали в устройство "беличье колесо" (NATSUME SEISAKUSHO) через 0,5 часов после введения тестируемого соединения и подсчитывали количество оборотов беличьего колеса в течение периода времени в 1 час непосредственно для последующей оценки ингибирующего действия на двигательную активность.
Результаты оценки представлены на фиг.3. По вертикальной оси показано количество оборотов в тесте "беличье колесо". Более высокое значение указывает на то, что мыши являются более физически активными. По горизонтальной оси показано, как обрабатывали каждую группу.
Статистическое сравнение группы, обработанной носителем (носитель на фиг.3), и групп, обработанных лекарственным средством, проводили с использованием t-критерия Стьюдента после того, как находили равными дисперсии с использованием критерия Фишера (с уровнем значимости менее 5%).
Не обнаружено статистически значимое ингибирующее действие на двигательную активность в группе, обработанной 3 мг/кг одного прегабалина (прегабалин на фиг.3), и в группе, обработанной 0,3 мг/кг одного соединения 3 (соединение 3 на фиг.3). Кроме того, также не обнаружено статистически значимое ингибирующее действие на двигательную активность в группе, одновременно обработанной 3 мг/кг прегабалина и 0,3 мг/кг соединения 3 (прегабалин + соединение 3 на фиг.3). Эти результаты ясно указывают, что комбинированное применение соединения (I) и лиганда α2δ кальциевых каналов, каждого в дозе, не оказывающей негативного воздействия на центральную нервную систему, не оказывает негативного воздействия на центральную нервную систему.
Сравнительный пример 1. Действие лиганда α2δ кальциевых каналов в моделях нейропатической боли на мышах
Таким же образом, как в примере 1, оценивали действие при пероральном введении 1, 3, 10 и 30 мг/кг одного прегабалина через 1 час после введения на моделях нейропатической боли на мышах.
Результаты оценки представлены на фиг.4. Статистическое сравнение группы, обработанной носителем (носитель на фиг.4), и групп, обработанных прегабалином (1 мг/кг прегабалина, 3 мг/кг прегабалина, 10 мг/кг прегабалина и 30 мг/кг прегабалина на фиг.4), проводили с использованием критерия Уильямса (one-way) после того, как находили равными дисперсии с использованием критерия Бартлетта (с уровнем значимости менее 5%). Символ * на фигуре обозначает значимое отличие (*p<0,025) от группы, обработанной носителем.
При пероральном введении 1 или 3 мг/кг прегабалина не наблюдали анальгезирующего действия. С другой стороны, наблюдали статистически значимое анальгезирующее действие при пероральном введении 10 или 30 мг/кг одного прегабалина. Кроме того, предполагают, что анальгезирующее действие 30 мг/кг прегабалина находилось приблизительно на том же уровне, что и при комбинированном введении 3 мг/кг прегабалина и 0,3 мг/кг соединения 3.
Сравнительный пример 2. Действие лиганда α2δ кальциевых каналов в тесте "беличье колесо" на мышах
Таким же образом, как в примере 2, оценивали ингибирующее действие на двигательную активность при пероральном введении 30 и 100 мг/кг прегабалина.
Результаты оценки представлены на фиг.5. Статистическое сравнение группы, обработанной носителем (носитель на фиг.5), и групп, обработанных 30 и 100 мг/кг прегабалина (30 мг/кг прегабалина и 100 мг/кг прегабалина на фиг.5, соответственно), проводили с использованием критерия Уильямса (one-way) после того, как находили равными дисперсии с использованием критерия Бартлетта (с уровнем значимости менее 5%). Символ * на фигуре обозначает значимое отличие (*p<0,025) от группы, обработанной носителем.
Пероральное введение 30 или 100 мг/кг одного прегабалина статистически значимо уменьшало количество оборотов, таким образом, подтверждая ингибирующее действие на двигательную активность.
Применимость в промышленности
Настоящее изобретение представляет собой средство, содержащее в качестве активных ингредиентов соединение (I) и лиганд α2δ кальциевых каналов, и его можно использовать в качестве фармацевтического, особенно в качестве терапевтического средства или профилактического средства для нейропатической боли.




Изобретение относится к терапевтическому средству для лечения или профилактики нейропатической боли, содержащему в качестве активных ингредиентов производное циклогексана, представленное следующей ниже формулой, или его фармацевтически приемлемую соль, и лиганд α2δ кальциевых каналов, который представляет собой прегабалин или габапентин. Терапевтическое средство обладает синергически увеличенным анальгезирующим действием при дозе, при которой лиганд α2δ кальциевых каналов не оказывает каких-либо побочных эффектов, а также при которой средство не оказывает каких-либо новых побочных эффектов на центральную нервную систему. 2 з.п. ф-лы, 5 ил., 5 табл., 4 пр.
1. Терапевтическое или профилактическое средство для лечения или профилактики нейропатической боли, где указанное средство содержит в качестве активных ингредиентов производное циклогексана, представленное формулой (I)
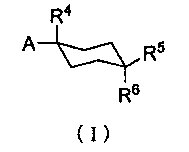
где
А представляет собой заместитель, представленный формулой (IIa)

каждый R1 и R2 независимо представляет собой C1-C4 алкильную группу или C1-C4 алкоксигруппу;
R3 представляет собой атом водорода;
R4 представляет собой гидроксильную группу;
каждый R5 и R6 независимо представляет собой атом водорода или гидроксильную группу;
каждый R7 и R8 независимо представляет собой атом водорода;
Z представляет собой метиновую группу;
или его фармацевтически приемлемую соль;
и лиганд α2δ кальциевых каналов, который представляет собой прегабалин или габапентин.
2. Терапевтическое или профилактическое средство по п. 1, где каждый R1 и R2 независимо представляет собой метильную группу или метоксигруппу.
3. Терапевтическое или профилактическое средство по п. 1 или 2, где R1 представляет собой метильную группу и R2 представляет собой метоксигруппу.
| ПРОИЗВОДНОЕ ЦИКЛОГЕКСАНА И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2009 |
|
RU2478621C2 |
| WO 2004016259 A1, 26.02.2004 | |||
| WO 2005016331 A1, 24.02.2005 | |||
| Способ изготовления древесностружечных плит | 1981 |
|
SU1027050A1 |
| US 6942876 B2, 13.09.2005 | |||
Авторы
Даты
2015-03-20—Публикация
2011-07-29—Подача