Хлорзамещенные фенилендиамины представляют интерес в качестве мономеров для термостойких огнестойких высокопрочных волокон, пленок и лаков.
Известен способ получения 2-хлор-1,4-фенилендиамина (2,5-диаминохлорбензола (ХПФДА)) электрохимическим восстановлением 2-хлор-4-нитроанилина (ХНА) (А.с. SU 1511257, МПК C07C 87/60, опубл. 30.09.1989). Недостатком способа является использование дорогостоящего платинового анода, очень высокая коррозионная активность рабочей среды [9,4-12% HCl или H2SO4, 0,4-0,8% TiCl4, TiCl3, Ti(SO4)2, Ti2(SO4)3 в воде], образование примесей в процессе восстановления, о чем свидетельствует фиолетовая окраска электролита.
Известен способ получения 2-хлор-1,4-фенилендиамина каталитическим гидрированием ХНА водородом под давлением до 10 МПа на стационарном платиновом катализаторе в среде этилацетата (Патент RU 2083540, МПК C07B 31/00, опубл. 10.07.1997). Условия выделения продукта, показатели его качества и выход не приведены. Недостаток способа - проведение процесса под высоким давлением, обуславливающим необходимость применения дорогостоящего оборудования.
Известен способ получения 2,5-дихлор-1,4-фенилендиамина восстановлением 2,5-дихлор-4-нитроацетанилида железными опилками в среде воды в присутствии муравьиной кислоты и диспергатора с последующим гидролизом 2,5-дихлор-4-амино-1-ацетанилида (А.с. ЧССР CS195789, МПК C07C 87/60, опубл. 15.05.1982). После завершения восстановления реакционную массу нейтрализуют окисью магния. Выход 2,5-дихлор-4-аминоацетанилида на стадии восстановления составляет 68% от теоретического. Деацетилирование проводят гидролизом 2,5-дихлор-4-аминоацетанилида в присутствии двукратного мольного избытка серной кислоты с последующей очисткой активированным углем и кизельгуром. Свободное основание выделяют нейтрализацией кальцинированной содой с последующей промывкой водой и сушкой. Выход 2,5дихлор-1,4-фенилендиамина на стадии деацетилирования 89,8%. Таким образом, суммарный выход целевого фенилендиамина на стадиях восстановления и деацетилирования лишь 61% от теоретического. Какие-либо характеристики полученного продукта в описании не приведены. Отмечается, что он может быть использован в качестве сырья при получении азопигментов для крашения пластмасс и волокон. Процесс характеризуется громоздкостью, низким выходом. Очевидно, что предложная методика не обеспечивает получение 2,5-дихлор-1,4-фенилендиамина мономерной степени чистоты.
Известен способ получения 2,5-дихлор-1,4-фенилендиамина восстановлением 4-нитро-2,5-дихлоранилина избытком гидразингидрата в присутствии хлорида железа и активированного угля в среде этилового спирта (Китайский пат. 1974540, C07C 209/36, опубл. 06.06.2007). Выход 2,5-дихлор-1,4-фенилендиамина 93%, содержание основного вещества 99,5% (высокоэффективная жидкостная хроматография, ВЭЖХ), температура плавления 164-165°C. Недостаток способа - использование дорогостоящего сильно ядовитого гидразингидрата.
Известен способ получения 4-хлор-1,3-фенилендиамина каталитическим гидрированием 2,4-динитрохлорбензола (ДНХБ) в смеси сложного эфира и спирта под давлением водорода до 7 МПа в присутствии катализатора платина на угле (Патент Великобритании GB 1417662, МПК B07J 23/00, C07C 209/96, опубл. 10.12.1975). Гидрирование протекает при температуре 60-140°C. После завершения гидрирования растворитель удаляют вакуумной дистилляцией. Кубовый остаток перекристаллизовывают из воды с получением 4-хлор-1,3-фенилендиамина с температурой плавления 88-91°C и степенью чистоты 97%. Выход целевого продукта 89% от теоретического. Недостаток метода низкая степень чистоты продукта в случае использования его в качестве мономера при получении высокомолекулярного полимера.
Известно также, что основной проблемой при выделении орто-, мета- и пара-фенилендиаминов высокой степени чистоты является их склонность к окислению кислородом, всегда присутствующим в растворенном виде в воде и органических растворителях. Так 1,4-фенилендиамин и его замещенные в ядре производные легко окисляются в хинондиимин,
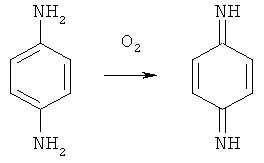
который далее реагирует с 1,4-фенилендиамином с образованием индаминового красителя, подвергающегося дальнейшим превращениям в результате реакций окисления и конденсации [J.F. Corbett. J. Chem. Soc. Perkin Trans, II, 1972, №8, p.999-1005; А.А. Кирюшкин, И.Н. Ковальчук, X.M. Аванесова, А.Ю. Шибаев. Журн. орг. хим., том. XX, вып.5, 1052-1055 (1984)]
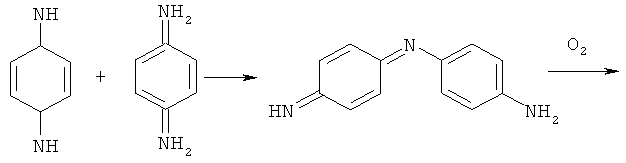
Поэтому при выделении хлорзамещенного фенилендиамина отгонкой растворителя при нагревании протекают процессы окисления и осмоления целевых продуктов, сопровождающиеся снижением выхода и отложением смолистых веществ на внутренних поверхностях аппаратуры.
Наиболее близким к предлагаемому способу является способ, описанный в патенте GB 1417662.
Задачей предлагаемого изобретения является усовершенствование процесса получения хлорзамещенных фенилендиаминов, заключающееся в повышении их качества путем предотвращения окисления и образования продуктов уплотнения (конденсации) в процессе выделения.
Поставленная задача решается предлагаемым способом получения хлорзамещенных фенилендиаминов, например, таких как 4-хлор-1,3-фенилендиамин, 2-хлор-1,4-фенилендиамин, 2,6-дихлор-1,4-фенилендиамин, 2,5-дихлор-1,4-фенилендиамин восстановлением соответствующих хлорзамещенных динитробензолов или хлорзамещенных нитроанилинов в среде растворителя с последующим выделением целевого продукта.
Предлагаемый способ отличается тем, что раствор продуктов восстановления после отделения от каталитической системы или восстановительной среды обрабатывают минеральной кислотой, выделяют хлорзамещенный фенилендиамин в виде соли минеральной кислоты и далее хлорзамещенный фенилендиамин выделяют в виде свободного основания обработкой его соли щелочным агентом в присутствии антиокислителя с последующей экстракцией органическим растворителем, и далее из раствора в органическом растворителе кристаллизацией.
В качестве растворителя для проведения процесса восстановления используют один из ряда: вода, диметилацетамид (ДМАА), диметилформамид (ДМФА), N-метилпиролидон (NМП), метиловый спирт, этиловый спирт, изопропиловый спирт, смеси указанных растворителей с водой, этилацетат, бензол или толуол.
Восстановление ведут водородом в присутствии катализатора или железом. В качестве катализатора восстановления водородом используют платину, палладий или другие металлы платиновой группы на носителе или палладий, модифицированный никелем и железом на носителе, или скелетный никель или никель-хромовый. Процесс восстановления может быть осуществлен как периодическим так и непрерывным способом. Восстановление железом проводят в водосодержащем растворителе в присутствии электролита, например NH4Cl или FeCl2.
В качестве минеральной кислоты используют одну из ряда соляная, серная, фосфорная или газообразный хлорид водорода.
В качестве щелочного агента для выделения хлорзамещенного фенилендиамина из соли используют гидроксид натрия, гидроксид калия, гидроксид кальция, окись кальция, карбонат натрия, карбонат калия, карбонат кальция, сульфит натрия, сульфит калия.
В качестве антиокислителя в процессе выделения хлорзамещенного фенилендиамина из соли используют сульфит натрия (Na2SO3) или сульфит калия (K2SO3) или пиросульфит натрия (Na2S2O5) или гидразингидрат.
В качестве органического растворителя для экстракции в процессе выделения хлорзамещенного фенилендиамина из соли используют один из ряда метиленхлорид, хлороформ, этиацетат, бензол, толуол, гексан, гептан, петролейный эфир, бензин-растворитель (нефрас) или смесь растворителей из ряда.
С целью более полного выделения минеральной соли хлорзамещенного фенилендиамина после восстановления из таких растворителей, как амидные, вода или их смеси, растворимость минеральной соли хлорзамещенного фенилендиамина может быть понижена путем добавления растворителей, в которых эти соли малорастворимы. К таким растворителям относятся низшие алифатические спирты, ацетон, алифатические и ароматические углеводороды (таблица).
При необходимости соли хлорзамещенных фенилендиаминов могут быть очищены перекристаллизацией из водных растворов соответствующих кислот в присутствии активированного угля. При этом кислотные маточники, образующиеся после отделения соли, могут быть снова использованы для перекристаллизации новой порции соли. Таким образом достигается малоотходность стадии перекристаллизации соли.
Предлагаемый способ позволяет значительно усовершенствовать процесс получения хлорзамещенного фенилендиамина, предотвращает осмоление в процессе выделения, обеспечивает повышения качества продукта. Соли минеральных кислот хлорзамещенных фенилендиаминов устойчивы при хранении на воздухе, их можно накапливать и использовать по мере необходимости, тогда как при хранении свободных хлорзамещенных фенилендиаминов необходимо принимать специальные меры предосторожности, которые все равно не обеспечивают достаточной стабильности целевых продуктов
Изобретение иллюстрируется следующими примерами, которые не призваны дать исчерпывающее описание метода.
Пример 1. Синтез 4-хлор-1,3-фенилендиамина (ХМФДА)
В реактор из нержавеющей стали емкостью 0,5 дм3, снабженный мешалкой, рубашкой для обогрева и охлаждения, штуцерами ввода и вывода газа, донным клапаном, обогреваемым фильтром и приемником раствора продуктов гидрирования, загружают 40,5 г 4-хлор-1,3-динитробензола, 150 см3 этилацетата, 100 см3 этилового спирта и 2,0 г катализатора 2% Pt/C. Восстановление ведут при температуре 50-110°С под давлением водорода 5,0 МПа. После завершения поглощения водорода раствор продуктов гидрирования отфильтровывают от катализатора и вводят 23 см3 60%-ной серной кислоты, что соответствует 5%-ному молярному избытку по отношению к теоретическому количеству 4-хлор-1,3-фенилендиамина (ХМФДА). Сразу выпадает белый с сиреневым оттенком осадок моносернокислой соли 4-хлор-1,3-фенилендиамина (ХМФДА·H2SO4). Суспензию отфильтровывают с отсасыванием, осадок соли промывают спиртом и высушивают. Выход соли 46,2 г (96% от теоретического), содержание серной кислоты (титриметрия) 41% (100,6% от теоретического).
42,0 г соли ХМФДА·H2SO4 помещают в 200 см3 2%-ного водного раствора сульфита натрия (Na2SO3, восстановитель), и нейтрализуют водным раствором гидроксида натрия до pH 7.5. Основание ХМФДА экстрагируют метиленхлоридом. Растворитель отгоняют в роторном испарителе. Получают 22,9 г 4-хлор-1,3-фенилендиамина (92% от теоретического). Порошок белого цвета с лиловатым оттенком. Температура плавления 90-91°C, содержание основного вещества 99,2% (определено методом газожидкостной хроматографии - GC).
Пример 2. Синтез 4-хлор-1,3-фенилендиамина (ХМФДА)
В трехгорлую колбу емкостью 250 см3 помещают 75 г порошка распыленного железа, 50 см3 воды, 10 см3 диметилацетамида и 8 см3 концентрированной соляной кислоты. Смесь нагревают при перемешивании до 90°C и постепенно вводят раствор 30 г 4-хлор-1,3-динитробензола в 30 см3 диметилацетамида. Далее смесь перемешивают при нагревании 0,5 час, фильтруют от осадка оксида железа, промывают осадок гидроксида железа 20 см3 диметилацетамида, присоединяя промывной фильтрат к основному фильтрату. Объединенные фильтраты - раствор ХМФДА в водном диметилацетамиде охлаждают до 10°C и вводят 17,2 см3 60%-ной серной кислоты. Далее вводят 100 см3 изопропилового спирта и оставляют на 2 часа в холодильнике для созревания осадка. Суспензию соли фильтруют, осадок соли промывают изопропиловым спиртом. Выход соли ХМФДА·H2SO4 31,9 г (89,5%), содержание H2SO4 40,6% (99,6% от теоретического).
30,0 г соли ХМФДА·H2SO4 помещают в 150 см3 2%-ного водного раствора сульфита калия (K2SO3, восстановитель) и нейтрализуют водным раствором гидроксида калия до pH 7,5. Основание - ХМФДА экстрагируют хлороформом. Растворитель отгоняют в роторном испарителе. Получают 16,7 г (94%) ХМФДА. Белый порошок с лиловатым оттенком. Температура плавления 90-91°C, содержание основного вещества 99,0% (GC).
Пример 3. Синтез 4-хлор-1,3-фенилендиамина (ХМФДА)
Синтез проводят в реакторе, описанном в примере 1. В реактор загружают 30 г 2,4-динитрохлорбензола (ДНХБ), 300 см3 бензола и 2 г катализатора 0,5% Pt/C. Восстановление ведут при температуре 30-60°C и давлении водорода 5,0 МПа. После завершения поглощения водорода раствор продуктов гидрирования отфильтровывают от катализатора. Отгонкой 1/4 объема растворителя удаляют реакционную воду в виде азеотропа с бензолом и в обезвоженный раствор пропускают ток хлорида водорода. Дигидрохлорид 4-хлор-1,3-фенилендиамина выделяется из раствора в виде белого кристаллического осадка, который отфильтровывают и высушивают. Получают дигидрохлорид 4-хлор-1,3-фенилендиамина с содержанием хлорида водорода 33,86% масс. (теоретическое содержание хлорида водорода 33,84% масс.). Выход дигидрохлорида 31,45 г (98,5% от теоретического). Нейтрализацией дигидрохлорида в водной суспензии, используя в качестве нейтрализующего агента карбонат натрия, в качестве антиокислителя сульфит натрия и в качестве экстрагента бензол, получают 17,31 г 4-хлор-1,3-фенилендиамина (82% от теоретического на ДНХБ). Светло-серый порошок с лиловатым оттенком. Температура плавления 90-91°C. Содержание основного вещества 99,4% (GC).
Пример 4. Синтез 2-хлор-1,4-фенилендиамина (ХПФДА)
В реактор, описанный в примере 1, загружают 19 г 2-хлор-4-нитроанилина (ХНА), 170 см3 этилацетата и 1,0 г катализатора 2% Pt/C. Восстановление ведут при температуре 30-50°C и давлении водорода 2,0 МПа. После завершения поглощения водорода раствор продуктов гидрирования отфильтровывают от катализатора и обрабатывают 20 см3 36,0%-ной соляной кислоты. Суспензию дигидрохлорида 2-хлор-1,4-фенилендиамина (ДГХ ХПФДА) фильтруют, осадок промывают 20%-ной соляной кислотой. ДГХ ХПФДА - белый порошок. Содержание хлорида водорода 33,9% (теоретическое содержание хлорида водорода 33,84% масс.). Выход 23,26 г (98% от теоретического).
20 г соли ДГХ ХПФДА помещают в 80 см3 бензола и нейтрализуют при перемешивании 10%-ным водным раствором гидроксида натрия, содержащим 1,5% сульфита натрия. Слои разделяют, водный слой промывают 50 см3 бензола. Бензольные вытяжки объединяют и отгоняют бензол в роторном испарителе. Получают 12,7 г ХПФДА (96,0% от теоретического). Кристаллический плав белого цвета с легким бежевым оттенком. Температура плавления 65,5°C. Цветность 1,0 ед. Содержание основного вещества 99,8% (GC).
Пример 5. Синтез 2-хлор-1,4-фенилендиамина (ХПФДА)
В реактор, описанный в примере 1, загружают 19 г 2-хлор-4-нитроанилина, 170 см3 изопропилового спирта и 1,0 г катализатора 0,5% Pt/C. Восстановление ведут при температуре 30-50°C и давлении водорода 2,0 МПа. После завершения поглощения водорода раствор продуктов гидрирования фильтруют от катализатора и обрабатывают 12,6 см 60%-ной серной кислоты. Сразу выпадает моносернокислая соль ХПФДА (ХПФДА·H2SO4). Суспензию фильтруют, осадок промывают изопропиловым спиртом. Белый порошок с легким лиловатым оттенком. Выход 25,97 г (98% от теоретического). Содержание серной кислоты 40,8% (100,1% от теоретического).
25,0 г соли ХПФДА·H2SO4 помещают в 80 см3 2%-ного водного раствора сульфита натрия (Na2SO3, антиокислитель) и нейтрализуют водным раствором гидроксида натрия до pH 7,5. Основание - ХПФДА экстрагируют при 50°C смесью бензол:гексан. Экстракт охлаждают до 5°C. При этом выкристаллизовывается ХПФДА. Суспензию фильтруют, осадок промывают гексаном и высушивают. Выход 13,8 г (93%). Белый кристаллический порошок с легким лиловатым оттенком. Температура плавления 65,5°C, цветность 1,8 ед. Содержание основного вещества 99,6% (GC).
Пример 6. Синтез 2-хлор-1,4-фенилендиамина (ХПФДА)
В реактор, описанный в примере 1, загружают 38 г 2-хлор-4-нитроанилина, 170 см3 диметилацетамида и 4,0 г катализатора 0,5% Pt/Al1O3. Восстановление ведут при температуре 40-50°C и давлении водорода 2,0 МПа. После завершения поглощения водорода и отделения катализатора в гидрогенизат вводят 200 см3 изопропилового спирта и 25,2 см3 60%-ной серной кислоты. Выпавшую в осадок моносернокислую соль ХПФДА·H2SO4 отфильтровывают и промывают ацетоном. Белый порошок. Выход соли ХПФДА·H2SO4 51,4 г (97% от теоретического). Содержание H2SO4 в соли 40,8% (100,1% от теоретического).
40,0 г соли ХПФДА·H2SO4 помещают в 130 см3 2%-ного водного раствора сульфита натрия, вводят 100 см3 бензола и нейтрализуют водным раствором гидроксида натрия до pH 7,5. Бензольный слой отделяют. Водный слой промывают еще 100 см3 бензола. Бензольные вытяжки объединяют, упаривают в роторном испарителе до половины начального объема. Концентрат охлаждают, выпавшие кристаллы ХПФДА отфильтровывают и высушивают. Выход 19,4 г (82% от теоретического). Белый кристаллический порошок с лиловатым оттенком. Температура плавления 65°C. Цветность 1,8 ед. Содержание основного вещества 99,8% (GC).
Из бензольного маточника выделяют дополнительное количество продукта, который подвергают очистке.
Пример 7. Синтез 2-хлор-1,4-фенилендиамина (ХПФДА)
Синтез проводят аналогично описанному в примере 6, используя в качестве катализатора 0,8% Pd/C. Получают 50,3 г (94,9% от теоретического) соли ХПФДА·H2SO4. Белый порошок. Содержание H2SO4 в соли 40,84% (100,2% от теоретического). 40 г соли ХПФДА·H2SO4 нейтрализуют аналогично описанному в примере 6. Получают 19,0 г ХПФДА (80,3% от теоретического). Белый кристаллический порошок с лиловатым оттенком. Температура плавления 65°C. Цветность 2,3 ед. Содержание основного вещества 99,2% (GC).
Пример 8. Синтез 2-хлор-1,4-фенилендиамина (ХПФДА)
Синтез проводят аналогично описанному в примере 6, используя в качестве катализатора смешанный катализатор НПФ-1 0,2% Pd; 0,2% Ni; 0,2% Fe/C. Получают 50,1 г соли ХПФДА·H2SO4 (94,5% от теоретического). Белый порошок. Содержание H2SO4 в соли 40,80% (100,1% от теоретического). 40 г соли ХПФДА·H2SO4 нейтрализуют аналогично описанному в примере 6. Получают 19,2 г ХПФДА (81,1% от теоретического). Белый кристаллический порошок с лиловатым оттенком. Температура плавления 65°C. Цветность 3,4 ед. Содержание основного вещества 99,3% (GC).
Пример 9. Синтез 2-хлор-1,4-фенилендиамина (ХПФДА)
Синтез проводят аналогично описанному в примере 6, используя в качестве катализатора скелетный никель (никель Ренея). Получают 49,7 г (93,2% от теоретического) соли ХПФДА·H2SO4. Содержание H2SO4 в соли 40,84% (100,2% от теоретического). Белый порошок. 40 г соли ХПФДА·H2SO4 нейтрализуют аналогично описанному в примере 6. Получают 18,9 г ХПФДА (79,8% от теоретического). Белый кристаллический порошок с лиловатым оттенком. Температура плавления 65°C. Цветность 2,8 ед. Содержание основного вещества 99,1% (GC).
Пример 10. Синтез 2-хлор-1,4-фенилендиамина (ХПФДА)
Каталитическое гидрирование проводят в реакторе, описанном в примере 1.
В реактор загружают 38 г 2-хлор-4-нитроанилина 170 см3 этилацетата и 4 г катализатора 0,5% Pt/Al2O3. Восстановление ведут при температуре 40-50°C и давлении водорода 2,0 МПа. После завершения поглощения водорода и отделения катализатора в гидрогенизат вводят по каплям 15,7 г 88,5%-ной ортофосфорной кислоты. Температура раствора при этом повышается с 30 до 34°C. Через несколько минут после окончания добавления ортофосфорной кислоты начинает выделяться белый осадок. После выдержки в холодильнике в течение 2 часов при 10°C суспензию фильтруют, осадок на фильтре промывают этилацетатом и высушивают. Выход монофосфорнокислой соли ХПФДА·H3PO4 51,94 г (98% от теоретического). Порошок белого цвета. Содержание Н3РО4 40,732% (100,0% от теоретического).
40 г соли ХПФДА·H3PO4 помещают в 130 см3 2%-ного водного раствора сульфита калия, вводят 100 см3 этилацетата и нейтрализуют водным раствором гидроксида калия до pH 7,5. Этилацетатный слой отделяют. Водный слой промывают 100 см3 этилацетата. Этилацетатные вытяжки объединяют и этилацетат отгоняют в роторном испарителе. Выход ХПФДА 21,1 г (97,5% от теоретического). Белый кристаллический плав с бежеватым оттенком. Температура плавления 65°С, цветность 1,2 ед. Содержание основного вещества 99,7% (GC).
Пример 11. Синтез 2-хлор-1,4-фенилендиамина (ХПФДА)
В трехгорлую колбу емкостью 1 дм3, снабженную мешалкой, обратным холодильником и термометром, загружают 600 см3 воды, 117 г порошка железа и 10 см3 концентрированной соляной кислоты. Смесь нагревают при перемешивании и постепенно вводят 78 г 2-хлор-4-нитроанилина. После завершения добавления массу нагревают еще 0,5 часа при перемешивании. Раствор продуктов восстановления отделяют от железного шлама и в него постепенно вводят 52 см3 60%-ной серной кислоты. Сразу выделяется белый осадок соли ХПФДА·H2SO4. Суспензию соли фильтруют, осадок промывают водой. Выход моносернокислой соли ХПФДА·H2SO4 94,7 г (87% от теоретического). Содержание H2SO4 в соли 41,1% масс. (100,9% от теоретического).
80 г соли ХПФДА·H2SO4 помещают в 260 см3 2%-ного водного раствора сульфита натрия, вводят 200 см бензола и нейтрализуют водным раствором гидроксида натрия до pH 8,0. Бензольный слой отделяют. Водный слой промывают еще 100 см3 бензола. Бензольные вытяжки объединяют, упаривают в роторном испарителе. Концентрат охлаждают, выпавшие кристаллы ХПФДА отфильтровывают и высушивают. Выход ХПФДА 40,7 г (85,9% от теоретического). Белый кристаллический порошок с легким лиловатым оттенком. Температура плавления 65,0°C. Цветность 1,6 ед. Содержание основного вещества 99,8% (GC).
Обработкой бензольного маточника 60%-ной серной кислотой получают дополнительное количество ХПФДА·H2SO4.
Пример 12. Синтез 2,6-дихлор-1,4-фенилендиамина (2,6-ДХПФДА)
В трехгорлую колбу емкостью 500 см3, снабженную мешалкой, обратным холодильником и термометром, загружают 150 см3 воды, 150 см3 диметилацетамида, 30 г железного порошка и 2 см3 концентрированной соляной кислоты, которая, взаимодействуя с железом, дает электролит - хлористое железо FeCl2. Смесь при перемешивании нагревают до кипения, охлаждают до 90°C и постепенно вводят 36,0 г 2,6-дихлор-4-нитроанилина (2,6-ДХНА). Реакционную массу фильтруют в горячем состоянии от железного шлама в атмосфере азота и к фильтрату добавляют 156 см3 36,3%-ной соляной кислоты. Суспензию дигидрохлорида 2,6-дихлор-1,4-фенилендиамина (ДГХ 2,6-ДХПФДА) фильтруют, осадок промывают 20%-ной соляной кислотой. Соль ДГХ 2,6-ДХПФДА - белый порошок, содержание хлорида водорода 29,25% масс. (теоретическое содержание хлорида водорода 29,2% масс.). Выход 40,0 г (92% от теоретического).
30 г соли ДГХ 2,6-ДХПФДА помещают в 100 см3 2%-ного водного раствора сульфита натрия, вводят 100 см3 хлороформа и нейтрализуют водным раствором гидроксида натрия до pH 7,5. Хлороформный слой отделяют. Водный слой промывают 50 см3 хлороформа. Из объединенных хлороформных вытяжек отгоняют растворитель в роторном испарителе. Выход 2,6-ДХПФДА 18,9 г (89,0% от теоретического). Белый кристаллический порошок. Температура плавления 124°C. Содержание основного вещества 99,1% (GC).
Пример 13. Синтез 2,5-дихлор-1,4-фенилендиамина (2,5-ДХПФДА)
Восстановление проводят аналогично описанному в примере 12, используя 36,0 г 2,5-дихлор-4-нитроанилина. Выделение дигидрохлорида 2,5-дихлор-1,4-фенилендиамина (ДГХ 2,5-ДХПФДА) из раствора продуктов восстановления проводят после отделения железного шлама, подавая при перемешивании под слой раствора продуктов восстановления через барботер 30 г газообразного хлорида водорода. Выделившиеся кристаллы ДГХ 2,5-ДХПФДА отфильтровывают. ДГХ 2,5-ДХПФДА - белый порошок. Содержание хлорида водорода 29,3% масс.(100,34% от теоретического), выход 41,3 г (95% от теоретического). Нейтрализацией 30,0 г соли ДГХ 2,5-ДХПФДА, аналогично описанной в примере 12, получают 19,8 г 2,5-ДХПФДА (93,2%, от теоретического). Кристаллический порошок. Температура плавления 165°C. Содержание основного вещества 99,3% (GC).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРЗАМЕЩЕННЫХ 4,4'-ДИАМИНОБЕНЗАНИЛИДОВ | 2013 |
|
RU2547268C2 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРЗАМЕЩЕННЫХ 4,4-ДИАМИНОБЕНЗАНИЛИДОВ | 2007 |
|
RU2385861C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2-ХЛОР-1,4-ФЕНИЛЕНДИАМИНА | 2023 |
|
RU2818254C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРЗАМЕЩЕННЫХ АМИНОАНИЛИДОВ АРОМАТИЧЕСКИХ КАРБОНОВЫХ КИСЛОТ | 2006 |
|
RU2323207C1 |
| Способ получения п-фенилендиамина | 1979 |
|
SU825505A1 |
| СПОСОБ ПОЛУЧЕНИЯ 5(6)-АМИНО-2-(4-АМИНОФЕНИЛ)БЕНЗИМИДАЗОЛА ИЗ 2',4,4'-ТРИНИТРОБЕНЗАНИЛИДА | 2013 |
|
RU2547261C2 |
| СПОСОБ ПОЛУЧЕНИЯ N, N-БИС-АЦЕТОАЦЕТАРИЛАМИДОВ | 2005 |
|
RU2283300C1 |
| СПОСОБ ПОЛУЧЕНИЯ 5(6)-АМИНО-2-(4-АМИНОФЕНИЛ)БЕНЗИМИДАЗОЛА | 2013 |
|
RU2547210C2 |
| НОВЫЕ ЦВЕТООБРАЗУЮЩИЕ КОМПОЗИЦИИ И ЗАПИСЫВАЮЩИЙ МАТЕРИАЛ | 2001 |
|
RU2245873C2 |
| ИНСЕКТИЦИДНАЯ КОМПОЗИЦИЯ | 1988 |
|
RU2009642C1 |
Изобретение относится к способу получения хлорзамещенных фенилендиаминов, которые могут быть использованы в качестве мономеров для термостойких огнестойких высокопрочных волокон, пленок и лаков. Способ осуществляют путем восстановления соответствующих хлорзамещенных нитроанилинов или динитробензолов в среде растворителя. Раствор продуктов восстановления обрабатывают минеральной кислотой (соляной, серной или фосфорной или газообразным хлоридом водорода), полученную соль минеральной кислоты переводят в основание обработкой щелочным агентом в присутствии антиокислителя (сульфита натрия, сульфита калия или пиросульфита натрия). Целевое соединение выделяют экстракцией и кристаллизацией. В качестве растворителя в процессе восстановления используют воду, диметилацетамид или смесь диметилацетамида с водой, диметилформамид или смесь диметилформамида с водой, метиловый спирт, этиловый спирт, изопропиловый спирт, этилацетат, бензол или толуол. Процесс восстановления ведут водородом в присутствии катализатора: платины, или палладия, или другого металла платиновой группы на носителе, или палладия, модифицированного никелем или железом, на носителе, или скелетного никеля или никель-хромового. Или восстановление проводят железом в водосодержащем растворителе в присутствии электролита. Технический результат - усовершенствованный способ получения хлорзамещенных фенилендиаминов, позволяющий получить целевые продукты высокого качества за счет предотвращения окисления и образования продуктов уплотнения (конденсации) в процессе выделения. 7 з.п. ф-лы, 1 табл., 13 пр.
1. Способ получения хлорзамещенных фенилендиаминов восстановлением соответствующих хлорзамещенных нитроанилинов или динитробензолов в среде растворителя с последующим выделением целевого продукта, отличающийся тем, что раствор продуктов восстановления обрабатывают минеральной кислотой, образовавшуюся соль отделяют от растворителя и затем переводят в основание обработкой щелочным агентом в присутствии антиокислителя с последующими экстракцией и кристаллизацией.
2. Способ по п.1, отличающийся тем, что в качестве растворителя для восстановления используют один из ряда: вода, диметилацетамид или смесь диметилацетамида с водой, диметилформамид или смесь диметилформамида с водой, метиловый спирт, этиловый спирт, изопропиловый спирт, этилацетат, бензол или толуол.
3. Способ по п.1, отличающийся тем, что восстановление ведут водородом в присутствии в качестве катализатора платины, или палладия, или других металлов платиновой группы на носителе или палладия, модифицированного никелем или железом, на носителе, или скелетного никеля, или никель-хромового.
4. Способ по п.1, отличающийся тем, что восстановление ведут железом в водосодержащем растворителе в присутствии электролита.
5. Способ по п.1, отличающийся тем, что выделение соли хлорзамещенного фенилендиамина из раствора продуктов восстановления ведут в присутствии ацетона или низшего алифатического спирта.
6. Способ по п.1, отличающийся тем, что в качестве минеральной кислоты используют соляную кислоту, или серную кислоту, или ортофосфорную кислоту, или газообразный хлорид водорода.
7. Способ по п.1, отличающийся тем, что в качестве антиокислителя используют сульфит натрия, или сульфит калия, или пиросульфит натрия.
8. Способ по п.1, отличающийся тем, что экстракцию хлорзамещенного фенилендиамина ведут органическим растворителем, одним из ряда: метиленхлорид, хлороформ, этилацетат, бензол, толуол, алифатический углеводород или смесью растворителей из ряда.
| ВИДЕНИНА Р.Ф | |||
| и др., 2,6-дихлор-1,4-фенилендиамин, Методы получения химических реактивов и препаратов, Москва, ИРЕА, 1974, вып.26, с.126-127 | |||
| CS 273921 B1, 11.04.1991 | |||
| CN 101514162 B, 23.05.2012 | |||
| GB 1417662 A, 10.12.1975 | |||
| US 3166594 A1, 19.01.1965 |
Авторы
Даты
2015-04-10—Публикация
2013-08-07—Подача