Изобретение относится к биотехнологии, конкретно к областям медицинской биохимии, диагностической медицинской микробиологии, прикладной иммунохимии и разработке диагностических тест-систем, касается разработки нового способа для высокочувствительного определения белка ботулинического нейротоксина типа А (BoNT/A) в инфицированных образцах биологического происхождения и контаминированных пищевых продуктах, представляет собой способ детекции белка BoNT/A при помощи высокоаффинных поликлональных антител к ботулотоксину типа А, комбинированный с амплификацией специфического сигнала за счет использования сопряженной с антителом ДНК-матрицы для проведения полимеразной цепной реакции.
Основной областью применения предлагаемого способа определения ботулинического нейротоксина типа А являются биомедицина, микробиологическая диагностика, микробиологические исследования, разработка средств ранней и высокоэффективной специфической диагностики ботулизма, санитарно-гигиенический контроль за наличием токсина возбудителя ботулизма в продуктах питания, предотвращение угрозы биотерроризма.
Ботулотоксины представляют собой нейротоксины белковой природы, продуцируемые анаэробными грамположительными спорообразующими бактериями Clostridium botulinum. Токсины ботулизма ответственны за развитие смертельно опасной интоксикации с преимущественно алиментарным путем инфицирования -ботулизма. Семейство ботулотоксинов содержит семь серологически и биохимически отличных типов токсина, секретируемых различными штаммами С.botulinum, и являющихся сильнейшими ядами из всех известных науке органических токсинов в целом, летальная доза которых (LD50) составляет 1-5 нг/кг массы тела. Также отмечены штаммы с одновременной комбинированной продукцией двух серотипов нейротоксинов [Montecucco С, Molgo J. // Current Opinion in Pharmacology. - 2005. - V.5, N. 3. - P. 274-279; Kukreja R, Singh BR. // Microbial Toxins: Current Research and Future Trends. - Caister Academic Press. - 2009 - ISBN 978-1-904455-44-8]. Вариабельность аминокислотных последовательностей различных типов токсинов может оставлять до 70%, однако все они имеют схожую конформацию и вызывают идентичные патофизиологические процессы в организме, но вместе с тем могут иметь неидентичные молекулярные мишени [Capek Р., Dickerson T.J. // Toxins. - 2010. - V.2. - Р. 24-53].
Ботулинический нейротоксин продуцируется в форме неактивного гетеродимера с молекулярной массой 150 kDa, активируемого посредством протеолитического расщепления на легкую цепь (LC), которая представляет собой Zn-зависимую металлопротеазу (50 kDa), и тяжелую цепь (НС), состоящую из связывающего и транслокационного доменов (100 kDa). Легкая и тяжелая цепи связаны посредством дисульфидной связи и множества нековалентных взаимодействий между двумя пептидными цепями [Capek Р., Dickerson T.J. // Toxins. - 2Q10. - V.2. - Р. 24-53].
При интоксикация ботулотоксином происходит блокада выброса ацетилхолина в соматических и вегетативных нервных окончаниях, вызывая паралич мышц. Токсическое действие ботулотоксина проходит в три этапа. На первом этапе происходит специфическое связывание тяжелой цепи токсина с двумя рецепторами на поверхности нервного окончания. Токсин ассоциирует в первую очередь с ганглиозидом (полисиалоганглиозид) с последующей миграцией комплекса к белковому рецептору синаптических везикул - синаптотагмину 1 или 2 (SV1 или SV2) [Rummel A. et al. // Journal of Neurochemistry. - 2009. - V. 110. - P. 1942-1954]. После связывания комплекса с рецепторами инициируется рецепторно-опосредованный эндоцитоз. За эндоцитозом следует высвобождение протеолитического домена ботулотоксина в цитозоль посредством эндосомальной мембранной транслокации. Считается, что снижение значения pH в эндосоме является фактором, вызывающим последующие изменения в конформации токсина. В результате, тяжелая цепь токсина действует как транспортный канал и шаперон, обеспечивающий транслокацию легкой цепи через эндосомальную мембрану и в цитозоль. В цитозоле протеолитический домен действует как металлопротеаза и расщепляет белки SNARE-комплекса, которые выступают частью аппарата экзоцитоза, что приводит к ингибированию высвобождения нейромедиатора ацетилхолина [Simpson L.L. // Annu. Rev. Pharmacol. Toxicol. - 2004. - V.44. - P. 167-193.; Capek P, Dickerson T.J. // Toxins. - 2010. - V.2. - P.24-53].
Основные типы ботулинических нейротоксинов, вызывающие заболевание у человека, составляют типы А, В и Е, из них наиболее тяжелые случаи интоксикации связаны с BoNT/A. В этиологии ботулизма можно выделить две общие категории: первичная интоксикация и первичная инфекция, за которой следует вторичная интоксикация. При первичной интоксикации ботулинические токсины попадают в организм алиментарным путем, с контаминированными С.botulinum продуктами питания, при обработке и заготовке которых сложились условия, удовлетворяющие требованиям роста и развития вегетативной формы клостридий ботулизма. Зрелая культура клостридий подвергается автолизу, в результате чего ботулотоксин выделяется в среду. Таким образом, заражение происходит при употреблении в пищу продуктов, содержащих токсин.
При употреблении пищи, содержащей споры возбудителя ботулизма, способные прорастать в организме человека и колонизировать кишечник, происходит развитие первичной инфекции. В процессе роста, размножения и автолиза токсин выделяется в организм in situ, в результате чего развивается вторичная интоксикация [Simpson L.L. // Annu. Rev. Pharmacol. Toxicol. - 2004. - V. 44.-P. 167-193].
Инкубационный период развития симптомов ботулизма составляет от нескольких часов до пяти суток и зависит от типа и дозы токсина. При попадании ботулинических нейротоксинов в организм человека или при их накоплении вследствие первичной инфекции в первую очередь страдают скелетные мышцы, смертельную опасность представляет паралич дыхательных и висцеральных мышц, также наблюдаются нарушения со стороны вегетативной нервной системы. Выздоровление наступает медленно и может потребовать подключения к аппарату искусственной вентиляции легких, наибольшие сроки восстановительного периода наблюдаются при интоксикации BoNT/A.
Диагностика ботулизма на ранних этапах заболевания, а также определение токсина в подозрительных продуктах питания и своевременно примененная терапия обеспечивают благоприятный прогноз исхода заболевания. Применение в клинической практике специфичных и высокочувствительных диагностических тест систем, способных определять крайне низкие (менее 5 пг/мл) концентрации BoNT/A способно уменьшить риск летального исхода и ускорить выздоровление.
На сегодняшний день в рутинной лабораторной практике диагностики ботулизма применяют комбинацию культурального метода и мышиного летального теста, которая, несмотря на довольно высокую его чувствительность (20 пг/мл BoNT/A), не позволяет получить лабораторное подтверждение заболевания в короткие сроки.
Известны методы, основанные на эндопептидазной активности ботулинического нейротоксина, такие как иммуноблоттинг, FRET (Fluorescence Resonance Energy Transfer - передача энергии посредством флуоресцентного резонанса), позволяющие определять все типы ботулинических токсинов в концентрации от 35 пг/мл до 150 нг/мл в зависимости от серотипа, используемого субстрата и времени экспозиции. Однако эти методы имеют ряд ограничений - они предъявляют высокие требования к условиям реакции, компоненты данных систем подвержены ингибированию, использование сложных матриц обуславливает высокую вероятность неспецифического взаимодействия и приводит к недостаточной специфичности детекции [Dorner М.В., Schulz К.М., Kull S., Dorner B.G.// Curr Top Microbiol Immunol. - 2013. - V. 364. -P. 219-255].
Известно применение масс-спектрометрического метода для определения ботулинических нейротоксинов в формате эндопетдидазной масс-спектрометрии (Endopeptidase-Mass Spectrometry (Endopep-MS) Assay), который обладает высокой чувствительностью (0,05-50 пг/мл), но осуществление подобного типа анализа осложняется необходимостью проведения сложной пробоподготовки и моделирования специфической мишени [Barr J.R., Moura Н., Boyer А.Е. с соавт. // Emerg Infect Dis. - 2005, October. - V. 11. - N.10. - P. 1578-1583.].
Известен традиционно применяемый в практике иммуноферментный анализ (ИФА) и его вариации (иммуноанализ на микросферах, Luminex® хМАР технология, электрохемилюминесценция, DIG-ELISA), однако данные методы не обладают достаточной чувствительностью (0,5-2 нг/мл) для успешного определения ботулотоксина типа А в клинических образцах, особенно в случаях интоксикации средней и легкой тяжести [Abbasova, S., Rudenko, N., Gorokhovatskii с соавт. // Russian Journal of Bioorganic Chemistry. - 2001. - V. 37. - N. 3. - P. 307-315; Dorner M.B., Schulz K.M., Kull S., Dorner B.G. // Curr Top Microbiol Immunol. - 2013. - V. 364. - P. 219-255; Ferreira, J L., Maslanka, S, Johnson, E., and Goodnough, M. // JAOAC International. - 2003. - V. 86. - P. 314-331].
Известно использование классической полимеразной цепной реакции (ПЦР), которое позволяет лишь определить наличие целевого микроорганизма в случае первичной инфекции или исследования подозрительных продуктов питания и сильно зависит от качества и количества детектируемой матрицы, однако, даже детекция специфических фрагментов генома С.botulinum не дает исчерпывающей информации о продукции токсина и его серотипе, так как были обнаружены штаммы С.botulinum, продуцирующие два типа токсина, а также штаммы, несущие ″молчащие″ гены токсина [Santos-Buelga, J. A., Collins М. D., and А. К. East. // Curr. Microbiol. - 1998. - V. 37. - Р. 312-318; G. Franciosa, F. Floridi, A. Maugliani, and P. Aureli. // Appl. Environ. Microbiol. - 2004. - V. 70. - P. 7192-7199].
На данный момент большинство этих методов выявления ботулинических нейротоксинов находится на стадии экспериментальных разработок и не существуют в виде стандартизованных коммерчески доступных диагностических тест-систем.
Известен и активно разрабатывается подход к детекции биологических молекул, объединяющий преимущества специфичности иммунологической детекции с высокой чувствительностью полимеразной цепной реакции [US Patent 5665539]. Данный подход, получивший название иммуно-ПЦР, в своем простейшем варианте основан на иммобилизации антигена на твердой фазе с последующей детекцией его при помощи специфического антитела, ковалентно или нековалентно связанного с ДНК-матрицей, позволяющей провести амплификацию сигнала при помощи ПЦР. Оптимизированными вариантами данного способа являются иммобилизация на твердой фазе антитела к одному из эпитопов антигена и последующая детекция антигена антителом к его другому эпитопу [Komatsu М., Kobayashi D., Saito К. с соавт. // Clin. Chem. - 2001. -V. 47, N. 7. - Р. 1297-1301], повышение чувствительности за счет апмлификации ДНК-матрицы при помощи различных вариантов ПЦР в режиме реального времени с применением флуоресцентной метки [Canto C.L., Sumita L.M., Machado A.F. с соавт. // Rev. Inst. Med. Trop.Sao Paulo. - 2008. - V. 50, N. 1 - P. 61-63], внедрение улучшенных коньюгатов и модификаций матриц ДНК [Niemeyer СМ., Wacker R, and Adler М // Nucleic Acids Res. - 2003. - V. 31, N. 16. - P. 90] и др. Технология иммуно-ПЦР успешно применялась для детекции различных инфекционных патогенов, в частности, для детекции Шига-токсина патогенных штаммов E.coli [Не X., Qi W., Quinones В. с соавт. // Appl. Environ. Microbiol. - 2011. - V. 77, N. 11 - P. 3558-3564], вирусов [Barletta J., Bartolome A., and Constantine N.T. // J. Virol. Methods. - 2009. - V. 157, N. 2 - P. 122-132], стафилококкового энтеротоксина [Fischer A., von Eiff C, Kuczius Т. С соавт. // J. Mol. Med. (Berl). - 2007. - V. 85, N. 5. - P. 461-469] и др.
Известен способ прямой детекции ботулотоксина типа А методом иммуно-ПЦР при использовании 96-луночного планшета, на поверхности лунок которого иммобилизирован токсин. После блокирования активных несвязанных центров планшета к образцам добавляют конъюгат моноклональных антител против BoNT/A с репортерной ДНК. Конъюгат образован через ковалентные связи амино- и сульфгидрильных групп антитела и матричной ДНК. Реакцию амплификации ДНК-матрицы проводят в планшете, результат детектируют проведением электрофореза в агарозном геле. Данный формат позволяет обнаруживать BoNT/A в количестве до 5 пг/мл буфера, но имеет высокую вероятность детекции неспецифических взаимодействий, а также не был адаптирован для проведения анализа в смешанных образцах [Wu НС, Huang YL, Lai SC с соавт. // Lett. Appl. Microbiol. - 2001. - V. 32. - P. 321-325].
Известны варианты метода детекции BoNT/A: непрямая и непрямая сэндвич иммуно-ПЦР. Постановку анализа проводят в 96-луночном планшете, связь детектирующего антитела и ДНК-матрицы осуществляют через взаимодействие биотин-стрептавидин, амплификационная смесь вносят в лунки планшета. Результат детектируют посредством электрофореза в агарозном геле. Непрямая иммуно-ПЦР позволяет определять до 50 фг BoNT/A на реакцию в чистом буфере. Однако использование в качестве твердой фазы поверхности планшета увеличивает вероятность неспецифического связывания компонентов реакции и получения ложноположительного ответа, а также данный метод не оптимизирован для анализа многокомпонентных проб [Chao H-Y, Wang Y-C, Tang S-S с соавт. // Toxicon. - 2004. - V. 43. - P. 27-34].
Известен наиболее технически близкий к заявленному метод иммуно-ПЦР с флуоресцентной детекцией в режиме реального времени по ″конечной точке″ (Endpoint RT-PCR) в формате непрямого сэндвич анализа для обнаружения ботулинических нейротоксинов типов А и В в полуобезжиренном молоке. Связывающие антитела иммобилизуют в лунках планшета, детектирующее антитело конъюгируют с матричной ДНК посредством связи биотин-стрептавидин. Наличие амплифицированной матрицы визуализируют ПЦР в режиме реального времени. Анализ позволяет определить до 3,75 пг BoNT/A в 1 мл молока, однако такая чувствительность недостаточна для детекции интоксикации ботулотоксином на ранних стадиях процесса, а также уступает по этому показателю предлагаемому способу определения токсина типа А возбудителя ботулизма [Rajkovic A., El Moualij В., Fikri Y. с соавт. // Food Anal Methods. - 2012. - V. 5. -Р. 319-326].
Изобретение решает задачу создания высокочувствительного способа идентификации ботулинического нейротоксина типа А на основе иммунодетекции, сопряженной с ПЦР в режиме реального времени, применимого для его выявления в образцах биологических жидкостей и тканей на ранних и поздних этапах развития ботулизма, а также в продуктах питания, употребимого для работы как с инфекционно опасными, так и с инактивированными пробами.
Поставленная задача решается за счет применения метода пробоподготовки, предусматривающего гомогенизацию исследуемого материала с раствором, содержащим ингибиторы протеаз и серии последовательных центрифугирований для удаления материала, затрудняющего проведение тестирования по методу иммунодетекции, сопряженной с ПЦР-амплификацией.
Поставленная задача решается за счет способа детекции ботулинического нейротоксина типа А с помощью поликлональных антител, специфичных к рецептор-связывающему домену тяжелой цепи ботулотоксина А, одно из которых, иммобилизованое на твердом носителе (парамагнитных частицах) за счет взаимодействия с белком G бактерий рода Streptococcus, служит для связывания BoNT/A, находящегося в исследуемой пробе, а второе (биотинилированное) антитело детектирует BoNT/A и посредством мостика, образованного тетравалентной молекулой нейтравидина, связывается с биотинилированными фрагментами ДНК, используемыми в качестве субстрата для ПЦР-амплификации с флуоресцентной детекцией сигнала в режиме реального времени.
Также поставленная задача решается за счет применения покрытых белком G бактерий рода Streptococcus парамагнитных частиц, которые позволяют иммобилизовать на поверхности частиц антитело к ботулотоксину типа А, провести специфическое связывание BoNT/A из жидких образцов, избавиться от содержащихся в образцах загрязнений на ранних этапах эксперимента и провести отделение ДНК-матрицы, применяемой для конечной ПЦР-амплификации, от других компонентов детекционного комплекса.
Также поставленная задача решается за счет высокоаффинных поликлональных антител к рецептор-связывающему домену тяжелой цепи BoNT/A, которые позволяют добиться высокой специфичности анализа. Также поставленная задача решается за счет коньюгата ДНК с нейтравидином, образующего молекулярную ″сетку″, при использовании которой для детекции возможно увеличить количество матричных молекул ДНК, связанных с единичной молекулой биотинилированного антитела и, таким образом, амплифицировать сигнал.
Также поставленная задача решается за счет блокировки поверхности твердой фазы раствором Денхардт-ДНК, которая препятствует неспецифической сорбции коньюгата ДНК-нейтравидин на поверхности магнитных частиц и пробирок стрипов и снижает вероятность ложноположительных результатов эксперимента.
Также поставленная задача решается за счет отделения ДНК-матрицы, применяемой для конечной ПЦР-амплификации, от прочих компонентов образованного детекционного комплекса посредством обработки специфической эндонуклеазой рестрикции, не нарушающей возможность проведения амплификации матричной ДНК с использованием специфичных праймеров в режиме реального времени по методу TaqMan, что способствует снижению фонового сигнала в эксперименте.
Также поставленная задача решается за счет применения в анализе редко встречающейся в окружающей среде ДНК-матрицы, оптимизированной для проведения ПЦР-амплификации с флуоресцентной детекцией сигнала в режиме реального времени, что снижает вероятность возникновения ложноположительного сигнала при детекции, позволяет существенно повысить чувствительность метода и провести количественное определение содержания BoNT/A в исследуемых образцах.
Техническим результатом изобретения является создание эффективного высокочувствительного способа детекции ботулинического нейротоксина типа А, применимого для нужд клинической диагностики и мониторинга качества продуктов питания. Отличием предлагаемого способа является осуществление детекции на базе специфических поликлональных антител к рецептор-связывающему домену тяжелой цепи BoNT/A, одно из которых посредством биотин-нейтравидинового взаимодействия связывается с ДНК, служащей матрицей для проведения ПЦР-амплификации с флуоресцентной детекцией сигнала в режиме реального времени. С использованием разработанного способа можно детектировать BoNT/A в концентрации до 1 пг/мл.
В предлагаемом техническом решении специфичность узнавания BoNT/A обеспечивается за счет высокоаффинных поликлональных антител, взаимодействующих с эпитопом тяжелой цепи молекулы BoNT/A, а чувствительность обеспечивается использованием ДНК-матрицы в качестве субстрата для амплификации сигнала результата реакции. Антитела, используемые для изоляции токсина из образца, иммобилизуют на магнитных частицах, а антитела, применяемые для детекции токсина, подвергают биотинилированию для последующего присоединения коньюгата ДНК с нейтравидином.
Предлагаемое техническое решение предусматривает использование нековалентного коньюгата ДНК с нейтравидином, который представляет собой молекулярную ″сетку″, образованную за счет взаимодействия биотина, находящегося на 5′-концах двухцепочечного фрагмента ДНК с тетравалетной молекулой нейтравидина. Наиболее эффективным является формирование таких комплексов в молярном соотношении биотинилированной ДНК к белку нейтравидина как 1:2. Нейтравидин является белком авидинового ряда, характеризующимся высокой специфичностью и эффективностью взаимодействия с биотином (константа аффинности 1015 л/моль). Применение молекулярной ″сетки″ вместо индивидуальных фрагментов биотинилированной ДНК повышает количество ДНК-матрицы, удерживаемой единичной молекулой антитела, и более чем в 10 раз увеличивает чувствительность метода.
Существенным условием успешного использования заявленного способа является блокировка свободных валентностей связывания твердой фазы, которая осуществляется пятикратным раствором Денхардт, содержащим 1% ДНК спермы лосося для предотвращения неспецифического связывания с поверхностью коньюгата ДНК-нейтравидин.
Важным достоинством предлагаемого способа определения BoNT/A является применение в качестве носителя комплекса парамагнитных частиц, которые допускают проведение автоматизации этого метода детекции с использованием роботизированных дозаторов и промывочных устройств и минимизирует контакт оператора с потенциально инфицированным материалом.
К преимуществам заявленного способа определения ботулинического нейротоксина типа А относятся: 1) высокая чувствительность метода, позволяющая провести диагностику первичной или вторичной интоксикации ботулотоксином типа А на ранних стадиях заболевания ботулизмом, провести мониторинговые исследования на предмет наличия ботулотоксина типа А в продуктах питания, своевременно начать терапию пострадавшего, предотвратить возможность возникновения новых случаев заболевания или нейтрализовать последствия биотеррористической атаки; 2) гомологичность заявленного метода в части реагентов, материалов и оборудования стандартному иммуноферментному анализу и технологиям ПЦР-диагностики, применяемым в клинической практике; 3) высокая специфичность детекции BoNT/A, обеспечивающаяся примененным принципом иммунодетекции, и низкая вероятность получения ложноположительных сигналов по сравнению со стандартными методами ПЦР-диагностики; 4) возможность проведения быстрого автоматизированного анализа большого количества образцов; 5) дешевизна большинства используемых в анализе материалов; 6) возможность экстраполяции разработанного способа для детекции любых других патогенных и непатогенных молекул при подборе соответствующих специфических детектирующих антител.
Изобретение осуществляют следующим образом:
Поликлональные антитела, специфичные к рецептор-связывающему домену тяжелой цепи ботулинического токсина типа А, полученные иммунизацией рекомбинантым фрагментом тяжелой цепи токсина (Фиг. 1), связывают на парамагнитных частицах за счет взаимодействия с иммобилизованным на их поверхности белком G бактерий рода Streptococcus. Свободные валентности поверхности планшета или пробирки типа ″эппендорф″ и парамагнитных частиц блокируют пятикратным раствором Денхардт, содержащим 1% ДНК спермы лосося. Троекратно промывают планшет и частицы раствором, содержащим 20 мМ трис-НС1 pH 7,5, 100 мМ хлорида натрия и 5 мМ ЭДТА, помещая планшет или пробирки на магнитную плату для фиксации частиц за счет магнитного взаимодействия
Проводят подготовку проб биологического материала или образцов продуктов питания. Для этого биологические жидкости центрифугируют с охлаждением и добавляют к супернатанту 1/10 раствора, содержащего 200 мМ трис-НС1, 1 М хлорида натрия и 50 мМ ЭДТА и ингибиторы протеаз. Твердые образцы продуктов питания гомогенизируют с раствором, содержащим 40 мМ трис-HCl pH 7,5, 200 мМ хлорида натрия и 10 мМ ЭДТА и ингибиторы протеаз, и инкубируют при встряхивании на шейкере в течение 10 минут, после чего удаляют твердые частицы центрифугированием.
Подготовленные пробы инкубируют с антителами, иммобилизованными на поверхности парамагнитных частиц в течение 1 часа. После трехкратной промывки частиц раствором, содержащим 20 мМ трис-HCl pH 7,5, 100 мМ хлорида натрия и 5 мМ ЭДТА, к ним добавляют биотинилированные антитела и инкубируют парамагнитные частицы с биотинилированными антителами при комнатной температуре со встряхиванием в течение 30 минут, после чего повторяют промывку парамагнитных частиц. К связанному на поврехности парамагнитных частиц сэндвичу ″антитело - ботулотоксин А - биотинилированное антитело″ добавляют раствор нековалентного коньюгата ДНК с нейтравидином (молекулярная ″сетка″) и инкубируют парамагнитные частицы с коньюгатом в течение 30 минут. Промывку поверхности частиц от несвязавшегося коньюгата с ДНК проводят раствором, содержащим 20 мМ трис-HCl pH 7,5, 300 мМ хлорида натрия.
После полного удаления промывочного раствора в лунки планшета или пробирки добавляют буферный раствор для эндонуклеазы рестрикции Sac I, содержащий фермент Sac I в концентрации 50 ед/мл. Рестрикцию проводят при 37°C в течение 1 часа, затем помещают планшет или пробирки на магнитную плату для фиксации частиц за счет магнитного взаимодействия и переносят супернатант из лунок планшета в пробирки для ПЦР.
В пробирки для ПЦР, содержащие продукты рестрикции, отобранные с парамагнитных частиц, обработанных рестриктазой Sac I, вносят 10 объемов смеси для амплификации, содержащей буфер для ПЦР-амплификации, праймеры, рекомбинантную Taq-полимеразу и пробу TaqMan для проведения реакции ПЦР в режиме реального времени. Детекция флуоресцентного сигнала проводится при температуре отжига праймеров 57°C и времени элонгации 1 минута с использованием прибора для ПЦР в режиме реального времени в течение 45 циклов амплификации.
Отрицательные контрольные значения флуоресцении фиксируются в пробирках, не содержащих тестируемых образцов. Положительные контрольные значения флуоресценции регистрируются в лунках или пробирках, содержащих фиксированные количества белка ботулинического нейротоксина типа А, взятого в известной концентрации. Предел детекции BoNT/A составляет 1 пг токсина на 1 мл исследуемого раствора, или 10 фг на одну ПЦР-реакцию.
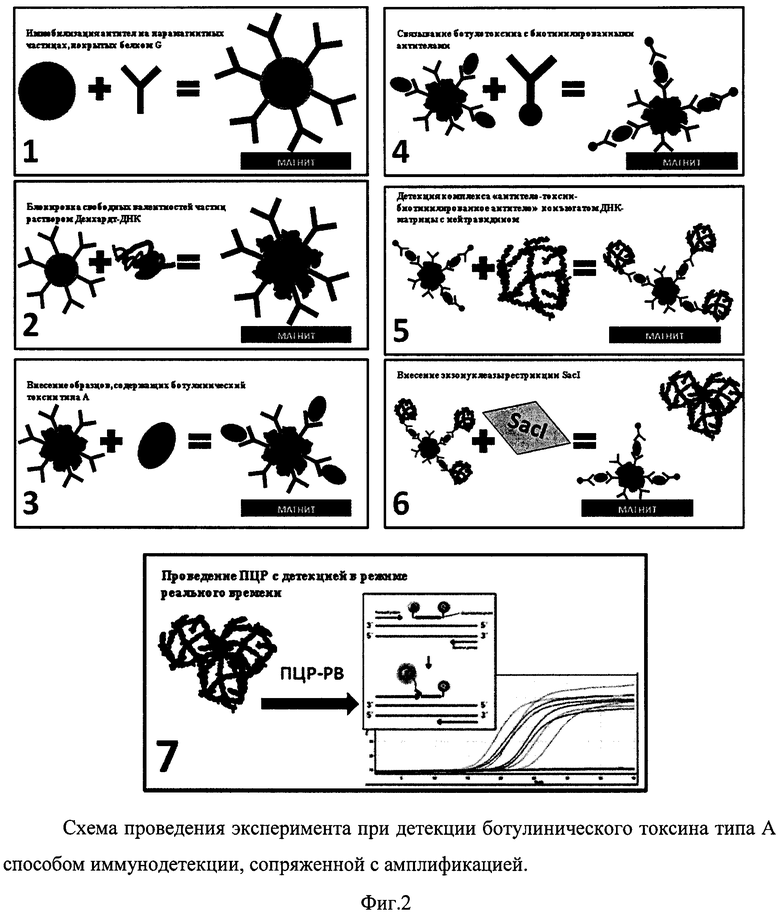
Принципиальная схема осуществления изобретения приведена на фиг. 2.
Изобретение иллюстрируют следующие графические материалы:
Фиг. 1. Аминокислотная последовательность рекомбинантного полипептида, соответствующего рецептор-связывающему домену тяжелой цепи нейротоксина ботулизма типа А, использованного для иммунизации кроликов для получения высокоспецифичных поликлональных антител к нейротоксину.
Фиг. 2. Схема постановки эксперимента при определении ботулинического нейротоксина типа А способом иммунодетекции, сопряженной с ПЦР-амплификацией. Фиг. 3. Последовательности ДНК, используемые для синтеза ДНК-матрицы, а также для определения ботулинического нейротоксина типа А способом иммунодетекции, сопряженной с ПЦР-амплификацией в режиме реального времени.
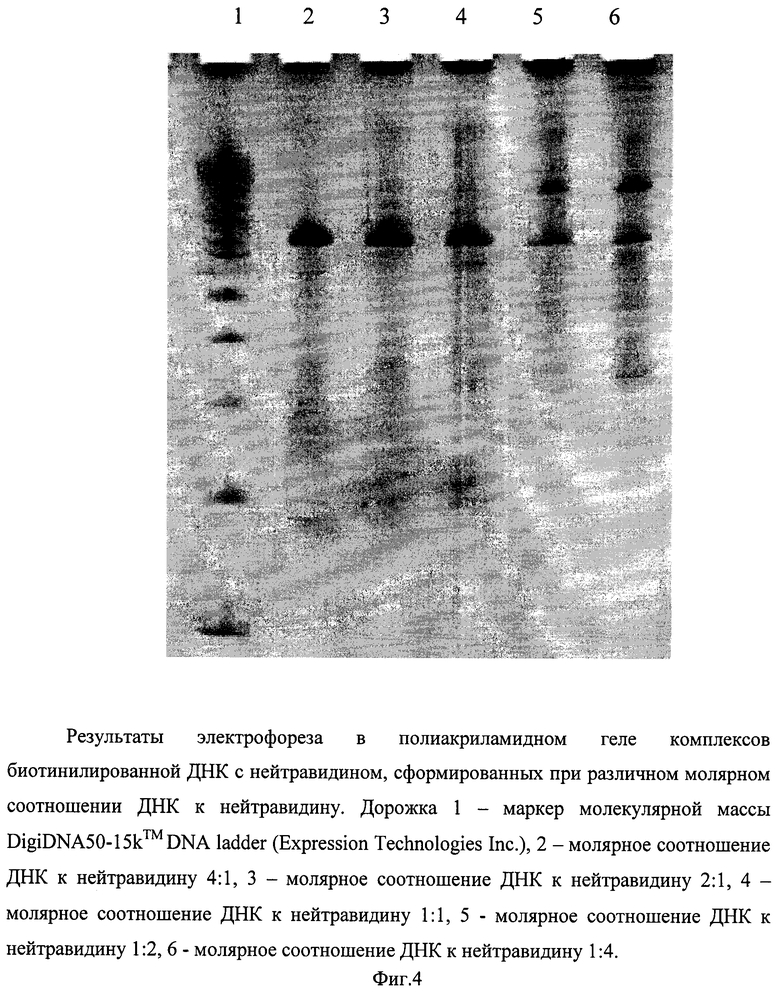
Фиг. 4. Получение коньюгата биотинилированной ДНК с нейтравидином для определения ботулинического нейротоксина типа А способом иммунодетекции, сопряженной с ПЦР-амплификацией.
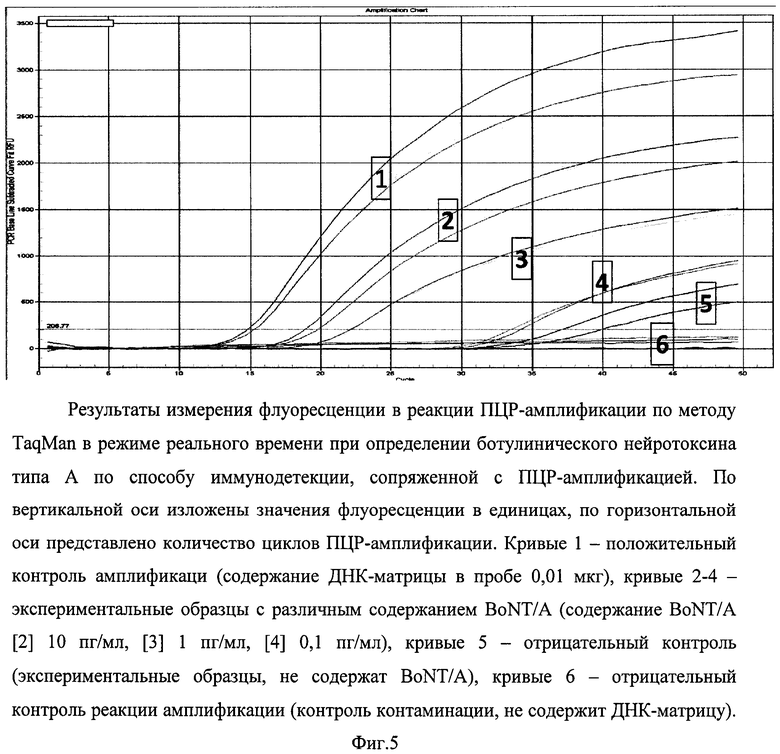
Фиг. 5. Типичные результаты определения ботулинического нейротоксина типа А способом иммунодетекции, сопряженной с ПЦР-амплификацией в режиме реального времени.
Для лучшего понимания сущности изобретения ниже следуют примеры его конкретного выполнения.
Пример 1. Получение биотинилированного антитела для определения ботулинического нейротоксина типа А способом иммунодетекции, сопряженной с ПЦР-амплификацией.
Выделение поликлональных антител для детекции ботулинического нейротоксина типа А проводят из сыворотки крови кроликов. Отобранную кровь подвергают центрифугированию при 10000 об/мин в течение 15 минут для удаления клеточного дебриса. К полученному супернатанту добавляют равный объем буфера, содержащего 40 мМ трис-HCl pH 7,5, 200 мМ хлорида натрия и проводят высаливание антитела из раствора добавлением насыщенного сульфата аммония до концентрации 50%, а затем выдерживают сульфатный раствор в течение 1 часа при температуре +4°C для формирования осадка. Полученный сульфатный осадок собирают центрифугированием при 12000 об/мин в течение 15 минут и растворяют в буфере, содержащем 50 мМ трис-HCl pH 7,5, 100 мМ хлорида натрия. Полученный белковый раствор центрифугируют при 12000 об/мин в течение 15 минут для удаления нерастворенных примесей и наносят на колонку Protein G (GE Healthcare, США), уравновешенную 10 объемами буфера, использованного для растворения белка. Колонку промывают 10 объемами того же буфера для удаления несвязавшегося белка и элюируют белок антитела раствором, содержащим 100 мМ глицин-HCl pH 2,6 и 100 мМ хлорида натрия. Приводят значение pH раствора к 8.0 добавлением раствора 1 М триса-основание с использованием pH-бумаги. Определяют концентрацию полученного белка антитела спектрофотометрически и анализируют его чистоту электрофорезом в денатурирующем полиакриламидном геле по методике Laemmli. Концентрация полученного белка составляет 1,6 мг/мл, электрофоретическая чистота белка не менее 95%. Полученный белок антитела троекратно диализуют против 100 объемов фосфатного буфера, содержащего 20 мМ Na2HPO4 и 100 мМ хлорида натрия для удаления аминогрупп. Готовят раствор NHS-биотина в DMSO из расчета 1 мг/мл и добавляют полученный раствор к раствору антитела в объемном соотношении 1:8. Проводят реакцию биотинилирования при +4°C в течение ночи со встряхиванием и троекратно диализуют против 100 объемов фосфатного буфера, содержащего 20 мМ Na2HPO4 и 100 мМ хлорида натрия для удаления не связавшегося биотина. Концентрацию конечного биотинилированного продукта определяют спектрофотометрически. Концентрация биотинилированных антител составляет 0,28 мг/мл.
Полноту биотинилирования контролируют постановкой иммуноблота с детекцией биотинилированного антитела коньюгатом нейтравидин-пероксидаза (Pierce, США). При визуализации иммуноблота определяют полосы массой 22 kDa (легкая цепь lgG) и 55 kDa (тяжелая цепь), соответствующие полосам при электрофоретическом анализе очищенных антител до реакции биотинилирования.
Пример 2. Приготовление проб для определения ботулинического нейротоксина типа А способом иммунодетекции, сопряженной с ПЦР-амплификацией.
Подготовку проб биологического материала проводят следующим образом. Отобранные согласно МУ ″Ботулизм″ N 824-69 от 22 октября 1969 г. образцы биологических жидкостей (промывные воды желудка, рвотные массы, кал, кровь, секционный материал - кусочки печени, обрезки тонкого кишечника, желудка с содержимым, кровь) центрифугируют при 5000 об/мин и температуре +4°C для освобождения от клеточного дебриса, отбирают супернатант и повторно центрифугируют его при 10000 об/мин в течение 15 минут. К супернатанту добавляют 1/10 стерильного раствора, содержащего 200 мМ трис-HCl, 1 М хлорида натрия, 50 мМ ЭДТА, а также добавляют 1/50 стерильного раствора ингибитора протеазы Complete™ Protease Inhibitor Cocktail, EDTA-free (Roche, Швейцария).
К твердым образцам биологических тканей и продуктов питания добавляют раствор, содержащий 40 мМ трис-HCl pH 7,5, 200 мМ хлорида натрия и 10 мМ ЭДТА из расчета один объем раствора (в мл) на одну единицу массы твердого образца (в г), а также 1/25 раствора ингибитора протеазы ™ Protease Inhibitor Cocktail, EDTA-free и растирают в гомогенизаторе Дунса (20 ударов плотно прилегающего пестика) во льду. Полученный однородный гомогенат встряхивают на шейкере при температуре +4°C в течение 10 минут и удаляют твердые частицы центрифугированием при 10000 об/мин в течение 15 минут.
Материал, подлежащий исследованию, хранят при температуре +4°C до проведения анализа, но оптимально используют в течение трех суток. Консервирующие вещества к отобранным пробам не добавляют.
Пример 3. Приготовление коньюгата биотинилированной ДНК с нейтравидином для определения ботулинического нейротоксина типа А способом иммунодетекции, сопряженной с ПЦР-амплификацией.
В качестве ДНК для получения коньюгата с нейтравидином и матрицы для последующей ПЦР-амплификации в режиме реального времени используют фрагмент геномной ДНК Fusarium avenaceum длиной 747 пар оснований и праймеры для амплификации фрагмента на 5′-концах модифицируют биотином (фиг. 3). Наработку биотинилированного фрагмента ДНК проводят ПЦР амплификацией при помощи Taq-полимеразы при температуре отжига праймеров 56°C и времени элонгации фрагмента 1 минута. Продукты ПЦР-реакции осаждают 3 объемами этанола с добавлением 1/10 объема ацетата натрия pH 5,2 и растворяют в 0,5 мл буфера, содержащего 20 мМ трис-HCl pH 7,5 и 300 мМ хлорида натрия, 5 мМ ЭДТА. Раствор ДНК центрифугируют для удаления нерастворенных примесей и наносят на гель-фильтрационную колонку Superdex-200 (GE-Healthcare, Великобритания), уравновешенную тем же буфером, для удаления побочных продуктов синтеза и не задействованных в синтезе олигонуклеотидов. Гель-фильтрацию проводят при скорости потока 0,5 мл/мин, выход разделяемых продуктов контролируют спектрофотометрически при длине волны 260 нм. Определяют содержание целевого фрагмента ДНК во фракциях гель-фильтрации электрофорезом в агарозном геле. Для дальнейшей работы отбирают фракции, содержащие фрагмент длиной 747 п. н. Фракции, содержащие синтезированный фрагмент, осаждают 3 объемами этанола с добавлением 1/10 объема ацетата натрия pH 5,2 и растворяют в буфере, содержащем 20 мМ трис-HCl, 100 мМ хлорида натрия и 5 мМ ЭДТА. Количество ДНК в полученном растворе определяют спектрофотометрически. Концентрация ДНК-матрицы составляет 48 мкг/мл.
Готовят раствор нейтравидина (Pierce, США) из расчета 1 мг/мл и смешивают его с раствором ДНК в соотношении 2:1 соответственно. Смесь инкубируют при +4°C в течение ночи. Образование молекулярной ″сетки″ биотинилированной ДНК с нейтравидином контролируют электрофорезом ДНК в полиакриламидном геле по замедлению скорости миграции продуктов разделения против исходного фрагмента ДНК (фиг. 4). Полученный коньюгат биотинилированной ДНК с нейтравидином очищают от несвязанной ДНК и нейтравидина гель-фильтрацией на колонке Superdex-200 (GE-Healthcare, Великобритания), уравновешенной буфером, содержащим 20 мМ трис-HCl pH 7,5, 300 мМ хлорида натрия и 5 мМ ЭДТА. Содержание коньюгата во фракциях гель-фильтрации контролируют электрофорезом в агарозном геле. Оптимально определяют полосы, соответствующие ДНК длиной не менее 2988 п. н. при отсутствии фрагментов длиной 747 п. н. Очищенный коньюгат концентрируют с использованием Microcon YM-50 (Millipore, США). Спектрофотометрически определяют концентрацию коньюгата по ДНК и белку и на основании этих данных рассчитывают соотношение ДНК к белку в полученной молекулярной ″сетке″. Концентрация ДНК и белка составляет 32 мкг/мл и 14,6 мкг/мл соответственно, что указывает на молярное соотношение ДНК к белку как 1:2. К коньюгату добавляют глицерин до 50% и хранят по аликвотам при температуре -70°C.
Пример 4. Постановка иммунодетекции ботулотоксина А и связывание его с ДНК-матрицей для последующей ПЦР-амплификации в режиме реального времени.
Парамагнитные частицы с иммобилизованным белком G бактерий семейства Streptococcus (Protein G Magnetic Beads, New England Biolabs, США) наносят в лунки микропланшета или в пробирки типа ″эппендорф″ объемом 1,5 мл в количестве 10 мкл суспензии частиц на лунку/пробирку. В лунки иммунологического микропланшета или пробирки разносят раствор Денхардт (20 мМ трис-HCl, pH 7,5, 100 мМ хлорида натрия, 1% Ficoll 400, 1% поливинилпирролидон, 1% бычий сывороточный альбумин), содержащего 1% ДНК спермы лосося - в лунки микропланшета по 300 мкл, в пробирки по 1,5 мл - и инкубируют в течение 1 часа при 37°C для блокировки свободных валентностей поверхности. Помещают планшет на магнитную плату прибора ELx405 Magna (BioTek, США) и шестикратно промывают парамагнитные частицы, удерживаемые магнитным взаимодействием, буферным раствором, содержащим 20 мМ трис-HCl pH 7,5, 100 мМ хлорида натрия, 5 мМ ЭДТА в объеме 300 мкл. Микропробирки помещают на магнитный штатив Invitrogen DynaMag™-2 и отмывают аналогично внесением 1,5 мл отмывающего буфера с использованием шагового механического дозатора Ленпипет Степпер для внесения буферного раствора и аспиратора Gilson Safe Aspiration Station (Gilson, США) для отбора жидкости. В лунки микропланшета или пробирки разносят по 100 мкл подготовленных образцов, содержащих известное количество BoNT/A в различных концентрациях (десятикратные разведения от 10 нг/мл до 0,1 пг/мл) - в качестве положительного контроля и для построения калибровочной кривой, а также исследуемые образцы. В лунки, служащие отрицательным контролем, добавляют буферный раствор, содержащий 20 мМ трис-HCl pH 7,5, 100 мМ хлорида натрия, 5 мМ ЭДТА, либо экспериментальные образцы, заведомо не содержащие ботулотоксин А. В качестве контроля специфичности выступают образцы, содержащие 10 пг/мл белковых токсинов иной структуры: шига-токсин энтерогеморрагической Е. coli, дифтерийный токсин, токсин тканевого шока S. aureus, холерный токсин, стафилококковый энтеротоксин А. Инкубируют планшет или пробирки при встряхивании в течение 1 часа при комнатной температуре. Шестикратно промывают парамагнитные частицы раствором, содержащим 20 мМ трис-HCl pH 7,5, 100 мМ хлорида натрия, 5 мМ ЭДТА с применением прибора ELx405 Magna или использованием шагового механического дозатора Ленпипет и аспиратора Gilson Safe Aspiration Station. В лунки планшета или микропробирки добавляют по 100 мкл раствора, содержащего биотинилированные антитела, и инкубируют планшет при встряхивании в течение 30 минут при комнатной температуре. Шестикратно промывают парамагнитные частицы раствором, содержащим 20 мМ трис-HCl pH 7,5, 100 мМ хлорида натрия, 5 мМ ЭДТА с применением прибора ELx405 Magna или использованием шагового механического дозатора Ленпипет и аспиратора Gilson Safe Aspiration Station. В лунки планшета или пробирки добавляют по 100 мкл раствора 20 мМ трис-HCl pH 7,5, 300 мМ хлорида натрия, 5 мМ ЭДТА, содержащего коньюгат биотинилированной ДНК с нейтравидином в количестве 0,1 мкг ДНК на лунку/пробирку и инкубируют при встряхивании в течение 30 минут при комнатной температуре, после чего десятикратно промывают парамагнитные частицы раствором, содержащим 20 мМ трис-HCl pH 7,5, 300 мМ хлорида натрия с применением прибора ELx405 Magna или использованием шагового механического дозатора Ленпипет и аспиратора Gilson Safe Aspiration Station.
После полного удаления промывочного раствора в лунки планшета или микропробирки разносят по 50 мкл однократного буферного раствора для эндонуклеазы рестрикции Sac I, содержащий фермент Sac I в концентрации 50 ед/мл. Инкубируют при 37°C в течение 1 часа, помещают планшет на магнитную плату, пробирки на магнитный сепаратор и переносят супернатант в пробирки для ПЦР. К 1/10 отобранного супернатанта добавляют смесь для ПЦР-амплификации в режиме реального времени.
Пример 5. Проведение ПЦР-амплификации с флуоресцентной детекцией сигнала в режиме реального времени для определения ботулинического нейротоксина типа А способом иммунодетекции, сопряженной с ПЦР-амплификацией.
Для проведения ПЦР-амплификации в режиме реального времени в пробирки для ПЦР, содержащие по 5 мкл продуктов рестрикции ДНК-матрицы, отобранных с парамагнитных частиц, обработанных рестриктазой Sac I, разносят по 50 мкл 1х реакционную смесь для амплификации (Реакционная смесь 2,5х для проведения ПЦР-РВ, ″Синтол″, Россия), содержащую по 300 нМ каждого из праймеров для амплификации, 1 единицу рекомбинантной Taq-полимеразы и 200 нМ зонда TaqMan (фиг. 3). Реакцию амплификации проводят на приборе для ПЦР амплификации в режиме реального времени MiniOpticon Real-Time PCR Detection System (Bio-Rad, США) с использованием следующего протокола:

Регистрацию нарастания флуоресценции ведут при длине волны 520 нм. Положительный контроль амплификации показывает нарастание сигнала флуоресценции до 15 цикла реакции амплификации. Пробы, содержащие BoNT/A выше предела детекции, показывают нарастание флуоресценции с 15 по 25 циклы реакции амплификации. Нарастания флуоресценции в отрицательных контрольных пробах и в пробах, содержащих BoNT/A ниже предела определения, в диапазоне циклов реакции с 5 по 30 не обнаруживают (фиг. 5). Применив калибровочную кривую, построенную на основании зависимости номера цикла, на котором начинает регистрироваться изменение флуоресценции, от значений концентрации белка ботулотоксина А в контрольных образцах, определяют концентрацию белка BoNT/A в исследуемых пробах. Чувствительность метода составляет 1 пг/мл ботулотоксина типа А. Анализ специфической активности показывает отсутствие перекрестного взаимодействия с белковыми токсинами иной природы.
| название | год | авторы | номер документа |
|---|---|---|---|
| ШТАММ ГИБРИДНЫХ КЛЕТОК ЖИВОТНЫХ Mus musculus 1G7 - ПРОДУЦЕНТ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ, СПЕЦИФИЧНЫХ К БОТУЛИНИЧЕСКОМУ ТОКСИНУ ТИПА В | 2014 |
|
RU2571208C1 |
| ШТАММ ГИБРИДНЫХ КЛЕТОК ЖИВОТНЫХ Mus musculus 3F11 - ПРОДУЦЕНТ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ, СПЕЦИФИЧНЫХ К БОТУЛИНИЧЕСКОМУ ТОКСИНУ ТИПА B | 2014 |
|
RU2566553C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЛЕТАЛЬНОГО ФАКТОРА СИБИРСКОЙ ЯЗВЫ НА ОСНОВЕ ИММУНОДЕТЕКЦИИ, СОПРЯЖЕННОЙ С ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИЕЙ | 2011 |
|
RU2486524C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НАЛИЧИЯ БАКТЕРИЙ Escherichia coli O157:H7 В БИОЛОГИЧЕСКИХ И ПИЩЕВЫХ ОБРАЗЦАХ НА ОСНОВЕ ИММУНОДЕТЕКЦИИ, СОПРЯЖЕННОЙ С ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИЕЙ | 2014 |
|
RU2569196C1 |
| ПОСЛЕДОВАТЕЛЬНОСТЬ ДНК-АПТАМЕРОВ, СВЯЗЫВАЮЩАЯСЯ С ПРОТЕОЛИТИЧЕСКОЙ СУБЪЕДИНИЦЕЙ НЕЙРОТОКСИНА ТИПА A CLOSTRIDIUM BOTULINUM | 2014 |
|
RU2571210C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НАЛИЧИЯ ПРОТЕКТИВНОГО АНТИГЕНА СИБИРСКОЙ ЯЗВЫ НА ОСНОВЕ ИММУНОДЕТЕКЦИИ, СОПРЯЖЕННОЙ С ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИЕЙ | 2011 |
|
RU2470307C1 |
| УЧАСТОК СВЯЗЫВАНИЯ АНТИГЕНА (Fab), В ТОМ ЧИСЛЕ ГУМАНИЗИРОВАННЫЙ Fab, ПРОТИВ БОТУЛИНИЧЕСКОГО НЕЙРОТОКСИНА С (ВАРИАНТЫ), СПОСОБ ПОЛУЧЕНИЯ Fab С ИСПОЛЬЗОВАНИЕМ ДРОЖЖЕЙ, СПОСОБ И НАБОР ДЛЯ ДЕТЕКЦИИ БОТУЛИНИЧЕСКОГО НЕЙРОТОКСИНА С | 2016 |
|
RU2623157C1 |
| ПОСЛЕДОВАТЕЛЬНОСТЬ ДНК, ПРИМЕНИМАЯ В КАЧЕСТВЕ ЗОНДА ДЛЯ ОБЕСПЕЧЕНИЯ МАКСИМАЛЬНОГО СООТНОШЕНИЯ "СИГНАЛ/ФОН" В ТЕСТ-СИСТЕМАХ НА ОСНОВЕ ИММУНО-ПЦР | 2014 |
|
RU2566550C1 |
| Штамм гибридных культивируемых клеток Homo sapiens/Mus musculus 1B9C7 - продуцент человеческих моноклональных антител, специфичных к протеолитическому домену ботулинического токсина типа A | 2021 |
|
RU2783897C1 |
| Способ направленного истощения олигонуклеотидных библиотек для снижения неспецифической адсорбции при твердофазной селекции аптамеров на основе нуклеиновых кислот | 2015 |
|
RU2618872C1 |


Изобретение относится к области медицины и предназначено для определения наличия ботулинического нейротоксина типа А (BoNT/A). На парамагнитных частицах, несущих иммобилизованный белок G бактерий семейства Streptococcus, с блокированными раствором Денхардт-ДНК адсорбируют белок BoNT/A при помощи специфических высокоаффинных поликлональных антител. Детектируют образование комплекса белка BoNT/A с биотинилированным антителом посредством нековалентного коньюгата фрагментов ДНК с нейтравидином. Проводят ПЦР-амплификацию ДНК-матрицы с флуоресцентной детекцией сигнала в режиме реального времени. Регистрацию присутствия BoNT/A в исследуемых образцах проводят по изменению уровня флуоресценции против контрольных. Изобретение обеспечивает эффективный способ определения наличия BoNT/A в пробах биологических жидкостей и тканей при первичной и вторичной интоксикации, а также в продуктах питания и может быть использовано для анализа как инфекционно опасных, так и инактивированных образцов. 5 ил., 1 табл., 5 пр.
Способ определения наличия ботулинического нейротоксина типа А на основе иммунодетекции, сопряженной с полимеразной цепной реакцией, включающий адсорбцию белка ботулотоксина типа А на парамагнитных частицах, несущих иммобилизованный белок G бактерий семейства Streptococcus, с блокированными раствором Денхардт-ДНК свободными валентностями частиц, при помощи специфических высокоаффинных поликлональных антител, узнающих рецептор-связывающий домен тяжелой субъединицы ботулотоксина типа А, связывание иммобилизованного белка ботулотоксина типа А при помощи биотинилированных поликлональных антител, детекцию комплекса белка ботулинического нейротоксина типа А с биотинилированным антителом посредством нековалентного коньюгата фрагментов неспецифической оптимизированной ДНК с нейтравидином, освобождение ДНК-матрицы из образованного твердофазного комплекса при помощи эндонуклеазы рестрикции с последующим проведением ее ПЦР-амплификации с флуоресцентной детекцией сигнала в режиме реального времени с использованием специфических праймеров и метки TaqMan и регистрацией присутствия ботулотоксина типа А в исследуемых образцах по изменению уровня флуоресценции в соответствующих пробирках, лунках планшета или пробирках стрипа против контрольных.
| RAJKOVIC A | |||
| et al | |||
| Detection of Clostridium botulinum neurotoxins A and B in milk by ELISA and immuno-PCR at higher sensitivity than mouse bio-assay | |||
| Food Analytical Methods | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| КОЗЫРЬ А.В | |||
| и др | |||
| Разработка технодиагностикумов бактериальных инфекций на основе метода иммуно-ПЦР | |||
| Теоретические и практические аспекты современной | |||
Авторы
Даты
2015-04-27—Публикация
2013-12-03—Подача