Настоящая заявка претендует на приоритет предварительной заявки на патент США № 61/244051, поданной 20 сентября 2009 г.
Делается перекрестная ссылка на следующие находящиеся на рассмотрении заявки на патенты США, предмет которых имеет отношение к настоящей заявке: заявка № 12/770112, озаглавленная «Липидные составы промотора апоптоза»; заявка № 12/770174, озаглавленная «Стабилизированные липидные составы промотора апоптоза»; заявка № 12/770205, озаглавленная «Твердые пероральные составы ABT-263»; и заявка № 12/770 299, озаглавленная «Составы промотора апоптоза для перорального введения», где все указанные заявки поданы 29 апреля 2010 г.
Содержание каждой из перечисленных выше заявок полностью включено в настоящую заявку посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к апоптоз-активирующему агенту ABT-263, к его твердым формам, составам, содержащим эти твердые формы и/или полученным с их применением, а также к способам их применения для лечения заболеваний, характеризующихся избыточной экспрессией антиапоптотических белков семейства Bcl-2. Более конкретно, изобретение относится к кристаллическим формам ABT-263, применимым, например, в качестве действующего фармацевтического ингредиента (API) для получения фармацевтических композиций для введения ABT-263 субъекту, который нуждается в этом.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Отсутствие апоптоза является отличительным признаком рака (Hanahan & Weinberg (2000) Cell 100:57-70). Раковые клетки должны преодолевать непрерывное воздействие клеточных стрессов, таких как повреждение ДНК, активация онкогенов, аномальное развитие клеточного цикла и агрессивные воздействия микросреды, которые могли бы вынудить нормальные клетки подвергнуться апоптозу. Один из основных путей, за счет которого раковые клетки избегают апоптоза, является повышающая регуляция антиапоптотических белков семейства Bcl-2.
Соединения, которые занимают карман связывания BH3 белков Bcl-2, были описаны, например, Bruncko et al. (2007) J.Med.Chem. 50:641-662. В число этих соединений входил N-(4-(4-((4'-хлор-(1,1'-бифенил)-2-ил)метил)пиперазин-1-ил)бензоил)-4-(((1R)-3-(диметиламино)-1-((фенилсульфанил)метил)пропил)амино)-3-нитробензолсульфонамид, известный также под наименованием ABT-737 и имеющий приведенную ниже формулу:
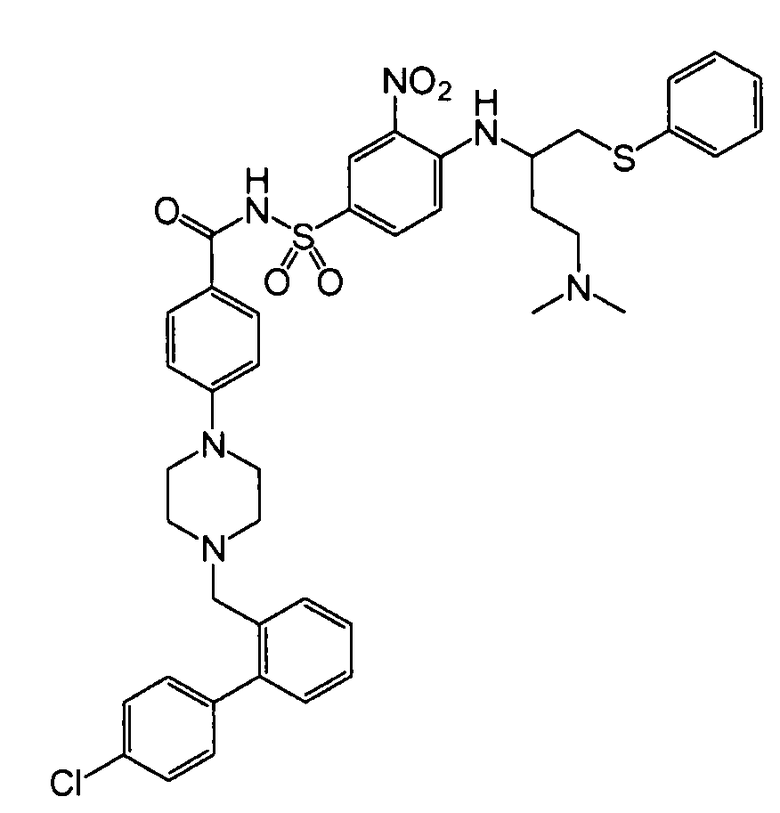 .
.
ABT-737 с высоким сродством (<1 нМ) связывается с белками семейства Bcl-2 (конкретно Bcl-2, Bcl-XL и Bcl-w). Он проявляет самостоятельную активность против мелкоклеточного рака легких (SCLC) и лимфоидных злокачественных опухолей, а также потенцирует проапоптотическое действие других химиотерапевтических агентов. ABT-737 и родственные соединения, а также способы получения этих соединений, раскрыты в опубликованной заявке на патент США № 2007/0072860, поданной Bruncko et al.
Позднее была выявлена еще одна группа соединений, имеющих высокое сродство к связыванию с белками семейства Bcl-2. Эти соединения и способы их получения раскрыты в опубликованной заявке на патент США № 2007/0027135, поданной Bruncko et al. (далее по тексту именуемой «заявкой 135»), включенной в настоящую заявку с помощью ссылки в полном объеме, и, как можно видеть из их формулы, структурно родственны ABT-737.
Одно из соединений, полученных в «заявке 135», а именно в примере 1, представляет собой N-(4-(4-((2-(4-хлорфенил)-5,5-диметил-1-циклогекс-1-ен-1-ил)метил)пиперазин-1-ил)бензоил)-4-(((1R)-3-(морфолин-4-ил)-1-((фенилсульфанил)метил)пропил)амино)-3-((трифторметил)сульфонил)бензолсульфонамид, известный так же, как ABT-263. Это соединение имеет молекулярную массу 974,6 г/моль и приведенную ниже формулу:
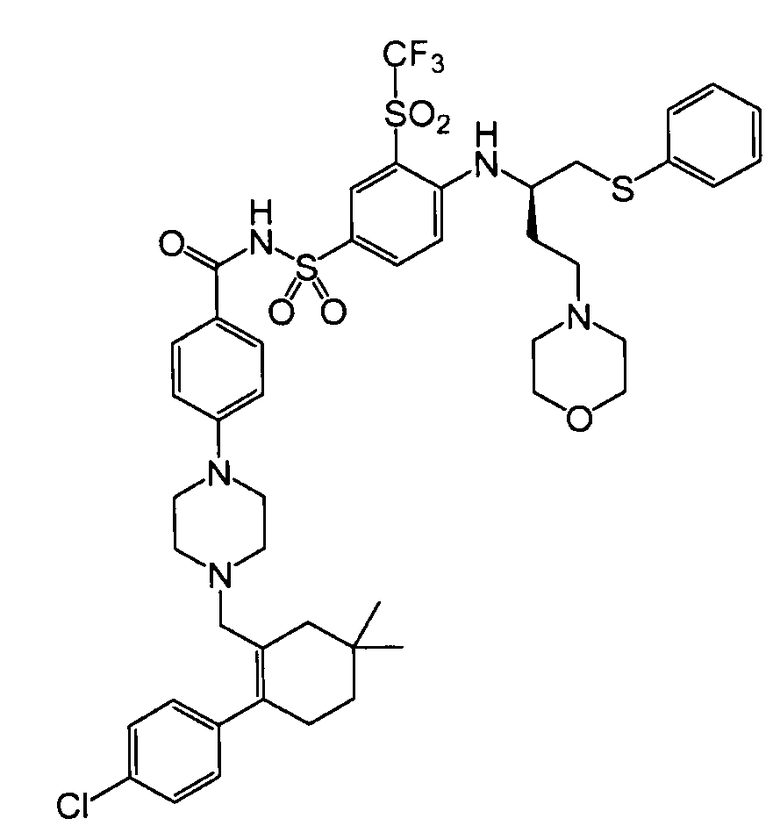 .
.
В статье Tse et al. (2008) Cancer Res. 68:3421-3428 и дополнительных данных к этой статье, доступных на Cancer Research Online (cancerres.aacrjournals.org/), сообщалось о проведенных на животных фармакокинетических исследованиях ABT-263, который был синтезирован, как описано в «заявке 135». Состав препарата готовили в виде раствора в 10% диметилсульфоксиде (ДМСО) в полиэтиленгликоле (PEG) 400 или в смеси 10% этанол/30% PEG400/60% Phosal 50-PGTM.
Конкретным типом заболеваний, лечение которых необходимо улучшить, являются неходжкинские лимфомы (NHL). NHL является шестым из наиболее распространенных типов среди всех вновь появляющихся раковых заболеваний в США и развивается, в основном, у пациентов в возрасте 60-70 лет. NHL не является единым заболеванием, а представляет собой семейство родственных заболеваний, которые классифицируют на основе нескольких характеристик, включая клинические признаки и гистологию.
Один из способов классификации относит различные гистологические подтипы к двум основным категориям, на основе истории развития заболевания, т.е. является ли заболевание неактивным или агрессивным. Как правило, неактивные подтипы растут медленно и в основном неизлечимы, в то время как агрессивные подтипы растут быстро и являются потенциально излечимыми. Фолликулярные лимфомы чаще всего относятся к неактивному подтипу, а диффузные крупноклеточные лимфомы, как правило, относятся к агрессивному подтипу. Онкобелок Bcl-2 был первоначально описан в неходжкинских B-клеточных лимфомах.
Лечение фолликулярной лимфомы, как правило, состоит из химиотерапии на биологической основе или комбинированной химиотерапии. Обычно применяется комбинированная терапия, включающая ритуксимаб, циклофосфамид, доксорубицин, винкристин и преднизон (R-CHOP), а также комбинированная терапия, включающая ритуксимаб, циклофосфамид, винкристин и преднизон (RCVP). Кроме того, применяют монотерапию, вводя ритуксимаб (нацеленный на CD20, т.е. фосфопротеин, непрерывно экспрессируемый на поверхности B-клеток) или флударабин. Добавление ритуксимаба к химиотерапевтическим схемам лечения может привести к улучшению скорости реакции и увеличению выживаемости без прогрессирования заболевания.
Для лечения рефрактерной или рецидивирующей неходжкинской лимфомы можно применять радиоиммунотерапевтические средства, химиотерапию в высоких дозах или трансплантаты стволовых клеток. В настоящее время не существует одобренной схемы лечения, которая приводит к исцелению, и действующие директивы рекомендуют лечить пациентов в контексте клинических испытаний даже в схеме лечения первой линии.
Лечение первой линии пациентов с агрессивной лимфомой из крупных B-клеток, как правило, состоит из ритуксимаба, циклофосфамида, доксорубицина, винкристина и преднизона (R-CHOP) или комбинации подобранных дозировок этопозида, преднизона, винкристина, циклофосфамида, доксорубицина и ритуксимаба (DA-EPOCH-R).
Большинство лимфом первоначально реагируют на любой из указанных способов лечения, но, как правило, опухоли рецидивируют и постепенно становятся устойчивыми к лечению. Чем больше число схем лечения, получаемых пациентом, тем более устойчивым к химиотерапии становится заболевание. В среднем, реакция на терапию первой линии наблюдается примерно в 75% случаев, на терапию второй линии в 60% случаев, на терапию третьей линии в 50% случаев и на терапию четвертой линии примерно в 35-40% случаев. Величина реакции, приближающаяся к 20%, для индивидуального агента в случае многократно рецидивировавшей опухоли считается положительным результатом и служит основанием для дальнейших исследований.
Имеющиеся в наличии химиотерапевтические средства проявляют свое противоопухолевое действие, вызывая апоптоз, через различные механизмы. Однако многие опухоли, в конце концов, становятся устойчивыми к этим средствам. Bcl-2 и Bcl-XL, как было показано в кратковременном исследовании выживаемости in vitro, придают опухоли устойчивость к химиотерапии, и позднее тот же результат был получен in vivo. Это позволяет предположить, что если можно разработать улучшенную терапию, направленную на подавление деятельности Bcl-2 и Bcl-XL, то упомянутую устойчивость к химиотерапии можно было бы с успехом преодолеть.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Если получать соединение ABT-263 по методике примера 1 «заявки 135», оно выделяется в виде аморфного стеклообразного твердого вещества, которое не очень удобно применять в качестве действующего фармацевтического ингредиента (API) для последующего изготовления лекарственных составов. Более конкретно, эту аморфную форму ABT-263 трудно и, следовательно, дорого очищать, и возникают проблемы при регулировании процесса ее переработки. Один из подходов, пример которого раскрыт в находящейся в процессе одновременного рассмотрения предварительной заявке на патент США № 61/174274, поданной 30 апреля 2009 г. (включенной в настоящую заявку с помощью ссылки без признания того, что она относится к известному уровню техники по сравнению с настоящим изобретением), заключается в получении ABT-263 в форме кристаллической соли. В рамках другого подхода авторам настоящего изобретения удалось получить ряд новых кристаллических форм ABT-263 в виде свободного основания, подходящих для применения в качестве API в широком круге составов различного типа, включая такие составы, в которых API находится в форме мелких частиц совместно с эксципиентами, например таблетки или капсулы для перорального приема.
В одном из вариантов осуществления настоящее изобретение относится к N-(4-(4-((2-(4-хлорфенил)-5,5-диметил-1-циклогекс-1-ен-1-ил)метил)пиперазин-1-ил)бензоил)-4-(((1R)-3-(морфолин-4-ил)-1-((фенилсульфанил)метил)пропил)амино)-3-((трифторметил)сульфонил)бензолсульфонамиду (ABT-263) в виде свободного основания в твердой кристаллической форме.
В другом варианте осуществления изобретение относится к не содержащему растворителя кристаллическому полиморфу свободного основания ABT-263, охарактеризованному в настоящей заявке и названному формой I свободного основания ABT-263.
В следующем варианте осуществления изобретение относится к не содержащему растворителя кристаллическому полиморфу свободного основания ABT-263, охарактеризованному в настоящей заявке и названному формой II свободного основания ABT-263.
В ряде других вариантов осуществления настоящее изобретение относится к сольватированным кристаллическим формам свободного основания ABT-263, включающим органические растворители.
В еще одном варианте осуществления изобретение относится к фармацевтической композиции, включающей кристаллическое свободное основание ABT-263 (например, в упомянутой выше форме I или форме II), а также один или несколько фармацевтически приемлемых эксципиентов.
В другом варианте осуществления изобретение относится к способу получения фармацевтической композиции ABT-263 в форме раствора, включающему растворение кристаллического свободного основания ABT-263 (например, в упомянутой выше форме I или форме II) в фармацевтически приемлемом растворителе или смеси растворителей.
В следующем варианте осуществления изобретение относится к способу лечения заболевания, характеризующегося нарушением апоптоза и/или избыточной экспрессией антиапоптотических белков семейства Bcl-2, включающему введение субъекту, у которого имеется такое заболевание, терапевтически эффективного количества свободного основания ABT-263 в кристаллической форме (например, в упомянутой выше форме I или форме II) или фармацевтической композиции, включающей свободное основание ABT-263 в кристаллической форме (например, в упомянутой выше форме I или форме II), а также один или несколько фармацевтически приемлемых наполнителей. Примеры подобных заболеваний включают многие неопластические расстройства, в том числе раковые заболевания. Конкретным иллюстративным типом рака, который можно лечить способом по настоящему изобретению, является неходжкинская лимфома. Другим конкретным иллюстративным типом рака, который можно лечить способом по настоящему изобретению, является хронический лимфоцитарный лейкоз. Еще одним конкретным иллюстративным типом рака, который можно лечить способом по настоящему изобретению, является острый лимфоцитарный лейкоз, например, у пациентов детского возраста.
Помимо перечисленного изобретение относится к способу поддержания у пациентов из числа людей с раком, например пациентов с неходжкинской лимфомой, терапевтически эффективной концентрации в плазме ABT-263 и/или одного или нескольких его метаболитов, включающему введение субъекту фармацевтической композиции, содержащей свободное основание ABT-263 в кристаллической форме (например, в упомянутой выше форме I или форме II), а также один или несколько фармацевтически приемлемых эксципиентов, в количестве от примерно 50 до примерно 1000 мг ABT-263 в день при среднем интервале между введениями от примерно 3 часов до примерно 7 дней.
Дополнительные варианты осуществления настоящего изобретения, включая более конкретные аспекты изложенных выше вариантов, будут раскрыты в приведенном ниже подробном описании изобретения или будут ясны из этого описания.
КРАТКОЕ ОПИСАНИЕ ФИГУР
Фиг.1 представляет собой рентгенограмму PXRD не содержащей растворителя кристаллической полиморфной формы I свободного основания ABT-263.
Фиг.2 представляет собой рентгенограмму PXRD не содержащей растворителя кристаллической полиморфной формы II свободного основания ABT-263.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Термин «свободное основание» применяется в настоящей заявке для удобства обозначения ABT-263 в форме исходного соединения, чтобы отличать данную форму от любой солевой формы этого соединения, с учетом того факта, что исходное соединение, строго говоря, является цвиттерионным и поэтому не всегда проявляет свойства истинного основания.
Термин «не содержащий растворителя» в настоящей заявке относится к кристаллической решетке полиморфа свободного основания ABT-263, например, формы I или формы II, из которой в результате десольватации был удален растворитель. Растворитель может присутствовать в небольших количествах в твердых частицах соединения, не являясь частью кристаллической решетки и не оказывая влияния на кристаллическую структуру полиморфа; такое присутствие растворителя в рамках настоящей заявки все-таки согласуется с использованием термина «не содержащий растворителя» в отношении полиморфа.
ABT-263 в форме свободного основания можно получить способом, описанным в примере 1 упомянутой выше опубликованной заявки на патент США № 2007/0027135, содержание которой полностью включено в настоящую заявку посредством ссылки. Продукт этого способа представляет собой аморфное стеклообразное твердое вещество. Из этого продукта можно получить порошок, например, с помощью лиофильной сушки или осаждения.
Сольваты свободного основания ABT-263 получали, как описано ниже. Исходным веществом могла являться любая твердая форма свободного основания ABT-263, включая аморфную форму, полученную по методике «заявки 135».
Определенное количество свободного основания ABT-263 (как указано выше, можно использовать любую твердую форму) суспендировали в каждом из набора растворителей или смесей растворителей, показанных в таблице 1. Полученную суспензию перемешивали при комнатной температуре, защищая от действия света. Через определенный период времени, достаточный для осуществления сольватации свободного основания ABT-263 в каждом случае, собирали кристаллы с помощью центрифугирования с фильтрованием. Полученные сольваты характеризовали дифракцией рентгеновских лучей на порошке (PXRD).
Получение кристаллических сольватов свободного основания
ABT-263
Данные PXRD регистрировали, используя дифрактометр G3000 (Inel Corp., Artenay, France), снабженный изогнутым позиционно-чувствительным детектором и оптикой параллельных пучков. В дифрактометре использовали трубчатый медный анод (1,5 кВт, с тонкой фокусировкой) при напряжении 40 кВ и токе 30 мА. Германиевый монохроматор падающего пучка обеспечивал монохромное излучение. Дифрактометр калибровали с использованием ослабленного прямого пучка с интервалами в один градус. Калибровку проверяли по положению стандартных эталонных линий порошка кремния (NIST 640c). Прибор управлялся компьютером с помощью программы Symphoix software (Inel Corp., Artenay, France) и данные анализировали с помощью программы Jade (версия 6.5, Materials Data, Inc., Livermore, CA). Образец помещали на алюминиевый держатель для образцов и выравнивали стеклянной пластиной.
Пики рентгенограмм PXRD индивидуальных сольватов, зарегистрированные в описанных выше условиях, перечислены в таблицах 2-14. Положение пиков, как правило, приведено с точностью ±0,2 градуса по углу два-тета (°2θ).
Перечень пиков на рентгенограмме PXRD сольвата свободного основания ABT-263 с 1-пропанолом
Перечень пиков на рентгенограмме PXRD сольвата свободного основания ABT-263 с 2-пропанолом
Перечень пиков на рентгенограмме PXRD сольвата свободного основания ABT-263 с бензолом
Перечень пиков на рентгенограмме PXRD сольвата свободного основания ABT-263 с хлороформом
Перечень пиков на рентгенограмме PXRD сольвата свободного основания ABT-263 с 1,4-диоксаном/гексаном
Перечень пиков на рентгенограмме PXRD сольвата свободного основания ABT-263 с метилацетатом/гексаном
Перечень пиков на рентгенограмме PXRD сольвата свободного основания ABT-263 с метанолом
Перечень пиков на рентгенограмме PXRD сольвата свободного основания ABT-263 с толуолом
Перечень пиков на рентгенограмме PXRD сольвата свободного основания ABT-263 с этанолом/этилацетатом
Перечень пиков на рентгенограмме PXRD сольвата свободного основания ABT-263 с этилацетатом
Перечень пиков на рентгенограмме PXRD сольвата свободного основания ABT-263 с изопропилацетатом
Перечень пиков на рентгенограмме PXRD сольвата свободного основания ABT-263 с метилацетатом
Перечень пиков на рентгенограмме PXRD сольвата свободного основания ABT-263 с трифтортолуолом
Кроме того, описанными ниже способами получали монокристаллы сольватов анизола, пиридина и 2-пропанола для рентгеноструктурного анализа. Индивидуальные кристаллы закрепляли на полиимидной подставке MiTeGen. Данные по интенсивности регистрировали на системе Bruker D8, снабженной CCD камерой APEX II. Данные регистрировали при 100К, используя излучение Mo Ka (λ=0,71073 Å), монохроматизированное графитовым монохроматором. Регистрировали четыре массива данных, используя ω-φ развертку с шагами 0,5° по ω и 90° по φ. Данные регистрировали с помощью 20-секундных экспозиций для каждого снимка. Обработку данных осуществляли с помощью программы APEX2. Применяли коррекцию на поляризационные эффекты Лоренца. Поглощением пренебрегали. Все структуры рассчитывали с использованием прямых методов, которые позволяли определить положение не водородных атомов. Положения всех имеющихся в структуре атомов водорода определяли по разностным Фурье-картам электронной плотности. Положение всех не водородных атомов уточняли в анизотропном приближении. Положение атомов водорода, связанных с атомами углерода, уточняли в геометрически ограниченных положениях «наездника». Атомы водорода, связанные с атомами кислорода, включали в структуру в локализованных положениях. Уточнение структуры осуществляли с помощью кристаллографической программы SHELXTL.
Для получения монокристаллов сольвата с анизолом аморфное свободное основание ABT-263 растворяли в 0,5 мл анизола. Образование монокристаллов наблюдалось через два дня. Кристаллографические данные сольвата с анизолом представлены в таблице 15, и сведения о пиках PXRD, вычисленных из этой кристаллической структуры, приведены в таблице 16.
Кристаллографические сведения о сольвате свободного основания ABT-263 с анизолом
Перечень пиков на рентгенограмме PXRD сольвата свободного основания ABT-263 с анизолом (вычислены на основании кристаллической структуры)
Для получения монокристаллов сольвата с пиридином кристаллическое свободное основание ABT-263 (900 мг) суспендировали в смеси пиридин/гексан (8 мл, 1:4 объем/объем). Этой суспензии давали отстояться, удаляли супернатант и нагревали до 50°C. Аморфное свободное основание ABT-263 (100 мг) растворяли в этом супернатанте при 50°C и охлаждали полученный раствор до комнатной температуры. Образование монокристаллов наблюдалось через неделю, причем было обнаружено, что они являются сольватом с пиридином. Кристаллографические данные для сольвата с пиридином представлены в таблице 17 и перечень пиков PXRD, вычисленных из кристаллической структуры, приведен в таблице 18.
Кристаллографические сведения о сольвате свободного основания ABT-263 с пиридином
Перечень пиков на рентгенограмме PXRD сольвата свободного основания ABT-263 с пиридином (вычислены на основании кристаллической структуры)
Для получения монокристаллов сольвата с 2-пропанолом приблизительно 100 мг свободного основания ABT-263 растворяли примерно в 1 г этилацетата. Полученный раствор добавляли к 2,7 г 2-пропанола. Добавляли кристаллические затравки формы I свободного основания ABT-263. Образование монокристаллов наблюдалось через два дня. Кристаллографические данные для сольвата с 2-пропанолом представлены в таблице 19 и перечень пиков PXRD, вычисленных из кристаллической структуры, приведен в таблице 20.
Кристаллографические сведения о сольвате свободного основания ABT-263 с 2-пропанолом
Перечень пиков на рентгенограмме PXRD сольвата свободного основания ABT-263 с 2-пропанолом (вычислены на основании кристаллической структуры)
Сравнение с таблицей 3 показывает близкое соответствие между положениями пиков, вычисленных из данных рентгеноструктурного анализа монокристалла, с пиками, обнаруженными на рентгенограмме PXRD. Незначительные смещения некоторых пиков могут отражать различные температурные условия, использованные при осуществлении двух указанных методик (100К для монокристаллов, комнатная температура для PXRD).
Описанная выше методика кристаллизации суспензии является лишь одним из нескольких путей достижения перенасыщенности раствора, необходимой для получения сольватированных кристаллов. Другие пути включают:
- добавление антирастворителя (ABT-263 растворяют в первом растворителе или смеси растворителей, в которых основание растворимо в высокой концентрации, и затем к полученному раствору добавляют антирастворитель, который смешивается с первым растворителем или смесью растворителей);
- варианты описанной выше методики добавления антирастворителя, в которых, например, раствор ABT-263 добавляют к антирастворителю;
- температурный градиент (ABT-263 растворяют в растворителе или смеси растворителей при повышенной температуре и охлаждают полученный раствор до более низких температур, например ниже комнатной температуры);
- выпаривание растворителя (ABT-263 растворяют в растворителе или смеси растворителей, которые затем выпаривают); и
- кристаллизацию в результате реакции (ABT-263 в форме соли с кислотой растворяют в растворителе или смеси растворителей и полученный раствор добавляют к раствору нейтрализующего агента, например гидроксида натрия, карбоната натрия или бикарбоната натрия, что приводит к выделению свободного основания и его кристаллизации; в качестве альтернативы можно использовать соль ABT-263 с основанием, и в этом случае понижают pH добавлением кислого нейтрализующего агента, вызывая выделение и кристаллизацию свободного основания).
При желании можно использовать комбинации перечисленных выше методик. Конкретные детали, например скорость генерации перенасыщения (например, скорость добавления антирастворителя или нейтрализующего агента, скорость охлаждения или скорость выпаривания растворителя), могут быть легко оптимизированы рядовым специалистом в данной области без чрезмерно большого объема экспериментальной работы.
Десольватация сольвата с этанолом/этилацетатом, например, высушиванием на воздухе приводит к получению кристаллической формы свободного основания ABT-263, не содержащей растворителя. Эта кристаллическая форма именуется формой I. Рентгенограмма PXRD формы I свободного основания ABT-263 показана на фиг.1. Пики на рентгенограмме PXRD формы I свободного основания ABT-263 перечислены в таблице 21. Рентгенограмма PXRD, на которой имеются пики, в основном соответствующие показанным на фиг.1 и перечисленным в таблице 21, может использоваться для идентификации кристаллического свободного основания ABT-263, более конкретно, кристаллической формы I свободного основания ABT-263. Фраза «в основном соответствующие показанным» в данном контексте означает: содержащая пики, которые сдвинуты от указанных положений не более чем на 0,2° по углу 2θ.
Перечень пиков на рентгенограмме PXRD не содержащего растворителя кристаллического полиморфа формы I свободного основания ABT-263
Десольватация большинства сольватов, включая сольваты с 1-пропанолом, 2-пропанолом, метанолом, диоксаном/гексаном, метилацетатом/гексаном, этилацетатом, метилацетатом, изопропилацетатом и хлороформом, приводит к получению не содержащей растворителя кристаллической формы свободного основания ABT-263, которая по данным PXRD идентична кристаллической форме, полученной путем десольватации сольвата с этанолом/этилацетатом.
Десольватация сольватов с пиридином, анизолом и трифтортолуолом приводит к получению не содержащей растворителя кристаллической формы свободного основания ABT-263, которая, как показывают данные PXRD, отличается от формы, образующейся при десольватации сольвата с этанолом/этилацетатом. Эта кристаллическая форма, полученная при десольватации сольватов с пиридином, анизолом или трифтортолуолом, именуется формой II. Рентгенограмма PXRD кристаллической формы II свободного основания ABT-263 показана на фиг.2. Пики на рентгенограмме PXRD формы II свободного основания ABT-263 перечислены в таблице 22. Рентгенограмма PXRD, на которой имеются пики, в основном соответствующие показанным на фиг.2 и перечисленным в таблице 22, может использоваться для идентификации кристаллического свободного основания ABT-263, более конкретно, кристаллической формы II свободного основания ABT-263.
Перечень пиков на рентгенограмме PXRD не содержащего растворителя кристаллического полиморфа формы II свободного основания ABT-263
Десольватация сольватов с бензолом и толуолом протекала в разных случаях по-разному с образованием кристаллов, идентифицированных как форма I или форма II. Если образуется продукт с более высокой кристалличностью, он наиболее близко соответствует форме II.
Пики рентгенограммы PXRD, которые особенно характерны для формы I свободного основания ABT-263, в том числе особенно подходят для того, чтобы отличить форму I от формы II, включают пики при значениях угла 2θ 6,21, 6,72, 12,17, 18,03 и 20,10 градусов, в каждом случае ±0,2° 2θ. В одном из вариантов осуществления форма I свободного основания ABT-263 характеризуется наличием пика по крайней мере в каком-либо одном или нескольких из указанных положений. В другом варианте осуществления форма I свободного основания ABT-263 характеризуется по крайней мере наличием пика в каждом из указанных положений. В еще одном варианте осуществления форма I свободного основания ABT-263 характеризуется наличием пика в каждом из положений, показанных в таблице 21.
Пики рентгенограммы PXRD, которые особенно характерны для формы II свободного основания ABT-263, в том числе особенно подходят для того, чтобы отличить форму II от формы I, включают пики при значениях угла 2θ 5,79, 8,60, 12,76, 15,00 и 20,56 градусов, в каждом случае ±0,2° 2θ. В одном из вариантов осуществления форма II свободного основания ABT-263 характеризуется по крайней мере наличием пика в каком-либо одном или нескольких из указанных положений. В другом варианте осуществления форма II свободного основания ABT-263 характеризуется по крайней мере наличием пика в каждом из указанных положений. В еще одном варианте осуществления форма II свободного основания ABT-263 характеризуется наличием пика в каждом из положений, показанных в таблице 22.
Любая из кристаллических форм свободного основания ABT-263, включая сольватированные формы, может применяться в качестве API для получения фармацевтических композиций. Однако не содержащие растворителя формы, например форма I и форма II, как правило, более предпочтительны для этой цели.
Как показано выше, сольватированные формы применимы в качестве интермедиатов способа получения форм, не содержащих растворителя, например формы I и формы II. Следовательно, из настоящего описания должно быть ясно, что один из вариантов настоящего изобретения относится к свободному основанию ABT-263 в кристаллической форме, сольватированному органическим растворителем. Следует понимать, что термин «органический растворитель» в настоящей заявке охватывает индивидуальные органические растворители и смеси органических растворителей. Более конкретно, согласно этому варианту осуществления, изобретение относится к кристаллическому сольвату свободного основания ABT-263, выбранному из группы, состоящей из сольватов с 1-пропанолом, 2-пропанолом, метанолом, бензолом, толуолом, диоксаном/гексаном, метилацетатом/гексаном, этанолом/этилацетатом, этилацетатом, метилацетатом, изопропилацетатом, хлороформом, пиридином, анизолом и трифтортолуолом.
Кроме того, из настоящей заявки должно быть ясно, что один из вариантов осуществления настоящего изобретения относится к способу получения формы I свободного основания ABT-263, включающему десольватацию сольвата свободного основания ABT-263, выбранного из группы, состоящей из сольватов с 1-пропанолом, 2-пропанолом, метанолом, диоксаном/гексаном, метилацетатом/гексаном, этанолом/этилацетатом, этилацетатом, метилацетатом, изопропилацетатом и хлороформом.
Далее, из настоящей заявки должно быть ясно, что один из вариантов осуществления настоящего изобретения относится к способу получения формы II свободного основания ABT-263, включающему десольватацию сольвата свободного основания ABT-263, выбранного из группы, состоящей из сольватов с пиридином, анизолом и трифтортолуолом. В родственном варианте осуществления способ получения формы II свободного основания ABT-263 включает десольватацию сольвата свободного основания ABT-263, выбранного из группы, состоящей из сольватов с бензолом и толуолом.
Кристаллическое свободное основание ABT-263, например форму I, форму II или их комбинацию, можно применять в получении фармацевтических композиций, подходящих для введения любым путем, в том числе пероральным, субъекту при наличии такой необходимости. Таким образом, в некоторых вариантах осуществления настоящего изобретения разработана фармацевтическая композиция, включающая кристаллическое свободное основание ABT-263, а также один или несколько фармацевтически приемлемых эксципиентов. Такие композиции можно получать любыми известными в фармацевтике способами. В одном из вариантов осуществления композиция включает кристаллическую форму I свободного основания ABT-263. В другом варианте осуществления композиция включает кристаллическую форму II свободного основания ABT-263. Согласно любому из этих вариантов осуществления композиция может быть предназначена для доставки, например, пероральным путем. Другие пути введения включают, не ограничиваясь этим, парентеральный, сублингвальный, буккальный, интраназальный, легочный, местный, трансдермальный, интрадермальный, глазной, ушной, ректальный, вагинальный, внутрижелудочный, внутричерепной, интрасиновиальный и внутрисуставный пути.
Если желательно получить свободное основание ABT-263 в форме раствора, например в виде жидкого состава, для перорального или парентерального введения, свободное основание ABT-263, разумеется, не будет присутствовать в таком составе в кристаллической форме; в действительности, наличие кристаллов в таких составах, как правило, нежелательно. Однако кристаллическое свободное основание ABT-263 по настоящему изобретению все же может играть важную роль в качестве API в способе получения таких составов. Таким образом, настоящее изобретение помимо перечисленного относится к способу получения фармацевтической композиции ABT-263 в форме раствора, включающему растворение кристаллического свободного основания ABT-263 в фармацевтически приемлемом растворителе или смеси растворителей. В одном из вариантов осуществления этот способ включает растворение кристаллической формы I свободного основания ABT-263 в растворителе или смеси растворителей. В другом варианте осуществления этот способ включает растворение кристаллической формы II свободного основания ABT-263 в растворителе или смеси растворителей.
Даже если желаемый состав является составом, содержащим свободное основание ABT-263 в аморфной форме, например твердым составом, полученным плавлением, кристаллическое свободное основание ABT-263 может по-прежнему найти применение в качестве API в способе получения такого состава. Например, иллюстративный способ получения твердой дисперсии свободного основания ABT-263 включает:
(a) растворение API, включающего (i) кристаллическое свободное основание ABT-263, (ii) фармацевтически приемлемый водорастворимый полимерный носитель и (iii) фармацевтически приемлемое ПАВ, в подходящем растворителе; и
(b) удаление растворителя с получением твердой матрицы, включающей полимерный носитель и ПАВ и содержащей свободное основание ABT-263, диспергированное в этом носителе в основном в некристаллической форме.
Другой иллюстративный способ включает добавление кристаллического свободного основания ABT-263 к, как минимум, одному фармацевтически приемлемому полимеру и, как минимум, одному солюбилизатору; получение гомогенного расплава из полученной смеси; и оставление расплава для затвердевания с получением твердой дисперсии.
Кристаллические формы свободного основания ABT-263, например форма I, форма II или их смеси, обладают преимуществами перед доступными до настоящего времени аморфными формами в качестве API. Например, очистка API до высокой степени чистоты, требуемой большинством регулирующих органов, более эффективна и, следовательно, является менее дорогостоящей, если API имеет кристаллическую форму в противоположность аморфной форме. Физическая и химическая устойчивость и, следовательно, срок хранения твердого API, как правило, лучше для кристаллической формы по сравнению с аморфной. Легкость обработки кристаллической формы выше, чем у аморфной, которая часто бывает маслянистой или липкой. Высушивание вызывает меньше затруднений и его легче регулировать в случае кристаллических веществ, которые обладают хорошо определяемой температурой высушивания и десольватации, по сравнению с аморфными веществами, которые обладают большим сродством к органическим растворителям и не имеют выраженной температуры высушивания. Распределение размеров частиц можно легче регулировать у кристаллических материалов, например, подбирая условия процесса кристаллизации. Последующая переработка при применении кристаллического API позволяет лучше управлять процессом. При получении жидких составов, например раствора в липидном носителе, кристаллический ABT-263 растворяется быстрее и менее склонен образовывать гель при растворении. Эти преимущества являются иллюстративными и неограничивающими.
Фармацевтические композиции, содержащие кристаллическое свободное основание ABT-263 или полученные с применением кристаллического свободного основания ABT-263 в качестве API, содержат ABT-263 в количестве, которое может быть терапевтически эффективным при введении субъекту, у которого имеется в этом необходимость, в соответствии с подходящей схемой лечения. Дозировки в настоящей заявке выражены в эквивалентных количествах свободного основания, если контекст не предполагает иного. Как правило, разовая доза (количество, вводимое за один прием), которую можно вводить с подходящей частотой, например от двух раз в день до одного раза в неделю, составляет от примерно 10 до примерно 1000 мг. Если частота введения составляет один раз в день (q.d.), разовая доза и дневная доза являются одинаковыми. В качестве иллюстрации, разовая доза ABT-263 в составе композиции по настоящему изобретению может находиться в диапазоне от примерно 25 до примерно 1000 мг, чаще от примерно 50 до примерно 500 мг, например может составлять примерно 50, примерно 100, примерно 150, примерно 200, примерно 250, примерно 300, примерно 350, примерно 400, примерно 450 или примерно 500 мг. Если композицию получают в виде дискретной дозированной формы, например таблеток или капсул, разовая доза может вводиться с помощью одной единицы дозированной формы или небольшого количества единиц дозированной формы, чаще всего от 1 до примерно 10 единиц дозированной формы.
Чем выше разовая доза, тем более желательным становится выбор эксципиентов, которые допускают относительно высокое содержание API (в данном случае свободного основания ABT-263) в составе. Как правило, концентрация свободного основания ABT-263 в составе, полученном по настоящему изобретению, составляет, как минимум, примерно 1%, например, от примерно 1% до примерно 25% по массе, но в конкретных случаях могут оказаться приемлемыми или достижимыми более высокие или более низкие концентрации. В качестве иллюстрации, эквивалентная концентрация свободного основания ABT-263 в различных вариантах осуществления составляет, как минимум, примерно 2%, например от примерно 2% до примерно 20% по массе, например примерно 5%, примерно 10% или примерно 15% по массе от массы состава.
Композиция, полученная в соответствии с настоящим изобретением, помимо API включает один или несколько фармацевтически приемлемых эксципиентов. Если композицию необходимо получить в виде твердой формы для перорального введения, например, в виде таблеток или капсул, она, как правило, включает, как минимум, один или несколько твердых разбавителей и одно или несколько твердых дезинтегрирующих средств. Кроме этого, в число эксципиентов необязательно входят одно или несколько связующих средств, смачивающих средств и/или антифрикционных средств (смазывающих средств, средств против адгезии и/или средств, способствующих скольжению). Многие наполнители в фармацевтической композиции имеют две или несколько функций. Приведенное в настоящей заявке указание на ту или иную функцию конкретного эксципиента, например разбавителя, дезинтегрирующего средства, связующего средства и т.д., не следует истолковывать, как ограничение только этой функцией. Дополнительную информацию об эксципиентах можно найти в стандартных справочных руководствах, например Handbook of Pharmaceutical Excipients, 3rd ed. (Kibbe, ed. (2000), Washington: American Pharmaceutical Association).
Подходящие разбавители, в качестве иллюстрации, включают, индивидуально или в составе комбинации, лактозу, в том числе безводную лактозу и моногидрат лактозы; лактит; мальтит; маннит; сорбит; ксилит; декстрозу и моногидрат декстрозы; фруктозу; сахарозу и разбавители на основе сахарозы, например прессованный сахар, кондитерский сахар и сахарные шарики; мальтозу; инозит; гидролизованные твердые компоненты злаков; крахмалы (например, кукурузный крахмал, пшеничный крахмал, рисовый крахмал, картофельный крахмал, крахмал маниока и т.д.), крахмалистые компоненты, например амилоза и декстраты и модифицированные или обработанные крахмалы, например прежелатинизированный крахмал; декстрины; целлюлозы, включая порошкообразную целлюлозу, микрокристаллическую целлюлозу, силицифицированную микрокристаллическую целлюлозу, α- и аморфную целлюлозу и порошкообразную целлюлозу из пищевых источников, и ацетат целлюлозы; кальциевые соли, включая карбонат кальция, трехосновный фосфат кальция, дигидрат двухосновного фосфата кальция, моногидрат одноосновного сульфата кальция, сульфат кальция и гранулированный тригидрат лактата кальция; карбонат магния; оксид магния; бентонит; каолин; хлорид натрия; и т.п. Эти разбавители, если они присутствуют в композиции, как правило, составляют в общей сложности от примерно 5% до примерно 95%, например от примерно 20% до примерно 90% или от примерно 50% до примерно 85% от массы композиции. Выбранный растворитель или растворители предпочтительно демонстрируют подходящую сыпучесть и, если желательно получить таблетки, прессуемость.
Микрокристаллическая целлюлоза и силицифицированная микрокристаллическая целлюлоза являются особенно подходящими разбавителями и необязательно применяются в комбинации с водорастворимыми разбавителями, например маннитом. В качестве иллюстрации, подходящее массовое соотношение микрокристаллической целлюлозы или силицифицированной микрокристаллической целлюлозы и маннита составляет от примерно 10:1 до примерно 1:1, но в определенных обстоятельствах могут найти применение соотношения, выходящие за пределы этого диапазона.
Подходящие дезинтегрирующие средства включают, либо индивидуально, либо в комбинации, крахмалы, в том числе прежелатинизированный крахмал и натрий крахмал гликолят; глины; силикат алюминия магния; дезинтегрирующие средства на основе целлюлозы, например порошкообразную целлюлозу, микрокристаллическую целлюлозу, метилцеллюлозу, низкозамещенную гидроксипропилцеллюлозу, кармеллозу, кальций кармеллозу, натрий кармеллозу и натрий кросскармеллозу; альгинаты; повидон; кросповидон; калий полакрилин; камеди, например агар, гуаровую камедь, камедь плодов рожкового дерева, камедь карайи, пектин и камедь трагаканта; коллоидный диоксид кремния, и т.п. Одно или несколько дезинтегрирующих средств, если они присутствуют в композиции, как правило, в общей сложности составляют от примерно 0,2% до примерно 30%, например от примерно 0,5% до примерно 20% или от примерно 1% до примерно 10% от массы композиции.
Натрий крахмал гликолят является особенно подходящим дезинтегрирующим средством, и, как правило, его количество составляет в общей сложности от примерно 1% до примерно 20%, например от примерно 2% до примерно 15% или от примерно 5% до примерно 10% от массы композиции.
Связующие средства или адгезивы являются важными эксципиентами, особенно, если композиция имеет форму таблеток. Эти связующие средства и адгезивы должны придавать достаточную силу сцепления смеси, предназначенной для таблетирования, чтобы обеспечить нормальное проведение таких операций, как, например, придание размера, смазывание, прессование и упаковка, но в то же время позволять таблетке распадаться и абсорбироваться после приема. Подходящие связующие средства и адгезивы включают, либо индивидуально, либо в комбинации, гуммиарабик; трагакант; глюкозу; полидекстрозу; крахмал, включая предварительно желатинизированный крахмал; желатин; модифицированные целлюлозы, включая метилцеллюлозу, натрий кармеллозу, гидроксипропилметилцеллюлозу (HPMC), гидроксипропилцеллюлозу, гидроксиэтилцеллюлозу и этилцеллюлозу; декстрины, включая мальтодекстрин; зеин; альгиновую кислоту и соли альгиновой кислоты, например альгинат натрия; алюмосиликат магния; бентонит; полиэтиленгликоль (PEG); полиэтиленоксид; гуаровую камедь; полисахаридные кислоты; поливинилпирролидон (повидон или PVP), например повидон K-15, K-30 и K-29/32; полиакриловые кислоты (карбомеры); полиметакрилаты, и т.п. Одно или несколько связующих средств и/или адгезивов, если они присутствуют в композиции, составляют в общей сложности от примерно 0,5% до примерно 25%, например от примерно 1% до примерно 15% или от примерно 1,5% до примерно 10% от массы композиции.
Особенно подходящими связующими веществами для получения таблеток являются повидон и гидроксипропилцеллюлоза, либо индивидуально, либо в комбинации, и, если эти вещества входят в состав, их количество, как правило, составляет от примерно 0,5% до примерно 15%, например от примерно 1% до примерно 10% или от примерно 2% до примерно 8% от массы композиции.
Смачивающие средства, если они присутствуют в композиции, обычно выбирают таким образом, чтобы поддержать тесное взаимодействие лекарственного средства с водой, т.е. условия, которые могут улучшить биодоступность композиции. Неограничивающие примеры ПАВ, которые могут применяться в качестве смачивающих средств, включают, индивидуально либо в комбинации, четвертичные аммониевые соединения, например бензалкония хлорид, бензетония хлорид и цетилпиридиния хлорид; диоктил сульфосукцинат натрия; полиоксиэтилен алкилфениловые эфиры, например ноноксинол 9, ноноксинол 10 и октоксинол 9; полоксамеры (блок-сополимеры полиоксиэтилена и полиоксипропилена); глицериды и масла полиоксиэтилен жирных кислот, например полиоксиэтилен (8) каприловой/каприновой кислоты моно- и диглицериды, полиоксиэтилен (35) касторовое масло и полиоксиэтилен (40) гидрированное касторовое масло; полиоксиэтилен алкиловые простые эфиры, например цетет-10, лаурет-4, лаурет-23, олет-2, олет-10, олет-20, стеарет-2, стеарет-10, стеарет-20, стеарет-100 и полиоксиэтилен (20) цетостеариловый эфир; сложные эфиры полиоксиэтилена и жирных кислот, например полиоксиэтилена (20) стеарат, полиоксиэтилена (40) стеарат и полиоксиэтилена (100) стеарат; сложные эфиры сорбитана, например сорбитана монолаурат, сорбитана моноолеат, сорбитана монопальмитат и сорбитана моностеарат; полиоксиэтилен сорбитановые эфиры, например полисорбат 20 и полисорбат 80; сложные эфиры пропиленгликоля и жирных кислот, например пропиленгликоля лаурат; натрия лаурилсульфат; жирные кислоты и их соли, например олеиновая кислота, олеат натрия и триэтаноламина олеат; эфиры глицерина и жирных кислот, например глицерил моноолеат, глицерил моностеарат и глицерил пальмитостеарат; тилоксапол, и т.п. Одно или несколько смачивающих средств, если они входят в состав композиции, как правило, составляют в общей сложности от примерно 0,1% до примерно 15%, например от примерно 0,2% до примерно 10% или от примерно 0,5% до примерно 7% от массы композиции.
Неионные ПАВ, более конкретно полоксамеры, являются примерами смачивающих средств, которые могут применяться в составах по настоящему изобретению. В качестве иллюстрации, полоксамер, например PluronicTM F127, если он включен в композицию, может составлять от примерно 0,1% до примерно 10%, например от примерно 0,2% до примерно 7% или от примерно 0,5% до примерно 5% от массы композиции.
Смазывающие средства уменьшают трение между таблетируемой смесью и таблетирующим оборудованием во время прессования таблеток. Подходящие смазывающие средства включают, индивидуально или в комбинации, глицерил бегенат; стеариновую кислоту и ее соли, включая стеараты магния, кальция и натрия; гидрированные растительные масла; глицерил пальмитостеарат; тальк; воски; бензоат натрия; ацетат натрия; фумарат натрия; стеарилфумарат натрия; полиэтиленгликоли (ПЭГ) (например, ПЭГ 4000 и ПЭГ 6000); полоксамеры; поливиниловый спирт; олеат натрия; лаурилсульфат натрия; лаурилсульфат магния, и т.п. Одно или несколько смазывающих средств, если они включены в композицию, как правило, составляют в общей сложности от примерно 0,05% до примерно 10%, например от примерно 0,1% до примерно 5% или от примерно 0,2% до примерно 2% от массы композиции. Особенно подходящим смазывающим средством является стеарилфумарат натрия.
Средства против адгезии уменьшают прилипание состава таблеток к поверхностям оборудования. Подходящие средства против адгезии включают, индивидуально либо в комбинации, тальк, коллоидный диоксид кремния, крахмал, DL-лейцин, лаурилсульфат натрия и стеараты металлов. Одно или несколько средств против адгезии, если они включены в композицию, как правило составляют в общей сложности от примерно 0,05% до примерно 10%, например от примерно 0,1% до примерно 7%, от примерно 0,2% до примерно 5% от массы композиции. Особенно подходящим средством против адгезии является коллоидный диоксид кремния.
Средства для улучшения скольжения улучшают сыпучесть и снижают статическое усилие в таблетируемой смеси. Подходящие средства для улучшения скольжения включают, индивидуально либо в комбинации, коллоидный диоксид кремния, крахмал, порошкообразную целлюлозу, лаурилсульфат натрия, трисиликат магния и стеараты металлов. Одно или несколько средств для улучшения скольжения, если они включены в композицию, как правило, составляют в общей сложности от примерно 0,05% до примерно 10%, например от примерно 0,1% до примерно 7% или от примерно 0,2% до примерно 5% от массы композиции. Особенно подходящим средством для улучшения скольжения является коллоидный диоксид кремния.
В фармацевтической технике известны и могут применяться в композициях по настоящему изобретению другие эксципиенты, например буферирующие средства, стабилизаторы, антиоксиданты, противомикробные средства, красители, вкусоароматические добавки и подсластители. Таблетки могут не иметь покрытия или могут включать ядро, которое покрыто, например, нефункциональной пленкой или покрытием, модифицирующим высвобождение, или кишечным покрытием. Капсулы могут иметь твердые или мягкие оболочки, включающие, например, желатин (в форме твердых желатиновых капсул или мягких эластичных желатиновых капсул), крахмал, каррагенан и/или HPMC, необязательно совместно с одним или несколькими пластификаторами.
Твердые композиции для пероральной доставки по настоящему изобретению не ограничиваются каким-либо способом их получения. Может применяться любой подходящий способ фармацевтики, включая смешивание с непосредственным прессованием или без него, а также влажное или сухое гранулирование.
Если композицию необходимо получить в жидкой форме (включая инкапсулированную жидкую форму), API (кристаллическое свободное основание ABT-263) можно, например, растворить в подходящем носителе, как правило, носителе, включающем липидный растворитель для API. Чем выше разовая доза, тем более желательно выбрать носитель, который допускает относительно высокие концентрации действующего средства в растворе. Как правило, эквивалентная концентрация свободного основания API в носителе составляет не менее чем примерно 10 мг/мл, например от приблизительно 10 до приблизительно 500 мг/мл, но более низкие и более высокие концентрации могут быть приемлемы или достижимы в конкретных случаях. В качестве иллюстрации, концентрация действующего средства в различных вариантах осуществления составляет, как минимум, от примерно 10 мг/мл, например от примерно 10 до примерно 250 мг/мл, или от примерно 20 мг/мл, например от примерно 20 до примерно 200 мг/мл, например примерно 20, примерно 25, примерно 30, примерно 40, примерно 50, примерно 75, примерно 100 или примерно 150 мг/мл.
Носитель может быть в основном неводным, т.е. не содержать воды или содержать незначительное количество воды, достаточно малое для того, чтобы с практической точки зрения она почти не оказывала вредного воздействия на эффективность или свойства композиции. Как правило, носитель включает от нуля до менее примерно 5% по массе воды. Следует понимать, что некоторые ингредиенты, применяемые в композиции, могут связывать небольшие количества воды своими молекулами или надмолекулярными структурами; такая связанная вода, если она присутствует в композиции, не влияет на «в основном неводный» характер носителя, определенный выше по тексту абзаца.
В некоторых вариантах осуществления носитель включает один или несколько глицеридов. Подходящие глицериды включают, не ограничиваясь этим, моно-, ди- или триглицериды с цепями от средних до длинных. Термин «средняя цепь» в настоящей заявке относится к углеводородным цепям, каждая из которых содержит не менее примерно 6 и менее примерно 12 атомов углерода, включая, например, цепи C8-C10. В настоящей заявке примерами глицеридов «со средней цепью» являются глицериды, включающие каприлильные и каприльные цепи, например моно-, ди- или триглицериды каприловой/каприновой кислоты. Термин «длинная цепь» в настоящей заявке относится к углеводородным цепям, каждая из которых содержит не менее примерно 12, например от приблизительно 12 до приблизительно 18 атомов углерода, включая, например, такие углеводородные остатки, как лаурил, миристил, цетил, стеарил, олеил, линолеил и линоленил. Углеводородные группы со средними-длинными цепями в глицеридах могут быть насыщенными, моно- или полиненасыщенными.
В одном из вариантов осуществления носитель включает триглицериды со средними и/или длинными цепями. Подходящими примерами триглицерида с цепью средней длины являются триглицериды каприловой/каприновой кислот, как, например, Captex 355 EPTM Abitec Corp. и продукты, в основном эквивалентные ему. Подходящие примеры триглицеридов с длинной цепью включают фармацевтически приемлемые растительные масла, например масло канолы, кокосовое масло, кукурузное масло, масло хлопчатника, льняное масло, оливковое масло, пальмовое масло, саффлоровое масло, кунжутное масло, соевое масло и подсолнечное масло, а также смеси этих масел. Кроме того, можно применять жиры животного происхождения, в том числе, например, рыбий жир.
Было обнаружено, что особенно подходящая система носителей включает два основанных компонента: фосфолипид и фармацевтически приемлемый солюбилизирующий агент для фосфолипида. Следует понимать, что упоминание фосфолипида, солюбилизирующего агента или других ингредиентов композиции в единственном числе в настоящей заявке включает и множественное число; таким образом, комбинации, например, смеси более чем одного фосфолипида или более чем одного солюбилизирующего агента, в явном виде входят в объем настоящей заявки. Солюбилизирующий агент или комбинация солюбилизирующих агентов и фосфолипид также солюбилизируют действующий ингредиент, хотя другие носители, например ПАВ или спирт, такой как этанол, необязательно входящий в носитель, могут в некоторых ситуациях обеспечить улучшенную солюбилизацию действующего ингредиента.
Может применяться любой фармацевтически приемлемый фосфолипид или смесь фосфолипидов. В основном такие фосфолипиды являются сложными эфирами фосфорной кислоты, которые образуются при гидролизе фосфорной кислоты, жирной кислоты (кислот), спирта и азотистого основания. Фармацевтически приемлемые фосфолипиды могут включать, не ограничиваясь этим, фосфатидилхолины, фосфатидилсерины и фосфатидилэтаноламины. В одном из вариантов осуществления композиция по настоящему изобретению включает фосфатидилхолин, полученный, например, из природного лецитина. Может применяться лецитин из любого источника, включая животные продукты, например яичный желток, но, как правило, предпочтительными являются растительные продукты. Соя представляет собой особенно богатый источник лецитина, который может обеспечить получение фосфатидилхолина для применения в настоящем изобретении.
В качестве иллюстрации, подходящее количество фосфолипида составляет от примерно 15% до примерно 75%, например от примерно 30% до примерно 60% от массы носителя, хотя в конкретных случаях могут применяться большие и меньшие количества.
Ингредиенты, применимые в качестве компонентов солюбилизирующего агента, конкретно не ограничены и в определенной степени зависят от желаемой концентрации действующего средства и от фосфолипида. В одном из вариантов осуществления солюбилизирующий агент включает один или несколько гликолей, один или несколько гликолидов и/или один или несколько глицеридов.
Гликоли, как правило, подходят только для неинкапсулированных составов, или если предполагается применять капсулы с мягкой оболочкой, и они обычно несовместимы с твердыми оболочками, например твердыми желатиновыми оболочками. Подходящие гликоли включают пропиленгликоль и полиэтиленгликоли (ПЭГ), имеющие молекулярную массу от примерно 200 до примерно 1000 г/моль, например ПЭГ-400, который имеет среднюю молекулярную массу примерно 400 г/моль. Такие гликоли могут обеспечить относительно высокую растворимость действующего ингредиента; однако потенциал окислительного разложения ABT-263 может увеличиться, если соединение растворено в носителе, включающем такие гликоли, например, из-за способности гликолей образовывать супероксиды, пероксиды и/или свободные гидроксильные радикалы. Чем выше содержание гликоля в носителе, тем больше может быть тенденция к разрушению ABT-263. Поэтому, в одном из вариантов осуществления, в композиции присутствует один или несколько гликолей в общем количестве не менее примерно 1%, но менее примерно 50%, например менее примерно 30%, менее примерно 20%, менее примерно 15%, менее примерно 10% от массы носителя. В другом варианте осуществления носитель в основном не содержит гликоля.
Гликолиды представляют собой гликоли, например пропиленгликоль или ПЭГ, этерифицированные одной или несколькими органическими кислотами, например жирными кислотами со средней-длинной цепью. Подходящие примеры включают монокаприлат пропиленгликоля, монолаурат пропиленгликоля и дилаурат пропиленгликоля, например такие продукты, как Capmul PG-8TM, Capmul PG-12TM и Capmul PG-2LTM, соответственно, производства Abitec Corp. и продукты, в основном эквивалентные указанным.
Глицериды, подходящие для совместного применения с фосфолипидами, включают, не ограничиваясь этим, перечисленные выше продукты. Если один или несколько глицеридов присутствуют в качестве основного компонента солюбилизирующего агента, подходящее общее количество глицеридов является количеством, эффективным для солюбилизации фосфолипида и в комбинации с другими компонентами носителя является эффективным для удержания действующего ингредиента и антиоксиданта в растворе. Например, глицериды, такие как триглицериды со средней и/или длинной цепью, могут присутствовать в общем количестве от примерно 5% до примерно 70%, например от примерно 15% до примерно 60% или от примерно 25% до примерно 50% от массы носителя.
При желании можно включать в состав дополнительные солюбилизирующие агенты, которые не являются гликолями, гликолидами или глицеридами. Такие агенты, например, N-замещенные амидные растворители, например диметилформамид (ДМФА) и N,N-диметилацетамид (DMA), в отдельных случаях могут способствовать увеличению предела растворимости действующего ингредиента в носителе, позволяя, тем самым, увеличить его содержание в препарате. Однако носители, применяемые в настоящем изобретении, обычно обеспечивают достаточную растворимость ABT-263 без таких дополнительных агентов.
Даже если имеется достаточное количество гликоля, гликолида или глицерида для солюбилизации фосфолипида, полученный раствор в носителе и/или система действующий ингредиент-носитель могут быть слишком вязкими и их обработка может оказаться сложной или неудобной. В таких случаях может оказаться желательным включение в носитель агента, снижающего вязкость, в количестве, эффективном для достижения приемлемо низкой вязкости. Примером такого агента является спирт, более конкретно этанол, который предпочтительно вводят в форме, в основном не содержащей воды, например в форме 99% этанола, дегидратированного спирта USP или абсолютного этанола. Однако, как правило, следует избегать избыточно высоких концентраций этанола. Это особенно справедливо, если, например, систему действующий ингредиент-носитель предполагается вводить в желатиновой капсуле, поскольку высокие концентрации этанола обычно приводят к механическому разрушению капсулы. Как правило, подходящие количества этанола находятся в пределах от 0% до примерно 25%, например от примерно 1% до примерно 20%, от примерно 3% до примерно 15% от массы носителя. Гликоли, например, пропиленгликоль или ПЭГ и моно- и диглицериды со средней цепью (например, моно- и диглицериды каприловой/каприновой кислот), также могут нуждаться в понижении вязкости; если систему действующий ингредиент-носитель предполагается инкапсулировать в твердые капсулы, например твердые желатиновые капсулы, в этом случае особенно применимы моно- и диглицериды со средней цепью.
Необязательно, носитель по настоящему изобретению дополнительно включает фармацевтически приемлемое нефосфолипидное ПАВ. Специалист в данной области будет способен выбрать подходящее ПАВ для применения в композиции по настоящему изобретению. В качестве иллюстрации, в состав композиции можно включить такое ПАВ, как полисорбат 80, в количестве от 0% до примерно 5%, например от примерно 0% до примерно 2% или от 0% до примерно 1% от массы носителя.
Как правило, доступны готовые, заранее полученные смеси, содержащие комбинацию подходящего фосфолипида и солюбилизирующего агента, для применения в композициях по настоящему изобретению. Применение готовых смесей фосфолипида и солюбилизирующего агента может быть предпочтительным с точки зрения облегчения получения композиций по настоящему изобретению.
Иллюстративным примером готовой смеси фосфолипида и солюбилизирующего агента является продукт Phosal 50 PGTM, который можно приобрести у Phospholipid GmbH, Germany, и который включает, по массе, не менее 50% фосфатидилхолина, не более 6% лизофосфатидилхолина, примерно 35% пропиленгликоля, примерно 3% моно- и диглицеридов из подсолнечного масла, примерно 2% соевых жирных кислот, примерно 2% этанола и примерно 0,2% аскорбилпальмитата.
Другим иллюстративным примером является Phosal 53 MCTTM, который также можно приобрести у Phospholipid GmbH и который включает, по массе, не менее 53% фосфатидилхолина, не более 6% лизофосфатидилхолина, примерно 29% триглицеридов со средней цепью, 3-6% (как правило, примерно 5%) этанола, примерно 3% моно- и диглицеридов из подсолнечного масла, примерно 2% олеиновой кислоты и примерно 0,2% аскорбилпальмитата (типовой состав). Продукт, имеющий указанный выше или в основном эквивалентный состав, независимо от того, продается ли он под торговым наименованием Phosal 53 MCTTM или иным, как правило, именуется в настоящей заявке «фосфатидилхолин + триглицериды со средней цепью 53/29». Продукт, имеющий «в основном эквивалентный состав», в данном контексте означает имеющий состав, в основном подобный типовому составу с точки зрения перечня ингредиентов и относительных количеств ингредиентов и не проявляющий практического различия в свойствах с точки зрения применения продукта по настоящей заявке.
Следующим иллюстративным примером является Lipoid S75TM, который можно приобрести у Lipoid GmbH, который содержит, по массе, не менее 70% фосфатидилхолина в солюбилизирующей системе. Этот продукт можно дополнительно смешать с триглицеридами со средней цепью, например, в соотношении 30/70 по массе с получением продукта («Lipoid S75TM MCT»), содержащего, по массе, не менее 20% фосфатидилхолина, 2-4% фосфатидилэтаноламина, не более 1,5% лизофосфатидилхолина и 67-73% триглицеридов со средней цепью.
Еще одним иллюстративным примером является Phosal 50 SA+TM, который можно приобрести у Phospholipid GmbH, и который включает, по массе, не менее 50% фосфатидилхолина, не более 6% лизофосфатидилхолина, в солюбилизирующей системе, включающей саффлоровое масло и другие ингредиенты.
Фосфатидилхолиновый компонент каждой из этих готовых смесей получен из соевого лецитина. Продукты в основном эквивалентного состава можно приобрести у других поставщиков.
Готовые смеси, например, Phosal 50 PGTM, Phosal 53 MCTTM, Lipoid S75TM MCT или Phosal 50 SA+TM в некоторых вариантах осуществления могут практически целиком составлять систему носителя в композиции по настоящему изобретению. В других вариантах осуществления присутствуют дополнительные ингредиенты, например этанол (дополнительно к любому количеству, которое, возможно, присутствует в упомянутой готовой смеси), нефосфолипидное ПАВ, например, полисорбат 80, полиэтиленгликоль и/или другие ингредиенты. Эти дополнительные ингредиенты, если они присутствуют, как правило, включены в композицию лишь в незначительных количествах. В качестве иллюстрации, компонент «фосфатидилхолин + триглицериды со средней цепью 53/29» может быть включен в количестве от примерно 50% до 100%, например от примерно 80% до 100% от массы носителя.
В опубликованной заявке на патент США № 2009/0149461, поданной Krivoshik и включенной в настоящую заявку посредством ссылки, без признания того, что она составляет известный уровень техники по отношению к настоящему изобретению, описано клиническое испытание, в котором в качестве исследуемого препарата участвовал ABT-263 в форме порошка для приготовления перорального раствора, который получали смешиванием (25 мг/мл) с разбавителями, входящими в состав Phosal 53 MCTTM и дегидратированным спиртом.
ABT-263 чувствителен к разрушению в окислительной среде; таким образом, часто может оказаться желательным включение в композицию по настоящему изобретению антиоксиданта. Антиоксиданты, применяемые в фармацевтических композициях, чаще всего являются агентами, которые ингибируют образование окисляющих частиц, как, например, триплетного или синглетного кислорода, супероксидов, пероксидов и свободных гидроксильных радикалов, или агентами, которые поглощают эти окисляющие частицы после их образования. Примеры широко применяемых антиоксидантов этих классов включают бутилированный гидроксианизол (BHA), бутилированный гидрокситолуол (BHT), ретинилпальмитат, токоферол, пропилгаллат, аскорбиновую кислоту и аскорбилпальмитат. В композициях по настоящему изобретению могут применяться перечисленные антиоксиданты; в качестве альтернативы особенно подходящими могут являться антиоксиданты, включающие атомы тяжелых халькогенов.
Халькогены представляют собой элементы 16 группы (ранее известной как группа VIA) периодической системы элементов, включая кислород, серу, селен и теллур. Термин «тяжелые халькогены» в настоящей заявке означает халькогены с большей атомной массой, чем у кислорода, и конкретно в их число входят сера и селен. «Антиоксидант, включающий тяжелый халькоген» или «HCA» является соединением, обладающим антиоксидантными свойствами, которые содержат один или несколько способных к окислению атомов серы или селена, более конкретно атомы серы. Не ограничиваясь какой-либо конкретной теорией, полагают, что HCA действуют, в первую очередь, как конкурентные субстраты, т.е. «жертвенные» антиоксиданты, которые, в первую очередь, атакуются окисляющими частицами, тем самым, защищая действующий ингредиент от чрезмерного разрушения.
В некоторых вариантах осуществления HCA включают один или несколько антиоксидантов формулы (II):
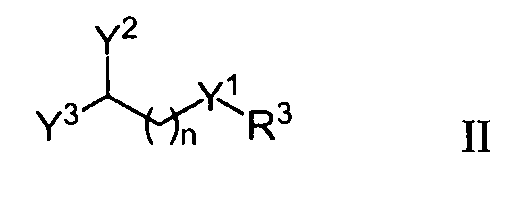
где
n означает 0, 1 или 2;
Y1 означает S или Se;
Y2 означает NHR1, OH или H, где R1 представляет собой алкил или алкилкарбонил;
Y3 означает COOR2 или CH2OH, где R2 представляет собой H или алкил; и
R3 означает H или алкил;
где алкильные группы независимо необязательно замещены одним или несколькими заместителями, независимо выбранными из группы, состоящей из карбоксила, алкилкарбонила, алкоксикарбонила, амино и алкилкарбониламино; или их фармацевтически приемлемых солей; или, если Y1 означает S и R3 означает H, -S-S- димеров соединений формулы (II) или фармацевтически приемлемых солей этих димеров.
В других вариантах осуществления HCA представляет собой антиоксидант формулы (III):
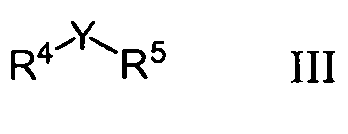
где
Y означает S, Se или S-S; и
R4 и R5 независимо выбраны из H, алкила и фрагмента (CH2)nR6, где n означает 0-10; и R6 представляет собой арилкарбонил, алкилкарбонил, алкоксикарбонил, карбоксил или CHR7R8-замещенный алкил, где R7 и R8 независимо означают CO2R9, CH2OH, водород или NHR10, где R9 представляет собой H, алкил, замещенный алкил или арилалкил, и R10 означает водород, алкил, алкилкарбонил или алкоксикарбонил.
«Алкильный» заместитель или «алкильная» или «алкокси» группы, образующие часть заместителя в формуле (II) или формуле (III), представляют собой группы, включающие от 1 до примерно 18 атомов углерода, и могут иметь линейную или разветвленную цепь.
«Арильная» группа, образующая часть заместителя в формуле (III), является фенильной группой, незамещенной или замещенной одной или несколькими гидрокси, алкокси или алкильными группами.
В некоторых вариантах осуществления R1 в формуле (II) означает C1-4алкил (например, метил или этил) или (C1-4алкил)карбонил (например, ацетил).
В некоторых вариантах осуществления R2 в формуле (II) означает H или C1-18алкил, например, метил, этил, пропил (например, н-пропил или изопропил), бутил (например, н-бутил, изобутил или т-бутил), октил (например, н-октил или 2-этилгексил), додецил (например, лаурил), тридецил, тетрадецил, гексадецил или октадецил (например, стеарил).
R3, как правило, представляет собой H или C1-4алкил (например, метил или этил).
HCA может представлять собой, например, природную или синтетическую аминокислоту или ее производное, например, алкиловый эфир или N-ацильное производное или соль такой аминокислоты или производного. Если аминокислота или ее производное получены из природных источников, они, как правило, находятся в L-конфигурации; однако имеется в виду, что можно получать замещенные D-изомеры и смеси D,L-изомеров, если это необходимо.
Неограничивающие примеры HCA, применимых в настоящем изобретении, включают β-алкилмеркаптокетоны, цистеин, цистин, гомоцистеин, метионин, тиодигликолевую кислоту, тиодипропионовую кислоту, тиоглицерин, селеноцистеин, селенометионин и их соли, сложные эфиры, амиды и тиоэфиры; а также их комбинации. Более конкретно, один или несколько HCA могут быть выбраны из N-ацетилцистеина, бутилового эфира N-ацетилцистеина, додецилового эфира N-ацетилцистеина, этилового эфира N-ацетилцистеина, метилового эфира N-ацетилцистеина, октилового эфира N-ацетилцистеина, пропилового эфира N-ацетилцистеина, стеарилового эфира N-ацетилцистеина, тетрадецилового эфира N-ацетилцистеина, тридецилового эфира N-ацетилцистеина, N-ацетилметионина, бутилового эфира N-ацетилметионина, додецилового эфира N-ацетилметионина, этилового эфира N-ацетилметионина, метилового эфира N-ацетилметионина, октилового эфира N-ацетилметионина, пропилового эфира N-ацетилметионина, стеарилового эфира N-ацетилметионина, тетрадецилового эфира N-ацетилметионина, тридецилового эфира N-ацетилметионина, N-ацетилселеноцистеина, бутилового эфира N-ацетилселеноцистеина, додецилового эфира N-ацетилселеноцистеина, этилового эфира N-ацетилселеноцистеина, метилового эфира N-ацетилселеноцистеина, октилового эфира N-ацетилселеноцистеина, пропилового эфира N-ацетилселеноцистеина, стеарилового эфира N-ацетилселеноцистеина, тетрадецилового эфира N-ацетилселеноцистеина, тридецилового эфира N-ацетилселеноцистеина, N-ацетилселенометионина, бутилового эфира N-ацетилселенометионина, додецилового эфира N-ацетилселенометионина, этилового эфира N-ацетилселенометионина, метилового эфира N-ацетилселенометионина, октилового эфира N-ацетилселенометионина, пропилового эфира N-ацетилселенометионина, стеарилового эфира N-ацетилселенометионина, тетрадецилового эфира N-ацетилселенометионина, тридецилового эфира N-ацетилселенометионина, цистеина, бутилового эфира цистеина, додецилового эфира цистеина, этилового эфира цистеина, метилового эфира цистеина, октилового эфира цистеина, пропилового эфира цистеина, стеарилового эфира цистеина, тетрадецилового эфира цистеина, тридецилового эфира цистеина, цистина, дибутилового эфира цистина, ди(додецилового)эфира цистина, диэтилового эфира цистина, диметилового эфира цистина, диоктилового эфира цистина, дипропилового эфира цистина, дистеарилового эфира цистина, ди(тетрадецилового)эфира цистина, ди(тридецилового)эфира цистина, N,N-диацетилцистина, дибутилового эфира N,N-диацетилцистина, диэтилового эфира N,N-диацетилцистина, ди(додецилового)эфира N,N-диацетилцистина, диметилового эфира N,N-диацетилцистина, диоктилового эфира N,N-диацетилцистина, дипропилового эфира N,N-диацетилцистина, дистеарилового эфира N,N-диацетилцистина, ди(тетрадецилового) эфира N,N-диацетилцистина, ди(тридецилового) эфира N,N-диацетилцистина, дибутил тиодигликолята, дибутил тиодипропионата, ди(додецил) тиодигликолята, ди(додецил) тиодипропионата, диэтил тиодигликолята, диэтил тиодипропионата, диметил тиодигликолята, диметил тиодипропионата, диоктил тиодигликолята, диоктил тиодипропионата, дипропил тиодигликолята, дипропил тиодипропионата, дистеарил тиодигликолята, дистеарил тиодипропионата, ди(тетрадецил) тиодигликолята, ди(тетрадецил) тиодипропионата, гомоцистеина, бутилового эфира гомоцистеина, додецилового эфира гомоцистеина, этилового эфира гомоцистеина, метилового эфира гомоцистеина, октилового эфира гомоцистеина, пропилового эфира гомоцистеина, стеарилового эфира гомоцистеина, тетрадецилового эфира гомоцистеина, тридецилового эфира гомоцистеина, метионина, бутилового эфира метионина, додецилового эфира метионина, этилового эфира метионина, метилового эфира метионина, октилового эфира метионина, пропилового эфира метионина, стеарилового эфира метионина, тетрадецилового эфира метионина, тридецилового эфира метионина, S-метилцистеина, бутилового эфира S-метилцистеина, додецилового эфира S-метилцистеина, этилового эфира S-метилцистеина, метилового эфира S-метилцистеина, октилового эфира S-метилцистеина, пропилового эфира S-метилцистеина, стеарилового эфира S-метилцистеина, тетрадецилового эфира S-метилцистеина, тридецилового эфира S-метилцистеина, селеноцистеина, бутилового эфира селеноцистеина, додецилового эфира селеноцистеина, этилового эфира селеноцистеина, метилового эфира селеноцистеина, октилового эфира селеноцистеина, пропилового эфира селеноцистеина, стеарилового эфира селеноцистеина, тетрадецилового эфира селеноцистеина, тридецилового эфира селеноцистеина, селенометионина, бутилового эфира селенометионина, додецилового эфира селенометионина, этилового эфира селенометионина, метилового эфира селенометионина, октилового эфира селенометионина, пропилового эфира селенометионина, стеарилового эфира селенометионина, тетрадецилового эфира селенометионина, тридецилового эфира селенометионина, тиодигликолевой кислоты, тиодипропионовой кислоты, тиоглицерина, их изомеров и смесей их изомеров, а также их солей.
Соли HCA могут являться кислотно-аддитивными солями, например ацетатами, адипатами, альгинатами, бикарбонатами, цитратами, аспартатами, бензоатами, бензолсульфонатами (бесилатами), бисульфатами, бутиратами, камфоратами, камфорсульфонатами, диглюконатами, формиатами, фумаратами, глицерофосфатами, глутаматами, гемисульфатами, гептаноатами, гексаноатами, гидрохлоридами, гидробромидами, гидройодидами, лактобионатами, лактатами, малеатами, мезитиленсульфонатами, метансульфонатами, нафтиленсульфонатами, никотинатами, оксалатами, памоатами, пектинатами, персульфатами, фосфатами, пикратами, пропионатами, сукцинатами, тартратами, тиоцианатами, трихлорацетатами, трифторацетатами, пара-толуолсульфонатами и ундеканоатами. В конкретном варианте осуществления в композиции по настоящему изобретению присутствует гидрохлорид одного из индивидуально упомянутых выше соединений в антиоксидантно-эффективном количестве.
Не ограничиваясь какой-либо теорией, обычно полагают, что антиоксиданты, включающие тяжелые халькогены, например, перечисленные выше, защищают ABT-263 за счет того, что они способны окисляться легче и, следовательно, окисляются преимущественно по сравнению с ABT-263. Как правило, для того чтобы указанный механизм защиты обеспечивал приемлемую степень защиты ABT-263, антиоксидант формулы (II) или формулы (III) должен присутствовать в значительном количестве, например в мольном отношении к ABT-263 не менее чем примерно 1:10. В некоторых вариантах осуществления мольное отношение антиоксиданта к ABT-263 составляет от примерно 1:10 до примерно 2:1, например от примерно 1:5 до примерно 1,5:1. В некоторых случаях наилучшие результаты получаются, если мольное соотношение составляет приблизительно 1:1, т.е. от примерно 8:10 до примерно 10:8.
Несмотря на антиоксидантную эффективность серосодержащих антиоксидантов формулы (II) или формулы (III), было обнаружено, что при мольных соотношениях примерно 1:1 эти антиоксиданты склонны образовывать растворы, которые мутнеют при хранении, если ABT-263 применяется в форме свободного основания.
Однако было обнаружено, что свободное основание ABT-263 менее склонно к образованию сульфоксидов, чем ABT-263 в форме соли, например бис-гидрохлорида ABT-263, при включении в липидный раствор (но в отсутствие антиоксиданта). Для извлечения преимущества из этого факта, в комбинации с ABT-263 можно применять другой класс серосодержащих соединений, а именно неорганические антиоксиданты таких классов, как сульфиты, бисульфиты, метабисульфиты и тиосульфаты. Дело осложняется тем, что эти антиоксиданты плохо растворимы в липидах, и если желателен липидный состав, их необходимо вводить в носитель или систему действующий ингредиент-носитель в водном растворе. Наличие воды способствует образованию сульфоксидов в растворе ABT-263, т.е. приводит к тому самому результату, который предполагалось минимизировать. Для ограничения количества добавляемой воды, в одном из вариантов осуществления изобретения, плохо растворимые в липидах антиоксиданты добавляют в значительно меньших количествах, чем необходимо для достижения мольной эквивалентности с ABT-263.
Если применяется плохо растворимый в липидах антиоксидант, например сульфит, бисульфит, метабисульфит или тиосульфат, вместе с ним в систему действующий ингредиент-носитель добавляют воду в количестве, не превышающем примерно 1% по массе, например от примерно 0,2% до примерно 0,8% по массе. Количество указанных антиоксидантов, которое можно ввести в таком малом количестве воды, как правило, не превышает примерно 0,2% по массе и составляет, например, от приблизительно 0,02% до примерно 0,2% или от примерно 0,05% до примерно 0,15% от массы системы действующий ингредиент-носитель.
Для минимизации количества добавляемой к составу воды желательно применять антиоксидант в форме водного концентрата с относительно высоким содержанием антиоксиданта, например, содержащего не менее примерно 10 масс.% антиоксиданта. Однако было обнаружено, что если применять водный концентрат, содержащий слишком много антиоксиданта (например, приблизительно 20% или выше), это может привести к нежелательному выпадению в осадок твердых веществ в составе. Подходящее содержание антиоксиданта в концентрате, как правило, составляют от примерно 10% до примерно 18%, в качестве иллюстрации примерно 15 масс.%.
В качестве антиоксидантов по настоящему изобретению применимы натриевые и калиевые производные сульфитов, бисульфитов, метабисульфитов и тиосульфатов; более конкретно метабисульфиты натрия и калия.
Для дальнейшего снижения образования сульфоксидов, необязательно добавляют хелатообразующие соединения, например EDTA или ее соли (например, динатрий EDTA или кальций динатрий EDTA), например, в количестве от примерно 0,002% до примерно 0,02% от массы системы действующий ингредиент-носитель. EDTA можно добавлять в виде водного концентрата таким же образом, как и антиоксидант. Если это желательно, антиоксидант и EDTA можно добавлять в качестве компонентов одного и того же концентрата. Хелатообразующий агент связывает ионы металлов, которые могут способствовать окислительному распаду.
Даже при очень низких концентрациях антиоксиданта, предусмотренных в настоящем изобретении (как правило, мольное отношение плохо растворимого в липидах антиоксиданта к ABT-263 по настоящему изобретению не превышает примерно 1:20), было обнаружено, что образование сульфокидов сохраняется в приемлемых рамках.
Образование сульфоксидов может быть дополнительно уменьшено за счет выбора ингредиентов состава с низким пероксидным числом. Пероксидное число является хорошо известной характеристикой фармацевтических эксципиентов и, как правило, выражается (как и в настоящей заявке) в единицах, соответствующих миллиэквивалентам пероксидов на килограмм эксципиента (мэкв/кг). Некоторые эксципиенты по своей природе имеют низкое пероксидное число, но другие, например, включающие фрагменты ненасыщенной жирной кислоты, например олеиловые фрагменты, и полиоксиэтиленовые цепи, могут являться источниками пероксидов. В случае, например, полисорбата 80, предпочтительно выбирать источник полисорбата 80, имеющего пероксидное число не более примерно 5, например не более примерно 2. Подходящие продукты включают Crillet 4HPTM и Super-Refined Tween 80TM, оба можно приобрести у Croda.
Не ограничиваясь какой-либо теорией, полагают, что терапевтическая эффективность ABT-263, по крайней мере отчасти, связана с его способностью связывать белки семейства Bcl-2, например Bcl-2, Bcl-XL или Bcl-w, таким образом, что происходит ингибирование антиапоптотического действия этих белков, например, занимая связывающий карман белка BH3.
В еще одной группе вариантов осуществления изобретения, разработан способ лечения заболевания, характеризующегося нарушением апоптоза и/или избыточной экспрессией антиапоптотических белков семейства Bcl-2, включающий введение субъекту, у которого имеется такое заболевание, терапевтически эффективного количества кристаллического свободного основания ABT-263 или фармацевтической композиции, включающей кристаллическое свободное основание ABT-263 и один или несколько фармацевтически приемлемых эксципиентов. В одном из вариантов осуществления этот способ включает введение субъекту кристаллической формы I свободного основания ABT-263 или фармацевтической композиции, включающей кристаллическую форму I свободного основания ABT-263 и один или несколько фармацевтически приемлемых эксципиентов. В другом варианте осуществления этот способ включает введение субъекту кристаллической формы II свободного основания ABT-263 или фармацевтической композиции, включающей кристаллическую форму II свободного основания ABT-263 и один или несколько фармацевтически приемлемых эксципиентов.
В ряде других вариантов осуществления изобретения, разработан способ лечения заболевания, характеризующегося нарушением апоптоза и/или избыточной экспрессией антиапоптотических белков семейства Bcl-2, включающий (a) растворение кристаллического свободного основания ABT-263 в фармацевтически приемлемом растворителе или смеси растворителей (например, выбранных из растворителей, упоминавшихся выше по тексту в качестве эксципиентов), и (b) введение полученного раствора в терапевтически эффективном количестве субъекту, у которого имеется указанное заболевание. В одном из вариантов осуществления кристаллическое свободное основание представляет собой кристаллическую форму I свободного основания ABT-263. В другом варианте осуществления кристаллическое свободное основание представляет собой кристаллическую форму II свободного основания ABT-263.
Упомянутый субъект может являться или не являться человеком (например, может быть сельскохозяйственным животным, животным из зоопарка, рабочим животным или животным-компаньоном, или лабораторным животным, используемым в качестве модели), но в одном из важных вариантов осуществления субъект является пациентом из числа людей, которому необходимо лекарственное средство по настоящему изобретению, например, для лечения заболевания, характеризующегося нарушением апоптоза и/или избыточной экспрессией антиапоптотических белков семейства Bcl-2. Субъект из числа людей может быть мужчиной или женщиной любого возраста. Как правило, пациент является взрослым, но способ по настоящему изобретению может применяться для лечения детского рака, например лейкоза, например острого лимфоцитарного лейкоза у пациентов детского возраста.
Композицию по настоящему изобретению обычно вводят в количестве, обеспечивающем терапевтически эффективную дневную дозу лекарственного средства. Термин «дневная доза» в настоящей заявке означает количество лекарственного средства, вводимого в течение суток, независимо от частоты введения. Например, если субъект получает разовую дозу 150 мг дважды в день, дневная доза составляет 300 мг. Не следует понимать использование термина «дневная доза» как предположение, что указанная доза обязательно вводится один раз в день. Однако в отдельных вариантах осуществления частота введения составляет один раз в день (q.d.), и в этом варианте осуществления дневная доза и разовая доза являются одним и тем же.
Величина терапевтически эффективной дозы зависит от биодоступности конкретного состава, субъекта (включая биологический вид и массу тела субъекта), заболевания, подвергаемого лечению (например, конкретного типа рака), стадии и/или тяжести заболевания, индивидуальной переносимости субъектом действующего ингредиента, применяется ли действующий ингредиент в рамках монотерапии или в комбинации с одним или несколькими другими лекарственными средствами, например другими химиотерапевтическими средствами для лечения рака, а также от других факторов. Поэтому дневная доза может меняться в широких пределах, например от примерно 10 до примерно 1000 мг. В определенных ситуациях могут оказаться подходящими большие или меньшие дозы. Следует понимать, что упоминание «терапевтически эффективной дозы» в тексте настоящей заявки необязательно требует, чтобы лекарственное средство было терапевтически эффективным при введении только одной дозы; как правило, терапевтическая эффективность основана на неоднократном введении композиции в соответствии со схемой, предполагающей необходимую частоту и продолжительность введения. Хотя выбранная дневная доза достаточна для обеспечения благоприятного результата с точки зрения лечения рака, весьма предпочтительно, чтобы дневная доза не была достаточной для проявления вредных побочных эффектов в неприемлемой или непереносимой степени. Подходящая терапевтически эффективная доза может быть подобрана рядовым врачом без проведения слишком большого объема экспериментальной работы на основе описания изобретения и процитированных источников известного уровня техники, с учетом ряда факторов, например, упомянутых выше. Врач может, например, начать курс лечения ракового пациента с относительной низких дневных доз и постепенно повышать дозу в течение нескольких дней или недель для уменьшения риска нежелательных побочных эффектов.
В качестве иллюстрации, подходящие дозы ABT-263 обычно составляют от примерно 25 до примерно 1000 мг/день, или от примерно 50 до примерно 1000 мг/день, чаще от примерно 50 до примерно 500 мг/день, или от примерно 200 до примерно 400 мг/день, например примерно 50, примерно 100, примерно 150, примерно 200, примерно 250, примерно 300, примерно 350, примерно 400, примерно 450, примерно 500, примерно 750 или примерно 1000 мг/день, при введении со средним интервалом от примерно 3 часов до примерно 7 дней, например от примерно 8 часов до примерно 3 дней, или от примерно 12 часов до примерно 2 дней. В большинстве случаев подходит режим введения один раз в день (q.d.).
«Средний интервал между введениями» определяется в настоящей заявке как частное от деления определенного промежутка времени, например одного дня или одной недели, на количество разовых доз, вводимых за этот промежуток времени. Например, если лекарственное средство вводят три раза в день в районе 8 часов утра, в районе полудня и в районе 6 часов вечера, средний интервал между введениями составляет 8 часов (24-часовой промежуток времени, деленный на 3). Если действующий ингредиент входит в состав дискретной дозированной формы, например, таблеток или капсул, несколько (например, от 2 до примерно 10) единиц дозированной формы, введенных в одно и то же время, при определении среднего интервала между введениями, считаются разовой дозой.
В некоторых вариантах осуществления дневную дозу и интервал между введениями можно выбрать таким образом, чтобы поддерживать концентрацию ABT-263 в плазме в диапазоне от примерно 0,5 до примерно 10 мкг/мл. Таким образом, согласно этим вариантам осуществления, во время курса лечения ABT-263 равновесная максимальная концентрация в плазме (Cmax), как правило, не должна превышать примерно 10 мкг/мл, и равновесная минимальная концентрация в плазме (Cmin), как правило, не должна опускаться ниже примерно 0,5 мкг/мл. Далее, как правило, желательно выбрать, в пределах указанных выше диапазонов, дневную дозу и средний интервал между введениями, которые позволяют обеспечить отношение Cmax/Cmin в равновесном состоянии не более 5, например не более примерно 3. Следует понимать, что более продолжительные интервалы между введениями препарата приведут к большим значениям отношения Cmax/Cmin. В качестве иллюстрации, способ по настоящему изобретению позволяет достигать для ABT-263 в равновесном состоянии Cmax от примерно 3 до примерно 8 мкг/мл и Cmin от примерно 1 до примерно 5 мкг/мл. Равновесные величины Cmax и Cmin могут быть определены при исследованиях PK у человека, например, проводимых по стандартным протоколам, включая, но не ограничиваясь этим, протоколы, одобренные регулирующими организациями, например, U.S. Food and Drug Administration (FDA) (Управление по надзору за качеством пищевых продуктов и лекарственных препаратов США).
Поскольку считается, что композиции по настоящему изобретению подвергаются лишь минимальному влиянию со стороны пищи, введение композиции по данному варианту осуществления может происходить вместе с пищей либо без пищи, т.е. пациентам, принимающим либо не принимающим пищу. Как правило, предпочтительно вводить композиции по настоящему изобретению пациентам, не отказывающимся от приема пищи.
Составы по настоящему изобретению подходят для применения в форме монотерапии, либо в комбинированной терапии, например, в сочетании с другими химиотерапевтическими средствами или ионизирующим излучением. Конкретное преимущество настоящего изобретения заключается в том, что оно допускает пероральное введение препарата один раз в день, т.е. схему, которая является удобной для пациента, которого лечат другими препаратами, перорально вводимыми один раз в день. Пероральное введение легко осуществляется дома самим пациентом либо лицом, осуществляющим уход за ним; кроме того, пероральное введение является удобным путем введения для пациентов, находящихся в больницах или других учреждениях, где за ними осуществляется постоянный уход.
В качестве иллюстрации, комбинированная терапия включает введение композиции, включающей (или полученной с применением в качестве API) кристаллическое свободное основание ABT-263, одновременно с одним или нескольким соединениями, выбранными из бортезомида, карбоплатина, цисплатина, циклофосфамида, дакарбазина, дексаметазона, доцетаксела, доксорубицина, этопозида, флударабина, гидроксидоксорубицина, иринотекана, паклитаксела, рапамицина, ритуксимаба, винкристина и т.п., например одновременно с политерапией, такой как CHOP (циклофосфамид+гидроксидоксорубицин+винкристин+преднизон), RCVP (ритуксимаб+циклофосфамид+винкристин+преднизон), R-CHOP (ритуксимаб+CHOP) или DA-EPOCH-R (комбинация этопозида, преднизона, винкристина, циклофосфамида, доксорубицина и ритуксимаба с подобранными дозировками).
Композиция ABT-263 может вводиться в схеме комбинированной терапии совместно с одним или несколькими терапевтическими средствами, в число которых входят, не ограничиваясь этим, ингибиторы ангиогенеза, антипролиферативные средства, другие промоторы апоптоза (например, ингибиторы Bcl-xL, Bcl-w и Bfl-1), активаторы сигнального пути рецепторов гибели клеток, антитела BiTE (биспецифичные активаторы T-клеток), связывающие белки с двойным вариабельным доменом (DVD), ингибиторы белков апоптоза (IAP), микроРНК, митоген-активируемые ингибиторы внеклеточной сигнал-регулируемой киназы, мультивалентные связывающие белки, ингибиторы полимеразы поли-ADP(аденозиндифосфат)рибозы (PARP), малые интерферирующие рибонуклеиновые кислоты (siRNA), ингибиторы киназ, ингибиторы рецепторной тирозинкиназы, ингибиторы aurora киназы, ингибиторы polo-подобной киназы, ингибиторы bcr-abl киназы, ингибиторы факторов роста, ингибиторы COX-2, нестероидные противовоспалительные средства (NSAID), антимитотические средства, алкилирующие агенты, антиметаболиты, интеркалирующие (включающиеся) антибиотики, платиносодержащие химиотерапевтические средства, ингибиторы факторов роста, ионизирующая радиация, ингибиторы клеточного цикла, ферменты, ингибиторы топоизомеразы, модификаторы биологической реакции, иммунологические средства, антитела, гормональные терапевтические средства, ретиноиды, дельтоиды, растительные алкалоиды, ингибиторы протеасомы, ингибиторы HSP-90, ингибиторы гистондеацетилазы (HDAC), аналоги пурина, аналоги пиримидина, ингибиторы MEK, ингибиторы CDK, ингибиторы рецептора ErbB2, ингибиторы mTOR, а также другие противоопухолевые средства.
В число ингибиторов ангиогенеза входят, не ограничиваясь этим, ингибиторы EGFR, ингибиторы PDGFR, ингибиторы VEGFR, ингибиторы TIE2, ингибиторы IGF1R, ингибиторы матричной металлопротеиназы 2 (MMP-2), ингибиторы матричной металлопротеиназы 9 (MMP-9) и аналоги тромбоспондина.
Примеры ингибиторов EGFR включают, не ограничиваясь этим, гефитиниб, эрлотиниб, цетуксимаб, EMD-7200, ABX-EGF, HR3, антитела против IgA, TP-38 (IVAX), слитый белок EGFR, EGF-вакцину, анти-EGFR иммунолипосомы и лапатиниб.
Примеры ингибиторов PDGFR включают, не ограничиваясь этим, CP-673451 и CP-868596.
Примеры ингибиторов VEGFR включают, не ограничиваясь этим, бевацизумаб, сунитиниб, сорафениб, CP-547632, акситиниб, вандетаниб, AEE788, AZD-2171, ловушку VEGF, ваталиниб, пегаптаниб, IM862, пазопаниб, ABT-869 и ангиозим.
Ингибиторы семейства белков Bcl-2, отличные от ABT-263 или соединений формулы (I) настоящей заявки, включают, не ограничиваясь этим, AT-101 ((-)госсипол), GenasenseTM Bcl-2-нацеливающий антисмысловой олигонуклеотид (G3139 или облимерсен), IPI-194, IPI-565, ABT-737, GX-070 (обатоклакс) и т.п.
Активаторы сигнального пути рецептора гибели клеток включают, не ограничиваясь этим, TRAIL, антитела или другие агенты, которые нацеливают рецепторы гибели клеток (например, DR4 и DR5), например апомаб, конатумумаб, ETR2-ST01, GDC0145 (лексатумумаб), HGS-1029, LBY-135, PRO-1762 и трастузумаб.
Примеры аналогов тромбоспондина включают, не ограничиваясь этим, TSP-1, ABT-510, ABT-567 и ABT-898.
Примеры ингибиторов aurora киназы включают, не ограничиваясь этим, VX-680, AZD-1152 и MLN-8054.
Пример ингибитора polo-подобной киназы включает, не ограничиваясь этим, BI-2536.
Примеры ингибиторов bcr-abl киназы включают, не ограничиваясь этим, иматиниб и дазатиниб.
Примеры платиносодержащих средств включают, не ограничиваясь этим, цисплатин, карбоплатин, эптаплатин, лобаплатин, недаплатин, оксалиплатин и сатраплатин.
Примеры ингибиторов mTOR включают, не ограничиваясь этим, CCI-779, рапамицин, темсиролимус, эверолимус, RAD001 и AP-23573.
Примеры ингибиторов HSP-90 включают, не ограничиваясь этим, гелданамицин, радицикол, 17-AAG, KOS-953, 17-DMAG, CNF-101, CNF-1010, 17-AAG-nab, NCS-683664, эфунгумаб, CNF-2024, PU3, PU24FCl, VER-49009, IPI-504, SNX-2112 и STA-9090.
Примеры ингибиторов HDAC включают, не ограничиваясь этим, субероиланилид гидроксамовую кислоту (SAHA), MS-275, вальпроевую кислоту, TSA, LAQ-824, трапоксин и депсипептид.
Примеры ингибиторов MEK включают, не ограничиваясь этим, PD-325901, ARRY-142886, ARRY-438162 и PD-98059.
Примеры ингибиторов CDK включают, не ограничиваясь этим, флавопиридол, MCS-5A, CVT-2584, селициклиб ZK-304709, PHA-690509, BMI-1040, GPC-286199, BMS-387032, PD-332991 и AZD-5438.
Примеры ингибиторов COX-2 включают, не ограничиваясь этим, целекоксиб, парекоксиб, деракоксиб, ABT-963, эторикоксиб, люмиракоксиб, BMS-347070, RS 57067, NS-398, вальдекоксиб, рофекоксиб, SD-8381, 4-метил-2-(3,4-диметилфенил)-1-(4-сульфамоилфенил)-1H-пиррол, T-614, JTE-522, S-2474, SVT-2016, CT-3 и SC-58125.
Примеры NSAID включают, не ограничиваясь этим, салсалат, дифлунизал, ибупрофен, кетопрофен, набуметон, пироксикам, напроксен, диклофенак, индометацин, сулиндак, толметин, этодолак, кеторолак и оксапрозин.
Примеры ингибиторов рецептора ErbB2 включают, не ограничиваясь этим, CP-724714, канертиниб, трастузумаб, петузумаб, TAK-165, ионафамиб, GW-282974, EKB-569, PI-166, dHER2, APC-8024, биспецифичное анти-HER/2neu антитело B7.her21gG3 и трифункциональные биспецифичные антитела против HER2 mAB AR-209 и mAB 2B-1.
Примеры алкилирующих агентов включают, не ограничиваясь этим, N-оксиды азотистых ипритов, циклофосфамид, ифосфамид, трофосфамид, хлорамбуцил, мелфалан, бусульфан, митобронитол, карбоквон, тиотепу, ранимустин, нимустин, CloretazineTM (ларомустин), AMD-473, алтретамин, AP-5280, апазиквон, бросталлицин, бендамустин, кармустин, эстрамустин, фотемустин, глуфосфамид, KW-2170, мафосфамид, митолактол, ломустин, треосульфан, дакарбазин и темозоломид.
Примеры антиметаболитов включают, не ограничиваясь этим, метотрексат, 6-меркаптопурин рибозид, меркаптопурин, 5-фторурацил (5-FU) индивидуально или в комбинации с лейковорином, тегафур, UFT, доксифлуридин, кармофур, цитарабин, цитарабина окфосфат, эноцитабин, S-1, пеметрексед, гемцитабин, флударабин, 5-азацитидин, капецитабин, кладрибин, клофарабин, децитабин, эфлорнитин, этенилцитидин, цитозина арабинозид, гидроксимочевину, TS-1, мелфалан, неларабин, нолатрексед, динатрий пеметрексед, пентостатин, пелитрексол, ралтитрексед, триапин, триметрексат, видарабин, микофеноловую кислоту, окфосфат, пентостатин, тиазофурин, рибавирин, EICAR, гидроксимочевину и дефероксамин.
Примеры антибиотиков включают, не ограничиваясь этим, интеркалирующие антибиотики, акларубицин, актиномицин D, амрубицин, аннамицин, адриамицин, блеомицин, даунорубицин, доксорубицин (в том числе липосомальный доксорубицин), элсамитруцин, эпирубицин, гларубицин, идарубицин, митомицин C, неморубицин, неокарциностатин, пепломицин, пирарубицин, ребеккамицин, стималамер, стрептозоцин, валрубицин, зиностатин и их комбинации.
Примеры средств, ингибирующих топоизомеразу, включают, не ограничиваясь этим, акларубицин, амонафид, белотекан, камптотекин, 10-гидроксикамптотекин, 9-аминокамптотекин, амсакрин, дексразоксан, дифломотекан, иринотекан HCl, эдотекарин, эпирубицин, этопозид, экзатекан, бекатекарин, гиматекан, луртотекан, оратецин, BN-80915, митоксантрон, пирарбуцин, пиксантрон, рубитекан, собузоксан, SN-38, тафлупозид и топотекан.
Примеры антител включают, не ограничиваясь этим, ритуксимаб, цетуксимаб, бевацизумаб, трастузумаб, CD-40-специфичные антитела и IGF1R-специфичные антитела, chTNT-1/B, деносумаб, эдреколомаб, WX G250, занолимумаб, линтузумаб и тицилимумаб.
Примеры гормональных терапевтических средств включают, не ограничиваясь этим, севеламера карбонат, рилостан, гормон, высвобождающий лютеинизирующий гормон, модрастан, экземестан, леупролида ацетат, бусерелин, цетрореликс, деслорелин, гистрелин, анастрозол, фосрелин, госерелин, дегареликс, доксеркальциферол, фадрозол, форместан, тамоксифен, арзоксифен, бикалутамид, абареликс, трипторелин, финастерид, фульвестрант, торемифен, ралоксифен, трилостан, лазофоксифен, летрозол, флутамид, мегестерол, мифепристон, нулутамид, дексаметазон, преднизон и другие глюкокортикоиды.
Примеры ретиноидов или дельтоидов включают, не ограничиваясь этим, сеокальцитол, лексакальцитол, фенретинид, алиретиноин, третиноин, бексаротен и LGD-1550.
Примеры растительных алкалоидов включают, не ограничиваясь этим, винкристин, винбластин, виндезин и винорелбин.
Примеры ингибиторов протеасом включают, не ограничиваясь этим, бортезомиб, MG-132, NPI-0052 и PR-171.
Примеры иммунологических средств включают, не ограничиваясь этим, интерфероны и широкий круг других средств, улучшающих иммунитет. Интерфероны включают интерферон альфа, интерферон альфа-2a, интерферон альфа-2b, интерферон бета, интерферон гамма-1a, интерферон гамма-1b, интерферон гамма-n1 и их комбинации. В число других средств входят филграстим, лентинан, сизофилан, живые BCG, убенимекс, WF-10 (тетрахлордекаоксид или TCDO), алдеслейкин, алемтузумаб, BAM-002, дакарбазин, даклизумаб, денилейкин, гемтузумаб, озогамицин, ибритумомаб, имиквимод, ленограстим, вакцины против меланомы, молграмостим, саргарамостим, тасонермин, теклейкин, тимальфазин, тозитумомаб, VirulizinTM иммунотерапевтический препарат Lorus Pharmaceuticals, Z-100 (специфическое вещество (вакцина) Маруямы или SSM), ZevalinTM (90Y-ибритумомаб тиуксетан), эпратузумаб, митумомаб, ореговомаб, пемтумомаб, ProvengeTM (сипулейцел-T), тецелейкин, TherocysTM (бацилла Кальметта-Герена), антитела против цитотоксичного лимфоцитарного антигена 4 (CTLA 4) и агенты, способные блокировать CTLA4, например, MDX-010.
Примерами модификаторов биологической реакции являются агенты, которые модифицируют защитные механизмы живых организмов или биологические реакции, такие как выживание, рост или дифференцировку клеток тканей, чтобы побудить их к противоопухолевой активности. Эти агенты включают, не ограничиваясь этим, крестин, лентинан, сизофуран, пицибанил, PF-3512676 и убенимекс.
Примеры аналогов пиримидина включают, не ограничиваясь этим, 5-фторурацил, флоксуридин, доксифлуридин, ралтитрексед, цитарабин, цитозина арабинозид, флударабин, триацетилуридин, троксацитабин и гемцитабин.
Примеры аналогов пурина включают, не ограничиваясь этим, меркаптопурин и тиогуанин.
Примеры антимитотических средств включают, не ограничиваясь этим, N-(2-((4-гидроксифенил)амино)пиридин-3-ил)-4-метоксибензолсульфонамид, паклитаксел, доцетаксел, ларотаксел, эпотилон D, PNU-100940, батабулин, иксабепилон, патупилон, XRP-9881, винфлунин и ZK-EPO (синтетический эпотилон).
Примеры радиационной терапии включают, не ограничиваясь этим, наружную лучевую терапию (XBRT), дистанционную терапию, брахитерапию, радиотерапию с использованием герметизированных источников и радиотерапию с использованием негерметизированных источников.
Антитела BiTE представляют собой биспецифичные антитела, которые стимулируют атаку раковых клеток T-клетками за счет одновременного связывания с двумя этими клетками. После этого T-клетки атакуют целевые раковые клетки. Примеры антител BiTE включают, не ограничиваясь этим, адекатумумаб (Micromet MT201), блинатумомаб (Micromet MT103) и т.п. Не ограничиваясь какой-либо теорией, одним из механизмов, благодаря которому T-клетки вызывают апоптоз целевых раковых клеток, является экзоцитоз компонентов цитолитических гранул, которые включают перфорин и гранзим B. В связи с этим было показано, что Bcl-2 ослабляет активацию апоптоза как перфорином, так и гранзимом B. Эти данные позволяют предположить, что ингибирование Bcl-2 могло бы улучшить цитотоксические эффекты, вызываемые T-клетками, при их нацеливании на раковые клетки (Sutton et al. (1997) J.Immunol. 158:5783-5790).
siRNA представляют собой молекулы, включающие эндогенные РНК основания или химически модифицированные нуклеотиды. Модификации не отменяют клеточную активность, но придают повышенную стабильность и/или увеличивают клеточную активность. Примеры химических модификаций включают фосфортиоатные группы, 2'-дезоксинуклеотиды, 2'-OCH3-содержащие рибонуклеотиды, 2'-F-рибонуклеотиды, 2'-метоксиэтил рибонуклеотиды, их комбинации и т.п. siRNA могут иметь различную длину (например, 10-200 пар оснований) и структуры (например, «шпилек», одиночных/двойных нитей, петель, одноцепочечных разрывов/пропусков, нарушений комплементарности) и обрабатываются в клетках, приводя к активному подавлению экспрессии генов. Двухцепочечная siRNA (dsRNA) может включать одно и то же количество нуклеотидов в каждой цепочке (тупые концы) или асимметрические концы (выступающие концы). Выступающий конец длиной 1-2 нуклеотида может присутствовать на смысловой и/или антисмысловой нити, а также присутствовать на 5'- и/или 3'-конце данной нити. Например, было показано, что siRNA, нацеливающие Mcl-1, усиливают активность ABT-263 (Tse et al. (2008), см. выше и приведенные в этой работе ссылки).
Мультивалентные связывающие белки представляют собой связывающие белки, включающие два или несколько сайтов связывания антигена. Мультивалентные связывающие белки, включающие три или более сайта связывания антигена, как правило, являются антителами, не встречающимися в природе. Термин «мультиспецифичный связывающий белок» означает связывающий белок, способный к связыванию с двумя или более родственными или неродственными мишенями. Связывающие белки с двойным вариабельным доменом (DVD) являются тетравалентными или мультивалентными связывающими белками, включающими два или более антигенсвязывающих сайта. Такие DVDs могут быть моноспецифичными (т.е. способными к связыванию одного антигена) или мультиспецифичными (т.е. способными к связыванию с двумя или несколькими антигенами). Связывающие белки DVD, включающие два DVD полипептида тяжелых цепей и два DVD полипептида легких цепей, именуются DVD Ig (иммуноглобулинами). Каждая половина DVD Ig включает DVD полипептид тяжелой цепи, DVD полипептид легкой цепи и два антигенсвязывающих сайта. Каждый связывающий сайт включает вариабельный домен тяжелой цепи и вариабельный домен легкой цепи, имеющие в общей сложности 6 CDR, принимающих участие в связывании с антигеном, на антигенсвязывающий сайт.
Ингибиторы PARP включают, не ограничиваясь этим, ABT-888, олапариб, KU-59436, AZD-2281, AG-014699, BSI-201, BGP-15, INO-1001, ONO-2231 и т.п.
Дополнительно или в качестве альтернативы, композиции, включающие кристаллическое свободное основание ABT-263 (или полученные с применением этого основания в качестве API), могут вводиться в схеме комбинированной терапии совместно с одним или несколькими противоопухолевыми реагентами, выбранными из ABT-100, N-цетилколхинол-O-фосфата, ацитретина, AE-941, агликон протопанаксадиола, арглабина, триоксида мышьяка, AS04 адъювант-адсорбированной вакцины против ВИЧ, L-аспарагиназы, атаместана, атрасентана, AVE-8062, босентана, канфосфамида, CanvaxinTM, катумаксомаба, CeaVacTM, целмолейкина, комбрестатина A4P, контусугена ладеновека, CotaraTM, ципротерона, деоксикоформицина, дексразоксана, N,N-диэтил-2-(4-(фенилметил)фенокси)этанамина, 5,6-диметилксантенон-4-уксусной кислоты, докозагексаеновой кислоты/паклитаксела, дискодермолида, эфапроксирала, энзастаурина, эпотилона B, этинилурацила, экзисулинда, фалимарева, GastrimmuneTM, вакцины GMK, GVAXTM, галофуджинона, гистамина, гидроксикарбамида, ибандроновой кислоты, ирбитумомаб тиуксетана, IL-13-PE38, иналимарева, интерлейкина 4, KSB-311, ланреотида, леналидомида, лонафарниба, ловастатина, 5,10-метилентетрагидрофолата, мифамуртида, милтефосина, мотексафина, облимерсена, OncoVAXTM, OsidemTM, наночастиц паклитаксела, стабилизированных альбумином, паклитаксел полиглумекса, памидроната, панитумумаба, пэгинтерферона альфа, пэгаспаргазы, феноксодиола, поли(I)-поли(C12U), прокарбазина, ранпирназы, ребимастата, рекомбинантной квадравалентной вакцины HPV, скваламина, стауроспорина, вакцины STn-KLH, T4 эндонуклазы V, тазаротена, 6,6',7,12-тетраметокси-2,2'-диметил-1β-бербамана, талидомида, TNFeradeTM, 131I-тозитумомаба, трабектедина, триазона, фактора некроза опухолей, UkrainTM, вакцины vaccinia-MUC-1, L-валин-L-боропролина, VitaxinTM, витеспена, золедроновой кислоты и зорубицина.
В одном из вариантов осуществления композицию, включающую кристаллическое свободное основание ABT-263 (или полученную с применением этого основания в качестве API), вводят в терапевтически эффективном количестве субъекту, у которого имеется необходимость в лечении заболевания, при котором наблюдается избыточная экспрессия антиапоптотического белка Bcl-2, антиапоптотического белка Bcl-XL и антиапоптотического белка Bcl-w.
В другом варианте осуществления композицию, включающую кристаллическое свободное основание ABT-263 (или полученную с применением этого основания в качестве API), вводят в терапевтически эффективном количестве субъекту, у которого имеется необходимость в лечении заболевания, при котором происходит аномальный рост клеток и/или нарушено регулирование апоптоза.
Примеры таких заболеваний включают, не ограничиваясь перечисленными, рак, мезотелиому, рак мочевого пузыря, рак поджелудочной железы, рак кожи, рак органов головы и шеи, кожную или внутриглазную меланому, рак яичников, рак груди, рак матки, карциному фаллопиевых труб, карциному эндометрия, карциному шейки матки, карциному влагалища, карциному вульвы, рак костей, рак толстой кишки, рак прямой кишки, рак анальной области, рак желудка, рак желудочно-кишечного тракта (желудка, колоректальный и/или дуоденальный), хронический лимфоцитарный лейкоз, острый лимфоцитарный лейкоз, рак пищевода, рак тонкого кишечника, рак эндокринной системы, рак щитовидной железы, рак околощитовидной железы, рак надпочечника, саркому мягких тканей, рак мочеиспускательного канала, рак пениса, рак яичек, гепатоклеточный (печени и/или желчного протока) рак, первичные или вторичные опухоли центральной нервной системы, первичные или вторичные опухоли мозга, болезнь Ходжкина, хронический или острый лейкоз, хронический миелоидный лейкоз, лимфоцитарную лимфому, лимфобластный лейкоз, фолликулярную лимфому, лимфоидные злокачественные новообразования T-клеточного или B-клеточного происхождения, меланому, множественную миелому, рак ротовой полости, немелкоклеточный рак легких, рак простаты, мелкоклеточный рак легких, рак почек и/или мочеточника, карциному почечных клеток, карциному почечной лоханки, новообразования центральной нервной системы, первичную лимфому центральной нервной системы, неходжкинскую лимфому, опухоли спинного мозга, глиому ствола мозга, аденому гипофиза, рак коры надпочечников, рак желчного пузыря, рак селезенки, холангиокарциному, фибросаркому, нейробластому, ретинобластому и их комбинации.
В более конкретном варианте осуществления композицию, включающую кристаллическое свободное основание ABT-263 (или полученную с применением этого основания в качестве API), вводят в терапевтически эффективном количестве субъекту, у которого имеется необходимость в лечении рака мочевого пузыря, рака мозга, рака груди, рака костного мозга, рака шейки матки, хронического лимфоцитарного лейкоза, острого лимфоцитарного лейкоза, колоректального рака, рака пищевода, гепатоклеточного рака, лимфобластного лейкоза, фолликулярной лимфомы, лимфоидных злокачественных новообразований T-клеточного или B-клеточного происхождения, меланомы, миелогенного лейкоза, миеломы, рака ротовой полости, рака яичников, немелкоклеточного рака легких, рака простаты, мелкоклеточного рака легких или рака селезенки.
Согласно любому из этих вариантов осуществления, композицию по настоящему изобретению можно вводить в форме монотерапии или в схеме комбинированной терапии вместе с одним или несколькими другими терапевтическими агентами.
Например, способ лечения мезотелиомы, рака мочевого пузыря, рака поджелудочной железы, рака кожи, рака органов головы и шеи, кожной или внутриглазной меланомы, рака яичников, рака груди, рака матки, карциномы фаллопиевых труб, карциномы эндометрия, карциномы шейки матки, карциномы влагалища, карциномы вульвы, рака костей, рака толстой кишки, рака прямой кишки, рака анальной области, рака желудка, рака желудочно-кишечного тракта (желудка, колоректального и/или дуоденального), хронического лимфоцитарного лейкоза, острого лимфоцитарного лейкоза, рака пищевода, рака тонкого кишечника, рака эндокринной системы, рака щитовидной железы, рака околощитовидной железы, рака надпочечника, саркомы мягких тканей, рака мочеиспускательного канала, рака пениса, рака яичек, гепатоклеточного (печени и/или желчного протока) рака, первичных или вторичных опухолей центральной нервной системы, первичных или вторичных опухолей мозга, болезни Ходжкина, хронического или острого лейкоза, хронического миелоидного лейкоза, лимфоцитарной лимфомы, лимфобластного лейкоза, фолликулярной лимфомы, лимфоидных злокачественных новообразований T-клеточного или B-клеточного происхождения, меланомы, множественной миеломы, рака ротовой полости, немелкоклеточного рака легких, рака простаты, мелкоклеточного рака легких, рака почек и/или мочеточника, карциномы почечных клеток, карциномы почечной лоханки, новообразований центральной нервной системы, первичной лимфомы центральной нервной системы, неходжкинской лимфомы, опухолей спинного мозга, глиомы ствола мозга, аденомы гипофиза, рака коры надпочечников, рака желчного пузыря, рака селезенки, холангиокарциномы, фибросаркомы, нейробластомы, ретинобластомы или их комбинаций у субъекта включает введение субъекту терапевтически эффективных количеств (a) композиции, включающей кристаллическое свободное основание ABT-263 (или полученной с применением этого основания в качестве API), и (b) одного или нескольких препаратов из числа этопозида, винкристина, CHOP, ритуксимаба, рапамицина, R-CHOP, RCVP, DA-EPOCH-R или бортезомиба.
В конкретных вариантах осуществления композицию, включающую кристаллическое свободное основание ABT-263 (или полученную с применением этого основания в качестве API), вводят в терапевтически эффективном количестве субъекту при наличии такой необходимости, в схеме комбинированной терапии вместе с этопозидом, винкристином, CHOP, ритуксимабом, рапамицином, R-CHOP, RCVP, DA-EPOCH-R или бортезомибом в терапевтически эффективном количестве, для лечения лимфоидных злокачественных заболеваний, например, B-клеточной лимфомы или неходжкинской лимфомы.
В других конкретных вариантах осуществления композицию, включающую кристаллическое свободное основание ABT-263 (или полученную с применением этого основания в качестве API), вводят в терапевтически эффективном количестве субъекту при наличии такой необходимости, в схеме монотерапии или комбинированной терапии вместе с этопозидом, винкристином, CHOP, ритуксимабом, рапамицином, R-CHOP, RCVP, DA-EPOCH-R или бортезомибом в терапевтически эффективном количестве, для лечения хронического лимфоцитарного лейкоза или острого лимфоцитарного лейкоза.
Дополнительную информацию, имеющую отношение к настоящему изобретению, можно найти в недавно опубликованной статье Tse et al. (2008) Cancer Res. 68:3421-3428, и дополнительные данные к этой статье доступны на Cancer Research Online (cancerres.aacrjournals.org/). Эта статья и дополнительные данные к ней включены в настоящую заявку в полном объеме посредством ссылки.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЛИ И КРИСТАЛЛИЧЕСКИЕ ФОРМЫ ИНДУЦИРУЮЩЕГО АПОПТОЗ АГЕНТА | 2011 |
|
RU2628560C2 |
| КАПСУЛА АВТ-263 | 2010 |
|
RU2550956C2 |
| СТАБИЛИЗИРОВАННАЯ ЛИПИДНАЯ ПРЕПАРАТИВНАЯ ФОРМА ПРОМОТОРА АПОПТОЗА | 2010 |
|
RU2530642C2 |
| ТВЕРДЫЕ ДИСПЕРСИИ, СОДЕРЖАЩИЕ СПОСОБСТВУЮЩЕЕ АПОПТОЗУ | 2010 |
|
RU2550134C2 |
| СОЛИ ДАСАТИНИБА В КРИСТАЛЛИЧЕСКОЙ ФОРМЕ | 2014 |
|
RU2662805C2 |
| МНОГОКОМПОНЕНТНЫЕ КРИСТАЛЛЫ, СОДЕРЖАЩИЕ ДАЗАТИНИБ И ОПРЕДЕЛЕННЫЕ СОКРИСТАЛЛОБРАЗОВАТЕЛИ | 2013 |
|
RU2650524C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ ИЗОХИНОЛИНОНОВ И ТВЕРДЫЕ ФОРМЫ ИЗОХИНОЛИНОНОВ | 2012 |
|
RU2626883C2 |
| СОЛИ И ПОЛИМОРФНЫЕ МОДИФИКАЦИИ ИНГИБИТОРА VEGF-R | 2006 |
|
RU2369607C1 |
| ФАРМАЦЕВТИЧЕСКАЯ ДОЗИРОВАННАЯ ФОРМА ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ ИНГИБИТОРА СЕМЕЙСТВА BCL-2 | 2010 |
|
RU2568599C2 |
| КРИСТАЛЛИЧЕСКИЕ ИНГИБИТОРЫ БРОМОДОМЕНОВ | 2014 |
|
RU2675268C2 |
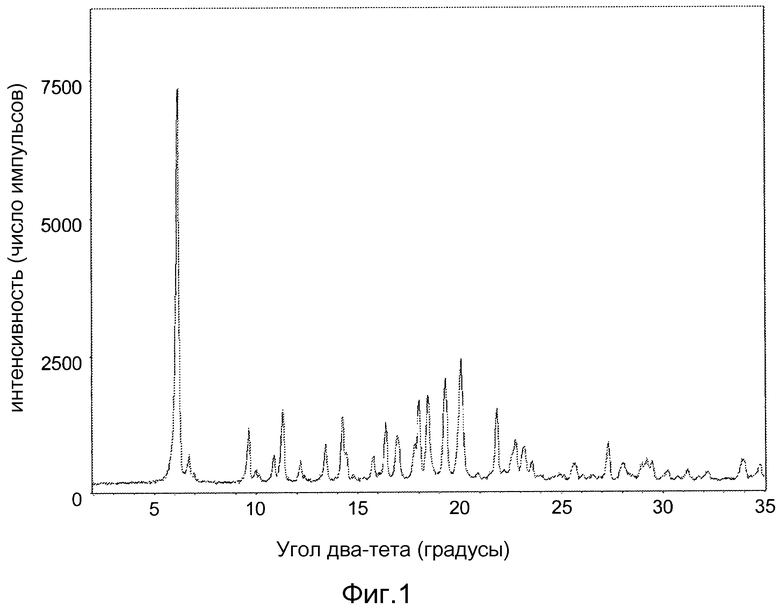
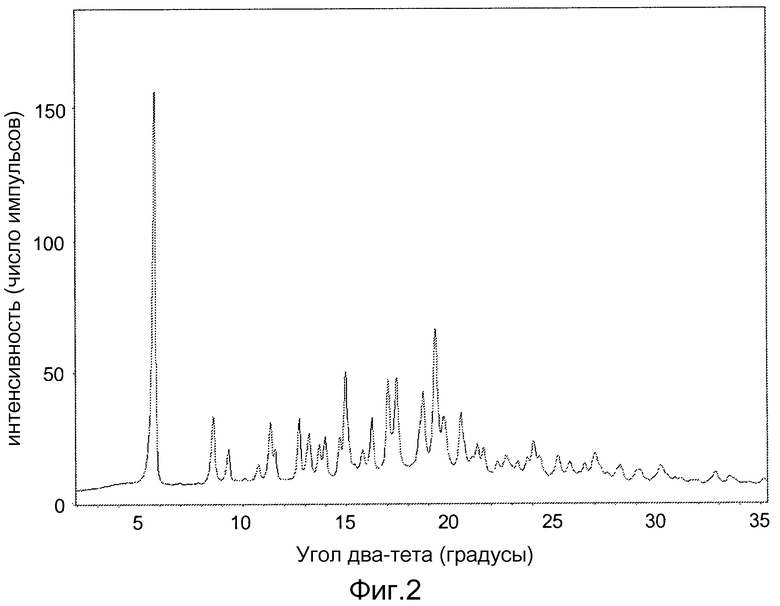
Изобретение относится к области органической химии, а именно к N-(4-(4-((2-(4-хлорфенил)-5,5-диметил-1-циклогекс-1-ен-1-ил)метил)пиперазин-1-ил)бензоил)-4-(((1R)-3-(морфолин-4-ил)-1-((фенилсульфанил)метил)пропил)-амино)-3-((трифторметил)сульфонил)бензолсульфонамиду (АВТ-263) в твердой кристаллической форме. Также изобретение относится к фармацевтической композиции на основе указанных кристаллических форм, способу лечения заболеваний, характеризующихся нарушением апоптоза и/или избыточной экспрессией антиапоптических белков семейства Bcl-2. Технический результат: получены новые кристаллические формы АВТ-263, обладающие полезными биологическими свойствами. 7 н. и 28 з.п. ф-лы, 2 ил., 22 табл.
1. Соединение N-(4-(4-((2-(4-хлорфенил)-5,5-диметил-1-циклогекс-1-ен-1-ил)метил)пиперазин-1-ил)бензоил)-4-(((1R)-3-(морфолин-4-ил)-1-((фенилсульфанил)метил)пропил)амино)-3-((трифторметил)сульфонил)бензолсульфонамид в твердой кристаллической форме, где указанная кристаллическая форма является формой I свободного основания АВТ-263, которая характеризуется по крайней мере наличием пиков на картине дифракции рентгеновских лучей на порошке в одном или нескольких из следующих положений: 6,21, 6,72, 12,17, 18,03 и 20,10° 2θ, ±0,2° 2θ.
2. Соединение по п.1, где указанная кристаллическая форма является формой I свободного основания АВТ-263, которая характеризуется по крайней мере наличием дифракционных пиков на картине дифракции рентгеновских лучей на порошке в каждом из указанных положений.
3. Соединение по п.1, где указанная кристаллическая форма является формой I свободного основания АВТ-263, которая характеризуется по крайней мере наличием пиков на картине дифракции рентгеновских лучей на порошке в каждом из следующих положений: 6,21, 6,72, 9,66, 10,92, 11,34, 12,17, 14,28, 16,40, 16,95, 17,81, 18,03, 18,47, 19,32, 20,10 и 21,87° 2θ, ±0,2° 2θ.
4. Соединение N-(4-(4-((2-(4-хлорфенил)-5,5-диметил-1-циклогекс-1-ен-1-ил)метил)пиперазин-1-ил)бензоил)-4-(((1R)-3-(морфолин-4-ил)-1-((фенилсульфанил)метил)пропил)амино)-3-((трифторметил)сульфонил)бензолсульфонамид в твердой кристаллической форме, где указанная кристаллическая форма является формой II свободного основания АВТ-263, которая характеризуется по крайней мере наличием пиков на картине дифракции рентгеновских лучей на порошке в одном или нескольких из следующих положений: 5,79, 8,60, 12,76, 15,00 и 20,56° 2θ, ±0,2° 2θ.
5. Соединение по п.4, где указанная кристаллическая форма является формой II свободного основания АВТ-263, которая характеризуется по крайней мере наличием дифракционных пиков на картине дифракции рентгеновских лучей на порошке в каждом из указанных положений.
6. Соединение по п.4, где указанная кристаллическая форма является формой II свободного основания АВТ-263, которая характеризуется по крайней мере наличием пиков на картине дифракции рентгеновских лучей на порошке в каждом из следующих положений: 5,79, 8,60, 9,34, 10,79, 11,36, 11,59, 12,76, 13,23, 13,73, 14,01, 14,72, 15,00, 16,28, 17,07, 17,48, 18,75, 19,34, 19,71, 20,56 и 21,35° 2θ, ±0,2° 2θ.
7. Соединение N-(4-(4-((2-(4-хлорфенил)-5,5-диметил-1-циклогекс-1-ен-1-ил)метил)пиперазин-1-ил)бензоил)-4-(((1R)-3-(морфолин-4-ил)-1-((фенилсульфанил)метил)пропил)амино)-3-((трифторметил)сульфонил)бензолсульфонамид в твердой кристаллической форме, где кристаллическая форма является сольватом, включающим свободное основание АВТ-263, сольватированное органическим растворителем.
8. Соединение по п.7, где сольват выбран из группы, состоящей из сольватов со смесью этанола/этилацетата, 1-пропанолом, 2-пропанолом, метанолом, бензолом, толуолом, смесью диоксана/гексана, смесью метилацетата/гексана, хлороформом, этилацетатом, изопропилацетатом, метилацетатом, пиридином, анизолом и трифтортолуолом.
9. Фармацевтическая композиция обладающая активирующей апоптоз активностью, содержащая соединение по любому из пп.1, 4 и 7 в твердой кристаллической форме и один или несколько фармацевтически приемлемых эксципиентов.
10. Способ получения фармацевтической композиции АВТ-263 в форме раствора, включающий растворение соединения по любому из пп.1, 4 и 7 в фармацевтически приемлемом растворителе или смеси растворителей.
11. Способ по п.10, где кристаллическое свободное основание АВТ-263 включает форму I свободного основания АВТ-263.
12. Способ по п.10, где кристаллическое свободное основание АВТ-263 включает форму II свободного основания АВТ-263.
13. Способ лечения заболевания, характеризующегося нарушением апоптоза и/или избыточной экспрессией антиапоптотического белка семейства Bcl-2, включающий введение субъекту, у которого имеется такое заболевание, композиции, содержащей терапевтически эффективное количество соединения по любому из пп.1, 4 и 7 и один или несколько фармацевтически приемлемых эксципиентов, где заболеванием является неопластическое заболевание, выбранное из рака, мезотелиомы, рака мочевого пузыря, рака поджелудочной железы, рака кожи, рака органов головы и шеи, кожной или внутриглазной меланомы, рака яичников, рака груди, рака матки, карциномы фаллопиевых труб, карциномы эндометрия, карциномы шейки матки, карциномы влагалища, карциномы вульвы, рака костей, рака толстой кишки, рака прямой кишки, рака анальной области, рака желудка, рака желудочно-кишечного тракта (желудка, колоректального и/или дуоденального), хронического лимфоцитарного лейкоза, острого лимфоцитарного лейкоза, рака пищевода, рака тонкого кишечника, рака эндокринной системы, рака щитовидной железы, рака паращитовидной железы, рака надпочечника, саркомы мягких тканей, рака мочеиспускательного канала, рака пениса, рака яичек, гепатоцеллюлярного (печени и/или желчного протока) рака, первичной или вторичной опухоли центральной нервной системы, первичной или вторичной опухоли головного мозга, болезни Ходжкина, хронического или острого лейкоза, хронического миелоидного лейкоза, лимфоцитарной лимфомы, лимфобластного лейкоза, фолликулярной лимфомы, лимфоидных злокачественных новообразований Т-клеточного или В-клеточного происхождения, меланомы, множественной миеломы, рака ротовой полости, немелкоклеточного рака легких, рака простаты, мелкоклеточного рака легких, рака почек и/или мочеточника, карциномы почечных клеток, карциномы почечной лоханки, новообразований центральной нервной системы, первичной лимфомы центральной нервной системы, неходжкинской лимфомы, опухоли спинного мозга, глиомы ствола мозга, аденомы гипофиза, рака коры надпочечников, рака желчного пузыря, рака селезенки, холангиокарциномы, фибросаркомы, нейробластомы, ретинобластомы и их комбинаций.
14. Способ по п.13, где соединение включает форму I свободного основания АВТ-263.
15. Способ по п.14, где соединение включает форму II свободного основания АВТ-263.
16. Способ по п.13, где соединение включает сольват, содержащий свободное основание АВТ-263, сольватированное органическим растворителем.
17. Способ по п.16, где сольват выбран из группы, состоящей из сольватов со смесью этанола/этилацетата, 1-пропанолом, 2-пропанолом, метанолом, бензолом, толуолом, смесью диоксана/гексана, смесью метилацетата/гексана, хлороформом, этилацетатом, изопропилацетатом, метилацетатом, пиридином, анизолом и трифтортолуолом.
18. Способ по п.13, где композицию вводят пероральным, парентеральным, сублингвальным, буккальным, интраназальным, легочным, местным, трансдермальным, интрадермальным, глазным, ушным, ректальным, вагинальным, внутрижелудочным, внутричерепным, интрасиновиальным или внутрисуставным путем.
19. Способ по п.13, где неопластическое заболевание представляет собой лимфоидное злокачественное заболевание.
20. Способ по п.19, где лимфоидное злокачественное заболевание является неходжкинской лимфомой.
21. Способ по п.13, где композицию вводят перорально в количестве от примерно 50 до примерно 1000 мг АВТ-263 в день со средним интервалом между введениями от примерно 3 часов до примерно 7 дней.
22. Способ по п.13, где композицию вводят перорально один раз в день в количестве от примерно 200 до примерно 400 мг эквивалента свободного основания АВТ-263 в день.
23. Способ лечения заболевания, характеризующегося нарушением апоптоза и/или избыточной экспрессией антиапоптотического белка семейства Bcl-2, включающий растворение терапевтически эффективного количества соединения по любому из пп.1, 4 и 7 в фармацевтически приемлемом растворителе или смеси растворителей и введение полученного раствора субъекту, у которого имеется это заболевание; где заболеванием является неопластическое заболевание, выбранное из рака, мезотелиомы, рака мочевого пузыря, рака поджелудочной железы, рака кожи, рака органов головы и шеи, кожной или внутриглазной меланомы, рака яичников, рака груди, рака матки, карциномы фаллопиевых труб, карциномы эндометрия, карциномы шейки матки, карциномы влагалища, карциномы вульвы, рака костей, рака толстой кишки, рака прямой кишки, рака анальной области, рака желудка, рака желудочно-кишечного тракта (желудка, колоректального и/или дуоденального), хронического лимфоцитарного лейкоза, острого лимфоцитарного лейкоза, рака пищевода, рака тонкого кишечника, рака эндокринной системы, рака щитовидной железы, рака паращитовидной железы, рака надпочечника, саркомы мягких тканей, рака мочеиспускательного канала, рака пениса, рака яичек, гепатоцеллюлярного (печени и/или желчного протока) рака, первичной или вторичной опухоли центральной нервной системы, первичной или вторичной опухоли головного мозга, болезни Ходжкина, хронического или острого лейкоза, хронического миелоидного лейкоза, лимфоцитарной лимфомы, лимфобластного лейкоза, фолликулярной лимфомы, лимфоидных злокачественных новообразований Т-клеточного или В-клеточного происхождения, меланомы, множественной миеломы, рака ротовой полости, немелкоклеточного рака легких, рака простаты, мелкоклеточного рака легких, рака почек и/или мочеточника, карциномы почечных клеток, карциномы почечной лоханки, новообразований центральной нервной системы, первичной лимфомы центральной нервной системы, неходжкинской лимфомы, опухоли спинного мозга, глиомы ствола мозга, аденомы гипофиза, рака коры надпочечников, рака желчного пузыря, рака селезенки, холангиокарциномы, фибросаркомы, нейробластомы, ретинобластомы и их комбинаций.
24. Способ по п.23, где соединение включает форму I свободного основания АВТ-263.
25. Способ по п.23, где соединение включает форму II свободного основания АВТ-263.
26. Способ по п.23, где соединение включает сольват, содержащий свободное основание АВТ-263, сольватированное органическим растворителем.
27. Способ по п.26, где сольват выбран из группы, состоящей из сольватов со смесью этанола/этилацетата, 1-пропанолом, 2-пропанолом, метанолом, бензолом, толуолом, смесью диоксана/гексана, смесью метилацетата/гексана, хлороформом, этилацетатом, изопропилацетатом, метилацетатом, пиридином, анизолом и трифтортолуолом.
28. Способ по п.23, где указанный раствор вводят пероральным, парентеральным, сублингвальным, буккальным, интраназальным, легочным, местным, трансдермальным, интрадермальным, глазным, ушным, ректальным, вагинальным, внутрижелудочным, внутричерепным, интрасиновиальным или внутрисуставным путем.
29. Способ по п.23, где неопластическое заболевание представляет собой лимфоидное злокачественное заболевание.
30. Способ по п.29, где лимфоидное злокачественное заболевание является неходжкинской лимфомой.
31. Способ по п.23, где указанный раствор вводят перорально в количестве от примерно 50 до примерно 1000 мг АВТ-263 в день со средним интервалом между введениями от примерно 3 часов до примерно 7 дней.
32. Способ по п.23, где указанный раствор вводят перорально один раз в день в количестве от примерно 200 до примерно 400 мг эквивалента свободного основания АВТ-263 в день.
| Wang G | |||
| Железнодорожный снегоочиститель на глубину до трех сажен | 1920 |
|
SU263A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
Авторы
Даты
2015-05-20—Публикация
2010-09-15—Подача