2420-171930RU/010
ВАРИАНТЫ CRIg С СОЗРЕВШЕЙ АФФИННОСТЬЮ
Описание
Область техники, к которой относится изобретение
Настоящее изобретение относится к вариантам CRIg с созревшей аффинностью. В частности, настоящее изобретение относится к вариантам CRIg, обладающим более высоким сродством связывания с C3b и сохраняющим способность избирательного связывания с C3b по сравнению с С3.
Уровень техники
Система комплемента
Система комплемента представляет собой сложный каскад ферментов, состоящий из серии сывороточных гликопротеинов, которые обычно находятся в форме неактивных проферментов. Существуют три основных пути активации комплемента: классический путь, альтернативный путь и путь, опосредуемый манноза-связывающим лектином, которые соединяются на уровне С3, где две подобные конвертазы расщепляют С3 с образованием С3а и C3b.
Макрофаги являются специализированными клетками, обладающими природной способностью распознавать едва различимые отличия в структуре экспрессированных на поверхности клеток идентифицирующих меток, так называемых молекулярных паттернов (Taylor, et al., Eur. J. Immunol. 33, 2090-1097 (2003); Taylor, et al., Annu. Rev. Immunol. 23, 901-944 (2005)). Хотя прямое распознавание таких поверхностных структур является основным признаком врожденного иммунитета, опсонизация позволяет рецепторам родовых макрофагов опосредовать поглощение клеткой частиц в процессе фагоцитоза, повышая эффективность и расширяя спектр распознавания фагоцита (Stuart and Ezekowitz, Immunity 22, 539-550 (2005)). Процесс фагоцитоза включает многочисленные взаимодействия рецепторов с лигандами, и в настоящее время известно, что разные опсонины, включая иммуноглобулины, коллектины и компоненты комплемента, управляют активностью клеток, необходимой для интернализации патогенных микроорганизмов в результате взаимодействия с рецепторами макрофагов на поверхности клеток (обзор в публикации Aderem and Underhill, Annu. Rev. Immunol. 17, 593-623 (1999); Underhill and Ozinsky, Annu. Rev. Immunol. 20, 825-852 (2002)). Несмотря на то, что природные иммуноглобулины, кодированные генами зародышевых клеток, могут распознавать целый ряд патогенных микроорганизмов, большинство опсонизирующих IgG образуется в результате приобретенного иммунитета, поэтому эффективный клиренс, опосредованный Fc-рецепторами, не является немедленным (Carroll, Nat. Immunol. 5, 981-986 (2004)). Комплемент, с другой стороны, быстро распознает молекулы на поверхности патогенного микроорганизма и стимулирует поглощение такой частицы рецепторами комплемента (Brown, Infect. Agents Dis. 1, 63-70 (1991)).
Комплемент состоит из более чем 30 сывороточных белков, которые опсонизируют целый ряд патогенных микроорганизмов, благодаря чему их могут распознавать рецепторы комплемента. В зависимости от исходного пускового механизма каскада можно различить три пути (обзор в публикации Walport, N., Engl. J. Med. 344, 1058-1066 (2001)). Все три пути характеризуются общей стадией активации центрального компонента С3, но отличаются характером распознавания и исходными стадиями биохимических процессов, вызывающих активацию С3. Классический путь активируется антителами, связанными с поверхностью патогенного микроорганизма, которые в свою очередь связываются с компонентом комплемента C1q, активируя каскад сериновых протеаз, которые в конце концов расщепляют С3 с образованием его активной формы C3b. Путь, опосредуемый лектином, активируется после распознавания углеводных фрагментов белками лектина. В настоящее время идентифицированы три члена указанного пути: манноза-связывающие лектины (MBL), семейство SIGN-R1 лектинов и фиколины (Pyz et al., Ann. Med. 38, 242-251 (2006)). Как MBL, так и фиколины связаны с сериновыми протеазами, которые действуют подобно С1 в классическом пути, активируя компоненты С2 и С4, вызывающие главную стадию С3. Альтернативный путь отличается от классического пути и пути, опосредуемого лектином, тем, что его активация происходит в результате прямого взаимодействия внутреннего сложного эфира С3 с узнаваемыми фрагментами на поверхности патогенного микроорганизма. Первоначальное связывание С3 с активирующей поверхностью вызывает быструю амплификацию отложения C3b под воздействием протеаз альтернативного пути, фактора В и фактора D. Важно отметить, что классический путь или путь, опосредуемый лектином, также может вызывать амплификацию отложения C3b под воздействием факторов В и D. Во всех трех путях активации комплемента основной стадией в опсонизации является превращение компонента С3 в C3b. Расщепление С3 ферментами каскадов комплемента вызывает нуклеофильную атаку сложного тиоэфира, обеспечивающую ковалентное связывание C3b с поверхностями антигена при помощи домена сложного тиоэфира. Указанное связывание является начальной стадией в опсонизации комплемента. Последующий протеолиз связанного C3b вызывает образование фрагментов iC3b, С3с и C3dg, которые распознаются разными рецепторами (Ross and Medof, Adv. Immunol. 37, 217-267 (1985)). Такое расщепление устраняет способность C3b далее амплифицировать отложение C3b и активирует последующие компоненты каскада комплемента, включая мембраноатакующий комплекс, способный непосредственно разрушать мембрану. Однако фагоцитарные рецепторы макрофага предпочтительно распознают C3b и его фрагменты; благодаря разнообразию образования сложноэфирных связей С3-опосредуемая опсонизация имеет главное значение для распознавания патогенных микроорганизмов (Holers et al., Immunol. Today 13, 231-236 (1992)), поэтому рецепторы для разных продуктов расщепления С3 играют важную роль в иммунном ответе хозяина.
С3 представляет собой сложный и гибкий белок, состоящий из 13 разных доменов. Ядро молекулы состоит из 8 так называемых доменов макроглобулина (MG), которые образуют плотно упакованные α- и β-цепи С3. В указанную структуру встроены домены CUB (C1r/C1s, Uegf и Bone морфогенетический белок-1) и TED, при этом последний домен содержит сложную тиоэфирную связь, которая делает возможным ковалентное связывание C3b с поверхностями патогенных микроорганизмов. Остальные домены содержат С3а или действуют в качестве линкеров и спейсеров внутренних доменов. Сравнение структур C3b и С3а с С3 показывает, что данная молекула подвергается значительной конформационной перестройке с каждым протеолизом, в результате чего обнажается не только домен TED, но также дополнительные новые поверхности молекулы, которые могут взаимодействовать с клеточными рецепторами (Janssen and Gros, Mol. Immunol. 44, 3-10 (2007)).
Рецепторы комплемента С3 на фагоцитарных клетках
Известны три надсемейства генов рецепторов комплемента: модули короткого консенсусного повтора (SCR), кодирующего CR1 и CR2, члены CR3 и CR4 семейства бета-2 интегринов и член CRIg надсемейства иммуноглобулинов Ig.
CR1 является гликопротеином с молекулярной массой 180-210 кДа, состоящим из 30 коротких консенсусных повторов (SCR), и играет важную роль в клиренсе иммунного комплекса. Короткие консенсусные повторы (SCR) являются модульными структурами, состоящими примерно из 60 аминокислот, каждая из которых имеет две пары дисульфидных связей, обеспечивающих жесткость структуры. Высокое сродство связывания с C3b и C4b определяется двумя отдельными сайтами, состоящими из 3 SCR (обзор в публикации Krych-Goldberg and Atkinson, Immunol. Rev. 180, 112-122 (2001)). Структура сайта связывания C3b, находящегося внутри коротких консенсусных повторов (SCR) 15-17 гликопротеина CR1 (сайт 2), была определена методом MRI (Smith et al., Cell 108, 769-780 (2002)), показавшим, что три модуля расположены в направлении от глобулярного участка к концевому участку, при этом гибкость обеспечивает сочленение на сайтах 16-17. Определяемый структурой мутагенез позволил идентифицировать положительно заряженную поверхностную область на модуле 15, которая имеет важное значение для связывания C4b. Указанный участок вместе с основными боковыми цепями модуля 16, находящимися на той же поверхности CR1, необходим для связывания C3b. Основная функция CR1, первоначально описанного как рецептор иммунной адгезии (Rothman et al., J. Immunol. 115, 1312-1315 (1975)), состоит в улавливании IC на эритроцитах с целью переноса в печень для клиренса (Taylor et al., Clin. Immunol. Immunopathol. 82, 49-59 (1997)). В процессе фагоцитоза CR1 воздействует на нейтрофилы, а не на тканевые макрофаги (Sengelov et al., J. Immunol. 153, 804-810 (1994)). Помимо участия в клиренсе иммунных комплексов, гликопротеин CR1 является сильным ингибитором активации классического и альтернативного пути в результате его взаимодействия с соответствующими конвертазами (Krych-Goldberg and Atkinson, 2001, см. выше; Krych-Goldberg et al., J. Biol. Chem. 274, 31160-31168 (1999)). У мыши CR1 и CR2 являются двумя продуктами одного гена, образующимися в результате альтернативного сплайсинга, которые связаны главным образом с В-лимфоцитами и фолликулярными дендритными клетками и в основном регулируют реакции В-клеток (Molina et al., 1996). Мышиный функциональный эквивалент CR1, Crry, инактивирует ферменты классического и альтернативного путей и действует скорее в качестве природного регулятора активации комплемента, а не фагоцитарного рецептора (Molina et al., Proc. Natl. Acad. Sci. USA 93, 3357-3361 (1992)).
CR2 (CD21) связывает iC3b и C3dg и является основным рецептором комплемента, усиливающим В-клеточный иммунитет (Carroll, Nat. Immunol. 5, 981-986 (2004); Weis et al., Proc. Natl. Acad. Sci. USA 81, 881-885 (1984)). Поглощение C3b-покрытого антигена родственными В-клетками вызывает усиление сигнала, передаваемого рецептором В-клеточного антигена. Таким образом, связывание корецептора CD21-CD19-CD81 с рецептором В-клеточного антигена снижает порог активации В-клеток и формирует важный сигнал выживания (Matsumoto et al., J. Exp. Med. 173, 55-64 (1991)). Сайт связывания CR2 на iC3b был картирован частично на границе между доменами TED и MG1 (Clemenza and Isenman, J. Immunol. 165, 3839-3848 (2000)).
CR3 и CR4 являются трансмембранными гетеродимерами, состоящими из альфа-субъединицы (соответственно CD11b или αМ и CD11c или αХ) и общей бета-цепи (CD18 или β2), которые участвуют в адгезии с внеклеточным матриксом и другими клетками, а также в распознавании iC3b. Указанные рецепторы относятся к семейству интегринов и выполняют определенные функции не только в фагоцитозе, но также в процессе направленной миграции и перемещении лейкоцитов, формировании и костимуляции синапса (обзор в публикации Ross, Adv. Immunol. 37, 217-267 (2000)). Адгезивность интегрина регулируется процессом, именуемым передачей перевернутого сигнала, трансформирующего интегрины из низкоаффинного в высокоаффинное состояние связывания (Liddington and Ginsberg, J. Cell Biol. 158, 833-839 (2002)). Кроме того, связывание с лигандом вызывает передачу сигналов из внеклеточного домена в цитоплазму. Сайты связывания iC3b картированы в нескольких доменах альфа-цепи CR3 и CR4 (Diamond et al., J. Cell Biol. 120, 1031-1043 (1993); Li and Zhang, J. Biol. Chem. 278, 34395-34402 (2003); Xiong and Zhang, J. Biol. Chem. 278, 34395-34402 (2001)). Несколько лигандов для CR3: iC3b, бета-глюкан и ICAM-1, по-видимому, связываются с частично перекрывающимися сайтами, находящимися в I домене CD11b (Balsam et al., 1998; Diamond et al., 1990; Zhang and Plow, 1996). Специфическое распознавание протеолитически инактивированной формы C3b, iC3b, было предсказано на основании структурных исследований, которые позволили локализовать сайты связывания CR3 в остатках, открываемых при развертывании домена CUB в C3b (Nishida et al., Proc. Natl. Acad. Sci. USA 103, 19737-19742 (2006)), что происходит при расщеплении α'-цепи регуляторной протеазой комплемента, фактором I.
CRIg является ассоциированным с макрофагом рецептором, гомологичным антигену А33 и JAM1, который необходим для клиренса патогенных микроорганизмов из кровотока. Белок CRIg человека был первоначально клонирован из библиотеки плодной кДНК человека при использовании вырожденных затравок, узнающих консервативные домены Ig JAM1 человека. Секвенирование нескольких клонов выявило открытую рамку считывания, состоящую из 400 аминокислот. Исследования при помощи Blast подтвердили сходство с Z39Ig, трансмембранным белком типа 1 (Langnaese et al., Biochim. Biophys. Acta 1492 (2000) 522-525). Было установлено, что внеклеточная область данной молекулы состоит из двух Ig-подобных доменов, включающих N-концевой домен V-популяции и С-концевой домен С2-популяции. Новый белок человека первоначально был определен как ”единичный трансмемблранный член надсемейства Ig, ассоциированный с макрофагом (huSTIgMA)”. Затем при использовании 3'- и 5'-концевых затравок был клонирован сплайсированный вариант huSTIgMA, в котором отсутствует близкий к мембране домен IgC и который короче на 50 аминокислот. Более короткий сплайсированный вариант данного белка человека получил название huSTIgMAкороткий. Аминокислотная последовательность huSTIgMA (определяемая как PRO362) и кодирующая полинуклеотидная последовательность описаны в патенте США № 6410708, выданном 25 июня 2002 г. Кроме того, huSTIgMA и huSTIgMAкороткий, а также мышиный белок STIgMA (muSTIgMA) и последовательности нуклеиновой кислоты описаны в публикации РСТ WO 2004031105, опубликованной 15 апреля 2004 г.
Кристаллическая структура CRIg и комплекс C3b:CRIg описаны в публикации заявки на патент США № 2008/0045697, опубликованной 21 февраля 2008 г.
Клетки Купфера (КС), находящиеся в синусоидальной полости печени, образуют самую большую популяцию макрофагов в теле. Несмотря на то, что клетки Купфера имеют маркеры аналогично другим тканевым макрофагам, они выполняют специальные функции, обеспечивающие эффективный клиренс кишечных бактерий, микробных остатков, бактериальных эндотоксинов, иммунных комплексов и мертвых клеток, присутствующих в крови воротной вены, поступающей из системы микрососудов пищеварительного тракта (Bilzer et al., Liver Int. 26, 1175-1186 (2006)). Эффективное связывание патогенных микроорганизмов с поверхностью клеток Купфера является важной стадией первичной иммунной защиты от патогенных микроорганизмов (Benacerraf et al., J. Exp. Med. 110, 27-48 (1959)). Центральная роль клеток Купфера в быстром клиренсе патогенных микроорганизмов из кровотока проиллюстрирована значительным увеличением смертности у мышей с отсутствием клеток Купфера (Hirakata et al., Infect. Immun. 59, 289-294 (1991)). Идентификация CRIg еще больше подтвердила важную роль комплемента и клеток Купфера в первичной иммунной защите от патогенных микроорганизмов, циркулирующих в кровотоке.
Единственными рецепторами комплемента С3, идентифицированными в клетках Купфера мышей, являются CRIg и CR3 (Helmy et al., Cell 124, 915-927 (2006)), в то время как в клетках Купфера человека выявлена дополнительная экспрессия CR1 и CR4 (Hinglais et al., 1989). Рецепторы CRIg и CR3 в клетках Купфера способствуют связыванию с опсонизированными частицами iC3b in vitro (Helmy et al., Lab. Invest. 61, 509-514 (2006)). In vivo роль КС-экспрессируемого рецептора CR3 в связывании с iC3b-покрытыми патогенными микроорганизмами является менее очевидной. Было сделано предположение, что CR3 косвенно способствует клиренсу патогенных микроорганизмов путем рекрутинга нейрофилов и взаимодействия с экспрессирующим нейтрофилы ICAM1 (Conlan and North, Exp. Med. 179, 259-268 (1994); Ebe et al., Pathol. Int. 49, 519-532 (1999); Gregory et al., J. Immunol. 157, 2514-2520 (1996); Gregory and Wing, J. Leukoc. Biol. 72, 239-248 (2002); Rogers and Unanue, Infect. Immun. 61, 5090-5096 (1993)). В отличие от этого CRIg непосредственно участвует в улавливании патогенных микроорганизмов, проходящих через синусоидальную полость печени (Helmy et al., 2006, см. выше). Различие в биологии CRIg и CR3 частично нашло отражение в различии характеристик связывания двух указанных рецепторов. CRIg, экспрессированный на клетках Купфера, конститутивно связывается с мономерными фрагментами С3, в то время как CR3 связывается только с iC3b-опсонизированными частицами (Helmy et al., 2006, см. выше). Способность CRIg эффективно улавливать мономерные компоненты C3b и iC3b, а также C3b/iC3b-покрытые частицы отражает повышенную авидность, созданную множественным взаимодействием между молекулами CRIg, сконцентрированными на конце удлинений мембраны макрофагов (Helmy et al., 2006, см. выше), и многомерами C3b и iC3b, присутствующими на поверхности патогенного микроорганизма. В то время как CR3 связывается только с iC3b-покрытыми частицами, CRIg дополнительно связывается с C3b, первым продуктом расщепления С3, образованным на патогенных микроорганизмах, опсонизированных сывороткой (Croize et al., Infect. Immun. 61, 5134-5139 (1993)). Так как большое число молекул C3b, связанных с поверхностью патогенного микроорганизма, защищено от расщепления факторами Н и I (Gordon et al., J. Infect. Dis. 157, 697-704 (1988)), узнавание лигандов C3b рецептором CRIg обеспечивает быстрое связывание и клиренс. Таким образом, несмотря на то, что на клетках Купфера экспрессированы как CRIg, так и CR3, указанные рецепторы характеризуются разной специфичностью к лигандам, разными свойствами связывания и разной кинетикой клиренса патогенных микроорганизмов.
Примерами патогенных микроорганизмов, использующих рецепторы на поверхности клеток для проникновения в клетку, являются вирусы, такие как вирус иммунодефицита человека (ВИЧ), внутриклеточные бактерии, такие как Mycobacterium tuberculosum, Mycobacterium leprae, Yersinia pseudotuberculosis, Salmonella typhimurium и Listeria Monocytogenes, и паразиты, такие как простигматоид Leishmania major (Cossart and Sansonetti, Science 304:242-248 (2004); Galan, Cell 103:363-366 (2000); Hornef et al., Nat. Immunol. 3:1033-1040 (2002); Stoiber et al., Mol. Immunol. 42:153-160 (2005)).
Как было указано выше, CRIg является недавно обнаруженным рецептором комплемента С3, экспрессированным в субпопуляции тканевых макрофагов. Помимо функционирования в качестве рецептора комплемента для белков С3, внеклеточный домен IgV рецептора CRIg избирательно ингибирует альтернативный путь активации комплемента путем связывания с C3b и ингибирования протеолитической активации С3 и С5. Однако сродство связывания CRIg с субъединицей конвертазы C3b является низким (IC50>1 мкМ), требуя относительно высокой концентрации белка для достижения почти полного ингибирования комплемента. Поэтому существует потребность в полипептидах CRIg, обладающих улучшенной терапевтической эффективностью. Настоящее изобретение относится к таким полипептидам.
Сущность изобретения
Настоящее изобретение по меньшей мере частично относится к созданию варианта CRIg с повышенным сродством связывания. Белок CRIg-ECD, содержащий комбинированные замены аминокислот Q64R и M86Y, характеризуется 30-кратным увеличением сродства связывания и 7-кратным улучшением активности ингибирования комплемента по сравнению с вариантом CRIg дикого типа. Кроме того, лечение гибридным белком CRIg с улучшенным сродством связыввния в мышиной модели артрита вызывало значительное снижение клинических оценок по сравнению с лечением белком CRIg дикого типа.
Таким образом, настоящее изобретение относится к вариантам CRIg.
Одним объектом настоящего изобретения является вариант CRIg, включающий замену аминокислот в области, выбираемой из группы, состоящей из Е8-К15, R41-T47, S54-Q64, E85-Q99 и Q105-K111 аминокислотной последовательности SEQ ID NO:2.
В одном варианте осуществления изобретения вариант избирательно связывается с C3b по сравнению с С3 или его фрагментом.
В другом варианте осуществления изобретения вариант CRIg обладает более высоким сродством связывания с C3b по сравнению с CRIg человека с нативной последовательностью SEQ ID NO:2, при этом сродство связывания может быть увеличено, например, по меньшей мере в 2 раза, по меньшей мере в 3 раза, по меньшей мере в 4 раза, по меньшей мере в 5 раз, по меньшей мере в 6 раз, по меньшей мере в 7 раз, по меньшей мере в 9 раз, по меньшей мере в 10 раз, по меньшей мере в 15 раз, по меньшей мере в 20 раз, по меньшей мере в 30 раз, по меньшей мере в 40 раз, по меньшей мере в 50 раз, по меньшей мере в 70 раз, по меньшей мере в 80 раз, по меньшей мере в 90 раз или по меньшей мере в 100 раз.
В другом варианте осуществления изобретения вариант CRIg является более сильным ингибитором альтернативного пути активации комплемента по сравнению с CRIg человека с нативной последовательностью SEQ ID NO:2.
В другом варианте осуществления изобретения вариант CRIg включает замену аминокислот в одном или нескольких положениях, выбираемых из группы, состоящей из положений 8, 14, 18, 42, 44, 45, 60, 64, 86, 99, 105 и 110 в аминокислотной последовательности SEQ ID NO:2.
В еще одном варианте осуществления изобретения вариант CRIg включает замену аминокислот в одном или нескольких положениях 60, 64, 86, 99, 105 и 110 в аминокислотной последовательности SEQ ID NO:2.
В дополнительном варианте осуществления изобретения вариант CRIg включает одну или несколько замен, выбираемых из группы, состоящей из E8W, W14F, E84Y/W14F; P45F; G42D/D44H/P45F; Q60I; Q64R; Q60I/Q64R; M86Y; M86W, M86F, M86W/Q9R; M86F/Q99R; K110D, K11N; Q105R/K110N; Q105R/K110Q и Q105K/K110D.
В другом варианте осуществления изобретения вариант CRIg включает одну или несколько замен, выбираемых из группы, состоящей из Q64R/M86Y; Q60I/Q64R/E8Y; Q60I/Q64R/G42D; Q60I/Q64R/P45F; Q60I/Q64R/G42D/D44H/P45F; Q60I/Q64R/M86Y; Q60I/Q64R/Q105R; Q60I/Q64R/Q105K; Q60I/Q64R/K110N; Q60I/Q105R/K110N; M86Y/E8Y; M86Y/G42D/D44H/P45F; M86Y/P45F; M86Y/G42D/D44H/P45F и M86Y/Q99K/M86Y/Q99R/M86Y/Q105R/M86Y/Q105K/M86Y/Q105R/K110N.
В еще одном варианте осуществления изобретения вариант CRIg включает одну или несколько замен, выбираемых из группы, состоящей из Q60I, Q64R, Q60I/Q64R, M86Y, Q99L, Q105K/K110D, E8W/Q105R/K110N, Q64R/M86Y, Q60I/Q64R/E8Y, Q60I/Q64R/G42D, Q60I/Q64R/P45F, Q60I/Q64R/G42D/D44H/P45F, Q60I/Q64R/M86Y, Q60I/Q64R/Q105R, Q60I/Q64R/Q105K, Q60I/Q64R/K110N, M86Y/P45F и M86Y/Q105K.
В более конкретном варианте осуществления изобретения вариант CRIg включает замену Q60I/Q64R/M86Y или Q60I/Q64R/G42D/D44H/P45F.
Другим объектом настоящего изобретения является химерная молекула, включающая вариант CRIg по настоящему изобретению.
В одном варианте осуществления изобретения химерная молекула является иммуноадгезином.
В другом варианте осуществления изобретения иммуноадгезин включает вариант CRIg, который короче непроцессированного CRIg SEQ ID NO:2.
В еще одном варианте осуществления изобретения химерная молекула включает внеклеточный домен CRIg.
Другим объектом настоящего изобретения является фармацевтическая композиция, включающая вариант CRIg или химерную молекулу, например, иммуноадгезин по настоящему изобретению, в смеси с фармацевтически приемлемым наполнителем.
Другим объектом настоящего изобретения является способ профилактики или лечения комплемент-ассоциированного заболевания или состояния, который включает введение субъекту, нуждающему в таком лечении, профилактически или терапевтически эффективного количества варианта CRIg или химерной молекулы, такой как иммуноадгезия, включающий такой вариант.
В одном варианте осуществления изобретения комплемент-ассоциированное заболевание является воспалительным заболеванием или аутоиммунным заболеванием.
В другом варианте осуществления изобретения комплемент-ассоциированное заболевание выбирают из группы, включающей ревматоидный артрит (RA), респираторный дистресс-синдром у взрослых (ARDS), поражение удаленных тканей после ишемии и реперфузии, активацию комплемента во время хирургической операции с искусственным кровообращением, дерматомиоцитоз, пемфигус, люпус-нефрит и проистекающие из него гломерулонефрит и васкулит, искусственное кровообращение, дисфункцию коронарного эндотелия, вызванную кардиоплегией, мембранозно-пролиферативный гломерулонефрит типа II, IgA-обусловленную нефропатию, острую почечную недостаточность, криоглобулемию, антифосфолипидный синдром, возрастную дегенерацию желтого пятна, увеит, диабетическую ретинопатию, аллотрансплантацию, сверхострое отторжение, гемодиализ, хроническое обструктивное заболевание легких (COPD), астму, аспирационную пневмонию, утрикарию, хроническую идиопатическую утрикарию, гемолитико-уремический синдром, эндометриоз, кардиогенный шок, ишемическую реперфузию и рассеянный склероз (MS).
В другом варианте осуществления изобретения комплемент-ассоциированное заболевание выбирают из группы, включающей воспалительное заболевание кишечника (IBD), системную красную волчанку, ревматоидный артрит, юношеский хронический артрит, спондилоартропатию, системный склероз (склеродерму), идиопатические воспалительные миопатии (дерматомиозит, полимиозит), ксеродерматоз (синдром Шегрена), системный васкулит, саркоидоз, аутоиммунную гемолитическую анемию (иммунную панцитопению, ночную пароксизмальную гемоглобинурию), аутоиммунную тромбоцитопению (идиопатическую тромботическую пурпуру, иммунную тромбоцитопению), тиреоидит (болезнь Грейвса, тиреоидит Хашимото, юношеский лимфоцитарный тиреоидит, атрофический тиреоидит), сахарный диабет, иммунное заболевание почек (гломерулонефрит, тубулоинтерстициальный нефрит), демиелинизирующие заболевания центральной и периферической нервной системы, такие как рассеянный склероз, идиопатическую полиневропатию, желчно-почечные заболевания, такие как инфекционный гепатит (гепатит А, В, С, D, Е и другие негепатотропные вирусы), аутоиммунный хронический активный гепатит, первичный билиарный цирроз печени, грануломатозный гепатит и склерозирующий холангит, воспалительные и фиброзные заболевания легких (например, муковисцидоз), глютензависимую энтеропатию, болезнь Уиппла, аутоиммунные или иммунные кожные заболевания, включающие буллезные кожные заболевания, полиморфную эритему и контактный дерматит, псориаз, аллергическмие заболевания легкого, такие как эозинофильная пневмония, идиопатический фиброз легких и аллергическая пневмония (пневмония с гиперчувствительностью), заболевания, обусловленные трансплантацией, включающие отторжение трансплантата, реакцию трансплантат-против-хозяина, болезнь Альцгеймера, ночную пароксизмальную гемоглобинурию, наследственный ангионевротический отек, атеросклероз и мембранозно-пролиферативный гломерулонефрит типа II.
В предпочтительном варианте осуществления изобретения комплемент-ассоциированное заболевание является ревматоидным артритом (RA).
В другом предпочтительном варианте осуществления изобретения комплемент-ассоциированное заболевание является комплемент-ассоциированным глазным заболеванием.
В другом варианте осуществления изобретения комплемент-ассоциированное глазное заболевание выбирают из группы, включающей все стадии возрастной дегенерации желтого пятна (AMD), увеит, диабетическую и другие обусловленные ишемией ретинопатии, эндофтальмит и другие внутриглазные заболевания, вызванные образованием новых сосудов.
В другом варианте осуществления изобретения внутриглазное заболевание, вызванное образованием новых сосудов, выбирают из группы, включающей диабетический отек желтого пятна, патологическую миопию, болезнь Гиппеля-Линдау, гистоплазмоз глаза, окклюзию центральной вены сетчатки (CRVO), образование новых сосудов в роговице и образование новых сосудов в сетчатке.
В еще одном варианте осуществления изобретения комплемент-ассоциированное глазное заболевание выбирают из группы, включающей возрастную дегенерацию желтого пятна (AMD), образование новых сосудов в сосудистой оболочке глаза (CNV), диабетическую ретинопатию (DR) и эндофтальмит, при этом возрастная дегенерация желтого пятна (AMD) включает влажную, сухую или атрофическую AMD.
В одном варианте осуществления изобретения субъект является млекопитающим, предпочтительно человеком.
Другим объектом настоящего изобретения является способ ингибирования продуцирования фрагмента комплемента C3b у млекопитающего, который включает введение указанному млекопитающему эффективного количества варианта CRIg по настоящему изобретению или иммуноадгезина, включающего такой вариант.
Другим объектом настоящего изобретения является способ избирательного ингибирования альтернативного пути активации комплемента у млекопитающего, который включает введение указанному млекопитающему эффективного количества варианта CRIg по настоящему изобретению или иммуноадгезина, включающего такой вариант.
Краткое описание чертежей
На фигурах 1А-1В показаны нуклеотидная и аминокислотная последовательности непроцессированной длинной формы нативного CRIg человека из 399 аминокислот (huCRIg, SEQ ID NO:1 и 2, соответственно).
На фигурах 2А-2В показаны нуклеотидная и аминокислотная последовательности короткой формы нативного CRIg человека (huCRIg-короткий, SEQ ID NO:3 и 4, соответственно).
На фигурах 3А-3С показаны нуклеотидная и аминокислотная последовательности нативного CRIg мыши из 280 аминокислот (muCRIg, SEQ ID NO:5 и 6, соответственно)
Фигура 4. Активность мутантов CRIg, определяемая при выполнении анализа связывания и анализа ингибирования. Сродство связывания CRIg измеряли в виде конкурентного замещения C3b (A), и биологическую активность измеряли при помощи анализа ингибирования гемолиза. PUR10680 был контрольным веществом дикого типа (красный), RIL 41 (синий) и RL41 (зеленый) были двумя мутантами (В). (С) Поэтапная оптимизация границы связывания CRIg.
Фигура 5. Корреляция между конкурентно-связывающим анализом ELISA и анализом ингибирования гемолиза.
Фигура 6. Мутант CRIg Q64R/M86Y характеризуется улучшенным сродством связывания по результатам анализа Biacore. (А) Сенсограммы SPR, полученные в результате введения C3b в возрастающих концентрациях по сравнению с CRIg дикого типа с оболочкой и белками CRIg Q64R M86Y. (В) Стационарный анализ данных связывания показывает, что значение Kd равно 0,2 микромоль для мутанта Q64R/M86Y и 1,1 микромоль для CRIg дикого типа.
Фигура 7. CRIg с улучшенным сродством связывания избирательно связывается с C3b. При помощи конкурентно-связывающего анализа Alpha Screen анализировали очищенные С3 и C3b.
Фигура 8. Улучшенная активность ингибирования комплемента мутанта CRIg Q64R/M86Y по сравнению с CRIg дикого типа. (А) Ингибирование комплемента CRIg дикого типа и мутантом CRIg Q46R/M86Y сравнивали при помощи анализа ингибирования гемолиза, специфичного к альтернативному пути, используя эритроциты кролика и сыворотку человека, не содержащую C1q. (В) Ингибирование комплемента CRIg дикого типа и мутантом CRIg Q46R/M86Y сравнивали при помощи анализа ELISA альтернативного пути с использованием микропланшета, сенсибилизированного LPS и сывороткой человека, не содержащей C1q.
Фигура 9. Мутант CRIg Q64R/M86Y характеризуется лучшей активностью in vivo по сравнению с CRIg дикого типа.
(А) Клинические оценки мышей, которым вводили сыворотку KRN и лечили разными вариантами рекомбинантных белков CRIg человека и мыши дикого типа и с созревшей аффинностью в разных концентрациях. Данные представляют собой среднее значение для 4-7 мышей в группе. (В) Графики дисперсий клинических оценок для отдельных мышей на 6-й день после введения сыворотки. (С) Окрашенные гематоксилином и эозином срезы мышей, которым вводили CRIg дикого типа или мутант CRIg Q64R/M86Y через 6 дней после введения сыворотки. (D) Графики дисперсий гистологических оценок для мышей, которым вводили CRIg дикого типа или мутант CRIg Q64R/M86Y через 6 дней после введения сыворотки.
Таблица 1. Библиотеки фагов. Для охвата области контакта между CRIg и C3b было создано пять рандомизированных библиотек.
Таблица 2. Поэтапное создание CRIg с более высоким сродством связывания методом отображения на фаге. Мутанты CRIg против C3b, отобранные из пяти рандомизированных библиотек. В каждом блоке показаны клоны, которые были отобраны из каждой библиотеки на основании сродства связывания с C3b. Последовательность обозначена однобуквенным кодом аминокислот. В каждом блоке отдельные мутанты сравниваются с консенсусными последовательностями и исходными последовательностями дикого типа (WT). Остатки окрашены соответствующим образом: синие - рандомизированное положение; серые - не рандомизированные; желтые - отобранные остатки, отличающиеся от остатков дикого типа (WT). В таблице 2 представлены соответственно SEQ ID NO:21-63 и 63-67 в порядке следования.
Таблица 3. Сравнение сродства связывания, определенного при помощи конкурентно-связывающего анализа ELISA и ингибирования гемолиза in vivo для отобранных мутантов. Мутанты с более чем 5-кратным увеличением сродства связывания и более высокой активностью in vivo окрашены желтым цветом.
Таблица 4. Сравнение сродства связывания и ингибирования гемолиза in vivo для мутантов второго поколения (исходные последовательности окрашены серым цветом). Мутанты с более чем 5-кратным увеличением сродства связывания по сравнению с исходным мутантом выделены синим цветом, мутанты с более чем 90-кратным увеличением сродства связывания выделены желтым цветом. Аналогичным образом мутанты с более высокой активностью in vivo по сравнению с исходными последовательностями выделены оранжевым цветом.
Подробное описание изобретения
1. Определения терминов
Термины ”CRIg”, “PRO362”, “JAM4” и “STIgMA” имеют взаимозаменяемые значения и служат для определения полипептидов CRIg с нативной последовательностью и их вариантов.
“CRIg с нативной последовательностью” означает полипептид, имеющий такую же аминокислотную последовательность, что и природный полипептид CRIg независимо от способа получения. Таким образом, CRIg с нативной последовательностью может быть выделен из природного источника или получен методами рекомбинантных ДНК и/или путем синтеза. В определение термина “CRIg с нативной последовательностью” входят природные усеченные или секретированные формы CRIg (например, последовательность внеклеточного домена), природные варианты (например, альтернативно сплайсированные формы) и природные аллельные варианты CRIg. Полипептиды CRIg с нативной последовательностью включают полноразмерный (непроцессированный) полипептид CRIg человека длиной 399 аминокислот, представленный SEQ ID NO:2 (huCRIg, показанный на фигурах 1А и 1В), который имеет или не имеет N-концевую сигнальную последовательность, имеет или не имеет инициирующий метионин в положении 1 и имеет или не имеет любой или все трансмембранные домены в положениях аминокислот 277-307 SEQ ID NO:2. В другом варианте осуществления изобретения полипептид CRIg с нативной последовательностью состоит из 305 аминокислот и представляет собой короткую форму CRIg человека (huCRIg-короткий, SEQ ID NO:4, показанный на фигурах 2А и 2В), который имеет или не имеет N-концевую сигнальную последовательность, имеет или не имеет инициирующий метионин в положении 1 и имеет или не имеет любой или все трансмембранные домены в положениях 183-213 SEQ ID NO:4. В другом варианте осуществления изобретения полипептид CRIg с нативной последовательностью имеет длину 280 аминокислот и представляет собой полноразмерный полипептид CRIg мыши SEQ ID NO:6 (muCRIg, показанный на фигурах 3А-3С), который имеет или не имеет N-концевую сигнальную последовательность, имеет или не имеет инициирующий метионин в положении 1 и имеет или не имеет любой или все трансмембранные домены в положениях аминокислот 181-211 SEQ ID NO:6. В определение данного термина входят полипептиды CRIg других животных, отличных от человека, включая высших приматов и млекопитающих.
“Внеклеточный домен” CRIg или “ECD” CRIg означает форму полипептида CRIg, в которой по существу отсутствуют трансмембранные и цитоплазматические домены соответствующих полноразмерных молекул. ECD CRIg обычно содержит менее 1% таких трансмембранных и/или цитоплазматических доменов, предпочтительно менее 0,5% таких доменов. ECD CRIg может включать аминокислотные остатки в положении от 1 или примерно 21 до Х SEQ ID NO:2, 4 или 6, где Х означает любую аминокислоту в положении от около 271 до 281 в SEQ ID NO:2, любую аминокислоту в положении от около 178 до 186 в SEQ ID NO:4 и любую аминокислоту в положении от около 176 до 184 в SEQ ID NO:6.
Термин ”вариант CRIg” в использованном здесь значении означает активный полипептид CRIg, описанный ниже, в котором аминокислотная последовательность по меньшей мере примерно на 80% идентична полипептиду CRIg с нативной последовательностью и который включает, не ограничиваясь ими, непроцессированный huCRIg (SEQ ID NO:2), huCRIg-короткий (SEQ ID NO:4) и muCRIg (SEQ ID NO:6), каждый из которых имеет или не имеет N-концевой инициирующий метионин, имеет или не имеет N-концевую сигнальную последовательность, имеет или не имеет все или часть трансмембранных доменов и имеет или не имеет внутриклеточный домен. В конкретном варианте осуществления изобретения вариант CRIg имеет аминокислотную последовательность, которая по меньшей мере примерно на 80% гомологична аминокислотной последовательности зрелого, непроцессированного пептида, представленного SEQ ID NO:2. В другом варианте осуществления изобретения вариант CRIg имеет аминокислотную последовательность, которая по меньшей мере примерно на 80% гомологична аминокислотной последовательности зрелого, непроцессированного пептида, представленного SEQ ID NO:4. В еще одном варианте осуществления изобретения вариант CRIg имеет аминокислотную последовательность, которая по меньшей мере примерно на 80% гомологична аминокислотной последовательности зрелого, непроцессированного пептида, представленного SEQ ID NO:6. Вариант CRIg обычно имеет аминокислотную последовательность, которая по меньшей мере примерно на 80%, по меньшей мере примерно на 85%, по меньшей мере примерно на 90%, по меньшей мере примерно на 95%, по меньшей мере примерно на 98% или по меньшей мере примерно на 99% идентична зрелой аминокислотной последовательности, представленной SEQ ID NO:2, 4 или 6. В описании изобретения, включая примеры, термин ”дикого типа” или “WT” означает зрелую, непроцессированную короткую форму CRIg человека (CRIg(S)) (SEQ ID NO:4), при этом нумерация аминокислотных остатков в вариантах CRIg соответствует последовательности SEQ ID NO:4.
Варианты CRIg по настоящему изобретению являются агонистами CRIg, как описано ниже. В частности, варианты CRIg сохраняют способность избирательно связываться с C3b по сравнению с С3, где термин ”избирательное связывание” служит для обозначения связывания с C3b и отсутствия связывания с С3. Кроме того, в предпочтительном варианте осуществления изобретения варианты CRIg по настоящему изобретению обладают более высоким сродством связывания с C3b по сравнению с полипептидом CRIg с нативной последовательностью, таким как длинная форма CRIg человека (SEQ ID NO:2). В разных вариантах осуществления изобретения сродство связывания увеличено по меньшей мере примерно в 2 раза, по меньшей мере примерно в 3 раза, по меньшей мере примерно в 4 раза, по меньшей мере примерно в 5 раз, по меньшей мере примерно в 6 раз, по меньшей мере примерно в 7 раз, по меньшей мере примерно в 8 раз, по меньшей мере примерно в 9 раз, по меньшей мере примерно в 10 раз, по меньшей мере примерно в 15 раз, по меньшей мере примерно в 20 раз, по меньшей мере примерно в 25 раз, по меньшей мере примерно в 30 раз, по меньшей мере примерно в 35 раз, по меньшей мере примерно в 40 раз, по меньшей мере примерно в 45 раз, по меньшей мере примерно в 50 раз, по меньшей мере примерно в 55 раз, по меньшей мере примерно в 60 раз, по меньшей мере примерно в 65 раз, по меньшей мере примерно в 70 раз, по меньшей мере примерно в 75 раз, по меньшей мере примерно в 80 раз, по меньшей мере примерно в 85 раз, по меньшей мере примерно в 90 раз, по меньшей мере примерно в 95 раз или по меньшей мере примерно в 100 раз по сравнению с полипептидом CRIg человека с нативной последовательностью SEQ ID NO:2. В других вариантах осуществления изобретения сродство связывания с C3b по сравнению с полипептидом CRIg человека с нативной последовательностью SEQ ID NO:2 увеличено примерно в 5-10 раз, примерно в 5-15 раз, примерно в 5-20 раз, примерно в 5-25 раз, примерно в 5-30 раз, примерно в 5-35 раз, примерно в 5-40 раз, примерно в 5-45 раз, примерно в 5-50 раз, примерно в 5-55 раз, примерно в 5-60 раз, примерно в 5-65 раз, примерно в 5-70 раз, примерно в 5-75 раз, примерно в 5-80 раз, примерно в 5-85 раз, примерно в 5-90 раз, примерно в 5-95 раз или примерно в 5-100 раз.
“Процентная (%) идентичность аминокислотной последовательности” с вариантами CRIg в настоящем описании изобретения определена как процентное содержание аминокислотных остатков в последовательности варианта CRIg, идентичных сравниваемым аминокислотным остаткам в нативной последовательности CRIg после совмещения последовательностей и введения, при необходимости, разрывов для достижения максимальной процентной идентичности последовательностей без учета любых консервативных замен в качестве части идентичности последовательности. Для последовательностей разной длины процентную идентичность последовательностей определяют относительно более длинной последовательности на протяжении всей длины более длинных последовательностей. Сравнительный анализ с целью определения процентной идентичности аминокислотных последовательностей может быть выполнен разными способами, известными специалистам в данной области, например, при помощи общедоступного программного обеспечения, такого как BLAST, BLAST-2, ALIGN или Megalign (DNASTAR). Специалисты в данной облачти могут определить соответствующие параметры, необходимые для выполнения сравнительного анализа, которые включают любые алгоритмы, требуемые для достижения максимального совмещения сравниваемых последовательностей по всей длине. Идентичность последовательностей затем вычисляют относительно более длинной последовательности, то есть, даже если более короткая последовательность на 100% идентична части более длинной последовательности, общая идентичность последовательностей будет меньше 100%.
“Процентная (%) идентичность последовательности нуклеиновой кислоты” с последовательностями, кодирующими вариант CRIg по настоящему изобретению, определена как процентное содержание нуклеотидов в последовательности-кандидате, которые идентичны нуклеотидам в последовательности, кодирующей вариант CRIg, после совмещения последовательностей и введения, при необходимости, разрывов для достижения максимальной процентной идентичности последовательностей. Сравнительный анализ с целью определения процентной идентичности последовательности нуклеиновой кислоты может быть выполнен разными способами, известными в данной области, например, при помощи общедоступного программного обеспечения, такого как BKAST, BLAST-2, ALIGN или Megalign (DNASTAR). Специалисты в данной области могут определить соответствующие параметры, необходимые для выполнения сравнительного анализа, которые включают любые алгоритмы, требуемые для достижения максимального совмещения сравниваемых последовательностей по всей длине. Идентичность последовательностей затем вычисляют относительно более длинной последовательности, то есть, даже если более короткая последовательность на 100% идентична части более длинной последовательности, общая идентичность последовательностей будет меньше 100%.
В определение варианта CRIg входят все варианты аминокислотных последовательностей, рассмотренные выше в настоящем описании изобретения, независимо от способа идентификации или получения. В данное определение особо входят варианты, модифицированные путем введения части, отличной от природной аминокислоты, химическими, ферментативными или другими приемлемыми способами, при условии, что указанные варианты сохраняют биологические свойства CRIg с нативной последовательностью. Примеры замен природных аминокислот включают нижеописанные замены.
Аминокислотные остатки разделены на четыре основные группы:
Кислотные: остаток имеет отрицательный заряд вследствие потери иона Н при физиологическом значении рН и притягивается водным раствором, занимая поверхностное положение в конформации содержащего его пептида при нахождении данного пептида в водном растворе.
Основные: остаток имеет положительный заряд вследствие ассоциации с ионом Н при физиологическом значении рН и притягивается водным раствором, занимая поверхностное положение в конформации содержащего его пептида при нахождении данного пептида в водной среде при физиологическом значении рН.
Нейтральные/неполярные: остаток не имеет заряда при физиологическом значении рН и отталкивается водным раствором, занимая внутреннее положение в конформации содержащего его пептида при нахождении данного пептида в водной среде. Указанные остатки именуются также ”гидрофобными остатками”.
Нейтральные/полярные: остаток не имеет заряда при физиологическом значении рН, но притягивается водным раствором, занимая внешнее положение в конформации содержащего его пептида при нахождении данного пептида в водной среде.
Аминокислотные остатки далее могут быть классифицированы как циклические или нециклические, ароматические или неароматические с учетом групп в боковой цепи, и такие обозначения хорошо известны квалифицированным специалистам.
Обычно встречающиеся аминокислоты, не кодированные генетическим кодом, включают 2-аминоадипиновую кислоту (Aad) для Glu и Asp; 2-аминопимелиновую кислоту (Apm) для Glu и Asp; 2-аминомасляную кислоту (Abu) для Met, Leu и других алифатических аминокислот; 2-аминогептановую кислоту (Ahe) для Met, Leu и других алифатических аминокислот; 2-аминоизомасляную кислоту (Aib) для Gly; циклогексилаланин (Cha) для Val, Leu и Ile; гомоаргинин (Har) для Arg и Lys; 2,3-диаминопропионовую кислоту (Dpr) для Lys, Arg и His; N-этилглицин (EtGly) для Gly, Pro и Ala; N-этиласпарагин (EtAsn) для Asn и Gln; гидроксиллизин (Hyl) для Lys; аллогидроксиллизин (AHyl) для Lys; 3-(и 4)гидроксипролин (3Hyp, 4Hyp) для Pro, Ser и Thr; аллоизолейцин (AIle) для Ile, Leu и Val; амидинофенилаланин для Ala; N-метилглицин (MeGly, саркозин) для Gly, Pro и Ala; N-метилизолейцин (MrIle) для Ile; норвалин (Nva) для Met и других алифатических аминокислот; норлейцин (Nle) для Met и других алифатических аминокислот; орнитин (Orn) для Lys, Arg и His; цитрулин (Cit) и метионинсульфоксид (MSO) для Thr, Asn и Gln; N-метилфенилаланин (MePhe), триметилфенилаланин, галоген (F, Cl, Br и I)фенилаланин, трифлуорилфенилаланин для Phe.
В используемом здесь значении термин ”иммуноадгезин” означает антителоподобные молекулы, которые объединяют специфичность связывания гетерологичного белка (”адгезин”) с эффекторными функциями константных доменов иммуноглобулина. В структурном отношении иммуноадгезины представляют собой гибрид аминокислотной последовательности, обладающей требуемой специфичностью связывания, которая не является антигенузнающим и антигенсвязывающим центром антитела (то есть является ”гетерологичным”) с последовательностью константного домена иммуноглобулина. Адгезин, являющийся частью молекулы иммуноадгезина, обычно представляет собой смежную аминокислотную последовательнтость, включающую по меньшей мере сайт связывания рецептора или лиганда. Последовательность константной области иммуноглобулина в иммуноадгезине может быть получена из любого иммуноглобулина, такого как подтипы IgG-1, IgG-2, IgG-3 или IgG-4, IgA (включая IgA-1 и IgA-2), IgE, IgD или IgM.
“Лечение” означает вмешательство с целью предотвращения развития или изменения патологии нарушения. Таким образом, термин ”лечение” означает как терапевтическое лечение, так и профилактические или превентивные меры. Субъекты, нуждающиеся в лечении, являются субъектами, уже имеющими нарушение, а также субъектами, у которых необходимо предупредить возникновение нарушения.
Термин “уменьшение интенсивности симптомов заболевания” в используемом здесь значении означает улучшение состояния.
Термин ”млекопитающее” в используемом здесь значении означает любое животное, классифицируемое как млекопитающее, которое включает, не ограничиваясь ими, человека, приматов кроме человека, домашних и сельскохозяйственных животных, животных, содержащихся в зоопарке, спортивных животных или домашних питомцев, таких как лошади, поросята, крупный рогатый скот, собаки, кошки, хорьки и т.д. В предпочтителдьлном варианте осуществления изобретения млекопитающее является высшим приматом, наиболее предпочтительно человеком.
Термин ”комплемент-ассоциированное заболевание” использован в настоящем описании изобретения в самом широком смысле и включает все заболевания и патологические состояния, патогенез которых предполагает нарушение активации системы комплемента, такое как, например, отсутствие комплемента. Указанный термин служит для определения заболеваний и патологических состояний, на которые благоприятное воздействие оказывает ингибирование конвертазы С3. В определение данного термина дополнительно входят заболевания и патологические состояния, на которые благоприятное воздействие оказывает ингибирование, включая избирательное ингибирование, альтернативного пути активации комплемента. Комплемент-ассоциированные заболевания включают, не ограничиваясь ими, воспалительные заболевания и аутоиммунные заболевания, такие как, например, ревматоидный артрит (RA), респираторный дистресс-синдром у взрослых (ARDS), поражение удаленных тканей после ишемии и реперфузии, активация комплемента во время хирургической операции с искусственным кровообращением, дерматомиоцитоз, пемфигус, люпус-нефрит и проистекающие из него гломерулонефрит и васкулит, искусственное кровообращение, дисфункция коронарного эндотелия, вызванная кардиоплегией, мембранозно-пролиферативный гломерулонефрит типа II, нефропатия, вызываемая IgA, острая почечная недостаточность, криоглобулемия, антифосфолипидный синдром, возрастная дегенерация желтого пятна, увеит, диабетическая ретинопатия, аллотрансплантация, сверхострое отторжение, гемодиализ, хроническое обструктивное заболевание легких (COPD), астма, аспирационная пневмония. В предпочтительном варианте осуществления изобретения ”комплемент-ассоциированное заболевание” является заболеванием, в котором важную роль играет альтернативный путь активации комплемента, и включает ревматоидный артрит (RA), комплемент-ассоциированные глазные заболевания, такие как возрастная дегенерация желтого пятна, антифосфолипидный синдром, поражение кишечника и почек, вызванное ишемией и реперфузией, и мембранозно-пролиферативный гломерулонефрит типа II.
Термин ”комплемент-ассоциированное глазное заболевание” использован в настоящем описании изобретения в самом широком смысле и включает все глазные заболевания, патология которых обусловлена комплементом, включая классический и альтернативный пути, и, в частности, альтернативный путь активации комплемента. В данную группу входят все глазные заболевания, связанные с альтернативным путем, возникновение, развитие или прогрессирование которых можно контролировать, ингибируя альтернативный путь активации комплемента. Комплемент-ассоциированные глазные заболевания включают, не ограничиваясь ими, дегенеративные заболевания желтого пятна, такие как все стадии возрастной дегенерации желтого пятна (AMD), включающие сухую и влажную (неэкссудативную и экссудативную) формы, образование новых сосудов в сосудистой оболочке глаза (CNV), увеит, диабетическую и другие обусловленные ишемией ретинопатии, эндофтальмит и другие внутриглазные заболевания, вызванные образованием новых сосудов, такие как диабетический отек желтого пятна, патологическая миопия, болезнь Гиппеля-Линдау, гистоплазмоз глаза, окклюзия центральной вены сетчатки (CRVO), образование новых сосудов в роговице и образование новых сосудов в сетчатке. В предпочтительную группу комплемент-ассоциированных глазных заболеваний входят возрастная дегенерация желтого пятна (AMD), в том числе неэкссудативная (влажная) и экссудативная (сухая или атрофическая) AMD, образование новых сосудов в сосудистой оболочке глаза (CNV), диабетическая ретинопатия (DR) и эндофтальмит.
Термины ”воспалительное заболевание” и “воспалительное нарушение” имеют взаимозаменяемые значения и означают заболевание или нарушение, в которых компонент иммунной системы млекопитающего вызывает, опосредует или каким-либо другим образом способствует возникновению воспалительной реакции, вызывающей заболевание млекопитающего. В указанную группу входят также заболевания, в которых ослабление воспалительной реакции оказывает благоприятное воздействие на развитие заболевания. В определение данного термина входят иммунные воспалительные заболевания, включая аутоиммунные заболевания.
Термин ”опосредованное Т-клетками” заболевание означает заболевание, в котором Т-клетки прямо или косвенно опосредуют или каким-либо другим образом способствуют заболеванию млекопитающего. Опосредованное Т-клетками заболевание может быть связано с клеточноопосредованным воздействием, лимфокин-опосредованным воздействием и т.д., и даже с воздействием, ассоциированным с В-клетками, если В-клетки стимулируются, например, лимфокинами, секретируемыми Т-клетками.
Примеры иммунных и воспалительных заболеваний, некоторые из которых опосредованы Т-клетками, включают, не ограничиваясь ими, воспалительное заболевание кишечника (IBD), системную красную волчанку, ревматоидный артрит, юношеский хронический артрит, спондилоартропатию, системный склероз (склеродерму), идиопатические воспалительные миопатии (дерматомиозит, полимиозит), ксеродерматоз, системный васкулит, саркоидоз, аутоиммунную гемолитическую анемию (иммунную панцитопению, ночную пароксизмальную гемоглобинурию), аутоиммунную тромбоцитопению (идиопатическую тромботическую пурпуру, иммунную тромбоцитопению), тиреоидит (болезнь Грейвса, тиреоидит Хашимото, юношеский лимфоцитарный тиреоидит, атрофический тиреоидит), сахарный диабет, иммунное заболевание почек (гломерулонефрит, тубулоинтерстициальный нефрит), демиелинизирующие заболевания центральной и периферической нервной системы, такие как рассеянный склероз, идиопатическую полиневропатию, желчно-почечные заболевания, такие как инфекционный гепатит (гепатит А, В, С, D, Е и другие негепатотропные вирусы), аутоиммунный хронический активный гепатит, первичный билиарный цирроз печени, грануломатозный гепатит и склерозирующий холангит, воспалительные и фиброзные заболевания легких (например, муковисцидоз), глютензависимую энтеропатию, болезнь Уиппла, аутоиммунные или иммунные кожные заболевания, включающие буллезные кожные заболевания, полиморфную эритему и контактный дерматит, псориаз, аллергическмие заболевания легкого, такие как эозинофильная пневмония, идиопатический фиброз легких и аллергическая пневмония, заболевания, обусловленные трансплантацией, включающие отторжение трансплантата, реакцию трансплантат-против-хозяина, болезнь Альцгеймера и атеросклероз.
Введение ”в комбинации с” одним или несколькими другими лекарственными средствами означает одновременное и последовательное введение в любом порядке.
Термины ”активный” или “активность” применительно к вариантам полипептидов CRIg по настоящему изобретению означают формы таких полипептидов, которые сохраняют биологическую и/или иммунологическую активность нативного или природного полипептида по настоящему изобретению. Предпочтительная биологическая активностью представляет собой способность связываться с C3b и/или воздействовать на комплемент или активацию комплемента, в частности, ингибировать альтернативный путь активации комплемента и/или конвертазу С3. Ингибирование конвертазы С3 можно, например, определить, измеряя ингибирование кругооборота С3 в нормальной сыворотке в случае артрита, вызванного коллагеном или антителом, или ингибирование отложения С3 в суставах, пораженных артритом.
Термин ”биологическая активность” применительно к полипептиду, который имитирует биологическую активность CRIg, частично означает способность таких молекул связываться с C3b и/или воздействовать на комплемент или активацию комплемента, в частности, ингибировать альтернативный путь активации комплемента и/или конвертазу С3.
Термин ”агонист” CRIg использован в самом широком смысле и означает любую молекулу, которая имитирует биологическую активность (определение которой дано выше) полипептида CRIg с нативной последовательностью.
Термин ”функционально связанный” означает смежное положение, при котором компоненты могут нормально функционировать. Так, кодирующая последовательность, ”функционально связанная” с регуляторными последовательностями, представляет собой конфигурацию, в которой кодирующая последовательность может быть экспрессирована под управлением указанных последовательностей, связываемые последовательности ДНК являются смежными и, в случае секреторной лидерной последовательности, являются смежными и находятся в фазе считывания. Например, ДНК для предпоследовательности или секреторной лидерной последовательности функционально связана с ДНК для полипептида, если она выражена в виде предбелка, участвующего в секреции данного полипептида; промотор или энхансер функционально связан с кодирующей последовательностью, если он влияет на транскрипцию последовательности; или сайт связывания рибосомы функционально связан с кодирующей последовательностью, если его расположение облегчает трансляцию. Связывание осуществляется путем лигирования на удобных сайтах рестрикции. При отсутствии таких сайтов используют синтетические олигонуклеотидные адапторы или линкеры в соответствии с известной практикой.
Термин ”регуляторные последовательности” означает последовательности ДНК, необходимые для экспрессии функционально связанной кодирующей последовательности в конкретном организме-хозяине. Регуляторные последовательности, пригодные для прокариотических организмов, включают, например, промотор, необязательно операторную последовательность и сайт связывания рибосомы. Известно, что в эукариотических клетках используются промоторы, сигналы полиаденилирования и энхансеры.
Термин ”экспрессирующая система” означает последовательности ДНК, содержащие требуемую кодирующую последовательность и регуляторные последовательности, функционально связанные друг с другом, благодаря чему хозяева, трансформированные указанными последовательностями, могут продуцировать кодироованные белки. Для трансформации хозяина экспрессирующая система может быть введена в вектор; однако, соответствующая ДНК может быть также встроена в хромосому хозяина.
В используемом здесь значении термины “клетка”, “линия клеток” и “культура клеток” имеют взаимозаменяемые значения и служат для обозначения потомства. Таким образом, ”трансформанты” или “трансформированные клетки” означают первичные клетки субъекта и полученные из них культуры независимо от числа пассажей. Кроме того, следует отметить, что все потомство не может быть совершенно идентично в отношении ДНК из-за возможности намеренных или случайных мутаций. В определение данного термина входит мутантное потомство, обладающее такой же функциональной способностью, что и первоначально трансформированная клетка. Использование других обозначений будет видно из контекста.
“Плазмиды” обозначаются строчной буквой ”р” с предшествующими и/или последующими прописными буквами и/или цифрами. Исходные плазмиды можно приобрести коммерческим путем на неограниченной основе или создать из таких общедоступных плазмид известными методами. Кроме того, в данной области существуют другие эквивалентные плазмиды, которые должны быть известны специалисту.
Термин ”библиотека отображения на фаге” означает библиотеку экспрессии белков, в которой экспрессирована коллекция клонированных белковых последовательностей в виде гибридов с белком оболочки фага. Таким оброазом, фраза ”библиотека отображения на фаге” означает коллекцию фага (например, нитчатого фага), экспрессирующего наружный (обычно гетерологичный) белок. Наружный белок может взаимодействовать (связываться) с другими частями, с которыми контактирует фаг. Каждый фаг, отображающий наружный белок, является ”членом” библиотеки отображения на фаге.
Термин ”нитчатый фаг” означает вирусную частицу, способную отображать гетерогенный полипептид на своей поверхности, и включает, не ограничиваясь ими, f1, fd Pf1 и М13. Нитчатый фаг может содержать селектируемый маркер, такой как тетрациклин (например, ”fd-tet”). Специалистам в данной области хорошо известны разные системы отображения на нитчатом фаге (см., например, публикации Zacher et al., Gene, 9:127-140 (1980), Smith et al., Science, 228:1315-1317 (1985); и Parmley and Smith, Gene, 73: 305-318 (1988)).
Термин ”пэннинг” означает несколько циклов процесса скрининга по идентификации и выделению фагов, несущих соединения, такие как антитела, с высоким сродством и специфичностью к мишени.
Фраза ”консервативные аминокислотные остатки” означает аминокислотные остатки, которые идентичны в двух или более аминокислотных последовательностях, подвергнутых сравнительному анализу.
II. Подробное описание изобретения
Комплемент является важным компонентом врожденного и приобретенного иммунного ответа, при этом продукты расщепления комплемента, образованные в результате активации каждого из трех путей активации комплемента (классического, альтернативного и опосредуемого лектином), могут вызывать воспаление и разрушение ткани. Таким образом, неконтролируемая активация комплемента вследствие отсутствия соответствующей регуляции вызывает разные хронические воспалительные заболевания. В указанном воспалительном каскаде преобладают продукты расщепления комплемента С3а и С5а, которые действуют в качестве хемоаттрактанта и активаторов нейрофилов и воспалительных макрофагов через рецепторы С3а и С5а (Mollnes, T.E., W.C. Song, and J.D. Lambris. 2002. Complement in inflammatory tissue damage and disease. Trends Immunol. 23:61-64).
CRIg является недавно обнаруженным рецептором комплемента, который экспрессирован на субпопуляции оседлых тканевых макрофагов. Являясь функциональным рецептором, внеклеточный домен IgV рецептора CRIg представляет собой избирательный ингибитор альтернативного пути активации комплемента (Wiesmann et al., Nature, 444(7116): 217-20, 2006). Установлено, что растворимая форма CRIg может устранять воспаление и разрежение кости в экспериментальных моделях артрита путем ингибирования альтернативного пути активации комплемента в суставе. Кроме того, установлено, что альтернативный путь активации комплемента необходим не только для возникновения заболевания, но и для прогрессирования заболевания. Таким образом, ингибирование альтернативного пути рецептором CRIg создает многообещающее терапевтическое направление для профилактики и лечения заболеваний и нарушений, патогенез которых определяет альтернативный путь активации комплемента. Для более подробного ознакомления с данной темой см., например, публикации Helmy et al., Cell, 125(1):29-32, 2006) и Katschke et al., J. Exp. Med. 204(6):1319-1325 (2007).
Однако сродство CRIg к субъединице конвертазы C3b является низким (в микромолярном диапазоне). Для создания более сильного ингибитора с целью получения лекарственного средства была использована кристаллическая структура CRIg в комплексе с C3b, и методом отображения на фаге были созданы варианты CRIg с улучшенным сродством связывания с C3b.
Таким образом, настоящее изобретение относится к вариантам CRIg с улучшенными свойствами, такими как улучшенное сродство связывания с C3b и более высокая эффективность ингибирования.
Идентификация вариантов CRIg с созревшей аффинностью
Как более подробно описано в примере, отображение белковых или пептидных библиотек на фаге является пригодным методом для отбора вариантов CRIg с улучшенным сродством связывания с C3b и/или другими улучшенными свойствами, такими как более высокая биологическая активность (Smith, G.P., (1991) Curr. Opin. Biotechnol. 2:668-673). Высокоаффинные моновалентные белки, отображаемые в виде гибридов с белками оболочки гена III М13 (Clackson, T., (1994) et al., Trends Biotechnol. 12:173-183), можно идентифицировать путем клонирования и секвенирования соответствующей ДНК, упакованной в фаговые частицы после нескольких циклов отбора характеристик связывания.
Созревание аффинности с использованием отображения на фаге описано, например, в публикации Lowman et al., Biochemistry 30(45):10832-10838 (1991), см. также публикацию Hawkins et al., J. Mol. Biol. 254: 889-896 (1992) и в приведенном ниже примере. Не придерживаясь строго нижеследующего описания, указанный процесс можно кратко описать следующим образом: несколько сайтов в заранее определенной области мутируют с выполнением всех возможных замен аминокислот на каждом сайте. Полученные таким образом мутанты антител отображают в виде моновалентного антитела на частицах нитчатого фага, образующего гибрид с продуктом гена III М13, упакованный в каждой частице Фаг, экспрессирующий разные мутанты, может быть подвергнут нескольким циклам отбора характеристик связывания с последующим выделением и секвенированием мутантов, отличающихся высоким сродством. Указанный метод описан также в патенте США № 5750373, выданном 12 мая 1998 г.
Модифицированный метод, включающий отображение совокупной аффинности, описан в публикации Cunningham, B.C. et al., EMBO J. 13(11), 2508-2515 (1994). Указанный метод, позволяющий отобрать новые связывающиеся полипептиды, включает а) создание реплицирующего экспрессирующего вектора, включающего первый ген, кодирующий полипептид, второй ген, кодирующий по меньшей мере часть природного или дикого белка оболочки фага, при этом первый и второй гены являются гетерологичными, и элемент, регулирующий транскрипцию, функционально связан с первым и вторым генами с образованием гибрида гена, кодирующего гибридный белок; b) мутирование вектора в одном или нескольких выбранных положениях в первом гене с образованием семейства родственных плазмид; с) трансформацию приемлемых клеток-хозяев указанными плазмидами; d) инфицирование трансформированных клеток-хозяев фагом-хелпером, содержащим ген, кодирующий белок оболочки фага; е) культивирование трансформированных инфицированных клеток-хозяев в условиях, пригодных для образования рекомбинантных фаговых частиц, содержащих по меньшей мере часть плазмиды и способных трансформировать хозяина, при этом условия регулируют таким образом, чтобы незначительное число фаговых частиц отображало более одной копии гибридного белка на поверхности частицы; f) контактирование фаговых частиц с молекулой-мишенью с тем, чтобы по меньшей мере часть фаговых частиц связалась с молекулой-мишенью, и g) отделение фаговых частиц, которые связываются, от тех, которые не связываются. Указанный метод далее предпочтительно включает трансформацию приемлемых клеток-хозяев рекомбинантными фаговыми частицами, связывающимися с молекулой-мишенью, и повторение стадий d) - g) один или несколько раз.
Следует отметить, что, хотя варианты CRIg по настоящему изобретению были идентифицированы путем отображения на фаге, для идентификации вариантов CRIg с улучшенными свойствами, включая варианты CRIg с созревшей аффинностью, могут быть также использованы другие методы отображения.
Варианты CRIg с созревшей аффинностью по настоящему изобретению были созданы для заполнения области контактирования между CRIg и C3b, которая была идентифицирована с использованием кристаллической структуры CRIg и комлпекса C3b:CRIg, описанного в публикации заявки на патент США № 20080045697. В частности, как показано в таблице 1, библиотеки 1-5 были созданы соответственно для остатков E8-K15, R41-T47, S54-Q64, E85-Q99 и Q105-K111 непроцессированной молекулы CRIg с нативной последовательностью SEQ ID NO:2.
В одном варианте осуществления изобретения варианты CRIg включают замену аминокислот в одном или нескольких положениях аминокислот, выбираемых из группы, состоящей из положений 8, 14, 18, 42, 44, 45, 60, 64, 86, 99, 105 и 110 в аминокислотной последовательности SEQ ID NO:2.
Типичные варианты CRIg по настоящему изобретению приведены в таблице 3.
Замену предпочтительно выполняют в одном или нескольких положениях аминокислот 60, 64, 86, 99, 105 и 110 аминокислотной последовательности непроцессированного нативного CRIg SEQ ID NO:2.
Варианты CRIg с созревшей аффинностью включают, не ограничиваясь ими, одну или несколько следующих замен в SEQ ID NO:2: E8W, W14F, E84Y/W14F, P45F, G42D/D44H/P45F, Q60I, Q64R, Q60I/Q64R, M86Y, M86W, M86F, M86W/Q9R, M86F/Q99R, K110D, K11N, Q105R/K110N, Q105R/K110Q и Q105K/K110D.
Другие варианты CRIg с нативной последовательностью SEQ ID NO:2 с двумя или более заменами аминокислот показаны в таблице 3. В указанную группу входят Q64R/M86Y, Q60I/Q64R/E8Y, Q60I/Q64R/G42D, Q60I/Q64R/P45F, Q60I/Q64R/G42D/D44H/P45F, Q60I/Q64R/M86Y, Q60I/Q64R/Q105R, Q60I/Q64R/Q105K, Q60I/Q64R/K110N, Q60I/Q105R/K110N, M86Y/E8Y, M86Y/G42D/D44H/P45F, M86Y/P45F, M86Y/G42D/D44H/P45F; M86Y/Q99K/M86Y/Q99R/M86Y/Q105R/M86Y/Q105K/M86Y/Q105R/K110N.
Предпочтительные варианты CRIg по настоящему изобретению включают мутации, выбираемые из группы, состоящей из: Q60I, Q64R, Q60I/Q64R, M86Y, Q99L, Q105K/K110D, E8W/Q105R/K110N, Q64R/M86Y, Q60I/Q64R/E8Y, Q60I/Q64R/G42D, Q60I/Q64R/P45F, Q60I/Q64R/G42D/D44H/P45F, Q60I/Q64R/M86Y, Q60I/Q64R/Q105R, Q60I/Q64R/Q105K, Q60I/Q64R/K110N, M86Y/P45F; M86Y/Q105K.
Особенно предпочтительные варианты включают мутации Q60I/Q64R/M86Y или Q60I/Q64R/G42D/D44H/P45F.
В объем настоящего изобретения предпочтительно входят варианты, содержащие одну или несколько мутаций, указанных выше или приведенных в таблицах 3 и 4, но в остальном сохраняющие нативную последовательность CRIg SEQ ID NO:2. Такие варианты представлены в настоящем описании изобретения с указанием конкретной мутации, предшествующей ”CRIg”. Так, например, вариант, который отличается от CRIg с нативной последовательностью SEQ ID NO:2 только мутацией E8W, обозначен как ”E8W CRIg”, вариант, который отличается от CRIg с нативной последовательностью SEQ ID NO:2 только мутациями Q60I/Q64R/M86Y, обозначен как ”Q60I/Q64R/M86Y CRIg” и т.д.
Получение вариантов CRIg
ДНК, которая может кодировать белки, используемые для рекомбинантного синтеза вариантов CRIg по настоящему изобретению, может быть получена разными методами. Например, ДНК можно получить на основе природных последовательностей ДНК, кодирующих изменения в аминокислотной последовательности полученного белка. Такие мутантные ДНК могут быть использованы для получения вариантов CRIg по настоящему изобретению. При изложении в упрощенной форме указанные методы включают получение гена, кодирующего полипептид CRIg с нативной последовательностью, модификацию полученных генов методами рекомбинантных ДНК, описанными ниже, введение генов в соответствующий экспрессирующий вектор, введение вектора в соответствующую клетку-хозяина, культивирование клетки-хозяина для экспрессии требуемого варианта CRIg и очистку полученной молекулы.
Более конкретно последовательность ДНК, кодирующую вариант CRIg по настоящему изобретению, получают путем искусственного создания последовательности ДНК в соответствии с описанием, приведенным в стандартных учебниках, таких как, например, Sambrook, J. et al., Molecular Cloning (2nd ed.), Cold Spring Harbor Laboratory, N.Y., (1989).
а. Мутагенез с использованием олигонуклеотидов
Мутагенез с использованием олигонуклеотидов является предпочтительлным методом получения вариантов полипептида CRIg с нативной последовательностью или его фрагмента путем замены, делеции и инсерции. Указанный метод хорошо известен в данной области и описан в публикации Zoller et al., Nucleic Acids Res. 10:6487-6504 (1987). В соответствии с кратким изложением указанного метода нуклеиновую кислоту, кодирующую исходную полипептидную последовательность, изменяют, гибридизируя олигонуклеотид, кодирующий требуемую мутацию, с матричной ДНК, в которой матрица является одноцепочечной формой плазмиды, содержащей неизмененную или нативную последовательность ДНК кодирующей нуклеиновой кислоты. После гибридизации используют ДНК-полимеразу для синтеза всей второй комплементарной цепи матрицы, которая, таким образом, будет включать олигонуклеотидную затравку и кодировать выбранное изменение исходной нуклеиновой кислоты.
Обычно используют олигонуклеотиды, состоящие по меньшей мере из 25 нуклеотидов. Оптимальный олигонуклеотид содержит 12-15 нуклеотидов, которые полностью комплементарны матрице с любой стороны нуклеотида(ов), кодирующего мутацию. Таким образом гарантируется правильная гибридизация олигонуклеотида с молекулой одноцепочечной матричной ДНК. Олигонуклеотиды можно легко синтезировать методами, известными в данной области, которые описаны в публикации Crea et al., Proc. Natl. Acad. Sci. USA 75:5765 (1978).
При использовании метода отображения на фаге матричная ДНК может быть создана только теми векторами, которые получены из векторов на основе бактериофага М13 (пригодны общедоступные векторы M13mp18 и M13mp19), или векторами, содержащими ориджин реплипакации одноцепочечного фага, которые описаны в публикации Viera et al., Meth. Enzymol. 153:3 (1987). Таким образом, требуемую мутации ДНК необходимо ввести в один из указанных векторов для создания одноцепочечной матрицы. Получение одноцепочечной матрицы описано в разделах 4.21-4.41 публикации Sambrook et al., см. выше.
Для изменения нативной последовательности ДНК олигонуклеотид гибридизируют с одноцепочечной матрицей в приемлемых условиях гибридизации. Затем добавляют ДНК-полимеризирующий фермент, обычно фрагмент Кленова ДНК-полимеразы I, для синтеза комплементарной цепи матрицы, используя олигонуклеотид в качестве затравки для синтеза. Таким образом образуется гетеродуплексная молекула, в которой одна цепь ДНК кодирует мутированную форму CRIg и другая цепь (первоначальная матрица) кодирует нативную, неизмененную последовательность CRIg. Указанную гшетеродуплексную молекулу затем переносят в приемлемую клетку-хозяина, обычно в прокариотическую клетку, такую как E. coli JM-101. Выращенные клетки наносят на чашки с агарозой и исследуют, используя олигонуклеотидную затравку, меченную радиоактивным изотопом 32фосфатом, для выявления колоний бактерий, содержащих мутированную ДНК.
Вышеописанный метод может быть модифицирован с созданием гомодуплексной молекулы, в которой обе цепи плазмиды содержат мутации. Модификации выполняют следующим образом: одноцепочечный олигонуклеотид гибридизируют с одноцепочечной матрицей в соответствии с приведенным выше описанием. Смесь трех дезоксирибонуклеотидов, а именно дезоксирибоаденозина (dATP), дезоксирибогуанозина (dGTP) и дезоксириботимидина (dTTP), объединяют с модифицированным тиодезоксирибоцитозином, именуемым dCTP-(aS) (Amersham). Полученную смесь добавляют к комплексу матрица-олигонуклеотид. После добавления ДНК-полимеразы к смеси образуется цепь ДНК, которая идентична матрице за исключением мутированных оснований. Кроме того, новая цепь ДНК будет содержать dCTP-(aS) вместо dCTP, которая защищает ее от расщепления рестрикционной эндонуклеазой. Матричная цепь двухцепочечного гетеродуплекса, после того как она разрезана соответствующим рестрикционным ферментом, может быть расщеплена нуклеазой ExoIII или другой соответствующей нуклеазой позади области, содержащей сайт, подвергаемый мутагенезу. Затем реакцию прекращают, получая при этом молекулу, которая лишь частично является одноцепочечной. Затем образуют полный гомодуплекс двухцепочечной ДНК, используя ДНК-полимеразу в присутствии всех четырех дезоксирибонуклеотид-трифосфатов, АТР и ДНК-лигазы. Указанную молекулу гомодуплекса затем можно перенести в приемлемую клетку-хозяина, такую как E. coli JM101, как было описано выше.
Мутанты с заменой более одной аминокислоты могут быть созданы одним из нескольких способов. Аминокислоты, расположенные рядом друг с другом в полипептидной цепи, могут быть мутированы одновременно с использованием одного олигонуклеотида, кодирующего все требуемые аминокислотные замены. Однако, если аминокислоты расположены на некотором расстоянии друг от друга (разделены более чем примерно десятью аминокислотами), труднее создать один олигонуклеотид, кодирующий все требуемые изменения. В данном случае можно использовать один или два альтернативных метода.
В соответствии с первым методом создают отдельный олигонуклеотид для каждой заменяемой аминокислоты. Олигонуклеотиды одновременно гибридизируют с одноцепочечной матричной ДНК, при этом вторая цепь ДНК, синтезированная из матрицы, будет кодировать все требуемые аминокислотные замены. Альтернативный метод включает два или более циклов мутагенеза для получения требуемого мутанта. Первый цикл аналогичен описанному для единичных мутантов: ДНК дикого типа используют в качестве матрицы и олигонуклеотид, кодирующий первую аминокислотную замену(ы), гибридизируют с матрицей, в результате чего образуется молекула ДНК гетеродуплекса. Во втором цикле мутагенеза мутированную ДНК, полученную в первом цикле мутагенеза, используют в качестве матрицы. Таким образом, указанная матрица уже содержит одну или несколько мутаций. Олигонуклеотид, кодирующий дополнительную требуемую аминокислотную замену, затем гибридизируют с матрицей, благодаря чему полученная цепь ДНК теперь кодирует мутации, полученные как в первом, так и во втором циклах мутагенеза. Полученная ДНК может быть использована в качестве матрицы в третьем цикле мутагенеза и так далее.
b. Кластерный мутагенез
Данный метод также является предпочтительным методом получения вариантов CRIg с заменой, делецией и инсерцией. В основе данного метода лежит метод, описанный в публикации Wells et al., Gene 34:315 (1985). Исходным материалом является плазмида (или другой вектор), включающий ген 1, ген, подвергаемый мутации. Идентифицируют кодоны, подвергаемые мутации в нуклеиновой кислоте, кодирующей молекулу исходного CRIg. С каждой стороны идентифицированных сайтов мутации должен находиться однозначно определяемый сайт рестрикции эндонуклеазы. Если такие сайты рестрикции отсутствуют, их можно создать вышеописанным методом мутагенеза с использованием олигонуклеотидов и ввести в соответствующие положения в гене 1. Плазмиду после введения в нее сайтов рестрикции разрезают у указанных сайтов для линеаризации. Стандартными методами синтезируют двухцепочечный олигонуклеотид, кодирующий последовательность ДНК между сайтами рестрикции, но содержащий требуемые мутации. Две цепи синтезируют отдельно и затем гибридизируют вместе стандартными методами. Такой двухцепочечный олигонуклеотид именуется кластером. Указанный кластер имеет 3'- и 5'-концы, совместимые с концами линеаризованной плазмиды, с помощью которых кластер может быть прямо лигирован с плазмидой. Теперь плазмида содержит мутированную последовательность ДНК рецептора CRIg.
с. Получение вариантов CRIg методами рекомбинантных ДНК
ДНК, кодирующую варианты, вводят в соответствующую плазмиду или вектор. Полученным вектором трансформируют клетку-хозяина. В указанных хозяевах обычно используют плазмидные векторы, содержащие реплицирующиеся и регуляторные последовательности, выделенные из вида, совместимого с клеткой-хозяином. Вектор обычно содержит сайт репликации, а также последовательности, которые кодируют белки, способные производить отбор по фенотипу в трансформированных клетках.
Например, E. coli может быть трансформирован при помощи плазмиды pBR322, выделенной из вида E. coli (Mandel, M. et al., (1970) J. Mol. Biol. 53:154). Плазмида pBR322 содержит гены, определяющие устойчивость к ампициллину и тетрациклину, и, таким образом, являются простым средством отбора. Другие векторы могут содержать разные промоторы, которые часто имеют важное значение для экспрессии. Например, плазмиды pKK223-3, pDR720 и pPL-λ представляют собой экспрессирующие векторы с промоторами tac, trp или PL, которые в настоящее время могут быть приобретены коммерческим путем (Pharmacia Biotechnology).
Другие предпочтительные векторы могут быть созданы стандартными методами путем объединения родственных признаков векторов, рассмотренных в настоящем описании изобретения. Родственные признаки вектора включают промотор, сайт связывания рибосомы, вариантный или гибридный ген, сигнальную последовательность, маркеры устойчивости к антибиотикам, число копий и соответствующие ориджины репликапции.
Приемлемые клетки-хозяева, пригодные для клонирования или экспрессии ДНК в векторах, включают прокариотические клетки, дрожжевые клетки или высшие эукариотические клетки. Прокариотические клетки, пригодные для указанной цели, включают эубактерии, такие как грамотрицательные или грамположительные организмы, например, Enterobacteriaceae, такие как Escherichia, например, E. coli, Enterobacter, Erwinia, Klebsiella, Proteus, Salmonella, например, Salmonella typhimurium, Serrafia, например, Serratia marcescans, и Shigeila, а также Bacilli, такие как B. subtilis и B. licheniformis (например, B. licheniformis 41P, описанные в патенте DD 266710, опубликованном 12 апреля 1989 г.), Pseudomonas, такие как P. aeruginosa, и Streptomyces. Одним предпочтительным хозяином для клонирования E. coli является E. coli 294 (ATCC 31446), хотя приемлемы и другие штаммы, такие как E. coli B, E. coli X 1776 (ATCC 31537) и E. coli W3110 (ATCC 27325). Указанные примеры являются иллюстративными и не ограничивают объем изобретения.
Помимо прокариотических клеток, приемлемыми клонирующими или экспрессирующими хозяевами для антителокодирующих векторов являются эукариотические микробы, такие как нитевидные грибы или дрожжи. Saccharomyces cerevisiae или обычные пекарские дрожжи являются наиболее часто используемыми низшими эукариотическими микроорганизмами-хозяевами. Однако в настоящем изобретении может быть использован целый ряд других родов, видов и штаммов, таких как Schizosaccharomyces pombe; хозяева Kluyveromyces, такие как, например, K. lactis, K. fragilis (ATCC 12424), K. bulgaricus (ATCC 16045), K. wickeramii (ATCC 24178), K. waltii (ATCC 56500), K. drosophilarum (ATCC 36906), K. thermotolerans и K. marxianus; yarrowia (EP 402226); Pichia pastoris (EP 183070); Candida; Trichoderma reesia (EP 244234); Neurospora crassa; Schwanniomyces, такие как Schwanniomyces occidentalis; и нитевидные грибы, такие как, например, Neurospora, Penicillium, Tolypocladium, и хозяева Aspergillus, такие как A. nidulans и A. niger.
Клетки-хозяева, приемлемые для экспрессии гликозилированного антитела, выделяют из многоклеточных организмов. Примеры клеток беспозвоночных включают растительные клетки и клетки насекомых. Идентифицированы многочисленные бакуловирусные штаммы и варианты, а также соответствующие допустимые клетки-хозяева насекомых, выделяемые из таких хозяев как Spodoptera frugiperda (гусеница), Aedes aegypti (комар), Aedes albopictus (комар), Drosophila melanogaster (дрозофила) и Bombyx mori. Разные вирусные штаммы также доступны для трансфекции, например, варианты L-1 Autographa californica NPV и штамм Bm-5 Bombyx mori NPV, и такие вирусы могут быть использованы в настоящем изобретении, в частности, для трансфекции клеток Spodoptera frugiperda. В качестве хозяев могут быть также использованы культуры растительных клеток хлопчатника, кукурузы, картофеля, сои, петунии, помидоров и табака.
Однако наибольший интерес представляют клетки позвоночных, и размножение клеток позвоночных в культуре (культура ткани) является обычной практикой. Примерами приемлемых линий клеток-хозяев млекопитающих являются линия клеток CV1 почки обезьяны, трансформированных вирусом SV40 (COS-7, ATCC CRL 1651); линия эмбриональных клеток почки человека (клетки 293 или клетки 293, субклонированные для выращивания в суспензионной культуре, Graham et al., J. Gen. Virol. 36:59 (1977); клетки почки детеныша хомячка (ВНК, ATCC CCL 10); клетки яичника китайского хомячка/-DHFR (CHO, Urlaub et al., Proc. Natl. Acad. Sci. USA 77:4216 (1980)); клетки сертоли мыши (ТМ4, Mather, Biol. Reprod. 23:243-251 (1980)); клетки почки обезьяны (CV1 ATCC CCL 70); клетки почки африканской зеленой мартышки (VERO-76, ATCC CRL-1587); клетки рака шейки матки человека (HELA, ATCC CCL 2); клетки почки собаки (MDCK, ATCC CCL 34); клетки печени буйволовой крысы (BRL 3A, ATCC CRL 1442); клетки легкого человека (W138, ATCC CCL 75); клетки печени человека (Hep G2, HB 8065); опухоль молочной железы мыши (ММТ 060562, АТСС CCL51); клетки TRI (Mather et al., Annals N.Y. Acad. Sci. 383:44-68 (1982)); клетки MRC 5; клетки FS4 и линия клеток гепатомы человека (Нер G2).
Клетки-хозяева трансформируют вышеописанными экспрессирующими или клонирующими векторами для получения вариантов CRIg по настоящему изобретению, культивируют в стандартных питательных средах, модифицированных соответствующим образом для индукции промоторов, отбирают трансформанты или амплифицируют гены, кодирующие требуемые последовательности.
Клетки-хозяева, используемые для получения вариантов CRIg по настоящему изобретению, можно культивировать в разных средах. Для культивирования клеток-хозяев пригодны коммерчески доступные среды, такие как среда Хэма F10 (Sigma), минимальная поддерживающая среда ((МЕМ), (Sigma), RPMI-1640 (Sigma) и модифицированная по способу Дульбекко среда Игла ((DMEM), Sigma). Кроме того, в качестве культуральных сред для клеток-хозяев могут быть использованы любые среды, описанные в публикации Ham et al., Meth. Enz. 58:44 (1979), Barnes et al., Anal. Biochem. 102:255 (1980), в патентах США № 4767704, 4657866, 4927762, 4560655 или 5122469; WO 90/03430; WO 87/00195 или патенте США с регистрационным номером 30985. Любые из указанных сред при необходимости могут содержать гормоны и/или другие факторы роста (такие как инсулин, трансферрин или эпидермальный фактор роста), соли (такие как хлорид натрия, фосфат кальция и магния), буферы (такие как HEPES), нуклеотиды (такие как аденозин и тимидин), антибиотики (такие как GENTAMYCIN™), следовые элементы (определяемые как неорганические соединения, обычно присутствующие в конечных концентрациях в микромолярном диапазоне) и глюкозу или эквивалентный источник энергии. Могут быть также введены другие необходимые добавки в соответствующих концентрациях, известных специалистам в данной области. Условия культивирования, такие как температура, рН и тому подобные, соответствуют ранее использовавшимся для клеток-хозяев, отобранных для экспрессии, и должны быть очевидны специалисту в данной области.
При использовании методов рекомбинантных ДНК вариант CRIg может быть получен внутри клетки, в периплазматическом пространстве, или секретирован прямо в среду. При получении варианта CRIg внутри клетки в качестве первой стадии удаляют дебрис клеток-хозяев или лизированных клеток, например, путем центрифугирования или ультрафильтрации. Если вариант CRIg секретируют в среду, супернатанты таких экспрессирующих систем обычно сначала концентрируют, используя коммерчески доступный фильтр для концентрирования белка, например, ультрафильтрующее устройство Amicon или Millipore Pellicon. Ингибитор протеазы, такой как PMSF, может быть использован на любой из вышеуказанных стадий для ингибирования протеолиза, и антибиотики могут быть использованы для предотвращения роста случайных загрязняющих веществ.
Вариант CRIg, полученный из клеток, может быть очищен известными методами, например, при помощи хроматографии на колонке с гидроксилапатитом, гель-электрофореза, диализа и/или аффинной хроматографии.
Другие модификации вариантов CRIg
Варианты CRIg по настоящему изобретению могут быть также модифицированы с образованием химерной молекулы, включающей вариант CRIg, в том числе его фрагменты, гибридизированные с другим гетерологичным полипептидом или аминокислотной последовательностью. В одном варианте осуществления изобретения такая химерная молекула включает гибрид варианта CRIg или его фрагмента с меченым полипептидом, образующим эпитоп, с которым может избирательно связываться антитело против данной метки. Метка эпитопа обычно находится у амино- или карбоксиконца полипептида варианта CRIg. Присутствие таких форм варианта CRIg с меченым эпитопом можно обнаружить, используя антитело против меченого полипептида. Кроме того, наличие метки эпитопа позволяет легко очистить полипептид CRIg путем аффинной очистки с использованием антитела против метки или другого типа аффинной матрицы, связывающейся с меткой эпитопа. В данной области известны разные меченые полипептиды и соответствующие антитела. Примеры включают полигистидиновые (поли-his) или полигистидинглициновые (поли-his-gly) метки; меченый полипептид flu HA и антитело к нему 12СА5 [Field et al., Mol. Cell. Biol., 8:2159-2165 (1988)]; метку c-myc и антитела 8F9, 3C7, 6Е10, G4, B7 и 9Е10 к ней (Evan et al., Molecular and Cellular Biology, 5:3610-3616 (1985)); гликопротеин D вируса простого герпеса (gD) и антитело к данной метке (Paborsky et al., Protein Engineering, 3(6):547-553 (1990)). Другие меченые полипептиды включают Flag-пептид (Hopp et al., Bio Technology, 6:1204-1210 (1988)); пептид эпитопа КТ3 (Martin et al., Science, 255:192-194 (1992)); пептид эпитопа тубулин с четвертичной структурой [Skinner et al., J. Biol. Chem., 266:15163-15166 (1991)]; и белковый пептид 10 гена Т7 (Lutz-Freyermuth et al., Proc. Natl. Acad. Sci. USA, 87:6393-6397 (1990)).
В другом варианте осуществления изобретения химерная молекула может включать гибрид варианта CRIg или его фрагмента с иммуноглобулином или определенной областью иммуноглобулина. Для двухвалентной формы химерной молекулы такой гибрид может быть получен с Fc-областью молекулы IgG. Такие гибридные полипептидны являются антителоподобными молекулами, совмещающими специфичность связывания гетерологичного белка (”адгезин”) с эффекторными функциями константных доменов иммуноглобулина, и часто определяются как иммуноадгезины. В структурном отношении иммуноадгезины представляют собой гибрид аминокислотной последовательности, обладающей требуемой специфичностью связывания, которая отличается от антигенузнающего и связывающего центра антитела (то есть является ”гетерологичной”), и последовательности константного домена иммуноглобулина. Адгезин, являющийся частью молекулы иммуноадгезина, обычно представляет собой смежную аминокислотную последовательность, включающую по меньшей мере сайт связывания рецептора или лиганда. Последовательность константного домена иммуноглобулина в иммуноадгезине может быть получена из любого иммуноглобулина, такого как подтипы IgG-1, IgG-2, IgG-3 или IgG-4, IgA (включая IgA-1 и IgA-2), IgE, IgD или IgM.
В самой простой структуре иммуноадгезина объединены области связывания белка ”адгезина” с шарнирной областью и Fc-областью тяжелой цепи иммуноглобулина. При получении CRIg-иммуноглобулиновых химер по настоящему изобретению С-конец нуклеиновой кислоты, кодирующей внеклеточный домен CRIg, обычно гибридизируют с нуклеиновой кислотой, кодирующей N-конец последовательности константного домена иммуноглобулина, однако, также возможны N-концевые гибриды.
В таких гибридах кодированный химерный полипептид обычно сохраняет по меньшей мере функционально активную шарнирную область, СН2- и СН3-домеы константной области тяжелой цепи иммуноглобулина. Получают также гибриды с С-концом Fc-части константного домена или N-конца с СН1 тяжелой цепи или соответствующей области легкой цепи.
Точный сайт, на котором может быть получен гибрид, не имеет критического значения; конкретные сайты хорошо известны и могут быть выбраны с учетом оптимизации биологической активности, секреции или характеристик связывания CRIg-иммуноглобулиновых химер.
В некоторых вариантах осуществления изобретения CRIg-иммуноглобулиновые химеры получают в виде мономеров, гетеро- или гомомногомеров и, в частности, в виде димеров или тетрамеров, аналогичных приведенным в публикации WO 91/08298.
В предпочтительном варианте осуществления изобретения последовательность внеклеточного домена CRIg гибридизируют с N-концом С-концевой части антитела (в частности, Fc-доменом), выполняющего эффекторные функции иммуноглобулина, например, иммуноглобулина G.sub.1 (IgG 1). Можно гибридизировать всю константную область тяжелой цепи с последовательностью внеклеточного домена CRIg. Однако более предпочтительно в гибриде используют последовательность, начинающуюся в шарнирной области вверху от сайта расщепления папаином (которая в химическом отношении определяет Fc-область IgG; остаток 216, при этом первым остатком константной области тяжелой цепи является остаток 114 или аналогичные сайты других иммуноглобулинов). В особенно предпочтительном варианте осуществления изобретения аминокислотную последовательность CRIg гибридизируют с шарнирной областью, СН2 и СН3 или с СН1, шарнирной областью, СН2 и СН3 доменами тяжелой цепи IgG1, IgG2 или IgG3. Точный сайт, на котором может быть получен гибрид, не имеет критического значения, при этом оптимальный сайт можно определить обычным экспериментированием.
В некоторых вариантах осуществления изобретения CRIg-иммуноглобулиновые химеры получают в виде многомеров и, в частности, в виде гомодимеров или гомотетрамеров. Такие собранные иммуноглобулины обычно имеют известные элементарные структуры. Основное четырехцепное структурное звено представляет собой форму, в которой существуют IgG, IgD и IgE. Четырехцепное звено повторяется в иммуноглобулинах с более высокой молекулярной массой; IgM обычно существует в виде пентамера основных четырехцепных звеньев, связанных дисульфидными связями. Глобулин IgA и иногда глобулин IgG могут также существовать в многомерной форме в сыворотке. В случае многомера все четырехцепные звенья могут быть одинаковыми или разными.
Альтернативно последовательность внеклеточного домена CRIg может быть вставлена между последовательностями тяжелой цепи и легкой цепи иммуноглобулина, в результате чего получают иммуноглобулин, включающий химерную тяжелую цепь. В данном варианте осуществления изобретения последовательность CRIg гибридизируют с 3'-концом тяжелой цепи иммуноглобулина в каждом спейсере иммуноглобулина между шарнирной областью и СН2 доменом или между СН2 и СН3 доменами. Аналогичные конструкции были представлены в публикации Hoogenboom et al., Mol. Immunol., 28:1027-1037 (1991).
Хотя наличие легкой цепи иммуноглобулина не требуется в иммуноадгезинах по настоящему изобретению, легкая цепь иммуноглобулина может присутствовать, будучи ковалентно связанной с гибридным полипептидом CRIg и тяжелой цепи иммуноглобулина или прямо гибридизированной с внеклеточным доменом CRIg. В первом случае ДНК, кодирующая легкую цепь иммуноглобулина, обычно коэкспрессирована с ДНК, кодирующей гибридный белок CRIg и тяжелой цепи иммуноглобулина. В процессе секреции тяжелая цепь и легкая цепь гибрида ковалентно сввязываются, образуя иммуноглобулинподобную структуру, включающую две пары тяжелой цепи-легкой цепи иммуноглобулина, связанные дисульфидными связями. Способы получения таких структур, например, описаны в патенте США № 4816567, выданном 28 марта 1989 г.
Фармацевтические композиции
Варианты CRIg по настоящему изобретению можно вводить для лечения заболеваний, патология которых обусловлена альтернативным путем активации комплемента.
Терапевтические препараты получают с возможностью хранения, смешивая активную молекулу, обладающую требуемой степенью чистоты, с необязательными фармацевтически приемлемыми носителями, наполнителями или стабилизаторами (Remington's Pharmaceutical Sciences, 16th edition, Osol, A. Ed. [1980]), в виде лиофилизованных препаратов или водных растворов. Приемлемые носители, наполнители или стабилизаторы не должны быть токсичными для реципиентов в используемых дозах и концентрациях и включают буферы, такие как фосфат, цитрат и другие органические кислоты; антиоксиданты, включающие аскорбиновую кислоту и метионин; консерванты (такие как хлорид октадецилдиметилбензиламмония; хлорид гексаметония; хлорид бензалкония, хлорид бензетония; феноловый, бутиловый или бензиловый спирт; алкилпарабены, такие как метил- или пропилпарабен; катехин; резорцин; циклогексанол; 3-пентанол и м-крезол); низкомолекулярные (менее примерно 10 остатков) полипептиды; белки, такие как сывороточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, гистидин, аргинин или лизин; моносахариды, дисахариды и другие углеводы, включающие глюкозу, маннозу или декстрины; хелатообразователи, такие как EDTA; сахара, такие как сахароза, маннит, трегалоза или сорбит; солеобразующие противоионы, такие как натрий; комплексы металлов (например, Zn-белковые комплексы); и/или неионогенные поверхностно-активные вещества, такие как TWEEN™, PLYRONIC™ или полиэтиленгликоль (PEG).
Липофектины или липосомы также могут быть использованы для доставки в клетки полипептида, антитела или фрагмента антитела. При использовании фрагментов антитела предпочтительным является наименьший фрагмент, который специфически связывается с доменом связывания белка-мишени. Например, на основе последовательностей вариабельной области антитела могут быть получены пептидные молекулы, которые сохраняют способность связываться с последовательностью белка-мишени. Такие пептиды могут быть синтезированы химическими методами и/или получены методами рекомбинантных ДНК (см., например, публикацию Marasco et al., Proc. Natl. Acad. Sci. USA 90, 7889-7893 [1993]).
Препарат по настоящему изобретению может также содержать несколько активных соединений, необходимых для лечения конкретного заболевания, предпочтительно обладающих комплементарной активностью и не оказывающих вредного влияния друг на друга. Такие молекулы присутствуют в комбинации в количествах, обеспечивающих эффективное достижение поставленной цели.
Активные молекулы могут быть также заключены в микрокапсулы, полученные, например, методами коацервации или межфазной полимеризации, такие как, например, гидроксиметилцеллюлозные или желатиновые микрокапсулы и поли(метилметакрилатные) микрокапсулы, соответственно, в коллоидные системы доставки лекарственных средств (например, липосомы, альбуминовые микросферы, микроэмульсии, наночастицы и нанокапсулы) или в макроэмульсии. Такие методы описаны в публикации Remington's Pharmaceutical Sciences 16th edition, Osol, A. Ed. (1980).
Препараты, предназначенные для введения in vivo, должны быть стерильными. Стерильность легко достигается путем фильтрации через стерильные фильтрующие мембраны.
Могут быть получены препараты с пролонгированным действием. Приемлемые примеры препаратов с пролонгированным действием включают полупроницаемые матрицы из твердых гидрофобных полимеров, содержащие антитело, которые имеют форму формованных изделий, например пленок, или микрокапсулы. Примеры матриц с пролонгированным высвобождением включают сложные полиэфиры, гидрогели (например, поли(2-гидроксиэтилметакрилат) или поли(виниловый спирт)), полилактиды (патент США № 3773919), сополимеры L-глутаминовой кислоты и гамма-этил-L-глутамата, нерасщепляемый этиленвинилацетат, расщепляемые сополимеры молочной кислоты и гликолевой кислоты, такие как LUPRON DEPOT™ (инъецируемые микросферы, состоящие из сополимера молочной кислоты и гликолевой кислоты и лейпролидацетата), и поли-D-(-)-3-гидроксимасляную кислоту. Хотя такие полимеры, как этиленвинилацетат и сополимер молочной кислоты и гликолевой кислоты, позволяют высвобождать молекулы в течение более 100 дней, существуют определенные гидрогели, высвобождающие белки в течение более коротких периодов времени. Если инкапсулированные антитела остаются в теле в течение длительного времени, они могут денатурировать или агрегировать под воздействием влаги при 37°С, утрачивая, таким образом, биологическую активность и вызывая возможные изменения иммуногенности. Препарат может быть рационально стабилизирован в зависимости от используемого механизма. Например, если установлено, что механизм агрегации включает образование межмолекулярных S-S связей в результате тиодисульфидного обмена, стабилизация может быть достигнута путем модификации сульфгидрильных остатков, лиофилизации из кислотных растворов, контроля влажности, использования соответствующих добавок и создания специальных композиций на основе полимерной матрицы.
Способы лечения
Благодаря своей способности ингибировать активацию комплемента, в частности, альтернативный путь активации комплемента, варианты CRIg по настоящему изобретению находят применение в профилактике и/или лечении комплемент-ассоциированных заболеваний и патологических состояний. Такие заболевания и состояния включают, не ограничиваясь ими, комплемент-ассоциированные, воспалительные и аутоиммунные заболевания.
Конкретные примеры комплемент-ассоциированных, воспалительных и иммунных заболеваний и нарушений, на которые могут направленно воздействовать варианты CRIg по настоящему изобретению, приведены выше.
Настоящее изобретение далее будет более подробно проиллюстрировано приведенными ниже примерами, не ограничивающими объем изобретения.
Пример 1
Получение вариантов CRIg с созревшей аффинностью
Материалы и методы
Материалы
Материалы - Ферменты и фаг-хелпер М13-КО7 (New England Biolabs); планшеты для иммуноанализа Maxisorp (Nunc. Roskilde, Denmark); 96-луночный полипропиленовый планшет с U-образными лунками (COSTAR; № по каталогу 3365); 96-луночный планшет с плоскими лунками, не вызывающий связывания (NUNC; № по каталогу 269620); конъюгат пероксидазы из хрена/антитела против М13 (Pharmacia); субстрат из 3,3',5,5'-тетраметилбензидина, субстрат пероксидазы Н2О2 (ТЕВ) (Kirkegaard and Perry Laboratories, Inc); Escherichia coli XL1-синий и E. coli BL21 (DE3) (Stratagene); бычий сывороточный альбумин (BSA) и Твин-20 (Sigma); агароза Ni-NTA (Qiagen); эритроциты (RBC) кролика (Colorado Serum Company; № по каталогу CS1081); вероналовый буфер с желатином (GVB) [100 мл вероналового буфера (Bio Whittaker; № по каталогу 12-624Е); желатин (из бычьей кожи типа В; SIGMA; № по каталогу G9391-100G); сыворотка с отсутствием C1q (CompTech; № по каталогу А300); fH-белок (Complement Technology; № по каталогу А137); антитело против FLAG-HRP в 50% глицерине, Sigma, № по каталогу А-8592, 1,1 мг/мл.
Создание библиотек отображения CRIg на фаге
Фрагмент ДНК, кодирующий CRIg, лигировали с фаговым вектором, расщепляемым XhoI и SpeI (p3DvlzDZ-gD) (Kunkel et al., Methods Enzymol. 154:367-382 (1987)), и использовали в качестве контрольного образца дикого типа и матрицы для создания вариантов CRIg. Затем из клеток E. coli CJ239 получали матрицы с терминирующим кодоном ТАА в каждом остатке, обеспечивающим направленную рандомизацию (Kunkel et al., 1987, см выше). Варианты CRIg отбирали методом мягкой рандомизации, в соответствии с которым в выбранном положении задавали частоту мутаций, равную примерно 50%, используя метод на основе олигонуклеотида с ядом и смесями оснований 70-10-10-10, благоприятно воздействующими на нуклеотиды дикого типа. В библиотеках: 5 = 50% А, 10% G, 10% С и 10% Т; 6 = 50% G, 10% A, 10% C и 10% Т; 7 = 50% С, 10% А, 10% G и 10% Т; 8 = 50% Т, 10% А, 10% G и 10% С.
Было создано пять библиотек.
BCR1, ATC CTG GAA GTG CAA 656 (SEQ ID NO:7) AGT GTA ACA GGA CCT 866 (SEQ ID NO:8) 555 GGG GAT GTG AAT CTT (SEQ ID NO:9) в библиотеке 1;
BCR2, AAG TGG CTG GTA CAA 768 (SEQ ID NO:10) 668 ТСА 657 775 688 577 АТС ТТТ (SEQ ID NO:11) 786 CGT 657 TCT TCT GGA GAC CAT (SEQ ID NO:12) в библиотеке 2;
BCR3, TTT CTA CGT GAC TCT (SEQ ID NO:13) 877 668 657 757 588 756 756 678 555 ТАС 756 GGC CGC CTG CAT GTVG (SEQ ID NO:14) в библиотеке 3;
BCR4, CAA TTG AGC ACC CTG (SEQ ID NO:15) 656 586 657 GAC 768 AGC CAC TAC ACG TGT 656 (SEQ ID NO:16) GTC ACC TGG 756 (SEQ ID NO:17) ACT CCT GAT GGC AAC (SEQ ID NO:18) в библитеке 4;
BCR5, ACT CCT GAT GGC AAC 756 (SEQ ID NO:19) GTC 688 768 657 555 ATT ACT GAG CTC CGT (SEQ ID NO:20) в библиотеке 5.
Сайт-направленный мутагенез для точковых мутаций выполняли вышеописанным методом, используя подходящие кодоны для получения соответствующих мутаций, при этом правильные клоны определяли путем секвенирования.
Сортировка и скрининг библиотек для отбора вариантов CRIg
Планшеты для иммуноанализа Maxisorp сенсибилизировали в течение ночи при 4°С комплементом C3b (5 мкг/мл) и блокировали в течение 1 часа при комнатной температуре физиологическим раствором с фосфатным буфером (PBS) и 0,05% (масс./об.) бычьим сывороточным альбумином (BSA). Библиотеки фагов наносили на C3b-сенсибилизированные планшеты и инкубировали при комнатной температуре в течение 3 часов. Планшеты промывали десять раз, связанный фаг элюировали 50 мМ HCl и нейтрализовали равным объемом 1,0 М трис-основания (рН 7,5). Выделенные фаги амплифицировали, пассируя на E. coli XL1-синем, и использовали для выполнения дополнительных циклов отбора связывания. После выполнения 5 циклов были отобраны 12 отдельных клонов из каждой библиотеки, которые выращивали на 96-луночных планшетах в 500 мкл бульона 2YT, содержащего карбенициллин и фаг-хелпер М13-КО7. Культуральные супернатанты, подвергнутые двукратному последовательному разведению, наносили на 384-луночные планшеты, сенсибилизированные C3b, антителом против gD, BSA и неродственным белком в требуемых положениях. Для определения концентрации фага измеряли сродство связывания, для чего C3b вводили в значительно большем количестве, чем антило против gD, что не относилось к BSA и неродственному белку. Концентрацию фага фиксировали, исследуя примерно 200 клонов из каждой библиотеки одинаковым методом, в результате чего было отобрано 24-48 клонов, которые в значительной степени связывались с C3b по сравнению с антителом против gD в каждой библиотеке, затем их секвенировали для выполнения анализа.
Конкурентно-связывающий анализ фагов ELISA
Для определения сродства связывания выполняли модифицированный анализ фагов ELISA. 96-луночные титрационные микропланшеты сенсибилизировали 2 мкг/мл 3Cb в 50 мМ карбонатного буфера (рН 9,6) в течение ночи при 4°С. Затем планшеты блокировали PBS, 0,5% BSA в течение 1 часа при комнатной температуре. Фаг, отображающий варианты CRIg, последовательно разводили в буфере РВТ и измеряли связывание для определения концентрации фага, подавая 50% сигнал при насыщении. Концентрацию фага при частичном насыщении фиксировали, фаг предварительно инкубировали в течение 2 часов при последовательных разведениях C3b и переносили смесь на аналитические планшеты, сенсибилизированные C3b. После инкубации в течение 15 минут планшеты промывали PBS, 0,05% Твин-20 и инкубировали в течение 30 минут с конъюгатом пероксидазы из хрена/антитела против М13 (разведение в отношении 1:5000 в буфере РВТ). Планшеты промывали, проявляли субстратом ТМВ, гасили 1,0 М раствором Н3РО4 и считывали спектрофотометром для прочтения планшетов при длине волны 450 нм. Сродство (IC50) вычисляли в виде концентрации конкурирующего C3b, обеспечивающей половину от максимального связывания фага.
Очистка белка
Единичную колонию E. coli BL12 (DE3), содержащую экспрессирующую плазмиду, инокулировали в 30 мл среды LB, содержащей 50 мкг/мл карбенициллина (среда LB/углеводы) и выращивали в течение ночи при 37°С. Бактерии собирали, промывали, ресуспендировали и инокулировали в 500 мл среды LB/углеводы. Культуру выращивали при 37°С до средней лог-фазы (А600 = 0,8). Экспрессию белка индуцировали 0,4 мМ изопропил-1-тио-D-галактопиранозида и культуру выращивали в течение 24 часов при 30°С. Бактерии центрифугировали при ускорении 4000 g в течение 15 минут, дважды промывали физиологическим раствором с фосфатным буфером (PBS) и замораживали в течение 8 часов при -80°С. Осадок ресуспендировали в 50 мл PBS и бактерии лизировали, пропуская их через микрофлюидизатор или ультразвуковое оборудование. Белки вариантов CRIg очищали 2 мл агарозы NI-NTA и гель-фильтрацией.
Конкурентно-связывающий анализ mutCRIg-huFc в жидкой фазе методом ELISA
huCRIg(L)-LFH разводили до 2 мкг/мл в PBS, рН 7,4, наносили на 384-луночные планшеты с плоскими лунками Maxisorp (Nunc, Neptune, NJ) и инкубировали в течение ночи (16-18 часов) при 4°С (25 мкл/лунка). Планшеты трижды промывали в промывочном буфере (PBS, рН 7,4, 0,05% Твин-20) и в каждую лунку добавляли 50 мкл/лунка блокирующего буфера (PBS, рН 7,4, 0,5% BSA). Планшеты блокировали в течение 1-3 часов; данную и все последующие инкубации выполняли на ротационном шейкере при комнатной температуре. На стадии блокирования C3b (очищенный в компании Genetech) разводили до 20 нМ в аналитическом буфере (PBS, рН 7,4, 0,5% BSA, 0,05% Твин-20) и молекулы mutCRIg-huFc также последовательно разводили в аналитическом буфере в диапазоне концентраций 20000 - 0,34 нМ. Затем C3b и молекулы mutCRIg-huFc смешивали в отношении 1:1 и предварительно инкубировали в течение 0,5-1 часа. Блокированные планшеты промывали три раза (как было описано выше) и на реакционные планшеты наносили комплексы C3b:mutCRIg-huFc (25 мкл/лунка). После инкубации в течение 1-2 часов планшеты для анализа ELISA промывали три раза (как было описано выше) и обнаруживали связанный с планшетом C3b, добавляя антитело против C3b человека (клон 5F202, US Biological, Swampscott, MA; 600 нг/мл, 25 мкл/лунка). Планшеты инкубировали в течение 1-2 часов и промывали вышеописанным способом. Затем добавляли HRP-конъюгированный IgG против Fc мыши (Jackson ImmunoResearch, West Grove, PA), разведенный в отношении 1:2000, (25 мкл/лунка) и планшеты инкубировали в течение 1-2 часов. После конечной промывки на планшеты для анализа ELISA наносили 25 мкл/лунка субстрата ТМВ (Kirkegaard & Perry Laboratories, Gaithersburg, MD). Примерно через 8 минут прекращали проявление цвета, добавляя 25 мкл/лунка 1,0 М раствора фосфорной кислоты. Оптическую плотность при 450 нм и 650 нм определяли при помощи спектрофотометра для прочтения титрационных микропланшетов SpectraMax 250 (Molecular Devices, Sunnyvale, CA).
Анализ активации комплемента
Способность mutCRIg-Fc ингибировать активацию комплемента определяли, используя набор для альтернативного пути активации комплемента Wieslab™ (Alpco Diagnostics, Salem, NH). Последовательно разведенный mutCRIg-Fc (от 400 до 0,2 нМ) и человеческую сыворотку с отсутствием C1q (5%) (Complement Technology, Tyler, TX) получали в концентрации, которая была в два раза выше требуемой конечной концентрации, в виде смеси с соотношением 1:1, предварительно инкубировали в течение 5 минут на ротационном шейкере со скоростью 300 оборотов/мин и наносили на LPS-сенсибилизированные планшеты для анализа ELISA (100 мкл/лунка). Остальную часть анализа выполняли в соответствии с инструкциями производителя. Кратко, образцы на планшетах для анализа ELISA инкубировали в течение 60-70 минут при 37°С и трижды промывали в промывочном буфере (PBS, рН 7,4, 0,05% Твин-20). На планшет для анализа ELISA наносили 100 мкл/лунка конъюгата антитела против C5b-9. После инкубации в течение 30 минут при комнатной температуре планшет для анализа ELISA промывали вышеописанным способом, в каждую лунку добавляли 100 мкл субстрата и планшеты инкубировали при комнатной температуре в течение еще 30 минут. Проявление цвета прекращали, добавляя 50 мкл/лунка 5 мМ EDTA. Оптическую плотность при 405 нм определяли, используя спектрофотометр для прочтения титрационных микропланшетов MultiSkan Ascent (Thermo Fisher Scientific, Milford, MA).
Анализ ингибирования гемолиза
Эритроциты кролика (Colorado Serum Company, Denver, CO) трижды промывали вероналовым буфером (Sigma, St. Louis, MO), содержащим 0,1% желатина бычьей кожи (Sigma) (GVB), и после каждой промывки центрифугировли со скоростью 1500 оборотов/мин при 4°С в течение 10 минут. После выполнения последней стадии центрифугирования клетки ресуспендировали в GVB в конечной концентрации 2×109 клеток/мл. Ингибиторы комплемента, последовательно разведенные в GVB, наносили на 96-луночные полипропиленовые планшеты с U-образными лунками (Costar, Cambridge, MA) в количестве 50 мкл/лунка и затем добавляли 20 мкл/лунка эритроцитов кролика, разведенных в отношении 1:2 в 0,1 М MgCl2/0,1M EGTA/GVB. Каскад активации комплемента на планшете запускали, добавляя 30 мкл/лунка сыворотки с отсутствием C1q (Complement Technology, Tyler, TX), которую предварительно разводили GVB в отношении 1:3. Планшет(ы) инкубировали, осторожно встряхивая, в течение 30 минут при комнатной температуре, после чего реакцию прекращали, добавляя 100 мкл/лунка 10 мМ EDTA/GVB. Планшет(ы) центрифугировали со скоростью 1500 оборотов/мин в течение 5 минут, затем супернатанты переносили на чистые 96-луночные планшеты с плоскими лунками, не вызывающие связывания (Nunc, Neptune, NJ) и определяли оптическую плотность при 412 нм, используя спектрофотометр для прочтения микропланшетов (Molecular Devices, Sunnyvale, CA).
Конкурентно-связывающий анализ Alpha Screen
Потенциальную перекрестную реактивность молекул мутантного CRIg в отношении С3 определяли при помощи набора для обнаружения гистидина (хелат никеля) AlphaScreen® (PerkinElmer, Waltham MA). Последовательно разведенные комплементы человека С3 и C3b (от 3000 до 0,7 нМ), биотинилированный iC3b в постоянных концентрациях (30 нМ) и молекулы мутантного CRIg (mutCRIg) и CRIg дикого типа (15-60 нМ) получали в концентрации, которая была в три раза выше требуемой конечной концентрации, в виде смеси с соотношением 1:1:1 и предварительно инкубировали при комнатной температуре в течение 30 минут на ротационном шейкере со скоростью вращения 3000 оборотов/мин. Смесь донорных гранул стрептавидина и акцепторных гранул хелата никела с соотношением 1:1 (по 0,1 мг/мл каждое) получали в концентрации, которая была в четыре раза выше требуемой конечной концентрации, и добавляли в реакционную смесь. Реакционный планшет инкубировали при комнатной температуре в течение 60 минут на ротационном шейкере со скоростью вращения 3000 оборотов/мин в темноте. Планшет анализировали с помощью анализатора для микропланшетов AlphaQuest®-HTS (PerkinElmer, Waltham, MA).
Резонанс поверхностных плазмонов
Сродство C3b к мутантным CRIg и CRIg дикого типа определяли путем измерения резонанса поверхностных плазмонов в устройстве А100 Biacore® (GE healthcare). Использовали иммобилизованное антитело против Fc и вычисляли значение K D, выполняя измерения равновесного связывания. Сенсорный чип получали, используя набор иммобилизованных антител против muFc (BR-1008-38) в соответствии с инструкциями производителя. Мутантные CRIg и CRIg дикого типа разводили в разделяющем буфере (10 мМ HEPES, рН 7,4, 150 мМ NaCl, 0,01% Твин-20) до концентрации 1 мкг/мл и вводили 60 мкл таким образом, что одним пятном поверхности чипа было захвачено ~100 крысиных единиц (RU) гибридного белка. Сенсограммы регистрировали для растворов с разными концентрациями C3b, которые наносили на пятно CRIg на 10 минут, за вычетом сигнала для эталонного пятна, содержащего иммобилизованное антитело без CRIg. Данные были получены для серии 2-кратных разведений C3b в концентрации от 4 мкМ до 15,6 нМ при скорости потока 10 мкл/мин и температуре 25°С. Поверхность регенерировали между циклами связывания путем введения 10 мМ Gly-HCl, рН 1,7, на 30 секунд. Ровные значения, полученные в конце каждого введения C3b, использовали для вычисления К D при помощи алгоритма сродства программного обеспечения Biacore A100, версия 1.1 (Safsten et al. (2006) Anal. Biochem. 353:181).
Результаты
Создание библиотек фагов
Для создания библиотек фагов была использована кристаллическая структуроа CRIg совместно с C3b. Было создано пять библиотек для охвата всей площади контакта между CRIg и C3b (фигура 4). Библиотеки CRIg были созданы в виде гибрида с минорным белком оболочки g3p в одновалентном векторе отображения на фаге (Zhang et al., J. Biol. Chem. 281(31):22299-311 (2006)). Путем мутагенеза были введены терминирующие кодоны в CRIg-кодирующую часть фаговой плазмиды в положении каждого рандомизируемого остатка. Все конструкции, содержащие терминирующий кодон, затем использовали для создания библиотеки отображения на фаге (см. раздел ”Материалы и методы”). Метод ”мягкой рандомизации” был использован для отбора связующих, необходимых для сохранения смещения последовательности дикого типа с тем, чтобы выбранные положения были мутированы только в течение 50% времени. Все пять библиотек были получены со средней вариабельностью >1010 независимых последовательностей в одной библиотеке (таблица 1).
Отбор при помощи библиотеки отображения CRIg на фаге
После выполнения четырех циклов отбора связывания было получено 38 уникальных клонов из пяти библиотек (таблица 2). В библиотеке 1 был сохранен лизин в положении 15. Глутаминовая кислота в положении 8 была заменена ароматическими остатками, тирозином и триптофаном. В положении 14 находился исходный триптофан или гомологичный фенилаланин. В библиотеке 2 были секвенированы 24 клона, и все они соответствовали друг другу. В положениях 42, 46 и 47 были сохранены остатки, присутствующие в последовательности дикого типа. Последовательность дикого типа в положениях 43, 44 и 45 была заменена аспарагином, гистидином и фенилаланином. В библиотеке 3 были произвольно заменены остатки в 10 положениях при полном сохранении остатков в положениях 54, 55, 56, 57, 58, 61, 62 и 63. В положении 60 находился изолейцин или лизин. Глутамин в положении 64 был заменен аргинином или сохранен. В библиотеке 4 в положении 86 преобладали ароматические остатки и в положении 99 преобладали гомологичные основные остатки, аргинин и лизин. Остатки в положениях 85, 87 и 95 также были произвольно заменены, но оставались высоко консервативными. В библиотеке 5 в положении 105 вместо глутамина были предпочтительно использованы два значительных гомологичных основных остатка, лизин и аргинин. В положении 110 преобладали отрицательно заряженные остатки, аспарагиновая кислота или кислотные остатки, аспарагин.
Сродство некоторых мутантов определяли при помощи конкурентно-связывающего анализа фагов ELISA (данные отсутствуют), при этом было установлено, что в библиотеке 3 находились клоны, которые примерно в восемь раз лучше связывали C3b по сравнению с CRIg дикого типа.
Определение сродства связывания in vitro и биологической активности in vivo
Чтобы определить остатки, особенно важные для увеличения сродства связывания с C3b и активности, при выполнении анализа ингибирования гемолиза, было создано второе поколение вариантов CRIg путем введения доминантной единичной мутации и сохранения в других положениях остатков дикого типа или отбора 2-3 высокоаффинных клонов из библиотек фагов первого поколения, которые были определены при помощи анализа фагов методом ELISA. Для точного измерения сродства и активности мутантов все варианты были экспрессированы в виде выделенных белков. Результаты (таблица 3), полученные в результате выполнения анализа ингибирования гемолиза, показали, что L12 из библиотеки 1, L33 из библиотеки 2 и L41 из библиотеки 4 характеризовались значительным увеличением активности в 4-10 раз по сравнению с клонами дикого типа, использованными при выполнении анализа ингибирования гемолиза. L32 из библиотеки 3 характеризовался 10-кратным увеличением значения IC50 по сравнению с CRIg дикого типа. Полученные данные также показали, что значения сродства связывания и активности, измеренные при помощи клеточных анализов, не были коррелированы.
Комбинация мутантов
На основании результатов, полученных при исследовании библиотек второго поколения, было создано третье поколение мутантов для дальнейшего повышения активности, установленной при выполнении анализа ингибирования гемолиза, и сродства связывания. В качестве матрицы были выбраны три мутанта с наибольшей биологической активностью (L12-8W, L33-Q60I/L32-Q64R и L41-M86Y) и один мутант с самым высоким сродством связывания (L32-Q64R). Затем указанные мутанты были объединены с другими биологически активными клонами, полученными в библиотеках второго поколения, для определения оптимального набора повышающих активность мутаций при выполнении анализа ингибирования гемолиза и сродства связывания. Варианты CRIg были экспрессированы и очищены для проведения детального анализа. Данные показали (таблица 4), что комбинированные мутанты, полученные из L12, не улучшили активность ингибирования и даже характеризовались более низкой активностью по сравнению с исходным мутантом, несмотря на 3-6-кратное увеличение сродства связывания мутантов WL41 и WL59. Среди мутантов, полученных из L32, мутант RL41 характеризовался сродством связания, которое было в 1,8 раза выше, чем в диком типе, и 6-кратным повышением активности при выполнении анализа ингибирования гемолиза. Все мутанты из группы L33 характеризовались значителным увеличением сродства связывания примерно в 27-226 раз по сравнению с диким типом, хотя при этом не произошло значительного повышения активности при выполнении анализа ингибирования гемолиза. Кроме того, было отмечено, что остатки 60I-64R и 86Y присутствовали в большинстве комбинированных клонов с улучшенным сродством связывания.
Улучшенное сродство связывания и повышенная активность ингибирования комплемента мутанта CRIg Q64R M86Y
Для дальнейшего анализа был выбран мутант Q64R M86Y, который характеризовался наибольшим сродством связывания при выполнении конкурентно-связывающего анализа ELISA (фиг. 4 и таблица 3). Для определения сродства связывания CRIg дикого типа и CRIg Q64R M86Y в отношении C3b выполняли анализ Biacore CRIg дикого типа и CRIg Q64R M86Y. Сродство связывания CRIg Q64R M86Y было улучшено в 5 раз по сравнению с CRIg дикого типа (фиг. 6). Предшествующие исследования показали, что CRIg дикого типа избирательно связывается с C3b, но не связывается с нативным С3 (Wiesman et al., Nature, 444(7116):217-20, 2006). Так как мутагенез может изменить указанную избирательность, сравнивали сродство связывания CRIg Q64R M86Y с C3b и С3 при выполнении конкурентно-связывающего анализа в жидкой фазе Alpha Screen. CRIg Q64R M86Y конкурировал с растворимым C3b, но не конкурировал с растворимым С3, из чего следует, что мутагенез не повлиял на избирательность CRIg в отношении активного компонента C3b (фиг. 7). Указанная избирательность была далее подтверждена анализом остатков в структуре CRIg Q64R M86Y в комплексе с C3b (данные отсутствуют).
Для проверки того, что лучшая эффективность является результатом улучшенного сродства связывания и сохраненной избирательности в отношении C3b, CRIg Q64R M86Y и CRIg дикого типа испытывали при выполнении анализа ингибирования гемолиза на основе эритроцитов, который обладает избирательностью в отношении альтернативного пути активации комплемаента. CRIg Q64R M86Y характеризовался 4-кратным увеличением значения IC50 по сравнению с CRIg дикого типа (фиг. 8А). Для дальнейшего подтверждения наличия более высокой активности в отношении ингибирования комплемента альтернативного пути ингибирующую активность CRIg Q64R M86Y сравнивали с CRIg дикого типа при помощи анализа на основе LPS, обладающего избирательностью в отношении альтернативного пути активации комплемента. В данном случае CRIg характеризовался 180-кратным увеличением значения IC50 по сравнению с рекомбинантным белком дикого типа. CRIg дикого типа и CRIg Q64R M86Y не влияли на активацию комплемента в классическом пути. Таким образом, замена двух аминокислот в области связывания CRIg-C3b вызывает образование молекулы с улучшенным сродством связывания и более высокой активностью ингибирования комплемента при выполнении двух разных анализов, обладающих избирательностью в отношении альтернативного пути активации комплемента.
Для дальнейшего определения того, что улучшенное сродство связывания и активность обеспечивают лучшую терапевтическую эффективность, сравнивали защитное действие CRIg дикого типа и варианта Q64R M86Y рецептора CRIg сывороточной модели артрита. Предшествующие исследования показали, что CRIg интенсивно ингибирует воспаление и разрежение кости в случае артрита, индуцированного коллагеном и антителом (Katschke et al., J. Exp. Med. 204(6):1319-1325 (2007)).
Эффективность CRIg испытывали в третьей преклинической модели артрита, опосредованного иммунным комплексом. Спонтанная мышиная модель ревматоидного артрита, К/BxN, имитирует многие клинические и гистологические признаки артрита у человека. В 0-й день мышам инъецировали 50 мкл сыворотки, полученной у мышей, страдающих K/BxN. Состояние животных ежедневно контролировали и степень заболевания оценивали по результатам визуального осмотра. Все мыши были умерщвлены на 6-й день.
Мышам ежедневно подкожно инъецировали указанное количество контрольного изотипа или рекомбинантных белков hCRIg-mIgG1 или hCRIg-RL41-mIgG1 в 100 мкл стерильного физиологического раствора, начиная с 1-го дня.
Мониторинг и оценка:
Оценка для каждой лапы.
0 = Отсутствие эритемы и опухания
1 = Эритема и небольшое опухание, ограниченное средней частью стопы (предплюсной) или голеностопным суставом
2 = Эритема и небольшое опухание от голеностопного сустава до середины стопы
3 = Эритема и умеренное опухание от голеностопного сустава до плюсневых сочленений
4 = Эритема и сильное опухание, охватывающие голеностопный сустав, стопу и пальцы
Средняя оценка = сумма оценок для 4 лап.
Стадии заболевания включают легкую (средняя оценка 1-3), умеренную (средняя оценка 4-8) и тяжелую (средняя оценка 9 и выше) формы заболевания. Средняя оценка соответствует числу пораженных суставов.
На 6-й день перед умерщвлением животных у них брали пробы крови путем внутрисердечной пункции, выполняемой под анестезией. В сыворотке измеряли количество гибридных белков hCRIg-Fc. Суставы собирали для гистологического исследования.
Переливание сыворотки мышей KRN мышам-реципиентам Balb/c вызывало быстрый и устойчивый иммунный ответ, характеризующийся симметричным воспалением суставов. Возникновение артрита опосредовано аутоантителами против глюкозо-6-фосфат-изомеразы, которые образуют провоспалительные иммунные комплексы в суставах (Kouskoff, V., Korganow, A.S., Duchatelle, V., Degott, C., Benoist, C., and Mathis, D. (1996). Organ-specific disease provoked by systemic autoimmunity. Cell 87, 811-822). Прогрессирование артрита полностью зависит от интактного альтернативного пути активации комплемента и функции Fc-рецепторов, о чем свидетельствует отсутствие заболевания у мышей, лишенных компонентов комплемента альтернативного пути, и у мышей, лишенных гамма-цепи Fc-рецептора (Ji, H., Ohmura, K., Mahmood, U., Lee, D.M., Hofhuis, F.M., Boackle, S.A. Takahashi, K., Holers, V.M., Walport, M., Gerard, C., et al. (2002). Arthritis critically dependent on innate immune system players. Immunity 16, 157-168). В связи с быстрым возникновением и тяжестью заболевания лечение гибридным белком CRIg дикого типа - Fc уменьшило оценки артрита только на 22% (фиг. 9А, В). Лечение CRIg Q64R M86Y вызвало снижение оценок артрита на 66%. Гистологическое исследование показало значительное уменьшение инфильтрации иммунокомпетентных клеток, состоящих главным образом из нейтрофилов и макрофагов, у мышей, которым вводили CRIg Q64R M86Y, по сравнению с мышами, которым вводили CRIg дикого типа или контрольный гибридный белок (фиг. 9С, D). Концентрации CRIg дикого типа и CRIg Q64R M86Y в сыворотке были одинаковыми, указывая на то, что различие в оценках артрита не было связано с разным временем полужизни CRIg дикого типа по сравнению с белком CRIg Q64R M86Y. Таким образом, было установлено, что лучшее сродство связывания CRIg с C3b-мишенью является показателем значительно более высокой терапевтической эффективности.
Все патенты и литературные источники, приведенные в настоящем описании изобретения, полностью включены в качестве ссылки.
Несмотря на то, что настоящее изобретение было описано со ссылкой на конкретные варианты осуществления, должно быть понятно, что данное изобретение не ограничено такими вариантами осуществления. Наоборот в объем настоящего изобретения входят разные модификации и эквиваленты, определяемые существом и объемом прилагаемой формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА ПРОТИВ C3b И СПОСОБЫ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ СВЯЗАННЫХ С КОМПЛЕМЕНТОМ НАРУШЕНИЙ | 2008 |
|
RU2473563C2 |
| ПРОФИЛАКТИКА И ЛЕЧЕНИЕ ПАТОЛОГИЧЕСКИХ СОСТОЯНИЙ ГЛАЗ, ВЫЗВАННЫХ КОМПЛЕМЕНТОМ | 2008 |
|
RU2522976C2 |
| ПОЛИПЕПТИДНЫЕ ВАРИАНТЫ С ИЗМЕНЕННОЙ ЭФФЕКТОРНОЙ ФУНКЦИЕЙ | 2005 |
|
RU2367667C2 |
| КОМПОЗИЦИИ ДЛЯ ИНГИБИРОВАНИЯ MASP-2-ЗАВИСИМОЙ АКТИВАЦИИ КОМПЛЕМЕНТА | 2012 |
|
RU2636038C2 |
| УЛУЧШЕННОЕ АНТИ-IGE АНТИТЕЛО (ВАРИАНТЫ) И СПОСОБ УЛУЧШЕНИЯ ПОЛИПЕПТИДОВ | 1998 |
|
RU2242515C2 |
| МОНОКЛОНАЛЬНОЕ АНТИТЕЛО, НАПРАВЛЕННОЕ ПРОТИВ GNA33 ПЕПТИДА, И ЕГО ПРИМЕНЕНИЕ | 2002 |
|
RU2355704C2 |
| АНТИТЕЛА ПРОТИВ ФАКТОРА D И ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2799044C2 |
| МОЛЕКУЛЯРНЫЕ МИМЕТИКИ ЭПИТОПОВ МЕНИНГОКОККА В, КОТОРЫЕ ВЫЗЫВАЮТ ВЫРАБОТКУ ФУНКЦИОНАЛЬНО АКТИВНЫХ АНТИТЕЛ | 2002 |
|
RU2322451C2 |
| СПОСОБ ЛЕЧЕНИЯ ДИССЕМИНИРОВАННОГО ВНУТРИСОСУДИСТОГО СВЕРТЫВАНИЯ КРОВИ ПУТЕМ ИНГИБИРОВАНИЯ MASP-2 ЗАВИСИМОЙ АКТИВАЦИИ КОМПЛЕМЕНТА | 2010 |
|
RU2600876C2 |
| МОЛЕКУЛЫ, СВЯЗЫВАЮЩИЕСЯ С PSL PSEUDOMONAS, И ПУТИ ИХ ПРИМЕНЕНИЯ | 2012 |
|
RU2708977C2 |

































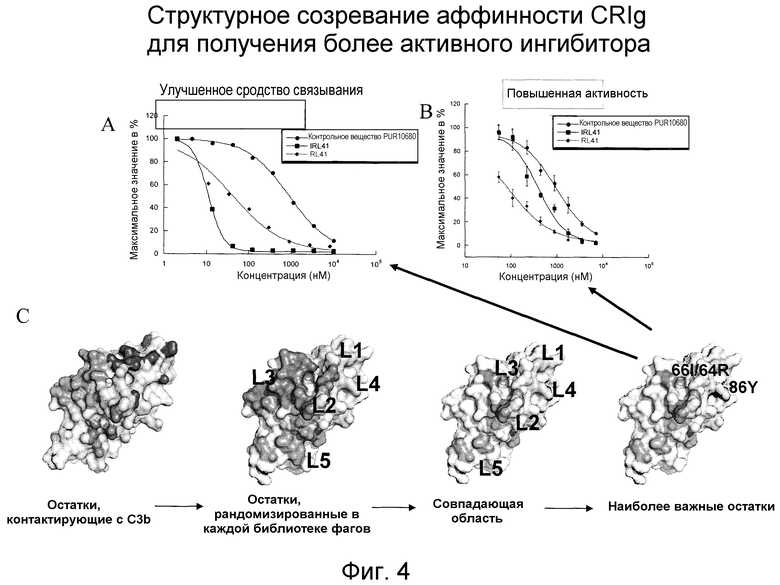
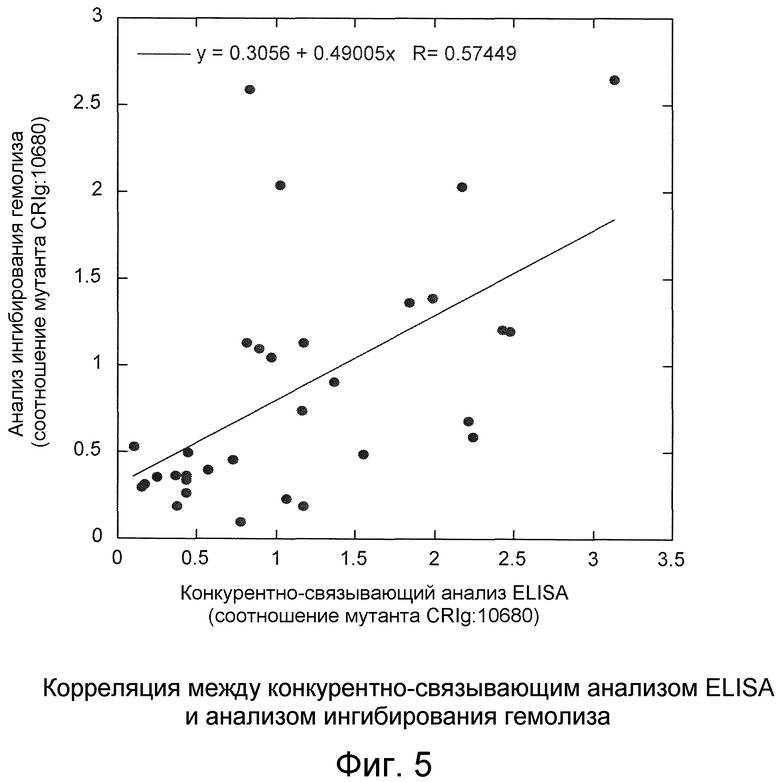
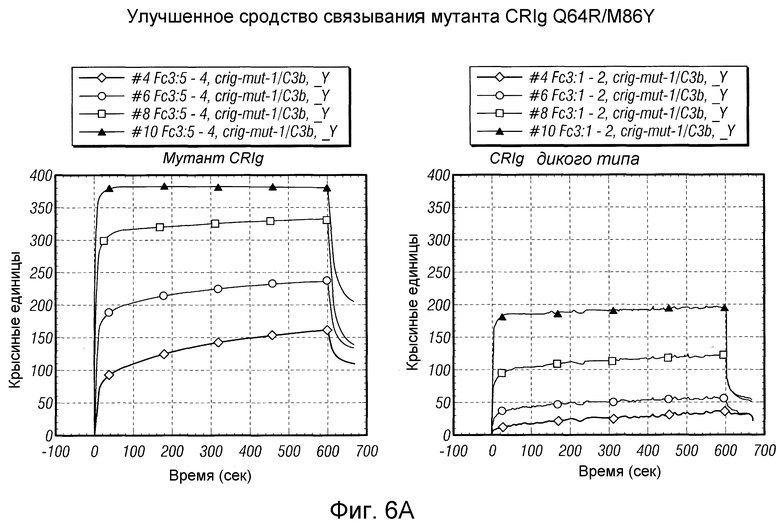

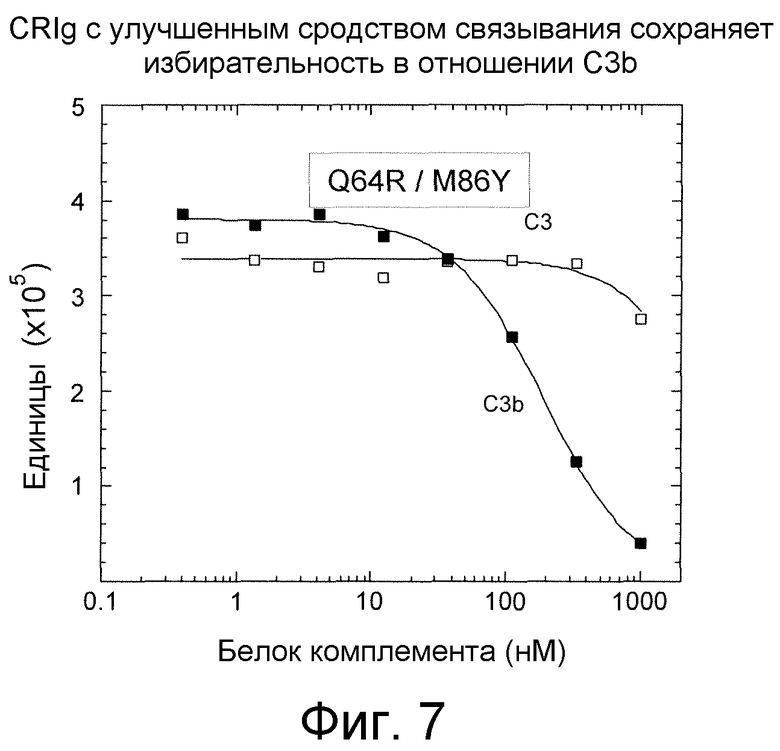
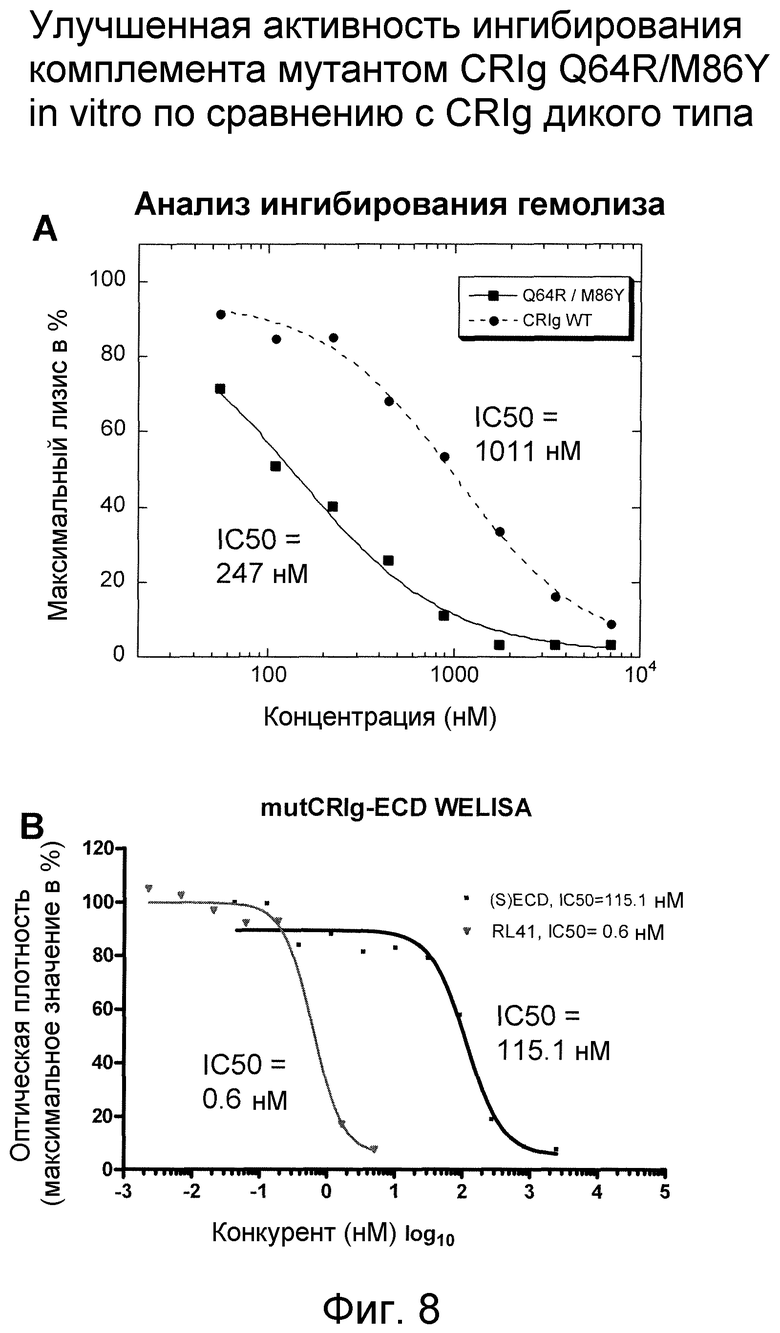
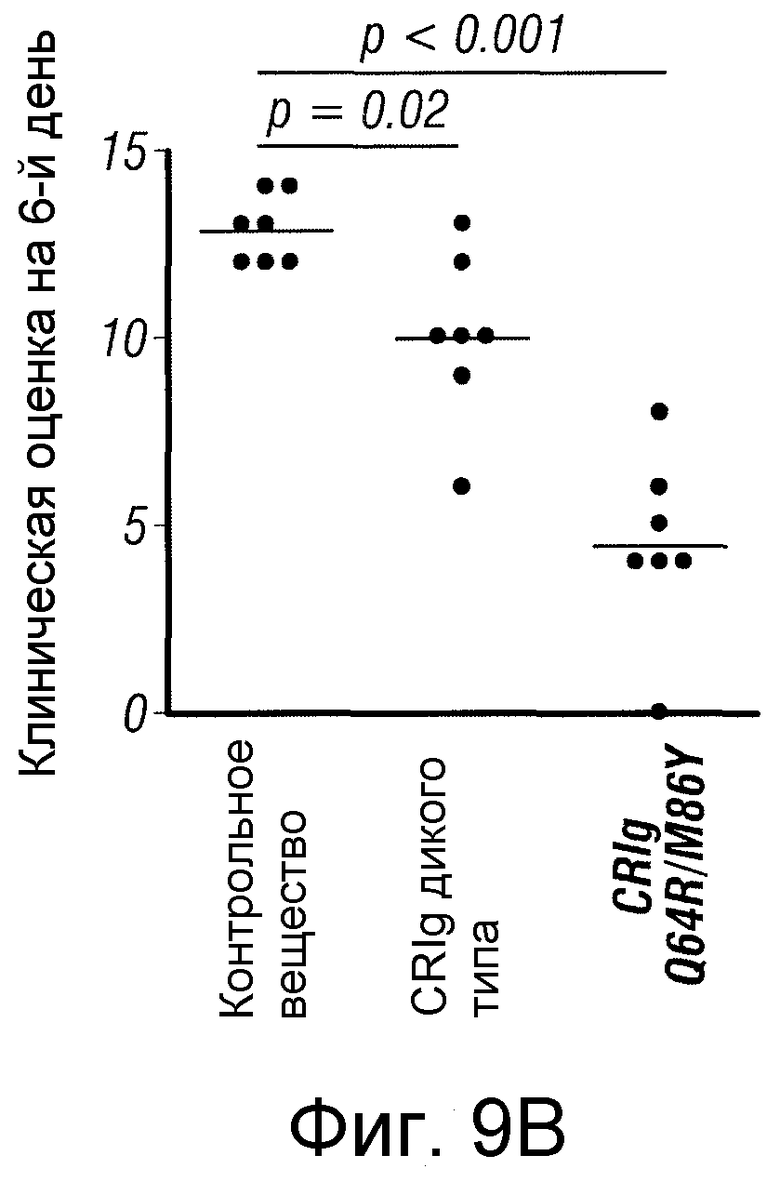
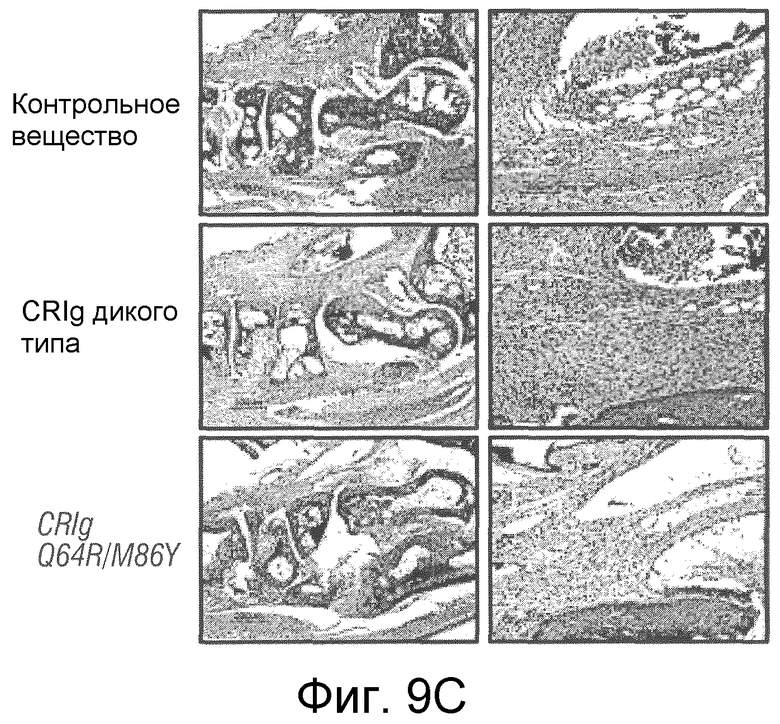
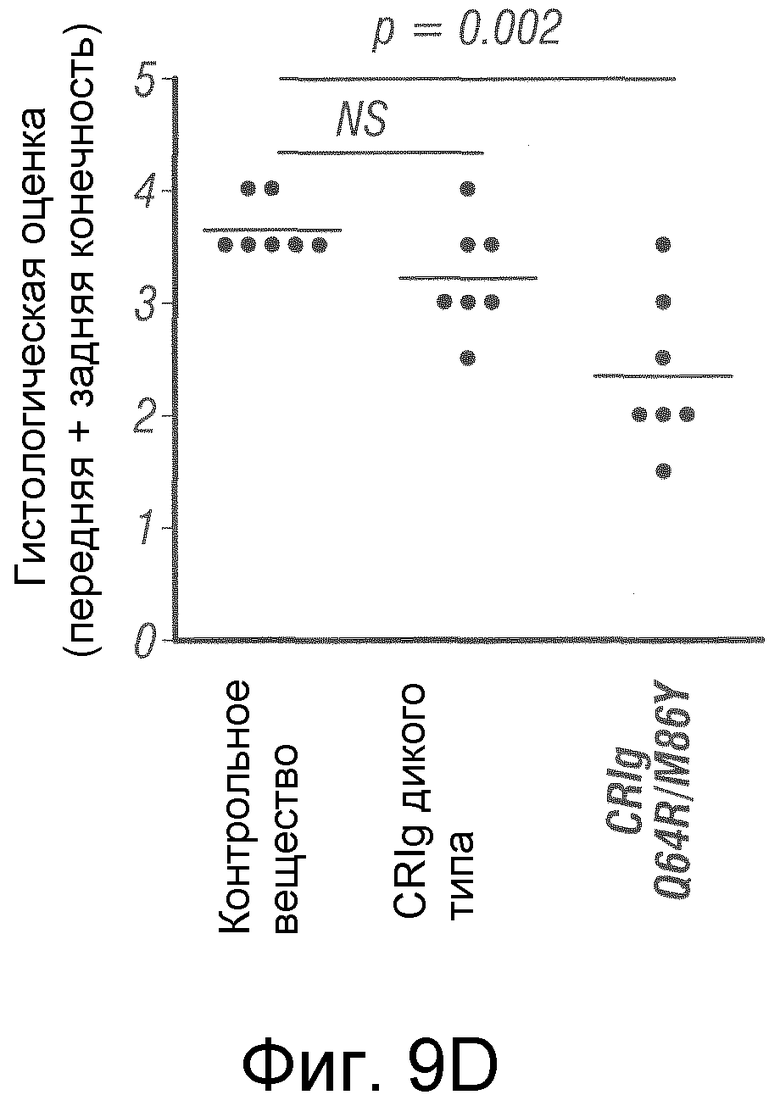
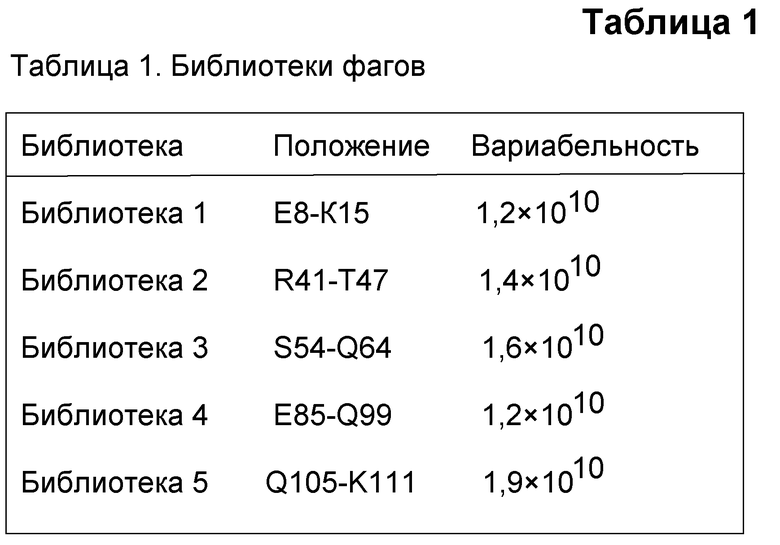
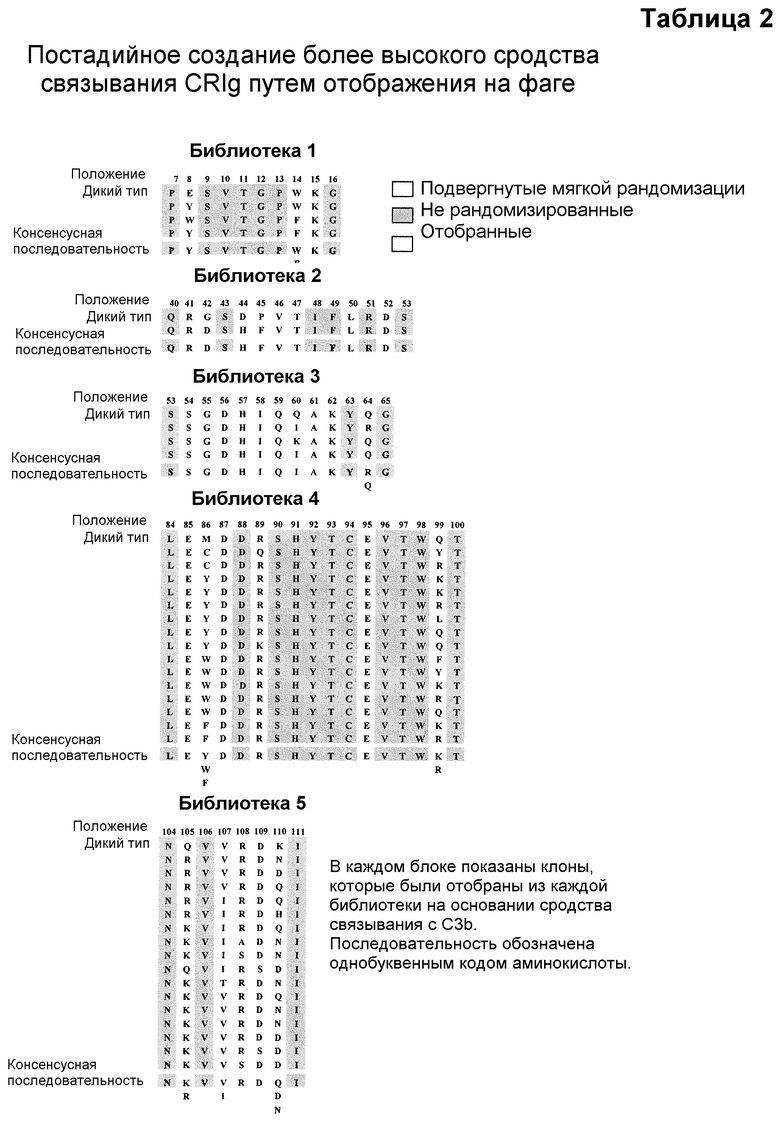
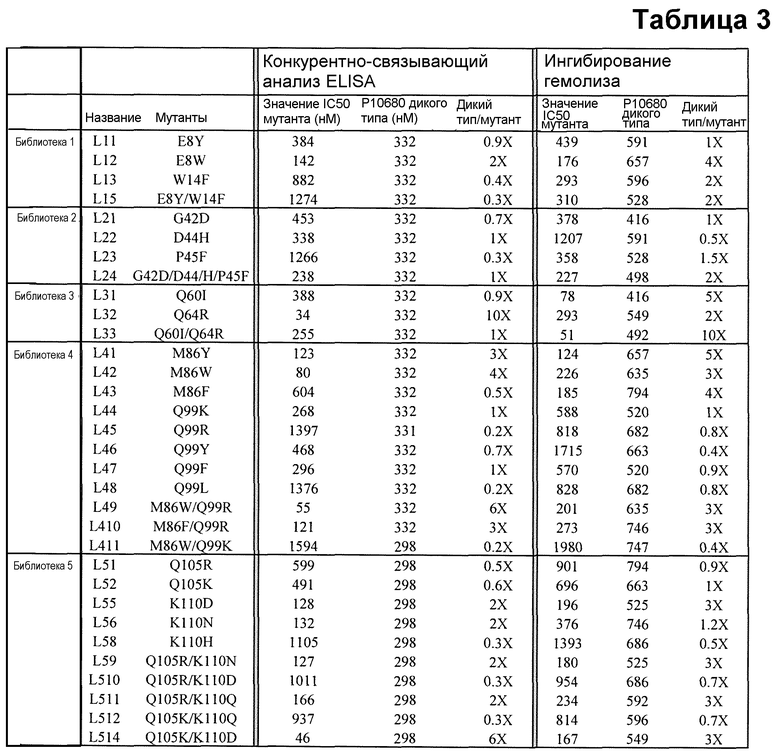
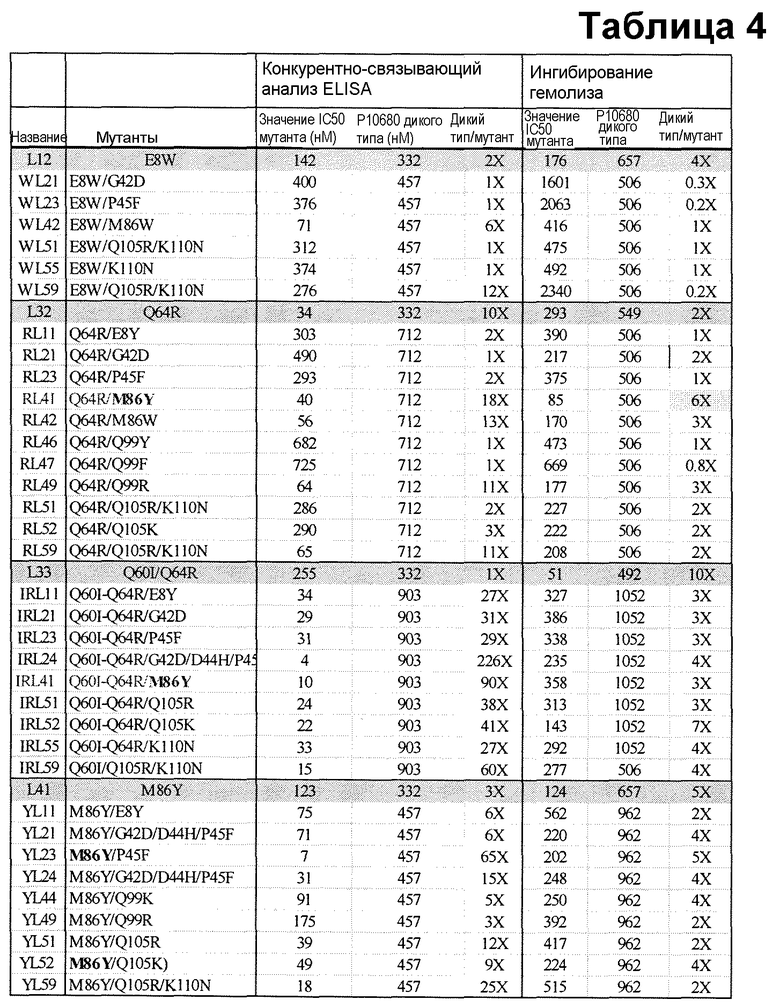
Изобретение относится к области биохимии, в частности к вариантам CRIg с созревшей аффинностью. Заявлен вариант CRIg, который является по меньшей мере в 2 раза более сильным ингибитором альтернативного пути активации комплемента, чем CRIg человека с нативной последовательностью, и необязательно обладает повышенным по меньшей мере в 2 раза сродством связывания с C3b. Также заявлены содержащие указанный вариант CRIg химерная молекула и фармацевтическая композиция. Вариант CRIg может применяться для получения лекарственного средства для лечения комплемент-ассоциированного заболевания или состояния. Изобретение позволяет улучшить терапевтическую эффективность полипептидов CRIg. 4 н. и 13 з.п. ф-лы, 17 ил., 4 табл., 1 пр.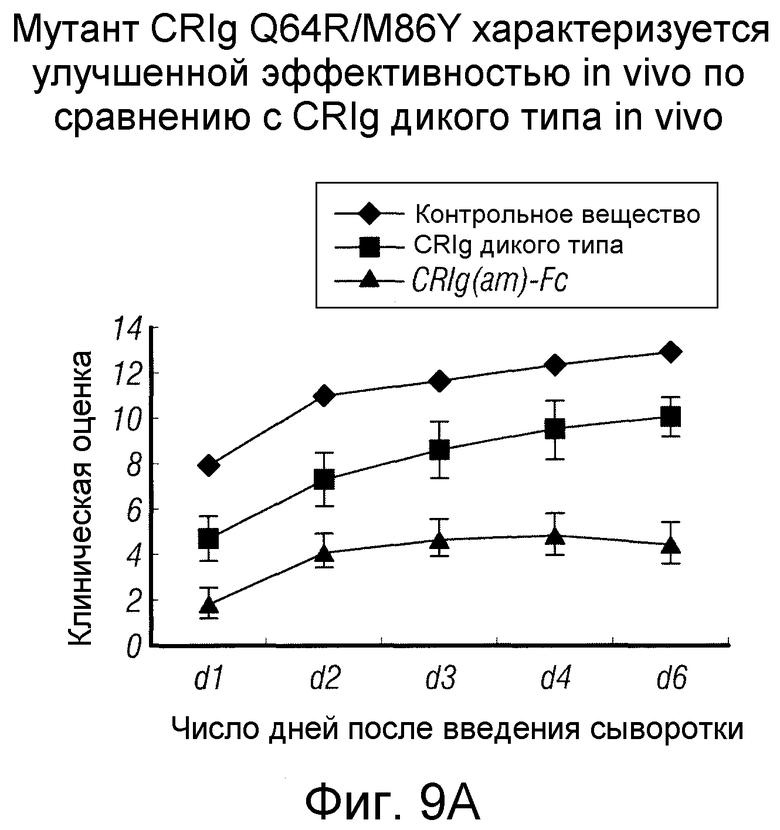
1. Вариант CRIg, включающий замену аминокислот в одном или нескольких положениях аминокислотной последовательности SEQ ID NO:2, или его биологически активный фрагмент, где указанная замена выбрана из группы, состоящей из E8W, W14F, E8Y/W14F, G42D/D44H/P45F, Q60I, Q64R, Q60I/Q64R, M86Y, M86W, M86F, M86W/Q99R, M86F/Q99R, K110D, K110N, Q105R/K110N, Q105R/K110Q, Q105K/K110D, Q64R/M86Y, Q60I/Q64R/E8Y, Q60I/Q64R/G42D, Q60I/Q64R/P45F, Q60I/Q64R/G42D/D44H/P45F, Q60I/Q64R/M86Y, Q60I/Q64R/Q105R, Q60I/Q64R/Q105K, Q60I/Q64R/K110N, Q60I/Q105R/K110N, M86Y/E8Y, M86Y/G42D/D44H/P45F, M86Y/P45F, M86Y/G42D/D44H/P45F, M86Y/Q99K, M86Y/Q99R, M86Y/Q105R, M86Y/Q105K, M86Y/Q105R/K110N, и
где указанный вариант CRIg или его фрагмент является по меньшей мере в 2 раза более сильным ингибитором альтернативного пути активации комплемента, чем CRIg человека с нативной последовательностью SEQ ID NO:2, и необязательно обладает повышенным по меньшей мере в 2 раза сродством связывания с C3b по сравнению с CRIg человека с нативной последовательностью SEQ ID NO:2.
2. Вариант по п.1, который избирательно связывается с C3b или его биологически активным фрагментом по сравнению с С3.
3. Вариант по п.1, в котором сродство связывания увеличено по меньшей мере в 5 раз.
4. Вариант по п.1, в котором сродство связывания увеличено по меньшей мере в 10 раз.
5. Вариант по п.1, в котором сродство связывания увеличено по меньшей мере в 90 раз.
6. Вариант по п.1, включающий замену аминокислот в одном или нескольких положениях 60, 64, 86, 99, 105 и 110 в аминокислотной последовательности SEQ ID NO:2.
7. Химерная молекула, которая является по меньшей мере в 2 раза более сильным ингибитором альтернативного пути активации комплемента, чем CRIg человека с нативной последовательностью SEQ ID NO:2, и необязательно обладает повышенным по меньшей мере в 2 раза сродством связывания с C3b по сравнению с CRIg человека с нативной последовательностью SEQ ID NO:2, включающая вариант по любому из пп.1-6, гибридизированный с другим, гетерологичным полипептидом или аминокислотной последовательностью.
8. Химерная молекула по п.7, представляющая собой иммуноадгезин.
9. Химерная молекула по п.8, в которой указанный вариант CRIg короче, чем непроцессированный CRIg SEQ ID NO:2.
10. Химерная молекула по п.9, включающая внеклеточный домен CRIg.
11. Фармацевтическая композиция для использования при лечении комплемент-ассоциированного заболевания у субъекта, нуждающегося в этом, включающая эффективную концентрацию варианта CRIg по любому из пп.1-6 или иммуноадгезина по любому из пп.8-10 в смеси с фармацевтически приемлемым наполнителем.
12. Композиция по п. 11, где указанный субъект является млекопитающим и где указанное млекопитающее необязательно является человеком.
13. Применение варианта CRIg по любому из пп.1-6 или иммуноадгезина по любому из пп.8-10 при получении лекарственного средства для лечения комплемент-ассоциированного заболевания или состояния.
14. Применение по п.13, в котором указанное комплемент-ассоциированное заболевание:
(i) является воспалительным заболеванием или аутоиммунным заболеванием; или
(ii) выбрано из группы, включающей ревматоидный артрит (RA), респираторный дистресс-синдром у взрослых (ARDS), поражение удаленных тканей после ишемии и реперфузии, активацию комплемента во время хирургической операции с искусственным кровообращением, дерматомиоцитоз, пемфигус, люпус-нефрит и проистекающие из него гломерулонефрит и васкулит, искусственное кровообращение, дисфункцию коронарного эндотелия, вызванную кардиоплегией, мембранозно-пролиферативный гломерулонефрит типа II, IgA-обусловленную нефропатию, острую почечную недостаточность, криоглобулемию, антифосфолипидный синдром, возрастную дегенерацию желтого пятна, увеит, диабетическую ретинопатию, аллотрансплантацию, сверхострое отторжение, гемодиализ, хроническое обструктивное заболевание легких (COPD), астму, аспирационную пневмонию, утрикарию, хроническую идиопатическую уртикарию, гемолитико-уремический синдром, эндометриоз, кардиогенный шок, ишемическую реперфузию и рассеянный склероз (MS); или
(iii) выбрано из группы, включающей воспалительное заболевание кишечника (IBD), системную красную волчанку, ревматоидный артрит, юношеский хронический артрит, спондилоартропатию, системный склероз (склеродерму), идиопатические воспалительные миопатии (дерматомиозит, полимиозит), ксеродерматоз, системный васкулит, саркоидоз, аутоиммунную гемолитическую анемию (иммунную панцитопению, ночную пароксизмальную гемоглобинурию), аутоиммунную тромбоцитопению (идиопатическую тромботическую пурпуру, иммунную тромбоцитопению), тиреоидит (болезнь Грейвса, тиреоидит Хашимото, юношеский лимфоцитарный тиреоидит, атрофический тиреоидит), сахарный диабет, иммунное заболевание почек (гломерулонефрит, тубулоинтерстициальный нефрит), демиелинизирующие заболевания центральной и периферической нервной системы, такие как рассеянный склероз, идиопатическую полиневропатию, желчно-почечные заболевания, такие как инфекционный гепатит (гепатит А, В, С, D, Е и другие негепатотропные вирусы), аутоиммунный хронический активный гепатит, первичный билиарный цирроз печени, грануломатозный гепатит и склерозирующий холангит, воспалительные и фиброзные заболевания легких (например, муковисцидоз), глютензависимую энтеропатию, болезнь Уиппла, аутоиммунные или иммунные кожные заболевания, включающие буллезные кожные заболевания, полиморфную эритему и контактный дерматит, псориаз, аллергические заболевания легкого, такие как эозинофильная пневмония, идиопатический фиброз легких и аллергическая пневмония, заболевания, обусловленные трансплантацией, включающие отторжение трансплантата, реакцию трансплантат-против-хозяина, болезнь Альцгеймера, ночную пароксизмальную гемоглобинурию, наследственный ангионевротический отек, атеросклероз и мембранозно-пролиферативный гломерулонефрит типа II; или
(iv) является ревматоидным артритом (RA); или
(v) является комплемент-ассоциированным глазным заболеванием, где указанное комплемент-ассоциированное глазное заболевание необязательно выбрано из группы, включающей все стадии возрастной дегенерации желтого пятна (AMD), увеит, диабетическую и другие обусловленные ишемией ретинопатии, эндофтальмит и другие внутриглазные заболевания, вызванные образованием новых сосудов, и где внутриглазное заболевание, вызванное образованием новых сосудов, необязательно выбрано из группы, включающей диабетический отек желтого пятна, патологическую миопию, болезнь Гиппеля-Линдау, гистоплазмоз глаза, окклюзию центральной вены сетчатки (CRVO), образование новых сосудов в роговице и образование новых сосудов в сетчатке.
15. Применение по п.14, часть (v), в котором указанное комплемент-ассоциированное глазное заболевание выбрано из группы, включающей возрастную дегенерацию желтого пятна (AMD), образование новых сосудов в сосудистой оболочке глаза (CNV), диабетическую ретинопатию (DR) и эндофтальмит.
16. Применение по п.14, в котором указанная дегенерация желтого пятна (AMD) является влажной дегенерацией желтого пятна.
17. Применение по п.14, в котором указанная дегенерация желтого пятна (AMD) является сухой или атрофической дегенерацией желтого пятна.
| WO 2006042329 A2, 20.04.2006 | |||
| WIESMANN C | |||
| et al., Structure of C3b in complex with CRIg gives insights into regulation of complement activation, Nature, 2006, vol.444, no.9, pp.217-220 | |||
| US 20060002944 A1, 05.01.2006 | |||
| СПОСОБ ТРАНСПЛАНТАЦИИ ЖИВОТНОЙ КЛЕТКИ, ТКАНИ ИЛИ ОРГАНА РЕЦИПИЕНТУ И СРЕДСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1990 |
|
RU2195956C2 |
| KATSCHKE K.J | |||
| Jr | |||
| et al., A novel inhibitor of the alternative pathway of complement reverses inflammation | |||
Авторы
Даты
2015-06-20—Публикация
2009-05-06—Подача