Изобретение относится к области медицины и может быть использовано для предупреждения развития у детей неконтролируемых форм бронхиальной астмы, обусловленных контаминацией биосред тяжелыми металлами: марганцем и ванадием.
Актуальность предлагаемого способа определяется широкой распространенностью бронхиальной астмы в детском возрасте на территориях с повышенной нагрузкой химическими веществами промышленного происхождения. Бронхиальная астма (далее БА) у детей по своей распространенности, тяжести и особенностям течения, несмотря на огромные успехи в ее диагностике и лечении, продолжает оставаться одной из самых актуальных проблем педиатрии. Указанное заболевание за последние полвека продолжает расти и показатель ее распространенности у детей на территории России достигает в настоящее время 8-10%. В связи с этим на современном этапе проблема совершенствования профилактики неконтролируемых форм бронхиальной астмы у детей особенно актуальна, так как клинически такую астму вылечить, даже высокотехнологичными методами, значительно сложнее, чем предупредить.
Принципиальным отличием неконтролируемой, сложно поддающейся терапии, бронхиальной астмы является более выраженное воспаление воздухоносных путей с массивной нейтрофильной и эозинофильной инфильтрацией тканей, приводящее к достоверно более тяжелому клиническому течению болезни. Термин «неконтролируемая БА» подразумевает отсутствие контроля над симптомами болезни по любым причинам.
Особенно важны вопросы разработки и внедрения эффективной профилактики неконтролируемой бронхиальной астмы у детей, проживающих в условиях повышенной химической техногенной нагрузки. Научно доказано, что промышленные токсиканты, особенно тяжелые металлы - марганец, ванадий, вносят существенный негативный вклад в трансформацию инфекционно-аллергических заболеваний органов дыхания, в неконтролируемую бронхиальную астму.
Химиотоксиканты I-II классов опасности неорганической природы оказывают прямое системное токсическое и ферментопатологическое воздействие на детей с респираторными аллергозами. Длительное ирритативное действие на барьерные ткани поддерживает неспецифическое воспаление в бронхо-легочной системе, вызывая формирование иммунопатологических реакций - основы развития бронхиальной астмы. После соединения с белками крови тяжелые металлы сами становятся истинными аллергенами и вызывают дополнительную специфическую сенсибилизацию у детей, потенцируют развитие аутоиммунных процессов в слизистой оболочке бронхов с последующим формированием резистентности к стандартному лечению. Кроме того, промышленные токсиканты повышают иммунологическую агрессивность природных аллергенов.
В настоящее время, в соответствии с рекомендациями GINA (GINA - Global Initiative for Asthma, пересмотр 2011 г.) «Глобальная стратегия лечения и профилактики бронхиальной астмы», выбор базисной медикаментозной терапии зависит от текущего уровня контроля БА и терапии пациента. С точки зрения экспертов GINA, БА считается контролируемой при соблюдении следующих критериев: количество дневных симптомов менее 2 эпизодов в неделю, отсутствие ночных симптомов и пробуждений, ограничений активности, обострений, потребности в препаратах неотложной помощи, наличие не более двух эпизодов БА в неделю, при этом показатели объема форсированного выдоха за первую секунду (ОФВ1) или пиковой скорости выдоха (ПСВ) находятся в пределах нормальных величин.
Для частично контролируемого течения заболевания достаточно наличия любого из вышеперечисленных проявлений БА в течение недели при снижении значений ОФВ1 и ПСВ на 20% и более от должных для данного пациента.
Наличие трех и более признаков частично контролируемой БА в течение недели характерно для неконтролируемой формы болезни [Чучалин А.Г. (ред.) Глобальная стратегия лечения и профилактики бронхиальной астмы, с.16. М.: Атмосфера; 2006].
В качестве базисной терапии рекомендуется назначать комбинацию низких доз ингаляционных глюкокортикостероидов (ИГКС) и β2-агониста длительного действия, альтернативой является монотерапия высокими дозами ИГКС. Кроме того, еще одним вариантом терапии является комбинация низких доз ИГКС с антилейкотриеновым препаратом [Чучалин А.Г. (ред.) Глобальная стратегия лечения и профилактики бронхиальной астмы, с.32. М.: Атмосфера; 2006].
Однако рекомендуемая и проводимая стандартная базовая терапия не всегда является достаточной, и не у всех больных удается добиться контроля над симптомами заболевания, применяя общепринятые схемы лечения глюкокортикостероидами. Существуют фенотипические варианты заболевания, обуславливающие введение концепции «астмы, плохо поддающейся лечению». В свою очередь, возраст - один из наиболее значимых критериев, определяющих фенотип бронхиальной астмы у детей. Выбор базовой терапии, зачастую, основывается только на мнении врача, которое достаточно субъективно, его предпочтениях, наличии опыта работы с определенной группой лекарственных средств. Поэтому в ряде случаев не обеспечивается полный контроль над БА, что чревато переходом ее в НФБА, особенно под воздействием химических токсикантов среды обитания.
Из патента РФ №2445082 известен способ лечения и профилактики неконтролируемых форм бронхиальной астмы, согласно которому пациенту проводят курс базисной терапии GINA сочетанным приемом лекарственных средств: Сальметерола и Флутиказона в соответствии с возрастными дозировками.
Из заявки на патент РФ №95111608 также известен способ профилактики бронхиальной астмы, включающий базисную терапию и дополнительно к ней в качестве профилактического средства назначают, как добавку к пище, напиток янтарной кислоты или ее соли, в частности монокалиевую и кальциевую, по 100 мг 1-3 раза в день. При этом предупреждается или уменьшается частота и тяжесть астматических приступов, облегчается их купируемость.
Данный известный способ эффективен только в отношении неосложненной БА на ранних стадиях ее развития. Основным недостатком данного способа является также и то, что у больных БА всегда присутствует аутосенсибилизация, которая может привести к появлению аллергической реакции на янтарную кислоту или ее соль и вызвать обострение основного заболевания.
Также из патента РФ №2459622 известен способ профилактики бронхиальной астмы у детей с рецидивирующим обструктивным бронхитом в условиях повышенной контаминации биосред тяжелыми металлами и альдегидами путем назначения в период ремиссии сочетанного приема следующих лекарственных средств:
Сингуляр + Энтеросгель + Полиоксидоний, причем курс сочетанного применения указанных лекарственных средств осуществляют не менее 2 раз в гол. Однако этот известный способ предназначен для профилактики обострения первичной БА и не предназначен для профилактики НФБА.
При этом из уровня техники не были выявлены известные способы профилактики у детей развития НФБА, ассоциированных с внешнесредовым воздействием марганца и ванадия, поэтому сделать выбор ближайшего аналога к заявляемому объекту не представляется возможным.
Технический результат, достигаемый предлагаемым изобретением, заключается в обеспечении эффективности предупреждения развития у детей старше 5 лет неконтролируемых форм бронхиальной астмы, связанных с воздействием химических токсикантов - марганца и ванадия, поступающих из атмосферного воздуха и повышения резистентности организма к указанным токсикантам.
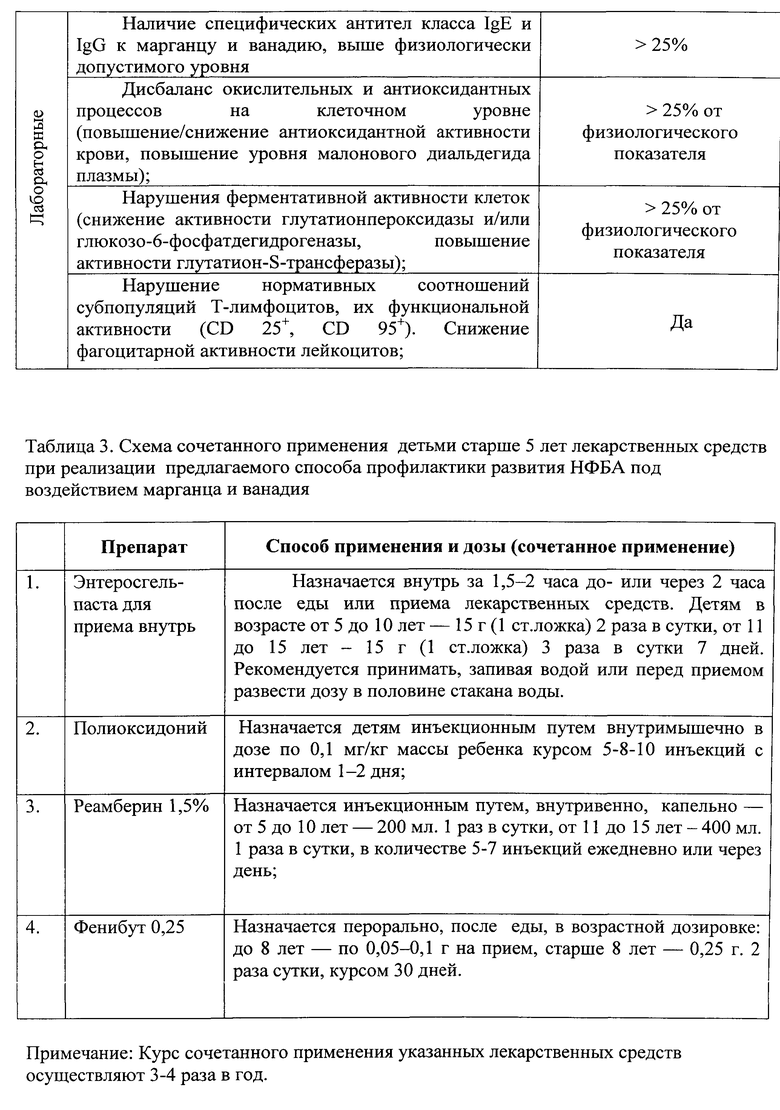
Поставленный технический результат достигается предлагаемым способом профилактики развития у детей старше 5 лет неконтролируемых форм бронхиальной астмы, обусловленных воздействием марганца и ванадия, путем назначения лекарственных средств согласно базисной ступенчатой терапии, при этом новым является то, что осуществляют дополнительное сочетанное применение детьми следующих лекарственных средств: Энтеросгель перорально за 1,5-2 часа до или через 2 часа после еды или после приема лекарственных средств детям в возрасте от 5 до 10 лет - 15 г 2 раза в сутки, от 11 до 15 лет - 15 г 3 раза в сутки курсом 7 дней; Полиоксидоний инъекционным путем внутримышечно в дозе по 0,1 мг/кг массы ребенка инъекций с интервалом 1-2 дня курсом 5-8-10 дней; Реамберин 1,5%-ный раствор инъекционным путем капельно в возрасте от 5 до 10 лет - 200 мл 1 раз в сутки или через день, от 11 до 15 лет - 400 мл 1 раз в сутки или через день, в количестве 5-7 инъекций; Фенибут перорально после еды в возрастной дозировке до 8 лет - по 0,05-0,1 г на прием, старше 8 лет - 0,25 г на прием 2 раза в сутки, курсом 30 дней, причем курс сочетанного применения указанных лекарственных средств осуществляют 3-4 раза в год.
Указанный технический результат достигается за счет следующего.
Для понимания существа вопроса следует пояснить. По результатам идентификации опасности установлено, что на территориях с превышением гигиенических нормативов (предельно-допустимая концентрация - ПДКс.с., содержания марганца и ванадия в атмосферном воздухе) риск развития заболеваний органов дыхания, в том числе бронхиальной астмы, превышает приемлемый уровень (индекс опасности развития заболеваний органов дыхания - от 1,34 до 17,22). Вклад ванадия в хронический индекс опасности развития патологии органов дыхания, в том числе БА, достигает 21-51%, марганца - 29-59%. Установлено наличие достоверной причинно-следственной связи между повышенным содержанием марганца и ванадия в атмосферном воздухе и возникновением у детей аллергических заболеваний органов дыхания (показатель отношения шансов OR=22,04; его доверительный интервал DI=2,25-177,19), при этом риск возникновения данной патологии в 2,6 раза выше, чем у детского населения, находящегося вне зоны влияния исследуемых факторов.
Повышенная частота регистрации БА у детей в условиях несоответствия качества атмосферного воздуха гигиеническим нормативам обусловлена особенностями воздействия марганца и ванадия на функционирование иммунной системы и органов дыхания. После соединения с белками крови марганец и ванадий приобретают свойства аллергенов, вызывают дополнительную специфическую сенсибилизацию, повышают иммунологическую агрессивность причинно-значимых аллергенов (бытовых, пыльцевых, пищевых).
Содержание марганца и ванадия в крови в концентрациях, в 1,5 раза и более превышающих референтные, активирует экспрессию эпителиоцитами бронхиального дерева М-холинорецепторов, повышает функциональную активность лейкотриеновых, H1-гистаминовых и адренергических рецепторов, что усиливает проявления бронхиальной обструкции у детей.
Развитие специфического иммунного воспалительного процесса и бронхиальной констрикции поддерживается индуцированными марганцем нарушениями гомеостаза окислительно-антиоксидантных процессов и энергетического баланса бронхиального эпителия. Активируемые марганцем процессы окислительной деградации клеточных и субклеточных мембран эпителиоцитов в сочетании с торможением фосфорилирования и синтеза АТФ, а также продукции коферментов А и Q на уровне митохондрий сопровождаются повреждением рецепторного аппарата клеток, способствуют нарушению их биокоммуникационной и функциональной активности, снижением регенерационных возможностей респираторного тракта.
У детей, проживающих в условиях хронического аэрогенного воздействия концентраций марганца и ванадия, установлены выраженные нарушения функции внешнего дыхания (ФВД). При риноманометрическом исследовании величина суммарного обструктивного показателя в 1,7 раза ниже, суммарного сопротивления - в 1,3 раза выше группы сравнения; рестриктивные и обструктивные нарушения ФВД при спирографическом исследовании выявляются до 1,6 раза чаще и в 27% случаев имеют выраженный характер.
Помимо прямого иммунотропного, сенсибилизирующего и прооксидантного действия указанных металлов, реализуются и опосредованные эффекты, связанные с расстройствами вегетативной (автономной) регуляции. Для хронического ингаляционного воздействия марганца и ванадия характерны симптомы вегетативной дисфункции с активацией преимущественно парасимпатического звена нервной системы и развитием исходной ваготонии (повышенная саливация и секреция слизи, особенно в ночное время, сужение просвета бронхов, снижение объема дыхательной экскурсии). Кроме того, хроническое воздействие повышенных концентраций марганца и ванадия в крови приводит к развитию морфофункциональных изменений подкорковых ганглиев, прежде всего, стриопалидарной системы, активации двигательного центра и «ассинопсии», что в совокупности реализуется в виде гипертонуса гладкой мускулатуры бронхо-альвеолярного отдела. В двигательном анализаторе возбуждение распространяется не только на корковые зоны синергистов, но и антагонистов, что приводит к ригидности мускулатуры.
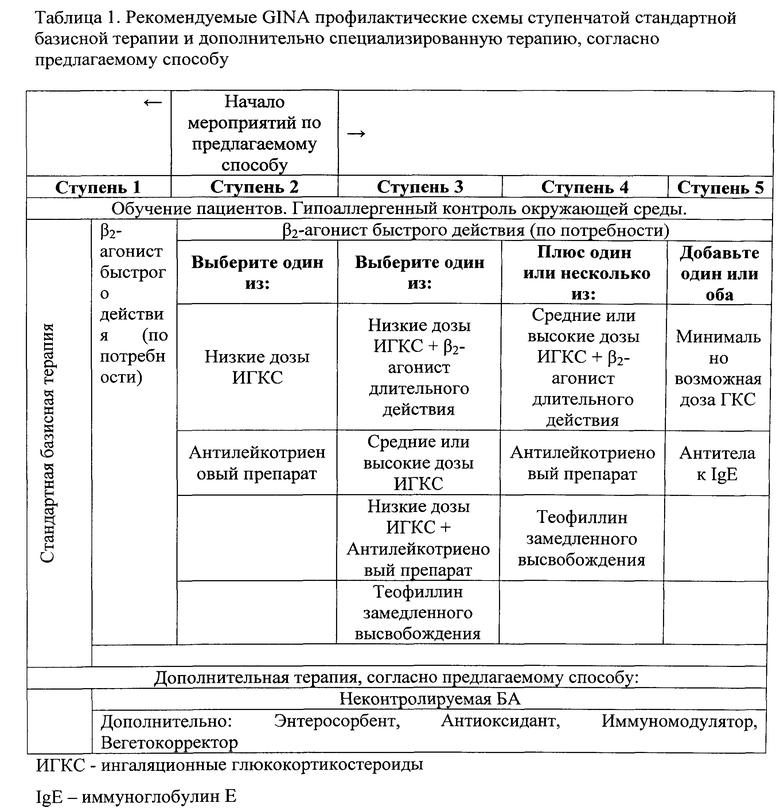
При наличии данных, указывающих на отсутствие контроля над течением БА (неконтролируемая форма бронхиальной астмы), тактика проведения лечебных мероприятий по предлагаемому способу в условиях негативного влияния тяжелых металлов (марганец, ванадий), начинается всегда со ступени 2 GINA и заключается по предлагаемому способу в дополнительном назначении к базисным препаратам, рекомендуемым на этой ступени, медикаментов, обладающих энтеросорбционными, антиоксидантыми, иммуномодулирующими и вегетокорректирующими свойствами. Своевременное назначение патогенетически обоснованных компонентов позволяет добиться контроля над течением БА на более нижних ступенях базисной терапии GINA (т.е. не переходить на более высокие ступени, а наоборот, добившись контроля над БА при реализации заявляемого способа, можно снизить базисную терапию до 1-й ступени), т.е. избежать назначения противоастматических средств, обладающих рядом побочных и нежелательных эффектов. В таблице 1 приведены рекомендуемые GINA профилактические схемы ступенчатой базисной терапии и дополнительно приведена специализированная терапия, согласно предлагаемому способу.
Благодаря сочетанному применению лекарственных средств, рекомендуемых предлагаемым способом, одновременно с использованием базисной терапии, обеспечивается высокая эффективность профилактики неконтролируемых форм бронхиальной астмы у детей, проживающих в условиях экологического неблагополучия.
ЭНТЕРОСГЕЛЬ® (Enterosgelum dulcis), например, в форме сладкой пасты для приема внутрь, 225 г. Международное название - Полиметилсилоксана полигидрат. Фармакотерапевтическая группа: Энтеросорбенты. Регистрационный номер Р N003719/02-28/03/2012. Химический состав: гидрогель метилкремниевой кислоты. Код АТС А07В10С. Энтеросорбирующее, обволакивающее, дезинтоксикационное средство. Обладает выраженными сорбционным и детоксикационным свойствами. В просвете желудочно-кишечного тракта препарат связывает и выводит из организма эндогенные и экзогенные токсические вещества различной природы, включая токсины, антигены, пищевые аллергены, соли тяжелых металлов. Энтеросгель® не уменьшает всасывания витаминов и микроэлементов, способствует восстановлению нарушенной микрофлоры кишечника и не влияет на его двигательную функцию.
ПОЛИОКСИДОНИЙ® (Polyoxidonium®). Фармакологическая группа: Иммуномодуляторы. АТХ: L03 Иммуностимуляторы. Действующее вещество - Азоксимера бромид. Обладает иммуномодулирующим, детоксицирующим, антиоксидантным и мембраностабилизирующим свойствами. Основой механизма иммуномодулирующего действия Полиоксидония является прямое воздействие на фагоцитирующие клетки и естественные киллеры, стимуляция исходно пониженной продукции цитокинов и усиление антителообразования В-лимфоцитами. Полиоксидоний существенно усиливает функциональную активность как факторов врожденного, так и приобретенного иммунитета. При его воздействии регистрируется усиление продукции провоспалительных цитокинов - ИЛ-1, ИЛ-6, ФНО и интерферона. Это способствует увеличению функциональной активности как клеточного, так и гуморального иммунитета. Препарат активирует лимфоидные клетки, находящиеся в бронхах, носовой полости и пазухах, евстахиевых трубах, повышает устойчивость этих органов к инфекционным агентам, восстанавливает иммунные реакции, нарушенные респираторными инфекциями у детей с РОБ. Наряду с иммуномодулирующим действием, полиоксидоний обладает выраженной антиоксидантной активностью в связи с активным подавлением процессов перекисного окисление липидов. Обладая отчетливым дезинтоксикационным действием, полиоксидоний способствует выведению из организма токсинов и солей тяжелых металлов. Код АТХ: L03AX.
«РЕАМБЕРИН®» (REAMBERIN) - действующее вещество меглюмина натрия сукцинат, вспомогательные вещества: натрия хлорид; калия хлорид; магния хлорид; натрия гидроксид; вода. Препарат реамберин представляет собой 1,5% раствор натрий-метилглютаминовой соли янтарной кислоты и сбалансированного набора микроэлементов - натрия, калия, магния. Введенный внутривенно реамберин положительно влияет на оксигенацию клеточной среды, стабилизирует структуру и функциональную активность митохондрий, электролитный обмен на уровне клетки. Дезинтоксикационное средство оказывает антигипоксическое и антиоксидантное действие. Уменьшает продукцию свободных радикалов и восстанавливает энергетический потенциал клеток. Активирует ферментативные процессы цикла Кребса и способствует утилизации жирных кислот и глюкозы клетками, нормализует кислотно-основной состав и газовый состав крови. Код АТХ: В05 ВВ.
«ФЕНИБУТ®» (PHENIBUT) - действующее вещество: аминофенилмасляная кислота. Это вегетокоррегирующее и ноотропное средство, облегчает ГАМК-опосредованную передачу нервных импульсов в центральную нервную систему (ЦНС) (прямое воздействие на ГАМК-рецепторы), оказывает также транквилизирующее, психостимулирующее, антиагрегантное и антиоксидантное действие. Улучшает функциональное состояние мозга за счет нормализации метаболизма тканей и влияния на мозговое кровообращение (увеличивает объемную и линейную скорость мозгового кровотока, уменьшает тонус сосудов мозга, улучшает микроциркуляцию, оказывает антиагрегантное действие). Способствует снижению или исчезновению чувства тревоги, напряженности, беспокойства и страха, нормализует сон, оказывает некоторое противосудорожное действие. Не влияет на холино- и адренорецепторы. Уменьшает проявления астении и вазовегетативные симптомы (в т.ч. головную боль, ощущение тяжести в голове, нарушения сна, раздражительность, эмоциональную лабильность), повышает умственную работоспособность. Улучшает психологические показатели (внимание, память, скорость и точность сенсорно-моторных реакций). При курсовом приеме повышает физическую и умственную работоспособность, улучшает память, нормализует сон; улучшает состояние больных с двигательными и речевыми нарушениями. Код АТХ: N06BX.
Опытным путем было установлено, что только использование комплексной схемы применения вышеуказанных лекарственных препаратов обеспечивает синергизм в достижении поставленного технического результата. Использованием их по отдельности или при схеме из двух, трех средств, не достигается увеличение сроков ремиссии, не обеспечивается максимально возможное воздействие на все звенья патогенеза перехода бронхиальной астмы в неконтролируемую форму.
Кроме того, следует пояснить, что в рамках стандарта GINA оказания медицинской помощи больным с неконтролируемой формой БА предусматривает своевременный переход на более высокие ступени с целью установления контроля над БА, с отменой препаратов лишь при положительных эффектах от назначения противоастматических средств.
При реализации предлагаемого способа осуществляют следующие операции в нижеуказанной последовательности:
1. Производят выбор территории по риску формирования у детей неконтролируемой бронхиальной астмы: промышленно развитые территории с высокой антропогенной нагрузкой, в частности, с высоким содержанием в атмосферном воздухе марганца и ванадия;
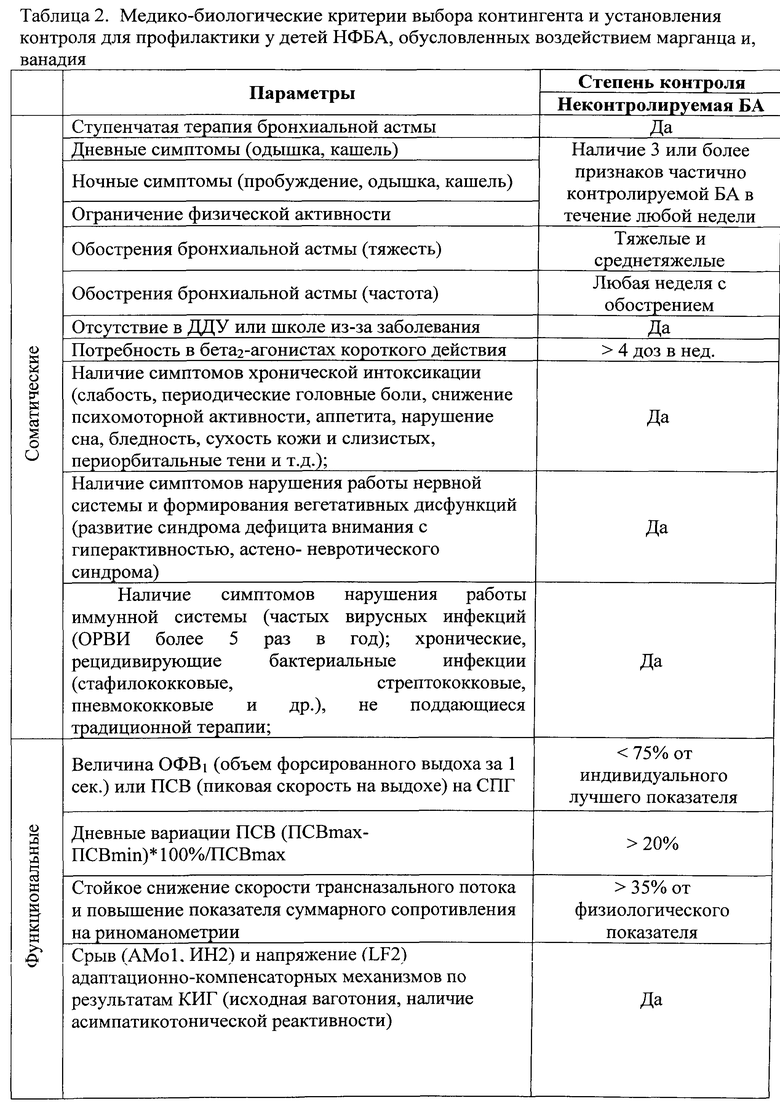
2. Производят отбор больных с этой территории для проведения у них профилактических мероприятий. Модель пациента. Например, дети в возрасте старше 5 лет с наличием бронхиальной астмы устойчивой к проведению стандартной базисной терапии; с превышением референтных концентраций марганца (0,011±0,004 мг/дм3) и ванадия (0,24±0,21 мг/дм3) в крови более чем в 1,5 раза, обусловленных внешнесредовым загрязнением; с наличием специфических антител класса иммуноглобулина Е (IgE) и иммуноглобулина G (IgG) к марганцу и ванадию, выше физиологически допустимого уровня; с наличием сопутствующего патологического процесса со стороны вегетативной нервной системы. О том, что у отобранных детей бронхиальная астма имеет форму неконтролируемой, используют следующие медико-биологические критерии, приведенные в таблице 2.
3. Осуществляют клинико-лабораторное обследование указанных детей: наличие специфических антител класса IgE и IgG к марганцу и ванадию, выше физиологически допустимого уровня; антиоксидантную активность (АОА) крови; уровень малонового диальдегида (МДА) плазмы; активность глутатионпероксидазы и/или глюкозо-6-фосфатдегидрогеназы; активность глутатион-S-трансферазы; уровень Т-лимфоцитов, CD 25+ и CD 95+ - лимфоцитов.
Объем исследований включает показатели, выполненные унифицированными общеклиническими, биохимическими и иммуноферментными методами, позволяющими оценить состояние и функции органов и систем с использованием диагностического оборудования:
- микроскоп лабораторный «Micros MC-200» с диапазоном увеличения до 1600х (Австрия), регистрационный номер МЗ РФ N 2002/801 (фагоцитарная активность лимфоцитов);
- спектрофотометр ПЭ-5300в (Россия, г. С-Петербург) (ОАО Экохим) (антиоксидантная активность крови, малоновый диальдегид);
- анализатор иммуноферментный микропланшетный автоматический «Infinite F50», (Тесап, Австрия) №1008007750 (гидроперекиси липидов, глутатионпероксидаза, глюкозо-6-фосфатдегидрогеназа, глутатион-S-трансфераза);
- анализатор лабораторный иммунологический «ELx808IU», (США) (Biotek) (IgE общий и специфический к марганцу и ванадию);
- атомно-абсорбционный спектрометре компании Perkin Elmer «Analyst-400», регистрационный номер в Государственном реестре №38267-08 (исследование марганца в крови);
- масс-спектрометр с индуктивно-связанной аргоновой плазмой фирмы «Agilent 0077cx» (определение ванадий в крови);
- показатели состояния иммунитета (иммуноглобулины A, M, G) оцениваются методом радиальной иммунодиффузии по Манчини;
- исследование фагоцитоза выполнено методом микроскопии с использованием в качестве объектов фагоцитоза формалинизированных эритроцитов барана (определение процента фагоцитоза, фагоцитарного числа, фагоцитарного индекса, абсолютного количества фагоцитов),
- изучение маркеров клеточной дифференцировки проведено методом проточной цитометрии с определением популяций и субпопуляций лимфоцитов (CD25+, CD95+) на проточном цитометре FACSCalibur фирмы «Becton Dickinson» с использованием универсальной программы CellQuestPrO.
В качестве критериев оценки отклонений лабораторных показателей используются возрастные физиологические уровни, а для содержания марганца и ванадия - референтные уровни (Н. Тиц, 2003).
При выполнении функциональной диагностики для оценки проходимости верхних дыхательных путей используется неинвазивный метод - передняя активная риноманометрия с автоматическим анализом объемно-скоростных показателей носового дыхания.
Исследование функции внешнего дыхания выполняется спирографическим тестом с форсированным выдохом. Для расчета должных величин показателей кривой "поток-объем" используются уравнения регрессии по Knudson (М.П. Анохин, 2003).
Состояние различных звеньев вегетативной нервной системы (ВНС) оценивается на компьютерном кардиокомплексе с помощью программы "Поли-Спектр", основанной на математическом анализе сердечного ритма (P.M. Баевский, 1979; Д. Жемайтите, 1989). Для анализа используются параметры, рекомендуемые кардиоритмографическими стандартами (HRV/Standards of measurements, 1996).
Далее осуществляют математическую обработку доказательной базы оценки эффективности рекомендуемого способа с помощью непараметрических методов статистики с построением и анализом двумерных таблиц сопряженности, метода однофакторного дисперсионного анализа, методов линейного и нелинейного регрессионного анализа. Для оценки достоверности полученных результатов используют критерий Фишера (оценка адекватности моделей), критерий Стьюдента (сравнение групп по количественным признакам), критерий χ2-квадрат (сравнение структуры признаков). Сравнительную оценку вероятностной взаимосвязи между признаками в группах оценивают по показателю отношения шансов (odd ratio - OR) с анализом доверительного интервала (Д1). Различия полученных результатов считают статистически значимыми при р<0,05.
4. Проводят профилактику отобранным в результате вышеприведенного обследования детям старше 5 лет с целью снижения риска развития у них НФБА на территории экологического неблагополучия путем комплексного назначения помимо стандартной базисной терапии четырех лекарственных средств по схеме, приведенной в таблице 3.
Пример конкретного осуществления:
1. Выбор территории проживания. Наиболее значимыми компонентами по вероятности трансформации БА в НФБА являются химические вещества, присутствующие в атмосферном воздухе в концентрациях выше одного ПДК: марганец и его соединения (II класс) в 1,3 раза; ванадий - в 1,2 раза.
2. Исследовано 114 детей с НФБА в возрасте от 5 до 14 лет (из них девочки - 46 чел., мальчики - 68 чел.), находившиеся в течение трех недель на стационарном обследовании и лечении в педиатрическом отделении клиники.
Клинические и анамнестические критерии при отборе детей приведены выше, а также в таблице 2.
У детей с НФБА, обусловленной воздействием аэрозолей соединений марганца и ванадия, доказаны достоверные причинно-следственные связи нарушений иммунного ответа (снижение относительного фагоцитоза и фагоцитарного числа при увеличении концентрации ванадия и марганца в крови, при этом доля дисперсии зависимой переменной составила: R2=0,12-0,39, р<0,05); снижение концентрации IgM при увеличении концентрации марганца в крови (R2=0,81, р<0,05); снижение содержания Ig G и Ig А в сыворотке крови при увеличении концентрации в крови марганца и ванадия (R2=0,11-0,41, р<0,05); увеличение Ig E общего при повышении концентрации марганца (R2=0,22 при р<0,05); снижение пула CD4+, CD25+ и CD95+-лимфoцитoв при увеличении концентрации ванадия), повышение продукции специфических IgG и IgE к ванадию и марганцу (R2=0,31 при р<0,05); увеличение абсолютного количества эозинофилов в крови, эозинофильно-лимфоцитарного индекса (R2=0,37 при р<0,05), дисбаланс окислительных и антиоксидантных процессов (повышение/снижение антиоксидантной активности сыворотки крови, повышение уровня малонового диальдегида плазмы, гидроперекиси липидов, ферментативной активности клеток (активности глутатионпероксидазы и глюкозо-6-фосфатдегидрогеназы, глутатион-S-трансферазы) при увеличении концентрации марганца и ванадия (R2=0,27-0,51, p<0,05).
Установлены достоверные причинно-следственные связи нарушений функциональных показателей: при риноманометрии - обратная корреляционная связь суммарного обструктивного показателя и содержания в крови ванадия (R2=0,52, р=0,04) и прямые корреляционные отношения суммарного сопротивления и содержания в крови марганца (R2=0,47, р=0,01); при спирографии - снижение PEF при повышении в крови марганца и ванадия (R2=-0,058-0,024, р=0,001); при проведении КИТ - исходная ваготония, наличие асимпатикотонической реактивности у более чем 1/3 обследованных детей, срыв (AMo1, ИН2) и напряжение (LF2) адаптационно-компенсаторных механизмов, в причинно-следственной связи с уровнем содержания марганца в крови (R2=0,44-0,60, р=0,05-0,001).
Потенцированное аллергическое воспаление, опосредованное воздействием марганца и ванадия, с развитием общетоксических и прооксидантных эффектов, на фоне вегетативных нарушений являются причинами формирования резистентности к стандартной базисной терапии: снижают эффективность использования нестероидных противовоспалительных средств и ингаляционных глюкокортикоидов, ведут к нарушению контроля над течением бронхиальной астмы, требуют проведения специализированных медико-профилактических мероприятий.
Указанные данные показывают, что отобранные в соответствии с критериями по таблице 2 дети с НФБА характеризуются развитием НФБА, ассоциированными именно с воздействием марганца и ванадия. Поэтому в дальнейшем они и проходили курс профилактики согласно предлагаемому способу, схема реализации которого приведена в таблице 3.
Данные по эффективности профилактики предлагаемым способом детей с НФБА, ассоциированной с марганцем и ванадием, приведены ниже (по данным катамнеза через 12 месяцев):
- наблюдалась положительная динамика клинической симптоматики (обострения протекают преимущественно в легкой форме у 87% детей, дневные и ночные симптомы БА находятся в пределах контроля у 93%, потребность в бета2-агонистах короткого действия, которые требуются в соответствии со стандартной базисной терапией, менее 4 доз в неделю у 98%);
- величина ОФВ1 (объемный форсированный выдох) по данным спирографии более 85% от индивидуального лучшего показателя отмечается у 96% детей, величина суммарного обструктивного показателя и суммарного сопротивления при риноманометрии в пределах возрастной нормы у 95%;
- купирование синдрома вегетативных дисфункций (в т.ч. синдромов дефицита внимания с гиперактивностью и астено-невротического синдромов) у 84% детей;
- наблюдается иммуномодулирующий эффект у 89% обследованных (повышение у 87% детей сниженного уровня Т-лимфоцитов, восстановление фагоцитарной активности лейкоцитов, активация пула CD4+, CD25+ и CD95+-лимфoцитoв, повышение содержания IgG и IgA, снижение продукции Ig E общего и специфических IgG и IgE к ванадию и марганцу у 68% детей);
- произошла нормализация баланса окислительных и антиоксидантных процессов (антиоксидантной активности сыворотки крови, малонового диальдегида плазмы, гидроперекиси липидов) у 78% детей и восстановление ферментативной активности клеток (повышение активности глутатионпероксидазы и глюкозо-6-фосфатдегидрогеназы, нормализация глутатион-8-трансферазы) у 57% детей.
Для доказательства синергизма воздействия в заявляемом способе именно четырех предлагаемых лекарственных средств ниже приводим таблицу 4, отражающую клиническую эффективность в катамнезе (через год) при различных схемах приема лекарств для профилактики НФБА.
Как показали исследования и данные, приведенные в таблице 4, эффект предлагаемого способа не является следствием простого действия используемых препаратов, а имеет место выраженный положительный синергизм лекарственных средств по профилактике развития НФБА у детей старше 5 лет (сумма эффектов отдельных препаратов в тех же дозах дает эффект существенно менее выраженный, чем при сочетанном применении рекомендуемых в заявляемом способе четырех лекарственных средств).
Повысилась резистентность организма к накоплению марганца и ванадия (снижение содержания марганца через 12 мес. на 35-47%, несмотря на то что дети, прошедшие лечение, продолжали проживать в условиях внешнесредового воздействия марганца и ванадия).
Таким образом, предложенный способ сочетанного применения Полиоксидония, Энтеросгеля, Реамберина и Фенибута у детей с НФБА и контаминацией биосред промышленными токсикантами - марганцем и ванадием, не только органично дополняет стандартную базисную схему GINA профилактики развития неконтролируемых форм БА у детей старше 5 лет и способствует значительному снижению риска возникновения таких форм.
Предлагаемый способ может быть рекомендован для профилактики НФБА у детей старше 5 лет, проживающих на индустриально развитых территориях и имеющих повышенный уровень в биосредах токсикантов - марганца и ванадия.

Изобретение относится к области медицины и может быть использовано для предупреждения развития у детей неконтролируемых форм бронхиальной астмы, обусловленных контаминацией биосред тяжелыми металлами: марганцем и ванадием. Сущность способа: дополнительно к базисной ступенчатой терапии дополнительно назначают сочетанное применение детьми следующих лекарственных препаратов: Энтеросгель перорально за 1,5-2 часа до или через 2 часа после еды или после приема лекарственных средств детям в возрасте от 5 до 10 лет - 15 г 2 раза в сутки, от 11 до 15 лет - 15 г 3 раза в сутки курсом 7 дней; Полиоксидоний инъекционным путем внутримышечно в дозе по 0,1 мг/кг массы ребенка инъекций с интервалом 1-2 дня курсом 5-8-10 дней; Реамберин 1,5%-ный раствор инъекционным путем капельно в возрасте от 5 до 10 лет - 200 мл 1 раз в сутки или через день, от 11 до 15 лет - 400 мл 1 раз в сутки или через день, в количестве 5-7 инъекций; Фенибут перорально после еды в возрастной дозировке до 8 лет - по 0,05-0,1 г на прием, старше 8 лет - 0,25 г на прием 2 раза в сутки, курсом 30 дней, причем курс сочетанного применения указанных лекарственных средств осуществляют 3-4 раза в год. Применение изобретения в здравоохранении обеспечивает эффективное предупреждение развития у детей старше 5 лет неконтролируемых форм бронхиальной астмы, связанных с воздействием химических токсикантов - марганца и ванадия, поступающих из атмосферного воздуха. Также изобретение дает возможность повышения резистентности организма к указанным токсикантам. 4 табл.
Способ профилактики развития у детей старше 5 лет неконтролируемых форм бронхиальной астмы, обусловленных воздействием марганца и ванадия, путем назначения лекарственных средств согласно базисной ступенчатой терапии, характеризующийся тем, что осуществляют дополнительное сочетанное применение детьми следующих лекарственных средств: Энтеросгель перорально за 1,5-2 часа до или через 2 часа после еды или после приема лекарственных средств детям в возрасте от 5 до 10 лет - 15 г 2 раза в сутки, от 11 до 15 лет - 15 г 3 раза в сутки курсом 7 дней; Полиоксидоний инъекционным путем внутримышечно в дозе по 0,1 мг/кг массы ребенка инъекций с интервалом 1-2 дня курсом 5-8-10 дней; Реамберин 1,5%-ный раствор инъекционным путем капельно в возрасте от 5 до 10 лет - 200 мл 1 раз в сутки или через день, от 11 до 15 лет - 400 мл 1 раз в сутки или через день, в количестве 5-7 инъекций; Фенибут перорально после еды в возрастной дозировке до 8 лет - по 0,05-0,1 г на прием, старше 8 лет - 0,25 г на прием 2 раза в сутки, курсом 30 дней, причем курс сочетанного применения указанных лекарственных средств осуществляют 3-4 раза в год.
| СПОСОБ ОПТИМИЗАЦИИ АНТИАСТМАТИЧЕСКОЙ ТЕРАПИИ | 2010 |
|
RU2445082C2 |
| НОВЫЕ ГИДАНТОИНОВЫЕ ПРОИЗВОДНЫЕ ДЛЯ ЛЕЧЕНИЯ ОБСТРУКТИВНЫХ ЗАБОЛЕВАНИЙ ДЫХАТЕЛЬНЫХ ПУТЕЙ | 2005 |
|
RU2386629C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ НЕКОНТРОЛИРУЕМОГО ТЕЧЕНИЯ ТЯЖЕЛОЙ БРОНХИАЛЬНОЙ АСТМЫ | 2011 |
|
RU2470582C1 |
| Тузлуков А.П | |||
| Применение микродоз хлористого марганца в лечении больных инфекционно-аллергической формой бронхиальной астмы/А | |||
| П | |||
| Тузлуков | |||
| Сплав для отливки колец для сальниковых набивок | 1922 |
|
SU1975A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
2015-07-10—Публикация
2014-04-29—Подача