Изобретение относится к медицине, а именно к токсикологии, касается способа биохимической идентификации высокотоксичных антихолинэстеразных ядов - О-изопропил-метил-фтор-фосфонат, О-пинаколил-метил-фтор-фосфонат, О-этил-S-диизопропил-аминоэтил-метил-тио-фосфонат, O-изобутил-S-диэтил-аминоэтил, который может быть использован в чрезвычайных ситуациях (аварии на объектах по уничтожению химического оружия) для отождествления указанных опасных для человека ядов.
В настоящее время антихолинэстеразные яды находят широкое применение в медицине, сельском хозяйстве и других областях народного хозяйства. Некоторые из этих химических соединений относятся к первому классу опасности [1], представляют чрезвычайную угрозу жизни и здоровью людей при попадании в окружающую среду и подлежат уничтожению в рамках реализации «Конвенции о запрещении разработки, производства, накопления и применения химического оружия и о его уничтожении» от 13.01.1993 г. К числу таких соединений относятся О-изопропил-метил-фтор-фосфонат, О-пинаколил-метил-фтор-фосфонат, О-этил-S-диизопропил-аминоэтил-метил-тио-фосфонат и O-изобутил-S-диэтил-аминоэтил-метил-тио-фосфонат Возможность идентификации этих опасных высокотоксичных ядов имеет важное практическое значение.
Одним из наиболее чувствительных методов обнаружения антихолинэстеразных ядов является биохимический метод, основанный на использовании холинэстераз. Классическая схема определения антихолинэстеразной активности, используемая в большинстве технических средств, предложена Олдриджем [2] и заключается в предварительном контакте фермента с антихолинэстеразным ядом и последующем измерении каталитической активности холинэстеразы. Его главным недостатком является относительно низкая специфичность. В известном смысле это парадоксально, поскольку принято считать, что чем выше чувствительность метода, тем больше и его специфичность [3, 4].
Дело в том, что высокая чувствительность в случае биохимического метода с использованием холинэстераз, достигающая величин 1·10-7 мг/мл (то есть 1·10-8 %), свидетельствует об очень высокой аналитической избирательности. Но даже в очень чистом растворителе с содержанием основного вещества не менее 99,9% на уровне концентраций 1·10-8 % в качестве примесей присутствует большое количество различных химических соединений [5]. Следовательно, специфичность взаимодействия, например, фермента ацетилхолинэстеразы с ингибиторами указанного фермента очень высока, если из этого набора различных соединений фермент реагирует именно с анализируемым веществом. Поэтому низкая специфичность биохимического метода объясняется не столько аналитическими возможностями используемого фермента, сколько тем, что эти возможности не используются в полной мере.
Аналитический сигнал, получаемый при реализации классического метода выявления антихолинэстеразных ядов и выражаемый в виде степени угнетения или величины остаточной каталитической активности (в % от значения исходной активности или абсолютных величинах активности), является функцией свободного, не связанного с ядом фермента и не несет практически никакой информации о химической природе анализируемого яда. Это объясняется тем, что одна и та же степень угнетения каталитической активности холинэстеразы может быть получена как при контакте фермента с каким-либо антихолинэстеразным пестицидом в концентрации 1·10-5 М или даже с неорганическими соединениями в концентрации 1·10-1 М, так и с высокотоксичными антихолинэстеразными ядами при концентрации 1·10-9 М.
Для увеличения специфичности биохимического метода анализа антихолинэстеразных ядов с использованием холинэстераз предложены его различные варианты, отличающиеся как использованием холинэстераз различного биологического происхождения, так и применением некоторых химических соединений (эффекторов), изменяющих сродство холинэстераз к антихолинэстеразному яду [6].
В качестве эффектора используют, например, хлорид бария. Так, был предложен способ идентификации высокотоксичных антихолинэстеразных ядов при их воздействии на бутирилхолинэстеразу на фоне присутствия хлорида бария и при его отсутствии [7]. Последующее определение отношения констант ингибирования, то есть выявление эффекта присутствия хлорида бария, позволяло судить о наличии в пробе отдельных высокотоксичных антихолинэстеразных ядов.
Известен способ идентификации высокотоксичных антихолинэстеразных ядов, предусматривающий использование в качестве тест-ферментов ацетилхолинзстеразу эритроцитов крови человека и пропионилхолинэстеразу зрительных ганглиев кальмара [8]. Сущность способа заключается в определении ингибирующего эффекта анализируемого раствора, подозрительного на содержание антихолинэстеразного яда, на две холинэстеразы различного биологического происхождения с последующим расчетом отношения констант ингибирования и сравнении полученного результата с табличными значениями, определенными заранее для всех актуальных высокотоксичных антихолинэстеразных ядов.
Существенным недостатком перечисленных способов-аналогов является то, что ни один из них не позволяет идентифицировать все рассматриваемые опасные антихолинэстеразные яды.
Известен способ идентификации антихолинэстеразных ядов, предусматривающий использование четырех холинэстераз различного биологического происхождения - ацетилхолинэстеразы эритроцитов крови человека, бутирилхолинэстеразы сыворотки крови лошади, ацетилхолинэстеразы тлей (злаковой и свекловичной) и холинэстеразы мух, позволяющий идентифицировать актуальные высокотоксичные антихолинэстеразные яды [9]. Данный способ биохимической идентификации антихолинэстеразных ядов наиболее близок по достигаемому техническому результату к заявляемому способу и принят в качестве способа-прототипа.
Недостатки способа-прототипа:
- относительно низкая чувствительность вследствие пониженного сродства ацетилхолинэстеразы тлей и холинэстеразы мух высокотоксичным антихолинэстеразным ядам;
- отсутствие коммерческой доступности ацетилхолинэстеразы тлей и холинэстеразы мух;
- сложность работы с ферментами насекомых.
Целью изобретения является разработка способа биохимической идентификации высоко-токсичных антихолинэстеразных ядов, подлежащих уничтожению в соответствии с Конвенцией, а именно О-изопропил-метил-фтор-фосфоната, О-пинаколил-метил-фтор-фосфоната, О-этил-S-диизопропил-аминоэтил-метил-тио-фосфоната, O-изобутил-S-диэтил-аминоэтил-метил-тио-фосфоната, простого в проведении и эффективного при отождествлении указанных опасных для человека высокотоксичных антихолинэстеразных ядов.
Идентифицирующей характеристикой взаимодействия конкретного высокотоксичного антихолинэстеразного яда с холинэтеразой является бимолекулярная константа скорости взаимодействия ингибитора с ферментом, для расчета которой необходимо знать концентрацию яда. Однако при анализе проб, подозрительных на заражение высокотоксичными антихолинэстеразными ядами, концентрация веществ, в них содержащихся, не известна.
Известно, что бимолекулярная константа скорости реакции взаимодействия фермента с ингибитором в отсутствие (k2) и присутствии субстрата (k2S) рассчитывается по формуле [9]:

где: Аост - остаточная активность фермента после контакта с ингибитором, %;
t - время контакта с ингибитором, мин;
С - концентрация ингибитора, М/л.
При необходимости расчета соотношения k2/k2S (то есть определения защитного эффекта субстрата) при работе с одним и тем же исходным раствором сначала находят разведение пробы, при котором ингибирующий эффект на фермент в присутствии субстрата составляет 25-75%.
Затем после разведения пробы в 10 или 100 раз определяют ингибирующий эффект в отсутствие субстрата. В этой связи для расчета величины отношения констант k2/k2S, то есть для расчета величины защитного эффекта (Р) субстрата, необходимо учитывать только разведение, а знать концентрацию при этом не нужно. Величина отношения констант k2/k2S зависит от химической природы ингибитора и может быть использована для идентификации высокотоксичных антихолинэстеразных ядов.
В связи с изложенным, цель изобретения достигается путем расчета защитного эффекта субстрата ацетилтиохолинйодида на ингибирование ацетилхолинэстеразы эритроцитов крови человека растворами высокотоксичного антихолинэстеразного яда, различающимися по содержанию яда в 10 или 100 раз. Полученное расчетное значение величины защитного эффекта субстрата сравнивают с табличными значениями, полученными заранее для каждого конкретного антихолинэстеразного яда, и при совпадении расчетных значений с табличными делают заключение о том, какой именно яд содержится в пробе.
Пример 1. Порядок реализации заявляемого способа биохимической идентификации высокотоксичных антихолинэстеразных ядов, подлежащих уничтожению согласно Конвенции.
При реализации заявляемого способа к 1,0 мл водного раствора фермента ацетилхолинэстеразы эритроцитов крови человека добавляют 1,0 мл 0,1 М фосфатного буфера (pH 7,5), 0,5 мл водного раствора субстрата ацетилтиохолинйодида в концентрации 5,78 мг/мл, 0,5 мл воды и 1,0 мл анализируемого раствора, содержащего высокотоксичное антихолинэстеразное соединение, а именно О-изопропил-метил-фтор-фосфонат, О-пинаколил-метил-фтор-фосфонат, О-этил-S-диизопропил-аминоэтил-метил-тио-фосфонат или О-изобутил-S-диэтил-аминоэтил-метил-тио-фосфонат. Инкубируют в течение 3 мин при температуре 37°C, а затем добавляют 0,5 мл воды и 0,5 мл водного раствора реактива Эллмана в концентрации 2·10-2 М и сразу измеряют оптическую плотность (D1) против раствора сравнения, отличающегося тем, что вместо 1,0 мл раствора фермента используют 1,0 мл воды. В контрольной пробе вместо анализируемого раствора используют воду. Затем анализируемую пробу разбавляют (в 10 или 100 раз в зависимости от свойств яда) и определяют величину ингибирующего эффекта в отсутствие субстрата. С этой целью к 1,0 мл водного раствора фермента добавляют 1,0 мл дистиллированной воды, 1,0 мл 0,1 М фосфатного буфера (pH 7,5) и 1,0 мл исследуемого раствора, разбавленного в 10 или 100 раз. Инкубируют в течение 3 мин при температуре 37°C, а затем добавляют 0,5 мл раствора Эллмана, 0,5 мл раствора субстрата и через 3 мин измеряют оптическую плотность.
Величину защитного эффекта (Р) рассчитывают по формуле:

где: A1ост и А2ост - остаточная активность фермента, определяемая при инкубации фермента с анализируемой пробой в отсутствие и в присутствии субстрата, соответственно, % от исходного значения;
t1 и t2 - время контакта фермента с ингибитором при определении A1ост и А2ост, соответственно, мин;
K1 и K2 - коэффициенты, учитывающие разбавление пробы при определении A1ост и А2ост, соответственно.
Степень угнетения фермента при определении остаточной активности в отсутствие и в присутствии субстрата должна быть в пределах 25-75%.
Величины Аост рассчитывают по формуле:

где: D - оптическая плотность контрольной пробы;
D1 - оптическая плотность опытной пробы.
Измерения оптической плотности контрольной и опытной проб проводят с использованием спектрофотометра при длине волны 412 нм.
Полученное расчетное значение величины защитного эффекта субстрата (Р) сравнивают с табличными значениями, определенными для O-изопропил-метил-фтор-фосфоната, О-пинаколил-метил-фтор-фосфоната, О-этил-S-диизопропил-аминоэтил-метил-тио-фосфоната, О-изобутил-S-диэтил-аминоэтил-метил-тио-фосфоната, и при совпадении показаний делают заключение о наличии соответствующего ингибитора.
Пример 2. Идентификация высокотоксичных антихолинэстеразных ядов, подлежащих уничтожению в соответствии с Конвенцией, с использованием заявляемого способа.
В ходе эксперимента с использованием заявляемого способа проводили идентификацию опасных высокотоксичных антихолинэстеразных ядов, а именно О-изопропил-метил-фтор-фосфоната, О-пинаколил-метил-фтор-фосфоната, О-этил-S-диизопропил-аминоэтил-метил-тио-фосфоната, О-изобутил-S-диэтил-аминоэтил-метил-тио-фосфоната, для чего заранее экспериментально установили значения величин защитного эффекта (Р) субстрата, приведенные в таблице.
При идентификации О-этил-S-диизопропил-аминоэтил-метил-тио-фосфоната предварительно находили разведение пробы, подозреваемой на содержание указанного высокотоксичного антихолинэстеразного яда, оказывающее ингибирующий эффект на ацетилхолинэстеразу эритроцитов крови человека в присутствии и в отсутствие субстрата в пределах 25-75%. В ходе эксперимента получено значение 70% угнетения, то есть A1ост составляет 30%. Затем пробу необходимо было разбавить в 100 раз и получено значение эффекта угнетения в отсутствие субстрата, равное 45%, то есть А2ост составляет 55%. Время угнетения составило 3 мин.
Расчет величины защитного эффекта (Р) производили с использованием формулы (2):
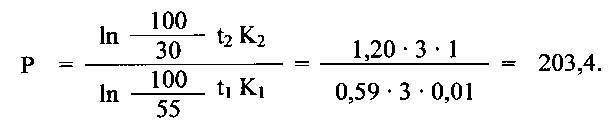
Полученный результат, согласно данных таблицы, свидетельствует о присутствии в пробе высокотоксичного антихолинэстеразного яда - O-этил-S-диизопропил-аминоэтил-метил-тио-фосфоната.
При идентификации О-изопропил-метил-фтор-фосфоната предварительно находили разведение пробы, подозреваемой на содержание данного высокотоксичного антихолинэстеразного яда, оказывающее ингибирующий эффект на ацетилхолинэстеразу эритроцитов крови человека в присутствии и в отсутствие субстрата в пределах 25-75%. В ходе эксперимента получено значение 70% угнетения, то есть A1ост составляет 30%. Затем пробу необходимо было разбавить в 10 раз и получено значение эффекта угнетения в отсутствие субстрата, равное 40%, то есть А2ост составляет 60%. Время угнетения составило 3 мин.
Расчет величины защитного эффекта (Р) производили с использованием формулы (2):
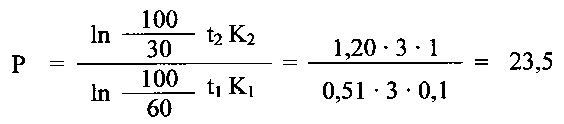
Полученный результат, согласно данным таблицы, свидетельствует о присутствии в пробе высокотоксичного антихолинэстеразного яда - О-изопропил-метил-фтор-фосфоната.
Таким образом, экспериментально доказана возможность идентификации с использованием заявляемого способа опасных высокотоксичных фосфорорганических ядов, подлежащих уничтожению согласно Конвенции:
- О-изопропил-метил-фтор-фосфонат;
- О-пинаколил-метил-фтор-фосфонат;
- О-этил-S-диизопропил-аминоэтил-метил-тио-фосфонат;
- О-изобутил-S-диэтил-аминоэтил-метил-тио-фосфонат.
Заявляемое изобретение удовлетворяет критерию «новизна», так как впервые для идентификации опасных высокотоксичных антихолинэстеразных ядов предложено использовать способ, предусматривающий определение величины защитного эффекта ацетилтиохолинйодида на фермент ацетилхолинэстеразу эритроцитов крови человека при взаимодействии ингибитора с ферментом.
Заявляемое изобретение удовлетворяет критерию «изобретательский уровень», так как в известных и доступных источниках информации, содержащих описания биохимических способов идентификации антихолинэстеразных соединении, нет сведений, указывающих на возможность и целесообразность определения для этой цели защитного эффекта субстрата (ацетилтиохолинйодида) на фермент (ацетилхолинэстеразу эритроцитов крови человека).
Соответствие заявляемого изобретения критерию «пригодность для применения» подтверждается результатами приведенных примеров, показавшими, что предлагаемый способ при простоте его проведения и доступности используемых реактивов и оборудования позволяет идентифицировать широко известные антихолинэстеразные яды, представляющие при попадании в окружающую среду чрезвычайную угрозу жизни и здоровью людей. Заявляемый способ может найти применение в чрезвычайных ситуациях (аварии на объектах по уничтожению химического оружия) для отождествления опасных для человека ядов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЦЕНКИ ТОКСИЧЕСКОЙ ОПАСНОСТИ АНТИХОЛИНЭСТЕРАЗНЫХ СОЕДИНЕНИЙ | 2013 |
|
RU2526817C1 |
| СПОСОБ ДИАГНОСТИКИ ОТРАВЛЕНИЙ МАЛЫМИ ДОЗАМИ ФОСФОРОРГАНИЧЕСКИХ ОТРАВЛЯЮЩИХ ВЕЩЕСТВ | 2012 |
|
RU2484469C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СОЕДИНЕНИЙ АНТИХОЛИНЭСТЕРАЗНОГО ДЕЙСТВИЯ В ВОДЕ И ВОДНЫХ ЭКСТРАКТАХ | 1999 |
|
RU2157850C1 |
| СПОСОБ ПЕРСОНАЛИЗИРОВАННОЙ ДИАГНОСТИКИ ПОРАЖЕННЫХ ТОКСИЧНЫМИ ХИМИКАТАМИ С ИСПОЛЬЗОВАНИЕМ МОБИЛЬНЫХ КОМПЛЕКСОВ | 2020 |
|
RU2748011C1 |
| СПОСОБ ОЦЕНКИ ПЕРСОНИФИЦИРОВАННОЙ ЧУВСТВИТЕЛЬНОСТИ ОРГАНИЗМА К ИНГИБИТОРАМ ХОЛИНЭСТЕРАЗ ПРИ ИССЛЕДОВАНИИ ЭФФЕКТИВНОСТИ И ТОКСИЧНОСТИ АНТИХОЛИНЭСТЕРАЗНЫХ СРЕДСТВ НА ДОКЛИНИЧЕСКОМ УРОВНЕ | 2021 |
|
RU2774587C1 |
| Способ определения фосфорорганических нестицидов в воде | 1985 |
|
SU1359741A1 |
| МАКРОЦИКЛИЧЕСКИЕ АЛКИЛАММОНИЕВЫЕ ПРОИЗВОДНЫЕ 6-МЕТИЛУРАЦИЛА, ОБЛАДАЮЩИЕ АНТИХОЛИНЭСТЕРАЗНОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2534903C1 |
| СОЛИ N,N-ДИМЕТИЛАМИНОЭТИЛ- β -(4-ГИДРОКСИ-3,5-ДИ-ТРЕТБУТИЛФЕНИЛ)ПРОПИОНАТА В КАЧЕСТВЕ ИНГИБИТОРА ХОЛИНЭСТЕРАЗЫ | 1992 |
|
RU2029760C1 |
| ЭКСПРЕСС-СПОСОБ ОПРЕДЕЛЕНИЯ ИНГИБИТОРОВ БУТИРИЛХОЛИНЭСТЕРАЗЫ В ВОДЕ И ВОДНЫХ ЭКСТРАКТАХ | 2019 |
|
RU2704264C1 |
| ГИДРОХЛОРИДЫ ЗАМЕЩЕННЫХ 2-[(ДИМЕТИЛАМИНО)МЕТИЛ]АРИЛДИМЕТИЛКАРБАМАТОВ, ОБЛАДАЮЩИЕ АНТИХОЛИНЭСТЕРАЗНОЙ АКТИВНОСТЬЮ | 2020 |
|
RU2754133C1 |
Изобретение относится к медицине, а именно к токсикологии, и касается способа биохимической идентификации высокотоксичных антихолинэстеразных ядов и может быть использовано в чрезвычайных ситуациях (аварии на объектах по уничтожению химического оружия) для отождествления опасных для человека ядов. Заявляемый способ предусматривает определение ингибирующего влияния раствора высокотоксичного антихолинэстеразного яда на активность холинэстеразы, в качестве которой используют ацетилхолинэстеразу эритроцитов крови человека, в присутствии и в отсутствие субстрата, в качестве которого используют ацетилтиохолинйодид. Ингибирующее влияние раствора высокотоксичного антихолинэстеразного яда на активность ацетилхолинэстеразы эритроцитов крови человека определяют сначала в присутствии субстрата, а затем в отсутствие его. Анализируемую пробу предварительно разводят в 10 или 100 раз для получения ингибирующего эффекта на ацетилхолинэстеразу эритроцитов крови человека в присутствии и в отсутствие субстрата в пределах 25-75%. Затем рассчитывают величину защитного эффекта ацетилтиохолинйодида и сравнивают полученное расчетное значение с табличными значениями, определенными экспериментально заранее для каждого конкретного высокотоксичного антихолинэстеразного яда. При совпадении расчетных значений с табличными делают заключение о наличии в анализируемой пробе соответствующего высокотоксичного антихолинэстеразного яда. 2 пр.
Способ биохимической идентификации высокотоксичных антихолинэстеразных ядов, а именно О-изопропил-метил-фтор-фосфоната, О-пинаколил-метил-фтор-фосфоната, О-этил-S-диизопропил-аминоэтил-метил-тио-фосфоната, О-изобутил-S-диэтил-аминоэтил-метил-тио-фосфоната, посредством определения ингибирующего влияния раствора высокотоксичного антихолинэстеразного яда на активность холинэстеразы, отличающийся тем, что в качестве холинэстеразы используют ацетилхолинэстеразу эритроцитов крови человека и определяют ингибирующее влияние растворов высокотоксичного антихолинэстеразного яда, различающихся по содержанию яда в 10 или 100 раз, на активность ацетилхолинэстеразы эритроцитов крови человека сначала в присутствии субстрата, в качестве которого используют ацетилтиохолинйодид, а затем в отсутствие его, причем величину защитного эффекта ацетилтиохолинйодида Р рассчитывают по формуле:
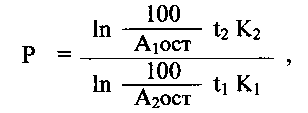
где: A1ост и А2ост - остаточная активность фермента, определяемая при инкубации фермента с анализируемой пробой в отсутствие и в присутствии субстрата, соответственно, % от исходного значения;
t1 и t2 - время контакта фермента с ингибитором при определении A1ост и А2ост, соответственно, мин;
K1 и K2 - коэффициенты, учитывающие разбавление пробы при определении A1ост и А2ост, соответственно,
величины Аост рассчитывают по формуле:
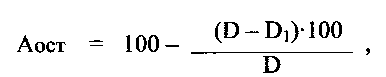
где: D - оптическая плотность контрольной пробы;
D1 - оптическая плотность опытной пробы,
измерения оптической плотности контрольной и опытной проб проводят с использованием спектрофотометра при длине волны 412 нм, затем полученное расчетное значение величины защитного эффекта ацетилтиохолинйодида Р сравнивают с табличными значениями, определенными экспериментально заранее для О-изопропил-метил-фтор-фосфоната, О-пинаколил-метил-фтор-фосфоната, О-этил-S-диизопропил-аминоэтил-метил-тио-фосфоната, O-изобутил-S-диэтил-аминоэтил-метил-тио-фосфоната, и при совпадении показаний делают заключение о наличии соответствующего опасного высокотоксичного антихолинэстеразного яда.
| СПОСОБ ОПРЕДЕЛЕНИЯ СОЕДИНЕНИЙ АНТИХОЛИНЭСТЕРАЗНОГО ДЕЙСТВИЯ В ВОДЕ И ВОДНЫХ ЭКСТРАКТАХ | 1999 |
|
RU2157850C1 |
| СПОСОБ ДИАГНОСТИКИ ОТРАВЛЕНИЙ МАЛЫМИ ДОЗАМИ ФОСФОРОРГАНИЧЕСКИХ ОТРАВЛЯЮЩИХ ВЕЩЕСТВ | 2012 |
|
RU2484469C1 |
| Никольская Е.Б., Моралев С.Н | |||
| Ферментная идентификация ингибиторов холинэстераз // Журнал Эволюционной Биохимии и Физиологии | |||
| Электрическое сопротивление для нагревательных приборов и нагревательный элемент для этих приборов | 1922 |
|
SU1997A1 |
| Способ сопряжения брусьев в срубах | 1921 |
|
SU33A1 |
| Методики определения микроконцентрацией фосфорорганических отравляющих веществ с использованием препаратов холинэстераз из различных биологических источников | |||
| - Пермь, 1978, с.4-14 | |||
| WO 1985004423 A1,10.10.1985 | |||
Авторы
Даты
2015-07-20—Публикация
2014-02-19—Подача