Изобретение относится к области экспериментальной фармакологии и токсикологии, в частности, к способам измерения фармакометрических и токсикометрических характеристик лекарственных средств и физиологически активных веществ с использованием ферментов, и может быть использовано при оценке эффективности и токсичности ингибиторов холинэстераз.
Антихолинэстеразный эффект реализуется за счет биоотклика всего пула сериновых гидролаз организма в ответ на воздействие ингибиторов холинэстераз. Механизмом действия ингибиторов холинэстераз является их обратимое или необратимое связывание с активными центрами ферментов. К основным представителям данной группы ферментов относят ацетил- и бутирилхолинэстераза. Активность ацетилхолинэстеразы относительно постоянна и поэтому не представляет интерес, как механизм потенциальной регуляции антихолинэстеразного эффекта. Выявленные генетические группы по фенотипу активности бутирилхолинэстеразы определяют неоднородную активность фермента и в клинической практике могут определяться по различной ингибирующей способности дибукаина в сыворотке крови (Старостина, В.К., Дегтева, С.А. Холинэстераза: методы анализа и диагностическое значение. Информационно-методическое пособие / В.К. Старостина [и др.]. - Новосибирск: «Вектор-Бест», 2008. - 35 с.).
Вопрос выбора и обоснования селективности антихолинэстеразной терапии является сложным ввиду отсутствия полного понимания необходимости ингибирования обеих эстераз или только ацетилхолинэстеразы. Однако при отсутствии активности бутирилхолинэстеразы (фенотипическая группа с «молчащей» формой фермента) выбор неселективной антихолинэстеразной терапии можно считать нецелесообразным. Обращает на себя внимание актуальность учета активности бутирилхолинэстеразы при оценке эффективности и токсичности антихолинэстеразных средств на доклиническом уровне. Данный подход позволяет персонифицированно подойти к экстраполяции полученных экспериментальных данных на человека и более прогнозируемо подобрать дозу антихолинэстеразных средств при планировании клинических исследований.
Известен способ определения эффективности ингибиторов ацетилхолинэстеразы, согласно которому критерий определен интервалами угнетения ацетилхолинэстеразы, (Куценко С.А. Военная токсикология, радиобиология и медицинская защита / С.А. Куценко [и др.]. - СПб.: Фолиант, 2004. - 528 с.). Также известен способ диагностики эффективности антихолинэстеразных веществ по уровням концентрации ацетилхолинэстеразы крови (Лужников Е. А. Острые отравления / Е.А. Лужников, Л.Г. Костомарова. - М.: Медицина, 1989. - 432 с.). Однако недостатком данных способов является отсутствие учета влияния реакционной способности бутирилхолинэстеразы в пуле сериновых гидролаз, что может исказить результаты оценки антихолинэстеразного эффекта.
Известен способ диагностики эффективности ингибиторов холинэстераз, основанный на определении каталитической активности ацетилхолинэстеразы и арилэстеразы (RU 2484469. Способ диагностики отравлений малыми дозами фосфорорганических веществ Фельд В.Э., Богданов С.Н., Манько Л.М., Плужников Н.Н.). Данный способ позволяет оценить вероятность эффекта малыми дозами ингибиторов холинэстераз без выявления клинических признаков интоксикации. Недостатком данного способа является отсутствие анализа каталитической активности фермента бутирилхолинэстеразы, что может повлечь за собой искажение интерпретации получаемых результатов исследований.
При несомненных достоинствах всех способов ни один из них не предполагает определения индивидуальной эффективности антихолинэстеразных средств. Ближайшим из аналогов является способ, описанный в методическом пособии В.К. Старостиной (Старостина В.К., Дегтева С.А. Холинэстераза: методы анализа и диагностическое значение. Информационно-методическое пособие [Текст] / В.К. Старостина [и др.]. - Новосибирск: Закрытое акционерное общество «Вектор-Бест», 2008. - 35 с.). Указанный способ имеет, несомненно, огромное значение для своевременной постановки правильного диагноза и лечения больных, а также для выявления пациентов, чувствительных к введению антихолинэстеразных препаратов, и имеет основное применение в клинической практике.
Предлагаемый способ предполагает новое применение известного способа для объективной оценки эффективности и токсичности исследуемых ингибиторов холинэстераз с учетом фенотипа по активности бутирилхолинэстеразы на доклиническом уровне конкретным алгоритмом действий, что позволит более персонализировано подойти к подбору доз новых антихолинэстеразных средств на дальнейших этапах исследований и в клинической практике.
Технический результат заключается в том, что применение предлагаемого способа определения персонифицированной чувствительности организма к ингибиторам холинэстераз при оценке их эффективности и токсичности на доклиническом уровне позволит повысить объективность и достоверность интерпретации экспериментальных данных, а также уменьшить трудозатраты при планировании клинических исследований антихолинэстеразных средств.
Способ определения персонифицированной чувствительности организма к ингибиторам холинэстераз при оценке их эффективности и токсичности на доклиническом уровне включает предварительное разделение объектов исследования на фенотипические группы, которые характеризуются различной способностью ингибирования активности бутирилхолинэстеразы дибукаином, согласно предлагаемому техническому решению разделяют выборку животных, используя дибукаиновый тест на фенотипические группы; далее внутримышечно (или другой вид аппликации) вводят исследуемый ингибитор холинэстераз животным из каждой фенотипической группы в дозах, необходимых для определения медианной дозы, и определяют персонифицированную чувствительность фенотипических групп к ингибиторам холинэстераз по критерию угнетения активности ацетилхолинэстеразы одним из колориметрических методов (например, по методу Hestrin); количественную оценку эффективности и токсичности исследуемого ингибитора на исследуемой выборке животных производят, используя метод пробит-анализа, после чего проводят экстраполяцию экспериментальных данных применительно к человеку.
Суть дибукаинового теста заключается в оценке активности бутирилхолинэстеразы с ингибированием и без ингибирования дибукаином in vitro. Дибукаиновый тест представляет собой стандартный набор реактивов, предназначенный для определения in vitro дибукаинового числа посредством автоматического биохимического анализатора Metrolab 2300. В качестве биологического материала используется сыворотка крови биообъектов.
Расчет дибукаинового числа проводится по формуле (1)
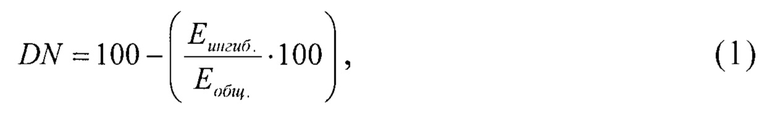
где: DN - значение дибукаинового числа, %;
Еингиб. - значение активности бутирилхолинэстеразы, ингибированной дибукаином, Е⋅л-1;
Еобщ. - значение активности бутирилхолинэстеразы, Е⋅л-1. Диапазон значений дибукаинового числа представлен на таблице 1.

Следующим этапом оценки эффективности антихолинэстеразных средств является введение (внутривенное, подкожное и тд.) модельного препарата экспериментальным животным.
После оценивается активность ацетилхолинэстеразы по методу Hestrin (Hestrin S.J. The reaction of acetilholine and acid derivates with hydroxylamine and analytical application [Текст] / S.J. Hestrin // J. Biol. Chem. - 1949. - V. 180. - №1. - P. 249). Критерий эффекта при определении дозы может быть индивидуален для различных целей исследования.
Дизайн исследования по реализации способа при проведении доклинического исследования модельного препарата с антихолинэстеразной активностью представлен в таблице 2.

Результаты оценки персонифицированной чувствительности организма различных фенотипических групп по бутирилхолинэстеразе (ED50) к исследуемому образцу представлены в таблице 3.
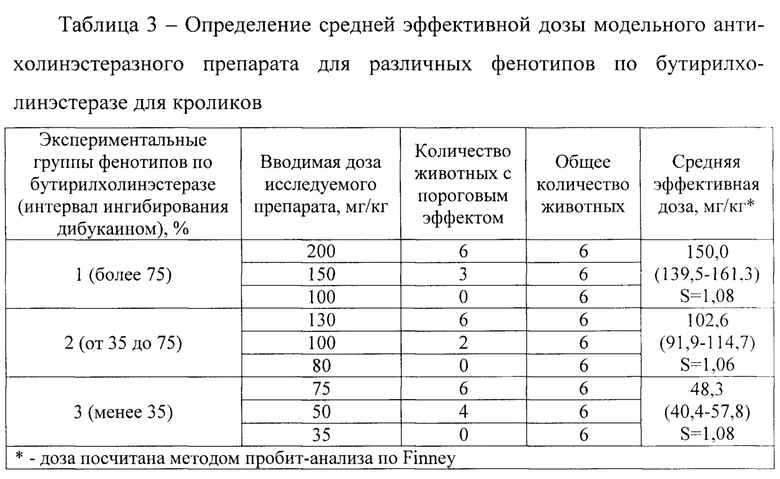
Экстраполяцию экспериментальных данных применительно к человеку осуществляли табличным способом (Estimating the Maximum Safe Starting Dose in Initial Clinical Trials for Therapeutics in Adult Healthy Volunteers. Guidance for Industry, 2005) по формуле (2):
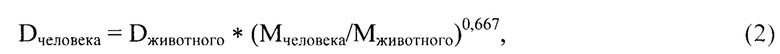
где: Dчеловека - прогнозируемое числовое значение дозы искомой вероятности целевого эффекта для человека, мг/кг;
Dживотного - определенное числовое значение дозы искомой вероятности целевого эффекта для экспериментального животного, мг/кг;
Мчеловека/животного - средняя масса тела человека/животного (для кроликов - 12, для человека - 70), кг.
Результаты прогноза применительно к человеку представлены в таблице 4.
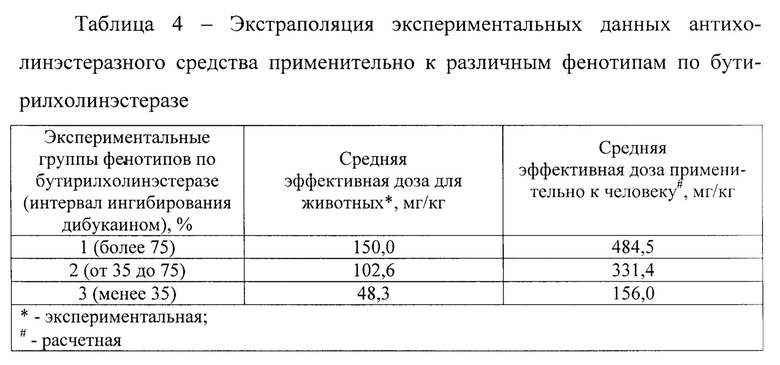
Расчетные дозы исследуемого антихолинэстеразного средства при экстраполяции экспериментальных данных с животных применительно к человеку позволяют более прогнозируемо определить целевой эффект при проведении клинических исследований и в практике терапии нейродегенеративных и других неврологических заболеваний. Персонифицированный подход к определению антихолинэстеразной активности на доклиническом уровне позволяет упростить подтверждение расчетных доз антихолинэстеразных средств для человека, учитывая фенотип по бутирилхолинэстеразе.
Персонифицированное определение токсикометрических характеристик физиологически активных веществ, обладающих антихолинэстеразной активностью, позволяет провести дальнейшие исследования по определению оптимальной эфферентной терапии при отравлениях ингибиторами холинэстераз, учитывая фенотип по бутирилхолинэстеразе.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПЕРСОНАЛИЗИРОВАННОЙ ДИАГНОСТИКИ ПОРАЖЕННЫХ ТОКСИЧНЫМИ ХИМИКАТАМИ С ИСПОЛЬЗОВАНИЕМ МОБИЛЬНЫХ КОМПЛЕКСОВ | 2020 |
|
RU2748011C1 |
| МАКРОЦИКЛИЧЕСКИЕ АЛКИЛАММОНИЕВЫЕ ПРОИЗВОДНЫЕ 6-МЕТИЛУРАЦИЛА, ОБЛАДАЮЩИЕ АНТИХОЛИНЭСТЕРАЗНОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2534903C1 |
| СПОСОБ БИОХИМИЧЕСКОЙ ИДЕНТИФИКАЦИИ ВЫСОКОТОКСИЧНЫХ АНТИХОЛИНЭСТЕРАЗНЫХ ЯДОВ | 2014 |
|
RU2557535C1 |
| СРЕДСТВО НА ОСНОВЕ ПРОИЗВОДНОГО УРАЦИЛА ДЛЯ ТЕРАПИИ БОЛЕЗНИ АЛЬЦГЕЙМЕРА | 2014 |
|
RU2565756C1 |
| ГИДРОХЛОРИД (1-МЕТИЛПИПЕРИДИН-4-ИЛ)-2-ПРОПИЛПЕНТАНОАТА, ОБЛАДАЮЩИЙ ХОЛИНОЛИТИЧЕСКОЙ И ПРОТИВОСУДОРОЖНОЙ АКТИВНОСТЬЮ | 2019 |
|
RU2714135C1 |
| 2,2,2-ТРИФТОР-1-ТРИФТОРМЕТИЛЭТИЛОВЫЙ ЭФИР ЦИКЛОГЕКСИЛКАРБАМИНОВОЙ КИСЛОТЫ В КАЧЕСТВЕ ЭФФЕКТИВНОГО СРЕДСТВА ДЛЯ СЕЛЕКТИВНОГО НЕОБРАТИМОГО ИНГИБИРОВАНИЯ КАРБОКСИЛЭСТЕРАЗЫ | 2011 |
|
RU2449988C1 |
| ПРОИЗВОДНЫЕ ПИРИДОКСИНА С АНТИХОЛИНЭСТЕРАЗНОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2550080C1 |
| ЭКСПРЕСС-СПОСОБ ОПРЕДЕЛЕНИЯ ИНГИБИТОРОВ БУТИРИЛХОЛИНЭСТЕРАЗЫ В ВОДЕ И ВОДНЫХ ЭКСТРАКТАХ | 2019 |
|
RU2704264C1 |
| ГИДРОХЛОРИДЫ ЗАМЕЩЕННЫХ 2-[(ДИМЕТИЛАМИНО)МЕТИЛ]АРИЛДИМЕТИЛКАРБАМАТОВ, ОБЛАДАЮЩИЕ АНТИХОЛИНЭСТЕРАЗНОЙ АКТИВНОСТЬЮ | 2020 |
|
RU2754133C1 |
| ОКСАЛАТ N, N-ДИМЕТИЛ-2-N, N-ДИМЕТИЛАМИНОМЕТИЛПИРИДИЛ-3-КАРБАМАТ, ОБЛАДАЮЩИЙ АНТИХОЛИНЭСТЕРАЗНОЙ АКТИВНОСТЬЮ И СПОСОБНОСТЬЮ УЛУЧШАТЬ КОГНИТИВНЫЕ ФУНКЦИИ | 2007 |
|
RU2339620C1 |
Изобретение относится к медицине, а именно к фармакологии и токсикологии, и может быть использовано для определения персонифицированной эффективной дозы ингибиторов холинэстераз для организма на доклиническом уровне. Проводят предварительное разделение экспериментальных животных на функциональные группы по значению дибукаинового числа по бутирилхолинэстеразе: более 75%, от 35 до 75%, менее 35%. Расчет дибукаинового числа проводят по формуле
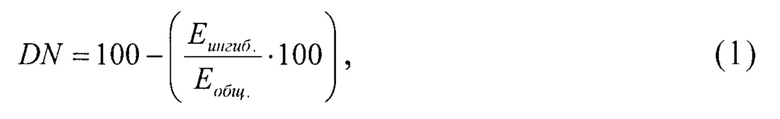
где DN - значение дибукаинового числа, %; Еингиб. - значение активности бутирилхолинэстеразы, ингибированной дибукаином, Е⋅л-1; Еобщ. - значение активности бутирилхолинэстеразы, Е⋅л-1. Далее вводят исследуемый ингибитор холинэстераз экспериментальным животным в соответствии с определенной функциональной группой, начиная со средней дозы Dживотного, согласно табл.3 описания, до достижения целевого эффекта у экспериментального животного – угнетения ацетилхолинэстеразы от 20 до 30%, критерий которого определяют колориметрическим методом. После чего проводят экстраполяцию экспериментальных данных применительно к человеку, рассчитывая эффективную дозу исследуемого ингибитора холинэстераз применительно к человеку по формуле
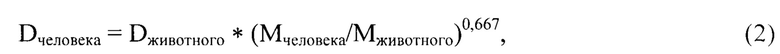
где Dчеловека - прогнозируемое числовое значение дозы искомой вероятности целевого эффекта для человека, мг/кг; Dживотного - определенное числовое значение дозы искомой вероятности целевого эффекта для экспериментального животного, мг/кг; Мчеловека/животного - средняя масса тела человека/животного, кг. Способ обеспечивает возможность повысить объективность и достоверность интерпретации экспериментальных данных, а также уменьшить трудозатраты при планировании клинических исследований антихолинэстеразных средств, за счет объективной оценки эффективности и токсичности исследуемых ингибиторов холинэстераз с учетом функциональных различий по активности бутирилхолинэстеразы на доклиническом уровне с помощью определенного алгоритма действий. 4 табл.
Способ определения персонифицированной эффективной дозы ингибиторов холинэстераз для организма на доклиническом уровне, заключающийся в предварительном разделении экспериментальных животных на функциональные группы по значению дибукаинового числа по бутирилхолинэстеразе: более 75%, от 35 до 75%, менее 35%, причем расчет дибукаинового числа проводят по формуле
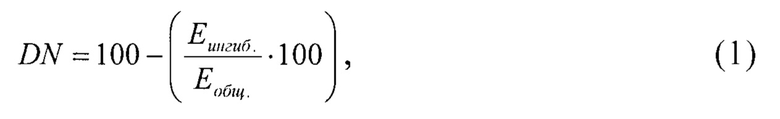
где DN - значение дибукаинового числа, %;
Еингиб. - значение активности бутирилхолинэстеразы, ингибированной дибукаином, Е⋅л-1;
Еобщ. - значение активности бутирилхолинэстеразы, Е⋅л-1;
далее вводят исследуемый ингибитор холинэстераз экспериментальным животным в соответствии с определенной функциональной группой, начиная со средней дозы Dживотного, согласно табл.3 описания, до достижения целевого эффекта у экспериментального животного – угнетения ацетилхолинэстеразы от 20 до 30%, критерий которого определяют колориметрическим методом; после чего проводят экстраполяцию экспериментальных данных применительно к человеку, рассчитывая эффективную дозу исследуемого ингибитора холинэстераз применительно к человеку по формуле
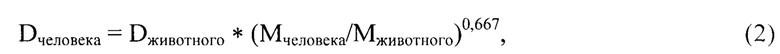
где Dчеловека - прогнозируемое числовое значение дозы искомой вероятности целевого эффекта для человека, мг/кг;
Dживотного - определенное числовое значение дозы искомой вероятности целевого эффекта для экспериментального животного, мг/кг;
Мчеловека/животного - средняя масса тела человека/животного, кг.
| СТЕПАНОВ Я.А | |||
| Потенциальная возможность персонифицированной терапии деменции на основе генетически обусловленной вариабельности активности | |||
| Известия Российской Военно-медицинской академии | |||
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| RU 2018142719 A, 03.06.2020 | |||
| СПОСОБ БИОХИМИЧЕСКОЙ ИДЕНТИФИКАЦИИ ВЫСОКОТОКСИЧНЫХ АНТИХОЛИНЭСТЕРАЗНЫХ ЯДОВ | 2014 |
|
RU2557535C1 |
| СПОСОБ ДИАГНОСТИКИ ОТРАВЛЕНИЙ МАЛЫМИ ДОЗАМИ ФОСФОРОРГАНИЧЕСКИХ ОТРАВЛЯЮЩИХ ВЕЩЕСТВ | 2012 |
|
RU2484469C1 |
| МАХАЕВА Г.Ф | |||
| и др | |||
| Ингибиторы холинэстераз | |||
Авторы
Даты
2022-06-21—Публикация
2021-06-15—Подача