Настоящее изобретение относится к N-сульфатированным олигосахаридам-агонистам системы FGF/FGFR, их получению и применению в терапии.
Ангиогенез представляет собой процесс образования новых капиллярных сосудов. При обструкции кровеносного сосуда ангиогенез, сочетающийся с артериогенезом (укрупнением капилляров), улучшает реваскуляризацию зоны обструкции. In vitro и in vivo показано, что многие факторы роста, такие как Fibroblast Growth Factors (FGF, факторы роста фибробластов), стимулируют процесс неоваскуляризации.
FGF представляют собой группу из 23 членов. FGF2 (или базовый FGF) представляет собой белок массой 18 кДа. FGF2 на уровне эндотелиальных клеток индуцирует в культуре их пролиферацию, миграцию и продуцирование протеаз. In vivo FGF2 благоприятствует явлениям неоваскуляризации. FGF2 взаимодействует с эндотелиальными клетками посредством двух классов рецепторов: рецепторов с высоким сродством к активности тирозинкиназы (FGFR) и рецепторов с низким сродством типа гепарансульфатпротеогликана (HSPG).
Известно, что рецепторы активности тирозинкиназы, находящиеся на поверхности клеток, ассоциируются в виде димера с комплексом, образованным двумя молекулами лиганда, и с молекулой гепарансульфата. Образование данного комплекса позволяет запустить каскад внутриклеточных сигналов, ведущих к активации пролиферации и клеточной миграции, представляющих собой два ключевых процесса, вовлеченных в ангиогенез.
Таким образом, FGF2 и его рецепторы представляют собой очень подходящие цели для терапии, направленной на активацию или ингибирование процессов ангиогенеза.
Синтетические олигосахариды также были объектом исследований взаимодействий с рецепторами FGF и показали свое действие по ингибированию связи FGF-2 с его рецептором на клетках гладких мышц с IC50, равной 16 мкг/мл, а также по ингибированию пролиферации данных клеток, индуцированной посредством FGF-2, с IC50, равной приблизительно 23 мкг/мл (C. Tabeur et al., Bioorg. & Med. Chem., 1999, 7, 2003-2012; C. Noti et al., Chem. Eur. J., 2006, 12, 8664-8686).
В настоящее время заявителями найдены новые синтетические олигосахаридные соединения, способные облегчать образование комплекса FGF/FGFR, благоприятствовать таким образом выживанию эндотелиальных клеток in vitro и увеличивать образование новых сосудов in vitro и in vivo.
Настоящее изобретение относится к новым олигосахаридным соединениям, соответствующим формуле (I):

где
- R1 представляет собой -OSO3 - или гидроксигруппу;
- R2 представляет собой -O-алкил или моносахарид формулы (II), где R представляет собой алкил:
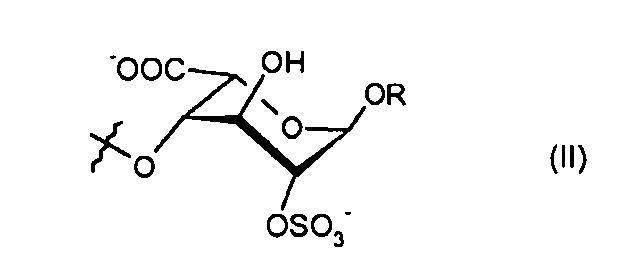
- R3 представляет собой дисахарид формулы (III):
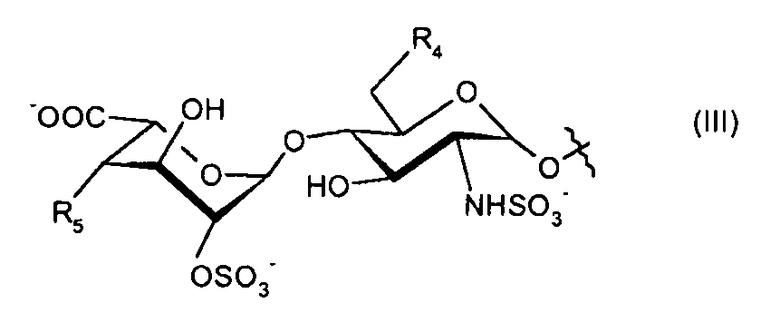
где
- R4 представляет собой -OSO3 - или гидроксигруппу;
- R5 представляет собой дисахарид формулы (IV):

где
- R6 представляет собой -OSO3 - или гидроксигруппу;
- R7 представляет собой гидроксигруппу или дисахарид формулы (VI):

где
- R8 представляет собой -OSO3 - или гидроксигруппу;
- R9 представляет собой гидроксигруппу, или -O-алкил, или дисахарид формулы (VII):

где R10 представляет собой -O-алкил;
при условии, что R9 представляет собой гидроксигруппу или -O-алкил, если R2 представляет собой моносахарид формулы (II), определенной ранее; R7 представляет собой дисахарид определенной ранее формулы (VI), если R2 представляет собой -O-алкил; а R1, R4, R6 и R8 не представляют собой гидроксигруппы одновременно.
В рамках настоящего изобретения, если в тексте не указано иное, под термином "алкил" понимают линейную или разветвленную насыщенную алифатическую группу, содержащую от 1 до 4 атомов углерода. В качестве примеров можно упомянуть метил, этил, пропил, изопропил, бутил, изобутил и трет-бутил. В соединениях по настоящему изобретению, включенных в любую из подгрупп соединений, определенных в последующем далее тексте, алкилы предпочтительно представляют собой метильные группы, за исключением заместителей R9 и R10, в которых алкилы -O-алкильных групп предпочтительно представляют собой пропильные группы.
Соединения по настоящему изобретению представляют собой синтетические олигосахариды, то есть, они являются соединениями, полученными исключительно синтезом, исходя из промежуточных синтонов соответственно приведенному далее подробному описанию. В этом качестве они отличаются от олигосахаридов, полученных деполимеризацией или выделением исходя из сложных смесей полисахаридов типа гепаринов или гепаринов с низкой молекулярной массой. В частности, соединения по настоящему изобретению обладают четко определенной структурой, образующейся при их химическом синтезе, и представляют собой чистые олигосахариды, то есть, свободные от других олигосахаридных соединений.
Настоящее изобретение относится в целом к соединениям формулы (I) в виде кислоты или в виде любой из их фармацевтически приемлемых солей. В виде кислоты группы -COO- и -SO3 - представляют собой -COOH и -SO3H соответственно.
Под фармацевтически приемлемой солью соединения по настоящему изобретению понимают соединение, в котором одна или несколько функциональных групп -COO- или/и -SO3 - связаны ионной связью с фармацевтически приемлемым катионом. Предпочтительными по настоящему изобретению солями являются соли, в которых катион выбран из катионов щелочных металлов и предпочтительно представляет собой катион Na+.
Соединения формулы (I) по настоящему изобретению включают также соединения, в которых один или несколько атомов водорода или углерода замещены их радиоактивными изотопами, например, тритием или углеродом 14C. Такие меченые соединения являются полезными при исследовании метаболизма или фармакокинетики в качестве лигандов в биохимических испытаниях.
В формуле (I) соединений по настоящему изобретению понимают, что:
- моносахарид формулы (II) связан с дисахаридным звеном, соответствующим формуле (I), через атом кислорода, находящийся в положении 4 его звена уроновой кислоты;
- дисахарид формулы (III) связан с дисахаридным звеном, соответствующим формуле (I), через атом кислорода, находящийся в положении 1 его глюкозаминового звена;
- аналогичным образом, дисахарид формулы (IV) связан с дисахаридом формулы (III) через атом кислорода, находящийся в положении 1 его глюкозаминового звена;
- аналогичным образом, дисахарид формулы (VI) связан с дисахаридом формулы (IV) через атом кислорода, находящийся в положении 1 его глюкозаминового звена;
- аналогичным образом, дисахарид формулы (VII) связан с дисахаридом формулы (VI) через атом кислорода, находящийся в положении 1 его глюкозаминового звена.
Под термином "глюкозаминовое звено" понимают моносахаридное звено следующей формулы:

Другой тип сахаридных звеньев, содержащихся в соединениях по настоящему изобретению, представляет собой уроновую кислоту и более точно идуроновую кислоту, соответствующую следующей формуле:
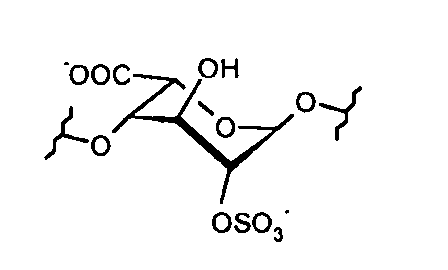
Таким образом, соединения формулы (I) по настоящему изобретению также могут быть представлены приведенной далее формулой (I'), в которой чередуются идуроновые и глюкозаминовые звенья, а R1, R2, R4, R6 и R7 имеют определенные ранее значения:

Таким образом, в зависимости от значений R2 и R7 олигосахариды по настоящему изобретению могут содержать от 7 до 10 сахаридных звеньев.
Среди соединений формулы (I)/(I'), являющихся объектами настоящего изобретения, можно упомянуть соединения, в которых:
- R1, R3, R4, R5 и R6 имеют определенные ранее значения;
- R2 представляет собой моносахарид формулы (II), определенной ранее;
- R7 представляет собой гидроксигруппу.
Такие соединения представляют собой гептасахариды. Они соответствуют приведенной далее формуле (I-1), в которой R7 представляет собой гидроксигруппу, а R, R1, R4 и R6 имеют определенные ранее значения, и находятся в виде кислоты или в виде любой из их фармацевтически приемлемых солей.
Среди соединений формулы (I)/(I'), являющихся объектами настоящего изобретения, можно упомянуть подгруппу соединений, в которых R2 представляет собой -O-алкил.
Такие соединения представляют собой октасахариды или декасахариды. Они соответствуют приведенной далее формуле (I-2), в которой R1, R4, R6, R8 и R9 имеют определенные ранее значения, а R2 представляет собой -O-алкил, и находятся в виде кислоты или в виде любой из их фармацевтически приемлемых солей.
Среди соединений формулы (I)/(I'), являющихся объектами настоящего изобретения, можно назвать подгруппу соединений, в которых:
- R2 представляет собой -O-алкил;
- R7 представляет собой дисахарид определенной ранее формулы (VI), в которой R9 представляет собой дисахарид формулы (VII), определенной ранее.
Такие соединения представляют собой декасахариды. Они соответствуют приведенной далее формуле (I-3), в которой R1, R4, R6, R8 и R10 имеют определенные ранее значения, и находятся в виде кислоты или в виде любой из их фармацевтически приемлемых солей.

Среди соединений формулы (I), являющихся объектами настоящего изобретения, можно назвать подгруппу соединений, в которых:
- R2 представляет собой -O-алкил; и
- R7 представляет собой дисахарид определенной ранее формулы (VI), в которой R9 представляет собой гидроксигруппу или -O-алкил.
Такие соединения представляют собой октасахариды и соответствуют определенной ранее формуле (I-2), в которой R1, R4, R6 и R8 имеют определенные ранее значения, R2 представляет собой -O-алкил, а R9 представляет собой гидроксигруппу или -O-алкил.
В октасахаридах по настоящему изобретению R9 предпочтительно представляет собой -O-алкил.
Другие подгруппы соединений по настоящему изобретению могут иметь несколько характеристик, указанных ранее для каждой из определенных ранее подгрупп.
Настоящее изобретение относится, в частности к следующим олигосахаридам:
- метил-(4-O-пропил-2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-[(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил-(1→4)]2-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозид (№ 1);
- метил-(4-O-пропил-2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-[(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил-(1→4)]3-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозид (№ 2);
- [метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-[(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)]2-2-O-натрийсульфонато-α-L-идопиранозид]уронат натрия (№ 3);
- метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозид (№ 4);
- метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозид (№ 5);
- метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозид (№ 6);
- метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозид (№ 7);
- метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-[(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)]2-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-6-O-натрийсульфонато-2-(сульфонато)амино-α-D-глюкопиранозид (№ 8);
- метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонато)амино-α-D-глюкопиранозил)-[(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)]2-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозид (№ 9).
Принципиально в способе получения соединений по настоящему изобретению используют основные синтоны ди- или олигосахаридов, полученные соответственно приведенным ранее литературным источникам. В частности, можно сослаться на патенты или заявки EP 0 300 099, EP 0 529 715, EP 0 621 282 и EP 0 649 854, а также на публикацию C. Van Boeckel и M. Petitou в Angew. Chem. Int. Ed. Engl., 1993, 32, 1671-1690. Затем такие синтоны сочетают друг с другом таким образом, чтобы получить полностью защищенный эквивалент соединения по настоящему изобретению. Затем этот защищенный эквивалент превращают в соединение по настоящему изобретению. В указанных реакциях сочетания ди- или олигосахарид-"донор", активированный по своему аномерному углероду, взаимодействует с ди- или олигосахаридом-"акцептором", обладающим свободной гидроксигруппой.
Таким образом, настоящее изобретение относится к способу получения соединений формулы (I)/(I'), отличающемуся тем, что:
- на первой стадии синтезируют полностью защищенный эквивалент требуемого соединения (I);
- на второй стадии вводят группы -COO- и -OSO3 - и/или снимают с них защиту;
- на третьей стадии снимают защиту со всего соединения;
- на четвертой стадии вводят N-сульфатные группы.
Синтез полностью защищенного эквивалента требуемого соединения (I) осуществляют по реакциям, хорошо известным специалистам в данной области техники, используя способы синтеза олигосахаридов (например, G.J. Boons, Tetrahedron (1996), 52, 1095-1121 и заявки WO 98/03554 и WO 99/36443), в которых олигосахарид-донор гликозидной связи сочетают с олигосахаридом-акцептором гликозидной связи для получения другого олигосахарида, представляющего собой совокупность двух реагентов. Данную последовательность повторяют до получения соединения формулы (I)/(I') при необходимости в защищенном виде. Природу и профиль заряда требуемого конечного соединения определяет природа химических звеньев, использованных на различных стадиях синтеза, согласно правилам, хорошо известным специалистам в данной области техники. Можно сослаться, например, на C. Van Boeckel et M. Petitou, Angew. Chem. Int. Ed. Engl. (1993), 32, 1671-1690 или также на H. Paulsen, "Advances in selective chemical syntheses of complex oligosaccharides", Angew. Chem. Int. Ed. Engl. (1982), 21, 155-173.
Соединения по настоящему изобретению могут быть получены с использованием различных стратегий, известных специалистам в области синтеза олигосахаридов. Способ, описанный ранее, представляет собой предпочтительный способ по настоящему изобретению. Тем не менее, соединения формулы (I)/(I') могут быть получены другими способами, хорошо известными в химии сахаров и описанными, например, в "Monosaccharides, their chemistry and their roles in natural products", P.M. Collins et R.J. Ferrier, J. Wiley & Sons (1995), и G.J. Boons в Tetrahedron (1996), 52, 1095-1121.
Защитные группы, используемые в способе получения соединений формулы (I)/(I'), представляют собой группы, которые позволяют, с одной стороны, защищать реакционно-способную функциональную группу, такую как гидрокси- или аминогруппа, в ходе синтеза, а с другой стороны, восстанавливать реакционно-способную функциональную группу в исходном виде в конце синтеза. Для осуществления способа по настоящему изобретению используют защитные группы, традиционно используемые в химии сахаров, такие как описанные, например, в "Protective Groups in Organic Synthesis", Green et al., 3rd Edition (John Wiley & Sons, Inc., New York). Защитные группы выбирают, например, из таких групп, как ацетил, галогенметил, бензоил, левулинил, бензил, аллил, трет-бутилдифенилсилил (tBDPS).
Также могут быть использованы активирующие группы; речь идет о группах, традиционно используемых в химии сахаров, например, согласно G.J. Boons, Tetrahedron (1996), 52, 1095-1121. Такие активирующие группы выбирают, например, из имидатов и тиогликозидов.
Способ, описанный ранее, позволяет получать соединения по настоящему изобретению в виде солей и предпочтительно в виде солей натрия. Для получения соответствующих кислот соединения по настоящему изобретению в виде солей могут быть приведены в контакт с катионообменными смолами в кислой форме. Затем соединения по настоящему изобретению в виде кислот могут быть нейтрализованы основанием для получения требуемой соли. Для получения солей соединений формулы (I)/(I') можно использовать любое неорганическое или органическое основание, образующее с соединениями формулы (I)/(I') фармацевтически приемлемые соли.
Настоящее изобретение относится также к соединениям приведенной далее формулы 20A, в которой Pg, Pg' и Pg", являющиеся одинаковыми или отличающимися друг от друга, представляют собой защитные группы:

Такие соединения являются полезными в качестве промежуточных соединений в синтезе соединений формулы (I)/(I').
Настоящее изобретение предпочтительно относится к соединению 20A, в котором Pg, Pg' и Pg" представляют собой бензил, аллил и ацетил, соответственно. Данное соединение соответствует дисахариду 20, поясненному приведенной далее схемой 2 и являющемуся приемлемым для синтеза соединений №№ 1 и 2 по настоящему изобретению, конкретизированного в последующем тексте:

В приведенных далее примерах описано получение некоторых соединений по настоящему изобретению и промежуточных соединений, используемых в синтезе. Данные примеры не являются ограничительными и приведены только для пояснения настоящего изобретения. Исходные вещества и реагенты, способы получения которых не описаны конкретно, имеются в продаже или описаны в литературе, или могут быть получены способами, описанными в литературе или известными специалистам в данной области техники.
Приняты следующие сокращения:
[α]D: оптическое вращение;
Ac: ацетил;
All: аллил;
Bn: бензил;
Bz: бензоил;
ТСХ (CCM): тонкослойная хроматография;
CrO3: триоксид хрома;
DDQ: 2,3-дихлор-5,6-дициано-1,4-бензохинон;
ИЭР (ESI): ионизация электрораспылением;
ч: час;
H2SO4: серная кислота;
Lev: левулинил;
Me: метил;
мин: минута;
Rf: фактор замедления (время удерживания, измеренное при ТСХ по отношению к фронту элюирующего растворителя);
tBDPS: трет-бутилдифенилсилил;
Z: бензилоксикарбонил.
Получение промежуточных соединений, используемых в синтезе
СХЕМА 1. Получение дисахарида-донора 15

(Бензил-2-O-ацетил-3-O-бензил-4-O-левулиноил-α-L-идопиранозилуронат)-(1→4)-1,6-ангидро-2-азидо-3-O-бензил-2-дезокси-β-D-глюкопираноза (12)
К раствору соединения 11 (11,6 г, 16,2 ммоль) (описанного в методике получения соединения № 8 заявки WO 2006/021653) в безводном диоксане (340 мл) последовательно прибавляют 4-диметиламинопиридин (2,12 г, 17,3 ммоль), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (6,5 г, 34,3 ммоль) и левулиновую кислоту (3,6 мл, 34,3 ммоль). После перемешивания в течение 4 ч 30 мин смесь разбавляют дихлорметаном (1800 мл). Органическую фракцию последовательно промывают 10%-м водным раствором гидросульфата калия, насыщенным раствором хлорида натрия, насыщенным водным раствором гидрокарбоната натрия и водой, сушат над сульфатом натрия, фильтруют и затем упаривают досуха. Остаток очищают хроматографией на колонке с силикагелем (толуол/ацетон, 5/1 об./об.) с получением 12,7 г соединения 12.
ТСХ: Rf=0,42, силикагель, толуол/ацетон, 3/1 об./об.
(Бензил-2-O-ацетил-3-O-бензил-4-O-левулиноил-α-L-идопиранозилуронат)-(1→4)-1,6-ди-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α,β-D-глюкопираноза (13)
К раствору соединения 12 (12,76 г, 16,2 ммоль) в уксусном ангидриде (160 мл) при 0°C прибавляют трифторуксусную кислоту (14,1 мл, 183 ммоль). Реакционную смесь перемешивают в течение 16 часов при комнатной температуре. После концентрирования смесь упаривают совместно с толуолом. После очистки остатка хроматографией на колонке с силикагелем (толуол/ацетон, 4/1 об./об.) получают 10,5 г соединения 13.
ТСХ: Rf=0,49, силикагель, (толуол/ацетон, 4/1 об./об.)
(Бензил-2-O-ацетил-3-O-бензил-4-O-левулиноил-α-L-идопиранозилуронат)-(1→4)-6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α,β-D-глюкопираноза (14)
Раствор соединения 13 (10,5 г, 12,0 ммоль) и бензиламина (50 мл, 457 ммоль) в диэтиловом эфире (360 мл) перемешивают при комнатной температуре в течение 2 часов. Реакционную смесь разбавляют диэтиловым эфиром (2000 мл). Органическую фракцию промывают холодным 1 M водным раствором соляной кислоты и водой, сушат над сульфатом натрия, фильтруют и затем концентрируют досуха. Остаток очищают хроматографией на колонке с силикагелем (толуол/ацетон, 3/1 об./об.) с получением 7,14 г соединения 14.
ТСХ: Rf=0,40, силикагель, толуол/ацетон, 3/1 об./об.
Трихлорацетимидат (бензил-2-O-ацетил-3-O-бензил-4-O-левулиноил-α-L-идопиранозилуронат)-(1→4)-6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α,β-D-глюкопиранозы (15)
Трихлорацетонитрил (4,3 мл, 42,8 ммоль) и карбонат цезия (1,89 г, 13,7 ммоль) прибавляют к раствору соединения 14 (7,14 г, 8,56 ммоль) в дихлорметане (160 мл). После перемешивания в течение 30 минут реакционную смесь фильтруют и затем концентрируют. Остаток очищают хроматографией на колонке с силикагелем (толуол/ацетон, 2/1 об./об. + 0,1% триэтиламина) с получением 7,0 г соединения 15.
ТСХ: Rf=0,37 и 0,28, силикагель, толуол/ацетон, 2/1 об./об.
СХЕМА 2. Получение донора глюкозила 20

(Бензил-2-O-ацетил-4-O-(аллилокси)карбонил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-1,6-ангидро-2-азидо-3-O-бензил-2-дезокси-β-D-глюкопираноза (16)
К раствору соединения 11 (11,7 г, 17,3 ммоль) (описанного в методике получения соединения № 8 заявки WO 2006/021653) в безводном тетрагидрофуране при 0°C последовательно прибавляют пиридин (14 мл, 173 ммоль), 4-диметиламинопиридин (2,12 г, 17,3 ммоль) и аллилхлорформиат (18,3 мл, 173 ммоль). После перемешивания в течение 16 ч при комнатной температуре прибавляют при 0°C воду (47 мл). После перемешивания в течение 30 мин смесь разбавляют этилацетатом (800 мл). Органическую фракцию последовательно промывают 10%-м водным раствором гидросульфата калия, водой, насыщенным водным раствором гидрокарбоната натрия и еще раз водой, сушат над сульфатом натрия, фильтруют и затем упаривают досуха. Остаток очищают хроматографией на колонке с силикагелем (циклогексан/этилацетат, 2/1 об./об.) с получением 11,4 г соединения 16.
ТСХ: Rf=0,37, силикагель, циклогексан/этилацетат, 2/1 об./об.
(Бензил-2-O-ацетил-4-O-аллил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-1,6-ангидро-2-азидо-3-O-бензил-2-дезокси-β-D-глюкопираноза (17)
Соединение 16 (11,44 г, 15,1 ммоль) растворяют в тетрагидрофуране (100 мл). Прибавляют ацетат палладия (67,6 мг, 0,30 ммоль) и трифенилфосфин (395 мг, 1,5 ммоль). После перемешивания в течение 2 ч при нагревании с обратным холодильником реакционную смесь концентрируют досуха. Остаток очищают хроматографией на колонке с силикагелем (циклогексан/этилацетат, 3/1 об./об.) с получением 8,0 г соединения 17.
ТСХ: Rf=0,33, силикагель, циклогексан/этилацетат, 2/1 об./об.
(Бензил-2-O-ацетил-4-O-аллил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-1,6-ди-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α,β-D-глюкопираноза (18)
К раствору соединения 16 (7,96 г, 11,1 ммоль) в уксусном ангидриде (105 мл), охлажденному до 0°C, прибавляют трифторуксусную кислоту (9,4 мл). Реакционную смесь перемешивают в течение 16 часов при комнатной температуре. После концентрирования смесь упаривают совместно с толуолом (5×200 мл). После очистки остатка хроматографией на колонке с силикагелем (циклогексан/этилацетат, 2/1 об./об.) получают 7,72 г соединения 18.
ТСХ: Rf=0,40, силикагель, циклогексан/этилацетат, 2/1 об./об.
(Бензил-2-O-ацетил-4-O-аллил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α,β-D-глюкопираноза (19)
Раствор соединения 18 (7,72 г, 9,44 ммоль) и бензиламина (3,9 мл, 35,2 ммоль) в диэтиловом эфире (280 мл) перемешивают при комнатной температуре в течение 6 часов. Реакционную смесь разбавляют диэтиловым эфиром (800 мл). Органическую фракцию промывают 1 M водным раствором соляной кислоты и водой, сушат над сульфатом натрия, фильтруют и затем концентрируют досуха. Остаток очищают хроматографией на колонке с силикагелем (толуол/этилацетат, 5/2 об./об.) с получением 6,14 г соединения 19.
ТСХ: Rf=0,45, силикагель, толуол/этилацетат, 5/3 об./об.
Трихлорацетимидат (бензил-2-O-ацетил-4-O-аллил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α,β-D-глюкопиранозы (20)
Трихлорацетонитрил (4 мл, 39,6 ммоль) и карбонат цезия (4,13 г, 12,7 ммоль) прибавляют к раствору соединения 19 (6,14 г, 7,9 ммоль) в дихлорметане (150 мл). После перемешивания в течение 30 минут реакционную смесь фильтруют и затем концентрируют. Остаток очищают хроматографией на колонке с силикагелем (толуол/этилацетат, 4/1 об./об.) с получением 6,5 г соединения 20.
ТСХ: Rf=0,50, силикагель, толуол/этилацетат, 3/1 об./об.
Химические сдвиги аномерных протонов (500 МГц, CDCl3) δ: 5,27 IdoUA", 5,57 Glc'β и 5,28 IdoUA", 6,36 Glc'α
ЖХ-МС: m/z 798,2 [(M + Na)+]. TR1=13,59 мин и TR2=13,75 мин
СХЕМА 3. Получение октасахарида 26

Метил-(бензил-2-O-ацетил-3-O-бензил-4-O-левулиноил-α-L-идопиранозилуронат)-(1→4)-6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-6-O-ацетил-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (22)
Смесь имидата 15 (541 мг, 0,553 ммоль), акцептора глюкозила 21 (650 мг, 0,83 ммоль) (полученного способом, описанным в Carbohydrate Research (1987), 167, 67-75) и молекулярного сита 4 Å (412 мг) в смеси "толуол/дихлорметан" (23 мл, 20/3 об./об.) перемешивают в атмосфере аргона в течение 1 часа при 25°C. Реакционную смесь охлаждают до -25°C и прибавляют 1 M раствор трет-бутилдиметилсилилтрифлата в дихлорметане (82,5 мкл). Через 15 минут реакционную смесь нейтрализуют прибавлением гидрокарбоната натрия в твердом состоянии. Полученный после фильтрования и концентрирования остаток очищают эксклюзионной хроматографией (Sephadex® LH20, 120×3 см, дихлорметан/этанол, 1/1 об./об.) с получением 746 мг соединения 22.
ТСХ: Rf=0,37, силикагель, циклогексан/этилацетат, 5/6 об./об.
Метил-(бензил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-6-O-ацетил-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (23)
К раствору соединения 22 (2,3 г, 1,44 ммоль) в смеси "толуол/этанол", 1/2 об./об., (290 мл) прибавляют гидразинацетат (662,3 мг, 7,2 ммоль). Реакционную смесь перемешивают в течение 2 часов при комнатной температуре. Полученный после концентрирования остаток очищают флэш-хроматографией на колонке с силикагелем (циклогексан/этилацетат, 5/6 об./об.) с получением 1,84 г соединения 23.
ТСХ: Rf=0,48, силикагель, циклогексан/этилацетат, 5/6 об./об.
Метил-(бензил-2-O-ацетил-3-O-бензил-4-O-левулиноил-α-L-идопиранозилуронат)-(1→4)-(6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(бензил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил-(1→4)-(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-6-O-ацетил-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (24)
Смесь акцептора глюкозила 23 (1,97 г, 1,12 ммоль), имидата 15 (1,63 г, 1,66 ммоль) и молекулярного сита 4 Å (2,6 г) в смеси "дихлорметан/толуол", 1/1 об./об., (75 мл) перемешивают в атмосфере аргона в течение 1 часа при 25°C. Реакционную смесь охлаждают до -20°C и прибавляют 1 M раствор трет-бутилдиметилсилилтрифлата в дихлорметане (250 мкл). Через 10 минут реакционную смесь нейтрализуют прибавлением гидрокарбоната натрия в твердом состоянии. Полученный после фильтрования и концентрирования остаток очищают эксклюзионной хроматографией (Sephadex® LH20, 190×3,2 см, дихлорметан/этанол, 1/1 об./об.) с получением 1,63 г соединения 24.
ТСХ: Rf=0,33, силикагель, толуол/ацетон, 3/1 об./об.
Метил-(бензил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(бензил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-6-O-ацетил-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (25)
К раствору соединения 24 (1,7 г, 0,73 ммоль) в смеси "толуол/этанол", 1/2 об./об., (145 мл) прибавляют гидразинацетат (338 мг, 3,67 ммоль). Реакционную смесь перемешивают в течение 2 часов при комнатной температуре. Полученный после концентрирования остаток очищают флэш-хроматографией на колонке с силикагелем (циклогексан/этилацетат, 1/1 об./об.) с получением соединения 25 (1,41 г).
ТСХ: Rf=0,47, силикагель, циклогексан/этилацетат, 1/1 об./об.
Метил-(бензил-2-O-ацетил-4-O-аллил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-[(бензил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил-(1→4)] 2 -(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-6-O-ацетил-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (26)
Смесь имидата 20 (0,681 мг, 0,74 ммоль), акцептора глюкозила 25 (1,10 г, 0,5 ммоль) и молекулярного сита 4 Å (0,555 г) в смеси "дихлорметан/толуол", 1/1 об./об., (26 мл) перемешивают в атмосфере аргона в течение 1 часа при 25°C. Реакционную смесь охлаждают до -20°C и прибавляют 1 M раствор трет-бутилдиметилсилилтрифлата в дихлорметане (111 мкл). Через 20 минут реакционную смесь нейтрализуют прибавлением гидрокарбоната натрия в твердом состоянии. Полученный после фильтрования через Celite® и концентрирования остаток подвергают хроматографии на колонке для эксклюзионной хроматографии (Sephadex® LH20, 190×3,2 см, дихлорметан/этанол, 1/1 об./об.) и последовательно получают 468 мг октасахарида 26 и 842 мг смеси, содержащей гексасахарид 25 и октасахарид 26.
Данную смесь (842 мг) обрабатывают в описанных ранее условиях для получения соединения 26 (513,6 мг) после обработки и хроматографии на колонке (Sephadex® LH20, 190×3,2 см, дихлорметан/этанол, 1/1 об./об.).
Две фракции (468 мг и 513,6 мг) объединяют и очищают препаративной ВЭЖХ на колонке с силикагелем (толуол/этилацетат, 2/1 об./об.) с получением соединения 26 (1,03 г).
ТСХ: Rf=0,44, силикагель, толуол/этилацетат, 2/1 об./об.
СХЕМА 4. Получение октасахарида 30

Метил-(метил-4-O-аллил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил-(1→4)-[(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил-(1→4)] 2 -(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (27)
К раствору соединения 26 (819 мг, 0,27 ммоль) в смеси "дихлорметан/метанол", 2/3 об./об., (83 мл), содержащей цеолит 3 Å (10,3 г), при 0°C в атмосфере аргона прибавляют 1 M раствор метилата натрия в метаноле (1,65 мл). После выдерживания в течение 16 часов при -18°C реакционную смесь нейтрализуют смолой Dowex® 50WX4 в H+-форме. Полученный после фильтрования и концентрирования остаток очищают эксклюзионной хроматографией (Sephadex® LH20, 120×3 см, дихлорметан/этанол, 1/1 об./об.) с последующей хроматографией на колонке с силикагелем (толуол/ацетон, 4/3 об./об.) с получением 605 мг соединения 27.
ТСХ: Rf=0,41, силикагель, толуол/ацетон, 4/3 об./об.
Метил-(метил-4-O-аллил-3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозил)-(1→4)-[(метил-3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат]-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозил-(1→4)] 2 -(метил-3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозид (28)
Соединение 27 (300 мг, 0,12 ммоль) сушат совместной отгонкой с N,N-диметилформамидом (3×10 мл) и затем растворяют в N,N-диметилформамиде (11 мл). К данному раствору прибавляют комплекс "триоксид серы-триэтиламин" (902 мг, 4,98 ммоль). Смесь перемешивают в течение 16 часов при 55°C без доступа света и затем нейтрализуют метанолом (202 мкл, 4,98 ммоль). Реакционную смесь вносят в колонку с гелем Sephadex® LH20 (95×2 см) и элюируют смесью "дихлорметан/этанол", 1/1 об./об., с получением соединения 28 (426 мг).
ТСХ: Rf=0,32, силикагель, этилацетат/пиридин/уксусная кислота/вода, 11/7/1,6/4 об./об./об./об.
Метил-(4-O-аллил-3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-литийсульфонато-α-D-глюкопиранозил)-(1→4)-[(3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-литийсульфонато-α-D-глюкопиранозил-(1→4)] 2 -(3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-6-O-литийсульфонато-α-D-глюкопиранозид (29)
К раствору соединения 28 (459 мг, 0,12 ммоль) в смеси "тетрагидрофуран/метанол", 1/1 об./об., (19 мл) при 0°C прибавляют 0,7 M раствор гидроксида лития в воде (7,6 мл; в количестве, достаточном для получения конечной концентрации 0,2 M). После выдерживания в течение 1 часа при 0°C и затем в течение 16 часов при комнатной температуре реакционную смесь охлаждают до 0°C, нейтрализуют уксусной кислотой (305 мкл) и затем вносят в колонку Sephadex® LH20 (95×2 см) и элюируют смесью "метанол/вода", 4/1 об./об., с получением соединения 29 (368 мг).
ТСХ: Rf=0,25, силикагель, этилацетат/пиридин/уксусная кислота/вода, 27/19/4,2/11 об./об./об./об.
Метил-(4-O-н-пропил-2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозил)-(1→4)-[2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозил-(1→4)] 2 -(2-O-сульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозид (30)
Раствор соединения 29 (170 мг) в смеси "трет-бутанол/вода", 2/3 об./об., (27 мл) обрабатывают в атмосфере водорода под давлением (1 бар) в присутствии 10%-го палладия на угле (340 мг) при 30°C в течение 24 часов. После фильтрования (фильтр Millipore® LSWP, 5 мкм) реакционную смесь вносят в колонку Sephadex® G-25 fine (90×3 см) и элюируют 0,2 M водным раствором хлорида натрия. Фракции, содержащие требуемое вещество, концентрируют и освобождают от соли, используя ту же самую колонку и элюируя водой. После концентрирования досуха получают соединение 30 (205 мг).
Масса: способ ИЭР, электроотрицательный режим: теоретическая масса=2327,55; экспериментальная масса: 2239 а.е.м. (идуроновые кислоты, наблюдаемые в COOH-форме).
СХЕМА 5. Получение декасахарида 33
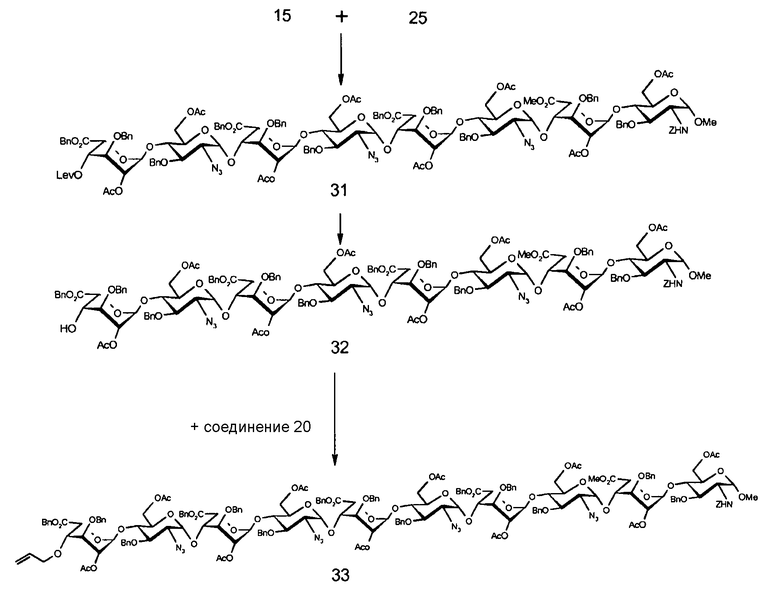
Метил-(бензил-2-O-ацетил-3-O-бензил-4-O-левулиноил-α-L-идопиранозилуронат)-(1→4)-(6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-[(бензил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил-(1→4)] 2 -(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-6-O-ацетил-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (31)
Смесь имидата 15 (250 мг, 0,255 ммоль), акцептора глюкозила 25 (376 мг, 0,169 ммоль) и молекулярного сита 4 Å (396 мг) в смеси "дихлорметан/толуол", 1/1 об./об., (11,4 мл) перемешивают в атмосфере аргона в течение 1 часа при 25°C. Реакционную смесь охлаждают до -20°C и прибавляют 0,1 M раствор трет-бутилдиметилсилилтрифлата в дихлорметане (381 мкл). Через 12 минут реакционную смесь нейтрализуют прибавлением гидрокарбоната натрия в твердом состоянии. Полученный после фильтрования и концентрирования остаток подвергают хроматографии на колонке Sephadex® LH20 (120×3 см, дихлорметан/этанол, 1/1 об./об.) и последовательно получают 150 мг неочищенного соединения 31 и 318 мг смеси, содержащей гексасахарид 25 и октасахарид 31.
Смесь, содержащую гексасахарид 25 и октасахарид 33, обрабатывают в описанных ранее условиях с получением после эксклюзионной хроматографии (Sephadex® LH20) 151 мг неочищенного соединения 31 и 191 мг смеси, содержащей гексасахарид 25 и октасахарид 31. Данную операцию повторяют два раза до исчерпания гексасахарида 25.
Фракции, содержащие неочищенный октасахарид 31, объединяют и очищают флэш-хроматографией на колонке с силикагелем (толуол/этилацетат, 7/3 об./об.) с получением соединения 31 (351 мг).
ТСХ: Rf=0,37, силикагель, толуол/этилацетат, 7/5 об./об.
Метил-(бензил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-[(бензил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил-(1→4)] 2 -(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-6-O-ацетил-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (32)
К раствору соединения 31 (335 мг, 0,11 ммоль) в смеси "толуол/этанол", 1/2 об./об., (22 мл) прибавляют гидразинацетат (51 мг, 0,55 ммоль). Реакционную смесь перемешивают в течение 2 часов при комнатной температуре. Реакционную смесь разбавляют дихлорметаном (50 мл). Органическую фракцию промывают 2%-м водным раствором гидросульфата калия и водой, затем сушат над сульфатом натрия, фильтруют и далее концентрируют досуха. Остаток очищают хроматографией на колонке с силикагелем (толуол/ацетон, 7/3 об./об.) с получением соединения 32 (238 мг).
ТСХ: Rf=0,50, силикагель, циклогексан/этилацетат, 5/6 об./об.
Метил-(бензил-2-O-ацетил-4-O-аллил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-[(бензил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил-(1→4)] 3 -(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-6-O-ацетил-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (33)
Смесь имидата 20 (64 мг, 0,066 ммоль), акцептора глюкозила 32 (130 мг, 0,044 ммоль) и молекулярного сита 4 Å (49 мг) в смеси "дихлорметан/толуол", 1/1 об./об., (2,2 мл) перемешивают в атмосфере аргона в течение 1 часа при 25°C. Реакционную смесь охлаждают до -20°C и прибавляют 0,1 M раствор трет-бутилдиметилсилилтрифлата в дихлорметане (100 мкл). Через 10 минут реакционную смесь нейтрализуют прибавлением гидрокарбоната натрия в твердом состоянии. Полученный после фильтрования и концентрирования остаток подвергают хроматографии на колонке Sephadex® LH20 (120×3 см, дихлорметан/этанол, 1/1 об./об.) и последовательно получают 61 мг неочищенного соединения 33 и 87,7 мг смеси, содержащей октасахарид 32 и декасахарид 33.
Полученную смесь (87,7 мг) обрабатывают в описанных ранее условиях с получением неочищенного соединения 33 (120 мг) после хроматографии на колонке Sephadex® LH20 (120×3 см, дихлорметан/этанол, 1/1 об./об.).
Две фракции, содержащие неочищенное соединение, объединяют и очищают флэш-хроматографией на колонке с силикагелем (толуол/этилацетат, 7/2 об./об.) с получением соединения 33 (120 мг).
ТСХ: Rf=0,52, силикагель, циклогексан/этилацетат, 1/1 об./об.
СХЕМА 6. Получение декасахарида 37
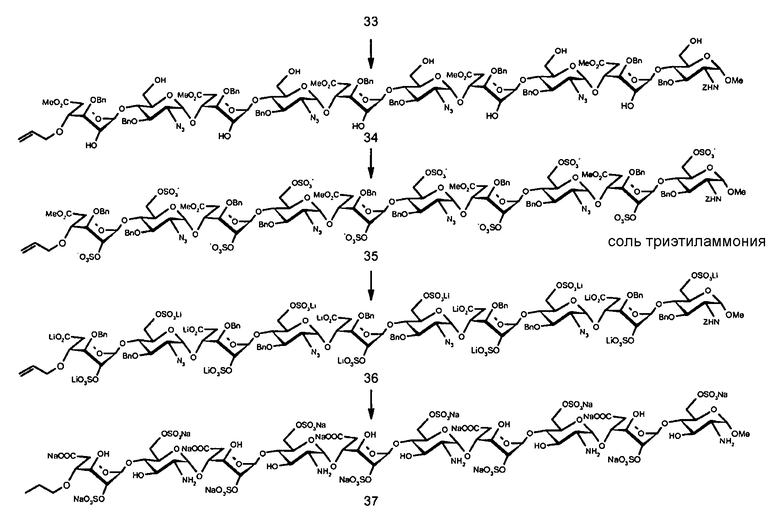
Метил-(метил-4-O-аллил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-[(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил-(1→4)] 3 -(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (34)
К охлажденному до 0°C раствору соединения 33 (51,8 мг, 0,014 ммоль) в смеси "дихлорметан/метанол", 2/3 об./об., (982 мкл), содержащей цеолит 3 Å (125 мг), в атмосфере аргона прибавляют 1 M раствор метилата натрия в метаноле (21,0 мкл). После выдерживания в течение 5 часов при комнатной температуре реакционную смесь нейтрализуют смолой Dowex® 50WX4 в H+-форме. Полученный после фильтрования и концентрирования остаток очищают эксклюзионной хроматографией (Sephadex® LH20, 95×2 см, дихлорметан/этанол, 1/1 об./об.) с получением соединения 34 (31,4 мг).
ТСХ: Rf=0,47, силикагель, дихлорметан/ацетон, 7/3 об./об.
Метил-(метил-4-O-аллил-3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозил)-(1→4)-[(метил-3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозил-(1→4)] 3 -(метил-3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозид (35)
Соединение 34 (31,5 мг, 10,6 мкмоль) обрабатывают аналогично получению соединения 28 с получением соединения 35 (47,0 мг) после эксклюзионной хроматографии (Sephadex® LH20, 100×1,2 см, дихлорметан/метанол, 1/1 об./об.).
ТСХ: Rf=0,55, силикагель, этилацетат/пиридин/уксусная кислота/вода, 16/11/2,6/7 об./об./об./об.
Метил-(4-O-аллил-3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-литийсульфонато-α-D-глюкопиранозил)-(1→4)-[(3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-литийсульфонато-α-D-глюкопиранозил-(1→4)] 3 -(3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-6-O-литийсульфонато-α-D-глюкопиранозид (36)
К раствору соединения 35 (47 мг, 12,5 мкмоль) в смеси "тетрагидрофуран/метанол", 1/1 об./об., (2,0 мл) при 0°C прибавляют 1 M раствор гидроксида лития в воде (500 мкл; в количестве, достаточном для получения конечной концентрации 0,2 M). После выдерживания в течение 1 часа при 0°C и затем в течение 4 часов при комнатной температуре реакционную смесь нейтрализуют уксусной кислотой и затем выдерживают при -20°C в течение 16 часов. Реакционную смесь вносят в колонку с гелем Sephadex® LH20 и элюируют смесью "метанол/вода", 4/1 об./об., с получением соединения 36 (38,9 мг).
Метил-(4-O-пропил-2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозил)-(1→4)-[(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозил-(1→4)] 3 -(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозид (37)
Раствор соединения 36 (40 мг, 10,8 мкмоль) в смеси "трет-бутанол/вода", 6/9 об./об., (1 мл) обрабатывают в атмосфере водорода под давлением (11 бар) в присутствии 10%-го палладия на угле (80 мг, 2-кратное количество по отношению к восстанавливаемому соединению) при 40°C в течение 4 часов. После фильтрования (фильтр Millipore® LSWP, 5 мкм) раствор вносят в колонку со смолой Chelex® 100 (1 мл), элюируют водой и затем концентрируют досуха. Неочищенное соединение, полученное таким образом, (27 мг) используют в таком виде на следующей стадии.
Масса: способ ИЭР, электроотрицательный режим: теоретическая масса = 2781,10; экспериментальная масса: 2782,05±0,30 а.е.м.
СХЕМА 7. Получение гептасахарида 43

Метил-[метил-(метил-2-O-ацетил-3-O-бензил-4-O-левулиноил-α-L-идопиранозилуронат)-(1→4)-(6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-2-O-ацетил-3-O-бензил-α-L-идопиранозид]уронат (40)
Смесь имидата 38 (1,1 г, 1,22 ммоль), полученного по методике, описанной в C. Tabeur et al., BioOrg. Med. Chem. (1999) 7, 2003-2012, акцептора глюкозила 39 (864 мг, 2,44 ммоль), полученного по методике, описанной в Koshida, S. et al., Tetrahedron Lett., 1999, 40, 5725-5728, и молекулярного сита 4 Å (914 мг) в толуоле (43 мл) перемешивают в атмосфере аргона в течение 1 часа при 25°C. Реакционную смесь охлаждают до -20°C и прибавляют 1 M раствор трет-бутилдиметилсилилтрифлата в дихлорметане (183 мкл). После перемешивания в течение 1 часа реакционную смесь нейтрализуют прибавлением гидрокарбоната натрия в твердом состоянии. Полученный после фильтрования через Celite® и концентрирования остаток подвергают хроматографии на колонке Sephadex® LH20 (120×3 см, дихлорметан/этанол, 1/1 об./об.) с последующей хроматографией на колонке с силикагелем (толуол/этилацетат, 1/1 об./об.) с получением соединения 40 (936 мг).
ТСХ: Rf=0,38, силикагель, толуол/этилацетат, 1/1 об./об.
Метил-[метил-(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-2-O-ацетил-3-O-бензил-α-L-идопиранозид]уронат (41)
Соединение 40 (2,56 г, 2,34 ммоль) обрабатывают аналогично методике, описанной для синтеза соединения 23, с получением соединения 41 (2,17 г) после флэш-хроматографии на колонке с силикагелем (толуол/этилацетат, 1/1 об./об.).
ТСХ: Rf=0,35, силикагель, толуол/этилацетат, 1/1 об./об.
Метил-[метил-(метил-2-O-ацетил-3-O-бензил-4-O-левулиноил-α-L-идопиранозилуронат)-(1→4)-(6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-2-O-ацетил-3-O-бензил-α-L-идопиранозид]уронат (42)
Смесь имидата 38 (1,1 г, 1,22 ммоль), акцептора глюкозила 41 (1,2 г, 1,20 ммоль) и молекулярного сита 4 Å (903 мг) в дихлорметане (42 мл) перемешивают в атмосфере аргона в течение 1 часа при 25°C. Реакционную смесь охлаждают до -20°C и прибавляют 1 M раствор трет-бутилдиметилсилилтрифлата в дихлорметане (181 мкл). Через 15 минут реакционную смесь нейтрализуют прибавлением гидрокарбоната натрия в твердом состоянии. Полученный после фильтрования и концентрирования остаток очищают на колонке для эксклюзионной хроматографии (Sephadex® LH20, 190×3,2 см, дихлорметан/этанол, 1/1 об./об.) с последующей хроматографией на колонке с силикагелем (толуол/этилацетат, 1/1 об./об.) с получением 1,63 г соединения 42.
ТСХ: Rf=0,30, силикагель, толуол/этилацетат, 1/1 об./об.
Метил-[метил-(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-2-O-ацетил-3-O-бензил-α-L-идопиранозид]уронат (43)
Соединение 42 (3,90 г, 2,25 ммоль) обрабатывают аналогично методике, описанной для синтеза соединения 23. После хроматографии на колонке с силикагелем (толуол/этилацетат, 1/1 об./об.) получают соединение 43 (3,39 г).
ТСХ: Rf=0,33, силикагель, толуол/этилацетат, 1/1 об./об.
СХЕМА 8. Получение дисахарида 50

(3,4-Ди-O-бензил-2-O-(4-метокси)бензил-6-O-трет-бутилдиметилсилил-α-L-идопиранозил)-(1→4)-1,6-ангидро-2-азидо-3-O-бензил-2-дезокси-β-D-глюкопираноза (45)
К раствору соединения 44 (32,3 г, 42,2 ммоль) (описанного в методике получения соединения № 108 заявки WO 2006/021653) в N,N-диметилформамиде (210 мл) при 0°C в атмосфере аргона прибавляют бензилбромид (25 мл, 211 ммоль) и затем 55%-й NaH (3 г, 126 ммоль). После перемешивания в течение 20 минут магнитной мешалкой прибавляют метанол (30 мл) и реакционную смесь концентрируют в вакууме, неочищенный продукт реакции разбавляют этилацетатом, промывают водой и затем насыщенным водным раствором хлорида натрия, сушат (над Na2SO4), фильтруют и концентрируют. Полученный остаток используют на следующей стадии без очистки.
ЖХ-МС: m/z 871,7 [(M+NH4)+]. TR=13,86 мин
(2-O-Ацетил-3,4-ди-O-бензил-6-O-трет-бутилдиметилсилил-α-L-идопиранозил)-(1→4)-1,6-ангидро-2-азидо-3-O-бензил-2-дезокси-β-D-глюкопираноза (46)
К раствору неочищенного соединения 45 (38,6 г) в дихлорметане (1,6 л) прибавляют воду (80 мл) и затем при 0°C прибавляют DDQ (14,2 г). После перемешивания в течение 4 ч 45 мин при 0°C смесь разбавляют дихлорметаном и прибавляют водный раствор гидрокарбоната натрия. Затем органическую фракцию промывают водой, сушат (над Na2SO4), фильтруют и концентрируют. Полученное соединение используют на следующей стадии без очистки.
Полученный остаток растворяют в дихлорметане (350 мл) и затем прибавляют триэтиламин (13 мл), 4-диметиламинопиридин (2 г) и уксусный ангидрид (60 мл). После перемешивания в течение 10 минут магнитной мешалкой при 0°C и затем в течение 1 ч 45 мин при комнатной температуре реакционную смесь разбавляют дихлорметаном, затем последовательно промывают 10%-м водным раствором гидросульфата калия и водой и далее органическую фракцию сушат (над Na2SO4), фильтруют и концентрируют.
Полученный остаток очищают на диоксиде кремния (этилацетат/циклогексан) с получением соединения 46 (26,8 г).
ЖХ-МС: m/z 798,3 [(M+Na)+]. TR=12,97 мин
(Метил-2-O-ацетил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-1,6-ангидро-2-азидо-3-O-бензил-2-дезокси-β-D-глюкопираноза (47)
К раствору соединения 46 (26,3 г, 33,9 ммоль) в ацетоне (1,4 л) при 0°C прибавляют раствор CrO3 (10,5 г) в 3,5 M водном растворе H2SO4 (47 мл). После перемешивания в течение 4 ч механической мешалкой при 0°C реакционную смесь разбавляют дихлорметаном, промывают водой до нейтральной реакции и затем органическую фракцию сушат (над Na2SO4), фильтруют и концентрируют. Полученное соединение используют на следующей стадии без очистки.
Полученный остаток растворяют в N,N-диметилформамиде (210 мл) и прибавляют гидрокарбонат калия (17 г) и метилиодид (21 мл). Реакционную смесь перемешивают при комнатной температуре в течение 16 ч и затем концентрируют в вакууме. Остаток разбавляют этилацетатом, затем промывают водой, насыщенным водным раствором тиосульфата натрия и насыщенным водным раствором хлорида натрия и далее сушат (над Na2SO4), фильтруют и концентрируют. Полученное соединение используют на следующей стадии без очистки.
ЖХ-МС: m/z 707,3 [(M+NH4)+]. TR=10,37 мин
(Метил-2-O-ацетил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-1,6-ди-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α,β-D-глюкопираноза (48)
Неочищенный остаток, полученный на предыдущей стадии, растворяют в уксусном ангидриде (177 мл) и затем прибавляют трифторуксусную кислоту (ТФУ) (17,7 мл). Реакционную смесь перемешивают в течение 16 ч, затем концентрируют, упаривают совместно с толуолом и очищают на силикагеле (циклогексан/этилацетат) с получением соединения 48 (17,4 г).
ЖХ-МС: m/z 809,3 [(M+NH4)+]. TR=10,81 мин
(Метил-2-O-ацетил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α,β-D-глюкопираноза (49)
К раствору соединения 48 (7 г, 8,84 ммоль) в диэтиловом эфире (303 мл) при 0°C в атмосфере аргона прибавляют бензиламин (BnNH2) (29,7 мл). После перемешивания в течение 1 ч магнитной мешалкой при 0°C и затем в течение 6 ч при комнатной температуре реакционную смесь нейтрализуют холодным 1 н. водным раствором HCl, промывают водой, сушат (над Na2SO4), фильтруют, концентрируют и очищают на силикагеле (этилацетат/циклогексан) с получением соединения 49 (5,95 г).
ЖХ-МС: m/z 767,7 [(M+NH4)+]. TR=1,64 мин
Трихлорацетимидат (метил-2-O-ацетил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α,β-D-глюкопиранозы (50)
К раствору соединения 49 (5,94 г, 7,9 ммоль) в дихлорметане (150 мл) в атмосфере аргона прибавляют карбонат цезия (Cs2CO3) (4,1 г) и затем трихлорацетонитрил (CCl3CN) (3,9 мл). После перемешивания в течение 45 минут при комнатной температуре реакционную смесь фильтруют и затем концентрируют. Остаток очищают на силикагеле (этилацетат/циклогексан + 0,1% триэтиламина) с получением соединения 50 (5,7 г).
ЖХ-МС: m/z 912,0 [(M+NH4)+]. TR=1,81 мин
СХЕМА 9. Получение гептасахарида 55

Метил-{метил-(метил-2-O-ацетил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-(6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-[(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(6-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)] 2 -2-O-ацетил-3-O-бензил-α-L-идопиранозид}уронат (51)
Смесь акцептора глюкозила 43 (200 мг, 0,12 ммоль), имидата 50 (163 мг, 0,18 ммоль) и молекулярного сита 4 Å (137 мг) в дихлорметане (6,5 мл) перемешивают в атмосфере аргона в течение 1 часа при 25°C. Реакционную смесь охлаждают до -20°C и прибавляют 1 M раствор трет-бутилдиметилсилилтрифлата в дихлорметане (27 мкл). Через 1 час реакционную смесь нейтрализуют прибавлением гидрокарбоната натрия в твердом состоянии. Полученный после фильтрования и концентрирования остаток очищают на колонке для эксклюзионной хроматографии (Sephadex® LH20, 90×3 см, дихлорметан/этанол, 1/1 об./об.) с последующей хроматографией на колонке с силикагелем (толуол/этилацетат, 2/1 об./об.) с получением соединения 51 (212 мг).
ТСХ: Rf=0,38, силикагель, толуол/этилацетат, 1/1 об./об.
Метил-{метил-(метил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-[(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)] 2 -3-O-бензил-α-L-идопиранозид}уронат (52)
Соединение 51 (271 мг, 0,11 ммоль) обрабатывают аналогично методике, описанной для синтеза соединения 27, с получением соединения 52 (186 мг) после хроматографии на колонке для эксклюзионной хроматографии (Sephadex® LH20, 120×3 см, дихлорметан/этанол, 1/1 об./об.) с последующей хроматографией на колонке с силикагелем (толуол/ацетон, 5/3 об./об.).
ТСХ: Rf=0,65, силикагель, толуол/этилацетат, 4/3 об./об.
Метил-{метил-(метил-3,4-ди-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозил)-(1→4)-[(метил-3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозил)-(1→4)] 2 -3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозид}уронат (53)
Соединение 52 (172 мг, 0,08 ммоль) обрабатывают аналогично методике, описанной для синтеза соединения 28, с получением соединения 53 (196 мг) после эксклюзионной хроматографии (Sephadex® LH20, 120×3 см, дихлорметан/этанол, 1/1 об./об.).
ЯМР 1H (D2O) δ основных аномерных протонов: 5,41; 5,38; 5,34; 5,15; 5,14; 5,05; 5,15; 5,02 м.д.
{Метил-(3,4-ди-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-литийсульфонато-α-D-глюкопиранозил)-(1→4)-[(3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-литийсульфонато-α-D-глюкопиранозил)-(1→4)] 2 -3-O-бензил-2-O-литийсульфонато-α-L-идопиранозид}уронат лития (54)
Соединение 53 (186 мг, 70,7 мкмоль) обрабатывают аналогично методике, описанной для синтеза соединения 29, с получением соединения 54 (141 мг) после эксклюзионной хроматографии (Sephadex® LH20, 120×3 см, дихлорметан/этанол/вода, 50/50/1 об./об./об.).
ТСХ: Rf=0,24, силикагель, этилацетат/пиридин/уксусная кислота/вода, 27/19/4,2/11 об./об./об./об.
Метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозил)-(1→4)-[(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозил)-(1→4)] 2 -2-O-натрийсульфонато-α-L-идопиранозид}уронат натрия (55)
Раствор соединения 54 (60,0 мг, 0,022 ммоль) в смеси "трет-бутанол/вода", 1/1 об./об., (6 мл) обрабатывают в атмосфере водорода под давлением (<200 мбар) в присутствии 10%-го палладия на угле (60 мг) при комнатной температуре. После перемешивания в течение 24 часов реакционную смесь фильтруют (фильтр Millipore® LSWP, 5 мкм) и затем концентрируют досуха. Полученное таким образом неочищенное соединение 55 (48,7 мг) используют в таком виде на следующей стадии.
СХЕМА 10. Получение акцептора гликозида 60

Метил-(метил-2-O-ацетил-3-O-бензил-4-O-левулиноил-α-L-идопиранозилуронат)-(1→4)-6-O-ацетил-3-O-бензил-2-бензилоксикарбониламино-2-дезокси-α-D-глюкопиранозид (57)
К раствору соединения 56 (23,5 г, 30 ммоль; получено способом, описанным в Carbohydrate Research (1987), 167, 67-75) в дихлорметане (600 мл) при 0°C в инертной атмосфере прибавляют 4-диметиламинопиридин (733 мг, 6 ммоль), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (11,5 г, 60 ммоль) и левулиновую кислоту (6,2 мл, 60 ммоль). После перемешивания в течение 16 часов при комнатной температуре смесь разбавляют дихлорметаном (1,5 л). Органическую фракцию последовательно промывают 10%-м водным раствором гидросульфата калия, водой, насыщенным раствором гидрокарбоната натрия и еще раз водой, сушат над сульфатом натрия, фильтруют и затем упаривают досуха. Остаток очищают флэш-хроматографией на колонке с силикагелем (циклогексан/этилацетат, 1/3) с получением соединения 57 (22,6 г).
Rf=0,37, силикагель, циклогексан/этилацетат, 1/3 об./об.
Метил-(метил-2-O-ацетил-3-O-бензил-4-O-левулиноил-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-бензилоксикарбониламино-2-дезокси-α-D-глюкопиранозид (58)
К раствору соединения 57 (20,2 г, 23 ммоль) в смеси "тетрагидрофуран/метанол", 1/1, (140 мл) в инертной атмосфере прибавляют [tBu2SnCl(OH)]2 (226 мг, 0,79 ммоль), полученный согласно A. Orita et al., Chem. Eur. J. (2001) 7, 3321. Реакционную смесь перемешивают в течение 38 часов при 35°C. Полученный после концентрирования остаток (20,8 г) используют без очистки на следующей стадии.
Rf=0,23, силикагель, циклогексан/этилацетат, 1/3 об./об.
Метил-(метил-2-O-ацетил-3-O-бензил-4-O-левулиноил-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-бензилоксикарбониламино-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозид (59)
К раствору неочищенного соединения 58 (23 ммоль) в дихлорметане (190 мл) при 0°C в инертной атмосфере прибавляют триэтиламин (8 мл, 57,5 ммоль), 4-диметиламинопиридин (1,4 г, 11,5 ммоль) и трет-бутилдифенилсилилхлорид (12 мл, 46,0 ммоль). Реакционную смесь перемешивают в течение 16 часов при комнатной температуре. Реакционную смесь разбавляют дихлорметаном. Органическую фракцию последовательно промывают насыщенным водным раствором хлорида натрия и водой, сушат над сульфатом натрия, фильтруют и затем упаривают. Остаток очищают флэш-хроматографией на колонке с силикагелем (циклогексан/этилацетат, 2/1) с получением соединения 59 (24,4 г).
Rf=0,42, силикагель, циклогексан/этилацетат, 2/1 об./об.
Метил-(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-бензилоксикарбониламино-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозид (60)
К раствору соединения 59 (22,6 г, 20,0 ммоль) в смеси "толуол/этанол", 1/2 (2,5 л) прибавляют гидразинацетат (9,21 г, 100,0 ммоль). Реакционную смесь перемешивают в течение 30 минут при комнатной температуре. Полученный после концентрирования остаток очищают флэш-хроматографией на колонке с силикагелем (циклогексан/этилацетат, 2/1) с получением 17,6 г соединения 60.
Rf=0,40, силикагель, циклогексан/этилацетат, 2/1 об./об.
СХЕМА 11. Получение донора гликозида 65

(Метил-2-O-ацетил-3-O-бензил-4-O-левулиноил-α-L-идопиранозилуронат)-(1→4)-1-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопираноза (62)
К раствору соединения 61 (11 г, 13,7 ммоль) (полученного по методике, описанной в C. Tabeur et al., Carbohydr. Res., 281 (1996) 253-276) в смеси "метанол/тетрагидрофуран", 1/1, (80 мл) прибавляют [tBu2SnCl(OH)]2 (0,55 г), полученный согласно A. Orita et al., Chem. Eur. J. (2001) 7, 3321. После перемешивания при 35°C в течение 5,5 ч, далее при комнатной температуре в течение 16 ч и затем снова при 35°C в течение 4 ч реакционную смесь концентрируют в вакууме и очищают хроматографией с получением соединения 62 (5,97 г).
ЖХ-МС: m/z 780,2 [(M+Na)+]. TR=9,14 мин
(Метил-2-O-ацетил-3-O-бензил-4-O-левулиноил-α-L-идопиранозилуронат)-(1→4)-1-O-ацетил-2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопираноза (63)
Соединение 62 (5,97 г, 7,88 ммоль) растворяют в дихлорметане (63 мл). При 0°C в атмосфере аргона последовательно прибавляют 4-диметиламинопиридин (0,481 г), триэтиламин (2,7 мл) и трет-бутилдифенилсилилхлорид (4 мл). После перемешивания в течение 4 ч магнитной мешалкой реакционную смесь разбавляют дихлорметаном, промывают 10%-м водным раствором гидросульфата калия и водой, сушат (над Na2SO4), фильтруют и концентрируют. Полученный остаток очищают на диоксиде кремния (этилацетат/гептан) с получением соединения 63 (7 г).
ЖХ-МС: m/z 1018,3 [(M+Na)+]. TR=12,33 мин
(Метил-2-O-ацетил-3-O-бензил-4-O-левулиноил-α-L-идопиранозилуронат)-(1→4)-2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α,β-D-глюкопираноза (64)
К раствору соединения 63 (7 г, 7,03 ммоль) в диэтиловом эфире (70 мл) при 0°C прибавляют бензиламин (BnNH2) (29 мл). После перемешивания в течение 15 минут при 0°C и затем в течение 6 ч при комнатной температуре реакционную смесь разбавляют этилацетатом, затем нейтрализуют холодным 1 н. раствором HCl, промывают водой, сушат (над Na2SO4), фильтруют, концентрируют и очищают на силикагеле (этилацетат/толуол) с получением соединения 64 (5,86 г).
ЖХ-МС: m/z 976,3 [(M+Na)+]. TR=27,6/27,8 мин
Трихлорацетимидат (метил-2-O-ацетил-3-O-бензил-4-O-левулиноил-α-L-идопиранозилуронат)-(1→4)-2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α,β-D-глюкопиранозы (65)
К раствору соединения 64 (6,5 г, 6,81 ммоль) в дихлорметане (140 мл) в присутствии молекулярного сита 4 Å (7 г) в атмосфере аргона прибавляют карбонат цезия (Cs2CO3) (3,5 г) и затем при 0°C прибавляют трихлорацетонитрил (CCl3CN) (3,4 мл). После перемешивания в течение 15 мин при 0°C и затем в течение 5 ч при комнатной температуре реакционную смесь фильтруют и далее концентрируют. Остаток очищают на силикагеле (этилацетат/толуол, 1/4 + 0,1% триэтиламина) с получением соединения 65 (6,33 г).
ЖХ-МС: m/z 1119,1 [(M+Na)+]. TR=31,2
СХЕМА 12. Получение тетрасахарида 67

Метил-(метил-2-O-ацетил-3-O-бензил-4-O-левулиноил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-бензилоксикарбониламино-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозид (66)
Смесь акцептора глюкозила 59 (8,80 мг, 9,00 ммоль), имидата 65 (6,58 г, 6,00 ммоль) и молекулярного сита 4 Å (4,50 г) в дихлорметане (210 мл) перемешивают в атмосфере аргона в течение 1 часа при 25°C. Реакционную смесь охлаждают до -20°C и
прибавляют 1 M раствор трет-бутилдиметилсилилтрифлата в дихлорметане (900 мкл). Через 1 час 20 мин реакционную смесь нейтрализуют прибавлением гидрокарбоната натрия в твердом состоянии. Полученный после фильтрования через Celite® и концентрирования остаток подвергают хроматографии на колонке Sephadex® LH20 (190×3,2 см, дихлорметан/этанол, 1/1) с получением 8,26 г соединения 66.
Rf=0,30, силикагель, циклогексан/этилацетат, 2/1.
Метил-(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-бензилоксикарбониламино-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозид (67)
Соединение 66 (8,26 г, 4,31 ммоль) превращают в соединение 67 (6,41 г) аналогично методике, описанной для синтеза соединения 23.
Rf=0,34, силикагель, циклогексан/этилацетат, 2/1.
СХЕМА 13. Получение гексасахарида 69
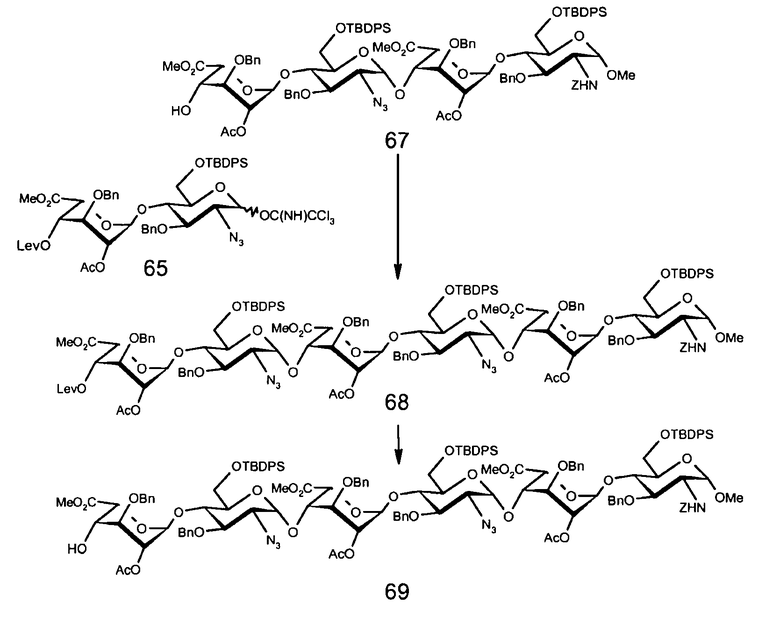
Метил-(метил-2-O-ацетил-3-O-бензил-4-O-левулиноил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-бензилоксикарбониламино-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозид (68)
Смесь акцептора глюкозила 67 (7,42 мг, 4,09 ммоль), имидата 65 (6,73 г, 6,1 ммоль) и молекулярного сита 4 Å (4,60 г) в дихлорметане (215 мл) перемешивают в атмосфере аргона в течение 1 часа при 25°C. Реакционную смесь охлаждают до -20°C и прибавляют 1 M раствор трет-бутилдиметилсилилтрифлата в дихлорметане (920 мкл). Через 1 ч 30 мин реакционную смесь нейтрализуют прибавлением гидрокарбоната натрия в твердом состоянии. После фильтрования через Celite® реакционную смесь разбавляют дихлорметаном (800 мл). Органическую фракцию последовательно промывают 2%-м водным раствором гидрокарбоната натрия и водой, затем сушат над сульфатом натрия, фильтруют и далее упаривают досуха. Полученный остаток очищают хроматографией на колонке Sephadex® LH20 (190×3,2 см, дихлорметан/этанол, 1/1) с последующей хроматографией на колонке с силикагелем (толуол/этилацетат, 6/1) с получением 6,13 г соединения 68.
Rf=0,46, силикагель, толуол/этилацетат, 4/1 об./об.
Метил-(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-бензилоксикарбониламино-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозид (69)
Соединение 68 (7,14 г, 2,59 ммоль) превращают в соединение 69 (6,07 г) аналогично методике, описанной для синтеза соединения 23.
Rf=0,37, силикагель, циклогексан/этилацетат, 2/1 об./об.
СХЕМА 14. Получение дисахарида 73

(3,4-Ди-O-бензил-2-O-(4-метокси)бензил-6-O-трет-бутилдиметилсилил-α-L-идопиранозил)-(1→4)-1,6-ангидро-2-азидо-3-O-бензил-2-дезокси-β-D-глюкопираноза (70)
К раствору соединения 44 (32,3 г, 42,2 ммоль) (описанного в методике получения соединения № 108 заявки WO 2006/021653) в N,N-диметилформамиде (210 мл) при 0°C в атмосфере аргона прибавляют бензилбромид (25 мл) и затем 55%-й NaH (3 г). После перемешивания в течение 20 мин магнитной мешалкой прибавляют метанол (30 мл) и реакционную смесь концентрируют в вакууме, неочищенный продукт реакции разбавляют этилацетатом, промывают водой и затем насыщенным водным раствором хлорида натрия, сушат (над Na2SO4), фильтруют и концентрируют. Полученный остаток (38,6 г) используют на следующей стадии без очистки.
ЖХ-МС: m/z 871,7 [(M+NH4)+]. TR=13,86 мин
(2-O-Ацетил-3,4-ди-O-бензил-6-O-трет-бутилдиметилсилил-α-L-идопиранозил)-(1→4)-1,6-ангидро-2-азидо-3-O-бензил-2-дезокси-β-D-глюкопираноза (71)
К раствору неочищенного соединения 70 (38,6 г) в дихлорметане (1,6 л) прибавляют воду (80 мл) и затем при 0°C прибавляют DDQ (14,2 г). После перемешивания в течение 4 ч 45 мин при 0°C смесь разбавляют дихлорметаном и прибавляют водный раствор гидрокарбоната натрия. Затем органическую фракцию промывают водой, сушат (над Na2SO4), фильтруют и концентрируют. Полученное соединение используют на следующей стадии без очистки.
Полученный остаток растворяют в дихлорметане (350 мл) и затем прибавляют триэтиламин (13 мл), 4-диметиламинопиридин (2 г) и уксусный ангидрид (60 мл). После перемешивания в течение 10 минут магнитной мешалкой при 0°C и затем в течение 1 ч 45 мин при комнатной температуре реакционную смесь разбавляют дихлорметаном, затем последовательно промывают 10%-м водным раствором гидросульфата калия и водой и далее органическую фракцию сушат (над Na2SO4), фильтруют и концентрируют. Полученный остаток очищают на диоксиде кремния (этилацетат/циклогексан) с получением соединения 71 (26,8 г).
ЖХ-МС: m/z 798,3 [(M+Na)+]. TR=12,97 мин
(Метил-2-O-ацетил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-1,6-ангидро-2-азидо-3-O-бензил-2-дезокси-β-D-глюкопираноза (72)
К раствору соединения 71 (26,3 г, 33,9 ммоль) в ацетоне (1,4 л) при 0°C прибавляют раствор CrO3 (10,5 г) в 3,5 M водном растворе H2SO4 (47 мл). После перемешивания в течение 4 ч механической мешалкой при 0°C реакционную смесь разбавляют дихлорметаном, промывают водой до нейтральной реакции и затем органическую фракцию сушат (над Na2SO4), фильтруют и концентрируют. Полученное соединение используют на следующей стадии без очистки.
Полученный остаток растворяют в N,N-диметилформамиде (210 мл) и прибавляют гидрокарбонат калия (17 г) и метилиодид (21 мл). Реакционную смесь перемешивают при комнатной температуре в течение 16 ч и затем концентрируют в вакууме. Остаток разбавляют этилацетатом, затем промывают водой, насыщенным водным раствором тиосульфата натрия и насыщенным водным раствором хлорида натрия и далее сушат (над Na2SO4), фильтруют и концентрируют. Полученное соединение используют на следующей стадии без очистки.
ЖХ-МС: m/z 707,3 [(M + NH4)+]. TR=10,37 мин
(Метил-2-O-ацетил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-1,6-ди-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α,β-D-глюкопираноза (73)
Неочищенный остаток, полученный на предыдущей стадии, растворяют в уксусном ангидриде (177 мл) и затем прибавляют трифторуксусную кислоту (ТФУ) (17,7 мл). Реакционную смесь перемешивают в течение 16 ч, затем концентрируют, упаривают совместно с толуолом и очищают на силикагеле (циклогексан/этилацетат) с получением соединения 73 (17,4 г).
ЖХ-МС: m/z 809,3 [(M+NH4)+]. TR=10,81 мин
СХЕМА 15. Получение донора глюкозила 77

(Метил-2-O-ацетил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-1-O-ацетил-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопираноза (74)
К раствору соединения 73 (5,05 г, 6,3 ммоль) в смеси "метанол/тетрагидрофуран", 1/1, (76 мл) прибавляют [tBu2SnCl(OH)]2 (0,25 г, 0,88 ммоль), полученный согласно A. Orita et al., Chem. Eur. J. (2001) 7, 3321. После перемешивания при комнатной температуре в течение 72 ч реакционную смесь концентрируют в вакууме и затем очищают хроматографией с получением соединения 74 (2,89 г).
ЖХ-МС: m/z 772,4 [(M+Na)+]. TR=10,23 мин
(Метил-2-O-ацетил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-1-O-ацетил-2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопираноза (75)
Соединение 74 (2,89 г, 3,86 ммоль) растворяют в дихлорметане (31 мл). При 0°C в атмосфере аргона последовательно прибавляют триэтиламин (1,3 мл), 4-диметиламинопиридин (0,235 г) и трет-бутилдифенилсилилхлорид (2 мл). После перемешивания в течение 3 ч магнитной мешалкой реакционную смесь разбавляют дихлорметаном, промывают 10%-м водным раствором гидросульфата калия и водой, сушат (над Na2SO4), фильтруют и концентрируют. Полученный остаток очищают на диоксиде кремния (этилацетат/циклогексан) с получением соединения 75 (3,4 г).
ЖХ-МС: m/z 1010,6 [(M+Na)+]. TR=13,10 мин
(Метил-2-O-ацетил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α,β-D-глюкопираноза (76)
К раствору соединения 75 (3,44 г, 3,48 ммоль) в диэтиловом эфире (35 мл) при 0°C прибавляют бензиламин (BnNH2) (14,5 мл). После перемешивания в течение 8 ч при комнатной температуре реакционную смесь выдерживают при -18°C в течение 16 ч и затем в течение 2,5 ч снова при комнатной температуре. Далее смесь разбавляют этилацетатом, нейтрализуют холодным 1 н. раствором HCl, промывают водой, сушат (над Na2SO4), фильтруют, концентрируют и очищают на силикагеле (этилацетат/циклогексан, 15/85) с получением соединения 76 (3,83 г).
ЖХ-МС: m/z 963,6 [(M+NH4)+]. TR=12,37, 12,47 мин
Трихлорацетимидат (метил-2-O-ацетил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α,β-D-глюкопиранозы (77)
К раствору соединения 76 (2,99 г, 3,16 ммоль) в дихлорметане (60 мл) в присутствии молекулярного сита 4 Å (3 г) при 0°C в атмосфере аргона прибавляют карбонат цезия (Cs2CO3) (1,6 г) и затем трихлорацетонитрил (CCl3CN) (1,6 мл). После перемешивания в течение 20 мин при 0°C и далее в течение 7 ч при комнатной температуре, выдерживания при -18°C в течение 16 ч, затем после перемешивания магнитной мешалкой в течение 8 ч при комнатной температуре, выдерживания при -18°C в течение 16 ч и заключительного перемешивания магнитной мешалкой в течение 1 ч при комнатной температуре реакционную смесь фильтруют и далее концентрируют. Остаток очищают на силикагеле (этилацетат/циклогексан, 15/85 + 0,1% триэтиламина) с получением соединения 77 (2,69 г).
ЖХ-МС: m/z 1113,4 [(M+Na)+]. TR=14,58 мин
СХЕМА 16. Получение октасахарида 79

Метил-(метил-2-O-ацетил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-[(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)] 2 -(метил-2-O-ацетил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-бензилоксикарбониламино-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозид (78)
Смесь акцептора глюкозила 69 (3,50 г, 1,32 ммоль), имидата 77 (2,16 г, 1,98 ммоль) и молекулярного сита 4 Å (1,48 г) в дихлорметане (69 мл) перемешивают в атмосфере аргона в течение 1 часа при комнатной температуре. Реакционную смесь охлаждают до -20°C и прибавляют 1 M раствор трет-бутилдиметилсилилтрифлата в дихлорметане (297 мкл). Через 2 ч 30 мин реакционную смесь нейтрализуют прибавлением гидрокарбоната натрия в твердом состоянии. После фильтрования через Celite® реакционную смесь разбавляют дихлорметаном (400 мл). Органическую фракцию последовательно промывают 2%-м водным раствором гидрокарбоната натрия и водой, затем сушат над сульфатом натрия, фильтруют и далее упаривают досуха. Полученный остаток очищают хроматографией на колонке Sephadex® LH20 (190×3,2 см, дихлорметан/этанол, 1/1) с последующей хроматографией на колонке с силикагелем (циклогексан/этилацетат, 4/1) с получением 3,04 г соединения 78.
Rf = 0, 30, силикагель, циклогексан/этилацетат, 3/1.
Метил-(метил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-[(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)] 2 -(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-бензилоксикарбониламино-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозид (79)
К раствору соединения 78 (2,23 г, 0,623 ммоль) в смеси "дихлорметан/метанол", 2/3, (187 мл), содержащей цеолит 3 Å (78 мг), в атмосфере аргона при 0°C прибавляют 1 M раствор метилата натрия в метаноле (99,7 мкл). После выдерживания в течение 24 часов при комнатной температуре реакционную смесь нейтрализуют смолой Dowex AG 50 WX4 в H+-форме. Полученный после фильтрования и концентрирования остаток подвергают хроматографии на колонке Sephadex® LH20 (120×3 см, дихлорметан/этанол, 1/1) с последующей флэш-хроматографией на колонке с силикагелем (циклогексан/этилацетат, 100/0→66/34) с получением 1,80 г соединения 79.
Rf=0,38, силикагель, циклогексан/этилацетат, 3/1 об./об.
СХЕМА 17. Получение октасахаридов 80, 81, 82, 83, 84, 85, 86 и 87

Метил-(метил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-[(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)] 2 -(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (80)
Метил-(метил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (81)
Метил-(метил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (82)
Метил-(метил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-[(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)] 2 -(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (87)
К раствору соединения 79 (373 мг, 0,11 ммоль) в метаноле (14 мл) прибавляют фторид аммония (324 мг, 8,74 ммоль). После перемешивания в течение 20 часов при комнатной температуре реакционную смесь вносят в колонку с гелем Sephadex® LH20 (120×3 см, дихлорметан/этанол, 1/1 об./об.) с последующей флэш-хроматографией на колонке с силикагелем (толуол/ацетон, 1/0→7/3 об./об.) последовательно получают:
- соединение 80 (58,8 мг);
ТСХ: Rf=0,63, силикагель, толуол/ацетон, 65/35 об./об.;
- соединение 81 (44,4 мг);
ТСХ: Rf=0,53, силикагель, толуол/ацетон, 65/35 об./об.;
- соединение 82 (37,7 мг);
ТСХ: Rf=0,45, силикагель, толуол/ацетон, 65/35 об./об.;
- смесь соединения 83 и соединения 84 (54,0 мг);
- смесь соединения 85 и соединения 86 (48,3 мг);
- соединение 87 (26,6 мг);
ТСХ: Rf=0,14, силикагель, толуол/ацетон, 65/35 об./об.
Метил-(метил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (83)
Метил-(метил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-[(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)] 2 -(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (84)
Смесь соединений 83 и 84 (260 мг) очищают флэш-хроматографией на колонке с силикагелем (толуол/метанол, 100/0→85/15 об./об.) с получением соединения 83 (27,8 мг).
ТСХ: Rf=0,22, силикагель, толуол/метанол, 85/15 об./об.
Оставшиеся фракции снова очищают флэш-хроматографией на колонке с силикагелем (дихлорметан/метанол, 100/0→97/3 об./об.) с получением соединения 84 (45,3 мг).
ТСХ: Rf=0,13, силикагель, толуол/метанол, 85/15 об./об.
Метил-(метил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (85)
Метил-(метил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (86)
Смесь соединений 85 и 86 (135 мг) очищают способом ВЭЖХ на колонке с силикагелем C18 (Waters® Sunfire, 5 мкм, 150×19 мм, ацетонитрил/вода, 9/1 + трифторуксусная кислота, 0,1%) и последовательно получают:
- соединение 85 (32,6 мг), после эксклюзионной хроматографии (Sephadex® LH20, 120×3 см, дихлорметан/этанол, 1/1 об./об.);
масса: способ ИЭР, электроотрицательный режим: теоретическая масса = 2698,96; экспериментальная масса: 2698,55±0,65 а.е.м.;
- соединение 86 (26,5 мг), после эксклюзионной хроматографии (Sephadex® LH20, 120×3 см, дихлорметан/этанол, 1/1 об./об.);
масса: способ ИЭР, электроотрицательный режим: теоретическая масса = 2698,96; экспериментальная масса: 2698,95±1,05 а.е.м.
СХЕМА 18. Получение октасахарида 91

Метил-(метил-3,4-ди-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозид (88)
Соединение 81 (69 мг, 23,5 мкмоль) обрабатывают аналогично методике, описанной для синтеза соединения 28, с получением соединения 88 (85,1 мг) после эксклюзионной хроматографии (Sephadex® LH20, 120×3 см, дихлорметан/этанол, 1/1 об./об.).
ТСХ: Rf=0,62, силикагель, этилацетат/пиридин/уксусная кислота/вода, 17/9/2,2/5 об./об./об./об.
Метил-(метил-3,4-ди-O-бензил-2-O-аммонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-2-O-аммонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-2-O-аммонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-аммонийсульфонато-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-2-O-аммонийсульфонато-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-6-O-аммонийсульфонато-α-D-глюкопиранозид (89)
К раствору соединения 88 (85,1 мг, 21,1 мкмоль) в метаноле (2,7 мл) прибавляют фторид аммония (31,3 мг, 0,846 ммоль). После нагревания в течение 48 часов при 55°C реакционную смесь вносят в колонку с гелем Sephadex® LH20 (95×2 см) и элюируют N,N-диметилформамидом с получением соединения 89 (64 мг).
[α]D=19,4° (c=1,0; MeOH)
Метил-(3,4-ди-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-литийсульфонато-α-D-глюкопиранозил)-(1→4)-(3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-6-O-литийсульфонато-α-D-глюкопиранозид (90)
Соединение 89 (63,3 мг, 17,8 мкмоль) обрабатывают аналогично методике, описанной для синтеза соединения 29. После хроматографии на колонке с гелем Sephadex® LH20 (120×3 см, дихлорметан/этанол/вода, 50/50/1 об./об./об.) получают соединение 90 (49,8 мг).
[α]D=14,6° (c=1,0; MeOH)
Метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-амино-2-дезокси-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-амино-2-дезокси-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозид (91)
К раствору соединения 90 (7,6 мг, 2,6 мкмоль) в смеси "трет-бутанол/вода", 1/1 об./об., (516 мкл) при комнатной температуре последовательно прибавляют формиат аммония (21,2 мг, 0,33 мкмоль) и 10%-й палладий на угле (49,4 мг). После перемешивания в течение 4 часов реакционную смесь фильтруют (фильтр Millipore® LSWP, 5 мкм), вносят в колонку с гелем Sephadex® G-25 fine (95×2 см) и элюируют 0,2 M водным раствором NaCl. Фракции, содержащие требуемое соединение, объединяют, вносят в колонку с гелем Sephadex® G-25 fine (95×2 см) и элюируют водой. Полученное таким образом неочищенное соединение 91 (5,5 мг) используют в таком виде на следующей стадии.
СХЕМА 19. Получение октасахарида 95

Метил-(метил-3,4-ди-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-2-О-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-трет-бутилдифенилсилил-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозид (92)
Соединение 82 (16,5 мг, 5,6 мкмоль) обрабатывают аналогично методике, описанной для синтеза соединения 28, с получением соединения 92 (21,5 мг) после хроматографии на колонке с гелем Sephadex® LH20 (120×3 см, дихлорметан/этанол, 1/1 об./об.).
ТСХ: Rf=0,73, силикагель, этилацетат/пиридин/уксусная кислота/вода, 28/16/3,8/9 об./об./об./об.
Метил-(метил-2-O-аммонийсульфонато-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-2-O-аммонийсульфонато-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(6-O-аммонийсульфонато-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-2-O-аммонийсульфонато-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-2-O-аммонийсульфонато-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-6-O-аммонийсульфонато-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (93)
Соединение 92 (21,5 мг, 5,3 мкмоль) обрабатывают аналогично методике, описанной для синтеза соединения 89, с получением соединения 93 (21,5 мг) после эксклюзионной хроматографии (Sephadex® LH20, 95×2 см, N,N-диметилформамид).
ТСХ: Rf=0,63, силикагель, этилацетат/пиридин/уксусная кислота/вода, 11/7/1,6/4 об./об./об./об.
Метил-(3,4-ди-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-литийсульфонато-α-D-глюкопиранозил)-(1→4)-(3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-6-O-литийсульфонато-α-D-глюкопиранозид (94)
Соединение 93 (14,7 мг, 4,1 мкмоль) обрабатывают аналогично методике, описанной для синтеза соединения 31, с получением соединения 94 (13,0 мг) после эксклюзионной хроматографии (Sephadex® LH20, 95×2 см, дихлорметан/этанол/вода, 50/50/1 об./об./об.).
ТСХ: Rf=0,56, силикагель, этилацетат/пиридин/уксусная кислота/вода, 28/16/3,8/9 об./об./об./об.
Метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-амино-2-дезокси-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-амино-2-дезокси-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозид (95)
К раствору соединения 94 (13 мг, 4,4 мкмоль) в смеси "трет-бутанол/вода", 1/1 об./об., (883 мкл) прибавляют формиат аммония (36 мг, 0,57 ммоль) и 10%-й палладий на угле (34 мг). После перемешивания в течение 4 часов при комнатной температуре реакционную смесь фильтруют (фильтр Millipore® LSWP, 5 мкм) и концентрируют досуха. Остаток вносят в колонку с гелем Sephadex® G-25 fine (95×2 см) и элюируют 0,2 M водным раствором NaCl. Фракции, содержащие требуемое соединение, объединяют, вносят в колонку с гелем Sephadex® G-25 fine (95×2 см) и элюируют водой. Полученное таким образом неочищенное соединение 95 (2,5 мг) используют в таком виде на следующей стадии.
СХЕМА 20. Получение октасахарида 99
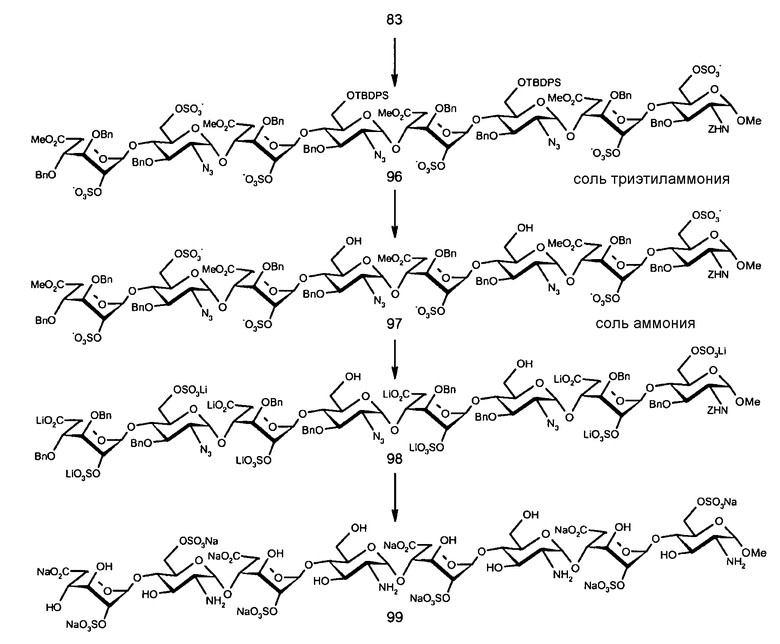
Метил-(метил-3,4-ди-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозил)-(1→4)-[(метил-3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)] 2 -3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозид (96)
Соединение 83 (35,1 мг, 12,0 мкмоль) обрабатывают аналогично методике, описанной для синтеза соединения 28, с получением соединения 96 (46,3 мг) после хроматографии на колонке с гелем Sephadex® LH20 (120×3 см, дихлорметан/этанол, 1/1 об./об.).
[α]D=111° (c=0,95; CH2Cl2)
Метил-(метил-2-O-аммонийсульфонато-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-(6-O-аммонийсульфонато-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-2-O-аммонийсульфонато-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-2-O-аммонийсульфонато-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-2-O-аммонийсульфонато-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-6-O-аммонийсульфонато-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (97)
Соединение 96 (45,0 мг, 11,2 мкмоль) обрабатывают аналогично методике, описанной для синтеза соединения 89, с получением соединения 97 (30,8 мг) после хроматографии на колонке с гелем Sephadex® LH20 (95×2 см, N,N-диметилформамид).
[α]D=14,7° (c=0,95; MeOH)
Метил-(3,4-ди-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-литийсульфонато-α-D-глюкопиранозил)-(1→4)-[(3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)] 2 -(метил-3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-6-O-литийсульфонато-α-D-глюкопиранозид (98)
Соединение 97 (27,1 мг, 7,6 мкмоль) обрабатывают аналогично методике, описанной для синтеза соединения 29, с получением соединения 98 (20,7 мг) после хроматографии на колонке с гелем Sephadex® LH20 (95×2 см, дихлорметан/этанол/вода, 50/50/1 об./об./об.).
[α]D=14,4° (c=1,01; MeOH)
Метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозил)-(1→4)-[(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-амино-2-дезокси-α-D-глюкопиранозил)-(1→4)] 2 -(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозид (99)
Соединение 98 (17,5 мг, 5,9 мкмоль) обрабатывают аналогично методике, описанной для синтеза соединения 91, с получением соединения 99 (9,5 мг).
Масса: способ ИЭР, электроотрицательный режим: теоретическая масса = 2081,38; экспериментальная масса: 1993,28±0,14 а.е.м. (идуроновые кислоты, наблюдаемые в COOH-форме).
СХЕМА 21. Получение октасахарида 104

Метил-(метил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-[(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)]-(1→4] 2 -(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-6-O-бензоил-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (100)
Раствор соединения 80 (355 мг, 0,117 ммоль), бензойный ангидрид (75,8 мг, 0,335 ммоль) и триэтиламин (47,3 мкл, 0,335 ммоль) в 1,2-дихлорэтане (5,6 мл) перемешивают при 60°C в течение 24 часов и затем в течение 64 часов при комнатной температуре. Реакционную смесь вносят в колонку с гелем Sephadex® LH20 (120×3 см) и элюируют смесью "дихлорметан/этанол", 1/1 об./об., с последующей флэш-хроматографией на колонке с силикагелем (толуол/ацетон, 100/0→85/15 об./об.) с получением соединения 100 (193,2 мг).
ТСХ: Rf=0,38, силикагель, циклогексан/этилацетат, 2/1 об./об.
Метил-(метил-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-[(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)] 2 -(метил-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-6-O-бензоил-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (101)
Соединение 100 (60,0 мг, 0,018 ммоль) обрабатывают аналогично методике, описанной для синтеза соединения 89, с получением соединения 101 (46,1 мг) после хроматографии на колонке с гелем Sephadex® LH20 (120×3 см, дихлорметан/этанол, 1/1 об./об.).
Масса: способ ИЭР, электроотрицательный режим: теоретическая масса = 2564,66; экспериментальная масса: 2563,66±0,19 а.е.м.
Метил-(метил-3,4-ди-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозил)-(1→4)-[(метил-3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозил)-(1→4)] 2 -(метил-3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-6-O-бензоил-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (102)
Соединение 101 (42,9 мг, 0,016 ммоль) обрабатывают аналогично методике, описанной для синтеза соединения 28, с получением соединения 102 (28,7 мг) после хроматографии на колонке Sephadex® LH20 (120×3 см, дихлорметан/этанол, 1/1 об./об.) и затем флэш-хроматографии на колонке с силикагелем C18 (40-60 мкм; A: метанол, вода, 5%, ацетат аммония, 23 мМ; B: ацетонитрил, метанол, 45%, вода, 5%, ацетат аммония, 17 мМ; A→B: 100/0→70/30) с последующим освобождением от соли на колонке Sephadex® LH20 (95×2 см, дихлорметан/этанол/вода, 50/50/1 об./об./об.).
Метил-(3,4-ди-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-литийсульфонато-α-D-глюкопиранозил)-(1→4)-[(3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-литийсульфонато-α-D-глюкопиранозил)-(1-4)] 2 -(3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-3-O-бензил-2-{[(бензилокси)карбонил]амино}-2-дезокси-α-D-глюкопиранозид (103)
Соединение 102 (28,7 мг, 7,5 мкмоль) обрабатывают аналогично методике, описанной для синтеза соединения 29, с получением неочищенного соединения 103 (17,3 мг).
Метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозил)-(1→4)-[(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозил)-(1-4)] 2 -(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-амино-2-дезокси-α-D-глюкопиранозид (104)
Соединение 103 (17,3 мг, 5,7 мкмоль) обрабатывают аналогично методике, описанной для синтеза соединения 91. Полученное таким образом неочищенное соединение 104 еще раз омыляют. К раствору неочищенного соединения 104 в смеси "тетрагидрофуран/метанол", 1/1 об./об., (506 мкл) при 0°C прибавляют 0,7 M раствор гидроксида лития в воде (202 мкл; в количестве, достаточном для получения конечной концентрации 0,2 M). После выдерживания в течение 1 часа при 0°C и затем в течение 16 часов при комнатной температуре реакционную смесь подвергают хроматографии на колонке для эксклюзионной хроматографии (Sephadex® G-25 fine, 95×2 см, 0,2 M раствор NaCl, затем Sephadex® G-25 fine, 95×2 см, вода) с получением соединения 104 (6,5 мг).
1H ЯМР [600 МГц] (D2O) δ аномерных протонов: 5,45; 5,44; 5,43; 5,26; 5,25; 5,24; 5,18; 4,98 м.д.
СХЕМА 22. Получение октасахарида 108
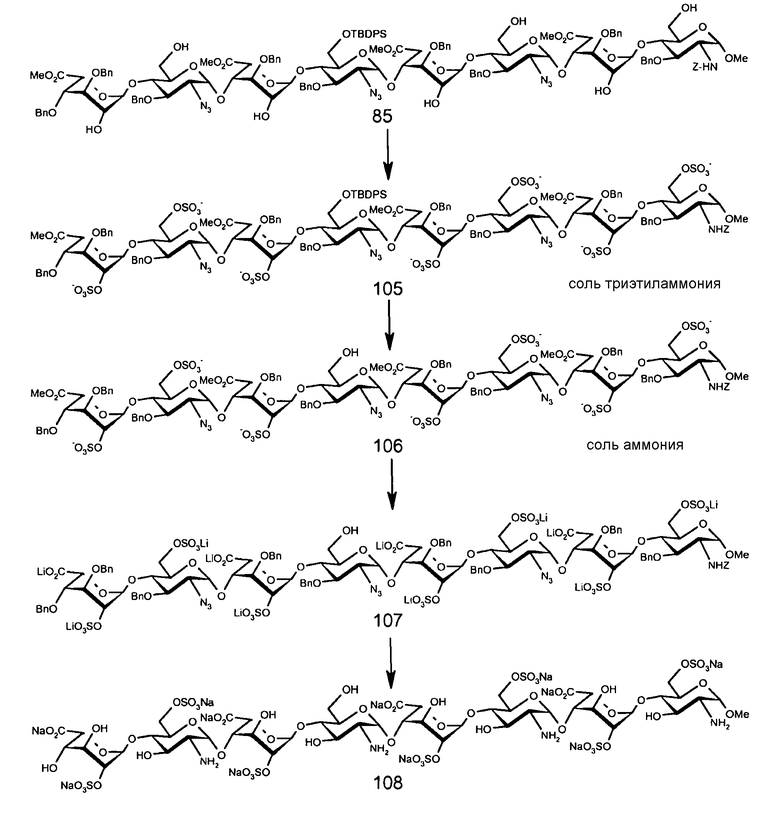
Метил-(метил-3,4-ди-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-6-O-трет-бутилдифенилсилил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозил)-(1→4)-(метил-3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-дезокси-2-[(бензилокси)карбонил]амино-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозид (105)
Соединение 85 (31,4 мг, 11,6 мкмоль) обрабатывают аналогично методике, описанной для синтеза соединения 28, с получением соединения 105 (40,2 мг) после хроматографии на колонке с гелем Sephadex® LH20 (120×3 см, дихлорметан/этанол/вода, 50/50/1 об./об./об.).
Метил-(метил-2-O-аммонийсульфонато-3,4-ди-O-бензил-α-L-идопиранозилуронат)-(1→4)-(6-O-аммонийсульфонато-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-2-O-аммонийсульфонато-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-2-O-аммонийсульфонато-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-(6-O-аммонийсульфонато-2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(метил-2-O-аммонийсульфонато-3-O-бензил-α-L-идопиранозилуронат)-(1→4)-6-O-аммонийсульфонато-3-O-бензил-2-[(бензилокси)карбонил]амино-2-дезокси-α-D-глюкопиранозид (106)
Соединение 105 (38,4 мг, 9,68 мкмоль) обрабатывают аналогично методике, описанной для синтеза соединения 89, с получением соединения 106 (28,4 мг) после хроматографии на колонке с гелем Sephadex® LH20 (95×2 см, N,N-диметилформамид).
Rf=0,21 (AcOEt-пиридин-AcOH-H2O, 28/16/3,8/9).
Метил-(3,4-ди-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-литийсульфонато-α-D-глюкопиранозил)-(1→4)-(3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-α-D-глюкопиранозил)-(1→4)-(3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-литийсульфонато-α-D-глюкопиранозил)-(1→4)-(3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-3-O-бензил-2-дезокси-2-[(бензилокси)карбонил]амино-6-O-литийсульфонато-α-D-глюкопиранозид (107)
Соединение 106 (28,4 мг, 7,62 мкмоль) обрабатывают аналогично методике, описанной для синтеза соединения 89, с получением соединения 107 (28,0 мг) после хроматографии на колонке с гелем Sephadex® LH20 (95×2 см, дихлорметан/этанол/вода, 50/50/1 об./об./об.).
Rf=0,12 (AcOEt-пиридин-AcOH-H2O, 28/16/3,8/9).
Метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-амино-2-дезокси-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозид (108)
Соединение 107 (5,8 мг, 2,85 мкмоль) обрабатывают аналогично методике, описанной для синтеза соединения 91 с получением соединения 108 (2,5 мг), используемого в таком виде на следующей стадии.
1H ЯМР [600 МГц] (D2O) δ аномерных протонов: 5,45; 5,44; 5,42; 5,26; 5,25; 5,24; 5,17; 5,03 м.д.
СХЕМА 23. Получение октасахарида 111

Метил-(метил-3,4-ди-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозил)-[(1→4)-(метил-3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозил)] 2 -(1→4)-(метил-3-O-бензил-2-O-триэтиламмонийсульфонато-α-L-идопиранозилуронат)-(1→4)-3-O-бензил-2-бензилоксикарбониламино-2-дезокси-6-O-триэтиламмонийсульфонато-α-D-глюкопиранозид (109)
Соединение 87 (37,0 мг, 0,15 ммоль) сушат совместной отгонкой с N,N-диметилформамидом (3×1,4 мл) и затем растворяют в N,N-диметилформамиде (1,4 мл). К данному раствору прибавляют комплекс "триоксид серы-триэтиламин" (109 мг, 6,01 ммоль). Смесь перемешивают в течение 16 часов при 55°C без доступа света, затем избыток реактива нейтрализуют метанолом (25 мкл). Реакционную смесь вносят в колонку Sephadex® LH20 (120×3 см) и элюируют смесью "дихлорметан/этанол", 1/1, с получением соединения 109 (59,8 мг).
Rf=0,26, силикагель, этилацетат/пиридин/уксусная кислота/вода, 28/16/3,8/9.
Метил-(3,4-ди-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-литийсульфонато-α-D-глюкопиранозил)-[(1→4)-(3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-(2-азидо-3-O-бензил-2-дезокси-6-O-литийсульфонато-α-D-глюкопиранозил)] 2 -(1→4)-(3-O-бензил-2-O-литийсульфонато-α-L-идопиранозилуронат лития)-(1→4)-3-O-бензил-2-бензилоксикарбониламино-2-дезокси-6-O-литийсульфонато-α-D-глюкопиранозид (110)
К раствору соединения 109 (57,3 мг, 13,7 мкмоль) в смеси "тетрагидрофуран/метанол", 1/1 об./об., (2,2 мл) при 0°C прибавляют 0,7 M раствор гидроксида лития в воде (0,88 мл; в количестве, достаточном для получения конечной концентрации 0,2 M). После выдерживания в течение 1 часа при 0°C и затем в течение 16 часов при комнатной температуре реакционную смесь вносят в колонку Sephadex® LH20 (120×3 см) и элюируют смесью "дихлорметан/этанол"/вода, 50/50/1 об./об./об., с получением соединения 110 (38,1 мг).
[α]D=13,1° (c=1,0; MeOH)
Метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозил)-[(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозил)] 2 -(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-амино-2-дезокси-6-O-натрийсульфонато-α-D-глюкопиранозид (111)
К раствору соединения 110 (40 мг, 12,8 мкмоль) в смеси "трет-бутанол/вода", 1/1 об./об., (2,6 мл) прибавляют формиат аммония (105 мг, 1,67 ммоль) и 10%-й палладий на угле (260 мг). После перемешивания в течение 4 часов при комнатной температуре реакционную смесь фильтруют (фильтр Millipore® LSWP, 5 мкм) и концентрируют досуха. Остаток вносят в колонку с гелем Sephadex® G-25 fine (95×2 см) и элюируют 0,2 M водным раствором NaCl. Фракции, содержащие требуемое соединение, объединяют, вносят в колонку с гелем Sephadex® G-25 fine (95×2 см) и элюируют водой. Полученное таким образом неочищенное соединение 111 (48,7 мг) используют в таком виде на следующей стадии.
Масса: способ ИЭР, электроотрицательный режим: теоретическая масса = 2285,47; экспериментальная масса: 2197,20±0,34 а.е.м. (идуроновые кислоты, наблюдаемые в COOH-форме).
Примеры соединений по настоящему изобретению
ПРИМЕР 1. Метил-(4-O-пропил-2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-[(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил-(1→4)] 2 -(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозид (соединение № 1)
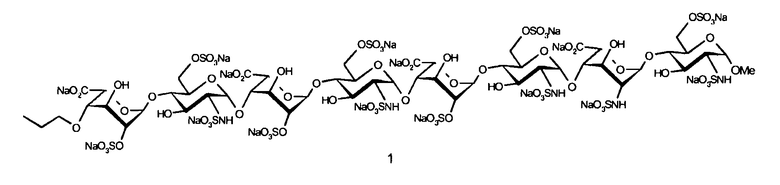
К раствору соединения 30 (180 мг, 0,077 ммоль) в свежеприготовленном насыщенном водном растворе гидрокарбоната натрия (15 мл, 100 мл/ммоль) при 0°C в атмосфере аргона прибавляют гидрокарбонат натрия в твердом состоянии (1,17 г, 13,9 ммоль) и затем порциями прибавляют в течение 30 минут комплекс "пиридин-триоксид серы" (985 мг, 6,19 ммоль). После выдерживания в течение 16 часов при комнатной температуре реакционную смесь вносят в колонку Sephadex® G-25 fine (90×3 см) и элюируют 0,2 M водным раствором NaCl. Фракции, содержащие требуемое соединение, объединяют, вносят в колонку Sephadex® G-25 fine (90×3 см) и элюируют водой. После концентрирования фракций, содержащих требуемое соединение, получают 200 мг соединения 1.
1H ЯМР [600 МГц] (D2O) δ аномерных протонов: 5,45; 5,42 (2H); 5,22; 5,21; 5,20; 5,18; 5,03 м.д.
Масса: способ ИЭР, электроотрицательный режим: теоретическая масса = 2735,72; экспериментальная масса: 2734 а.е.м.
ПРИМЕР 2. Метил-(4-O-пропил-2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-[(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил-(1→4)] 3 -(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозид (соединение № 2)

Соединение 37 (29,5 мг, 11,56 мкмоль) обрабатывают аналогично методике, описанной для синтеза по примеру 1, с получением соединения 2 (7,4 мг) после очистки ионообменной хроматографией (колонка SAX, условия: 0,5 мл/мин, A: H2O, B: 2 M раствор NaCl, градиент B от 30 до 90% в течение 30 мин) с последующей хроматографией на колонке с гелем Sephadex® G-25 fine (54×1,7 см, вода).
1H ЯМР [600 МГц] (D2O) δ аномерных протонов: 5,45; 5,42; 5,41 (2H); 5,22; 5,21 (2H); 5,20; 5,18; 5,03 м.д.
Масса: способ ИЭР, электроотрицательный режим: теоретическая масса = 3401,12; экспериментальная масса: 3400,40±0,76 а.е.м.
ПРИМЕР 3. [Метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-[(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)] 2 -2-O-натрийсульфонато-α-L-идопиранозид]уронат натрия (соединение № 3)

Неочищенное соединение 55 (48,7 мг) обрабатывают аналогично методике, описанной для синтеза по примеру 1, с получением соединения 3 (37,6 мг).
1H ЯМР [600 МГц] (D2O) δ аномерных протонов: 5,43 (2H); 5,35; 5,25; 5,24; 5,19; 5,18; 5,09 м.д.
ПРИМЕР 4. Метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозид (соединение № 4)

Соединение 91 (5,5 мг, 2,64 мкмоль) обрабатывают аналогично методике, описанной для синтеза по примеру 1, с получением соединения 4 (4,5 мг).
1H ЯМР [600 МГц] (D2O) δ аномерных протонов: 5,44; 5,40; 5,31; 5,25; 5,24; 5,22; 5,16; 5,03 м.д.
Масса: способ ИЭР, электроотрицательный режим: теоретическая масса = 2489,55; экспериментальная масса: 2465,63±0,64 а.е.м.
ПРИМЕР 5. Метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозид (соединение № 5)
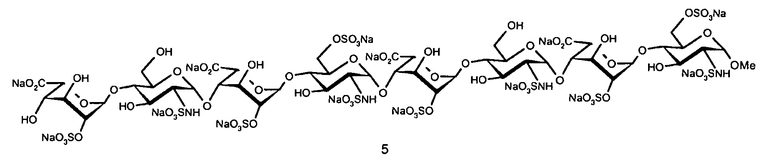
Соединение 95 (2,5 мг, 1,2 мкмоль) обрабатывают аналогично методике, описанной для синтеза по примеру 1, с получением соединения 5 (1,9 мг).
1H ЯМР [600 МГц] (D2O) δ аномерных протонов: 5,45; 5,43; 5,33; 5,25; 5,23; 5,21; 5,16; 5,05 м.д.
ПРИМЕР 6. Метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозид (соединение № 6)

Соединение 99 (8,9 мг, 4,28 мкмоль) обрабатывают аналогично методике, описанной для синтеза по примеру 1, с получением соединения 6 (7,3 мг).
1H ЯМР [600 МГц] (D2O) δ аномерных протонов: 5,46; 5,32 (2H); 5,26; 5,25; 5,21; 5,20; 5,05 м.д.
Масса: способ ИЭР, электроотрицательный режим: теоретическая масса = 2489,55; экспериментальная масса: 2488,00±1,5 а.е.м.
ПРИМЕР 7. Метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозид (соединение № 7)
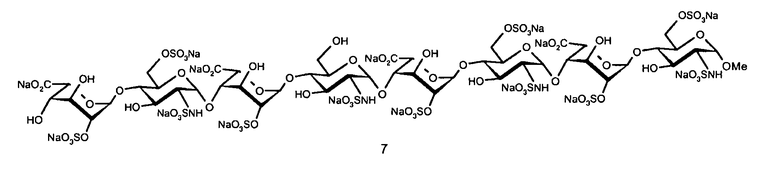
Соединение 108 (3,7 мг, 1,42 мкмоль) обрабатывают аналогично методике, описанной для синтеза по примеру 1, с получением соединения 7 (1,8 мг).
1H ЯМР [600 МГц] (D2O) δ аномерных протонов: 5,46; 5,42; 5,31; 5,26; 5,24; 5,22; 5,18; 5,03 м.д.
ПРИМЕР 8. Метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-[(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)] 2 -(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-6-O-натрийсульфонато-2-(сульфонато)амино-α-D-глюкопиранозид (соединение № 8)

Соединение 111 (42 мг, 18,4 мкмоль) обрабатывают аналогично методике, описанной для синтеза по примеру 1, с получением соединения 8 (44,1 мг).
1H ЯМР [600 МГц] (D2O) δ аномерных протонов: 5,45; 5,44; 5,25; 5,24 (2H); 5,20; 5,04 м.д.
Масса: способ ИЭР, электроотрицательный режим: теоретическая масса = 2693,84; экспериментальная масса: 2692,97±0,18 а.е.м.
ПРИМЕР 9. Метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонато)амино-α-D-глюкопиранозил)-[(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)] 2 -(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозид (соединение № 9)
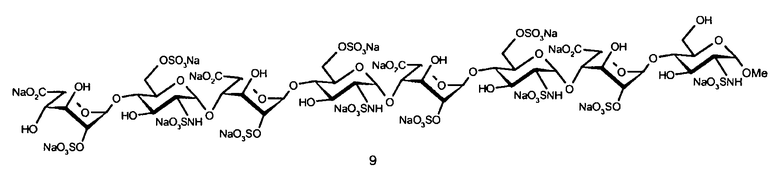
Соединение 104 (6,5 мг, 2,98 мкмоль) обрабатывают аналогично методике, описанной для синтеза по примеру 1, с получением соединения 9 (6,0 мг).
1H ЯМР [600 МГц] (D2O) δ аномерных протонов: 5,44 (2H); 5,43; 5,22 (2H); 5,19; 5,18; 5,05 м.д.
Масса: способ ИЭР, электроотрицательный режим: теоретическая масса = 2591,60; экспериментальная масса: 2591,80±0,33 а.е.м.
Соединения по настоящему изобретению были объектами фармакологических испытаний, позволивших определить их агонистическое действие на рецепторы FGF и их активность в отношении ангиогенеза, а также в отношении постишемической реваскуляризации.
Модель ангиогенеза in vitro: специфическая активность в отношении FGF2
Модель ангиогенеза in vitro соответствует перегруппировке клеток венозного эндотелия человека на биологической матрице. Матрицу реализуют, внося в каждую из лунок 96-луночного планшета (Becton Dickinson 353872) 60 мкл реактива Matrigel®, разбавленного в соотношении 1/3 (Growth factor reduced Matrigel® (реактив Matrigel®, восстанавливающий фактор роста): Becton Dickinson 356230) в коллагене (коллаген хвоста крысы, тип I: Becton Dickinson 354249). Биологическая матрица затвердевает в течение 1 часа при 37°C.
Клетки венозного эндотелия человека (HUVEC, позиция по каталогу: C-12200-Promocell) засевали на биологической матрице из расчета 7800 клетка/лунка в 120 мкл среды EBM® (Endothelial Basal Medium (эндотелиальная основная питательная среда), Lonza C3121) + 2% SVF (эмбриональная телячья сыворотка - Lonza) + 10 мкг/мл hEGF (Epidermal Growth Factor Humaine Recombinante (рекомбинантный эпидермальный фактор роста человека) - Lonza). Клетки стимулировали посредством FGF2 (R&D Systems/234-FSE-0 50) в концентрации 10 нг/мл или соединениями по настоящему изобретению в течение 18 часов при 37°C в атмосфере с 5% CO2. Через 24 часа клетки наблюдали под микроскопом (объектив с 4-кратным увеличением) и осуществляли анализ длин псевдотубул посредством программы визуализации (BIOCOM-logiciel Visiolab 2000).
В этом тесте на ангиогенез in vitro соединения по настоящему изобретению показали специфическую активность в интервале от 10-6 М до 10-12 M. Например, соединения №№ 1 и 7 являются активными при 10-6 M.
Соединение 10 следующей формулы:

испытанное в виде соли натрия, также показало активность в этом тесте на ангиогенез in vitro.
В то же время, в испытании с клетками in vitro было показано, что октасахарид № 8 по настоящему изобретению, гептасахарид № 3 и декасахарид № 2 являются более хорошими активаторами FGF-2, чем их гексасахаридный аналог (соединение, описанное C. Tabeur et al. в Bioorg. & Med. Chem., 1999, 7, 2003-2012). Кроме того, большая часть других октасахаридных соединений по настоящему изобретению, таких как, например, соединение № 7, обладают такой же активностью, что и октасахарид № 8 в модели in vitro.
Модель имплантата на целлюлозе у мышей
Эта модель представляет собой адаптацию модели, описанной Andrade et al. (Microvascular Research, 1997, 54, 253-61), с целью испытаний фармакологических соединений, способных активировать появление ангиогенеза.
Животных (близкородственных белых мышей BALB/c J) анестезировали введением внутрибрюшинно смеси "ксилазин (Rompun®, 10 мг/кг)/кетамин (Imalgene 1000, 100 мг/кг)". Спину животного брили и дезинфицировали средством Héxomédine®. На спине мыши создавали воздушный мешок инъекцией подкожно 5 мл стерильного воздуха. В верхней части спины животного выполняли разрез приблизительно 2 см длиной для введения имплантата из стерильной целлюлозы (диск диаметром 1 см, толщиной 2 мм, Cellspon®, позиция по каталогу 0501), пропитанного 50 мкл стерильного раствора, содержащего испытуемое соединение. Затем разрез зашивали и дезинфицировали средством Héxomédine®.
В последующие после внедрения имплантата дни мышам вводили в имплантат испытуемое соединение инъекцией чрескожно (50 мкл/имплантат/день) после ингаляционной анестезии (5%-й изофлюран (Aerrane®, Baxter)).
Через семь дней после внедрения губки мышей умерщвляли введением внутрибрюшинно летальной дозы пентобарбитала натрия (CEVA santé animale). Затем для изъятия кожи и губки кожу разрезали на расстоянии приблизительно 1 см вокруг губки, избегая шва. Далее губку разрезали на несколько кусков и помещали в пробирки Ribolyser®, содержащие 1 мл лизирующего буферного раствора (Cell Death Detection ELISA, Roche). Пробирки перемешивали последовательно 4 раза в течение 20 секунд при режиме 4 на измельчителе клеток (FastPrep® FP 120). Затем пробирки центрифугировали в течение 10 минут при 2000 g и 20°C и надосадочные жидкости замораживали при -20°C перед последующим количественным определением гемоглобина. В день анализа после размораживания пробирки снова центрифугировали и определяли концентрацию гемоглобина с реактивом Драбкина (Sigma, об./об.) на спектрофотометре при 405 нм по сравнению с эталонной серией бычьего гемоглобина (Sigma).
Концентрацию гемоглобина в каждом образце выражали в мг/мл соответственно полиномиальной регрессии, полученной исходя из эталонной серии. Результаты выражали как среднее значение (± СКО) для каждой группы. Различия между группами проверяли методом ANOVA с последующей проверкой по критерию Даннетта относительно квадратного корня значений.
В этом тесте in vivo соединения по настоящему изобретению показали специфическую активность в интервале от 5 до 45 нг/сайт. Например, соединения №№ 1 и 7 являются активными при концентрации 45 нг/сайт.
Таким образом, представляется, что соединения по настоящему изобретению обладают агонистической активностью в отношении рецепторов FGF и активностью в отношении ангиогенеза, а также в отношении постишемической реваскуляризации. Таким образом, эти соединения могут быть использованы для получения лекарственных средств, в частности лекарственных средств, приемлемых для лечения болезней, требующих активации рецепторов FGF, или лекарственных средств, приемлемых при патологиях, требующих активации ангиогенеза и постишемической реваскуляризации.
Таким образом, согласно другому из аспектов настоящее изобретение относится к лекарственным средствам, содержащим соединение формулы (I)/(I') или соединение 10, или их фармацевтически приемлемые соли.
В более общем случае, настоящее изобретение относится к лекарственным средствам, содержащим соединение формулы (I):
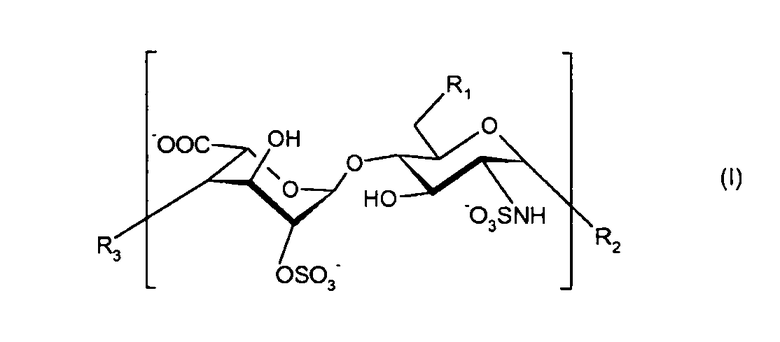
где
- R1 представляет собой -OSO3 - или гидроксигруппу;
- R2 представляет собой -O-алкил или моносахарид формулы (II), где R представляет собой алкил:
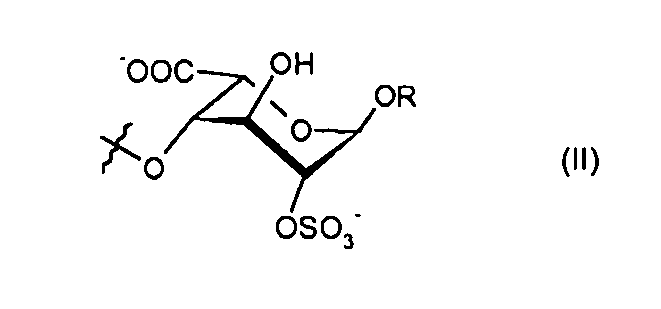
- R3 представляет собой дисахарид формулы (III):

где
- R4 представляет собой -OSO3 - или гидроксигруппу;
- R5 представляет собой дисахарид формулы (IV):
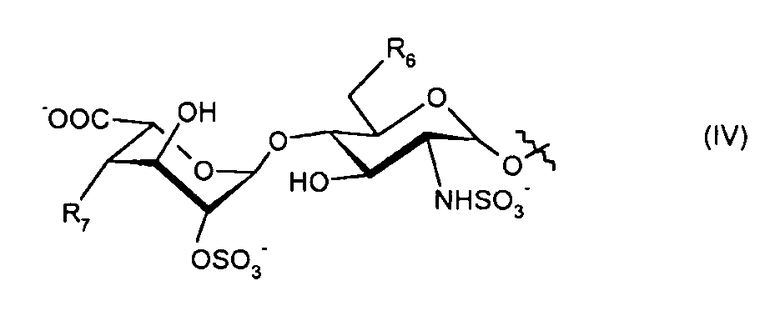
где
- R6 представляет собой -OSO3 - или гидроксигруппу;
- R7 представляет собой гидроксигруппу или моносахарид формулы (V), приведенной далее, или дисахарид формулы (VI):

где
- R8 представляет собой -OSO3 - или гидроксигруппу;
- R9 представляет собой гидроксигруппу или -O-алкил, или дисахарид формулы (VII):
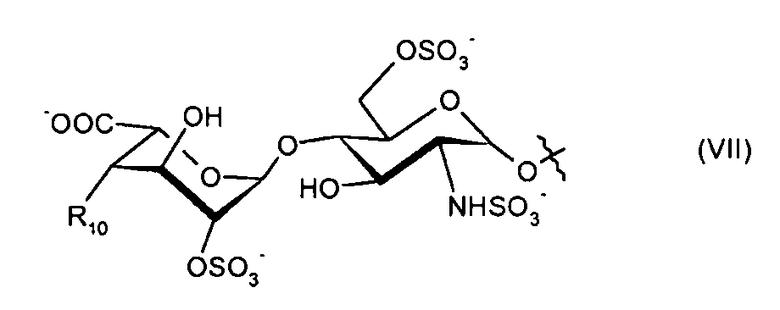
где R10 представляет собой -O-алкил;
при условии, что: R9 представляет собой гидроксигруппу или -O-алкил, если R2 представляет собой моносахарид формулы (II), определенной ранее; R7 представляет собой дисахарид определенной ранее формулы (VI), если R2 представляет собой -O-алкил; а R1, R4, R6 и R8 не представляют собой гидроксигруппы одновременно.
Такие соединения включают определенные ранее соединения формулы (I)/(I'), а также определенный ранее гептасахарид 10, описанный в US 2006/0079483 A1.
Такие лекарственные средства находят применение в терапии, в частности при лечении ишемии (ишемии сердца, артериальной ишемии нижних конечностей), при лечении заболеваний, связанных со стенозом или обструкцией артерий, или артериитов, при лечении стенокардии, облитерирующего тромбангиита, атеросклероза, для подавления рестеноза после ангиопластики или эндартерэктомии, для заживления ран, при регенерации мышц, для выживания миобластов, при лечении периферической нейропатии, послеоперационных повреждений нервов, нейрогенной недостаточности, такой как болезнь Паркинсона, болезнь Альцгеймера, прионная болезнь и дегенерация нейронов у алкоголиков, при лечении деменции, для улучшения выживания биоинженерных трансплантатов поджелудочной железы у больных диабетом, для улучшения реваскуляризации крупных имплантатов и выживания трансплантатов, при лечении дегенерации сетчатки, пигментного ретинита, остеоартрита, преэклампсии или повреждений сосудов и острого респираторного дистресс-синдрома, при восстановлении хрящей, при восстановлении и защите костей, при восстановлении и защите волосяных фолликулов и для защиты и регулирования роста капилляров.
Ишемия представляет собой уменьшение артериальной циркуляции в органе, вызывающее понижение концентрации кислорода в поврежденных тканях. В механизмах постишемической реваскуляризации играют роль два главных механизма: ангиогенез и артериогенез. Ангиогенез представляет собой процесс образования новых капиллярных сосудов на основе ранее существовавших сосудов. Артериогенез способствуют развитию (увеличению размеров и крупности) сосудов, расположенных вокруг зоны, пораженной ишемией или лишенной сосудов.
Среди факторов роста, вовлеченных в процессы реваскуляризации, наиболее широко описана группа FGF, в частности FGF-2 (Post, M.J., Laham, R., Sellke, F.W. & Simons, M. Therapeutic angiogenesis in cardiology using protein formulations. Cardiovasc. Res. 49, 522-31, 2001).
Таким образом, FGF2 и его рецепторы представляют собой очень подходящие цели для терапии, направленной на индуцирование процессов ангиогенеза и артериогенеза (Khurana, R. & Simons, M. Insights from angiogenesis trials using fibroblast growth factor for advanced arteriosclerotic disease. Trends Cardiovasc. Med. 13, 116-22, 2003).
Одно из применений соединений по настоящему изобретению представляет собой постишемическое лечение после окклюзии сосудов в области сердца или периферических артерий. Касательно лечения ишемии сердца одно из наиболее многообещающих клинических испытаний представляло собой клиническое испытание, при котором FGF-2 был заключен в альгинатные микросферы в присутствии гепарина (Laham, R.J. et al. Local perivascular delivery of basic fibroblast growth factor in patients undergoing coronary bypass surgery: results of a phase I randomized, double-blind, placebo-controlled trial. Circulation 100, 1865-71, 1999). Данные микросферы имплантировали рядом с ишемическим очагом на уровне миокарда. Через 90 дней у всех больных, прошедших лечение с применением FGF2, отсутствовали какие-либо симптомы ишемии сердца. По сравнению с этим в контрольной группе у 3 из 7 больных через 90 дней сохранились стойкие симптомы, а 2 больным были сделаны хирургические операции на сосудах. Интересно, что полезный эффект терапии сохранился спустя 3 года наблюдений. Данные наблюдения дают основания полагать, что соединения, имитирующие FGF2, могут обеспечивать действенную терапию при лечении последствий ишемии сердца.
При лечении стеноза коронарных артерий были осуществлены три клинических испытания по инъекции FGF2 в коронарную артерию (Laham, R.J. et al. Intracoronary basic fibroblast growth factor (FGF-2) in patients with severe ischemie heart disease: results of a phase I open-label dose escalation study. J. Am. Coll. Cardiol. 36, 2132-9, 2000; Simons, M. et al. Pharmacological treatment of coronary artery disease with recombinant fibroblast growth factor-2: double-blind, randomized, controlled clinical trial. Circulation, 105, 788-93, 2002; Unger, E.F. et al. Effects of a single intracoronary injection of basic fibroblast growth factor in stable angina pectoris. Am. J. Cardiol. 85, 1414-9, 2000). Результаты трех испытаний показали, что интракоронарные инфузии FGF2 хорошо переносятся и значительно улучшают состояние больных. Таким образом, соединения, описанные в настоящем изобретении, могут находить применение при лечении заболеваний, связанных со стенозом коронарных артерий, и, в частности, при лечении стенокардии.
Болезни дистальных артерий и, в частности, артерииты нижних конечностей возникают вследствие хронической обструкции артериол, снабжающих кровью крайние точки. Такие патологии касаются, главным образом, нижних конечностей. В клиническом испытании I фазы больные с патологиями периферических артерий, вызывающими хромоту, получали инъекции FGF2 (Lazarous, D.F. et al., Basic fibroblast growth factor in patients with intermittent claudication: results of a phase I trial. J. Am. Coll. Cardiol. 36, 1239-44, 2000). В данном случае FGF2 хорошо переносился такими больными, при этом клинические данные указывают на благоприятное действие FGF2, в частности, в отношении улучшения ходьбы. Упомянутые клинические данные указывают на то, что соединения по настоящему изобретению представляют собой действенное терапевтическое средство для лечения болезней, связанных с обструкцией дистальных артерий.
Болезнь Бюргера или облитерирующий тромбангиит поражает дистальные сосудистые структуры и характеризуется дистальным артериитом ног с болями и изъязвлениями. В данном случае индукция ангиогенеза и васкулогенез могут представлять собой терапию при такой патологии. Соединения по настоящему изобретению обеспечивают действенную терапию при облитерирующем тромбангиите.
Периферическая нейропатия представляет собой аксональное или демиелинизирующее поражение двигательного и/или чувствительного периферического нерва, которое вызывает потерю чувствительности дистальных членов. Одно из наиболее серьезных вторичных осложнений диабета представляет собой хроническое развитие периферической нейропатии. В данном случае было показано, что FGF2 индуцировал регенерацию аксонов, что может обеспечивать действенную терапию при лечении повреждений периферических нервов и, таким образом, при периферической нейропатии (Basic fibroblast growth factor isoforms promote axonal elongation and branching of adult sensory neurons in vitro. Klimaschewski L., Nindl W., Feurle J., Kavakebi P., Kostron H. Neuroscience. 2004; 126(2):347-53). Благодаря агонистической активности в отношении рецепторов FGF соединения по настоящему изобретению могут обеспечивать действенное лечение при периферической нейропатии здоровых лиц и больных диабетом.
Четко установлено, что FGF2 представляет собой активатор нервных клеток в ходе развития. Недавно полученные результаты дают основания полагать, что FGF2 может быть также основным фактором для стимуляции регенерации нейронов у взрослых (Sapieha P.S., Peltier M., Rendahl K.G., Manning W.C., Di Polo A., Fibroblast growth factor-2 gene delivery stimulates axon growth by adult retinal ganglion cells after acute optic nerve injury. Mol. Cell. Neurosci. 2003, Nov; 24(3):656-72.). Благодаря своей агонистической активности в отношении рецепторов FGF соединения по настоящему изобретению могут обеспечивать действенную терапию при устранении послеоперационных повреждений нервов, устранении нейрогенной недостаточности, такой как болезнь Паркинсона, болезнь Альцгеймера, прионная болезнь, дегенерация нейронов у алкоголиков, или в случае деменции.
Пролиферация и миграция клеток гладких мышц сосудов способствуют гипертрофии интимы артерий и играет, таким образом, определяющую роль в атеросклерозе и рестенозе после ангиопластики и эндартерэктомии. Было показано, что ангиогенный фактор VEGF значительно уменьшал утолщение интимы, ускоряя реэндотелиализацию (Van Belle, E., Maillard, L., Tio, F.O. & Isner, J.M. Accelerated endothelialization by local delivery of recombinant human vascular endothelial growth factor reduces in-stent intimal formation. Biochem. Biophys. Res. Commun. 235, 311-6, 1997). Таким образом, соединения по настоящему изобретению, обладающие проангиогенной активностью, могут быть приемлемыми для лечения атеросклероза и подавления рестеноза после ангиопластики или эндартерэктомии.
Сосудистая сеть имеет существенное значение для развития и сохранения тканей. Способствуя доставке питательных веществ, кислорода и клеток, кровеносные сосуды помогают поддерживать функциональную и структурную целостность тканей. В данном случае ангиогенез и васкулогенез позволяют сохранять и осуществлять перфузию тканей после ишемии. Ангиогенные факторы роста, такие как VEGF и FGF2, благоприятствуют, таким образом, реваскуляризации для регенерации тканей. Соединения по настоящему изобретению могут обеспечивать действенное лечение при регенерации мышц.
Процессы мышечной регенерации дистрофически измененных или нормальных мышц зависят от доставки цитокинов и ангиогенных факторов роста на локальном уровне (Fibbi, G., D'Alessio, S., Pucci, M., Cerletti, M. & Del Rosso, M. Growth factor-dependent proliferation and invasion of muscle satellite cells require the cell-associated fibrinolytic System. Biol. Chem. 383, 127-36, 2002). Было сделано предположение, что система FGF представляет собой систему, являющуюся критической для регенерации мышц, выживания и пролиферации миобластов (Neuhaus, P. et al. Reduced mobility of fibroblast growth factor (FGF)-deficient myoblasts might contribute to dystrophic changes in the musculature of FGF2/FGF6/mdx triple-mutant mice. Mol. Cell. Biol. 23, 6037-48, 2003). FGF2, а также соединения по настоящему изобретению, могут быть использованы для содействия регенерации сердца. Таким образом, они могут улучшать перфузию миокарда после ишемии (Hendel, R.C. et al. Effect of intracoronary recombinant human vascular endothelial growth factor on myocardial perfusion: evidence for a dose-dependent effect. Circulation, 101, 118-21, 2000), а также выживание и распространение трансплантированных миобластов, в частности, при мышечной дистрофии Дюшенна.
Ангиогенез представляет собой феномен, имеющий существенное значение в ходе заживления ран кожи. Новообразованные сосуды доставляют кислород и питательные вещества, необходимые для восстановления тканей. В случае больных диабетом заживление представляет собой медленный и затрудненный процесс, при котором имеет место недостаточность ангиогенеза. Факторы FGF относятся к факторам роста, в наибольшей степени вовлеченным в процессы ангиогенеза в ходе заживления. Некоторые факторы FGF в значительной степени сверхэкспрессируются в клетках кожи после ранения кожи. Благодаря своей агонистической активности в отношении рецепторов FGF соединения по настоящему изобретению могут обеспечивать действенную терапию при заживлении в случае здоровых лиц и больных диабетом.
Трансплантация биоинженерных эквивалентов поджелудочной железы представляет собой многообещающую технологию для лечения некоторых типов диабета. На крысах, больных диабетом, было показано, что васкуляризация биоинженерных эквивалентов поджелудочной железы была более значительной в случае, когда поджелудочная железа была насыщена микросферами, содержавшими FGF2 (Sakurai, Tomonori; Satake, Akira, Sumi, Shoichiro, Inoue, Kazutomo, Nagata, Natsuki, Tabata, Yasuhiko. The Efficient Prevascularization Induced by Fibroblast Growth Factor 2 With a Collagen-Coated Device Improves the Cell Survival of a Bioartificial Pancreas. Pancreas. 28(3):e70-e79, April, 2004). Таким образом, такая реваскуляризация улучшает выживание имплантированных биоинженерных эквивалентов поджелудочной железы и, следовательно, выживание трансплантатов. Благодаря своей агонистической активности в отношении рецепторов FGF соединения по настоящему изобретению могут обеспечивать действенную терапию для улучшения выживания биоинженерных трансплантатов поджелудочной железы у больных диабетом и, в более общем случае, для улучшения реваскуляризации крупных имплантатов и, следовательно, для выживания трансплантатов.
Пигментный ретинит представляет собой патологию, вызывающую прогрессирующую дегенерацию сетчатки, характеризующуюся дегенерацией фоторецепторов и облитерацией сосудов сетчатки. Lahdenranta et al. (An anti-angiogenic state in mice and humans with retinal photoreceptor cell degeneration. Proc. Natl. Acad. Sci. USA, 98, 10368-73, 2001) предположили, что ангиогенные факторы роста регулируют невральную координацию и васкуляризацию, связанную с сетчаткой, функционируя одновременно в качестве факторов выживания фоторецепторов и в качестве регуляторов эндотелиальных клеток. В данном случае инъекция FGF2 в стекловидное тело замедляет дегенерацию фоторецепторов, воздействуя на выживание и ангиогенез в сетчатке (Faktorovich, E.G., Steinberg, R.H., Yasumura, D., Matthes, M.T. & LaVail, M.M. Basic fibroblast growth factor and local injury protect photoreceptors from light damage in the rat. J. Neurosci. 12, 3554-67, 1992). Данные наблюдения показывают перспективность соединений по настоящему изобретению для терапии при дегенерации сетчатки и, в частности, в случае пигментного ретинита.
Касательно остеоартрита осуществлено множество исследований по восстановлению разрушенных суставных хрящей. В данном случае имеются сообщения, что FGF2 стимулировал пролиферацию и дифференцировку хондроцитов in vitro (Kato Y., Gospodarowicz D. Sulfated proteoglycan synthesis by confluent cultures of rabbit costal chondrocytes grown in the presence of fibroblast growth factor. J. Cell. Biol. 1985, Feb; 100(2):477-85). Кроме того, Cuevas et al. показали, что FGF2 индуцирует восстановление хрящей in vivo (Cuevas P., Burgos J., Baird A. Basic fibroblast growth factor (FGF) promotes cartilage repair in vivo. Biochem. Biophys. Res. Commun. 1988, Oct. 31; 156(2):611-8). Takafuji et al. также показали, что имплантаты FGF2 значительным образом улучшают состояние височно-нижнечелюстных хрящей кроликов, больных остеоартритом (Takafuji H., Suzuki T., Okubo Y., Fujimura K., Bessho K. Regeneration of articular cartilage defects in the temporomandibular joint of rabbits by fibroblast growth factor-2: a pilot study. Int. J. Oral Maxillofac. Surg. 2007, Oct; 36(10):934-7). Данные наблюдения показывают перспективность соединений по настоящему изобретению для терапии при лечении остеоартрита и восстановлении хрящей.
В случае восстановления костей одна из существенных потребностей состоит в нахождении агентов, стимулирующих образование костной ткани. В отношении главных факторов роста установлено, что системное введение FGF2 облегчает восстановление костей (Acceleration of fracture healing in nonhuman primates by fibroblast growth factor-2. Kawaguchi H., Nakamura K., Tabata Y., Ikada Y., Aoyama I., Anzai J., Nakamura T., Hiyama Y., Tamura M. J. Clin. Endocrinol. Metab. 2001, Feb; 86(2), 875-880). Локальное введение FGF2 в желатиновую матрицу ускоряет восстановление костей у приматов, что ведет к предположению о клинической пользе FGF2 при лечении переломов. Благодаря агонистическим свойствам в отношении рецепторов FGF соединения по настоящему изобретению могут обеспечивать действенное лечение при восстановлении костей.
Преэклампсия представляет собой патологию плаценты, связанную с дефектами васкуляризации (Sherer, D.M. & Abulafia, O. Angiogenesis during implantation, and placental and early embryonic development. Placenta, 22, 1-13, 2001). Такие дефекты васкуляризации могут быть обусловлены недостаточностью ангиогенеза и могут вызывать повреждения на уровне плаценты, которые могут приводить к смерти плода. Соединения по настоящему изобретению могут обеспечивать действенное лечение для смягчения недостаточности ангиогенеза в плаценте при преэклампсии.
Помимо индуцирующего действия в отношении ангиогенеза факторы роста, такие как VEGF или FGF2, защищают эндотелиальные клетки от внутренних и внешних индукторов апоптоза. Внутренний путь сигнализации активируют митохондрии в ответ на стресс, такой как депривация или повреждения ДНК, тогда как внешний путь сигнализации индуцируется связыванием проапоптотических факторов, таких как TNF-α или Fas. В настоящее время выяснено, что VEGF и FGF2 представляют собой два фактора выживания эндотелиальных клеток (Role of Raf in Vascular Protection from Distinct Apoptotic Stimuli: A. Alavi, J.D. Hood, R. Frausto, D.G. Stupack, D.A. Cheresh: Science, 4, July, 2003: Vol. 301. no. 5629, pp. 94-96). Острый респираторный дистресс-синдром (ARDS) характеризуется сердечно-сосудистыми и нейропсихиатрическими проблемами. В плане сердечно-сосудистых проблем у больных имеют место значительные повреждения сосудов и, в частности, повышенная индукция апоптоза эндотелиальных клеток. Hamacher & al. недавно показали, что жидкости бронхоальвеолярных лаважей больных, страдающих ARDS, проявили проапоптотическую активность в отношении эндотелиальных клеток микрососудов легкого (Tumor necrosis factor-alpha and angiostatin are mediators of endothelial cytotoxicity in bronchoalveolar lavages of patients with acute respiratory distress syndrome. Am. J. Respir. Crit. Care Med. 2002, Sep. 1; 166(5):651-6: Hamacher J., Lucas R., Lijnen H.R., Buschke S., Dunant Y., Wendel A., Grau G.E., Suter P.M., Ricou B.). Благодаря своей активности в отношении выживания эндотелиальных клеток соединения по настоящему изобретению могут обеспечивать действенное лечение для улучшения сосудистой системы больных, имеющих повреждения сосудов, и, в частности, больных, страдающих ARDS.
Эндогенная сверхэкспрессия FGF7 (или KGF) и FGF18, возможно, представляет собой важный механизм благоприятствования пролиферации, миграции и защите волосяных фолликулов в случаях патологий или при противоопухолевом лечении (Comprehensive Analysis of FGF and FGFR Expression in Skin: FGF18 Is Highly Expressed in Hair Follicles and Capable of Inducing Anagen from Telogen Stage Hair Follicles. Mitsuko Kawano, Akiko Komi-Kuramochi, Masahiro Asada, Masashi Suzuki, Junko Oki, Ju Jiang and Toru Imamura). Благодаря своей агонистической активности в отношении рецепторов FGF соединения по настоящему изобретению могут обеспечивать действенное лечение для восстановления и защиты волосяных фолликулов и для защиты и регулирования роста капилляров.
Согласно другому из аспектов настоящее изобретение относится к фармацевтическим композициям, содержащим в качестве активного вещества соединение по настоящему изобретению или соединение 10. Такие фармацевтические композиции содержат эффективную дозу по меньшей мере одного соединения по настоящему изобретению или соединения 10, или фармацевтически приемлемую соль упомянутого соединения, а также по меньшей мере один фармацевтически приемлемый эксципиент. Эксципиенты выбирают из традиционных эксципиентов, известных специалистам в данной области техники, в соответствии с требуемыми фармацевтической формой и способом введения.
Таким образом, настоящее изобретение относится к фармацевтической композиции, содержащей в качестве действующего начала по меньшей мере одно соединение формулы (I), в которой:
- R1 представляет собой -OSO3 - или гидроксигруппу;
- R2 представляет собой -O-алкил или моносахарид формулы (II), где R представляет собой алкил:

- R3 представляет собой дисахарид формулы (III):

где
- R4 представляет собой -OSO3 - или гидроксигруппу;
- R5 представляет собой дисахарид формулы (IV):

где
- R6 представляет собой -OSO3 - или гидроксигруппу;
- R7 представляет собой гидроксигруппу или моносахарид формулы (V), приведенной далее, или дисахарид формулы (VI):

где
- R8 представляет собой -OSO3 - или гидроксигруппу;
- R9 представляет собой гидроксигруппу или -O-алкил, или дисахарид формулы (VII):
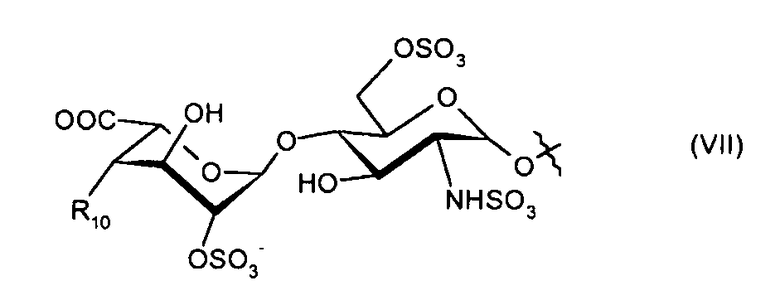
где R10 представляет собой -O-алкил;
при условии, что: R9 представляет собой гидроксигруппу или -O-алкил, если R2 представляет собой моносахарид формулы (II), определенной ранее; R7 представляет собой дисахарид определенной ранее формулы (VI), если R2 представляет собой -O-алкил; а R1, R4, R6 и R8 не представляют собой гидроксигруппы одновременно;
или фармацевтически приемлемую соль указанного соединения, а также по меньшей мере один фармацевтически приемлемый эксципиент.
Такие соединения включают определенные ранее соединения формулы (I)/(I'), а также определенный ранее гептасахарид 10, описанный в US 2006/0079483 A1.
В фармацевтических композициях по настоящему изобретению, предназначенных для перорального, сублингвального, подкожного, внутримышечного, внутривенного, топического, местного, интратрахеального, интраназального, чрескожного или ректального введения, указанное выше действующее начало или его соль может вводиться в стандартной лекарственной форме в смеси с обычными фармацевтическими эксципиентами животным и человеку для профилактики или лечения указанных выше нарушений или заболеваний.
Соответствующие стандартные лекарственные формы включают формы для перорального введения, такие как таблетки, капсулы с мягкой или твердой желатиновой оболочкой, порошки, гранулы и растворы или суспензии для перорального введения, формы для сублингвального, трансбуккального, интратрахеального, интраокулярного, интраназального введения, введения путем ингаляции, формы для топического, чрескожного, подкожного введения, внутримышечного или внутривенного введения, формы для ректального введения и имплантаты. Для топического нанесения соединения по настоящему изобретению можно использовать в кремах, гелях, мазях или лосьонах.
Более предпочтительные формы для инъекций представляют собой формы, содержащие обычным образом активное соединение, растворенное в воде для инъекций в присутствии хлорида натрия. Разовая доза активного соединения должна быть адаптирована для получения требуемого терапевтического эффекта; она может находиться, например, в интервале от 0,1 до 100 мг действующего начала.
Настоящее изобретение согласно другому из его аспектов относится также к применению соединения по настоящему изобретению или соединения 10, или одной из их фармацевтически приемлемых солей для лечения указанных выше патологий.
Таким образом, настоящее изобретение относится к соединению формулы (I), в которой:
- R1 представляет собой -OSO3 - или гидроксигруппу;
- R2 представляет собой -O-алкил или моносахарид формулы (II), где R представляет собой алкил:

- R3 представляет собой дисахарид формулы (III):

где
- R4 представляет собой -OSO3 - или гидроксигруппу;
- R5 представляет собой дисахарид формулы (IV):
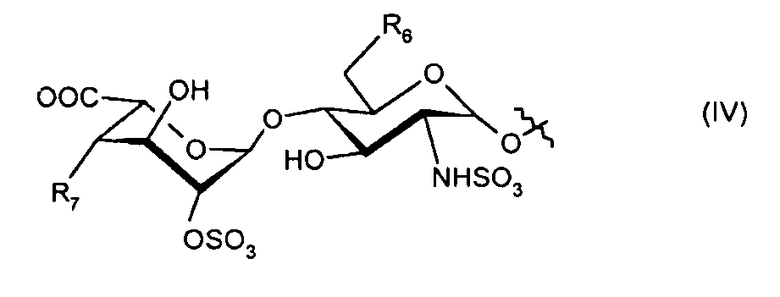
где
- R6 представляет собой -OSO3 - или гидроксигруппу;
- R7 представляет собой гидроксигруппу или моносахарид формулы (V), приведенной далее, или дисахарид формулы (VI):
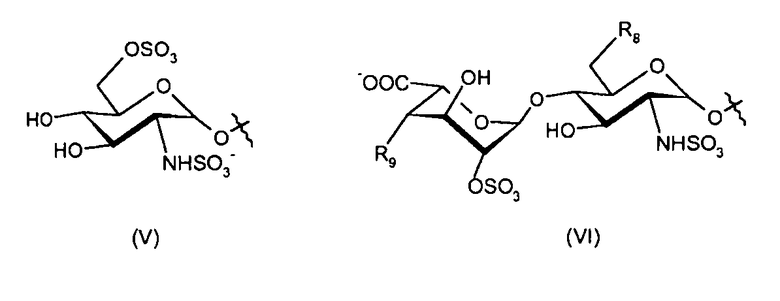
где
- R8 представляет собой -OSO3 - или гидроксигруппу;
- R9 представляет собой гидроксигруппу или -O-алкил, или дисахарид формулы (VII):

где R10 представляет собой -O-алкил;
при условии, что R9 представляет собой гидроксигруппу или -O-алкил, если R2 представляет собой моносахарид формулы (II), определенной ранее; R7 представляет собой дисахарид определенной ранее формулы (VI), если R2 представляет собой -O-алкил; а R1, R4, R6 и R8 не представляют собой гидроксигруппы одновременно;
или к фармацевтически приемлемой соли упомянутого соединения;
для лечения упомянутых ранее патологий.
Такие соединения включают определенные ранее соединения формулы (I)/(I'), а также определенный ранее гептасахарид 10, описанный в US 2006/0079483 A1.
Настоящее изобретение согласно другому из его аспектов относится также к способу лечения указанных выше патологий, включающему введение больному эффективной дозы соединения по настоящему изобретению или соединения 10, или одной из их фармацевтически приемлемых солей.
Лекарственные средства, фармацевтические композиции и способ лечения по настоящему изобретению могут относиться также к любой из определенных ранее подгрупп соединений.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ ПЕНТАСАХАРИДЫ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 1999 |
|
RU2193040C2 |
| СИНТЕТИЧЕСКИЕ ПОЛИСАХАРИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1997 |
|
RU2167163C2 |
| ПРОИЗВОДНЫЕ 3-ДЕЗОКСИОЛИГОСАХАРИДОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ), ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1994 |
|
RU2133752C1 |
| ПРОИЗВОДНЫЕ ГЕКСОЗЫ, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2015 |
|
RU2731563C2 |
| ПРОИЗВОДНОЕ ОЛИГОСАХАРИДОВ | 2004 |
|
RU2290408C2 |
| Способ получения пентасахарида | 1983 |
|
SU1694065A3 |
| СПОСОБЫ ПОЛУЧЕНИЯ АМИНОАЛКИЛГЛЮКОЗАМИНИДФОСФАТОВ И ДИСАХАРИДНЫХ ИММУНОЭФФЕКТОРОВ И ИХ ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ | 2003 |
|
RU2340621C2 |
| ИНДОЛОПИРРОЛОКАРБАЗОЛЬНЫЕ ПРОИЗВОДНЫЕ САХАРОВ, СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ИНГИБИРОВАНИЯ РОСТА ОПУХОЛЕЙ | 1997 |
|
RU2167880C2 |
| НОВЫЕ СУЛЬФАТИРОВАННЫЕ ПРОИЗВОДНЫЕ ОЛИГОСАХАРИДОВ | 2008 |
|
RU2483074C2 |
| СИНТЕТИЧЕСКИЕ ГЛЮКОПИРАНОЗИЛЛИПИДНЫЕ АДЪЮВАНТЫ | 2010 |
|
RU2560182C2 |
Настоящее изобретение относится к олигосахаридам, активирующим рецепторы FGF, и их применению в медицине, формулы (I):

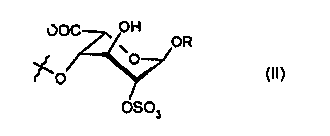

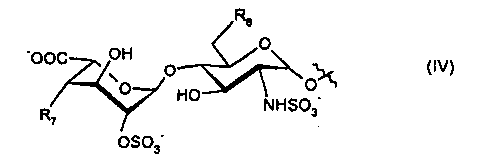
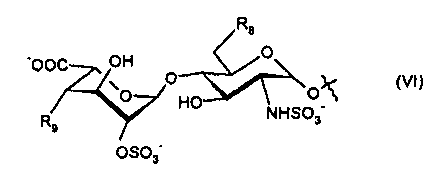
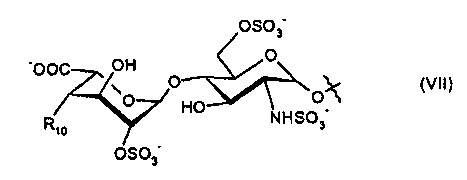
где R2 представляет собой -О-алкил или моносахарид формулы (II), R представляет собой алкил, R3 - дисахарид формулы (III), R5 - дисахарид формулы (IV), R7 представляет собой ОН или дисахарид формулы (VI), R1, R4, R6 и R8 представляют собой -OSO3 - или ОН, но не являются ОН-группами одновременно, R9 представляет собой ОН, -О-алкил или дисахарид формулы (VII), R10 представляет собой -О-алкил, при условии, что R9 представляет собой ОН или -О-алкил, если R2 - моносахарид формулы (II), R7 представляет собой дисахарид формулы (VI), если R2 представляет собой -О-алкил. Предложены новые вещества, стимулирующие образование сосудов. 11 н. и 13 з.п. ф-лы, 9 пр.
1. Олигосахаридные соединения, соответствующие формуле (I):

где
- R1 представляет собой -OSO3 - или гидроксигруппу;
- R2 представляет собой -О-алкил или моносахарид формулы (II), где R представляет собой алкил:

- R3 представляет собой дисахарид формулы (III):

где
- R4 представляет собой -OSO3 - или гидроксигруппу;
- R5 представляет собой дисахарид формулы (IV):

где
- R6 представляет собой -OSO3 - или гидроксигруппу;
- R7 представляет собой гидроксигруппу или дисахарид формулы (VI):

где
- R8 представляет собой -OSO3 - или гидроксигруппу;
- R9 представляет собой гидроксигруппу или -О-алкил, или дисахарид формулы (VII):

где R10 представляет собой -О-алкил;
при условии, что R9 представляет собой гидроксигруппу или -О-алкил, если R2 представляет собой моносахарид формулы (II), определенной ранее; R7 представляет собой дисахарид определенной ранее формулы (VI), если R2 представляет собой -О-алкил; a R1, R4, R6 и R8 не представляют собой гидроксигруппы одновременно;
в виде кислоты или в виде любой из их фармацевтически приемлемой соли.
2. Соединения по п. 1, в которых R2 представляет собой моносахарид формулы (II), a R7 представляет собой гидроксигруппу.
3. Соединения по п. 1, соответствующие приведенной далее формуле (I-1), в которой R7 представляет собой гидроксигруппу, а R, R1, R4 и R6 имеют значения, определенные в п. 1:

в виде кислоты или в виде любой из их фармацевтически приемлемой соли.
4. Соединения по п. 1, в которых R2 представляет собой -О-алкил.
5. Соединения по п. 1, соответствующие приведенной далее формуле (I-2), в которой R2 представляет собой -О-алкил, a R1, R4, R6, R8 и R9 имеют значения, определенные в п. 1:

в виде кислоты или в виде любой из их фармацевтически приемлемой соли.
6. Соединения по п. 1, в которых
- R2 представляет собой -О-алкил;
- R7 представляет собой дисахарид определенной в п. 1 формулы (VI), в которой R9 представляет собой дисахарид формулы (VII), определенной в п. 1.
7. Соединения по п. 1, соответствующие приведенной далее формуле (I-3), в которой R2 и R9 имеют значения, определенные в п. 6, a R1, R4, R6, R8 и R10 имеют значения, определенные в п. 1:

в виде кислоты или в виде любой из их фармацевтически приемлемой соли.
8. Соединения по п. 1, в которых:
- R2 представляет собой -О-алкил;
- R7 представляет собой дисахарид определенной в п. 1 формулы (VI), в которой R9 представляет собой гидроксигруппу или -О-алкил.
9. Соединения по п. 1, соответствующие приведенной далее формуле (I-2), в которой R1, R4, R6 и R8 имеют значения, определенные в п. 1, R2 представляет собой -О-алкил, a R9 представляет собой гидроксигруппу или -О-алкил:
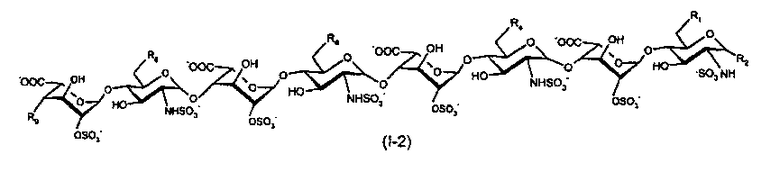
в виде кислоты или в виде любой из их фармацевтически приемлемой соли.
10. Соединения по п. 8, в которых R9 представляет собой -O-алкил.
11. Соединения по п. 1, отличающиеся тем, что они соответствуют формуле (I′), в которой R1, R2, R4, R6 и R7 имеют значения, определенные в любом из пп. 1-9:
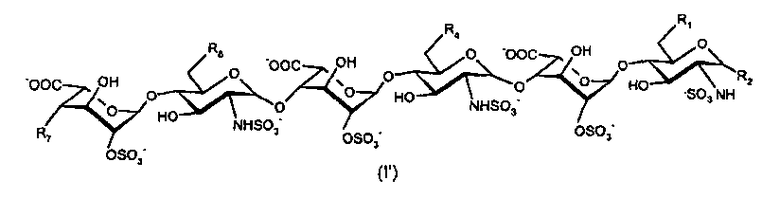
12. Соединения по п. 1, выбранные из следующих соединений:
- метил-(4-O-пропил-2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-[(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил-(1→4)]2-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозид (№1);
- метил-(4-O-пропил-2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-[(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил-(1→4)]3-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозид (№2);
- [метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-[(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)]2-2-O-натрийсульфонато-α-L-идопиранозид]уронат натрия (№3);
- метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозид (№4);
- метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозид (№5);
- метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-О-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозид (№6);
- метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-О-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозид (№7);
- метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)-[(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)]2-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-6-O-натрийсульфонато-2-(сульфонато)амино-α-D-глюкопиранозид (№8);
- метил-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонато)амино-α-D-глюкопиранозил)-[(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-(2-дезокси-6-O-натрийсульфонато-2-натрий(сульфонатоамино)-α-D-глюкопиранозил)]2-(1→4)-(2-O-натрийсульфонато-α-L-идопиранозилуронат натрия)-(1→4)-2-дезокси-2-натрий(сульфонатоамино)-α-D-глюкопиранозид (№9).
13. Лекарственное средство для лечения патологий, требующих активации рецепторов FGF, отличающееся тем, что оно включает в себя соединение по любому из пп. 1-12, в котором R7 представляет собой гидроксигруппу или моносахарид приведенной далее формулы (V), или дисахарид формулы (VI), в которой R8 и R9 имеют значения, определенные в любом из пп. 1-10:

или его фармацевтически приемлемую соль.
14. Лекарственное средство по п. 13, отличающееся тем, что оно включает соединение по любому из пп. 1-12 или его фармацевтически приемлемую соль.
15. Лекарственное средство по п. 13, отличающееся тем, что оно включает соединение 10:

или его фармацевтически приемлемую соль.
16. Фармацевтическая композиция для лечения патологий, требующих активации рецепторов FGF, отличающаяся тем, что она включает соединение по любому из пп. 1-12, в котором R7 представляет собой гидроксигруппу или моносахарид приведенной далее формулы (V), или дисахарид формулы (VI), в которой R8 и R9 имеют значения, определенные в любом из пп. 1-10:

или его фармацевтически приемлемую соль, а также по меньшей мере один фармацевтически приемлемый эксципиент.
17. Фармацевтическая композиция для лечения патологий, требующих активации рецепторов FGF, отличающаяся тем, что она включает соединение по любому из пп. 1-12 или его фармацевтически приемлемую соль, а также по меньшей мере один фармацевтически приемлемый эксципиент.
18. Фармацевтическая композиция для лечения патологий, требующих активации рецепторов FGF, отличающаяся тем, что она включает соединение 10:

или его фармацевтически приемлемую соль, а также по меньшей мере один фармацевтически приемлемый эксципиент.
19. Соединение по любому из пп. 1-12, в котором R7 представляет собой гидроксигруппу или моносахарид приведенной далее формулы (V), или дисахарид формулы (VI), в которой R8 и R9 имеют значения, определенные в любом из пп. 1-10:

для применения в лечении патологий, требующих активации рецепторов FGF.
20. Соединение по любому из пп. 1-12 или его фармацевтически приемлемая соль для применения в лечении патологий, требующих активации рецепторов FGF.
21. Соединение 10 или его фармацевтически приемлемая соль:

для применения в лечении патологий, требующих активации рецепторов FGF.
22. Соединение по любому из пп. 19-21 для применения в лечении патологий, требующих активации ангиогенеза и постишемической реваскуляризации.
23. Соединение по любому из пп. 19-22 для применения в лечении ишемии, такой как ишемия сердца и артериальная ишемия нижних конечностей, в лечении заболеваний, связанных со стенозом или обструкцией артерий, или артериитов, в лечении стенокардии, облитерирующего тромбангиита, атеросклероза, для подавления рестеноза после ангиопластики или эндартерэктомии, для заживления ран, в регенерации мышц, для выживания миобластов, в лечении периферической нейропатии, послеоперационных повреждений нервов, нейрогенной недостаточности, такой как болезнь Паркинсона, болезнь Альцгеймера, прионная болезнь и дегенерация нейронов у алкоголиков, в лечении деменции, для улучшения выживания биоинженерных трансплантатов поджелудочной железы у больных диабетом, для улучшения реваскуляризации крупных имплантатов и выживания трансплантатов, в лечении дегенерации сетчатки, пигментного ретинита, остеоартрита, преэклампсии или повреждений сосудов и острого респираторного дистресс-синдрома, в восстановлении хрящей, в восстановлении и защите костей, в восстановлении и защите волосяных фолликулов и для защиты и регулирования роста волос.
24. Соединение формулы 20А, в которой Pg, Pg′ и Pg″, являющиеся одинаковыми или отличающимися друг от друга, представляют собой защитные группы:
 , в котором Pg, Pg′ и Pg″ представляют собой бензил, аллил и ацетил, соответственно.
, в котором Pg, Pg′ и Pg″ представляют собой бензил, аллил и ацетил, соответственно.
| WO 1992018546 A1, 29.10.1992 | |||
| Способ измерения напряженности электрического поля по равенству трех составляющих | 2023 |
|
RU2800074C1 |
| US 2004068108 А1, 08.04.2004 | |||
| ЭПИМЕРИЗОВАННЫЕ ПРОИЗВОДНЫЕ ПОЛИСАХАРИДА К5 С ВЫСОКОЙ СТЕПЕНЬЮ СУЛЬФАТИРОВАНИЯ | 2003 |
|
RU2333222C2 |
| Codee Jeroen D.C | |||
| et al, Drug discovery today, 2004, 317-326 | |||
| C | |||
| Tabeur et al, Bioorganic&Medicinal Chemistry, 1999, vol | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
2015-08-10—Публикация
2010-08-12—Подача