Перекрестная ссылка на родственные заявки
По данной заявке испрашивается приоритет на основании предварительной патентной заявки США №61/736856, поданной 13 декабря 2012 г. Полное содержание всего вышеуказанного включено в настоящий документ посредством ссылки.
Ссылка на список последовательностей, предоставленный в электронном виде
Официальная копия списка последовательностей предоставлена в электронном виде через EFS-Web в виде списка последовательностей в формате ASCII с файлом, озаглавленным «Способ обнаружения ДНК», создан 26 ноября 2012 г., имеет размер 3640 байт и подан одновременно со спецификацией. Список последовательностей, содержащийся в данном документе в формате ASCII, является частью спецификации и включен в настоящий документ посредством ссылки в полном объеме.
Область техники, к которой относится изобретение
Настоящее изобретение частично относится к способу скрининга геномных локусов растительных объектов. Более конкретно, настоящее изобретение частично относится к высокопроизводительному способу обнаружения и идентификации растительных объектов, которые содержат нарушения в целевых геномных локусах. Кроме того, настоящее изобретение частично относится к высокопроизводительному способу обнаружения и идентификации растительных объектов, которые содержат экзогенный донорский полинуклеотид ДНК, вставленный в целевые геномные локусы. Способ легко применим для скрининга растительных объектов, полученных методом таргетинга, основанном на использовании сайт-специфической нуклеазы.
Уровень техники изобретения
Направленная модификация генома растений являлась давней и труднодостижимой целью как прикладных, так и фундаментальных исследований. Для достижения этой цели разрабатываются методы и композиции для таргетинга и расщепления геномной ДНК с помощью сайт-специфических нуклеаз (нуклеаз с «цинковыми пальцами» (ZFN), мегануклеаз, CRISPR и TALEN). Сайт-специфическое расщепление геномных локусов с помощью ZFN можно использовать, например, для индукции направленного мутагенеза, индукции направленных делеций последовательностей клеточной ДНК и содействия направленной рекомбинации экзогенного донорского полинуклеотида ДНК в заранее определенном геномном локусе. Смотри, например, патентные публикации США №№20030232410, 20050208489, 20050026157, 20050064474 и 20060188987, а также международную патентную публикацию №WO 2007/014275, содержание которых включено в настоящий документ посредством ссылки в полном объеме и для всех целей. В патентной публикации США №20080182332 описано использование неканонических нуклеаз с «цинковыми пальцами» (ZFN) для направленной модификации геномов растений и в патентной публикации США №20090205083 описана опосредованная ZFN направленная модификация геномного локуса EPSPs растения. Кроме того, в статье Moehle et al. (2007) Proc. Natl. Acad. Sci. USA 104(9): 3055-3060 описано использование сконструированных ZFN для направленного добавления гена в определенный локус генома. Современные методы таргетинга, как правило, включают совместную трансформацию ткани растения донорским полинуклеотидом ДНК, содержащим по меньшей мере один трансген, и сайт-специфической нуклеазой (например, ZFN), которая предназначена для связывания и расщепления определенного геномного локуса. Донорский полинуклеотид ДНК стабильно встраивается в расщепленный геномный локус, что приводит к направленному добавлению гена в определенный геномный локус.
К сожалению, согласно сообщениям, наблюдаемая частота направленной модификации генома свидетельствует о том, что таргетинг геномных локусов в растениях является относительно неэффективным. Имеющая место неэффективность приводит к необходимости скрининга большого числа растительных объектов для идентификации конкретного объекта, содержащего целевые геномные локусы. Большинство известных современных анализов растительных объектов опираются на единственный аналитический метод для подтверждения таргетинга, что может приводить к неточной оценке частоты таргетинга и низкой достоверности результатов.
Следовательно, в данной области существует потребность в способах скрининга, возможно, применимых в качестве высокопроизводительных способов, для быстрой идентификации растительных объектов, содержащих целевые геномные локусы. Кроме того, поскольку направленная вставка генов происходит в сочетании со случайной вставкой генов, желательные способы скрининга позволяли бы специфически идентифицировать таргетинг геномных локусов на фоне случайных вставок.
Сущность изобретения
В одном из вариантов осуществления изобретение относится к способу определения присутствия донорского полинуклеотида ДНК, вставленного в целевой геномный локус, включающему амплификацию в первой реакции амплификации образца геномной ДНК, содержащей целевой геномный локус, с использованием первого набора олигонуклеотидов, которые связываются в условиях гибридизации в непосредственной близости от целевого геномного локуса, для получения, таким образом, первого ампликона, содержащего целевой геномный локус, и обнаружение наличия или отсутствия первого ампликона, при этом отсутствие первого ампликона указывает на присутствие донорского полинуклеотида ДНК в целевом геномном локусе.
В следующем варианте осуществления способ включает амплификацию во второй реакции амплификации образца геномной ДНК с использованием второго набора олигонуклеотидов, которые связываются в условиях гибридизации в непосредственной близости от целевого геномного локуса и в пределах донорского полинуклеотида ДНК, для получения второго ампликона, содержащего по меньшей мере часть целевого геномного локуса и по меньшей мере часть донорского полинуклеотида ДНК, и обнаружение наличия или отсутствия второго ампликона, при этом наличие амплифицированного продукта указывает на присутствие донорского полинуклеотида ДНК в целевом геномном локусе.
В другом варианте осуществления способ включает определение нарушения геномного локуса во множестве растительных клеток, включающее амплификацию в первой реакции амплификации образца геномной ДНК, содержащей нарушенный геномный локус, с использованием набора олигонуклеотидов, которые связываются в условиях гибридизации в непосредственной близости от нарушенного геномного локуса, для получения первого ампликона, содержащего нарушенный геномный локус, количественное определение результатов первой реакции амплификации, амплификацию во второй реакции амплификации образца геномной ДНК, содержащей нарушенный геномный локус, с использованием набора олигонуклеотидов, которые связываются в условиях гибридизации в непосредственной близости от нарушенного геномного локуса, для получения, таким образом, второго ампликона, содержащего нарушенный геномный локус, количественное определение результатов второй реакции амплификации и сравнение количественных результатов первой и второй реакций амплификации, при этом количественный результат первой реакции амплификации соответствует меньшему количеству амплифицированного продукта по сравнению со второй реакцией амплификации, что свидетельствует о нарушении геномного локуса в образцах первого ампликона.
В другом варианте осуществления изобретение относится к способу определения нарушения геномного локуса, включающему амплификацию в первой реакции амплификации образца геномной ДНК, содержащей нарушенный геномный локус, с использованием набора олигонуклеотидов, которые связываются в условиях гибридизации в непосредственной близости от нарушенного геномного локуса, для получения первого ампликона, содержащего нарушенный геномный локус, и обнаружение наличия или отсутствия первого ампликона, при этом отсутствие ампликона свидетельствует о нарушении геномного локуса.
Другие варианты осуществления способа включают количественное определение результатов первой реакции амплификации, количественное определение результатов второй реакции амплификации, сравнение результатов первой и второй реакций амплификации, и определение присутствия или отсутствия донорского полинуклеотида ДНК в целевом геномном локусе, при этом подтверждением вставки донорского полинуклеотида ДНК в целевой геномный локус является отсутствие первого ампликона и наличие второго ампликона.
В одном из вариантов осуществления первую или вторую реакции амплификации проводят в одной пробирке или лунке в мультиплексном формате.
В другом аспекте вариант осуществления изобретения включает количественное определение результатов первой и второй реакций амплификации, включающее получение сигнатурного профиля для одной или обеих из первой и второй реакций амплификации. В иллюстративном аспекте данного варианта осуществления сигнатурный профиль может быть выбран из группы, состоящей из сигнатурного профиля кривой температуры плавления и сигнатурного профиля флуоресценции.
Дополнительные варианты осуществления включают сигнатурный профиль, полученный от интеркалирующего красителя ДНК или флуоресцентного красителя. При этом интеркалирующий краситель представляет собой цианиновый краситель, такой как краситель SYTO13®. В одном из вариантов осуществления краситель SYTO13® используют в реакции амплификации в концентрации менее 10 мкМ, менее 4 мкМ или менее 2,7 мкМ. В дополнительных вариантах осуществления флуоресцентный краситель выбирают из группы, состоящей из флуоресцентного красителя HEX, флуоресцентного красителя FAM, флуоресцентного красителя JOE, флуоресцентного красителя TET, флуоресцентного красителя Cy 3, флуоресцентного красителя Cy 3,5, флуоресцентного красителя Cy 5, флуоресцентного красителя Cy 5,5, флуоресцентного красителя Cy 7 и флуоресцентного красителя ROX. В одном из вариантов осуществления первый или второй набор олигонуклеотидов, или оба, содержат флуоресцентный краситель.
В вариантах осуществления настоящее изобретение относится к способам и композициям для определения присутствия донорской вставки в целевом геномном локусе и выбора трансгенного объекта, содержащего донорскую вставку в целевом геномном локусе. Дополнительный вариант осуществления относится к растению, представляющему собой трансгенный объект.
Другие варианты осуществления могут относиться к двудольному растению, при этом двудольное растение выбирают из группы, состоящей из растения сои, растения канолы и растения хлопка. Кроме того, дополнительные варианты осуществления могут относиться к однодольному растению, при этом однодольное растение выбирают из группы, состоящей из растения кукурузы, растения риса и растения пшеницы.
Дополнительные варианты осуществления относятся к геномному локусу, который расщепляется сайт-специфической нуклеазой. Иллюстративные сайт-специфические нуклеазы могут включать нуклеазу с «цинковыми пальцами», мегануклеазу, нуклеазу CRISPR или TALEN, или любую другую сайт-специфическую нуклеазу.
В другом аспекте варианты осуществления изобретения относятся к реакции амплификации, при этом амплификацию выполняют с использованием полимеразной цепной реакции.
Другие варианты осуществления изобретения относятся к ампликону, содержащему 5'-область соединения и 3'-область соединения донорского полинуклеотида ДНК и целевого геномного локуса. Кроме того, варианты осуществления изобретения относятся к ампликону, содержащему 5'-область соединения или 3'-область соединения донорского полинуклеотида ДНК и целевого геномного локуса.
Варианты осуществления также относятся к донорскому полинуклеотиду ДНК, содержащему по меньшей мере одну генную экспрессионную кассету.
В дополнение к иллюстративным аспектам и вариантам осуществления, описанным выше, дополнительные аспекты и варианты осуществления станут очевидны при изучении следующего описания.
Краткое описание чертежей
На фигуре 1 показан аналитический способ идентификации растительных объектов, содержащих целевой геномный локус.
На фигуре 2 представлены полученные методом количественной ПЦР (кПЦР) результаты анализа нарушения целевого локуса с помощью ZFN: результаты скрининга подгруппы объектов. Стрелкой отмечен трансгенный объект с нарушенным локусом, о чем свидетельствуют падение детектируемого сигнала кПЦР.
На фигуре 3 представлен скрининг, проведенный методом внутренней-внешней (In-Out) ПЦР-амплификации. На фигуре 3A изображен целевой геномный локус («локус») без трансгенной вставки. Внутренняя-внешняя ПЦР не приводит к образованию амплифицированного продукта. На фигуре 3B изображен локус с направленной трансгенной вставкой. Внутренняя-внешняя ПЦР приводит к образованию ампликона размером 2 т.п.н. с 5'-конца локуса и ампликона размером 1,5 т.п.н. с 3'-конца.
На фигуре 4 представлен анализ внутренней-внешней ПЦР. На фигуре 4A изображен сигнатурный профиль флуоресцентного сигнала, генерируемого в реакциях амплификации с использованием красителя SYTO13® (Invitrogen, Carlsbad, CA), который можно использовать для идентификации положительных по трансгенной вставке объектов. На фигуре 4B изображены сигнатурные профили температуры плавления, генерируемые в реакциях амплификации образцов, по сравнению с положительным контролем, которые можно использовать для подтверждения положительных флуоресцентных сигналов.
На фигуре 5 приведены целевые объекты, которые были идентифицированы с использованием анализа нарушения локуса и реакции внутренней-внешней ПЦР раскрытого в настоящем документе объекта изобретения.
На фигуре 6 приведен анализ вызванного ZFN нарушения локуса. Образцы в верхней скобке не содержат нарушенный геномный локус, а образцы в нижней скобке содержат нарушенный геномный локус.
На фигуре 7 приведен другой анализ вызванного ZFN нарушения локуса. Образцы в верхней скобке не содержат нарушенный геномный локус, а образцы в нижней скобке содержат нарушенный геномный локус.
На фигуре 8 приведен анализ вызванного eZFN нарушения в области локуса ELP. На фигуре 8 (a) приведена иллюстрация геномного фрагмента, содержащего ELP, который был получен путем вставки T-цепи из pDAB105818. На этой схеме указано относительное расположение праймеров и зондов (MAS621, MAS622 и зонда UPL67), используемых для анализа нарушения локуса. На фигуре 8 (b) приведены результаты скрининга 354 pat-положительных объектов. На нарушенный локус ELP указывает падение детектируемого сигнала кПЦР. Соответственно, образцы в верхней скобке не содержат нарушенный геномный локус ELP, а образцы в нижней скобке содержат нарушенный геномный локус ELP.
На фигуре 9 приведен анализ внутренней-внешней ПЦР. На фигуре 9A изображен сигнальный профиль температуры плавления, генерируемый в реакциях амплификации 5'-области соединения донора/локуса ELP с использованием красителя SYTO13® (Invitrogen, Carlsbad, CA), который можно использовать для идентификации положительных по трансгенной вставке объектов. На фигуре 9B изображен сигнальный профиль температуры плавления, генерируемый в реакциях амплификации 3'-области соединения донора/локуса ELP с использованием красителя SYTO13® (Invitrogen, Carlsbad, CA), который можно использовать для идентификации положительных по трансгенной вставке объектов.
На фигуре 10 приведена иллюстрация последовательностей связывания ZF с соответствующими «цинковыми пальцами» и гидролизные зонды, используемые в анализе нарушения локуса ELP: линия eZFN8 представляет зонд для обнаружения активностей от eZFN8 со спейсером GTGAGA между последовательностями сайтов связывания SBS15590 и SBS18473, и линия eZFN1 представляет зонд для обнаружения активностей от eZFN1 со спейсером GTGGAT между вторым набором последовательностей сайтов связывания, SBS15590 и SBS8196. Верхняя последовательность соответствует SEQ ID NO: 39 и комплементарная последовательность, приведенная внизу на фигуре, соответствует SEQ ID NO: 40.
На фигуре 11 показан график наложения для нормированного числа копий aad-1 (кружки) и ELP (плюсы). На фигуре 11 (a) приведены результаты анализа нарушения локуса в 1125 образцах от скрещивания с растениями, содержащими вырезающие фрагменты eZFN1: 425 с числом копий ELP менее 0,05 (разрезание), 95 - от 0,05 до 0,4 (химерные). На фигуре 11 (b) приведены результаты анализа нарушения локуса в 697 образцах от скрещивания с растениями, содержащими вырезающие фрагменты eZFN8: 488 с числом копий ELP менее 0,05, 1 - от 0,05 до 0,4.
На фигуре 12 показано выравнивание последовательностей для образцов геномного локуса ELP, разрезанного eZFN1 (pDAB105825) и eZFN8 (pDAB105828). Полинуклеотидные спейсеры между сайтами узнавания ZFN отмечены красным цветом. Основания, изображенные чертой (-), являются делециями, представляющими собой минимум одно пропущенное основание последовательности.
Подробное описание
Изобретены новые способы для быстрого скрининга, идентификации и характеризации таргетированных с помощью сайт-специфической нуклеазы растительных объектов. Способы можно использовать для анализа невредимости геномного целевого локуса с помощью первой реакции амплификации для определения того, был ли нарушен геномный целевой локус. Объекты, идентифицированные как содержащие нарушенный геномный локус, затем могут быть подвергнуты скринингу с помощью второй реакции амплификации для подтверждения присутствия экзогенного донорского полинуклеотида ДНК в целевом геномном локусе. В силу этого, большое количество растительных объектов можно анализировать и подвергать скринингу для идентификации и отбора определенных объектов, у которых донорский полинуклеотид ДНК вставлен в целевой геномный локус. Раскрытый в настоящем документе объект изобретения дополнительно включает растения и растительные клетки, содержащие таргетированные с помощью нуклеазы растительные объекты, выбранные с помощью новых способов скрининга.
В настоящем документе описаны новые способы скрининга растительных объектов на нарушение геномного локуса, которое является результатом расщепления геномной ДНК сайт-специфической нуклеазой. Нарушенный геномный локус может содержать присутствующий донорский полинуклеотид ДНК, или нарушенный геномный локус может содержать вставки и/или делеции (также обозначенные InDel). В способах используют две исходные реакции амплификации в качестве аналитического скрининга. Первая реакция амплификации представляет собой анализ нарушения, в котором присутствие донорского полинуклеотида ДНК, вставленного в целевой геномный локус, определяют при помощи реакции амплификации, при этом отсутствие ампликона свидетельствует о том, что донорский полинуклеотид ДНК присутствует в целевом геномном локусе. Вторая реакция амплификации представляет собой реакцию «внутренней-внешней» ПЦР-амплификации для скрининга последовательностей 3' и/или 5'-области соединения донорского полинуклеотида ДНК и целевого геномного локуса. Наличие амплифицированного продукта, содержащего последовательность 3' и/или 5'-области соединения, свидетельствует о том, что донорский полинуклеотид ДНК присутствует в целевом геномном локусе.
При использовании аналитического скрининга с двумя различными реакциями амплификации, реакции амплификации для выявления нарушения локуса и внутренней-внешней реакции амплификации, вероятность идентификации положительного целевого объекта среди большого числа нецелевых объектов значительно возрастает. Реакция амплификации для выявления нарушения локуса была разработана для быстрого анализа большого количества образцов высокопроизводительным образом. Кроме того, данный анализ позволяет идентифицировать и характеризовать объекты как в отношении вставки донорского полинуклеотида ДНК, так и в отношении расщепления за счет ZFN в целевом геномном локусе. Внутренняя-внешняя реакция амплификации является альтернативным аналитическим подходом. Этот анализ используют для выявления наличия 3' и 5'-областей соединения с целью подтверждения присутствия донорского полинуклеотида ДНК, вставленного в целевой геномный локус. Внутреннюю-внешнюю реакцию амплификации можно использовать для подтверждения того, что целевые объекты, идентифицированные в анализе на нарушение локуса, действительно содержат целую полноразмерную целевую вставку в геномном локусе. Если реакцию амплификации на выявление нарушения локуса проводят в сочетании с внутренней-внешней реакцией амплификации, скомпилированные данные могут быть проанализированы для определения лимитирующих факторов для направленной вставки донорского полинуклеотида ДНК в геномный локус (например, расщепление ZFN или вставка донора как лимитирующий фактор для получения объектов, содержащих донорский полинуклеотид ДНК в целевом геномном локусе). Использование двух различных анализов скрининга с разными методологиями увеличивает вероятность нахождения целевого объекта, содержащего донорский полинуклеотид ДНК в целевом геномном локусе. Более того, раскрытые способы можно использовать в качестве высокопроизводительных анализов, позволяющих быстро и эффективно определять подгруппу образцов, которые в дальнейшем могут быть проанализированы другими молекулярными методами для подтверждения. Раскрытые анализы скрининга включают высококачественные высокопроизводительные способы определения и получения трансгенных объектов с целевыми вставками. Кроме того, данная методология легко применима для анализа любых видов растений.
Если не указано иное, все технические и научные термины, используемые в настоящем документе, имеют то же значение, которое им обычно придают специалисты в области, к которой относится изобретение. В случае конфликта, настоящая заявка, включая определения, будет иметь преимущественную силу. Если иное не подразумевается по контексту, употребляемые в единственном числе термины включают и их множественное число, и употребляемые во множественном числе термины включают и их единственное число. Все публикации, патенты и другие литературные источники, упомянутые в настоящем документе, включены посредством ссылки в полном объеме для всех целей, как если бы было указано, что каждая отдельная публикация или патентная заявка специально и индивидуально включена посредством ссылки, если только не указано, что только определенные разделы патентов или патентных публикаций включены посредством ссылки.
Для дополнительного разъяснения данного изобретения приведены следующие термины, аббревиатуры и определения.
Используемые в настоящем документе термины «содержит», «содержащий», «включает», «включающий», «имеет», «имеющий», «содержит в себе» или «содержащий в себе», или любые другие их вариации являются не исключающими или открытыми. Например, композиция, смесь, процесс, способ, продукт или устройство, содержащие список элементов, не обязательно ограничены только этими элементами, но могут включать и другие элементы, специально не перечисленные и не присущие такой композиции, смеси, процессу, способу, продукту или устройству. Кроме того, если прямо не указано иное, «или» означает включающее «или», а не исключающее «или». Например, условие A или B удовлетворяет одному из следующих: A является истинным (или присутствует) и B является ложным (или не присутствует), A является ложным (или не присутствует) и B является истинным (или присутствует), и как A, так и B являются истинными (или присутствуют).
Кроме того, употребление слов «некий» или «один из» применительно к элементу или компоненту варианта осуществления изобретения не следует понимать как ограничение по количеству экземпляров, то есть, числу элементов или компонентов. Таким образом, слова «некий» или «один из» следует понимать как подразумевающие «один» или «по меньшей мере один», и форма единственного числа элемента или компонента также включает и форму множественного числа, если по смыслу не очевидно, что имеется в виду единственное число.
Используемый в настоящем документе термин «изобретение» или «настоящее изобретение» является неограничивающим термином и не относится к какому-либо одному варианту осуществления конкретного изобретения, а охватывает все возможные варианты осуществления, раскрытые в данной заявке.
Используемый в настоящем документе термин «растение» включает, но не ограничивается ими, любое потомство, клетку, ткань или часть растения.
В настоящем документе описаны способы определения присутствия донорского полинуклеотида ДНК, вставленного в целевые геномные локусы. Полинуклеотиды ДНК, предназначенные для вставки, могут также называться, и должны включать, «экзогенные» полинуклеотиды, «донорские» полинуклеотиды или «молекулы», или «трансгены».
В некоторых вариантах осуществления донорский полинуклеотид ДНК включает последовательности (например, кодирующие последовательности, также называемые трансгенами) длиной более 1 т.п.н., например, от 2 до 200 т.п.н., от 2 до 10 т.п.н. (или любое значение между ними). Донорский полинуклеотид ДНК может также включать по меньшей мере один сайт-мишень для сайт-специфической нуклеазы, например, по меньшей мере один сайт-мишень для ZFN, мегануклеазы, CRISPR или TALEN может быть включен в донорский полинуклеотид ДНК. Донорский полинуклеотид ДНК может включать по меньшей мере 1 сайт-мишень, например, для узнавания, связывания и расщепления парой ZFN, CRISPR или TALEN. Как правило, сайты-мишени для нуклеазы находятся за пределами последовательностей трансгенов, например, с 5' или 3'-стороны от последовательностей трансгенов, для расщепления и удаления находящегося между ними трансгена, при необходимости. Сайт(ы) расщепления нуклеазой могут быть для любой нуклеазы(нуклеаз). В некоторых вариантах осуществления сайт(ы) расщепления нуклеазой, находящиеся в двухцепочечном донорском полинуклеотиде ДНК, предназначены для той же нуклеазы(нуклеаз), которую используют для расщепления эндогенной геномной мишени, в которую вставляют донорский полинуклеотид ДНК.
Трансгены, содержащиеся в последовательностях донорских полинуклеотидов ДНК, описанных в настоящем документе, могут быть выделены из плазмид, клеток или других источников с использованием стандартных методов, известных в данной области, таких как ПЦР. Используемые последовательности донорских полинуклеотидов ДНК могут иметь топологию различных типов, включая кольцевую суперскрученную, кольцевую релаксированную, линейную и тому подобное. Альтернативно, они могут быть химически синтезированы с использованием стандартных методов синтеза олигонуклеотидов. Кроме того, последовательности донорских полинуклеотидов ДНК могут быть метилированными или не метилированными. Последовательности донорских полинуклеотидов ДНК могут быть в форме бактериальных или дрожжевых искусственных хромосом (BAC или YAC), или в форме плазмидных векторов. Последовательности донорских полинуклеотидов ДНК могут быть из T-цепи, которую вводят в растительную клетку с помощью Agrobacterium tumefaciens.
Двухцепочечные донорские полинуклеотиды ДНК, описанные в настоящем документе, могут содержать одно или более неприродных оснований и/или каркасов. В частности, вставку последовательности донорского полинуклеотида ДНК с метилированными остатками цитозина можно осуществлять с использованием способов, описанных в настоящем документе, чтобы достичь состояния покоя транскрипции в интересующей области.
Донорский полинуклеотид ДНК может содержать любую экзогенную интересующую последовательность. Иллюстративные последовательности донорского полинуклеотида ДНК включают, но не ограничиваются ими, любую кодирующую полипептид последовательность (например, кДНК), последовательности промоторов, последовательности энхансеров, эпитопные маркеры, маркерные гены, сайты узнавания расщепляющими ферментами и различные типы экспрессионных конструктов. Маркерные гены включают, но не ограничивается ими, последовательности, кодирующие белки, опосредующие устойчивость к гербицидам (например, устойчивость к HPPD, устойчивость к 2,4-D, устойчивость к глюфозинату или устойчивость к глифосату, в дополнение к другим известным белкам устойчивости к гербицидам), последовательности, кодирующие цветные или флуоресцентные, или люминесцентные белки (например, зеленый флуоресцентный белок, улучшенный зеленый флуоресцентный белок, красный флуоресцентный белок, люциферазу), а также белки, опосредующие усиленный рост клеток и/или амплификацию генов (например, дигидрофолатредуктазу). Эпитопные маркеры включают, например, одну или более копий FLAG, HIS, MYC, TAP, HA или любой поддающейся обнаружению аминокислотной последовательности.
Термины «полинуклеотид», «нуклеиновая кислота» и «молекула нуклеиновой кислоты» охватывают одну нуклеиновую кислоту, а также множество нуклеиновых кислот, фрагмент, вариант или производное нуклеиновой кислоты, или конструкт, например, матричную РНК (мРНК) или плазмидную ДНК (пДНК). Полинуклеотид или нуклеиновая кислота может содержать нуклеотидную последовательность полноразмерной последовательности кДНК или ее фрагмента, включая нетранслируемые 5' и 3'-последовательности и кодирующие последовательности. Если не указано иное, полинуклеотид или нуклеиновая кислота может состоять из любых полирибонуклеотидов или полидезоксирибонуклеотидов, которые могут представлять собой немодифицированную РНК или ДНК, или модифицированную РНК или ДНК. Например, полинуклеотид или нуклеиновая кислота может состоять из одно- и двухцепочечной ДНК, ДНК, представляющей собой смесь одно- и двухцепочечных областей, одно- и двухцепочечной РНК, а также РНК, представляющей собой смесь одно- и двухцепочечных областей, гибридных молекул, содержащих ДНК и РНК, которые могут быть одноцепочечными или, в основном, двухцепочечными или смесью одно- и двухцепочечных областей. Эти термины также охватывают химически, ферментативно или метаболически модифицированные формы полинуклеотида или нуклеиновой кислоты.
Последовательность полинуклеотида или нуклеиновой кислоты можно называть «выделенной», если она была извлечена из своего естественного окружения. Например, гетерологичный полинуклеотид или нуклеиновая кислота, кодирующая полипептид или фрагмент полипептида, который обладает способностью придавать устойчивость к глифосату, содержащаяся в векторе, считается выделенной для целей настоящего изобретения. Дополнительные примеры выделенного полинуклеотида или нуклеиновой кислоты включают рекомбинантный полинуклеотид, находящийся в гетерологичных клетках-хозяевах, или очищенный (частично или в значительной степени) полинуклеотид или нуклеиновую кислоту в растворе. Выделенный полинуклеотид или нуклеиновая кислота в соответствии с вариантами осуществления настоящего изобретения дополнительно включает такие молекулы, получаемые методом синтеза. Выделенный полинуклеотид или нуклеиновая кислота в форме полимера ДНК может состоять из одного или более сегментов кДНК, геномной ДНК или синтетической ДНК.
Термин «ген» означает последовательность нуклеиновой кислоты, кодирующую молекулы функционального продукта, либо РНК, либо белка, необязательно содержащую регуляторные последовательности, которые предшествуют (5'-некодирующие последовательности) и следуют за (3'-некодирующие последовательности) кодирующей последовательностью.
Используемый в настоящем документе термин «кодирующая область» относится к последовательности ДНК, которая кодирует определенную аминокислотную последовательность. «Соответствующие регуляторные последовательности» означают нуклеотидные последовательности, расположенные выше (5'-некодирующие последовательности), внутри или ниже (3'-некодирующие последовательности) кодирующей последовательности, которые влияют на транскрипцию, процессинг или стабильность РНК, или трансляцию связанной кодирующей последовательности. Регуляторные последовательности могут включать промоторы, лидерные последовательности трансляции, интроны, узнаваемые последовательности полиаденилирования, сайт процессинга РНК, сайт связывания эффектора и структуру типа стебель-петля.
Используемый в настоящем документе термин «полипептид» охватывает один «полипептид», а также множество «полипептидов» и их фрагментов, и означает молекулу, состоящую из мономеров (аминокислот), связанных в линейной последовательности амидными связями (также известными как пептидные связи). Термин «полипептид» относится к любой цепи или цепям из двух или более аминокислот и не подразумевает конкретную длину продукта. Таким образом, пептиды, дипептиды, трипептиды, олигопептиды, «белок», «аминокислотная цепь» или любые другие термины, используемые для обозначения цепи или цепей из двух или более аминокислот, включены в понятие «полипептид», и термин «полипептид» можно использовать вместо, или взаимозаменяемо с любым из этих терминов. Полипептид может быть получен из природного биологического источника или получен с помощью рекомбинантных технологий, а не обязательно транслирован с определенной нуклеотидной последовательности. Он может быть получен любым способом, в том числе, химическим синтезом.
«Выделенный» полипептид или его фрагмент, вариант или производное означает полипептид, который находится не в своем естественном окружении. Никакого особого уровня очистки не требуется. Таким образом, определение «выделенный» означает «дело рук человека», как описано в настоящем документе. Например, выделенный полипептид может быть извлечен из его естественного или природного окружения. Рекомбинантные полипептиды и белки, экспрессируемые в клетках-хозяевах, считаются выделенными для целей данного изобретения, так же как и природные или рекомбинантные полипептиды, которые были отделены, фракционированы, либо частично или в значительной степени очищены при помощи любого подходящего метода.
Используемый в настоящем документе термин «природный» относится к форме полинуклеотида, гена или полипептида, которая встречается в природе с их собственными регуляторными последовательностями, при наличии.
Используемый в настоящем документе термин «эндогенный» относится к природной форме полинуклеотида, гена или полипептида в их естественном местонахождении в организме или в геноме организма. «Эндогенный полинуклеотид» включает природный полинуклеотид в его естественном местонахождении в геноме организма. «Эндогенный ген» включает природный ген в его естественном местонахождении в геноме организма. «Эндогенный полипептид» включает природный полипептид в его естественном местонахождении в организме.
Используемый в настоящем документе термин «гетерологичный» относится к полинуклеотиду, гену или полипептиду, который обычно не встречается в организме хозяина, но который введен в организм хозяина. «Гетерологичный полинуклеотид» включает природную кодирующую область, или ее часть, которая вновь введена в исходный организм в форме, отличающейся от соответствующего природного полинуклеотида. «Гетерологичный ген» включает природную кодирующую область, или ее часть, которая вновь введена в исходный организм в форме, отличающейся от соответствующего природного гена. Например, гетерологичный ген может включать природную кодирующую область, которая является частью химерного гена, содержащего неприродные регуляторные области, который вновь введен в организм естественного хозяина. «Гетерологичный полипептид» включает природный полипептид, который вновь введен в исходный организм в форме, которая отличается от соответствующего природного полипептида. Конкретные гены и белки могут быть слиты с другими генами и белками для получения химерных или слитых белков. Гены и белки, полезные в соответствии с вариантами осуществления конкретного изобретения, включают не только приведенные в качестве примера полноразмерные последовательности, но также и части, сегменты и/или фрагменты (включая непрерывные фрагменты и внутренние и/или концевые делеции по сравнению с полноразмерными молекулами) таких последовательностей, их вариантов, мутантов, химерных и слитых продуктов.
В одном из вариантов осуществления донорский полинуклеотид ДНК содержит полинуклеотид, кодирующий любой полипептид, экспрессия которого в клетке желательна, включая, но не ограничиваясь ими, генную экспрессионную кассету, содержащую промоторы, 3'-UTR, признаки устойчивости к гербицидам, признаки устойчивости к насекомым, признаки модифицированного жирового состава, важные в агрономическом отношении признаки, а также функциональные фрагменты любого из вышеперечисленных. Кодирующие последовательности могут представлять собой, например, кДНК.
Термин «промотор» означает последовательность ДНК, способную контролировать экспрессию кодирующей последовательности или функциональной РНК. Как правило, кодирующая последовательность расположена в 3'-положении по отношению к последовательности промотора. Промоторы могут происходить полностью из природного гена или быть составлены из различных элементов, полученных из разных промоторов, встречающихся в природе, или даже содержать синтетические сегменты ДНК. Специалисты в данной области понимают, что разные промоторы могут направлять экспрессию гена в разных типах тканей или клеток, или на разных стадиях развития, или в ответ на различные экологические или физиологические условия. Промоторы, которые вызывают экспрессию гена в большинстве типов клеток в большинстве случаев, обычно называют «конститутивными промоторами». Понятно также, что, поскольку в большинстве случаев точные границы регуляторных последовательностей полностью не определены, фрагменты ДНК разной длины могут иметь идентичную промоторную активность.
Термин «функционально связанные» означает такую связь нуклеотидных последовательностей на одном фрагменте нуклеиновой кислоты, что на функцию одной оказывает влияние другая. Например, промотор функционально связан с кодирующей последовательностью, если он способен влиять на экспрессию этой кодирующей последовательности (например, кодирующая последовательность находится под транскрипционным контролем промотора). Кодирующие последовательности могут быть функционально связаны с регуляторными последовательностями в смысловой или антисмысловой ориентации.
Используемый в настоящем документе термин «экспрессия» означает транскрипцию и стабильное накопление смысловой (мРНК) или антисмысловой РНК, полученной с фрагмента нуклеиновой кислоты по вариантам осуществления изобретения. Термин «экспрессия» может также относиться к трансляции мРНК в полипептид.
Используемый в настоящем документе термин «избыточная экспрессия» означает экспрессию, которая превышает эндогенную экспрессию того же или родственного гена. Гетерологичный ген является избыточно экспрессированным, если его экспрессия выше, чем экспрессия сопоставимого эндогенного гена.
Используемый в настоящем документе термин «трансформация» означает перенос и интегрирование нуклеиновой кислоты или фрагмента в организм хозяина, что приводит к генетически стабильному наследованию. Организмы-хозяева, содержащие введенные трансформацией фрагменты нуклеиновой кислоты, называют «трансгенными» или «рекомбинантными» или «трансформированными» организмами. Известные методы трансформации включают опосредованную Agrobacterium tumefaciens или Agrobacterium rhizogenes трансформацию, трансформацию с использованием фосфата кальция, трансформацию с использованием полибрена, слияние протопластов, электропорацию, методы с использованием ультразвука (например, сонопорацию), трансформацию с использованием липосом, микроинъекцию, введение «голой» ДНК, плазмидных векторов, вирусных векторов, биолистику (бомбардировку микрочастицами), опосредованную карбидом кремния WHISKERS™ трансформацию, аэрозольную инжекцию или трансформацию с использованием ПЭГ, а также другие возможные методы.
Используемые в настоящем документе термины «плазмида» и «вектор» относятся к внехромосомному элементу, часто несущему гены, которые не являются частью центрального метаболизма клетки, и обычно находящемуся в форме кольцевой двухцепочечной молекулы ДНК. Такие элементы могут представлять собой автономно реплицируемые последовательности, интегрируемые в геном последовательности, фаговые или нуклеотидные последовательности, линейные или кольцевые, одно- или двухцепочечных ДНК или РНК, полученные из любого источника, в которых несколько нуклеотидных последовательностей объединены или скомпонованы в уникальную конструкцию, способную вводить фрагмент промотора и последовательность ДНК для выбранного генного продукта, наряду с соответствующей 3'-нетранслируемой последовательностью, в клетку.
Используемый в настоящем документе термин «вырожденность кодонов» относится к характерной особенности генетического кода, допускающей вариации в нуклеотидной последовательности без влияния на аминокислотную последовательность закодированного полипептида. Специалисту хорошо известно «предпочтение кодонов», демонстрируемое определенной клеткой-хозяином в использовании нуклеотидных кодонов для кодирования конкретной аминокислоты. Вследствие этого, при синтезе гена для улучшенной экспрессии в клетке-хозяине желательно конструировать ген таким образом, чтобы его частота использования кодонов приближалась к частоте использования кодонов, предпочтительной для клетки-хозяина.
Термин «кодон-оптимизированный» при использовании применительно к генам или кодирующим областям молекул нуклеиновой кислоты, предназначенных для трансформации различных хозяев, означает изменение кодонов в гене или кодирующих областях молекул нуклеиновой кислоты для отражения типичного использования кодонов в организме хозяина без изменения полипептида, кодируемого ДНК. Такая оптимизация включает замену по меньшей мере одного или более чем одного, или значительного числа кодонов одним или более кодонами, которые более часто используются в генах данного организма.
Термин «процент идентичности» (или «% идентичности»), как известно в данной области, означает отношение между двумя или более полипептидными последовательностями, или двумя или более полинуклеотидными последовательностями, определяемое при сравнении последовательностей. В данной области «идентичность» также означает степень родства последовательностей между полипептидными или полинуклеотидными последовательностями, в зависимости от обстоятельств, определяемую путем сравнения между цепями таких последовательностей. «Идентичность» или «сходство» можно с легкостью рассчитывать известными методами, включая, но не ограничиваясь ими, те, которые описаны в: 1) Computational Molecular Biology (Lesk, A. M., Ed.) Oxford University: NY (1988), 2) Biocomputing: Informatics and Genome Projects (Smith, D. W., Ed.) Academic: NY (1993), 3) Computer Analysis of Sequence Data, Part I (Griffin, A. M., and Griffin, H. G., Eds.) Humania: NJ (1994), 4) Sequence Analysis in Molecular Biology (von Heinje, G., Ed.) Academic (1987) и 5) Sequence Analysis Primer (Gribskov, M. and Devereux, J., Eds.) Stockton: NY (1991).
Методики определения идентичности нуклеотидных и аминокислотных последовательностей известны в данной области. Как правило, такие методики включают определение нуклеотидной последовательности мРНК для гена и/или определение аминокислотной последовательности, кодируемой им, и сравнение этой последовательности со второй нуклеотидной или аминокислотной последовательностью. Геномные последовательности также можно определять и сравнивать таким образом. Как правило, идентичность означает точное соответствие между нуклеотидами или аминокислотами в двух полинуклеотидных или полипептидных последовательностях, соответственно. Две или более последовательностей (полинуклеотидных или аминокислотных) можно сравнивать, определяя процент их идентичности. Процент идентичности двух последовательностей, либо нуклеотидных, либо аминокислотных последовательностей, представляет собой число точных совпадений между двумя выровненными последовательностями, разделенное на длину более короткой последовательности и умноженное на 100. Смотри статью Russell, R., and Barton, G., «Structural Features can be Unconserved in Proteins with Similar Folds», J. Mol. Biol. 244, 332-350 (1994), p. 337, полное содержание которой включено в настоящий документ посредством ссылки.
Кроме того, методы определения идентичности и сходства лежат в основе общедоступных компьютерных программ. Выравнивания последовательностей и расчеты процента идентичности можно выполнять, например, с использованием программы AlignX пакета программ Vector NTI® (Invitrogen, Carlsbad, CA) или программы MegAlign™ пакета программ LASERGENE™ для биоинформатики (DNASTAR Inc., Madison, WI). Множественное выравнивание последовательностей выполняют с использованием «метода выравнивания Clustal», который включает несколько разновидностей алгоритма, в том числе «метод выравнивания Clustal V», соответствующий методу выравнивания, обозначенному Clustal V (описано Higgins and Sharp, CABIOS. 5: 151-153 (1989), Higgins, D.G. et al., Comput. Appl. Biosci., 8: 189-191 (1992)) и используемому в программе MegAlign™ пакета компьютерных программ LASERGENE™ для биоинформатики (DNASTAR Inc.). Для множественных выравниваний значения по умолчанию соответствуют: штраф за делецию = 10 и штраф за удлинение делеции = 10. Параметры по умолчанию для парных выравниваний и расчетов процента идентичности белковых последовательностей с использованием метода Clustal соответствуют: участок максимального совпадения = 1, штраф за делецию = 3, окно = 5 и сохраненные диагонали = 5. Для нуклеиновых кислот эти параметры соответствуют: участок максимального совпадения = 2, штраф за делецию = 5, окно = 4 и сохраненные диагонали = 4. После выравнивания последовательностей с использованием программы Clustal V, можно определять «процент идентичности», обращаясь к таблице «расстояние между последовательностями» в той же программе. Кроме того, доступен «метод выравнивания Clustal W», который соответствует методу выравнивания, обозначенному Clustal W (описано Higgins and Sharp, CABIOS. 5: 151-153 (1989), Higgins, D.G. et al., Comput. Appl. Biosci. 8: 189-191(1992)) и используемому в программе MegAlign™ v6.1 пакета компьютерных программ LASERGENE™ для биоинформатики (DNASTAR Inc.). Параметры по умолчанию для множественного выравнивания (штраф за делецию = 10, штраф за удлинение делеции = 0,2, задержка различающихся последовательностей (%) = 30, вес транзиций ДНК = 0,5, матрица сравнения аминокислот = Gonnet Series, матрица сравнения нуклеотидов = IUB). После выравнивания последовательностей с использованием программы Clustal W можно определять «процент идентичности», обращаясь к таблице «расстояние между последовательностями» в той же программе.
Нуклеотидные зонды и праймеры по вариантам осуществления настоящего изобретения можно гибридизовать в условиях гибридизации с целевой последовательностью ДНК в реакции амплификации. Можно использовать любой общепринятый метод гибридизации или амплификации нуклеиновых кислот для определения присутствия донорского полинуклеотида ДНК, вставленного в целевой геномный локус. Молекулы нуклеиновой кислоты, олигонуклеотиды или их фрагменты способны специфически гибридизоваться с другими молекулами нуклеиновой кислоты в определенных условиях. В настоящем документе считается, что две молекулы нуклеиновой кислоты способны специфически гибридизоваться друг с другом, если две молекулы способны образовывать антипараллельную, двухцепочечную структуру нуклеиновой кислоты. Молекула нуклеиновой кислоты считается «комплементом» другой молекулы нуклеиновой кислоты, если две молекулы нуклеиновой кислоты проявляют полную комплементарность. В настоящем документе считается, что молекулы проявляют «полную комплементарность», если каждый нуклеотид одной молекулы комплементарен нуклеотиду другой молекулы. Молекулы, проявляющие полную комплементарность, как правило, будут гибридизоваться друг с другом с достаточной стабильностью, чтобы они могли оставаться гибридизованными друг с другом в общепринятых «очень строгих» условиях. Общепринятые очень строгие условия описаны в Sambrook et al., 1989.
Две молекулы считаются проявляющими «минимальную комплементарность», если они могут гибридизоваться друг с другом с достаточной стабильностью, чтобы они могли оставаться гибридизованными друг с другом по меньшей мере в общепринятых «нестрогих» условиях. Общепринятые нестрогие условия описаны в Sambrook et al., 1989. Для того чтобы молекула нуклеиновой кислоты служила в качестве праймера или зонда, она должна проявлять лишь минимальную комплементарность последовательности, чтобы быть способной к образованию стабильной двухцепочечной структуры при использовании конкретного растворителя и концентраций соли.
Факторы, влияющие на строгость условий гибридизации, хорошо известны специалистам в данной области и включают, но не ограничиваются ими, температуру, pH, ионную силу и концентрацию органических растворителей, таких как, например, формамид и диметилсульфоксид. Как известно специалистам в данной области, строгость условий гибридизации возрастает с повышением температуры, снижением ионной силы и снижением концентрации растворителя.
Термин «строгие условия» или «строгость условий» функционально определяют применительно к гибридизации нуклеотидного зонда с целевой нуклеиновой кислотой (то есть, с конкретной интересующей нуклеотидной последовательностью) по методу специфической гибридизации, описанному в Sambrook et al., 1989.
Как правило, строгие условия являются такими, при которых концентрация соли составляет менее чем примерно 1,5 M ионов Na+, как правило, концентрация примерно 0,01-1,0 M ионов Na+ (или других солей) при pH 7,0-8,3 и температура по меньшей мере примерно 30°C для коротких зондов (например, 10-50 нуклеотидов) и по меньшей мере примерно 60°C для длинных зондов (например, более 50 нуклеотидов). Строгие условия могут быть также достигнуты за счет добавления дестабилизаторов, таких как формамид. Иллюстративные нестрогие условия включают гибридизацию в буферном растворе 30-35% формамида, 1,0 M NaCl, 0,1% SDS (додецилсульфат натрия) при 37°C и промывание 1X-2X SSC (20X SSC = 3,0 M NaCl/0,3 M цитрат тринатрия) при 50-55°C. Иллюстративные умеренно строгие условия включают гибридизацию в 40-45% формамиде, 1,0 M NaCl, 0,1% SDS при 37°C и промывание в 0,5X-1X SSC при 55-60°C. Иллюстративные очень строгие условия включают гибридизацию в 50% формамиде, 1,0 M NaCl, 0,1% SDS при 37°C и промывание в 0,1X SSC при 60-65°C.
Специфичность, как правило, зависит от промываний после гибридизации, при этом критическими факторами являются ионная сила и температура последнего промывающего раствора. Для ДНК-ДНК гибридов Tm может быть аппроксимирована из уравнения Tm=81,5°C+16,6(logM)+0,41(%GC)-0,61(%форм.)-500/L, где M представляет собой молярность одновалентных катионов, %GC означает процентное содержание нуклеотидов гуанозина и цитозина в ДНК, % форм. означает процентное содержание формамида в растворе гибридизации и L представляет собой длину гибрида в парах оснований (Meinkoth and Wahl, 1984). Tm представляет собой температуру (при определенной ионной силе и pH), при которой 50% комплементарной целевой последовательности гибридизуется с идеально соответствующим зондом. Tm уменьшается примерно на 1°C для каждого 1% несовпадений, таким образом, Tm гибридизации и/или условия промывания можно корректировать для гибридизации последовательностей желаемого качества. Например, если нужны последовательности с 90% идентичности, Tm можно уменьшать на 10°C. Как правило, строгость условий выбирают так, чтобы температура была примерно на 5°C ниже, чем температура плавления (Tm) для определенной последовательности и ее комплемента при определенных значениях ионной силы и pH. Однако для очень строгих условий можно использовать гибридизацию и/или промывание при температуре на 1, 2, 3 или 4°C ниже, чем температура плавления (Tm); для умеренно строгих условий можно использовать гибридизацию и/или промывание при температуре на 6, 7, 8, 9 или 10°C ниже, чем температура плавления (Tm); для нестрогих условий можно использовать гибридизацию и/или промывание при температуре на 11-20°C ниже, чем температура плавления (Tm). Используя уравнение, композиции для гибридизации и промывания, а также желательную Tm, специалисты понимают, что по своей природе имеют место вариации условий строгости гибридизации и/или промывающих растворов. Если желаемая степень несоответствия имеет место при Tm менее 45°C (водный раствор) или 32°C (раствор формамида), предпочтительно повышать концентрацию SSC так, чтобы можно было использовать более высокую температуру. Подробное руководство по гибридизации нуклеиновых кислот можно найти в (1997) Ausubel et al., Short Protocols in Molecular Biology, pages 2-40, 3rd Ed. (1997) и Sambrook et al. (1989).
В одном из вариантов осуществления изобретение относится к введению донорского полинуклеотида ДНК, который вставляется в целевой геномный локус. Стандартные методы рекомбинантной ДНК и молекулярного клонирования для конструирования донорского полинуклеотида ДНК, который в одном из вариантов осуществления содержит генную экспрессионную кассету, описанную в настоящем документе, хорошо известны в данной области и описаны, например, в Sambrook et al., Molecular Cloning: A Laboratory Manual, Second Edition, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY (1989), и в Silhavy et al., Experiments with Gene Fusions, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY (1984), а также в Ausubel et al., Current Protocols in Molecular Biology, издательства Greene Publishing Assoc. и Wiley-Interscience (1987).
В способах, раскрытых в настоящем документе, можно использовать ряд промоторов, которые направляют экспрессию гена в растении. Такие промоторы можно выбирать из конститутивных, химически регулируемых, индуцируемых, тканеспецифичных и действующих предпочтительно в семенах промоторов. Промотор, используемый для направления экспрессии нуклеиновой кислоты, зависит от конкретного применения. Например, сильный конститутивный промотор, подходящий для клетки-хозяина, как правило, используют для экспрессии и очистки экспрессированных белков.
Неограничивающие примеры предпочтительных растительных промоторов включают последовательности промоторов из убикитина-10 (ubi-10) A. thaliana (Callis, et al., 1990, J. Biol. Chem., 265: 12486-12493), маннопин-синтазы (Δmas) A. tumefaciens (Petolino et al., патент США №6730824), и/или вируса мозаики жилок маниоки (CsVMV) (Verdaguer et al., 1996, Plant Molecular Biology 31: 1129-1139). Другие конститутивные промоторы включают, например, промотор 35S вируса мозаики цветной капусты (Odell et al. (1985) Nature 313: 810-812), промотор актина риса (McElroy et al. (1990) Plant Cell 2: 163-171), промотор убиквитина кукурузы (патент США номер 5510474, Christensen et al. (1989) Plant Mol. Biol. 12: 619-632 и Christensen et al. (1992) Plant Mol. Biol. 18: 675-689), промотор pEMU (Last et al. (1991) Theor. Appl. Genet. 81: 581-588), промотор ALS (патент США номер 5659026), промотор гистона кукурузы (Chabouté et al. Plant Molecular Biology, 8: 179-191 (1987)), и тому подобные.
Другие применимые растительные промоторы включают тканеспецифичные и индуцируемые промоторы. Индуцируемый промотор представляет собой промотор, способный к прямой или опосредованной активации транскрипции одной или более последовательностей ДНК или генов в ответ на индуктор. В отсутствие индуктора последовательности ДНК или гены не будут транскрибироваться. Как правило, белковый фактор, который связывается специфически с индуцируемым регуляторным элементом для активации транскрипции, присутствует в неактивной форме, которая затем прямо или опосредованно превращается в активную форму с помощью индуктора. Индуктором может быть химическое вещество, такое как белок, метаболит, регулятор роста, гербицид или фенольное соединение, либо физиологический стресс, вызываемый непосредственно жарой, холодом, солью или токсичными элементами, или опосредованно через действие патогена или болезнетворного агента, такого как вирус. Как правило, белковый фактор, который связывается специфически с индуцируемым регуляторным элементом для активации транскрипции, присутствует в неактивной форме, которая затем прямо или опосредованно превращается в активную форму с помощью индуктора. Индуктором может быть химическое вещество, такое как белок, метаболит, регулятор роста, гербицид или фенольное соединение, либо физиологический стресс, вызываемый непосредственно жарой, холодом, солью или токсичными элементами, или опосредованно через действие патогена или болезнетворного агента, такого как вирус. Растительная клетка, содержащая индуцируемый регуляторный элемент, может подвергаться действию индуктора при внешнем нанесении индуктора на клетку или растение, например, путем опрыскивания, полива, нагревания или аналогичных способов.
В вариантах осуществления настоящего изобретения можно использовать любой индуцируемый промотор. Смотри Ward et al., Plant Mol. Biol. 22: 361-366 (1993). Иллюстративные индуцируемые промоторы включают промоторы рецептора экдизона (патент США №6504082), промоторы из системы ACE1, реагирующие на медь (Mett et al., Proc. Natl. Acad. Sci. 90: 4567-4571 (1993)), промоторы генов In2-1 и In2-2 из кукурузы, реагирующие на антидоты бензолсульфонамидных гербицидов (патент США №5364780, Hershey et al., Mol. Gen. Genetics 227: 229-237 (1991) и Gatz et al., Mol. Gen. Genetics 243: 32-38 (1994)), Tet репрессор из Tn10 (Gatz et al., Mol. Gen. Genet. 227: 229-237 (1991) или промоторы из гена стероидного гормона, транскрипционная активность которых индуцируется глюкокортикостероидным гормоном, Schena et al., Proc. Natl. Acad. Sci. U.S.A. 88: 10421 (1991) и McNellis et al., (1998) Plant J. 14(2): 247-257, промотор GST кукурузы, который активируется гидрофобными электрофильными соединениями, используемыми в качестве довсходовых гербицидов (смотри патент США №5965387 и международную публикацию патентной заявки №WO 93/001294), а также промотор PR-1a табака, который активируется салициловой кислотой (смотри Ono S., Kusama M., Ogura R., Hiratsuka K., «Evaluation of the Use of the Tobacco PR-1a Promoter to Monitor Defense Gene Expression by the Luciferase Bioluminescence Reporter System», Biosci Biotechnol Biochem. 2011 Sep 23, 75(9): 1796-800). Другие представляющие интерес химически регулируемые промоторы включают тетрациклин-индуцируемые и тетрациклин-репрессируемые промоторы (смотри, например, Gatz et al., (1991) Mol. Gen. Genet. 227: 229-237, и патенты США номера 5814618 и 5789156).
Другие представляющие интерес регулируемые промоторы включают реагирующий на холод регуляторный элемент или регуляторный элемент теплового шока, транскрипция которого может осуществляться в ответ на воздействие холода или тепла, соответственно (Takahashi et al., Plant Physiol. 99: 383-390, 1992), промотор гена алкогольдегидрогеназы (Gerlach et al., PNAS USA 79: 2981-2985 (1982), Walker et al., PNAS 84(19): 6624-6628 (1987)), индуцируемый анаэробными условиями, и индуцируемый светом промотор из гена rbcS гороха или гена psaDb гороха (Yamamoto et al., (1997) Plant J. 12(2): 255-265), индуцируемый светом регуляторный элемент (Feinbaum et al., Mol. Gen. Genet. 226: 449, 1991, Lam and Chua, Science 248: 471, 1990, Matsuoka et al. (1993) Proc. Natl. Acad. Sci. USA 90(20): 9586-9590, Orozco et al. (1993) Plant Mol. Bio. 23(6): 1129-1138), индуцируемый растительным гормоном регуляторный элемент (Yamaguchi-Shinozaki et al., Plant Mol. Biol. 15: 905, 1990, Kares et al., Plant Mol. Biol. 15: 225, 1990), и тому подобное. Индуцируемым регуляторным элементом может также быть промотор генов In2-1 и In2-2 кукурузы, реагирующий на антидоты бензолсульфонамидных гербицидов (Hershey et al., Mol. Gen. Gene. 227: 229-237, 1991, Gatz et al., Mol. Gen. Genet. 243: 32-38, 1994), а также Tet репрессор из транспозона Tn10 (Gatz et al., Mol. Gen. Genet. 227: 229-237, 1991). Индуцируемые стрессом промоторы включают промоторы, индуцируемые солевым/водным стрессом, такие как P5CS (Zang et al., (1997) Plant Sciences 129: 81-89), индуцируемые холодом промоторы, такие как cor15a (Hajela et al., (1990) Plant Physiol. 93: 1246-1252), cor15b (Wilhelm et al., (1993) Plant Mol Biol 23: 1073-1077), wsc1 (Ouellet et al., (1998) FEBS Lett. 423-324-328), ci7 (Kirch et al., (1997) Plant Mol Biol. 33: 897-909), ci21A (Schneider et al., (1997) Plant Physiol. 113: 335-45), индуцируемые засухой промоторы, такие как Trg-31 (Chaudhary et al., (1996) Plant Mol. Biol. 30: 1247-57), rd29 (Kasuga et al., (1999) Nature Biotechnology 18: 287-291), осмотически индуцируемые промоторы, такие как Rab17 (Vilardell et al., (1991) Plant Mol. Biol. 17: 985-93) и осмотин (Raghothama et al., (1993) Plant Mol Biol 23: 1117-28), а также индуцируемые теплом промоторы, такие как белки теплового шока (Barros et al., (1992) Plant Mol. 19: 665-75, Marrs et al., (1993) Dev. Genet. 14: 27-41), smHSP (Waters et al., (1996) J. Experimental Botany 47: 325-338), и индуцируемый тепловым шоком элемент из промотора убиквитина петрушки (WO 03/102198). Другие индуцируемые стрессом промоторы включают rip2 (патент США №5332808 и патентная публикация США №2003/0217393) и rd29a (Yamaguchi-Shinozaki et al., (1993) Mol. Gen. Genetics 236: 331-340). Некоторые промоторы индуцируются повреждениями, включая промотор pMAS Agrobacterium (Guevara-Garcia et al., (1993) Plant J. 4(3): 495-505) и промотор ORF13 Agrobacterium (Hansen et al., (1997) Mol. Gen. Genet. 254(3): 337-343).
Тканепредпочтительные промоторы можно использовать для целевой усиленной транскрипции и/или экспрессии в конкретной ткани растения. При упоминании предпочтительной экспрессии имеется в виду то, что в конкретной ткани растения экспрессия имеет место на более высоком уровне, чем в других тканях растения. Примеры промоторов таких типов включают предпочтительную экспрессию в семенах, которую обеспечивает промотор фазеолина (Bustos et al., (1989) The Plant Cell Vol. 1, 839-853) и гена глобулина-1 кукурузы (Belanger, et al. (1991) Genetics 129: 863-972). У двудольных растений предпочтительные для семян промоторы включают, но не ограничиваются ими, промоторы β-фазеолина фасоли, напина, β-конглицинина, лектина сои, круциферина и тому подобные. У однодольных растений предпочтительные для семян промоторы включают, но не ограничиваются ими, промоторы 15-кДа зеина, 22-кДа зеина, 27-кДа зеина, γ-зеина, восковый, shrunken 1, shrunken 2, глобулина 1 кукурузы, и так далее. Предпочтительные для семян промоторы также включают такие промоторы, которые направляют экспрессию гена преимущественно к специфическим тканям в семени, такие как, например, предпочтительный для эндосперма промотор γ-зеина, криптический промотор из табака (Fobert et al., (1994) T-DNA tagging of a seed coat-specific cryptic promoter in tobacco. Plant J. 4: 567-577), промотор P-гена кукурузы (Chopra et al., (1996) Alleles of the maize P gene with distinct tissue specificities encode Myb-homologous proteins with C-terminal replacements. Plant Cell 7: 1149-1158, Erratum in Plant Cell, 1997, 1: 109), промотор глобулина-1 кукурузы (Belenger and Kriz (1991) Molecular basis for Allelic Polymorphism of the maize Globulin-1 gene. Genetics 129: 863-972), а также промоторы, которые направляют экспрессию к семенной оболочке или кожице зерен кукурузы, например, специфичный для околоплодника промотор глутаминсинтетазы (Muhitch et al., (2002) Isolation of a Promoter Sequence From the Glutamine Synthetase1-2 Gene Capable of Conferring Tissue-Specific Gene Expression in Transgenic Maize. Plant Science 163: 865-872).
Помимо промотора, экспрессионный вектор, как правило, содержит транскрипционную единицу или экспрессионную кассету, содержащую все дополнительные элементы, необходимые для экспрессии нуклеиновой кислоты в клетках-хозяевах, либо прокариотических, либо эукариотических. Таким образом, типичная экспрессионная кассета содержит промотор, функционально связанный, например, с последовательностью нуклеиновой кислоты, кодирующей белок, и сигналы, необходимые, например, для эффективного полиаденилирования транскрипта, терминации транскрипции, сайтов связывания рибосомы или терминации трансляции. Дополнительные элементы кассеты могут включать, например, энхансеры и гетерологичные сигналы сплайсинга.
Могут быть включены другие компоненты вектора, также в зависимости от предполагаемого использования гена. Примеры включают селективные маркеры, направляющие или регуляторные последовательности, последовательности транзитных пептидов, такие как оптимизированная последовательность транзитного пептида (смотри патент США №5510471), стабилизирующие последовательности, такие как RB7 MAR (смотри Thompson and Myatt, (1997) Plant Mol. Biol., 34: 687-692 и международную патентную публикацию №WO 9727207) или лидерные последовательности, интроны и так далее. Общее описание и примеры экспрессионных векторов растений и репортерных генов можно найти в Gruber, et al., «Vectors for Plant Transformation» в Methods in Plant Molecular Biology and Biotechnology, Glick et al. Eds, CRC Press pp. 89-119 (1993). Выбор соответствующего экспрессионного вектора будет зависеть от хозяина и метода введения экспрессионного вектора в организм хозяина. Экспрессионная кассета будет также включать на 3'-конце интересующей гетерологичной нуклеотидной последовательности области терминации транскрипции и трансляции, функциональные в растениях. Область терминации может происходить из одного источника с нуклеотидной последовательностью промотора по вариантам осуществления настоящего изобретения, может происходить из одного источника с интересующей последовательностью ДНК или может быть получена из другого источника. Подходящие области терминации можно получать из Ti-плазмиды A. tumefaciens, например, области терминации октопинсинтазы и нопалинсинтазы (nos) (Depicker et al., Mol. and Appl. Genet. 1: 561-573 (1982) и Shaw et al. (1984) Nucleic Acids Research vol. 12, No. 20 pp. 7831-7846 (nos)), смотри также Guerineau et al. Mol. Gen. Genet. 262: 141-144 (1991), Proudfoot, Cell 64: 671-674 (1991), Sanfacon et al. Genes Dev. 5: 141-149 (1991), Mogen et al. Plant Cell 2: 1261-1272 (1990), Munroe et al. Gene 91: 151-158 (1990), Ballas et al., Nucleic Acids Res. 17: 7891-7903 (1989), Joshi et al. Nucleic Acids Res. 15: 9627-9639 (1987).
Кроме того, экспрессионные кассеты могут содержать 5'-лидерные последовательности. Такие лидерные последовательности могут способствовать усилению трансляции. Трансляционные лидерные последовательности известны в данной области и включают в качестве примера лидерные последовательности пикорнавируса, лидерную последовательность EMCV (5'-некодирующая область из вируса энцефаломиокардита), Elroy-Stein et al., Proc. Nat. Acad. Sci. USA 86: 6126-6130 (1989), лидерные последовательности потивирусов, например, лидерную последовательность TEV (вирус гравировки табака) Carrington and Freed, Journal of Virology, 64: 1590-1597 (1990), лидерную последовательность MDMV (вирус карликовой мозаики кукурузы), Allison et al., Virology 154: 9-20 (1986), белка, связывающего тяжелую цепь иммуноглобулинов человека (BiP), Macejak et al., Nature 353: 90-94 (1991), нетранслируемую лидерную последовательность из мРНК белка оболочки вируса мозаики люцерны (AMV RNA 4), Jobling et al., Nature 325: 622-625 (1987), лидерную последовательность вируса табачной мозаики (TMV), Gallie et al., (1989) Molecular Biology of RNA, pages 237-256, и лидерную последовательность вируса хлоротичной крапчатости кукурузы (MCMV) Lommel et al., Virology 81: 382-385 (1991). Смотри также Della-Cioppa et al., Plant Physiology 84: 965-968 (1987).
Конструкт может также содержать последовательности, которые усиливают трансляцию и/или стабильность мРНК, такие как интроны. Примером одного такого интрона является первый интрон гена II варианта H3.III гистона из Arabidopsis thaliana. Chaubet et al., Journal of Molecular Biology, 225: 569-574 (1992).
В тех случаях, когда желательно, чтобы экспрессированный продукт гетерологичной нуклеотидной последовательности направлялся в конкретную органеллу, в частности, пластиду, амилопласт, или в эндоплазматический ретикулум, или секретировался на поверхности клетки или внеклеточно, экспрессионная кассета может дополнительно содержать кодирующую последовательность для транзитного пептида. Такие транзитные пептиды хорошо известны в данной области и включают, но не ограничивается ими, транзитный пептид для ацил белка-носителя, малой субъединицы RUBISCO, EPSP синтазы растений и Helianthus annuus (патент США №5510417), транзитный пептид хлоропласта для Brittle-1 Zea mays (Nelson et al., Plant Physiol 117(4): 1235-1252 (1998), Sullivan et al., Plant Cell 3(12): 1337-48, Sullivan et al., Planta (1995) 196(3): 477-84, Sullivan et al., J. Biol. Chem. (1992) 267(26): 18999-9004) и тому подобное. Кроме того, в данной области известны химерные транзитные пептиды хлоропласта, такие как оптимизированный транзитный пептид (патент США №5510471). Дополнительные транзитные пептиды хлоропласта ранее описаны в патенте США №5717084 и патенте США №5728925. Специалисты в данной области без труда поймут множество имеющихся вариантов экспрессии продукта в конкретной органелле. Например, последовательность альфа-амилазы ячменя часто используют для направления экспрессии в эндоплазматический ретикулум (Rogers, J. Biol. Chem. 260: 3731-3738 (1985)).
Специалистам в данной области понятно, что использование технологий рекомбинантной ДНК позволяет усовершенствовать контроль экспрессии трансфицированных молекул нуклеиновой кислоты за счет манипулирования, например, числом копий молекул нуклеиновой кислоты в клетке-хозяине, эффективности, с которой эти молекулы нуклеиновой кислоты транскрибируются, эффективности, с которой полученные транскрипты транслируются, и эффективности посттрансляционных модификаций. Кроме того, генно-инженерными методами может быть сконструирована последовательность промотора для повышения уровня экспрессии по сравнению с природным промотором. Рекомбинантные методы, полезные для контроля экспрессии молекул нуклеиновой кислоты, включают, но не ограничиваются ими, стабильную интеграцию молекул нуклеиновой кислоты в одну или более хромосом клетки-хозяина, добавление векторных стабилизирующих последовательностей в плазмиды, замены или модификации сигналов контроля транскрипции (например, промоторов, операторов, энхансеров), замены или модификации сигналов контроля трансляции (например, сайтов связывания рибосом, последовательностей Шайна-Дальгарно или Козак), модификацию молекул нуклеиновой кислоты для соответствия предпочтительному использованию кодонов клетки-хозяина, а также делецию последовательностей, дестабилизирующих транскрипты.
В трансформирующие векторы можно включать репортерные или маркерные гены для отбора трансформированных клеток или тканей, или частей растений, или растений. Примеры селективных маркеров включают те, которые придают устойчивость к антиметаболитам, таким как гербициды или антибиотики, например, дигидрофолатредуктаза, которая придает устойчивость к метотрексату (Reiss, Plant Physiol. (Life Sci. Adv.) 13: 143-149, 1994, смотри также Herrera Estrella et al., Nature 303: 209-213, (1983), Meijer et al., Plant Mol. Biol. 16: 807-820, (1991)), неомицин фосфотрансфераза, которая придает устойчивость к аминогликозидам неомицину, канамицину и паромицину (Herrera-Estrella, EMBO J. 2: 987-995, 1983 и Fraley et al., Proc. Natl. Acad. Sci USA 80: 4803 (1983)), и гигромицин фосфотрансфераза, которая придает устойчивость к гигромицину (Marsh, Gene 32: 481-485, (1984), смотри также Waldron et al., Plant Mol. Biol. 5: 103-108, (1985), Zhijian et al., Plant Science 108: 219-227, (1995)), trpB, который позволяет клеткам утилизировать индол вместо триптофана, hisD, который позволяет клеткам утилизировать гистинол вместо гистидина (Hartman, Proc. Natl. Acad. Sci., USA 85: 8047, (1988)), манноза-6-фосфат-изомераза, которая позволяет клеткам утилизировать маннозу (международная патентная заявка №WO 94/20627), орнитин декарбоксилаза, которая придает устойчивость к ингибитору орнитин декарбоксилазы, 2-(дифторметил)-DL-орнитин (DFMO, McConlogue, 1987, In: Current Communications in Molecular Biology, Cold Spring Harbor Laboratory ed.) и дезаминаза из Aspergillus terreus, которая придает устойчивость к бластицидину S (Tamura, Biosci. Biotechnol. Biochem. 59: 2336-2338, (1995)).
Дополнительные селективные маркеры включают, например, мутантную ацетолактатсинтазу, которая придает устойчивость к имидазолинону или сульфонилмочевине (Lee et al., EMBO J. 7: 1241-1248, (1988)), мутантный psbA, который придает устойчивость к атразину (Smeda et al., Plant Physiol. 103: 911-917, (1993)), или мутантную протопорфириноген-оксидазу (смотри патент США №5767373), или другие маркеры, придающие устойчивость к такому гербициду, как глюфозинат. Примеры подходящих генов селективных маркеров включают, но не ограничиваются ими, гены, кодирующие признак устойчивости к хлорамфениколу (Herrera Estrella et al., EMBO J. 2: 987-992, (1983)), стрептомицину (Jones et al., Mol. Gen. Genet. 210: 86-91, (1987)), спектиномицину (Bretagne-Sagnard et al., Transgenic Res. 5: 131-137, (1996)), блеомицину (Hille et al., Plant Mol. Biol. 7: 171-176, (1990)), сульфонамиду (Guerineau et al., Plant Mol. Biol. 15: 127-136, (1990)), бромоксинилу (Stalker et al., Science 242: 419-423, (1988)), глифосату (Shaw et al., Science 233: 478-481, (1986)), фосфинотрицину (DeBlock et al., EMBO J. 6: 2513-2518, (1987)), и тому подобные.
Одним из вариантов используемого селективного гена является ДНК, кодирующая признак устойчивости к глюфозинату, и в одном из вариантов осуществления может быть использован ген фосфинотрицин ацетил трансферазы (pat), оптимизированный ген pat или ген bar кукурузы под контролем промотора вируса мозаики жилок маниоки. Эти гены придают устойчивость к биалафосу. Смотри (Wohlleben et al., (1988) Gene 70: 25-37), Gordon-Kamm et al., Plant Cell 2: 603, 1990, Uchimiya et al., BioTechnology 11: 835, 1993, White et al., Nucl. Acids Res. 18: 1062, 1990, Spencer et al., Theor. Appl. Genet. 79: 625-631, 1990 и Anzai et al., Mol. Gen. Gen. 219: 492, 1989). Вариантом гена pat является оптимизированный ген pat кукурузы, описанный в патенте США №6096947.
Кроме того, можно использовать маркеры, облегчающие идентификацию растительной клетки, содержащей полинуклеотид, кодирующий маркер. Полезными являются маркеры, позволяющие производить подсчет или отбор трансформантов, при этом присутствие последовательности приводит к образованию поддающегося измерению продукта и продукт может образовываться без разрушения растительной клетки. Примеры включают ген β-глюкуронидазы, или uidA (GUS), кодирующий фермент, для которого известны различные хромогенные субстраты (например, патенты США №№5268463 и 5599670), хлорамфеникол-ацетил-трансферазы (Jefferson et al. The EMBO Journal vol. 6 No. 13 pp. 3901-3907) и щелочной фосфатазы. В предпочтительном варианте осуществления используемый маркер представляет собой бета-каротин или провитамин A (Ye et al., Science 287: 303-305 (2000)). Этот ген был использован для повышения питательности риса, но в данном случае он, вместо этого, используется в качестве скринируемого маркера, и присутствие гена, связанного с интересующим геном, определяют по возникающей золотистой окраске. В отличие от ситуации, когда ген используют для повышения питательной ценности растения, для целей маркировки достаточно меньшего количества белка. Другие скринируемые маркеры в основном включают гены антоцианов/флавоноидов (смотри обсуждение в статье Taylor and Briggs, The Plant Cell (1990)2: 115-127), в том числе, например, ген R-локуса, кодирующий продукт, который регулирует производство пигментов антоцианов (красного цвета) в тканях растений (Dellaporta et al., in Chromosome Structure and Function, Kluwer Academic Publishers, Appels and Gustafson eds., pp. 263-282 (1988)), гены, контролирующие биосинтез пигментов флавоноидов, такие как ген C1 кукурузы (Kao et al., Plant Cell (1996) 8: 1171-1179, Scheffler et al., Mol. Gen. Genet. (1994) 242: 40-48) и C2 кукурузы (Wienand et al., Mol. Gen. Genet. (1986) 203: 202-207), ген B (Chandler et al., Plant Cell (1989) 1: 1175-1183), ген p1 (Grotewold et al., Proc. Natl. Acad. Sci USA (1991) 88: 4587-4591, Grotewold et al., Cell (1994) 76: 543-553, Sidorenko et al., Plant Mol. Biol. (1999)39: 11-19), ген локуса bronze (Ralston et al., Genetics (1988) 119: 185-197, Nash et al., Plant Cell (1990) 2(11): 1039-1049), среди прочих.
Дополнительные примеры подходящих маркеров включают ген голубого флуоресцентного белка (CYP) (Bolte et al., (2004) J. Cell Science 117: 943-54 и Kato et al., (2002) Plant Physiol 129: 913-42), ген желтого флуоресцентного белка (PHIYFP™ от компании Evrogen, смотри Bolte et al., (2004) J. Cell Science 117: 943-54), ген lux, кодирующий люциферазу, присутствие которого можно обнаруживать с использованием, например, рентгеновской пленки, сцинтилляционного измерения, флуоресцентной спектрофотометрии, низкоуровневых видеокамер, камер с устройством подсчета фотонов или микропланшетного люминометра (Teeri et al. (1989) EMBO J. 8: 343), ген зеленого флуоресцентного белка (GFP) (Sheen et al., Plant J. (1995) 8(5): 777-84) и ген DsRed2, когда растительные клетки, трансформированные маркерным геном, имеют красный цвет и, таким образом, могут быть обнаружены визуально (Dietrich et al., (2002) Biotechniques 2(2): 286-293). Дополнительные примеры включают ген β-лактамазы (Sutcliffe, Proc. Natl. Acad. Sci. U.S.A. (1978) 75: 3737), кодирующий фермент, для которого известны различные хромогенные субстраты (например, PADAC, хромогенный цефалоспорин), ген xylE (Zukowsky et al., Proc. Natl. Acad. Sci. U.S.A. (1983) 80: 1101), кодирующий катехол-диоксигеназу, которая может превращать хромогенные катехолы, ген α-амилазы (Ikuta et al., Biotech. (1990) 8: 241) и ген тирозиназы (Katz et al., J. Gen. Microbiol. (1983) 129: 2703), кодирующий фермент, способный окислять тирозин до ДОФА и допахинона, который в свою очередь конденсируется, с образованием легко обнаруживаемого соединения меланина. Очевидно, что многие из таких маркеров доступны и известны специалисту в данной области.
В некоторых вариантах осуществления нуклеотидная последовательность необязательно может быть объединена с другой интересующей нуклеотидной последовательностью. Термин «интересующая нуклеотидная последовательность» относится к молекуле нуклеиновой кислоты (которую также можно называть полинуклеотидом), которая может представлять собой транскрибированную молекулу РНК, а также молекулу ДНК, кодирующую желаемый полипептид или белок, но также может относиться к молекулам нуклеиновой кислоты, которые не представляют собой полный ген и которые необязательно кодируют полипептид или белок (например, промотор). Например, в некоторых вариантах осуществления молекула нуклеиновой кислоты может быть объединена или «пакетирована» с другой молекулой, которая обеспечивает дополнительную устойчивость или толерантность к глифосату или другому гербициду, и/или обеспечивает устойчивость к определенным насекомым или заболеваниям, и/или улучшение питательных свойств, и/или улучшенные агрономические характеристики, и/или белки или другие продукты, полезные для кормов, продуктов питания, имеющие промышленное, фармацевтическое или другое применение. «Пакетирование» двух или более интересующих нуклеотидных последовательностей в растительном геноме можно осуществлять, например, путем общепринятой селекции растений с использованием двух или более объектов, трансформации растения конструктом, который содержит интересующие последовательности, повторной трансформации трансгенного растения или добавления новых признаков за счет направленной интеграции через гомологичную рекомбинацию.
Такие интересующие нуклеотидные последовательности включают, но не ограничиваются ими, примеры, приведенные ниже:
1. Гены или кодирующие последовательности (например, иРНК), придающие устойчивость к вредителям или заболеваниям
(A) Гены устойчивости к заболеваниям растений. Защита растений часто активируется путем специфического взаимодействия между продуктом гена устойчивости к заболеванию (R) в растении и продуктом соответствующего гена авирулентности (Avr) в патогене. Сорт растений можно трансформировать клонированным геном устойчивости для получения растений, устойчивых к определенным штаммам патогена. Примеры таких генов включают ген Cf-9 томата для устойчивости к Cladosporium fulvum (Jones et al., 1994 Science 266: 789), ген Pto томата, кодирующий протеинкиназу, для устойчивости к Pseudomonas syringae pv. tomato (Martin et al., 1993 Science 262: 1432) и ген RSSP2 Arabidopsis для устойчивости к Pseudomonas syringae (Mindrinos et al., 1994 Cell 78: 1089).
(B) Белок Bacillus thuringiensis, его производное или синтетический полипептид, смоделированный на его основе, например, нуклеотидная последовательность гена δ-эндотоксина Bt (Geiser et al., 1986 Gene 48: 109), и растительный инсектицидный (VIP) ген (смотри, например, Estruch et al., (1996) Proc. Natl. Acad. Sci. 93: 5389-94). Кроме того, молекулы ДНК, кодирующие гены δ-эндотоксинов, можно получать из Американской коллекции типовых культур (Rockville, Md.) под регистрационными номерами ATCC 40098, 67136, 31995 и 31998.
(C) Лектин, например, нуклеотидные последовательности некоторых генов лектинов, связывающих маннозу, из Clivia miniata (Van Damme et al., 1994 Plant Molec. Biol. 24: 825).
(D) Связывающий витамин белок, такой как авидин и гомологи авидина, которые полезны в качестве ларвицидов против насекомых-вредителей. Смотри патент США №5659026.
(E) Ингибитор фермента, например, ингибитор протеазы или ингибитор амилазы. Примеры таких генов включают ингибитор цистеиновой протеазы риса (Abe et al., 1987 J. Biol. Chem. 262: 16793), ингибитор I протеазы табака (Huub et al., 1993 Plant Molec. Biol. 21: 985) и ингибитор α-амилазы (Sumitani et al., 1993 Biosci. Biotech. Biochem. 57: 1243).
(F) Специфичный для насекомых гормон или феромон, такой как экдистероид и ювенильный гормон, его вариант, миметик на его основе или его антагонист или агонист, например, экспрессированная в бакуловирусе клонированная эстераза ювенильного гормона, инактиватор ювенильного гормона (Hammock et al., 1990 Nature 344: 458).
(G) Специфичный для насекомых пептид или нейропептид, который при экспрессии нарушает физиологию подвергнутого воздействию вредителя (J. Biol. Chem. 269: 9). Примеры таких генов включают ген рецептора диуретического гормона насекомых (Regan, 1994), аллостатина, обнаруженного в Diploptera punctata (Pratt, 1989), и специфичных для насекомых паралитических нейротоксинов (патент США №5266361).
(H) Специфичный для насекомых яд, в природе вырабатываемый змеями, осами и так далее, такой как токсичный для насекомых пептид скорпиона (Pang, (1992) Gene 116: 165).
(I) Фермент, отвечающий за избыточную аккумуляцию монотерпена, сесквитерпена, стероида, гидроксамовой кислоты, фенилпропаноидного производного или другой небелковой молекулы с инсектицидной активностью.
(J) Фермент, участвующий в модификации, в том числе посттрансляционной модификации, биологически активной молекулы, например, гликолитический фермент, протеолитический фермент, липолитический фермент, нуклеаза, циклаза, трансаминаза, эстераза, гидролаза, фосфатаза, киназа, фосфорилаза, полимераза, эластаза, хитиназа и глюканаза, либо природный, либо синтетический. Примеры таких генов включают ген каллы (опубликованная PCT заявка WO 93/02197), кодирующие хитиназу последовательности (которые доступны, например, из ATCC под регистрационными номерами 3999637 и 67152), ген хитиназы нематоды табака (Kramer et al., (1993) Insect Molec. Biol. 23: 691) и ген полиубиквитина ubi4-2 петрушки (Kawalleck et al., (1993) Plant Molec. Biol. 21: 673).
(K) Молекула, стимулирующая сигнальную трансдукцию. Примеры таких молекул включают нуклеотидные последовательности для клонов кДНК калмодулина маша (Botella et al., (1994) Plant Molec. Biol. 24: 757) и нуклеотидную последовательность клона кДНК калмодулина кукурузы (Griess et al., (1994) Plant Physiol. 104: 1467).
(L) Пептид гидрофобного момента. Смотри патенты США №№5659026 и 5607914, в последнем описаны синтетические противомикробные пептиды, придающие устойчивость к заболеванию.
(M) Мембранная пермеаза, создающая канал или блокирующая канал, такая как аналог литического пептида цекропина-β (Jaynes et al., (1993) Plant Sci. 89: 43), которая придает трансгенным растениям табака устойчивость к Pseudomonas solanacearum.
(N) Вирусный инвазивный белок или комплексный токсин, полученный из него. Например, накопление белков вирусной оболочки в трансформированных клетках растения придает устойчивость к вирусной инфекции и/или развитию заболевания, вызванного вирусом, из которого был получен ген белка оболочки, а также родственными вирусами. Опосредованная белком оболочки устойчивость придается трансформированным растениям в отношении вируса мозаики люцерны, вируса мозаики огурца, вируса полосатости табака, вируса X картофеля, вируса Y картофеля, вируса гравировки табака, вируса погремковости табака и вируса табачной мозаики. Смотри, например, Beachy et al., (1990) Ann. Rev. Phytopathol. 28: 451.
(O) Специфичное для насекомых антитело или полученный на его основе иммунотоксин. Таким образом, антитело, нацеленное на критическую метаболическую функцию в кишечнике насекомых, будет инактивировать подвергнутый воздействию фермент, уничтожая насекомое. Например, в работе Taylor et al., (1994) Abstract №497, Seventh Int'l. Symposium on Molecular Plant-Microbe Interactions продемонстрирована инактивация фермента в трансгенном растении табака в результате продукции одноцепочечных фрагментов антитела.
(P) Специфическое для вируса антитело. Смотри, например, Tavladoraki et al., (1993) Nature 266: 469, где описано, что трансгенные растения, экспрессирующие гены рекомбинантного антитела, защищены от атаки втруса.
(Q) Останавливающий развитие белок, в природе продуцируемый патогеном или паразитом. Так, грибковые эндо-α-1,4-D-полигалактуроназы способствуют колонизации грибков и высвобождению питательных веществ из растения за счет солюбилизации клеточной стенки растения гомо-α-1,4-D-галактуроназой (Lamb et al., (1992) Bio/Technology 10: 1436). Клонирование и характеристика гена, кодирующего ингибирующий эндополигалактуроназу белок из фасоли, описаны в статье Toubart et al., (1992) Plant J. 2: 367.
(R) Останавливающий развитие белок, в природе продуцируемый растениями, например, ген инактивирующего рибосому белка ячменя, который обеспечивает повышенную устойчивость к грибковому заболеванию (Longemann et al., (1992). Bio/Technology 10: 3305).
(S) РНК-интерференция, при которой полинуклеотид ДНК, кодирующий молекулу РНК, используют для ингибирования экспрессии гена-мишени. Молекула РНК в одном примере является частично или полностью двухцепочечной, что запускает реакцию сайленсинга, приводящую к расщеплению дцРНК на короткие интерферирующие РНК, которые затем входят в направляемый комплекс, который разрушает гомологичные мРНК. Смотри, например, Fire et al., патент США №6506559, Graham et al., патент США №6573099.
2. Гены, придающие устойчивость к гербицидам
(A) Гены, кодирующие признаки устойчивости или толерантности к гербициду, подавляющему точку роста или меристему, такому как гербицид имидазолинон, сульфонанилид или сульфонилмочевина. Иллюстративные гены в этой категории кодируют мутантный фермент ALS (Lee et al., (1988) EMBO J. 7: 1241), также известный как фермент AHAS (Miki et al., (1990) Theor. Appl. Genet. 80: 449).
(B) Один или более дополнительных генов, кодирующих признак устойчивости или толерантности к глифосату, придаваемой мутантными генами EPSP-синтазы и aroA, или путем метаболической инактивации за счет таких генов как GAT (глифосат ацетилтрансфераза) или GOX (глифосат оксидаза), и другим фосфоновым соединениям, таким как глюфозинат (гены pat и bar, DSM-2), а также арилоксифеноксипропионовым кислотам и циклогександионам (гены, кодирующие ингибитор ACCазы). Смотри, например, патент США №4940835, в котором раскрыта нуклеотидная последовательность формы EPSP, придающей устойчивость к глифосату. Молекула ДНК, кодирующая мутантный ген aroA, доступна в ATCC под регистрационным номером 39256, и нуклеотидная последовательность мутантного гена раскрыта в патенте США №4769061. В европейской патентной заявке №0333033 и патенте США №4975374 описаны нуклеотидные последовательности генов глутамин-синтетазы, которые придают устойчивость к таким гербицидам, как L-фосфинотрицин. Нуклеотидная последовательность гена фосфинотрицин-ацетил-трансферазы приведена в европейской патентной заявке №0242246. В статье De Greef et al., (1989) Bio/Technology 7: 61 описано получение трансгенных растений, экспрессирующих химерные гены bar, кодирующие фосфинотрицин-ацетил-трансферазную активность. Примерами генов, придающих устойчивость к арилоксифеноксипропионовым кислотам и циклогександионам, таким как сетоксидим и галоксифоп, являются гены Accl-S1, Accl-S2 и Accl-S3, описанные в статье Marshall et al., (1992) Theor. Appl. Genet. 83: 435.
(C) Гены, кодирующие устойчивость или толерантность к гербициду, который ингибирует фотосинтез, такому как триазин (гены psbA и gs+) и бензонитрил (ген нитрилазы). В статье Przibilla et al., (1991) Plant Cell 3: 169 описано использование плазмид, кодирующих мутантные гены psbA, для трансформации Chlamydomonas. Нуклеотидные последовательности для генов нитрилазы описаны в патенте США №4810648, и молекулы ДНК, содержащие эти гены, доступны в ATCC под регистрационными номерами 53435, 67441 и 67442. Клонирование и экспрессия ДНК, кодирующей глутатион-S-трансферазу, описаны в статье Hayes et al., (1992) Biochem. J. 285: 173.
(D) Гены, кодирующие устойчивость или толерантность к гербициду, который связывается с гидроксифенилпируват диоксигеназами (HPPD), ферментами, катализирующими реакцию, в которой пара-гидроксифенилпируват (HPP) превращается в гомогентизат. Сюда относятся такие гербициды, как изоксазолы (европейский патент №418175, европейский патент №470856, европейский патент №487352, европейский патент №527036, европейский патент №560482, европейский патент №682659, патент США №5424276), в частности, изоксафлутол, который является избирательным гербицидом для кукурузы, дикетонитрилы (европейский патент №496630 и европейский патент №496631), в частности, 2-циано-3-циклопропил-1-(2-SO2CH3-4-CF3фенил)пропан-1,3-дион и 2-циано-3-циклопропил-1-(2-SO2CH3-4-2,3Cl2фенил)пропан-1,3-дион, трикетоны (европейский патент №625505, европейский патент №625508, патент США №5506195), в частности, сулкотрион, и пиразолинаты. Ген, который производит избыток HPPD в растениях, может обеспечивать толерантность или устойчивость к таким гербицидам, включая, например, гены, описанные в патентах США №№6268549 и 6245968 и публикации патентной заявки США №20030066102.
(E) Гены, кодирующие признак устойчивости или толерантности к фенокси ауксиновым гербицидам, таким как 2,4-дихлорфеноксиуксусная кислота (2,4-D), и которые также могут придавать устойчивость или толерантность к арилоксифеноксипропионатным (AOPP) гербицидам. Примеры таких генов включают ген фермента α-кетоглутарат-зависимой диоксигеназы (aad-1), описанный в патенте США №7838733.
(F) Гены, кодирующие признак устойчивости или толерантности к фенокси ауксиновым гербицидам, таким как 2,4-дихлорфеноксиуксусная кислота (2,4-D), и которые также могут придавать устойчивость или толерантность к пиридилоксиауксиновым гербицидам, таким как флуроксипир или триклопир. Примеры таких генов включают ген фермента α-кетоглутарат-зависимой диоксигеназы (aad-12), описанный в WO 2007/053482 A2.
(G) Гены, кодирующие признак устойчивости или толерантности к дикамбе (смотри, например, патентную публикацию США №20030135879).
(H) Гены, кодирующие признак устойчивости или толерантности к гербицидам, которые ингибируют протопорфириноген оксидазу (PPO) (смотри патент США №5767373).
(I) Гены, обеспечивающие устойчивость или толерантность к триазиновым гербицидам (например, атразину) и гербицидам на основе производных мочевины (например, диурону), которые связываются с сердцевинными белками реакционных центров фотосистемы II (PS II) (смотри Brussian et al., (1989) EMBO J. 1989, 8(4): 1237-1245.
3. Гены, которые придают или вносят вклад в добавляющий ценность признак:
(A) модифицированный метаболизм жирных кислот, например, путем трансформации кукурузы или Brassica антисмысловым геном стеарил-ACP-десатуразы для увеличения содержания стеариновой кислоты в растении (Knultzon et al., (1992) Proc. Nat. Acad. Sci. USA 89: 2624.
(B) сниженное содержание фитатов
(1) введение кодирующего фитазу гена, такого как ген фитазы из Aspergillus niger (Van Hartingsveldt et al., (1993) Gene 127: 87), приводит к повышенному разрушению фитатов, добавляя больше свободного фосфата для трансформированного растения.
(2) можно вводить ген для снижения содержания фитатов. В кукурузе, например, это можно осуществлять путем клонирования и затем повторного введения ДНК, ассоциированной с одним аллелем, который является причиной появления мутантов кукурузы, характеризующихся низкими уровнями фитиновой кислоты (Raboy et al., (1990) Maydica 35: 383).
(C) модифицированный углеводный состав, получаемый, например, путем трансформации растений геном, кодирующим фермент, который изменяет характер ветвления крахмала. Примеры генов таких ферментов включают ген фруктозилтрансферазы Streptococcus mucus (Shiroza et al., (1988) J. Bacteriol. 170: 810), ген левансахаразы Bacillus subtilis (Steinmetz et al., (1985) Mol. Gen. Genel. 200: 220), ген α-амилазы Bacillus licheniformis (Pen et al., (1992) Bio/Technology 10: 292), гены инвертазы томатов (Elliot et al., (1993), ген амилазы ячменя (Sogaard et al., (1993) J. Biol. Chem. 268: 22480) и ген фермента ветвления крахмала II эндосперма кукурузы (Fisher et al., (1993) Plant Physiol. 102: 10450).
В настоящем документе описаны способы определения присутствия донорского полинуклеотида ДНК, вставленного в целевые геномные локусы. В качестве дополнительного варианта осуществления можно использовать сайт-специфическую нуклеазу для расщепления не модифицированного эндогенного геномного локуса растения, ранее таргетированного геномного локуса растения или ранее вставленной экзогенной ДНК. Таргетирование эндогенных геномных локусов является одним из вариантов осуществления изобретения.
В вариантах осуществления в способах и композициях, описанных в настоящем документе, используют сайт-специфическую нуклеазу, которая включает сконструированную (не существующую в природе) мегануклеазу (также называемую хоминг-эндонуклеазой). Последовательности узнавания хоминг-эндонуклеаз или мегануклеаз, таких как I-SceI, I-CeuI, PI-PspI, PI-Sce, I-SceIV, I-CsmI, I-PanI, I-SceII, I-PpoI, I-SceIII, I-CreI, I-TevI, I-TevII и I-TevIII, известны. Смотри также патент США №5420032, патент США №6833252, Belfort et al. (1997) Nucleic Acids Res. 25: 3379-30 3388, Dujon et al. (1989) Gene 82: 115-118, Perler et al. (1994) Nucleic Acids Res. 22, 11127, Jasin (1996) Trends Genet. 12: 224-228, Gimble et al. (1996) J. Mol. Biol. 263: 163-180, Argast et al. (1998) J. Mol. Biol. 280: 345-353 и каталог New England Biolabs. Кроме того, можно разрабатывать ДНК-связывающую специфичность хоминг-эндонуклеаз и мегануклеаз для связывания неприродных сайтов-мишеней. Смотри, например, Chevalier et al. (2002) Molec. Cell 10: 895-905, Epinat et al. (2003) Nucleic Acids Res. 5 31: 2952-2962, Ashworth et al. (2006) Nature 441: 656-659, Paques et al. (2007) Current Gene Therapy 7: 49-66, патентную публикацию США №20070117128. ДНК-связывающие домены хоминг-эндонуклеаз и мегануклеаз можно изменять в контексте целой нуклеазы (то есть, так, что нуклеаза содержит родственный расщепляющий домен) или можно производить их слияние с гетерологичным расщепляющим доменом.
В других вариантах осуществления ДНК-связывающий домен одной или более из нуклеаз, используемых в способах и композициях, описанных в настоящем документе, включает природный или сконструированный (не существующий в природе) ДНК-связывающий домен TAL эффектора. Смотри, например, патентную публикацию США №20110301073, полное содержание которой включено в настоящий документ посредством ссылки. Патогенные для растений бактерии рода Xanthomonas, как известно, вызывают множество заболеваний важных сельскохозяйственных культур. Патогенность Xanthomonas зависит от консервативной системы секреции III типа (T3S), которая инъецирует несколько различных эффекторных белков в растительную клетку. Среди этих инъецированных белков находятся подобные активаторам транскрипции (TALEN) эффекторы, которые имитируют активаторы транскрипции растений и управляют транскриптомом растения (смотри Kay et al. (2007) Science 318: 648-651). Эти белки содержат ДНК-связывающий домен и домен активации транскрипции. Одним из наиболее хорошо охарактеризованных TAL-эффекторов является AvrBs3 из Xanthomonas campestgris pv. Vesicatoria (смотри Bonas et al. (1989) Mol Gen Genet 218: 127-136 и WO 2010079430). TAL-эффекторы содержат централизованный домен тандемных повторов, при этом каждый повтор содержит примерно 34 аминокислоты, которые являются ключевыми для специфичности ДНК-связывания данных белков. Кроме того, они содержат последовательность с ядерной локализацией и кислый домен активации транскрипции (для обзора смотри Schornack S, et al. (2006) J Plant Physiol 163(3): 256-272). Кроме того, в фитопатогенных бактериях Ralstonia solanacearum обнаружены два гена, обозначенные brg11 и hpx17, которые гомологичны семейству AvrBs3 из Xanthomonas, в R. solanacearum биоваре 1 штамме GMI1000 и в биоваре 4 штамме RS1000 (смотри Heuer et al. (2007) Appl and Envir Micro 73(13): 4379-4384). Эти гены на 98,9% идентичны друг другу по нуклеотидной последовательности, но отличаются делецией 1,575 п.н. в домене повтора hpx17. Однако оба генных продукта имеют менее 40% идентичности последовательности с белками семейства AvrBs3 из Xanthomonas. Смотри, например, патентную публикацию США №20110301073, полное содержание которой включено посредством ссылки.
Специфичность этих TAL-эффекторов зависит от последовательностей, находящихся в тандемных повторах. Повторяющаяся последовательность содержит примерно 102 п.н. и повторы, как правило, на 91-100% гомологичны друг другу (Bonas et al., там же). Полиморфизм повторов, как правило, имеет место в положениях 12 и 13 и, как представляется, существует точное соответствие между характером гипервариабельных двух остатков в положениях 12 и 13 и характером смежных нуклеотидов в последовательности-мишени TAL-эффектора (смотри Moscou и Bogdanove, (2009) Science 326: 1501 и Boch et al. (2009) Science 326: 1509-1512). Природный код для узнавания ДНК этих TAL-эффекторов был определен экспериментально так, что последовательность HD в положениях 12 и 13 приводит к связыванию с цитозином (C), NG связывается с T, NI с A, C, G или T, NN связывается с A или G и ING связывается с T. Эти ДНК-связывающие повторы были собраны в белки с новыми комбинациями и числом повторов для создания искусственных факторов транскрипции, которые способны взаимодействовать с новыми последовательностями и активировать экспрессию не эндогенного репортерного гена в растительных клетках (Boch et al., там же). Сконструированные TAL-белки были связаны с расщепляющим полудоменом FokI для получения слитого белка TAL эффектора с доменом нуклеазы (TALEN), проявляющего активность в репортерном анализе в дрожжах (мишень на основе плазмиды).
Нуклеазная система CRISPR (кластерные короткие палиндромные повторы, разделенные регулярными промежутками)/Cas (CRISPR-ассоциированный локус) представляет собой недавно разработанную нуклеазную систему на основе бактериальной системы, которую можно использовать для конструирования генома. Она основана на части адаптивного иммунного ответа многих бактерий и Archea. Когда вирус или плазмида проникает в бактерию, сегменты привносимой ДНК преобразуются в РНК CRISPR (crРНК) в результате «иммунного» ответа. Эта crРНК затем связывается через область частичной комплементарности с РНК другого типа, называемой tracrРНК для направления нуклеазы Cas9 к области, гомологичной для crРНК, в ДНК-мишени, называемой «протоспейсер». Cas9 расщепляет ДНК, с образованием тупых концов на ДЦР (DSB) в сайтах, определяемых 20-нуклеотидной направляющей последовательностью, содержащейся в транскрипте crРНК. Cas9 нуждается как в crРНК, так и в tracrРНК для сайт-специфического узнавания и расщепления ДНК. Эта система была сконструирована таким образом, что crРНК и tracrРНК могут быть объединены в одной молекуле («одиночная направляющая РНК»), и эквивалентную crРНК часть одиночной направляющей РНК можно сконструировать для направления нуклеазы Cas9 на любую желаемую последовательность- мишень (смотри Jinek et al. (2012) Science 337, p. 816-821, Jinek et al., (2013), eLife 2: e00471, и David Segal, (2013) eLife 2: e00563). Таким образом, систему CRISPR/Cas можно сконструировать для создания двухцепочечного разрыва (ДЦР) на желаемом сайте-мишени в геноме, и на репарацию ДЦР можно оказывать влияние путем использования ингибиторов репарации с тем, чтобы вызвать увеличение ошибочной репарации.
В некоторых вариантах осуществления белок Cas может представлять собой «функциональное производное» природного белка Cas. «Функциональное производное» полипептида с природной последовательностью представляет собой соединение, имеющее качественное биологическое свойство, общее с полипептидом, имеющим природную последовательность. «Функциональные производные» включают, но не ограничиваются ими, фрагменты природной последовательности и производные полипептида с природной последовательностью и его фрагментов, при условии, что они имеют общую биологическую активность с соответствующим полипептидом, имеющим природную последовательность. Биологическая активность, подразумеваемая в настоящем документе, представляет собой способность функционального производного гидролизовать ДНК-субстрат на фрагменты. Термин «производное» охватывает как варианты аминокислотной последовательности полипептида, ковалентные модификации, так и их слитые продукты. Подходящие производные полипептида Cas или его фрагмента включают, но не ограничиваются ими, мутанты, слитые продукты, ковалентные модификации белка Cas или его фрагмента. Белок Cas, который включает белок Cas или его фрагмент, а также производные белка Cas или его фрагмента, можно получать из клетки или синтезировать химически или с использованием сочетания этих двух способов. Клетка может быть клеткой, которая естественным образом продуцирует белок Cas, или клеткой, которая естественным образом продуцирует белок Cas и модифицирована генно-инженерными методами для продуцирования эндогенного белка Cas на более высоком уровне экспрессии, или для продуцирования белка Cas из экзогенно введенной нуклеиновой кислоты, каковая нуклеиновая кислота кодирует Cas, который является таким же или отличающимся от эндогенного Cas. В некоторых случаях клетка не продуцирует белок Cas естественным образом и является генетически модифицированной для продукции белка Cas. Белок Cas вводится в действие в клетках млекопитающих (и предположительно в клетках растений) за счет совместной экспрессии нуклеазы Cas с направляющей РНК. Можно использовать две формы направляющих РНК для облегчения опосредованного Cas расщепления генома, как описано в статье Le Cong, F., et al., (2013) Science 339(6121): 819-823.
В некоторых вариантах осуществления ДНК-связывающий домен одной или более нуклеаз, используемых для in vivo расщепления и/или направленного расщепления генома клетки, содержит белок с «цинковыми пальцами». В некоторых вариантах осуществления белок с «цинковыми пальцами» не является природным, а сконструирован для связывания с выбранным сайтом-мишенью. Смотри, например, Beerli et al. (2002) Nature Biotechnol. 20: 135-141, Pabo et al. (2001) Ann. Rev. Biochem. 70: 313-340, Isalan et al. (2001) Nature Biotechnol. 19: 656-660, Segal et al. (2001) Curr. Opin. Biotechnol. 12: 632-637, Choo et al. (2000) Curr. Opin. Struct. Biol. 10: 411-416, патенты США №№6453242, 6534261, 6599692, 6503717, 6689558, 7030215, 6794136, 7067317, 7262054, 7070934, 7361635, 7253273 и патентные публикации США №№2005/0064474, 2007/0218528, 2005/0267061, полное содержание которых включено в настоящий документ посредством ссылки.
Сконструированный связывающий домен «цинковый палец» может иметь новую специфичность связывания в сравнении с природным белком с «цинковыми пальцами». Способы конструирования включают, но не ограничиваются ими, рациональное проектирование и различные виды отбора. Рациональное проектирование включает, например, использование баз данных, содержащих триплетные (или квадруплетные) нуклеотидные последовательности и отдельные аминокислотные последовательности «цинковых пальцев», при этом каждая триплетная или квадруплетная нуклеотидная последовательность связана с одной или более аминокислотными последовательностями «цинковых пальцев», которые связывают конкретную триплетную или квадруплетную последовательность. Смотри, например, патенты США №№6453242 и 6534261, включенные в настоящий документ посредством ссылки в полном объеме.
Выбор сайтов-мишеней, ZFP и способы разработки и конструирования слитых белков (и полинуклеотидов, кодирующих их) известны специалистам в данной области и подробно описаны в патентах США №№61400815, 789538, 6453242, 6534261, 5925523, 6007988, 6013453, 6200759, WO 95/19431, WO 96/06166, WO 98/53057, WO 98/54311, WO 00/27878, WO 01/60970, WO 01/88197, WO 02/099084, WO 98/53058, WO 98/53059, WO 98/53060, WO 02/016536 и WO 03/016496.
Кроме того, как раскрыто в данных и других литературных источниках, домены «цинковые пальцы» и/или белки с несколькими «цинковыми пальцами» могут быть связаны вместе при помощи любых подходящих последовательностей линкеров, включая, например, линкеры из 5 или более аминокислот в длину. Смотри также патенты США №№6479626, 6903185 и 7153949 для иллюстративных последовательностей линкеров, имеющих 6 или более аминокислот в длину. Белки, описанные в настоящем документе, могут содержать любое сочетание подходящих линкеров между отдельными «цинковыми пальцами» белка.
Таким образом, сайт-специфическая нуклеаза содержит ДНК-связывающий домен, который специфически связывается с сайтом-мишенью в любом гене, в который желательно вставить донорский полинуклеотид ДНК (то есть, содержащий по меньшей мере один трансген).
Любой подходящий расщепляющий домен можно функционально связывать с ДНК-связывающим доменом, получая нуклеазный слитый белок. Например, ДНК-связывающие домены ZFP были слиты с доменами нуклеазы, с получением ZFN - функционального элемента, способного узнавать предназначенную для него нуклеиновую кислоту-мишень за счет его сконструированного (ZFP) ДНК-связывающего домена и вызывать разрезание ДНК рядом с сайтом связывания ZFP за счет нуклеазной активности. Смотри, например, Kim et al. (1996) Proc Natl Acad Sci USA 93(3): 1156-1160. Совсем недавно ZFN были использованы для модификации генома в различных организмах. Смотри, например, патентные публикации США 20030232410, 20050208489, 20050026157, 20050064474, 20060188987, 20060063231 и международную публикацию WO 07/014275. Аналогично, ДНК-связывающие домены TALEN были слиты с доменами нуклеазы для получения TALEN. Смотри, например, патентную публикацию США №20110301073.
Как отмечалось выше, расщепляющий домен может быть гетерологичным для ДНК-связывающего домена, например, ДНК-связывающий домен «цинковый палец» и расщепляющий домен из другой нуклеазы или ДНК-связывающий домен TALEN и расщепляющий домен из другой нуклеазы, или ДНК-связывающий домен мегануклеазы и расщепляющий домен из другой нуклеазы. Гетерологичные расщепляющие домены можно получать из любой эндонуклеазы или экзонуклеазы. Иллюстративные эндонуклеазы, из которых расщепляющий домен может быть получен, включают, но не ограничиваются ими, эндонуклеазы рестрикции и хоминг-эндонуклеазы. Смотри, например, 2002-2003 Catalogue, New England Biolabs, Beverly, MA, и Belfort et al. (1997) Nucleic Acids Res. 25: 3379-3388. Известны дополнительные ферменты, которые расщепляют ДНК (например, нуклеаза S1, нуклеаза золотистой фасоли, панкреатическая ДНКаза I, микрококковая нуклеаза, дрожжевая HO эндонуклеаза, смотри также Linn et al. (eds.) Nucleases, Cold Spring Harbor Laboratory Press, 1993). Один или более из этих ферментов (или их функциональных фрагментов) можно использовать в качестве источника расщепляющих доменов и расщепляющих полудоменов.
Аналогично, расщепляющий полудомен можно получать из любой нуклеазы или ее части, как указано выше, которой требуется димеризация для расщепляющей активности. Как правило, для расщепления необходимы два слитых белка, если слитые белки содержат расщепляющие полудомены. Альтернативно, можно использовать один белок, содержащий два расщепляющих полудомена. Два расщепляющих полудомена можно получать из одной и той же эндонуклеазы (или ее функциональных фрагментов) или каждый расщепляющий полудомен можно получать из отдельной эндонуклеазы (или ее функциональных фрагментов). Кроме того, сайты-мишени для двух слитых белков предпочтительно расположены по отношению друг к другу таким образом, что связывание двух слитых белков с их соответствующими сайтами-мишенями приводит к размещению расщепляющих полудоменов в такой пространственной ориентации по отношению друг к другу, которая позволяет расщепляющим полудоменам образовывать функциональный расщепляющий домен, например, в результате димеризации. Таким образом, в некоторых вариантах осуществления ближние края сайтов-мишеней разделены 5-8 нуклеотидами или 15-18 нуклеотидами. Однако любое целое число нуклеотидов или пар нуклеотидов может находиться между двумя сайтами-мишенями (например, от 2 до 50 пар нуклеотидов или более). Как правило, сайт расщепления лежит между сайтами-мишенями.
Эндонуклеазы рестрикции (ферменты рестрикции) присутствуют во многих видах и способны к специфичному для последовательности связыванию с ДНК (в сайте узнавания) и расщеплению ДНК в сайте связывания или рядом с ним. Некоторые ферменты рестрикции (например, типа IIS) расщепляют ДНК в сайтах, удаленных от сайта узнавания, и имеют разделяемые связывающие и расщепляющие домены. Например, фермент FokI типа IIS катализирует двухцепочечное расщепление ДНК через 9 нуклеотидов от его сайта узнавания на одной цепи и через 13 нуклеотидов от его сайта узнавания на другой. Смотри, например, патенты США №№5356802, 5436150 и 5487994, а также Li et al. (1992) Proc. Natl. Acad. Sci. USA 89: 4275-4279, Li et al. (1993) Proc. Natl. Acad. Sci. USA 90: 2764-2768, Kim et al. (1994a) Proc. Natl. Acad. Sci. USA 91: 883-887, Kim et al. (1994b) J. Biol. Chem. 269: 31978-31982. Таким образом, в одном варианте осуществления слитые белки содержат расщепляющий домен (или расщепляющий полудомен) из по меньшей мере одного фермента рестрикции типа IIS и один или более связывающих доменов «цинковых пальцев», которые могут быть или не быть сконструированными.
Иллюстративным ферментом рестрикции типа IIS, расщепляющий домен которого отделим от связывающего домена, является FokI. Этот конкретный фермент активен в форме димера. Bitinaite et al. (1998) Proc. Natl. Acad. Sci. USA 95: 10570-10575. Соответственно, для целей настоящего изобретения часть фермента FokI, используемую в описанных слитых белках, считают расщепляющим полудоменом. Таким образом, для направленного двухцепочечного расщепления и/или направленной замены клеточных последовательностей с использованием слитых белков «цинковый палец»-FokI, два слитых белка, каждый из которых содержит расщепляющий полудомен FokI, можно использовать для восстановления каталитически активного расщепляющего домена. Альтернативно, также можно использовать одну полипептидную молекулу, содержащую связывающий домен «цинковый палец» и два расщепляющих полудомена FokI. Параметры для направленного расщепления и направленного изменения последовательности с использованием слитых белков «цинковый палец»-FokI приведены в другом месте данного описания.
Расщепляющий домен или расщепляющий полудомен может представлять собой любую часть белка, сохраняющую расщепляющую активность или сохраняющую способность к мультимеризации (например, димеризации), с образованием функционального расщепляющего домена.
Иллюстративные ферменты рестрикции типа IIS описаны в публикации международной патентной заявки WO 07/014275, полное содержание которой включено в настоящий документ посредством ссылки. Дополнительные ферменты рестрикции также содержат разделяемые связывающие и расщепляющие домены, и они предусмотрены по настоящему изобретению. Смотри, например, Roberts et al. (2003) Nucleic Acids Res. 31: 418-420.
В некоторых вариантах осуществления расщепляющий домен содержит один или более сконструированных расщепляющих полудоменов (также называемых димеризующимися мутантными доменами), которые сводят к минимуму или предотвращают гомодимеризацию, как описано, например, в патентных публикациях США №№20050064474, 20060188987, 20070305346 и 20080131962, полное содержание всех из которых включено в настоящий документ посредством ссылки. Аминокислотные остатки в положениях 446, 447, 479, 483, 484, 486, 487, 490, 491, 496, 498, 499, 500, 531, 534, 537 и 538 в FokI все являются мишенями, влияющими на димеризацию расщепляющих полудоменов FokI.
Иллюстративные сконструированные расщепляющие полудомены FokI, которые образуют облигатные гетеродимеры, включают пару, в которой первый расщепляющий полудомен содержит мутации аминокислотных остатков в положениях 490 и 538 в FokI и второй расщепляющий полудомен содержит мутации аминокислотных остатков 486 и 499.
Таким образом, в одном варианте осуществления мутация в положении 490 заменяет Glu (E) на Lys (K), мутация в положении 538 заменяет Iso (I) на Lys (K), мутация в положении 486 заменяет Gln (Q) на Glu (E) и мутация в положении 499 заменяет Iso (I) на Lys (K). Конкретно, сконструированные расщепляющие полудомены, описанные в настоящем документе, были получены в результате мутаций в положениях 490 (E→K) и 538 (I→K) в одном расщепляющем полудомене, с получением сконструированного расщепляющего полудомена, обозначенного «E490K:I538K», и в результате мутаций в положениях 486 (Q→E) и 499 (I→L) в другом расщепляющем полудомене, с получением сконструированного расщепляющего полудомена, обозначенного «Q486E:I499L». Сконструированные расщепляющие полудомены, описанные в настоящем документе, являются облигатными мутантными гетеродимерами, для которых аберрантное расщепление сведено к минимуму или устранено. Смотри, например, патентную публикацию США №2008/0131962, содержание которой включено в настоящий документ посредством ссылки в полном объеме для всех целей. В некоторых вариантах осуществления сконструированный расщепляющий полудомен содержит мутации в положениях 486, 499 и 496 (нумерация соответствует FokI дикого типа), например, мутации, которые заменяют остаток Gln (Q) дикого типа в положении 486 на остаток Glu (E), остаток Iso (I) дикого типа в положении 499 на остаток Leu (L) и остаток Asn (N) дикого типа в положении 496 на остаток Asp (D) или Glu (E) (в так называемых доменах «ELD» и «ELE», соответственно). В других вариантах осуществления сконструированный расщепляющий полудомен содержит мутации в положениях 490, 538 и 537 (нумерация соответствует FokI дикого типа), например, мутации, которые заменяют остаток Glu (E) дикого типа в положении 490 на остаток Lys (K), остаток Iso (I) дикого типа в положении 538 на остаток Lys (K) и остаток His (H) дикого типа в положении 537 на остаток Lys (K) или остаток Arg (R) (в так называемых доменах «KKK» и «KKR», соответственно). В других вариантах осуществления сконструированный расщепляющий полудомен содержит мутации в положениях 490 и 537 (нумерация соответствует FokI дикого типа), например, мутации, которые заменяют остаток Glu (E) дикого типа в положении 490 на остаток Lys (K) и остаток His (H) дикого типа в положении 537 на остаток Lys (K) или остаток Arg (R) (в так называемых доменах «KIK» и «KIR», соответственно). (Смотри патентную публикацию США №20110201055). В других вариантах осуществления сконструированный расщепляющий полудомен содержит «Sharkey» и/или мутации «Sharkey» (смотри Guo et al., (2010) J. Mol. Biol. 400(1): 96-107).
Сконструированные расщепляющие полудомены, описанные в настоящем документе, можно получать с использованием любого подходящего метода, например, путем сайт-направленного мутагенеза расщепляющих полудоменов (FokI) дикого типа, как описано в патентных публикациях США №№20050064474, 20080131962 и 20110201055.
Альтернативно, нуклеазы могут быть собраны in vivo в целевом сайте нуклеиновой кислоты с использованием так называемой технологии «разделенных ферментов» (смотри, например, патентную публикацию США №20090068164). Компоненты таких разделенных ферментов могут экспрессироваться либо на отдельных экспрессионных конструктах, либо могут быть связаны в одной открытой рамке считывания, в которой отдельные компоненты разделены, например, последовательностью саморасщепляющегося пептида 2A или IRES. Компоненты могут представлять собой отдельные связывающие домены «цинковые пальцы» или домены связывающего нуклеиновую кислоту домена мегануклеазы.
Можно проводить скрининг нуклеаз на активность перед использованием, например, в системе на основе хромосом дрожжей, как описано в WO 2009/042163 и 20090068164. Экспрессионные конструкты нуклеаз могут быть легко разработаны с использованием способов, известных в данной области. Смотри, например, патентные публикации США 20030232410, 20050208489, 20050026157, 20050064474, 20060188987, 20060063231 и международную публикацию WO 07/014275. Экспрессия нуклеазы может находиться под контролем конститутивного промотора или индуцируемого промотора.
«Мишень» или «сайт-мишень» или «целевой геномный локус» означает нуклеотидную последовательность, которая представляет собой часть нуклеиновой кислоты, с которой связывающая молекула (например, сайт-специфическая нуклеаза) будет связываться, при условии наличия подходящих для связывания условий.
В одном из вариантов осуществления последовательность геномного локуса включает последовательности, которые присутствуют в хромосомах, эписомах, геномах органелл (например, митохондрий, хлоропластов), искусственных хромосомах и нуклеиновых кислотах любого другого типа, присутствующих в клетке, такие как, например, амплифицированные последовательности, двойные микрохромосомы и геномы эндогенных или инфицирующих бактерий и вирусов. Последовательности геномных локусов могут быть нормальными (то есть, дикого типа) или мутантными; мутантные последовательности могут содержать, например, вставки (например, ранее вставленные экзогенные полинуклеотиды), делеции, транслокации, перестановки и/или точечные мутации. Последовательность геномного локуса может также содержать один из нескольких различных аллелей.
В настоящем документе в качестве варианта осуществления изобретения также описаны способы вставки последовательности донорского полинуклеотида ДНК в геномные локусы. Сообщаемая и наблюдаемая частота направленной модификации генома свидетельствует о том, что таргетинг геномных локусов в растениях является относительно неэффективным. Успешность таких способов невелика отчасти из-за слабой эффективности гомологичной рекомбинации и высокой частоты неспецифических вставок донорской ДНК в области генома, отличные от сайта-мишени. Настоящее изобретение относится к способам определения донорского полинуклеотида ДНК в целевых геномных локусах.
Способы по настоящему изобретению включают получение и использование сайт-специфических нуклеаз (например, сконструированных связывающих доменов «цинковые пальцы», слитых с расщепляющими доменами) для создания одного или более направленных двухцепочечных разрывов в клеточной ДНК. Поскольку двухцепочечные разрывы в клеточной ДНК стимулируют клеточные репарационные механизмы в несколько тысяч раз больше в непосредственной близости от сайта расщепления, такое направленное расщепление позволяет проводить изменение или замену (путем управляемой гомологией репарации) последовательностей практически в любом месте в геноме.
В дополнение к слитым молекулам, описанным в настоящем документе, для направленной замены выбранной геномной последовательности также необходимо введение последовательности заменяющего или донорского полинуклеотида ДНК. Последовательность донорского полинуклеотида ДНК можно вводить в клетку до, одновременно или после экспрессии слитого белка(ов). Донорский полинуклеотид ДНК имеет достаточную степень гомологии с геномной последовательностью для поддержания гомологичной рекомбинации (или управляемой гомологией репарации) между ним и геномной последовательностью, с которой он имеет гомологию. Примерно 25, 50, 100, 200, 500, 750, 1000, 1500, 2000 или более нуклеотидов гомологии последовательностей между донорским полинуклеотидом ДНК и геномным локусом (или любое целое число от 10 до 2000 нуклеотидов, или более) будут поддерживать гомологичную рекомбинацию между ними. Последовательности донорского полинуклеотида ДНК могут иметь диапазон длин от 10 до 5000 нуклеотидов (или любое целое число нуклеотидов между этими значениями) или более. Очевидно, что последовательность донорского полинуклеотида ДНК, как правило, не идентична геномной последовательности, которую она заменяет. Например, последовательность донорского полинуклеотида ДНК может содержать одно или более одиночных изменений оснований, вставок, делеций, инверсий или перестроек относительно геномной последовательности, до тех пор, пока сохраняется достаточная степень гомологии с хромосомными последовательностями. Альтернативно, последовательность донорского полинуклеотида ДНК может содержать негомологичную последовательность, фланкированную двумя областями гомологии. Кроме того, последовательности донорского полинуклеотида ДНК могут содержать молекулу вектора, содержащую последовательности, которые не гомологичны интересующей области в клеточном хроматине. Как правило, гомологичная область(и) последовательности донорского полинуклеотида ДНК будет иметь по меньшей мере 50% идентичности последовательности с геномным локусом, с которым желательна рекомбинация. В некоторых вариантах осуществления имеет место 60%, 70%, 80%, 90%, 95%, 98%, 99% или 99,9% идентичности последовательности. Может иметь место любая степень от 1% до 100% идентичности последовательности, в зависимости от длины донорского полинуклеотида ДНК.
Молекула донорского полинуклеотида ДНК может содержать несколько прерывистых областей гомологии с клеточным хроматином. Например, для направленной вставки последовательностей, обычно не присутствующих в интересующей области, указанные последовательности могут присутствовать в молекуле донорского полинуклеотида ДНК и быть фланкированы областями гомологии с последовательностью в интересующей области.
Донорский полинуклеотид может представлять собой ДНК или РНК, одноцепочечную или двухцепочечную, и может быть введен в клетку в линейной или кольцевой форме. В случае введения в линейной форме, концы донорской последовательности могут быть защищены (например, от экзонуклеолитической деградации) методами, известными специалистам в данной области. Например, один или более дидезоксинуклеотидных остатков добавляют к 3'-концу линейной молекулы и/или самокомплементарные олигонуклеотиды лигируют с одной или обеих сторон. Смотри, например, Chang et al., (1987) Proc. Natl Acad. Sd. USA 84: 4959-4963, Nehls et al., (1996) Science 272: 886-889. Дополнительные способы защиты экзогенных полинуклеотидов от деградации включают, но не ограничиваются ими, добавление концевой аминогруппы(групп) и использование модифицированных межнуклеотидных связей, таких как, например, фосфоротиоаты, фосфорамидаты, а также остатки O-метилрибозы или дезоксирибозы.
Донорский полинуклеотид ДНК можно вводить в клетку как часть молекулы вектора, имеющей дополнительные последовательности, такие как, например, точки начала репликации, промоторы и гены, кодирующие устойчивость к антибиотикам. Кроме того, донорские полинуклеотиды ДНК можно вводить в виде «голой» нуклеиновой кислоты, в виде нуклеиновой кислоты в комплексе с таким средством, как липосома или полоксамер, или можно доставлять с помощью бактерий или вирусов (например, Agrobacterium sp., Rhizobium sp. NGR234, Sinorhizoboium meliloti, Mesorhizobium loti, вируса табачной мозаики, вируса X картофеля, вируса мозаики цветной капусты и вируса мозаики жилок маниоки. Смотри, например, Chung et al. (2006) Trends Plant Sd. 11(1): 1-4).
Без привязки к какой-либо теории, похоже, что присутствие двухцепочечного разрыва в клеточной последовательности, в сочетании с присутствием экзогенной молекулы ДНК, имеющей гомологию с областью, находящейся рядом или окружающей разрыв, активизирует клеточные механизмы, которые устраняют разрыв, перенося содержащую информацию последовательность из донорской молекулы в клеточную (например, геномную или хромосомную) последовательность; то есть, посредством управляемой гомологией репарации, также известной как «конверсия генов». В способах, предложенных авторами настоящей заявки, выгодно объединены мощные направляющие способности сконструированных ZFP с расщепляющим доменом (или расщепляющим полудоменом) для специфического направления двухцепочечного разрыва в область генома, в которую желательна вставка экзогенной последовательности.
Для изменения хромосомной последовательности нет необходимости в том, чтобы вся последовательность донора была скопирована в хромосому, при условии, что скопирована достаточная часть донорской последовательности для осуществления изменения желаемой последовательности.
Эффективность вставки донорских последовательностей путем гомологичной рекомбинации обратно пропорциональна расстоянию в клеточной ДНК между двухцепочечным разрывом и сайтом, в котором желательна рекомбинация. Иными словами, более эффективная гомологичная рекомбинация наблюдается, когда двухцепочечный разрыв расположен ближе к сайту, в котором желательна рекомбинация. В тех случаях, когда точный сайт рекомбинации заранее не определен (например, желаемое событие рекомбинации может происходить на некотором протяжении геномной последовательности), длину и последовательность донорской нуклеиновой кислоты, наряду с сайтом(ами) расщепления, выбирают для получения желаемого события рекомбинации. В случаях, когда желаемое событие предназначено для изменения последовательности одной пары нуклеотидов в геномной последовательности, клеточный хроматин расщепляют в пределах 10000 нуклеотидов по обе стороны от данной пары нуклеотидов. В некоторых вариантах осуществления расщепление происходит в пределах 1000, 500, 200, 100, 90, 80, 70, 60, 50, 40, 30, 20, 10, 5 или 2 нуклеотидов, или любого целого числа от 2 до 1000 нуклеотидов, по обе стороны от пары нуклеотидов, последовательность которых должна быть изменена.
Как подробно описано выше, сайты связывания для двух слитых белков, каждый из которых содержит связывающий домен «цинковый палец» и расщепляющий полудомен, могут быть расположены на расстоянии 5-8 или 15-18 нуклеотидов, которое измеряют от края каждого сайта связывания до ближайшей точки другого сайта связывания, и расщепление происходит между сайтами связывания. Происходит ли расщепление в одном сайте или в нескольких сайтах между сайтами связывания является несущественным, поскольку расщепляемые геномные последовательности заменяются донорскими последовательностями. Таким образом, для эффективного изменения последовательности одной пары нуклеотидов путем направленной рекомбинации середина области между сайтами связывания находится в пределах 10000 нуклеотидов от этой пары нуклеотидов, предпочтительно в пределах 1000 нуклеотидов или 500 нуклеотидов, или 200 нуклеотидов, или 100 нуклеотидов, или 50 нуклеотидов, или 20 нуклеотидов, или 10 нуклеотидов, или 5 нуклеотидов, или 2 нуклеотидов, или одного нуклеотида, или на интересующей паре нуклеотидов.
В некоторых вариантах осуществления гомологичная хромосома может служить в качестве донорского полинуклеотида ДНК. Таким образом, например, коррекцию мутации в гетерозиготе можно осуществлять, конструируя слитые белки, которые связываются и расщепляют мутантную последовательность на одной хромосоме, но не расщепляют последовательность дикого типа на гомологичной хромосоме. Двухцепочечный разрыв на несущей мутацию хромосоме стимулирует основанный на гомологии процесс «конверсии генов», в котором последовательность дикого типа из гомологичной хромосомы копируется в расщепляемую хромосому, таким образом, восстанавливая две копии последовательности дикого типа.
Также предложены способы и композиции, способные повышать уровни направленной рекомбинации, включая, но не ограничиваясь ими, использование дополнительных слитых белков ZFP-функциональный домен для активации экспрессии генов, вовлеченных в гомологичную рекомбинацию, таких как, например, члены группы RAD52 эпистаза (например, Rad50, Rad51, Rad51B, RadSIC, RadSID, Rad52, Rad54, Rad54B, Mrell, XRCC2, XRCC3), гены, продукты которых взаимодействуют с вышеуказанными продуктами генов (например, BRCA1, BRCA2), и/или гены в комплексе NBS1. Смотри, например, Boyko et al. (2006) Plant Physiology 141: 488-497 и LaFarge et al. (2003) Nucleic Acids Res. 31(4): 1148-1155. Аналогично, слитые белки ZFP-функциональный домен можно использовать в сочетании со способами и композициями, раскрытыми в настоящем документе, для подавления экспрессии генов, вовлеченных в негомологичное соединение концов (например, Ku70/80, XRCC4, поли(ADP рибоза) полимераза, ДНК лигаза 4). Смотри, например, Riha et al. (2002) EMBO 21: 2819-2826, Freisner et al. (2003) Plant J. 34: 427-440, Chen et al. (1994) European Journal of Biochemistry 224: 135-142. Способы активации и подавления экспрессии генов с использованием слитых белков из связывающего домена «цинковый палец» и функционального домена описаны, например, в патентах США 6534261, 6824978 и 6933113 того же заявителя. Дополнительные способы подавления включают использование антисмысловых олигонуклеотидов и/или коротких интерферирующих РНК (киРНК или РНКи), направленных на последовательность гена, который необходимо подавлять.
Генетические манипуляции с рекомбинантным организмом- хозяином, описанные в настоящем документе, можно выполнять с использованием стандартных генетических методов в любой клетке-хозяине, подходящей для генетической манипуляции. В некоторых вариантах осуществления рекомбинантная клетка-хозяин, раскрытая в настоящем документе, может быть любым организмом или микроорганизмом-хозяином, полезным для генетической модификации и рекомбинантной экспрессии гена. В некоторых вариантах осуществления рекомбинантный хозяин может представлять собой, но без ограничения, любое высшее растение, включая как двудольные, так и однодольные растения, и потребляемые человеком растения, в том числе сельскохозяйственные культуры и растения, используемые ради их масел. Таким образом, можно выбирать любой вид растений или растительных клеток, как описано ниже.
В некоторых вариантах осуществления растения, содержащие донорский полинуклеотид ДНК, вставленный в целевой геномный локус, в соответствии с настоящим изобретением (например, растительные клетки-хозяева), включают, но не ограничиваются ими, любые высшие растения, включая как двудольные, так и однодольные растения, и в частности, потребляемые человеком растения, в том числе сельскохозяйственные культуры. Такие растения могут включать, но не ограничиваются ими, например: люцерну, сою, хлопок, рапс (также называемый канолой), лен, кукурузу, рис, брахиарию, пшеницу, сафлор, сорго, сахарную свеклу, подсолнечник, табак и дернообразующие травы. Таким образом, можно выбирать любой вид растений или растительных клеток. В вариантах осуществления растительные клетки, используемые по настоящему изобретению, и растения, выращенные или полученные из них, включают, но не ограничиваются ими, клетки, получаемые из семян рапса (Brassica napus), индийской горчицы (Brassica juncea), эфиопский горчицы (Brassica carinata), репы (Brassica rapa), капусты (Brassica oleracea), сои (Glycine max), льняного семени/льна (Linum usitatissimum), маиса (также называемого кукурузой) (Zea mays), сафлора (Carthamus tinctorius), подсолнечника (Helianthus annuus), табака (Nicotiana tabacum), Arabidopsis thaliana, бразильского ореха (Betholettia excelsa), клещевины (Ricinus communis), кокоса (Cocus nucifera), кориандра (Coriandrum sativum), хлопка (Gossypium spp.), арахиса (Arachis hypogaea), жожоба (Simmondsia chinensis), масличной пальмы (Elaeis guineeis), маслины (Olea eurpaea), риса (Oryza sativa), сквоша (Cucurbita maxima), ячменя (Hordeum vulgare), сахарного тростника (Saccharum officinarum), риса (Oryza sativa), пшеницы (Triticum spp., включая Triticum durum и Triticum aestivum) и ряски (Lemnaceae sp.). В некоторых вариантах осуществления генетический фон среди видов растений может варьироваться.
Используемый в настоящем документе термин «части растения» включает любые части растения, в том числе, но не ограничиваясь ими, семена (включая зрелые семена и незрелые семена), черенки растения, клетку растения, культуру клеток растения, орган растения, пыльцу, зародыши, цветы, плоды, побеги, листья, корни, стебли, эксплантаты и так далее. Клетка растения представляет собой структурную и физиологическую единицу растения, включающую протопласт и клеточную стенку. Клетка растения может находиться в виде изолированной одиночной клетки или совокупности клеток, такой как рыхлый каллус, или культивируемой клетки, или может быть частью более высокоорганизованной единицы, например, ткани растения, органа растения или растения. Таким образом, клетка растения может представлять собой протопласт, продуцирующую гаметы клетку, либо клетку или совокупность клеток, которые могут регенерировать в целое растение. Таким образом, семя, которое содержит множество растительных клеток и способно к регенерации в целое растение, считается клеткой растения для целей данного изобретения. Ткань растения или орган растения может представлять собой семя, протопласт, каллус или любые другие группы растительных клеток, которые организованы в структурную или функциональную единицу. Особенно полезные части растения включают собираемые части и части, используемые для распространения растений-потомков. Собираемые части растения могут представлять собой любую полезную часть растения, например, цветы, пыльцу, сеянцы, клубни, листья, стебли, плоды, семена, корни и тому подобное. Часть растения, используемая для распространения, включает, например, семена, плоды, черенки, сеянцы, клубни, корневища и тому подобное. Культура ткани предпочтительно будет способна к регенерации в растения, имеющие физиологические и морфологические характеристики вышеуказанного инбредного растения, к регенерации в растения, имеющие по существу тот же генотип, что и вышеуказанное инбредное растение. В одном из вариантов осуществления регенерируемые клетки в таких культурах тканей будут представлять собой зародыши, протопласты, клетки меристемы, каллус, пыльцу, листья, пыльники, корни, кончики корня, шелк, цветы, зерна, початки, стержни початков, листовые обертки или цветоножки. Кроме того, варианты осуществления настоящего изобретения относятся к растениям, регенерированным из культур тканей по вариантам осуществления изобретения.
Что касается производства растений, содержащих донорский полинуклеотид ДНК, вставленный в геномный локус, методы трансформации растений хорошо известны в данной области. Например, разработано множество методов трансформации растений, включая биологические и физические методы трансформации для двудольных растений, а также для однодольных растений (например, Goto-Fumiyuki et al., Nature Biotech 17: 282-286 (1999), Miki et al., Methods in Plant Molecular Biology and Biotechnology, Glick, B. R. and Thompson, J. E. Eds., CRC Press, Inc., Boca Raton, pp. 67-88 (1993)). Кроме того, доступны векторы, содержащие генные экспрессионные кассеты, и методы культивирования in vitro для трансформации и регенерации клеток и тканей растений описаны, например, в Gruber et al., Methods in Plant Molecular Biology and Biotechnology, Glick, B. R. and Thompson, J. E. Eds., CRC Press, Inc., Boca Raton, pp. 89-119 (1993).
Доступно большое количество методов для вставки ДНК, содержащей генную экспрессионную кассету, в клетку-хозяина растения. Эти методы включают трансформацию обезвреженной T-ДНК с использованием Agrobacterium tumefaciens или Agrobacterium rhizogenes в качестве средства трансформации, кальций-фосфатную трансфекцию, трансформацию с использованием полибрена, слияние протопластов, электропорацию, методы с использованием ультразвука (например, сонопорацию), трансформацию с использованием липосом, микроинъекцию, введение «голой» ДНК, плазмидных векторов, вирусных векторов, биолистику (бомбардировку микрочастицами), опосредованную карбидом кремния WHISKERS™ трансформацию, аэрозольную инжекцию или опосредованную полиэтиленгликолем трансформацию, а также и другие возможные методы.
Например, конструкт ДНК, содержащий генную экспрессионную кассету, можно вводить непосредственно в геномную ДНК клетки растения с использованием таких методов, как электропорация и микроинъекция в протопласты клеток растений, или конструкты ДНК можно вводить непосредственно в ткани растений с использованием биолистических методов, таких как бомбардировка частицами, покрытыми ДНК (смотри, например, Klein et al. (1987) Nature 327: 70-73). Дополнительные методы трансформации клеток растений включают микроинъекции с помощью опосредованного карбидом кремния WHISKERS™ поглощения ДНК (Kaeppler et al. (1990) Plant Cell Reporter 9: 415-418). Альтернативно, конструкт ДНК можно вводить в клетку растения с помощью трансформации наночастицами (смотри, например, патентную заявку США №12/245685, полное содержание которой включено в настоящий документ посредством ссылки).
Другим известным методом трансформации растений является опосредованная микрочастицами трансформация, когда ДНК нанесена на поверхность микрочастиц. В данном методе экспрессионный вектор вводят в ткани растений с помощью биолистического устройства, которое ускоряет микрочастицы до скоростей, достаточных для проникновения через клеточные стенки и мембраны растений. Sanford et al., Part. Sci. Technol. 5: 27 (1987), Sanford, J. C., Trends Biotech. 6: 299 (1988), Sanford, J. C., Physiol. Plant 79: 206 (1990), Klein et al., Biotechnology 10: 268 (1992).
Альтернативно, методы переноса генов и трансформации включают, но не ограничиваются ими, трансформацию протопластов путем осаждения хлоридом кальция, опосредованное полиэтиленгликолем (ПЭГ) или электропорацией поглощение ДНК (смотри Paszkowski et al. (1984) EMBO J 3: 2717-2722, Potrykus et al. (1985) Molec. Gen. Genet. 199: 169-177, Fromm et al. (1985) Proc. Nat. Acad. Sci. USA 82: 5824-5828 и Shimamoto (1989) Nature 338: 274-276) и электропорацию тканей растений (D'Halluin et al. (1992) Plant Cell 4: 1495-1505).
Широко используемый метод введения вектора, содержащего генную экспрессионную кассету, в растения основан на природной системе трансформации Agrobacterium. Horsch et al., Science 227: 1229 (1985). Известно, что A. tumefaciens и A. rhizogenes являются патогенными для растений почвенными бактериями, которые генетически трансформируют растительные клетки. Ti и Ri-плазмиды A. tumefaciens и A. rhizogenes, соответственно, несут гены, ответственные за генетическую трансформацию растения. Kado, C. I., Crit. Rev. Plant. Sci. 10: 1 (1991). Описания векторных систем Agrobacterium и методов опосредованного Agrobacterium переноса генов также можно найти, например, в Gruber et al., выше, Miki et al., выше, Moloney et al., Plant Cell Reports 8: 238 (1989) и патентах США №№4940838 и 5464763.
Если для трансформации используют Agrobacterium, ДНК, которую предстоит встраивать, должна быть клонирована в специальные плазмиды, а именно, либо в промежуточный вектор, либо в бинарный вектор. Промежуточные векторы не могут реплицироваться в Agrobacterium. Промежуточный вектор может быть перенесен в Agrobacterium tumefaciens при помощи хелперной плазмиды (конъюгация). Супербинарная система японского табака является примером такой системы (обзор в Komari et al., (2006) In: Methods in Molecular Biology (K. Wang, ed.) No. 343: Agrobacterium Protocols (2nd Edition, Vol. 1) Humana Press Inc., Totowa, NJ, pp. 15-41 и Komori et al., (2007) Plant Physiol. 145: 1155-1160). Бинарные векторы могут реплицироваться как в E. coli, так и в Agrobacterium. Они содержат ген селективного маркера и линкер или полилинкер, которые обрамлены справа и слева пограничными последовательностями T-ДНК. Они могут быть введены трансформацией непосредственно в Agrobacterium (Holsters, 1978). Agrobacterium, используемая в качестве клетки-хозяина, должна содержать плазмиду, несущую область vir. Ti или Ri-плазмида также содержит область vir, необходимую для переноса T-ДНК. Область vir необходима для переноса T-ДНК в клетку растения. Может содержаться и дополнительная T-ДНК.
Вирулентные функции хозяина Agrobacterium tumefaciens будут направлять вставку T-цепи, содержащей конструкт и находящийся рядом маркер, в ДНК клетки растения при инфицировании клетки бактериями с использованием бинарного T-ДНК вектора (Bevan (1984) Nuc. Acid Res. 12: 8711-8721) или процедуры совместного культивирования (Horsch et al. (1985) Science 227: 1229-1231). Как правило, систему трансформации Agrobacterium используют для генетической инженерии двудольных растений (Bevan et al. (1982) Ann. Rev. Genet 16: 357-384, Rogers et al. (1986) Methods Enzymol. 118: 627-641). Систему трансформации Agrobacterium можно также использовать для трансформации, а также переноса ДНК в однодольные растения и растительные клетки. Смотри патент США №5591616, Hernalsteen et al. (1984) EMBO J 3: 3039-3041, Hooykass-Van Slogteren et al. (1984) Nature 311: 763-764, Grimsley et al. (1987) Nature 325: 1677-179, Boulton et al. (1989) Plant Mol. Biol. 12: 31-40 и Gould et al. (1991) Plant Physiol. 95: 426-434.
После введения генетического конструкта, содержащего генную экспрессионную кассету, в клетки растения, клетки растения можно выращивать и после появления дифференцированных тканей, таких как побеги и корни, могут быть получены зрелые растения. В некоторых вариантах осуществления можно получать несколько растений. Методологии регенерации растений известны специалистам в данной области и их можно найти, например, в: Plant Cell and Tissue Culture, 1994, Vasil and Thorpe Eds. Kluwer Academic Publishers и в: Plant Cell Culture Protocols (Methods in Molecular Biology 111, 1999 Hall Eds Humana Press). Генетически модифицированное растение, описанное в настоящем документе, можно культивировать в ферментационной среде или выращивать в подходящей среде, такой как почва. В некоторых вариантах осуществления подходящая среда для роста высших растений может включать любую среду для роста растений, в том числе, но не ограничиваясь ими, почву, песок, любые другие состоящие из частиц среды, которые поддерживают рост корней (например, вермикулит, перлит и так далее), или гидропонную культуру, а также подходящее освещение, воду и питательные вещества, которые оптимизируют рост высших растений.
Трансформированные клетки растения, полученные при помощи любого из вышеуказанных методов трансформации, можно культивировать для регенерации целого растения, обладающего трансформированным генотипом и, следовательно, желаемым фенотипом. В основе таких методов регенерации лежит использование определенных фитогормонов в ростовой среде для культивирования тканей, как правило, с применением биоцидного и/или гербицидного маркера, который был введен вместе с желаемыми нуклеотидными последовательностями. Регенерация растений из культивируемых протопластов описана в статье Evans, et al., «Protoplasts Isolation and Culture» в Handbook of Plant Cell Culture, pp. 124-176, Macmillian Publishing Company, New York, 1983, и Binding, Regeneration of Plants, Plant Protoplasts, pp. 21-73, CRC Press, Boca Raton, 1985. Регенерацию можно также осуществлять из каллуса, эксплантатов, органов, пыльцы, зародышей или частей растения. Такие методы регенерации описаны, в основном, в статье Klee et al. (1987) Ann. Rev. of Plant Phys. 38: 467-486.
Нуклеиновые кислоты, введенные в клетку растения, можно использовать для придания желаемых признаков практически любому растению. Самые разнообразные растения и системы клеток растений могут быть генетически модифицированы для придания желаемых физиологических и агрономических характеристик, описанных в настоящем документе, с использованием конструктов нуклеиновой кислоты по настоящему изобретению и различных методов трансформации, упомянутых выше. В предпочтительных вариантах осуществления растения и клетки растений для генетической модификации включают, но не ограничиваются ими, однодольные и двудольные растения, такие как сельскохозяйственные культуры, в том числе зерновые культуры (например, пшеница, кукуруза, рис, просо, ячмень), плодовые культуры (например, томат, яблоня, груша, клубника, апельсин), кормовые культуры (например, люцерна), корнеплодные овощные культуры (например, морковь, картофель, сахарная свекла, батат), листовые овощные культуры (например, салат, шпинат), цветущие растения (например, петуния, розы, хризантемы), хвойные и сосновые деревья (например, сосна, ель, канадская ель), растения, используемые в фиторемедиации (например, накапливающие тяжелые металлы растения), масличные культуры (например, подсолнечник, рапс), а также растения, используемые для экспериментальных целей (например, Arabidopsis). Таким образом, раскрытые способы и композиции находят применение для широкого диапазона растений, включая, но не ограничиваясь ими, виды из родов Asparagus, Avena, Brassica, Citrus, Citrullus, Capsicum, Cucurbita, Daucus, Erigeron, Glycine, Gossypium, Hordeum, Lactuca, Lolium, Lycopersicon, Malus, Manihot, Nicotiana, Orychophragmus, Oryza, Persea, Phaseolus, Pisum, Pyrus, Prunus, Raphanus, Secale, Solanum, Sorghum, Triticum, Vitis, Vigna и Zea mays.
Трансформированную растительную клетку, каллус, ткань или растение можно идентифицировать и выделять путем отбора или скрининга генетически модифицированного растительного материала на наличие признаков, кодируемых маркерными генами, присутствующими в трансформирующей ДНК. Например, отбор можно производить, выращивая генетически модифицированный растительный материал на средах, содержащих ингибирующее количество антибиотика или гербицида, к которому трансформирующий генный конструкт придает устойчивость. Кроме того, трансформированные растения и клетки растений можно также идентифицировать путем скрининга на визуально определяемую активность маркерных генов (например, генов β-глюкуронидазы, люциферазы или gfp), которые могут присутствовать в конструктах рекомбинантной нуклеиновой кислоты. Такие методологии отбора и скрининга хорошо известны специалистам в данной области.
Термин «введенный» в контексте вставки нуклеиновой кислоты в клетку включает введение трансформацией в клетку, а также скрещивание растения, содержащего определенную последовательность, с другим растением таким образом, что второе растение будет содержать гетерологичную последовательность, как в общепринятых методах селекции растений. Такие методы селекции хорошо известны специалистам в данной области. Для получения информации о методах селекции растений смотри Poehlman (1995) Breeding Field Crops. AVI Publication Co., Westport Conn, 4th Edit. Можно использовать методы обратного скрещивания для введения гена в растения. Этот метод использовали в течение многих десятилетий для введения признаков в растение. Пример описания этого и других методов селекции растений, которые хорошо известны, можно найти в таких литературных источниках как Poehlman, выше, и Plant Breeding Methodology, edit. Neal Jensen, John Wiley & Sons, Inc. (1988). В типичном протоколе обратного скрещивания растение исходного интересующего сорта (рекуррентный родитель) скрещивают с растением второго сорта (нерекуррентный родитель), которое несет один интересующий ген, подлежащий переносу. Полученное от этого скрещивания потомство затем вновь скрещивают с рекуррентным родителем, и процесс повторяют до тех пор, пока не будет получено растение, в котором практически все желаемые морфологические и физиологические характеристики рекуррентного родителя будут восстановлены в преобразованном растении, в дополнение к одному перенесенному гену от нерекуррентного родителя.
Термин трансгенный «объект» относится к рекомбинантному растению, полученному путем трансформации и регенерации из одной растительной клетки с гетерологичной ДНК, например, экспрессионной кассетой, содержащей интересующий ген. Термин «объект» относится к исходному трансформанту и/или потомкам трансформанта, содержащим гетерологичную ДНК. Термин «объект» также относится к потомкам, полученным путем полового ауткросса между трансформантом и другим растением. Даже после повторного обратного скрещивания с рекуррентным родителем вставленная ДНК и фланкирующая ДНК из трансформированного родителя присутствует в потомках от скрещивания в той же хромосомной локализации. Как правило, в результате трансформации ткани растения образуются несколько объектов, все из которых имеют вставку конструкта ДНК в разных участках в геноме клетки растения. На основании экспрессии трансгена или других желаемых характеристик выбирают конкретный объект. В вариантах осуществления настоящего изобретения конкретный объект содержит донорский полинуклеотид ДНК, вставленный в целевой геномный локус.
«Трансген» означает ген, вставленный путем генетической манипуляции в геном организма с целью изменения его генотипа.
«Трансгенное растение» означает растение, имеющее одну или более растительных клеток, которые содержат экспрессионный вектор, содержащий генную экспрессионную кассету. Термин «матричная РНК (мРНК)» относится к РНК, которая не содержит интроны и которая может транслироваться в белок клеткой.
Используемый в настоящем документе термин «ДНК-вставка» означает гетерологичную ДНК в составе донорского полинуклеотида ДНК, содержащего генную экспрессионную кассету, используемую для трансформации растительного материала, в то время как «фланкирующая ДНК» или «ДНК области соединения» может содержать либо геномную ДНК, естественным образом присутствующую в организме, таком как растение, либо чужеродную (гетерологичную) ДНК, введенную в процессе трансформации, которая является посторонней для основной вставленной молекулы ДНК, например, фрагменты, ассоциированные с событием трансформации. Используемый в настоящем документе термин «область соединения» или «фланкирующая область», или «фланкирующая последовательность» относится к последовательности из по меньшей мере 20, 50, 100, 200, 300, 400, 1000, 1500, 2000, 2500 или 5000 или более пар оснований, которая расположена либо непосредственно перед и граничит с, либо непосредственно после и граничит с основной чужеродной вставленной молекулой ДНК.
В одном из вариантов осуществления изобретение относится к способу определения присутствия донорского полинуклеотида ДНК в целевом геноме при помощи реакции амплификации, в которой образуется ампликон. Обнаружение отсутствия ампликона указывает на то, что геномный локус был нарушен. В дополнительных вариантах осуществления наличие ампликона указывает на то, что донорский полинуклеотид ДНК вставлен в геномный локус.
В некоторых вариантах осуществления изобретения в сочетании с реакцией амплификации можно использовать различные анализы. Следующие методы полезны во многих ситуациях, и в одном варианте осуществления полезны для обнаружения присутствия молекулы нуклеиновой кислоты и/или кодируемого полипептида в клетке растения. Например, присутствие молекулы можно определять различными способами, в том числе с использованием праймера или зонда для последовательности. Трансген может избирательно экспрессироваться в некоторых тканях растения или на некоторых стадиях развития, или трансген может экспрессироваться практически во всех тканях растения, практически на протяжении всего его жизненного цикла. Однако также применим любой комбинаторный вид экспрессии.
Амплификацию выбранной или целевой нуклеотидной последовательности можно осуществлять любыми подходящими способами. Смотри, в основном, Kwoh et al., Am. Biotechnol. Lab. 8, 14-25 (1990). Примеры подходящих методик амплификации включают, но не ограничиваются ими, полимеразную цепную реакцию, лигазную цепную реакцию, амплификацию замещением цепей (смотри, в основном, G. Walker et al., Proc. Natl. Acad. Sci. USA 89, 392-396 (1992), G. Walker et al., Nucleic Acids Res. 20, 1691-1696 (1992)), амплификацию на основе транскрипции (смотри D. Kwoh et al., Proc. Natl. Acad Sci. USA 86, 1173-1177 (1989)), самоподдерживающуюся репликацию последовательности (или «3SR») (смотри J. Guatelli et al., Proc. Natl. Acad. Sci. USA 87, 1874-1878 (1990)), систему Qβ-репликазы (смотри P. Lizardi et al., BioTechnology 6, 1197-1202 (1988)), амплификацию, основанную на последовательности нуклеиновых кислот (или «NASBA») (смотри R. Lewis, Genetic Engineering News 12 (9), 1 (1992)), репаративную цепную реакцию (или «РЦР» («RCR»)) (смотри R. Lewis, выше) и бумеранговую ДНК-амплификацию (или «БДА» («BDA»)) (смотри R. Lewis, выше). Как правило, полимеразная цепная реакция является предпочтительной.
«Амплификация» представляет собой особый случай репликации нуклеиновой кислоты со специфичностью в отношении матрицы. Ее следует отличать от репликации без специфичности в отношении матрицы (то есть, репликации, которая зависит от матрицы, но не зависит от конкретной матрицы). Матричная специфичность в настоящем документе отличается от точности репликации (то есть, синтеза правильной полинуклеотидной последовательности) и нуклеотидной (рибо- или дезоксирибо-) специфичности. Матричную специфичность часто называют специфичностью в отношении «мишени». Целевые последовательности являются «мишенями» в том смысле, что они целенаправленно выбираются из других нуклеиновых кислот. Методы амплификации разработаны в первую очередь для такой сортировки.
Используемый в настоящем документе термин «полимеразная цепная реакция» и «ПЦР» в общем смысле относится к способу повышения концентрации сегмента целевой последовательности в смеси геномной ДНК без клонирования или очистки (патенты США №№4683195, 4683202 и 4965188, включенные в настоящий документ посредством ссылки). Данный способ амплификации целевой последовательности включает введение избытка двух олигонуклеотидных праймеров в смесь ДНК, содержащую желаемую целевую последовательность, с последующим выполнением точной последовательности термических циклов в присутствии ДНК-полимеразы. Два праймера комплементарны их соответствующим цепям двухцепочечной целевой последовательности. Для осуществления амплификации смесь денатурируют и затем праймеры отжигают с их комплементарными последовательностями в целевой молекуле. После отжига праймеры удлиняют с помощью полимеразы так, что образуется новая пара комплементарных цепей. Стадии денатурации, отжига праймеров и полимеразного удлинения можно повторять много раз (то есть, денатурация, отжиг и удлинение составляют один «цикл»; «циклов» может быть много) для получения высокой концентрации амплифицированного сегмента желаемой целевой последовательности. Длина амплифицированного сегмента желаемой целевой последовательности определяется относительными положениями праймеров по отношению друг к другу, и следовательно, эта длина является контролируемым параметром. В силу повторяющегося характера процесса, метод называют «полимеразной цепной реакцией» (далее по тексту «ПЦР»). Поскольку желаемые амплифицированные сегменты целевой последовательности становятся преобладающими последовательностями (по концентрации) в смеси, говорят, что они «ПЦР-амплифицированы».
Используемый в настоящем документе термин «множество» означает два или более, например, три, четыре, пять или более, в том числе десять, двадцать, пятьдесят или более полинуклеотидов, нуклеотидных зондов и тому подобного.
Термин «с обратной транскриптазой» или «ОТ-ПЦР» относится к типу ПЦР, в которой исходным материалом является мРНК. Исходная мРНК ферментативно превращается в комплементарную ДНК или «кДНК» с участием фермента обратной транскриптазы. Затем кДНК используют в качестве «матрицы» для реакции «ПЦР».
В одном из вариантов осуществления реакция амплификации является количественной. В других вариантах осуществления реакцию амплификации количественно определяют с использованием сигнатурного профиля, при этом сигнатурный профиль выбирают из группы, состоящей сигнатурного профиля температуры плавления или сигнатурного профиля флуоресценции.
Молекулу нуклеиновой кислоты по вариантам осуществления изобретения или ее сегменты можно использовать в качестве праймеров для ПЦР-амплификации. При проведении ПЦР-амплификации допускается определенная степень несоответствия между праймером и матрицей. Вследствие этого, мутации, делеции и вставки (особенно добавление нуклеотидов на 5' или 3'-конце) в приведенных в качестве примера праймерах входят в объем настоящего изобретения. Мутации, вставки и делеции могут быть внесены в конкретный праймер методами, известными квалифицированному специалисту в данной области.
Описаны молекулярные маяки для использования в обнаружении последовательности. Вкратце, разработан олигонуклеотидный зонд FRET, который перекрывает область соединения фланкирующей геномной последовательности и ДНК-вставки. Уникальная структура зонда FRET приводит к тому, что он содержит вторичную структуру, которая удерживает флуоресцентный и гасящий флуоресценцию фрагменты в непосредственной близости. Проводят цикл реакций зонда FRET и ПЦР-праймеров (один праймер во вставленной последовательности ДНК и один во фланкирующей геномной последовательности) в присутствии термостабильной полимеразы и набора дНТФ. После успешной ПЦР-амплификации гибридизация зонда(ов) FRET с целевой последовательностью приводит к исчезновению вторичной структуры зонда и пространственному разделению флуоресцентного и гасящего флуоресценцию фрагментов. Флуоресцентный сигнал указывает на присутствие фланкирующей геномной/трансгенной вставленной последовательности в результате успешной амплификации и гибридизации. Такой анализ с помощью молекулярного маяка для обнаружения продуктов реакции амплификации является одним из вариантов осуществления настоящего изобретения.
Анализ гидролиза зонда, также известный как TAQMAN® (Life Technologies, Foster City, Calif.), представляет собой метод обнаружения и количественного определения присутствия последовательности ДНК. Вкратце, разработан олигонуклеотидный зонд FRET с одним олигонуклеотидом в трансгене и одним во фланкирующей геномной последовательности для специфического обнаружения объекта. Проводят цикл реакций зонда FRET и ПЦР-праймеров (один праймер во вставленной последовательности ДНК и один во фланкирующей геномной последовательности) в присутствии термостабильной полимеразы и набора дНТФ. Гибридизация зонда FRET приводит к расщеплению и высвобождению флуоресцентного фрагмента от гасящего флуоресценцию фрагмента на зонде FRET. Флуоресцентный сигнал указывает на присутствие фланкирующей/трансгенной вставленной последовательности в результате успешной амплификации и гибридизации. Такой анализ гидролиза зонда для обнаружения продуктов реакции амплификации является одним из вариантов осуществления настоящего изобретения.
Анализы KASPar представляют собой метод обнаружения и количественного определения присутствия последовательности ДНК. Вкратце, образец геномной ДНК, содержащей целевой геномный локус, подвергают скринингу путем анализа на основе полимеразной цепной реакции (ПЦР), известного как аналитическая система KASPar®. В анализе KASPar®, используемом в практике настоящего изобретения, можно использовать смесь для ПЦР-анализа KASPar®, содержащую несколько праймеров. Праймеры, используемые в смеси для ПЦР-анализа, могут включать по меньшей мере один прямой праймер и по меньшей мере один обратный праймер. Прямой праймер содержит последовательность, соответствующую определенной области донорского полинуклеотида ДНК, и обратный праймер содержит последовательность, соответствующую определенной области геномной последовательности. Кроме того, праймеры, используемые в смеси для ПЦР-анализа, могут включать по меньшей мере один прямой праймер и по меньшей мере один обратный праймер. Например, в смеси для ПЦР-анализа KASPar® могут быть использованы два прямых праймера, соответствующие двум разным аллелям, и один обратный праймер. Один из прямых праймеров содержит последовательность, соответствующую определенной области эндогенной геномной последовательности. Второй прямой праймер содержит последовательность, соответствующую определенной области донорского полинуклеотида ДНК. Обратный праймер содержит последовательность, соответствующую определенной области геномной последовательности. Такой анализ KASPar® для обнаружения продуктов реакции амплификации является одним из вариантов осуществления настоящего изобретения.
В некоторых вариантах осуществления флуоресцентный сигнал или флуоресцентный краситель выбран из группы, состоящей из флуоресцентного красителя HEX, флуоресцентного красителя FAM, флуоресцентного красителя JOE, флуоресцентного красителя TET, флуоресцентного красителя Cy 3, флуоресцентного красителя Cy 3,5, флуоресцентного красителя Cy 5, флуоресцентного красителя Cy 5,5, флуоресцентного красителя Cy 7 и флуоресцентного красителя ROX.
В других вариантах осуществления реакцию амплификации проводят с использованием подходящих второстепенных флуоресцентных красителей ДНК, которые способны окрашивать клеточную ДНК в диапазоне концентраций, поддающихся измерению методом проточной цитометрии, и имеют спектр флуоресцентного излучения, поддающийся измерению в реальном времени при помощи термоциклера. Специалистам в данной области должно быть понятно, что известны и другие красители для нуклеиновых кислот и постоянно разрабатываются новые. Можно использовать любой подходящий краситель для нуклеиновых кислот с соответствующими спектрами возбуждения и излучения, такой как YO-PRO-1®, SYTOX Green®, SYBR Green I®, SYTO11®, SYTO12®, SYTO13®, BOBO®, YOYO® и TOTO®. В одном варианте осуществления второстепенный флуоресцентный краситель ДНК представляет собой SYTO13®, используемый в концентрации менее 10 мкМ, менее 4 мкМ или менее 2,7 мкМ.
Варианты осуществления настоящего изобретения дополнительно описаны в следующих далее примерах. Следует понимать, что эти примеры приведены исключительно с целью иллюстрации. На основании приведенного выше описания и данных примеров специалист в данной области может установить существенные признаки данного изобретения и, не отступая от сущности и объема изобретения, сможет вносить различные изменения и модификации в варианты осуществления изобретения, чтобы приспособить его к различным вариантам применения и условиям. Таким образом, различные модификации вариантов осуществления изобретения в дополнение к тем, которые показаны и описаны в настоящем документе, будут очевидны для специалистов в данной области из вышеприведенного описания. Такие модификации также должны входить в объем прилагаемой формулы изобретения. Следующие примеры приведены в качестве иллюстрации и не должны ограничивать объем изобретения.
ПРИМЕРЫ
Пример 1. Анализ целевых локусов в каллусе кукурузы
Таргетинг геномных локусов: Геномный локус для объекта кукурузы DAS-59132, ранее описанного в WO2009100188 METHODS FOR DETECTION OF CORN EVENT DAS-59132, полное содержание которого включено в настоящий документ посредством ссылки, был таргетирован с использованием нуклеазы с «цинковыми пальцами», разработанной для специфического связывания и расщепления геномной ДНК, что привело к образованию данного объекта. Полученные трансформанты поддерживали до завершения анализа для идентификации и характеристики нарушения геномных локусов в конкретных объектах путем реакции амплификации.
Белки с «цинковыми пальцами», направленные на последовательности ДНК, которые содержат геномный локус для DAS-59132, были разработаны, как описано ранее. Смотри, например, Urnov et al. (2005) Nature 435: 646-651. Разработанные последовательности «цинковых пальцев» для DAS-59132 были включены в векторы, кодирующие белок, имеющий по меньшей мере один «палец» со структурой CCHC. Смотри патентную публикацию США №2008/0182332. В частности, последний «палец» в каждом белке имел каркас CCHC для спирали узнавания. Неканонические кодирующие «цинковые пальцы» последовательности были слиты с нуклеазным доменом фермента рестрикции IIS типа, FokI (аминокислоты 384-579 последовательности из статьи Wah et al. (1998) Proc. Natl. Acad. Sci. USA 95: 10564-10569), через линкер из четырех аминокислот и сигнал ядерной локализации opaque-2, полученный из Zea mays, для получения нуклеаз с «цинковыми пальцами» (ZFN) для DAS-59132. Экспрессия слитых белков в бицистронном экспрессионном конструкте, где использован рибосомный сигнал прерывания 2A (2A ribosomal stuttering signal), как описано в статье Shukla et al. (2009) Nature 459: 437-441, направлялась относительно сильным конститутивным и эктопическим промотором, таким как промотор CsVMV.
Оптимальные ZFN проверяли на расщепляющую активность с использованием системы на основе почкующихся дрожжей, которая, как показано ранее, позволяет определять активные нуклеазы. Смотри, например, патентную публикацию США №20090111119, Doyon et al. (2008) Nat Biotechnol. 26: 702-708, Geurts et al. (2009) Science 325: 433. Из многочисленных ZFN, которые были разработаны, получены и протестированы на связывание с предполагаемыми целевыми сайтами геномного полинуклеотида DAS-59132, были определены предпочтительные ZFN, имеющие in vivo активность на высоких уровнях, и выбраны для дальнейших экспериментов. Эти ZFN были охарактеризованы как способные эффективно связываться и расщеплять целевые сайты геномного полинуклеотида DAS-59132 в растениях.
Плазмидные векторы, содержащие экспрессионные конструкты ZFN для иллюстративных нуклеаз с «цинковыми пальцами», которые были идентифицированы с помощью анализа в дрожжевой системе, были разработаны и получены с помощью навыков и методов, известных в данной области. Затем слитая последовательность сигнал ядерной локализации opaque-2::нуклеаза с «цинковыми пальцами» была спарена с комплементарной слитой последовательностью сигнал ядерной локализации opaque-2::нуклеаза с «цинковыми пальцами». Как таковой, каждый конструкт состоял из одной открытой рамки считывания, состоящей из двух слитых последовательностей сигнал ядерной локализации opaque-2::нуклеаза с «цинковыми пальцами», разделенных последовательностью 2A из вируса Thosea asigna (Mattion et al. (1996) J. Virol. 70: 8124-8127). Экспрессия кодирующей последовательности ZFN находилась под управлением обеспечивающего высокий уровень экспрессии конститутивного промотора убиквитина 1 из Zea mays (Christensen et al. (1992) Plant Mol. Biol. 18(4): 675-89), и она была фланкирована 3'-полиA нетранслируемой областью Per 5 Zea mays (патент США №6699984).
Был разработан донорский конструкт для интегрирования в расщепленную ZFN геномную ДНК геномного локуса DAS-59132. Эта экспрессионная кассета одного гена включала управляющий промотор актина 1 риса (Os Act1 промотор)::кодирующую последовательность фосфинотрицин ацетилтрансферазы (PAT; патент США №7838733):: и заканчивалась 3'-нетранслируемой областью липазы Zea mays (ZmLip 3'UTR). Кроме того, была сконструирована плазмида донора с 1 т.п.н. последовательностью (плечи гомологии) на каждом конце целевого гена PAT, которая гомологична последовательности на каждом конце сайта разрезания ZFN в геномном локусе DAS-59132. Плечи гомологии служили в качестве субстрата, используемого аппаратом гомологичной рекомбинации для вставки трансгена в геномный сайт разрезания ZFN. Различные генные элементы были собраны в многокопийную плазмиду на основе pUC.
Направленная интеграция: Трансгенные события были направлены на эндогенный геномный локус DAS-59132. Описанные ранее конструкты содержали донорскую последовательность (pDAB107855) и DAS-59132 ZFN 6 (pDAB105906). Совместная трансформация этими двумя плазмидами привела к получению 854 трансгеннных объектов PAT, которые были подвергнуты скринингу способом определения присутствия донорского полинуклеотида ДНК в целевом геномном локусе по настоящему изобретению.
Клетки каллуса кукурузы, представляющие собой 12 мл объема осажденных клеток (PCV) из ранее замороженной клеточной линии плюс 28 мл кондиционированной среды, субкультивировали в 80 мл жидкой среды GN6 в 500-мл колбе Эрленмейера и помещали на шейкер, установленный на 125 об/мин, при температуре 28°C. Этот этап повторяли два раза, используя ту же линию клеток, так что в общей сложности 36 мл PCV были разлиты в три колбы. Через 24 часа жидкую среду GN6 удаляли и заменяли на 72 мл осмотической среды GN6 S/M. Колбу инкубировали в темноте в течение 30-35 минут при 28°C при умеренном перемешивании (125 об/мин). Во время периода инкубации готовили суспензию карбида кремния WHISKERS™ (Advanced Composite Materials, LLC, Greer, SC) в концентрации 50 мг/мл, добавляя 8,1 мл жидкой среды GN6 S/M к 405 мг стерильного карбида кремния WHISKERS™.
После инкубации в осмотической среде GN6 S/M содержимое всех колб объединяли в 250-мл центрифужной колбе. После того, как все клетки в колбе осели на дно, объем содержимого свыше примерно 14 мл жидкой среды GN6 S/M отбирали и помещали в стерильную 1-л колбу для будущего использования. Предварительно увлажненную суспензию WHISKERS™ перемешивали с максимальной скоростью на вихревой мешалке в течение 60 секунд, а затем добавляли в центрифужную колбу.
В этом примере ДНК плазмид pDAB107855 (донорская последовательность) и pDAB105906 (ZFN) добавляли в каждую колбу. После добавления плазмидной ДНК колбу немедленно помещали в модифицированный коммерческий смеситель краски Red Devil 5400™ (Red Devil Equipment Co., Plymouth, MN) и перемешивали в течение 10 секунд. После перемешивания коктейль из клеток, среды, WHISKERS™ и плазмидной ДНК добавляли к содержимому 1-л колбы наряду с 125 мл свежей жидкой среды GN6 для снижения количества осмотиканта. Клетки оставляли для восстановления на шейкере, установленном на 125 об/мин, в течение 2 часов. 6 мл дисперсной суспензии фильтровали на фильтровальной бумаге Whatman №4 (5,5 см), используя стеклянную ячейку для сбора клеток, соединенную с домашним вакуумным трубопроводом, так что на колбу было получено 60 фильтров. Фильтры помещали в чашки размером 60×20 мм с твердой средой GN6 и культивировали при 28°C в темноте в течение 1 недели.
Через одну неделю после доставки ДНК бумажные фильтры переносили в чашки размером 60×20 мм с селективной средой GN6 (1H), содержащей селективный агент. Эти селективные чашки инкубировали при 28°C в течение одной недели в темноте. Через 1 неделю отбора в темноте ткань погружали в свежую среду, соскребая ½ клеток с каждой чашки в пробирку, содержащую 3,0 мл среды GN6 с агарозой, поддерживаемую при температуре 37-38°C.
Смесь агароза/ткань разделяли шпателем и затем 3 мл смеси агароза/ткань равномерно выливали на поверхность чашки Петри размером 100×25 мм, содержащей среду GN6 (1H). Этот процесс повторяли для обеих половин каждой чашки. После того, как вся ткань была залита, чашки инкубировали при 28°C в темноте в течение срока до 10 недель. Предположительно трансформированные изоляты, которые росли в этих селективных условиях, удаляли с залитых чашек и переносили в свежую селективную среду в чашках размером 60×20 мм. Если примерно через 2 недели был заметен устойчивый рост, считали, что объект является устойчивым к применяемому гербициду (селективному агенту), и аликвоту клеток затем собирали для анализа генотипа. В этом примере из обработанных колб было получено большое количество объектов. Эти объекты далее подвергали молекулярному анализу для подтверждения интегрирования трансгена в геномный локус объекта кукурузы DAS-59132.
Выделение ДНК: Образцы ткани каллуса собирали в 96-луночные планшеты (Qiagen, Valencia, CA) и затем лиофилизировали в течение 48 часов. Ткань разрушали измельчителем ткани Klecko™ (Garcia Manufacturing, Visalia, CA) в лизирующем буфере Biosprint96 AP1™ (Qiagen) с одной гранулой из нержавеющей стали. После мацерации ткани геномную ДНК выделяли в высокопроизводительном формате с использованием набора Biosprint96™ для растений (Qiagen) с роботом-экстрактором Biosprint96™ (Qiagen). Образец геномной ДНК затем разбавляли до концентрации 2 нг/мкл перед проведением реакций кПЦР для достижения соответствующих показателей Cp (цикл количественного определения), которые приводили к получению сигнатурного профиля.
Анализ нарушения локуса DAS-59132: Опосредованная Whiskers™ трансформация клеток каллуса Hi-II плазмидой DAS-59132-ZFN и плазмидой донора приводила к направленным и случайным вставкам трансгена. Чтобы отличить объекты со случайными вставками от популяций таргетированных объектов, все 854 полученных объекта вначале подвергали скринингу с использованием анализа нарушения локуса. Этот анализ позволяет определять, остается ли сайт связывания ZFN в локусе интактным или он был нарушен в результате расщепления ZFN или вставки донора. Свидетельство нарушения в геномном локусе является первым доказательством того, что ZFN расщепила эндогенный целевой локус DAS-59132, и свидетельствует о направленной вставке донорской молекулы ДНК. Были разработаны праймеры для амплификации эндогенной целевой области, содержащей сайты узнавания ZFN, и подготовлены образцы для анализа методом кПЦР. Амплификация интактной области, свидетельствующей о ненаправленном событии трансформации, приводила к образованию ампликона из 140 п.н., что измеряли в виде детектируемого сигнала кПЦР. Успешное направленное интегрирование донорской молекулы приводило к нарушению детектируемого сигнала кПЦР и проявлялось в виде сниженного общего сигнала по сравнению с контролем.
Анализ нарушения локуса DAS-59132 проводили методом ПЦР в реальном времени с использованием системы LightCycler® 480 (Roche Applied Science, Indianapolis, IN). Анализы были разработаны для мониторинга последовательностей DAS-59132 для связывания ZFN (25716/25717) в локусе DAS-59132 (и внутреннем эталонном гене IVF (регистрационный №Genbank: U16123.1|ZMU16123) с использованием программы для разработки зондов LightCycler® Probe Design Software 2.0. Для амплификации мастер-микс зондов LightCycler® 480 (Roche Applied Science, Indianapolis, IN) готовили в конечной концентрации 1X в объеме 10 мкл мультиплексной реакционной смеси, содержащей 0,4 мкМ каждого праймера и 0,2 мкМ каждого зонда (таблица 1). Проводили двухступенчатую реакцию амплификации с удлинением при 55°C в течение 30 секунд с приращением сигнала флуоресценции. Результаты анализа на нарушение локуса анализировали, используя отношение мишени к эталону.
Последовательности олигонуклеотидных праймеров и зондов для анализа нарушения локуса DAS-59132
854 объекта, полученные в результате точной трансформации, подвергали скринингу в анализе нарушения локуса, и локус считали нарушенным на основании значительного уменьшения отношения сигнала мишени к сигналу эталона. Результаты свидетельствовали о том, что 63 из 854 проанализированных объектов имели нарушенный сигнал в локусе DAS-59132, что указывало на целевую вставку гена (фигура 2). Несмотря на количественные показатели нарушенного локуса, получаемые в анализе нарушения локуса, данный анализ не позволяет отличать направленные вставки от мутаций в сайте расщепления, возникающих в результате неточной репарации разрыва. Был разработан вторичный анализ методом внутренней-внешней ПЦР для параллельного скрининга объектов с целью обеспечения надежной и точной оценки всех объектов.
Анализ локуса DAS-59132 методом внутренней-внешней ПЦР: Объекты, отобранные в анализе нарушения локуса, также подвергали скринингу в анализе локус-специфической ПЦР с детекцией по «конечной точке» в локусе DAS-59132. Один олигонуклеотидный праймер был разработан для отжига с областью целевой геномной ДНК за пределами сайта расщепления ZFN и второй олигонуклеотидный праймер был разработан для отжига только с областью трансгена донорской ДНК. Праймеры были разработаны для анализа 5' и 3'-областей соединения с ДНК-вставкой целевого сайта в локусе DAS-59132. Многие из объектов, полученных в результате трансформации, имели случайные вставки и, следовательно, при внутренней-внешней ПЦР амплификация на происходила, поскольку донорская последовательность не находилась в непосредственной близости от целевой последовательности (фигура 3A). Поскольку праймеры разработаны только для амплификации областей донорской ДНК и геномной ДНК, которые вставлены в целевую область, амплификация является результатом наличия таргетированного трансгенного объекта (фигура 3B). Этот ПЦР-анализ, называемый «внутренней-внешней» ПЦР, гарантирует, что получена полная картина направленной вставки гена, поскольку праймеры разработаны для направления как на целевую последовательность, так и на вставленную донорскую последовательность и анализируются как 5', так и 3'-области соединения. После ПЦР амплифицированные образцы анализировали методом электрофореза, и образцы с трансгенной вставкой в целевом сайте в локусе DAS-59132 характеризовались амплификацией двух полос, соответствующих 2 т.п.н. и 1,5 т.п.н. Это свидетельствовало об интегрированной целевой последовательности в 5' и 3'-областях соединения трансгена.
Реакции амплификации внутренней-внешней ПЦР проводили с использованием набора Takara Ex Taq HS kit™ (Clontech Laboratories, Inc., Mountain View, CA). Каждую реакцию ПЦР проводили в конечном объеме 15 или 20 мкл реакционной смеси, содержащей 1x Ex Taq буфер, 200 нМ прямых и обратных праймеров, 10-20 нг геномной ДНК-матрицы и Ex Taq HS полимеразу в конечной концентрации 0,05 единиц/мкл. Для внутренней-внешней ПЦР в реальном времени в реакционную смесь для ПЦР включали краситель SYTO13® от компании Invitrogen (Grand Island, NY) в конечной концентрации 4 мкМ или 2,67 мкМ. Первоначально зеленый флуоресцентный краситель SYTO13® использовали в рекомендованных производителем концентрациях, поскольку ранее показано, что он повышает общую чувствительность анализа и незначительно ингибирует полимеразную активность. Использование этого красителя позволяло получать более сильный сигнал и более стабильные результаты, однако высокопроизводительная система все еще имела ограничения. Фоновая флуоресценция продолжала оставаться проблемой, поскольку образование димеров праймеров или неспецифический отжиг праймеров (следствие недостаточно чистых праймеров) генерировали ложноположительные сигналы. Вследствие этого, концентрации, использованные в анализе, были ниже, от 10 мкМ до 4 мкМ или 2,67 мкМ. Снижение концентрации красителя приводило к получению сигнатурного профиля, обеспечивающего надежное обнаружение и количественное определение в ПЦР-анализе.
Внутреннюю-внешнюю ПЦР в реальном времени выполняли с использованием ABI VIIA7 PCR system™ (Life Technologies Corporation, Carlsbad, CA). После первоначальной денатурации программа амплификации включала 40 циклов при 98°C в течение 10 сек, 66°C в течение 30 сек и 68°C в течение 2 мин с приращением сигнала флуоресценции перед программой анализа температуры плавления. После этапа амплификации реакционную смесь выдерживали при температуре 65°C в течение 30 сек и 72°C в течение 10 мин, и наконец, выдерживали при температуре 4°C. Для анализа образца использовали как прямые флуоресцентные сигналы, так и профили температуры плавления. Положительные образцы, идентифицированные в системе реального времени, дополнительно подтверждали с использованием стандартного анализа гелевого сдвига.
Последовательности праймеров и зондов для анализа «внутренней-внешней» ПЦР локуса DAS-59132
В попытке дифференцировать ПЦР-ампликоны направленной вставки от ложноположительных результатов был разработан протокол для определения сигнатурного профиля каждого полученного продукта ПЦР. Профили температуры плавления ПЦР-ампликонов сравнивали с положительным контролем, и совпадающие кривые выявляли положительные продукты внутренней-внешней ПЦР (фигуры 4A и 4B). Сочетание анализа внутренней-внешней ПЦР с использованием сигнатурного профиля, включающего профиль температуры плавления как 3', так и 5'-концов последовательности, является новой аналитической методологией, позволяющей более надежно определять объект с направленной вставкой донорского полинуклеотида ДНК в геномном локусе.
Результаты анализа нарушения локуса и анализа локуса DAS-59132 методом внутренней-внешней ПЦР дополнительно подтверждали саузерн-блоттингом и секвенированием (стандартным секвенированием следующего поколения (NGS)).
Результатом нового анализа явился надежный аналитический способ определения объектов с направленной вставкой донорского полинуклеотида ДНК в сайт расщепления ZFN в растениях кукурузы. Эндогенные геномные локусы были успешно таргетированы и объекты с направленной вставкой были эффективно выявлены с помощью нового анализа. В общей ложности 854 образца были проанализированы с использованием описанного анализа. Анализ нарушения локуса проводили для всех предполагаемых объектов, при этом в 63 объектах было обнаружено нарушение локуса. Для всех данных объектов проводили внутреннюю-внешнюю ПЦР и идентифицировали 8 положительных объектов. В результате, в общей сложности получено 8 объектов, которые достоверно имели направленные вставки (фигура 5).
Пример 2. Анализ целевых локусов в растениях кукурузы
Получали зародыши трансгенной кукурузы B104, в которых локус DAS-59132 был таргетирован при помощи конструкта нуклеазы с «цинковыми пальцами», pDAB105906, и конструкта донора, pDAB104179. Эти конструкты были введены трансформацией в ткань растения с использованием метода биолистической трансформации, описанного в примере 7 патентной заявки США №2011/0191899, полное содержание которой включено в настоящий документ посредством ссылки. Предположительно трансформированные зародыши определяли отбором с помощью гербицида фосфинотрицина.
Предположительно выявленные трансгенные зародыши анализировали с использованием анализа нарушения локуса для определения объектов, содержащих донорский полинуклеотид ДНК, вставленный в целевой геномный локус. Анализ нарушения локуса с помощью ZFN проводили, используя протоколы и реагенты, описанные выше. У объектов, которые не были таргетированы или не имели нарушение, наблюдали отношение мишени к эталону в диапазоне 0,4-0,6; у образцов, которые имели нарушение или были таргетированы, имело место отношение в диапазоне 0,2-0,35 (вариации между чашками) (фигура 6). В случае таргетированных объектов без образования ампликона наблюдали меньшее количество амплифицированного продукта, как показано на графике.
Затем проводили локус-специфическую внутреннюю-внешнюю ПЦР с использованием протокола и реагентов, описанных выше. Результаты внутренней-внешней ПЦР позволяли определять конкретные объекты, содержащие трансгенную вставку в локусе DAS- 59132.
В общей сложности анализировали 1223 объекта. Для каждого объекта проводили анализ нарушения локуса и определили 85 объектов, демонстрирующих нарушение. Внутреннюю-внешнюю ПЦР проводили для всех 1223 объектов и определили 11 положительных объектов и 2 частично положительных объекта. Выполняли саузерн-блоттинг и секвенирование для подтверждения того, что идентифицированные объекты содержали полные трансгенные вставки в геномном локусе DAS-59132.
Пример 3. Анализ целевых локусов в растениях кукурузы
Получали зародыши трансгенной кукурузы B104, в которых локус - сконструированная посадочная площадка (Engineered Landing Pad, ELP) (патентная заявка США №2011/0191899, полное содержание которой включено в настоящий документ посредством ссылки) был таргетирован с использованием конструкта нуклеазы с «цинковыми пальцами» и конструкта донора, введенных биолистической трансформацией в ткань растения. Было проведено несколько трансформаций для направления конструкта донора в локус - сконструированную посадочную площадку. Первую серию трансформаций выполняли с использованием конструкта донора pDAB109714 и конструкта нуклеазы с «цинковыми пальцами» pDAB105941. Вторую серию трансформаций выполняли с использованием конструкта донора pDAB109715 и конструкта нуклеазы с «цинковыми пальцами» pDAB105943. Третью серию трансформаций выполняли с использованием конструкта донора pDAB109716 и конструкта нуклеазы с «цинковыми пальцами» pDAB105942. Последнюю серию трансформаций выполняли с использованием конструкта донора pDAB109717 и конструкта нуклеазы с «цинковыми пальцами» pDAB105945. Предположительно трансформированные зародыши определяли отбором с помощью гербицида фосфинотрицина.
Анализ нарушения локуса ELP: Были разработаны праймеры для амплификации эндогенной целевой области, содержащей сайты узнавания ZFN, и подготовлены образцы для анализа методом кПЦР. Амплификация интактной области, свидетельствующей о ненаправленном событии трансформации, приводила к образованию ампликона из 193 пар нуклеотидов, что измеряли в виде детектируемого сигнала кПЦР. Успешное направленное интегрирование донорских молекул в соответствующий объект ELP приводило к нарушению детектируемого сигнала кПЦР и проявлялось в виде сниженного общего сигнала по сравнению с контролем.
Анализ нарушения локуса ELP проводили методом ПЦР в реальном времени с использованием системы LightCycler® 480 (Roche Applied Science, Indianapolis, IN). Анализы были разработаны для мониторинга последовательностей ELP для связывания ZFN в локусе ELP и внутреннем эталонном гене IVF с использованием программы для разработки зондов LightCycler® Probe Design Software 2.0. Для амплификации мастер-микс зондов LightCycler® 480 (Roche Applied Science, Indianapolis, IN) готовили в конечной концентрации 1X в объеме 10 мкл мультиплексной реакционной смеси, содержащей 0,4 мкМ каждого праймера и 0,2 мкМ каждого зонда (таблица 3). Проводили двухступенчатую реакцию амплификации с удлинением при 55°C в течение 30 секунд с приращением сигнала флуоресценции. Результаты анализа на нарушение локуса анализировали, используя отношение мишени к эталону.
Последовательности праймеров и зондов для анализа нарушения локуса ELP. Реакции ELP1 и ELP2 были мультиплексированы с праймерами и зондами для IVF, последовательности которых приведены в таблице 1
1738 объектов, полученных в результате точной трансформации, подвергали скринингу в анализе нарушения локуса, и локус считали нарушенным на основании значительного уменьшения отношения сигнала мишени к сигналу эталона. Результаты свидетельствовали о том, что 158 из 1738 проанализированных объектов имели нарушенный сигнал в локусе ELP, что указывало на целевую вставку гена (фигура 7). Несмотря на количественные показатели нарушенного локуса, получаемые в анализе нарушения локуса, данный анализ не позволяет отличать направленные вставки от мутаций в сайте расщепления, возникающих в результате неточной репарации разрыва. Вследствие этого, был разработан вторичный анализ методом внутренней-внешней ПЦР для параллельного скрининга объектов с целью обеспечения надежной и точной оценки всех объектов.
Анализ локуса ELP методом внутренней-внешней ПЦР: Объекты, отобранные в анализе нарушения локуса, также подвергали скринингу в новом разработанном анализе локус-специфической ПЦР с детекцией по «конечной точке» в локусе ELP. Один праймер был разработан для отжига с областью целевой геномной ДНК за пределами сайта расщепления ZFN и второй праймер был разработан для отжига только с областью трансгена донорской ДНК. Праймеры были разработаны для анализа 5' и 3'-областей целевого сайта в локусе ELP. Поскольку праймеры разработаны только для амплификации областей донорской ДНК и геномной ДНК, которые вставлены в целевую область, амплификация является результатом наличия таргетированного трансгенного объекта; были проанализированы как 5', так и 3'-области соединения.
Реакции амплификации внутренней-внешней ПЦР проводили с использованием набора Takara Ex Taq HS kit™ (Clontech Laboratories, Inc., Mountain View, CA). Каждую реакцию ПЦР проводили в конечном объеме 15 или 20 мкл реакционной смеси, содержащей 1x Ex Taq буфер, 200 нМ прямых и обратных праймеров, 10-20 нг геномной ДНК-матрицы и Ex Taq HS полимеразу в конечной концентрации 0,05 единиц/мкл. Для внутренней-внешней ПЦР в реальном времени в реакционную смесь для ПЦР включали краситель SYTO13® (Invitrogen, Carlsbad, CA) в конечной концентрации 4 мкМ или 2,67 мкМ.
Внутреннюю-внешнюю ПЦР в реальном времени выполняли с использованием ABI VIIA7 PCR system™ (Life Technologies Corporation, Carlsbad, CA). После первоначальной денатурации программа амплификации включала 40 циклов при 98°C в течение 10 сек, 66°C в течение 30 сек и 68°C в течение 2 мин с приращением сигнала флуоресценции перед программой анализа температуры плавления. После этого реакционную смесь выдерживали при температуре 65°C в течение 30 сек и 72°C в течение 10 мин, и наконец, выдерживали при температуре 4°C. Для анализа образца использовали как прямые флуоресцентные сигналы, так и профили температуры плавления. Положительные образцы, идентифицированные в системе реального времени, дополнительно подтверждали с использованием стандартного анализа гелевого сдвига.
Последовательности праймеров и зондов для анализа «внутренней-внешней» ПЦР локуса ELP
В попытке дифференцировать ПЦР-ампликоны от ложноположительных результатов был разработан протокол для определения сигнатурного профиля каждого полученного продукта ПЦР. Профили температуры плавления ПЦР-ампликонов сравнивали с положительным контролем, и совпадающие кривые выявляли положительные продукты внутренней-внешней ПЦР. Сочетание анализа внутренней-внешней ПЦР с использованием сигнатурного профиля, включающего профиль температуры плавления как 3', так и 5'-концов последовательности, является аналитической методологией, позволяющей более надежно определять объект с направленной вставкой трансгена.
В общей сложности 1738 PAT-положительных образцов использовали в данном проекте. Анализ нарушения локуса и внутреннюю-внешнюю ПЦР проводили для всех объектов. Результаты показали, что 158/1738 объектов были положительными в отношении нарушения локуса и 46/1738 из этих объектов были положительными в реакциях внутренней-внешней ПЦР-амплификации как для 3', так и для 5'-областей.
Пример 4. Анализ целевых локусов в растениях кукурузы
Растения Zea mays сорта B104 трансформировали генным конструктом сконструированной посадочной площадки (pDAB105817 или pDAB105818), как описано ранее в патентной заявке США №2011/0191899. Получали трансформированные растения кукурузы и подтверждали, что они содержат ELP. Растения четырех ELP линий кукурузы: 105817[1]-015.Sx001.Sx011, 105818[1]-269.Sx001.Sx008, 105818[1]-271.Sx001.Sx005 и 105818[2]-388.Sx001.Sx008 скрещивали с растениями Zea mays сорта B104 для получения гемизигот. Полученные растения-потомки были совместно трансформированы либо eZFN плазмидой pDAB105941, кодирующей eZFN1, и соответствующей плазмидой донора pDAB104182, либо eZFN плазмидой pDAB105948, кодирующей eZFN8, и плазмидой донора pDAB104183. Трансформации осуществляли путем бомбардировки микрочастицами выделенных зародышей, проведенной один раз с использованием PDS-1000 (Bio-Rad) в соответствии с инструкциями производителя. В общей сложности 20896 зародышей (примерно 5000 зародышей для каждой целевой линии) подвергали бомбардировке и отбирали на устойчивость к биалафосу: 12404 подвергали совместной бомбардировке pDAB105941 и ее соответствующим донором, и 8492 зародышей подвергали совместной бомбардировке pDAB105948 и ее соответствующим донором.
После бомбардировки зародыши культивировали в среде и выращивали до стадии проростков. Трансгенные объекты определяли методом кПЦР, который был разработан для скрининга и обнаружения присутствия трансгена pat. Число копий определяли путем сравнения значений мишень/эталон (инвертаза) для неизвестных образцов (на выходе из LightCycler 480™) со значениями мишень/эталон стандартов с известным числом копий (1-копия: геми, 2-копии: гомо). Всего выжили 614 регенерированных растений, 354 (или 58%) растений были идентифицированы как положительные в отношении присутствия гена pat и оставлены для дальнейшего анализа.
Анализ нарушения локуса ELP: Был разработан анализ нарушения локуса с помощью ZFN для мониторинга изменений в интегрированном ELP. В не таргетированном ELP ПЦР-праймеры MAS621 и MAS622 (таблица 5) амплифицировали 214 п.н. продукт, охватывающий сайты связывания eZFN. Интегрирование (или модификация) в сайт связывания eZFN в локусе ELP нарушало бы амплификацию методом кПЦР с небольшим временем удлинения, что приводило бы либо к отсутствию сигнала, либо к значительному снижению сигнала, производимого в реакции кПЦР. Контрольную реакцию кПЦР для амплификации гена инвертазы также включали в качестве эталонного внутреннего контроля.
Для амплификации мастер-микс зондов LightCycler® 480 (Roche Applied Science, Indianapolis, IN) готовили в конечной концентрации 1X в объеме 10 мкл мультиплексной реакционной смеси, содержащей 0,4 мкМ каждого праймера и 0,2 мкМ каждого зонда. Проводили трехступенчатую реакцию амплификации с денатурацией в течение 10 секунд при 95°C, отжигом в течение 35 секунд при 60°C и 1 секундой при 72°C для приращения сигнала флуоресценции. Флуоресцентный фрагмент FAM возбуждался при оптической плотности 465/510 нм и HEX при 533/580 нм. Число копий определяли путем сравнения значений мишень/эталон (инвертаза) для неизвестных образцов (на выходе из LightCycler 480™) со значениями мишень/эталон известных однокопийных гемизигот.
Чтобы дифференцировать объекты со случайной вставкой от ELP-таргетированных объектов, 354 образца, которые были идентифицированы путем кПЦР-скрининга на ген pat, дополнительно анализировали, используя анализ нарушения локуса. Анализ нарушения ELP был разработан для мониторинга больших вставок/делеций в сайте расщепления eZFN. В не таргетированном ELP амплифицировался 214 п.н. ПЦР-продукт, охватывающий сайты связывания eZFN, и генерировал сильные флуоресцентные сигналы. Интегрирование (или модификация) в сайт связывания eZFN нарушало бы амплификацию и приводило бы либо к отсутствию сигнала, либо к значительному снижению уровней флуоресцентного сигнала, производимого в реакции кПЦР. Из 354 pat-положительных объектов примерно 8% (28 объектов), судя по всему, имели нарушения (фигура 8b), что указывало на потенциальный таргетинг.
Праймеры и зонды, используемые для анализа нарушения локуса
Внутренняя-внешняя ПЦР: Анализ нарушения локуса выявил изменения в области связывания eZFN на ELP. Любое изменение в сайтах связывания праймеров или случайные вставки в локусе являются возможными признаками нарушения в локусе, вызванного расщеплением ZFN. Далее использовали внутреннюю-внешнюю ПЦР для подтверждения присутствия донорской вставки в локусе ELP. Оба конца последовательностей областей соединения, включающих целевой локус и донора. Один праймер был разработан для отжига с предварительно интегрированной областью ELP, присутствующей только в целевых линиях, и второй праймер был разработан для отжига только с донорскими последовательностями ДНК, которые присутствовали только в конструкте донора. Амплификация методом ПЦР являлась свидетельством направленной вставки донора в геномный локус ELP. В случае любых объектов, полученных в результате случайных вставок, ПЦР-амплификация не происходила.
Для внутренней-внешней ПЦР 5'-области соединения донора/ELP был разработан прямой праймер для связывания области OsAct1 (5OsF3, SEQ ID NO: 23 ATTTCACTTTGGGCCACCTT) донорской вставки, при этом обратный праймер (5R3, SEQ ID NO: 24 AGGCTCCGTTTAAACTTGCTG) был разработан для связывания 193 п.н. последовательности, уникальной для целевой линии, в левом плече ELP. Для внутренней-внешней ПЦР 3'-области соединения донора/локуса ELP был разработан прямой праймер (3PAF1, SEQ ID NO: 25 ATGGTGGATGGCATGATGTT) для связывания в области PATv6 донорской вставки, и обратный праймер (3R1, SEQ ID NO: 26 TGGAGGTTGACCATGCTAGG) был разработан для связывания 192 п.н. последовательности, уникальной для целевой линии, в правом плече ELP. Амплификация имела место только если прямые и обратные праймеры связывались с последовательностями, находящимися в непосредственной близости друг от друга. Интегрированные случайным образом донорские последовательности нельзя было обнаружить с использованием вышеописанных ПЦР-праймеров. Для повышения производительности метода обнаружения внутренней-внешней ПЦР анализ кривой плавления проводили с использованием зеленого флуоресцентного красителя для нуклеиновых кислот, SYTO13®. ПЦР-амплификацию проводили, используя систему ПЦР в реальном времени LightCycler 480™, в 15 мкл реакционной среды, содержащей 0,75 единиц ДНК-полимеразы TaKaRa Ex Taq™ (Takara Bio Inc., Shiga, Japan), 200 нМ набора дНТФ, 200 нМ каждого из прямого и обратного праймеров, 2,67 мкМ SYTO13® и 10 нг геномной ДНК. Амплификацию начинали 2-минутным циклом денатурации при 95°C, затем 30 циклов при 98°C в течение 20 секунд, 60°C в течение 30 секунд и 68°C в течение 90 секунд, с последующим анализом кривой плавления при 97°C со скоростью линейного изменения температуры 0,11°C/с.
С помощью реакции ПЦР были проанализированы как 5', так и 3'-фланкирующие концы. Для объекта с направленной вставкой донора в локус ELP был получен 1,1 т.п.н. фрагмент для реакции внутренней-внешней ПЦР 5'-области и 1,4 т.п.н. фрагмент для реакции внутренней-внешней ПЦР 3'-области. Результаты реакций ПЦР определяли путем анализа кривой плавления, в котором получали различные графические результаты в зависимости от длины и состава ампликона (фигура 9). Короткие ПЦР-ампликоны, как правило, демонстрируют кривую температуры плавления (Tm) с одним пиком, которые выглядят как плоская линия с низкими уровнями флуоресцентного сигнала при графическом изображении. Но для длинных ампликонов (то есть, 1-2 т.п.н. фрагментов), профиль Tm выглядит более сложным, с несколькими пиками (в зависимости от локальных подпоследовательностей ампликонов) и высокими уровнями флуоресцентного сигнала. Пять объектов были идентифицированы как положительные в реакциях ПЦР как 5', так и 3'-области. В каждой из четырех целевых линий был образован объект, содержащий последовательность донора, вставленную в геномный локус ELP. Все положительные по результатам внутренней-внешней ПЦР объекты подвергали гель-электрофорезу, в котором они демонстрировали только одну полосу ПЦР-ампликона, как и ожидалось.
Молекулярное подтверждение: были использованы дополнительные методы молекулярной детекции для подтверждения того, что результаты анализа нарушения локуса и реакций внутренней-внешней ПЦР не были ложноположительными результатами. Выполняли саузерн-блотинг и секвенирование 5' и 3'-областей соединения донорской вставки/геномного локуса ELP. Результаты подтвердили, что объекты, идентифицированные в анализе нарушения локуса и в анализе внутренней-внешней ПЦР, содержали донорскую вставку в геномном локусе ELP.
Пример 5. Анализ нарушенных локусов в растениях кукурузы
Доставку ZFN в геномный локус целевой линии растений осуществляли, используя стратегию скрещивания растений, описанную ранее в патентной публикации США №20110191877. Отдельно целевой растительный объект и растительный объект с вырезающим фрагментом были получены на базе растений Zea mays сорта B104. Пять линий целевых растений были получены в результате трансформации конструктами pDAB105816, pDAB105817, pDAB105818, pDAB105820 и pDAB105821. Эти конструкты содержали пакет трансгенов, ген селективного маркера aad-1 и ELP, содержащий сайты связывания eZF1 и eZF8. Затем были получены две линии растений с вырезающим фрагментом в результате трансформации конструктами pDAB105828 и pDAB105825. Конструкт pDAB105828 содержал ZFN8 под управлением промотора убиквитина 1 Zea mays и заканчивался 3'UTR Per5 Zea mays. Конструкт pDAB105825 содержал ZFN1 под управлением промотора убиквитина 1 Zea mays и заканчивался 3'UTR Per5 Zea mays. Оба конструкта вырезающего фрагмента также содержали ген селективного маркера pat. Были получены трансгенные растения, что было подтверждено соответствующими молекулярными анализами. Растения подвергали самоопылению для получения гомозиготных потомков. Полученные гомозиготные целевой объект и объект с вырезающим фрагментом были скрещены, с получением потомков. Потомков анализировали для определения того, будет ли трансген ZFN, полученный от родительского объекта с вырезающим фрагментом расщеплять целевой локус ELP, полученный от другого родительского целевого объекта. Большую часть всех скрещиваний выполняли, используя растения целевых линий в качестве женских, и растения линий с вырезающим фрагментом в качестве мужских растений. Только одно контрольное скрещивание было проведено с использованием растений линии с вырезающим фрагментом в качестве женских, а растений целевой линии в качестве мужских растений. Целевые растения и растения с вырезающим фрагментом скрещивали для получения потомков, которые подвергали скринингу с применением Assure II™ (квизалофоп) (184 г кэ/га + 1% COC) и Ignite™ 280 SL (глюфозинат) (480 г кэ/га) на стадии развития V3. Всех выживших потомков отбирали для дальнейшего молекулярного анализа, который включал скрининг на наличие трансгена aad-1 методом кПЦР. Всего 1902 образца генотипировали на наличие локуса aad-1 анализом кПЦР с использованием гена инвертазы в качестве эталонного гена. Отношения мишени к эталону для aad-1 рассчитывали и нормировали на известные стандарты, при этом отношение, равное 2, 1 или 0 указывало на гомозиготность, гетерозиготность или на нулевой статус, соответственно. Было подтверждено, что 1822 растения являются гемизиготными по aad-1.
Анализ нарушения локуса ZFN: Анализ нарушения локуса, основанный на ПЦР, был разработан для непрямого измерения разрезающей активности ZFN в отношении целевого геномного локуса ELP. Анализы были разработаны таким образом, что флуоресцентно меченые зонды располагались поверх спейсера, необходимого для целостности функций ZFN (фигура 10). Анализ нарушения локуса eZFN1 приводил к обнаружению 69 п.н. фрагмента, покрывающего всю последовательность сайта связывания eZFN1. Анализ нарушения локуса eZFN8 приводил к обнаружению 109 п.н. фрагмента, фланкирующего последовательность сайта связывания eZFN8. В обоих анализах использовали зонды MGB, синтезированные в компании Life Technologies (Grand Island, NY). Когда ZFN расщепляли геномный локус ELP, разрыв восстанавливался за счет NHEJ, результатом чего являлось включение InDel в геномные последовательности, изменяющее геномную последовательность, которая была использована для разработки ПЦР-праймеров. Как следствие, любые реакции ПЦР-амплификации, разработанные для амплификации и обнаружения ампликона на протяжении последовательности связывания ZFN в геномном локусе ELP, не продуцировали флуоресцентный сигнал (поскольку геномные последовательности содержали делеции или перестановки и праймеры не могли связаться с этими геномными последовательностями).
Проводили биплексные анализы ПЦР в реальном времени или кПЦР с использованием системы LightCycler® 480 (Roche Applied Science, Indianapolis, IN). Контрольную реакцию проводили, используя ген инвертазы в качестве эндогенного эталонного гена. Для амплификации мастер-микс зондов LightCycler® 480 (Roche Applied Science, Indianapolis, IN) готовили в конечной концентрации 1X в объеме 10 мкл мультиплексной реакционной смеси, содержащей 0,4 мкМ каждого праймера и 0,2 мкМ каждого зонда (таблица 6). Проводили трехступенчатую реакцию амплификации, начиная с денатурации в течение 10 секунд при 95°C, затем отжиг в течение 35 секунд при 60°C и 1 секунда при 72°C для приращения сигнала флуоресценции. Результаты анализа на нарушение локуса анализировали, используя отношения мишени к эталону и проводя нормирование на известные гомозиготы. Результаты ПЦР-анализа приведены на фигуре 11.
Праймеры, используемые для обнаружения методом кПЦР
Для определения степени разрезания eZFN геномного локуса ELP образцы листьев F1 растений от скрещивания вначале анализировали на зиготность и затем тестировали на нарушение ELP с использованием кПЦР анализа, который позволяет обнаруживать интактные сайты связывания eZFN. Если геномный локус ELP подвергался InDel в процессе репарации ДЦР на сайте связывания eZFN, наблюдалось исчезновение или снижение детектируемого сигнала в кПЦР анализе. Нормированные отношения для ELP сравнивали с отношениями в сестринских линиях. Если отношение составляло 0-0,05, считали, что локусы были разрезаны ZFN (с неточной репарацией); если отношение составляло 0,05-0,4, локусы считали химерными, имея в виду, что не все копии ELP были разрезаны ZFN; если отношение было выше 0,4, считали, что локусы не были разрезаны ZFN (могли также быть разрезаны, но с правильной репарацией). Считая вместе случаи полного разрезания и химерные, активность eZFN1, обнаруженная в анализе нарушения локуса, составляла 46,6% (524 из 1125 растительных объектов) и активность eZFN8 составляла 70,2% (489 из 697 растительных объектов). (Таблица 7). Критерий Тьюки-Крамера выявил значительные различия среди потомков от скрещивания в отношении частоты расщепления. Сочетание линии L2BG и линии с вырезающим фрагментом оказалось решающим для успеха расщепления (p<0,0001).
Расщепляющие активности ZFN среди потомков 5 целевых ELP линий и линии с вырезающим фрагментом
Анализ последовательности, расщепляемой ZFN: Для подтверждения основанных на кПЦР данных о нарушении локуса ELP репрезентативные образцы от скрещивания потомков и два отрицательных контроля, представленных родительскими целевыми линиями, были выбраны для глубокого секвенирования ампликонов методом NGS. Прочтения высокого качества были выровнены против эталонной последовательности из конструкта ELP, и вставки и/или делеции (InDel) были идентифицированы. Как и ожидалось, две родительские линии имели очень незначительный процент (<0,1%) InDel в сайте расщепления ZFN при сравнении с эталонной последовательностью, скорее всего, вследствие ошибок ПЦР-амплификации и/или секвенирования (фигура 12). Существовала корреляция между данными кПЦР и секвенирования. В четырех скрещиваниях с наблюдаемой 100% эффективностью разрезания, исходя из данных кПЦР, наблюдали 91% или более модифицированных ELP при секвенировании. В итоге, данные глубокого секвенирования ампликонов методом NGS совпадали с данными кПЦР и подтверждали, что способ анализа нарушения локуса является высокочувствительным. Кроме того, как показано, анализ нарушения локуса ELP является эффективным анализом для оценки разрезающей активности ZFN (или любой другой сайт-специфической нуклеазы) в растениях.
Хотя аспекты данного изобретения описаны в некоторых вариантах осуществления, они могут быть дополнительно модифицированы в пределах сущности и объема данного изобретения. Вследствие этого, данная заявка должна включать любые изменения, варианты применения или адаптации вариантов осуществления изобретения, использующие его основные принципы. Кроме того, данная заявка должна включать такие отклонения от настоящего изобретения, которые находятся в пределах обычной практики в области, к которой данные варианты осуществления относятся и которые попадают в границы прилагаемой формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| БЫСТРЫЙ НАПРАВЛЕННЫЙ АНАЛИЗ СЕЛЬСКОХОЗЯЙСТВЕННЫХ КУЛЬТУР ДЛЯ ОПРЕДЕЛЕНИЯ ДОНОРНОЙ ВСТАВКИ | 2014 |
|
RU2668819C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ОПОСРЕДОВАННОЙ НУКЛЕАЗОЙ НАПРАВЛЕННОЙ ИНТЕГРАЦИИ ТРАНСГЕНОВ | 2013 |
|
RU2650819C2 |
| ФУНКЦИОНАЛЬНЫЕ ЛОКУСЫ FAD2 И СООТВЕТСТВУЮЩИЕ СПЕЦИФИЧНЫЕ ДЛЯ САЙТА-МИШЕНИ СВЯЗЫВАЮЩИЕСЯ БЕЛКИ, СПОСОБНЫЕ ИНДУЦИРОВАТЬ НАПРАВЛЕННЫЕ РАЗРЫВЫ | 2013 |
|
RU2656158C2 |
| ЛОКУСЫ FAD3 ДЛЯ ВЫПОЛНЕНИЯ ОПЕРАЦИЙ И СООТВЕТСТВУЮЩИЕ СВЯЗЫВАЮЩИЕСЯ СО СПЕЦИФИЧЕСКИМИ САЙТАМИ-МИШЕНЯМИ БЕЛКИ, СПОСОБНЫЕ К ВЫЗОВУ НАПРАВЛЕННЫХ РАЗРЫВОВ | 2013 |
|
RU2665811C2 |
| ОБОГАЩЕНИЕ АКТИВИРУЕМОЙ ФЛУОРЕСЦЕНЦИЕЙ СОРТИРОВКИ КЛЕТОК (FACS) ДЛЯ СОЗДАНИЯ РАСТЕНИЙ | 2013 |
|
RU2679510C2 |
| УНИВЕРСАЛЬНАЯ ДОНОРНАЯ СИСТЕМА ДЛЯ НАПРАВЛЕННОГО ВОЗДЕЙСТВИЯ НА ГЕНЫ | 2014 |
|
RU2687369C2 |
| СКОНСТРУИРОВАННАЯ СПОСОБАМИ ИНЖЕНЕРИИ ПЛАТФОРМА ДЛЯ ВСТРАИВАНИЯ ТРАНСГЕНА (ETIP) ДЛЯ НАЦЕЛИВАНИЯ ГЕНОВ И СТЭКИНГА ПРИЗНАКОВ | 2013 |
|
RU2666916C2 |
| ЛОКУСЫ ФУНКЦИОНАЛЬНОСТИ FAD2 И СООТВЕТСТВУЮЩИЕ СПЕЦИФИЧНЫЕ К УЧАСТКУ-МИШЕНИ СВЯЗЫВАЮЩИЕ БЕЛКИ, СПОСОБНЫЕ ИНДУЦИРОВАТЬ НАПРАВЛЕННЫЕ РАЗРЫВЫ | 2013 |
|
RU2656159C2 |
| ОПТИМАЛЬНЫЕ ЛОКУСЫ СОИ | 2014 |
|
RU2719150C2 |
| НАПРАВЛЕННАЯ МОДИФИКАЦИЯ МАЛАТДЕГИДРОГЕНАЗЫ | 2013 |
|
RU2658437C2 |

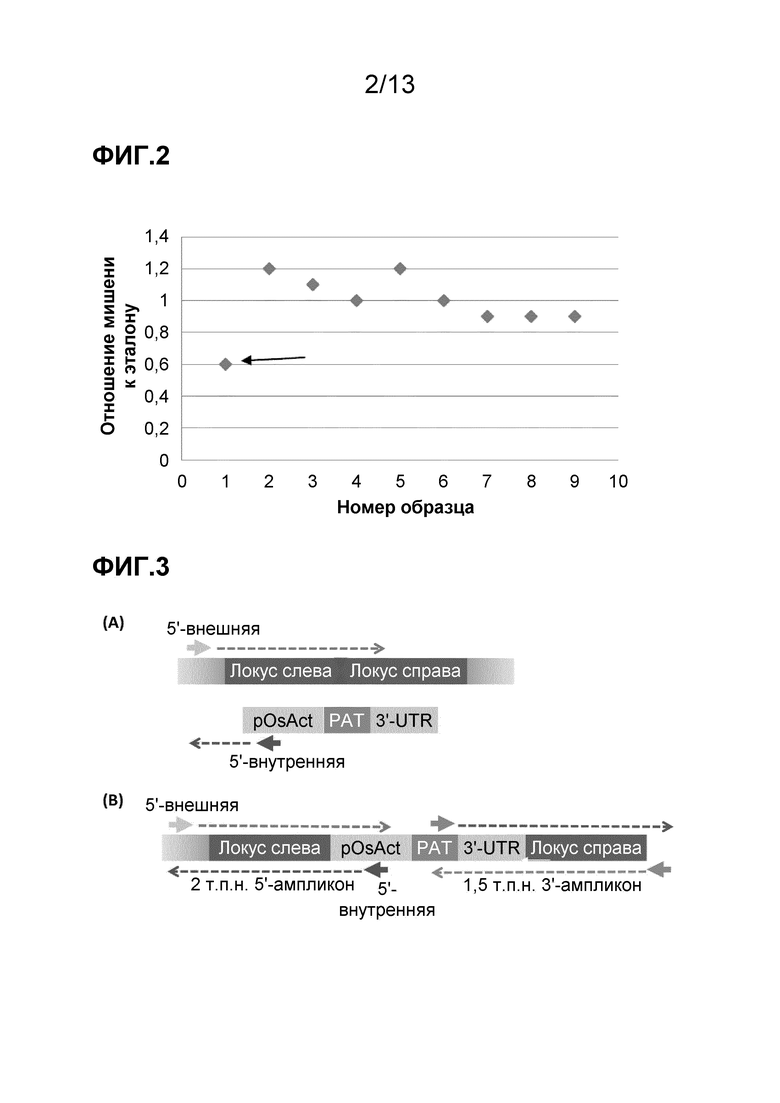

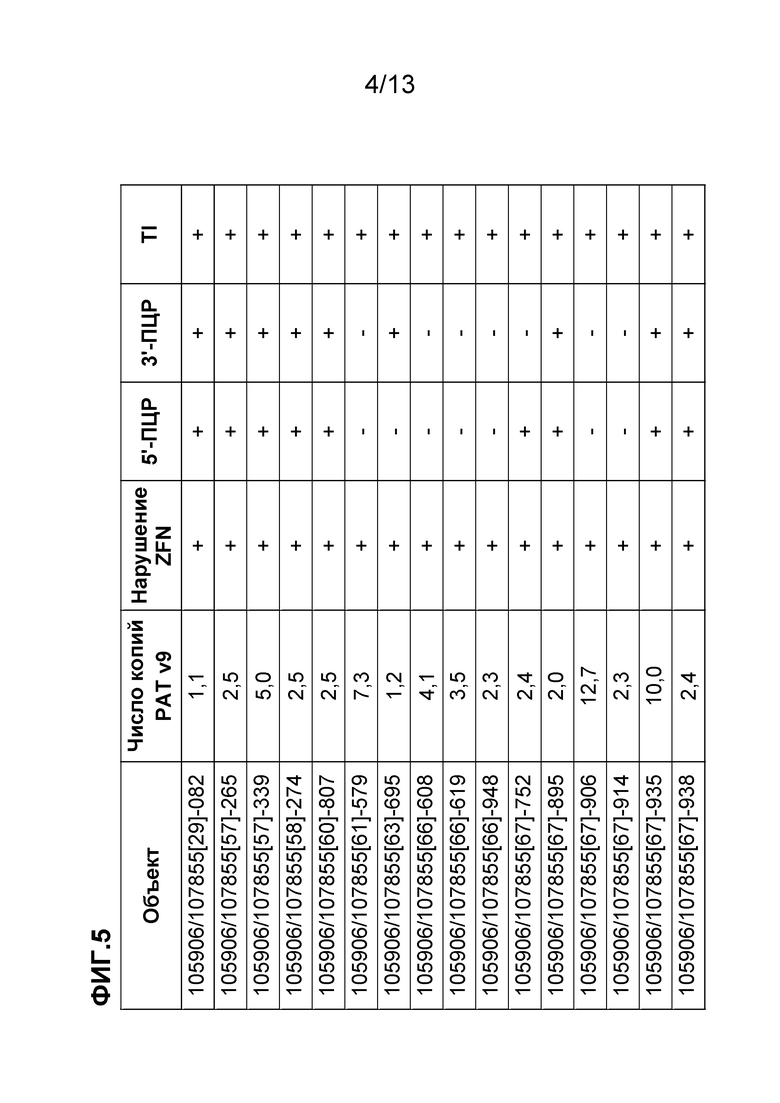
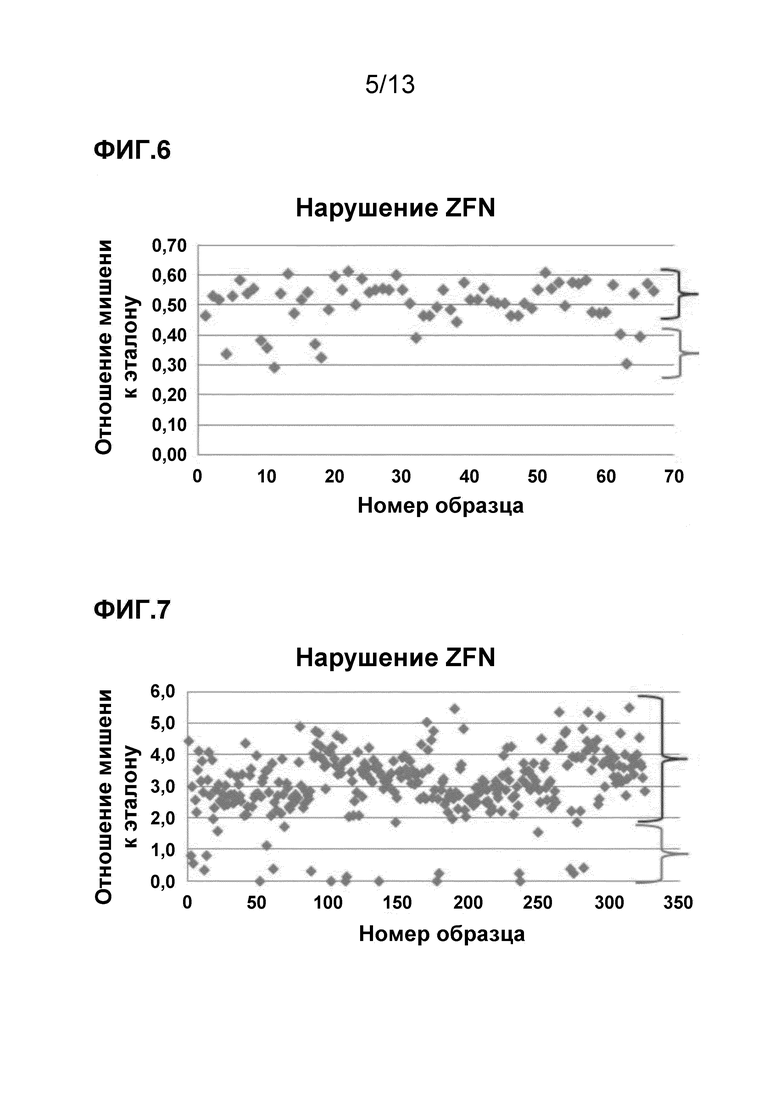
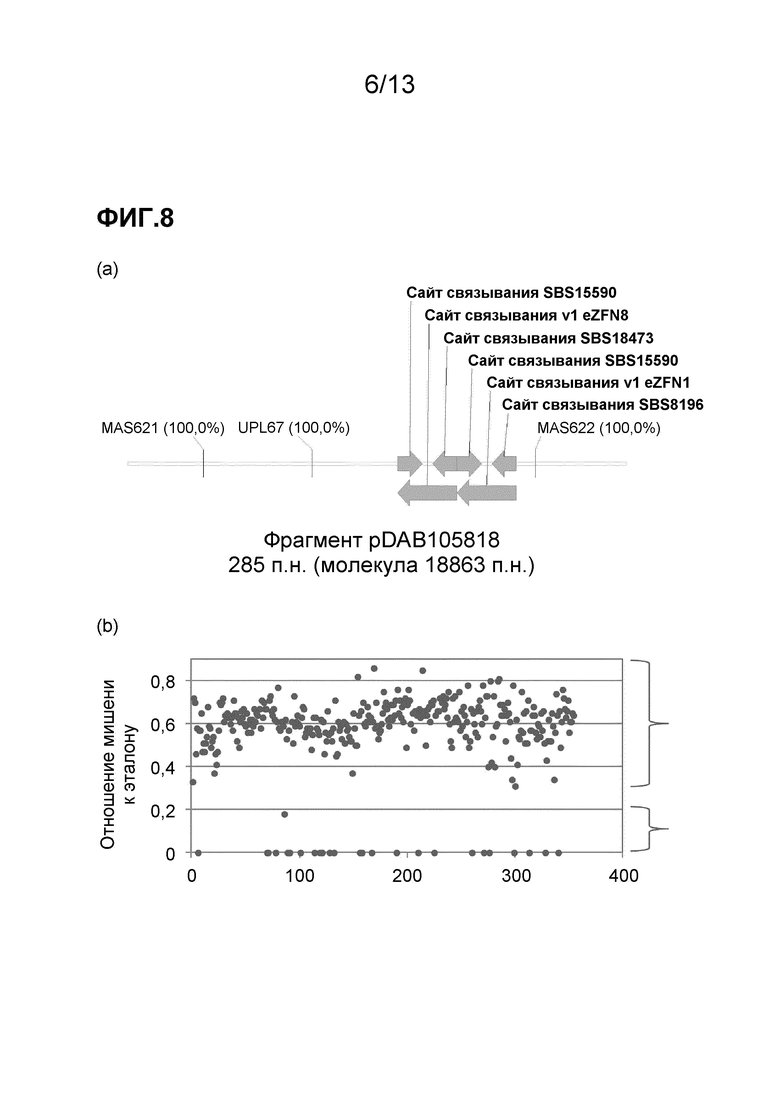
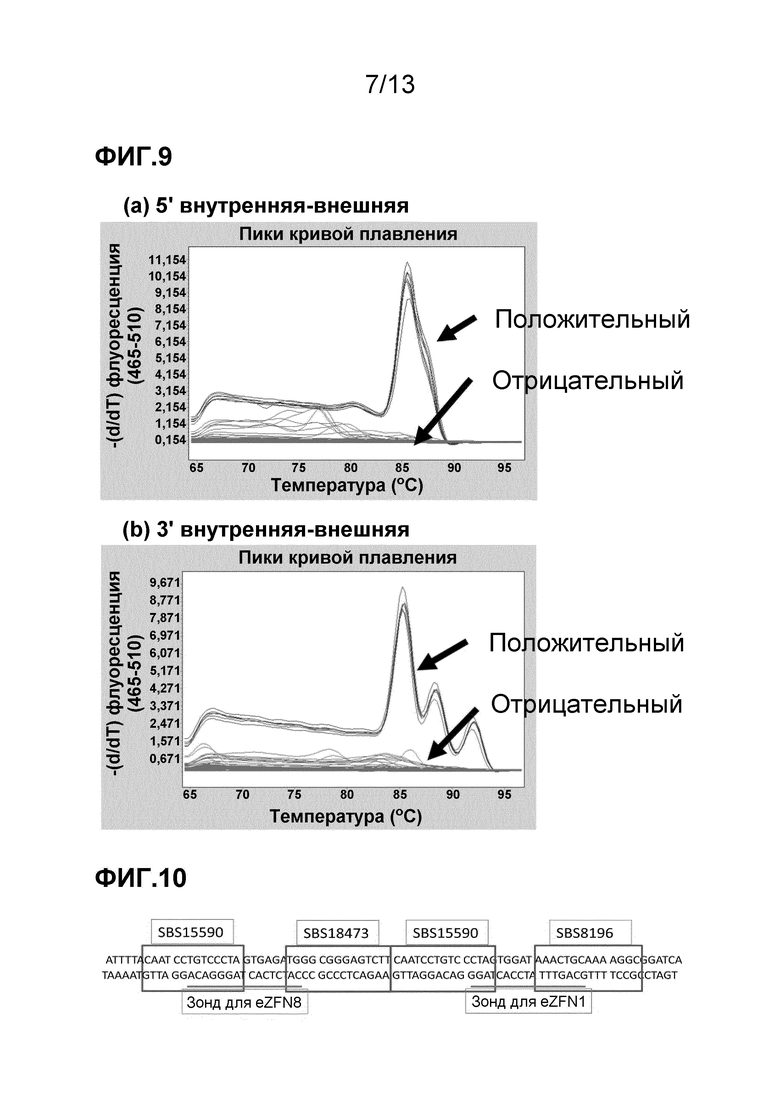






Изобретение относится к области биохимии, в частности к способу определения присутствия экзогенного донорского полинуклеотида ДНК, вставленного в целевой геномный локус DAS-59132 растения кукурузы. Вышеуказанный способ включает: амплификацию образца геномной ДНК, содержащего целевой геномный локус, с использованием набора олигонуклеотидов, имеющих SEQ ID NO: 1-5, для получения первого ампликона, содержащего целевой геномный локус, и обнаружение наличия или отсутствия первого ампликона, причем отсутствие первого ампликона указывает на присутствие донорского полинуклеотида ДНК в целевом геномном локусе. Изобретение позволяет определять присутствие экзогенного донорского полинуклеотида ДНК в целевом геномном локусе DAS-59132 с высокой эффективностью. 7 з.п. ф-лы, 12 ил., 7 табл., 5 пр.
1. Способ определения присутствия экзогенного донорского полинуклеотида ДНК, вставленного в целевой геномный локус DAS-59132 растения кукурузы, включающий:
a) амплификацию в первой реакции амплификации образца геномной ДНК, содержащей целевой геномный локус, с использованием первого набора олигонуклеотидов, имеющих SEQ ID NO:1-5, которые связываются в условиях гибридизации в непосредственной близости от целевого геномного локуса, для получения, таким образом, первого ампликона, содержащего целевой геномный локус; и
b) обнаружение наличия или отсутствия первого ампликона, при этом отсутствие первого ампликона указывает на присутствие донорского полинуклеотида ДНК в целевом геномном локусе,
где донорский полинуклеотид ДНК представляет собой донорский конструкт, содержащий кодирующую последовательность РАТ, придающую устойчивость к гербицидам,
где геномный локус расщепляют сайт-специфической нуклеазой на основе цинковых пальцев, направленной на последовательности, содержащие геномный локус DAS-59132.
2. Способ по п. 1, дополнительно включающий:
a) амплификацию во второй реакции амплификации образца геномной ДНК с использованием второго набора олигонуклеотидов, имеющих SEQ ID NO:6-9, которые связываются в условиях гибридизации в непосредственной близости от целевого геномного локуса и в пределах донорского полинуклеотида ДНК, для получения, таким образом, второго ампликона, содержащего по меньшей мере часть целевого геномного локуса и по меньшей мере часть донорского полинуклеотида ДНК; и
b) обнаружение наличия или отсутствия второго ампликона, при этом наличие второго ампликона указывает на присутствие донорского полинуклеотида ДНК в целевом геномном локусе.
3. Способ по п. 2, дополнительно включающий:
a) количественное определение результатов первой реакции амплификации;
b) количественное определение результатов второй реакции амплификации;
c) сравнение результатов первой и второй реакций амплификации; и
d) определение присутствия или отсутствия донорского полинуклеотида ДНК в целевом геномном локусе, при этом подтверждением вставки донорского полинуклеотида ДНК в целевой геномный локус является отсутствие первого ампликона и наличие второго ампликона,
необязательно дополнительно включающий мультиплексную реакцию, когда первую и вторую реакции амплификации проводят в одной пробирке или лунке,
где количественное определение результатов первой и второй реакций амплификации включает получение сигнатурного профиля для одной или обеих из первой и второй реакций амплификации,
где сигнатурный профиль выбран из группы, состоящей из сигнатурного профиля кривой температуры плавления и сигнатурного профиля флуоресценции, или
где сигнатурный профиль получают от интеркалирующего красителя ДНК,
где интеркалирующий краситель ДНК включает цианиновый краситель,
где цианиновый краситель используют в реакции амплификации в концентрации менее 4 мкМ, или
где цианиновый краситель используют в реакции амплификации в концентрации менее 2,7 мкМ, или
где сигнатурный профиль получают от флуоресцентного красителя.
4. Способ по п. 1, дополнительно включающий:
a) выбор трансгенного объекта, содержащего донорский полинуклеотид ДНК в целевом геномном локусе.
5. Способ по п. 1, отличающийся тем, что амплификация включает амплификацию в полимеразной цепной реакции.
6. Способ по п. 2, отличающийся тем, что второй ампликон содержит 5’-область соединения донорского полинуклеотида ДНК и целевого геномного локуса,
где второй ампликон содержит 3’-область соединения донорского полинуклеотида ДНК и целевого геномного локуса.
7. Способ по п. 1, отличающийся тем, что донорский полинуклеотид ДНК содержит по меньшей мере одну генную экспрессионную кассету.
8. Способ по п. 1 или 2, отличающийся тем, что первый или второй набор олигонуклеотидов или оба содержат флуоресцентный краситель,
где флуоресцентный краситель выбирают из группы, состоящей из флуоресцентного красителя HEX, флуоресцентного красителя FAM, флуоресцентного красителя JOE, флуоресцентного красителя TET, флуоресцентного красителя Cy 3, флуоресцентного красителя Cy 3,5, флуоресцентного красителя Cy 5, флуоресцентного красителя Cy 5,5, флуоресцентного красителя Cy 7 и флуоресцентного красителя ROX.
| Колосоуборка | 1923 |
|
SU2009A1 |
| MAO ET AL | |||
| "Characterization of EvaGreen and the implication of its physicochemical properties for qPCR applications", BMC BIOTECHNOLOGY, vol | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Аппарат, предназначенный для летания | 0 |
|
SU76A1 |
| CARROLL D | |||
| "A CRISPR Approach to Gene Targeting", MOLECULAR THERAPY, vol | |||
| Прибор для промывания газов | 1922 |
|
SU20A1 |
| Металлический ключ для пчеловодов | 1924 |
|
SU1658A1 |
| ЛУТОВА Л.А | |||
| Биотехнология высших растений, Издательство С.-Петербургского университета, 2010, стр | |||
| Способ крашения тканей | 1922 |
|
SU62A1 |
Авторы
Даты
2019-01-22—Публикация
2013-12-13—Подача