Перекрестная ссылка на родственные заявки
Для данной заявки испрашивается приоритет по предшествующей предварительной заявке на патент США, серийный номер 61/328,723, зарегистрированной 28 апреля 2010 г., предварительной заявке на патент США, серийный номер 61/411,071, зарегистрированной 8 ноября 2010 г., и предварительной заявке на патент США, серийный номер 61/435,939, зарегистрированной 25 января 2011 г., содержание которых полностью включено в настоящий документ в качестве ссылки.
Уровень техники
Давно осуществляются поиски способа целевой доставки лекарственного средства, при которой препарат (например, лекарственное или терапевтическое средство) предусмотрен в активном состоянии для конкретного типа клетки или ткани при эффективной концентрации. Для достижения этой цели необходимо преодолеть множество трудностей. Например, препарат сначала необходимо доставить в целевое место. Основные способы доставки, используемые в настоящее время, включают пероральный способ введения и инъекции. Однако инъекции болезненны, и оба способа имеют тенденцию обеспечивать пиковую, а не предпочтительную распределенную доставку препаратов. Кроме того, организм человека выработал множество систем, предотвращающих поступление посторонних веществ, например, ферментативное расщепление в желудочно-кишечном тракте, структурные компоненты которого предотвращают всасывание через эпителий, печеночный клиренс и иммунный ответ и реакция на инородное тело.
За длительное время при попытке обеспечить безболезненный способ доставки активных препаратов разработаны материалы для трансдермальной доставки. Для успешного решения проблемы трансдермальная структура должна обеспечивать доставку препарата через эпидермис, который связан с первичной функцией выведения инородных веществ. Внешний слой эпидермиса, роговой слой, обладает структурной прочностью, обеспечиваемой наложением рогоцитов и перекрестно-сшитых волокон кератина, удерживаемых вместе корнеодесмосомами и внедренных в липидную матрицу, которые все вместе обеспечивают превосходную барьерную функцию. Под роговым слоем находится зернистый слой, в пределах которого между кератоцитами сформированы плотные контакты. Плотные контакты представляют собой барьерные структуры, которые включают сеть трансмембранных белков, окруженных примыкающими плазменными мембранами (например, клаудины, окклюдины и молекулы адгезивного контакта), а также многочисленных белков, образующих бляшки (например, ZO-1, ZO-2, ZO-3, цингулин, симплекин). Плотные контакты обнаружены во внутреннем эпителии (например, кишечный эпителий, гематоэнцефалический барьер), а также в зернистом слое кожи. Под роговым слоем и зернистым слоем расположен средний слой кожи stratum spinosum. Средний слой кожи включает клетки Лангерганса, которые представляют собой дендритные клетки, которые могут стать полностью функциональными представляющим антиген клетками и могут устанавливать иммунный ответ и/или реакцию на инородное тело на поступающий препарат.
Несмотря на трудности преодоления естественных ограничений, достигнут прогресс в доставке активных препаратов, например, путем трансдермальной доставки.
К сожалению, способы трансдермальной доставки в настоящее время ограничены препаратами с низкой молекулярной массой, которые обладают умеренной липофильностью и не имеют заряда. Даже при успешно преодолении естественного ограничения, все еще существует проблема в отношении поддержания уровня активности доставляемых препаратов и устранения их реакции на инородное тело и иммунного ответа.
Этот способ доставки улучшен за счет вспомогательных способов для облегчения трансдермальной доставки активных препаратов. Например, обнаружено, что устройства с микроиглами пригодны для транспортировки вещества в или через кожу. В основном, устройство с микроиглами содержит массив игл, которые могут проникать через роговой слой кожи и достигать лежащего ниже слоя. Примеры устройств с микроиглами описаны в патенте США №6,334,856, Allen, et al., и патенте США №7,226,439, Prausnitz, et al., которые включены в настоящий документ в качестве ссылки. Однако, как указано выше, трансдермальная доставка представляет дополнительные трудности после барьерного рогового слоя. В частности, когда препарат доставлен в целевую область, все-таки необходимо, чтобы происходило правильное использование без деструкции препарата или инициации иммунного ответа. Например, стимуляция эндоцитоза активного препарата, направленного во внутреннюю часть клетки, представляет определенную трудность.
Исследования привели к пониманию мира молекул, в котором происходит доставка, при попытке преодолеть такие проблемы. Например, обнаружено, что хитозан эффективно размыкает плотные контакты в кишечном эпителии (см., например, Sapra, et al. AAPS Pharm. Sci. Tech., 10(1), March, 2009; Kaushal, et al., Sci. Pharm., 2009; 77; 877-897), и предлагается доставка активных препаратов посредством эндоцитоза меченых наночастиц (см., например, патенты США №№7,563,451, Lin, et al. и 7,544,770, Havnie). Кроме того, обнаружено, что нанотопография поверхности, примыкающей к клетке, влияет на характеристики адгезии между ними, а также на характеристики клетки, включая морфологию, подвижность, структуру клеточного скелета, пролиферацию и дифференциацию (см., например, Hart, et al., European Cells and Materials, Vol.10, Suppl. 2, 2005; Lim, et al. J R Soc Interface, March 22, 2005, 2(2). 97-108; Yim, et al. Biomaterials, September, 2005, 26(26), 5405-5413). Это первоначальное исследование было продолжено изучением нанотопографии опорных субстратов для использования в тканевой инженерии (см., например, заявки на патенты США №2008/0026464, Borenstein, et al. и №2008/0311 172, Schapira, et al.).
Несмотря на описанный выше прогресс в этой области, существует дальнейшая возможность для усовершенствования. Например, были бы предпочтительны устройства и способы, которые обеспечивают эффективную доставку активных препаратов, снижая при этом потенциальный иммунный ответ и реакцию на инородное тело, как для устройства доставки, так и для доставляемых препаратов.
Сущность изобретения
По одному варианту осуществления настоящего изобретения предлагается медицинское устройство, которое содержит массив микроигл, выступающих наружу из опоры. По меньшей мере одна из микроигл содержит множество наноструктур, сформированных на ее поверхности, наноструктуры образуют заранее определенный узор.
По другому варианту осуществления настоящего изобретения предлагается способ доставки лекарственного соединения в субдермальную область. Способ включает проникновение через роговой слой микроиглы, которая представляет собой канал текучей среды для лекарственного соединения, микроигла содержит множество наноструктур, сформированных на ее поверхности и образующих узор; и транспортировку лекарственного соединения через микроиглу и через роговой слой.
В другом варианте осуществления настоящего изобретения предлагается медицинское устройство, которое содержит множество структур наноразмера, которые созданы на поверхности и образуют изготовленную нанотопографию. Также предлагается способ создания медицинского устройства, который включает создание узора из наноструктур на поверхности микроиглы.
Краткое описание чертежей
Полное и всесторонне описание сущности изобретения, включая его предпочтительный режим, предназначенное для специалистов в этой области, изложено более подробно далее в описании со ссылкой на приложенные чертежи, на которых:
На фиг.1 показан один вариант осуществления устройства с микроиглами.
На фиг.2 показан другой вариант осуществления устройства с микроиглами.
На фиг.3 показан один вариант осуществления микроиглы, содержащей поверхность, образующую нанотопографию, которая может взаимодействовать с внеклеточной матрицей (ECM).
На фиг.4 показан один вариант осуществления сложного узора, который может быть сформирован на поверхности микроиглы.
На фиг.5 показан узор, включающий несколько повторений сложного узора по фиг.4.
На фиг.6 показан треугольный фрактал Серпинского.
На фиг.7А-7Г показаны нанотопография со сложным фракталом и фракталоподобная нанотопография.
На фиг.8 показан другой сложный узор, который может быть сформирован на поверхности микроиглы.
На фиг.9 показан пример плотности размещения, которое может быть использовано для структур наноразмера, описанных в настоящем документе и образующих узор с упаковкой в квадрате (фиг.9А), узор с гексагональной упаковкой (фиг.9Б) и узор с круговой упаковкой (фиг.9В).
На фиг.10 показан способ определения TEER слоя клеток.
На фиг.11А-11В схематично показан способ нанесения нанорельефа давлением, который может быть использован в одном варианте осуществления при формировании устройства.
На фиг.12 схематично показан один вариант осуществления устройства.
На фиг.13 показан вид в перспективе одного варианта осуществления трансдермального пластыря перед доставкой лекарственного соединения.
На фиг.14 показан вид спереди пластыря по фиг.13.
На фиг.15 показан вид в перспективе пластыря по фиг.13, в котором отсоединяемый элемент частично удален с пластыря.
На фиг.16 показан вид спереди пластыря по фиг.13.
На фиг.17 показан вид в перспективе трансдермального пластыря по фиг.13 после удаления отсоединяемого элемента и во время использования.
На фиг.18 показан вид спереди пластыря по фиг.17.
На фиг.19 показан вид в перспективе другого варианта осуществления трансдермального пластыря перед доставкой лекарственного соединения.
На фиг.20 показан вид спереди пластыря по фиг.19.
На фиг.21 показан вид в перспективе пластыря по фиг.19, в котором отсоединяемый элемент частично отодран от пластыря.
На фиг.22 показан вид спереди пластыря по фиг.21.
На фиг.23 показан вид в перспективе пластыря по фиг.19, в котором отсоединяемый элемент полностью отодран от пластыря.
На фиг.24 показан вид в перспективе трансдермального пластыря по фиг.19 после удаления отсоединяемого элемента и во время использования.
На фиг.25А-25Д показаны несколько узоров нанотопографии, описанных в настоящем документе.
На фиг.26 показано изображение сканирующего электронного микроскопа пленки, содержащей поверхность с наноузором.
На фиг.27А и 27Б показаны два изображения сканирующего электронного микроскопа пленки, содержащей поверхность с другим наноузором.
На фиг.28 показано изображение сканирующего электронного микроскопа пленки, содержащей поверхность с другим наноузором.
На фиг.29 показано изображение сканирующего электронного микроскопа пленки, содержащей поверхность с другим наноузором.
На фиг.30 показано изображение сканирующего электронного микроскопа пленки, содержащей поверхность с другим наноузором.
На фиг.31 показано изображение сканирующего электронного микроскопа пленки, содержащей поверхность с другим наноузором.
На фиг.32 показано изображение сканирующего электронного микроскопа пленки, содержащей поверхность с другим наноузором.
На фиг.33 показано изображение сканирующего электронного микроскопа пленки, содержащей поверхность с другим наноузором.
На фиг.34 показано изображение сканирующего электронного микроскопа пленки, содержащей поверхность с другим наноузором.
На фиг.35 графически показан эффект повышения проницаемости для альбумина бычьей сыворотки (BSA) в монослое клеток на пленках полистирола со сформированным наноузором, описанным в настоящем документе.
На фиг.36А и 36Б графически показан эффект повышения проницаемости для иммуноглобулина-G (IgG) в монослое клеток на пленках полистирола со сформированным наноузором, описанным в настоящем документе.
На фиг.37А и 37Б показаны 3D живые/неподвижные изображения с окрашиванием флуоресцеином, иллюстрирующие параклеточный и трансклеточный транспорт иммуноглобулина-G через монослой клеток на поверхности пленки полистирола с узором, описанным в настоящем документе.
На фиг.38 графически показан эффект повышения проницаемости для BSA в монослое клеток на поверхности пленок полипропилена со сформированным наноузором, описанным в настоящем документе.
На фиг.39 графически показан эффект повышения проницаемости для иммуноглобулина-G в монослое клеток на поверхности пленок полипропилена со сформированным наноузором, описанным в настоящем документе.
На фиг.40А и 40Б показаны 3D живые/неподвижные изображения с окрашиванием флуоресцеином, иллюстрирующие параклеточный транспорт иммуноглобулина-G через монослой клеток на поверхности пленок полипропилена со сформированным узором, описанным в настоящем документе.
На фиг.41А-41Е показаны изображения сканирующего электронного микроскопа (SEM) культуры клеток на поверхностях с наноузором, описанным в настоящем документе.
На фиг.42 показан эффект повышения проницаемости для этанерцепта в монослое клеток на пленках полипропилена или полистирола со сформированным наноузором, описанным в настоящем документе.
На фиг.43 показано повышение проницаемости этанерцепта слоя клеток с последующими двумя часами контакта с пленками полипропилена или полистирола со сформированным наноузором, описанным в настоящем документе.
На фиг.44 показан массив микроигл, содержащий поверхностный слой, с образованным на нем узором из наноструктур.
На фиг.45 показана одна микроигла массива по фиг.44.
На фиг.46 графически показан профиль фармакокинетики белкового терапевтического средства, доставляемого устройством, описанным в настоящем документе.
На фиг.47А и 47Б показаны изображения в сечении кожи с последующей трансдермальной доставкой белкового терапевтического средства через кожу. На фиг.47А показан вид в сечении кожи, находящейся в контакте с трансдермальным устройством, образующим на ней нанотопографию, и на фиг.47Б показан вид в сечении кожи, находящейся в контакте с трансдермальным устройством, не содержащим сформированного на нем узора нанотопографии.
На фиг.48 графически показана концентрация в сыворотке крови белкового терапевтического средства, доставляемого устройством, описанным в настоящем документе.
Подробное описание репрезентативных вариантов осуществления
Далее подробно описаны различные варианты осуществления, раскрывающие сущность изобретения, один или более примеров которого пояснены далее.
Каждый пример подразумевает пояснение, а не ограничение. Действительно, для специалистов в этой области очевидно, что различные модификации и изменения могут быть внесены в настоящее описание без отступления от объема и сущности настоящего изобретения. Например, особенности, показанные или описанные, как часть одного варианта осуществления, могут быть использованы в другом варианте осуществления, чтобы получить еще один вариант осуществления. Таким образом, подразумевается, что настоящее изобретение охватывает такие модификации и изменения, как входящие в объем заявленной формулы изобретения и ее эквивалентов.
В настоящем документе предлагается медицинское устройство, которое содержит узор изготовленных на поверхности структур, по меньшей мере участок которых изготовлен в масштабе нанометров. Используемый в настоящем документе термин "изготовленный" в основном относится к структуре, которая специально разработана, создана или сконструирована для существования у поверхности медицинского устройства и не выровнена с особенностями поверхности, которые являются просто случайным результатом процесса формирования устройства. Таким образом, на поверхности микроигл существует заранее определенный узор из наноструктур.
Медицинское устройство может быть сконструировано из различных материалов, включая металлы, керамику, полупроводники, органические вещества, полимеры и т.д., а также их композиты. Например, могут быть использованы нержавеющая сталь фармацевтической категории, титан, никель, железо, золото, олово, хром, медь, сплавы этих или других металлов, кремний, диоксид кремния и полимеры. Обычно устройство изготовлено из биосовместимого материала, который способен удерживать узор из структур, описанных в настоящем документе, на поверхности. Термин "биосовместимый" в основном относится к материалу, который по существу не оказывает вредного влияния на клетки или ткани в области, в которую доставляется устройство. Также подразумевается, что этот материал не вызывает каких-либо значительных нежелательных с медицинской точки зрения эффектов в какой-либо другой области живого организма. Биосовместимые материалы могут быть синтетическими или натуральными. Некоторые примеры подходящих биосовместимых материалов, которые также являются поддающимися биологическому разложению, включают полимеры гидроксикислот, таких как оксипропионовая кислота и полилактид гликолевой кислоты, полигликолид, полилактид-ко-гликолид, сополимеры с полиэтиленгликолем, полиангидриды, сложные поли(ортоэфиры), полиуретаны, полимасляная кислота, поливалериановая кислота и полилактид-ко-капролактон. Другие подходящие материалы могут включать, без ограничения, поликарбонат, полиметакриловую кислоту, этиленвинилацетат, политетрафторэтилен и сложные полиэфиры. Устройство аналогично может быть непористым или пористым по своей природе, может быть однородным или неоднородным по всему устройству в отношении материалов, геометрии, цельности и т.д., и может иметь жестко фиксированную или полуфиксированную форму.
Что касается используемых материалов, медицинское устройство может быть использовано для взаимодействия с тканью, например, при доставке биоактивного препарата в клетку. Например, медицинское устройство может быть использовано для доставки препарата в ткань или к одному или более типам клеток ткани, для структурной поддержки ткани, для удаления участка или компонента ткани и т.д. Медицинское устройство может быть использовано в одном варианте осуществления для транспорта вещества через один или несколько слоев кожи. Во время использования устройство может взаимодействовать с окружающими биологическими компонентами и регулировать или моделировать (т.е. изменять) внутриклеточную и/или межклеточную сигнальную трансдукцию, связанную с взаимодействиями между клетками, эндоцитозом, воспалительной реакцией и т.д. Например, посредством взаимодействия между нанотопографией на поверхности медицинского устройства и окружающими биологическими материалами или структурами устройство может регулировать и/или модулировать трансмембранный потенциал, мембранные белки и/или межклеточные контакты (например, плотные контакты, щелевые контакты и/или десмосомы). Устройство может быть использовано для трансдермальной доставки препаратов или удаления веществ, не вызывая реакцию на инородное тело или иммунный ответ.
В одном варианте осуществления устройство представляет собой микроиглу или массив микроигл, хотя следует понимать, что устройства не ограничиваются микроиглами. Микроиглы могут использоваться при транспорте вещества через биологические барьеры, такие как кожа, гематоэнцефалический барьер, ткани слизистой оболочки, кровеносные и лимфатические сосуды и т.д. На фиг.1 показано типичное устройство 10 с микроиглами. Как можно видеть, устройство содержит массив отдельных игл 12, каждая из которых сформирована с размером и формой, позволяющими проникать через биологический барьер без поломки отдельных микроигл. Микроиглы могут быть сплошными, как на фиг.1, пористыми, или могут содержать полый участок. Микроигла может содержать полый участок, например, круглый канал, который может продолжаться через всю или участок иглы, продолжаясь параллельно направлению иглы или ответвляясь или выходя вбок от иглы, если это необходимо. Например, на фиг.2 показан массив микроигл 14, каждая из которых содержит канал 16 в боковой стороне иглы, которые могут быть использованы, например, для доставки препарата в субдермальную область. Например, канал 16 может быть, по меньшей мере, частично совмещен с отверстием в основании 15, чтобы создавать контакт между отверстием и каналом 16, обеспечивая прохождение вещества через канал 16.
Размеры канала 16, если он имеется, могут быть выбраны специально, чтобы вызвать в капилляре течение лекарственного соединения. Течение в капилляре в основном возникает, когда силы смачивания текучей средой стенок канала больше, чем силы сцепления между молекулами жидкости. В частности, внутрикапиллярное давление обратно пропорционально размерам в сечении канала 16 и прямо пропорционально поверхностному натяжению жидкости, умноженному на косинус краевого угла контакта текучей среды с материалом, образующим канал. Таким образом, чтобы облегчить течение в капилляре в пластыре, размер в сечении (например, ширина, диаметр и т.д.) канала 16 можно задавать по выбору, причем меньшие размеры приводят к более высокому внутрикапиллярному давлению. Например, в некоторых вариантах осуществления размер в сечении канала обычно составляет в диапазоне от примерно 1 до примерно 100 микрометров, в некоторых вариантах осуществления от примерно 5 до примерно 50 микрометров и в некоторых вариантах осуществления от примерно 10 до примерно 30 микрометров. Этот размер может быть постоянным, или он может меняться в зависимости от длины канала 16. Длина канала также может меняться для соответствия разным объемам, скорости потока и времени задержки для лекарственного соединения. Например, длина канала может составлять от примерно 10 до примерно 800 микрометров, в некоторых вариантах осуществления от примерно 50 до примерно 500 микрометров, и в некоторых вариантах осуществления от примерно 100 до примерно 300 микрометров. Площадь сечения канала также может быть различна. Например, площадь в сечении может составлять от примерно 50 до примерно 1000 квадратных микрометров, в некоторых вариантах осуществления от примерно 100 до примерно 500 квадратных микрометров и в некоторых вариантах осуществления от примерно 150 до примерно 350 квадратных микрометров. Кроме того, отношение размеров (длина/размер в сечении) канала могут составлять в диапазоне от примерно 1 до примерно 50, в некоторых вариантах осуществления от примерно 5 до примерно 40 и в некоторых вариантах осуществления от примерно 10 до примерно 20. В случаях, когда размер в сечении (например, ширина, диаметр и т.д.) и/или длина меняется в зависимости от длины, отношение размеров может быть определено по средним размерам.
Следует понимать, что число микроигл, показанных на чертежах, предназначено только для целей иллюстрации. Фактическое число микроигл, используемых для сборки микроигл, может, например, составлять в диапазоне от примерно 500 до примерно 10000, в некоторых вариантах осуществления от примерно 2000 до примерно 8000 и в некоторых вариантах осуществления от примерно 4000 до примерно 6000.
Отдельная микроигла может быть прямой или с кончиком конической формы. В одном варианте осуществления диаметр микроиглы может быть максимальным у конца основания микроиглы и суженным на конус на удаленном от основания конце. Микроигла также может быть изготовлена с трубкой, которая содержит и прямой (без сужения), и конический участок.
Микроигла может быть сформирована с трубкой, которая является круглой или некруглой в сечении. Например, сечение микроиглы может быть многоугольным (например, в форме звезды, квадрата, треугольника), вытянутым или любой другой формы. Трубка может иметь одно или более отверстий или каналов.
Размер отдельных игл может быть оптимизирован в зависимости от нужной глубины конусности, требований к прочности иглы во избежание поломки для конкретного типа ткани и т.д. Например, размер в сечении трансдермальной микроиглы может составлять от примерно 10 нанометров (нм) до 1 миллиметра (мм), или от примерно 1 до примерно 200 микрометров (мкм), или от примерно 10 до примерно 100 микрометров. Наружный диаметр может составлять от примерно 10 до примерно 100 микрометров, и внутренний диаметр полой иглы может составлять от примерно 3 до примерно 80 микрометров. Кончик обычно имеет радиус меньше или равный примерно 1 микрометру.
Длина микроиглы в основном зависит от требуемого применения. Например, микроигла может составлять от примерно 1 микрометра до примерно 1 миллиметра в длину, например, примерно 500 микрометров или меньше, или от примерно 10 до примерно 500 микрометров, или от примерно 30 до примерно 200 микрометров.
Массив микроигл необязательно содержит микроиглы, которые все идентичны друг другу. Массив может включать смесь микроигл с разной длиной, наружным диаметром, внутренним диаметром, формой в сечении, наноструктурированными поверхностями и/или промежутками между микроиглами. Например, микроиглы могут быть расположены с промежутком равномерным образом, например, в прямоугольной или квадратной сетке или концентрическими кругами. Промежуток может зависеть от большого числа факторов, включая высоту и ширину микроигл, а также количество и тип вещества, которое предполагается доставлять через микроиглы. Хотя применимо разнообразное расположение микроигл, особенно пригодно расположение микроигл с промежутком между микроиглами "от кончика до кончика" примерно 50 микрометров или больше, в некоторых вариантах осуществления от примерно 100 до примерно 800 микрометров, и в некоторых вариантах осуществления от примерно 200 до примерно 600 микрометров.
Как показано на фиг.1, микроиглы могут удерживаться на подложке 20 (т.е. присоединены или составляют единое целое с подложкой), так что они ориентированы перпендикулярно или под углом к подложке. В одном варианте осуществления микроиглы могут быть ориентированы перпендикулярно подложке, и может быть обеспечена большая плотность микроигл на единицу площади подложки. Однако массив микроигл может включать смесь ориентации микроигл, высот, материалов или других параметров. Подложка 20 может быть сконструирована из жесткого или гибкого листа металла, керамики, пластмассы или другого материала. Подложка 20 может быть разной толщины в соответствии с назначением устройства, например, примерно 1000 микрометров или меньше, в некоторых вариантах осуществления от примерно 1 до примерно 500 микрометров, и в некоторых вариантах осуществления от примерно 10 до примерно 200 микрометров.
По настоящему изобретению на поверхности микроиглы может быть создана нанотопография с произвольным или упорядоченным узором. На фиг.3 схематично показаны кончики двух репрезентативных микроигл 22. Микроиглы 22 образуют центральный канал 24, который может быть использован для доставки препарата через микроиглы 22. Поверхность 25 микроигл 22 образует нанотопографию 26. В этом конкретном варианте осуществления нанотопография 26 образует произвольный узор на поверхности 25 микроиглы 22.
Микроигла может содержать множество идентичных структур, сформированных на поверхности, или может содержать различные структуры, сформированные с разным размером, формой и их комбинациями. Заранее (предварительно, то есть перед изготовлением) определенный узор из структур может содержать смесь структур разной длины, диаметра, формы в сечении и/или с разными промежутками между структурами. Например, структуры могут быть расположены с промежутком равномерным образом, например, в прямоугольной или квадратной сетке или концентрическими кругами. В одном варианте осуществления структуры могут быть различны по размеру и/или форме и могут образовывать сложную нанотопографию. Например, сложная нанотопография может образовывать фрактальную или фракталоподобную геометрию.
Используемый в настоящем документе термин "фрактал" в основном относится к геометрической или физической структуре с фрагментированной формой в любом масштабе измерений от максимального до минимального, так что некоторые математические или физические свойства этой структуры обладают свойствами, как если бы размеры этой структуры были больше, чем ее пространственные размеры. Интересующие математические или физические свойства могут включать, например, периметр кривой или скорость потока в пористой среде. Геометрическая форма фрактала может быть разделена на части, каждая из которых образует самоподобие. Кроме того, фрактал имеет рекурсивное определение и обладает тонкими структурами произвольно малого масштаба.
Используемый в настоящем документе термин "фракталоподобный" в основном относится к геометрической или физической структуре с одной или более, но не всеми, из характеристик фрактала. Например, фракталоподобная структура может включать геометрическую форму, которая содержит самоподобные части, но может не содержать тонких структур при произвольно малом масштабе. В другом примере фракталоподобная геометрическая форма или физическая структура может не уменьшаться (или увеличиваться) в масштабе равномерно между итерациями масштабирования, как фрактал, хотя она может
увеличиваться или уменьшаться между рекурсивными итерациями геометрической формы узора. Фракталоподобный узор может быть проще, чем фрактал. Например, он может быть регулярным и относительно просто описанным на традиционном языке эвклидовой геометрии, в то время, как фрактал не может.
Поверхность микроиглы, образующая сложную нанотопографию, может содержать структуры одной и той же общей формы (например, столбики), и могут быть образованы столбики разного масштаба (например, столбики наномасштаба, а также столбики микромасштаба). В другом варианте осуществления микроигла может содержать на поверхности структуры, которые меняются и по масштабу размеров, и по форме, или которые меняются только по форме, хотя они образованы в одном и том же масштабе наноразмеров. Кроме того, структуры могут быть сформированы в виде упорядоченного массива или произвольного распределения. В основном, по меньшей мере участок структур может представлять собой наноструктуры, сформированные в масштабе наноразмеров, например, составляющие размер в сечении меньше примерно 500 нанометров, например, меньше примерно 400 нанометров, меньше примерно 250 нанометров или меньше примерно 100 нанометров. Размер наноструктуры в сечении может быть в основном больше примерно 5 нанометров, например, больше примерно 10 нанометров или больше примерно 20 нанометров. Например, наноструктуры могут обладать размером в сечении от примерно 5 до примерно 500 нанометров, от примерно 20 до примерно 400 нанометров или от примерно 100 до примерно 300 нанометров. В случаях, когда размер наноструктуры в сечении меняется в зависимости от высоты наноструктуры, размер в сечении можно определить, как среднее от основания до кончика наноструктуры, или как максимальный размер структуры в сечении, например, размер в сечении у основания конусообразной наноструктуры.
На фиг.4 показан один вариант осуществления сложной нанотопографии, которая может быть образована на поверхности. Этот конкретный узор включает большой центральный столбик 100 и окружающие столбики 102, 104 меньшего размера, предусмотренные на регулярном узоре. Как можно видеть, этот узор включает итерацию столбиков, каждый из которых имеет одну и ту же общую форму, но разных в отношении размера по горизонтали. Этот конкретный сложный узор представляет собой пример фракталоподобного узора, который не включает идентичного изменения по масштабу между последовательными рекурсивными итерациями. Например, в то время как столбики 102 являются первыми наноструктурами, которые определяют размер по горизонтали, который составляет примерно одну треть от этого размера большого столбика 100, который представляет собой микроструктуру, столбики 104 являются второй наноструктурой, которая определяет размер по горизонтали, который составляет примерно половину от этого размера столбиков 102.
Узор, который включает наноструктуры разного размера, может включать более крупные структуры, обладающие размером в сечении, сформированным большего масштаба, например, микроструктуры с размером в сечении больше примерно 500 нанометров, в сочетании с меньшими наноструктурами. В одном варианте осуществления микроструктуры сложной нанотопографии могут обладать размером в сечении от примерно 500 нанометров до примерно 10 микрометров, от примерно 600 нанометров до примерно 1,5 микрометров, или от примерно 650 нанометров до примерно 1,2 микрометра. Например, сложная нанотопография по фиг.4 включает столбики 100 микроразмера с размером в сечении примерно 1,2 микрометра.
Когда узор включает одну или больше микроструктур большего размера, например, с размером в сечении больше примерно 500 нанометров, определенным либо как средний, либо как максимальный размер этой структуры в сечении, сложная нанотопография также может включать наноструктуры, например, первые наноструктуры, вторые наноструктуры другого размера и/или формы и т.д. Например, столбики 102 сложной нанотопографии по фиг.4, обладающие размером в сечении примерно 400 нанометров, и столбики 104, обладающие размером в сечении примерно 200 нанометров.
Нанотопография может быть сформирована из любого числа различных элементов. Например, узор из элементов может включать два различных элемента, три различных элемента, пример которого показан на фиг.4, четыре различных элемента или больше. Относительные пропорции повторения каждого из разных элементов также могут меняться. В одном варианте осуществления самые малые элементы узора представлены в большем количестве, чем более крупные элементы. Например, в узоре по фиг.4, имеется восемь столбиков 104 для каждого столбика 102, и имеется восемь столбиков 102 для центрального большого столбика 100. По мере возрастания элементов по размеру, в основном может быть меньше повторений элемента в нанотопографии. Например, первый элемент, который составляет примерно 0,5, например от примерно 0,3 до примерно 0,7 по размеру в сечении относительно второго, большего элемента, может быть представлен в топографии чаще примерно в пять раз или более, чем второй элемент. Первый элемент, который составляет приблизительно 0,25, или от примерно 0,15 до примерно 0,3 по размеру в сечении относительно второго, большего элемента, может быть представлен в топографии чаще примерно в 10 раз или более, чем второй элемент.
Промежуток между отдельными элементами также может быть различен. Например, промежуток от центра до центра отдельных структур может составлять от примерно 50 нанометров до примерно 1 микрометра, например, от примерно 100 до примерно 500 нанометров. Например, промежуток от центра до центра может быть в масштабе наноразмеров. Например, при рассмотрении промежутка структур наноразмера промежуток от центра до центра структур может быть меньше примерно 500 нанометров. Это не является требованием топографии, однако и отдельные структуры могут быть разнесены дальше. Промежуток от центра до центра структур может быть различен в зависимости от размера структур. Например, отношение среднего размеров в сечении двух соседних структур к промежутку от центра до центра между этими двумя структурами может составлять от примерно 1:1 (например, касание) до примерно 1:4, от примерно 1:1,5 до примерно 1:3,5 или от примерно 1:2 до примерно 1:3. Например, промежуток от центра до центра может составлять приблизительно двойную среднюю величину размеров в сечении двух соседних структур. В одном варианте осуществления две соседние структуры с размером в сечении приблизительно 200 нанометров каждая могут иметь промежуток от центра до центра примерно 400 нанометров. Таким образом, отношение среднего диаметров к промежутку от центра до центра в этом случае составляет 1:2.
Промежуток между структурами может быть одним и тем же, т.е. они расположены с равными промежутками, или может быть различен для структур в узоре. Например, самые малые структуры узора могут быть расположены друг от друга на первом расстоянии, и промежуток между этими самыми малыми структурами и большей структурой узора или между двумя более крупными структурами узора может быть одним и тем же или другим, чем это первое расстояние.
Например, в узоре по фиг.4, самые малые структуры 104 расположены с промежутком от центра до центра примерно 200 нанометров. Расстояние между большими столбиками 102 и каждым из окружающих столбиков 104 меньше примерно 100 нанометров. Расстояние между самым большим столбиком 100 и каждым из окружающих столбиков 104 также меньше промежутка от центра до центра между самыми малыми столбиками 104 и составляет примерно 100 нанометров. Безусловно, это не является требованием, и все структуры могут быть расположены с равными промежутками друг от друга или на любом другом расстоянии. В одном варианте осуществления разные структуры могут соприкасаться друг с другом, например, одна над другой, как дополнительно описано далее, или примыкать одна к другой и соприкасаться одна с другой.
Все структуры топографии могут быть сформированы одной и той же высоты, в основном от примерно 10 нанометров до примерно 1 микрометра, но это не является требованием, и отдельные структуры узора могут быть разными по размеру в одном, двух или трех измерениях. В одном варианте осуществления некоторые или все структуры топографии могут обладать высотой меньше примерно 20 микрометров, меньше примерно 10 микрометров или меньше примерно 1 микрометра, например, меньше примерно 750 нанометров, меньше примерно 680 нанометров или меньше примерно 500 нанометров. Например, структуры могут обладать высотой от примерно 50 нанометров до примерно 20 микрометров или от примерно 100 до примерно 700 нанометров. Например, наноструктуры или микроструктуры могут обладать высотой от примерно 20 до примерно 500 нм, от примерно 30 до примерно 300 нм или от примерно 100 до примерно 200 нм, хотя следует понимать, что структуры могут быть наноразмера в сечении и могут обладать высотой, измеряемой в масштабе микроразмеров, например больше примерно 500 нм. Структуры микроразмера могут обладать высотой, аналогичной или отличающейся от структур в масштабе наноразмеров одного и того же узора. Например, структуры микроразмера могут обладать высотой от примерно 500 нанометров до примерно 20 микрометров, или от примерно 1 до примерно 10 микрометров в другом варианте осуществления. Структуры микроразмера также могут обладать размером в сечении в микромасштабе больше примерно 500 нм и могут обладать высотой в масштабе наноразмеров меньше примерно 500 нм.
Отношение сторон структур (отношение высоты структуры к размеру в сечении этой структуры) может составлять от примерно 0,15 до примерно 30, от примерно 0,2 до примерно 05, от примерно 0,5 до примерно 3,5 или от примерно 1 до примерно 2,5. Например, отношение сторон наноструктуры может попадать в эти диапазоны.
Поверхность устройства может содержать один узор, как показано на фиг.4, или может содержать повторение одного и того же или разных узоров. Например, на фиг.5 показан узор, содержащий узор по фиг.4, при многократном повторении на поверхности.
Формирование нанотопографии на поверхности может увеличивать площадь поверхности без соответствующего увеличения объема. Считается, что увеличение отношения площади поверхности к объему повышает площадь взаимодействия с окружающими биологическими материалами. Например, считается, что увеличение отношения площади поверхности к объему улучшает механическое взаимодействие между нанотопографией и окружающими белками, например белками внеклеточной матрицы (ECM) и/или белками плазматической мембраны.
В основном, отношение площади поверхности к объему устройства может быть больше примерно 10000 см-1, больше примерно 150000 см-1 или больше примерно 750000 см-1. Определение отношения площади поверхности к объему может быть выполнено в соответствии с любым стандартным способом, известным в этой области. Например, удельная площадь поверхности может быть получена физическим методом газовой адсорбции (метод B.E.T.) с азотом в качестве адсорбирующего газа, широко известным в этой области и описанным в публикации Brunauer, Emmet и Teller (J. Amer. Chem. Soc, vol. 60, Feb., 1938, pp.309-319), включенной в настоящий документ в качестве ссылки. В одном варианте осуществления площадь поверхности BET может быть меньше примерно 5 м2/г, например, от примерно 0,1 до примерно 4,5 м2/г или от примерно 0,5 до примерно 3,5 м2/г. Значения площади поверхности и объема также могут быть оценены по геометрии пресс-формы, используемой для формирования поверхности, в соответствии со стандартными геометрическими расчетами. Например, объем может быть оценен по расчетному объему для каждого элемента узора и общему числу элементов узора на заданной площади, например, по поверхности одной микроиглы.
Для устройства, которое образует сложный узор нанотопографии на поверхности, нанотопографию можно охарактеризовать путем определения размеров фрактала узора. Размер фрактала представляет собой статистическую величину, которая дает указание того, насколько плотно фрактал, по-видимому, заполняет пространство по мере того, как последовательные итерации становятся все меньшего и меньшего масштаба. Размер фрактала двухмерной структуры можно представить, как:
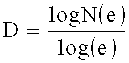
где N(e) - число самоподобных структур, необходимое для охвата всего объекта, когда объект уменьшается на 1/e в каждом пространственном направлении.
Например, при рассмотрении 2-мерного фрактала, известного как треугольник Серпинского, показанного на фиг.6, в котором срединные точки трех сторон равностороннего треугольника соединены, и полученный внутренний треугольник удален, размер фрактала рассчитывается следующим образом:
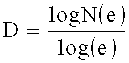
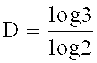
D≈1,585
Таким образом, фрактал треугольника Серпинского обнаруживает увеличение длины линий относительно исходного двухмерного равностороннего треугольника. Кроме того, этого увеличения длины линий не происходит при соответствующем увеличении площади.
Фрактальный размер узора, показанного на фиг.4, равен приблизительно 1,84. В одном варианте осуществления нанотопография поверхности устройства может обнаруживать размер фрактала больше примерно 1, например, от примерно 1,2 до примерно 5, от примерно 1,5 до примерно 3 или от примерно 1,5 до примерно 2,5.
На фиг.7А и 7Б показаны с возрастающим увеличением изображения другого примера сложной нанотопографии. Нанотопография по фиг.7А и 7Б включает массив напоминающих волокно столбиков 70, расположенных на подложке. На удаленном кончике каждого отдельного столбика он расщепляется на несколько меньших волокон 60. На удаленном кончике каждого из этих меньших волокон 60 каждое волокно также расщепляется на несколько нитей (не видны на фиг.7А и 7Б). Структуры, сформированные на поверхности, обладающей отношением сторон больше примерно 1, могут быть гибкими, как структуры, показанные на фиг.7А и 7Б, или они могут быть жесткими.
На фиг.7В и 7Г показан другой пример сложной нанотопографии. В этом варианте осуществления на подложке сформировано множество столбиков 72, каждый из которых содержит кольцевое полое сквозное отверстие 71 через него. На удаленном кончике каждого полого столбика сформировано множество меньших столбиков 62. Как можно видеть, столбики по фиг.7В и 7Г сохраняют свою жесткость и вертикальную ориентацию. Кроме того, и в противоположность предыдущим узорам, меньшие столбики 62 в этом варианте осуществления отличаются по форме от больших столбиков 72. В частности, меньшие столбики являются не полыми, а сплошными. Таким образом, нанотопография, содержащая структуры, сформированные разного масштаба, необязательно содержит все структуры, сформированные одной формы, и структуры могут отличаться и по размеру, и по форме от структур другого масштаба.
На фиг.8 показан другой узор, включающий структуры наноразмера, которые могут быть сформированы на поверхности устройства. Как можно видеть, в этом варианте осуществления структуры с конкретным узором могут быть сформированы одного и того же общего размера, но с ориентацией и формой, отличающимися друг от друга.
Дополнительно или альтернативно к упомянутым выше способам поверхность может быть охарактеризована другими способами, включая, но, не ограничиваясь этим, шероховатость поверхности, модуль упругости и поверхностную энергию.
Способами определения шероховатости поверхности в основном являются способы, известные в этой области. Например, обработка в атомно-силовом микроскопе в контактном или бесконтактном режиме может быть использована в соответствии со стандартной практикой для определения шероховатости поверхности материала. Шероховатость поверхности, которая может быть использована, чтобы охарактеризовать микроиглу, может включать среднюю шероховатость (RA), среднеквадратичную шероховатость, асимметрию и/или коэффициент эксцесса. В основном, средняя шероховатость поверхности (т.е. арифметическое среднее высоты поверхности представляет собой параметр шероховатости, как указано в стандарте ISO 25178 серии) для поверхности, образованной изготовленной на ней нанотопографией, может составлять меньше примерно 200 нанометров, меньше примерно 190 нанометров, меньше примерно 100 нанометров или меньше примерно 50 нанометров. Например, средняя шероховатость поверхности может составлять от примерно 10 до примерно 200 нанометров или от примерно 50 до примерно 190 нанометров.
Устройство может быть охарактеризовано модулем упругости поверхности с наноузором, например, изменением модуля упругости при добавлении нанотопографии на поверхности. В основном, добавление множества структур, образующих нанотопографию на поверхности, может снижать модуль упругости материала, поскольку добавление структур наноразмера на поверхности может привести к снижению непрерывности поверхности и соответствующему изменению площади поверхности. По сравнению с аналогичной поверхностью, образованной в соответствии с тем же самым способом и из тех же самых материалов, но для некоторого узора нанотопографии на поверхности, устройство, включающее нанотопографию на нем, может обнаруживать снижение модуля упругости от примерно 35% до примерно 99%, например, от примерно 50% до примерно 99% или от примерно 75% до примерно 80%. Например, эффективный модуль сжатия поверхности с наноузором может составлять меньше примерно 50 МПа или меньше примерно 20 МПа. В одном варианте осуществления эффективный модуль сжатия может составлять от примерно 0,2 до примерно 50 МПа, от примерно 5 до примерно 35 МПа или от примерно 10 до примерно 20 МПа. Эффективный модуль сдвига может составлять меньше примерно 320 МПа или меньше примерно 220 МПа. Например, в одном варианте осуществления эффективный модуль сдвига может составлять от примерно 4 до примерно 320 МПа или от примерно 50 до примерно 250 МПа.
Устройство, включающее нанотопографию на нем, также может обнаруживать увеличение поверхностной энергии по сравнению с аналогичной микроиглой, которая не обладает поверхностью, образующей на ней узор нанотопографии. Например, микроигла, содержащая сформированную на ней нанотопографию, может обнаруживать увеличение поверхностной энергии по сравнению с аналогичной микроиглой из тех же самых материалов и сформированной в соответствии теми же самыми способами, но без включения узора нанотопографии на поверхности. Например, для воды краевой угол смачивания поверхности, содержащей нанотопографию, может составлять больше примерно 80°, больше примерно 90°, больше примерно 100° или больше примерно 110°. Например, в одном варианте осуществления для воды краевой угол смачивания поверхности может составлять от примерно 80° до примерно 150°, от примерно 90° до примерно 130° или от примерно 100° до примерно 120°.
При формировании наноструктур на поверхности устройства плотность упаковки структур может быть максимальной. Например, упаковка в квадрате (фиг.9А), гексагональная упаковка (фиг.9Б) или некоторое их изменение может быть использовано для узора из элементов на подложке. При создании узора, в котором элементы разного размера по площади сечения A, B и C примыкают друг к другу на подложке, можно использовать упаковку в круге, как показано на фиг.9В. Безусловно, изменение плотности упаковки и определение соответствующего изменения характеристик поверхности зависят от навыка специалиста в этой области.
Во время использования устройство с микроиглами может взаимодействовать с одним или более компонентами соединительной ткани дермы. Соединительная ткань - это каркас, на который опираются другие типы ткани, т.е. эпителиальная, мышечная и нервная ткани. Соединительная ткань в основном содержит отдельные клетки, удерживаемые внутри EMC. ECM, в свою очередь, содержит межклеточное основное вещество (например, минеральные вещества кости, плазму крови и т.д.) и волокнистый компонент, включая коллаген, фибронектин, ламинины и т.д. Соединительная ткань может предполагать самую разнообразную структуру, начиная от крови, в которой волокнистый компонент отсутствует, и основным веществом является текучая среда, до плотной соединительной ткани, как обнаруживаемая в коже, которая содержит относительно высокую долю внеклеточных волокон (например, коллагена) и может содержать мало других компонентов соединительной ткани. Имеется много специальных типов соединительной ткани в коже, одним из примеров которой является эластичная соединительная ткань, в которой эластичные волокна являются основным компонентом ткани, и большое количество факторов, обычно обнаруживаемых в других типах соединительной ткани, таких как коллаген и протеогликаны, могут быть минимальны.
Нанотопография поверхности микроиглы может обеспечивать улучшенное взаимодействие между микроиглой и биологическими компонентами соединительной ткани дермы области доставки. Например, микроиглы трансдермального устройства могут взаимодействовать непосредственно с белками ECM и/или отдельными клетками, такими как кератиноциты, клетки Лангерганса шиповатого слоя или недифференцированные базальные клетки росткового слоя. Более длинные иглы трансдермальных устройств могут быть использованы для доступа к компонентам дермы, например, к клеткам крови капиллярного русла. Благодаря улучшенному взаимодействию между устройством и локальными биологическими компонентами, окружающая ткань менее вероятно обнаруживает реакцию на инородное тело, что может снизить локальное воспаление и улучшить доставку активных препаратов. В одном варианте осуществления устройство может играть более активную роль в доставке препаратов. Например, взаимодействие между нанотопографией и окружающими биологическими компонентами может способствовать доставке материалов с высокой молекулярной массой, например, через отверстие плотных контактов в зернистом слое.
Не желая ограничиваться какой-либо конкретной теорией, предполагается, что нанотопография облегчает улучшение взаимодействия с биологическими компонентами посредством двух механизмов. Согласно одному механизму, нанотопография может облегчать способность микроиглы имитировать ECM на участке доставки. Например, нанотопография микроиглы может имитировать один или более компонентов базальной мембраны на участке доставки. При использовании клетка может контактировать с нанотопографией микроиглы и реагировать аналогично типичному контакту с естественной структурой (например, белком базальной мембраны), который имитирует нанотопография. Соответственно, устройство может непосредственно взаимодействовать с клеткой, чтобы регулировать или моделировать (т.е. менять) поведение клетки, например, сигнальную трансдукцию клетки, тем самым улучшая доставку препарата через естественные барьеры, а также улучшая эндоцитоз препаратов, доставляемых устройством.
Согласно второму механизму, нанотопография может взаимодействовать с неклеточными биологическими компонентами локальной соединительной ткани, такими как белки ECM. Например, белки ECM могут адсорбироваться и десорбироваться из поверхности микроиглы. Адсорбция/десорбция белков ECM может менять химический состав локального окружения, что может приводить к изменению поведения клетки. Согласно этому второму механизму, устройство может косвенно влиять на поведение клетки. Например, адсорбция одного или более белков ECM на поверхности устройства может косвенно регулировать или моделировать внутриклеточную и/или межклеточную сигнальную трансдукцию.
Благодаря улучшенному взаимодействию с окружающими биологическими компонентами, устройства могут облегчать улучшенное поступление доставляемого препарата. Например, фармакокинетический (PK) профиль (т.е. профиль всасывания через эпителиальные мембраны) белкового терапевтического средства может быть улучшен посредством использования устройства, содержащего узор с нанотопографией. Например, белковое терапевтическое средство с молекулярной массой более 100 кДа, например от примерно 100 до примерно 200 кДа или до примерно 150 кДа, может быть доставлено трансдермально посредством пластыря с образованной на нем нанотопографией. В одном варианте осуществления пластырь может быть использован для доставки однократной дозы белкового терапевтического средства, например от примерно 200 до примерно 500 мкл или до примерно 250 мкл. После присоединения трансдермального пластыря к коже у пациента можно обнаруживать профиль PK, который отражает быстрый рост концентрации в сыворотке крови от примерно 500 до примерно 1000 нанограмм терапевтического средства на миллилитр на квадратный сантиметр площади пластыря, например от примерно 750 до примерно 850 нанограмм терапевтического средства на миллилитр на квадратный сантиметр площади пластыря, в пределах от примерно 1 до примерно 4 часов приема. Этот быстрый первоначальный рост уровня в сыворотке крови, который отражает быстрое поступление терапевтического средства через дермальный барьер, может сопровождаться менее быстрым спадом концентрации в сыворотке крови за период более от примерно 20 до примерно 30 часов, например, более примерно 24 часов, до пренебрежимо малой концентрации терапевтического средства в сыворотке крови. Более того, быстрое поступление доставляемого терапевтического средства может сопровождаться незначительным воспалением, или его может не быть вообще. В частности, помимо способствования улучшенной доставке препарата через трансдермальный барьер, устройства также могут ограничивать реакцию на инородное тело и другие нежелательные реакции, такие как воспаление. Использование известных ранее устройств, таких как трансдермальные пластыри без нанотопографии, образованной на поверхности, контактирующей с кожей, часто приводит к локальным областям воспаления и раздражения.
Структуры нанотопографии могут имитировать и/или взаимодействовать с одним или более белками ECM, такими как коллаген, ламинин, фибронектин и т.д. Это может прямо или косвенно менять мембранный белок клетки в отношении одной или более характеристик, таких как свободная энергия и локальная плотность. Примеры мембранных белков клетки включают, но не ограничиваются этим, интегрины, винкулин или другие адгезивные белки фокального контакта, клатрин, рецепторы мембраны клетки, такие как G-белок сопряженные рецепторы и т.д. Этот переход может вызывать изменения на поверхности клетки и/или внутри клетки посредством низлежащих эффектов через цитоскелет и внутри цитоплазмы.
Клетки в локальной области, окружающей устройство, могут поддерживать противовоспалительную микросреду, тем более что устройство может лучше имитировать локальное окружение либо напрямую, либо опосредованно, благодаря адсорбции белков на поверхности. Таким образом, вещества могут доставляться путем использования устройства без развития реакции на инородное тело или иммунного ответа.
Специфические типы клеток, на которые может напрямую или опосредованно влиять присутствие микроигл, могут включать клетки окружающей соединительной ткани дермы. Например, поверхность микроигл, образующая нанотопографию, может быть расположена в области, которая включает клетки Лангерганса, макрофаги и/или T-клетки, не вызывая реакцию на инородное тело или иммунный ответ. Клетки Лангерганса могут поглощать и обрабатывать антиген, чтобы стать полностью функциональной клеткой, представляющей антиген. Макрофаги и T-клетки играют основную роль в инициации и поддержании иммунного ответа. Когда они активируются патологическим или иммуногенным стимулом, например, посредством клеток Лангерганса, T-клетки могут выделять IL-2, IL-4, INF-γ и другие воспалительные цитокины. Макрофаги отвечают в этом процессе за выделение множества медиаторов воспаления, включая TNF-α, IL-1, IL-8, IL-11, IL-12, оксид азота, IL-6, GM-CSF, G-CSF, M-CSF, IFN-α, IFN-β и другие. Выделенные цитокины активируют другие иммунные клетки, и некоторые из них также могут действовать, как независимые цитотоксические вещества. Чрезмерное выделение произведенных макрофагами и T-клетками медиаторов воспаления может привести к повреждению нормальных клеток и окружающих тканей.
Не желая оказаться связанными какой-либо конкретной теорией, предполагают, что посредством взаимодействия с подложкой с наноузором, отдельные клетки могут проявлять повышенную или пониженную регуляцию выработки некоторых цитокинов, включая некоторые хемокины. Посредством этого изменения профиля экспрессии клеточный отклик на устройство доставки лекарственного средства может быть минимизирован. Например, воспаление и/или реакция на инородное тело могут быть минимизированы посредством повышенной регуляции одного или более противовоспалительных цитокинов и/или пониженной регуляцией одного или более противовоспалительных цитокинов. Многие цитокины охарактеризованы в соответствии с их воздействием на воспаление. Противовоспалительные цитокины, которые могут обнаруживать измененные профили экспрессии, когда на экспрессию клеток влияет присутствие устройства, содержащего изготовленную на нем нанотопографию, могут включать, без ограничения, IL-1α, IL-1β, IL-2, IL-6, IL-8, IL-10, IL-12, IL16, MIG, MIP-1α, MIP-1β, КС, МСР-1, TNF-α, GM-CSI, VEGF и подобные. Противовоспалительные цитокины, которые могут обнаруживать измененный профиль экспрессии, могут включать, без ограничения, IL-1α, IL-4, IL-10, IL-13 и подобные. Цитокины, связанные с реакцией на инородное тело, которые могут обнаруживать измененный профиль экспрессии, могут включать, без ограничения, IL-4, IL-10, IL-13 и т.д.
Оксид азота признан, как медиатор и регулятор воспалительных реакций. Влияя на локальное окружение, микроигла может ограничивать выделение оксида азота из окружающих клеток. Это может быть полезно, поскольку оксид азота может обладать токсическими свойствами по отношению к доставляемому активному препарату и может также обладать вредным воздействием на собственную ткань пациента (Korhonen et al., Curr Drug Targets Inflamm Allergy 4(4): 471 - 9, 2005). Оксид азота также может взаимодействовать с молекулярным кислородом и супероксид-анионом для производства реактивных форм кислорода (ROS), которые могут модифицировать различные клеточные функции. Эти косвенные эффекты оксида азота играют значительную роль в воспалении, при котором оксид азота может быть выработан в большом количестве за счет индуцибельной синтазы оксида азота (iNOS), и ROS может быть синтезирован активированными воспалительными клетками.
Оксид азота может быть выработан кератиноцитами, фибробластами, эндотелиальными клетками и, возможно, другими, на некоторые из которых может напрямую или опосредованно влиять нанотопография микроиглы. Ингибирование синтеза оксида азота, которое может быть обеспечено нанотопографией поверхности микроиглы, может влиять на закрытие раны, изменять организацию коллагена и менять толщину неоэпидермиса. Ингибирование оксида азота также может влиять на миграцию тучных клеток и ангиогенез в ранах. Благодаря различным путям регуляции и, не ограничиваясь какой-либо конкретной теорией, устройство может повышать выработку оксида азота и/или замедлять разложение оксида азота, в то время как в другом варианте осуществления устройство может снижать выработку оксида азота и/или ускорять разложение оксида азота.
Взаимодействие устройства с компонентами клеточной сети или слоем эпидермиса может модулировать (т.е. менять) в ней структуру межклеточных контактов. Внутриклеточное соединение может представлять собой по меньшей мере одно соединение, выбранное из группы, состоящей из плотных контактов, щелевых контактов и десмосом. Например, взаимодействие между биологическими компонентами и структурами нанотопографии может модулировать белки клеточной сети, чтобы индуцировать открытие плотных контактов зернистого слоя, тем самым, обеспечивая улучшенную доставку активного препарата через эпидермис, и в одном конкретном варианте осуществления, активного препарата с высокой молекулярной массой.
Нанотопография устройства может имитировать и/или адсорбировать один или более компонентов ECM. В основном, ECM включает и интерстициальную матрицу, и базальную мембрану. Интерстициальная матрица состоит из сложных смесей белков и протеогликанов и, в случае кости, минеральных отложений. Базальная мембрана включает и базальный слой, и сетчатый слой, и фиксирует и поддерживает эпителий и эндотелий. Конкретный состав ECM может быть различен в зависимости от конкретного типа ткани, но в основном включает различные коллагены, ламинины, фибронектин и эластины. Таким образом, нанотопография устройства может быть разработана для взаимодействия с компонентами конкретного места или в альтернативном варианте может быть в основном разработана, например, для взаимодействия с компонентами структур дермы, обычных для большей части кожи.
Структуры нанотопографии могут взаимодействовать с коллагеном, который представляет собой общий белок базальной мембраны, обнаруживаемый в ECM дермы. Коллагены представляют собой нерастворимые, внеклеточные гликобелки, которые обнаруживаются у всех животных и являются наиболее распространенными белками в организме человека. Они являются важными структурными компонентами большинства соединительных тканей, включая хрящ, кость, сухожилия, связки, соединительнотканные оболочки и кожу. На сегодняшний день у человека обнаружено 19 типов коллагенов. Основные типы включают Тип I, который является главным компонентом сухожилий, связок и костей; Тип II, который представляет более 50% белка в хряще, а также используется для построения спинной струны эмбрионов позвоночных; Тип III, который упрочняет стенки полых структур, таких как артерии, кишечник и матка, и Тип IV, который формирует базальный слой эпителия. Ячеистая структура коллагенов IV Типа обеспечивает фильтр для кровеносных капилляров и клубочков почек. Другие 15 типов коллагена, хотя и менее распространенные, но не менее важны для функции ECM.
Базовой единицей коллагенов является полипептид, который часто следует образцу Gly-Pro-Y (Глицин-Пролин-Y) или Gly-X-Hyp (Глицин-Х-Гипоксантин), где X и Y могут быть любыми из различных других аминокислотных остатков. Результирующий полипептид перекручен в удлиненную левозакрученную спираль. При синтезе N-концевые и C-концевые фрагменты полипептида имеют глобулярные домены, которые поддерживают растворимость молекулы.
Используемый в настоящем документе термин "полипептид" в основном относится к молекулярной цепи аминокислот и не относится к конкретной длине продукта. Таким образом, пептиды, олигопептиды и белки включены в определение полипептида. Также подразумевается, что этот термин включает полипептиды, которые подверглись постэкспрессионной модификации, например, такой как гликолизирование, ацетилирование, фосфорилирование и т.д. Используемый в настоящем документе термин "белок" в основном относится к молекулярной цепи аминокислот, которая обладает способностью взаимодействовать структурно, ферментативным путем или иным образом с другими белками, полипептидами или любой другой органической или неорганической молекулой.
Аббревиатуры символов общих аминокислот, приведенные далее в Табл.1, используются по всему описанию.
Тропоколлаген - это структурная единица больших соединений коллагена, таких как фибриллы. Он имеет приблизительно 300 нанометров в длину и 1,5 нанометра в диаметре, состоит из трех полипептидных цепей, каждая из которых обладает левоспиральной конформацией.
Нанотопография поверхности устройства может взаимодействовать с и/или имитировать тропоколлаген, а также коллаген. В одном варианте осуществления нанотопография может быть более сложной и может имитировать и/или взаимодействовать и с тропоколлагеном в наномасштабе, и с коллагеном в микромасштабе. Например, больший компонент нанотопографии может имитировать три левозакрученные спирали тропоколлагена, которые перекручены вместе в правозакрученную двойную спираль, тройную спираль или "суперспираль", совместную четырехкомпонентную структуру, стабилизированную многочисленными водородными связями. С коллагеном I типа и, возможно, всеми фибриллярными коллагенами, если не всеми коллагенами, каждая тройная спираль соединяется в правозакрученную супер-супер спираль, которая называется коллагеновой микрофибриллой. Каждая микрофибрилла переплетается с соседними микрофибриллами. В некоторых коллагенах (например, Тип II), три полипептида, которые составляют микрофибриллу, идентичны. В других коллагенах (например, Тип I), два полипептида одного вида (генный продукт) соединяются со вторым аналогичным, но другим полипептидом.
Ламинин является другим часто встречающимся белком базальной мембраны кожи, который может быть обнаружен в локальной области устройства. Ламинин является одним из семейства гетеротримерных белковых комплексов, сформированных из разных комбинаций различных цепей α-, β- и γ-субъединиц. Ламинины в основном могут быть обнаружены главным образом в базальных мембранах ECM и взаимодействовать с другими макромолекулами матрицы, чтобы давать вклад в дифференциацию, перемещение и снабжение клетки. Различные цепи ламининов, от α-1 до α-5, от β-1 до β-3 и от γ-1 до γ-3, теоретически могут формировать большое число различных тримерных изоформ, но подтверждено существование только 15 из возможных изоформ.
Ламинины имеют форму креста, включающего три более коротких плеча и одно длинное плечо. Три более коротких плеча особенно подходят для связывания с другими молекулами ламининов, что приводит к формированию пластинок в базальной мембране. Длинное плечо в основном является местом связывания клетки, связывания с клеточными мембранами и другими молекулами ECM, что способствует привязке клеток живой ткани к мембране.
Кроме того, ламинины включают субдомены со специфической геометрией. Например, концевой участок цепи ламинин-332 α3, G домен, кроме того, подразделяется на 5 субдоменов, G1, G2, G3, G4 и G5. Показано, что G субдомены цепи ламинина-332 α3 необходимы для сцепления ламинина-332 с клетками, которые содержат некоторые интегрины-рецепторы на поверхности их клеток. Соответственно, структуры наноразмера, относящиеся к нанотопографии, могут имитировать один или более субдоменов ламинина. В более сложном узоре эти структуры наноразмера могут быть скомбинированы с более крупными структурами, которые могут имитировать весь белок ламинин. Нанотопография также или в альтернативном варианте может адсорбировать/десорбировать ламинин и, тем самым, влиять на локальное окружение.
Нанотопография может взаимодействовать с фибронектином, который участвует в восстановлении тканей, эмбриогенезе, свертывании крови и миграции и адгезии клеток. В ECM фибронектин существует, как нерастворимый димер гликобелка. Структура фибронектина является палочкоподобной, состоящей из трех различных типов гомологичных, повторяющихся модулей, Типов I, II и III. Эти модули, хотя все отделились от одной и той же цепи аминокислот, обычно представляют в виде "бусинок на нитке", каждая из которых присоединена к соседней короткими линкерами.
Двенадцать модулей Типа I составляют аминоконцевую и карбоксиконцевую области белка и участвуют, главным образом, в связывании с фибрином и коллагеном. Только два модуля Типа II обнаруживают в фибронектине. Они играют важную роль в связывании коллагена. Наиболее распространенным модулем в фибронектине является Тип III, который содержит последовательность распознавания рецептора фибронектина RGD вместе с участками связывания для других интегринов и гепарина. В зависимости от типа ткани и/или состояния клетки молекула фибронектина состоит из 15-17 модулей III типа. Кроме того, существует модуль, который не попадает ни в одну из этих категорий, называемый IIICS. Этот модуль, вместе с EDB и EDA (оба модуля III типа), стабилизируют посредством альтернативного сплайсинга пре-мРНК ФН. Молекулы фибронектина могут образовывать два дисульфидных мостика на их карбоксиконцевых фрагментах, создавая димер, соединенный ковалентной связью. Клетка в контакте с нанотопографией устройства с микроиглами может взаимодействовать с устройством аналогичным образом, что и при обычном взаимодействии клетки с фибронектином.
Другим распространенным белком ECM, с которым может взаимодействовать устройство, является эластин и/или полипептидный фрагмент эластина. Эластин представляет собой составляющую белка из соединительной ткани, ответственную за эластичность и упругость ткани. Кроме того, эластин довольно распространен в соединительной ткани. Цепи тропоэластина естественным образом перекрестно сшиты вместе для формирования эластичных волокон. В отличие от коллагена, молекулы эластина могут раскручиваться в более вытянутую конформацию, когда волокно растянуто, и спонтанно скручиваться, как только сила растяжения ослабла. Эластин состоит главным образом из Gly, Val, Ala и Pro. Он образует скрученную конформацию неправильной или произвольной формы.
Помимо наиболее распространенных волокнистых белков дермы, нанотопография устройства может имитировать и/или адсорбировать другие компоненты ECM, такие как протеогликаны. Протеогликаны представляют собой гликобелки, но состоят в гораздо большей степени из углеводов, чем белок; т.е. они представляют собой огромные скопления цепей углеводов, часто присоединенных к главной белковой цепи. Некоторые сахара входят в протеогликаны. Наиболее распространенным является N-ацетилглюкозамин (NAG). Длинные цепи остатков сахаров присоединены к остаткам серина в главной белковой цепи; т.е. они "O-связаны". Сульфатные группы также добавляются к сахарам перед выделением. Примеры общих протеогликанов ECM включают, без ограничения, хондроитин сульфат, гепарин сульфат, кетаран сульфат и гиалуроновую кислоту (которая не имеет белкового компонента).
Нанотопография на поверхности может напрямую и/или опосредованно влиять на клетку в локальной области устройства. Она может включать клетку барьерного слоя, который лежит между поверхностью кожи и участком доставки препарата, доставляемого устройством с микроиглами, а также клетку, к которой нужно доставить препарат. Специфическое действие на клетку за счет присутствия устройства может включать изменение конформации, связывание лигандов или каталитическую активность связанного с мембраной белка.
Присутствие устройства может модулировать проводимость клеточной мембраны, включая, в одном аспекте, проводимость всей клетки. Кроме того, модулирование проводимости всей клетки может включать модулирование, по меньшей мере, зависящей от линейного или нелинейного напряжения проводимости всей клетки. Устройство может модулировать, по меньшей мере, клеточный трансмембранный потенциал или проводимость клеточной мембраны. Например, устройство может прямо или косвенно влиять на зависящие от кальция пути или систему клеточного обмена сообщениями.
Нанотопография устройства может влиять на компонент цитоплазматической мембраны, который может влиять на сигнальные пути, которые являются низлежащими эффекторами транскрипционных факторов. Например, посредством имитации или взаимодействия с компонентом ECM, устройство может влиять на генетическую транскрипцию и/или трансляцию внутри локальной клетки. Присутствие устройства может влиять на локализацию и/или конформацию мембранных белков. Это, в свою очередь, может влиять на свободную энергию локального окружения, что приводит к стимулированию эндоцитоза активного препарата, доставляемого устройством. Присутствие устройства может влиять на формирование соединений между клетками, например, плотных контактов, приводящих к улучшенной доставке препаратов через биологический барьер.
Считается, что устройство может напрямую или опосредованно влиять на клетку посредством связанного с мембраной белка. Связанные с мембраной белки могут включать по меньшей мере одно из, без ограничения, поверхностных рецепторов, трансмембранных рецепторов, белков ионных каналов, белков межклеточных контактов, белков клеточной адгезии, интегринов и т.д. По некоторым аспектам трансмембранный рецептор может представлять собой G-белок сопряженный рецептор (GPCR). Например, устройство может имитировать компонент ECM, который взаимодействует с GPCR, который, в свою очередь, взаимодействует с α-субъединицей G белка. А-субъединица G белка может представлять собой любое из Gαs, Gαj, Gαq и Gα12. При взаимодействии с α компонентом ECM устройство может влиять на кадгерины, фокальные адгезии, десмосомы, интегрины, клатрин, кавеолин, рецептор лимфопоэтина из стромы тимуса (TSLP), (3-2 анденергический рецептор, рецептор брадикинина, белки ионных каналов и т.д. В одном варианте осуществления присутствие микроиглы может модулировать адгезионные молекулы контактов, включая, без ограничения, JAM 2 и 3, GJA1, 3, 4 и 5 (соединительные адгерины), окклюдины (OCLN), клаудины (например, CLDN 3, 5, 7, 8, 9, 10) и белок 1 плотных контактов (TJP1).
Устройство может влиять на клеточную активность не только на поверхности клетки, но также и внутри. Например, устройство может влиять на фокальную адгезию. Фокальная адгезия представляет собой большие скопления вещества, которые могут включать 100 или более различных белков одновременно. Они являются динамическими в большинстве типов клеток и обеспечивают путь для передачи информации, и механический, и химический, от ECM к внутренней части клетки. Модификации фокальных адгезии происходят при изменении состава молекул, физической структуры, а также физических сил, присутствующих в ECM.
Фокальные адгезии обеспечивают соединение между цитоскелетом и ECM и в основном считаются сигнальным хабом и для механической силы, и для химической передачи сигналов. Большая часть фокальных адгезий расположена под клеточной мембраной, с присоединением к ECM в основном посредством интегринов, хотя соединение также может осуществляться посредством других трансмембранных веществ, включая белки, связывающие гуалуроновую кислоту и гепарин сульфат.
Интегрины представляют собой большое семейство необходимых гетеродимерных трансмембранных гликобелков, которые присоединяют клетки к белкам ECM (например, ламинин) базальной мембраны или к лигандам на других клетках. Нанотопография устройства может влиять на интегрин на цитоплазматической мембране, чтобы изменить поведение клетки, например, посредством фокальной адгезий. Интегрины содержат большие (α) и малые (β) субъединицы размера 120-170 кДа и 90-100 кДа, соответственно. У млекопитающих охарактеризовано 18 α и β субъединиц. Некоторые интегрины медиируют клетку напрямую для распознавания и взаимодействия с клеткой. Интегрины содержат связующие участки для двухвалентных катионов Mg2+ и Ca2+ которые необходимы для их адгезионной функции. Интегрины млекопитающих образуют несколько подсемейств, обладающих общими β субъединицами, которые соединяются с различными α субъединицами. И α, и β субъединицы содержат два отдельных хвоста, оба из которых проникают через цитоплазматическую мембрану и обладают малыми цитоплазматическими доменами. Исключением является β-4 субъединица, которая обладает цитоплазматическим доменом из 1088 аминокислот, одним из самых больших известных цитоплазматических доменов каких-либо мембранных белков. Участки проникновения могут взаимодействовать с белками в пределах фокальной адгезий для передачи информации в отношении ECM цитоскелету и внутренней части клетки. Вне цитоплазматической мембраны α и β цепи лежат близко друг к другу вдоль участка длиной примерно 23 нанометра, с конечными 5 нанометрами на N-концах каждой цепи, формирующей связанную лигандом область для ECM.
Первичные белки, известные в пределах фокальных адгезий, на которые может влиять присутствие нанотопографии в области поверхности клетки, включают винкулин, паксилин, талин, α-актинин и зиксин. Фокальные адгезивные белки передают информацию цитоскелету, например, посредством взаимодействия с актином и через цитоплазму. Фокальные адгезии находятся в постоянном состоянии притока, однако и белки постоянно соединяются и разъединяются с этим комплексом, передавая информацию от ECM другим частям клетки. Динамическое присоединение и отсоединение фокальных адгезии от структуры фокальных комплексов на переднем краю ламмелиподий для отсоединения фокальной адгезии на заднем краю клетки играет главную роль в миграции клетки. Активация Src киназы благодаря внеклеточным механическим силам, приложенным к внутренней части клетки посредством фокальной адгезии, является указанием роли, которую фокальные адгезии играют в восприятии механических сил ECM. Соответственно, устройство может модулировать активность внутренней части клетки, включая низлежащие функции, связанные с миграцией клетки, через мембранные белки плазмы, связанные с фокальными адгезиями.
Другие структуры поверхности клетки, на которые может влиять нанотопография устройства, включают мембранные белки, участвующие в эндоцитозе. Например, при взаимодействии с клеточной мембраной устройство может обнаруживать повышенную энергию адгезии благодаря нанотопографии контактирующей поверхности. Эта энергия адгезии может имитировать энергию адгезии типичной связи рецептор-лиганд.
Без привязки к какой-либо конкретной теории предполагается, что при адгезии между поверхностью устройства и рецептором, медиирующим эндоцитоз, другие рецепторы, медиирующие эндоцитоз в клеточной мембране, могут диффундировать от однородного распределения перед адгезией на клеточной мембране до участка адгезии. Эти мембранные белки затем могут прилипать к поверхности устройства и, тем самым, понижать свободную энергию взаимодействия между поверхностью клетки и устройством. Более низкая свободная энергия может способствовать эндоцитозу препаратов на поверхности клетки, например, активных препаратов, доставляемых через устройство. В частности, когда имеет место адгезия между поверхностью устройства и рецептором, выделяемая энергия, т.е. повышенная свободная энергия, может приводить к обертыванию мембраны вокруг частиц на или около участка адгезии. В альтернативном варианте адсорбция неклеточных компонентов ECM на поверхности устройства может менять локальный химический состав, что приводит к повышению внутриклеточной активности клеток в этой области. Пути эндоцитоза, который может быть медиирован благодаря присутствию устройства, могут подразделяться на четыре категории, включающие клатрин-медиированный эндоцитоз, ямки на поверхности клетки, макропиноцитоз и фагоцитоз.
Клатрин-медиированный эндоцитоз медиируется небольшими везикулами примерно 100 нанометров в диаметре, которые обладают морфологически характерным кристаллическым покрытием из комплекса белков, которые, главным образом, соединяются с клатрином цитоплазматического белка. Эти покрытые клатрином везикулы (CCVs) обнаруживают практически во всех клетках, и они формируют покрытые клатрином ямки на цитоплазматической мембране. Покрытые клатрином ямки могут включать повышенную концентрацию больших внеклеточных молекул, которые обладают различными рецепторами, ответственными за медиируемый рецепторами эндоцитоз лигандов, например, липобелок низкой плотности, трансферрин, стимуляторы роста, антитела и многое другое.
Нанотопография устройства может влиять на мембранные белки, связанные с ямками на поверхности клетки. Ямки на поверхности клетки представляют собой эндоцитозное впячивание мембраны, которое лишь немного менее распространено, чем покрытые клатрином ямки, и существует на поверхности многих, но не всех типов клеток. Оно состоит из белка кавеолина, связывающего холестерин (Vip21) с двухслойной структурой, обогащенной холестерином и гликолипидами. Ямки на поверхности клетки меньше, чем CCVs, примерно 50 нанометров в диаметре, и образуют ямки в форме колбы в мембране. Они могут составлять до трети площади цитоплазматической мембраны клеток некоторых тканей, особенно распространены в фибробластах, адипоцитах и эндотелиальных клетках, которые могут обнаруживаться в коже. Считается, что поступление внеклеточных молекул медиируется, в частности, рецепторами в ямках, на которые может влиять нанотопография микроиглы.
Макропиноцитоз, который обычно возникает от сильно сморщенных областей цитоплазматической мембраны, описывает сокращение клеточной мембраны для образования кармана, который затем смыкается в клетку для формирования крупной везикулы (0,5-5 мкм в диаметре), заполненной большим объемом внеклеточной текучей среды и молекулами внутри нее (эквивалентно от 103 до 106 CCVs). Заполнение кармана происходит неспецифическим образом. Везикула затем перемещается в цитозоль и сливается с другими везикулами, такими как эндосомы и липосомы.
Фагоцитоз описывает связывание и интернализацию вещества в виде частиц больше примерно 0,75 мкм в диаметре, таких как частицы пыли малого размера, клеточный детрит, микроорганизмы и даже апоптотические клетки, что происходит только в определенных клетках. Эти процессы включают усвоение большими участками мембраны, чем при пути медиированного клатрином эндоцитоза и ямок.
Нанотопография устройства также может влиять на кадгерины поверхности клетки. Кадгерины представляют собой семейство рецепторов, в основном участвующих в медиировании кальций-зависимой гомофильной адгезии клетка-клетка. Кадгерины особенно важны при эмбриогенезе, но также играют важную роль в формировании устойчивых контактов клетка-клетка и сохранении структур нормальной ткани у взрослых. Кадгерины являются суперсемейством трансмембранных белков, группируемых за счет присутствия одного или более повторов кадгеринов в их внеклеточных доменах. Множество этих доменов с приблизительно 110 остатками образует межмолекулярные поверхности, ответственные за формирование медиированных кадгеринами взаимодействий клетка-клетка. Структурная информация по анализу нескольких доменов кадгеринов указывает, что ионы кальция связываются на участках между соседними повторами кадгеринов (CRs), формируя жесткий стержень. Кадгерины обычно содержат пять последовательно соединенных повторенных внеклеточных доменов, один перекрывающий мембрану сегмент и цитоплазматическую область.
В одном варианте осуществления устройство может влиять на E-кадгерин, который обнаруживают в эпителиальной ткани. E-кадгерин содержит 5 повторов кадгеринов (EC1 ~ EC5) во внеклеточном домене, один трансмембранный домен и внутриклеточный домен, который связывает р120-катенин и β-катенин. Внутриклеточный домен содержит сильнофосфорилированную область, которая считается крайне необходимой для связывания β-катенина и, следовательно, для функции E-кадгерина, β-катенин также может связываться в α-катенином, и α-катенин участвует в регулировании актин-содержащих филаментов цитоскелета. В эпителиальных клетках E-кадгерин-содержащие контакты клетка-клетка часто примыкают к актин-содержащим филаментам цитоскелета.
Другая активность, на которую можно повлиять благодаря присутствию устройства в локальной области, включает параклеточный и трансклеточный транспорт. Например, посредством адсорбции белков ECM на поверхности устройства можно изменить локальный химический состав области, что приводит к улучшенному параклеточному транспорту доставляемого препарата в локальную область, которая может включать не только ближайшую к устройству область, но также области, лежащие глубже в дерме. Например, присутствие устройства может способствовать параклеточному транспорту доставляемого препарата в капиллярное русло дермы и через стенки капилляров, так что он доставляется в кровоток для системной доставки.
Во время использования устройство может взаимодействовать с одним или более компонентами контактирующей эпителиальной ткани для увеличения пористости ткани за счет механизмов параклеточного и/или трансклеточного транспорта. Эпителиальная ткань является одним из основных типов ткани организма. Эпителиальная ткань, которую можно сделать более пористой в соответствии с настоящим описанием, может содержать и простой, и слоистый эпителий, включающий и ороговевший эпителий, и промежуточный эпителий. Кроме того, эпителиальная ткань, о которой идет речь в настоящем документе, может содержать любые типы клеток эпителиального слоя, включая, без ограничения, кератиноциты, спущенные клетки, клетки, имеющие форму цилиндров, кубов и псевдомногослойные клетки.
Присутствие устройства может влиять на формирование и сохранение контактов клетка/клетка, включая плотные контакты и десмосомы для стимулирования параклеточного транспорта. Как указано выше, плотные контакты обнаружены в зернистом слое, и размыкание плотных контактов может обеспечивать параклеточный путь для улучшенной доставки активных препаратов, особенно активных препаратов с высокой молекулярной массой и/или препаратов, которые обнаруживают низкую липофильность, которые ранее невозможно было доставить трансдермально. Основные три типа белков плотных контактов - это клаудины, окклюдины и молекулы адгезивного контакта.
Взаимодействие между локальным компонентом и структурами нанотопографии может разомкнуть десмосомы в барьерном слое для стимулирования параклеточного транспорта. Десмосомы образуются главным образом из десмоглеина и десмоколлина, оба относятся к кадгеринам и участвуют в адгезии клетка-клетка. Десмосома содержит домен внеклеточной сердцевины (десмоглию), в которой белки десмоглеина и десмоколлина соседних клеток связываются друг с другом. Соседние клетки разделены слоем ECM примерно 30 нанометров шириной. Под мембраной сформированы тяжелые структуры в форме пластинок, известные как наружные плотные бляшки и внутренние плотные бляшки. Бляшки перекрываются белком десмоплакина. Наружные плотные бляшки - это место, где цитоплазматические домены кадгеринов присоединены к десмоплакину посредством плакоглобина и плакофилина. Внутренние плотные бляшки - это место, где десмоплакин присоединен к промежуточным филаментам клетки.
Взаимодействие между отдельными клетками и структурами нанотопографии может вызывать прохождение препарата через барьерную клетку и стимулировать трансклеточный транспорт. Например, взаимодействие с кератиноцитами рогового слоя может способствовать разделению препарата на кератиноциты, сопровождающееся диффузией через клетки и снова через липидную двухслойную структуру. Хотя препарат может пересечь барьер и по параклеточному, и по трансклеточному пути, трансклеточный путь может преобладать для сильно гидрофильных молекул, хотя, безусловно, преобладающий путь транспорта может быть различен в зависимости от природы препарата, при этом гидрофильность является одной из определяющих характеристик.
По одному варианту осуществления повышенная проницаемость клеточного слоя может быть определена путем измерения трансэпителиального электрического сопротивления (TEER, также упоминаемого в настоящем документе, как трансэпителиальное сопротивление или TER) через весь слой. Как в основном известно, снижение TEER через клеточный слой является надежным показателем повышения проницаемости клеточного слоя за счет, например, меньшего формирования или размыкания плотных контактов клеточного слоя. Очевидно, что в эндотелии и некоторой части эпителия способность плотных контактов ограничивать параклеточный поток неизменна. Скорее, эта функция пропускания плотных контактов способна к динамической регуляции (Madara, 1988; Rubin, 1992). В частности, активация путей сигнальной трансдукции либо за счет лигандов рецепторов, либо специфических проникающих через мембрану модуляторов, может обладать поразительным воздействием на проницаемость параклеточного пути. Например, активация C-киназой белка вызывает значительное повышение проницаемости плотных контактов в клетках MDCK (Ojakian, 1981), линии эпителиальных клеток. Циклический подъем AMP снижает проницаемость эндотелиальных клеток головного мозга в культуре, системе модели для исследования гематоэнцефалического барьера (Rubin et al., 991). Циклический подъем AMP также снижает проницаемость плотных контактов в периферических эндотелиальных клетках (Steizner et al., 1989; Langeieretal., 1991).
Свойства проницаемости плотного контакта также зависят от целостности адгезионного контакта. Разрыв адгезионного контакта путем удаления внеклеточного Ca2+ ведет к размыканию плотных контактов в клетках MDCK (см. публикации Martinez-Palomo et al., 1980; Gumbiner и Simons, 1986) и в эндотелиальных клетках (публикация Rutten et al., 1987). Киназы белков, по-видимому, участвуют в этой опосредованной модуляции целостности плотных контактов в клетках MDCK (Citi, 1992). Компонентами, чувствительными к Ca2+, комплекса адгезионных контактов являются кадгерины (обзор Geiger и Avalon, 1992). Эти трансмембранные белки медиируют внутриклеточную адгезивность Ca2+-зависимым, гомофильным образом через свои внеклеточные домены. Цитоплазматический домен кадгеринов связывается с тремя дополнительными белками, имеющими на конце α-, β- и γ-катенин (Ozawa et al., 1989), которые связывают кадгерины с актиновым цитоскелетом и необходимы для адгезивности кадгеринов (публикации Hirano et al., 1987; Nagaruchi и Takeichi, 1988; Ozawa et al., 1990; Kintner, 1992; см. Stappert и Kemler, 1993).
По настоящему изобретению контакт между эпителиальным слоем и поверхностью устройства, которая содержит заранее определенный узор из структур, изготовленных на этой поверхности, по меньшей мере участок которых изготовлен в масштабе нанометров, может повышать проницаемость и снижать TEER эпителиального слоя. Например, TEER эпителиального слоя может падать до менее примерно 95%, менее примерно 85% или менее примерно 70% его исходного значения после контакта между слоем и поверхностью с наноузором в течение некоторого периода времени. Например, примерно через 30 минут контакта между эпителиальным слоем и поверхностью, содержащей узор из наноструктур, TEER слоя может составлять от примерно 90% до примерно 95% его исходного значения. Через 60 минут TEER слоя может составлять от примерно 80% до примерно 90% его исходного значения, и через 120 минут TEER слоя может составлять от примерно 60% до примерно 75% его исходного значения.
На фиг.10 показан один способ определения TEER эпителиального слоя. В этом варианте осуществления слой клеток, например, монослой эпителиальных клеток, может быть выращен или иным образом расположен у основания апикальной камеры. Основание апикальной камеры может представлять собой микропористую фильтрующую мембрану, как показано, чтобы обеспечивать поток между двумя камерами и предотвратить прохождение отдельных клеток в базальную камеру. Например, микропористая фильтрующая мембрана может содержать поры размером примерно 0,4 микрометра при плотности примерно 4×106 пор/сантиметр. Безусловно, конкретные параметры различных компонентов системы не критичны и могут быть различны, как известно в этой области. Апикальная камера может быть образована вкладышем Transwell, которая может входить в больший карман, как показано, тем самым, образуя базальную камеру системы. Во время использования первый электрод 1 и второй электрод 2 могут быть расположены на одной из сторон монослоя эпителиальных клеток, и омметр 4 может быть присоединен между двумя электродами. Омметр 4 может измерять TEER монослоя клеток. Известны системы для определения TEER слоя клеток, например, может быть использована система электрического сопротивления Millicell™ (предлагаемая компанией Millipore of Bedford, MA).
Контакт между слоем эпителиальных клеток и поверхностью, содержащей изготовленные на ней наноструктуры, может приводить к падению TEER, что указывает на повышение проницаемости слоя. Соответственно, после контакта между эпителиальным слоем и наноструктурированной поверхностью способность транспортировать соединения через слой может быть сильно повышена. Это может улучшить трансдермальную доставку соединений, которые ранее не могли эффективно доставляться этим способом. Например, трансдермальная доставка соединений с высокой молекулярной массой, липофильных соединений и/или заряженных соединений может быть улучшена путем использования описанных способов и устройств.
Безусловно, структуры наноразмера устройства могут напрямую или опосредованно влиять на другие компоненты окружающей микросреды и представлены в настоящем документе только в качестве репрезентативного примера таких структур.
Устройство, содержащее изготовленную нанотопографию на поверхности устройства, может быть сформировано по одноэтапному способу. В альтернативном варианте может быть использован способ с несколькими этапами, в котором узор из наноструктур изготовлен на предварительно сформированной поверхности. Например, сначала может быть сформирован массив микроигл, а затем произвольный или упорядоченный узор из наноструктур может быть изготовлен на поверхности сформированных микроигл. При одноэтапном или двухэтапном способе структуры могут быть изготовлены на поверхности или на поверхности пресс-формы по любому подходящему способу изготовления нанотопографии, включая, без ограничения, наноимпринтинг, литьевое прессование, литографскую печать, рельефное прессование и т.д.
В основном, массив микроигл может быть сформирован по любому стандартному методу микроизготовления, включая, без ограничения, литографскую печать; способы травления, такие как удаление жидкими реактивами, сухими реактивами и удаление фоторезиста; термическое оксидирование кремния; электроосаждение и нанесение покрытий химическим путем; диффундирование, такое как диффундирование бора, фосфора, мышьяка и сурьмы; имплантация ионным пучком; напыление пленок, такое как испарение (нити, электронным пучком, дуговым разрядом и оттенением и сглаживанием ступеньки), металлизация напылением, химическое осаждение из паровой фазы (CVD), эптаксия (паровой фазы, жидкой фазы и молекулярного пучка), электроосаждение, трафаретная печать наслаивание, стереолитографская печать, лазерная обработка и удаление воздействием лазерного излучения (включая лазерную абляцию с использованием проекционной системы).
Может быть использован способ электролитического травления, в котором используется электролитическое травление твердого кремния до пористого кремния для создания чрезвычайно тонких (порядка 0,01 мкм) кремниевых сеток, которые можно использовать в качестве прокалывающих структур. В этом способе может быть использовано электролитическое анодирование кремния в водном растворе фтористоводородной кислоты, теоретически в комбинации со светом, для протравливания каналов в кремнии. Меняя концентрацию легирующей примеси кремниевой подложки для травления, электролитический потенциал при травлении, интенсивность падающего света и концентрацию электролита, можно добиться контроля над окончательной структурой пор. Не протравленный материал (т.е. оставшийся кремний) формирует микроиглы.
Также можно использовать плазменное травление, при котором выполняется глубокое плазменное травление кремния для создания микроигл диаметром порядка 0,1 микрометра или больше. Иглы могут быть изготовлены опосредованно путем управления напряжением (как при электролитическом травлении).
Способы литографской печати, включая фотолитографскую печать, электронно-лучевую литографскую печать, рентгеновскую литографскую печать и т.д. можно использовать для определения первичного узора и формирования эталонного штампа. Затем можно выполнить реплику для формирования устройства, содержащего массив микроигл. Общие способы репликации включают, без ограничения, микроформовку с использованием растворителя и литье, рельефное прессование, литьевое прессование и т.д. Технологии самосборки, включая способы расслоения полимера и блок-сополимера, разделенных на фазы, и коллоидной литографской печати также могут быть использованы для формирования нанотопографии на поверхности.
Как известно, могут быть использованы комбинации способов. Например, подложки с коллоидным узором можно подвергнуть реактивному ионному травлению (RIE, также известному, как сухое травление), чтобы улучшить характеристики изготовленных наноструктур, такие как диаметр наностолбика, профиль, высота, шаг и т.д. Мокрое травление также может быть использовано для получения альтернативных профилей для изготовленных наноструктур, первоначально сформированных различными способами, например, способами расслоения полимеров.
Диаметром, формой и шагом между структурами можно управлять путем выбора соответствующих материалов и способов. Например, травление металлов, первоначально испаряемых на подложки с узором из коллоида, с последующей взрывной литографией коллоида в основном приводит к созданию столбиков призматической формы. Затем процесс травления можно использовать для завершения создания нужных структур. Упорядоченные несферические полимерные наноструктуры также могут быть изготовлены посредством способов спекания с регулируемым нагревом, при которых получают разнообразные упорядоченные трехгранные нанометрические особенности в промежутках между коллоидами с последующим селективным растворением полимерных наночастиц. Эти и другие подходящие способы формирования в основном известны в этой области (см., например, публикацию Wood, J R Soc Interface, 2007 February 22; 4(12): 1-17, включенную в настоящий документ в качестве ссылки).
Другие способы, которые могут быть использованы при формировании микроигл, включающие изготовление нанотопографии на поверхности, включают способы наноимпринт-литографии с использованием ультра-высокопрецизионных способов лазерной обработки, примеры которых указаны Hunt, et al. (патент США №6,995,336) и Guo, et al. (патент США №7,374,864), которые оба включены в настоящий документ в качестве ссылки. Импринт-литография представляет собой способ литографской печати наноразмера, в котором используется гибридная пресс-форма, которая действует, и как пресс-форма наноимпринт-литографии, и как маска фотолитографской печати. Схема способа наноимпринт-литографии показана на фиг.11А-11В. Во время изготовления гибридная пресс-форма 30 впечатывается в подложку 32 посредством приложения давления для формирования особенностей (например, микроигл, образующих нанотопографию) на слое резиста (фиг.11А). В основном, поверхность подложки 32 может быть нагрета до сцепления с пресс-формой 30 до температуры выше ее температуры стеклования (Tg). В то время как гибридная пресс-форма 30 сцепляется с подложкой 32, поток вязкого полимера может быть закачан в полости пресс-формы для формирования особенностей 34 (фиг.11Б). Пресс-форма и подложка затем могут быть подвергнуты воздействию ультрафиолетового излучения. Гибридная пресс-форма в основном пропускает УФ-излучение за исключением некоторых загороженных областей. Таким образом, УФ-излучение проходит через пропускающие участки и в слой резиста. Давление сохраняется во время охлаждения пресс-формы и подложки. Гибридную пресс-форму 30 затем удаляют из охлажденной подложки 32 при температуре ниже Tg подложки и полимера (фиг.11В).
Чтобы облегчить освобождение подложки 32 с наноимпринтом, включающей изготовленные особенности 34, из пресс-формы 30, как показано на фиг.11В, предпочтительно обработать пресс-форму 30 низкоэнергетическим покрытием, чтобы уменьшить адгезию с подложкой 32, так как более низкая поверхностная энергия пресс-формы 30 и результирующая большая разность поверхностных энергий между пресс-формой 30, подложкой 32 и полимером может облегчить расцепление между этими материалами. Например, может быть использовано покрытие пресс-формы кремнием, а именно тридека-(1,1,2,2-тетрагидро)-октитрихлоросиланом (F13-TCS).
Способ наноимпринтинга является динамическим способом, который включает заполнение пресс-формы с последующим отщеплением сформованного полимера от пресс-формы. Для заполнения особенностей пресс-формы температура полимера должна быть повышена до достаточно высокого уровня, чтобы инициировать поток при приложенном давлении. Чем выше температура, тем ниже вязкость полимера, и тем быстрее и легче будет заполняться пресс-форма. Более высокое давление также повышает скорость заполнения и общее заполнение для лучшего моделирования пресс-формы. Чтобы освободить подложку с наноимпринтом из пресс-формы, температуру подложки можно снизить до точки, когда предел текучести превышает силы адгезии, испытываемые пресс-формой. Меняя температуру также можно изменить конусность особенностей полимера во время расцепления, чтобы получить различные структуры, например, структуры, показанные на фиг.8.
Структуры также могут быть сформированы способами добавления химических веществ. Например, напыление пленок, металлизация напылением, химическое осаждение из паровой фазы (CVD), эптаксия (паровой фазы, жидкой фазы и молекулярного пучка), электроосаждение, и т.д. могут быть использованы для построения структур на поверхности.
Могут быть использованы способы самосборки монослоя, известные в этой области, чтобы сформировать узор из структур на поверхности. Например, способность блок-сополимеров самоорганизовываться может быть использована для формирования узора из монослоя на поверхности. Узор затем можно использовать в качестве шаблона для выращивания нужных структур, например, коллоидов, в соответствии с узором монослоя.
Например, двухмерная сеть перекрестно сшитых полимеров может быть создана из мономеров с двумя или более реактивными участками. Такие перекрестно-сшитые монослои изготовлены с использованием самособирающегося монослоя (SAM) (например, система золото/алифатический радикал) или способы монослоев Ленгмюра-Блоджетта (LB) (Ahmed et al., Thin Solid Films 187: 141-153 (1990)) известны в этой области. Мономер может быть перекрестно-сшитым, что может привести к формированию структурно более прочного монослоя.
Мономеры, используемые для формирования монослоя с узором, могут содержать все структурные фрагменты, необходимые для нужного способа полимеризации и/или способа формирования монослоя, а также для влияния на такие свойства, как общая растворимость, способы диссоциации и способы литографии. Мономер может содержать по меньшей мере одну и более часто по меньшей мере две реактивные функциональные группы.
Молекула, используемая для формирования органического монослоя, может включать любые различные органические функциональные группы, вставленные в промежутки цепей метиленовых групп. Например, молекула может представлять собой углеродную структуру с длинной цепью, содержащую метиленовые цепочки для облегчения упаковки. Упаковка между метиленовыми группами может обеспечивать слабые Ван-дер-Ваальсовы силы, повышая устойчивость создаваемого монослоя и противодействие снижению энтропии, связанное с формированием упорядоченной фазы. Кроме того, различные концевые фрагменты, такие как фрагменты с водородной связью, могут присутствовать на одном конце молекул, чтобы обеспечивать рост структур на сформированном монослое, при этом полимеризуемые химические фрагменты могут быть помещены в середину цепи или на противоположные концы. Для формирования этого соединения может быть использован любой подходящий химический анализ для распознавания молекул. Например, структуры могут быть собраны на монослое на основании электростатического взаимодействия, Ван-дер-ваальсовых сил, хелатирования металлов, координационного связывания (т.е. взаимодействий кислоты по Льюису/основания), ионного связывания, ковалентного связывания или водородного связывания.
При использовании системы на основе SAM для формирования шаблона может быть использована дополнительная молекула. Эта дополнительная молекула может обладать соответствующими функциональными группами на конце, чтобы сформировать SAM. Например, на поверхности золота может быть включена тиольная группа на конце. Для воздействия на репликацию имеется широкое разнообразие органических молекул. Топографически полимеризуемые фрагменты, такие как диены и диацетилены, особенно предпочтительны в качестве компонентов полимеризации. Они могут быть вставлены в промежутки метиленовых линкеров разной длины.
Для монослоя LB (Ленгмюра-Блоджетта) нужна только одна молекула мономера, поскольку фрагмент для молекулярного распознавания также может служить в качестве полярной функциональной группы для целей формирования пленки LB. Литографскую печать можно выполнить на монослое LB, перенесенном на подложку, или непосредственно в ванночке. Например, монослой LB мономеров диацетилена может быть смоделирован путем воздействия УФ-излучения через маску или путем нанесения узора электронным пучком.
Формирование монослоя можно облегчить за счет использования молекул, которые претерпели топохимическую полимеризацию в фазе монослоя. Когда скомпонованная пленка подвергнута воздействию катализатора полимеризации, пленка может расти в условиях in situ и перейти из динамического молекулярного соединения в более прочное полимеризованное соединение.
Любой из способов, известных в этой области, может быть использован для формирования узора из монослоя. Способы, используемые для создания узора из монослоя, включают, но не ограничиваются этим, фотолитографскую печать, способы электронно-лучевой обработки, способы фокусировки ионного пучка и мягкую литографию. Различные схемы защиты, такие как фоторезист, могут быть использованы для систем на основе SAM. Аналогично, узоры из блок-сополимера могут быть сформированы на золоте и выборочно протравлены для формирования узоров. Для двухкомпонентной системы нанесение узора также может быть достигнуто легко доступными способами.
Способы мягкой литографской печати могут быть использованы для создания узора, в котором для создания узора могут быть использованы ультрафиолетовое излучение и маска. Например, монослой основания без узора можно использовать в качестве платформы для сборки монослоя реактивного мономера под действием пучка УФ/частиц. На монослой мономера затем может быть нанесен узор посредством УФ фотолитографской печати, электронно-лучевой литографской печати или литографской печати ионным пучком, даже хотя основной SAM не имеет узора.
Рост структур на монослое с узором может достигаться посредством различных механизмов роста, таких как соответствующее химическое восстановление солей металлов и использование центров или зародышей кристаллизации. При использовании элементов распознавания на монослое, рост неорганических соединений можно ускорить катализатором в этом месте раздела фаз различными способами. Например, могут быть сформированы неорганические соединения в форме коллоидов, обладающие формой органического монослоя с узором. Например, структуры из карбоната кальция или кремния могут составлять узоры за счет различных карбонильных функциональных групп, таких как карбоновые кислоты и амиды. Управляя условиями роста кристаллов, можно контролировать толщину и морфологию кристаллов во время роста минеральных соединений. Также для создания узора пригоден диоксид титана.
Способы создания узора путем нанесения покрытий химическим путем можно использовать для синтеза металлов с помощью существующих органических функциональных групп. В частности, путем образования хелатных соединений атомов металлов с карбонильными фрагментами узора из органического вещества, осаждение металлов способом химического восстановления можно катализировать на узоре, формируя металлические коллоиды с узором. Например, Cu, Au, Ni, Ag, Pd, Pt и многие другие металлы, фотоформа которых изготавливается путем нанесения покрытий химическим путем, могут быть использованы для формирования металлических структур в форме органического монослоя. Управляя условиями нанесения покрытий химическим путем, можно контролировать толщину металлических структур с электролитическим покрытием.
Могут быть использованы другие способы выращивания типа "вверх дном", известные в этой области, например, способ, предложенный в патенте США №7,189,435, Tuominen, et al., который включен в настоящий документ в качестве ссылки. В этом способе проводящая или полупроводниковая подложка (например, такой металл, как золото) может контактировать с пленкой блок-сополимера (например, блок-сополимер метилметакрилата и стирола), когда один компонент сополимера образует наноскопические цилиндры в матрице другого компонента сополимера. Проводящий слой затем может быть помещен поверх сополимера, чтобы сформировать композитную структуру. При вертикальной ориентации композитной структуры часть первого компонента может быть удалена, например, посредством воздействия УФ-излучения, электронным пучком или деструкцией под действием озона или подобным для формирования наноскопических пор в этой области второго компонента.
В другом варианте осуществления, предложенном в патенте США №6,926,953, Nealey, et al., включенном в настоящий документ в качестве ссылки, структуры сополимеров могут быть сформированы путем воздействия на подложку с репродуцированным слоем на ней, например, самособранного монослоя алкилсилоксана или оксидецилтрихлорсилоксана, двумя или более пучками выбранной длины волны для формирования интерференционного узора на репродуцированном слое, чтобы изменить смачиваемость репродуцируемого слоя в соответствии с интерференционными узорами. Слой выбранного блок-сополимера, например, сополимера полистирола и поли(метилметакрилата) затем может быть осажден на внешний репродуцируемый слой и отожжен для разделения компонентов сополимера в соответствии с шаблоном смачиваемости и для получения реплики узора репродуцируемого слоя в слое сополимера. Таким образом, могут быть сформированы полосы или выделенные области разделенных компонентов с повторяющимся размером в диапазоне 100 нанометров или меньше.
Поверхность устройства может содержать произвольное распределение изготовленных наноструктур. Необязательно поверхность может содержать дополнительные материалы вместе с изготовленными наноструктурами. Например, поверхность микроиглы может содержать изготовленный на ней электроспряденный волокнистый слой, и произвольный или упорядоченный узор из структур может быть изготовлен на этом электроспряденном слое.
Электропрядение включает использование устройства подачи высокого напряжения для приложения электрического поля к расплаву или раствору полимера, удерживаемого в капиллярной трубке, индуцируя заряд на отдельных молекулах полимера. При приложении электрического поля заряд и/или диполярная ориентация индуцируется на границе раздела воздух-поверхность. Индукция порождает силу, которая препятствует поверхностному натяжению. При критической напряженности поля электростатические силы преодолевают силы поверхностного натяжения, и струя полимера выбрасывается из капиллярной трубки в направлении проводящей заземленной поверхности. Струя удлиняется и ускоряется под действием внешнего электрического поля, когда она выходит из капиллярной трубки. По мере того, как струя перемещается в воздухе, часть растворителя может испариться, оставляя позади себя заряженные волокна полимера, которые могут быть собраны на поверхности. По мере получения волокон, отдельные и еще влажные волокна могут прилипнуть друг к другу, формируя нетканый материал на поверхности. Узор из наноструктур затем может быть изготовлен на электроспряденной поверхности, например, посредством способа рельефного прессования с использованием пресс-формы, образующей нужные наноструктуры. Приложение пресс-формы к поверхности микроиглы при соответствующей температуре и давлении позволяет переносить узор на поверхность микроиглы. Поверхность произвольных электроспряденных волокон наноразмера, кроме того, может улучшать нужные характеристики поверхности микроиглы, например, одно или более из отношения площади поверхности к объему, шероховатости поверхности, поверхностной энергии и т.д., и может обеспечивать соответствующие преимущества.
Поверхность микроигл может приобрести дополнительные функциональные особенности для улучшенного взаимодействия с тканями или отдельными клетками во время использования. Например, одна или более биомолекул, таких как полинуклеотиды, полипептиды, все белки, полисахариды и подобное могут быть связаны со структурированной поверхностью перед использованием.
В некоторых вариантах осуществления поверхность, содержащая сформированные на ней структуры, уже может обладать подходящей реактивностью, чтобы необходимую дополнительную функциональную особенность можно было спонтанно присоединить к поверхности без необходимости предварительной обработки поверхности. Однако в других вариантах осуществления может быть выполнена предварительная обработка структурированной поверхности перед присоединением к нужному соединению. Например, реактивность структурированной поверхности может быть увеличена за счет добавления или создания аминных, карбоновых, гидроксильных, альдегидных, тиольных или сложноэфирных групп на поверхности. В одном репрезентативном варианте осуществления поверхность микроигл, содержащая узор из сформированных на ней наноструктур, может быть аминирована посредством контакта с аминсодержащим соединением, таким как 3-аминопропилтриэтоксисилан, чтобы увеличить количество аминных функциональных групп на поверхности и связать одну или более биомолекул с поверхностью посредством добавленных аминных функциональных групп.
Вещества, которые может быть предпочтительно связать с поверхностью устройства с узором, могут включать белки ECM, такие как ламинины, тропоэластин или эластин, тропоколлаген или коллаген, фибронектин и подобные. Короткие фрагменты полипептидов могут быть связаны с поверхностью устройства с узором, например, последовательность RGD (аргинил-глицил-аспартил), которая является частью последовательности распознавания связи интегрина с многими белками ECM. Таким образом, повышение функциональных возможностей поверхности микроиглы с RGD может способствовать взаимодействию устройства с белками ECM и, кроме того, ограничивать реакцию на инородное тело устройства во время использования.
Устройства могут быть связаны с препаратом для доставки через устройство. Например, трансдермальный пластырь с микроиглами может быть использован для доставки веществ ниже рогового слоя в средний слой, stratum spinosum, или ниже росткового слоя, stratum germinativum, или даже глубже в дерму. В основном, препарат может транспортироваться через роговой слой вместе с микроиглой, например, внутри микроиглы или на поверхности микроиглы.
Устройство может включать емкость, например сосуд, пористую матрицу и т.д., которые позволяют хранить препарат и обеспечивать препарат для доставки. Устройство может содержать емкость внутри самого устройства. Например, устройство может содержать полость или множество пор, которые могут переносить один или более препаратов для доставки. Препарат может выбрасываться из устройства посредством разрушения участка или всего устройства или посредством диффузии препарата из устройства.
На фиг.12А и 12Б репрезентативно представлено устройство с емкостью. Устройство 110 содержит емкость 112, образованную непроницаемым защитным слоем 114 и массивом 116 микроигл. Защитный слой и массив 116 микроигл соединены вместе около наружной части устройства, как указано выноской 118. Непроницаемый защитный слой 114 может быть присоединен адгезивом, термосваркой или подобным. Устройство 110 также содержит множество микроигл 120. Покровная пленка 122 может быть удалена перед использованием устройства, чтобы обнажить микроиглы 120.
Состав, содержащий один или более препаратов, может удерживаться внутри емкости 112. Материалы, пригодные для использования в качестве непроницаемого защитного слоя 114, могут включать такие материалы, как сложные полиэфиры, полиэтилен, полипропилен и другие синтетические полимеры. Материал в основном может уплотняться теплом или иным способом относительно защитного слоя, чтобы обеспечить барьер для поперечного потока содержимого емкости.
Емкость 112, образованная пространством или зазором между непроницаемым защитным слоем 14 и основанием массива 16 микроигл, обеспечивает структуру для хранения, в которой удерживается суспензия назначаемых препаратов. Емкость может быть сформирована из разнообразных материалов, которые совместимы с содержащимся в них препаратом. Например, емкость может быть сформирована из натуральных и синтетических полимеров, металлов, керамики, полупроводников и их композитов.
В одном варианте осуществления емкость может быть присоединена к подложке, на которой расположены микроиглы. В другом варианте осуществления емкость может быть отделена и разъемно присоединяться к массиву микроигл или сможет сообщаться с массивом микроигл по потоку текучей среды, например, посредством соответствующих трубок, насадок Люэра и т.д.
Устройство может содержать одну или несколько емкостей для хранения доставляемых препаратов. Например, устройство может содержать одну емкость, в которой хранится состав, содержащий один или несколько препаратов, или устройство может содержать несколько емкостей, в каждой из которых хранится один или более препаратов для доставки во все или на участок массива микроигл. В случае нескольких емкостей, в каждой могут храниться разные вещества, которые могут быть скомбинированы для доставки. Например, первая емкость может содержать препарат, например лекарственное средство, а вторая емкость может содержать наполнитель, например физиологический раствор. Различные препараты могут смешиваться перед доставкой. Смешивание может быть начато любыми способами, включая, например, механическое разрушение (т.е. прокалывание, разрушение или разрыв), изменение пористости или электрохимическое разрушение стенок или мембран, разделяющих камеры. Несколько емкостей могут содержать различные активные препараты для доставки, которые можно доставлять вместе с другими или по очереди.
В одном варианте осуществления емкость может сообщаться по потоку текучей среды с одной или более микроиглами трансдермального устройства, и микроиглы могут образовывать структуру (например, центральный или боковой канал) для обеспечения транспорта доставляемых препаратов под барьерный слой.
В альтернативных вариантах осуществления устройство может содержать сборку микроигл и сборку емкости, чтобы предотвратить поток между ними до использования. Например, устройство может содержать отсоединяемый элемент, расположенный с примыканием и к емкости, и к массиву микроигл. Отсоединяемый элемент может быть отделен от устройства перед использованием, так что во время использования емкость и массив микроигл сообщаются по потоку текучей среды друг с другом. Разделение может быть осуществлено посредством частичного или полного отсоединения отсоединяемого элемента. Например, как показано на фиг.13-18, в одном варианте осуществления показан отсоединяемый элемент, который сконструирован для отсоединения от трансдермального пластыря для инициации потока лекарственного соединения. Более конкретно, на фиг.13-14 показан трансдермальный пластырь 300, который содержит сборку 370 доставки лекарственного средства и сборки 380 микроигл. Сборка 370 доставки лекарственного средства содержит емкость 306, расположенную с примыканием к мембране 308, управляющей скоростью доставки.
Мембрана, управляющая скоростью доставки, может способствовать замедлению скорости потока лекарственного соединения при его выпускании. В частности, жидкостные лекарственные соединения, проходящие из емкости с лекарственным средством в сборку микроигл через микрофлюидальные каналы, могут испытывать перепад давлений, который приводит к снижению скорости потока. Если этот перепад слишком большой, может быть создано некоторое обратное давление, которое может препятствовать потоку соединения и, возможно, преодолевать внутрикапиллярное давление текучей среды через микрофлюидальные каналы. Таким образом, использование мембраны, управляющей скоростью доставки, может повысить этот перепад давлений и обеспечить введение лекарственного соединения в микроиглу при более контролируемой скорости потока. Конкретные материалы, толщина и т.д. мембраны, управляющей скоростью доставки, могут быть различны в зависимости от многих факторов, таких как вязкость лекарственного соединения, необходимое время доставки и т.д.
Мембрана, управляющая скоростью доставки, может быть изготовлена из проницаемых, полупроницаемых или микропористых материалов, известных в этой области, чтобы управлять расходом лекарственных соединений, и обладающих проницаемостью относительно усилителя проницаемости ниже, чем у емкости с лекарственным средством. Например, материал, используемый для формирования мембраны, управляющей скоростью доставки, может обладать средним размером пор от примерно 50 нанометров до примерно 5 микрометров, в некоторых вариантах осуществления от примерно 100 нанометров до примерно 2 микрометров, и в некоторых вариантах осуществления от примерно 300 нанометров до примерно 1 микрометра (например, примерно 600 нанометров). Подходящие материалы мембраны включают, например, волокнистые материалы (например, тканые или нетканые), пленки с отверстиями, пеноматериалы, губки и т.д., которые сформированы из полимеров, таких как полиэтилен, полипропилен, поливинилацетат, сополимеры этилен н-бутилацетата и этилен винилацетата. Такие материалы мембраны также указаны более детально в патентах США №№3,797,494, 4,031,894, 4,201,211, 4,379,454, 4,436,741, 4,588,580, 4,615,699, 4,661,105, 4,681,584, 4,698,062, 4,725,272, 4,832,953, 4,908,027, 5,004,610, 5,310,559, 5,342,623, 5,344,656, 5,364,630 и 6,375,978, которые включены в настоящий документ во всей полноте в качестве ссылки для всех соответствующих целей. Особенно пригодным материалом для мембраны является материал, предлагаемый компанией Lohmann Therapie-Systeme.
Как показано на фиг.13-14, хотя это необязательно, сборка 370 также содержит адгезивный слой 304, расположенный с примыканием к емкости 306. Аналогично, сборка 380 микроигл содержит опору 312, из которой выступает множество микроигл 330 с каналами 331, как указано выше. Слои сборки 370 доставки лекарственного средства и/или сборки 380 микроигл могут быть соединены вместе, если это необходимо, с помощью любых известных способов присоединения, таких как адгезивное присоединение, термосварка, ультразвуковая сварка и т.д.
Несмотря на используемую конкретную конструкцию, пластырь 300 также содержит отсоединяемый элемент 310, который расположен между сборкой доставки лекарственного средства и сборкой 380 микроигл. Хотя отсоединяемый элемент 310 необязательно может быть присоединен к примыкающей опоре 312 и/или мембране 308, управляющей потоком, обычно предпочтительно, чтобы он был только слабо присоединен, если присоединен вообще, чтобы отсоединяемый элемент 310 можно было легко снять с пластыря 300. Если это необходимо, отсоединяемый элемент 310 также может содержать участок 371 язычка (фиг.13-14), который продолжается, по меньшей мере, частично за периметр пластыря 300, чтобы облегчить пользователю возможность захватить этот элемент и потянуть его в нужном направлении. В ее "неактивном" состоянии, как показано на фиг.13-14, сборка 370 доставки лекарственного средства пластыря 300 надежно удерживает лекарственное соединение 307, чтобы оно не вытекало до некоторой значимой степени в микроиглы 330. Пластырь может быть "активирован" простым приложением силы к отсоединяемому элементу, чтобы отсоединить его от пластыря.
Как показано на фиг.15-16, в одном варианте осуществления предложен пластырь 300, для активации которого отсоединяемый элемент 310 тянут в продольном направлении. Может быть удален весь отсоединяемый элемент 310, как показано на фиг.17-18, или он может быть просто частично отсоединен, как показано на фиг.15-16. Однако в любом случае уплотнение, сформированное ранее между отсоединяемым элементом 310 и отверстием (не показано) опоры 312, будет разрушено. Таким образом, лекарственное соединение 107 может начать вытекать из сборки 170 доставки лекарственного средства в каналы 131 микроигл 130 через опору 112. Примеры того, как лекарственное соединение 307 вытекает из емкости 306 в каналы 331, показаны на фиг.17-18. В частности, поток лекарственного соединения 307 инициируется пассивно и не требует каких-либо активных механизмов вытеснения (например, насосов).
В вариантах осуществления, показанных на фиг.13-18, отсоединение отсоединяемого элемента сразу же инициирует поток лекарственного соединения в микроиглы, поскольку сборка доставки лекарственного средства уже расположена с сообщением по потоку текучей среды со сборкой микроигл. Однако в некоторых вариантах осуществления может быть предпочтительно предусмотреть для пользователя большую степень управления выбором времени выпускания лекарственного соединения. Это можно осуществить путем использования компоновки пластыря, в котором сборка микроигл первоначально не сообщается по потоку текучей среды со сборкой доставки лекарственного средства. Когда нужно использовать пластырь, пользователь может физически привести две отдельные сборки в состояние сообщения по потоку текучей среды. Отсоединяемый элемент может быть отделен либо до, либо после такого физического приведения в состояние сообщения.
На фиг.19-24, например, показан один конкретный вариант осуществления пластыря 200. На фиг.19-20 показан пластырь 200 до использования, и показана первая секция 250, сформированная сборкой 280 микроигл, и вторая секция 260, сформированная сборкой 270 доставки лекарственного средства. Сборка 270 доставки лекарственного средства содержит емкость 206, расположенную с примыканием к мембране 208, управляющей потоком, как указано выше. Хотя это необязательно, сборка 270 также содержит слой 204 адгезива, который расположен с примыканием к емкости 206. Аналогично, сборка 280 микроигл содержит опору 212, из которой выступает множество микроигл 230 с каналами 231, как указано выше.
В этом варианте осуществления опора 212 и мембрана 208, управляющая скоростью доставки, исходно расположены горизонтально с примыканием друг к другу, и отсоединяемый элемент 210 выступает поверх опоры 212 и мембраны 208, управляющей скоростью доставки. В этом конкретном варианте осуществления в основном предпочтительно, чтобы отсоединяемый элемент 210 был съемно присоединен к опоре 212 и мембране 208, управляющей скоростью доставки, адгезивом (например, адгезивом, эффективным при кратковременном прижатии). В "неактивном "состоянии, как показано на фиг.19-20, сборка 270 доставки лекарственного средства пластыря 200 надежно удерживает лекарственное соединение 207, так что оно не вытекает до какой-либо значительной степени в микроиглы 230. Когда нужно "активировать" пластырь, отсоединяемый элемент 210 можно отодрать и удалить, как показано на фиг.21-22, чтобы разрушить ранее сформированное уплотнение между отсоединяемым элементом 210 и отверстием (не показано) опоры 212. Поэтому вторая секция 260 может быть согнута по линии сгиба "F", как показано направлением стрелки на фиг.23, чтобы элемент 208 управления скоростью доставки был расположен вертикально с примыканием к опоре 212 и с сообщением по потоку текучей среды с ней. В альтернативном варианте первая секция 250 может быть согнута. Тем не менее, сгибание секций 250 и/или 260 инициирует поток лекарственного соединения 207 от сборки 270 доставки лекарственного средства в каналы 231 микроигл 230 через опору 212 (см. фиг.24).
Устройство может доставлять препарат с такой скоростью, чтобы это было полезно в лечебных целях. С этой целью трансдермальное устройство может содержать корпус с микроэлектроникой и другими микроструктурами для управления скоростью доставки либо по заранее заданному графику, либо посредством активного взаимодействия с пациентом, медицинским работником или биодатчиком. Устройство может содержать вещество на поверхности с заранее заданной скоростью разложения, чтобы управлять выпусканием препарата, содержащегося внутри устройства. Скоростью доставки можно управлять путем регулирования разнообразных факторов, включая характеристики доставляемого состава (например, вязкость, электрический заряд и/или химический состав); размеры каждого устройства (например, наружный диаметр и объем каждого из отверстий); число микроигл на трансдермальном пластыре; число отдельных устройств в матрице носителя; применения внешней силы (например, градиента концентрации, градиента напряжения, градиента давления); использования клапана; и т.д.
Транспортировкой препаратов через устройство можно управлять или контролировать с помощью, например, различных комбинаций клапанов, насосов, датчиков, приводов и микропроцессоров. Эти компоненты могут быть изготовлены с использованием стандартных способов изготовления или микрообработки. Приводы, которые могут быть удобны с устройством, могут включать микронасосы, микроклапаны и локализаторы. Например, микропроцессор может быть запрограммирован для управления насосом или клапаном, тем самым, он управляет скоростью доставки.
Поток препарата через устройство может возникать вследствие диффузии или капиллярного действия или может быть вызван с использованием обычных механических насосов или немеханических движущих сил, таких как электроосмос или электрофорез или конвекция. Например, при электроосмосе электроды расположены на биологической поверхности (например, поверхности кожи), микроигле и/или подложке, примыкающей к микроигле, чтобы создать конвекционный поток, который переносит противоположно заряженные виды ионов и/или нейтральные молекулы к или на участок доставки.
Потоком препарата можно управлять путем выбора материала, образующего поверхность микроигл. Например, одна или более больших канавок, примыкающих к поверхности микроигл устройства, могут быть использованы для направления прохождения лекарственного средства, особенно в жидком состоянии. В альтернативном варианте физические свойства поверхности устройства можно регулировать либо, чтобы способствовать, либо, чтобы подавлять транспорт вещества вдоль поверхности, например, управляя гидрофильностью или гидрофобностью.
Поток препарата можно регулировать с помощью клапанов или затворов, известных в этой области. Клапаны могут многократно открываться и закрываться, или они могут быть одноразовыми клапанами. Например, в устройстве между емкостью и поверхностью с узором может быть установлен разрушаемый барьер или односторонний затвор. При готовности к использованию барьер разрушается, или затвор открывается, обеспечивая поток через него к поверхности микроигл. Другие клапаны или затворы, используемые в устройстве, могут быть активированы термически, электрохимически, механически или с помощью магнита для выборочной инициации, модуляции или останова потока молекул через устройство. В одном варианте осуществления потоком управляют путем использования ограничивающей поток мембраны в качестве "клапана".
В основном, любая система управления доставкой препаратов, включающая емкости, системы управления потоком, сенсорные системы и т.д., известные в этой области, может быть внедрена в устройство. Например, в патентах США №№7,250,037, 7,315,758, 7,429,258, 7,582,069 и 7,611,481 предлагается емкость и системы управления, которые могут быть внедрены в устройства.
Препараты, которые могут доставляться устройством, могут быть предназначены для локальной области около устройства или могут быть предназначены для более широкого распространения. Например, в одном варианте осуществления устройство может доставлять препараты для контроля боли или воспаления в локальной области вокруг сустава, например, при лечении остеоартрита или ревматоидного артрита.
Нанотопография устройства может улучшать доставку препаратов, при этом минимизируя реакцию на инородное тело и иммунный ответ. Это может оказаться особенно выгодным, когда речь идет о доставке олигонуклеотидов и других терапевтических средств в оболочку ядра. В прошлом доставка веществ (например, плазмидов, киРНК, интерферирующих РНК и т.д.), в оболочку ядра считалась проблематичной, поскольку даже при достижении эндоцитоза правильная эндосомальная доставка в оболочку ядра считалась трудной, главным образом, благодаря реакции на инородное тело и иммунному ответу. В цитоплазме доставляемое вещество часто перерабатывается поздними эндосомами или разрушается в липосоме. В соответствии с описанными способами взаимодействие микроигл с EMC может предотвращать реакцию на инородное тело внутри клетки после эндоцитоза и способствовать доставке веществ в ядро.
Доставка белковых терапевтических средств также считалась проблематичной. Например, доставка препаратов с высокой молекулярной массой, таких как белковые терапевтические средства, представляется трудной для путей трансдермальной доставки из-за естественных барьеров кожи. Присутствие нанотопографии на микроигле может благоприятно влиять на термодинамику EMC и повышать эффективность доставки и поступления белковых терапевтических средств. Используемый в настоящем документе термин "белковые терапевтические средства" в основном относится к любому биологически активному белковоподобному соединению, включая, без ограничения, натуральные, синтетические и рекомбинантные соединения, слитые белки, химерные организмы и т.д., а также соединения, включающие 20 стандартных аминокислот и/или синтетических аминокислот. Например, присутствие устройства в или около зернистого слоя может раскрыть плотные контакты и обеспечить параклеточный транспорт препаратов с высокой молекулярной массой. В одном варианте осуществления устройство может использоваться при трансдермальной доставке препаратов с высокой молекулярной массой (например, препаратов, образующих молекулярную массу больше примерно 400 Да, больше примерно 10 кДа, больше примерно 20 кДа или больше примерно 100 кДа, например, примерно 150 кДа). Кроме того, изменение отношения площади поверхности к объему устройства может быть использовано для изменения адсорбции белков на поверхности устройства, которое, в свою очередь, может менять доставку и клеточное поступление веществ. Таким образом, доставка конкретного вещества может быть оптимизирована посредством оптимизации отношения площади поверхности к объему устройства.
Даже при рассмотрении доставки препаратов с малой молекулярной массой, устройство может обеспечивать повышенную эффективность и улучшенное поступление благодаря взаимодействию устройства с компонентами соединительной ткани дермы и соответствующее снижение реакции на инородное тело и повышение локализованного химического потенциала в этой области.
Безусловно, устройства не ограничены целевой доставкой препаратов. Системная доставка препаратов также охватывается настоящим документом, как и удаление препарата у пациента через устройство.
Нет конкретного ограничения на препараты, которые можно доставлять с помощью этого устройства. Препараты могут включать белковоподобные препараты, такие как инсулин, иммуноглобулины (например, иммуноглобулин G, иммуноглобулин M, иммуноглобулин A, иммуноглобулин E), TNF-α, противовирусные лекарственные средства и т.д.; полинуклеотидные препараты, включая плазмиды, киРНК, интерферирующие РНК, нуклеозидные противораковые лекарственные средства, вакцины и т.д.; и препараты с небольшими молекулами, такие как алкалоиды, гликозиды, фенолы и т.д. Препараты могут включать противоинфекционные препараты, гормоны, лекарственные средства, которые регулируют сердечную деятельность или кровоснабжение, снимают боли и т.д. Другими веществами, которые можно доставлять по настоящему изобретению, являются препараты, полезные при предотвращении, диагностике, смягчении, терапии или лечении заболевания. Неограничивающий перечень препаратов включает препараты для антиангиогенеза, антидепрессанты, антидиабетические препараты, антигистаминные препараты, противовоспалительные препараты, буторфанол, тиреокальцитонин и аналоги, ингибиторы циклооксигеназы-2, дерматологические препараты, агонисты и антагонисты дофамина, энкефалины и другие опиоидные пептиды, эпидермальные стимуляторы роста, эритропоэтин и аналоги, фолликулостимулирующий гормон, глюкагон, гормон роста и аналоги (включая гормон высвобождения гормона роста), антагонисты гормона роста, гепарин, гирудин и аналоги гирудина, такие как гирулог, суппрессоры иммуноглобулина E и другие белковые ингибиторы, иммуносуппрессорные препараты, инсулин, инсулинотропин и аналоги, интерфероны, интерлейкины, лютеинизирующий гормон, гормон высвобождения лютеинизирующего гормона и аналоги, моноклональные или поликлональные антитела, препараты против укачивания, мышечные релаксанты, наркотические анальгетики, никотин, нестероидные противовоспалительные препараты, олигосахариды, паратиреоидный гормон и аналоги, антагонисты паратиреоидного гормона, антагонисты простагландина, простагландины, скополамин, седативные средства, агонисты и антагонисты серотонина, препараты при гиперфункции половых желез, тканевые активаторы плазминогена, транквилизаторы, вакцины с и без носителей/адъювантов, вазодилататоры, важные диагностические средства, такие как туберкулин и другие сверхчувствительные препараты, например, предложенные в патенте США №6,569,143, озаглавленном "Method of Intradermally Injecting Substances" (Способ внутридермального введения веществ), все содержание которого включено в настоящий документ в качестве ссылки. Составы вакцин могут включать антиген или составы антигенов, позволяющие вызвать иммунный ответ против патогена человека или других вирусных патогенов.
В одном предпочтительном варианте осуществления устройство может быть использовано при лечении хронического заболевания, такого как ревматоидный артрит, для доставки потока препарата пациенту. Лекарственные средства при ревматоидном артрите, которые можно доставлять посредством описанных устройств, могут включать соединения для подавления симптомов, такие как анальгетики и противовоспалительные лекарственные средства, включая и стероидные, и нестероидные противовоспалительные лекарственные средства (NSAID), а также модифицирующие течение заболевания противоревматические средства (DMARDs).
Устройство может содержать и доставлять соединения для подавления симптомов, такие как анальгетики и противовоспалительные лекарственные средства, а также DMARD соединения, включая биологические DMARDs. Без ограничения какой-либо конкретной теорией, понятно, что структуры наномасштаба, изготовленные на поверхности устройства, улучшают доставку соединений через дермальный барьер. За счет использования устройства лекарственные средства при ревматоидном артрите можно доставлять при установленной концентрации в течение установленного времени. Устройство позволяет предотвратить первоначальный всплеск концентрации, обычный, когда используются известные ранее способы доставки лекарственных средств при ревматоидном артрите, включая пероральный способ введения и инъекции.
Лекарственные средства при ревматоидном артрите, которые могут быть введены в устройство, могут включать, без ограничения, анальгетики, противовоспалительные средства, DMARDs, лекарственные средства растительного происхождения и их комбинации. Специфические соединения, безусловно, могут попасть в одну или более из общих категорий, описанных в настоящем документе. Например, многие соединения действуют и как анальгетики, и как противовоспалительные; лекарственные средства растительного происхождения могут аналогично действовать как DMARD, а также противовоспалительное средство.
Кроме того, множество соединений, которые могут попадать в одну категорию, могут быть внедрены в устройство. Например, устройство может содержать несколько анальгетиков, таких как ацетоминофен с кодеином, ацетоминофен с гидрокодоном (викодин) и т.д.
Примеры анальгетиков и/или NSAIDs, которые могут быть внедрены в устройства, включают анальгетики, продаваемые без рецепта (OTC) при относительно низкой дозировке, включая ацетамин (ацетоминофен или парацетамол), ацетилсалициловую кислоту (аспирин), ибупрофен, кетопрофен, напроксен и напроксен натрия и подобное. Назначение анальгетиков и/или противовоспалительных препаратов, которые могут быть введены в устройство, могут включать, без ограничения, анальгетики OTC с концентрацией, требующей рецепта, целекоксиб, силундак, оксапрозин, салсалат, пироксикам, индометацин, этодолак, мелоксикам, набуметон, кеторолок и кеторолак трометамина, толметин, диклофенак, дипроквалон и дифлунизал. Наркотические анальгетики могут включать кодеин, гидрокодон, оксикодон, фентанил и пропоксифен.
Устройство может содержать одно или более из стероидных противовоспалительных соединений, главным образом, гликокортикоидов, включая, без ограничения, кортизон, дексаметазон, преднизолон, преднизон, гидрокортизон, триамцинолон и метилпреднизолон, бетаметазон и альдостерон.
DMARDs, которые могут содержаться в устройстве, могут охватывать и лекарственные средства с небольшими молекулами, и биологические препараты. DMARDs могут быть синтезированы химически или могут быть получены способами генной инженерии (например, способами получения рекомбинантов).
Химически синтезированные DMARDs, охваченные настоящим документом, включают, без ограничения, азатиоприн, циклоспорин (циклоспорин, циклоспорин А), д-пенициллин, соли золота (например, ауранофин, натрий-ауротиомалат (Myocrism), хлорохин, гидрохлорохин, лефлуномид, метотриксат, миноциклин, сульфасалазин и циклофосфамид. Биологические DMARDs включают, без ограничения, TNF-α блокаторы, такие как этанерцепт (Энбрел®), инфликсимаб (Ремикад®), адалимумаб (Хумира®), цертолизумаб пегол (Цимзия®) и голимумаб (Симпони™); IL- блокаторы, такие как анакинра (Кинерет®); моноклональные антитела против B-клеток, включая ритуксимаб (Ритуксан®); блокаторы костимуляции T-клеток, такие как абатацепт (Оренсия®), и IL-6 блокаторы, такие как тоцилизумаб (РоАКТЕМРА®, Актемра®); ингибитор кальцийнейрина, такой как такролимус (Програф®).
Устройство может содержать одно или более лекарственных средств растительного происхождения или других природных лекарственных средств. Например, аюрведические соединения, такие как босвеллевая кислота (экстракт босвеллии, Boswellia serrata) и куркумин (куркуминоиды, экстракт корней Curcuma longa), а также другие природные соединения, такие как глюкозамин сульфат (полученный гидролизом внешней части панциря или ферментацией зерна) могут быть внедрены в устройство.
Устройство может содержать несколько лекарственных средств при ревматоидном артрите. Например, устройство может содержать комбинацию DMARDs в дополнение к анальгетику и/или противовоспалительному лекарственному средству. Общие комбинации DMARDs включают, например, метотриксат в комбинации с гидрохлорохином, метотриксат в комбинации с сульфасалазином, сульфасалазин в комбинации с гидрохлорохином и все эти три DMARDs вместе, т.е. гидрохлорохин, метотриксат и сульфасалазин.
Устройства могут успешно содержать соединения с большим и/или небольшой молекулярной массой. Например, в прошлом трансдермальная доставка белковых терапевтических средств считалась проблематичной из-за естественных барьеров кожи. Без ограничения какой-либо конкретной теорией, присутствие нанотопографии микроигл устройства позволяет им благоприятно взаимодействовать с клетками и EMC дермального барьера и повышать эффективность доставки и поступления белковых терапевтических лекарственных средств. Например, присутствие устройства в или около зернистого слоя может раскрыть плотные контакты и обеспечить параклеточный транспорт препаратов с высокой молекулярной массой. Используемый в настоящем документе термин препараты с высокой молекулярной массой в основном относится к препаратам, образующим молекулярную массу больше примерно 400 Да, больше примерно 10 кДа, больше примерно 20 кДа или больше примерно 100 кДа.
Даже при рассмотрении доставки лекарственных средств с меньшей молекулярной массой, устройство может обеспечивать повышенную эффективность и улучшенное поступление благодаря взаимодействию устройства с компонентами соединительной ткани дермы и соответствующее снижение реакции на инородное тело и повышение локализованного химического потенциала в этой области. Кроме того, устройство позволяет доставлять лекарственные средства при установленной концентрации в течение установленного времени, что может быть выгодно.
Настоящее изобретение можно лучше понять с учетом приведенных далее примеров.
Пример 1
Несколько различных пресс-форм подготовлены с помощью фотоспособов литографской печати, аналогичных использованным при разработке и изготовлении электрических схем. Отдельные этапы способа в основном известны в этой области и уже описаны.
Первоначально кремниевые подложки подготовлены путем чистки ацетоном, метанолом и изопропиловым спиртом, а затем покрыты слоем 258 нанометров (нм) диоксида кремния в соответствии со способом химического осаждения из паровой фазы.
Затем на каждой подложке сформирован узор по способу электронно-лучевой литографской печати, известному в этой области, с использованием системы JEOL JBX-9300FS EBL. Условия обработки следующие:
Ток электронного пучка = 11 нА
Ускоряющее напряжение = 100 кВ
Шаг съемки = 14 нм
Доза = 260 мкКи/см2
Резист = ZEP520A, толщиной ~330 нм
Проявитель = н-амилацетат
Проявление = 2 мин погружение с последующим ополаскиванием в течение 30 с изопропиловым спиртом.
Затем выполняют травление диоксида кремния улучшенным травителем диоксида кремния STS (АОЕ). Время травления составляет 50 секунд с использованием 55 стандартных кубических сантиметров в минуту (см3) He, 22 см3 CF4, 20 см3 C4F8 при 4 мТорр, катушки 400 Вт, мощности при реактивном ионном травлении (RIE) 200 Вт и смещении постоянного тока 404-411 В.
Затем выполняют травление кремния травителем диоксида кремния STS (SOE). Время травления составляет 2 минуты с использованием 20 см3 Cl2 и 5 см3 Ar при 5 мТорр, катушки 600 Вт, мощности при реактивном ионном травлении (RIE) 50 Вт и смещении постоянного тока 96-102 В. Глубина травления кремния составляет 500 нанометров.
Буферный травитель оксида (BOE) используют для удаление оставшегося оксида, что включает три минуты погружения в ВОЕ с последующим ополаскиванием деионизированной водой.
Наноимпринтер Obducat NIL-Eitre®6 используется для формирования наноузоров на различных полимерных подложках. В качестве охладителя используется дополнительная вода. УФ-блок используется с одной импульсной лампой с длиной волны от 200 до 1000 нанометров при мощности 1,8 Вт/см2. Используется УФ-фильтр 250-400 нанометров. Область воздействия составляет 6 дюймов с максимальной температурой 200°С и давлением 80 бар. Наноимпринтер включает полупроводниковый разделительный блок и извлечение из пресс-формы с автоматическим управлением.
Чтобы легче извлечь пленки с наноимпринтом из пресс-форм, пресс-формы обрабатывают тридека-(1,1,2,2-тетрагидро)-октилтрихлорсиланом (F13-TCS). Чтобы обработать пресс-форму, кремниевую пресс-форму сначала очищают, промывая ацетоном, метанолом и изопропиловым спиртом, и высушивают в атмосфере азота. Чашку Петри кладут на горячую пластинку в атмосфере азота и добавляют в чашку Петри 1-5 мл F13-TSC. Кремниевую пресс-форму кладут в чашку Петри и накрывают на 10-15 минут, чтобы дать парам F13-TSC испариться из кремниевой пресс-формы до удаления пресс-формы.
Пять разных полимеров, указанных в Табл.2 внизу, использовали для формирования различных узоров с нанотопографией.
Сформировано несколько разных узоров нанотопографии, схематичное представление которых показано на фиг.25А-25Г. Узор с нанотопографией, показанный на фиг.25Д, представляет собой поверхность плоской подложки, приобретенной в компании NTT Advanced Technology of Tokyo, Япония. Узоры были обозначены DN1 (фиг.25А), DN2 (фиг.25Б), DN3 (фиг.25В), DN4 (фиг.25Г) и NTTAT2 (фиг.25Д). Изображения SEM пресс-форм показаны на фиг.25А, 25Б и 25В, и изображения пленок показаны на фиг.25Г и 25Д. На фиг.8 показана пленка с наноузором, сформированная путем использования пресс-формы по фиг.25А (DN1). На этой конкретной пленке особенности полимера нанесены путем изменения температуры, как указано выше. Шероховатость поверхности узора на фиг.25Д составляет 34 нанометра.
Узор, показанный на фиг.7В и 7Г, также сформирован по этому способу импринтинга. Как показано, этот узор включает столбики 72 и столбики 62. Большие столбики 72 сформированы с диаметром 3,5 микрометра (мкм) и высотой 30 мкм при расстоянии от центра до центра 6,8 мкм. Столбики 62 составляют 500 нанометров в высоту и 200 нанометров в диаметре, и расстояние от центра до центра составляет 250 нанометров.
Условия способа импринтинга, используемого для пленок полипропилена, приведены далее в Табл.3.
Пример 2
Пленки формируют, как указано в Примере 1, включая различные узоры, либо из полистирола (PS), либо из полипропилена (РР). Лежащая внизу подложка различна по высоте. Используются узоры DN2, DN3 или DN4, сформированные с использованием способов, указанных в Примере 1. Пресс-формы узоров различаются по глубине отверстий и промежутку для формирования особенностей разного размера с заданными узорами. Образец №8 (обозначенный ВВ1) формируется путем использования микропористой поликарбонатной пленки 0,6 мкм в качестве пресс-формы. Полипропиленовую пленку толщиной 25 мкм кладут поверх фильтра, а затем нагревают до расплавления, чтобы полипропилен мог протекать в поры фильтра. Затем пресс-форму охлаждают, и поликарбонатную пресс-форму растворяют с помощью растворителя метиленхлорида.
Изображения SEM сформированных пленок показаны на фиг.26-34, и характеристики сформированных пленок сведены в Табл.4 внизу.
Чтобы охарактеризовать пленку, для каждого образца используется AFM.
Характеристики включают формирование изображений сканирующего электронного микроскопа (SEM), определение шероховатости поверхности, определение максимальной измеренной высоты особенности и определение размера фрактала.
Исследование с помощью атомно-силовой микроскопии (AFM) состоит из серии 16 проб кремния и кантилевера компании µMasch. Кантилевер обладает резонансной частотой 170 кГц, константой пружины 40 Н/м, длиной 230±5 мкм, шириной 40±3 мкм и толщиной 7,0±0,5 мкм. Наконечник датчика представляет собой кремниевый датчик, легированный фосфором n-типа, с типичным радиусом наконечника датчика 10 нанометров, полным углом конуса наконечника 40°, общей высотой наконечника 20-25 мкм и объемным удельным сопротивлением 0,01-0,05 Ом·см.
Значения шероховатости поверхности, приведенные в Табл.4, представляют собой среднее арифметическое высоты параметра шероховатости области поверхности (Sa), как определено в стандарте ISO 25178 серии.
Фрактальный размер рассчитывается для разных углов посредством анализа спектра Фурье амплитуд; для разных углов выделяется профиль Фурье амплитуд, и рассчитывается логарифм координат частоты и амплитуды. Фрактальный размер, D, затем рассчитывается для каждого направления, как
D=(6+s)/2,
где s - отрицательный уклон двойных логарифмических кривых. Приведенный фрактальный размер представляет собой среднее по всем направлениям.
Фрактальный размер также может быть оценен по 2D спектру Фурье путем применения двойной логарифмической функции. Если поверхность представляет собой фрактал, двойная логарифмическая кривая должна быть линейной с отрицательным уклоном (см., например, Fractal Surfaces, John С.Russ, Springer-Verlag New York, LLC, July, 2008).
Пример 3
HaCaT клетки эпителия кожи человека выращивают в DMEM (модифицированной по способу Дульбекко среде Игла), 10% эмбриональной бычьей сыворотке, 1% пенициллина/стрептомицина при температуре 37°С, 5% CO2 в течение 24 часов при концентрации 25000 клеток/см2 в 6-луночных планшетах. Планшеты либо содержат пленки полипропилена с наноузором, как указано выше в Примере 1, и обозначенные DN1, DN2 (образец 4 Табл.4), DN3, либо необработанную поверхность на дне лунки. Пленки с наноузором приклеены на месте цианоакрилатом.
Клетки отсоединяют от поверхности 1 мл трипсина на каждую лунку в течение 10 минут, охлаждают 1 мл питательной среды (как и выше), затем переносят в микроцентрифужную пробирку и осаждают центрифугированием на скорости 1200 оборотов/мин в течение 7 минут.
РНК выделяют из центрифугированных клеток с использованием предварительно подготовленного мини-комплекта RNeasy компании Qiagen в соответствии с протоколом изготовителя. Вкратце, клетки лизируют, смешивают с этанолом и скручивают в столбик. Затем лизат промывают в течение 3 минут, обрабатывают ДНКазой и элюируют в объемы 40 мл.
Комплементарную ДНК получают из изолированной РНК с использованием комплекта синтеза первой цепи RT (обратной транскриптазы) компании SA Biosciences. Вкратце, РНК обрабатывают ДНКазой повторно при температуре 42°C в течение 5 минут. Добавляют случайные праймеры и фермент обратной транскриптазы и инкубируют при температуре 42°C в течение 15 минут, затем инкубируют при температуре 95°C в течение 5 минут, чтобы остановить реакцию.
Затем на образцах комплементарной ДНК выполняется количественная ПЦР с использованием специального комплекта ПЦР профилей RT компании SA Biosciences с праймерами для IL1-β, IL6, IL8, IL10, IL1R1, TNF-α, TGFβ-1, PDGFA, GAPDH, HDGC, RTC и РРС. Вкратце, комплементарную ДНК смешивают с красителем SYBR green и водой, и затем добавляют к микропланшету для ПЦР с предварительно внедренной правильной парой смыслового и антисмыслового праймера для гена интереса. Микропланшет затем обрабатывают на аппарате компании ABI StepOnePlus для ПЦР, нагревая до температуры 95°C в течение 10 минут, затем в течение 45 циклов: 15 секунд при температуре 95°C и 1 минуту при температуре 60°C.
Анализ по методу Delta delta CT выполняют с использованием GAPDH в качестве внутреннего контроля. Уровни HDGC, RTC и PPC используются в качестве дополнительного внутреннего контроля активности и геномной контаминации ДНК.
Однофакторный дисперсионный анализ и критерий Тьюки попарного сравнения затем используют для определения статистической значимости различий между поверхностями.
В Табл.5, ниже, представлены экспрессии белка, полученные в виде кратности изменения экспрессии структур с наноимпринтингом, полученных на пропиленовых пленках, относительно экспрессии на неструктурированной пленке.
Пример 4
Способы, описанные в Примере 3, используются для изучения уровня экспрессии различных цитокинов из HaCaT клеток эпителия кожи человека, когда клетки развиваются на различных пленках из полипропилена (PP) или полистирола (PS), после формирования и нанесения узора, как указано выше. Уровень экспрессии для каждого цитокина сравнивают с уровнем экспрессии клетки того же типа, выращенной на стандартной пленке из полистирола для культуры тканей (TCPS) и индуцированной липополисахаридом (LPS). Результаты показаны в Табл.6 внизу.
Обнаружено, что клетки, выращенные на пленке полипропилена с наноузором DN2, как указано выше (образец 4 Табл.4), повышающе регулируют экспрессию 1L-1β, IL-1ra, IL-10, и MIP-1β понижающе регулирует экспрессию IL-4, IL-13, MIG, КС, IL-2, MIP-1, TNF-α, IL-12, IL-16, и IL-1α по сравнению с TCPS.
Изучают влияние некоторых других пленок на клеточную экспрессию различных цитокинов. Пленки обозначены следующим образом:
1 - DN2 узор на пленке полистирола 75 мкм (образец 3 Табл.4)
2 - DN3 узор на пленке полистирола 75 мкм (образец 1 Табл.4)
3 - DN4 узор на пленке полистирола 75 мкм (образец 6 Табл.4)
4 - пленка полистирола 75 мкм без импринтинга
5 - DN2 узор на пленке полипропилена 25,4 мкм (образец 4 Табл.4)
6 - DN4 узор на пленке полипропилена 25,4 мкм (образец 7 Табл.4)
7 - DN2 узор на пленке полипропилена 5 мкм (образец 2 Табл.4)
8 - bb1 полипропилен пленка (образец 8 Табл.4)
9 - пленка полипропилена 25,4 мкм без импринтинга
10 - пленка полипропилена 5 мкм без импринтинга
Результаты приведены в Табл.6 внизу. Результаты следующие:
-- уровень экспрессии ниже порога испытаний
- уровень экспрессии ниже уровня экспрессии для TCPS
= уровень экспрессии аналогичен уровню экспрессии для TCPS
+ уровень экспрессии выше уровня экспрессии для TCPS, но ниже при индуцировании LPS
++ уровень экспрессии аналогичен уровню экспрессии для индуцирования LPS
+++ уровень экспрессии выше уровня экспрессии для индуцирования LPS
Пример 5
HaCaT клетки эпителия кожи человека выращивают в DMEM (модифицированной по способу Дульбекко среде Игла), 10% эмбриональной бычьей сыворотке, 1% пенициллина/стрептомицина при температуре 37°С, 5% CO2 в течение 24 часов при концентрации 25000 клеток/см2 в 6-луночных планшетах. Планшеты либо содержат пленки полипропилена, сформированные, как указано выше в Примере 1, и обозначенные DN1, DN2 (образец 4 Табл.4), DN3, либо необработанную поверхность на дне лунки. Пленки с наноузором приклеены на месте цианоакрилатом.
Среду собирают из каждой лунки и анализируют на выработку цитокинов с набором Milliplex Map компании Millipore. Для обнаружения IL-β, IL-1ra, IL-6, IL-8, IL- 10, PDGF-AA, PGGF-AB/BB и TNF-α используют частицы. Данные получают по показаниям прибора BioRad BioPlex. Вкратце, среду помещают в лунки микропланшета с фильтрами. Добавляют исходные частицы и инкубируют при комнатной температуре в течение 1 часа с шейкированием. Затем микропланшеты промыкают и инкубируют с обнаружением антител в течение 30 минут при комнатной температуре с шейкированием. Добавляют стрепавидин-фикоэртитрин и инкубируют при комнатной температуре в течение дополнительных 30 минут. Затем микропланшеты промывают, частицы перерастворяют в буфере для анализа, и выполняют анализ медианной интенсивности флюоресценции на приборе BioPlex.
Пример 6
Уровень проницаемости пленок с узором, описанных в настоящем документе, определяют на монослое клеток Caco-2 (эпителиальные клетки человека при колоректальной аденокарциноме).
Пленки, сформированные, как указано выше в Примере 1 и 2, используют с пленками полипропилена (PP) или полистирола (PS), сформированными с узорами, обозначенными DN2, DN3 и DN4. Также используется четвертая пленка, обозначенная BB1 (описана в Примере 2 выше). Протокол выполняют с несколькими образцами пленок каждого типа.
Общий протокол для каждой пленки следующий:
Материалы
Вставки для культуры клеток из мембраны HDPET (компании BD Falcon) с размером пор 0,4 мкм
24-луночный микропланшет (компании BD Falcon)
Среда Caco-2
Наноструктурированные мембраны, как указано выше
FITC-меченый иммуноглобулин G (компания Sigma Aldrich) FITC-меченый бычий сывороточный альбумин (BSA) (компания Sigma Aldrich)
Среда MEM (Minimum Essential Medium) без таблеток phenol red (компания Invitrogen)
Вольтметр TEER
Подогретый забуференный фосфатом физиологический раствор
Черный 96-луночный микропланшет
Алюминиевая фольга
Протокол
1. Выполните посев клеток Сасо-2 на покрытые коллагеном вставки в лунки за 2 недели до выполнения анализа. Подготовьте покрытые коллагеном микропланшеты, изготовив раствор 1:1 по объему 100% этанола к коллагену. Просушите поверхности в стерильном вытяжном шкафу с вечера, чтобы они высохли.
2. Подготовьте раствор 0,1 мг/мл представляющих интерес меченых FITC молекул (BSA, иммуноглобулин G и т.д.) в среде Alpha MEM без красителя Phenol red. Заверните в алюминиевую фольгу для защиты от света.
3. Проверьте конфлюэнтность клеток Caco-2, измерив сопротивление. Для конфлюэнтности сопротивление должно быть выше ~600 Ом.
4. Аспирируйте старую среду из вставок в микропланшеты на апикальной и базолатеральной сторонах. Промойте PBS для удаления остатков красителя phenol red.
5. Добавьте 0,5 мл меченого FITC раствора на апикальной стороне каждой вставки.
6. В другой 24-луночный микропланшет со вставками добавьте 0,5 мл подогретого забуференного фосфатом физиологического раствора.
7. Перенесите вставки на микропланшет с PBS. Получите реплику промоканием вставки салфеткой Kirn wipe, чтобы удалить остаточный фенол красный (phenol red).
8. t=0 - временная точка: отберите 75 мкл с базолатеральной стороны вставки и перенесите на 96-луночный микропланшет с черным дном. Замените объем 75 мкл подогретым забуференным фосфатом физиологическим раствором. Запишите сопротивление каждой лунки, используя электроды-щупы.
9. Аккуратно добавьте мембрану в соответствующим образом помеченную лунку. Контролем является мембрана без импринтинга и клетки в чистом виде. Убедитесь, проверив под микроскопом, что мембрана непосредственно контактирует с клетками. Вы должны увидеть ровный круг, указывающий на контакт с клетками.
10. t=0 временная точка: повторите шаг 7, а затем поместите в термостат на 1 час
11. t=1 временная точка: проворите шаг 7, а затем поместите в термостат на 1 час
12. t=2 временная точка: повторите шаг 7
13. Измерьте сигнал флюоресценции с помощью спектрофлюориметра для прочтения планшетов
FITC (возбуждение 490 нанометров, эмиссия = 520 нанометров)
Результаты
Используемые пленки и полученные результаты приведены в Табл.7 внизу.
Модули определяют по стандартным способам, известным в этой области, например, предложенным Schubert, et al. (Sliding induced adhesion of stiff polymer microfiber arrays: 2. Microscale behaviour, Journal Royal Society, Interface, Jan. 22, 2008. 10.1098/rsif.2007.1309).
Краевые углы измеряют, поместив каплю воды на поверхность в соответствии со стандартной практикой. (См., например, Woodward, First Ten Angstroms, Portsmouth, VA).
На фиг.35 графически показан эффект повышения проницаемости для альбумин бычьей сыворотки (BSA) в монослое клеток на пленках полистирола со сформированным наноузором, описанным в настоящем документе. Как указано, узоры на пленках включают узор DN2 (образец №3), узор DN3 (образец №5) и узор DN4 (образец №6). Также показаны результаты для пленки из полистирола без узоров (помечена PSUI на фиг.35) и слоя клеток без примыкающей пленки (помечено "клетки" на фиг.35). Результаты показаны в виде кратности увеличения проницаемости в зависимости от времени в часах.
На фиг.36А и 36Б графически показан эффект повышения проницаемости для иммуноглобулина-G (IgG) в монослое клеток на пленках полистирола со сформированным наноузором, описанным в настоящем документе. Как указано, узоры на пленках включают узор DN2 (образец №3), узор DN3 (образец №5) и узор DN4 (образец №6). Также показаны результаты для пленки без узоров (помечена PSUI на фиг.36А и 36Б) и слоя клеток без примыкающей пленки (помечено "клетки" на фиг.36А и 36Б). На двух чертежах показаны данные в двух разных временных шкалах.
Сигнал BSA считывается на флюорометре, а сигнал иммуноглобулина G (IgG) считывается на спектрофотометре.
На фиг.37А и 37Б показаны 3D живые/неподвижные изображения с окрашиванием флуоресцеином, иллюстрирующие параклеточный и трансклеточный транспорт иммуноглобулина-G через монослой клеток на поверхности полистирола с узором DN4 (образец №6).
На фиг.38 графически показан эффект повышения проницаемости для BSA в монослое клеток на поверхности пленок полипропилена со сформированным наноузором, описанным в настоящем документе. Как указано, узоры включают BB1 (образец №8), DN2 (образец №4) и DN4 (образец №7). Также показаны результаты для пленки без узора (помечена PPUI на фиг.38) и слоя клеток без примыкающей пленки (помечено "клетки" на фиг.38).
На фиг.39 графически показан эффект повышения проницаемости для иммуноглобулина-G в монослое клеток на поверхности пленок полипропилена со сформированным наноузором, описанным в настоящем документе. Как указано, узоры включают ВВ1 (образец №8), DN2 (образец №4) и DN4 (образец №7). Также показаны результаты для пленки без узоров (помечена PSUI на фиг.39) и слоя клеток без примыкающей пленки (помечено "клетки" на фиг.39).
На фиг.40А и 40Б показаны 3D живые/неподвижные изображения с окрашиванием флуоресцеином, иллюстрирующие параклеточный транспорт иммуноглобулина-G через монослой клеток на поверхности полипропилена с узором DN2 (образец №4).
На фиг.41А-41Е показаны изображения сканирующего электронного микроскопа (SEM) клетки Сасо-2 в культуре на поверхностях с наноузором. В частности, на фиг.41А и 41Б показаны клетки Сасо-2 на гладкой пленке контроля из полистирола. На фиг.41В и 41Г показаны клетки Caco-2 на пленке из полистирола с узором DN2 (образец №3), как указано выше, и на фиг.41Д и 41Е показаны клетки Caco-2 на пленке из полистирола с узором DN3 (образец №5), как указано выше.
Пример 7
Способ, описанный в Примере 6, используется для изучения проницаемости монослоя клеток Caco-2 терапевтического этанерцепта белка слияния (торговое название на рынке энбрел -Enbrel®). На фиг.42 графически показаны результаты для слоев клеток, выращенных на нескольких подложках с разным узором, включая и полипропилен (DN2 РР - Образец 4 Табл.4), и полистирол (DN2 PS - образец 3 Табл.4 и DN3 PS - образец 1 Табл.4), а также мембрану из полистирола без импринтинга (PSUI) и слой клеток без мембраны (клетки). Результаты показаны в виде кратности изменения относительно исходной проницаемости со временем. На фиг.43 показано в виде кратности увеличения проницаемости от исходной t=o за два часа (t=2) после добавления мембраны в лунку для подложек и клеточного слоя по фиг.42.
Пример 8
Сформирован массив микроигл, содержащих поверхность с наноузором. Исходно массив микроигл, показанный на фиг.2, сформирован на кремниевой пластине посредством способа фотолитографской печати. Каждая игла имеет два расположенных друг напротив друга боковых канала, совмещенных с одним сквозным отверстием в основании иглы (не видно на фиг.2).
Микроиглы сформированы в соответствии с типичным способом микрообработки на пластине на основе кремния. Пластины расположены слоями с резистом и/или слоями оксида с последующим выборочным травлением (травление оксида, глубокое реактивно-ионное травление (DRIE), травление по ISO), отделением резиста, отделением оксида и способами литографской печати (например, литографская печать по ISO, литографская печать с контактными отверстиями, литографская печать с зазором) в соответствии со стандартными способами формирования массива микроигл.
После формирования массива микроигл 5 мкм полипропиленовую пленку со сформированным на ней узором DN2, описанным в Примере 1, характеристики которой указаны для образца 2 в Табл.4, накладывают на массив микроигл. Структура пластина/пленка удерживается в нагретой вакуумной камере (вакуум на уровне 3 дюймов водяного столба) при повышенной температуре (130°C) в течение одного часа для аккуратного наложения пленки на поверхности микроигл, сохраняя при этом поверхность пленки с наноузором.
На фиг.44 показана пленка поверх массива микроигл, и на фиг.45 показан укрупненный вид одной иглы из массива, содержащей наложенную поверх кончика иглы пленку с наноузором.
Пример 9
Сформированы трансдермальные пластыри, содержащие массивы микроигл, сформированные, как описано в Примере 8. Пластыри сформированы либо с узором DN2, либо с узором DN3 на массиве микроигл. Пленки, образующие узоры, которые наложены на микроиглы, описаны в Табл.8 внизу. Пленка 1 эквивалентна образцу №2 Табл.4, и пленка 2 эквивалентна образцу №9 Табл.4.
Также формируют пластыри контроля, которые не имеют сформированного на пленке узора, который впоследствии накладывают на массив микроигл. Трансдермальные и чрескожные составы этанерцепта (энбрел -Enbrel®) подготавливают в соответствии с указаниями поставщика лекарственного средства. Состав чрескожной дозы (для положительного контроля) подготавливают для обеспечения чрескожной дозы лекарственного средства 4 мг/кг. Концентрация Enbrel® для трансдермальной доставки отрегулирована, чтобы предполагаемая дозировка 200 мг/кг достигалась в течение периода 24 часов.
Всего в исследовании используется популяция 10 мышей BALB/C (назначения №1-№10), 8 с трансдермальной дозой Enbrel® (группа 1) и 2 с чрескожной дозой Enbrel® (группа 2), как указано в Табл.9 внизу. Трансдермальные пластыри накладывают на побритые области кожи, и отверстия образуются около кончиков микроигл при наложении пластыря на кожу.
Используемые трансдермальные пластыри включают и образующие нанотопографию на поверхности (DN2 и DN3 узоры, как указано выше), а также пластыри без узоров с нанотопографией.
Образцы цельной крови отбирают в моменты времени, указанные в Табл.8. Приблизительно от 100 до 200 мкл крови отбирают посредством кровотечения нижнечелюстного канала, а затем центрифугируют на скорости приблизительно 1300 оборотов/мин в течение 10 минут в охлаждаемой центрифуге (установленной на 4°C). Полученную сыворотку аспирируют и переносят в течение 30 минут отбора/центрифугирования в соответствующим образом помеченные пробирки. Пробирки замораживают и хранят в темноте при температуре ≤-70°C, пока выполняется анализ уровней Enbrel® с использованием комплекта ELISA sTNF-рецептора человека (компании R&D Systems, №по каталогу DRT200). Временной промежуток между двумя отборами крови у одного и того же объекта составляет 24 часа, чтобы предотвратить ненужный стресс объекта.
На фиг.46 графически показан средний РК профиль трансдермальных пластырей, который образует на нем нанотопографию. Среднее результатов для всех пластырей, содержащих нанотопографию, используется для представления общего эффекта введенной нанотопографии в соединении с трансдермальным пластырем с микроиглами. Как можно видеть, уровень сыворотки крови быстро вырастает до более 800 нг/мл/см2 площади пластыря в первые два часа после его присоединения. Затем уровень сыворотки крови постепенно падает до пренебрежимо малого уровня в течение 24 часов присоединения. Данные, использованные для фиг.46, приведены ниже в Табл.10.
На фиг.47А и 47Б показаны изображения электронного микроскопа для кожи в сечении, которая удерживается в контакте с пластырями. Изображения получают после удаления пластырей (72 часа после присоединения). Образец на фиг.47А находится в контакте с пластырем, содержащим нанотопографию на поверхности. В частности, узор DN2, как указано выше, сформирован на поверхности пластыря. Образец на фиг.47Б удерживается в контакте с трансдермальным пластырем, на котором нет узора с нанотопографией на поверхности. Как можно видеть, образец на фиг.47Б обнаруживает признаки воспаления и высокую плотность присутствия макрофагов.
Пример 10
Сформированы трансдермальные пластыри, содержащие массивы микроигл, сформированные, как описано в Примере 8. Пластыри сформированы либо с узором DN2, либо с узором DN3 на массиве микроигл, как указано в Табл.8 Примера 9. Пластыри контроля также сформированы без узора на пленке, впоследствии накладываемой на массив микроигл. Трансдермальные и чрескожные составы этанерцепта (Enbrel®) подготавливают в соответствии с указаниями поставщика лекарственного средства.
Испытуемые объекты (кролики) получают дозу Enbrel® трансдермально, либо чрескожно (SubQ). Результаты показаны графически на фиг.48, на котором концентрация сыворотки крови в пг/мл показана в зависимости от времени. Данные по фиг.48 приведены ниже в Табл.11.
Хотя сущность изобретения подробно описана в отношении его конкретных вариантов осуществления, очевидно, что специалисты в этой области, поняв вышеизложенное, могут легко представить варианты, изменения и эквиваленты этих вариантов осуществления. Соответственно, следует оценить объем настоящего описания, как объем приложенной формулы изобретения и ее эквивалентов.
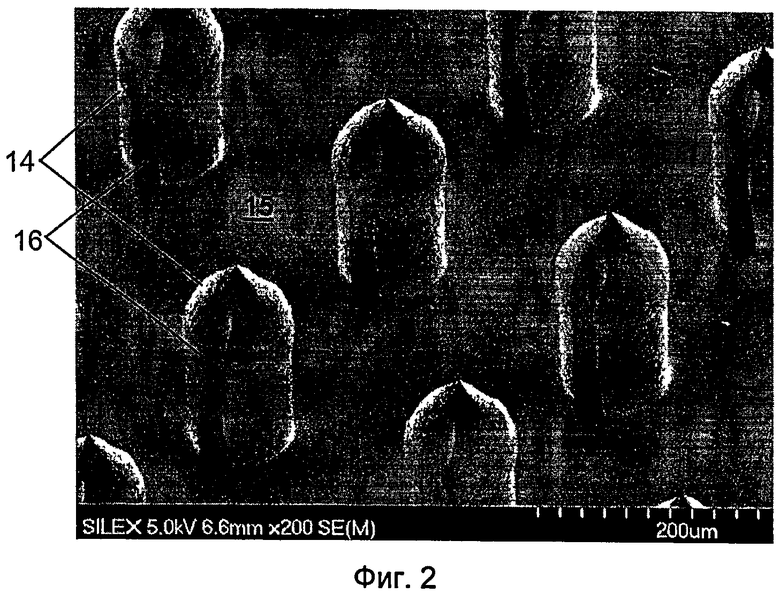
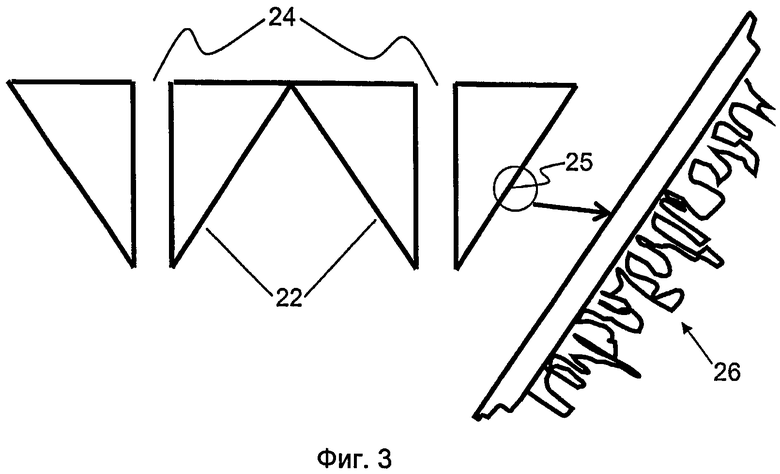
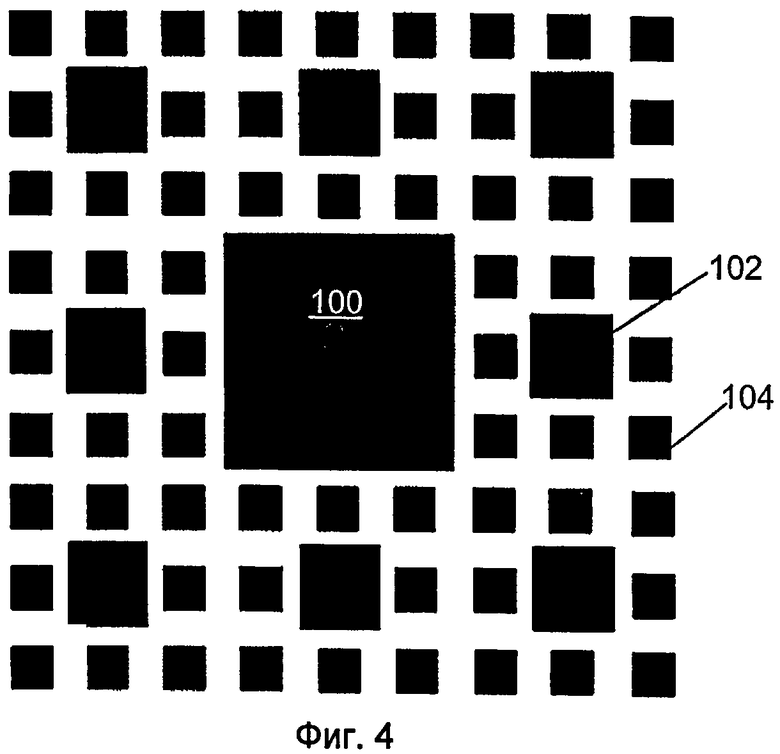
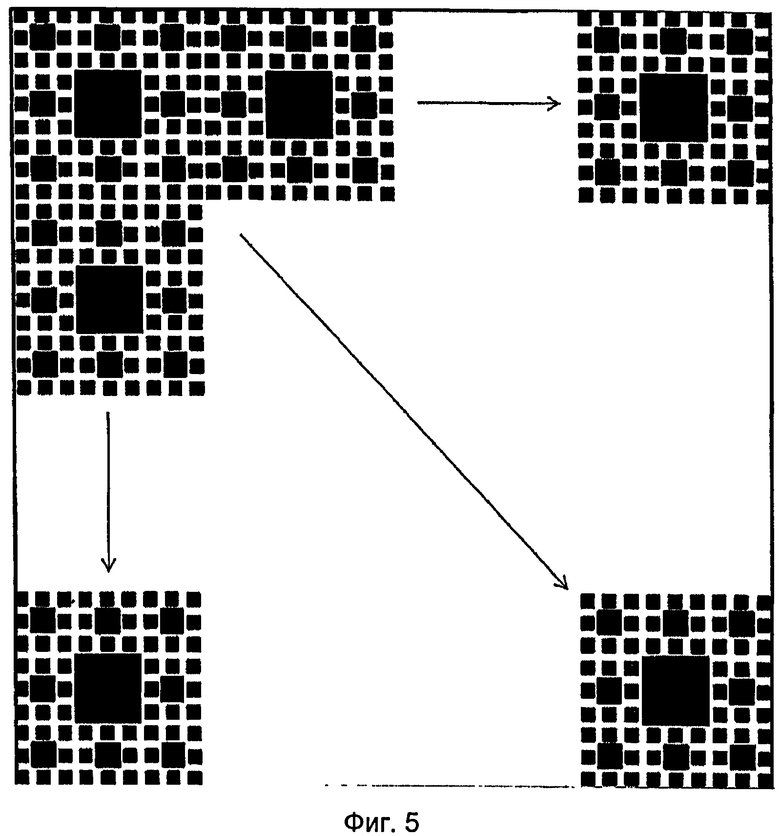



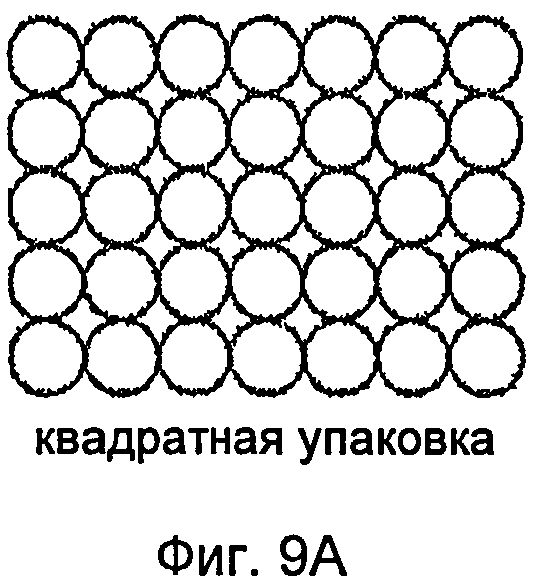
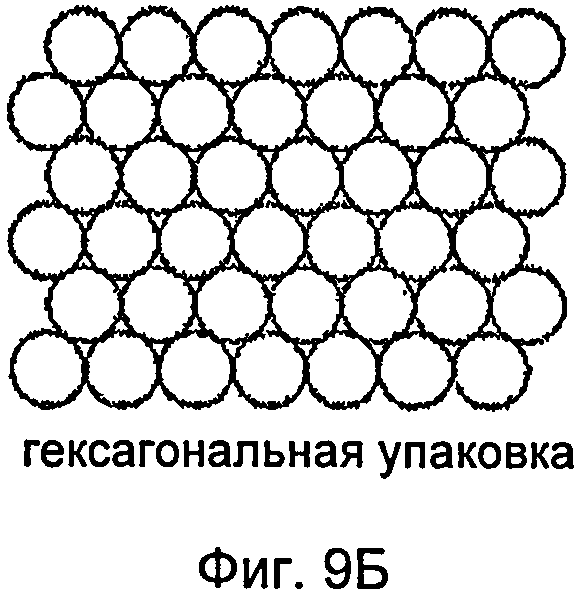
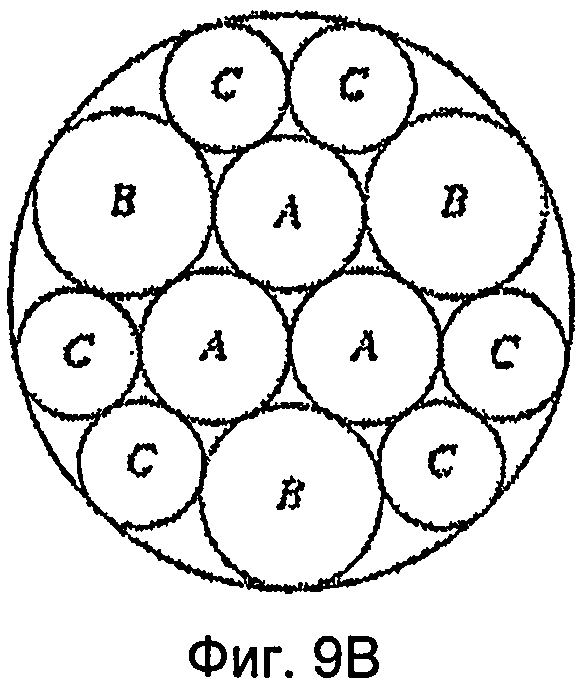
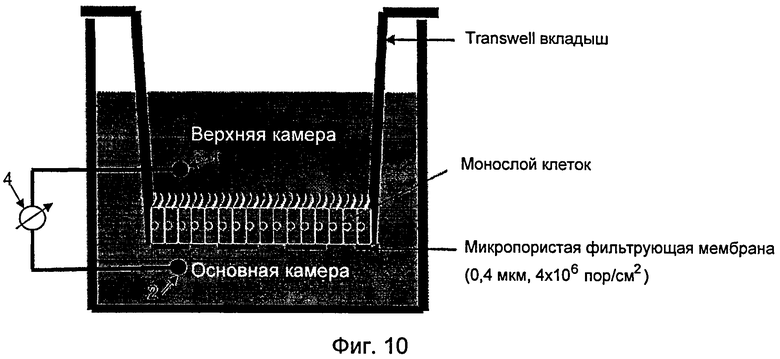
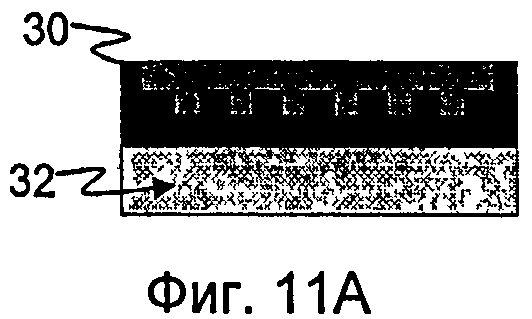
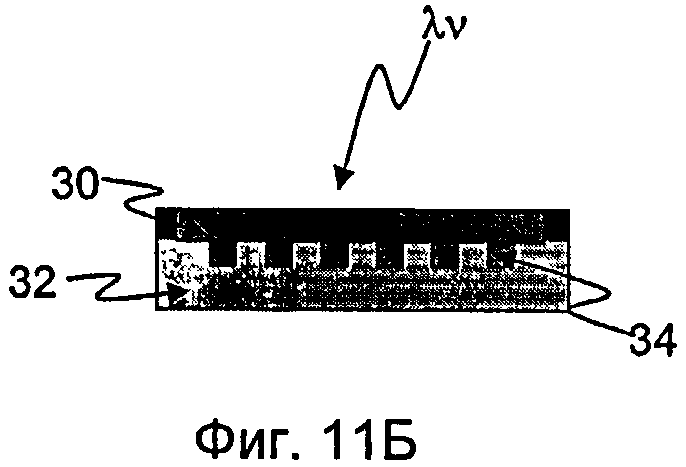
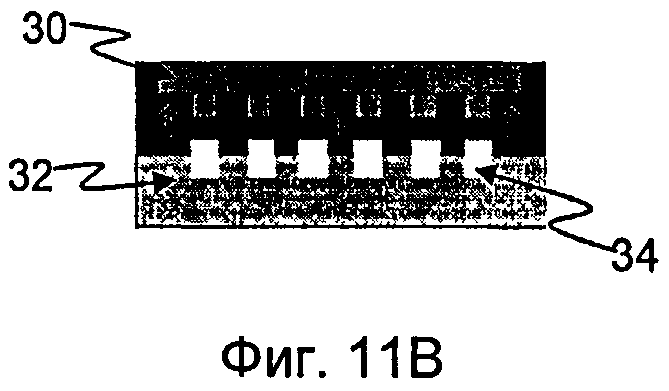

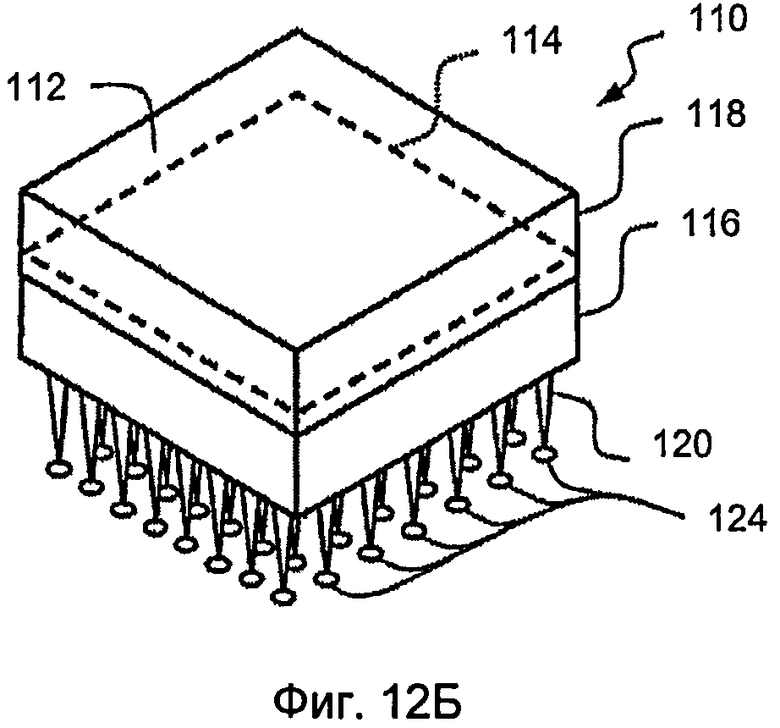
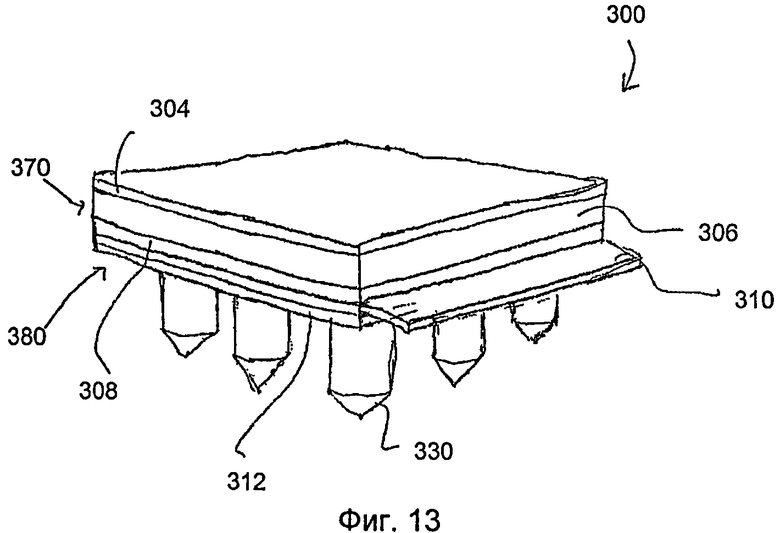

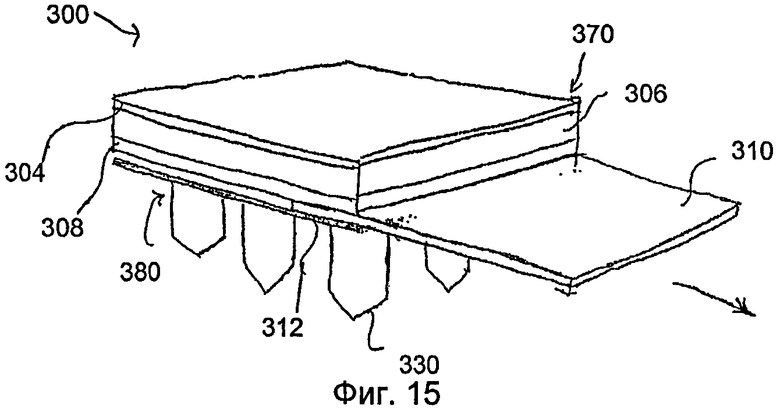
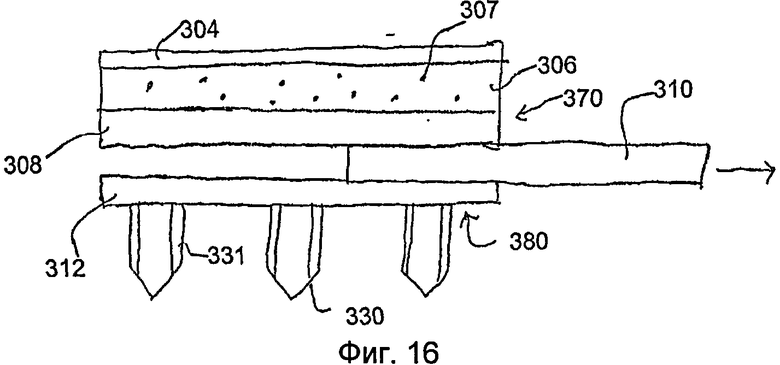
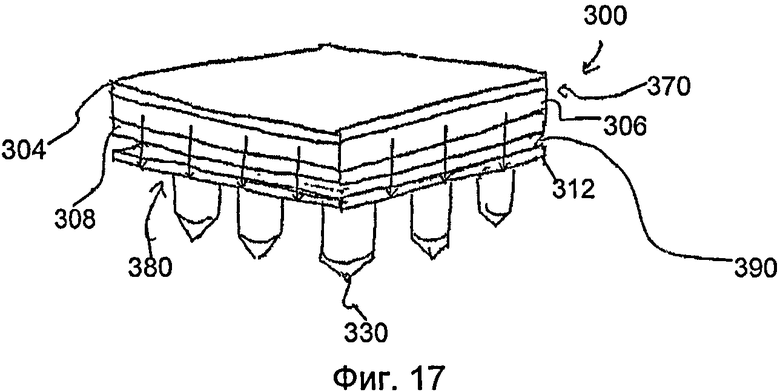
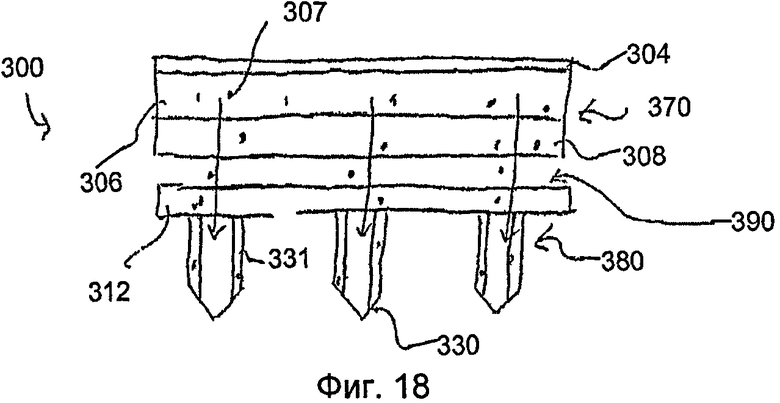

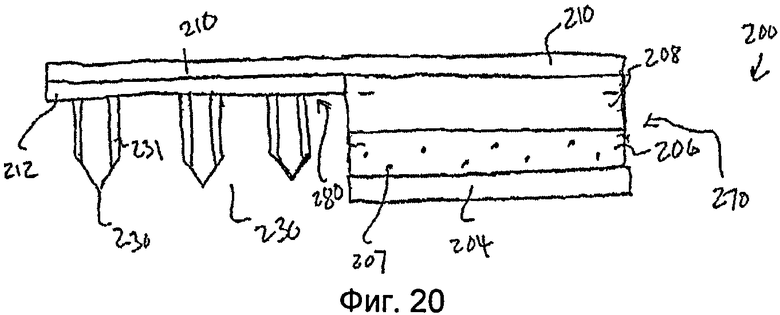
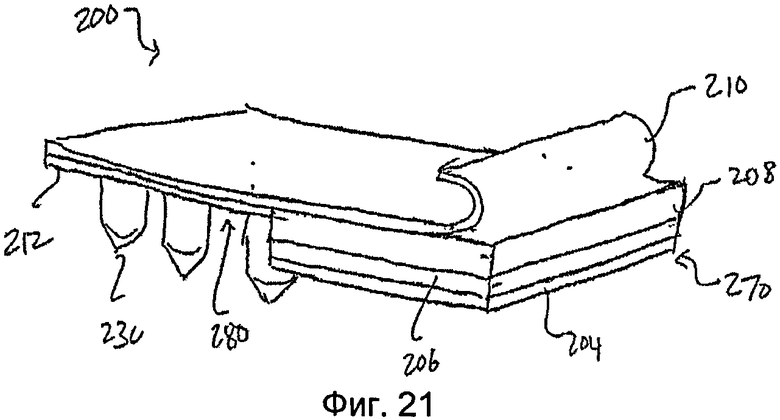
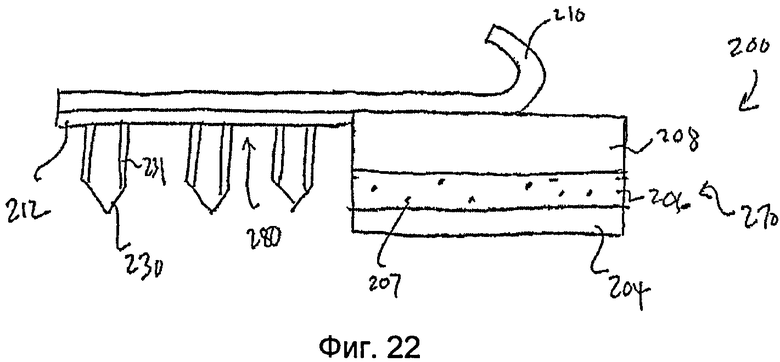
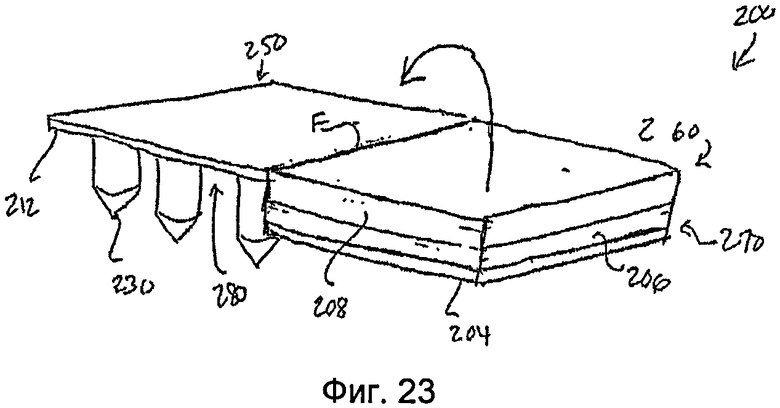

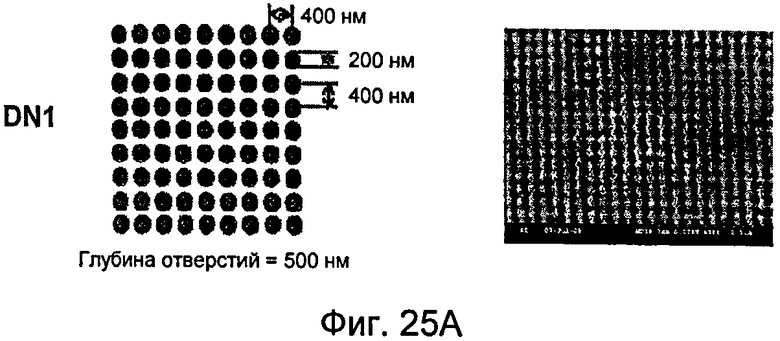
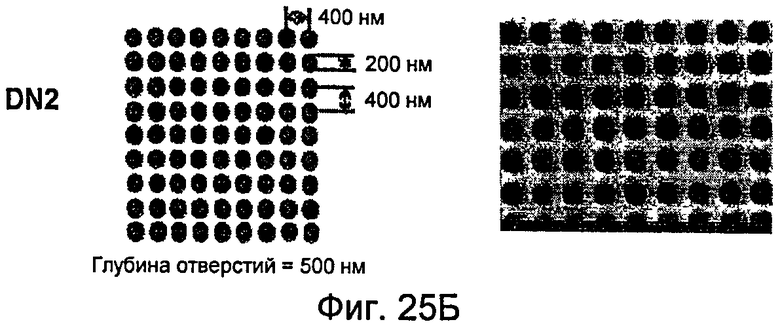
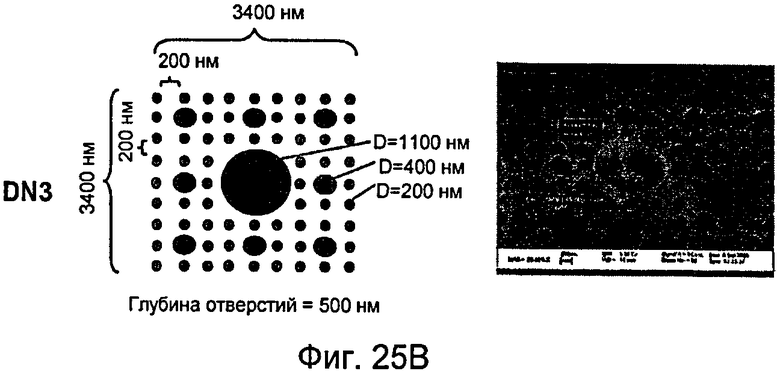


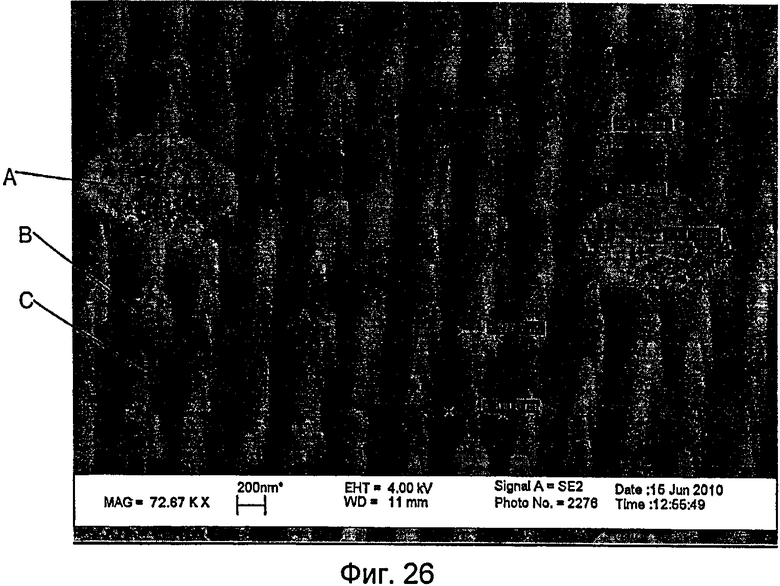



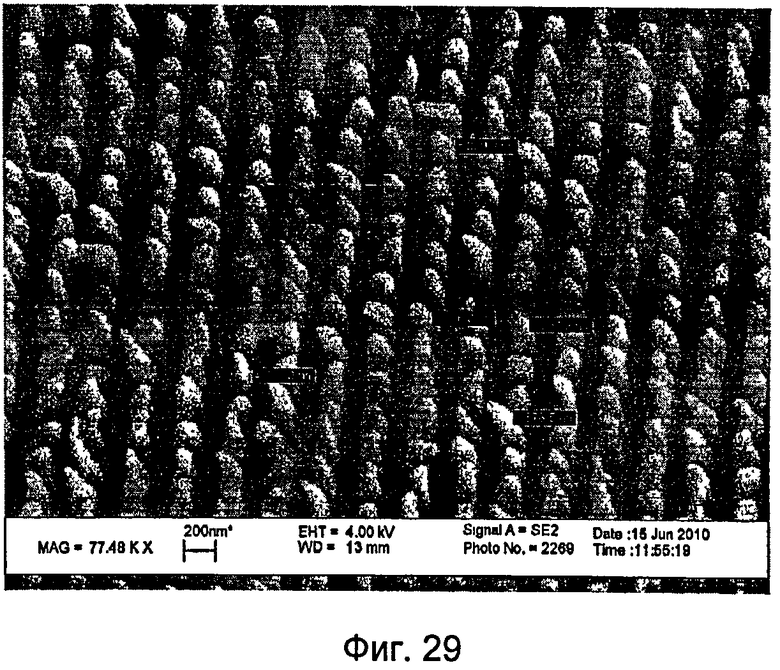

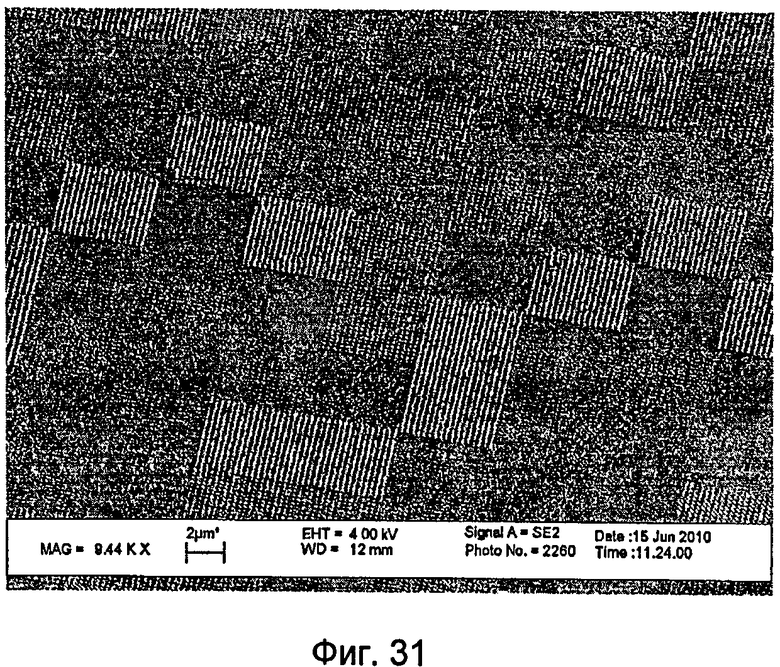



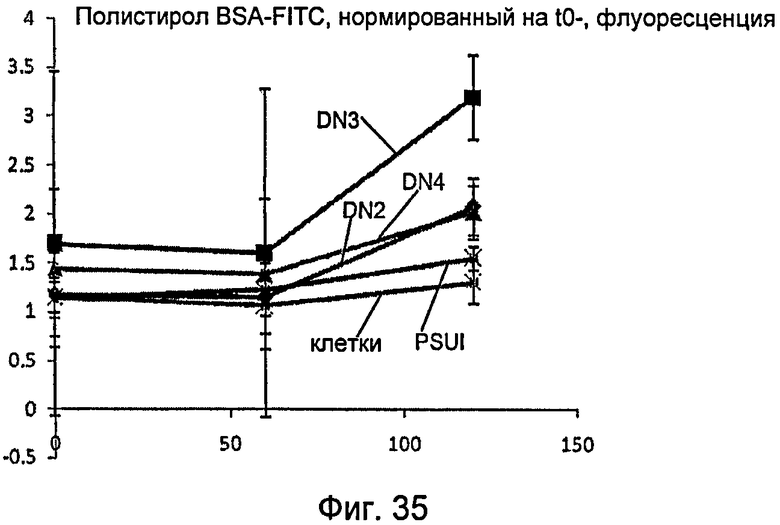

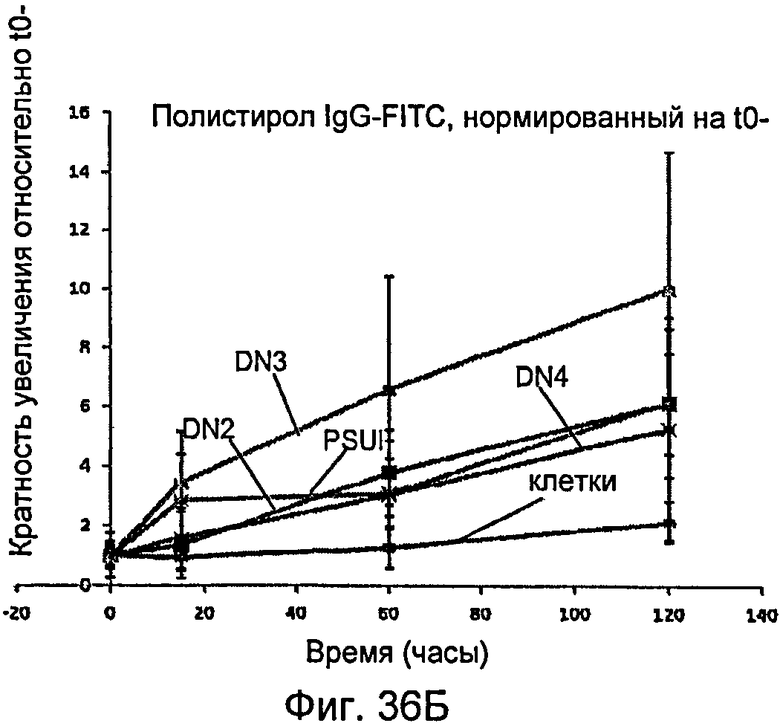

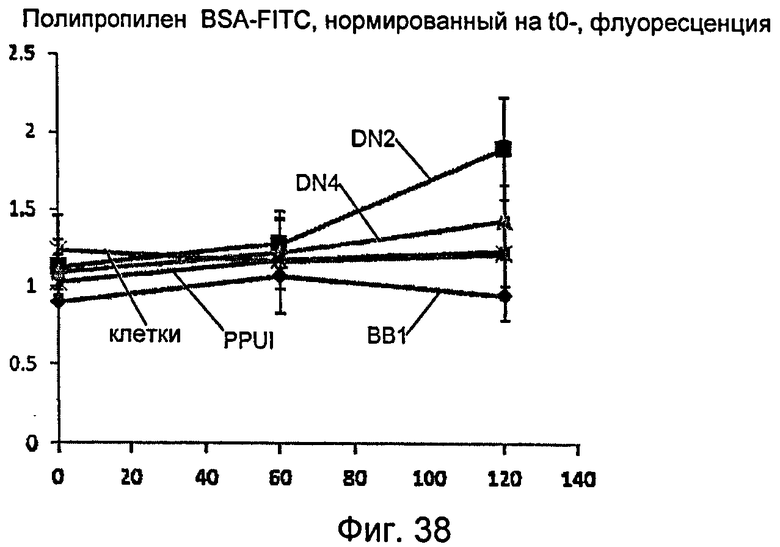
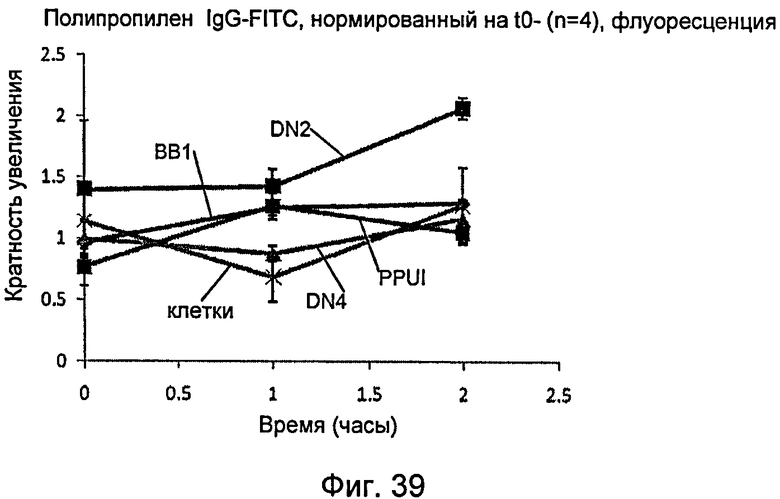


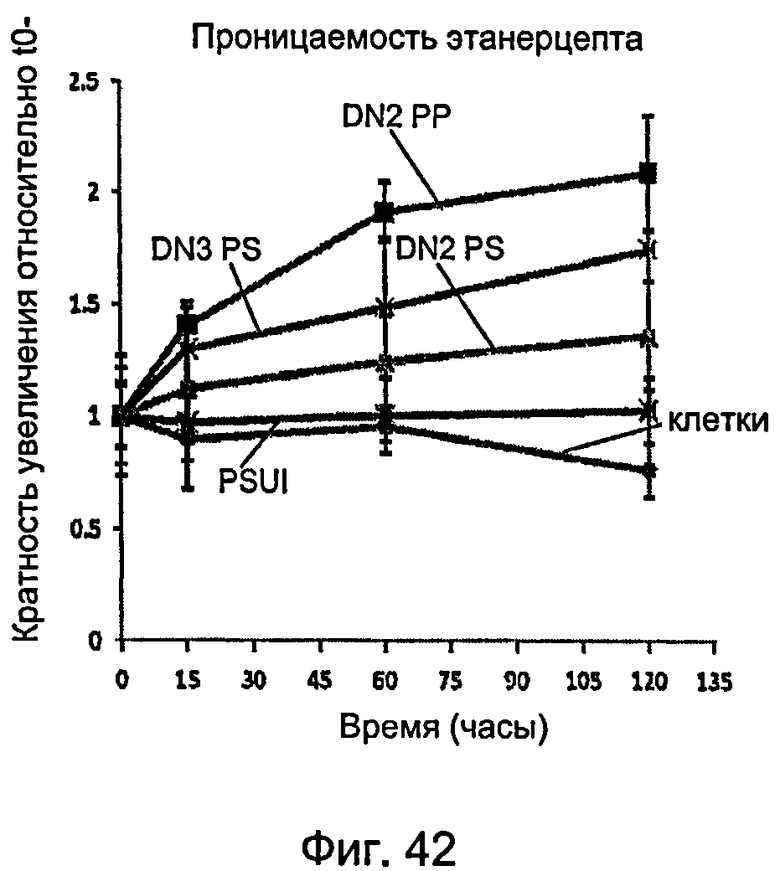



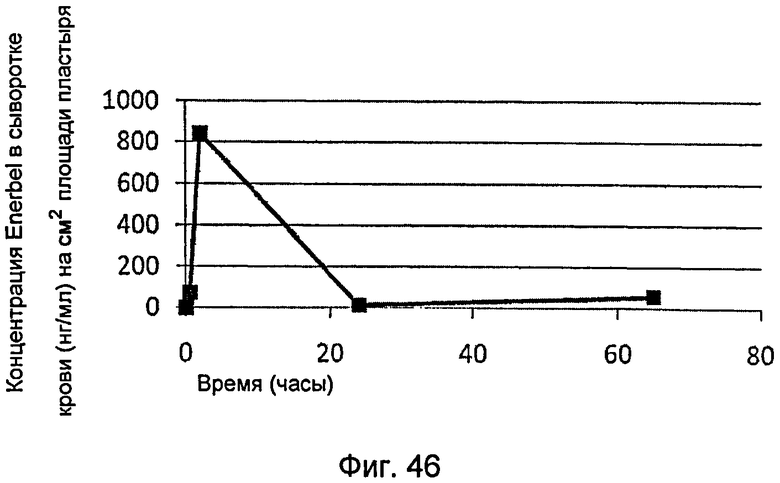


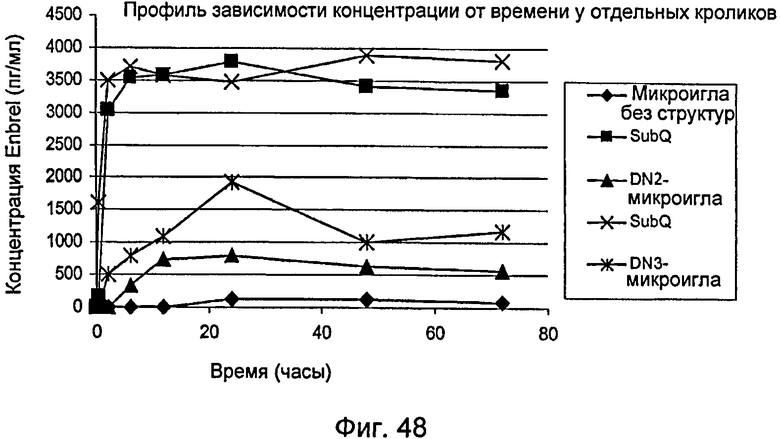
Группа изобретений относится к медицине. Описаны способы и устройства на основе нанотопографии для взаимодействия с компонентом соединительной ткани дермы. Устройства содержат структуры, изготовленные на поверхности, для формирования нанотопографии. Произвольный или упорядоченный узор из структур может быть изготовлен в виде сложного узора, включающего структуры разного размера и/или формы. Микроиглы могут быть успешно использованы для доставки препарата в клетку или ткань. Устройства могут быть использованы, чтобы напрямую или опосредованно менять поведение клетки посредством взаимодействия изготовленной нанотопографии с цитоплазматической мембраной клетки и/или с компонентом внеклеточной матрицы. 3 н. и 17 з.п. ф-лы, 48 ил., 11 табл.
1. Медицинское устройство, содержащее массив микроигл, выступающих наружу из опоры, в котором по меньшей мере одна из микроигл содержит первое множество отдельных наноструктур, сформированных на ее поверхности, причем первые наноструктуры образуют предварительно определенный узор и имеют форму столбиков.
2. Медицинское устройство по п. 1, в котором, по меньшей мере, участок наноструктур обладает размером в поперечном сечении меньше примерно 500 и больше примерно 5 нм или размером в поперечном сечении меньше примерно 300 и больше примерно 100 нм или обладает приблизительно тем же самым размером в поперечном сечении.
3. Медицинское устройство по п. 1, в котором узор дополнительно содержит микроструктуры, причем первые наноструктуры обладают размером в поперечном сечении меньше, чем микроструктуры, например микроструктуры обладают размером в поперечном сечении больше примерно 500 нм.
4. Медицинское устройство по п. 3, дополнительно содержащее вторые наноструктуры с размером в поперечном сечении меньше размера в поперечном сечении микроструктур и больше размера в поперечном сечении первых наноструктур.
5. Медицинское устройство по п. 1, в котором промежуток между центрами, по меньшей мере, части наноструктур составляет от примерно 50 нм до примерно 1 мкм.
6. Медицинское устройство по п. 1, в котором отношение размера в поперечном сечении двух соседних наноструктур к промежутку между центрами этих двух структур составляет от примерно 1:1 до примерно 1:4.
7. Медицинское устройство по п. 1, в котором, по меньшей мере, на некотором участке наноструктуры расположены с равным промежутком между ними.
8. Медицинское устройство по п. 1, в котором, по меньшей мере, на некотором участке наноструктуры обладают высотой от примерно 10 нм до примерно 20 мкм или от примерно 100 до примерно 700 нм.
9. Медицинское устройство по п. 1, в котором, по меньшей мере, на некотором участке наноструктуры обладают отношением размеров от примерно 0,15 до примерно 30 или от примерно 0,2 до примерно 5.
10. Медицинское устройство по п. 1, в котором узор обладает фрактальным размером больше примерно 1, например от примерно 1,5 до примерно 2,5.
11. Медицинское устройство по п. 1, в котором поверхность микроигл содержит множество наноструктур, обладающих одной или несколькими из следующих характеристик: средняя шероховатость поверхности от примерно 10 до примерно 200 нм, эффективный модуль сжатия от примерно 4 до примерно 320 МПа, эффективный модуль сдвига от примерно 0,2 до примерно 50 МПа и краевой угол смачивания от примерно 80° до примерно 150°.
12. Медицинское устройство по п. 1, дополнительно содержащее емкость для удержания лекарственного соединения, например лекарственное соединение обладает молекулярной массой больше примерно 100 кДа.
13. Медицинское устройство по п. 12, в котором лекарственное соединение представляет собой белковое терапевтическое средство, например TNF-α блокатор.
14. Медицинское устройство по п. 1, в котором по меньшей мере одна из микроигл содержит канал для доставки лекарственного соединения.
15. Способ доставки лекарственного соединения в субдермальную область, способ включает:
проникновение через роговой слой микроиглы, которая представляет собой канал текучей среды для лекарственного соединения, причем микроигла содержит первое множество отдельных наноструктур в форме столбиков, сформированных на ее поверхности и образующих узор; и
транспортировку лекарственного соединения через микроиглу и через роговой слой.
16. Способ по п. 15, дополнительно включающий приведение белка внеклеточной матрицы, белка цитоплазматической мембраны, такого как белок фокальной адгезии, опосредующего эндоцитоз рецептора или трансмембранного белка или их комбинации в контакт с наноструктурами.
17. Способ по п. 15, в котором наноструктуры меняют или проводимость мембраны клетки, или структуру внутриклеточного соединения, такую как плотный контакт, или и то, и другое.
18. Способ по п. 15, в котором лекарственное соединение доставляется в цитоплазму клетки или оболочку ядра клетки.
19. Способ формирования медицинского устройства, включающий изготовление узора из первых отдельных наноструктур в форме столбиков на поверхности микроиглы.
20. Способ по п. 19, в котором узор из наноструктур изготовлен по способу, выбранному из группы, состоящей из фотолитографской печати, электронно-лучевой литографской печати, рентгеновской литографской печати, способов самосборки, реактивного ионного травления, мокрого травления, напыления пленок, металлизации напылением, осаждения паров химических веществ, эпитаксии, электроосаждения, литографской печати с наноимпринтингом и их комбинаций.
| US 20080108958 A1, 08.05.2008 | |||
| US 20040028875 A1, 12.02.2004 | |||
| US 20100076035 A1, 25.03.2010 | |||
| ТРАНСКОРНЕАЛЬНАЯ СИСТЕМА ВЫСВОБОЖДЕНИЯ ЛЕКАРСТВА | 1996 |
|
RU2209640C2 |
| УСТРОЙСТВО И СПОСОБ ДЛЯ ПРОКАЛЫВАНИЯ КОЖИ МИКРОВЫСТУПАМИ | 2001 |
|
RU2275871C2 |
Авторы
Даты
2015-09-10—Публикация
2011-04-27—Подача