Область техники, к которой относится изобретение
В общем, настоящее изобретение относится к получению и применению композиций внеклеточного матрикса или кондиционированной среды и конкретнее к композициям и/или белкам, полученным культивированием клеток в гипоксических условиях в подходящей культуральной среде.
Уровень техники
Внеклеточный матрикс (ECM) представляет собой сложное структурное образование, окружающее и поддерживающее клетки, которые имеют место в условиях in vivo в тканях млекопитающих. Часто ECM относят к соединительной ткани. В основном ECM состоит из трех основных классов биологических молекул, включающих структурные белки, такие как коллагены и эластины, специализированные белки, такие как фибриллины, фибронектины и ламинины, и протеогликаны.
В данной области описано культивирование композиций ECM в условиях in vitro и их использование в различных терапевтических и медицинских применениях. Одно из подобных терапевтических применений таких композиций ECM включает лечение и восстановление дефектов мягких тканей и кожи, таких как морщины и рубцы.
Доказано, что восстановить или аугментировать дефекты мягких тканей, вызванных такими причинами, как угри, хирургический шов или старение, очень трудно. С различным успехом использовался ряд материалов для коррекции дефектов мягких тканей, однако отсутствует материал, который был бы полностью безопасным и эффективным. Например, силикон вызывает различные физиологические и клинические проблемы, включая продолжительные побочные эффекты, такие как образование узелков, рецидивирующий целлюлит и кожные язвы.
Коллагеновые композиции также применяли в качестве инъекционного материала для аугментации мягких тканей. Коллаген представляет собой основной белок соединительной ткани и является наиболее распространенным белком у млекопитающих, составляя 25% от общего содержания белков. В настоящее время имеется 28 типов коллагена, описанных в литературе (смотри таблицы 1 и 2 ниже, подробный перечень). Однако более 90% коллагена в организме составляют коллагены I, II, III и IV.
Для лечения дефектов мягких тканей использовали различные коллагеновые материалы, такие как восстановленный инъекционный бычий коллаген, поперечно сшитый коллаген или другие ксеногенные коллагены. Однако существует несколько проблем с такими коллагенами. Наиболее распространенной проблемой является сложность и высокая стоимость получения имплантационных материалов для удаления потенциально иммуногенных веществ во избежание проявления аллергических реакций у субъекта. Кроме того, эффект лечения с использованием таких коллагенов был непродолжительным.
Также были описаны другие материалы, которые можно использовать для восстановления или аугментации мягких тканей, такие как биосовместимые керамические частицы в водных гелях (патент США № 5204382), термопластичные и/или термореактивные материалы (патент США № 5278202) и полимерные смеси на основе молочной кислоты (патент США № 4235312). Кроме того, описано применение композиций на основе естественно секретируемого ECM (патент США № 6284284). Однако все такие материалы имеют ограничения.
Следовательно, необходимы новые материалы для восстановления или аугментации мягких тканей, чтобы преодолеть недостатки материалов предшествующего уровня.
Существует потребность в обеспечении безопасного, инъекционного, долговечного, биоабсорбируемого материала для восстановления и аугментации мягких тканей.
Культивируемые в условиях in vitro композиции на основе ECM также можно использовать для лечения поврежденной ткани, такой как поврежденная ткань сердечной мышцы и связанная ткань. Композиции являются пригодными в качестве имплантатов или биологических покрытий на имплантируемых устройствах, таких как стенты; сосудистые протезы для обеспечения васкуляризации в органах, таких как сердце и близкая ткань, и устройства, пригодные для лечения грыжи, восстановления мышц тазового дна, заживления ран и восстановления вращательной манжеты плеча, такие как пластыри и тому подобное.
Коронарная болезнь сердца (CHD), также называемая болезнью коронарных артерий (CAD), ишемической болезнью сердца и атеросклеротической болезнью сердца, характеризуется сужением мелких кровеносных сосудов, которые доставляют кровь и кислород к сердцу. Причиной коронарной болезни сердца обычно является состояние, называемое атеросклерозом, которое имеет место, когда жировое вещество и бляшки откладываются на стенках артерий, вызывая сужение артерий. По мере сужения артерий поток крови к сердцу может замедлиться или вовсе прекратиться, вызвав боль в области грудной клетки (стабильную стенокардию), дыхательную недостаточность, сердечный приступ и другие симптомы.
Коронарная болезнь сердца (CHD) является основной причиной смерти женщин и мужчин в США. По данным Американской Ассоциации Сердца более 15 млн. людей страдают определенной формой заболевания. Несмотря на то, что симптомы и признаки коронарной болезни сердца проявляются на поздней стадии заболевания, у большинства субъектов с коронарной болезнью сердца в течение десятилетий не проявляются признаки заболевания по мере прогрессирования болезни до того, как происходят внезапный сердечный приступ. Болезнь является наиболее частой причиной внезапной смерти и также наиболее частой причиной смерти мужчин и женщин в возрасте старше 20 лет. Согласно имеющимся в настоящее время прогнозам в США у половины здоровых мужчин в возрасте 40 лет в будущем разовьется CHD, а также у одной из трех здоровых 40-летних женщин.
Существующие в настоящее время способы улучшения кровотока в больном или пораженном иначе сердце включают инвазивные хирургические методы, такие как коронарное шунтирование, ангиопластика и эндартерэктомия. Для таких методов естественно характерна большая степень риска во время и после операции, и часто обеспечивается только временное улучшение состояния сердца при ишемии. Следовательно, необходимы новые варианты лечения для повышения эффективности имеющихся в настоящее время способов лечения CHD и близких заболеваний.
Культивируемые в условиях in vitro композиции ECM также можно использовать для восстановления и/или регенерации поврежденных клеток или ткани, таких как хрящевые или остеохондральные клетки. Остеохондральная ткань представляет собой любую ткань, которая относится или содержит кость или хрящ. Композиции по настоящему изобретению подходят для лечения остеохондральных дефектов, таких как дегенеративные заболевания соединительной ткани, такие как ревматоидный артрит и/или остеоартрит, а также дефектов у пациентов с хрящевыми поражениями в результате травмы.
Существующие в настоящее время попытки восстановления остеохондральных дефектов включают имплантацию человеческих хондроцитов в биосовместимых и биодеградируемых гидрогелевых трансплантатах для улучшения возможностей восстановить участки поражения хрящей суставов. Кроме того, описан способ культивирования хондроцитов на альгинатных шариках или матриксе, содержащих полисульфатированный альгинат, для получения гиалиноподобной хрящевидной ткани. Однако попытки восстановления энхондральных участков поражения суставного хряща посредством имплантации человеческих аутологичных хондроцитов имеют ограниченный успех. Следовательно, требуются новые варианты лечения для повышения эффективности существующих в настоящее время способов лечения остеохондральных дефектов.
Культивируемые в условиях in vitro композиции ECM также пригодны в системах тканевых культур для получения ткане-инженерных имплантатов. Область тканевой инженерии включает применение технологии культивирования клеток для получения новых биологических тканей или восстановления поврежденных тканей. Технология тканевой инженерии, начатая в прошлом с революционного применения стволовых клеток, предлагает возможность регенерации и замещения тканей после травмы или при лечении дегенеративных заболеваний. Также ее можно использовать в отношении косметических процедур.
Способы тканевой инженерии можно использовать для получения аутологичной и гетерологичной ткани или клеток с использованием различных типов клеток и методов культивирования. При создании аутологичного имплантата донорную ткань можно отобрать и разделить на отдельные клетки и затем присоединить и культивировать на субстрате, предназначенном для имплантации в требуемую область функционирующей ткани. Многие типы выделенных клеток можно культивировать в условиях in vitro, используя методы культивирования клеток, однако для прикрепления клеток, зависимых от якорной подложки, требуются специфические окружающие условия, часто включающие наличие трехмерной поддерживающей структуры, служащей в качестве матрикса для роста.
Существующая в настоящее время технология тканевой инженерии в основном обеспечивает искусственные имплантаты. Терапия на основе эффективной трансплантации клеток зависит от разработки подходящих субстратов для культивирования тканей в условиях in vitro и in vivo. Таким образом, разработка ECM, который содержит только природные вещества и подходит для имплантации, будет обеспечивать больше характеристик эндогенной ткани. Следовательно, создание материала на основе природного ECM представляет собой актуальную задачу в области тканевой инженерии.
Сущность изобретения
Настоящее изобретение частично основано на основополагающем обнаружении того, что клетки, культивированные (например, в двумерных или трехмерных координатах) в условиях, стимулирующих эмбриональное развитие на ранних стадиях (например, гипоксия и низкие гравитационные силы), обеспечивают композиции ECM с эмбриональными свойствами. Композиции ECM, полученные культивированием клеток в гипоксических условиях, содержащие один или более эмбриональных белков, имеют различные полезные применения.
В одном варианте осуществления настоящее изобретение относится к способу получения композиций ECM, содержащих один или более эмбриональных белков. Способ включает культивирование клеток в гипоксических условиях (например, двумерный или трехмерный рост) в подходящей культуральной среде с получением растворимой и нерастворимой фракции. В различных аспектах композиции включают растворимую и нерастворимую фракцию по отдельности, а также комбинации растворимой и нерастворимой фракций. В различных аспектах полученные композиции включают активацию экспрессии генов и продукции ламининов, коллагенов и факторов Wnt. В еще одних аспектах полученные композиции включают подавление экспрессии генов ламининов, коллагенов и факторов Wnt. В еще одних аспектах композиции являются видоспецифическими и содержат клетки и/или биологическое вещество от одного вида животного. Несмотря на то, что культивированные in vitro композиции ECM пригодны для лечения людей, композиции можно использовать для других видов животных. Следовательно, такие композиции хорошо подходят для ветеринарных применений.
В еще одном варианте осуществления настоящее изобретение относится к способу получения белка Wnt и фактора роста сосудистого эндотелия (VEGF). Способ включает культивирование клеток в гипоксических условиях (например, двумерный или трехмерный рост) в подходящей культуральной среде с получением тем самым белка Wnt и VEGF. В различных аспектах культуральная среда представляет бессывороточную среду, и гипоксические условия включают 1-5% кислорода. В близких аспектах типы Wnt позитивно регулируются по сравнению со средой, полученной в условиях с нормальным содержанием кислорода, составляющим 15-20% кислорода. В приведенном в качестве примера аспекте типы Wnt представляют собой wnt 7a и wnt 11. В других вариантах осуществления кондиционированную среду выделяют в качестве композиции, содержащей различные белки, как описано в данном документе.
В еще одном варианте осуществления настоящее изобретение относится к способу восстановления и/или регенерации клеток контактированием клеток, предназначенных для восстановления или регенерации, с композициями ECM, описанными в данном документе. В одном аспекте клетки представляют остеохондральные клетки. Следовательно, способ предполагает восстановление остеохондральных дефектов.
В еще одном варианте осуществления композиции ECM являются пригодными в качестве имплантатов или биологических покрытий на имплантируемых устройствах. В различных аспектах композиции по настоящему изобретению включаются в имплантаты или применяются в качестве биологических покрытий на имплантируемых устройствах, таких как стенты и сосудистые протезы, для стимуляции васкуляризации в органах, таких как сердце и близкие ткани. В близком аспекте композиции включаются в пластыри или имплантаты для регенерации тканей, пригодные для лечения грыжи, восстановления тазового дна, заживления ран и восстановления вращательной манжетки плеча и тому подобное.
В еще одном варианте осуществления настоящее изобретение относится к способу улучшения поверхности кожи у субъекта, включающему введение субъекту в область морщины композиции ECM или кондиционированной среды, описанных в одном документе. В еще одном варианте осуществления настоящее изобретение включает способ восстановления или аугментации мягких тканей у субъекта, включающий введение субъекту в область морщины композиций ECM, описанных в одном документе.
В еще одном варианте осуществления настоящее изобретение относится к системам тканевых культур. В различных аспектах культуральная система состоит из композиций ECM или культивированной среды, описанных в данном документе, на двумерных или трехмерных подложках. В еще одном аспекте композиции ECM, описанные в данном документе, служат в качестве подложки или двумерной или трехмерной подложки для роста клеток различных типов. Например, культуральную систему можно использовать для поддержания роста стволовых клеток. В одном аспекте стволовые клетки представляют эмбриональные стволовые клетки, мезенхимальные стволовые клетки и нейрональные стволовые клетки.
В еще одном варианте осуществления композиции по настоящему изобретению можно использовать для обеспечения поверхностного покрытия, используемого в ассоциации с имплантацией устройства субъекту, для стимуляции эндотелизации и васкуляризации.
В еще одном варианте осуществления изобретение относится к получению стволовых клеток культивированием клеток (например, фибробластов, в гипоксических условиях), с получением тем самым клеток, экспрессирующих гены, характерные для стволовых клеток на уровне, по меньшей мере, в 3 раза выше по сравнению с культивированием в нормальных кислородных условиях. Такие гены могут включать, например, гены Oct4, Sox2, KLF4, NANOG и cMyc.
Стволовые клетки, полученные способом по изобретению, предпочтительно являются плюрипотентными. Можно использовать любые стромальные или нестволовые клетки в качестве клеток исходного типа.
В еще одном варианте осуществления композиции по настоящему изобретению можно использовать для обеспечения способа лечения поврежденной ткани. Способ включает контактирование поврежденной ткани с композицией, полученной культивированием клеток в гипоксических условиях на двухмерной или трехмерной подложке, содержащей один или более эмбриональных белков, в условиях, которые позволяют лечить поврежденную ткань.
В еще одном варианте осуществления настоящее изобретение относится к биологическому носителю для доставки или поддержания клеток в месте доставки, включающему композиции ECM, описанные в данном документе. Носитель можно использовать в таких применениях, как инъекционное введение клеток, таких как стволовые клетки, в поврежденную сердечную мышцу или для восстановления сухожилия и связки.
В еще одном варианте осуществления настоящее изобретение относится к способу стимуляции или активации роста волос. Способ включает контактирование клетки с композициями ECM или кондиционированной средой, описанными в данном документе. В приведенном в качестве примера аспекте клетка представляет клетку волосяного фолликула. В различных аспектах клетка может контактировать в условиях in vivo или ex vivo.
Краткое описание чертежей
На фигуре 1 показано графическое представление образования FBGC через 2 недели после имплантации полипропиленовой сетки, покрытой hECM. На фигуре 1а показано количество FBGC на волокно через 2 недели после имплантации непокрытых (первая колонка) и покрытых hECM волокон (вторая колонка). На фигуре 1В показано количество FBGC на волокно через 2 недели после имплантации непокрытых (колонки 1-3) и покрытых ECM волокон (колонки 4-6). * указывает р<0,05.
На фигуре 2 показано графическое представление образования FBGC через 5 недель после имплантации полипропиленовой сетки, покрытой hECM. На фигуре 2а показано количество FBGC на волокно через 5 недель после имплантации непокрытых (первая колонка) и покрытых hECM волокон (вторая колонка). На фигуре 2В показано количество FBGC на волокно через 5 недель после имплантации непокрытых (колонки 1 и 3) и покрытых ECM волокон (колонки 2 и 4).
На фигуре 3 показаны клетки волосяных фолликулов человека. На фигуре 3А показаны клетки волосяных фолликулов человека после культивирования клеток в течение четырех недель в присутствии hECM и последующей трансплантации мыши и рост еще в течение 4 недель, в то время как на фигуре 3В показаны клетки контрольных фолликулов.
На фигуре 4 приведено графическое представление метаболического ответа фибробластов на композиции внеклеточного матрикса (мышиного ECM и человеческого ECM) по данным МТТ-теста.
На фигуре 5 приведено графическое представление числа клеток в ответ на воздействие на фибробласты hECM по данным теста Pico Green.
На фигуре 6 приведено графическое представление оценки эритемы у 41 субъекта на 3; 7 и 14 сутки после лазерной обработки кожи. Степень эритемы оценивали по шкале от 0 (отсутствие) до 4 (сильная). Каждая группа из 4 рядов данных (0,1X hECM, 1X hECM, 10X hECM и контроль слева направо) представляет результаты оценки на сутки 3 (слева), 7 (в середине) и 14 (справа).
На фигуре 7 приведено графическое представление оценки отека у 41 субъекта на 3; 7 и 14 сутки после лазерной обработки кожи. Степень эритемы оценивали по шкале от 0 (отсутствие) до 2,5 (сильная). Каждая группа из 4 рядов данных (0,1X hECM, 1X hECM, 10X hECM и контроль слева направо) представляет результаты оценки на сутки 3 (слева), 7 (в середине) и 14 (справа).
На фигуре 8 приведено графическое представление оценки образования корки у 41 субъекта на 3; 7 и 14 сутки после лазерной обработки кожи. Степень эритемы оценивали по шкале от 0 (отсутствие) до 3,5 (сильная). Каждая группа из 4 рядов данных (0,1X hECM, 1X hECM, 10X hECM и контроль слева направо) представляет результаты оценки на сутки 3 (слева), 7 (в середине) и 14 (справа).
На фигуре 9 приведено графическое представление оценки трансэпидермальной потери влаги (TWEL) у 41 субъекта на 3; 7 и 14 сутки после лазерной обработки кожи. Степень TWEL оценивали по шкале от 0 (отсутствие) до 4 (сильная). Каждая группа из 4 рядов данных (0,1X hECM, 1X hECM, 10X hECM и контроль слева направо) представляет результаты оценки на сутки 3 (слева), 7 (в середине) и 14 (справа).
На фигуре 10 приведено графическое изображение трехмерной профилометрии силиконовых отпечатков из периокулярной области. Данные получали от 22 субъектов до лазерной обработки кожи, через 4 недели после обработки и через 10 недель после обработки. Данные серии А представляют значения при введении hECM; данные серии В представляют контроль.
На фигуре 11 приведено графическое представление результатов анализа применения вазелина после лазерной обработки кожи.
На фигуре 12 приведено графическое представление оценки кожной эритемы по данным, полученным на 0; 3; 5; 7; 10 и 14 сутки после лазерной обработки кожи.
На фигуре 13 приведено графическое представление мексаметрического анализа на 0; 3; 5; 7; 10 и 14 сутки после лазерной обработки кожи.
На фигуре 14 показано графическое представление образования FBGC через 2 недели после имплантации полипропиленовой сетки, покрытой hECM. На фигуре 14А показано количество FBGC на волокно через 2 недели после имплантации непокрытых (первая колонка) и покрытых hECM волокон (вторая колонка). На фигуре 14В показано количество FBGC на волокно через 5 недель после имплантации непокрытых и покрытых ECM волокон.
На фигуре 15 показано графическое представление образования FBGC через 5 недель после имплантации полипропиленовой сетки, покрытой hECM. На фигуре 15А показано количество FBGC на волокно через 5 недель после имплантации непокрытых (первая колонка) и покрытых hECM волокон (вторая колонка). На фигуре 15В показано количество FBGC на волокно через 5 недель после имплантации непокрытых и покрытых ECM волокон.
На фигуре 16 показано графическое представление средней толщины фиброзной капсулы через 2 недели после имплантации полипропиленовой сетки, покрытой hECM. На фигуре 16А показана средняя толщина фиброзной капсулы через 2 недели после имплантации непокрытых (первая колонка) и покрытых hECM волокон (вторая колонка). На фигуре 16В показана средняя толщина фиброзной капсулы через 2 недели после имплантации непокрытых и покрытых ECM волокон.
На фигуре 17 показано графическое представление средней толщины фиброзной капсулы через 5 недель после имплантации полипропиленовой сетки, покрытой hECM. На фигуре 17А показана средняя толщина фиброзной капсулы через 5 недель после имплантации непокрытых (первая колонка) и покрытых hECM волокон (вторая колонка). На фигуре 17В показана средняя толщина фиброзной капсулы через 5 недель после имплантации непокрытых и покрытых ECM волокон.
На фигуре 18 приведена гистограмма, показывающая характеристики роста волос после введения hECM, содержащего wnt 7a.
На фигуре 19 приведены таблицы, показывающие характеристики роста волос у двух субъектов, принимающих участие в испытании, через 12 недель после начала исследования по оценке эффективности введения hECM, содержащего wnt 7a.
На фигуре 20 приведены таблицы, показывающие характеристики роста волос у двух субъектов, принимающих участие в испытании, через 22 недели после начала исследования по оценке эффективности введения hECM, содержащего wnt 7a.
На фигуре 21 показано графическое представление результатов по агрегатам у контрольных субъектов по сравнению с субъектами, подвергшимися лечению, не включающему пертурбацию. На фигуре 21А приведены результаты на 3 месяца. На фигуре 21В приведены результаты на 5 месяцев.
На фигуре 22 показано графическое представление результатов по агрегатам у контрольных субъектов по сравнению с субъектами, подвергшимися лечению, не включающему пертурбацию. На фигуре 22А приведены результаты на 3 месяца. На фигуре 22В приведены результаты на 5 месяцев.
На фигуре 23 показано графическое представление распределения ответов у субъектов на лечение hECM по плотности терминальных волос через 3 месяца.
На фигуре 24 показано графическое представление распределения ответов у субъектов на лечение hECM по плотности пушковых волос через 3 месяца.
На фигуре 25 показано графическое представление распределения ответов у субъектов на лечение hECM по плотности толщине волос через 3 месяца.
На фигуре 26 показано графическое представление распределения ответов у субъектов на лечение hECM по средним значениям толщины волос через 3 месяца.
На фигуре 27 показано графическое представление оценки роста волос.
На фигуре 28 показано графическое представление данных инфракрасной спектроскопии с преобразованием Фурье (FTIR).
Подробное описание изобретения
Настоящее изобретение относится к способу получения композиций ECM или кондиционированной среды, содержащих один или более эмбриональных белков. В частности, композиции получают культивированием клеток в гипоксических условиях (например, двумерный или трехмерный рост) в подходящей культуральной среде. С помощью способа культивирования получают растворимую и нерастворимую фракцию, которые можно использовать по отдельности или в комбинации, с получением физиологически приемлемых композиций, имеющих различные применения.
На деление, дифференцировку и функцию стволовых клеток и мультипотентных клеток-предшественников оказывают влияние сложные сигналы в микросреде, включая доступность кислорода. Сильный недостаток кислорода (гипоксия) возникает в опухолях, например, за счет быстрого клеточного деления и аномального образования кровеносных сосудов. Индуцируемые гипоксией факторы (HIF) опосредуют транскрипционные ответы на локализованную гипоксию в нормальных тканях и в злокачественных опухолях, и могут стимулировать прогрессирование опухолей изменением клеточного метаболизма и стимуляцией ангиогенеза. Недавно было показано, что HIF активируют специфические сигнальные пути, такие как Notch, и экспрессию транскрипционных факторов, таких как Oct4, которые контролируют обновление и мультипотентность самих стволовых клеток. Поскольку полагают, что многие злокачественные опухоли развиваются из небольшого числа трансформированных, самообновляющихся и мультипотентных «раковых стволовых клеток», то на основании этих данных можно предположить о новой роли HIF в развитии опухолей. Данные, приведенные в настоящих примерах, указывают, что клетки, культивированные в гипоксических условиях, экспрессируют гены, обычно ассоциированные с плюрипотентными клетками, например, такие как Oct4, NANOG, Sox2, KLF4 и cMyc.
Композиции по настоящему изобретению имеют различные применения, включая, не ограничиваясь этим, стимуляцию восстановления и/или регенерации поврежденных клеток или тканей, применение в пластырях и имплантатах для стимуляции регенерации тканей (например, для лечения грыжи, восстановления тазового дна, восстановления вращательной манжетки плеча и заживления ран), применение в системах тканевых культур для культивирования клеток, таких как стволовые клетки, применение в поверхностных покрытиях, используемых в ассоциации с имплантируемыми устройствами (например, кардиостимуляторами, стентами, стентовыми трансплантатами, сосудистыми протезами, сердечными клапанами, шунтами, портами для доставки лекарственных препаратов или катетерами, пластырями для лечения грыжи и восстановления тазового дна), стимуляцию восстановления, аугментации мягких тканей и/или улучшения поверхности кожи, такой как морщины, применения после травмы кожи (например, после лазерной обработки), рост волос, применение в качестве биологического антиадгезивного средства или в качестве биологического носителя для доставки или поддержания клеток в месте доставки.
Настоящее изобретение частично основано на установлении того факта, что клетки, культивированные на микрошариках (микроносителях) или трехмерных поддерживающих структурах в условиях, стимулирующих эмбриональное развитие на ранних стадиях (например, гипоксия и низкие гравитационные силы), до ангиогенеза обеспечивают композиции ECM с эмбриональными свойствами, включая синтез эмбриональных белков. Рост клеток в гипоксических условиях демонстрирует уникальный ECM и кондиционированную среду с эмбриональными свойствами и экспрессию ростовых факторов. В отличие от культивирования ECM в обычных условиях культивирования более 5000 генов дифференциально экспрессируется в гипоксических условиях. Это дает культивированный ECM, обладающий другими свойствами и другим биологическим составом. Например, ECM, полученный в гипоксических условиях, аналогичен эмбриональной мезенхимальной ткани в том отношении, что он относительно богат коллагенами типа III, IV и V, и гликопротеинами, такими как фибронектин, SPARC, тромбоспондин и гиалуроновая кислота.
Также гипоксия повышает экспрессию факторов, которые регулируют заживление и органогенез ран, таких как VEGF, FGF-7 и TGF-β, а также многочисленные факторы Wnt, включая wnt 2b, 4, 7a, 10a и 11. Культивированный эмбриональный человеческий ECM также стимулирует повышение метаболической активности в человеческих фибробластах in vitro, что определяли по повышенной ферментативной активности. Кроме того, имеется увеличение числа клеток в ответ на воздействие культивированного эмбрионального ECM.
Перед описанием настоящих композиций и способов, следует указать, что очевидно, понятно, что данное изобретение не ограничивается конкретными описанными композициями, способами и условиями, поскольку такие композиции, способы и условия могут варьировать. Также, очевидно, понятно, что терминология используется в данном документе только для целей описания конкретных вариантов осуществления, и не предназначается для ограничения, поскольку объем настоящего изобретения ограничивается только прилагаемой формулой изобретения.
В том смысле, в котором в данной заявке и прилагаемой формуле изобретения используются единичные формы «а», «an» и «the», они включают многочисленные ссылки, если в контексте четко не указывается иначе. Так, например, обращение к «способу» включает один или более способов и/или стадий типа, описанного в данном документе, которые станут очевидными для специалистов в данной области при ознакомлении с данным раскрытием и так далее.
В различных вариантах осуществления настоящее изобретение относится к способам получения композиций ECM, которые содержат один или более эмбриональных белков, и их применениям. В частности, композиции получают культивированием клеток в гипоксических условиях в подходящей культуральной среде. В настоящем изобретении предусматривается рост в виде монослоев или на шариках/микроносителях. Кроме того, композиции можно получить культивированием клеток на трехмерном каркасе с получением многослойной клеточной культуральной системы. Клетки, культивированные на трехмерном каркасе-подложке согласно настоящему изобретению, растут в виде многочисленных слоев, образуя клеточный матрикс. Рост культивированных клеток в гипоксических условиях приводит к дифференциальной экспрессии генов за счет гипоксических культуральных условий по сравнению с обычным культивированием ECM и кондиционированной среды.
ECM представляет композицию белков и биополимеров, которые в основном составляют ткань, полученную культивированием клеток. Стромальные клетки, такие как фибробласты, являются клетками, зависимыми от якорной подложки, для которых требуется рост при прикреплении к материалам и поверхностям, подходящим для культивирования клеток. Вещества ECM, продуцированные культивированными клетками, откладываются в трехмерном порядке, образуя пространства для образования тканеподобных структур.
Материалы для культивирования, обеспечивающие трехмерные структуры, относятся к поддерживающим структурам. Пространства для отложения ECM находятся в виде отверстий внутри, например, переплетенной сетки, или, если желательно, в виде интерстициальных пространств, имеющихся в компактной конфигурации сферических шариков, называемых микроносителями.
В том смысле, в котором в данном документе используется термин «композиция внеклеточного матрикса», он включает растворимую и нерастворимую фракции или любые их части. Нерастворимая фракция включает секретированные белки ECM и биологические компоненты, которые откладываются на подложке или поддерживающей структуре. Растворимая фракция относится к культуральной среде или кондиционированной среде, в которую клетки секретировали активное вещество(а), и она включает белки и биологические компоненты, которые не откладываются на поддерживающей структуре. Можно собрать обе фракции и затем необязательно обработать, и использовать индивидуально или в комбинации в различных применениях, как описано в данном документе.
Трехмерная подложка или поддерживающая структура, используемая для культивирования стромальных клеток, может быть изготовлена из любого материала и/или может иметь любую форму, которые позволяют клеткам прикрепляться к ней (или ее можно модифицировать для того, чтобы клетки прикреплялись к ней); и позволяет клеткам расти в более чем одном слое (т.е. клетки образуют трехмерную ткань, аналогичную росту ткани в условиях in vitro). В еще одних вариантах осуществления можно использовать по существу двухмерный лист или мембрану для культивирования клеток, которые являются достаточно трехмерными по форме.
Биосовместимый материал формуют в трехмерную структуру или поддерживающую структуру, где структура имеет интерстициальные пространства для прикрепления и роста клеток с образованием трехмерной ткани. Отверстия и/или интерстициальные пространства в каркасе в некоторых вариантах осуществления имеют соответствующий размер для того, чтобы клетки могли прорасти через отверстия или пространства. Оказалось, что поддержание активно растущих клеток, растягивающихся по каркасу, повышает продукцию репертуара ростовых факторов, ответственных за активности, описанные в данном документе. Если отверстия являются слишком маленькими, то клетки могут быстро достичь слияния, но не будут способными легко выйти из сетки. Такие захваченные клетки могут проявлять контактное ингибирование и перестать продуцировать соответствующие факторы, необходимые для поддержания пролиферации и поддержания непрерывных культур. В том случае, если отверстия являются слишком крупными, то клетки могут быть не способны прорасти через отверстия, что может привести к снижению продукции в стромальных клетках соответствующих факторов, необходимых для поддержания пролиферации и поддержания непрерывных культур. Как правило, интерстициальные пространства имеют размер, по меньшей мере, примерно 100 мкм, по меньшей мере, примерно 140 мкм, по меньшей мере, примерно 150 мкм, по меньшей мере, примерно 180 мкм, по меньшей мере, примерно 200 мкм или, по меньшей мере, примерно 220 мкм. При использовании сетчатого типа матрикса, приведенного в качестве примера в данном документе, авторы установили, что отверстия размером в пределах примерно от 100 мкм до примерно 220 мкм будут функционировать удовлетворительно. Однако в зависимости от трехмерной структуры и сложности каркаса возможны другие размеры. Любая форма или структура, позволяющая клеткам простираться и продолжать реплицироваться, и расти в течение длительных периодов времени, может функционировать с продукцией клеточных факторов согласно способам, описанным в данном документе.
В некоторых аспектах трехмерный каркас изготовлен из полимеров или нитей, которые сплетены, закручены, связаны или соединены иначе с образованием каркаса, такого как сетка или ткань. Также материалы можно получить формованием материала или изделия в пену, матрикс или губчатую поддерживающую структуру. В других аспектах трехмерный каркас находится в форме спутанных волокон, полученных прессованием полимеров, или других волокон вместе с получением материала с интерстициальными пространствами. Трехмерный каркас может иметь любую форму или геометрию для роста клеток в культуре. Таким образом, другие формы каркаса, дополнительно описанные ниже, могут подходить для получения соответствующей кондиционированной среды.
Для получения поддерживающей структуры или каркаса можно использовать ряд различных материалов. Такие материалы включают неполимерные и полимерные материалы. Полимеры, когда они применяются, могут представлять любой тип полимера, такой как гомополимеры, статистические полимеры, сополимеры, блок-полимеры, соблок-полимеры (например, ди, три и т.д.), линейные или разветвленные полимеры и сшитые или несшитые полимеры. Неограничивающие примеры материалов, которые можно использовать в качестве поддерживающих структур или каркасов, включают среди прочего, не ограничиваясь этим, стекловолокно, полиэтилены, полипропилены, полиамиды (например, найлон), полиэфиры (например, дакрон), полистиролы, полиакрилаты, поливиниловые производные (например, поливинилхлорид; PVC), поликарбонаты, политетрафторэтилены (PTFE; TEFLON), терманокс (TPX), нитроцеллюлозу, полисахариды (например, целлюлозы, хитозан, агарозу), полипептиды (например, шелк, желатин, коллаген), полигликолевую кислоту (PGA) и декстран.
В некоторых аспектах каркас или микроносители/шарики могут быть сделаны из материалов, которые деградируют в течение времени в условиях применения. Биодеградируемый также относится к всасыванию или деградации соединения или композиции при введении in vivo или в условиях in vitro. Биодеградация может иметь место посредством действия биологических агентов прямо или опосредованно. Неограничивающие примеры биодеградируемых материалов включают среди прочего, не ограничиваясь этим, полилактид, полигликолид, поли(триметиленкарбонат), поли(лактид-со-гликолид) (т.е. PLGA), полиэтилентерефталат (PET), поликапролактон, шовный материал кетгут, коллаген (например, лошадиная коллагеновая пена), полимолочную кислоту или гиалуроновую кислоту. Например, данные материалы можно сплести в трехмерный каркас, такой как коллагеновая губка или коллагеновый гель.
В других аспектах, когда культуры предназначены для поддержания в течение длительных периодов времени в криоконсервированном состоянии и/или когда требуется дополнительная структурная целостность, то трехмерный каркас может состоять из небиодеградируемого материала. В том смысле, в котором в данном документе используется термин «небиодеградируемый материал», он относится к материалу, который не деградирует или не разлагается в значительной степени в условиях культуральной среды. Примеры недеградируемых материалов включают, в качестве неограничивающих примеров, найлон, дакрон, полистирол, полиакрилаты, поливинилы, политетрафторэтилены (PTFE), растянутый PTFE (ePTFE) и целлюлозу. Приведенный в качестве примера недеградируемый трехмерный каркас включает найлоновую сетку под торговым названием Nitex®, найлоновую сетку для фильтрования со средним размером пор 140 мкм и средним диаметром найлонового волокна 90 мкм (#3-210/36, Tetko, Inc., N.Y.).
В других аспектах шарики, поддерживающие структуры или каркасы представляют комбинацию биодеградируемого и небиодеградируемого материалов. Небиодеградируемый материал обеспечивает стабильность трехмерной поддерживающей структуры во время культивирования, в то время как биодеградируемый материал позволяет формировать интерстициальные пространства, достаточные для образования клеточных сеток, продуцирующих клеточные факторы для терапевтических применений. Биодеградируемый материал можно нанести на небиодеградируемый материал или переплести, оплести или превратить в сетку. Можно использовать различные комбинации биодеградируемого и небиодеградируемого материалов. В качестве примера можно привести комбинацию материала из полиэтилентерефталата (PET), покрытого тонкой пленкой биодеградируемого полимера поли[D,L-молочная-со-гликолевая кислота)] для получения полярной структуры.
В различных аспектах материал поддерживающей структуры или сетки можно предварительно обработать перед инокуляцией клеток для повышения прикрепления клеток. Например, перед инокуляцией клеток найлоновые сетки в некоторых вариантах осуществления обрабатывают 0,1 М уксусной кислотой и инкубируют в полилизине, фетальной бычьей сыворотке и/или коллагене для покрытия найлона. Аналогичным образом можно обработать полистирол с использованием серной кислоты. В еще одних вариантах осуществления рост клеток на трехмерном каркасе-подложке можно дополнительно повысить добавлением в каркас или в его покрытие белков (например, коллагенов, эластиновых волокон, ретикулярных волокон), гликопротеинов, гликозаминогликанов (например, гепарансульфата, хондроитин-4-сульфата, хондроитин-6-сульфата, дерматансульфата, кератансульфата), фибронектинов и/или гликополимера (поли[N-п-винилбензил-D-лактоамида], PVLA) для повышения прикрепления клеток. Обработка поддерживающей структуры или каркаса является подходящей, когда материал представляет собой слабый субстрат для прикрепления клеток.
В одном аспекте сетку используют для продукции ECM. Сетка представляет плетенный найлон 6 в форме плоского плетения с отверстиями размером примерно 100 мкм и толщиной примерно 125 мкм. В культуре фибробласты прикрепляются к найлону посредством взаимодействий заряженных белков и прорастают в пустоты сетки, продуцируя и откладывая белки ECM. Отверстия сетки, которые являются слишком большими или маленькими, могут быть неэффективными, но, тем не менее, они могут отличаться от отверстий, описанных выше, без существенного изменения способности продуцировать или откладывать ECM. В еще одном аспекте для продукции ECM используют другие плетеные материалы, такие как полиолефины в плетенных конфигурациях, обеспечивая адекватную геометрию для клеточного роста и отложения ECM.
Например, найлоновую сетку готовят для культивирования на любой из стадий изобретения разрезанием до требуемого размера, промыванием 0,1-0,5 М уксусной кислотой с последующим промыванием водой высокой чистоты и затем стерилизацией паром. Для применения в качестве трехмерной поддерживающей структуры для получения ECM сетку разделяют на квадраты размером примерно 10 см×10 см. Однако сетка может иметь любой размер, подходящий для предназначенного применения, и ее можно использовать в любом из способов по настоящему изобретению, включая способы культивирования для инокуляции, роста клеток и продукции ECM, и получения конечного продукта.
В еще одних аспектах поддерживающая структура для получения культивированных тканей состоит из микроносителей, которые представляют собой шарики или частицы. Шарики могут быть микроскопическими или макроскопическими, и им можно дополнительно задать размеры для обеспечения проникновения в ткани или придать форму с конкретной геометрией. Комплекс частиц и клеток достаточного размера вводят в ткани или органы, например, инъекцией или с помощью катетера. Как правило, шарики или микроносители рассматриваются в качестве двумерной системы или поддерживающей структуры, и обычно обеспечивают двумерный рост (например, в виде монослоя).
В том смысле, в котором в данном документе используется термин «микроносители», он относится к частице с размером на уровне от нанометров до микрометров, где частицы могут иметь любую форму или геометрию, например, будучи неровными, несферическими, сферическими или эллипсоидными.
Размер микроносителей, подходящий для целей настоящего изобретения, может представлять любой размер, подходящий для конкретного применения. В некоторых вариантах осуществления размер микроносителей, подходящий для изобретения, может быть размером, подходящим для инъекционного введения. В некоторых вариантах осуществления микроносители имеют размер частиц, составляющий, по меньшей мере, примерно 1 мкм, по меньшей мере, примерно 10 мкм, по меньшей мере, примерно 25 мкм, по меньшей мере, примерно 50 мкм, по меньшей мере, примерно 100 мкм, по меньшей мере, примерно 200 мкм, по меньшей мере, примерно 300 мкм, по меньшей мере, примерно 400 мкм, по меньшей мере, примерно 500 мкм, по меньшей мере, примерно 600 мкм, по меньшей мере, примерно 700 мкм, по меньшей мере, примерно 800 мкм, по меньшей мере, примерно 900 мкм, по меньшей мере, примерно 1000 мкм.
В некоторых аспектах микроносители изготовлены из биодеградируемых материалов. В некоторых аспектах можно использовать микроносители, состоящие из двух или более слоев из различных биодеградируемых полимеров. В некоторых вариантах осуществления, по меньшей мере, наружный первый слой обладает биодеградируемыми свойствами для образования тканей в культуре, в то время как, по меньшей мере, биодеградируемый внутренний второй слой со свойствами, отличающимися от первого слоя, выполнен для деградации при введении в ткань или орган.
В некоторых аспектах микроносители являются пористыми микроносителями. Пористые микроносители относятся к микроносителям, содержащим щели, через которые молекулы могут диффундировать внутрь или из микрочастицы. В еще одних вариантах осуществления микроносители являются непористыми микроносителями. Непористая микрочастица относится к микрочастице, в которую молекулы выбранного размера не диффундируют внутрь или из микрочастицы.
Микроносители для применения в композициях являются биосовместимыми и обладают низкой токсичностью для клеток или токсичность отсутствует вовсе. Подходящие микроносители можно выбрать в зависимости от ткани, предназначенной для лечения, типа повреждения, которое лечится, продолжительности требуемого лечения, продолжительности жизни клеточной культуры в условиях in vivo и времени, необходимого для образования трехмерных тканей. Микроносители могут состоять из различных полимеров, природных или синтетических, заряженных (т.е. анионогенных или катионогенных) или незаряженных, биодеградируемых или небиодеградируемых. Полимеры могут быть гомополимерами, статическими сополимерами, блок-сополимерами, привитыми сополимерами и разветвленными полимерами.
В некоторых аспектах микроносители представляют небиодеградируемые микроносители. Небиодеградируемые микрокапсулы и микроносители включают, не ограничиваясь этим, изготовленные из полисульфонов, поли(акрилонитрил-со-винилхлорида), этилен-винилацетата, сополимеров гидроксиэтилметакрилата-метилметакрилата. Они пригодны для получения объемных свойств тканей, или для вариантов осуществления, в которых микроносители элиминируются организмом.
В некоторых аспектах микроносители представляют деградируемые поддерживающие структуры. Они включают микроносители, сделанные из встречающихся в природе полимеров, неограничивающие примеры которых, включают среди прочего, фибрин, казеин, сывороточный альбумин, коллаген, желатин, лецитин, хитозан, альгинат или полиаминокислоты, такие как полилизин. В еще одних аспектах деградируемые микроносители делают из синтетических полимеров, неограничивающие примеры которых, включают среди прочего, полилактид (PLA), полигликолид (PGA), поли(лактид-со-гликолид) (PLGA), поли(капролактон), полидиоксанон триметиленкарбонат, полигидроксиалконаты (например, поли(гидроксибутират), поли(этилглутамат), поли(DTH-иминокарбонил(бисфенол А иминокарбонат), поли(ортоэфиры) и полицианоакрилаты.
В некоторых аспектах микроносители представляют гидрогели, которые, как правило, являются гидрофильными полимерными сетями, заполненными водой. Гидрогели обладают преимуществом избирательно «запускать» набухание полимера. В зависимости от состава полимерной сети набухание микрочастиц может «запускаться» различными факторами, включая рН, ионную силу, термическую, электрическую, ультразвуковую и ферментативную активности. Неограничивающие примеры полимеров, подходящих для гидрогелевых композиций, включают среди прочего, образованные из полимеров поли(лактид-со-гликолида); поли(N-изопропилакриламида); поли(метакриловой кислоты-g-полиэтиленгликоля); полиакриловой кислоты и поли(оксипропилен-со-оксиэтилен)гликоля и природных соединений, таких как хондроитансульфат, хитозан, желатин, фибриноген или смеси синтетических и природных полимеров, например, хитозан-поли(этиленоксид). Полимеры могут быть обратимо или необратимо сшиты с образованием гелей, адаптированных для образования трехмерных тканей.
В приведенных в качестве примера аспектах микроносители или шарики для применения в настоящем изобретении полностью или частично состоят из декстрана.
Согласно настоящему изобретению способ культивирования применим для пролиферации клеток различных типов, включая стромальные клетки, такие как фибробласты, и, в частности, первичные неонатальные фибробласты крайней плоти человека. В различных аспектах клетки, высеянные на поддерживающей структуре или каркасе, могут представлять собой стромальные клетки, содержащие фибробласты, с или без других клеток, как описано ниже. В некоторых вариантах осуществления клетки являются стромальными клетками, которые, как правило, получают из соединительной ткани, включая, не ограничиваясь этим: (1) кость; (2) рыхлую волокнистую соединительную ткань, содержащую коллаген и эластин; (3) фиброзную соединительную ткань, которая образует связки и сухожилия; (4) хрящ; (5) ECM крови; (6) жировую ткань, содержащую адипоциты и (7) фибробласты.
Стромальные клетки можно получить из различных тканей или органов, таких как кожа, сердце, кровеносные сосуды, костный мозг, скелетные мышцы, печень, поджелудочная железа, мозг, крайняя плоть, которые можно получить биопсией (когда это подходит) или при вскрытии. В одном аспекте эмбриональные фибробласты, такие как неонатальные фибробласты, можно получить в большом количестве из крайней плоти.
В некоторых аспектах клетки представляют фибробласты, которые могут происходить из плода, новорожденного, взрослого организма или их комбинации. В некоторых аспектах стромальные клетки представляют фетальные фибробласты, которые могут поддерживать рост ряда различных клеток и/или тканей. В том смысле, в котором в данном документе используется термин «фетальные фибробласты», он относится к фибробластам, полученным из эмбрионов. В том смысле, в котором в данном документе используется термин «неонатальные фибробласты», он относится к фибробластам, полученным из организма новорожденных. В соответствующих условиях фибробласты могут превращаться в другие клетки, такие как костные клетки, жировые клетки и клетки гладкой мускулатуры, и другие клетки мезодермального происхождения. В некоторых вариантах осуществления фибробласты включают кожные фибробласты, которые являются фибробластами, полученными из кожи. Нормальные фибробласты кожи человека можно выделить из крайней плоти новорожденных. Как правило, такие клетки криоконсервируют в конце первичной культуры.
В других аспектах трехмерную ткань можно получить с использованием стволовых клеток или клеток-предшественников, одних или в комбинации с клетками любых других типов. Стволовые клетки и клетки-предшественники включают, в качестве примера и без ограничений, эмбриональные стволовые клетки, гематопоэтические стволовые клетки, нейрональные стволовые клетки, эпидермальные стволовые клетки и мезенхимальные стволовые клетки.
В некоторых вариантах осуществления «специфическую» трехмерную ткань можно получить засеиванием трехмерной поддерживающей структуры клетками, полученными из конкретного органа, т.е. кожи, сердца и/или от конкретного субъекта, которому затем вводят клетки и/или ткани, выросшие в культуре согласно способам, описанным в данном документе.
Для некоторых применений в условиях in vivo предпочтительно получить стромальные клетки из собственных тканей пациента. Рост клеток в присутствии трехмерного стромального каркаса-подложки можно дополнительно усилить добавлением в каркас или покрытие каркаса-подложки белков, например, коллагенов, ламининов, эластических волокон, ретикулярных волокон, гликопротеинов; гликозаминогликанов, например, гепаринсульфата, хондроитин-4-сульфата, хондроитин-6-сульфата, дерматансульфата, кератансульфата и т.д.; клеточного матрикса и/или других веществ.
Таким образом, поскольку двумерные или трехмерные культуральные системы, описанные в данном документе, подходят для роста клеток и тканей различных типов, и в зависимости от ткани, предназначенной для культивирования и требуемых типов коллагена, то можно выбрать соответствующие стромальные клетки для посева на каркас.
Несмотря на то, что способы и применения по настоящему изобретению подходят для применения с различными типами клеток, такими как тканеспецифические клетки или различные типы стромальных клеток, как уже обсуждалось в данном документе, то источник клеток для применения по настоящему изобретению, также может быть видоспецифическим. Следовательно, можно получить композиции ECM, которые являются видоспецифическими. Например, клетки для применения в настоящем изобретении могут включать человеческие клетки. Например, клетки могут представлять собой человеческие фибробласты. Аналогично клетки могут происходить от другого вида животных, и представлять собой лошадиные (от лошади), собачьи (от собаки) или кошачьи (от кошки) клетки. Кроме того, клетки от одного вида или штамма вида можно использовать для получения композиций ECM для применения на другом виде или близких штаммах (например, аллогенных, сингенных и ксеногенных). Также, очевидно, понятно, что клетки, полученные от различных видов, можно комбинировать с получением поливидовых композиций ECM.
Следовательно, способы и композиции по настоящему изобретению подходят для применений, включающих животных, отличных от человека. В том смысле, в котором в данном документе используется термин «ветеринария», он относится к медицинской науке, касающейся или связанной с медицинским или хирургическим лечением животных, особенно домашних животных. Обычные животные-пациенты для ветеринарии могут включать млекопитающих, амфибий, птиц, рептилий и рыб. Например, типичные млекопитающие могут включать собак, кошек, лошадей, кроликов, приматов, грызунов и сельскохозяйственных животных, таких как коровы, лошади, козы, овцы и свиньи.
Как уже обсуждалось выше, в культуре вместе со стромальными клетками могут находиться дополнительные клетки. Такие дополнительные клетки могут оказывать ряд полезных эффектов, включая среди прочего, поддерживание длительного роста в культуре, усиленный синтез ростовых факторов и активацию прикрепления клеток к поддерживающей структуре. Дополнительные клеточные типы включают в качестве неограничивающих примеров, клетки гладкой мускулатуры, клетки сердечной мышцы, эндотелиальные клетки, клетки скелетной мускулатуры, эндотелиальные клетки, перициты, макрофаги, моноциты и адипоциты. Такие клетки можно посеять на каркас вместе с фибробластами, или в некоторых аспектах, в отсутствии фибробластов. Данные стромальные клетки могут происходить из соответствующих тканей или органов, включая в качестве примера и без ограничения, кожу, сердце, кровеносные сосуды, костный мозг, скелетные мышцы, печень, поджелудочную железу и мозг. В других аспектах один или более других клеточных типов, исключая фибробласты, высевают на поддерживающую структуру. В еще одних аспектах поддерживающие структуры засевают только фибробластами.
Фибробласты легко выделить дезагрегированием соответствующего органа или ткани, которые служат в качестве источника фибробластов. Например, ткань или орган можно дезагрегировать механически и/или обработкой расщепляющими ферментами и/или хелатирующими агентами, которые ослабляют связи между смежными клетками, делая возможным превратить ткань в суспензию отдельных клеток без значительного разрушения клеток. Ферментативную диссоциацию можно провести вместе с измельчением ткани и обработкой размельченной ткани рядом расщепляющих ферментов одних или в комбинации. Такие ферменты включают, не ограничиваясь этим, трипсин, химотрипсин, коллагеназу, эластазу, гиалуронидазу, ДНКазу, проназу и/или диспазу. Также можно провести механическое разъединение с помощью устройств, которые включают, не ограничиваясь этим, мельницу, блендеры, сита, гомогенизаторы, устройства для прессования клеток или для обработки ультразвуком, и это только некоторые из возможных аппаратов. В одном аспекте извлеченную ткань крайней плоти обрабатывают с использованием расщепляющих ферментов, как правило, коллагеназы и/или трипсиназы для отделения клеток от инкапсулирующих структур.
Выделение фибробластов можно провести, например, следующим образом: образцы свежей ткани тщательно промывают и измельчают в сбалансированном солевом растворе Хэнкса (HBSS) для удаления сыворотки крови. Измельченную ткань инкубируют 1-12 ч в свежеприготовленном растворе фермента, разъединяющего клетки, такого как трипсин. После инкубации разъединенные клетки суспендируют, осаждают центрифугированием и высевают на культуральные планшеты. Все фибробласты будут прикрепляться раньше других клеток, следовательно, можно избирательно выделить и культивировать соответствующие стромальные клетки. Затем выделенные фибробласты можно культивировать до слияния, приподнять над слитой культурой и посеять на трехмерный каркас, смотри Naughton et al., 1987, J. Med., 18(3&4):219-250. Инокуляция на трехмерный каркас с высоким титром стромальных клеток, например, примерно от 106 до 5×107 клеток/мл, будет обеспечивать получение трехмерной стромальной подложки в течение более короткого периода времени.
После измельчения ткани с получением суспензии отдельных клеток ее можно фракционировать на субпопуляции, из которых можно получить фибробласты и/или другие стромальные клетки, и/или их элементы. Эту процедуру также можно провести с использованием стандартных методов разделения клеток, включая, не ограничиваясь этим, клонирование и отбор клеток специфических типов, избирательное разрушение нежелательных клеток (негативная селекция), разделение, основанное на дифференциальной клеточной агглютинабельности в смешанной популяции, методы замораживания-оттаивания, различные адгезирующие свойства клеток в смешанной популяции, фильтрование, обычное или зональное центрифугирование, центрифужное отмучивание (противоточное центрифугирование), гравитационное разделение, противоточное распределение, электрофорез и флуоресцентно-активированный клеточный сортинг. Обзор по клональному отбору и методам разделения клеток смотри у Freshney, Culture of Animal Cells. A Manual of Basic Techniques, 2d Ed., A.R. Liss, Inc., New York, 1987, Ch. 11 and 12, pp. 137-168.
В одном аспекте выделенные фибробласты можно культивировать с получением банка клеток. Банки клеток создают для обеспечения инициации различных количеств и сроков культивирования партий и для упреждающего тестирования клеток на наличие загрязнений и специфические характеристики клеток. Фибробласты из банков клеток затем культивируют для увеличения числа клеток до соответствующих уровней для посева на поддерживающие структуры. Операции, включающие воздействие окружающей среды и материалов, контактирующих с клетками, проводят в асептических условиях для снижения вероятности их загрязнения чужеродными веществами или нежелательными микроорганизмами.
В еще одном аспекте изобретения после выделения клетки можно культивировать в нескольких пассажах до количества, подходящего для получения основных банков клеток. Затем банки клеток можно собрать и разлить в соответствующие резервуары и консервировать в криогенных условиях. Клетки в замороженных резервуарах из основных банков клеток можно разморозить и культивировать в нескольких дополнительных пассажах (обычно два или более). Затем клетки можно использовать для получения консервированных криогенным путем рабочих банков клеток.
На стадии размножения клеток используют флаконы с клетками со стадии получения рабочих банков клеток для дальнейшего увеличения числа клеток для посева на поддерживающие структуры или подложки, такие как сетки или микроносители. Каждый пассаж представляет серию стадий субкультивирования, которые включают посев клеток на подложки для культивирования, инкубацию, подпитку клеток и их сбор.
Культивирование банков клеток и размножение клеток можно проводить посевом в культуральные флаконы, такие как культуральные колбы, роллер-флаконы или микроносители. Стромальные клетки, такие как фибробласты, прикрепляются к предназначенным для роста поверхностям и растут в присутствии культуральных сред. Культуральные флаконы, такие как культуральные колбы, роллер-флаконы и микроносители, имеют специфическую форму для культивирования клеток и обычно изготовлены из различных пластиков, подходящих для предназначенных применений. Как правило, микроносители представляют собой микроскопические или макроскопические шарики и обычно они изготовлены из различных пластиков. Однако они могут быть сделаны из других материалов, таких как стекло и/или твердые/полутвердые биологические вещества, такие как коллагены и другие вещества, такие как декстран, модифицированный комплекс сахаров, которые обсуждались выше.
При культивировании израсходованную среду периодически замещают свежей средой во время роста клеток для достижения адекватной доступности питательных веществ и удаления продуктов, оказывающих ингибирующее влияние на культивирование (в тех случаях, когда кондиционированная среда не является предпочтительной). Культуральные флаконы и роллер-флаконы обеспечивают поверхность для роста клеток и обычно их используют для культивирования клеток, зависимых от якорной подложки.
В одном аспекте инкубацию проводят в камере при температуре 37°С. В топологиях культивирования, для которых требуется связь питательной среды и среды камеры, используется смесь 5% СО2 с воздухом (об/об) в газовом пространстве камеры для регуляции рН. Альтернативно можно использовать флаконы, снабженные устройствами для поддержания температуры и рН, при культивировании для размножения клеток и продукции ECM. Температура ниже 35°С или 38°С и концентрация СО2 ниже 3% или выше 12% могут быть не подходящими.
Сбор клеток с поверхностей прикрепления можно проводить удалением культуральной среды и отмывкой клеток забуференным солевым раствором для уменьшения содержания белка, конкурирующего с ферментами, применением разъединяющих ферментов, затем нейтрализацией ферментов после отделения клеток. Собирают суспензию собранных клеток и собранные жидкости отделяют центрифугированием. Можно отобрать пробы из клеточных суспензий субкультур для определения количества выделенных клеток и оценки других свойств клеток, и затем объединить со свежей средой, и использовать в качестве посевного материала. Количество пассажей, используемых для получения банков клеток и посевного материала для поддерживающей структуры, является критическим для достижения приемлемых характеристик ECM.
После получения подходящей поддерживающей структуры проводят его засев полученными стромальными клетками. Посев на поддерживающие структуры можно проводить различными способами, такими как седиментация. Готовят сетку, предназначенную для культивирования ECM в аэробных условиях, аналогично тому, как это делается для сетки, культивируемой в гипоксических условиях, за исключением того, что анаэробная камера не используется для обеспечения гипоксических условий.
Например, для обеих сеток, приготовленных для культивирования ECM в аэробных и гипоксических условиях, приготовленную и стерилизованную сетку помещают в стерильные чашки Петри диаметром 150 мм×глубиной 15 мм, и собирают в стопку на толщину примерно 10 сеток. Затем стопки сеток инокулируют седиментацией. К клеткам добавляют свежую среду с получением соответствующего титра клеток для инокулюма. Инокулюм добавляют к стопке сеток, где клетки оседают на найлоновые волокна и прикрепляются при инкубации. После адекватного периода времени индивидуально засеянные сетчатые листы можно асептически отделить от общей стопки и по отдельности поместить в отдельные чашки Петри 150 мм×15 мм, содержащие примерно 50 мл культуральной среды.
Инкубацию высеянной культуры проводят в гипоксических условиях, в которых, как было установлено, продуцируются ECM и среда с уникальными свойствами по сравнению с ECM, полученным в обычных культуральных условиях. В том смысле, в котором в данном документе используется термин «гипоксические условия», он означает условия с низкой концентрацией кислорода по сравнению с концентрацией кислорода в комнатном воздухе (примерно 15-25% кислорода). В одном аспекте гипоксические условия характеризуются концентрацией кислорода ниже 10%. В еще одном аспекте гипоксические условия означают условия с концентрацией кислорода примерно от 0,1% до 10%, от 1% до 10%, от 1% до 9%, от 1% до 8%, от 1% до 7%, от 1% до 6%, от 1% до 5%, от 1% до 4%, от 1% до 3% или от 1% до 2%. В некотором аспекте система содержит примерно 1-3% кислорода в культуральном флаконе. Гипоксические условия можно создать и поддерживать с использованием аппарата для культивирования, который позволяет контролировать концентрацию газов в окружающей среде, например, анаэробной камере.
Как правило, инкубацию клеточных культур проводят в нормальной атмосфере с содержанием 15-22% кислорода и 5% СО2 для размножения и посева, на данной точке культуры с низким содержанием кислорода разделяют на воздухонепроницаемую камеру, которую насыщают смесью 95% азота/5% СО2 таким образом, чтобы создать гипоксическую окружающую среду в культуральной среде.
Например, чашки Петри с сетками, культивированными для получения ECM в гипоксических условиях, первоначально культивируют инкубацией при 37°С и с газовой смесью 95% воздуха/5% СО2 в течение 2-3 недель. После периода культивирования почти в атмосферных условиях чашки Петри с сетками инкубируют в камере, предназначенной для анаэробного культивирования, которую продувают газовой смесью состава 95% азота и 5% СО2. Израсходованную культуральную среду замещают свежей средой при атмосферном уровне кислорода в течение периода культивирования и после замены среды чашки Петри с сетками помещают в анаэробную камеру, которую продувают смесью 95% азота/5% СО2 и инкубируют при 37°С. Культивированные сетки собирают, когда они достигают требуемого размера или содержат требуемые биологические компоненты.
Во время инкубации стромальные клетки растут линейно и обволакивают трехмерный каркас до начала роста в отверстиях каркаса. Растущие клетки продуцируют огромное количество ростовых факторов, регуляторных факторов и белков, некоторые из которых секретируются в окружающую среду, и другие откладываются на подложке, составляя ECM, более подробно обсуждаемый ниже. В культуру можно добавить ростовые и регуляторные факторы, но это необязательно. В результате культивирования стромальных клеток продуцируется нерастворимая и растворимая фракции. Клетки культивируют до соответствующей степени для обеспечения адекватного отложения белков ECM.
Во время культивирования трехмерных тканей, пролиферирующие клетки могут высвобождаться из каркаса и прилипать к стенкам культурального флакона, где они могут продолжать пролиферировать и образовать слитый монослой. Для минимизации такой вероятности, которая может отрицательно повлиять на рост клеток, высвобожденные клетки можно удалить по время подпитки или перенести трехмерную клеточную культуру в новый культуральный флакон. Удаление слитого монослоя или перенос культивированной ткани на свежую среду в новый флакон помогут сохранить или восстановить пролиферативную активность трехмерных культур. В некоторых аспектах удаление или перенос можно провести в культуральном флаконе с монослоем культивированных клеток, достигающих 25% слияния. Альтернативно культуру в некоторых вариантах осуществления встряхивают для предупреждения слипания высвобожденных клеток; в других случаях свежую среду постоянно вводят в систему. В некоторых аспектах два или более клеточных типа культивируют вместе одновременно или один после другого (например, фибробласты и клетки гладкой мускулатуры, или эндотелиальные клетки).
После заселения трехмерных поддерживающих структур клеточную культуру инкубируют в подходящей питательной среде и инкубационных условиях, которые поддерживают рост клеток с образованием трехмерных тканей. Многие обычные промышленно доступные среды, такие как среда Игла, модифицированная по способу Дульбекко (DMEM), RPMI 1640, среды Фишера, Искове и Маккоя, могут быть подходящими для поддержания роста клеточных культур. Среду можно обогатить дополнительными солями, источниками углерода, аминокислотами, сывороткой крови и компонентами сыворотки крови, витаминами, минеральными веществами, восстанавливающими агентами, буферами, липидами, нуклеозидами, антибиотиками, факторами, способствующими прикреплению и ростовыми факторами. Рецептуры культуральных сред разных типов описаны в различных источниках, известных специалистам в данной области (например, в «Methods for Preparation of Media, Supplements and Substrates for Serum Free Animal Cell Cultures», Alan R. Liss, New York (1984); «Tissue Culture: Laboratory Procedures», John Wiley&Sons, Chichester, England (1996); «Culture of Animal Cells, A Manual of Basic Techniques», 4th Ed., Wiley-Liss (2000)).
Питательные или культуральные среды, используемые на одной из стадий культивирования по настоящему изобретению, независимо от аэробных или гипоксических условий, могут включать сыворотку крови или быть бессывороточными. В одном аспекте среда представляет среду Игла, модифицированную по способу Дульбекко, с 4,5 г/л глюкозы, аланил-L-глутамина, экв 2 мМ, и номинально с добавлением 10% фетальной бычьей сыворотки. В еще одном аспекте среда представляет бессывороточную среду и является средой Игла, модифицированной по способу Дульбекко, с 4,5 г/л глюкозы основной средой с Glutamax® с добавлением 0,5% сывороточного альбумина, 2 мкг/мл гепарина, 1 мкг/мл рекомбинантного основного FGF, 1 мкг/мл соевого ингибитора трипсина, добавки 1X ITS (инсулин-трансферин-селен, Sigma, номер по каталогу I3146), добавки на основе жирной кислоты в разведении 1:1000 (Sigma, номер по каталогу 7050) и холестерина в разведении 1:1000. Кроме того, те же среды можно использовать для культивирования в гипоксических и аэробных условиях. В одном аспекте культуральную среду меняют со среды с сывороткой на бессывороточную среду после посева и первой недели роста.
Условия инкубации представляют условия с рН, температурой и газом (например, О2, СО2 и т.д.), подходящими для достижения гипоксических условий культивирования. В некоторых вариантах осуществления трехмерную клеточную культуру можно суспендировать в среде во время инкубации для достижения максимальной пролиферативной активности и продукции факторов, обеспечивающих требуемые биологические активности фракций. Кроме того, культуру можно периодически «подпитывать» для удаления израсходованной среды, удаления высвобожденных клеток и добавления новых источников питания. Во время инкубации культивированные клетки растут линейно вдоль и обволакивают волокна трехмерной поддерживающей структуры до начала прорастания в отверстиях поддерживающей структуры.
Во время инкубации в гипоксических условиях, по сравнению с инкубацией в атмосферных нормальных условиях с концентрацией кислорода примерно 15-20%, тысячи генов экспрессируются дифференциально. Было установлено, что некоторые гены подвергаются позитивной регуляции или негативной регуляции в таких композициях; это наиболее выражено для генов ламининов, коллагенов и факторов Wnt. В различных аспектах трехмерные ECM можно определить характерным фингерпринтингом или набором клеточных продуктов, продуцированных клетками, при росте в гипоксических условиях по сравнению с ростом в нормальных условиях. В конкретных композициях ECM, приведенных в качестве примера в данном документе, трехмерные ткани и окружающая среда характеризуются экспрессией и/или секрецией различных факторов.
Трехмерные ткани и композиции, описанные в данном документе, содержат ECM, который находится на скэффолде или каркасе. В некоторых аспектах ECM содержит различные типы ламининов и коллагенов за счет роста в гипоксических условиях и отбора клеток, выросших на подложке. Относительные количества отложенных белков ECM можно модифицировать или повысить отбором фибробластов, которые синтезируют соответствующий тип коллагенов, а также культивированием клеток в гипоксических условиях, в которых экспрессия специфических типов ламинина и коллагена подвергается позитивной регуляции или негативной регуляции.
Отбор фибробластов можно провести в некоторых аспектах с использованием моноклональных антител соответствующего изотипа или подкласса, с помощью которых можно определить конкретные типы коллагена. В еще одних аспектах можно использовать твердые субстраты, такие как магнитные шарики, для отбора или элиминации клеток, которые связывают антитело. Комбинацию данных антител можно использовать для отбора (позитивного или негативного) фибробластов, которые экспрессируют требуемый тип коллагена. Альтернативно строма, используемая для инокуляции каркаса, может представлять смесь клеток, которые синтезируют требуемые типы коллагенов. Распределение и происхождение примерных типов коллагена приводятся в таблице 1.
Распределение и источники различных типов коллагена
коллагена
Папиллярный слой дермы
Базальные мембраны
Кость
Базальные мембраны
Кость
Дополнительные типы коллагенов, которые могут присутствовать в композициях ECM, приведены в таблице 2.

Как уже осуждалось выше, композиции ECM, описанные в данном документе, содержат различные коллагены. Как показано в таблице 3 примера 1, было установлено, что экспрессия нескольких видов коллагена поддается позитивной регуляции в композициях ECM, культивированных в гипоксических условиях. Следовательно, в одном аспекте настоящего изобретения композиция ECM, содержащая один или более эмбриональных белков, включает активацию коллагенов по сравнению с условиями с нормальным содержанием кислорода на уровне примерно 15-20%. В еще одном аспекте коллагенами с позитивной регуляцией являются коллагены типов V альфа 1; IX альфа 1; IX альфа 2; VI альфа 2; VIII альфа 1; IV альфа 5; VII альфа 1; XVIII альфа 1 и XII альфа 1.
В дополнении к различным коллагенам композиции ECM, описанные в данном документе, содержат различные ламинины. Ламинины представляют семейство гликопротеинов гетеротримеров, состоящих из альфа-, бета- и гамма-субъединиц, соединенных через суперскрученный домен. К настоящему времени идентифицированы 5 альфа, 4 бета и 3 гамма цепи ламинина, которые могут объединяться с образованием 15 различных изоформ. В этой структуре установлены домены, которые обладают связывающей активностью по отношению к другим ламининам и молекулам базальной пластинки, и мембранным рецепторам. Домены VI, IVb и IVa образуют глобулярные структуры, и домены V, IIIb и IIIA (которые содержат богатые цистеином EGF-подобные элементы) образуют стержнеобразные структуры. Домены I и II трех цепей принимают участие в образовании трехцепочечной суперскрученной структуры (длинное плечо).
Цепи ламинина обладают общими и уникальными функциями, и экспрессируются со специфическим по времени (на определенных стадиях развития) и пространственным (тканеспецифическим) типом экспрессии. Полагают, что альфа-цепи ламинина являются важным функциональным фрагментом гетеротримеров, поскольку для них характерен тканеспецифический характер распределения и они содержат основные сайты клеточных взаимодействий. Известно, что в сосудистом эндотелии экспрессируется две изоформы ламинина с различным уровнем экспрессии в зависимости от стадии развития, типа сосудов и состояния активации эндотелия.
Следовательно, в одном аспекте настоящего изобретения композиция ECM, содержащая один или более эмбриональных белков, включает активацию или подавление различных ламининов по сравнению с продуцированной композицией ECM в условиях с нормальным содержанием кислорода на уровне примерно 15-20%.
Ламинин 8 состоит из цепей ламинина альфа-4, бета-1 и гамма-1. Цепь ламинина альфа-4 широко распространена во взрослых организмах и в период развития. У взрослых ее можно обнаружить в базальной мембране, покрывающей сердечные волокна, волокна скелетных мышц и гладкой мускулатуры, и в альвеолярных перегородках легких. Также известно, что она имеется в базальной мембране эндотелия капилляров и более крупных сосудов, и в перинейрональной базальной мембране периферических нервов, а также в интерсинусоидальных пространствах, крупных артериях и более мелких артериолах костного мозга. Ламинин 8 является основной изоформой ламинина в сосудистом эндотелии, который экспрессируется и адгезируется тромбоцитами, и синтезируется 3T3-L1 адипоцитами; было показано, что его уровень повышается при жировом перерождении клеток. Полагают, что ламинин 8 является изоформой ламинина, которая обычно экспрессируется в линиях дифференцировки мезенхимальных клеток с индукцией развития микрососудов в соединительных тканях. Также ламинин 8 был обнаружен в первичных культурах мышиных клеток костного мозга, стенках артериол и интерсинусоидальных пространствах, где он является основной изоформой ламинина в развивающемся костном мозге. За счет локализации в костном мозге взрослых с гематопоэтическими клетками, вероятно, изоформы ламинина, содержащие цепь альфа-4, обладают биологически релевантными взаимодействиями с развивающимися гематопоэтическими клетками.
Следовательно, в еще одном аспекте настоящего изобретения ECM включает активацию ламининов, таких как ламинин 8. В еще одном аспекте ламинины, продуцированные трехмерными тканями по настоящему изобретению, содержат, по меньшей мере, ламинин 8, который определяет характеристику или признак белков ламининов, присутствующих в композиции.
Композиции ECM, описанные в данном документе, могут содержать различные факторы Wnt. Семейство факторов Wnt представляет семейство сигнальных молекул, которые играют роль в огромном числе клеточных путей и взаимодействий типа «клетка-клетка». Сигнальный путь с участием Wnt принимает участие в развитии опухолей, формировании мезодермальных элементов в эмбрионах на ранней стадии развития, морфогенезе мозга и почек, регуляции пролиферации молочной железы и развитии болезни Альцгеймера. Как показано в таблице 4 примера 1, было установлено, что экспрессия нескольких видов белков Wnt имеет активацию в композициях ECM в гипоксических условиях. Следовательно, в одном аспекте настоящего изобретения композиция ECM, содержащая один или более эмбриональных белков, включает активацию типов Wnt по сравнению с композицией ECM, продуцированной в условиях с нормальным содержанием кислорода на уровне примерно 15-20%. Еще в одном аспекте типы Wnt с позитивной регуляцией представляют wnt 7a и wnt 11. В еще одном аспекте факторы Wnt, продуцированные трехмерными тканями по настоящему изобретению, включают, по меньшей мере, wnt 7a и wnt 11, которые определяют характерные свойства или признаки белков Wnt, присутствующих в композиции.
Также было показано, что способы культивирования, описанные в данном документе, включая культивирование в гипоксических условиях, индуцируют активацию экспрессии различных ростовых факторов. Следовательно, композиции ECM, описанные в данном документе, могут содержать различные ростовые факторы, такие как фактор роста сосудистого эндотелия (VEGF). В том смысле, в котором в данном документе используется термин «VEGF», он включает все известные члены семейства VEGF. VEGF представляет субсемейство ростовых факторов, конкретнее семейство тромбоцитарных ростовых факторов ростовых факторов с «цистиновым узлом». Представители субсемейства VEGF обладают хорошо известной ролью в васкулогенезе и ангиогенезе. Известно несколько VEGF, включая VEGF-А, который ранее был известен, как VEGF, до открытия других видов VEGF. Другие виды VEGF включают плацентарный ростовый фактор (PIGF), VEGF-B, VEGF-C и VEGF-D. Кроме того, хорошо известно несколько изоформ человеческого VEGF.
Согласно изобретению наряду с повышенной продукцией белков Wnt, а также ростовых факторов, при культивировании в гипоксических условиях, описанных в данном документе, настоящее изобретение дополнительно относится к способу получения белка Wnt и фактора роста эндотелия сосудов (VEGF). Способ может включать культивирование клеток в гипоксических условиях, как описано в данном документе, на трехмерной подложке в подходящей культуральной среде, с получением белка Wnt и VEGF. В приведенном в качестве примера аспекте типами Wnt являются wnt 7a и wnt 11, и VEGF представляет VEGF-А. Белки можно дополнительно обработать или собрать, как описано ниже в данном документе, или с помощью способов, известных в данной области.
Как уже обсуждалось, композиции ECM по настоящему изобретению содержат растворимую и нерастворимую фракции или их части. Очевидно, понятно, что композиции по настоящему изобретению могут содержать одну или обе фракции, а также любые их комбинации. Кроме того, из фракций можно выделить отдельные компоненты для применения по отдельности или в комбинации с другими изолятами или известными композициями.
Следовательно, в различных аспектах композиции ECM, продуцированные с использованием способов по настоящему изобретению, можно применять непосредственно или обработать различными путями, где способы могут быть применимы для обеих нерастворимой и растворимой фракций. Растворимую фракцию, содержащую бесклеточный супернатант и среду, можно лиофилизовать для хранения и/или концентрирования факторов. Когда это требуется, то для сохранения активности можно использовать различные консерванты, криопротекторы и стабилизаторы. Примеры биосовместимых агентов включают, среди прочего, глицерин, диметилсульфоксид и трегалозу. Лиофилизат также может содержать один или более наполнителей, таких как буферы, придающие объем вещества и модификаторы изотоничности. Лиофилизованную среду можно восстановить добавлением подходящего раствора или фармацевтического разбавителя, как дополнительно описано ниже.
В еще одних аспектах растворимую фракцию диализуют. Диализ представляет один из наиболее часто применяемых методов для разделения компонентов образца, который основан на избирательной диффузии через пористую мембрану. Размер пор определяет предельная отсечка по молекулярной массе (MWCO) мембраны, которая характеризуется молекулярной массой, при которой 90% растворенных веществ остается на мембране. В некоторых аспектах предусматриваются мембраны с любым размером пор, в зависимости от требуемой предельной отсечки. Типичные предельные отсечки равняются 5000 D, 10000 D, 30000 D и 100000 D, однако, предусматриваются любые размеры.
В некоторых аспектах растворимую фракцию можно обработать преципитацией активных компонентов (например, ростовых факторов) в среде. Для преципитации можно использовать различные методы, такие как высаливание сульфатом аммония или применение гидрофильных полимеров, например, полиэтиленгликоля.
В еще одних аспектах растворимую фракцию подвергают фильтрованию с использованием различных селективных фильтров. Обработка растворимой фракции фильтрованием пригодна для концентрирования факторов, находящихся во фракции, и также для удаления небольших молекул и растворенных веществ в растворимой фракции. Фильтры с селективностью для конкретных значений молекулярных масс включают <5000 D, <10000 D и <15000 D. Можно использовать другие фильтры и обработанную среду анализировать в отношении терапевтической активности, как описано ниже. В качестве примера фильтров и концентраторов можно привести системы, основанные, например, на полых волокнистых фильтрах, фильтрующих дисках и фильтрационных зондах (смотри, например, Amicon Stirred Ultrafiltration Cells).
В еще одних аспектах растворимую фракцию хроматографируют для удаления солей, примесей или фракционируют на различные компоненты среды. Можно использовать различные хроматографические методы, такие как гель-фильтрация, ионообменная хроматография, обратнофазовая хроматография и аффинная хроматография. Для обработки кондиционированной среды без существенной потери биологической активности можно использовать слабые хроматографические среды. Неограничивающие примеры включают, среди прочего, декстран, агарозу, среды для разделения на основе полиакриламида (например, доступные под различными торговыми названиями, такими как сефадекс, сефароза и сефакрил).
В еще одних аспектах кондиционированную среду формулируют в виде липосом. Ростовые факторы можно ввести или инкапсулировать в полости липосом для доставки и для удлинения периода полураспада активных факторов. Как известно в данной области, липосомы можно разделить на различные типы: мультиламеллярные (MLV), стабильные плюриламелярные (SPLV), небольшие униламеллярные (SUV) или крупные униламеллярные (LUV) везикулы. Липосомы можно приготовить из различных липидных соединений, которые могут быть синтетическими или встречающимися в природе, включая фосфатидиловые простые эфиры и сложные эфиры, такие как фосфатидилсерин, фосфатидилхолин, фосфатидилэтаноламин, фосфатидилинозит, димиристоилфосфатидилхолин; стероиды, такие как холестерин; цереброзиды; сфингомиелин; глицеролипиды и другие липиды (смотри, например, патент США № 5833948).
Растворимую фракцию можно использовать непосредственно без дополнительных добавок или приготовить в виде фармацевтических композиций с различными фармацевтически приемлемыми наполнителями, растворителями или носителями. Термин «фармацевтическая композиция» относится к форме растворимой и/или нерастворимой фракций и, по меньшей мере, с одним фармацевтически приемлемым растворителем, носителем или наполнителем. Для внутрикожного, подкожного или внутримышечного введения композиции можно приготовить в виде стерильных суспензий, растворов или эмульсий композиций ECM в водных или масляных растворителях. Также композиции могут содержать формообразующие агенты, такие как суспендирующие, стабилизирующие или диспергирующие агенты. Композиции для инъекции могут находиться в разовой лекарственной форме, ампулах в мультидозовых контейнерах с или без консервантов. Альтернативно композиции могут находиться в виде порошка для последующего восстановления подходящим растворителем, включая в качестве примера и без ограничения, стерильную непирогенную воду, солевой раствор, буфер или декстрозу.
В других аспектах трехмерные ткани представляют собой криоконсервированные препараты, которые размораживают перед применением. Фармацевтически приемлемые криопротекторы включают, среди прочего, глицерин, сахариды, полиолы, метилцеллюлозу и диметилсульфоксид. Сахариды включают моносахариды, дисахариды и другие олигосахариды с температурой зеркального перехода максимально замороженного-концентрированного раствора (Tg), которая составляет, по меньшей мере, -60°, -50°, -40°, -30°, -20°, -10° или 0°С. Примером сахарида для применения в криоконсервации является трегалоза.
В некоторых аспектах трехмерные ткани обрабатывают, чтобы убить клетки до применения. В некоторых аспектах ECM, отложенный на поддерживающей структуре, можно собрать и обработать для введения (смотри патенты США №№ 5830708 и 6280284, которые включены в данный документ для сведения).
В некоторых вариантах осуществления трехмерную ткань можно сконцентрировать и отмыть фармацевтически приемлемой средой для введения. В данной области имеются различные методы концентрирования композиций, такие как центрифугирование или фильтрование. Примеры включают седиментацию на декстране и дифференциальное центрифугирование. Формуляция трехмерной ткани может включать доведение ионной силы суспензии до изотоничности (т.е. примерно от 0,1 до 0,2) и до физиологического значения рН (т.е. рН от 6,8 до 7,5). Композиция также может содержать скользящие вещества или другие наполнители, способствующие введению или сохранению стабильности клеточной суспензии. Такие вещества включают, среди прочего, сахариды (например, мальтозу) и органические полимеры, такие как полиэтиленгликоль и гиалуроновую кислоту.
Как уже обсуждалось выше, композиции ECM по настоящему изобретению можно обработать различными путями в зависимости от предназначенного применения и соответствующей доставки или введения композиции ECM. Например, композиции можно доставить в виде трехмерных поддерживающих структур или имплантов, или композиции можно формулировать для инъекционного введения, как описано выше. Термины «введение» или «процесс введения» включают процесс обеспечения соединения или фармацевтической композиции по изобретению субъекту, нуждающемуся в лечении. В том смысле, в котором в данном документе используются выражения «парентеральное введение» и «введенный парентерально», они означают способы введения иные, чем энтеральное и местное введение, как правило, с помощью инъекций, и они включают, не ограничиваясь этим, внутривенную, внутримышечную, внутриартериальную, интратекальную, внутрикапсулярную, внутриглазную, внутрикардиальную, внутрикожную, внутрибрюшинную, транстрахеальную, подкожную, субкутикулярную, внутрисуставную, субарахноидальную, интраспинальную и интрастернальную инъекцию и инфузию. В том смысле, в котором в данном документе используются выражения «системное введение», «введенный системно», «периферическое введение», «введенный периферически», они означают введение соединения, лекарственного препарата или другого вещества иначе, чем непосредственно в центральную нервную систему, так, что оно поступает в систему субъекта, и таким образом, подвергается метаболизму или другим аналогичным процессам, например, это подкожное введение.
В том смысле, в котором в данном документе используется термин «субъект», он относится к индивидууму или пациенту, или животному, на котором проводятся способы по настоящему изобретению. Как правило, субъект является человеком, хотя, как понятно специалистам в данной области, субъект может представлять животное. Таким образом, другие животные, включая млекопитающих, таких как грызуны (включая мышей, крыс, хомяков и морских свинок), кошек, собак, кроликов, сельскохозяйственных животных, включая коров, лошадей, коз, овец, свиней и т.д., и приматов (включая обезьян, шимпанзе, орангутангов и горилл), входят в определение термина «субъект».
Композиции ECM по настоящему изобретению имеют различные применения, включая, не ограничиваясь этим, стимуляцию восстановления и/или регенерации поврежденных клеток или тканей, применение в пластырях для стимуляции регенерации ткани, применение в системах тканевых культур для культивирования клеток, таких как стволовые клетки, применение в поверхностных покрытиях, используемых в ассоциации с имплантируемыми устройствами (например, такими как кардиостимуляторы, стенты, стентовые трансплантаты, сосудистые протезы, сердечные клапаны, шунты, порты для доставки лекарственных препаратов или катетеры), стимуляцию восстановления, аугментации мягких тканей и/или улучшение поверхности кожи, такой как морщины, применение в качестве биологического антиадгезирующего средства или биологического носителя для доставки или сохранения клеток в месте доставки.
Кроме того, композиции ECM, полученные культивированием клеток, как описано в любом способе по изобретению, можно использовать в любом другом применении или способе по настоящему изобретению. Например, композиции ECM, полученные культивированием клеток с использованием систем тканевых культур по настоящему изобретению, можно использовать, например, в восстановлении и/или регенерации клеток, применении в пластырях для стимуляции регенерации ткани, применении в системах тканевых культур для культивирования клеток, таких как стволовые клетки, применении в поверхностных покрытиях, используемых в ассоциации с имплантируемыми устройствами (например, такими как кардиостимуляторы, стенты, стентовые трансплантаты, сосудистые протезы, сердечные клапаны, шунты, порты для доставки лекарственных препаратов или катетеры), стимуляции восстановления, аугментации мягких тканей и/или улучшения поверхности кожи, такой как морщины, применении в качестве биологического антиангезивного средства или биологического носителя для доставки или сохранения клеток в месте доставки.
В различных вариантах осуществления настоящее изобретение включает способы восстановления и/или регенерации клеток и тканей, и стимуляции восстановления мягких тканей. Один вариант осуществления включает способ восстановления и/или регенерации клеток контактированием клеток, предназначенных для восстановления или регенерации с композициями ECM по настоящему изобретению. Способ можно использовать для восстановления и/или регенерации различных клеток, как обсуждается в данном документе, включая остеохондральные клетки.
В одном аспекте способ включает восстановление остеохондральных дефектов. В том смысле, в котором в данном документе используется термин «остеохондральные клетки», он относится к хондрогенной или остеогенной линии дифференцировки или к клеткам, которые могут дифференцироваться в хондрогенную или остеогенную линию в зависимости от сигналов окружающей среды. Такую активность можно тестировать в условиях in vitro и in vivo. Таким образом, в одном аспекте композиции ECM по настоящему изобретению используют для восстановления и/или регенерации хондрогенных клеток, например, клеток, которые способны продуцировать хрящ, или клеток, которые могут сами по себе дифференцироваться в клетки, продуцирующие хрящ, включая хондроциты и клетки, которые могут сами по себе дифференцироваться в хондроциты (например, предшественники хондроцитов). Таким образом, в еще одном аспекте композиции по настоящему изобретению пригодны для восстановления и/или регенерации соединительной ткани. В том смысле, в котором в данном документе используется термин «соединительная ткань», он относится к одной из ряда структурных тканей в организме млекопитающего, включающих, не ограничиваясь этим, кость, хрящ, связки, сухожилие, мениски, дерму, гиподерму, мышцы, жировую ткань, суставную капсулу.
Композиции ECM по настоящему изобретению можно использовать для лечения остеохондральных дефектов диартроидного сустава, такого как колено, лодыжка, бедро, запястье, сустав пальца руки или пальца ноги, или височно-нижнечелюстного сустава. Такие остеохондральные дефекты могут быть результатом травматического повреждения (например, спортивной травмы или сильной нагрузки) или заболевания, такого как остеоартрит. Конкретный аспект относится к применению матрикса по настоящему изобретению в лечении или профилактике поверхностных очагов поражения хряща при остеоартрите. Кроме того, настоящее изобретение пригодно для лечения или профилактики остеохондральных дефектов, возникших в результате старения или родов. Остеохондральные дефекты в контексте настоящего изобретения следует понимать, как включающие состояния, при которых необходимо восстановление хряща и/или кости после хирургической операции, такой как, не ограничиваясь этим, косметическая операция (например, на носу, ушах). Такие дефекты могут иметь место в любом месте организма, где нарушается образование хряща или кости, или происходит повреждение хряща или кости, или имеет место их несостоятельность в результате генетического дефекта.
Как уже обсуждалось выше, ростовые факторы или другие биологические агенты, которые индуцируют или стимулируют рост конкретных клеток, могут быть включены в композиции ECM по настоящему изобретению. Тип ростовых факторов будет зависеть от типа клеток и применения, для которого предназначена композиция. Например, в случае остеохондральных клеток, могут присутствовать дополнительные биологически активные агенты, такие как клеточные ростовые факторы (например, TGF-β), вещества, которые стимулируют хондрогенез (например, BMP, которые стимулируют образование хряща, такие как BMP-2, BMP-12 и BMP-13), факторы, которые стимулируют миграцию стромальных клеток к поддерживающим структурам, факторы, которые стимулируют отложение матрикса, противовоспалительные вещества (например, нестероидные противовоспалительные препараты), иммуносупрессоры (например, циклоспорины). Также могут быть включены другие белки, такие как другие ростовые факторы, такие как факторы роста тромбоцитов (PDGF), инсулиноподобные ростовые факторы (IGF), факторы роста фибробластов (FGF), эпидермальный фактор роста (EGF), ростовый фактор клеток эндотелия человека (ECGF), колониестимулирующий фактор гранулоцитов-макрофагов (GM-CSF), фактор роста сосудистого эндотелия (VEGF), морфогенетический белок хрящевого происхождения (CDMP), другие костные морфогенетические белки, такие как OP-1, OP-2, BMP3, BMP4, BMP9, BMP11, BMP14, DPP, Vg-1, 60A и Vgr-1, коллагены, эластиновые волокна, ретикулярные волокна, гликопротеины, гликозаминогликаны, например, гепарансульфат, хондроитин-4-сульфат, хондроитин-6-сульфат, дерматансульфат, кератансульфат и т.д. Например, было установлено, что ростовые факторы, такие как TGF-β, с аскорбатом, «запускают» дифференцировку хондроцитов и образование хряща хондроцитами. Кроме того, гиалуроновая кислота является хорошим субстратом для прикрепления хондроцитов и других стромальных клеток, и их можно включить в качестве части поддерживающей структуры или покрыть поддерживающую структуру.
Кроме того, можно использовать другие факторы, оказывающие влияние на рост и/или активность конкретных клеток. Например, в случае хондроцитов такой фактор, как хондроитиназа, которая стимулирует продукцию хряща хондроцитами, можно добавить в матрикс для поддержания хондроцитов в гипертрофическом состоянии, как описано в заявке на патент США 2002/0122790, который включен в данный документ для сведения. В еще одном аспекте способы по настоящему изобретению включают присутствие полисульфатированных альгинатов или других полисульфатированных полисахаридов, таких как полисульфатированный циклодекстрин и/или полисульфатированный инулин, или других компонентов, способных стимулировать продукцию ECM клетками соединительной ткани, как описано в международной патентной публикации WO 2005/054446, включенной в данной документ для сведения.
Клетка или ткань, предназначенные для восстановления или регенерации, могут контактировать в условиях in vivo и in vitro любым способом, описанным в данном документе. Например, композиции ECM можно вводить или имплантировать (например, через ткань ECM, пластырь или покрытое устройство по настоящему изобретению) субъекту. В еще одном аспекте ткань или клетки, предназначенные для восстановления и/или регенерации, можно отобрать у субъекта и культивировать в условиях in vitro, и затем имплантировать или ввести субъекту с использованием известных хирургических процедур.
Как уже обсуждалось выше, композиции ECM по настоящему изобретению можно обработать различными путями. Следовательно, в одном варианте осуществления настоящее изобретение включает систему тканевых культур. В различных аспектах культуральная система состоит из композиций ECM, описанных в данном документе. Композиции ECM по настоящему изобретению можно включить в систему тканевых культур различными путями. Например, композиции можно включить в качестве покрытий, импрегнацией трехмерной поддерживающей структуры, как описано в данном документе, или включить в виде добавок в среду для культивирования клеток. Следовательно, в одном аспекте культуральная система может включать трехмерные подложки, импрегнированные любыми композициями ECM, описанными в данном документе, такими как ростовые факторы или эмбриональные белки.
Композиции ECM, описанные в данном документе, могут служить в качестве подложки или трехмерной подложки для культивирования клеток различных типов. Предусматривается клетка любого типа, способная к клеточному культивированию. В одном аспекте культуральную систему можно использовать для поддержания роста стволовых клеток. В еще одном аспекте стволовые клетки являются эмбриональными стволовыми клетками, мезенхимальными стволовыми клетками или нейрональными стволовыми клетками.
Систему тканевых культур можно использовать для получения дополнительных композиций ECM, таких как имплантируемая ткань. Следовательно, культивирование клеток с использованием системы тканевых культур по настоящему изобретению можно осуществить в условиях in vivo и in vitro. Например, систему тканевых культур по настоящему изобретению можно использовать для получения композиций ECM для инъекции или имплантации субъекту. Композиции ECM, полученные системы тканевых культур, можно обработать и использовать в любом способе, описанном в данном документе.
Композиции ECM по настоящему изобретению можно использовать в качестве биологического носителя для доставки клеток. Как описано в данном документе, композиции ECM могут включать растворимую и/или нерастворимую фракции. При этом еще в одном варианте осуществления настоящего изобретения описан биологический носитель для доставки или поддержания клеток в месте доставки, включающий композиции ECM по настоящему изобретению. Композиции ECM по настоящему изобретению, содержащие клетки и трехмерные тканевые композиции, можно использовать для стимуляции и/или поддержания роста клеток в условиях in vivo. Носитель можно использовать в любом соответствующем применении, например, для проведения инъекций клеток, таких как стволовые клетки, в поврежденную сердечную мышцу или для восстановления сухожилия или связок, как описано выше.
Соответствующие клеточные композиции (например, выделенные клетки ECM по настоящему изобретению и/или дополнительные биологические вещества) можно ввести до, после или во время имплантации или введения композиций ECM. Например, клетки можно посеять в месте введения, дефекта и/или имплантации до имплантации культуральной системы или биологического носителя для доставки субъекту. Альтернативно соответствующие клеточные композиции можно вводить после (например, инъекцией в область дефекта). Там клетки функционируют с индукцией регенерации ткани и/или восстановления клеток. Клетки можно посеять любым способом, позволяющим вводить клетки в область дефекта, например, инъекцией. Инъекционное введение клеток можно провести с использованием любого средства, при котором сохраняется жизнеспособность клеток, например, шприцом или артоскопом.
Описаны композиции ECM для стимуляции ангиогенеза в органах и тканях введением таких композиций для стимуляции эндотелизации и васкуляризации в сердце и близких тканях. Следовательно, в еще одном варианте осуществления настоящее изобретение включает поверхностное покрытие в ассоциации с имплантацией устройства субъекту, включая композиции ECM, описанные в данном документе. Покрытие можно нанести на любое устройство, используемое для имплантации или введения субъекту, такое как кардиостимулятор, стент, стентовый трансплантат, сосудистый протез, сердечный клапан, шунт, порт для доставки лекарственных препаратов или катетер. В некоторых аспектах покрытие можно использовать для модификации заживления раны, модификации воспаления, модификации образования фиброзной капсулы, модификации прорастания внутрь ткани или модификации прорастания внутрь клеток. В еще одном варианте осуществления настоящее изобретение включает способ лечения поврежденной ткани, такой как сердце, кишечник, инфарктная или ишемическая ткань. Ниже приводятся примеры, в которых описано получение композиций ECM, предусмотренных для таких применений. Получение и применение композиций ECM, культивированных в условиях с обычным содержанием кислорода, описано в заявке на патент США 2004/0219134, включенной в данной документ для сведения.
В еще одном варианте осуществления настоящее изобретение включает различные имплантируемые устройства и пластыри для регенерации тканей, содержащие композиции ECM, описанные в данном документе, которые обеспечивают такие преимущества, как прорастание внутрь тканей. Как уже обсуждалось в данном документе, композиции ECM могут служить в качестве покрытий на медицинских устройствах, таких как пластыри или другие имплантируемые устройства. В различных вариантах осуществления такие устройства пригодны для лечения грыжи, восстановления тазового дна (например, пролапса тазового органа), восстановления вращательной манжетки плеча и тому подобное. В близких аспектах покрытия пригодны для ортопедических имплантов, сердечнососудистых имплантатов, урологических слингов и слингов кардиостимулятора.
Например, основным проявлением грыжи является протрузия содержимого брюшной полости в дефект внутри фасции. Хирургические подходы лечения грыжи основаны на элиминации грыжи из брюшной полости и обеспечении твердого закрытия дефекта фасции с использованием протезных, аллогенных и аутогенных материалов. Применяли ряд методов для выполнения такого закрытия, однако, недостатки существующих в настоящее время продуктов и процедур приводят к рецидиву грыжи, когда закрытие вновь ослабевает, позволяя органам брюшной полости вновь опускаться в дефект. Для герниорафии можно использовать пластырь для корректирующей регенерации ткани, такой как биорезорбируемую или синтетическую сетку, покрытую композициями ECM.
В данной области известны различные методы для нанесения биологических покрытий на поверхности медицинских устройств, которые можно использовать в настоящем изобретении. Например, композиции ECM можно покрыть с использованием фотоактивных линкеров, обеспечивающих постоянное ковалентное связывание с поверхностями устройства при активации линкера под действием ультрафиолетового облучения. В качестве примера линкера можно привести линкер для поперечного сшивания TriLiteTM, который, как было показано, является нетоксичным, не вызывающим раздражения биологической ткани и не индуцирующим аллергических реакций. Вещества ECM можно не разделять или разделить на отдельные компоненты, такие как коллагены человека, гиалуроновая кислота (HA), фибронектин и тому подобное перед покрытием или включением в различные имплантируемые устройства. Кроме того, можно включить дополнительные ростовые факторы и подобные вещества для обеспечения полезных свойств имплантации, таких как повышенная клеточная инфильтрация.
В различных близких вариантах осуществления настоящее изобретение относится к способам и устройствам, используемым в косметических/космецевтических применениях, таких как, не ограничиваясь этим, антивозрастная косметика, косметика против морщин, кожные заполнители, аугментация пигментации, уплотнение кожи и тому подобное. Следовательно, в одном варианте осуществления настоящее изобретение относится к способу улучшения поверхности кожи у субъекта, включающему введение субъекту в область морщины композиций ECM, описанных в данном документе. В близком варианте осуществления настоящее изобретение относится к способу восстановления или аугментации мягких тканей у субъекта, включающему введение субъекту в область морщины композиций ECM, описанных в данном документе. В различных косметических применениях композиции можно формулировать в виде подходящих продуктов, таких как композиции для инъекционного и местного применения. Как обсуждается ниже в примерах, включенных в данный документ, было показано, что композиции ECM, формулированные в виде препаратов для местного применения, являются эффективными в различных кожных эстетических применениях, таких как применение против морщин, антивозрастное применение, а также в качестве вспомогательного средства при аблативной лазерной обработке кожи. Было показано несколько полезных эффектов ECM-содержащих препаратов для местного применения. Такие полезные эффекты включали: (1) стимуляцию реэпителизации после повторной чистки; (2) снижение симптомов после неаблативной и аблативной лазерной повторной чистки (например, эритемы, отека, образования корок и сенсориального дискомфорта); (3) получение гладкой, равномерно текстурированной кожи; (4) увлажнение кожи; (5) уменьшение мелких морщин/морщин; (6) повышение упругости и эластичности кожи; (7) снижение депигментации кожи и (8) уменьшение красной, покрытой пятнами кожи.
Композиции по настоящему изобретению можно приготовить, как это известно в данной области, однако с использованием новаторских способов культивирования, описанных в данном документе (например, культивированием в гипоксических условиях). Получение и применение композиций ECM, полученных в условиях культивирования с нормальным содержанием кислорода, для восстановления и/или регенерации клеток, улучшения поверхности кожи и восстановления мягких тканей, описано в патенте США № 5830708, включенном в данный документ для сведения.
В еще одном варианте осуществления настоящее изобретение включает биологическое антиадгезивное средство, содержащее композиции ECM, описанные в данном документе. Средство можно использовать в таких применениях, как антиадгезивные пластыри, применяемые после постановки кишечных анастомозов или анастозомов кровеносных сосудов.
Композиции или активные компоненты, использованные в данном документе, должны применяться в количестве, эффективном для лечения или профилактики конкретного заболевания, которое лечится. Композиции можно вводить терапевтически для достижения терапевтического эффекта или профилактически для достижения профилактического эффекта. Под терапевтическим эффектом понимается устранение или ослабление лежащего в основе состояния или расстройства, которое лечится. Терапевтический эффект также включает заживление или ослабление прогрессирования заболевания, независимо от того, насколько реализуется улучшение.
Количество вводимой композиции будет зависеть от различных факторов, включая, например, тип композиции, конкретное показание для лечения, способ введения, является требуемый эффект профилактическим или терапевтическим, тяжесть заболевания для лечения, и возраст и массу пациента, а также эффективность лекарственной формы. Эффективную дозу может определить специалист в данной области.
Исходные дозы первоначально можно установить по данным тестов in vitro. Исходные дозы также можно установить по данным, полученным в условиях in vivo, на животных моделях. Животные модели являются пригодными для оценки эффективности композиций, предназначенных для усиления роста волос, включая среди прочего, грызунов, приматов и других млекопитающих. Специалисты в данной области могут определить дозировки, подходящие для введения человеку, экстраполяцией данных in vitro и полученных на животных моделях.
Дозировки будут зависеть, среди прочих факторов, от активности кондиционированной среды, способа введения, состояния, которое лечится, и других факторов, которые обсуждались выше. Дозировки и интервал между введениями можно скорректировать индивидуально для обеспечения концентраций, достаточных для достижения терапевтического или профилактического эффекта.
Ниже приводятся примеры, в которых описывается получение композиций ECM, предусмотренных для указанных применений. Последующие примеры приводятся для дополнительной иллюстрации вариантов осуществления по настоящему изобретению, но они не предназначаются для ограничения объема изобретения. Несмотря на то, что они являются типичными из тех, которые можно использовать, альтернативно можно применять другие процедуры, методологии или методики, известные специалистам в данной области.
Пример 1
Дифференциальная экспрессия генов в композициях ECM, культивированных в гипоксических условиях
Первичные неонатальные фибробласты крайней плоти человека культивировали в виде обычных монослоев во флаконах для культивирования тканей и сравнивали с трехмерными культурами фибробластов с естественно секретированным эмбрионально-подобным ECM. Культуры культивировали, как описано в данном документе. Для оценки дифференциальной экспрессии генов образцы общей фракции РНК завершали с использованием микрочипов Agilent Whole Human Genome Oligo Microarrays® для общей экспрессии генов (включая не менее чем 40000 генов), следуя протоколу изготовителя.
При сравнительном анализе было установлено, что в фибробластах регулируется экспрессия генов коллагена и ECM в трехмерных культурах с естественно секретированным ECM при культивировании в гипоксических условиях. Данные по активации и подавлению экспрессии различных генов коллагенов и ECM приведены в таблице 3.
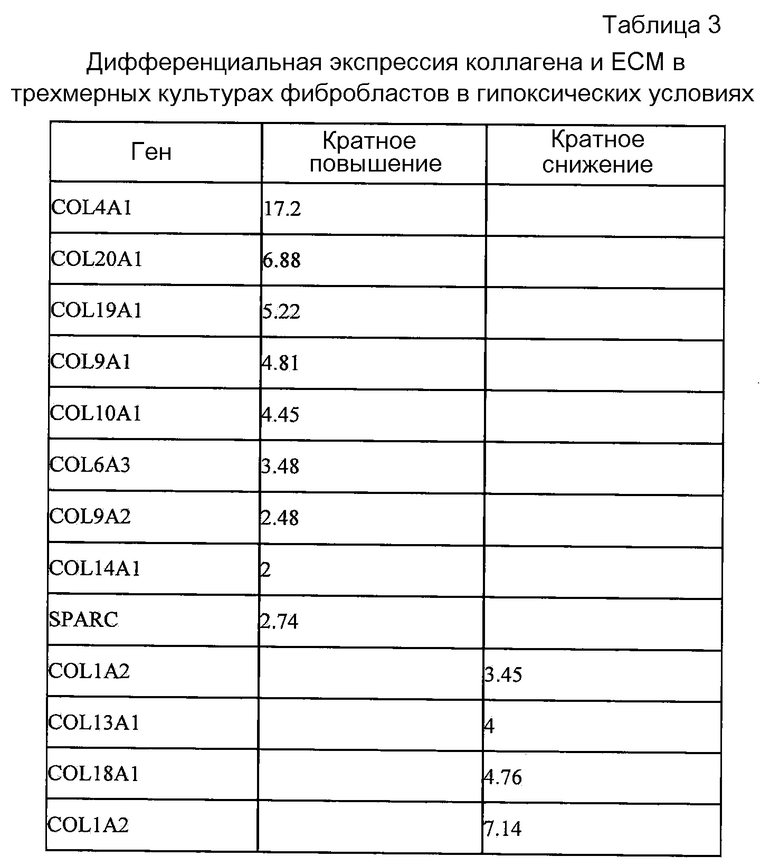
При сравнении было установлено, что в фибробластах регулируется экспрессия генов пути Wnt в трехмерных культурах с естественно секретированным ECM при культивировании в гипоксических условиях. Данные по активации и подавлению экспрессии различных генов пути Wnt приведены в таблице 4.


При сравнении было установлено, что в фибробластах регулируется экспрессия генов пути костного морфогенетического белка (BMP) в трехмерных культурах с естественно секретированным ECM при культивировании в гипоксических условиях. Данные по активации и подавлению экспрессии различных генов пути BMP приведены в таблице 5.

При сравнении было установлено, что в фибробластах регулируется экспрессия дополнительных генов в трехмерных культурах с естественно секретированным ECM при культивировании в гипоксических условиях. Данные по активации и подавлению экспрессии дополнительных генов приведены в таблице 6. Результаты свидетельствуют о том, что условия культивирования в гипоксических условиях приводят к повышению экспрессии мРНК индуцируемого гипоксией фактора (HIF 1A) в 14,78 раз и снижению экспрессии его ингибитора в 4,9 раза. На основании этих данных можно предположить, что культивированная в гипоксических условиях кондиционированная среда находится в среде с более низким парциальным давлением кислорода (гипоксия), поскольку мРНК HIF 1A, которая кодирует трансляцию белка, подвергается позитивной регуляции, а его ингибитор, напротив, подвергается негативной регуляции. Кроме того, VEGF-B (повышение в 4,33 раза), KGF (повышение в 11,51 раза) и IL-8 (повышение в 5,81 раза) также подвергались позитивной регуляции в гипоксических условиях культивирования.

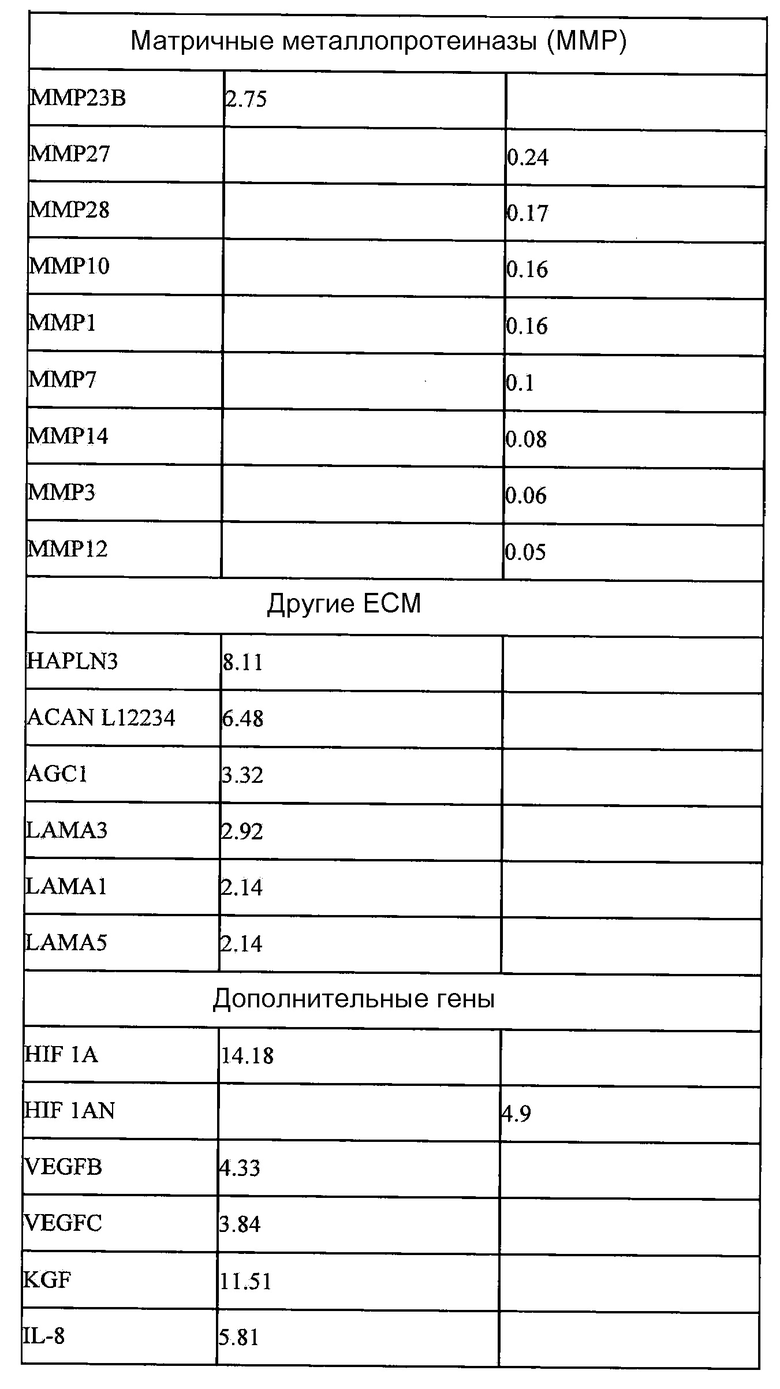

Пример 2
Получение ECM в гипоксических условиях с использованием первичных неонатальных фибробластов крайней плоти человека
Приводятся два примера культивирования ECM в гипоксических условиях с использованием первичной культуры неонатальных фибробластов крайней плоти человека.
Первичные неонатальные фибробласты крайней плоти человека размножали во флаконах для культивирования тканей в присутствии 10% фетальной бычьей сыворотки, 90% DMEM с высоким содержанием глюкозы и с 2 мМ L-глутамина (10% FBS/DMEM). Клетки субкультивировали с использованием раствора 0,05% трипсин/ЭДТА в 3 пассажах, после чего их высевали на декстрановые шарики Cytodex-1 из расчета 0,04 мг сухих шариков/мл среды (5×106 клеток/10 мг шариков во вращающихся колбах емкостью 125 мл, заполненных на 100-120 мл) или найлоновых сетках (25×106 клеток/6×100 см2 найлона). Все культуры поддерживали в нормальной атмосфере с 5% СО2 для размножения и посева, на этой точке культуры с низким содержанием кислорода разделяли на воздухонепроницаемую камеру, которую насыщали газовой смесью 95% азота/5% СО2, для создания в культуральной среде гипоксической среды. Данную систему поддерживали на 1-5% кислорода внутри культурального флакона. Клетки хорошо перемешивали в минимальном объеме, необходимом для покрытия найлона или шариков при посеве, и затем один раз перемешивали в течение 30 мин, затем давали возможность осесть в течение ночи во влажном термостате при 37°С. Культуры подпитывали смесью 10% FBS/DMEM еще в течение 2-4 недель с заменой во время этого периода 50-70% среды каждые 2-3 суток для того, чтобы как клетки пролиферировали и затем начинали откладывать ECM. Культуры подпитывали еще в течение 4-6 недель с использованием 10% бычьей сыворотки с добавлением железа и 20 мкг/мл аскорбиновой кислоты вместо FBS. Первоначально вращающиеся колбы перемешивали со скоростью 15-25 об/мин в примерно в течение 2-4 недель, затем скорость повышали до 45 об/мин и затем поддерживали на этой скорости. Культуры на шариках образовывали крупные аморфные структуры, содержащие ECM, шириной и диаметром примерно 0,5-1,0 см через 4 недели, и затем данные культуры становились гипоксичными за счет диффузии газа и высоких метаболических потребностей.
В дополнительном примере первичные неонатальные фибробласты крайней плоти человека размножали в колбах для получения монослоя и затем культивировали на найлоновых сетках поддерживающей структуры для продукции ECM. Фибробласты размножали в DMEM с высоким содержанием глюкозы, 2 мМ L-глутамина и 10% (об/об) фетальной бычьей сыворотки. Затем в культуры добавляли 20 мкг/мл аскорбиновой кислоты. Через 3 недели параллельные ECM-содержащие культуры с нормальным содержанием кислорода (примерно 16-20%) переводили на гипоксические условия культивирования (1-5% кислорода) в герметичной камере с интенсивным пропусканием газовой смеси 95% азота/5% диоксида углерода (Cat.#MC-101, Billups-Rothenberg, Inc., Del Mar, CA). Для гарантии элиминации атмосферного кислорода из культуральной среды через 2-3 ч атмосферу заменяли для гарантии того, что среда содержит примерно 1-3% кислорода. Оба ряда ECM-содержащих культур культивировали с подпиткой два раза в неделю еще в течение 4 недель и затем культуры готовили для выделения РНК. Общую клеточную фракцию РНК выделяли с использованием промышленно доступного набора, следуя инструкциям изготовителя (Cat.#Z3100, Promega, Inc.). Очищенные образцы РНК хранили при -80°С до подготовки к анализу экспрессии генов микрочипами с использованием Agilent Whole Human Genome Oligo Microarrays®.
Анализ полученных результатов свидетельствовал о том, что имело место примерно 5500 дифференциально экспрессированных транскриптов, детектированных из зондов, полученных при обычном содержании кислорода по сравнению с зондами из культур с низким содержанием кислорода с использованием Agilent Whole Human Genome Oligo Microarrays®. Из них примерно половина (2500) активировалась более чем в 2 раза при низком содержании кислорода, и примерно половина (2500) подверглась негативной регуляции при низком содержании кислорода. Это указывает на то, что низкий уровень кислорода приводил к достоверным изменениям в экспрессии генов в условиях in vitro. Особый интерес представляют транскрипты белков ECM; в частности, ряд генов коллагена подвергся позитивной регуляции, в то время как гены матрикс-деградирующих ферментов имели подавление.
Пример 3
Человеческий эмбриональный внеклеточный матрикс, полученный тканевой инженерией, для терапевтических применений
Эмбриональный ECM создает среду, обеспечивающую быструю клеточную пролиферацию и заживление ран без образования рубцов или адгезии. Была высказана гипотеза о том, что трехмерный рост человеческих неонатальных фибробластов в условиях, которые напоминают среду эмбрионов на ранней стадии развития, до ангиогенеза (гипоксия и пониженные гравитационные силы), будет стимулировать продукцию ECM с эмбриональными свойствами. Анализ генов с использованием микрочипов показал дифференциальную экспрессию более 5000 генов в гипоксических условиях по сравнению с обычными условиями культивирования тканей. Продуцированный ECM был аналогичен мезенхимальной ткани эмбрионов в том отношении, что он был относительно богат коллагенами типа III, IV и V, и гликопротеинами, такими как фибронектин, SPARC, тромбоспондин и гиалуроновая кислота. Поскольку ECM также играет важную регуляторную роль в связывании и презентации ростовых факторов в предполагаемых нишах, которые поддерживают регенеративные популяции стволовых клеток с ключевыми ростовыми факторами, то авторы оценивали влияние гипоксии на экспрессию ростовых факторов во время образования эмбрионально-подобного ECM в культуре. Также гипоксия может повышать экспрессию факторов, которые регулируют заживление и органогенез раны, таких как VEGF, FGF-7 и TGF-β, а также многочисленные wnt, такие как wnt 2b, 4, 7a, 10a и 11. Эмбриональный человеческий ECM также может стимулировать повышение метаболической активности в человеческих фибробластах в условиях in vitro, что определяли по повышенной активности ферментов с использованием MTT-теста. Кроме того, авторы детектировали повышение числа клеток в ответ на человеческий ECM. Данный человеческий ECM можно использовать в качестве биологического покрытия поверхностей и заполнителя тканей в различных терапевтических применениях, где требуется рост новых тканей и заживление без образования рубцов или адгезий.
Пример 4
Получение активности природного растворимого wnt для применений в регенеративной медицине
Стволовые клетки или клетки-предшественники, которые могут вызывать регенерацию тканей во взрослых организмах, таких как кожа или кровь, в некоторой степени повторяют эмбриональное развитие при осуществлении такой регенерации. Результаты все возрастающего числа исследований показали, что ключевые регуляторы плюрипотентности и линия-специфической дифференцировки, которые имеют место во время эмбриогенеза, в некоторых обстоятельствах реэкспрессируются во взрослых организмах. Семейство WNT секретируемых морфогенетических ростовых факторов и факторов, специфических для стадий развития, является одним из семейств ростовых факторов, которые могут потенциально обеспечить ценные исследовательские инструменты и в конечном итоге терапевтическое лечение в клинике. Однако было показано, что для WNT трудно применять современные методы обычной рекомбинантной экспрессии и очистки на промышленной основе, и отсутствуют сообщения о крупномасштабном получении WNT, которое способствовало бы клинической разработке продуктов на основе WNT. Были разработаны методы культивирования эмбрионально-подобного ECM в культуре с использованием неонатальных фибробластов кожи человека на различных поддерживающих структурах в культуре с получением трехмерных тканевых эквивалентов. При этом было установлено, что данные культуры могут быть источником биологически активных WNT в промышленном масштабе, которые находятся в бессывороточной кондиционированной среде, используемой для получения ECM. Авторы представляют данные по данному продукту-кандидату WNT.
Анализ экспрессии генов клеток показал, что, экспрессировалось, по меньшей мере, 3 гена WNT (wnt 5а, wnt 7а и wnt 11) и также небольшое число генов, связанных с сигнальным путем wnt; однако их функция полностью не ясна. Данные по экспрессии генов получали в биологическом тесте в условиях in vitro для wnt-сигнального пути (по транслокации в ядро β-катенина в первичных человеческих эпидермальных кератиноцитах) и оценивали активность wnt в стволовых клетках крови. Результаты обоих тестов демонстрировали активность, согласующуюся с активностью канонического wnt. Кроме того, кондиционированная среда из данных культур проявляла активность wnt при инъекционном введении в кожу мышей, индуцируя стволовые клетки волосяных фолликулов для вхождения в фазу анагена, стимулируя, таким образом, рост волос. Эти данные указывают на то, что для проявления активности стабилизированных WNT в определенной и бессывороточной кондиционированной среде не требуется их выделения. Этот продукт можно использовать для регенерации волосяных фолликулов и в качестве ценного исследовательского инструмента при культивировании различных стволовых клеток человека.
Пример 5
Фибробласты, культивированные в гипоксических условиях, демонстрируют продукцию уникального ECM и экспрессию ростовых факторов
Человеческие неонатальные фибробласты кожи продуцируют ECM при культивировании в условиях in vitro, который может заменять поврежденную дерму в применениях в регенеративной медицине, например, при заживлении раны. Поскольку в процессе заживления раны также повторяется эмбриональное развитие при стимуляции эмбриональной среды, то авторы высказали предположение о том, что продуцированный ECM будет обеспечивать повышенный ECM в применениях для регенерации тканей. Таким образом, ECM, продуцированный неонатальными фибробластами человека, культивировали в гипоксических условиях в культуре для стимуляции гипоксии, которая имеет место на ранней стадии развития эмбрионов до ангиогенеза. Целью было получение ECM с эмбриональными свойствами с использованием гипоксических условий во время развития тканей в культуре.
ECM, продуцированный в таких гипоксических культурах, был аналогичен эмбриональной мезенхимальной ткани в том отношении, что он относительно богат коллагенами типа III и V, и гликопротеинами, такими как фибронектин, SPARC, тромбоспондин и гиалуроновая кислота. Поскольку ECM также играет важную регуляторную роль в связывании и презентации ростовых факторов в предполагаемых нишах, которые поддерживают регенеративные популяции стволовых клеток с ключевыми ростовыми факторами, то авторы оценивали влияние гипоксии на экспрессию ростовых факторов во время образования эмбрионально-подобного ECM в культуре. Было показано, что гипоксия может повышать экспрессию факторов, которые регулируют заживление и органогенез раны, таких как VEGF, FGF-7 и TGF-β.
Человеческий ECM также стимулировал повышение метаболической активности в фибробластах человека в условиях in vitro по данным определения повышенной ферментативной активности с использованием MTT-теста. Кроме того, детектировали повышение числа клеток в ответ на человеческий ECM. Эти результаты обосновывают применение данного человеческого ECM в качестве покрытия/поддерживающей структуры в культурах эмбриональных клеток и в качестве биологического поверхностного покрытия/заполнителя в различных терапевтических применениях или медицинских устройствах.
Пример 6
Биолого-медицинские материалы, покрытые человеческим внеклеточным матриксом (hECM)
Сообщалось, что ECM создает среду, обеспечивающую быструю клеточную пролиферацию и заживление без образования рубцов или адгезии. С использованием способов, описанных в данном документе, получали уникальный эмбрионально-подобный человеческий ECM (hECM) культивированием неонатальных фибробластов при низком содержании кислорода и удельной плотности. Полученные результаты включали: ангиогенез, когда hECM помещали на хориоаллантоидную мембрану, и снижение миграции воспалительных клеток, когда hECM наносили на найлоновую сетку и имплантировали подкожно в боковую область мышам SCID. Основываясь на этих данных, была высказана гипотеза о том, что покрытие hECM полипропиленовой сетки будет отменять миграцию воспалительных клеток и фиброзное инкапсулирование на границе раздела материал-биологическое вещество в подкожной области мышей SCID.
Композиции ECM, продуцированные с использованием происходящих от человека веществ (hECM), наносили на пропиленовую сетку с использованием фотоактивного линкера. hECM наносили на биопсийный материал 6 мм, перфорированный полипропиленом, посредством ковалентного связывания, индуцированного УФ-светом (Innovative Surface Technologies (ISurTec) TriLiteTM Crosslinker). Покрытые и непокрытые hECM биопсийные штампы из полипропилена стерилизовали с использованием E-BeamTM (BeamOne LLC E-BEAMTM) или этиленоксида (ETO) (описаны ETO Flagstaff Medical Center). Затем каждый полипропиленовый диск 6 мм разделяли на две симметричных полукруглых прокладки. Наконец, полипропиленовые имплантаты вводили билатерально подкожно в боковой области мышей в асептических условиях. Образцы эксплантировали через 2 и 5 недель для проведения гистологических исследований.
Иммунофлуоресцентное окрашивание антителами к фибронектину hECM-покрытой полипропиленовой сетки показывало, что вещества ECM связывались и формировали равномерное покрытие на волокнах сетки в отличие от непокрытой сетки. Покрытая hECM сетка подходит для имплантируемых пластырей в медицинских применениях, таких как лечение грыжи и восстановления тазового дна. С помощью иммунофлуоресцентного окрашивания антителами к фибронектину было показано, что вещества ECM покрывают отдельные волокна сетки, что обеспечивает улучшенное клеточное врастание.
hECM имплантировали на хориоаллантоидную мембрану цыпленка (CAM), и при этом наблюдали стимуляцию микроваскулярного ответа по росту новых микрососудов. Кроме того, покрытая hECM найлоновая сетка, подкожно имплантированная мышам на четыре недели, демонстрировала повышенную биологическую совместимость по сравнению с непокрытой найлоновой сеткой. В частности, при имплантации покрытых hECM найлоновых волокон наблюдали меньшее количество воспалительных клеток и более тонкую фиброзную капсулу.
Оценку биологической совместимости проводили через 2 и 5 недель после имплантации покрытой hECM найлоновой сетки окрашиванием образцов гематоксилин-эозином. Для анализа FBGC образцы кодировали, исследовали с использованием морфометрии, разделяли в группы, проводили статистическую обработку, затем декодировали. Определяли число гигантских клеток инородных тел (FBGC). Число FBGC на волокно определяли через 2 недели после имплантации, как показано на фигурах 1А-В, а также проводили исследование дополнительных образцов, результаты которого приведены на фигурах 14А-В. Число гигантских клеток инородных тел на волокно через 5 недель после имплантации показано на фигурах 2А-В, а результаты исследования дополнительных образцов приведены на фигурах 15А-В. Очевидно снижение FBGC для покрытой hECM полипропиленовой сетки по сравнению с непокрытой сеткой. Через две недели установленное среднее число FBGC на образец было статистически выше (post-hoc тест с поправкой Бонферрони, анализ ANOVA, р<0,05) для непокрытого полипропилена (9,20±2,03) по сравнению с покрытым hECM полипропиленом (4,53±0,89). Через 5 недель среднее число FBGC на образец, которое определили для непокрытого полипропилена, было выше (10,95±2,15), хотя, различие по сравнению с покрытым hECM полипропиленом (8,17±1,41) не носило статистически значимый характер.
Результаты указывали, что покрытый hECM полипропилен может снижать образование фиброзных капсул. Фиброзное инкапсулирование оценивали через 2 и 5 недель с использованием окрашенных Trichrome образцов. Для анализа капсул образцы кодировали, исследовали с использованием морфометрии, разделяли в группы, проводили статистическую обработку, затем декодировали. Через 2 недели средняя толщина капсулы не была статистически достоверно выше (post-hoc тест с поправкой Бонферрони, анализ ANOVA, р<0,05) для покрытого hECM полипропилена (23,70±2,70 мкМ) по сравнению с непокрытым полипропиленом (19,70±3,00) (фигуры 16А-В). Через 5 недель средняя толщина капсулы для покрытого hECM полипропилена составила (10,40±1,10 мкМ) по сравнению с непокрытым hECM полипропиленом (12,30±1,20) (фигуры 17А-В). Вновь различия между покрытым hECM полипропиленом и непокрытым полипропиленом не были статистически достоверными. Хотя, при оценке средних процентных различий в образовании фиброзных капсул было установлено достоверное различие через 2 и 5 недель. Среднее процентное снижение фиброзного инкапсулирования в период между 2 и 5 неделями составило 37,6% для непокрытого hECM полипропилена по сравнению с 56,1% для покрытого hECM полипропилена.
Механизм выработки FBGC является результатом слияния макрофагов в иммунном ответе на имплантируемый биологический материал, такой как полипропилен. Такие крупные многоядерные клетки обеспечивают эффективное средство для количественной оценки воспалительного ответа на имплантируемые биологические материалы. Наблюдали достоверное снижение числа FBGC на образец из покрытого hECM полипропилена по сравнению с непокрытым полипропиленом через 2 недели. На основании этих данных можно предположить, что покрытие человеческим ECM может служить в качестве применения для различных имплантируемых устройств.
Ранее на эффективность и продолжительность действия имплантируемых устройств оказывали влияние специфические иммунные ответы, включая FBGC и образование фиброзной капсулы. В частности, FBGC могут выделять деградируемые агенты, такие как супероксиды и свободные радикалы, а также другие деградируемые агенты, оказывающие влияние на эффективность и продолжительность действия устройства. Такие негативные эффекты являются особенно важными, поскольку известно, что FBGC располагаются практически вокруг имплантата во время нахождения имплантата. Образование фиброзной капсулы, которая появляется в виде твердого сосудистого коллагенового инкапсулята вокруг имплантата для изоляции инородных имплантируемых устройств от организма хозяина или ткани хозяина. Данный ответ в некоторых случаях может не только вызвать дискомфорт у пациента, но также может сократить жизнеспособность устройства и даже снизить эффективность устройства. Таким образом, покрытие, которое снижает выработку FBGC и образование фиброзной капсулы, является очень желательным для продолжительного действия и высокой эффективности имплантируемых устройств.
Установление того факта, что hECM на полипропилене будет снижать присутствие FBGC и потенциально уменьшать образование фиброзной капсулы на границе материал-биологическое вещество обосновывает необходимость в дальнейшем проведении исследований. Дальнейшее изучение может включать наблюдения на более отдаленных временных точках за изменениями в толщине фиброзного инкапсулята с покрытыми hECM и непокрытыми биологическими материалами. Кроме того, тестирование других биологических материалов, таких как дакрон, найлон, нержавеющая сталь и титан в различных вариантах осуществления в условиях in vivo, может выявить другие желательные покрытые hECM биологические материалы.
Пример 7
Применение композиций внеклеточного матрикса для стимуляции роста волос
В данном примере показана стимуляция роста волос введением композиций ECM.
Получали клетки волосяных фолликулов человека и клетки, отобранные из волосяных фолликулов, для определения способности композиций ECM, описанных в данном документе, стимулировать и поддерживать образование волос. Клетки волосяных фолликулов получали от Alderans Research International. Клетки культивировали в присутствии ECM. Анализ клеток через 4 и 8 недель культивирования показывал наличие структур, напоминающих волосяные фолликулы, а также структур, напоминающих стержни волос, которые показаны на фигуре 3А и 3В. Через два месяца непрерывного культивирования клетки оставались живыми и растущими.
Клетки, культивированные в течение 4 недель в присутствии композиций ECM, трансплантировали мышам. Через 4 недели после трансплантации культивированные волосяные фолликулы человека образовывали множество крупных фолликулов в отличие от контрольных клеток, показывающих только нормальное число небольших «отдыхающих» волосяных фолликулов, что наблюдали с использованием микроскопического анализа.
Основываясь на этих установленных фактах, проводили определение роста волос в условиях in vivo у людей для оценки регенерации волосяных фолликулов de novo. В испытании участвовали 24 мужчины в возрасте от 18 до 45 лет, страдающих облысением по мужскому типу (MPHL). Всем участникам испытаний ранее не проводилось инвазивной или минимально инвазивной местной операции на скальпе или местного лечения MinoxidilTM или FinasterideTM. Использовали лазерный аппарат Palomar Starluz 550p (1540 неаблативный и 2940 аблативный). Продолжительность исследования составляла 12 месяцев по принципу продолженного наблюдения, исходный период и 5 месяцев (после одной подкожной инъекции). После инъекции в течение трехдневного периода вымывания проводили наблюдение, и субъекты пользовались только шампунем CetaphilTM в течение всех испытаний. До инъекции проводили комбинированное лечение лазером и микродермабразию.
Субъектам вводили носитель, смешанный с hECM, для определения активности белка wnt и включали wnt 7а трансдермально вместе с контрольным носителем и физиологическим раствором. Конечные точки исследования включали оценку по клинической шкале из 7 пунктов (3 хирурга по трансплантации волос «вслепую»), клиническую макрофотографию (число фолликулов), отбор биопсии кожи с помощью пробойника 2 мм и опросники самооценки.
Анализировали отдельные фолликулярные единицы у субъектов. На 12 неделе у одного и того же субъекта подсчитывали количество фолликулов и сравнивали с этим показателем в исходном периоде в начале испытаний. Наблюдали увеличение фолликулярных единиц у субъектов, которым вводили hECM, без пертурбации. Например, у одного субъекта лечение повышало количество видимых волосяных фолликулов от 217 в исходном периоде до 265 через 12 недель. Общее число волос у субъекта увеличилось от 307 до 360, что соответствовало в целом увеличению примерно на 20%. У других субъектов наблюдали следующие показатели увеличения числа фолликулов: субъект 009 (число волос в исходном периоде 179, через 12 недель число волос 193, через 5 месяцев число волос 201); субъект 013 (число волос в исходном периоде 266,5, через 12 недель число волос 267,5, через 5 месяцев число волос 294); субъект 024 (число волос в исходном периоде 335,5, через 12 недель число волос 415,5, через 5 месяцев число волос 433). У 12 из 13 пациентов (92,3%) введенный hECM в исследовании проявлял эффективность через 12 недель. На фигуре 18 приведены результаты дополнительной оценки роста волос через 3 месяца.
Дополнительные результаты приведены на фигурах 19 и 20, показывающие показатели роста волос у 2 испытуемых субъектов соответственно через 12 и 22 недель.
Во время испытания анализировали дополнительные параметры волос. На 12 и 20 неделе анализировали относительное количество волос по сравнению с исходным периодом (0 неделя), определяли число терминальных волос по сравнению с исходным периодом и анализировали толщину волос по сравнению с исходным периодом. Например, у одного субъекта в результате лечения через 12 недель количество волос, количество терминальных волос и толщина фолликулов увеличилось соответственно на 22,4, 27,8 и 23,9% по сравнению с исходным периодом. У другого субъекта в результате лечения увеличилось количество волос, количество терминальных волос и толщина фолликулов через 12 недель соответственно на 23,7, 24,2 и 22,2% по сравнению с исходным периодом. У субъекта 009 (имеющего в исходном периоде число волос 179, через 12 недель число волос составило 193, через 5 месяцев 201, как указано выше) в результате лечения увеличилось количество волос, количество терминальных волос и толщина фолликулов через 12 недель соответственно на 7,8, 48,5 и 19,2% по сравнению с исходным периодом; и через 20 недель на 12,9, 33,0 и 21,1% по сравнению с исходным периодом. У субъекта 013 (имеющего в исходном периоде число волос 266,5, через 12 недель число волос составило 267,5, через 5 месяцев 294, как указано выше) в результате лечения повысилось количество волос, количество терминальных волос и толщина фолликулов через 12 недель соответственно на 0,2, 25,0 и 8,3%; и через 20 недель на 10,3, 41,4 и 23,0% по сравнению с исходным периодом. У субъекта 024 (имеющего в исходном периоде число волос 335,5, через 12 недель число волос составило 415,5, через 5 месяцев 433, как указано выше) в результате лечения повысилось количество волос, количество терминальных волос и толщина фолликулов через 12 недель соответственно на 23,7, 24,2 и 22,2%; и через 20 недель на 29,1, 5,9 и 17,3% по сравнению с исходным периодом.
Результаты по агрегатам для 13 участников испытаний приведены на фигурах 21 и 22. Распределение ответов у участников испытаний через 3 месяца приведено на фигурах 23-26.
Следует отметить, что у участников испытаний наблюдали статистически достоверное повышение числа терминальных волос и увеличение плотности толщины через 3 месяца (84,6% pts). Кроме того, не наблюдали побочных реакций, в результате гистологических исследований не было выявлено патологии, и отсутствовали гамартомы.
Результаты указывают на возможное использование hECM в дополнительных применениях, таких как предупреждение потери волос после трансплантации и роста бровей и ресниц. У пациентов с трансплантацией волос, как известно, волосы выпадают, и обычно требуется 4-5 месяцев для их восстановления, таким образом, лечение hECM будет предупреждать потерю волос у таких субъектов после трансплантации.
Пример 8
Получение композиций человеческого внеклеточного матрикса (hECM)
Композицию человеческого ECM получали с использованием неонатальных фибробластов человека. Фибробласты высевали на шарикообразные структуры, кондиционированные жидкой средой. Условия культивирования оптимизировали без необходимости в применении фетальной бычьей сыворотки. В течение нескольких суток в условиях эмбриональной культуры, описанных в данном документе, клетки образовывали плотный эмбрионально-подобный ECM. Наблюдали секрецию белков семейства Wnt, а также нескольких ростовых факторов.
Культуры выращивали до слияния. Затем культуры обрабатывали стерильной водой для индукции равномерного лизиса клеток. Затем бесклеточный hECM промывали для гарантии удаления всех живых клеток и клеточного дебриса, и исследовали микроскопией для подтверждения удаления клеточного дебриса. Затем человеческие фибробласты помещали в культуральные флаконы, покрытые hECM, или высевали в необработанные флаконы, и затем покрывали толстым слоем матрикса. Белки ECM, идентифицированные в hECM, приведены в таблице 8.
Белки внеклеточного матрикса, обнаруженные в hECM
Наблюдали, что hECM индуцирует усиление метаболической активности клеток, что определяли по повышенной активности ферментов с использованием MTT-теста, как показано на фигуре 4. Человеческий ECM в отличие от мышиного ECM индуцировал повышение метаболической активности, зависимое от концентрации, по данным MTT-теста. Наблюдали, что клетки быстро и однородно инфильтрируют верхний слой hECM. В дополнении отмечали зависимое от концентрации увеличение числа клеток в ответ на hECM по данным теста Pico Green.
Как правило, известные покрытия, инъекционные препараты и имплантируемые матричные продукты представляют собой бычьи коллагены, свиные матричные белки из кишечника или мочевого пузыря, гиалуроновую кислоту или человеческий ECM, полученный из кожи трупов. Несмотря на то, что данные продукты имеют преимущества, заключающиеся в создании более физиологичной среды, ни один из них не является полностью человеческим и не содержит полный набор матричных белков, обнаруженных в молодых, развивающихся тканях. Продуцированный hECM содержит те же вещества ECM, обнаруженные в молодой здоровой ткани. Кроме того, наблюдали, что он поддерживает активную пролиферацию человеческих клеток, а также быстрое врастание клеток. Имеется несколько очевидных преимуществ в использовании hECM в применениях, включая применение у человека. Например, hECM способствует быстрой интеграции клеток-хозяев и усиленному заживлению (функционирует в качестве обычной поддерживающей структуры для клеток-хозяев и последующем ремоделировании). Кроме того, hECM устраняет проблему в отношении передачи вирусов от животного, отличного от человека, и человеческих тканей (в частности, BSE из тканей крупного рогатого скота и TSE из тканей человека). Кроме того, имеет место постоянный состав и функция продукта для hECM по сравнению с биологическими продуктами, в частности, дермы и широкой фасции человека. Дополнительно hECM снижает эрозию тканей хозяина по сравнению с синтетическими имплантатами.
Пример 9
Внеклеточный матрикс, полученный из человеческих фибробластов в гипоксических условиях, для медицинских эстетических применений
Проводили двойное слепое, рандомизированное испытание hECM для местного применения после аблативной лазерной обработки кожи на лице. В испытании участвовал 41 субъект в возрасте от 40 до 60 лет. Всем участникам испытаний ранее не проводилось инвазивной или минимально инвазивной операции или антивозрастного лечения в течение последних 12 месяцев. Лазерная процедура включала полную фракционную аблативную лазерную обработку, периокулярную, периоральную и на всем лице. Использовали лазерный аппарат Palomar Starluz 550p (1540 неаблативный и 2940 аблативный).
Субъектам вводили композиции hECM для местного применения один раз в день (в различной концентрации) или плацебо в течение 14 суток. Конечные точки испытаний включали клиническую фотосъемку (3 дерматолога, которые проводили оценку «вслепую»), оценку трансэпидермальной потери влаги (TEWL), проведение биопсии кожи с помощью пробойника и оценку эритемы, отека и образования корок.
Композиция hECM 10Х обеспечивала наиболее выраженное клиническое устранении симптомов по сравнению с контрольным растворителем (оценку проводили два косметолога-дерматолога «вслепую», которые не участвовали в проведении клинического испытания). Результаты приведены на фигурах 6 (эритема), 7 (отек) и 8 (образование корок). Фотографическая оценка также указывала на снижение выраженности эритемы у нескольких пациентов на 3, 7 и 14 сутки.
Также оценивали трансэпидермальную потерю влаги (TEWL) на 3, 7 и 14 сутки после лазерной обработки у всех 41 субъектов. Результаты приведены на фигуре 9. Композиция hECM 10Х приводила к наиболее существенному улучшению барьерной функции рогового слоя кожи на 3 и 7 сутки по сравнению с контрольным растворителем. На сутки 7 действие композиции hECM было статистически достоверным (р<0,05) по сравнению с контрольным растворителем. Данное наблюдение согласуется с тем фактом, что через 7 суток после аблативной фракционной лазерной обработки были субъекты, у которых наблюдали реэпителизацию.
Также проводили двойное слепое, рандомизированное испытание hECM для местного применения в антивозрастном лечении (например, при уменьшении морщин). В испытании участвовало 26 субъектов в возрасте от 40 до 65 лет. Всем участникам испытаний ранее не проводилось инвазивной или минимально инвазивной операции или антивозрастного лечения в течение последних 12 месяцев. Субъектам вводили композиции hECM для местного применения дважды в день или плацебо в течение 10 недель. Конечные точки испытаний включали клиническую фотосъемку (2 дерматолога-косметолога «вслепую»), корнеометрию влажности кожной поверхности, оценку эластичности с помощью кутометра, проведение биопсии кожи с помощью пробойника, молекулярную оценку (Epidermal Genetic Information Retrieval (EGIR)).
Фотографическая оценка лицевой области указывала на генерацию более светлой пигментации, более мягкой текстуры кожи, более ровного тона кожи и уменьшения мелких морщин и глубоких морщин через 10 недель после введения hECM.
Также проводили трехмерную профилометрию силиконовых отпечатков периокулярной области у 22 из 26 субъектов. Для постановки анализа коллимированный световой пучок направляли под углом 25°С к плоскости отпечатка. Отпечаток помещали в держатель, который фиксировал направление положения петли отпечатка таким образом, чтобы отпечаток можно было вращать для выравнивания нормального или параллельного направления петли со случайным направлением света. Делали отпечатки «гусиных лапок» возле каждого глаза в направлении петли к уху. Нормальная ориентация отбора проб обеспечивала оценку текстуры глубоких мимических морщин («гусиных лапок»). Параллельная ориентация отбора проб обеспечивала оценку текстуры небольших мелких морщин. Результаты приведены на фигуре 10.
Проводили двойное слепое, рандомизированное испытание hECM для местного применения после аблативной лазерной обработки кожи лица. В испытании принимало участие 49 субъектов в возрасте от 40 до 60 лет. Всем участникам испытаний ранее не проводилось инвазивной или минимально инвазивной операции или антивозрастного лечения в течение последних 12 месяцев. Лазерная процедура включала полную фракционную аблативную лазерную обработку кожи, периокулярную, периоральную и на всем лице. Использовали лазерный аппарат Palomar Starluz 550p (1540 неаблативный и 2940 аблативный). Субъектам вводили композиции hECM для местного применения два раза в день или плацебо в течение 14 суток. Конечные точки испытаний включали клиническую фотосъемку (3 дерматолога, которые проводили оценку «вслепую»), мексаметрию и субъективную оценку.
Фотографическая оценка лицевой области на 1, 3, 5, 7 и 14 сутки после операции указывала на очевидное снижение эритемы на все временные точки по сравнению с плацебо.
Количество дней применения вазелина оценивали после операции, как показано на фигуре 11. Оценку эритемы проводили, как показано на фигуре 12. Результаты мексаметрии приведены на фигуре 13 для обеих аблативных (2940) и неаблативных (1540) лазерных процедур.
Результаты испытаний указывали на несколько полезных характеристик средств, содержащих hECM, для местного применения. Такие полезные эффекты включали: (1) стимуляцию реэпителизации после повторной чистки; (2) снижение симптомов после неаблативной и аблативной лазерной повторной чистки (например, эритемы, отека, образования корок и сенсориального дискомфорта); (3) получение гладкой, равномерно текстурированной кожи; (4) увлажнение кожи; (5) уменьшение мелких морщин/морщин; (6) повышение упругости и эластичности кожи; (7) снижение депигментации кожи и (8) уменьшение красной, покрытой пятнами кожи.
Пример 10
Применение композиций внеклеточного матрикса для стимуляции роста волос
В данном примере показана стимуляция роста волос введением композиций ECM.
После проведения доклинических исследований по оценке безопасности и эффективности, результаты которых свидетельствовали о минимальных токсических свойствах, и на основании которых можно было предположить, что индукция фазы анагена в телогенных фолликулах на мышиной модели роста волос может ускоряться при инъекционном введении hECM, провели предварительное исследование активности препарата у мужчин. Клиническое испытание представляло собой двойное слепое, рандомизированное испытание в одном центре San Pedro Sula, Гондурас, и первоначально было спланировано для оценки безопасности в клиническом применении продукта hECM. Вторичной целью исследования была оценка клинической активности продукта или получение «доказательства концепции». Также в качестве фрагмента испытания оценивали насколько пертурбация/стимуляция скальпа до инъекционного введения hECM будет оказывать аддитивный эффект на рост волос. Выбирали три различных устройства для пертурбации: (1) микродермабразию (MegaPeelTM, DermaMed Intl, Inc., Lenni, PA); (2) перекрывающиеся пучки неаблативного 1540 и аблативного 2940 Erbium Laser (Palomar Medical Technologies, Inc., Burlington, MA) и (3) стимуляцию терапией низкочастотным светом с использованием Revage670TM (Apira Science Inc., Newport Beach, CA). Отобранных для испытаний участников произвольно распределяли на один из трех методов пертурбации. В данном испытании тестировали два препарата: 10х концентрированный, бессывороточный препарат и второй неконцентрированный препарат, содержащий бычью сыворотку. Присутствие белков Wnt в hECM, который использовали в данных испытаниях, оценивали иммуноблоттингом с использованием первичных антител, распознающих белок Wnt7a (Santa Cruz Biologicals, CA). Биологическую активность канонического Wnt в hECM подтверждали демонстрацией транслокации β-катенина в ядро эпидермальных кератиноцитов человека в условиях in vitro. LiCl использовали в качестве позитивного контроля (данные не приводятся), и обработка растворителем или hECM в присутствии антагониста рецептора Wnt DKK-1 не генерировала транслокацию β-катенина. Раствор hECM также содержал VEGF и KGF, что определяли ELISA.
После получения информированного согласия 26 здоровых субъектов в возрасте 18-55 лет были включены в испытание. Критерии для включения в испытание включали балл 4-6 по шкале Fitzpatrick I-IV, Norwood/Hamilton для оценки облысения по мужскому типу и отсутствие предшествующего лечения волос или иммунодефицита. В качестве области лечения определяли четыре зоны на скальпе каждого субъекта, две спереди и две сзади. Каждую область лечения маркировали татуировкой по периферии. Два передних участка рандомизировали и вводили один из двух препаратов hECM или плацебо (некондиционированная среда) без предварительной пертурбации. Задние участки для лечения пертубизировали с использованием одной из 3 обработок, указанных выше, с последующим немедленным инъекционным введением hECM или плацебо, также рандомизируя введение справа/слева. У всех пациентов на каждый участок приходилось по четыре равномерно сделанных внутрикожных инъекции по 0,1 см3 на нулевые сутки.
На сутки 0, через 12 и 22 недели проводили комплексное обследование, которое включало общую оценку исследователя, определение числа волос макрофотографией и самооценку испытуемого субъекта. У 6 пациентов проводили биопсию с использованием пробойника (4 мм) в исходном периоде и через 48 ч после визита на неделе 22 и использовали для гистопатологического анализа. Также оценивали безопасность посредством визуального осмотра клиницистом на каждую временную точку по наличию воспаления, покраснения, отека, зуда, жжения, набухания и других побочных эффектов. Общее состояние и макрофотографии оценивались независимыми дерматологами по любому наблюдаемому побочному эффекту, включая покраснение, набухание и вросшие волосы. Биологические и клинические эффекты лечения оценивались посредством получения макрофотографических изображений TrichoScan и анализа соотношения фаз анагена:телогена, диаметра волос, плотности волос, толщины волос и числа пушковых и непушковых волос. Исследователи применяли оценочную систему для определения визуального улучшения регионального роста волос.
Основной целью исследования была оценка клинической безопасности введения hECM людям. Все пациенты хорошо переносили процедуры и без существенных жалоб, сообщалось о клинических симптомах или признаках побочных реакций у всех субъектов. Результаты гистопатологического анализа биопсийного материала, отобранного на неделе 22 после обработки, свидетельствовали о минимальном или незначительном воспалении в месте инъекции, и отсутствии аномальной морфологии, гамартом или других патологических ответных реакций. Основываясь на данных наблюдениях, было сделано заключение о том, что однократная, внутрикожная инъекция hECM не приводит к какой-либо существенной токсичности, патологии или другим побочным эффектам во время курса лечения.
Вторичной целью была оценка клинического действия hECM на рост волос, которую проводили анализом изображений с помощью микроскопа Trichoscan. Результаты выражены в средних значениях±стандартная ошибка среднего, если не указано иначе. Равноценность участков лечения на нулевые сутки до проведения манипуляций оценивали с использованием одностороннего анализа ANOVA. Последующие различия между групповыми средними значениями в опытной группе на сутки 0, через 12 и 22 недели после лечения оценивали с использованием парного (для повторных определений), двухстороннего теста Стьюдента с t-критерием. Все другие различия между групповыми средними значениями оценивали с использованием непарного, двухстороннего теста Стьюдента с t-критерием. Статистическую значимость устанавливали на уровне α=0,05. Сравнение на сутки 0, т.е. групповые средние значения до лечения по показателю роста волос между необработанными и обработанными участками указывало на отсутствие достоверных различий. Следовательно, любые последующие различия в росте через 12 или 22 недели после начала лечения могут рассматриваться в качестве результата испытуемого лечения.
Анализ изображений с помощью микроскопа TrichoScan обработанных плацебо участков (n=12) на неделе 12 и 22 свидетельствовал об отсутствии достоверных улучшений по всем показателям роста волос. Кроме того, отсутствовали достоверные эффекты препарата hECM, содержащего сыворотку крови. Однако в течение первых 12 недель оценочного периода на участках, обработанных бессывороточными hECM в высоких концентрациях (n=13), наблюдали улучшение роста волос по всем показателям, за исключением плотности пушковых волос, которая оставалась без изменений в течение всего курса испытаний (фигуры 1D, 1E). Пертурбация до введения hECM не приводила к усилению роста волос по сравнению с введением одного бессывороточного hECM. Через 12 недель имело место статистически достоверное повышение по сравнению с 0 сутками толщины стержня волос (р<0,05), плотности толщины волос (р<0,05) и числа непушковых, терминальных волос (р<0,005) на участках, обработанных hECM (фигура 27). Улучшение, вызванное hECM, было статистически достоверно выше по сравнению с участками, обработанными плацебо, по толщине стержня волос (6,3±2,5% против -0,63±2,1%; р<0,05); плотности толщины (12,8±4,5% против -0,2±2,9%; р<0,05) и плотности терминальных волос (20,6±4,9% против 4,4±4,9%; р<0,05). У одного субъекта имело место повышение общего количества волос на 22,4% и увеличение числа терминальных волос на 27,8% через 3 месяца после однократной инъекции hECM. Несмотря на то, что аналогичную тенденцию наблюдали на неделе 22, статистическая достоверность этого эффекта отсутствовала, поскольку у субъектов не было дополнительного улучшения. Данные результаты указывают на то, что однократное внутрикожное введение hECM достоверно повышало рост волос у субъектов с андрогенной алопецией.
Данное впервые проведенное у людей клиническое испытание показало безопасность секретированного фибробластами белка hECM и свидетельствовало о его первоначальной эффективности в восстановлении волос. Белки hECM, продуцированные фибробластами, культивированными в гипоксических условиях, включают факторы, которые важны для регуляции цикла волос. В отношении клеточной дифференцировки фибробласты являются исходными клетками для клеток волосяных сосочков. В исследованиях in vitro было также установлено присутствие белков Wnt, VEGF, FGF, KGF и также фоллистатина. Установлена важная функция белков Wnt в волосяных фолликулах, которые играют ключевую роль в инициации роста волос. Кроме того, активность Wnt является важной в цикле волос, инициации более поздних стадий телогенной активации клеток и экспрессии генов, необходимых для образования волосяного зародыша из кератиноцитов, которые будут начинать следующую анагенную стадию роста волос. Следовательно, полагается, что стимуляция нового роста волос, индуцируемая введением hECM, является результатом, по меньшей мере, активности Wnt.
Результаты по эффективности при однократной инъекции hECM представляют новый подход в лечении облысения. FDA одобрил продукты миноксидил (пример, RogaineTM) и финастерид (например, PropeciaTM), для которых требуется ежедневное применение для индукции и поддержания эффективности. В частности, данные продукты проявляют наиболее высокую эффективность в снижении потери волос с небольшим процентом роста новых волос, наблюдаемым, по меньшей мере, через 4 месяца после ежедневного применения. В противоположность однократная инъекция hECM приводила к статистически значимому росту новых терминальных волос и увеличению плотности и толщины волос. Механизм(ы), ответственный за рост волос, изучался в течение десятилетий, и ученые установили основополагающее значение белков Wnt и раневых ростовых факторов в стимуляции дермальных стволовых клеток, ассоциированных с волосяными сосочками. Данное клиническое предварительное исследование является первой демонстрацией того, что препарат, содержащий белки Wnt и раневые ростовые факторы, оказывает биологически активное стимулирующее действие на индукцию роста новых волос у людей.
Пример 11
Изготовление гибкого протеза из полиэтилентерефталата, покрытого эмбриональным ECM
Имеющиеся в настоящее время синтетические сосудистые трансплантаты, такие как изготовленные из полиэтилентерефталата (PET), часто не выполняют своих функций при использовании для замены небольших по диаметру сосудов в результате тромбоза и гиперплазии интимы. Несостоятельность возникает за счет отсутствия слитого эндотелиального монослоя и несоответствия между сосудистым трансплантатом и окружающей тканью. Изготовили биомеханически гибкую с небольшим диаметром (1,5 мм) структуру из нетканого материала PET, содержащую человеческий внеклеточный матрикс (hECM), культивированный в эмбриональных условиях, и включающий белки со свойствами, напоминающими ECM природных кровеносных сосудов. Белки hECM наносили на нетканую волокнистую структуру из PET погружением и ковалентной аминопрививкой поли(винил)амина (PVA) к поверхности, для устранения основных причин несостоятельности трансплантатов. Белки hECM не сшивали с PET, обеспечивая поверхностное воздействие RGD и CS5 в качестве связывающихся с клетками областей для эндотелиальных клеток. Результаты предшествующих работ показали, что полипропиленовые полимеры, покрытые hECM погружением, не вызывают воспалительной реакции при имплантации крысам. Также в предшествующих исследованиях авторы оптимизировали поддерживающие структуры из нетканого волокна PET с диаметром и размером пор для роста эндотелиальных клеток (EC) и клеток гладкой мускулатуры (SMC), фенотипа и удерживания в условиях скалывающего напряжения, а также волокнистые структуры из нетканого PET с механическим поведением, напоминающим аорту с небольшим диаметром. В данном исследовании оценивали связывание hECM, дозировку и однородность покрытия на поддерживающей структуре из PET.
Использовали следующие методы. Для получения нетканых PET волокон использовали чистый PET (Dupont, Wilmington, DE) с использованием процесса продувки расплава со средним диаметром волокна 50 мкм и размещения рядом отдельных слоев волокна PET (0°/90°) для получения 3D структуры. hECM получали культивированием неонатальных фибробластов кожи на декстрановых микросферах в эмбриональных условиях в перемешиваемом реакторе в течение 8 недель. Первые 4 недели культивировали в среде, содержащей 10% бычьей сыворотки, затем переводили на бессывороточную среду. Покрытие hECM нетканых PET сосудистых поддерживающих структур проводили модификацией PET волокон аминогруппами с использованием 0,1 М NaOH, 0,1 М KCl, 750 мМ PVA-HCl (Polysciences, США), 400 мкл 1,4-диаксона с последующей обработкой ультразвуком и тепловой обработкой в течение 24 ч. Реагенты получали от Sigma Aldrich, Канада, если не указано иначе. Затем структуры из нетканого PET волокна (аминированного и необработанного) погружали в hECM (в концентрации от 0,1 мг/мл до 0,6 мг/мл, разведенный в PBS) на ночь при 4°С. Для снижения нековалентного связывания образцы промывали 3Х PBS в циклах обработки ультразвуком продолжительностью 10 мин. Покрытие hECM структур из нетканого PET волокна характеризовали химически: (1) инфракрасной спектроскопией с преобразованием Фурье (FTIR); (2) сканирующей электронной микроскопией (SEM) и энергодисперсной рентгеновской спектроскопией (EDX) для локальной химической идентификации; (3) определением гидрофильности методом падения капель (Video Contact Angle 2000) и (4) рентгеновской фотоэлектронной спектроскопией (XPS). Покрытие hECM также визуализировали на конфокальном микроскопе после связывания hECM с флуоресцентным родамином В изотиоцианатом (RBITC) с (LSCM, Leica, Германия). Концентрацию покрытия hECM количественно определяли трипсинизацией покрытия hECM и количественным анализом с помощью микрометода определения белка BCA (Pierce Chemical Co, IL).
Анализ FTIR показывал наличие трех основных пиков, возникающих в результате высокой концентрации покрытия hECM на нетканых волокнах аминированного PET: полоса 1522 см-1 (амид II sN-H и mC-N), полоса 1656 см-1 (амид I, sC=О) и полоса 3320 см-1 (sNH) (фигура 28). На основании результатов FTIR можно предположить, что наиболее высокое покрытие hECM волокон аминированного PET достигается при концентрации раствора hECM, составляющей 0,6 мг/мл. Обратную тенденцию наблюдали с волокнами неаминированного PET, когда появлялись только небольшие пики hECM при низких концентрациях hECM (от 0,1 мг/мл до 0,2 мг/мл).
Флуоресцентные микрофотографии SEM и RBITC свидетельствовали о равномерном покрытии hECM (hECM четко обнаруживали на поверхности PET) при наиболее высокой концентрации hECM (0,6 мг/мл) на волокнах аминированного PET, что подтверждалось FTIR. С другой стороны, hECM в низких концентрациях (до 0,2 мг/мл) лучше адгезировал к необработанным волокнам PET по данным FTIR. Результаты микрометода BSA показывали, что удерживание hECM, по меньшей мере, в 2 раза выше на аминированных PET волокнах по сравнению с необработанными (соответственно 0,1 и 0,04 мг/см2). Наконец, контактный угол PET (75°) уменьшался с аминированием PET (45°), дополнительно снижаясь до 32° при иммобилизации 0,6 мг/мл hECM.
Покрытие hECM аминированного PVA нетканого PET сосудистого волокна демонстрировало высокую плотность покрытия hECM без сшивания областей hECM, связывающихся с клетками, со структурой PET.
Пример 12
Эмбриональный ECM, нанесенный на сосудистые трансплантаты с маленьким диаметром
Удерживание эндотелиальных клеток аорты человека (HAoEC) на непокрытых и hECM-покрытых сосудистых поддерживающих структурах оценивали после воздействия пульсирующего проточного скалывающего напряжения в циркуляционном контуре, воспроизводящем условия бедренной артерии, и венозных проточных волнообразных колебаний и пульсации.
Поддерживающие структуры из нетканых волокон PET получали продуванием расплава. Функционализацию PET волокон hECM проводили с использованием поли(виниламина). HAoEC высевали (с титром 2,0×105/см2) на непокрытых и hECM-покрытых PET сосудистых поддерживающих структурах и статически совместно инкубировали в течение 3 суток перед переносом в васкулярный реометр, напоминающий физиологическую волну с пульсирующим потоком в условиях артерий (скорость сдвига 300 сек-1) и вены (скорость сдвига 100 сек-1). После инкубации удерживание клеток оценивали SEM, тестом оценки жизнеспособности с окрашиванием Alamar Blue и флуоресцентной визуализацией клеток HAoEC посредством мечения Alexa Fluor 488 (F-актином).
Достоверно меньшие потери клеток наблюдали на сосудистых поддерживающих структурах из hECM-покрытого PET по сравнению с сосудистыми поддерживающими структурами из непокрытого PET после обоих стрессовых артериальных и венозных условий. Количество клеток, оставшихся на сосудистых поддерживающих структурах из hECM-покрытого PET, было в 3 раза выше (степень удерживания ≈85%) по сравнению с сосудистыми поддерживающими структурами из непокрытого PET через 1 ч после воздействия потока, характерного для артерий. Аналогичные результаты по статистически более достоверному удерживанию HAoEC на hECM-покрытых трансплантатах наблюдали через 1 ч воздействия венозного потока. Эту тенденцию к более высокому удерживанию на сосудистых поддерживающих структурах из hECM-покрытого PET после артериального и венозного скалывающего напряжения также подтверждали по 3-кратному повышению метаболической активности (по данным теста оценки жизнеспособности при окрашивании Alamar Blue) и числу клеток (по данным подсчета на микрофотографиях SEM), полученным на этих поддерживающих структурах.
Функционализация трансплантатов из PET с небольшим диаметром (1,5 мм) покрытием с высокой плотностью hECM без сшивания RGD-связывающих областей эффективно повышала устойчивость HAoEC к имитирующим физиологические условия скалывающим силам в условиях in vitro.
Пример 13
Полимеры, покрытые hECM, достоверно повышают биологическую совместимость
Человеческий ECM, полученный в эмбриональных условиях, использовали для покрытия полимерных поддерживающих структур и тестировали на биологическую совместимость в условиях in vivo. hECM получали культивированием неонатальных фибробластов кожи на декстрановых микросферах в биореакторе. Найлоновые, нетканые из полипропилена (PPE) и полиэтилентерефталата (PET) поддерживающие структуры покрывали ECM. hECM присоединяли к полимерным поддерживающим структурам с использованием глутаральдегида, способом «dip&dry», UVA, травления уксусной кислотой, поли(виниламина) (PVA) и Sulfo Sanphah. Различные hECM-покрытия характеризовали с использованием инфракрасной спектроскопии с преобразованием Фурье (FTIR), энергодисперсной рентгеновской спектроскопии (EDX) и визуализации с использованием сканирующей электронной микроскопии (SEM), и иммунофлуоресценции. Затем наилучшие hECM-покрытые и непокрытые поддерживающие структуры хирургически имплантировали в подкожное пространство мышам SCID. Гистологические образцы извлеченных имплантатов оценивали на наличие воспалительной реакции, клеточной инфильтрации, образование гигантских клеток инородных тел и образования капсул.
Результаты FTIR дали основание предположить, что наиболее высокое покрытие ECM наблюдали с использованием PVA и UVA методик с раствором ECM с концентрацией 0,6 мг/мл. Высокая плотность раствора ECM обеспечивает полное покрытие полимера ECM через поверхностные активированные аминогруппы полимера. Полное покрытие ECM было желательным, чтобы «спрятать» полимер от физиологической среды. Данная тенденция подтверждалась SEM и флуоресцентными микрофотографиями, на которых видно гомогенное и густое покрытие ECM.
Эндотелиальные клетки аорты человека (HAoEC), которые высевали на hECM-покрытые и непокрытые поддерживающие структуры, оценивали на пролиферацию клеток тестом окрашивания Alamar Blue. Как правило, материалы, которые показывали наиболее высокое покрытие ECM (при анализе FTIR и SEM), также связывали клетки более эффективно и обеспечивали двукратное повышение пролиферации клеток.
Наконец, подкожно имплантированные ECM-покрытые (PET, PPE и найлоновые полимерные поддерживающие структуры) демонстрировали достоверное снижение инфильтрации иммунных клеток и образования гигантских клеток инородных тел по сравнению с непокрытыми поддерживающими структурами. Кроме того, наблюдали повышенное образование коллагеновых капсул и интеграцию тканей с различными ECM-покрытыми полимерами по сравнению с необработанными контролями.
Несмотря на то что изобретение описано с обращением к вышеприведенным примерам, очевидно, понятно, что модификации и вариации включаются в сущность и объем изобретения. Следовательно, изобретение ограничивается только последующей формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИИ ВНЕКЛЕТОЧНОГО МАТРИКСА ДЛЯ ЛЕЧЕНИЯ РАКА | 2009 |
|
RU2523339C2 |
| КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИЧЕСКОГО ИЛИ ТЕРАПЕВТИЧЕСКОГО ЛЕЧЕНИЯ СОСТОЯНИЙ, СВЯЗАННЫХ С ИЗМЕНЕНИЕМ КОЛИЧЕСТВА ВОЛОС | 2018 |
|
RU2716159C2 |
| КУЛЬТУРАЛЬНАЯ СРЕДА ДЛЯ ЭПИТЕЛИАЛЬНЫХ СТВОЛОВЫХ КЛЕТОК И ОРГАНОИДОВ, СОДЕРЖАЩИХ УКАЗАННЫЕ СТВОЛОВЫЕ КЛЕТКИ | 2010 |
|
RU2555545C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ ВОЛОСЯНЫХ МИКРОФОЛЛИКУЛОВ И DE NOVO СОСОЧКОВ И ИХ ПРИМЕНЕНИЕ ДЛЯ IN VITRO ТЕСТОВ И IN VIVO ИМПЛАНТАЦИЙ | 2009 |
|
RU2507254C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ ТКАНЕЙ | 2013 |
|
RU2733838C2 |
| ЛЕЧЕНИЕ АМИОТРОФИЧЕСКОГО БОКОВОГО СКЛЕРОЗА С ИСПОЛЬЗОВАНИЕМ ПОЛУЧЕННЫХ ИЗ ПУПОВИНЫ КЛЕТОК | 2012 |
|
RU2612391C2 |
| УЛУЧШЕННЫЙ СПОСОБ ДИФФЕРЕНЦИРОВКИ | 2017 |
|
RU2772435C2 |
| БИОЛОГИЧЕСКИЙ АКТИВНЫЙ КОМПЛЕКС ДЛЯ ОРГАНОГЕНЕЗА | 2003 |
|
RU2254146C2 |
| ДВОЙНЫЕ ТРУБЧАТЫЕ СТРУКТУРЫ | 2017 |
|
RU2756404C1 |
| КУЛЬТУРАЛЬНАЯ СРЕДА СТВОЛОВЫХ КЛЕТОК | 2012 |
|
RU2714256C2 |
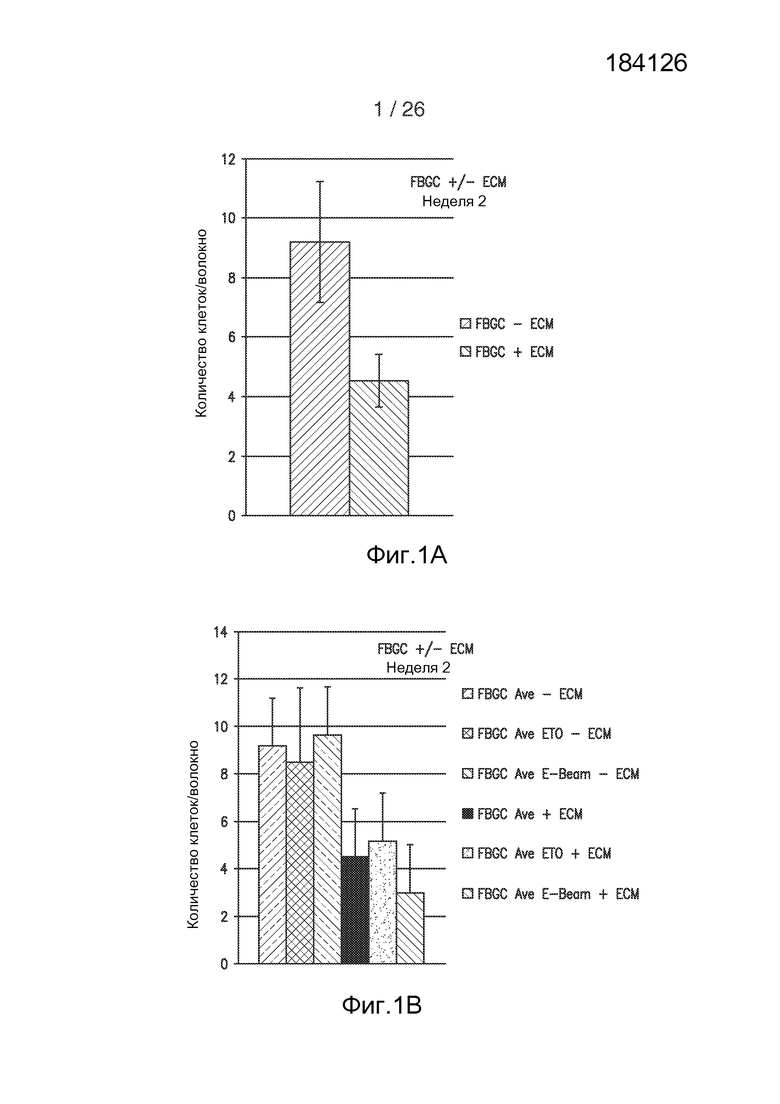


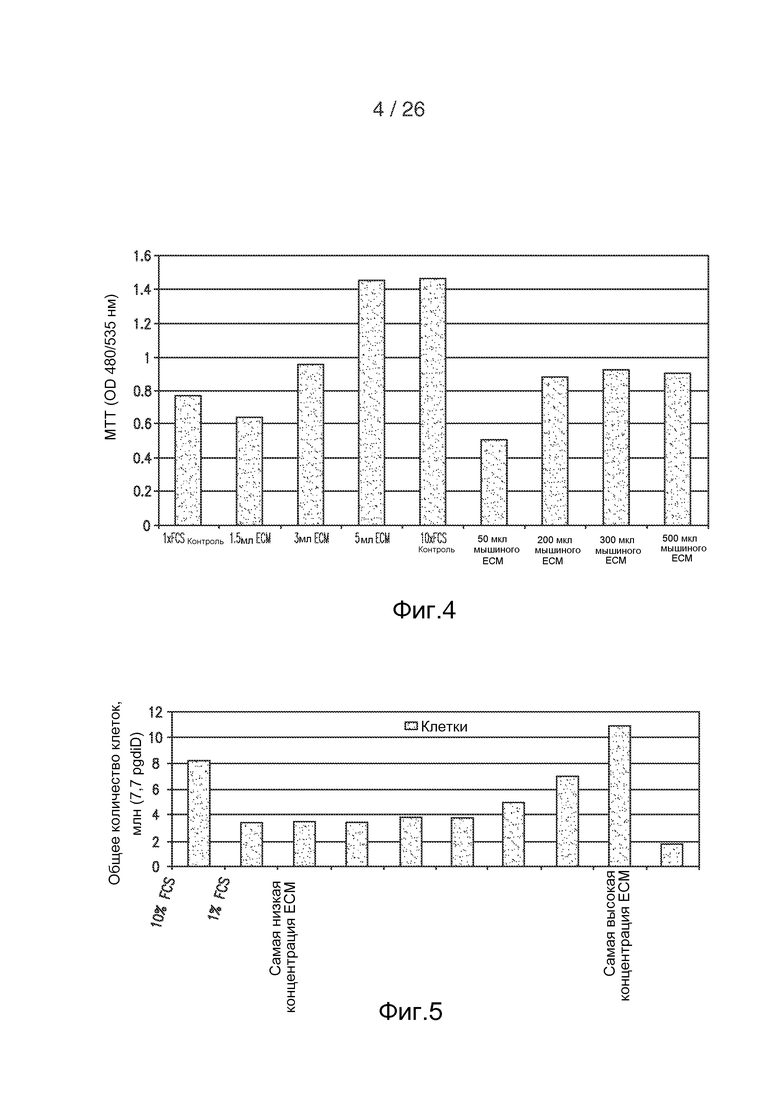
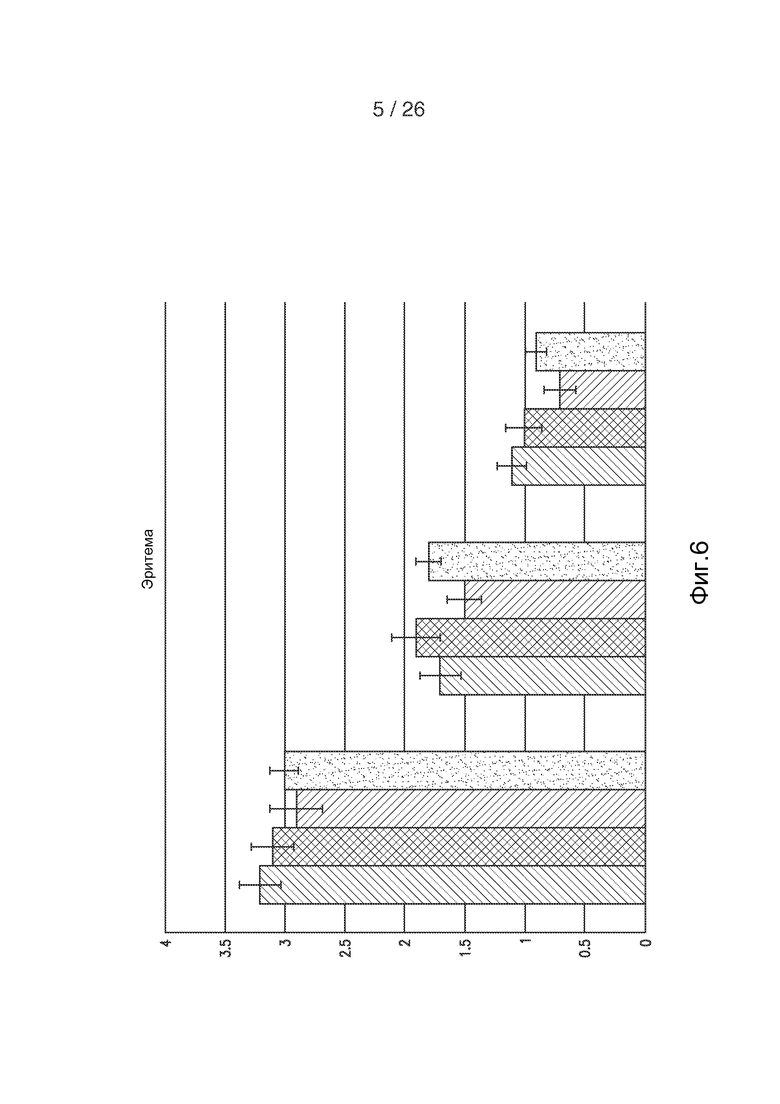

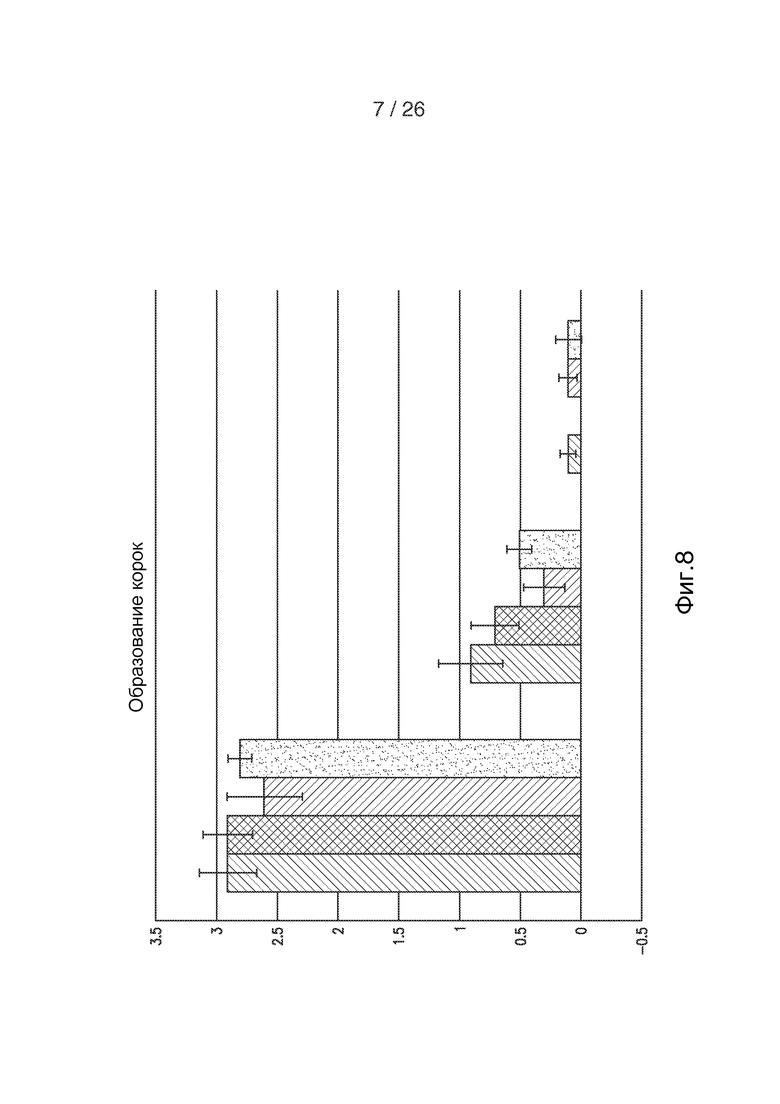


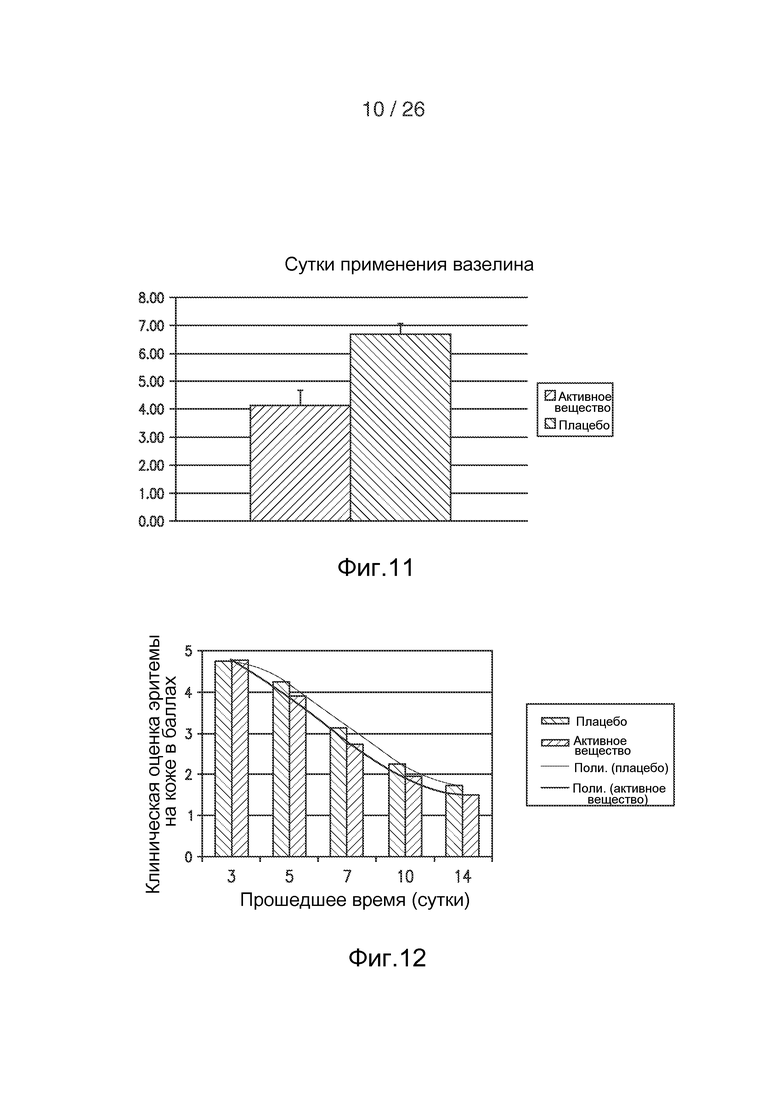



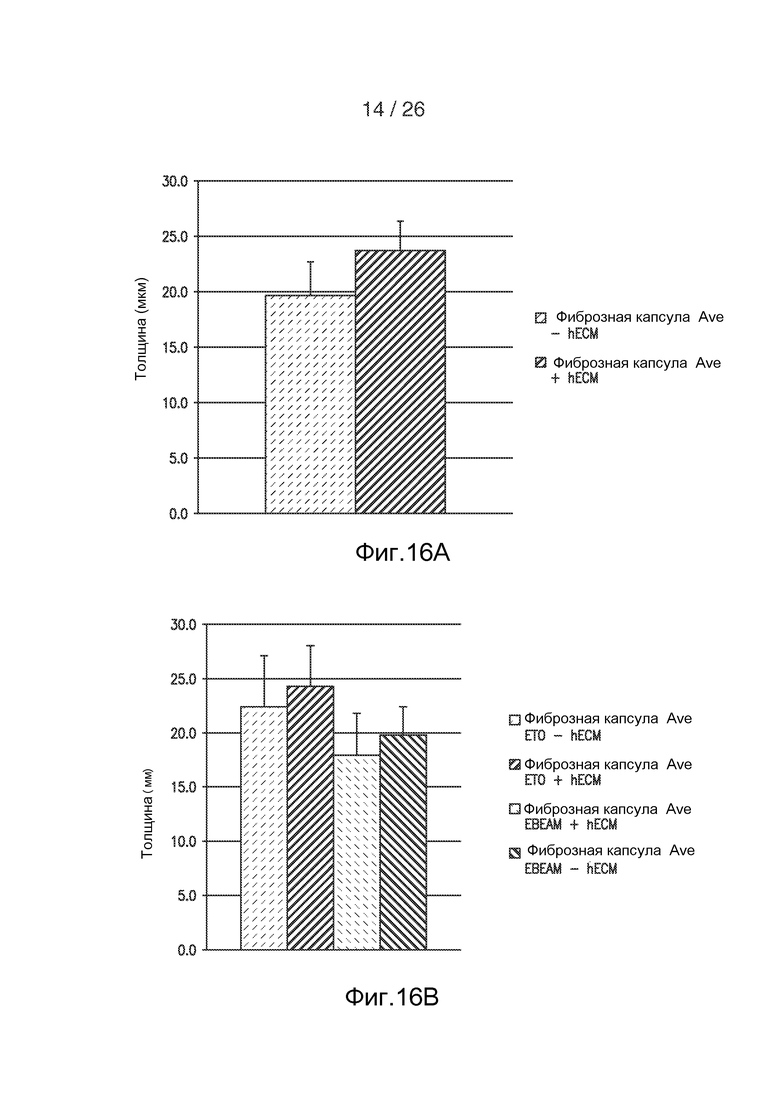

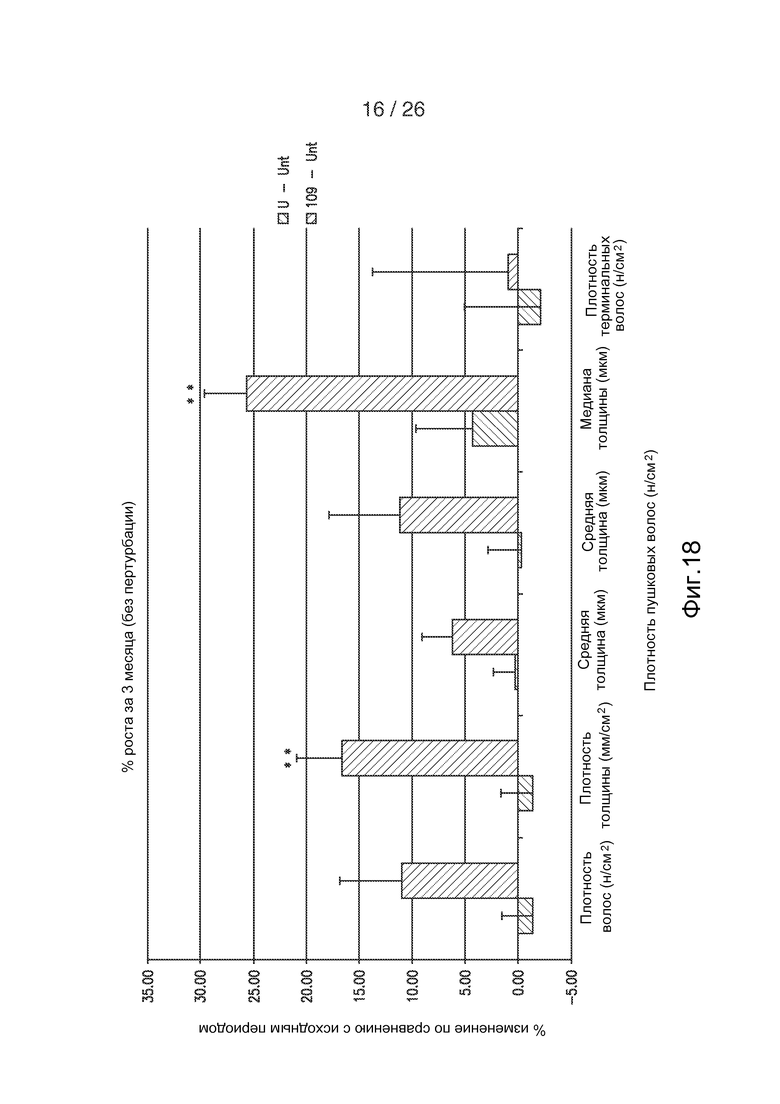

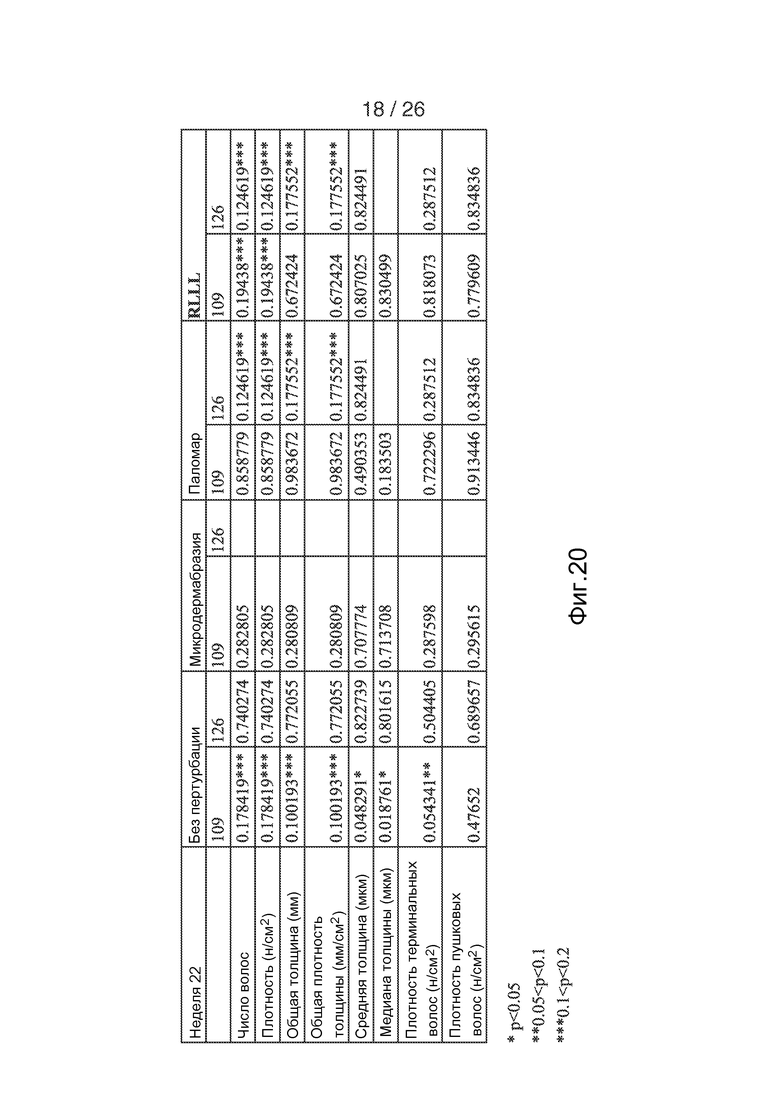



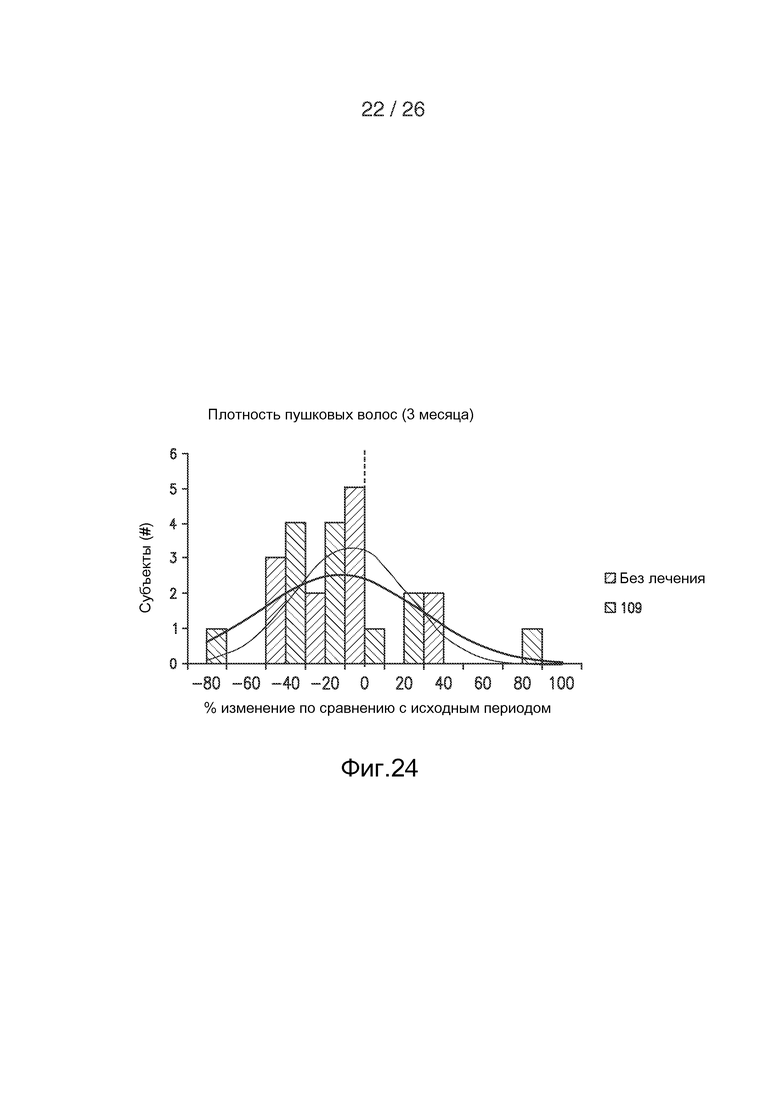



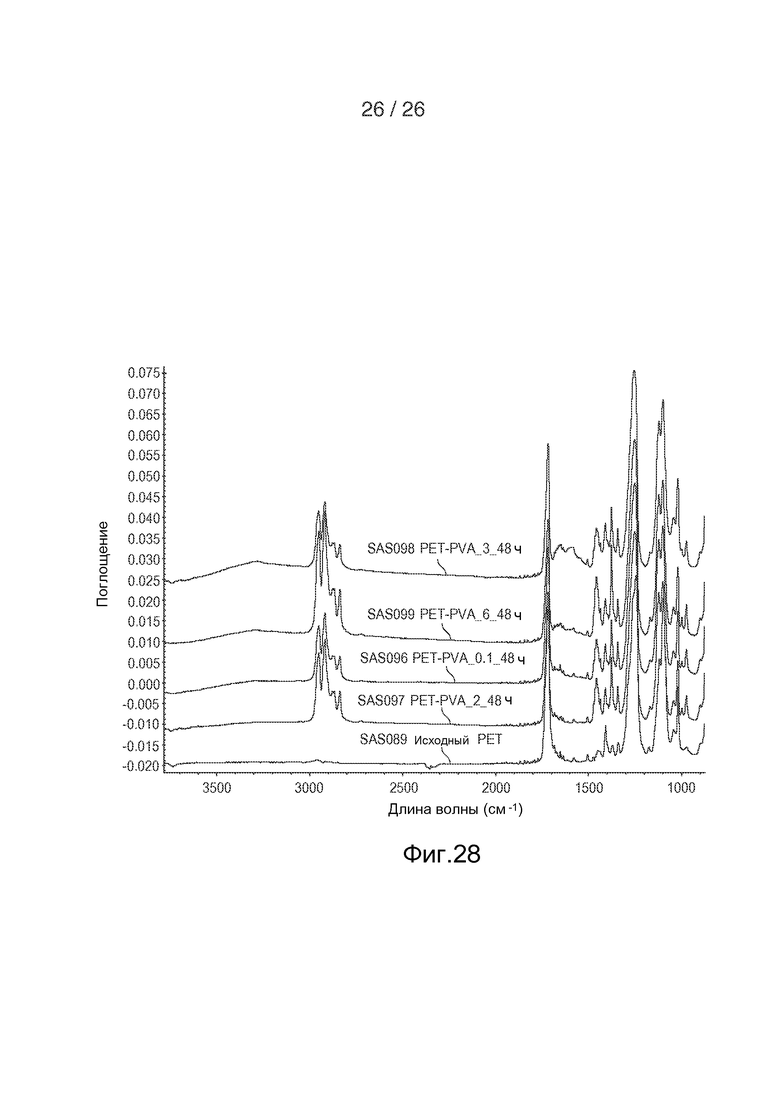
Предложенная группа изобретений относится к области медицины. Предложен способ получения композиции эмбриональных белков для стимуляции роста и/или восстановления волос, включающий культивирование фибробластов в гипоксических условиях при примерно 1-5% кислорода с получением мультипотентных стволовых клеток, культивирование мультипотентных стволовых клеток, продуцирующих композицию, содержащую секретируемые белки внеклеточного матрикса (ECM) и биологические компоненты, и сбор композиции после по меньшей мере двух недель. Предложены применение композиции, полученной вышеуказанным способом, для стимуляции роста волос и способ восстановления и/или регенерации клеток. Предложенная группа изобретений обеспечивает композиции ECM с эмбриональными свойствами. 3 н. и 20 з.п. ф-лы, 37 ил., 8 табл., 13 пр.
1. Способ получения композиции, содержащей один или более эмбриональных белков, для стимуляции роста и/или восстановления волос, где способ включает а) культивирование клеток фибробласт в гипоксических условиях при примерно 1-5% кислорода по крайней мере две недели на сетке или шариках в подходящей питательной среде, таким образом получая мультипотентные стволовые клетки; b) культивирование мультипотентных стволовых клеток, продуцирующих и секретирующих композицию, содержащую растворимую фракцию и нерастворимую фракцию, где нерастворимая фракция содержит секретируемые белки ЕСМ и биологические компоненты, которые откладываются на сетке или шариках, и растворимая фракция содержит белки и биологические компоненты, которые откладываются в указанной питательной среде; и с) сбор композиции после указанных по меньшей мере двух недель.
2. Способ по п. 1, в котором культуральная среда содержит сыворотку.
3. Способ по п. 1, в котором культуральная среда является бессывороточной.
4. Способ по п. 1, в котором одним или более эмбриональными белками является коллаген типа III, IV и V.
5. Способ по п. 4, в котором типы коллагена подвергаются активации по сравнению со средами, продуцированными в условиях с содержанием кислорода примерно 15-20%.
6. Способ по п. 1, в котором одним или более эмбриональными белками является ламинин.
7. Способ по п. 6, в котором тип ламинина представляет собой ламинин 8.
8. Способ по п. 1, в котором фибробласты являются неонатальными фибробластами.
9. Способ по п. 1, в котором клетки являются видоспецифическими.
10. Способ по п. 1, в котором одним или более эмбриональными белками является VEGF.
11. Способ по п. 10, в котором тип VEGF представляет собой VEGF-A или его изоформу.
12. Способ по п. 1, где мультипотентные стволовые клетки экспрессируют гены, характерные для стволовых клеток на уровне по меньшей мере в 3 раза выше по сравнению с культивированием в нормальных кислородных условиях.
13. Способ по п. 12, в котором гены выбраны из группы, состоящей из Oct4, Sox2, KLF4, NANOG и сМус.
14. Способ по п. 13, в котором ген является Oct4.
15. Способ восстановления и/или регенерации клеток, включающий контактирование клеток, предназначенных для восстановления или регенерации, с композицией, полученной способом по п. 1.
16. Способ по п. 15, где клеткой является волосяной фолликул.
17. Способ по п. 16, в котором клетка контактирует в условиях in vivo.
18. Способ по п. 16, в котором клетка контактирует в условиях ex vivo.
19. Способ по п. 18, в котором клетку трансплантируют субъекту.
20. Применение композиции, полученной способом по п. 1, для стимуляции роста волос, включающее контактирование клетки волосяного фолликула с композицией, полученной способом по п. 1, тем самым обеспечивая стимуляцию роста волос.
21. Применение по п. 20, в котором клетка контактирует в условиях in vivo.
22. Применение по п. 20, в котором клетка контактирует в условиях ex vivo.
23. Применение по п. 22, в котором клетку трансплантируют субъекту.
| СРЕДСТВО ДЛЯ ИЗМЕНЕНИЯ СКОРОСТИ РОСТА ИЛИ РЕПРОДУКЦИИ КЛЕТОК, СПОСОБ ЕГО ПОЛУЧЕНИЯ, СПОСОБ СТИМУЛЯЦИИ ЗАЖИВЛЕНИЯ РАН ИЛИ ЛЕЧЕНИЯ ОЖОГОВ, СПОСОБ КОРРЕКЦИИ КОСМЕТИЧЕСКОГО ДЕФЕКТА, СПОСОБ ИНГИБИРОВАНИЯ СТАРЕНИЯ КОЖИ И СПОСОБ СТИМУЛЯЦИИ РОСТА ВОЛОС | 2000 |
|
RU2280459C2 |
| US 2004005704 A1, 08.01.2004 | |||
| US 2003166272 A1, 04.09.2003 | |||
| US 2005032208 A1, 10.02.2005. | |||
Авторы
Даты
2017-09-22—Публикация
2010-07-09—Подача