Для данной заявки испрашивается приоритет по предварительной заявке США №61/297637, поданной 22 января 2010 года, которая включается в настоящий документ посредством ссылки.
Область техники, к которой относится изобретение
Один или несколько вариантов осуществления настоящего изобретения относятся к функционализованным полимерам и способам их получения.
Уровень техники
На современном уровне техники изготовления покрышек желательно использовать вулканизаты каучуков, которые характеризуются пониженным гистерезисом, то есть, меньшими потерями механической энергии на нагревание. Например, вулканизаты каучуков, которые характеризуются пониженным гистерезисом, выгодно использовать в компонентах покрышки, таких как боковины и протекторы, чтобы получить покрышки, характеризующиеся выгодно низким сопротивлением качению. Гистерезис вулканизата каучука зачастую приписывают свободным концам полимерных цепей в сетке сшитого каучука, а также диссоциации агломератов наполнителя.
Для уменьшения гистерезиса у вулканизатов каучуков использовались функционализованные полимеры. Функциональная группа функционализованного полимера может уменьшить количество свободных концов полимерных цепей в результате взаимодействия с частицами наполнителя. Кроме того, функциональная группа может уменьшить агломерирование наполнителя. Тем не менее, зачастую невозможно предсказать то, сможет ли конкретная функциональная группа, введенная в полимер, уменьшить гистерезис.
Функционализованные полимеры могут быть получены в результате проведения после полимеризации обработки реакционно-способных полимеров определенными функционализирующими агентами. Однако невозможно предсказать то, может ли реакционно-способный полимер быть функционализованным в результате обработки тем или иным конкретным функционализующим агентом. Например, функционализующие агенты, которые работают для одного типа полимера, необязательно работают для другого типа полимера, и наоборот.
Анионные инициаторы, как известно, подходят для использования при полимеризации сопряженных диеновых мономеров для получения полидиенов, содержащих комбинацию 1,2-, цис-1,4- и транс-1,4-звеньев. Анионные инициаторы также подходят для использования при сополимеризации сопряженных диеновых мономеров с винилзамещенными ароматическими соединениями. Полимеры, полученные при использовании анионных инициаторов, могут демонстрировать характеристики живых цепей в том смысле, что по завершении полимеризации полимерные цепи имеют живые концевые группы, которые способны вступать в реакцию с дополнительными мономерами для дополнительного роста цепи или в реакцию с определенными функционализующими агентами для получения функционализованных полимеров.
Вследствие выгодности функционализованных полимеров, в особенности при изготовлении покрышек, существует потребность в разработке новых функционализованных полимеров, которые характеризуются пониженным гистерезисом.
Раскрытие изобретения
Варианты осуществления настоящего изобретения раскрывают способ получения функционализованного полимера, включающий стадии: (i) полимеризации мономера с использованием анионного инициатора для получения реакционно-способного полимера; и (ii) проведения реакции между реакционно-способным полимером и нитрильным соединением, имеющим защищенную аминогруппу, где защищенная аминогруппа непосредственно присоединена к фрагменту, выбираемому из группы, состоящей из ациклических фрагментов, гетероциклических фрагментов и неароматических циклических фрагментов.
Варианты осуществления настоящего изобретения дополнительно раскрывают способ получения функционализованного полимера, включающий стадии: (i) полимеризации мономера с использованием анионного инициатора для получения реакционно-способного полимера; и (ii) проведения реакции между реакционно-способным полимером и нитрильным соединением, имеющим защищенную аминогруппу, описывающимся формулой I:

где R1 представляет собой двухвалентную органическую группу, а каждый из R2 и R3 независимо представляет собой одновалентную органическую группу или гидролизуемую группу, или R2 и R3 соединяются с образованием двухвалентной органической группы, при том условии, что R1 представляет собой ациклическую двухвалентную органическую группу, гетероциклическую двухвалентную органическую группу, неароматическую циклическую двухвалентную органическую группу, которая лишена гетероатомов, или двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, при том еще условии, что когда R1 представляет собой содержащую ароматическое кольцо двухвалентную органическую группу, которая лишена гетероатомов, защищенная аминогруппа не должна быть непосредственно присоединена к ароматическому кольцу.
Варианты осуществления настоящего изобретения дополнительно раскрывают функционализованный полимер, имеющий защищенную аминогруппу, при этом функционализованный полимер описывается формулой VII:

где π представляет собой полимерную цепь полидиена или сополимера сопряженного диена и сомономера, характеризующуюся средним или низким уровнем содержания цис-1,4-звеньев, R1 представляет собой двухвалентную органическую группу, а каждый из R2 и R3 независимо представляет собой одновалентную органическую группу или гидролизуемую группу, или R2 и R3 соединяются с образованием двухвалентной органической группы, при том условии, что R1 представляет собой ациклическую двухвалентную органическую группу, гетероциклическую двухвалентную органическую группу, неароматическую циклическую двухвалентную органическую группу, которая лишена гетероатомов, или двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, при том еще условии, что когда R1 представляет собой содержащую ароматическое кольцо двухвалентную органическую группу, которая лишена гетероатомов, защищенная аминогруппа не должна быть непосредственно присоединена к ароматическому кольцу.
Варианты осуществления настоящего изобретения дополнительно раскрывают функционализованный полимер, имеющий аминогруппу, при этом функционализованный полимер описывается формулой VIII:

где π представляет собой полимерную цепь полидиена или сополимера сопряженного диена и сомономера, характеризующуюся средним или низким уровнем содержания цис-1,4-звеньев, R1 представляет собой двухвалентную органическую группу, а каждый из R12 и R13 независимо представляет собой одновалентную органическую группу или атом водорода, или R12 и R13 соединяются с образованием двухвалентной органической группы, при том условии, что R1 представляет собой ациклическую двухвалентную органическую группу, гетероциклическую двухвалентную органическую группу, неароматическую циклическую двухвалентную органическую группу, которая лишена гетероатомов, или двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, при том еще условии, что когда R1 представляет собой содержащую ароматическое кольцо двухвалентную органическую группу, которая лишена гетероатомов, аминогруппа не должна быть непосредственно присоединена к ароматическому кольцу.
Краткое описание чертежей
Фиг.1 демонстрирует графическое представление зависимости потерь на гистерезис (tan δ) от вязкости по Муни (ML 1+4 при 130°С) для вулканизатов, полученных из функционализованного сополимера стирола и бутадиена, полученного в соответствии с одним или несколькими вариантами осуществления настоящего изобретения, в сопоставлении с соответствующими характеристиками вулканизата, полученного из нефункционализованного сополимера стирола и бутадиена.
Осуществление изобретения
В соответствии с одним или несколькими вариантами осуществления настоящего изобретения в результате проведения анионной полимеризации сопряженного диенового мономера и необязательно мономера, сополимеризуемого с ним, получают реакционно-способный полимер, и после этого данный реакционно-способный полимер функционализуют в результате проведения реакции с нитрильным соединением, имеющим защищенную аминогруппу. Получающиеся в результате функционализованные полимеры могут быть использованы при изготовлении компонентов покрышки. В одном или нескольких вариантах осуществления получающиеся в результате функционализованные полимеры позволяют получить компоненты покрышки, которые выгодным образом характеризуются низким гистерезисом.
Примеры сопряженного диенового мономера включают 1,3-бутадиен, изопрен, 1,3-пентадиен, 1,3-гексадиен, 2,3-диметил-1,3-бутадиен, 2-этил-1,3-бутадиен, 2-метил-1,3-пентадиен, 3-метил-1,3-пентадиен, 4-метил-1,3-пентадиен и 2,4-гексадиен. При сополимеризации также могут быть использованы и смеси двух и более сопряженных диенов.
Примеры мономера, сополимеризуемого с сопряженным диеновым мономером, включают винилзамещенные ароматические соединения, такие как стирол, п-метилстирол, α-метилстирол и винилнафталин.
В соответствии с настоящим изобретением реакционно-способный полимер получают в результате проведения анионной полимеризации, где мономер полимеризуют с использованием анионного инициатора. Ключевые признаки механизма анионной полимеризации описаны в книгах (например, Hsieh, H.L.; Quirk, R.P. Anionic Polymerization: Principles and Practical Applications; Marcel Dekker: New York, 1996) и обзорных статьях (например, Hadjichristidis, N.; Pitsikalis, M.; Pispas, S.; Iatrou, H.; Chem. Rev. 2001, 101 (12), 3747-3792). Анионные инициаторы выгодным образом могут приводить к получению живых полимеров, которые до гашения активных центров способны вступать в реакцию с дополнительными мономерами для дальнейшего роста цепи или вступать в реакцию с определенными функционализующими агентами для получения функционализованных полимеров.
Область использования данного изобретения не ограничивается набором каких-либо конкретных анионных инициаторов. В одном или нескольких вариантах осуществления использующимся анионным инициатором является функциональный инициатор, который вводит функциональную группу в голову полимерной цепи (то есть, в положение, с которого полимерная цепь начинается). В конкретных вариантах осуществления функциональная группа включает один или несколько представителей, выбираемых из гетероатомов (например, атомов азота, кислорода, бора, кремния, серы, олова и фосфора) или гетероциклических групп. В определенных вариантах осуществления функциональная группа уменьшает потери на гистерезис при 50°С для наполненных техническим углеродом вулканизатов, полученных из полимеров, имеющих функциональную группу, в сопоставлении с соответствующими характеристиками подобных наполненных техническим углеродом вулканизатов, полученных из полимера, который не имеет функциональной группы.
Примеры анионных инициаторов включают литийорганические соединения. В одном или нескольких вариантах осуществления литийорганические соединения могут включать гетероатомы. В этих или других вариантах осуществления литийорганические соединения могут иметь одну или несколько гетероциклических групп. Типы литийорганических соединений включают алкиллитий, производные ариллития и производные циклоалкиллития. Конкретные примеры литийорганических соединений включают этиллитий, н-пропиллитий, изопропиллитий, н-бутиллитий, втор-бутиллитий, трет-бутиллитий, н-амиллитий, изоамиллитий и фениллитий.
В конкретных вариантах осуществления литийорганические соединения включают циклическое аминсодержащее соединение, такое как литиогексаметиленимин. Эти и родственные подходящие для использования инициаторы описываются в патентах США №№5332810, 5329005, 5578542, 5393721, 5698646, 5491230, 5521309, 5496940, 5574109 и 5786441, которые посредством ссылки включаются в настоящий документ. В других вариантах осуществления литийорганические соединения включают литиированные алкилтиоацетали, такие как 2-литио-2-метил-1,3-дитиан. Эти и родственные подходящие для использования инициаторы описываются в публикациях США №№2006/0030657, 2006/0264590 и 2006/0264589, которые посредством ссылки включаются в настоящий документ. В еще одних вариантах осуществления литийорганические соединения включают алкоксисилилсодержащие инициаторы, такие как литиированный трет-бутилдиметилпропоксисилан. Эти и родственные подходящие для использования инициаторы описываются в публикации США №2006/0241241, которая посредством ссылки включается в настоящий документ.
Другие анионные инициаторы включают натрийорганические соединения, такие как фенилнатрий и 2,4,6-триметилфенилнатрий. Также могут быть использованы и те анионные инициаторы, которые приводят к получению полимеров, имеющих две живые группы, у которых обе концевые группы полимерной цепи являются живыми. Примеры таких инициаторов включают дилитиевые инициаторы, такие как те, которые получают в результате проведения реакции между 1,3-диизопропенилбензолом и втор-бутиллитием. Эти и родственные бифункциональные инициаторы описываются в патенте США №3652516, который посредством ссылки включается в настоящий документ. Также могут быть использованы и радикальные анионные инициаторы, в том числе те, которые описываются в патенте США №5552483, который посредством ссылки включается в настоящий документ.
В одном или нескольких вариантах осуществления использующимся анионным инициатором является производное триалкилоловолития, такое как три-н-бутилоловолитий. Эти и родственные подходящие для использования инициаторы описываются в патентах США №№3426006 и 5268439, которые посредством ссылки включаются в настоящий документ.
Если в результате анионной полимеризации получают эластомерные сополимеры, содержащие сопряженные диеновые мономеры и винилзамещенные ароматические мономеры, эти сопряженные диеновые мономеры и винилзамещенные ароматические мономеры могут быть использованы при массовом соотношении в диапазоне от 95:5 до 50:50 или в других вариантах осуществления - от 90:10 до 65:35. Для промотирования рандомизации сомономеров при сополимеризации и контроля микроструктуры полимера (как, например, контроля 1,2-звеньев сопряженного диенового мономера) совместно с анионным инициатором может быть использован рандомизатор, который обычно представляет собой полярный координатор.
Соединения, подходящие для использования в качестве рандомизаторов, включают те, которые содержат гетероатом кислорода или азота и несвязанную пару электронов. Примеры типов рандомизаторов включают линейные и циклические олигомерные оксоланилалканы; диалкиловые эфиры моно- и олигоалкиленгликолей (также известные под наименованием глимовых эфиров); «краун»-эфиры; третичные амины; линейные олигомеры ТГФ; алкоксиды щелочных металлов; и сульфонаты щелочных металлов. Линейные и циклические олигомерные оксоланилалканы описываются в патенте США №4429091, который посредством ссылки включается в настоящий документ. Конкретные примеры рандомизаторов включают 2,2-бис(2'-тетрагидрофурил)пропан, 1,2-диметоксиэтан, N,N,N',N'-тетраметилэтилендиамин (ТМЭДА), тетрагидрофуран (ТГФ), 1,2-дипиперидилэтан, дипиперидилметан, гексаметилфосфорамид, N,N'-диметилпиперазин, диазабициклооктан, диметиловый эфир, диэтиловый эфир, три-н-бутиламин, трет-амилат калия, 4-додецилсульфонат калия и их смеси.
Количество используемого рандомизатора может зависеть от различных факторов, таких как желательная микроструктура полимера, количественное соотношение между мономером и сомономером, температура полимеризации, а также природа конкретных использующихся рандомизатора и инициатора. В одном или нескольких вариантах осуществления количество использующегося рандомизатора может находиться в диапазоне от 0,05 до 100 молей в расчете на один моль анионного инициатора.
Анионный инициатор и рандомизатор могут быть введены в полимеризационную систему различными способами. В одном или нескольких вариантах осуществления анионный инициатор и рандомизатор могут быть раздельно либо постадийно, либо одновременно добавлены к полимеризуемому мономеру. В других вариантах осуществления анионный инициатор и рандомизатор могут быть предварительно смешаны вне полимеризационной системы либо в отсутствие какого-либо мономера, либо в присутствии небольшого количества мономера, а получающаяся в результате смесь при желании может быть подвергнута старению, а после этого добавлена к мономеру, который предполагается заполимеризовать.
В одном или нескольких вариантах осуществления, вне зависимости от того, какой тип анионного инициатора используется для получения реакционно-способного полимера, в качестве носителя либо для растворения, либо для суспендирования инициатора в целях облегчения доставки инициатора в полимеризационную систему может быть использован растворитель. В других вариантах осуществления в качестве носителя может быть использован мономер. В еще одних вариантах осуществления может быть использован чистый инициатор без примесей без какого-либо растворителя.
В одном или нескольких вариантах осуществления подходящие для использования растворители включают те органические соединения, которые не будут вступать в реакцию полимеризации или встраиваться в растущие полимерные цепи во время полимеризации мономера в присутствии инициатора. В одном или нескольких вариантах осуществления такие органические вещества являются жидкими при температуре и давлении окружающей среды. В одном или нескольких вариантах осуществления такие органические растворители являются инертными по отношению к инициатору. Примеры органических растворителей включают углеводороды, имеющие низкую или относительно низкую температуру кипения, такие как ароматические углеводороды, алифатические углеводороды и циклоалифатические углеводороды. Неограничивающие примеры ароматических углеводородов включают бензол, толуол, ксилолы, этилбензол, диэтилбензол и мезитилен. Неограничивающие примеры алифатических углеводородов включают н-пентан, н-гексан, н-гептан, н-октан, н-нонан, н-декан, изопентан, изогексаны, изопентаны, изооктаны, 2,2-диметилбутан, петролейный эфир, керосин и уайт-спириты. А неограничивающие примеры циклоалифатических углеводородов включают циклопентан, циклогексан, метилциклопентан и метилциклогексан. Также могут быть использованы и смеси вышеупомянутых углеводородов. Как известно на современном уровне техники, по экологическим причинам желательным может оказаться использование алифатических и циклоалифатических углеводородов. По завершении полимеризации низкокипящие углеводородные растворители от полимера обычно отделяют.
Другие примеры органических растворителей включают высококипящие углеводороды, имеющие высокие молекулярные массы, в том числе углеводородные масла, которые обычно используются для наполнения полимеров маслом. Примеры данных масел включают парафиновые масла, ароматические масла, нафтеновые масла, растительные масла, отличные от касторовых масел, и масла, характеризующиеся низким уровнем содержания ПАС (полициклических ароматических соединений), в том числе марки MES, TDAE, SRAE, тяжелые нафтеновые масла. Вследствие нелетучести данных углеводородов они обычно не требуют отделения и остаются введенными в полимер.
Получение реакционно-способного полимера по настоящему изобретению может быть осуществлено в результате проведения полимеризации сопряженного диенового мономера, необязательно совместно с мономером, сополимеризуемым с сопряженным диеновым мономером, в присутствии каталитически эффективного количества анионного инициатора. Введение инициатора, сопряженного диенового мономера, необязательного сомономера и какого-либо растворителя в случае использования такового формирует полимеризационную смесь, в которой образуется реакционно-способный полимер. Количество используемого инициатора может зависеть от комбинации различных факторов, таких как тип использующегося инициатора, степень чистоты ингредиентов, температура полимеризации, желательные скорость полимеризации и степень превращения, желательная молекулярная масса и множество других факторов. В соответствии с этим, конкретное количество инициатора не может быть указано однозначно, за исключением заявления о том, что могут быть использованы каталитически эффективные количества инициатора.
В одном или нескольких вариантах осуществления загрузка инициатора (например, производного алкиллития) может варьироваться в диапазоне от приблизительно 0,05 до приблизительно 100 ммоль, в других вариантах осуществления от приблизительно 0,1 до приблизительно 50 ммоль, а в еще одних вариантах осуществления от приблизительно 0,2 до приблизительно 5 ммоль, в расчете на 100 граммов мономера.
В одном или нескольких вариантах осуществления полимеризация может быть проведена в полимеризационной системе, которая включает существенное количество растворителя. В одном варианте осуществления может быть использована система растворной полимеризации, в которой как полимеризуемый мономер, так и полученный полимер являются растворимыми в растворителе. В еще одном варианте осуществления может быть использована система осадительной полимеризации в результате подбора растворителя, в котором полученный полимер является нерастворимым. В обоих случаях в полимеризационную систему обычно добавляют определенное количество растворителя в дополнение к тому количеству растворителя, которое может быть использовано при получении инициатора. Дополнительный растворитель может быть тем же самым, что и растворитель, использующийся при получении инициатора, или отличным от него. Примеры растворителей были приведены выше. В одном или нескольких вариантах осуществления уровень содержания растворителя в полимеризационной смеси может составлять более чем 20% (масс.), в других вариантах осуществления более чем 50% (масс.), а еще в одних вариантах осуществления более чем 80% (масс.) в расчете на совокупную массу полимеризационной смеси.
В других вариантах осуществления использующаяся полимеризационная система в общем случае может рассматриваться в качестве системы полимеризации в массе, которая по существу не включает растворителя или включает минимальное количество растворителя. Специалисты в соответствующей области техники должны понимать выгоды способов полимеризации в массе (то есть, способов, в которых мономер выступает в роли растворителя), и поэтому полимеризационная система должна включать меньше растворителя, чем то его количество, которое будет неблагоприятно сказываться на выгоде, полученной от проведения полимеризации в массе. В одном или нескольких вариантах осуществления уровень содержания растворителя в полимеризационной смеси может быть меньше приблизительно 20% (масс.), в других вариантах осуществления меньше приблизительно 10% (масс.), а в еще одних вариантах осуществления меньше приблизительно 5% (масс.) в расчете на совокупную массу полимеризационной смеси. В еще одном варианте осуществления полимеризационная смесь не содержит каких-либо растворителей, отличных от тех, которые неотъемлемо связаны с использующимися материалами исходного сырья. В еще одном варианте осуществления полимеризационная смесь по существу лишена растворителя, что соответствует отсутствию того количества растворителя, которое в противном случае оказывало бы ощутимое влияние на процесс полимеризации. Полимеризационные системы, которые по существу лишены растворителя, могут рассматриваться как по существу не включающие растворителя. В некоторых конкретных вариантах осуществления полимеризационная смесь совсем лишена растворителя.
Полимеризация может быть проведена в любых обычных полимеризационных емкостях, известных на современном уровне техники. В одном или нескольких вариантах осуществления растворная полимеризация может быть проведена в обычном корпусном реакторе с перемешиванием. В других вариантах осуществления в обычном корпусном реакторе с перемешиванием может быть проведена полимеризация в массе, в особенности в случае степени превращения мономера меньше приблизительно 60%. В еще одних вариантах осуществления, в особенности в случае степени превращения мономера в способе полимеризации в массе больше приблизительно 60%, что обычно в результате приводит к получению высоковязкого клея, полимеризация в массе может быть проведена в удлиненном реакторе, в котором вязкий полимеризуемый клей приводится в движение при помощи поршня или по существу при помощи поршня. Например, подходящими для использования в данных целях являются экструдеры, в которых клей проталкивают вперед с помощью самоочищающегося одночервячного или двухчервячного перемешивающего устройства. Примеры подходящих для использования способов полимеризации в массе описываются в патенте США №7351776, который посредством ссылки включается в настоящий документ.
В одном или нескольких вариантах осуществления все ингредиенты, использующиеся при полимеризации, могут быть объединены в одной емкости (например, обычном корпусном реакторе с перемешиванием), и все стадии способа полимеризации могут быть проведены в данной емкости. В других вариантах осуществления два и более ингредиента могут быть предварительно объединены в одной емкости, а после этого перенесены в другую емкость, в которой может быть проведена полимеризация мономера (или по меньшей мере основной его части).
Полимеризация может быть проведена периодическим способом, непрерывным способом или полунепрерывным способом. В полунепрерывном способе мономер по мере надобности периодически загружают для замещения того мономера, который уже был заполимеризован. В одном или нескольких вариантах осуществления можно контролировать условия, в которых протекает полимеризация, выдерживая температуру полимеризационной смеси в диапазоне от приблизительно -10°С до приблизительно 200°С, в других вариантах осуществления от приблизительно 0°С до приблизительно 150°С, а еще одних вариантах осуществления от приблизительно 20°С до приблизительно 100°С. В одном или нескольких вариантах осуществления теплота полимеризации может отводиться путем внешнего охлаждения при помощи терморегулируемой рубашки реактора, внутреннего охлаждения благодаря испарению и конденсации мономера с использованием дефлегматора, соединенного с реактором, или комбинации этих двух способов. Кроме того, условия проведения полимеризации можно контролировать, проводя полимеризацию под давлением в диапазоне от приблизительно 0,1 атмосферы до приблизительно 50 атмосфер, в других вариантах осуществления от приблизительно 0,5 атмосферы до приблизительно 20 атмосфер, а в еще одних вариантах осуществления от приблизительно 1 атмосферы до приблизительно 10 атмосфер. В одном или нескольких вариантах осуществления давления, при которых полимеризация может быть проведена, включают те, которые обеспечивают нахождение основной части мономера в жидкой фазе. В этих или других вариантах осуществления полимеризационную смесь можно выдерживать в анаэробных условиях.
До гашения активных центров полимеризационной смеси некоторое или все количество полимерных цепей в получающемся реакционно-способном полимере может иметь реакционно-способные концевые группы. Как отмечалось выше, реакционно-способный полимер, полученный при использовании анионного инициатора (например, алкиллитиевого инициатора), может рассматриваться в качестве живого полимера. В одном или нескольких вариантах осуществления полимеризационная смесь, включающая реакционно-способный полимер, может быть названа активной полимеризационной смесью. Процентное содержание полимерных цепей, имеющих реакционно-способные концевые группы, зависит от различных факторов, таких как тип инициатора, тип мономера, степень чистоты ингредиентов, температура полимеризации, степень превращения мономера и множество других факторов. В одном или нескольких вариантах осуществления реакционно-способную концевую группу имеют по меньшей мере приблизительно 20% полимерных цепей, в других вариантах осуществления реакционно-способную концевую группу имеют по меньшей мере приблизительно 50% полимерных цепей, а в еще одних вариантах осуществления реакционно-способную концевую группу имеют по меньшей мере приблизительно 80% полимерных цепей. В любом случае реакционно-способный полимер, или, говоря более конкретно, реакционно-способная концевая группа цепи полимера, может быть введен (введена) в реакцию с нитрильным соединением, имеющим защищенную аминогруппу, для получения функционализованного полимера по настоящему изобретению.
В одном или нескольких вариантах осуществления нитрильные соединения, имеющие защищенную аминогруппу, включают те соединения, которые имеют одну или несколько защищенных аминогрупп и одну или несколько цианогрупп. Для целей настоящего описания и для легкости объяснения нитрильные соединения, имеющие защищенную аминогруппу, могут называться просто нитрильными соединениями.
В одном или нескольких вариантах осуществления цианогруппа, которая может быть также названа нитрильной группой, может быть описана формулой -C≡N.
В одном или нескольких вариантах осуществления защищенные аминогруппы включают те аминогруппы, которые получают или производят в результате замещения двух атомов водорода исходной аминогруппы (то есть -NН2) другими заместителями, такими как гидрокарбильная или силильная группы. В одном или нескольких вариантах осуществления защищенная аминогруппа может быть описана формулой -NR2, где каждой группой R независимо являются гидрокарбильная группа или силильная группа. В случае включения в защищенную аминогруппу силильной группы и гидрокарбильной группы группа может быть названа моносилилированной аминогруппой. В случае включения в защищенную аминогруппу двух силильных групп группа может быть названа дисилилированной аминогруппой. В случае включения в защищенную аминогруппу двух гидрокарбильных групп группа может быть названа дигидрокарбиламиногруппой.
Примеры типов защищенных аминогрупп включают нижеследующие, но не ограничиваются только этими: бис(тригидрокарбилсилил)амино, бис(дигидрокарбилгидросилил)амино, 1-азадисила-1-циклогидрокарбильная, (тригидрокарбилсилил)(гидрокарбил)амино, (дигидрокарбилгидросилил)(гидрокарбил)амино, 1-аза-2-сила-1-циклогидрокарбильная, дигидрокарбиламино и 1-аза-1-циклогидрокарбильная группы.
Конкретные примеры бис(тригидрокарбилсилил)амино групп включают нижеследующие, но не ограничиваются только этими: бис(триметилсилил)амино, бис(триэтилсилил)амино, бис(триизопропилсилил)амино, бис(три-н-пропилсилил)амино, бис(триизобутилсилил)амино, бис(три-трет-бутилсилил)амино и бис(трифенилсилил)амино группы.
Конкретные примеры бис(дигидрокарбилгидросилил)амино групп включают нижеследующие, но не ограничиваются только этими: бис(диметилгидросилил)амино, бис(диэтилгидросилил)амино, бис(диизопропилгидросилил)амино, бис(ди-н-пропилгидросилил)амино, бис(диизобутилгидросилил)амино, бис(ди-трет-бутилгидросилил)амино- и бис(дифенилгидросилил)аминогруппы.
Конкретные примеры 1-азадисила-1-циклогидрокарбильных групп включают нижеследующие, но не ограничиваются только этими: 2,2,5,5-тетраметил-1-аза-2,5-дисила-1-циклопентильная, 2,2,5,5-тетраэтил-1-аза-2,5-дисила-1-циклопентильная, 2,2,5,5-тетрафенил-1-аза-2,5-дисила-1-циклопентильная, 2,2,6,6-тетраметил-1-аза-2,6-дисила-1-циклогексильная, 2,2,6,6-тетраэтил-1-аза-2,6-дисила-1-циклогексильная и 2,2,6,6-тетрафенил-1-аза-2,б-дисила-1-циклогексильная группы.
Конкретные примеры (тригидрокарбилсилил)(гидрокарбил)амино групп включают нижеследующие, но не ограничиваются только этими: (триметилсилил)(метил)амино, (триэтилсилил)(метил)амино, (трифенилсилил)(метил)амино, (триметилсилил)(этил)амино, (триэтилсилил)(фенил)амино и (триизопропилсилил)(метил)амино группы.
Конкретные примеры (дигидрокарбилгидросилил)(гидрокарбил)амино групп включают нижеследующие, но не ограничиваются только этими: (диметилгидросилил)(метил)амино, (диэтилгидросилил)(метил)амино, (диизопропилгидросилил)(метил)амино, (ди-н-пропилгидросилил)(этил)амино, (диизобутилгидросилил)(фенил)амино, (ди-трет-бутилгидросилил)(фенил)амино и (дифенилгидросилил)(фенил)амино группы.
Конкретные примеры 1-аза-2-сила-1-циклогидрокарбильных трупп включают нижеследующие, но не ограничиваются только этими: 2,2-диметил-1-аза-2-сила-1-циклопентильная, 2,2-диэтил-1-аза-2-сила-1-циклопентильная, 2,2-дифенил-1-аза-2-сила-1-циклопентильная, 2,2-диизопропил-1-аза-2-сила-1-циклогексильная, 2,2-дибутил-1-аза-2-сила-1-циклогексильная и 2,2-дифенил-1-аза-2-сила-1-циклогексильная группы.
Конкретные примеры дигидрокарбиламино групп включают нижеследующие, но не ограничиваются только этими: диметиламино, диэтиламино, ди-н-пропиламино, диизопропиламино, ди-н-бутиламино, диизобутиламино, дициклогексиламино, дифениламино, дибензиламино, (метил)(циклогексил)амино, (этил)(циклогексил)амино, (метил)(фенил)амино, (этил)(фенил)амино, (метил)(бензил)амино и (этил)(бензил)амино группы.
Конкретные примеры 1-аза-1-циклогидрокарбильных групп включают нижеследующие, но не ограничиваются только этими: азиридино, азетидино, пирролидино, пиперидино, гомопиперидино, морфолино, N-метилпиперазино и N-метилгомопиперазино группы.
В конкретных вариантах осуществления нитрильные соединения, имеющие защищенную аминогруппу, включают те соединения, в которых цианогруппа непосредственно присоединена к ациклическому фрагменту. В других конкретных вариантах осуществления нитрильные соединения, имеющие защищенную аминогруппу, включают те соединения, в которых защищенная аминогруппа непосредственно присоединена к ациклическому фрагменту. В еще одних конкретных вариантах осуществления нитрильные соединения включают те соединения, у которых как цианогруппа, так и защищенная аминогруппа непосредственно присоединены к ациклическому фрагменту.
В конкретных вариантах осуществления нитрильные соединения, имеющие защищенную аминогруппу, включают те соединения, в которых цианогруппа непосредственно присоединена к гетероциклическому фрагменту. В других конкретных вариантах осуществления нитрильные соединения, имеющие защищенную аминогруппу, включают те соединения, в которых защищенная аминогруппа непосредственно присоединена к гетероциклическому фрагменту. В еще одних конкретных вариантах осуществления нитрильные соединения включают те соединения, в которых как цианогруппа, так и защищенная аминогруппа непосредственно присоединены к гетероциклическому фрагменту.
В конкретных вариантах осуществления нитрильные соединения, имеющие защищенную аминогруппу, включают те соединения, в которых цианогруппа непосредственно присоединена к неароматическому циклическому фрагменту. В других конкретных вариантах осуществления нитрильные соединения, имеющие защищенную аминогруппу, включают те соединения, у которых защищенная аминогруппа непосредственно присоединена к неароматическому циклическому фрагменту. В других еще конкретных вариантах осуществления нитрильные соединения, имеющие защищенную аминогруппу, включают те соединения, у которых как цианогруппа, так и защищенная аминогруппа непосредственно присоединены к неароматическому циклическому фрагменту.
В конкретных вариантах осуществления нитрильные соединения, имеющие защищенную аминогруппу, включают те соединения, в которых цианогруппа непосредственно присоединена к ароматическому фрагменту (например, фенильному кольцу), который лишен гетероатомов, и защищенная аминогруппа непосредственно присоединена к ациклическому фрагменту, гетероциклическому фрагменту или неароматическому циклическому фрагменту.
В одном или нескольких вариантах осуществления данное изобретение конкретно включает те соединения, в которых цианогруппа, или в других вариантах осуществления в которых защищенная аминогруппа, или в других вариантах осуществления в которых как цианогруппа, так и защищенная аминогруппа непосредственно присоединены к ароматическому фрагменту (например, фенильному кольцу), который лишен гетероатомов.
В одном или нескольких вариантах осуществления нитрильные соединения, имеющие защищенную аминогруппу, могут быть описаны формулой I:

где R1 представляет собой двухвалентную органическую группу, а каждый из R2 и R3 независимо представляет собой одновалентную органическую группу или гидролизуемую группу, или R2 и R3 соединяются с образованием двухвалентной органической группы. В одном или нескольких вариантах осуществления двухвалентная органическая группа, полученная в результате соединения R2 и R3, может включать одну или несколько гидролизуемых групп. В одном или нескольких вариантах осуществления двухвалентная органическая группа R1 может иметь одну или несколько дополнительных защищенных аминогрупп и/или одну или несколько дополнительных цианогрупп. В одном или нескольких вариантах осуществления, в которых R2 и R3 соединяются с образованием двухвалентной органической группы, нитрильное соединение, имеющее защищенную аминогруппу, может быть описано формулой II:

где каждый из R1 и R5 независимо представляет собой двухвалентную органическую группу, а каждый из R4 и R6 независимо представляет собой связь или гидролизуемую группу.
В одном или нескольких вариантах осуществления одновалентные органические группы могут включать гидрокарбильные группы или замещенные гидрокарбильные группы, такие как нижеследующие, но не ограничивающиеся только этими: алкильная, циклоалкильная, алкенильная, циклоалкенильная, арильная, аллильная, аралкильная, алкарильная или алкинильная группы. Замещенные гидрокарбильные группы включают гидрокарбильные группы, в которых один или несколько атомов водорода замещены заместителем, таким как алкильная группа. В одном или нескольких вариантах осуществления данные группы могут содержать от одного атома углерода или минимального количества атомов углерода, подходящего для получения группы, до приблизительно 20 атомов углерода. Данные группы также могут содержать гетероатомы, такие как нижеследующие, но не ограничивающиеся только этими: атомы азота, бора, кислорода, кремния, серы, олова и фосфора.
В одном или нескольких вариантах осуществления гидролизуемые группы включают те группы или заместители, которые являются относительно стабильными и поэтому остаются химически связанными с атомом азота в неводных средах или средах, которые лишены или по существу лишены воды. Однако, сразу после воздействия водой, влагой или материалами, содержащими воду или влагу, гидролизуемые группы или заместители гидролизуются и, тем самым, отщепляются от атома азота. В результате гидролизуемые группы замещаются атомом водорода.
Примеры гидролизуемых групп включают тригидрокарбилсилильную и дигидрокарбилгидросилильную группы. Конкретные примеры тригидрокарбилсилильных групп включают триметилсилильную, триэтилсилильную, три-н-пропилсилильную, триизопропилсилильную, три-н-бутилсилильную, триизобутилсилильную, три-трет-бутилсилильную, трифенилсилильную и трет-бутилдиметилсилильную группы. Конкретные примеры дигидрокарбилгидросилильных групп включают диметилгидросилильную, диэтилгидросилильную, ди-н-пропилгидросилильную, диизопропилгидросилильную, ди-н-бутилгидросилильную, диизобутилгидросилильную, ди-трет-бутилгидросилильную и дифенилгидросилильную группы. Для удаления силильной группы с защищенной аминогруппы также может быть использован и катализатор. Подходящие для использования катализаторы включают фторид тетрабутиламмония, сильные кислоты, такие как хлористо-водородная кислота, и кислоты Льюиса, такие как тетрахлорид титана.
В одном или нескольких вариантах осуществления двухвалентные органические группы могут включать гидрокарбиленовые группы или замещенные гидрокарбиленовые группы, такие как нижеследующие, но не ограничивающиеся только этими: алкиленовая, циклоалкиленовая, алкениленовая, циклоалкениленовая, алкиниленовая, циклоалкиниленовая или гетероциклическая ариленовая (то есть, ариленовые группы, содержащие гетероатомы в кольце) группы. В конкретных вариантах осуществления специально исключаются негетероциклические ариленовые группы (например, фенильные группы); то есть, те ариленовые группы, которые не содержат гетероатомов в кольце. Замещенные гидрокарбиленовые группы включают гидрокарбиленовые группы, в которых один или несколько атомов водорода замещены заместителем, таким как алкильная группа. В одном или нескольких вариантах осуществления данные группы могут содержать от одного или минимального количества атомов углерода, необходимого для получения группы, до приблизительно 20 атомов углерода. Эти группы также могут содержать один или несколько гетероатомов, таких как нижеследующие, но не ограничивающихся только этими: атомы азота, кислорода, бора, кремния, серы, олова и фосфора.
В одном или нескольких вариантах осуществления двухвалентная органическая группа R1 является ациклической двухвалентной органической группой (либо линейной, либо разветвленной), которая может содержать, а может и не содержать один или несколько гетероатомов. В других вариантах осуществления двухвалентная органическая группа R1 является гетероциклической двухвалентной органической группой. В еще одних вариантах осуществления двухвалентная органическая группа R1 является неароматической циклической двухвалентной органической группой, которая лишена гетероатомов.
В одном или нескольких вариантах осуществления двухвалентная органическая группа R1 может содержать ароматическое кольцо (например, фенильное кольцо), которое лишено гетероатомов, при условии, что защищенная аминогруппа не должна быть непосредственно присоединена к ароматическому кольцу, (например, защищенная аминогруппа может быть присоединена к R1 через алкиленовую группу, боковую по отношению к ароматическому кольцу).
В конкретных вариантах осуществления R2 из формулы I представляет собой силильную группу, а нитрильное соединение, имеющее защищенную аминогруппу, может быть описано формулой III:

где R1 представляет собой двухвалентную органическую группу, R3 представляет собой одновалентную органическую группу или гидролизуемую группу, каждый R7 независимо представляет собой атом водорода или одновалентную органическую группу, или R3 и один R7 соединяются с образованием двухвалентной органической группы. В одном или нескольких вариантах осуществления двухвалентная органическая группа, образованная в результате соединения R3 и R7, может включать одну или несколько гидролизуемых групп. В одном или нескольких вариантах осуществления, в которых R3 и один R7 соединяются с образованием двухвалентной органической группы, нитрильное соединение, имеющее защищенную аминогруппу, может быть описано формулой IV:
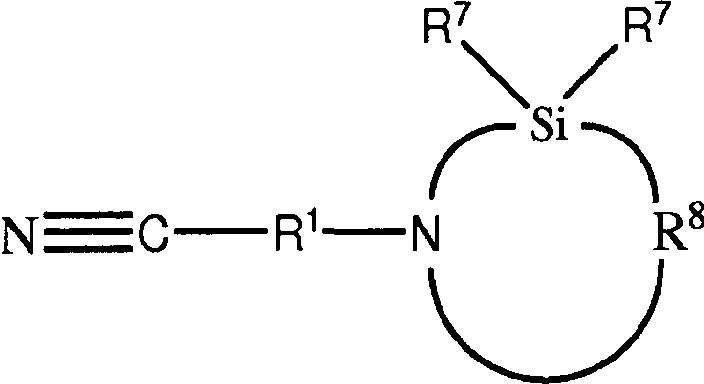
где каждый из R1 и R8 независимо представляет собой двухвалентную органическую группу, а каждый R7 независимо представляет собой атом водорода или одновалентную органическую группу.
В конкретных вариантах осуществления каждый из R2 и R3 из формулы I независимо представляет собой силильную группу, а нитрильное соединение, имеющее защищенную аминогруппу, может быть описано формулой V:
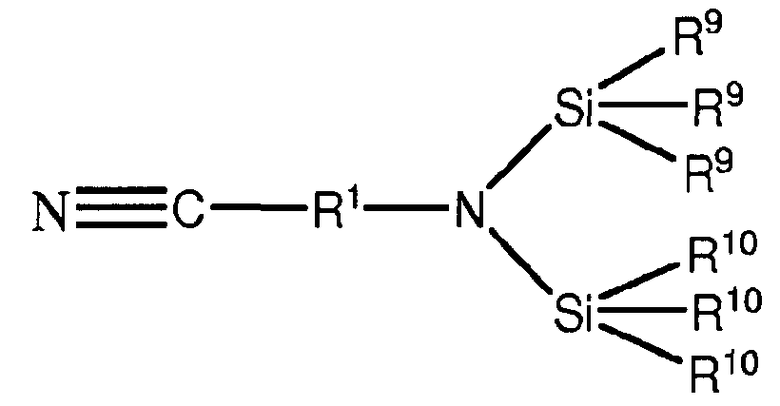
где R1 представляет собой двухвалентную органическую группу, и каждый из R9 и R10 независимо представляет собой атом водорода или одновалентную органическую группу, или по меньшей мере один R9 и по меньшей мере один R10 соединяются с образованием двухвалентной органической группы. В одном или нескольких вариантах осуществления, в которых один R9 и один R10 соединяются с образованием двухвалентной органической группы, нитрильное соединение, имеющее защищенную аминогруппу, может быть описано формулой VI:

где каждый из R1 и R11 независимо представляет собой двухвалентную органическую группу, а каждый из R9 и R10 независимо представляет собой атом водорода или одновалентную органическую группу.
Примеры типов нитрильных соединений, имеющих защищенную аминогруппу, включают те соединения, которые могут быть получены из нитрильных соединений, таких как аренкарбонитрильные соединения, алканкарбонитрильные соединения, алкенкарбонитрильные соединения, алкинкарбонитрильные соединения, циклоалканкарбонитрильные соединения, циклоалкенкарбонитрильные соединения, циклоалкинкарбонитрильные соединения и гетероциклические нитрильные соединения. Специалисты в соответствующей области техники должны понимать, что аренкарбонитрильные соединения включают ареновые соединения, у которых один или несколько атомов водорода в ареновом соединении замещены цианогруппами, и специалисты в соответствующей области техники должны понимать, что аналогичным образом могут быть определены и другие классы нитрильных соединений.
Примеры аренкарбонитрильных соединений, имеющих защищенную аминогруппу, включают те соединения, которые можно получить из аренкарбонитрильных соединений, таких как 2-метилбензонитрил, 3-метилбензонитрил, 4-метилбензонитрил, 2-этилбензонитрил, 3-этилбензонитрил, 4-этилбензонитрил, 2-циклогексилбензонитрил, 3-циклогексилбензонитрил и 4-циклогексилбензонитрил.
Примеры алканкарбонитрильных соединений, имеющих защищенную аминогруппу, включают те соединения, которые производят из алканкарбонитрильных соединений, таких как ацетонитрил, пропионитрил, бутиронитрил, изобутиронитрил, валеронитрил, изовалеронитрил, пивалонитрил, 1-гексаннитрил и 1-гептаннитрил.
Примеры алкенкарбонитрильных соединений, имеющих защищенную аминогруппу, включают те соединения, которые могут быть получены из алкенкарбонитрильных соединений, таких как акрилонитрил, метакрилонитрил, кротононитрил, 3-бутеннитрил, 2-метил-2-бутеннитрил, 2-пентеннитрил, 3-пентеннитрил, 4-пентеннитрил, 5-гексеннитрил, 2-метиленглутаронитрил, 6-гептеннитрил, фумаронитрил, метиленмалононитрил и бензилиденмалононитрил.
Примеры алкинкарбонитрильных соединений, имеющих защищенную аминогруппу, включают те соединения, которые производят из алкинкарбонитрильных соединений, таких как 3-бутиннитрил, 2-пентиннитрил, 3-пентиннитрил, 4-пентиннитрил и 5-гексиннитрил.
Примеры циклоалканкарбонитрильных соединений, имеющих защищенную аминогруппу, включают те соединения, которые производят из циклоалканкарбонитрильных соединений, таких как циклопропанкарбонитрил, циклобутанкарбонитрил, циклопентанкарбонитрил, циклогексанкарбонитрил и циклогептанкарбонитрил.
Примеры циклоалкенкарбонитрильных соединений, имеющих защищенную аминогруппу, включают те соединения, которые могут быть получены из циклоалкенкарбонитрильных соединений, таких как 1-циклопропенкарбонитрил, 1-циклобутенкарбонитрил, 1-циклопентенкарбонитрил, 1-циклогексенкарбонитрил и 1-циклогептенкарбонитрил.
Примеры гетероциклических нитрильных соединений, имеющих защищенную аминогруппу, включают те соединения, которые могут быть получены из гетероциклических нитрильных соединений, таких как 2-пиридинкарбонитрил, 3-пиридинкарбонитрил, 4-пиридинкарбонитрил, 2-пиримидинкарбонитрил, 4-пиримидинкарбонитрил, 5-пиримидинкарбонитрил, пиразинкарбонитрил, 3-пиридазинкарбонитрил и 4-пиридазинкарбонитрил.
Примеры типов аренкарбонитрильных соединений, имеющих защищенную аминогруппу, включают [бис(тригидрокарбилсилил)амино]аренкарбонитрил, [бис(дигидрокарбилгидросилил)амино]аренкарбонитрил, (1-азадисила-1-циклогидрокарбил)аренкарбонитрил, [(тригидрокарбилсилил)(гидрокарбил)амино]аренкарбонитрил, [(дигидрокарбилгидросилил)(гидрокарбил)амино]аренкарбонитрил, (1-аза-2-сила-1-циклогидрокарбил)аренкарбонитрил, (дигидрокарбиламино)аренкарбонитрил и (1-аза-1-циклогидрокарбил)аренкарбонитрил.
Примеры типов алканкарбонитрильных соединений, имеющих защищенную аминогруппу, включают [бис(тригидрокарбилсилил)амино]алканкарбонитрил, [бис(дигидрокарбилгидросилил)амино]алканкарбонитрил, (1-азадисила-1-циклогидрокарбил)алканкарбонитрил, [(тригидрокарбилсилил)(гидрокарбил)амино]алканкарбонитрил, [(дигидрокарбилгидросилил)(гидрокарбил)амино]алканкарбонитрил, (1-аза-2-сила-1-циклогидрокарбил)алканкарбонитрил, (дигидрокарбиламино)алканкарбонитрил и (1-аза-1-циклогидрокарбил)алканкарбонитрил.
Примеры типов алкенкарбонитрильных соединений, имеющих защищенную аминогруппу, включают [бис(тригидрокарбилсилил)амино] алкенкарбонитрил, [бис(дигидрокарбилгидросилил)амино] алкенкарбонитрил, (1-азадисила-1-циклогидрокарбил)алкенкарбонитрил, [(тригидрокарбилсилил)(гидрокарбил)амино]алкенкарбонитрил, [(дигидрокарбилгидросилил)(гидрокарбил)амино] алкенкарбонитрил, (1-аза-2-сила-1-циклогидрокарбил)алкенкарбонитрил, (дигидрокарбиламино)алкенкарбонитрил и (1-аза-1-циклогидрокарбил)алкенкарбонитрил.
Примеры типов алкинкарбонитрильных соединений, имеющих защищенную аминогруппу, включают [бис(тригидрокарбилсилил)амино] алкинкарбонитрил, [бис(дигидрокарбилгидросилил)амино] алкинкарбонитрил, (1-азадисила-1-циклогидрокарбил)алкинкарбонитрил, [(тригидрокарбилсилил)(гидрокарбил)амино]алкинкарбонитрил, [(дигидрокарбилгидросилил)(гидрокарбил)амино]алкинкарбонитрил, (1-аза-2-сила-1-циклогидрокарбил)алкинкарбонитрил, (дигидрокарбиламино)алкинкарбонитрил и (1-аза-1-циклогидрокарбил)алкинкарбонитрил.
Примеры типов циклоалканкарбонитрильных соединений, имеющих защищенную аминогруппу, включают [бис(тригидрокарбилсилил)амино]циклоалканкарбонитрил, [бис(дигидрокарбилгидросилил)амино]циклоалканкарбонитрил, (1-азадисила-1-циклогидрокарбил)циклоалканкарбонитрил, [(тригидрокарбилсилил)(гидрокарбил)амино]циклоалканкарбонитрил, [(дигидрокарбилгидросилил)(гидрокарбил)амино]циклоалканкарбонитрил, (1-аза-2-сила-1-циклогидрокарбил)циклоалканкарбонитрил, (дигидрокарбиламино)циклоалканкарбонитрил и (1-аза-1-циклогидрокарбил)циклоалканкарбонитрил.
Примеры типов циклоалкенкарбонитрильных соединений, имеющих защищенную аминогруппу, включают [бис(тригидрокарбилсилил)амино]циклоалкенкарбонитрил, [бис(дигидрокарбилгидросилил)амино]циклоалкенкарбонитрил, (1-азадисила-1-циклогидрокарбил)циклоалкенкарбонитрил, [(тригидрокарбилсилил)(гидрокарбил)амино]циклоалкенкарбонитрил, [(дигидрокарбилгидросилил)(гидрокарбил)амино]циклоалкенкарбонитрил, (1-аза-2-сила-1-циклогидрокарбил)циклоалкенкарбонитрил, (дигидрокарбиламино)циклоалкенкарбонитрил и (1-аза-1-циклогидрокарбил)циклоалкенкарбонитрил.
Примеры типов циклоалкинкарбонитрильных соединений, имеющих защищенную аминогруппу, включают [бис(тригидрокарбилсилил)амино]циклоалкинкарбонитрил, [бис(дигидрокарбилгидросилил)амино]циклоалкинкарбонитрил, (1-азадисила-1-циклогидрокарбил)пиклоалкинкарбонитрил, [(тригидрокарбилсилил)(гидрокарбил)амино]циклоалкинкарбонитрил, [(дигидрокарбилгидросилил)(гидрокарбил)амино]циклоалкинкарбонитрил, (1-аза-2-сила-1-циклогидрокарбил)циклоалкинкарбонитрил, (дигидрокарбиламино)циклоалкинкарбонитрил и (1-аза-1-циклогидрокарбил)циклоалкинкарбонитрил.
Примеры типов гетероциклических нитрильных соединений, имеющих защищенную аминогруппу, включают [бис(тригидрокарбилсилил)амино]гетероциклический нитрил, [бис(дигидрокарбилгидросилил)амино]гетероциклический нитрил, (1-азадисила-1-циклогидрокарбил)гетероциклический нитрил, [(тригидрокарбилсилил)(гидрокарбил)амино]гетероциклический нитрил, [(дигидрокарбилгидросилил)(гидрокарбил)амино]гетероциклический нитрил, (1-аза-2-сила-1-циклогидрокарбил)гетероциклический нитрил, (дигидрокарбиламино)гетероциклический нитрил и (1-аза-1-циклогидрокарбил)гетероциклический нитрил.
Конкретные примеры аренкарбонитрильных соединений, имеющих защищенную аминогруппу, включают 2-[бис(триметилсилил)аминометил]бензонитрил, 3-[бис(триметилсилил)аминометил]бензонитрил, 4-[бис(триметилсилил)аминометил]бензонитрил, 2-[(2,2,5,5-тетраметил-1-аза-2,5-дисила-1-циклопентил)метил]бензонитрил, 3-[(2,2,5,5-тетраметил-1-аза-2,5-дисила-1-циклопентил)метил]бензонитрил, 4-[(2,2,5,5-тетраметил-1-аза-2,5-дисила-1-циклопентил)метил]бензонитрил, 2-[(триметилсилил)(метил)аминометил]бензонитрил, 3-[(триметилсилил)(метил)аминометил]бензонитрил, 4-[(триметилсилил)(метил)аминометил]бензонитрил, 2-[(2,2-диметил-1-аза-2-сила-1-циклопентил)метил]бензонитрил, 3-[(2,2-диметил-1-аза-2-сила-1-циклопентил)метил]бензонитрил, 4-[(2,2-диметил-1-аза-2-сила-1-циклопентил)метил]бензонитрил, 2-(диметиламинометил)бензонитрил, 3-(диметиламинометил)бензонитрил, 4-(диметиламинометил)бензонитрил, 2-(азиридинометил)бензонитрил, 3-(азиридинометил)бензонитрил, 4-(азиридинометил)бензонитрил, 2-(азетидинометил)бензонитрил, 3-(азетидинометил)бензонитрил, 4-(азетидинометил)бензонитрил, 2-(пирролидинометил)бензонитрил, 3-(пирролидинометил)бензонитрил, 4-(пирролидинометил)бензонитрил, 2-(пиперидинометил)бензонитрил, 3-(пиперидинометил)бензонитрил, 4-(пиперидинометил)бензонитрил, 2-(гомопиперидинометил)бензонитрил, 3-(гомопиперидинометил)бензонитрил, 4-(гомопиперидинометил)бензонитрил, 2-(морфолинометил)бензонитрил, 3-(морфолинометил)бензонитрил, 4-(морфолинометил)бензонитрил, 2-[(N-метилпиперазино)метил]бензонитрил, 3-[(N-метилпиперазино)метил]бензонитрил, 4-[(N-метилпиперазино)метил]бензонитрил, 2-[(N-метилгомопиперазино)метил]бензонитрил, 3-[(N-метилгомопиперазино)метил]бензонитрил и 4-[(N-метилгомопиперазино)метил] бензонитрил.
Конкретные примеры алканкарбонитрильных соединений, имеющих защищенную аминогруппу, включают [бис(триметилсилил)амино]ацетонитрил, 3-[бис(триметилсилил)амино]пропионитрил, 4-[бис(триметилсилил)амино]бутиронитрил, 5-[бис(триметилсилил)амино]валеронитрил, (2,2,5,5-тетраметил-1-аза-2,5-дисила-1-циклопентил)ацетонитрил, 3-(2,2,5,5-тетраметил-1-аза-2,5-дисила-1-циклопентил)пропионитрил, 4-(2,2,5,5-тетраметил-1-аза-2,5-дисила-1-циклопентил)бутиронитрил, 5-(2,2,5,5-тетраметил-1-аза-2,5-дисила-1-циклопентил)валеронитрил, [(триметилсилил)(метил)амино]ацетонитрил, [(триметилсилил)(этил)амино]ацетонитрил, 3-[(триметилсилил)(метил)амино]пропионитрил, 3-[(триметилсилил)(этил)амино]пропионитрил, 4-[(триметилсилил)(метил)амино]бутиронитрил, 4-[(триметилсилил)(этил)амино]бутиронитрил, 5-[(триметилсилил)(метил)амино]валеронитрил, 5-[(триметилсилил)(этил)амино]валеронитрил, N-триметилсилил-3,3'-иминодипропионитрил, N-триметилсилилиминодиацетонитрил, (2,2-диметил-1-аза-2-сила-1-циклопентил)ацетонитрил, 3-(2,2-диметил-1-аза-2-сила-1-циклопентил)пропионитрил, 4-(2,2-диметил-1-аза-2-сила-1-циклопентил)бутиронитрил, 5-(2,2-диметил-1-аза-2-сила-1-циклопентил)валеронитрил, (диметиламино)ацетонитрил, (диэтиламино)ацетонитрил, (дифениламино)ацетонитрил, 3-(диметиламино)пропионитрил, 3-(диэтиламино)пропионитрил, 3-(ди-н-пропиламино)пропионитрил, 3-(диизопропиламино)пропионитрил, 3-(ди-н-бутиламино)пропионитрил, 3-(диизобутиламино)пропионитрил, 3-(дициклогексиламино)пропионитрил, 3-(дифениламино)пропионитрил, 3-[бис(цианоэтил)амино]пропионитрил, 3-(дибензиламино)пропионитрил, 3-[(метил)(циклогексил)амино]пропионитрил, 3-[(этил)(циклогексил)амино]пропионитрил, 3-[(метил)(фенил)амино]пропионитрил, 3-[(этил)(фенил)амино]пропионитрил, 3-[(метил)(бензил)амино]пропионитрил, 3-[(этил)(бензил)амино]пропионитрил, 4-(диметиламино)бутиронитрил, 4-(диэтиламино)бутиронитрил, 4-(ди-н-пропиламино)бутиронитрил, 4-(диизопропиламино)бутиронитрил, 4-(ди-н-бутиламино)бутиронитрил, 4-(диизобутиламино)бутиронитрил, 4-(дициклогексиламино)бутиронитрил, 4-(дифениламино)бутиронитрил, 4-(дибензиламино)бутиронитрил, 4-[(метил)(циклогексил)амино]бутиронитрил, 4-[(этил)(циклогексил)амино]бутиронитрил, 4-[(метил)(фенил)амино]бутиронитрил, 4-[(этил)(фенил)амино]бутиронитрил, 4-[(метил)(бензил)амино]бутиронитрил, 4-[(этил)(бензил)амино]бутиронитрил, 5-(диметиламино)валеронитрил, 5-(диэтиламино)валеронитрил, 5-(дифениламино)валеронитрил, азиридиноацетонитрил, азетидиноацетонитрил, пирролидиноацетонитрил, пиперидиноацетонитрил, гомопиперидиноацетонитрил, морфолиноацетонитрил, (N-метилпиперазино)ацетонитрил, (N-метилгомопиперазино)ацетонитрил, 3-азиридинопропионитрил, 3-азетидинопропионитрил, 3-пирролидинопропионитрил, 3-пиперидинопропионитрил, 3-гомопиперидинопропионитрил, 3-морфолинопропионитрил, 3-(N-метилпиперазино)пропионитрил, 3-(N-метилгомопиперазино)пропионитрил, 4-азиридинобутиронитрил, 4-азетидинобутиронитрил, 4-пирролидинобутиронитрил, 4-пиперидинобутиронитрил, 4-гомопиперидинобутиронитрил, 4-морфолинобутиронитрил, 4-(N-метилпиперазино)бутиронитрил, 4-(N-метилгомопиперазино)бутиронитрил, 5-азиридиновалеронитрил, 5-азетидиновалеронитрил, 5-пирролидиновалеронитрил, 5-пиперидиновалеронитрил, 5-гомопиперидиновалеронитрил, 5-морфолиновалеронитрил, 5-(N-метилпиперазино)валеронитрил и 5-(N-метилгомопиперазино)валеронитрил.
Конкретные примеры алкенкарбонитрильных соединений, имеющих защищенную аминогруппу, включают 3-[бис(триметилсилил)амино]кротононитрил, 3-[бис(триметилсилил)амино]-4-пентеннитрил, 3-[бис(триметилсилил)амино]-5-гексеннитрил, 3-(2,2,5,5-тетраметил-1-аза-2,5-дисила-1-циклопентил)кротононитрил, 3-(2,2,5,5-тетраметил-1-аза-2,5-дисила-1-циклопентил)-4-пентеннитрил, 3-(2,2,5,5-тетраметил-1-аза-2,5-дисила-1-циклопентил)-5-гексеннитрил, 3-[(триметилсилил)(метил)амино]кротононитрил, 3-[(триметилсилил)(этил)амино]кротононитрил, 3-[(триметилсилил)(метил)амино]-4-пентеннитрил, 3-[(триметилсилил)(этил)амино]-4-пентеннитрил, 3-[(триметилсилил)(метил)амино]-5-гексеннитрил, 3-[(триметилсилил)(этил)амино]-5-гексеннитрил, 3-(2,2-диметил-1-аза-2-сила-1-циклопентил)кротононитрил, 3-(2,2-диметил-1-аза-2-сила-1-циклопентил)-4-пентеннитрил, 3-(2,2-диметил-1-аза-2-сила-1-циклопентил)-5-гексеннитрил, 3-(диметиламино)акрилонитрил, 3-(диметиламино)кротононитрил, 3-(диэтиламино)кротононитрил, 3-(ди-н-пропиламино)кротононитрил, 3-(диизопропиламино)кротононитрил, 3-(ди-н-бутиламино)кротононитрил, 3-(диизобутиламино)кротононитрил, 3-(дициклогексиламино)кротононитрил, 3-(дифениламино)кротононитрил, 3-(дибензиламино)кротононитрил, 3-[(метил)(циклогексил)амино]кротононитрил, 3-[(этил)(циклогексил)амино]кротононитрил, 3-[(метил)(фенил)амино]кротононитрил, 3-[(этил)(фенил)амино]кротононитрил, 3-[(метил)(бензил)амино]кротононитрил, 3-[(этил)(бензил)амино]кротононитрил, 3-(диметиламино)-4-пентеннитрил, 3-(диэтиламино)-4-пентеннитрил, 3-(ди-н-пропиламино)-4-пентеннитрил, 3-(диизопропиламино)-4-пентеннитрил, 3-(ди-н-бутиламино)-4-пентеннитрил, 3-(диизобутиламино)-4-пентеннитрил, 3-(дициклогексиламино)-4-пентеннитрил, 3-(дифениламино)-4-пентеннитрил, 3-(дибензиламино)-4-пентеннитрил, 3-[(метил)(циклогексил)амино]-4-пентеннитрил, 3-[(этил)(циклогексил)амино]-4-пентеннитрил, 3-[(метил)(фенил)амино]-4-пентеннитрил, 3-[(этил)(фенил)амино]-4-пентеннитрил, 3-[(метил)(бензил)амино]-4-пентеннитрил, 3-[(этил)(бензил)амино]-4-пентеннитрил, 3-(диметиламино)-5-гексеннитрил, 3-(диэтиламино)-5-гексеннитрил, 3-(ди-н-пропиламино)-5-гексеннитрил, 3-(диизопропиламино)-5-гексеннитрил, 3-(ди-н-бутиламино)-5-гексеннитрил, 3-(диизобутиламино)-5-гексеннитрил, 3-(дициклогексиламино)-5-гексеннитрил, 3-(дифениламино)-5-гексеннитрил, 3-(дибензиламино)-5-гексеннитрил, 3-[(метил)(циклогексил)амино]-5-гексеннитрил, 3-[(этил)(циклогексил)амино]-5-гексеннитрил, 3-[(метил)(фенил)амино]-5-гексеннитрил, 3-[(этил)(фенил)амино]-5-гексеннитрил, 3-[(метил)(бензил)амино]-5-гексеннитрил, 3-[(этил)(бензил)амино]-5-гексеннитрил, 3-азиридинокротононитрил, 3-азетидинокротононитрил, 3-пирролидинокротононитрил, 3-пиперидинокротононитрил, 3-гомопиперидинокротононитрил, 3-морфолинокротононитрил, 3-(N-метилциперазино)кротононитрил, 3-(N-метилгомопиперазино)кротононитрил, 3-азиридино-4-пентеннитрил, 3-азетидино-4-пентеннитрил, 3-пирролидино-4-пентеннитрил, 3-пиперидино-4-пентеннитрил, 3-гомопиперидино-4-пентеннитрил, 3-морфолино-4-пентеннитрил, 3-(N-метилпиперазино)-4-пентеннитрил, 3-(N-метилгомопиперазино)-4-пентеннитрил, 3-азиридино-5-гексеннитрил, 3-азетидино-5-гексеннитрил, 3-пирролидино-5-гексеннитрил, 3-пиперидино-5-гексеннитрил, 3-гомопиперидино-5-гексеннитрил, 3-морфолино-5-гексеннитрил, 3-(N-метилпиперазино)-5-гексеннитрил и 3-(N-метилгомопиперазино)-5-гексеннитрил.
Конкретные примеры алкинкарбонитрильных соединений, имеющих защищенные аминогруппы, включают 3-[бис(триметилсилил)амино]-4-пентиннитрил, 3-[бис(триметилсилил)амино]-5-гексиннитрил, 3-(2,2,5,5-тетраметил-1-аза-2,5-дисила-1-циклопентил)-4-пентиннитрил, 3-(2,2,5,5-тетраметил-1-аза-2,5-дисила-1-циклопентил)-5-гексиннитрил, 3-[(триметилсилил)(метил)амино]-4-пентиннитрил, 3-[(триметилсилил)(этил)амино]-4-пентиннитрил, 3-[(триметилсилил)(метил)амино]-5-гексиннитрил, 3-[(триметилсилил)(этил)амино]-5-гексиннитрил, 3-(2,2-диметил-1-аза-2-сила-1-циклопентил)-4-пентиннитрил, 3-(2,2-диметил-1-аза-2-сила-1-циклопентил)-5-гексиннитрил, 3-(диметиламино)-4-пентиннитрил, 3-(диэтиламино)-4-пентиннитрил, 3-(ди-н-пропиламино)-4-пентиннитрил, 3 -(диизопропиламино)-4-пентиннитрил, 3-(ди-н-бутиламино)-4-пентиннитрил, 3-(диизобутиламино)-4-пентиннитрил, 3-(дициклогексиламино)-4-пентиннитрил, 3-(дифениламино)-4-пентиннитрил, 3-(дибензиламино)-4-пентиннитрил, 3-[(метил)(циклогексил)амино]-4-пентиннитрил, 3-[(этил)(циклогексил)амино]-4-пентиннитрил, 3-[(метил)(фенил)амино]-4-пентиннитрил, 3-[(этил)(фенил)амино]-4-пентиннитрил, 3-[(метил)(бензил)амино]-4-пентиннитрил, 3-[(этил)(бензил)амино]-4-пентиннитрил, 3-(диметиламино)-5-гексиннитрил, 3-(диэтиламино)-5-гексиннитрил, 3-(ди-н-пропиламино)-5-гексиннитрил, 3-(диизопропиламино)-5-гексиннитрил, 3-(ди-н-бутиламино)-5-гексиннитрил, 3-(диизобутиламино)-5-гексиннитрил, 3-(дициклогексиламино)-5-гексиннитрил, 3-(дифениламино)-5-гексиннитрил, 3-(дибензиламино)-5-гексиннитрил, 3-[(метил)(циклогексил)амино]-5-гексиннитрил, 3-[(этил)(циклогексил)амино]-5-гексиннитрил, 3-[(метил)(фенил)амино]-5-гексиннитрил, 3-[(этил)(фенил)амино]-5-гексиннитрил, 3-[(метил)(бензил)амино]-5-гексиннитрил, 3-[(этил)(бензил)амино]-5-гексиннитрил, 3-азиридино-4-пентиннитрил, 3-азетидино-4-пентиннитрил, 3-пирролидино-4-пентиннитрил, 3-пиперидино-4-пентиннитрил, 3-гомопиперидино-4-пентиннитрил, 3-морфолино-4-пентиннитрил, 3-(N-метилпиперазино)-4-пентиннитрил, 3-(N-метилгомопиперазино)-4-пентиннитрил, 3-азиридино-5-гексиннитрил, 3-азетидино-5-гексиннитрил, 3-пирролидино-5-гексиннитрил, 3-пиперидино-5-гексиннитрил, 3-гомопиперидино-5-гексиннитрил, 3-морфолино-5-гексиннитрил, 3-(N-метилпиперазино)-5-гексиннитрил и 3-(N-метилгомопиперазино)-5-гексиннитрил.
Конкретные примеры циклоалканкарбонитрильных соединений, имеющих защищенную аминогруппу, включают 3-[бис(триметилсилил)амино]циклопентанкарбонитрил, 4-[бис(триметилсилил)амино]циклогексанкарбонитрил, 3-(2,2,5,5-тетраметил-1-аза-2,5-дисила-1-циклопентил)пиклопентанкарбонитрил, 4-(2,2,5,5-тетраметил-1-аза-2,5-дисила-1 -циклопентил)пиклогексанкарбонитрил, 3-[(триметилсилил)(метил)амино]циклопентанкарбонитрил, 3-[(триметилсилил)(этил)амино]циклопентанкарбонитрил, 4-[(триметилсилил)(метил)амино]циклогексанкарбонитрил, 4-[(триметилсилил)(этил)амино]циклогексанкарбонитрил, 3-(2,2-диметил-1-аза-2-сила-1-циклопентил)циклопентанкарбонитрил, 4-(2,2-диметил-1-аза-2-сила-1-циклопентил)циклогексанкарбонитрил, 3-(3-диметиламинофенил)циклопропан-1,1,2,2-тетракарбонитрил, 3-(диметиламино)циклопентанкарбонитрил, 3-(диэтиламино)циклопентанкарбонитрил, 3-(ди-н-пропиламино)циклопентанкарбонитрил, 3-(диизопропиламино)циклопентанкарбонитрил, 3-(ди-н-бутиламино)циклопентанкарбонитрил, 3-(диизобутиламино)циклопентанкарбонитрил, 3-(дициклогексиламино)циклопентанкарбонитрчл, 3-(дифениламино)циклопентанкарбонитрил, 3-(дибензиламино)циклопентанкарбонитрил, 3-[(метил)(циклогексил)амино]циклопентанкарбонитрил, 3-[(этил)(циклогексил)амино]циклопентанкарбонитрил, 3-[(метил)(фенил)амино]циклопентанкарбонитрил, 3-[(этил)(фенил)амино]циклопентанкарбонитрил, 3-[(метил)(бензил)амино]циклопентанкарбонитрил, 3-[(этил)(бензил)амино]циклопентанкарбонитрил, 4-(диметиламино)циклогексанкарбонитрил, 4-(диэтиламино)циклогексанкарбонитрил, 4-(ди-н-пропиламино)циклогексанкарбонитрил, 4-(диизопропиламино)циклогексанкарбонитрил, 4-(ди-н-бутиламино)циклогексанкарбонитрил, 4-(диизобутиламино)циклогексанкарбонитрил, 3-(дициклогексиламино)циклогексанкарбонитрил, 4-(дифениламино)циклогексанкарбонитрил, 4-(дибензиламино)циклогексанкарбонитрил, 4-[(метил)(циклогексил)амино]циклогексанкарбонитрил, 4-[(этил)(циклогексил)амино]циклогексанкарбонитрил, 4-[(метил)(фенил)амино]циклогексанкарбонитрил, 4-[(этил)(фенил)амино]циклогексанкарбонитрил, 4-[(метил)(бензил)амино]циклогексанкарбонитрил, 4-[(этил)(бензил)амино]циклогексанкарбонитрил, 4-азиридиноциклопентанкарбонитрил, 3-азетидиноциклопентанкарбонитрил, 3-пирролидиноциклопентанкарбонитрил, 3-пиперидиноциклопентанкарбонитрил, 3-гомопиперидиноциклопентанкарбонитрил, 3-морфолиноциклопентанкарбонитрил, 3-(N-метилпиперазино)циклопентанкарбонитрил, 3-(N-метилгомопиперазино)циклопентанкарбонитрил, 4-азиридиноциклогексанкарбонитрил, 4-азетидиноциклогексанкарбонитрил, 4-пирролидиноциклогексанкарбонитрил, 4-пиперидиноциклогексанкарбонитрил, 4-гомопиперидиноциклогексанкарбонитрил, 4-морфолиноциклогексанкарбонитрил, 4-(N-метилпиперазино)циклогексанкарбонитрил и 4-(N-метилгомопиперазино)циклогексанкарбонитрил.
Конкретные примеры циклоалкенкарбонитрильных соединений, имеющих защищенную аминогруппу, включают 4-[бис(триметилсилил)амино]циклопентен-1-карбонитрил, 4-[бис(триметилсилил)амино]циклогексен-1-карбонитрил, 4-(2,2,5,5-тетраметил-1-аза-2,5-дисила-1-циклопентил)циклопентен-1-карбонитрил, 4-(2,2,5,5-тетраметил-1-аза-2,5-дисила-1-циклопентил)циклогексен-1-карбонитрил, 4-[(триметилсилил)(метил)амино]циклопентен-1-карбонитрил, 4-[(триметилсилил)(этил)амино]циклопентен-1-карбонитрил, 4-[(триметилсилил)(метил)амино]циклогексен-1-карбонитрил, 4-[(триметилсилил)(этил)амино]циклогексен-1-карбонитрил, 4-(2,2-диметил-1-аза-2-сила-1-циклопентил)циклопентен-1-карбонитрил, 4-(2,2-диметил-1-аза-2-сила-1-циклопентил)циклогексен-1-карбонитрил, 4-(диметиламино)циклопентен-1-карбонитрил, 4-(диэтиламино)циклопентен-1-карбонитрил, 4-(ди-н-пропиламино)циклопентен-1-карбонитрил, 4-(диизопропиламино)циклопентен-1-карбонитрил, 4-(ди-н-бутиламино)циклопентен-1-карбонитрил, 4-(диизобутиламино)циклопентен-1-карбонитрил, 4-(дициклогексиламино)циклопентен-1-карбонитрил, 4-(дифениламино)циклопентен-1-карбонитрил, 4-(дибензиламино)циклопентен-1-карбонитрил, 4-[(метил)(циклогексил)амино]циклопентен-1-карбонитрил, 4-[(этил)(циклогексил)амино]циклопентен-1-карбонитрил, 4-[(метил)(фенил)амино]циклопентен-1-карбонитрил, 4-[(этил)(фенил)амино]циклопентен-1-карбонитрил, 4-[(метил)(бензил)амино]циклопентен-1-карбонитрил, 4-[(этил)(бензил)амино]циклопентен-1-карбонитрил, 4-(диметиламино)циклогексен-1-карбонитрил, 4-(диэтиламино)циклогексен-1-карбонитрил, 4-(ди-н-пропиламино)циклогексен-1-карбонитрил, 4-(диизопропиламино)циклогексен-1-карбонитрил, 4-(ди-н-бутиламино)циклогексен-1-карбонитрил, 4-(диизобутиламино)циклогексен-1-карбонитрил, 4-(дициклогексиламино)циклогексен-1-карбонитрил, 4-(дифениламино)циклогексен-1-карбонитрил, 4-(дибензиламино)циклогексен-1-карбонитрил, 4-[(метил)(циклогексил)амино]циклогексен-1-карбонитрил, 4-[(этил)(циклогексил)амино]циклогексен-1-карбонитрил, 4-[(метил)(фенил)амино]циклогексен-1-карбонитрил, 4-[(этил)(фенил)амино]циклогексен-1-карбонитрил, 4-[(метил)(бензил)амино]циклогексен-1-карбонитрил, 4-[(этил)(бензил)амино]циклогексен-1-карбонитрил, 4-азиридиноциклопентен-1-карбонитрил, 4-азетидиноциклопентен-1-карбонитрил, 4-пирролидиноциклопентен-1-карбонитрил, 4-пиперидиноциклопентен-1-карбонитрил, 4-гомопиперидиноциклопентен-1-карбонитрил, 4-морфолиноциклопентен-1-карбонитрил, 4-(N-метилпиперазино)циклопентен-1-карбонитрил, 4-(N-метилгомопиперазино)циклопентен-1-карбонитрил, 4-азиридиноциклогексен-1-карбонитрил, 4-азетидиноциклогексен-1-карбонитрил, 4-пирролидиноциклогексен-1-карбонитрил, 4-пиперидиноциклогексен-1-карбонитрил, 4-гомопиперидиноциклогексен-1-карбонитрил, 4-морфолиноциклогексен-1-карбонитрил, 4-(N-метилпиперазино)циклогексен-1-карбонитрил и 4-(N-метилгомопиперазино)циклогексен-1-карбонитрил.
Конкретные примеры гетероциклических нитрильных соединений, имеющих защищенную аминогруппу, включают 5-[бис(триметилсилил)амино]-2-пиридинкарбонитрил, 5-[бис(триметилсилил)амино]-2-пиримидинкарбонитрил, 5-(2,2,5,5-тетраметил-1-аза-2,5-дисила-1-циклопентил)-2-пиридинкарбонитрил, 5-(2,2,5,5-тетраметил-1-аза-2,5-дисила-1-циклопентил)-2-пиримидинкарбонитрил, 5-[(триметилсилил)(метил)амино]-2-пиридинкарбонитрил, 5-[(триметилсилил)(этил)амино]-2-пиридинкарбонитрил, 5-[(триметилсилил)(метил)амино]-2-пиримидинкарбонитрил, 5-[(триметилсилил)(этил)амино]-2-пиримидинкарбонитрил, 5-(2,2-диметил-1-аза-2-сила-1-циклопентил)-2-пиридинкарбонитрил, 5-(2,2-диметил-1-аза-2-сила-1-циклопентил)-2-пиримидинкарбонитрил, 5-(диметиламино)-2-пиридинкарбонитрил, 3-(диэтиламино)-2-пиридинкарбонитрил, 5-(ди-н-пропиламино)-2-пиридинкарбонитрил, 5-(диизопропиламино)-2-пиридинкарбонитрил, 5-(ди-н-бутиламино)-2-пиридинкарбонитрил, 5-(диизобутиламино)-2-пиридинкарбонитрил, 5-(дициклогексиламино)-2-пиридинкарбонитрил, 5-(дифениламино)-2-пиридинкарбонитрил, 5-(дибензиламино)-2-пиридинкарбонитрил, 5-[(метил)(циклогексил)амино]-2-пиридинкарбонитрил, 5-[(этил)(циклогексил)амино]-2-пиридинкарбонитрил, 5-[(метил)(фенил)амино]-2-пиридинкарбонитрил, 5-[(этил)(фенил)амино]-2-пиридинкарбонитрил, 5-[(метил)(бензил)амино]-2-пиридинкарбонитрил, 5-[(этил)(бензил)амино]-2-пиридинкарбонитрил, 5-(диметиламино)-2-пиримидинкарбонитрил, 5-(диэтиламино)-2-пиримидинкарбонитрил, 5-(ди-н-пропиламино)-2-пиримидинкарбонитрил, 5-(диизопропиламино)-2-пиримидинкарбонитрил, 5-(ди-н-бутиламино)-2-пиримидинкарбонитрил, 5-(диизобутиламино)-2-пиримидинкарбонитрил, 5-(дициклогексиламино)-2-пиримидинкарбонитрил, 5-(дифениламино)-2-пиримидинкарбонитрил, 5-(дибензиламино)-2-пиримидинкарбонитрил, 5-[(метил)(циклогексил)амино]-2-пиримидинкарбонитрил, 5-[(этил)(циклогексил)амино]-2-пиримидинкарбонитрил, 5-[(метил)(фенил)амино]-2-пиримидинкарбонитрил, 5-[(этил)(фенил)амино]-2-пиримидинкарбонитрил, 5-[(метил)(бензил)амино]-2-пиримидинкарбонитрил, 5-[(этил)(бензил)амино]-2-пиримидинкарбонитрил, 5-азиридино-2-пиридинкарбонитрил, 5-азетидино-2-пиридинкарбонитрил, 5-пирролидино-2-пиридинкарбонитрил, 5-пиперидино-2-пиридинкарбонитрил, 5-гомопиперидино-2-пиридинкарбонитрил, 5-морфолино-2-пиридинкарбонитрил, 5-(N-метилпиперазино)-2-пиридинкарбонитрил, 5-(N-метилгомопиперазино)-2-пиридинкарбонитрил, 5-азиридино-2-пиримидинкарбонитрил, 5-азетидино-2-пиримидинкарбонитрил, 5-пирролидино-2-пиримидинкарбонитрил, 5-пиперидино-2-пиримидинкарбонитрил, 5-гомопиперидино-2-пиримидинкарбонитрил, 5-морфолино-2-пиримидинкарбонитрил, 5-(N-метилпиперазино)-2-пиримидинкарбонитрил и 5-(N-метилгомопиперазино)-2-пиримидинкарбонитрил.
В одном или нескольких вариантах осуществления нитрильные соединения, имеющие защищенную аминогруппу, могут быть синтезированы в результате проведения алкилирования или силилирования нитрильного соединения, имеющего первичную аминогруппу (то есть, -NН2) или вторичную аминогруппу, описывающуюся формулой -NH(R), где R представляет собой одновалентную органическую группу, такую как гидрокарбильная или силильная группа. Примеры алкилирующих реагентов включают алкилгалогениды. Примеры силилирующих реагентов включают триалкилсилилгалогениды, 1,2-бис(хлордиметилсилил)этан и триалкилсилилтрифторметансульфонат. Для нейтрализации кислоты, образующейся во время проведения реакции алкилирования или силилирования, может быть использовано основание, такое как триэтиламин.
Количество нитрильного соединения, имеющего защищенную аминогруппу, которое может быть добавлено в полимеризационную смесь для получения функционализованного полимера данного изобретения, может зависеть от различных факторов, в том числе от типа и количества инициатора, использующегося для синтеза реакционно-способного полимера, и желательной степени функционализации. В одном или нескольких вариантах осуществления количество использующегося нитрильного соединения, имеющего защищенную аминогруппу, может быть описано в связи с количеством катиона металла, ассоциированного с инициатором. Например, в случае использования литийорганического инициатора молярное соотношение между нитрильным соединением, имеющим защищенную аминогруппу, и катионом лития может находиться в диапазоне от приблизительно 0,3:1 до приблизительно 2:1, в других вариантах осуществления от приблизительно 0,6:1 до приблизительно 1,5:1, а в еще одних вариантах осуществления от 0,8:1 до приблизительно 1,2:1.
В одном или нескольких вариантах осуществления для получения функционализованного полимера, обладающего заданными свойствами, к полимеризационной смеси в дополнение к нитрильному соединению, имеющему защищенную аминогруппу, также может быть добавлен и софункционализующий агент. Также может быть использована и смесь двух и более софункционализующих агентов. Софункционализующий агент к полимеризационной смеси может быть добавлен до введения, совместно с введением или после введения нитрильного соединения. В одном или нескольких вариантах осуществления софункционализующий агент к полимеризационной смеси добавляют по истечении по меньшей мере 5 минут, в других вариантах осуществления по меньшей мере 10 минут, а в других вариантах осуществления по меньшей мере 30 минут, после введения нитрильного соединения.
В одном или нескольких вариантах осуществления софункционализующие агенты включают соединения или реагенты, которые могут вступать в реакцию с реакционно-способным полимером, полученным по настоящему изобретению, и, таким образом, приводить к получению полимера, имеющего функциональную группу, отличающуюся от растущей цепи, которая еще не вступила в реакцию с софункционализующим агентом. Функциональная группа может быть реакционно-способной или взаимодействующей с другими полимерными цепями (растущими и/или нерастущими) или с другими компонентами, такими как армирующие наполнители (например, технический углерод), которые могут быть скомбинированы с полимером. В одном или нескольких вариантах осуществления реакция между софункционализующим агентом и реакционно-способным полимером протекает по реакции присоединения или замещения.
Подходящие для использования софункционализующие агенты могут включать соединения, которые просто обеспечивают получение функциональной группы на конце полимерной цепи без соединения двух или более полимерных цепей друг с другом, а также соединения, которые могут обеспечивать сочетание или соединение двух или более полимерных цепей друг с другом благодаря функциональному соединительному звену с образованием одной макромолекулы. Последний тип софункционализующих агентов также может быть назван и сшивающими агентами.
В одном или нескольких вариантах осуществления софункционализующие агенты включают соединения, которые добавляют или вводят в полимерную цепь гетероатом. В конкретных вариантах осуществления софункционализующие агенты включают те соединения, которые вводят в полимерную цепь функциональную группу с образованием функционализованного полимера, который уменьшает потери на гистерезис при 50°С для наполненных техническим углеродом зулканизатов, полученных из функционализованного полимера, в сопоставлении с соответствующими характеристиками аналогичных наполненных техническим углеродом вулканизатов, полученных из нефункционализованного полимера. В одном или нескольких вариантах осуществления данное уменьшение потерь на гистерезис составляет по меньшей мере 5%, в других вариантах осуществления по меньшей мере 10%, а в еще одних вариантах осуществления по меньшей мере 15%.
В одном или нескольких вариантах осуществления подходящие для использования софункционализующие агенты включают те соединения, которые имеют группы, способные вступать в реакцию с реакционно-способными полимерами, полученными в соответствии с настоящим изобретением. Примеры софункционализующих агентов включают кетоны, хиноны, альдегиды, амиды, сложные эфиры, изоцианаты, изотиоцианаты, эпоксиды, имины, аминокетоны, аминотиокетоны и ангидриды кислот. Примеры данных соединений описываются в патентах США №№4906706, 4990573, 5064910, 5567784, 5844050, 6838526, 6977281 и 6992147; патентных публикациях США №№2006/0004131 A1, 2006/0025539 A1, 2006/0030677 А1 и 2004/0147694 A1; японских патентных заявках №№05-051406А, 05-059103А, 10-306113А и 11-035633А; которые посредством ссылки включаются в настоящий документ. Другие примеры софункционализующих агентов включают азиновые соединения, описывающиеся в документе U.S. Serial No. 11/640,711, гидробензамидные соединения, описывающиеся в документе U.S. Serial No. 11/710,713, нитросоединения, описывающиеся в документе U.S. Serial No. 11/710,845, и защищенные оксимы, описывающиеся в документе U.S. Serial No. 60/875,484, все из которых посредством ссылки включаются в настоящий документ.
В конкретных вариантах осуществления использующиеся софункционализующие агенты могут представлять собой галогениды металлов, галогениды металлоидов, алкоксисиланы, карбоксилаты металлов, карбоксилаты гидрокарбилметаллов, комплексы сложный эфир-карбоксилат гидрокарбилметаллов и алкоксиды металлов.
Примеры галогенидов металлов включают тетрахлорид олова, тетрабромид олова, тетраиодид олова, трихлорид н-бутилолова, трихлорид фенилолова, дихлорид ди-н-бутилолова, дихлорид дифенилолова, хлорид три-н-бутилолова, хлорид трифенилолова, тетрахлорид германия, тетрабромид германия, тетраиодид германия, трихлорид н-бутилгермания, дихлорид ди-н-бутилгермания и хлорид три-н-бутилгермания.
Примеры галогенидов металлоидов включают тетрахлорид кремния, тетрабромид кремния, тетраиодид кремния, метилтрихлорсилан, фенилтрихлорсилан, диметилдихлорсилан, дифенилдихлорсилан, трихлорид бора, трибромид бора, трииодид бора, трихлорид фосфора, трибромид фосфора и трииодид фосфора.
В одном или нескольких вариантах осуществления алкоксисиланы могут включать по меньшей мере одну группу, выбираемую из группы, состоящей из эпоксигруппы и изоцианатной группы.
Примеры алкоксисилановых соединений, имеющих эпоксигруппу, включают (3-глицидилоксипропил)триметоксисилан, (3-глицидилоксипропил)триэтоксисилан, (3-глицидилоксипропил)трифеноксисилан, (3-глицидилоксипропил)метилдиметоксисилан, (3-глицидилоксипропил)метилдиэтоксисилан, (3-глицидилоксипропил)метилдифеноксисилан, [2-(3,4-эпоксициклогексил)этил]триметоксисилан и [2-(3,4-эпоксициклогексил)этил] триэтоксисилан.
Примеры алкоксисилановых соединений, имеющих изоцианатную группу, включают (3-изоцианатопропил)триметоксисилан, (3-изоцианатопропил)триэтоксисилан, (3-изоцианатопропил)трифеноксисилан, (3-изоцианатопропил)метилдиметоксисилан, (3-изоцианатопропил)метилдиэтоксисилан, (3-изоцианатопропил)метилдифеноксисилан и (изоцианатометил)метилдиметоксисилан.
Примеры карбоксилатов металлов включают тетраацетат олова, бис(2-этилгексаноат) олова и бис(неодеканоат) олова.
Примеры карбоксилатов гидрокарбилметаллов включают 2-этилгексаноат трифенилолова, 2-этилгексаноат три-н-бутилолова, неодеканоат три-н-бутилолова, 2-этилгексаноат триизобутилолова, бис(2-этилгексаноат) дифенилолова, бис(2-этилгексаноат) ди-н-бутилолова, бис(неодеканоат) ди-н-бутилолова, трис(2-этилгексаноат) фенилолова и трис(2-этилгексаноат) н-бутилолова.
Примеры комплексов сложный эфир-карбоксилат гидрокарбилметалла включают бис(н-октилмалеат) ди-н-бутилолова, бис(н-октилмалеат) ди-н-октилолова, бис(н-октилмалеат) дифенилолова, бис(2-этилгексилмалеат) ди-н-бутилолова, бис(2-этилгексилмалеат) ди-н-октилолова и бис(2-этилгексилмалеат) дифенилолова.
Примеры алкоксидов металлов включают диметоксиолово, диэтоксиолово, тетраэтоксиолово, тетра-н-пропоксиолово, тетраизопропоксиолово, тетра-н-бутоксиолово, тетраизобутоксиолово, тетра-трет-бутоксиолово и тетрафеноксиолово.
Количество софункционализующего агента, которое может быть добавлено в полимеризационную смесь, может зависеть от различных факторов, в том числе от типа и количества инициатора, использующегося для синтеза реакционно-способного полимера, и желательной степени функционализации. В одном или нескольких вариантах осуществления количество использующегося нитрильного соединения, имеющего защищенную аминогруппу, может быть описано в связи с количеством катиона металла, ассоциированного с инициатором. Например, в случае использования литийорганического инициатора молярное соотношение между нитрилом, имеющим защищенную аминогруппу, и катионом лития может находиться в диапазоне от приблизительно 0,3:1 до приблизительно 2:1, в других вариантах осуществления от приблизительно 0,6:1 до приблизительно 1,5:1, а в еще одних вариантах осуществления от 0,8:1 до приблизительно 1,2:1.
Количество использующегося софункционализующего агента также может быть описано в связи с нитрильным соединением, имеющим защищенную аминогруппу. В одном или нескольких вариантах осуществления молярное соотношение между софункционализующим агентом и нитрильным соединением может находиться в диапазоне от приблизительно 0,05:1 до приблизительно 1:1, в других вариантах осуществления от приблизительно 0,1:1 до приблизительно 0,8:1, а в еще одних вариантах осуществления от приблизительно 0,2:1 до приблизительно 0,6:1.
В одном или нескольких вариантах осуществления нитрильное соединение, имеющее защищенную аминогруппу, (и необязательно софункционализующий агент) может быть введено в полимеризационную смесь в то место (например, в емкость), в котором проводили полимеризацию. В других вариантах осуществления нитрильное соединение может быть введено в полимеризационную смесь в другое место, которое отличается от того, в котором проводили полимеризацию. Например, нитрильное соединение может быть введено в полимеризационную смесь в емкости, расположенные дальше по ходу технологического потока, в том числе реакторы или резервуары, расположенные дальше по ходу технологического потока, реакторы или смесители, встроенные в технологическую линию, экструдеры или дегазаторы.
В одном или нескольких вариантах осуществления нитрильное соединение, имеющее защищенную аминогруппу, (и необязательно софункционализующий агент) может быть введено в реакцию с реакционно-способным полимером после достижения желательной степени превращения мономера, но до гашения активных центров полимеризационной смеси агентом гашения активных центров. В одном или нескольких вариантах осуществления реакция между нитрильным соединением и реакционно-способным полимером может протекать в течение 30 минут, в других вариантах осуществления в течение 5 минут, а в еще одних вариантах осуществления в течение одной минуты после достижения пиковой температуры полимеризации. В одном или нескольких вариантах осуществления реакция между нитрильным соединением и реакционно-способным полимером может протекать сразу после достижения пиковой температуры полимеризации. В других вариантах осуществления реакция между нитрильным соединением и реакционно-способным полимером может протекать после хранения реакционно-способного полимера. В одном или нескольких вариантах осуществления хранение реакционно-способного полимера проводят при комнатной температуре или при температуре, более низкой, чем комнатная, в инертной атмосфере. В одном или нескольких вариантах осуществления реакция между нитрильным соединением и реакционно-способным полимером может протекать при температуре в диапазоне от приблизительно 10°С до приблизительно 150°С, а в других вариантах осуществления от приблизительно 20°С до приблизительно 100°С. Время, необходимое для завершения реакции между нитрильным соединением и реакционно-способным полимером, зависит от различных факторов, таких как тип и количество катализатора или инициатора, использующихся для получения реакционно-способного полимера, тип и количество нитрильного соединения, а также температура, при которой проводят реакцию функционализации. В одном или нескольких вариантах осуществления реакция между нитрильным соединением и реакционно-способным полимером может быть проведена в течение периода времени продолжительностью приблизительно от 10 до 60 минут.
В одном или нескольких вариантах осуществления после проведения или завершения реакции между реакционно-способным полимером и нитрильным соединением, имеющим защищенную аминогруппу, (и, необязательно, софункционализующим агентом) в полимеризационную смесь может быть добавлен агент гашения активных центров для того, чтобы протонировать продукт реакции между реакционно-способным полимером и нитрильным соединением, дезактивировать какие-либо остаточные цепи реакционно-способного полимера и/или дезактивировать инициатор. Агент гашения активных центров может включать протонное соединение, которое включает нижеследующее, но не ограничивается только этим: спирт, карбоновая кислота, неорганическая кислота, вода или их смесь. Совместно с добавлением, до или после добавления агента гашения активных центров может быть добавлен антиоксидант, такой как 2,6-ди-трет-бутил-4-метилфенол. Количество использующегося антиоксиданта может находиться в диапазоне от 0,2% до 1% в расчете на массу полимерного продукта. В дополнение к этому, полимерный продукт может быть наполнен маслом в результате добавления масла к полимеру, который может иметь форму полимерного клея или полимера, растворенного или суспендированного в мономере. Практика настоящего изобретения не ограничивает количество масла, которое может быть добавлено, и поэтому могут быть добавлены обычные количества (например, 5-50 ч./сто ч. каучука). Подходящие для использования масла или наполнители, которые могут быть использованы, включают нижеследующие, но не ограничиваются только этими: ароматические масла, парафиновые масла, нафтеновые масла, растительные масла, отличные от касторовых масел, масла, характеризующиеся низким уровнем содержания ПАС, в том числе марки MES, TDAE, SRAE, и тяжелые нафтеновые масла.
После гашения в полимеризационной смеси активных центров может быть проведено извлечение различных составных частей полимеризационной смеси. В одном или нескольких вариантах осуществления из полимеризационной смеси может быть извлечен не вступивший в реакцию мономер. Например, мономер из полимеризационной смеси может быть отогнан при использовании методик, известных на современном уровне техники. В одном или нескольких вариантах осуществления для удаления из полимеризпционной смеси мономера может быть использован дегазатор. После удаления мономера из полимеризационной смеси мономер может быть отправлен на очистку, хранение и/или на рецикл обратно в технологический процесс полимеризации.
Полимерный продукт из полимеризационной смеси может быть извлечен при использовании методик, известных на современном уровне техники. В одном или нескольких вариантах осуществления могут быть использованы методики удаления растворителя и высушивания. Например, полимер может быть извлечен в результате перепускания полимеризационной смеси через обогреваемый червячный аппарат, такой как экструдер, удаляющий растворитель, в котором летучие вещества удаляют за счет выпаривания при надлежащих температурах (например, в диапазоне от приблизительно 100°С до приблизительно 170°С) и при атмосферном давлении или давлении, меньшем, чем атмосферное. Данную обработку используют для удаления не вступившего в реакцию мономера, а также какого-либо низкокипящего растворителя. В альтернативном варианте, полимер также может быть извлечен в результате проведения удаления из полимеризационной смеси растворителя под действием водяного пара с последующим высушиванием получающейся в результате полимерной крошки в канальной сушилке с обогревом горячим воздухом. Полимер также может быть извлечен и в результате непосредственного высушивания полимеризационной смеси на барабанной сушилке.
Несмотря на то, что, как представляется, реакционно-способный полимер и нитрильное соединение, имеющее защищенную аминогруппу, (и необязательно софункционализующий агент) вступают в реакцию с образованием нового функционализованного полимера, который может быть протонирован или дополнительно модифицирован, точная химическая структура функционализованного полимера, полученного в каждом варианте осуществления, не является известной с какой-либо большой степенью достоверности, в частности, не вполне ясно, как структура соотносится с остатком, введенным в концевую группу полимерной цепи нитрильным соединением и необязательно софункционализующим агентом. Действительно, структура функционализованного полимера предположительно может зависеть от различных факторов, таких как условия, использующиеся для получения реакционно-способного полимера, (например, тип и количество инициатора) и условия, использующиеся для проведения реакции между нитрильным соединением (и необязательно софункционализующим агентом) и реакционно-способным полимером, (например, типы и количества нитрильного соединения и софункционализующего агента).
В одном или нескольких вариантах осуществления один из продуктов, представляющих собой результат проведения реакции между реакционно-способным полимером и нитрильным соединением, имеющим защищенную аминогруппу, в частности, после проведения реакции с агентом гашения активных центров, может быть функционализованный полимер, имеющий защищенную аминогруппу, который описывается формулой VII:

где π представляет собой полимерную цепь полидиена или сополимера сопряженного диена и сомономера, характеризующуюся средним или низким уровнем содержания цис-1,4-звеньев, R1 представляет собой двухвалентную органическую группу, а каждый из R2 и R3 независимо представляет собой одновалентную органическую группу или гидролизуемую группу, или R2 и R3 соединяются с образованием двухвалентной органической группы, при том условии, что R1 представляет собой ациклическую двухвалентную органическую группу, гетероциклическую двухвалентную органическую группу, неароматическую циклическую двухвалентную органическую группу, которая лишена гетероатомов, или двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, с условием, что если R1 представляет собой двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, то защищенная аминогруппа (то есть, группа -N(R2)(R3) в формуле VII) не должна быть непосредственно присоединена к ароматическому кольцу.
Как представляется, после оказания воздействия водой, влагой или материалами, содержащими воду или влагу, функционализованный полимер, описывающийся формулой VII, может подвергаться реакции гидролиза, которая необязательно может быть катализирована при использовании кислоты, с образованием функционализованного полимера, имеющего аминогруппу, который описывается формулой VIII:

где π представляет собой полимерную цепь полидиена или сополимера сопряженного диена и сомономера, характеризующуюся средним или низким уровнем содержания цис-1,4-звеньев, R1 представляет собой двухвалентную органическую группу, а каждый из R12 и R13 независимо представляет собой одновалентную органическую группу или атом водорода, или R12 и R13 соединяются с образованием двухвалентной органической группы, при том условии, что R1 представляет собой ациклическую двухвалентную органическую группу, гетероциклическую двухвалентную органическую группу, неароматическую циклическую двухвалентную органическую группу, которая лишена гетероатомов, или двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, при условии, что если R1 представляет собой двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, то аминогруппа (то есть, группа -N(R12)(R13) в формуле VIII) не должна быть непосредственно присоединена к ароматическому кольцу.
В одном или нескольких вариантах осуществления функционализованные полимеры, полученные в соответствии с настоящим изобретением, могут содержать ненасыщенность. В этих или других вариантах осуществления функционализованные полимеры являются вулканизуемыми. В одном или нескольких вариантах осуществления функционализованные полимеры могут характеризоваться температурой стеклования (Tg) меньше 0°С, в других вариантах осуществления меньше -20°С, а в еще одних вариантах осуществления меньше -30°С. В одном варианте осуществления данные полимеры могут иметь одну температуру стеклования. В конкретных вариантах осуществления полимеры могут быть гидрированными или частично гидрированными.
Среднечисленная молекулярная масса (Мn) функционализованных полимеров, полученных в соответствии с данным изобретением, может находиться в диапазоне от приблизительно 1000 до приблизительно 1000000, в других вариантах осуществления от приблизительно 5000 до приблизительно 1000000, в других вариантах осуществления от приблизительно 50000 до приблизительно 500000, а в других вариантах осуществления от приблизительно 100000 до приблизительно 300000, как определяют с помощью гельпроникающей хроматографии (ГПХ), откалиброванной при использовании полистирольных стандартов и констант Марка-Хувинка для рассматриваемого полимера. Молекулярно-массовое распределение или полидисперсность (Mw/Mn) полимеров может находиться в диапазоне от приблизительно 1,0 до приблизительно 3,0, а в других вариантах осуществления от приблизительно 1,1 до приблизительно 2,0.
В одном или нескольких вариантах осуществления функционализованные полимеры по настоящему изобретению могут представлять собой полидиены или сополимеры сопряженного диена и сомономера, характеризующиеся средними или низкими уровнями содержания цис-1,4-звеньев. Такие полимеры характеризуются уровнем содержания цис-1,4-звеньев в диапазоне от приблизительно 10% до 60%, в других вариантах осуществления от приблизительно 15% до 55%, а в еще одних вариантах осуществления от приблизительно 20% до приблизительно 50%. Эти полимеры также могут характеризоваться уровнем содержания 1,2-звеньев в диапазоне от приблизительно 10% до приблизительно 90%, в других вариантах осуществления от приблизительно 10% до приблизительно 60%, в других вариантах осуществления от приблизительно 15% до приблизительно 50%, а в еще одних вариантах осуществления от приблизительно 20% до приблизительно 45%. В конкретных вариантах осуществления, в которых полимеры получают с использованием функционального анионного инициатора, голова полимерной цепи имеет функциональную группу, которая представляет собой остаток функционального инициатора.
В одном или нескольких вариантах осуществления функционализованный полимер по настоящему изобретению представляет собой полимер, выбираемый из группы, состоящей из полибутадиена, полиизопрена, сополимера стирола и бутадиена, сополимера стирола, бутадиена и изопрена, сополимера изопрена и стирола и сополимера бутадиена и изопрена.
В конкретных вариантах осуществления функционализованные полимеры по настоящему изобретению представляют собой сополимеры 1,3-бутадиена, стирола и необязательно изопрена. Данный сополимер может включать статистические сополимеры и блок-сополимеры.
Функционализованные полимеры данного изобретения выгодным образом могут обеспечить получение каучуковых композиций, которые демонстрируют пониженный гистерезис. Функционализованные полимеры являются в особенности хорошо подходящими для использования при получении каучуковых композиций, которые могут быть использованы при изготовлении компонентов покрышки. Методики составления каучуковых смесей и добавки, использующиеся в них, в общем случае описываются в публикации The Compounding and Vulcanization of Rubber, in Rubber Technology (2nd Ed. 1973).
Каучуковые композиции могут быть получены при использовании функционализованных полимеров по отдельности или совместно с другими эластомерами (то есть, полимерами, которые могут быть вулканизованы для получения композиций, обладающих свойствами каучука или эластомера). Другие эластомеры, которые могут быть использованы, включают природные и синтетические каучуки. Синтетические каучуки обычно производят в результате проведения полимеризации сопряженных диеновых мономеров, сополимеризации сопряженных диеновых мономеров с другими мономерами, такими как винилзамещенные ароматические мономеры, или сополимеризации этилена совместно с одним или несколькими α-олефинами и необязательно одним или несколькими диеновыми мономерами.
Примеры эластомеров включают натуральный каучук, синтетический полиизопрен, полибутадиен, сополимер изобутилена и изопрена, неопрен, сополимер этилена и пропилена, сополимер стирола и бутадиена, сополимер стирола и изопрена, сополимер стирола, изопрена и бутадиена, сополимер изопрена и бутадиена, сополимер этилена, пропилена и диена, полисульфидный каучук, акриловый каучук, уретановый каучук, силиконовый каучук, эпихлоргидриновый каучук и их смеси. Данные эластомеры могут включать мириады макромолекулярных структур, в том числе линейных, разветвленных и звездообразных структур.
Каучуковые композиции могут включать наполнители, такие как неорганические и органические наполнители. Примеры органических наполнителей включают технический углерод и крахмал. Примеры неорганических наполнителей включают диоксид кремния, гидроксид алюминия, гидроксид магния, слюду, тальк (гидратированный силикат магния) и глины (гидратированные силикаты алюминия). Наиболее часто встречающимися наполнителями, использующимися при изготовлении покрышек, являются разновидности технического углерода и диоксида кремния. В определенных вариантах осуществления выгодным образом может быть использована смесь различных наполнителей.
В одном или нескольких вариантах осуществления разновидности технического углерода включают печные сажи, канальные газовые сажи и ламповые сажи. Более конкретные примеры разновидностей технического углерода включают сверхзизносостойкие печные сажи, износостойкие печные сажи, высокоизносостойкие печные сажи, быстрошприцуемые печные сажи, высокодисперсные печные сажи, полуусиливающие печные сажи, среднеобрабатываемые канальные газовые сажи, труднообрабатываемые канальные газовые сажи, проводящие канальные газовые сажи и ацетиленовые сажи.
В некоторых вариантах осуществления разновидности технического углерода могут характеризоваться площадью удельной поверхности (EMSA), равной по меньшей мере 20 м2/г, а в других вариантах осуществления - по меньшей мере 35 м2/г; значения площади удельной поверхности могут быть определены методом ASTM D-1765 с использованием методики с применением бромида цетилтриметиламмония (БЦТА). Разновидности технического углерода могут иметь гранулированную форму или негранулированную хлопьевидную форму. Предпочтительная форма технического углерода может зависеть от типа смесительного оборудования, использующегося для перемешивания каучуковой смеси.
Количество технического углерода, использующееся в каучуковых композициях, может доходить вплоть до приблизительно 50 массовых частей в расчете на 100 массовых частей каучука (ч./сто ч. каучука), при этом обычное количество находится в диапазоне от приблизительно 5 до приблизительно 40 ч./сто ч. каучука.
Некоторые коммерчески доступные разновидности диоксида кремния, которые могут быть использованы, включают марки Hi-Sil™ 215, Hi-Sil™ 233 и Hi-Sil™ 190 (PPG Industries, Inc.; Питтсбург, Пенсильвания). Другие поставщики коммерчески доступного диоксида кремния включают компании Grace Davison (Балтимор, Мэриленд), Degussa Corp. (Парсиппани, Нью-Джерси), Rhodia Silica Systems (Кренбери, Нью-Джерси) и J.М. Huber Corp. (Эдисон, Нью-Джерси).
В одном или нескольких вариантах осуществления разновидности диоксида кремния могут быть охарактеризованы их площадями удельной поверхности, которые представляют собой меру их армирующих свойств. Признанным методом определения площади удельной поверхности является метод Брунауэра, Эммета и Теллера («БЭТ») (описанный в публикации J. Am. Chem. Soc., vol.60, р.309 et seq.). Определенная методом БЭТ площадь удельной поверхности диоксида кремния в общем случае является меньшей чем 450 м2/г. Подходящие для использования диапазоны площади удельной поверхности включают диапазоны от приблизительно 32 до приблизительно 400 м2/г, от приблизительно 100 до приблизительно 250 м2/г и от приблизительно 150 до приблизительно 220 м2/г.
Значения рН разновидностей диоксида кремния в общем случае находится в диапазоне от приблизительно 5 до приблизительно 7 или несколько более 7 или в других вариантах осуществления от приблизительно 5,5 до приблизительно 6,8.
В одном или нескольких вариантах осуществления, в которых в качестве наполнителя используют диоксид кремния (индивидуально или в комбинации с другими наполнителями), для улучшения взаимодействия диоксида кремния с эластомерами к каучуковым композициям во время перемешивания могут быть добавлены аппретирующий агент и/или экранирующий агент. Подходящие для использования аппретирующие агенты и экранирующие агенты описываются в патентах США №№3842111, 3873489, 3978103, 3997581, 4002594, 5580919, 5583245, 5663396, 5674932, 5684171, 5684172, 5696197, 6608145, 6667362, 6579949, 6590017, 6525118, 6342552 и 6683135, которые посредством ссылки включаются в настоящий документ.
Количество диоксида кремния, использующееся в каучуковых композициях, может находиться в диапазоне от приблизительно 1 до приблизительно 100 ч./сто ч. каучука или в других вариантах осуществления от приблизительно 5 до приблизительно 80 ч./сто ч. каучука. Подходящий для использования верхний диапазон ограничивается высокой вязкостью, придаваемой диоксидами кремния. В случае использования диоксида кремния совместно с техническим углеродом количество диоксида кремния может быть уменьшено до всего лишь приблизительно 1 ч./сто ч. каучука; по мере уменьшения количества диоксида кремния могут быть использованы все меньшие количества аппретирующих агентов и экранирующих агентов. В общем случае количества аппретирующих агентов и экранирующих агентов находятся в диапазоне от приблизительно 4% до приблизительно 20% в расчете на массу использующегося диоксида кремния.
Может быть использовано множество отвердителей каучуков (также называемых вулканизаторами), в том числе отверждающие системы на основе серы или пероксида. Отвердители описываются в публикациях Kirk-Othmer, Encyclopedia of Chemical Technology, Vol.20, pgs.365-468 (3rd Ed. 1982), в частности, Vulcanization Agents and Auxiliary Materials, pgs.390-402, и A.Y. Coran, Vulcanization, Encyclopedia of Polymer Science and Engineering (2nd Ed. 1989), которые посредством ссылки включаются в настоящий документ. Вулканизаторы могут быть использованы индивидуально или в комбинации.
В каучуковые композиции также могут быть добавлены и другие ингредиенты, которые обычно используют при составлении каучуковых смесей. Они включают ускорители, активаторы ускорителей, масла, пластификаторы, воска, ингибиторы подвулканизации, технологические добавки, оксид цинка, смолы, повышающие клейкость, армирующие смолы, жирные кислоты, такие как стеариновая кислота, пептизаторы и противостарители, такие как антиоксиданты и противоозоностарители. В конкретных вариантах осуществления используемые масла включают те, которые обычно используют в качестве масел для наполнения, которые описывались выше.
Все ингредиенты каучуковых композиций могут быть перемешаны при использовании стандартного смесительного оборудования, такого как смесители Banbury или Brabender, экструдеры, замесочные машины и двухвалковые вальцы. В одном или нескольких вариантах осуществления ингредиенты перемешивают на двух и более стадиях. На первой стадии (зачастую называемой стадией перемешивания маточной смеси) получают так называемую маточную смесь, которая обычно включает каучуковый компонент и наполнитель. Для предотвращения преждевременной вулканизации (также известной под наименованием подвулканизации) из маточной смеси могут быть исключены вулканизаторы. Маточная смесь может быть перемешана при начальной температуре в диапазоне от приблизительно 25°С до приблизительно 125°С с температурой выпуска в диапазоне от приблизительно 135°С до приблизительно 180°С. После получения маточной смеси в маточную смесь могут быть введены и примешаны вулканизаторы на стадии конечного перемешивания, которую обычно проводят при относительно низких температурах для уменьшения возможностей прохождения преждевременной вулканизации. Необязательно между стадией перемешивания маточной смеси и стадией конечного перемешивания могут осуществляться стадии дополнительного перемешивания, иногда называемые перевальцеваниями. В случае включения в каучуковую композицию в качестве наполнителя диоксида кремния зачастую используют одну или несколько стадий перевальцевания. Во время данных перевальцеваний могут быть добавлены различные ингредиенты, в том числе функционализованные полимеры по настоящему изобретению.
Методики и условия перемешивания, в частности, применимые для рецептур покрышек, наполненных диоксидом кремния, описываются в патентах США №№5227425, 5719207 и 5717022, а также в европейском патенте №890606, все из которых посредством ссылки включаются в настоящий документ. В одном варианте осуществления первоначальную маточную смесь получают в результате включения функционализованного полимера по настоящему изобретению и диоксида кремния по существу в отсутствие аппретирующих агентов и экранирующих агентов.
Каучуковые композиции, полученные из функционализованных полимеров по настоящему изобретению, в особенности хорошо подходят для использования при изготовлении компонентов покрышки, таких как протекторы, подпротекторы, боковины, наружные слои каркаса покрышки, шнур для заполнения закраины и тому подобное. Предпочтительно функциональные полимеры данного изобретения используют в рецептурах протектора и боковины. В одном или нескольких вариантах осуществления данные рецептуры протектора или боковины могут включать от приблизительно 10% до приблизительно 100% (масс.), в других вариантах осуществления от приблизительно 35% до приблизительно 90% (масс.), а в еще одних вариантах осуществления от приблизительно 50% до приблизительно 80% (масс.) функционализованного полимера в расчете на совокупную массу каучука в рецептуре.
В случае использования каучуковых композиций при изготовлении покрышек данные композиции могут быть переработаны в компоненты покрышки в соответствии с обычными методиками изготовления покрышки, включающими стандартные методики профилирования, формования и отверждения каучука. Обычно вулканизацию осуществляют в результате нагревания вулканизуемой композиции в форме; например, она может быть нагрета до температуры в диапазоне от приблизительно 140°С до приблизительно 180°С. Отвержденные или сшитые каучуковые композиции могут быть названы вулканизатами, которые в общем случае включают трехмерные полимерные сетки, которые являются термоотвержденными. Другие ингредиенты, такие как наполнители и технологические добавки, могут быть равномерно диспергированы по всему объему сшитой сетки. Пневматические покрышки могут быть изготовлены так, как это обсуждается в патентах США №№5866171, 5876527, 5931211 и 5971046, которые посредством ссылки включаются в настоящий документ.
Для демонстрации осуществления настоящего изобретения на практике были получены и подвергнуты испытаниям следующие далее примеры. Однако, примеры не должны рассматриваться в качестве ограничения объема изобретения. Для определения изобретения будет использоваться формула изобретения.
ПРИМЕРЫ
Пример 1. Синтез 4-[бис(триметилсилил)аминометил]бензонитрила (4-BTMSAMBZN)
В круглодонной реакционной колбе, охлаждаемой водяной баней со льдом, перемешивали приблизительно 5,20 г гидрохлорида 4-(аминометил)бензонитрила, 10,30 г триэтиламина и 10 мл толуола. К данной смеси покапельно добавляли раствор 15,1 г триметилсилилтрифторметансульфоната в 50 мл толуола. Получающуюся в результате смесь перемешивали при комнатной температуре в течение 3 дней, получая двухфазную смесь. Верхний слой переносили в другую колбу, а нижний слой экстрагировали, используя 40 мл толуола. Объединенный толуольный раствор упаривали в вакууме. Остаток экстрагировали, используя 100 мл гексана, и гексановый слой упаривали в вакууме, получая 4-[бис(триметилсилил)аминометил]бензонитрил (4-BTMSAMBZN) в виде белого твердого вещества (8,12 г, выход 95%). Данные анализа продукта методом 1Н ЯМР (С6D6, 25°С, при соотнесении сигнала с тетраметилсилановым стандартом) представляют собой нижеследующее: δ 7,00 (дублет, 2 Н, ароматические протоны), 6,83 (дублет, 2 Н, ароматические протоны), 3,72 (синглет, 2 Н, протоны СН2), - 0,06 (синглет, 18 Н, протоны Si-СН3). Исходя из данных метода 1Н ЯМР, структуру продукта определили следующим образом:

Пример 2. Синтез 5-[бис(триметилсилил)амино]-2-пиридинкарбонитрила (BTMSAPyCN)
В круглодонной реакционной колбе, охлаждаемой водяной баней со льдом, перемешивали приблизительно 6,17 г 5-амино-2-пиридинкарбонитрила, 11,54 г триэтиламина и 10 мл толуола. К данной смеси покапельно добавляли раствор 25,34 г триметилсилилтрифторметансульфоната в 70 мл толуола. Получающуюся в результате смесь нагревали до кипячения в течение 2,5 часов, а после этого упаривали в вакууме. Остаток экстрагировали, используя 100 мл гексана. Гексановый слой два раза промывали насыщенным водным раствором бикарбоната натрия (80 мл каждый раз), высушивали, используя безводный сульфат натрия, и упаривали в вакууме, получая 5-[бис(триметилсилил)амино]-2-пиридинкарбонитрил (BTMSAPyCN) в виде зеленого масла (8,67 г, выход 64%). Данные анализа продукта методом 1Н ЯМР (C6D6, 25°С, при соотнесении сигнала с тетраметилсилановым стандартом) представляют собой нижеследующее: δ 8,07 (дублет дублетов, 1 Н, ароматический протон), 6,70 (дублет дублетов, 1 Н, ароматический протон), 6,45 (дублет дублетов, 1 Н, ароматический протон), - 0,16 (синглет, 18 Н, протоны Si-СН3). Исходя из данных метода 1Н ЯМР, структуру продукта определили следующим образом:

Пример 3. Синтез 3-[бис(триметилсилил)амино]пропионитрила (3-BTMSAPN)
В круглодонной реакционной колбе, охлаждаемой водяной баней со льдом, перемешивали приблизительно 5,04 г 3-аминопропионитрила, 16,01 г триэтиламина и 10 мл толуола. К данной смеси покапельно добавляли раствор 35,16 г триметилсилилтрифторметансульфоната в 50 мл толуола. Получающуюся в результате смесь перемешивали при комнатной температуре в течение 2 дней, получая двухфазную смесь. Верхний слой переносили в другую колбу, а нижний слой экстрагировали, используя 50 мл толуола. Объединенный толуольный раствор упаривали в вакууме. Остаток экстрагировали, используя 100 мл гексана, и гексановый слой упаривали в вакууме, получая 3-[бис(триметилсилил)амино]пропионитрил (3-BTMSAPN) в виде белого твердого вещества (13,86 г, выход 90%). Данные анализа продукта методом 1Н ЯМР (С6D6, 25°С, при соотнесении сигнала с тетраметилсилановым стандартом) представляют собой нижеследующее: 5 2,65 (триплет, 2 Н, протоны CH2), 1,59 (триплет, 2Н, протоны СН2), - 0,05 (синглет, 18 Н, протоны Si-СН3). Исходя из данных метода 1Н ЯМР, структуру продукта определили следующим образом:

Пример 4. Синтез 3-[(триметилсилил)(метил)амино]пропионитрила (3-TMSMAPN)
К холодному раствору 3-(метиламино)пропионитрила (23,4 мл) в дихлорметане (350 мл) добавляли триэтиламин (38,3 мл) и триметилсилилхлорид (33,2 мл). Смесь перемешивали при комнатной температуре в течение 18 часов. Полученную соль триэтиламина и хлористо-водородной кислоты отфильтровывали и промывали, используя 40 мл гексана. Объединенный фильтрат упаривали с использованием ротационного испарителя. Остаточный сироп перегоняли под вакуумом, получая 3-[(триметилсилил)(метил)амино]пропионитрил (3-TMSMAPN) в виде желтой жидкости. Данные анализа продукта методом 1Н ЯМР (CDCl3, 25°C, при соотнесении сигнала с тетраметилсилановым стандартом) представляют собой нижеследующее: δ 3,07 (триплет, 2 Н, протоны N-CH2), 2,48 (синглет, 3 Н, протоны N-СН3), 2,42 (триплет, 2 Н, протоны CH2CN), 0,09 (синглет, 9 Н, протоны Si-СН3). Исходя из данных метода 1Н ЯМР, структуру продукта определили следующим образом:

Пример 5. Синтез N-триметилсилил-3,3'-иминодипропионитрила (TMSIDPN)
К холодному раствору 3,3'-иминодипропионитрила (24,2 мл) в дихлорметане (350 мл) добавляли триэтиламин (30,7 мл) и триметилсилилхлорид (26,6 мл). Смесь перемешивали при комнатной температуре в течение 18 часов. Полученную соль триэтиламина и хлористо-водородной кислоты отфильтровывали и промывали, используя 40 мл гексана. Объединенный фильтрат упаривали с использованием ротационного испарителя. Остаточный сироп перегоняли под вакуумом, получая N-триметилсилил-3,3'-иминодипропионитрил (TMSIDPN) в виде бледно-желтой жидкости. Данные анализа продукта методом 1H ЯМР (CDCl3, 25°C, при соотнесении сигнала с тетраметилсилановым стандартом) представляют собой нижеследующее: δ 3,15 (триплет, 4 Н, протоны N-CH2), 2,42 (триплет, 4 Н, протоны N-CH2), 0,15 (синглет, 9 Н, протоны Si-СН3). Исходя из данных метода 1Н ЯМР, структуру продукта определили следующим образом:

Пример 6. Синтез 3-[бис(триметилсилил)амино]бензонитрила (3-BTMSABZN)
В круглодонной реакционной колбе, охлаждаемой водяной баней со льдом, перемешивали приблизительно 5,87 г 3-аминобензонитрила, 11,57 г триэтиламина и 10 мл толуола. К данной смеси покапельно добавляли раствор 25,41 г триметилсилилтрифторметансульфоната в 50 мл толуола. Получающуюся в результате смесь нагревали до кипячения в течение 12 часов, получая двухфазную смесь. Верхний слой переносили в другую колбу, а нижний слой экстрагировали, используя 40 мл толуола. Объединенный толуольный раствор упаривали в вакууме. Остаток экстрагировали, используя 100 мл гексана, и гексановый слой упаривали в вакууме, получая 3-[бис(триметилсилил)амино]бензонйтрил (3-BTMSABZN) в виде коричневого масла (12,62 г, 97%-ный выход). Данные анализа продукта методом 1Н ЯМР (С6D6, 25°С, при соотнесении сигнала с тетраметилсилановым стандартом) представляют собой нижеследующее: δ 7,00 (мультиплет, 1 Н, ароматический протон), 6,81 (мультиплет, 1 Н, ароматический протон), 6,67 (мультиплет, 1 Н, ароматический протон), 6,59 (мультиплет, 1 Н, ароматический протон), - 0,10 (синглет, 18 Н, протоны Si-СН3). Исходя из данных метода 1Н ЯМР, структуру продукта определили следующим образом:

Пример 7. Синтез 4-[бис(триметилсилил)амино]бензонитрила (4-BTMSABZN)
В круглодонной реакционной колбе, охлаждаемой водяной баней со льдом, перемешивали приблизительно 5,09 г 4-аминобензонитрила, 10,03 г триэтиламина и 10 мл толуола. К данной смеси покапельно добавляли раствор 22,02 г триметилсилилтрифторметансульфоната в 50 мл толуола. Получающуюся в результате смесь нагревали до кипячения в течение 40 часов, получая двухфазную смесь. Верхний слой переносили в другую колбу, а нижний слой экстрагировали, используя 40 мл толуола. Объединенный толуольный раствор упаривали в вакууме. Остаток экстрагировали, используя 100 мл гексана, и гексановый слой упаривали в вакууме, получая 4-[бис(триметилсилил)амино]бензонйтрил (4-BTMSABZN) в виде коричневого масла (10,77 г, 95%-ный выход). Данные анализа продукта методом 1Н ЯМР (С6D6, 25°С, при соотнесении сигнала с тетраметилсилановым стандартом) представляют собой нижеследующее: δ 6,93 (дублет, 2 Н, ароматические протоны), 6,43 (дублет, 2 Н, ароматические протоны), - 0,07 (синглет, 18 Н, протоны Si-СН3). Исходя из данных метода 1Н ЯМР, структуру продукта определили следующим образом:

Пример 8. Синтез немодифицированного сополимера стирола и бутадиена
В продуваемый азотом реактор объемом 5 галлонов (18,9 дм3), снабженный лопастями турбинной мешалки, добавляли 5100 г гексана, 1278 г раствора стирола в гексане с концентрацией 33,0% (масс.) и 7670 г раствора 1,3-бутадиена в гексане с концентрацией 22,0% (масс.). В реактор загружали 11,98 мл раствора н-бутиллития в гексане с концентрацией 1,6 моль/л и 3,95 мл раствора 2,2-бис(2'-тетрагидрофурил)пропана в гексане с концентрацией 1,6 моль/л. Партию нагревали в результате подачи в рубашку реактора горячей воды. После достижения температурой партии 50°С рубашку реактора охлаждали холодной водой.
По истечении девяноста минут после добавления катализатора приблизительно 420 г получающегося в результате живого полимерного клея переносили из реактора в продуваемую азотом колбу и в результате добавления 3 мл раствора 2,6-ди-трет-бутил-4-метилфенола в изопропаноле с концентрацией 12% (масс.) проводили гашение активных центров. Получающуюся в результате смесь коагулировали с помощью 2 литров изопропанола, содержащего 0,5 г 2,6-ди-трет-бутил-4-метилфенола, и затем высушивали в барабанной сушилке.
Вязкость по Муни (ML1+4) для получающегося в результате полимера определили равной 13,6 при 100°С с использованием вискозиметра Alpha Technologies Mooney с большим ротором, одноминутным временем прогрева и четырехминутным временем работы. Согласно гельпроникающей хроматографии (ГПХ) полимер характеризовался среднечисленной молекулярной массой (Мn) 116600, среднемассовой молекулярной массой (Mw) 120200 и молекулярно-массовым распределением (Mw/Mn) 1,03. Анализ полимера методом 1H ЯМР свидетельствовал об уровнях содержания в полимере стирола 21,0% (масс.) и 1,2-звеньев (звеньев бутадиенового мономера) 55,5%. Свойства получающегося в результате немодифицированного сополимера стирола и бутадиена суммарно представлены в таблице 1.
Пример 9. Синтез немодифицированного сополимера стирола и бутадиена
В продуваемый азотом реактор объемом 2 галлона (7,57 дм3), снабженный лопастями турбинной мешалки, добавляли 1595 г гексана, 400 г раствора стирола в гексане с концентрацией 34,0% (масс.) и 2440 г раствора 1,3-бутадиена в гексане с концентрацией 22,3% (масс.). В реактор загружали 1,70 мл раствора н-бутиллития в гексане с концентрацией 1,6 моль/л и 0,56 мл раствора 2,2-бис(2'-тетрагидрофурил)пропана в гексане с концентрацией 1,6 моль/л. Смесь нагревали путем подачи в рубашку реактора горячей воды. После достижения смесью температуры 50°С рубашку реактора охлаждали холодной водой. По истечении приблизительно 2,5 часов после добавления катализатора в результате добавления 30 мл раствора 2,6-ди-трет-бутил-4-метилфенола в изопропаноле с концентрацией 12% (масс.) проводили гашение в полимеризационной смеси активных центров, полимеризационную смесь коагулировали, используя 12 литров изопропанола, содержащего 5 г 2,6-ди-трет-бутил-4-метилфенола, а после этого высушивали в барабанной сушилке. Свойства получающегося в результате немодифицированного БСК суммарно представлены в таблице 1.
Пример 10. Синтез сополимера стирола и бутадиена, модифицированного 4-[бис(триметилсилил)аминометил] бензонитрилом (4-BTMSAMBZN)
Приблизительно 335 г живого полимерного клея, синтезированного в примере 8, переносили из реактора в продуваемую азотом колбу с последующим добавлением 1,80 мл раствора 4-[бис(триметилсилил)аминометил]бензонитрила (4-BTMSAMBZN) в гексане с концентрацией 0,237 моль/л. Колбу в течение 30 минут переворачивали в водяной бане, выдерживаемой при 65°С. Проводили гашение активных центров в получающемся в результате полимерном клее с помощью 3 мл раствора 2,6-ди-трет-бутил-4-метилфенола в изопропаноле с концентрацией 12% (масс.), полимерный клей коагулировали, используя 2 литра изопропанола, содержащего 0,5 г 2,6-ди-трет-бутил-4-метилфенола, а после этого высушивали в барабанной сушилке. Свойства получающегося в результате модифицированного 4-BTMSAMBZN полимера суммарно представлены в таблице 1.
Пример 11. Синтез сополимера стирола и бутадиена, модифицированного 5-[бис(триметилсилил)амино]-2-пиридинкарбонитрилом (BTMSAPyCN)
Приблизительно 409 г живого полимерного клея, синтезированного в примере 8, переносили из реактора в продуваемую азотом колбу с последующим добавлением 2,22 мл раствора 5-[бис(триметилсилил)амино]-2-пиридинкарбонитрила (BTMSAPyCN) в гексане с концентрацией 0,230 моль/л. Колбу в течение 30 минут переворачивали в водяной бане, выдерживаемой при 65°С. Проводили гашение активных центров в получающемся в результате полимерном клее с использованием 3 мл раствора 2,6-ди-трет-бутил-4-метилфенола в изопропаноле с концентрацией 12% (масс.), полимерный клей коагулировали, используя 2 литра изопропанола, содержащего 0,5 г 2,6-ди-трет-бутил-4-метилфенола, а после этого высушивали в барабанной сушилке. Свойства получающегося в результате модифицированного BTMSAPyCN полимера суммарно представлены в таблице 1.
Пример 12. Синтез сополимера стирола и бутадиена, модифицированного 3-[бис(триметилсилил)амино] пропионитрилом (3-BTMSAPN)
Приблизительно 429 г живого полимерного клея, синтезированного в примере 8, переносили из реактора в продуваемую азотом колбу с последующим добавлением 2,68 мл раствора 3-[бис(триметилсилил)амино]пропионитрила (3-BTMSAPN) в толуоле с концентрацией 0,200 моль/л. Колбу в течение 30 минут переворачивали в водяной бане, выдерживаемой при 65°С. Проводили гашение активных центров в получающемся в результате полимерном клее с использованием 3 мл раствора 2,6-ди-трет-бутил-4-метилфенола в изопропаноле с концентрацией 12% (масс.), полимерный клей коагулировали, используя 2 литра изопропанола, содержащего 0,5 г 2,6-ди-трет-бутил-4-метилфенола, а после этого высушивали в барабанной сушилке. Свойства получающегося в результате модифицированного 3-TMSMAPN полимера суммарно представлены в таблице 1.
Пример 13. Синтез сополимера стирола и бутадиена, модифицированного 3-[(триметилсилил)(метил)амино]пропионитрилом (3-TMSMAPN)
Приблизительно 331 г живого полимерного клея, синтезированного в примере 8, переносили из реактора в продуваемую азотом колбу с последующим добавлением 1,24 мл раствора 3-[(триметилсилил)(метил)амино]пропионитрила (3-TMSMAPN) в толуоле с концентрацией 0,335 моль/л. Колбу в течениз 30 минут переворачивали в водяной бане, выдерживаемой при 65°С. Проводили гашение активных центров в получающемся в результате полимерном клее с использованием 3 мл раствора 2,6-ди-трет-бутил-4-метилфенола в изопропаноле с концентрацией 12% (масс.), полимерный клей коагулировали, используя 2 литра изопропанола, содержащего 0,5 г 2,6-ди-трет-бутил-4-метилфенола, а после этого высушивали в барабанной сушилке. Свойства получающегося в результате модифицированного 3-TMSMAPN полимера суммарно представлены в таблице 1.
Пример 14. Синтез сополимера стирола и бутадиена, модифицированного N-триметилсилил-3,3'-иминодипропионитрилом (TMSIDPN)
Приблизительно 337 г живого полимерного клея, синтезированного в примере 8, переносили из реактора в продуваемую азотом колбу с последующим добавлением 1,17 мл раствора N-триметилсилил-3,3'-иминодипропионитрила (TMSIDPN) в толуоле с концентрацией 0,361 моль/л. Колбу в течение 30 минут переворачивали в водяной бане, выдерживаемой при 65°С. Проводили гашение активных центров в получающемся в результате полимерном клее с использованием 3 мл раствора 2,6-ди-трет-бутил-4-метилфенола в изопропаноле с концентрацией 12% (масс.), полимерный клей коагулировали, используя 2 литра изопропанола, содержащего 0,5 г 2,6-ди-трет-бутил-4-метилфенола, а после этого высушивали в барабанной сушилке. Свойства получающегося в результате модифицированного TMSIDPN полимера суммарно представлены в таблице 1.
Пример 15 (сравнительный пример). Синтез сополимера стирола и бутадиена, модифицированного 3-[бис(триметилсилил)амино] бензонитрилом (3-BTMSABZN)
Приблизительно 344 г живого полимерного клея, синтезированного в примере 8, переносили из реактора в продуваемую азотом колбу с последующим добавлением 1,32 мл раствора 3-[бис(триметилсилил)амино]бензонитрила (3-BTMSABZN) в гексане с концентрацией 0,326 моль/л. Колбу в течение 30 минут переворачивали в водяной бане, выдерживаемой при 65°С. Проводили гашение активных центров в получающемся в результате полимерном клее с использованием 3 мл раствора 2,6-ди-трет-бутил-4-метилфенола в изопропаноле с концентрацией 12% (масс.), полимерный клей коагулировали, используя 2 литра изопропанола, содержащего 0,5 г 2,6-ди-трет-бутил-4-метилфенола, а после этого высушивали в барабанной сушилке. Свойства получающегося в результате 3-BTMSABZN-мoдифициpoвaннoгo полимера суммарно представлены в таблице 1.
Пример 16 (сравнительный пример). Синтез сополимера стирола и бутадиена, модифицированного 4-[бис(триметилсилЕзл)амино] бензонитрилом (4-BTMSABZN)
Приблизительно 334 г живого полимерного клея, синтезированного в примере 8, переносили из реактора в продуваемую азотом колбу с последующим добавлением 1,27 мл раствора 4-[бис(триметилсилил)амино]бензонитрила (4-BTMSABZN) в гексане с концентрацией 0,328 моль/л. Колбу в течение 30 минут переворачивали в водяной бане, выдерживаемой при 65°С. Проводили гашение активных центров в получающемся в результате полимерном клее с использованием 3 мл раствора 2,6-ди-трет-бутил-4-метилфенола в изопропаноле с концентрацией 12% (масс.), полимерный клей коагулировали, используя 2 литра изопропанола, содержащего 0,5 г 2,6-ди-трет-бутил-4-метилфенола, а после этого высушивали в барабанной сушилке. Свойства получающегося в результате 4-BTMSABZN-мoдифициpoвaннoгo полимера суммарно представлены в таблице 1.
Примеры 17-25. Оценка по составлению смесей
Образцы сополимеров стирола и бутадиена, полученные в примерах 8-16, оценивали в каучуковой композиции, наполненной техническим углеродом. Композиции вулканизатов представлены в таблице 2, где численные значения приведены в виде массовых частей на сто массовых частей совокупного каучука (ч./сто ч. каучука).
Вязкость по Муни (ML1+4) для неотвержденной каучуковой композиции определяли при 130°С при использовании вискозиметра Alpha Technologies Mooney с большим ротором, одноминутным временем прогрева и четырехминутным временем работы. Данные по эффекту Пэйна (ΔG') и данные по гистерезису (tan δ) для вулканизатов получали в эксперименте с динамической разверткой по деформации, который проводили при 60°С и 10 Гц при развертке по деформации в диапазоне от 0,25% до 15%. ΔG' представляет собой разность между G' при деформации 0,25% и G' при деформации 15%. Физические свойства вулканизатов суммарно представлены в таблице 3. На фиг.1 представлена графическая зависимость данных по tan δ от вязкостей по Муни для композиций.
Как можно видеть по таблице 3 и фиг.1, образцы модифицированного 4-BTMSAMBZN, BTMSAPyCN, 3-BTMSAPN, 3-TMSMAPN, TMSIDPN, 3-BTMSABZN и 4-BTMSABZN сополимера стирола и бутадиена имеют меньшие значения tan δ в сопоставлении с тем, что имеет место для немодифицированного полимера, что указывает на уменьшение гистерезиса в случае модифицирования сополимера стирола и бутадиена с помощью 4-BTMSAMBZN, BTMSAPyCN, 3-BTMSAPN, 3-TMSMAPN, TMSIDPN, 3-BTMSABZN и 4-BTMSABZN. Образцы модифицированного сополимера стирола и бутадиена также придают значительно меньшее значение ΔG' в сопоставлении с тем, что имеет место для немодифицированного полимера, что свидетельствует об уменьшении эффекта Пэйна вследствие взаимодействия между модифицированным полимером и техническим углеродом. В дополнение к этому, несмотря на наличие у 4-BTMSAMBZN, BTMSAPyCN, 3-BTMSABZN и 4-BTMSABZN одной и той же бис(триметилсилил)аминогруппы, образцы сополимера стирола и бутадиена (примеры 10, 11, 19 и 20), модифицированные с помощью 4-BTMSAMBZN или BTMSAPyCN, в которых бис(триметилсилил)аминогруппа непосредственно присоединена к ациклическому фрагменту или гетероциклическому фрагменту, приводят к получению меньшего значения tan δ и меньшего значения ΔG' по сравнению с тем, что имеет место для образцов сополимера стирола и бутадиена (примеры 15, 16, 24 и 25 (сравнительные)), модифицированных с помощью 3-BTMSABZN и 4-BTMSABZN, в которых бис(триметилсилил)аминогруппа непосредственно присоединена к ароматическому фрагменту, который лишен гетероатомов.
Специалистам в соответствующей области техники очевидны различные модификации и вариации, которые не отклоняются от объема и сущности настоящего изобретения. Настоящее изобретение не должно ограничиваться иллюстративными вариантами осуществления, представленными в настоящем документе.
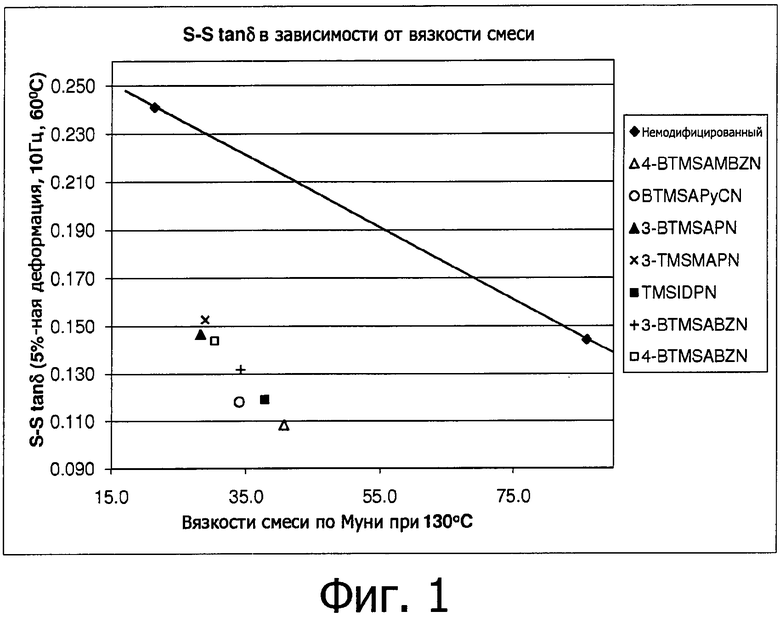
Изобретение относится к функционализованным полимерам и способу их получения. Способ получения функционализованного полимера включает стадии: полимеризации сопряженного диенового мономера и, необязательно, мономера, способного сополимеризоваться с ним, с использованием анионного инициатора для получения реакционно-способного полимера и проведения реакции между реакционно-способным полимером и нитрильным соединением, имеющим защищенную аминогруппу. Защищенная аминогруппа непосредственно присоединена к фрагменту, выбираемому из группы, состоящей из ациклических фрагментов, гетероциклических фрагментов и неароматических циклических фрагментов. Изобретение позволяет понизить гистерезис вулканизатов. 4 н. и 8 з.п. ф-лы, 1 ил., 3 табл., 25 пр.
1. Способ получения функционализованного полимера, включающий стадии:
(i) полимеризации сопряженного диенового мономера и, необязательно, мономера, способного сополимеризоваться с ним, с использованием анионного инициатора для получения реакционно-способного полимера; и
(ii) проведения реакции между реакционно-способным полимером и нитрильным соединением, имеющим защищенную аминогруппу и описывающимся формулой I:
 ,
,
где R1 представляет собой двухвалентную органическую группу, а каждый из R2 и R3 независимо представляет собой одновалентную органическую группу или гидролизуемую группу или R2 и R3 соединяются с образованием двухвалентной органической группы, включающей одну или несколько гидролизуемых групп, при условии, что R1 представляет собой ациклическую двухвалентную органическую группу, гетероциклическую двухвалентную органическую группу, неароматическую циклическую двухвалентную органическую группу, которая лишена гетероатомов, или двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, с тем условием, что если R1 представляет собой двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, то защищенная аминогруппа не должна быть непосредственно присоединена к ароматическому кольцу.
2. Способ по п. 1, в котором защищенную аминогруппу выбирают из группы, состоящей из бис(тригидрокарбилсилил)амино, бис(дигидрокарбилгидросилил)амино, 1-азадисила-1-циклогидрокарбильной, (тригидрокарбилсилил)(гидрокарбил)амино, (дигидрокарбилгидросилил)(гидрокарбил)амино, 1-аза-2-сила-1-циклогидрокарбильной, и дигидрокарбиламиногрупп.
3. Способ по п. 1, в котором нитрильное соединение, имеющее защищенную аминогруппу, является производным нитрильного соединения, выбираемого из группы, состоящей из аренкарбонитрильных соединений, алканкарбонитрильных соединений, алкенкарбонитрильных соединений, алкинкарбонитрильных соединений, циклоалканкарбонитрильных соединений, циклоалкенкарбонитрильных соединений, циклоалкинкарбонитрильных соединений и гетероциклических нитрильных соединений.
4. Способ по п. 1, в котором анионный инициатор представляет собой литийорганическое соединение, а мономер включает сопряженный диеновый мономер и,
необязательно, мономер, способный сополимеризоваться с ним.
5. Способ по п. 1, в котором как цианогруппа, так и защищенная аминогруппа нитрильного соединения, имеющего защищенную аминогруппу, непосредственно присоединены к фрагменту, выбираемому из группы, состоящей из ациклических фрагментов, гетероциклических фрагментов и неароматических циклических фрагментов.
6. Способ по п. 1, в котором нитрильное соединение, имеющее защищенную аминогруппу, описывается формулой II:

где каждый из R1 и R5 независимо представляет собой двухвалентную органическую группу, R4 представляет собой гидролизуемую группу, а R6 представляет собой связь или гидролизуемую группу при условии, что R1 представляет собой ациклическую двухвалентную органическую группу, гетероциклическую двухвалентную органическую группу, неароматическую циклическую двухвалентную органическую группу, которая лишена гетероатомов, или двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, с тем условием, что если R1 представляет собой двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, то защищенная аминогруппа не должна быть непосредственно присоединена к ароматическому кольцу; или
в котором нитрильное соединение, имеющее защищенную аминогруппу, описывается формулой III:

где R1 представляет собой двухвалентную органическую группу, R3 представляет собой одновалентную органическую группу или гидролизуемую группу, каждый R7 независимо представляет собой атом водорода или одновалентную органическую группу или R3 и один R7 соединяются с образованием двухвалентной органической группы при условии, что R1 представляет собой ациклическую двухвалентную органическую группу, гетероциклическую двухвалентную органическую группу, неароматическую циклическую двухвалентную органическую группу, которая лишена гетероатомов, или двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, с тем условием, что если R1 представляет собой двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, то защищенная аминогруппа не должна быть непосредственно присоединена к ароматическому кольцу, или
в котором нитрильное соединение, имеющее защищенную аминогруппу, описывается формулой V:

где R1 представляет собой двухвалентную органическую группу и каждый из R9 и R10 независимо представляет собой атом водорода или одновалентную органическую группу или по меньшей мере один R9 и по меньшей мере один R10 соединяются с образованием двухвалентной органической группы при условии, что R1 представляет собой ациклическую двухвалентную органическую группу, гетероциклическую двухвалентную органическую группу, неароматическую циклическую двухвалентную органическую группу, которая лишена гетероатомов, или двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, с тем условием, что если R1 представляет собой двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, то защищенная аминогруппа не должна быть непосредственно присоединена к ароматическому кольцу.
7. Способ по п. 1, в котором нитрильное соединение, имеющее защищенную аминогруппу, описывается формулой IV:

где каждый из R1 и R8 независимо представляет собой двухвалентную органическую группу, а каждый R7 независимо представляет собой атом водорода или одновалентную органическую группу при условии, что R1 представляет собой ациклическую двухвалентную органическую группу, гетероциклическую двухвалентную органическую группу, неароматическую циклическую двухвалентную органическую группу, которая лишена гетероатомов, или двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, с тем условием, что если R1 представляет собой двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, то защищенная аминогруппа не должна быть непосредственно присоединена к ароматическому кольцу, или
в котором нитрильное соединение, имеющее защищенную аминогруппу, описывается формулой VI:
 ,
,
где каждый из R1 и R11 независимо представляет собой двухвалентную органическую группу, а каждый из R9 и R10 независимо представляет собой атом водорода или одновалентную органическую группу при том условии, что R1 представляет собой ациклическую двухвалентную органическую группу, гетероциклическую двухвалентную органическую группу, неароматическую циклическую двухвалентную органическую группу, которая лишена гетероатомов, или двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, с тем условием, что если R1 представляет собой двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, то защищенная аминогруппа не должна быть непосредственно присоединена к ароматическому кольцу.
8. Способ по п. 1, в котором анионный инициатор представляет собой литийорганическое соединение.
9. Способ по п. 1, в котором упомянутая стадия проведения реакции приводит к получению продукта реакции, который впоследствии протонируют.
10. Функционализованный полимер, содержащий защищенную аминогруппу и описываемый формулой VII:
 ,
,
где π представляет собой полимерную цепь полидиена или сополимера сопряженного диена и сомономера, характеризующуюся содержанием цис-1,4-звеньев от 10 до 60%, R1 представляет собой двухвалентную органическую группу, а каждый из R2 и R3 независимо представляет собой одновалентную органическую группу или гидролизуемую группу при том условии, что R1 представляет собой ациклическую двухвалентную органическую группу, гетероциклическую двухвалентную органическую группу, неароматическую циклическую двухвалентную органическую группу, которая лишена гетероатомов, или двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, при условии, что если R1 представляет собой двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, то защищенная аминогруппа не должна быть непосредственно присоединена к ароматическому кольцу.
11. Функционализованный полимер, содержащий аминогруппу и описываемый формулой VIII:

где π представляет собой полимерную цепь полидиена или сополимера сопряженного диена и сомономера, характеризующуюся уровнем содержания цис-1,4-звеньев от 10 до 60%, R1 представляет собой двухвалентную органическую группу, а каждый из R12 и R13 независимо представляет собой одновалентную органическую группу или атом водорода при условии, что R1 представляет собой ациклическую двухвалентную органическую группу, гетероциклическую двухвалентную органическую группу, неароматическую циклическую двухвалентную органическую группу, которая лишена гетероатомов, или двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, с тем условием, что если R1 представляет собой двухвалентную органическую группу, содержащую ароматическое кольцо, которая лишена гетероатомов, то аминогруппа не должна быть непосредственно присоединена к ароматическому кольцу.
12. Компонент покрышки, включающий вулканизованный остаток функционализованного полимера по п. 10 или 11.
| Колосоуборка | 1923 |
|
SU2009A1 |
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| JP 4246401 A, 02.09.2002 | |||
| JP 2006152220 A, 15.06.2006 | |||
| KR 20020095212 A,20.12.2002 | |||
| СПОСОБ ИЗВЛЕЧЕНИЯ РАСТИТЕЛЬНЫХ МАСЕЛ | 1995 |
|
RU2090593C1 |
| WO 2008013904 A3,31.01.2008 | |||
| RU 94026093 A1,27.05.1996 | |||
| СПОСОБ ПОЛИМЕРИЗАЦИИ ОЛЕФИНОВ С РЕГУЛИРУЕМОЙ МОРФОЛОГИЕЙ | 2004 |
|
RU2339650C2 |
Авторы
Даты
2015-09-27—Публикация
2011-01-24—Подача