Изобретение относится к способу получения кристаллических катионных моноядерных динитрозильных комплексов железа общей формулы [Fe(SR)2(NO)2]n +X-, где n=1-4, Х = кислотный остаток, R представляет собой тиомочевину, а также ее производные реакцией взаимодействия водных растворов солей железа: FeSO4·7H2O или Na2[Fe2(S2O3)2(NO)4]·4H2O с Na2S2O3·5H2O в присутствие тиомочевины или ее производных (диметилтиомочевины; N-этилтиомочевины и др.) в кислой среде, а также к донорам монооксида азота на их основе.
Поиск новых подходов к созданию эффективных и нетоксичных лекарственных препаратов на основе координационных соединений металлов интенсивно ведется в ведущих лабораториях мира (J.C. Dabrowiak. Metals in Medicine. John Wiley & Sons, Ltd. 2009, 342). Особый интерес представляют соединения на основе биогенного металла - железа (Structure and Bonding 5© Springer-Verlag Berlin, Heidelberg 2013; Phoebe K. Allan, Russell E. Morris, Medical Applications of Solid Nitrosyl Complexes; R.L. Elliott, J.F. Head, J. Cancer Therapy, 3, 2012, 278, C. Ornelas, Application of ferrocene and its derivatives in cancer research, New J. Chem., 2011, 35, 1973-1985). Изучение реакций монооксида азота (NO) - универсального соединения, выполняющего многочисленные биологические функции: посредника в межклеточных взаимодействиях, цитотоксического эффектора иммунологической защиты организма, регулятора нейротрансмиссии, иммунитета, ингибитора агрегации тромбоцитов и их адгезии на стенках кровеносных сосудов и пр. (Lancaster J.R. Nitric Oxide: Biol. & Chem, 2010, 22, 13; N.M. Crawford, J. Of Experimental Botany, 2006, 57, 3, 471; P.C. Ford, L.E. Laverman, Coord. Chem. Rev., 2005, 249, 391; J.A. McCleverty, Chem. Rev., 2004, 104, 403;; A. Batler, R. Nicholson, Life, Death and Nitric Oxide: The Royal Society of Chemistry: Cambridge, 2003 и др.), позволило прояснить важные аспекты в механизмах возникновения NO-интермедиатов in vivo. К числу таких интермедиатов относятся нитрозильные ферредоксины - природные "депо" эндогенного NO (Butler A.R., Megson I.I., Chem. Rev., 2002, 102,. 1155; H. Lewandowska, M. Kalinowska, K. Brzoska, K. Wojciuk, G. Wojciuk, M. Kruszewski, Dalton Trans. 40, 2011, 8273) - динитрозильные комплексы железа с протеинами (protein-bound dinitrosyl iron complexes (DNICs)) и низко молекулярные динитрозильные комплексы железа (low molecular weight dinitrosyl iron complexes (LMW-DNICs)) (T. Ueno, Y. Susuki, S. Fujii, A.F. Vanin, T. Yoshimura, Biochem. Pharmacol., 2002, 63, 485-493; M.W. Foster, D.T. Hess, J.S. Stamler, Trends Mol. Med., 2009, 15, 391-404; D.T. Hess, A. Matusmoto, S.-O. Kim, H.E. Marshall, J.S. Stamler, Nat. Rev. Mol.Cell Biol., 2005, 6, 150-166). Поиск новых экспериментальных подходов к получению синтетических аналогов LMW-DNICs, исследование их свойств, включая NO-донирующую активность, открывает перспективы практического использования миметиков активных центров нитрозильных [1Fe-2S] ферредоксинов в качестве эффективных NO-генерирующих соединений в терапии социально-значимых заболеваний. Их водорастворимые синтетические аналоги могут успешно использоваться в качестве нового поколения лекарственных препаратов, применяемых в NO-терапии сердечно-сосудистых (A.F. Vanin, V.I. Lozinskii, V.I. Kapel′ko, inventors; Polymeric composition for synthesis of the stabilized form of dinitrosyl iron complex, and the procedure for synthesis of this form of the complex. RF Patent 2291880 C1. 2005; Санина H.А., Серебрякова Л.И., Шульженко B.C., Писаренко О.И., Руднева Т.Н., Алдошин С.М., Патент РФ №2460531 (2012); Санина Н.А., Серебрякова Л.И., Шульженко B.C., Писаренко О.И., Руднева Т.Н., Алдошин С.М., Патент РФ №2437667 (2011) и онкологических (Санина Н.А., Козуб Г.И., Кондратьева Т.А., Алдошин С.М., Патент РФ №2494104 (2013); Санина Н.А., Жукова О.С, Алдошин С.М., Емельянова Н.С, Герасимова Г.К., Патент РФ №2429242 (2011); Санина Н.А., Жукова О.С, Смирнова З.С., Руднева Т.Н., Шилов Г.В., Алдошин С.М., Давыдов М.И., Патент РФ №2441872 (2012); N.A. Sanina, K.A. Lysenko, O.S. Zhukova, T.N. Roudneva, N.S. Emel′yanova, S.M. Aldoshin, Patent No. US 8,067,628 B2 (2011)) заболеваний.
Основные требования к соединениям-донорам NO сформировались благодаря накопившемуся опыту в их исследовании и, в определенной степени, являются обоснованием целесообразности поиска новых биологически активных веществ в этом ряду соединений: 1) целевые продукты синтеза NO доноров должны быть выделены в чистом виде и твердом состоянии; 2) NO-доноры должны быстро разлагаться в водных растворах при физиологическом значении pH с высвобождением NO без дополнительной активации; 3) при разложении NO доноров должен образовываться оксид азота с количественным выходом.
Особый интерес представляют поиск методов получения солевых форм динитрозильных моноядерных комплексов железа (ДНКЖ) с различными серосодержащими лигандами. В настоящее время из солевых форм известны только анионные [1Fe-2S] ДНКЖ состава Q[Fe(SR)2(NO)2] (H. Strasdeit, В. Krebs, G. Henkel, Z. Naturforsch., 1986, 41B, 1357-1362. M.-Li Tsai, C.-C. Chen, I-J. Hsu, S.-C. Ke, C.-H. Hsieh, K.-An Chiang, Lee G.-H. Lee, Yu Wang, J.-M. Chen, J.-Fu Lee, W.-F. Liaw, Inorg. Chem., 2004, 43, 16, 5159-5167. Fu-Te Tsai, S.-J. Chiou, M.-C. Tsai, M.-Li Tsai, H.-W. Huang, M.-H. Chiang, W.-F. Liaw, Inorg. Chem., 2005, 44, 16, 5872-5881. T.-N. Chen, F.-C. Lo, M.-L. Tsai, K.-N. Shih, M.-H. Chiang, G.-H. Lee, W.-F. Liaw, Inorg. Chim. Acta., 2006, 359, 2525-2533. T.-T. Lu, S.-J. Chiou, C.-Y. Chen, W.-F. Liaw, Inorg. Chem., 2006, 45, 21, 8799-8806. M.-C. Hung, M.-C. Tsai, G.-H. Lee, W.-F. Liaw, Inorg. Chem., 2006, 45, 15, 6041-6047. S.-J. Chiou, C.-C. Wang, C.-M. Chang, J. Organomet. Chem., 2008, 693, 3582-3586. T.C. Harrop, Z.J. Tonzetich, E. Reisner, S.J. Lippard, J. Am. Chem. Soc, 2008, 130, 46, 15602-15610. J.-H. Wang, C.-H. Chen, Inorg. Chem., 2010, 49, 17, 7644-7646. Z.-S. Lin, F.-C. Lo, C.-H. Li, C.-H. Chen, W.-N. Huang, I-J. Hsu, J.-Fu Lee, Jia-C. Horng, W.-F. Liaw, Inorg. Chem., 2011, 50, 10417-10431) с Q - нефункциональными органическими или метал-органическими катионами. Эти соединения, с одной стороны являются водорастворимыми и, соответственно, биодоступными, а с другой стороны - малотоксичными: молекулы их содержат только один атом железа, координированный одновременно двумя типами фармакофоров - функциональными тиолилами и NO группами.
Первые анионные ДНКЖ получали в виде малостабильных водных растворов пропусканием газообразного NO через смесь сульфата железа (II) и соответствующего водорастворимого тиола, взятых в мольном соотношении 1:2, соответственно (L. Li. Some Coordination Chemistry of Non-heme Iron Nitrosyi Complexes. Comments on Inorganic Chemistry. 2002. Volume 23, issue 5, pp. 335-353; I.I. Lobysheva, V.A. Serezhenkov, R.A. Stucan, M.K. Bowman and A.F. Vanin. Redox Reactions and Stability of Dinitrosyi Iron Complexes with Thiolate Ligands as Potential Donors and Carriers of Nitric Oxide. Biochemistry, 1997, v. 62, N7, p. 801; M.V. Stupakova, I.I. Lobysheva, V.D. Mikojan, A.F. Vanin and S.V. VasiPeva. A Role of Iron Ions in the SOS DNA Repair Response Induced by Nitric Oxide in Escherichia coli. Biochemistry, 2000, v. 65, N6, p. 690; A. Mulsch, P.I. Mordvincev, A.F. Vanin and R. Buss. The potent vasodilating and guanylyl cyclase activating dinitrosyl-iron(II) complex is stored in a protein-bound form in vascular tissue and is released by thiols. FEBS Lett., 1991, v. 294, iss. 3, pp.252-256; I.Y. Malyshev, A.V. Malugin, L.Y. Golubeva, T.A. Zenina, E. B. Manukhina, V.D. Mikoyan and A.F. Vanin. Nitric oxide donor induces HSP70 accumulation in the heart and in cultured cells. FEBS Lett., 1996, v. 391, iss. 1-2, pp.21-23; A.L. Kleschyov, S. Strand, S. Schmitt, D. Gottfried, M. Skatchkov, N. Sjakste, A. Daiber, V. Umansky, T. Munzel. Dinitrosyl-iron triggers apoptosis in Jurkat cells despite overexpression of Bcl-2. / Free Radical Biology & Medicine 40 (2006) 1340-1348), или в форме лиофильно высушенных композитов этих растворов с водорастворимыми полимерами (Ванин А.Ф., Лозинский В.И. Капелько В.И., Полимерная композиция для получения стабилизированной формы динитрозильного комплекса железа и способ получения указанной формы комплекса. Патент RU 2291880 С1). Эти способы ограничивают широкое использование ДНКЖ в прикладных целях, связанное с неконтролируемостью исходного состава.
Существуют ряд способов получения анионных ДНКЖ с серосодержащими лигандами различной природы. К примеру, прямым нитрозилированием биомиметиков окисленных или восстановленных форм рубредоксина [Fe(SR)4]2-/1-(R2=Ph,Et) газообразным NO по схеме 1:
Схема 1.
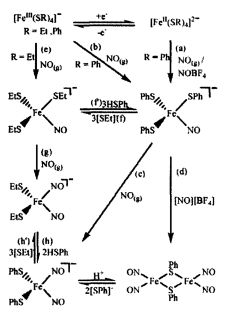
Анионные ДНКЖ состава Q[S5Fe(NO)2] с Q=PPN (µ-нитридо-бис(трифенилфосфоний)) и K-18-краун-6-эфиром были получены многочасовой реакцией мононитрозила железа с серой кристаллической (схема 2) с применением металлического натрия и токсичного тетрагидрофурана:
Схема 2.
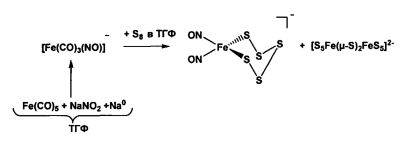
Такие анионные ДНКЖ, в свою очередь, могут служить прекурсорами для синтеза анионных ДНКЖ с R - ароматическими тиолилами (схема 3), полученными из соответствующих дисульфидов:
Схема 3.
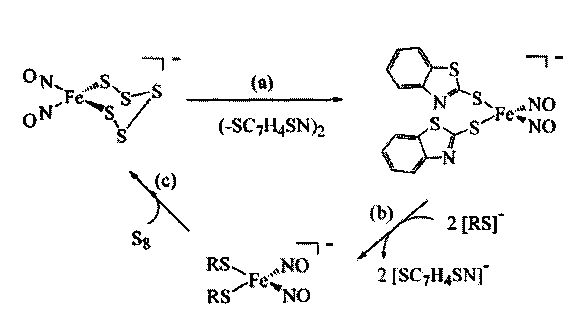
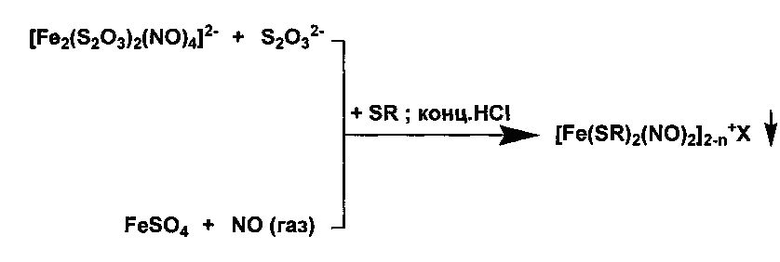
Реакцией 5,5′-дитио-бис(2-нитробензойной кислоты) с тетранитрозильным дианионом в растворе ацетонитрила были также получены анионные ДНКЖ с Na+ - 18-краун-6-эфиром в качестве противоиона (схема 4):
Схема 4.
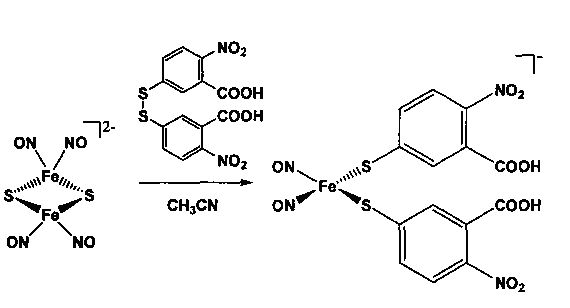
Кристаллический ДНКЖ (N2H5)+[Fe(SR)2(NO)2]- с R 5-нитропиридинилом был недавно получен реакцией Na2[Fe2(S2O3)2(NO)4]·H2O с продуктом восстановления 2,2′-дитиобис-(5-нитропиридина) гидразингидратом в водно-спиртовом растворе (схема 5):
Схема 5.
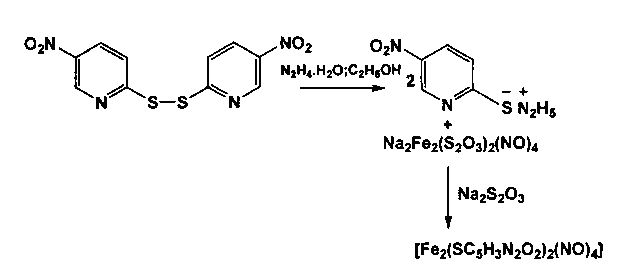
Прямое нитрозирование (Et4N)2[[Fe2S2(S-p-толил)4] газообразным NO в ацетонитриле по схеме 6 также ведет к образованию анионных ДНКЖ с серосодержащими лигандами ароматической природы:
Схема 6.
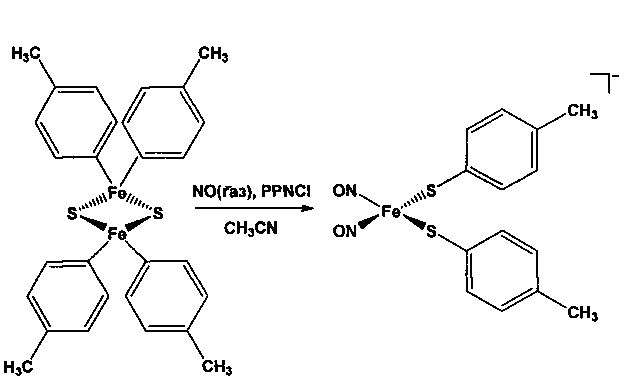
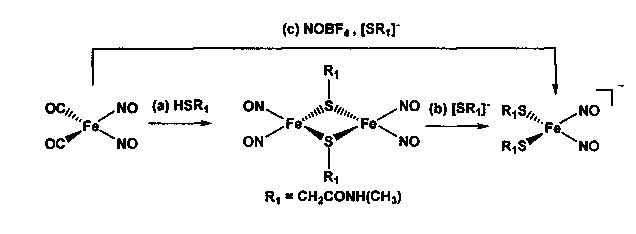
Анионные ДНКЖ с PPN+ катионом и алифатическими тиолилами R1 получают из смешанных моноядерных карбонил-нитрозилов железа ((a, c) в схеме 7) или нейтральных биядерных тетранитрозильных комплексов железа состава [Fe2(SR1)2(NO)4] ((b) в схеме 7) восстановлением с соответствующими алифатическими тиолами.
Схема 7.
Неустойчивость ДНКЖ вызывает большие трудности по их кристаллизации и изучению их строения и физико-химических свойств в твердой фазе. Таким образом, существует потребность в разработке новых способов получения ДНКЖ как эффективных и биосовместимых доноров NO, обладающих пониженной токсичностью.
Задачей настоящего изобретения является разработка принципиально нового способа получения моноядерных катионных динитрозильных комплексов железа.
В одном аспекте изобретение относится к способу получения моноядерных катионных динитрозильных комплексов железа общей формулы [Fe(SR)2(NO)2]n +X- где n=1-4, Х = кислотный остаток, R представляет собой тиомочевину, а также ее производные реакцией
взаимодействия водных растворов солей железа: FeSO4·H2O с газообразным NO или Na2[Fe2(S2O3)2(NO)4]·4H2O с Na2S2O3·5H2O в присутствие тиомочевины или ее производных в кислой среде. Этот способ позволяет впервые получить заявляемые комплексы в кристаллической форме.
Кроме того настоящее изобретение относится к донорам моноокисида азота, представляющим собой моноядерные динитрозильные комплексы железа с лигандами, охарактеризованными выше.
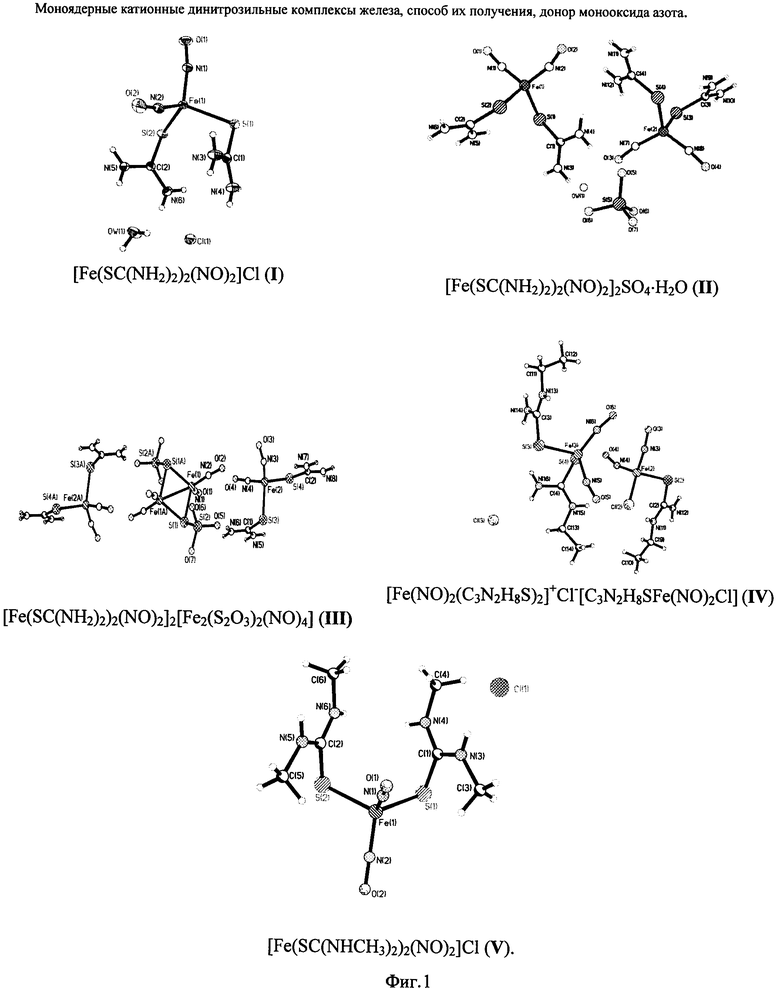
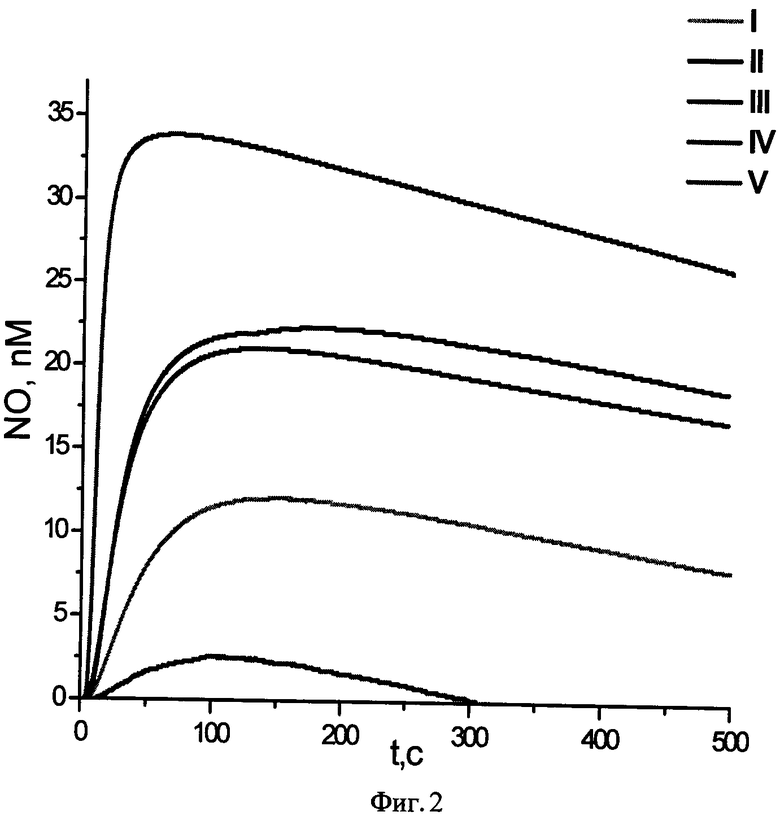
Описание фигур
На фиг. 1 показаны молекулярные структуры комплексов I-V. На фиг. 2 показана зависимость количества NO, генерируемого комплексами воде I-V в анаэробных условиях при pH 7, Т=25°C (концентрация комплексов 0.4·10-5 М) от времени.
Сущность изобретения заключается в следующем:
Монокристаллы комплексов I-V были получены реакцией смеси соли железа (+1) с восстановительными агентом - тиосульфатом натрия, либо реакцией пропускания гаообразного NO через раствор соли железа (+2) с тиомочевинной или ее производными в кислой среде, в инертной атмосфере, согласно схеме 8.
Схема 8.
В отличие от реакций замещения тиосульфатных лигандов ароматическими тиолилами, описанными нами ранее (N.A. Sanina, S.М. Aldoshin, Russ. Chem. Bull., 2011, 60, 7, 1223-1251), для которых требуется щелочная среда, в данном способе использовали кислый раствор соответствующего лиганда, т.к. тиомочевина или ее производные образуют хлористые соли, легко вступающие в реакции формирования ДНКЖ (см.схему 8). Комплексы I-V выделяются в виде монокристаллов с высокими выходами. Кристаллы I-V устойчивы при хранении в инертной атмосфере при Т=-8-10°C длительное время (>6 мес), о чем свидетельствуют ИК-спектры исследуемых образцов. Комплексы I-V хорошо растворимы в воде и других полярных растворителях. Метод позволяет не применять концентрированные растворы щелочей для перевода тиолов в солевые формы, использование которых, как правило, приводит к образованию Fe(OH)3 в качестве побочного продукта реакции и снижает выходы целевых продуктов.
В предлагаемом изобретении исследована NO - донорная активность I-V.
Методика эксперимента.
Количество NO, генерируемого комплексами I-V в растворе, осуществляли с помощью сенсорного электрода "amiNO-700" системы "inNO Nitric Oxide Measuring System" (Innovative Insruments, Inc., Tampa, FL, USA). Концентрацию NO для исследуемого комплекса фиксировали в течение ~500 секунд (с шагом 0.2 сек.) в водном растворе с концентрацией донора NO (0.4·10-5 М). Для калибровки электрохимического сенсора использовали стандартный водный раствор NaNO2 (100 мкмоль), который добавляли в смесь 0.12М KI и 2 мл 1М H2SO4 в 18 мл воды. Все эксперименты проводили в аэробных растворах при температуре 25°C при pH 7-9 (pH растворов измеряли с помощью мембранного pH-метра "HI 8314" (HANNA instruments, Germany).
По данным электрохимического анализа комплексы I-V разлагаются с образованием NO в первые секунды после растворения в анаэробном водном растворе. При этом, максимальные количества NO, генерируемые комплексами I-V при pH 7 составляют ~12-33 нМ/на моль комплекса. Кривые зависимости количества NO от времени имеют максимум: спустя ~1,5-2 минуты после начала разложения комплексов I-V наблюдается уменьшение генерированного NO и спустя ≈8 минут количество NO уменьшается. Эффективность (количество выделившегося NO и пролонгированность действия) генерирования NO возрастает в ряду: V<I<II=III<IV. Для сравнения, в растворах анионных комплексов наблюдалась меньшая NO-донорная активность в аналогичных экспериментальных условиях, к тому же, NO генерируется этими системами при дополнительной термо- или фотоактивации.
Т.о., водорастворимые комплексы I-V являются более эффективными NO донорами для биомедицинских применений в сравнении с большинством изученных ранее DNICs различных структурных типов.
Изобретение в части заявляемого способа характеризуется следующими примерами.
Пример 1. Синтез I проводили в инертной атмосфере по следующей методике. 0,88 г (1,5 ммоль) соли железа Na2[Fe2(S2O3)2(NO)4]·4H2O, синтезированной по методике (N.А. Sanina, S.М. Aldoshin, Т.N. Rudneva, N.I. Golovina, G.V. Shilov, Yu.M. Shul′ga, V.M. Martynenko, N.S. Ovanesyan, Russ.J. of Coord. Chem., 2005, 31, 5, 301-306), и 0,76 г (3 ммоль) Na2S2O3·5H2O растворяли в 4 мл Н2О при Т=45°C и помещали в трехгорлую колбу в инертной атмосфере, затем по каплям при перемешивании добавляли раствор 0,53 г (7 ммоль) SC(NH2)2 и 3 мл HCl (конц., 36 ммоль) в 3 мл Н2О при Т=25°C. Реакционную смесь перемешивали несколько минут и выдерживали в течении 3 часов при Т=+5°C. Образовавшийся черный осадок фильтровали и сушили в инертной атмосфере. Выход 0,61 г (63%).
Элементный анализ: FeC2H10N6O3S2Cl Найдено %: С - 7.0; Н - 3.3; N - 24.2; Fe - 17.3; S - 20.6. Рассчитано %: С - 7.5; Н - 3.1; N - 26.1; Fe - 17.4; S - 19.9; Cl - 11.0; О - 14.9.
ИК-спектр I: 3478 (сл), 3366 (ср), 3295 (ср), 3189 (ср), 2707 (оч.сл), 2076 (оч.сл), 1807 (c), 1744 (оч.с), 1636 (оч.с), 1509 (сл), 1431 (ср), 1216 (сл), 1023 (ср), 932 (оч.сл), 802 (сл), 709(ср), νNO=1807, 1744 см-1.
Пример 2. Синтез II проводили в инертной атмосфере по следующей методике. 2,78 г (0,01 моль) соли железа FeSO4·7H2O растворяли в 10 мл Н2О и помещали в трехгорлую колбу в инертной атмосфере, затем по каплям при перемешивании добавляли раствор 1,52 (0,02 моль) тиомочевины и 1 мл HCl (конц., 0,012 моль) в 10 мл Н2О при Т=25°C. Через реакционную смесь, окрашенную в бледно-розовый цвет, пропускали избыток газообразного NO в течение двух часов. Раствор выдерживали в холодильнике при Т=5°C в течение 18 часов, образовавшиеся черные монокристаллы к фильтровали и сушили в инертной атмосфере. Выход: 0,66 г (34%).
Элементный анализ Fe2C4H14N12O9S5. Найдено %: Fe - 17,52; С - 6,76; Н - 2,52; N - 24,62; S - 26,71; O - 20,34; Вычислено %: Fe - 17,72; С - 7,59; Н - 2,53; N - 26,58; S - 25,32; O - 20,25.
ИК-спектр II: 3474 (сл), 3393 (ср), 3300 (ср), 3124 (ср), 2735 (сл), 2351 (оч.сл), 2077 (оч.сл), 1808 (c), 1749 (c), 1734 (оч.с), 1637 (c), 1515 (сл), 1433 (ср), 1404 (ср), 1126 (ср), 1085 (c), 1062 (оч.с), 981 (сл), 714 (c), νNO=1808, 1748, 1734 см-1.
Пример 3. Синтез III проводили в инертной атмосфере по следующей методике. 0,88 г (1,5 ммоль) соли железа Na2[Fe2(S2O3)2(NO)4]·4H2O, синтезированной по методике (N.А. Sanina, S.M. Aldoshin, T.N. Rudneva, N.I. Golovina, G.V. Shilov, Yu. M. Shul′ga, V.M. Martynenko, N.S. Ovanesyan, Russ.J. of Coord. Chem., 2005, 31, 5, 301-306),, и 0,76 г (3 ммоль) Na2S2O3·5Н2О растворяли в 30 мл воды, и фильтрат помещали в трехгорлую колбу в инертной атмосфере. Затем по каплям при перемешивании к фильтрату добавляли смесь 0,53 г (7 ммоль) SC(NH2)2 и 1 мл HCl (конц., 36 ммоль) в 20 мл воды при Т=25°C. Реакционную смесь выдерживали сутки при комнатной температуре и фильтровали. Образующиеся при этом тонкие черно-красные длинные пластинки отфильтровывали и сушили в инертной атмосфере. Выход (57%).
Элементный анализ Fe6C4H12N16O14S8. Найдено %: Fe-23,00; С-4,87; Н-1,62; N-21,80; S-26,10; 0-22,52; Вычислено %: Fe-22,60; С-4,80; Н-1,60; N-22,60; S-25,80; 0-22,60.
ИК-спектр III: 3471 (сл), 3415 (сл), 3375 (сл), 3330 (ср), 3215 (ср), 3147 (ср), 2733 (оч.сл), 2405 (оч.сл), 1822 (c), 1798 (оч.с), 1756 (оч.с), 1732 (оч.с), 1661 (ср), 1636 (c), 1575 (сл), 1532 (сл), 1502 (сл), 1434 (ср), 1394 (ср), 1216 (c), 1182 (c), 1107 (сл), 1075 (сл), 1006 (оч.с), 886 (сл), 711 (ср), 702 (ср), νNO=1822, 1798, 1756, 1732 см-1.
Пример 4. Синтез IV проводили в инертной атмосфере по следующей методике. 2,78 г (0,01 моль) соли железа FeSO4·7H2O растворяли в 10 мл Н2О и помещали в трехгорлую колбу в инертной атмосфере, затем по каплям при перемешивании добавляли раствор 2,08 (0,02 моль) N-этилтиомочевины и 4 мл HCl (конц., 0,048 моль) в 10 мл Н2О при Т=25°C. Через реакционную смесь, окрашенную в темно-розовый цвет, пропускали избыток газообразного NO в течение двух часов. Реакционную смесь выдерживали в холодильнике при Т=5°C в течение 18 часов, образовавшийся черный осадок фильтровали и сушили в инертной атмосфере. Выход: 1,132 г (37%).
Элементный анализ Fe2C9H24N10O4S3Cl2. Найдено %, Fe - 18,80; С - 16,85; Н - 4,09; N - 21,88; S - 16,03; O - 14,60; Вычислено %, Fe - 18,21; С - 17,56; Н - 3,90; N - 22,76; S - 15,61; O - 14,93.
ИК-спектр IV: 3287 (ср), 3174 (ср), 2983 (сл), 2939 (сл), 2345 (оч.сл), 2267 (оч.сл), 1796 (c), 1737 (оч.с), 1724 (c), 1630 (оч.с), 1561 (ср), 1511 (ср), 1468 (сл), 1452 (ср), 1387 (сл), 1349 (сл), 1290 (ср), 1171 (оч.сл), 1120 (сл), 1031 (оч.сл), 910 (оч.сл), 823 (сл), 789 (сл), 742 (ср), νNO=1796, 1737, 1724 см-1.
Пример 5. Синтез V проводили в инертной атмосфере по следующей методике. 2,78 г (0,01 моль) соли железа FeSO4·7H2O растворяли в 10 мл Н2О и помещали в трехгорлую колбу в инертной атмосфере, затем по каплям при перемешивании добавляли раствор 2,08 г (0,02 моль) N,N′-диметилтиомочевины и 4 мл HCl (конц., 0,048 моль) в 10 мл Н2О при Т=25°C. Через реакционную смесь, окрашенную в светло-коричневый цвет, пропускали избыток газообразного NO в течение 2,5 часов. Раствор выдерживали в холодильнике при Т=5°C в течение 18 часов, образовавшийся темно-зеленый осадок фильтровали и сушили в инертной атмосфере. Выход: 0,84 г (24%).
Элементный анализ Fe1C6H16N6O2Cl. Найдено %, Fe - 14,90; С - 18,48; Н - 4,50; N - 20,76; S - 18,62; Вычислено %, Fe - 15,57; С - 20,03; Н - 4,45; N - 23,36; S - 17,80.
ИК-спектр V: 3305 (ср), 3044 (сл), 2948 (сл), 1791 (c), 1751 (ср), 1728 (c), 1653 (ср), 1599 (оч.с), 1535 (ср), 1515 (ср), 1444 (ср), 1424 (сл), 1372 (ср), 1304 (ср), 1187 (сл), 1147 (сл), 1035 (ср), 715 (cp), νNO=1791, 1751, 1728 см-1.
ИК-спектры (см-1) комплексов I-V регистрировали на приборе Perkin-ElmerSpectrum 100Х при комнатной температуре.
| название | год | авторы | номер документа |
|---|---|---|---|
| МОНОЯДЕРНЫЕ ДИНИТРОЗИЛЬНЫЕ КОМПЛЕКСЫ ЖЕЛЕЗА, СПОСОБ ПОЛУЧЕНИЯ МОНОЯДЕРНЫХ ДИНИТРОЗИЛЬНЫХ КОМПЛЕКСОВ ЖЕЛЕЗА, ДОНОР МОНООКСИДА АЗОТА, ПРИМЕНЕНИЕ МОНОЯДЕРНОГО ДИНИТРОЗИЛЬНОГО КОМПЛЕКСА ЖЕЛЕЗА В КАЧЕСТВЕ ПРОТИВООПУХОЛЕВОГО ЛЕКАРСТВЕННОГО СРЕДСТВА | 2011 |
|
RU2494104C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НИТРОЗОСОЕДИНЕНИЙ И НИТРИТА В БИООБЪЕКТАХ | 2008 |
|
RU2395096C2 |
| Применение нитрозильного комплекса железа с N,N-диэтилтиомочевиной в качестве нового NO-донорного противоопухолевого средства | 2016 |
|
RU2687269C2 |
| Средство, обладающее противовирусной активностью в отношении SARS-CoV-2, и способ его применения | 2022 |
|
RU2797619C1 |
| Супрамолекулярные ансамбли динитрозильных комплексов железа, способ их получения, доноры монооксида азота, ингибиторы фосфодиэстераз, применение супрамолекулярных ансамблей динитрозильных комплексов железа в качестве противовоспалительных лекарственных средств | 2023 |
|
RU2814108C1 |
| ПРИМЕНЕНИЕ БИЯДЕРНОГО СЕРА-НИТРОЗИЛЬНОГО КОМПЛЕКСА ЖЕЛЕЗА КАТИОННОГО ТИПА В КАЧЕСТВЕ ВАЗОДИЛАТАТОРНОГО ЛЕКАРСТВЕННОГО СРЕДСТВА | 2010 |
|
RU2460531C2 |
| КОМПОЗИЦИЯ ГИДРОГЕЛЯ ДЛЯ ЛЕЧЕНИЯ ДЕФЕКТОВ ПОКРОВНЫХ ТКАНЕЙ МЕТОДОМ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2020 |
|
RU2730850C1 |
| ПРИМЕНЕНИЕ БИЯДЕРНОГО СЕРА-НИТРОЗИЛЬНОГО КОМПЛЕКСА ЖЕЛЕЗА АНИОННОГО ТИПА В КАЧЕСТВЕ ВАЗОДИЛАТАТОРНОГО ЛЕКАРСТВЕННОГО СРЕДСТВА | 2010 |
|
RU2437667C1 |
| ОБРАТИМЫЙ ТЕРМОХИМИЧЕСКИЙ ИНДИКАТОР | 2012 |
|
RU2499800C1 |
| СРЕДСТВО ПРОТИВ ГИПОКСИИ МИОКАРДА | 2013 |
|
RU2522953C1 |
Настоящее изобретение относится к моноядерным катионным динитрозильным комплексам железа общей формулы [Fe(SR)2(NO)2]n +X-, где n=1-4, Х = кислотный остаток, R представляет собой тиомочевину, ее производные. Также предложены способ получения комплексов железа и донор монооксида азота. Изобретение позволяет получить новые динитрозильные комплексы железа, которые могут применяться в качестве эффективных доноров монооксида азота. 3 н.п. ф-лы, 2 ил., 5 пр.
1. Моноядерные катионные динитрозильные комплексы железа общей формулы [Fe(SR)2(NO)2]n +X-, где n=1-4, Х = кислотный остаток, R представляет собой тиомочевину, а также ее производные.
2. Способ получения моноядерных катионных динитрозильных комплексов железа по п. 1, заключающийся в реакции водного раствора соли Na2[Fe2(S2O3)2(NO)4]·4H2O с Na2S2O3·5H2O в присутствии тиомочевины или ее производных в кислой среде при комнатной температуре и в бескислородной атмосфере с последующим выделением целевого продукта известными приемами.
3. Донор монооксида азота, представляющий собой моноядерный катионный динитрозильный комплекс железа по п. 1.
| ВОДОРАСТВОРИМЫЕ БИЯДЕРНЫЕ КАТИОННЫЕ НИТРОЗИЛЬНЫЕ КОМПЛЕКСЫ ЖЕЛЕЗА С ПРИРОДНЫМИ АЛИФАТИЧЕСКИМИ ТИОЛИЛАМИ, ОБЛАДАЮЩИЕ ЦИТОТОКСИЧЕСКОЙ, АПОПТОТИЧЕСКОЙ И NO-ДОНОРНОЙ АКТИВНОСТЬЮ | 2008 |
|
RU2441873C2 |
| Способ приготовления сернистого красителя защитного цвета | 1915 |
|
SU63A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| ПНЕВМАТИЧЕСКИЙ НАСОС ДЛЯ ПОДЪЕМА ЖИДКОСТЕЙ ИЗ ГЛУБОКИХ КОЛОДЦЕВ | 1924 |
|
SU924A1 |
Авторы
Даты
2015-11-10—Публикация
2014-04-17—Подача