Изобретение относится к фармацевтической лекарственной форме, которая является стабильной по отношению к окислению.
Многие фармакологические активные соединения имеют потенциал быть неверно употребленными и, таким образом, выгодно обеспечить фармацевтические лекарственные формы в форме, прочной на излом. Яркими примерами таких фармакологически активных соединений являются опиоиды.
Известно, что лица, которые злоупотребляют наркотиками, раздавливают обычные таблетки, которые содержат опиоиды, для того, чтобы аннулировать замедленное высвобождение «микроинкапсулирования» и затем принимать внутрь получившийся порошок орально, ректально или путем введения инъекционного раствора.
Были разработаны различные концепции для предотвращения злоупотребления наркотиками. Одна концепция опирается на механические свойства фармацевтических лекарственных форма, в частности увеличилось сопротивление разрушению (устойчивость к дроблению). Главное преимущество таких фармацевтических лекарственных форм в том, что измельчение, в частности порошкование с помощью обычных средств, таких как измельчение в ступке или дробление с помощью молотка, является невозможным, или, по крайней мере, существенно усложняется.
Такие фармацевтические формы полезны для предотвращения злоупотребления лекарственными средствами, содержащими фармакологически активное соединение, так как они не могут превращаться в порок с помощью обычных средств и таким образом не могут быть введенными в порошковой форме, например, через нос. Механические свойства, в частности высокое сопротивление разрушению этих фармацевтических лекарственных форм делает их устойчивыми к взлому. В контексте таких устойчивых к взлому фармацевтических лекарственных форм может быть сделана ссылка на, например, WO 2005/016313, WO 2005/016314, WO 2005/ 063214, WO 2005/102286, WO 2006/002883, WO 2006/002884, WO 2006/002886, WO 2006/082097, WO 2006/082099, и WO 2008/107149.
Эти устойчивые к взлому фармацевтические лекарственные формы содержат синтетический или натуральный полимер, наиболее часто высокомолекулярный полиэтиленоксид в качестве материала матрицы.
Полиэтиленоксиды, как и другие алифатические эфиры, могут поддаваться автоокислению в присутствии кислорода с образованием гидроперекисей (смотри, например, С.W.McGary Jr., J.Polymer Sci., 2003, 46, 51-57). Последующие радикальные реакции получившихся пероксидов приводят к разрыву цепи. Эти естественные процессы старения катализируются другими агентами окисления и ускоряются УФ светом и/или повышенной температурой. Окислительный процесс деструкции в значительной степени зависит от молекулярного веса. Высокомолекулярные полиэтиленоксиды особенно склонны к процессам автоокисления и деструктируют быстрее, чем низкомолекулярные полиэтиленоксиды.
Кроме того, чувствительные к окислению фармакологически активные ингредиенты, такие как опиоиды, такие как оксиморфон, гидроморфон и оксикодон, являются чувствительными по отношению к окислительной деструкции и процессам разрушения.
В результате процессов деструкции лекарственная форма, содержащая материал матрицы, поддающийся окислительной деструкции и/или чувствительные к окислению фармакологически активные ингредиенты могут быть серьезно поражены. Например, вероятно произойдут потеря содержания фармакологически активного ингредиента, а также обесцвечивание, уменьшение механической прочности и ускоренное высвобождение препарата из-за укороченной полимерной цепи. Особенно сопротивление разрушению в значительной степени зависит от молекулярного массы полиалкиленоксида, содержащегося в лекарственной форме и следовательно, напрямую зависит от процессов разрыва цепи.
Окисление может быть вызвано молекулярным кислородом или радикалами или пероксидами, образованными соединениями, которые вступают в непосредственную близость с этими чувствительными к окислению материалами матрицы и/или фармакологически активными ингредиентами.
Фармацевтические вспомогательные вещества, такие как, например, полиэтиленгликоли, могут вызвать или катализировать окислительную деструкцию, например, в ходе процесса изготовления фармацевтических лекарственных форм. Кроме того, молекулярный кислород может генерировать указанные радикалы или пероксиды.
Как правило, разложение контролируется стандартными тестами на стабильность при хранении, например, при ускоренных условиях хранения, таких как 40°С/75% отн. влажности. При этих условиях деструкция и разложение обычно происходят быстрее, чем в условиях окружающей среды. Органы, утверждающие лекарства, такие как СНМР (The Committee for Medicinal Products for Human Use - Комитет по медицинским продуктам, предназначенным для человека) и FDA (Food and Drug Administration - Комиссия по контролю за лекарствами и питательными веществами) и международные союзы гармонизации, такие как ICH (International Conference on Harmonisation -Международная конференция по гармонизации), имеют набор стандартных параметров при хранении, которые должны быть выполнены для того, чтобы фармацевтическая лекарственная форма была одобрена.
Особые проблемы возникают тогда, когда такие фармацевтические лекарственные формы, содержащие материал матрицы, который поддается окислительному разложению и/или чувствительные к окислению фармакологически активные ингредиенты должны быть подвержены повышенным температурам в ходе производственного процесса, такого как экструзия горячего расплава, покрытие пленкой и тому подобное. При этих условиях указанные соединения даже являются еще более чувствительными к окислению. Например, несколько известных процессов для изготовления фармацевтических лекарственных форм, имеющих увеличенное сопротивление разрушению требуют, чтобы фармацевтическая композиция, содержащая фармакологически активные ингредиенты подвергалась определенному количеству давления при определенной повышенной температуре в течении определенного периода времени. В зависимости от составляющих фармацевтической композиции и их количества, температура, давление и время могут меняться в определенных пределах. Тем не менее, если минимальные требования не выполняются, сопротивление разрушению в получающейся в результате фармацевтической лекарственной форме является слишком низким.
Следовательно, некоторые обычные процессы для производства фармацевтических лекарственных форм, в частности для фармацевтических лекарственных форм, которые имеют увеличенное сопротивление разрушению, требуют сравнительно жестких условий процесса и, таким образом, они являются до сих пор не применимыми для чувствительных к окислению материалов матрицы и/или фармакологически активных ингредиентов, например, опиоидов. В частности, разрыв цепи фармацевтических наполнителей, таких как полиэтиленоксид во время экструзии горячего расплава создает риск формирования свободных радикалов, таким образом увеличивая окислительный стресс.
Меньшие дозы чувствительных к окислению фармакологически активных ингредиентов часто показывают высший процент окислительной деструкции и разложения, чем большие дозы. Таким образом, фармацевтические лекарственные формы, содержащие меньшие дозы чувствительных к окислению фармакологически активных ингредиентов требуют особого внимания, насколько стабильность при хранении сохраняется.
Влияние окислительных механизмов и химических взаимодействий на устойчивость полимерных систем для аморфного Δ9-тетрагидроканнабинола (не-опиоид), полученного путем расплава полимера описан в М. Munjal et al., J.Pharrn. Sciences, 95(11), 2006, 2473-85. Исследование показало, что для этого крайне нестабильного лекарства сложный характер взаимодействия включает совместимость лекарства-вспомогательного вещества, применение антиоксидантов, сшивателей в полимерных матрицах, микро рН среды и влияние влажности.
К.С.Waterman и др., Pharm. Develop.Tech. 7(1), 2002, 1-32 обзор стабильности лекарств о окислительной деструкции. Предложены различные методы для снижения окисления. Авторы делают заключение, что, в конце концов, каждый препарат представляет собой уникальную ситуацию.
WO 2008/107149 описывает оральные лекарственные формы, которые имеют повышенное сопротивление разрушению, которые могут содержать окислительно-восстановительные стабилизаторы, такие как комплексообразующие агенты, например ЭДТА.
WO 2008/086804 относится к композиции с контролируемым высвобождением, содержащей композицию матрицы, которая включает а) полимер или смесь полимеров, Ь) активное вещество лекарства и необязательно с) один или больше фармацевтически приемлемых наполнителей, в которой доза высвобождения не индуцированная спиртом и имеют отличные свойства по отношению к избежанию злоупотребления лекарственными средствами. Предпочтительно композиция является устойчивой к выделению и/или растворению действующего вещества препарата из композиции путем дробления, плавления и/или экстракцией этанола, в результате чего композиция является устойчивой к злоупотреблению лекарственными средствами. Лимонная кислота может присутствовать в качестве ароматизатора. Пример 2 относится к композиции, содержащей 7 мас.-% лимонной кислоты.
WO 2008/148798 описывает композицию, нанесенную слоями с продленным высвобождением активного вещества для длительного эффекта и способ обеспечения длительного эффекта, например введение один раз в день обеспечивает оптимальную абсорбцию активного вещества через желудочно-кишечный тракт, т.е. от желудка до прямой кишки.
Не существует общего решения для успешного подавления окислительной деструкции материалов матрицы, таких как полиэтиленоксид и чувствительных к окислению лекарствах в фармацевтических лекарственных формах. Комплекс отдельных механизмов окисления, который важен для конкретного материала матрицы или лекарства, а также множество возможных факторов, которые оказывают влияние на окислительные процессы, требуют обширных исследований в каждом конкретном случае с учетом конкретных обстоятельств. Возможными способами защиты лекарственной формы от процессов окислительной деструкции является добавление антиоксидантов, хранение в инертной атмосфере или применение пленочного покрытия в качестве противокислородной защиты. Последние два метода, однако, трудно применять на всех этапах производственного процесса.
Далее известно, что процессы окислительной деструкции особенно ускоряются, когда лекарственные формы подвергаются жестким условиям процесса, например, во время производственного процесса. Например, высокомолекулярный полиэтиленоксид имеет тенденцию деструктировать при экструзии горячего расплава. Полимерная деструкция, тем не менее, может привести к неконтролируемой кривой высвобождения, в частности, когда активный ингредиент внедрен в матрицу полиэтиленоксида, и это может быть еще одной причиной для окислительной деструкции фармакологически активных ингредиентов радикалами. Когда добавляют подходящие вспомогательные вещества с целью стабилизации высокомолекулярного полиэтиленоксида, такого как α-токоферол, должно быть принято во внимание, что указанные вспомогательные вещества в свою очередь могут иметь отрицательное влияние на стабильность других ингредиентов фармацевтических препаратов, например, фармакологически активного соединения.
Целью настоящего изобретения является обеспечение устойчивых к взлому фармацевтических лекарственных форм, содержащих фармакологически активные ингредиенты, в частности чувствительные к окислению опиоиды, которые имеют преимущества по сравнению с фармацевтическими лекарственными формами, известными из уровня техники. Фармацевтические лекарственные формы должны иметь улучшенную стабильность при хранении, так что они могут содержать чувствительные к окислению опиоиды, даже при сравнительно низких дозах. Кроме того, должна быть возможность готовить фармацевтические лекарственные формы обычным путем при обычных условиях, таких как повышенная температура и давление (например, в ходе термоформования экструзией горячего расплава).
Эта задача была решена объектом изобретения, изложенным в формуле изобретения.
Изобретение относится к термоформируемой фармацевтической лекарственной форме, которая имеет сопротивление разрушению по крайней мере 300 Н и включает
- фармакологически активный ингредиент (А),
- свободную физиологически приемлемую кислоту (В) в количестве от 0.001 до 5.0 мас.%, основанную на общей массе фармацевтической лекарственной формы, и
- полиалкиленоксид (С), который имеет среднемассовую молекулярную массу Mw по крайней мере 200,000 г/моль.
Неожиданно было обнаружено, что фармацевтические лекарственные формы, которые содержат полимеры, которые поддаются окислительной деструкции, такие как высокомолекулярный полиэтиленоксид можно предотвратить от окислительной деструкции и разрушения наличием подходящего количества кислоты (В) в фармацевтических лекарственных формах согласно изобретению. С помощью этого метода неожиданно было обнаружено, что определенные свойства материала лекарственной формы согласно изобретению, такие как сопротивление разрушению и замедленное высвобождение активного ингредиента могут быть сохранены в течении более длительного периода хранения.
Таким образом, повышенная стабильность полимерной матрицы отражена улучшенной стабильностью in vitro кривой высвобождения при хранении и/или улучшенной стабильностью механических свойств лекарственных форм. Оба свойства существенно зависят от материала полимерной матрицы.
Еще неожиданно было обнаружено, что некоторые производные морфинана, такие как оксиморфон являются окислительно деструктированными до N-оксидов (например, оксиморфон-N-оксид, N-оксиды в общем часто говорят являются токсичными и возможно канцерогенными) при производстве и хранении соответствующих лекарственных форм и что формирование указанных N-оксидов и других продуктов разложения может быть подавлено наличием подходящего количества кислоты (В) в фармацевтических лекарственных формах согласно изобретению.
Таким образом, увеличилась стабильность при хранении фармакологически активного ингредиента (А), что отражается уменьшением примесей, если таковые имеются и соответственно снижением уменьшения фармакологически активного ингредиента (А) во время хранения, если таковое происходит.
Хотя это не предназначено, для привязки к какой-либо теории, кислота (В) имеет влияние на значение микро-рН фармацевтического препарата, тем самым каким-то образом увеличивая его стабильность при хранении. Таким образом, насколько стабильность при хранении фармакологически активного ингредиента связана, стабилизирующий эффект кислоты (В) можно коррелировать с помощью значения pKA чувствительных к окислению лекарств. Например, значение pKA оксиморфона составляет 8.3. Обычные композиции оксиморфона, которые являются устойчивыми к взлому из-за их повышенного сопротивление разрушению, но которые не показывают желаемого срока хранения, дают значениие рН около 7.5, будучи диспергированными в воде. В этих условиях значительное количество оксиморфона присутствует в виде свободного основания (т.е. не протонированного), который может быть более чувствителен к окислению, чем (протонированная) солевая форма.
Эта концепция подтверждается также тем, что в отсутствие кислоты (В), лекарственные формы, как правило, имеют желтоватый, бежевый цвет, в то время как присутствие кислоты (В) приводит к более белым, например бесцветным таблеткам. Таким образом, присутствие кислоты (В) может уменьшить значение рН в пределах лекарственной формы, повышая таким образом стойкость лекарства и/или полимерную стойкость к окислительной деструкции.
По-видимому, кислотный характер кислоты (В) несет ответственность за его стабилизирующий эффект, но не за другие свойства. Эта концепция подтверждается тем фактом, что неорганические, также как органические кислоты оба повышают стабильность при хранении лекарственной формы. Неожиданно было обнаружено, что фармацевтические вспомогательные вещества, которые обычно применяют в целях улучшения устойчивости лекарства к окислительному разрушению, в особенности некоторые антиоксиданты, например, α-токоферол, могут быть анти-производительными и в значительной степени ухудшать, чем улучшать стабильность лекарства к окислительному разрушению.
Фигура 1 показывает in vitro кривую высвобождения фармацевтических лекарственных форм согласно изобретению примеры L1 и L3 и сравнительные примеры L2 и L4.
Фармацевтическая лекарственная форма согласно изобретению является темоформируемой, преимущественно путем экструзии, хотя также другие методы термоформования могут быть использованы в целях производства фармацевтической лекарственной формы согласно изобретения, такие как литье под давлением при повышенной температуре или нагревание таблеток, которые были изготовлены обычным сжатием на первом этапе и затем нагреваются выше температуры размягчения полимера в таблетке на втором этапе для формирования твердых таблеток. В преимущественном воплощении, фармацевтическая лекарственная форма является термоформируемой экструзией горячего расплава.
Преимущественно, фармацевтическая лекарственная форма представляет собой монолитную массу. Фармацевтическая лекарственная форма является преимущественно полученной путем экструзии горячего расплава. Расплав экструдированных стренг преимущественно нарезают в монолиты, которые затем преимущественно формируют в таблетки. В этой связи термин "таблетки" преимущественно не стоит понимать как лекарственные формы, которые были сделаны путем сжатия порошка или гранул (сжимаемость), а скорее, как форму эктрудатов.
Фармацевтическая лекарственная форма согласно изобретению содержит как компонент (А) фармакологически активный ингредиент (А), преимущественно чувствительный к окислению фармакологический активный ингредиент. Для целей описания, термин фармакологически активный ингредиент (А) также включает свободное основание и его физиологически приемлемые соли.
Для целей описания термин чувствительный к окислению фармакологически активный ингредиент включает все фармакологически активные ингредиенты, которые содержат одну или более функциональную группу, которая окисляется в процессе окислительной деструкции. Функциональные группы, чье окисление может привести фармакологически активный ингредиент к нестабильности по отношению к окислению, имеют двойные связи, кроме того, альдегидо, кето, гидроксильные группы, эфир ендиол, фенол и аминогруппы.
Лекарственная форма согласно изобретению в частности предпочтительно содержит один или более фармакологически активных ингредиентов (А), которые выбраны из группы, которая состоит из
- агенты для лечения и профилактики заболеваний пищеварительной системы и обмена веществ [А]; в частности, стоматологические препараты [А01], агенты для лечения и профилактики кислотнозависимых заболеваний [А02], агенты для лечения и профилактики функциональных расстройств желудочно-кишечного тракта [А03], серотонин 5НТЗ антагонисты [А04АА], антигистаминные препараты [А04АВ], агенты для терапии желчи и печени [А05], слабительные средства [А06], противоинфекционные препараты для желудочно-кишечного тракта [А07А], кишечные адсорбирующие препараты [А07В], электролиты с углеводами [А07С], противовоспалительные препараты для желудочно-кишечного тракта [А07Е], микробные антидиарейные средства [A07F], дижестивы, включающие энзимы [А09], препараты для лечения сахарного диабета [А10], витамины [АН], минералы [А12], анаболические средства для системного применения [А14] и стимуляторы аппетита [А15];
- агенты для лечения и профилактики заболеваний крови и кроветворных органов [В]; в частности антитромботические агенты [В01], останавливающие кровотечение [В02], противоанемические препараты [В03] и другие гематологические агенты [В06];
- агенты для лечения и профилактики заболеваний кардиоваскулярной системы [С]; в частности агенты для сердечной терапии [С01], противогипертонические лекарства [С02], мочегонные средства [С03], периферические сосудорасширяющие средства [С04], сосудозащищающие вещества [С05], антигипотензивные вещества [С06А], β-адренорцептора антагонисты [С07], блокаторы кальциевых канальцев [С08], агенты, воздействующие на ренин-ангиотензиновую систему [С09] и липидные восстанавливающие агенты [С10];
- дерматологические средства [D]; в частности противогрибковые средства для системного применения [D01B], антипсориатические вещества для системного применения [D05B], противоугревые препараты для системного применения [D10B];
- агенты для лечения и профилактики заболеваний мочеполовой системы и половых гормонов [G]; в частности гинекологические антимикробные средства и антисептики [G01], препараты, повышающие тонус миометрия [G02A], симпатомиметические супрессоры родовой деятельности [G02CA], ингибиторы пролактина [G02CB], гормональные контрацептивы для систематического применения [G03] и урологические средства [G04];
- системные гормональные препараты за исключением половых гормонов и инсулинов [Н]; в частности гипофизные и гипоталамические гормоны и аналоги [Н01], кортикостероиды для системного применения [Н02], препараты для щитовидной железы [Н03], гормоны поджелудочной железы [Н04], и агенты для регулирования гомеостаза кальция [Н05];
- противомикробные средства для системного применения [J]; в частности антибиотики для системного применения [J01], противогрибковые средства для системного применения [J02], антимикробактериальные вещества [J04], антивирусные препараты для системного применения [J05], антисыворотка и иммуноглобулины [J06], и вакцины [J07]);
- противоопухолевые и иммуномодулирующие средства [L] (в частности антинеопластические агенты [L01], агенты для эндокринной терапии [L02], иммуностимулирующие средства [L03] и иммуноподавляющие агенты [L04];
- агенты для лечения и профилактики заболеваний мускульно-костной системы [М]; в частности противовоспалительные и противоревматические средства [М01], мышечные релаксанты периферического действия [М03А], мышечные релаксанты прямого действия [М03С], противоподагрические препараты [М04] и агенты для лечения костных заболеваний [М05];
- агенты для лечения и профилактики заболеваний нервной системы [N]; в частности салициловая кислота, ее производные [N02BA], пиразолоны [N02BB], анилиды [N02BE], алкалоиды спорыньи [N02CA], производные кортикостероидов [N02CB], селективные агонисты серотинина-5НТ1 [N02CC], производные гидантоина [N03AB], производные оксазолидина [N03AC], производные сукцинимида [N03AD], производные карбоксамида [N03AF], производные жирных кислот [N03AG], лекарства против паркинсона [N04]), нейролептические препараты [N05A], антидепрессанты [N06A], лекарства от умственного снижения [N06D], парасимпатомиметики [N07A] и препараты против головокружения [N07C];
- противопаразитарные продукты, инсектициды и репелленты [Р]; в частности антипротозойные агенты [Р01], глистогонные средства [Р02] и электропаразитициды, включая средства от чесотки, инсектициды и репелленты [Р03];
- агенты для лечения и профилактики заболеваний респираторной системы [R]; в частности назальные препараты [R01], горловые препараты [R02], лекарства для обструктивных заболеваний дыхательных путей [R03], отхаркивающие средства, за исключением комбинаций средств от кашля [R05C] и антигистаминных средств для системного применения [R06];
- агенты для лечения и профилактики заболеваний органов чувств [S]; в частности отологические агенты [S02]; и
- продукты общей диеты [V06] и терапевтические радиофармпрепараты [V10],
где аббревиатуры, находящиеся в квадратных скобках здесь (и далее) соответствуют АТС Индексу, который используется как WHO для классификации фармацевтических веществ (предпочтительная версия: 2010).
В предпочтительном воплощении, лекарственная форма согласно изобретению содержит один или более фармакологически активных ингредиентов (А), выбранных из группы, которая состоит из агентов для сердечной терапии [С01], предпочтительно выбранных из группы, которая состоит из сердечных гликозидов [С01А], антиаритмических препаратов, класса i и iii [C01B], сердечных стимуляторов за исключением сердечных гликозидов [C01C], сосудорасширяющих средств, используемых при сердечных заболеваниях [C01D], и другие сердечные препараты [С01Е].
В другом предпочтительном воплощении, лекарственная форма согласно изобретению содержит один или более фармакологически активных ингредиентов (А), которые выбраны из группы, которая состоит из из противогипертонических средств [С02], предпочтительно выбранных из группы, которая состоит из антиадренергических веществ центрального действия [С02А], антиадренергических веществ, блокирующих кистозные образования [С02В], антиадренергических веществ поверхностного действия [С02С], агентов воздействующих на артериолярные гладкие мышцы [C02D], другие противогипертонические средства [С02К], противогипертонические средства и диуретические средства в сочетании [C02I], и комбинации противогипертонических средств in atc-gr. C02 [C02N].
В еще другом предпочтительном воплощении, лекарственная форма согласно изобретению содержит один или более фармакологически активных ингредиентов (А), которые выбраны из группы, которая состоит из диуретических средств [С03], предпочтительно выбранных из группы, которая состоит из низко-насыщаемых диуретических средств, тиазидов [С03А], низконасыщаемых диуретических средств, за исключением таизидов [С03В], высоконасыщаемых диуретических средств [С03С], калийсберегающих мочегонных средств [C03D], диуретических средств и калийсберегающих мочегонных средств в сочетании [С03Е], и других диуретических средств [С03Х].
В еще другом предпочтительном воплощении, лекарственная форма согласно изобретению содержит один или более фармакологически активных ингредиентов (А), которые выбраны из группы, которая состоит из средств с сосудорасширяющим фактором периферийного действия [С04], предпочтительно выбранные из группы, которая состоит из сосудорасширяющих средств периферийного действия [С04А].
В еще другом предпочтительном воплощении, лекарственная форма согласно изобретению содержит один или более фармакологически активных ингредиентов (А) которые выбраны из группы, которая состоит из сосудозащищающих средств [С05], предпочтительно выбраны из группы, которая состоит из агентов для лечения геморроидальных узлов и анальных трещин для местного применения [С05А], противоварикозной терапии [С05В], и капиллярных стабилизаторов [С05С].
В еще другом предпочтительном воплощении, лекарственная форма согласно изобретению содержит один или более фармакологически активных ингредиентов (А), которые выбраны из группы, которая состоит из антигипотензивных средств [С06А].
В еще другом предпочтительном воплощени, лекарственная форма согласно изобретению содержит один или более фармакологически активных ингредиентов (А), которые выбраны из группы, которая состоит из антагонистов □адренорецепторов [С07], предпочтительно выбранных из группы, которая состоит из бэта блокирующих агентов [С07А], бэта блокирующих агентов и тиазидов [С07В], бэта блокирующих агентов и других диуретических средств [С07С], бэта блокирующих агентов, тиазидов и других диуретических средств [C07D], бэта блокирующих агентов и сосудорасширяющих средств [С07Е], и бэта блокирующих агентов и других противогипертонических средств [C07F].
В еще другом предпочтительном воплощении, лекарственная форма согласно изобретению содержит один или более фармакологически активных ингредиентов (А) которые выбраны из группы, которая состоит из блокаторов кальциевых канальцев [С08], предпочтительно выбраны из группы, которая состоит из селективных блокаторов кальциевых канальцев с преимущественными сосудистыми эффектами [С08С], селективных блокаторов кальциевых канальцев с направленными сердечными эффектами [C08D], неселективных блокаторов кальциевых канальцев [С08Е], и блокаторов кальциевых канальцев и мочегонных средств [C08G].
В еще другом предпочтительном воплощении, лекарственная форма согласно изобретению содержит один или более фармакологически активных ингредиентов (А), которые выбраны из группы, которая состоит из агентов, действующих на ренин-ингиотензиновую систему [С09], предпочтительно выбранные из группы, которая состоит из АПФ ингибиторов, обычных [С09А], АПФ ингибиторов, комбинаций [С09В], антагонистов ангиотензина ii, обычных [С09С], антагонистов ангиотензина ii, комбинаций [C09D], и других агентов, воздейтствующих на ренин-ингиотензиновую систему [С09Х].
В еще предпочтительном воплощении, лекарственная форма согласно изобретению содержит один или более фармакологически активных ингредиентов (А), которые выбраны из группы, которая состоит из липидных восстанавливающих агентов [с10], предпочтительно выбраны из группы, которая состоит из липидных модифицирующих агентов, обычных [С10А], и липидных модифицирующих агентов, комбинаций [С10В].
В преимущественном воплощении, фармакологически активным ингредиентом (А) является ингибитор ангиотензинпревращающего фермента (АПФ), более предпочтительно АПФ-ингибитор выбран из группы, включающей беназеприл, каптоприл, цилазаприл, эналаприл, фзиноприл, имидаприл, лизиноприл, моэксиприл, периндоприл, хинаприл, рамиприл, спираприл, трандолаприл и зофеноприл.
В другом преимущественном воплощении, фармакологически активным ингредиентом является опиоид, более предпочтительно чувствительный к окислению опиоид, наиболее предпочтительно оксиморфон или оксикодон.
Согласно индексу АТС, опиоиды делятся на природные алкалоиды опиума, производные фенилпиперидина, производные дифенилпропиламина, производные бензоморфана, производные орипавина, производные морфинана и другие. Примерами природных алкалоидов опиума является морфин, опиум, никоморфин, оксикодон, дигидрокодеин, диаморфин, пантопон и кодеин. Дополнительными опиоидами (А) являются, например, этилморфин, гидрокодон, оксиморфон, и их физиологически приемлемые производные или соединения, преимущественно их соли и сольваты, преимущественно их гидрохлориды, физиологически приемлемые энантиомеры, стереоизомеры, диастереомеры и рацематы и их физиологически приемлемые производные, преимущественно этеры, эстеры или амиды.
Дополнительные преимущественные опиоиды включают N-(1-метил-2-пиперидиноэтил)-N-(2-пиридил)пропионамид, (1R,2R)-3-(3-диметиламино-1-этил-2-метил-пропил)фенол, (1R,2R,4S)-2-(диметиламино)метил-4-(р-фторбензилокси)-1-(m-метоксифенил)циклогексанол, (1R,2R)-3-(2-диметиламинометил-циклогексил)фенол, (1S,2S)-3-(3-диметиламино-1-этил-2-метил-пропил)фенол, (2R,3R)-1-диметиламино-3(3-метоксифенил)-2-метил-пентан-3-ол, (1RS,3RS,6RS)-6-диметиламинометил-1-(3-метоксифенил)-циклогексан-1,3-диол, преимущественно как рацемат, 3-(2-диметиламинометил-1-гидрокси-циклогексил)фенил 2-(4-изобутил-фенил)пропионат, 3-(2-диметиламинометил-1-гидрокси-циклогексил)фенил 2-(6-метокси-нафтален-2-ил)пропионат, 3-(2-диметиламинометил-циклогекс-1-энил)-фенил 2-(4-изобутил-фенил)пропионат, 3-(2-диметиламинометил-циклогекс-1-энил)-фенил 2-(6-метокси-нафтален-2-ил)пропионат, 3-(2-диметиламинометил-1-гидрокси-циклогексил)-фениловый сложный эфир (RR-SS)-2-ацетокси-4-трифторметил-бензойной кислоты, 3-(2-диметиламинометил-1-гидрокси-циклогексил)-фениловый сложный эфир (RR-SS)-2-гидрокси-4-трифторметил-бензойной кислоты, 3-(2-диметиламинометил-1-гидрокси-циклогексил)-фенил сложный эфир (RR-SS)-4-хлоро-2-гидрокси-бензойной кислоты, 3-(2-диметиламинометил-1-гидрокси-циклогексил)-фениловый сложный эфир (RR-SS)-2-гидрокси-4-метил-бензойной кислоты, 3-(2-диметиламинометил-1-гидрокси-циклогексил)-фениловый сложный эфир (RR-SS)-2-гидрокси-4-метокси-бензойной кислоты, 3-(2-диметиламинометил-1-гидрокси-циклогексил)-фенил сложный эфир (RR-SS)-2-гидрокси-5-нитро-бензойной кислоты, 3-(2-диметиламинометил-1-гидрокси-циклогексил)-фенил сложный эфир (RR-SS)-2',4'-дифторо-3-гидрокси-бифенил-4-карбоновой кислоты, 1,1-(3-диметиламино-3-фенилпентаметилен)-6-фтор-1,3,4,9-тетрагидропропан[3,4-b]индол, в частности его гемицитрат; 1,1-[3-диметиламино-3-(2-тиенил)пентаметилен]-1,3,4,9-тетрагидропропан[3,4-b]индол, в частности его цитрат; и 1,1-[3-диметиламино-3-(2-тиенил)пентаметилен]-1,3,4,9-тетрагидропропан[3,4-b]-6-фторо-индол, в частности его гемицитрат, и соответствующие стереоизомерные соединения, в каждом случае их соответствующие производные, физиологически приемлемые энантиомеры, стереоизомеры, диастереомеры и рацематы и их физиологически приемлемые производные, например этеры, эстеры или амиды, и в каждом случае их физиологически приемлемые соединения, в частности их соли и сольваты, например гидрохлориды.
Преимущественные опиоиды представлены общей формулой (I)
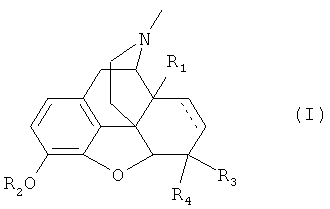
где
R1 представляет собой -Н, -ОН или -OC1-6-алкил;
R2 представляет собой -Н или -C1-6-алкил;
R3 представляет собой -Н или -ОН и R4 представляет собой -Н; или R3 и R4 вместе =O; и
---- представляет собой необязательно двойную связь;
или их физиологические соли.
В частности, преимущественные опиоиды включают оксиморфон, оксикодон, гидроморфон и их приемлемые физиологические соли.
В другом преимущественном воплощении, тем не менее, фармацевтическая лекарственная форма согласно изобретению не содержит ни одного опиоида, преимущественно ни одного чувствительного к окислению опиоида, как указано выше.
Содержание фармакологически активного ингредиента (А) в фармацевтической лекарственной форме является не ограниченным.
Преимущественно, его содержание находится в пределах от около 0.01 до 80 мас.%, более предпочтительно от 0.1 до 50 мас.%, еще более предпочтительно от 1 до 25 мас.%, основанного на общей массе фармацевтической лекарственной формы. В преимущественном воплощении, содержание фармакологически активного ингредиента (А) находится в диапазоне около 7±6 мас.%, более предпочтительно 7±5 мас.%, еще более предпочтительно 5±4 мас.%, 7±4 мас.% или 9±4 мас.%, наиболее предпочтительно 5±3 мас.%, 7±3 мас.% или 9±3 мас.%, и в частности 5±2 мас.%, 7±2 мас.% или 9±2 мас.%, основанного на общей массе фармацевтической лекарственной формы. В другом преимущественном воплощении, содержание фармакологически активного ингредиента (А) находится в пределах около 11±10 мас.%, более предпочтительно 11±9 мас.%, еще более предпочтительно 9±6 мас.%, 11±6 мас.%, 13±6 мас.% или 15±6 мас.%, наиболее предпочтительно 11±4 мас.%, 13±4 мас.% или 15±4 мас.%, и в частности 11±2 мас.%, 13±2 мас.% или 15±2 мас.%, основанного на общей массе фармацевтической лекарственной формы. В еще одном предпочтительном варианте, содержание фармакологически активного ингредиента (А) находится в пределах около 20±6 мас.%, более предпочтительно 20±5 мас.%, еще более предпочтительно 20±4 мас.%, наиболее предпочтительно 20±3 мас.%, и в частности 20±2 мас.%, основанного на общей массе фармацевтической лекарственной формы.
Преимущественно, общее количество фармакологически активного ингредиента (А), которое содержится в фармацевтической лекарственной форме находится в пределах от 0.01 до 200 мг, более предпочтительно от 0.1 до 190 мг, еще более предпочтительно от 1.0 до 180 мг, еще более предпочтительно от 1.5 до 160 мг, наиболее предпочтительно от 2.0 до 100 мг и, в частности, от 2.5 до 80 мг.
В предпочтительном воплощении, фармакологически активный ингредиент (А), содержится в фармацевтической лекарственной форме в количестве около 7.5±5 мг, 10±5 мг, 20±5 мг, 30±5 мг, 40±5 мг, 50±5 мг, 60±5 мг, 70±5 мг, 80±5 мг, 90±5 мг, 100±5 мг, 110±5 мг, 120±5 мг, 130±5 мг, 140±5 мг, 150±5 мг, или 160±5 мг. В другом предпочтительном варианте, фармакологически активный ингредиент (А) содержится в фармацевтической лекарственной форме в количестве около 5±2.5 мг, 7.5±2.5 мг, 10±2.5 мг, 15±2.5 мг, 20±2.5 мг, 25±2.5 мг, 30±2.5 мг, 35±2.5 мг, 40±2.5 мг, 45±2.5 мг, 50±2.5 мг, 55±2.5 мг, 60±2.5 мг, 65±2.5 мг, 70±2.5 мг, 75±2.5 мг, 80±2.5 мг, 85±2.5 мг, 90±2.5 мг, 95±2.5 мг, 100±2.5 мг, 105±2.5 мг, 110±2.5 мг, 115±2.5 мг, 120±2.5 мг, 125±2.5 мг, 130±2.5 мг, 135±2.5 мг, 140±2.5 мг, 145±2.5 мг, 150±2.5 мг, 155±2.5 мг, или 160±2.5 мг.
В особенно предпочтительном варианте фармакологически активным ингредиентом (А), преимущественно опиоидом является оксиморфон, предпочтительно его HCl соль, и фармацевтическая лекарственная форма адаптирована для введения дважды в день. В этом варианте, опиоид (А) преимущественно содержится в фармацевтической лекарственной форме в количестве от 5 до 40 мг. В другом, особенно предпочтительном варианте, фармакологически активным ингредиентом (А), преимущественно опиоидом является оксиморфон, преимущественно его HCl соль, и фармацевтическая лекарственная форма является адаптированной для введения один раз в день. В этом варианте, фармакологически активный ингредиент (А), преимущественно опиоид преимущественно содержится в фармацевтической лекарственной форме в количестве от 10 до 80 мг.
В другом, особенно предпочтительном варианте, фармакологически активным ингредиентом (А), предпочтительно опиоидом является оксикодон, преимущественно его HCl соль, и фармацевтическая лекарственная форма является адаптированной для введения дважды в день. В этом варианте фармакологически активный ингредиент (А), преимущественно опиоид, преимущественно содержится в фармацевтической лекарственной форме в количестве от 5 до 80 мг. В другом, особенно предпочтительном варианте, фармакологически активным ингредиентом (А), преимущественно опиоидом является оксикодон, преимущественно его HCl соль, и фармацевтическая лекарственная форма является адаптированной для введения один раз в день. В этом варианте фармакологически активный ингредиент (А), преимущественно опиоид, преимущественно содержится в фармацевтической лекарственной форме в количестве от 10 до 320 мг.
В еще одном особенно предпочтительном варианте фармакологически активным ингредиентом (А), преимущественно опиоидом, является гидроморфон, преимущественно его HCl соль, и фармацевтическая лекарственная форма является адаптированной для введения два раза в день. В этом варианте фармакологически активный ингредиент (А), преимущественно опиоид, преимущественно содержится в фармацевтической лекарственной форме в количестве от 2 до 52 мг. В другом особенно предпочтительном варианте, фармакологически активным ингредиентом (А), преимущественно опиоидом, является гидроморфон, преимущественно его HCl соль, и фармацевтическая лекарственная форма является адаптированной для введения один раз в день. В этом воплощении, фармакологически активный ингредиент (А), предпочтительно опиоид, предпочтительно содержится в фармацевтической лекарственной форме в количестве от 4 до 104 мг.
Фармацевтическая лекарственная форма согласно изобретению характеризуется отличной стабильностью при хранении.
Преимущественно, после хранения на протяжении 4 недель при 40°С и 75% отн. влажности, содержание фармакологически активного ингредиента (А), преимущественно опиоида, составляет не менее 98.0%, более предпочтительно, по крайней мере, 98.5%, еще более предпочтительно, по крайней мере, 99.0%, еще более предпочтительно по крайней мере 99.2%, наиболее предпочтительно по крайней мере 99.4% и в частности по крайней мере 99.6%, первоначального состава после хранения. Подходящие методы для измерения содержания фармакологически активного ингредиента (А) в фармацевтической лекарственной форме известны специалистам в данной области. В этой связи делается ссылка на Eur. Ph. (The European Pharmacopoeia) или USP (The United States Pharmacopeia), особенно на обращенную фазу ВЭЖХ анализа. Предпочтительно, фармацевтическая лекарственная форма хранится в закрытых, преимущественно плотно закрытых емкостях, преимущественно как описано в экспериментальной части, наиболее предпочтительно емкости оснащены поглотителем кислорода, который является эффективным даже при низкой относительной влажности.
Преимущественно, после хранения на протяжении 4 недель при 40°С и 75% отн. влажности, содержание материала матрицы, преимущественном полиалкиленоксида (С) составляет, по крайней мере, 98.0%, более предпочтительно, по крайней мере, 98.5%, еще более предпочтительно, по крайней мере, 99.0%, еще более предпочтительно по крайней мере 99.2%, наиболее предпочтительно по крайней мере 99.4% и в частности по крайней мере 99.6%, первоначального состава перед хранением. Подходящие методы для измерения содержания полиалкиленоксида (С) в фармацевтической лекарственной форме известны специалистам в данной области. В этой связи делается ссылка на Eur. Ph. или USP, особенно на обращенную фазу ВЭЖХ анализа.
Преимущественно, после хранения на протяжении 4 недель при 40°С и 75% отн. влажности, среднемассовая молекулярная масса полиалкиленоксида (С) составляет по крайней мере 70%, более предпочтительно по крайней мере 75%, еще более предпочтительно по крайней мере 80%, еще более предпочтительно по крайней мере 85%, наиболее предпочтительно по крайней мере 90% и в частности по крайней мере 95%, его первоначальной среднемассовой молекулярной массы перед хранением.
Подходящие методы для определения среднемассовой молекулярной массы полиалкиленоксида (С) в фармацевтической лекарственной форме известны специалистам в данной области. Изменение среднемассовой молекулярной массы полиалкиленоксида (С) может, например, быть оценено измерением вязкости после набухания лекарственной формы.
Неожиданно было обнаружено, что кислота (В) не только улучшает стабильность при хранении лекарственной формы, но также улучшает пригодность для переработки фармацевтических наполнителей, предпочтительно полиалкиленоксида (С) на производстве, в частности, в ходе термоформования, такого как экструзия горячего расплава. Существуют сравнительные экспериментальные доказательтва того, что из-за наличия кислоты (В) снижение вязкости полимера (С), которое обычно происходит при экструзии горячего расплава существенно снижается, когда кислота (В) присутствует в подходящих количествах.
Преимущественно, лекарственная форма согласно изобретению содержит кислоту (В) в таком количестве, что в ходе экструзии горячего расплава все вспомогательные вещества и ингредиенты в таком количестве, что в ходе экструзии горячего расплава всех вспомогательных веществ и ингредиентов вязкость геля однородного геля, приготовленного из лекарственной формы составляет по крайней мере 50%, более предпочтительно по крайней мере 60%, еще более предпочтительно, по крайней мере, 70%, еще более предпочтительно по крайней мере 80%, даже более предпочтительно по крайней мере 85%, наиболее предпочтительно по крайней мере 90% и в частности по крайней мере 95% вязкости геля однородного геля приготовленного из смеси всех вспомогательных веществ и ингредиентов лекарственной формы, но которые не поддавались экструзии горячего расплава. Более того, лекарственная форма согласно изобретению преимущественно содержит кислоту (В) в таком количестве, что после хранения лекарственной формы на протяжении 3 месяцев в ускоренных условиях хранения вязкость геля однородного геля приготовленного из лекарственной формы составляет, по крайней мере, 50%, более предпочтительно, по крайней мере, 60%, еще более предпочтительно, по крайней мере, 70%, еще более предпочтительно, по крайней мере, 80%, даже более предпочтительно по крайней мере 85%, наиболее предпочтительно по крайней мере 90% и в частности по крайней мере 95% вязкости геля однородного геля приготовленного из лекарственной формы перед хранением. Предпочтительно, чтобы условия экструзии были определены как в экспериментальной части. При подготовке однородного геля лекарственная форма, преимущественно является суспендированной в достаточном количестве воды так, чтобы в условиях окружающей среды (ротационный вискозиметр), вязкость получившегося однородного геля составляет около 500 мПа при 40 с-1 (диапазон линейности). Как только было определено подходящее количество воды путем предварительных испытания, все сравнительные испытания затем проводились при одинаковых условиях.
Предпочтительно, фармацевтическая лекарственная форма хранится в закрытых, преимущественно плотно закрытых емкостях, преимущественно как описано в экспериментальной части, наиболее предпочтительно емкости оснащены поглотителем кислорода, который является эффективным даже при низкой относительной влажности.
Фармацевтическая лекарственная форма согласно изобретению содержит, как компонент (В), свободную физиологически приемлемую кислоту в количестве от
0.001 до 5.0 мас.%, основанной на общей массе фармацевтической лекарственной формы.
Кислота может быть органической или неорганической, жидкой или твердой. Твердые кислоты являются предпочтительными, особенно кристаллические органические или неорганические кислоты.
Кислота (В) является свободной. Это означает, что кислотные функциональные группы кислоты (В) не все вместе являются составляющими соли фармакологически активного ингредиента (А). Если фармакологически активный ингредиент (А) присутствует в виде соли кислоты, например, в виде гидрохлорида, фармацевтическая лекарственная форма согласно изобретению преимущественно содержит как компонент (В) другую, химически отличающуюся кислоту, которая не присутствует в качестве составляющей соль фармакологически активного ингредиента (А). Другими словами, монокислоты, которые формируют соли с фармакологически активным ингредиентом (А) не следует рассматривать как свободные кислоты (В) в смысле настоящего изобретения. Когда кислота (В) имеет больше, чем одну кислотную функциональную группу (например, фосфорная кислота), кислота (В) может присутствовать в качестве составляющей соли фармакологически активного ингредиента (А), при условии, что, по крайней мере, одна из кислотных функциональных групп кислоты (В) не участвует в образовании соли, то есть является свободной. Преимущественно, тем не менее, все без исключения кислотные функциональные группы кислоты (В) не участвуют в образовании соли с фармакологически активным ингредиентом (А). Это также возможно, тем не менее, что свободная кислота (В) и кислота, формирующая соль с фармакологически активным ингредиентом (А) являются одинаковыми. В этих условиях кислота предпочтительно присутствует в молярном избытке по сравнению с фармакологически активным ингредиентом (А).
В преимущественном воплощении, кислота (В) содержит, по крайней мере, одну кислотную функциональную группу (например, -CO2H, -SO3H, -РО3Н2, -ОН и тому подобные), имеющую значение pKA в пределах диапазона 2.00±1.50, более предпочтительно 2.00±1.25, еще более предпочтительно 2.00±1.00, еще более предпочтительно 2.00±0.75, наиболее предпочтительно 2.00±0.50 и в частности 2.00±0.25. В другом предпочтительном воплощении, кислота содержит, по крайней мере одну кислотную функциональную группу, имеющую значение pKA в пределах диапазона 2.25±1.50, более предпочтительно 2.25±1.25, еще более предпочтительно 2.25±1.00, еще более предпочтительно 2.25±0.75, наиболее предпочтительно 2.25±0.50 и в частности 2.25±0.25. В другом предпочтительном воплощении, кислота (В) содержит, по крайней мере, одну кислотную функциональную группу, имеющую значение pKA в пределах диапазона 2.50±1.50, более предпочтительно 2.50±1.25, еще более предпочтительно 2.50±1.00, еще более предпочтительно 2.50±0.75, наиболее предпочтительно 2.50±0.50 и в частности 2.50±0.25. В другом предпочтительном воплощении, кислота (В) содержит, по крайней мере, одну кислотную функциональную группу, имеющую значение pKA в пределах диапазона 2.75±1.50, более предпочтительно 2.75±1.25, еще более предпочтительно 2.75±1.00, еще более предпочтительно 2.75±0.75, наиболее предпочтительно 2.75±0.50 и в частности 2.75±0.25. В другом предпочтительном воплощении, кислота (В) содержит, по крайней мере, одну кислотную функциональную группу, имеющую значение pKA в пределах диапазона 3.00±1.50, более предпочтительно 3.00±1.25, еще более предпочтительно 3.00±1.00, еще более предпочтительно 3.00±0.75, наиболее предпочтительно 3.00±0.50 и, в частности, 3.00±0.25. В еще одном предпочтительном варианте, кислота (В) содержит, по крайней мере, одну кислотную функциональную группу, имеющую значение pKA в пределах диапазона 3.25±1.50, более предпочтительно 3.25±1.25, еще более предпочтительно 3.25±1.00, даже более предпочтительно 3.25±0.75, наиболее предпочтительно 3.25±0.50 и в частности 3.25±0.25.
В еще одном предпочтительном варианте, кислота (В) содержит по крайней мере одну кислотную функциональную группу, имеющую значение pKA в пределах диапазона 4.50±1.50, более предпочтительно 4.50±1.25, еще более предпочтительно 4.50±1.00, еще более предпочтительно 4.50±0.75, наиболее предпочтительно 4.50±0.50 и в частности 4.50±0.25. В еще одном предпочтительном варианте, кислота (В) содержит по крайней мере одну кислотную функциональную группу, имеющую значение pKA в пределах диапазона 4.75±1.50, более предпочтительно 4.75±1.25, еще более предпочтительно 4.75±1.00, еще более предпочтительно 4.75±0.75, наиболее предпочтительно 4.75±0.50 и в частности 4.75±0.25. В еще одном предпочтительном варианте, кислота (В) содержит, по крайней мере, одну кислотную функциональную группу, имеющую значение pKA в пределах диапазона 5.00±1.50, более предпочтительно 5.00±1.25, еще более предпочтительно 5.00±1.00, еще более предпочтительно 5.00±0.75, наиболее предпочтительно 5.00±0.50 и в частности 5.00±0.25.
Предпочтительно, кислота (В) является органической карбоновой или сульфоновой кислотой, в частности, карбоновой кислотой. Многоосновные карбоновые кислоты и/или гидрокси-карбоновые кислоты являются особенно предпочтительными.
В случае многоосновной карбоновой кислоты неполные соли также следует рассматривать как многоосновные карбоновые кислоты, например, неполные соли натрия, калия или аммония. Например, лимонная кислота является многоосновной карбоновой кислотой, имеющей три карбоксильные группы. До тех пор, пока остается по крайней мере одна протонированная карбоновая группа (например, дигидроген цитрат-ион натрия или двунатриевый гидроген цитрат), соль следует рассматривать как многоосновную карбоновую кислоту. Предпочтительно, тем не менее, чтобы все карбоновые группы были протонированными.
Преимущественно, кислота (В) является низкомолекулярной, т.е. не полимеризуется. Как правило, молекулярная масса кислоты (В) ниже 500 г/мoль.
Примеры кислот включают насыщенные и ненасыщенные монокарбоновые кислоты, насыщенные и ненасыщенные бикарбоновые кислоты, трикарбоновые кислоты, α-гидроксикислоты и β-гидроксикислоты монокарбоновых кислот, α-гидрокси кислоты и β-гидроксикислоты бикарбоновых кислот, α-гидроксикислоты и β-гидроксикислоты трикарбоновых кислот, кетокислоты, α-кетокислоты, β-кетокислоты поликарбоновых кислот, полигидрокси монокарбоновых кислот, полигидрокси бикарбоновых кислот, полигидрокси трикарбоновых кислот.
Преимущественно, кислота (В) выбрана из группы, включающей такие кислоты как бензолсульфоновая кислота, лимонная кислота, α-глюкогептановая кислота, D-глюконовая кислота, гликолиевая кислота, молочная кислота, яблочная кислота, малоновая кислота, миндальная кислота, пропановая кислота, янтарная кислота, винная кислота (d, I, или dl), тозиловая кислота (толуолсульфоновая кислота), валериановая кислота, пальмитиновая кислота, памоевая кислота, себациновая кислота, стеариновая кислота, лауриновая кислота, уксусная кислота, адипиновая кислота, пентандиовая кислота, 4-хлоробензолсульфоновая кислота, этандисульфоновая кислота, этилсукциновая кислота, фумаровая кислота, галактаровая кислота (муциновая кислота), D-глюкуроновая кислота, 2-оксо-пентандиовая кислота, глицерофосфорная кислота, гиппуровая кислота, изэтионовая кислота (этансульфоновая кислота), лактобионовая кислота, малеиновая кислота, малеиновая кислота, 1,5-нафталене-дисульфоновая кислота, 2-нафталене-сульфоновая кислота, триметилуксусная кислота, терефталевая кислота, тиоциановая кислота, холевая кислота, п-додецилсульфат, 3-гидрокси-2-нафтойная кислота, 1-гидрокси-2- нафтойная кислота, масляная кислота, ундециленовая кислота, аскорбиновая кислота, (+)-камфорная кислота, d-камфорсульфокислота, дихлоруксусная кислота, этансульфоновая кислота, муравьиная кислота, метансульфоновая кислота, никотиновая кислота, оротовая кислота, щавелевая кислота, пикриновая кислота, L-пироглутаминовая кислота, сахарин, салициловая кислота, гентизиновая кислота, и/или 4-ацетамидобензойная кислота.
Содержание кислоты (В) находится в диапазоне от 0.001 до 5.0 мас.%, предпочтительно от 0.005 до 2.5 мас.%, более предпочтительно от 0.01 до 2.0 мас.%, еще более предпочтительно от 0.05 до 1.5 мас.%, наиболее предпочтительно от 0.1 до 1.0 мас.% и в частности от 0.2 до 0.9 мас.%, основанных на общей массе фармацевтической лекарственной формы.
Предпочтительно, кислота (В) является многоосновной карбоновой кислотой. Более предпочтительно, многоосновная карбоновая кислота выбрана из группы, включающей лимонную кислоту, малеиновую кислоту и фумаровую кислоту.
Лимонная кислота является преимущественно предпочтительной.
Многоосновная карбоновая кислота, преимущественно лимонная кислота, может быть в ее безводной форме или в виде сольвата и гидрата, соответственно, например, в виде моногидрата.
В преимущественном воплощении, содержание кислоты (В), преимущественно лимонной кислоты, находится в диапазоне 0.2±0.18 мас.%, более предпочтительно 0.2±0.15 мас.%, еще более предпочтительно 0.2±0.12 мас.%, еще более предпочтительно 0.2±0.09 мас.%, наиболее предпочтительно 0.2±0.06 мас.%, и в частности 0.2±0.03 мас.%, основанной на общей массе фармацевтической лекарственной формы.
В другом преимущественном воплощении, содержание кислоты (В), преимущественно лимонной кислоты, находится в диапазоне 0.3±0.18 мас.%, более предпочтительно 0.3±0.15 мас.%, еще более предпочтительно 0.3±0.12 мас.%, еще более предпочтительно 0.3±0.09 мас.%, наиболее предпочтительно 0.3±0.06 мас.%, и в частности 0.3±0.03 мас.%, основанной на общей массе фармацевтической лекарственной формы.
В еще одном преимущественном воплощении, содержание кислоты (В), преимущественно лимонной кислоты, находится в диапазоне 0.4±0.18 мас.%, более предпочтительно 0.4±0.15 мас.%, еще более предпочтительно 0.4±0.12 мас.%, еще более предпочтительно 0.4±0.09 мас.%, наиболее предпочтительно 0.4±0.06 мас.%, и в частности 0.4±0.03 мас.%, основанной на общей массе фармацевтической лекарственной формы.
В еще одном предпочтительном варианте, содержание кислоты (В), преимущественно лимонной кислоты, находится в диапазоне 0.5±0.18 мас.%, более предпочтительно 0.5±0.15 мас.%, еще более предпочтительно 0.5±0.12 мас.%, еще более предпочтительно 0.5±0.09 мас.%, наиболее предпочтительно 0.5±0.06 мас.%, и в частности 0.5±0.03 мас.%, основанной на общей массе фармацевтической лекарственной формы.
В еще одном предпочтительном варианте, содержание кислоты (В), преимущественно лимонной кислоты, находится в диапазоне 0.6±0.18 мас.%, более предпочтительно 0.6±0.15 мас.%, еще более предпочтительно 0.6±0.12 мас.%, еще более предпочтительно 0.6±0.09 мас.%, наиболее предпочтительно 0.6±0.06 мас.%, и в частности 0.6±0.03 мас.%, основанной на общей массе фармацевтической лекарственной формы.
В еще одном предпочтительном варианте, содержание кислоты (В), преимущественно лимонной кислоты, находится в диапазоне 0.7±0.18 мас.%, более предпочтительно 0.7±0.15 мас.%, еще более предпочтительно 0.7±0.12 мас.%, еще более предпочтительно 0.7±0.09 мас.%, наиболее предпочтительно 0.7±0.06 мас.%, и в частности 0.7±0.03 мас.%, основанной на общей массе фармацевтической лекарственной формы.
В еще одном предпочтительном варианте, содержание кислоты (В), преимущественно лимонной кислоты, находится в диапазоне 0.8±0.18 мас.%, более предпочтительно 0.8±0.15 мас.%, еще более предпочтительно 0.8±0.12 мас.%, еще более предпочтительно 0.8±0.09 мас.%, наиболее предпочтительно 0.8±0.06 мас.%, и в частности 0.8±0.03 мас.%, основанной на общей массе фармацевтической лекарственной формы.
В еще одном предпочтительном варианте, содержание кислоты (В), преимущественно лимонной кислоты, находится в диапазоне 0.85±0.18 мас.%, более предпочтительно 0.85±0.15 мас.%, еще более предпочтительно 0.85±0.12 мас.%, еще более предпочтительно 0.85±0.09 мас.%, наиболее предпочтительно 0.85±0.06 мас.%, и в частности 0.85±0.03 мас.%, основанной на общей массе фармацевтической лекарственной формы.
В еще одном предпочтительном варианте, содержание кислоты (В), преимущественно лимонной кислоты, находится в диапазоне 0.9±0.18 мас.%, более предпочтительно 0.9±0.15 мас.%, еще более предпочтительно 0.9±0.12 мас.%, еще более предпочтительно 0.9±0.09 мас.%, наиболее предпочтительно 0.9±0.06 мас.%, и в частности 0.9±0.03 мас.%, основанной на общей массе фармацевтической лекарственной формы.
В дополнительном предпочтительном варианте, содержание кислоты (В), преимущественно лимонной кислоты, находится в диапазоне 1.0±0.18 мас.%, более предпочтительно 1.0±0.15 мас.%, еще более предпочтительно 1.0±0.12 мас.%, еще более предпочтительно 1.0±0.09 мас.%, наиболее предпочтительно 1.0±0.06 мас.%, и в частности 1.0±0.03 мас.%, основанной на общей массе фармацевтической лекарственной формы.
Фармацевтическая лекарственная форма согласно изобретению включает как компонент (С) полиалкиленоксид (С), имеющий среднемассовую молекулярную массу Mw по крайней мере 200,000 г/моль, преимущественно по крайней мере 500,000 г/моль, более предпочтительно по крайней мере 750,000 г/моль, еще более предпочтительно по крайней мере 1,000,000 г/моль, наиболее предпочтительно по крайней мере 2,000,000 г/моль и в частности в диапазоне от 500,000 до 15,000,000 г/моль.
Преимущественно, полиалкиленоксиды выбраны из группы, включающей полиметиленоксид, полиэтиленоксид и полипропиленоксид, их сополимеры и смеси.
Полиалкиленоксид (С) может включать один полиалкиленоксид, имеющий в частности среднюю молекулярную массу, или смесь (композицию) различных полимеров, такую как два, три, четыре или пять полимеров, например, полимеры той же самой химической природы, но различной молекулярной массы, или полимеры различной химической природы, но одинаковой молекулярной массы, или полимеры различной химической природы, а также различной молекулярной массы.
Для целей описания, полиалкиленгликоль имеет молекулярную массу до 20,000 г/моль, тогда как полиалкиленоксид имеет молекулярную массу больше, чем 20,000 г/моль. В преимущественном воплощении, среднемасоовая величина всех молекулярных масс всех полиалкиленоксидов, содержащихся в фармацевтической лекарственной форме составляет, по крайней мере, 200,000 г/моль. Таким образом, полиалкиленгликоли, если таковые имеются, преимущественно не принимаются во внимание при определении среднемассовой молекулярной массы полиалкиленоксида (С).
Преимущественно, содержание полиалкиленоксида (С) находится в диапазоне от 20 до 99 мас.%, более предпочтительно от 25 до 95 мас.%, еще более предпочтительно от 30 до 90 мас.%, еще более предпочтительно от 30 до 85 мас.%, наиболее предпочтительно от 30 до 80 мас.% и в частности от 30 до 75 мас.%, основанного на общей массе фармацевтической лекарственной формы. В преимущественном воплощении, содержание полиалкиленоксида составляет по крайней мере 20 мас.%, более предпочтительно по крайней мере 25 мас.%, еще более предпочтительно по крайней мере 30 мас.%, еще более предпочтительно по крайней мере 35 мас.% и в частности по крайней мере 40 мас.%.
В преимущественном воплощении, общее содержание полиалкиленоксида (С) находится в диапазоне 25±20 мас.%, более предпочтительно 25±15 мас.%, наиболее предпочтительно 25±10 мас.%, и в частности 25±5 мас.%. В другом преимущественном воплощении, общее содержание полиалкиленоксида (С) находится в диапазоне 35±20 мас.%, более предпочтительно 35±15 мас.%, наиболее предпочтительно 35±10 мас.%, и в частности 35±5 мас.%. В еще одном предпочтительном варианте, общее содержание полиалкиленоксида (С) находится в диапазоне 45±20 мас.%, более предпочтительно 45±15 мас.%, наиболее предпочтительно 45±10 мас.%, и в частности 45±5 мас.%. В еще одном предпочтительном варианте, общее содержание полиалкиленоксида (С) находится в диапазоне 55±20 мас.%, более предпочтительно 55±15 мас.%, наиболее предпочтительно 55±10 мас.%, и в частности 55±5 мас.%. В дополнительном предпочтительном варианте, общее содержание полиалкиленоксида (С) находится в диапазоне 65±20 мас.%, более предпочтительно 65±15 мас.%, наиболее предпочтительно 65±10 мас.%, и в частности 65±5 мас.%. В еще одном предпочтительном варианте, общее содержание полиалкиленоксида (С) находится в диапазоне 75±20 мас.%, более предпочтительно 75±15 мас.%, наиболее предпочтительно 75±10 мас.%, и в частности 75±5 мас.%. В еще одном предпочтительном варианте, общее содержание полиалкиленоксида (С) находится в диапазоне 80±15 мас.%, более предпочтительно 80±10 мас.%, и наиболее предпочтительно 80±5 мас.%.
В преимущественном воплощении, полиалкиленоксид (С) является однородно распределенным в фармацевтической лекарственной форме согласно изобретению. Преимущественно, полиалкиленоксид (С) формирует матрицу, в которую опиоид (А) внедрен. В особенно предпочтительном варианте, опиоид (А) и полиалкиленоксид (С) тщательно гомогенно распределены в фармацевтической лекарственной форме так, что фармацевтическая лекарственная форма не содержит никаких сегментов, где любой опиоид (А) является присутствующим при том, что полиалкиленоксид (С) отсутствует или где полиалкиленоксид (С) присутствует в отсутствии опиоида (А).
Когда фармацевтическая лекарственная форма является покрытой пленкой, полиалкиленоксид (С) является преимущественно гомогенно распределенным в ядре фармацевтической лекарственной формы, т.е. пленочное покрытие не содержит полиалкиленоксида (С). Тем не менее, пленочное покрытие как таковое конечно может содержать один или более полимеров, которые, однако, преимущественно отличаются от полиалкиленоксида (С), содержащегося в ядре.
Полиалкиленоксид (С) может быть в сочетании с одним или более различными полимерами, выбранными из группы, включающей полиалкиленоксид, преимущественно полиметиленоксид, полиэтиленоксид, полипропиленоксид; полиэтилен, полипропилен, поливинилхлорид, поликарбонат, полистирол, поливинилпирролидон, поли(алк)акрилат, поли(гидрокси жирные кислоты), такие как например поли(3-гидроксибутират-ко-3-гидроксивалерат) (Biopol®), поли(гидроксивалериановая кислота); поликапролактон, поливиниловый спирт, полиамидоэфир, полиэтилен сукциннат, полилактон, полигликолид, полиуретан, полиамид, полилактид, полиацеталь (например, полисахариды, необязательно с модифицированными боковыми цепями), полилактид/гликолид, полилактон, полигликолид, полиортоэфир, полиангидрид, блок полимеры полиэтиленгликоля и полибутилентерефталата (Polyactive®), полиангидрид (Polifeprosan), их сополимеры, их блок-сополимеры, и смеси по крайней мере двух указанных полимеров, или других полимеров с указанными выше характеристиками.
Преимущественно, молекулярно-массовое распределение Mw/Mn полиалкиленоксида (С) находится в диапазоне 2.5±2.0, более предпочтительно 2.5±1.5, еще более предпочтительно 2.5±1.0, еще более предпочтительно 2.5±0.8, наиболее предпочтительно 2.5±0.6, и в частности 2.5±0.4.
Полиалкиленоксид (С) (исходный материал) преимущественно имеет вязкость при 25°С от 30 до 17,600 сП, более предпочтительно от 55 до 17,600 сП, еще более предпочтительно от 600 до 17,600 сП и наиболее предпочтительно от 4,500 до 17,600 сП, измеренной в 5 мас.% водного раствора с использованием модели RVF вискозиметра Брукфильда (шпиндель н. 2 / число оборотов 2 об/мин); от 400 до 4,000 сП, более предпочтительно от 400 до 800 сП или от 2,000 до 4,000 сП, измеренной в 2 мас.% водного раствора с использованием указанного вискозиметра (шпиндель н. 1 или 3 / число оборотов 10 об/мин); или от 1,650 до 10,000 сП, более предпочтительно от 1,650 до 5,500 сП, от 5,500 до 7,500 сП или от 7,500 до 10,000 сП, измеренной в 1 мас.% водного раствора с использованием указанного вискозиметра (шпиндель н. 2 / число оборотов 2 об/мин).
В преимущественном воплощении согласно изобретению полиалкиленоксид (С) имеет среднемассовую молекулярную массу по крайней мере 200,000 г/моль в сочетании с по крайней мере одним дополнительным полимером, преимущественно, но не обязательно также имеющим среднемассовую молекулярную массу (Mw) по крайней мере 200,000 г/моль, выбранным из группы, включающей полиэтилен, полипропилен, поливинилхлорид, поликарбонат, полистирол, полиакрилат, поли(гидрокси жирные кислоты), поликапролактон, поливиниловый спирт, полиамидоэфир, полиэтилен сукциннат, полилактон, полигликолид, полиуретан, поливинилпирролидон, полиамид, полилактид, полилактид/гликолид, полилактон, полигликолид, полиортоэфир, полиангидрид, блок полимеры полиэтиленгликоля и полибутилентерефталата, полиангидрид, полиацеталь, сложные эфиры целлюлозы, эфиры целлюлозы и их сополимеры. Сложные эфиры целлюлозы и эфиры целлюлозы являются преимущественно предпочтительными, например, метил целлюлоза, этил целлюлоза, гидроксиметилцеллюлоза, гидроксиэтилцеллюлоза, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, карбоксиметилцеллюлоза, и тому подобные.
В преимущественном воплощении, указанным дополнительным полимером не является полиалкиленоксид или полиалкиленгликоль. Тем не менее, фармацевтическая лекарственная форма может содержать полиалкиленгликоль, например, в качестве пластификатора, но затем фармацевтическая лекарственная форма преимущественно является тройной смесью полимеров: полиалкиленоксид (С)+дополнительный полимер + пластификатор.
В особенно предпочтительном воплощении указанным дополнительным полимером является гидрофильный эфир целлюлозы или эфир целлюлозы, преимущественно гидроксипропилметилцеллюлоза (ГПМЦ), гидрокси пропил целлюлоза (ГПЦ) или гидроксиэтилцеллюлоза (ГЭЦ), преимущественно имеющие среднюю величину вязкости (преимущественно измеряется капиллярной вискозиметрией или ротационной вискозиметрией) от 1,000 до 150,000 мПа·с, более предпочтительно от 3,000 до 150,000. В преимущественном воплощении имеющие средняя величина вязкости находится в диапазоне 110,000±50,000 мПа·с, более предпочтительно 110,000±40,000 мПа·с, еще более предпочтительно 110,000±30,000 мПа·с, наиболее предпочтительно 110,000±20,000 мПа·с, и в частности 100,000±10,000 мПа·с.
В преимущественном воплощении относительное соотношение массы указанного полиалкиленоксида (С) и указанного дополнительного полимера находится в диапазоне от 20:1 до 1:20, более предпочтительно от 10:1 до 1:10, еще более предпочтительно от 7:1 до 1:5, еще более предпочтительно от 5:1 до 1:1, наиболее предпочтительно от 4:1 до 1,5:1 и в частности от 3:1 до 2:1. В преимущественном воплощении, относительное соотношение массы указанного полиалкиленоксида (С) и указанного дополнительного полимера находится в диапазоне от 10:1 до 5:1, более предпочтительно от 8:1 до 5:1, наиболее предпочтительно от 7:1 до 5:1.
Преимущественно, содержание указанного дополнительного полимера составляет от 0.5 до 25 мас.%, более предпочтительно от 1.0 до 20 мас.%, еще более предпочтительно от 2.0 до 22.5 мас.%, еще более предпочтительно от 3.0 до 20 мас.% и наиболее предпочтительно от 4.0 до 17.5 мас.% и в частности от 5.0 до 15 мас.%, основанных на общей массе фармацевтической лекарственной формы.
В преимущественном воплощении, дополнительным полимером является сложный эфир целлюлозы или эфир целлюлозы, преимущественно ГПМЦ, с содержанием в пределах диапазона 10±8 мас.%, более предпочтительно 10±6 мас.%, еще более предпочтительно 10±5 мас.%, еще более предпочтительно 10±4 мас.%, наиболее предпочтительно 10±3 мас.%, и в частности 10±2 мас.%, основанного на общей массе фармацевтической лекарственной формы.
В другом преимущественном воплощении, дополнительным полимером является сложный эфир целлюлозы или эфир целлюлозы, преимущественно ГПМЦ, с содержанием в пределах диапазона 14±8 мас.%, более предпочтительно 14±6 мас.%, еще более предпочтительно 14±5 мас.%, еще более предпочтительно 14±4 мас.%, наиболее предпочтительно 14±3 мас.%, и в частности 14±2 мас.%, основанного на общей массе фармацевтической лекарственной формы.
Все полимеры предпочтительно применяются в виде порошков. Они могут быть растворимы в воде.
Кроме фармакологически активного ингредиента (А), кислоты (В) и полиалкиленоксида (С) фармацевтическая лекарственная форма согласно изобретению может содержать дополнительные компоненты, такие как обычно используемые вспомогательные вещества.
В предпочтительном воплощении, фармацевтическая лекарственная форма содержит антиоксидант. Подходящие антиоксиданты включают аскорбиновую кислоту, α-токоферол (витамин Е), бутилгидроксианизол, бутил гидрокситолуол, соли аскорбиновой кислоты (витамин С), аскорбилпальмитат, монотиоглицерин, конифериловый бензоат, нордигидрогваяретовая кислота, сложные эфиры галловой кислоты, фосфорная кислота, и их производные, такие как витамин Е-сукцинат или витамин Е-пальмитат и/или бисульфит натрия, более предпочтительно бутил гид рокситолуол (БГТ) или бутилгидроксианизол (БГА) и/или α-токоферол.
Предпочтительно, содержание антиоксиданта составляет в пределах от 0.001 до 5.0 мас.%, более предпочтительно от 0.002 до 2.5 мас.%, более предпочтительно от 0.003 до 1.5 мас.%, еще более предпочтительно от 0.005 до 1.0 мас.%, еще более предпочтительно от 0.01 до 0.5 мас.%, наиболее предпочтительно от 0.05 до 0.4 мас.% и в частности от 0.1 до 0.3 мас.%, от общей массы фармацевтической лекарственной формы.
В предпочтительном воплощении, содержание антиоксиданта составляет не более, чем 5.0 мас.%, более предпочтительно не более, чем 4.0 мас.%, еще более предпочтительно не более, чем 3.0 мас.%, еще более предпочтительно не более, чем 2.0 мас.%, еще более предпочтительно не более, чем 1.0 мас.%, наиболее предпочтительно не более, чем 0.5 мас.% и в частности не более, чем 0.25 мас.%, от общей массы фармацевтической лекарственной формы.
В частности предпочтительным антиоксидантом является α-токоферол. К удивлению было обнаружено, что α-токоферол стабилизирует полиалкиленоксид и в то же самое время дестабилизирует определенные опиоиды (А), такие как оксиморфон. Таким образом, в предпочтительном воплощении, содержание α-токоферола является сбалансированным между достаточной стабильностью полиалкиленоксида с одной стороны и достаточной стабильностью фармакологически активного ингредиента (А), предпочтительно опиоида, с другой стороны.
В предпочтительном воплощении, содержание α-токоферола имеет значение в пределах 0.2±0.18 мас.%, более предпочтительно 0.2±0.15 мас.%, еще более предпочтительно 0.2±0.12 мас.%, еще более предпочтительно 0.2+0.09 мас.%, наиболее предпочтительно 0.2±0.06 мас.%, и в частности 0.2±0.03 мас.%, от общей массы фармацевтической лекарственной формы.
В предпочтительном воплощении, соотношение относительной массы кислоты (В), предпочтительно лимонной кислоты, и антиоксиданта, предпочтительно α-токоферола, имеет значение в пределах от 10:1 до 1:10, более предпочтительно от 8:1 до 1:8, еще более предпочтительно от 6:1 до 1:6, еще более предпочтительно от 5:1 до 1:4, наиболее предпочтительно от 4:1 до 1:3 и в частности от 3:1 до 1:2.
В другом предпочтительном воплощении, фармацевтическая лекарственная форма не содержит никаких антиоксидантов как указано выше. Предпочтительно, фармацевтическая лекарственная форма не содержит ни бутилгидрокситолуола (БГТ), ни бутилгидроксианизола (БГА), ни α-токоферола.
Фармацевтическая лекарственная форма согласно изобретению может также содержать природный, полусинтетически и или синтетический воск. Воски с точкой плавления, по меньшей мере, 50°С, более предпочтительно 60°С являются предпочтительными. Карнаубский воск и пчелиный воск являются в частности предпочтительными, в особенности карнаубский воск.
Предпочтительно, кривая высвобождения фармакологически активного ингредиента (А), предпочтительно опиоида, представляет собой высвобождение из матрицы. Предпочтительно, фармакологически активный ингредиент (А), предпочтительно опиоид, является встроенным в матрицу, содержащую полиалкиленоксид, указанная матрица контролирует высвобождение фармакологического активного ингредиента (А), предпочтительно опиоида, из фармацевтической лекарственной формы.
Физиологически приемлемые материалы, которые являются известными для квалифицированного специалиста в данной области техники могут быть использованы в качестве дополнительных материалов матрицы. Полимеры, в частности предпочтительно простые эфиры целлюлозы, сложные эфиры целлюлозы и/или акриловые смолы являются предпочтительно используемыми в качестве гидрофильных материалов матрицы. Этилцеллюлоза, гидроксипропилметилцеллюлоза, гидроксипропилцеллюлоза, гидрокси метил-целлюлоза, гидроксиэтилцеллюлоза, поли(мет)акриловая кислота и/или их производные, такие как их соли, амиды или сложные эфиры являются в большей особенности предпочтительно используемыми в качестве материалов матрицы. Материалы матрицы, приготовленные из водоотталкивающие материалы, такие как водоотталкивающие полимеры, воски, жиры, жирные кислоты с длинными цепочками, жирные спирты или соответствующие сложные эфиры или простые эфиры или их смеси являются также предпочтительными. Моно- или диглицериды C12-С30 жирных кислот и/или С12-С30 жирные спирты и/или воски или их смеси являются в частности предпочтительно используемыми в качестве водоотталкивающих материалов. Также возможным является использование смесей указанных выше гидрофильных и водоотталкивающих материалов в качестве материалов матрицы.
Предпочтительно, соотношение относительной массы полиалкиленоксида к фармакологически активному ингредиенту (А), предпочтительно опиоиду, составляет по меньшей мере 0.5:1, более предпочтительно по меньшей мере 1:1, по меньшей мере 2:1, по меньшей мере 3:1, по меньшей мере 4:1, по меньшей мере 5:1, по меньшей мере 6:1, по меньшей мере 7:1, по меньшей мере 8:1 или по меньшей мере 9:1; еще более предпочтительно по меньшей мере 10:1 или по меньшей мере 15:1, еще более предпочтительно по меньшей мере 20:1, наиболее предпочтительно по меньшей мере 30:1 и в частности по меньшей мере 40:1. В предпочтительном воплощении, соотношение относительной массы полиалкиленоксида к фармакологически активному ингредиенту (А), предпочтительно опиоиду, имеет значение в пределах от 3:1 до 50:1, более предпочтительно от 3:1 до 40:1 ив частности от 3:1 до 30:1.
Фармацевтическая лекарственная форма согласно изобретению предпочтительно содержит пластифицирующую добавку. Пластифицирующая добавка обеспечивает пригодность к обработке полиалкиленоксида. Предпочтительная пластифицирующая добавка представляет собой полиалкиленгликоль, как, к примеру, полиэтиленгликоль, триуксусный эфир глицерина, жирные кислоты, сложные эфиры жирных кислот, воски и/или микрокристалические воски. В частности предпочтительными пластифицирующими добавками являются полиэтиленгликоли, такие как ПЭГ 6000.
Предпочтительно, содержание пластифицирующей добавки имеет значение в пределах от 0.1 до 25 мас.%, более предпочтительно то 0.5 до 22.5 мас.%, еще более предпочтительно от 1.0 до 20 мас.%, еще более предпочтительно от 2.5 до 17.5 мас.%, наиболее предпочтительно от 5.0 до 15 мас.% и в частности от 7.5 до 12.5 мас.%, от общей массы фармацевтической лекарственной формы.
В предпочтительном воплощении, пластифицирующая добавка представляет собой полиалкиленгликоль, который имеет содержание в диапазоне 10±8 мас.%, более предпочтительно 10±6 мас.%, еще более предпочтительно 10±5 мас.%, еще более предпочтительно 10±4 мас.%, наиболее предпочтительно 10±3 мас.%, и в частности 10±2 мас.%, от общей массы фармацевтической лекарственной формы.
В другом предпочтительном воплощении, пластифицирующая добавка представляет собой полиалкиленгликоль, который имеет содержание в диапазоне 15±8 мас.%, более предпочтительно 15±6 мас.%, еще более предпочтительно 15±5 мас.%, еще более предпочтительно 15±4 мас.%, наиболее предпочтительно 15±3 мас.%, и в частности 15±2 мас.%, от общей массы фармацевтической лекарственной формы.
В предпочтительном воплощении, соотношение относительной массы полиалкиленоксида к полиалкиленгликолю имеет значение в диапазоне 4.2±2:1, более предпочтительно 4.2±1.5:1, еще более предпочтительно 4.2±1:1, еще более предпочтительно 4.2±0.5:1, наиболее предпочтительно 4.2±0.2:1, и в частности 4.2±0.1:1. Это соотношение удовлетворяет требованиям относительно высокого содержания полиалкиленоксида и хорошей экструдируемости.
При изготовлении лекарственных форм из кусочков, которые получены посредством обрезания экструдированных лент, вес ломтиков определяет вес получающейся в результате лекарственной формы. Выраженные изменения в весе этих ломтиков приводит к соответственному весовому отклонению лекарственных форм от целевого веса. Изменение массы ломтиков сильно зависит от свойств поверхности экструдируемой ленты. Лента с полностью гладкой поверхностью позволяет генерировать проявление у ломтиков низких изменений веса. В противоположность этому, волнистые или с эффектов «акульей шкуры» ленты приводят в результате к проявлению у ломтиков высокого изменения веса, тем самым увеличивая количество брака.
Таким образом, к удивлению было обнаружено, что свойства поверхности экструдируемой ленты могут быть вызваны весовым соотношением полиалкиленоксида: полиалкиленгликоля.
Предпочтительные составы X1-Х32 фармацевтической лекарственной формы согласно изобретению собраны в таблице здесь ниже:
В предпочтительном воплощении, фармацевтическая лекарственная форма имеет общий вес в диапазоне 100±75 мг, более предпочтительно 100±50 мг, наиболее предпочтительно 100±25 мг. В другом предпочтительном воплощении, фармацевтическая лекарственная форма имеет общий вес в диапазоне 200±75 мг, более предпочтительно 200±50 мг, наиболее предпочтительно 200±25 мг. В другом предпочтительном воплощении, фармацевтическая лекарственная форма имеет общий вес в диапазоне 250±75 мг, более предпочтительно 250±50 мг, наиболее предпочтительно 250±25 мг. Еще в другом предпочтительном воплощении, фармацевтическая лекарственная форма имеет общий вес в диапазоне 300±75 мг, более предпочтительно 300±50 мг, наиболее предпочтительно 300±25 мг. Еще в другом предпочтительном воплощении, фармацевтическая лекарственная форма имеет общий вес в диапазоне 400±75 мг, более предпочтительно 400±50 мг, наиболее предпочтительно 400±25 мг.
В предпочтительном воплощении, фармацевтическая лекарственная форма имеет общий вес в диапазоне 500±250 мг, более предпочтительно 500±200 мг, наиболее предпочтительно 500±150 мг. В другом предпочтительном воплощении, фармацевтическая лекарственная форма имеет общий вес в диапазоне 750±250 мг, более предпочтительно 750±200 мг, наиболее предпочтительно 750±150 мг. В другом предпочтительном воплощении, фармацевтическая лекарственная форма имеет общий вес в диапазоне 1000±250 мг, более предпочтительно 1000±200 мг, наиболее предпочтительно 1000±150 мг. Еще в другом предпочтительном воплощении, фармацевтическая лекарственная форма имеет общий вес в диапазоне 1250±250 мг, более предпочтительно 1250±200 мг, наиболее предпочтительно 1250±150 мг.
В предпочтительном воплощении, фармацевтическая лекарственная форма согласно изобретению имеет объемную плотность в диапазоне 1.19±0.30 г/см3, более предпочтительно 1.19±0.25 г/см3, еще более предпочтительно 1.19±0.20 г/см3, еще более предпочтительно 1.19±0.15 г/см3, наиболее предпочтительно 1.19±0.10 г/см3, and в частности 1.19±0.05 г/см3. Предпочтительно, объемная плотность фармацевтической лекарственной формы согласно изобретению имеет значение в диапазоне 1.17±0.02 г/см3, 1.19±0.02 или 1.21±0.02. Метод измерения плотности лекарственной формы является известным для квалифицированного специалиста в данной области техники. Объемная плотность лекарственной формы может, к примеру, быть определена при помощи метода ртутной порометрии или методом гелиевой пикнометрии, как описано в Ph.Eur.
Предпочтительно, фармацевтическая лекарственная форма согласно изобретению является адаптированной для орального применения. Тем не менее, также возможно вводить фармацевтическую лекарственную форма посредством различных способов применения и таким образом, фармацевтическая лекарственная форма может альтернативно быть адаптированной для защечного, подъязычного, ректального или вагинального введения. Имплантаты также являются возможными.
В предпочтительном воплощении, фармацевтическая лекарственная форма согласно изобретению является адаптированной для введения один раз в день. В другом предпочтительном воплощении, фармацевтическая лекарственная форма согласно изобретению является адаптированной для введения два раза в день. Еще в другом предпочтительном воплощении, фармацевтическая лекарственная форма согласно изобретению является адаптированной для введения три раза в день.
Применительно к данному описанию, "два раза в день" подразумевает равные или почти равные интервалы времени, то есть, примерно каждые 12 часов, или различные интервалы времени, к примеру, 8 и 16 часов или 10 и 14 часов, между независимыми введениями.
Применительно к данному описанию, "три раза в день" подразумевает равные или почти равные интервалы времени, то есть, примерно каждые 8 часов, или различные интервалы времени, к примеру, 6, 6 и 12 часов; или 7, 7 и 10 часов, между независимыми введениями.
Предпочтительно, фармацевтическая лекарственная форма согласно изобретению является причиной, по меньшей мере, частично замедленного или пролонгированного высвобождения фармакологически активного ингредиента (А), предпочтительно опиоида (А).
Контролируемое или пролонгированное высвобождение согласно изобретению предпочтительно означает кривую высвобождения, в которой фармакологически активный ингредиент (А), предпочтительно опиоид, высвобождается в течение относительно длительного периода с пониженной частотой потребления с целью продлить терапевтическое действие. Предпочтительно, термин "пролонгированное высвобождение" имеет значение в соответствии с Европейским руководством по номенклатуре кривой высвобождения фармацевтические лекарственные формы (СНМР). Оно достигается в частности с пероральным введением. Выражение "по меньшей мере, частично замедленное или пролонгированное высвобождение" охватывает согласно изобретению любые фармацевтические лекарственные формы, которые обеспечивают изменение высвобождения фармакологически активных ингредиентов (А), предпочтительно опиоидов, содержащихся в них. Фармацевтические лекарственные формы предпочтительно содержат покрытые или непокрытые фармацевтические лекарственные формы, которые являются произведенными с конкретными вспомогательными веществами, посредством частных способов или посредством комбинирования двух возможных вариантов с целью целенаправленно изменять скорость высвобождения или место высвобождения.
В случае фармацевтических лекарственных форм согласно изобретению, кривая времени высвобождения формы с контролируемым высвобождением может быть модифицирована, к примеру, как указано далее: высвобождение активного вещества с отсрочкой, высвобождение с повторением действия, замедленное высвобождение и непрерывное высвобождение.
Применительно к данному описанию "контролируемое высвобождение" предпочтительно подразумевает продукт, в котором высвобождение активного соединения в течение времени является контролируемым посредством типа и композиции состава. Применительно к данному описанию " высвобождение активного вещества с отсрочкой" предпочтительно подразумевает продукт, в котором высвобождение активного соединения является задержанным на определенный период запаздывания, после чего высвобождение происходит беспрепятственно. Применительно к данному описанию "высвобождение с повторением действия" предпочтительно подразумевает продукт, в котором первая порция активного соединения высвобождается на начальном этапе, с последующим высвобождением, по меньшей мере, одной дополнительной порции активного соединения. Применительно к данному описанию "замедленное высвобождение" предпочтительно подразумевает продукт, в котором скорость высвобождения активного соединения из состава после введения будет уменьшена с течением времени, с целью поддержания терапевтической активности, для уменьшения терапевтических эффектов, или для некоторых других терапевтических целей. Применительно к данному описанию "непрерывное высвобождение" предпочтительно подразумевает такой путь составления лекарственного препарата, при котором он будет высвобождаться в организм постоянно, в течение длительного периода времени, таким образом позволяя снизить частоту дозирования. Для дополнительных деталей ссылка может быть сделана, к примеру, на К.Н.Bauer, Lehrbuch der Pharmazeutischen Technologie, 6th edition, WVG Stuttgart, 1999; and Eur.Ph.
Фармацевтическая лекарственная форма согласно изобретению может содержать один или более фармакологически активных ингредиентов (А), предпочтительно опиоидов, по меньшей мере, от части в дополнительной форме с контролируемым высвобождением, в которой контролируемое высвобождение может быть достигнуто с помощью обычно применимых материалов и процессов, известных квалифицированным специалистам в данной области техники, к примеру, посредством внедрения вещества в матрицу с контролируемым высвобождением или посредством применения одного или нескольких контролируемых высвобождение покрытий. Высвобождаемое вещество, тем не менее, должно быть контролируемо таким образом, чтоб добавление материалов с отсроченным высвобождением не нарушало необходимое сопротивление разрушению. Контролируемое высвобождение из фармацевтической лекарственной формы согласно изобретению предпочтительно достигается посредством внедрения вещества в матрицу. Предпочтительно, полиалкиленоксид (С) выступает в качестве такой матрицы. Вспомогательные вещества действуют как материалы матрицы по контролю высвобождения. Материалы матрицы могут, к примеру, быть гидрофильными, гелеобразующими материалами, из которых высвобождение происходит главным образом путем диффузии, или водоотталкивающие материалы, из которых высвобождение происходит главным образом путем диффузии из пор в матрице.
Предпочтительно, кривая высвобождения существенно управляема матрицей, предпочтительно посредством внедрения фармакологически активного ингредиента (А), предпочтительно опиоида (А), в матрицу, которая содержит полиалкиленоксид (С) и необязательно, дополнительные материалы матрицы. Предпочтительно, кривая высвобождения представляет собой не осмотическое приведение в действие. Предпочтительно, кинетика высвобождения не нулевого порядка.
Предпочтительно, при физиологических условиях фармацевтическая лекарственная форма согласно изобретению имеет высвобождение после 30 минут от 0.1 до 75%, после 240 минут от 0.5 до 95%, после 480 минут от 1.0 до 100% и после 720 минут от 2.5 до 100% фармакологически активного ингредиента (А), предпочтительно опиоида (А). Дополнительные предпочтительные кривые высвобождения R1-R6 собраны в таблице здесь ниже [все данные в мас.% высвобожденного фармакологически активного ингредиента (А), предпочтительно опиоида (А)]:
Дополнительно предпочтительные кривые высвобождения R1-R6 собраны в таблице здесь ниже [все данные в мас.% высвобожденного фармакологически активного ингредиента (А), предпочтительно опиоида (А)]:
Предпочтительно, кривая высвобождения фармацевтической лекарственной формы согласно настоящему изобретению является стабильной в результате хранения, предпочтительно в результате хранения при повышенной температуре, к примеру 37°С, в течение 3 месяцев в герметичных контейнерах. В данном отношении "стабильная" означает, что при сравнении начальной кривой высвобождения с кривой высвобождения после хранения, в любой выбранный момент времени отклонения кривых высвобождения одна от другой будут не более чем 20%, более предпочтительно не более чем 15%, еще более предпочтительно не более чем 10%, еще более предпочтительно не более чем 7.5%, наиболее предпочтительно не более чем 5.0% и в частности не более чем 2.5%.
Предпочтительно, при in vitro условиях фармацевтическая лекарственная форма имеет высвобождение спустя 0.5 ч от 1.0 до 35 мас.%, спустя 1 ч от 5.0 до 45 мас.%, спустя 2 ч от 10 до 60 мас.%, спустя 4 ч по меньшей мере 15 мас.%, спустя 6 ч по меньшей мере 20 мас.%, спустя 8 ч по меньшей мере 25 мас.% и спустя 12 ч по меньшей мере 30 мас.% фармакологически активного ингредиента (А), предпочтительно опиоида, который изначально содержался в фармацевтической лекарственной форме.
Подходящие in vitro условия являются известными для специалиста в данной области. В данном смысле они к ним могут относиться, к примеру, Eur.Ph. Предпочтительно, кривая высвобождения измеряется при следующих условиях: прибор с лопастью оборудованный грузилом, 50 оборотов в минуту, 37±5°С, 900 мл, воспроизводимый интестинальную жидкость с рН 6.8 (фосфатный буфер) или рН 4.5. В предпочтительном воплощении частота вращения лопасти увеличивается до 100 оборотов в минуту.
В предпочтительном воплощении, после предпочтительно орального введения фармацевтической лекарственной формы согласно изобретению, in vivo среднее значение пика уровня плазмы (Cmax) в среднем достигается после tmax 4.0±2.5 ч, более предпочтительно после tmax 4.0±2.0 ч, еще более предпочтительно после tmax 4.0±1.5 ч, наиболее предпочтительно после tmax 4.0±1.0 ч и в частности после tmax 4.0±0.5 ч. В другом предпочтительном воплощении, после предпочтительно орального введения фармацевтической лекарственной формы согласно изобретения, in vivo среднее значение пика уровня плазмы (Cmax) в среднем достигается после tmax 5.0±2.5 ч, более предпочтительно после tmax 5.0±2.0 ч, еще более предпочтительно после tmax 5.0±1.5 ч, наиболее предпочтительно после tmax 5.0±1.0 ч и, в частности, после tmax 5.0±0.5 ч. Еще в другом предпочтительном воплощении, после предпочтительно орального введения фармацевтической лекарственной формы согласно изобретению, in vivo среднее значение пика уровня плазмы (Cmax) в среднем достигается после tmax 6.0±2.5 ч, более предпочтительно после tmax 6.0±2.0 ч, еще более предпочтительно после tmax 6.0±1.5 ч, наиболее предпочтительно после tmax 6.0±1.0 ч и, в частности, после tmax 6.0±0.5 ч.
В предпочтительном воплощении, среднее значение для t1/2 после предпочтительно орального введения фармацевтической лекарственной формы согласно изобретению in vivo составляет 4.0±2.5 ч, более предпочтительно 4.0±2.0 ч, еще более предпочтительно 4.0±1.5 ч, наиболее предпочтительно 4.0±1.0 ч, и в частности 4.0±0.5 ч. В другом предпочтительном воплощении, среднее значение для t1/2 после предпочтительно орального введения фармацевтической лекарственной формы согласно изобретению in vivo составляет предпочтительно 5.0+2.5 ч, более предпочтительно 5.0±2.0 ч, еще более предпочтительно 5.0±1.5 ч, наиболее предпочтительно 5.0±1.0 ч, и в частности 5.0±0.5 ч. Еще в другом предпочтительном воплощении, среднее значение для t1/2 после предпочтительно орального введения фармацевтической лекарственной формы согласно изобретения in vivo составляет предпочтительно 6.0±2.5 ч, более предпочтительно 6.0±2.0 ч, еще более предпочтительно 6.0±1.5 ч, наиболее предпочтительно 6.0±1.0 ч, и в частности 6.0±0.5 ч.
Предпочтительно, фармацевтическая лекарственная форма согласно изобретению содержит покрытие, предпочтительно пленочное покрытие. Подходящие материалы для покрытий являются известными для специалиста в данной области. Подходящие материалы для покрытий являются доступными для приобретения, к примеру, под торговыми марками Opadry® и Eudragit®.
Примеры подходящих материалов включают сложные эфиры целлюлозы и простые эфиры целлюлозы, такие как метил целлюлоза (МЦ), гидроксипропилметилцеллюлоза (ГПМЦ), гидроксипропилцеллюлоза (ГПЦ), гидроксиэтилцеллюлоза (ГЭЦ), натриевая карбоксиметилцеллюлоза (Na-КЭЦ), этилцеллюлоза (ЭЦ), ацетатфталат целлюлозы (АФЦ), фталат гидроксипропилметилцеллюлозы (ГПМЦФ); поли(мет)акрилаты, такие как сополимеры аминоалкилметакрилата, сополимеры этилакрилата метилметакрилат, сополимеры метилметакрилата метакриловой кислоты, сополимеры метилметакрилата метакриловой кислоты; виниловые полимеры, такие как поливинилпирролидон, фталат поливинилацетата, поливиниловый спирт, поливинилацетат; и образователи естественных пленок, такие как шеллак.
В частном предпочтительном воплощении, покрытия являются растворимыми в воде. В предпочтительном воплощении, покрытие является основанным на поливиниловом спирте, таком как поливиниловый спирт - частично гидролизованный, и могут дополнительно содержать полиэтиленгликоль, такой как макрогол 3350, и/или пигменты. В другом предпочтительном воплощении, покрытие является основанным на гидроксипропилметилцеллюлозе, предпочтительно гипромеллозе типа 2910, которая имеет вязкость от 3 до 15 мПа.
Покрытие фармацевтической лекарственной формы может увеличивать свою стойкость против порчи при хранении.
Покрытие может быть устойчиво к воздействию желудочного сока и растворятся в зависимости от значения рН окружающей среды высвобождения. Посредством такого покрытия можно убедиться, что фармацевтическая лекарственная форма согласно изобретению проходит через желудок нерастворенной и активное соединение высвобождается только лишь в кишечнике. Покрытие, которое является устойчивым к воздействию желудочного сока, предпочтительно растворяется при рН значении между 5 и 7.5. Соответствующие материалы и способы замедления высвобождения активных соединений и нанесения покрытий, которые являются устойчивыми к воздействию желудочного сока являются известными для квалифицированного специалиста в данной области техники, к примеру, из " Coated Pharmaceutical dosage forms - Fundamentals, Manufacturing Techniques, Biopharmaceutical Aspects, Test Methods и Raw Materials" by Kurt h. Bauer, K.Lehmann, Hermann P.Osterwald, Rothgang, Gerhart, 1st edition, 1998, Medpharm Scientific Publishers.
В предпочтительном воплощении, фармацевтическая лекарственная форма согласно изобретению не содержит никаких веществ, которые раздражают носовые пути и/или глотку, то есть вещества, которые при введении внутрь через носовые пути и/или глотку, приводят к физической реакции, которая либо является такой неприятной для пациента, что он/она не имеет желания или не может продолжать введение, к примеру, жжение, либо физиологически противодействует принятию соответствующего активного соединения, к примеру, по причине усиления носовой секреции или чихания. Дополнительные примеры веществ, которые раздражают носовые пути и/или глотку представляет собой такие, которые вызывают жжение, зуд, желание чихнуть, усиление образования секреций или комбинацию, по меньшей мере, двух таких раздражителей. Соответствующие субстанции и их количественные параметры, которые являются обычно используемыми для использования являются известными для квалифицированного специалиста в данной области техники. Некоторые из веществ, которые раздражают носовые пути и/или глотку являются основанными соответственно на одном или более компонентах или одном или более частей растений горячего лекарственного вещества. Соответствующие горячие лекарственные вещества являются известными для квалифицированного специалиста в данной области техники и являются описанными, к примеру, в "Pharmazeutische Biologie - Drogen und ihre Inhaltsstoffe" by Prof. Dr.Hildebert Wagner, 2nd., revised edition, Gustav Fischer Verlag, Stuttgart-New York, 1982, pages 82 et seq.. Соответствующее описание тем самым является включенным в качестве ссылки и считается частью раскрытия предмета изобретения.
Фармацевтическая лекарственная форма согласно изобретению кроме того более предпочтительно не содержит никаких агентов, нейтрализующих действие фармакологически активного ингредиента (А), предпочтительно никаких опиоидных агентов, более предпочтительно никаких агентов, нейтрализующих действие психотропных веществ, в частности агентов, нейтрализующие действие опиоидов (А). Агенты, нейтрализующие действие других веществ, которые являются подходящими для данного фармакологически активного ингредиента (А) являются известными для квалифицированного специалиста в данной области техники и могут присутствовать как таковые или в виде соответствующих производных, в частности сложных эфиров или простых эфиров, или в каждом случае в форме соответствующих психологически приемлемых соединений, в частности в форме их солей или сольватов. Фармацевтическая лекарственная форма согласно изобретению предпочтительно не содержит никаких агентов, нейтрализующих действие других агентов, которые выбраны из числа группы, которая состоит из налоксона, налтрексона, налмефена, налида, налмексона, налорфина или налуфина, в каждом конкретном случае необязательно в форме соответствующего психологически приемлемого соединения, в частности в форме основания, соли или сольвата; и нейтрализующие действие нейролептических веществ, к примеру, соединение, выбранное из числа группы, которая состоит из галоперидола, прометацина, флуфеназина, перфеназина, левомепромазина, тиоридазина, перазина, хлорпромазина, хлорпротиксина, зуклопентиксола, флюпентиксола, протипендила, зотепина, бенперидола, пипамперона, мелперона и бромперидола.
Фармацевтическая лекарственная форма согласно изобретению кроме того более предпочтительно не содержит средства, вызывающие рвотный рефлекс. Средства, вызывающие рвотный рефлекс являются известными для квалифицированного специалиста в данной области техники и могут присутствовать как таковые или в виде соответствующих производных, в частности сложных эфиров или простых эфиров, или в каждом случае в форме соответствующих психологически приемлемых соединений, в частности в форме их солей или сольватов. Фармацевтическая лекарственная форма согласно изобретению предпочтительно не содержит средство, вызывающее рвотный рефлекс, которое основано на одном или более составляющих компонентов корня ипекакуаны (ипекакуана), к примеру, основано на составляющем компоненте эметина, такие, как, к примеру, описанные в "Pharmazeutische Biologie - Drogen und ihre Inhaltsstoffe" by Prof. Dr. Hildebert Wagner, 2nd, revised edition, Gustav Fischer Verlag, Stuttgart, New York, 1982. Описание в соответствующей литературе тем самым является включенным в качестве ссылки и считается частью раскрытия предмета изобретения. Фармацевтическая лекарственная форма согласно изобретению предпочтительно также не содержит апоморфина в качестве средства, вызывающего рвотный рефлекс.
В конце концов, фармацевтическая лекарственная форма согласно изобретению предпочтительно также не содержит горьких веществ. Горькие вещества и количества, эффективные для использования, могут быть найдены в US-2003/0064099 A1, соответствующее описание из которого следует считать описанием настоящего документа и тем самым является включенным в качестве ссылки. Примеры горьких веществ представляют собой ароматические масла, такие как масло мяты перечной, эвкалиптовое масло, масло горького миндаля, ментол, фруктовые ароматические вещества, ароматические вещества из лимона, апельсина, лайма, грейпфрута их смесей, и/или денатониум бензоат.
Таким образом, фармацевтическая лекарственная форма согласно изобретению предпочтительно не содержит ни вещества, которые раздражают носовые пути и/или глотку, ни агенты, которые подавляют действие фармакологически активного ингредиента (А), предпочтительно опиоид (А), ни средства, вызывающие рвоту, ни горькие вещества.
Фармацевтическая лекарственная форма согласно изобретению является предпочтительно адаптированной для орального введения.
Как правило, фармацевтическая лекарственная форма согласно изобретению имеет форму таблетки. Предпочтительно, фармацевтическая лекарственная форма не является ни в форме пленки, ни многочастичной.
Фармацевтическая лекарственная форма согласно изобретению является предпочтительно устойчивой к несанкционированному проникновению. Предпочтительно, устойчивость к несанкционированному проникновению достигается на основе механических свойств фармацевтической лекарственной формы таким образом, чтобы измельчение было предотвращено или, по меньшей мере, было обеспечено воспрепятствование. Согласно изобретению, термин измельчение означает размельчение фармацевтической лекарственной формы с использованием традиционных средств обычно доступных для недобросовестного пользователя, к примеру, толчейный пест и ступка, молоток, колотушка или другие обычно применяемые средства для размельчения под действием силы. Таким образом, устойчивость к несанкционированному проникновению предпочтительно означает что размельчение фармацевтической лекарственной формы с использованием обычно применяемых средств является предотвращенным или, по меньшей мере, обеспечено воспрепятствование.
Предпочтительно, механические свойства фармацевтической лекарственной формы согласно изобретению, в частности ее сопротивление разрушению, существенно зависят от наличия и пространственного распределения полиалкиленоксида (С), хотя само его присутствие является, как правило, не достаточным для достижения указанных свойств. Выгодные механические свойства фармацевтической лекарственной формы согласно изобретению не могут быть автоматически достигнуты посредством простой обработки фармакологически активного ингредиента (А), кислоты (В), полиалкиленоксида (С), и необязательно кроме того вспомогательных веществ при помощи обычно применяемых методов приготовления фармацевтических лекарственных форм. На самом деле, должны быть выбраны обычно подходящие аппараты для приготовления и критические параметры обработки должны быть скорректированы, в частности давление/сила, температура и время. Таким образом, даже если используются обычные аппараты, протоколы процесса, как правило, должны быть адаптированы для удовлетворения установленным критериям.
Фармацевтическая лекарственная форма согласно изобретению имеет сопротивление разрушению, по меньшей мере, 300 Н, предпочтительно по меньшей мере 400 Н, более предпочтительно по меньшей мере 500 Н, еще более предпочтительно по меньшей мере 750 Н, еще более предпочтительно по меньшей мере 1000 Н, наиболее предпочтительно по меньшей мере 1250 Н и в частности по меньшей мере 1500 Н.
"Сопротивление разрушению" (сопротивление раздавливанию) фармацевтической лекарственной формы является известным для квалифицированного специалиста в данной области техники. В связи с этим может быть сделана ссылка к, к примеру, W.A.Ritschel, Die Tablette, 2. Auflage, Edition Cantor Verlag Aulendorf, 2002; h Liebermann et al., Pharmaceutical dosage forms: Tablets, Vol.2, Informa Healthcare; 2 edition, 1990; and Encyclopedia of Pharmaceutical Technology, Informa Healthcare; 1 edition.
Для целей спецификации, сопротивление разрушению предпочтительно определяется как величина силы, которая является необходимой для разрушения фармацевтической лекарственной формы (= разрушающее усилие). Таким образом, для целей спецификации фармацевтическая лекарственная форма предпочтительно не проявляет желаемое сопротивление разрушению, когда такое появляется, то есть происходит перелом по меньшей мере двух независимых частей, которые являются отделенными друг от друга. В другом предпочтительном воплощении, тем не менее, фармацевтическая лекарственная форма рассматривается как такая, которая будет разрушатся, если сила уменьшится на 25% (пороговое значение) самого высокого значения силы, измеренной во время измерений (см. ниже).
Фармацевтические лекарственные формы согласно изобретению отличаются от обычно используемых фармацевтических лекарственных форм тем, что в виду их сопротивления разрушению, они не могут быть измельчены посредством применения силы с обычно используемыми средствами, такими как, к примеру, толчейный пест и ступка, молоток, колотушка или другие обычные средства для измельчения, в частности устройства, разработанные для этой цели (дробилки таблеток). В данном отношении "измельчение" означает дробление на маленькие частицы, чтобы немедленно высвободить фармакологически активное соединение (А), предпочтительно опиоид, в подходящей среде. Избежание размельчения практически исключает возможность неправильного употребления пероральным или парентеральным, в частности внутривенным или назальным способом.
Общепринятые таблетки имеют сопротивление разрушению значительно ниже 200 Н в любом направлении распространения. Сопротивление разрушению обычных круглых таблеток может быть оценено по следующей эмпирической формуле: Сопротивление разрушению [в N]=10 х диаметр таблетки [в мм]. Таким образом, согласно указанной эмпирической формуле, круглые таблетки, которые имеют сопротивление разрушению, по меньшей мере, 300 Н, соответствуют диаметру по меньшей мере 30 мм). Такие таблетки при этом нельзя проглотить. Вышеприведенная эмпирическая формула предпочтительно не распространяется на фармацевтические лекарственные формы изобретения, которые являются не обычными, а скорее специального назначения.
Кроме того, фактическая средняя сила при жевании составляет около 220 Н (см, к примеру, Р.А.Proeschel et al., J Dent Res, 2002, 81(7), 464-468). Это означает, что обычные таблетки, которые имеют сопротивление разрушению значительно ниже 200 Н могут быть разрушены при спонтанном жевании, в то время как фармацевтические лекарственные формы согласно изобретению не могут.
Более того, при применении ускорения силы свободного падения около 9.81 м/с2, 300 Н соответствуют гравитационной силе более чем 30 кг, то есть фармацевтические лекарственные формы согласно изобретению могут предпочтительно выдержать вес более чем 30 кг не будучи распыленными.
Способ измерения сопротивления разрушению фармацевтической лекарственной формы является известным для квалифицированного специалиста в данной области техники. Подходящие устройства являются коммерчески доступными.
К примеру, сопротивление разрушению (сопротивление раздавливанию) может быть измерено в соответствии с Eur. Ph. 5.0, 2.9.8 или 6.0, 2.09.08 "Resistance to Crushing of Tablets". Тест предназначен для определения, при определенных условиях, сопротивления раздавливанию таблеток, измеряет усилие, которое необходимо для того, чтобы разрушить их путем дробления. Аппарат состоит из 2 зажимных приспособлений находящихся лицом друг к другу, одно из которых движется в сторону другого. Плоские поверхности зажимных приспособлений перпендикулярны к направлению движения. Поверхности зажимных приспособлений являются плоскими и большими, чем зона контакта с таблеткой. Аппарат калибруется с помощью системы с точностью до 1 Ньютона. Таблетка помещается между зажимными приспособлениями, принимая во внимание количество, при необходимости, форму, метку-знак для обозначения пропуска между объектами и формулу рецепта; для каждого измерения таблетка является ориентированной таким же образом по отношению к направлению приложения силы (и направлению разрушения, в котором сопротивления разрушению должна быть измерено). Измерение осуществляется по 10 таблеток, соблюдая, чтобы все фрагменты таблеток были удалены перед каждым определением. Результат выражается как среднее, минимальное и максимальное значение измеряемой силы, все выражается в Ньютонах.
Аналогичное описание сопротивления разрушению (разрушающее усилие) можно найти в USP. Сопротивление разрушению может альтернативно быть измерено в соответствии с методом, описанным в нем, где заявляется, что сопротивление разрушению является силой, которая необходима для того, чтобы сломать таблетку (то есть, разрушить) в конкретной плоскости. Таблетки, как правило, помещают между двумя валиками, один из которых движется с применением к таблетке достаточной силы, чтобы вызвать перелом. Для обычных, круглых (круглого поперечного сечения) таблеток, загрузка происходит через их диаметр (в некоторых случаях называют диаметральной загрузкой), и разрушение происходит в плоскости. Разрушающее усилие таблеток обычно в фармацевтической литературе называют твердость; тем не менее, использование этого термина вводит в заблуждение. В материаловедении, термин твердость относится к сопротивлению поверхности проникновению или вдавливанию посредством малого зонда. Термин прочность при сдавливании также часто используется для описания сопротивления таблеток для применения сжимающей нагрузки. Хотя этот термин описывает истинную природу теста более точно, чем твердость, подразумевается, что таблетки фактически являются разрушенными во время теста, что часто бывает не так.
В качестве альтернативы, сопротивление разрушению (сопротивление раздавливанию) может быть измерено в соответствии с WO 2005/ 016313, WO 2005/016314, и WO 2006/082099, которые могут быть рассмотрены как разновидности метода, который описан в Eur. Ph. Аппаратом, используемым для измерения является предпочтительно установка для испытания материалов "Zwick Z 2.5", Fmax=2.5 кН с максимальным смещением 1150 мм, которая должна быть оборудована одной колонкой и одним шпинделем, промежуток ниже 100 мм и скорость теста подогнана между 0.1 и 800 мм/мин вместе с программным обеспечением для контроля испытаний. Измерение производится при помощи пневматического поршня с резьбовыми вставками и цилиндром (диаметр 10 мм), силового измерительного преобразователя, Fmax. 1 кН, диаметр = 8 мм, класс 0.5 от 10 Н, класс 1 от 2 Н до ISO 7500-1, с тестовым сертификатом производителя М в соответствии с DIN 55350-18 (Zwick грубой силы Fmax=1.45 кН) (все аппараты от Zwick GmbH & Со. KG, Ulm, Germany) с Order No BTC-FR 2.5 TH. D09 для тестера, Order No BTC-LC 0050N. P01 для силового измерительного преобразователя, Order No ВО 70000 S06 для центрирующего приспособления.
В предпочтительном воплощении изобретения, сопротивление разрушению измеряется с помощью тестера сопротивления разрушению, к примеру, Sotax®, тип НТ100 или тип НТ1 (Allschwil, Switzerland). Оба, Sotax® НТ100 и Sotax® HT1 могут измерять сопротивление разрушению в соответствии с двумя различными измерительными принципами: постоянная скорость (при котором тестовые зажимные приспособления двигаются с постоянной скоростью, регулируемой до 5-200 мм/мин) или постоянная сила (при котором тестовые зажимные приспособления линейно усиливаю силу, регулируемую до 5-100 Н/сек). В принципе, оба принципа измерения являются подходящими для измерения сопротивления разрушению фармацевтической лекарственной формы согласно изобретению. Предпочтительно, сопротивление разрушению измеряется при постоянной скорости, предпочтительно при постоянной скорости 120 мм/мин.
В предпочтительном воплощении, фармацевтическая лекарственная форма рассматривается как разрушенная, если она разломлена, по крайней мере, на две различные части.
Фармацевтическая лекарственная форма согласно изобретению предпочтительно проявляет механическую прочность в широком диапазоне температур, в добавок к сопротивлению разрушению (сопротивление сдавливанию) необязательно также достаточную твердость, прочность при ударе, ударная упругость, прочность на разрыв и/или модуль продольной упругости, необязательно также при низких температурах (к примеру ниже -24°С, ниже -40°С или в жидком азоте), для того, чтобы быть фактически невозможным к размельчению спонтанным жеванием, измельчением в ступке, толчением и т.д. Таким образом, предпочтительно, сравнительно высокое сопротивление разрушению фармацевтической лекарственной формы согласно изобретению сохраняется даже при низких и очень низких температурах, к примеру, когда фармацевтическая лекарственная форма является изначально охлажденной для увеличения своей хрупкости, к примеру, до температур ниже -25°С, ниже -40°С или даже в жидком азоте.
Фармацевтическая лекарственная форма согласно изобретению характеризуется определенной степенью сопротивление разрушению. Это не означает, что фармацевтическая лекарственная форма должна также проявлять определенную степень твердости. Твердость и сопротивление разрушению являются различными физическими свойствами. Таким образом, защищенность от несанкционированного вскрытия фармацевтической лекарственной формы не обязательно зависит от твердости фармацевтической лекарственной формы. К примеру, в виду его сопротивления разрушению, ударной вязкости, модуля упругости и прочности на разрыв, соответственно, фармацевтическая лекарственная форма может предпочтительно быть деформирована, к примеру, пластически, когда оказываются внешние усилия, к примеру при использовании молотка, но не могут быть распылены, то есть, быть рассыпанными на большое количество фрагментов. Другими словами, фармацевтическая лекарственная форма согласно изобретению характеризуется определенной степенью сопротивления разрушению, но не обязательно также определенной степенью остойчивости формы.
Таким образом, в значении описания, фармацевтическая лекарственная форма, которая деформируется когда будет подвержена усилию в определенном направлении смещения, но которая не ломастся (пластическая деформация или пластическая текучесть) является предпочтительно рассматриваемой как такая, которая имеет желаемое сопротивление разрушению в указанном направлении смещения.
В особенности предпочтительное воплощение изобретения относится к защищенной от несанкционированного нарушения фармацевтической лекарственной форме, которая имеет сопротивление разрушению, по меньшей мере, 300 Н и будет термоформируемой посредством экструзии горячего расплава, указанная фармацевтическая лекарственная форма содержит
- фармакологически активный ингредиент (А), предпочтительно опиоид, в частности предпочтительно опиоид, выбранный из группы, состоящей из оксиморфона, оксикодона, гидроморфона, и их физиологически подходящих солей;
- свободную физиологически приемлемую многоосновную карбоновую кислоту (В), предпочтительно лимонную кислоту, при этом содержание кислоты (В) будет иметь значение в диапазоне от 0.001 до 5.0 мас.%, от общей массы фармацевтической лекарственной формы;
- антиоксидант, при этом содержание антиоксиданта, предпочтительно α-токоферола, будет иметь значение в диапазоне от 0.001 до 5.0 мас.%, от общей массы фармацевтической лекарственной формы; и
- полиалкиленоксид (С), который имеет среднемассовую молекулярную массу Mw по меньшей мере 200,000 г/мол;
где
- фармакологически активный ингредиент (А) включен в матрицу, которая содержит полиалкиленоксид (С), указанная матрица контролирует высвобождение фармакологически активного ингредиента (А) из фармацевтической лекарственной формы; и
- после хранения в течение 4 недель при 40°С и 75% отн. влажности, содержание фармакологически активного ингредиента (А), предпочтительно опиоида (А), составляет, по меньшей мере, 98.0% от первоначального содержания перед хранением.
Фармацевтическая лекарственная форма согласно изобретению может быть произведена посредством различных способов, в частности предпочтительные из которых поясняются более детально ниже. Несколько подходящих способов уже были описаны в существующем уровне техники. В этом отношении могут быть ссылки на, к примеру, WO 2005/ 016313, WO 2005/016314, WO 2005/063214, WO 2005/102286, WO 2006/002883, WO 2006/002884, WO 2006/002886, WO 2006/082097, и WO 2006/082099.
Настоящее изобретение также относится к фармацевтическим лекарственным формам, которые могут быть получены любым из способов, описанных здесь ниже.
Главным образом, процесс производства фармацевтической лекарственной формы согласно изобретению предпочтительно содержит следующие этапы:
(a) смешивание всех ингредиентов;
(b) необязательно предварительное формирование смеси, полученной на этапе (а), предпочтительно посредством применения нагревания и/или усилия к смеси, полученной на этапе (а), количество поставляемого тепла предпочтительно не достаточное для нагрева полиалкиленоксида (С) вплоть до его температуры размягчения;
(c) упрочнение смеси посредством применения нагревания и усилия, при этом возможно применить нагревание во время и/или перед применением усилия и количество применяемого тепла будет достаточным для нагревания полиалкиленоксида (С) по меньшей мере вплоть до его температуры размягчения;
(d) необязательно разделение затвердевшей смеси;
(e) необязательно придание необходимой формы фармацевтической лекарственной форме; и
(f) необязательно обеспечение покрытия пленкой.
Тепло может быть подано непосредственно, к примеру, посредством контакта или при помощи горячего газа, такого как горячий воздух, или при помощи ультразвука. Может быть применено усилие и/или фармацевтическая лекарственная форма может быть подвержена формованию к примеру посредством направленного таблетирования или с помощью подходящего экструдера, в частности с помощью червячного экструдера, оснащенного двумя винтами (двухвинтовой экструдер) или с помощью экструдера с планетарным зубчатым механизмом.
Финальная форма фармацевтической лекарственной формы может быть обеспечена или в ходе затвердевания смеси с применением тепла и усилия (этап (с)) или на последующем этапе (этап (е)). В обоих случаях, смесь всех компонентов является вовлеченной в пластифицированную структуру, то есть предпочтительно, формование осуществляется при температуре, по меньшей мере, выше температуры размягчения полиалкиленоксида (С). Тем не менее, экструзия при более низких температурах, к примеру, температуре окружающей среды, является также возможной и может быть предпочтительнее.
Формование может быть выполнено, к примеру, при помощи таблеточного пресса, который содержит матрицу и компостер соответствующей формы.
В особенности предпочтительный способ производства фармацевтической лекарственной формы изобретения включает экструзию горячего расплава. В этом способе, фармацевтическая лекарственная форма согласно изобретению производится посредством горячего формования при использовании экструдера, предпочтительно без какого-либо наблюдаемого последующего изменения цвета экструдируемой заготовки. К удивлению было обнаружено, что кислота (В) является способной к сдерживанию обесцвечивания. В отсутствие кислоты (В), экструдируемая заготовка имеет тенденцию к проявлению окраски от бежевого до желтого цвета, в то время как в присутствии кислоты (В) экструдируемые заготовки являются существенным образом без цвета, то есть белыми.
Этот способ характеризуется тем, что
a) все компоненты смешиваются,
b) получившуюся в результате смесь нагревают в экструдере по меньшей мере вплоть до температуры размягчение полиалкиленоксида (С) и продавливается через выпускное отверстие экструдера посредством применения усилия,
c) все еще пластиковая экструдируемая заготовка разделяется поштучно и формуется в фармацевтическую лекарственную форму или
d) охлаждается и необязательно повторно нагретая разделенная поштучно экструдируемая заготовка формуется в фармацевтическую лекарственную форму.
Смешивание компонентов в соответствии с этапом способа а) может также быть произведено в экструдере.
Компоненты могут также быть смешаны в миксере, известном для квалифицированного специалиста в данной области техники. Миксером может быть, к примеру, вальцовый миксер, взбивательный миксер, миксер с высоким напряжением сдвига или смеситель принудительного действия.
Перед смешиванием с остальными компонентами, полиалкиленоксид (С) является предпочтительно обеспечен согласно изобретению с антиоксидантом, предпочтительно α-токоферолом. Это может происходить посредством смешивания двух компонентов, полиалкиленоксида (С) и антиоксиданта, предпочтительно посредством растворения или суспендирования антиоксиданта в легколетучем растворителе и однородного смешивания этого раствора или суспензии с полиалкиленоксидом (С) и удаления растворителя посредством высушивания, предпочтительно при атмосфере инертного газа.
Предпочтительно расплавленная смесь, которая была нагрета в экструдере по меньшей мере до температуры размягчения полиалкиленоксида (С) выдавливается из экструдера через матрицу с по меньшей мере одним отверстием.
Для способа согласно изобретению требуется использование подходящих экструдеров, предпочтительно червячных экструдеров. Червячные экструдеры, которые оборудованы двумя винтами (двухвинтовые экструдеры) являются в особенности предпочтительными.
Экструзия предпочтительно выполняется таким образом, что расширение лент за счет экструзии составляет не более чем 30%, то есть таким образом, что при использовании заготовки с отверстием, которое имеет проходной диаметр, к примеру, 6 мм, экструдированные ленты должны иметь диаметр не более, чем 8 мм. Более предпочтительно, расширение ленты составляет не более чем 25%, еще более предпочтительно не более чем 20%, наиболее предпочтительно не более чем 15% и в частности не более чем 10%.
Предпочтительно, экструзия производится в отсутствие воды, то есть, вода не добавляется. Тем не менее, капли воды (к примеру, вызванные атмосферной влажностью) могут присутствовать.
Экструдер предпочтительно содержит, по меньшей мере, две температурные зоны, с нагреванием смеси, по меньшей мере, вплоть до температуры размягчения полиалкиленоксида (С), что происходит в первой зоне, которая находится по направлению от зоны подачи и необязательно зоны смешивания. Выработка смеси составляет предпочтительно от 1.0 кг до 15 кг/час. В предпочтительном воплощении, выработка составляет от 1 до 3.5 кг/час. В другом предпочтительном воплощении, выработка составляет от 4 до 15 кг/час.
В предпочтительном воплощении, давление головки червячного пресса имеет значение в диапазоне от 25 до 100 бар. Давление головки червячного пресса может быть подогнано, в том числе посредством геометрии заготовки, температурных свойств и скорости экструзии.
Геометрия заготовки или геометрия скважины выбираются произвольно. Заготовка или скважина могут соответственно экспонировать округлое, продолговатое или овальное поперечное сечение, в котором круглое поперечное сечение предпочтительно имеет диаметр от 0.1 мм до 15 мм и продолговатое поперечное сечение предпочтительно имеет максимальное продольное расширение 21 мм и расширение в поперечном направлении 10 мм. Предпочтительно, заготовка или скважина имеет круговое поперечное сечение. Корпус экструдера, который используется согласно изобретению, может быть с подогревом или охлаждением. Соответствующие температурный контроль, то есть нагревание или охлаждение, устроен таким образом, что смесь которая будет экструдирована вводится, по меньшей мере, в средней температуре (температура продукта), которая соответствует температуре размягчения полиалкиленоксида (С) и не поднимастся выше температуры при которой фармакологически активный ингредиент (А), предпочтительно опиоид, который должен быть обработан, может быть поврежден. Предпочтительно, температура смеси, которая будет экструдирована подгоняется до уровня ниже 180°С, предпочтительно ниже 150°С, но по меньшей мере до температуры размягчения полиалкиленоксида (С). Типичные температуры экструзии составляют 120°С и 130°С.
В предпочтительном воплощении, крутящий момент экструдера находится в диапазоне от 30 до 95%. Крутящий момент экструдера может быть подогнан, в том числе посредством геометрии заготовки, температурных свойств и скорости экструзии.
После экструзии расплавленной смеси и необязательно охлаждения экструдированной ленты или экструдированных лент, экструдированные заготовки предпочтительно разделяют. Это разделение может предпочтительно быть произведено посредством обрезания экструдированных заготовок с помощью вращающихся или ротационных ножей, резчиками из водных струй, проволокой, лезвиями или с помощью лазерных фрез.
Предпочтительно, промежуточное или окончательное хранение необязательно разделенной экструдированной заготовки или окончательной формы фармацевтической лекарственной формы согласно изобретению, которая может быть достигнута, к примеру, при использовании поглотителя кислорода.
Разделенная экструдируемая заготовка может быть отпрессована в таблетки для того, чтобы придать окончательную форму фармацевтической лекарственной форме.
Применение усилия в экструдере к, по меньшей мере, пластифицированной смеси подгоняется посредством регулирования скорости вращения передаточного устройства в экструдере и ее геометрии и посредством задания размерности выпускного отверстия в такой способ, чтоб давление необходимое для экструдирования пластифицируемой смеси накапливалось в экструдере, предпочтительно непосредственно перед экструзией. Экструзионные параметры, которые для каждого конкретного состава являются необходимыми для получения фармацевтической лекарственной формы с желаемыми механическими свойствами, могут быть установлены посредством простого предварительного тестирования.
К примеру, но не ограничиваясь, экструзия может быть произведена при помощи двухвинтового экструдера типа ZSE 18 или ZSE 27 (Leistritz, Nurnberg, Germany), диаметр винтов 18 или 27 мм. Могут быть использованы винты, которые имеют внецентровые окончания. Могут быть использованы нагреваемые заготовки с круговыми скважинами диаметром 7, 8, или 9 мм. Экструзионные параметры могут быть подогнаны, к примеру, к следующим значениям: скорость вращения винтов: 120 Rpm; интенсивность подачи 2 кг/ч для ZSE 18 или 8 кг/ч для ZSE 27; температуры продукта: спереди заготовки 125°С и сзади заготовки 135°С; и температура в рубашке: 110°С.
Предпочтительно, экструзия производится при использовании двухвинтового экструдера или экструдера с планетарным зубчатым механизмом, двухвинтовые экструдеры (вращающиеся в одном направлении или противоположного вращения) будут в частности предпочтительными.
Фармацевтическая лекарственная форма согласно изобретению является предпочтительно произведенная посредством горячего формования с помощью экструдера без каких-либо наблюдаемых в последствии изменений цвета экструдируемых заготовок.
Процесс приготовления фармацевтической лекарственной формы согласно изобретению предпочтительно выполняется непрерывно. Предпочтительно, способ включает экструзию однородной смеси всех компонентов. Это в особенности выгодно, если полученные таким образом промежуточные продукты, к примеру, ленты полученные посредством экструзии, проявляют однородные свойства. В частности желательными являются однородная плотность, однородное распределение активного соединения, однородные механические свойства, однородная пористость, однородный вид поверхности, и т.д. Только при этих условиях однородность фармакологических свойств, таких как стабильность кривой высвобождения, может быть обеспечена и может быть низким количество брака.
Дополнительный объект изобретения относится к упаковкам, которые содержат фармацевтическую лекарственную форму согласно изобретению и поглотитель кислорода. Подходящие упаковки включают блистерные упаковки и бутылки, такие как стеклянные бутылки или бутылки, сделанные из термопластических полимеров.
Подходящие поглотители кислорода являются известными для квалифицированного специалиста в данной области техники. Поглотитель кислорода может быть любым поглотителем, известным в уровне техники, предназначенным для поглощения кислорода. Оба и органический и неорганический поглотители кислорода могут быть использованы.
В одном воплощении, поглотитель кислорода представляет собой любой металлический комплекс, проявляющий поглощающее кислород действие. Примеры включают комплексы, которые содержат один или более из алюминия, ферросилиций алюминия, сурьмы, бериллия, силицида кальция, церия, кобальта, галлия, гафния, железа, магниевого сплава, никелевого катализатора, селена, кремния, серебра, стронция, титана, цинка, и/или циркония.
В еще одном воплощении, один или несколько элементов из Группы IA периодической таблицы и их сплавы и соединения могут быть использованы в качестве поглотителей кислорода. Примеры элементов Группы IA включают цезий, литий, калий, натрий. Кроме того примеры неорганических поглотителей кислорода включают один или более из натриевой соли азотоводородной кислоты (NaN3), сернистокислого натрия (Na2SO3), гидразина и гидроксиламина.
В одном воплощении, поглотитель кислорода представляет собой органическое соединение. Примеры включают один или несколько из политерпенов, аскорбиновой кислоты, аминополикарбоксиловой кислоты, циклогександиона, тетраметил пиперидона, и гетероциклических соединений с N-замещенными аминогруппами.
Поглотители кислорода и их применение в фармацевтических упаковках являются известными для квалифицированного специалиста в данной области. В предпочтительном воплощении, поглотитель кислорода выбран из группы, которая состоит из метал-катализированных окисленных органических полимеров и антиоксидантов. В особенности предпочтительными являются такие поглотители кислорода, которые в состоянии действовать в сухих условиях ниже 60% относительной влажности, предпочтительно ниже 30% относительной влажности и которые являются комбинированными с осушителем. К примерам коммерчески доступных поглотителей кислорода, удовлетворяющих этим требованиям, относятся Pharmakeep® KD10 и KD20.
К удивлению было обнаружено, что стабильность при хранении фармацевтической лекарственной формы может быть увеличена при поддержании низкого содержания кислорода в атмосфере в рамках упаковки. Методы упаковок фармацевтических лекарственных форм и применение подходящих поглотителей кислорода являются известными для квалифицированного специалиста в данной области техники. В этом отношении может быть сделана ссылка на, к примеру, D.A.Dean, Pharmaceutical Packaging Technology, Taylor & Francis, 1st ed.; F.A.Paine et al.. Packaging Pharmaceutical и Healthcare Products, Springer, 1st ed.; и O.G.Piringer et al., Plastic Packaging: Interactions with Food и Pharmaceuticals, Wiley-VCH, 2nd ed.
Что касается упаковки, то круглые бутылки из полиолефинов, предпочтительно из ПЭНД, являются предпочтительными. Толщина стенки бутылки составляет предпочтительно по меньшей мере 0.25 мм, более предпочтительно по меньшей мере 0,5 мм, в противном случае бутылка может разрушится.
Что касается крышки упаковки, то упаковка является предпочтительно индукционной или теплоизолированной алюминиевой фольгой.
К удивлению было обнаружено, что выбрав соответствующую форму упаковки и запечатывания, вакуум, который создается посредством эффекта поглотителя кислорода (разрежение около 20,000 Па = 2 Н/см2) может быть обработан руками не вызывая разрушения упаковки. Индукционное закупоривание (к примеру, 3 секундная энергия) является предпочтительной. При уплотнении 75 мл бутылка с отверстием диаметром 1 дюйм с алюминиевой фольгой, разрежение 20,000 Па из-за поглощения кислорода приводит в результате к усилию около 10Н, что соответствует силе, которая оказывается под весом 1 кг.
Механическая стабильность уплотнения может быть протестирована либо путем введения соответствующего количества поглотителя кислорода в бутылку, запечатывания ее и ожидания достаточно длительного периода времени, к примеру 2 дней так, чтобы кислород был поглощен и разрежение около 20,000 Па было достигнуто. Кроме того, бутылка может быть закрыта без какого либо поглотителя кислорода в ее содержимом и вес в 1 кг можно разместить на алюминиевой фольге внешне таким образом, чтоб имитировать усилие.
Дополнительный аспект изобретения относится к использованию фармакологически активного ингредиента (А), предпочтительно опиоида, для производства фармацевтической лекарственной формы как описано выше для лечения боли.
Дополнительный аспект изобретения относится к использованию фармацевтической лекарственной формы как описано выше для предотвращения или препятствования злоупотреблению фармакологически активным ингредиентом (А), предпочтительно опиоидом, содержащимся в ней.
Дополнительный аспект изобретения относится к использованию фармацевтической лекарственной формы как описано выше для предотвращения или воспрепятствования непреднамеренной передозировке опиоида (А) содержащегося в ней.
В этом отношении, изобретение также относится к использованию фармакологически активного ингредиента (А), предпочтительно опиоида, как описано выше и/или полиалкиленоксида (С) как описано выше для производства фармацевтической лекарственной формы согласно изобретению для профилактики и/или лечения расстройств, тем самым предотвращая передозировку фармакологически активного ингредиента (А), предпочтительно опиоида, в частности в виду измельчения фармацевтической лекарственной формы посредством механического воздействия.
Кроме того, изобретение относится к методу профилактики и/или лечения расстройств, который включает введение фармацевтической лекарственной формы согласно изобретению, тем самым предотвращая передозировку фармакологически активного ингредиента (А), предпочтительно опиоида, в частности из-за измельчения фармацевтической лекарственной формы посредством механического воздействия. Предпочтительно, механическое воздействие выбран из группы, которая состоит из жевания, измельчения в ступке, дробления, и использования аппаратов для измельчения обычных фармацевтических лекарственных форм.
Следующие примеры иллюстрируют изобретение, но не должны толковаться как ограничение сферы его применения.
Пример 1
Таблетки были приготовлены посредством экструзии горячего расплава различных однородных составных смесей при следующих идентичных экструзии условиях:
Тип экструдера: Leistritz Extruder ZSE18PH 40D оборудованный высоко срезными винтами и головкой диаметром 9 мм
выработка: 1.0 кг/ч
скорость вращательного движения: 100 оборотов в минуту
температура корпуса: 100°С
температура экструдируемой заготовки: 120°С
Экструдируемую заготовку нарезают ломтиками 325 мг, которые содержат около 5 мг гидрохлорида оксиморфона.
Отдельные компоненты экструдированной смеси, а также общее количество продуктов деструкции до и после хранения при ускоренных условиях хранения собраны в таблице ниже:
Продукты деструкции были проанализированы посредством ВЭЖХ-УФ. Пик элюирования для оксиморфон-N-оксида не мог быть в достаточной степени базисно отделен от пика неизвестного продукта деструкции (называется "UK 0.83"). Таким образом, оба пика были совместно интегрированы. Очевидным становится из сравнения примеров A1-A5, что содержание оксиморфон-N-оксида перед хранением (oNo1) существенно не изменяется, когда содержание антиоксиданта α-токоферол снижается от 1.5 мас.% до 1.0 мас.%, 0.5 мас.%, 0.2 мас.% и даже 0 мас.%. При хранении (oNo2), тем не менее, содержание оксиморфон-N-оксида является пропорциональным содержанию α-токоферола. Это особенно удивительно, потому что оксиморфон-N-оксид представляет собой продукт окисления и можно было бы ожидать, что антиоксиданты как правило скорее подавляют, чем поддерживают образование продуктов окисления.
Тем не менее, полное выпадение антиоксиданта (α-токоферол) может иметь недостатки. Посредством измерений вязкости (в отсутствие кислоты (В)) может быть показано, что высокомолекулярный полиэтиленоксид разлагается при экструзии и/или хранении в отсутствие антиоксиданта. Тем не менее, к удивлению было обнаружено, что в определенной степени кислоты (В) в свою очередь может быть компенсирована такая деструкция, так что в некоторых воплощениях антиоксиданты могут быть опущены или их содержание может быть существенно уменьшено.
К удивлению было обнаружено, что около 0.2 мас.% α-токоферола достаточно для того, чтобы стабилизировать полиэтиленоксид; повышенное содержание α-токоферола не приведет к повышению вязкости полиалкиленоксида и, таким образом, не препятствует более выраженному ПЭО от разрушения. Таким образом, содержание антиоксиданта (α-токоферол) является предпочтительно сбалансировано таким образом, что с одной стороны высокомолекулярный полиэтиленоксид является в достаточной степени стабилизирован и с другой стороны, нежелательное образование оксиморфон-N-оксида поддерживается на низком уровне во время хранения.
Кроме того, из сравнения примеров B1-B4 и примеров C1-С4 становится очевидным, что частичная замена высокомолекулярного полиэтиленоксида или полная замена полиэтиленгликоля альтернативным пластификатором не приведет к существенному уменьшению содержания нежелательного оксиморфон-N-оксида. Это удивительно, потому что можно было бы ожидать, что полиэтиленоксид и полиэтиленгликоль являются потенциальными переносчиками пероксидов и что их сокращение может привести к снижению окислительных процессов, таких как окисление оксиморфона до оксиморфон-N-окисда.
Еще кроме того, из сравнения примеров D1-D5 и E1-E4 становится очевидным, что добавление физиологически приемлемых кислот, в частности лимонной кислоты, приводит к снижению образования оксиморфон-N-оксида. Этот эффект более выражен, когда количество кислоты увеличивается. При концентрации 0.1 мас.% эффект будет сравнительно слабым, но при концентрации 0.2 мас.% эффект будет сильнее и еще более усиливается, когда концентрация лимонной кислоты увеличивается. Не только количество оксиморфон-N-оксида увеличивается, но также общее количество продуктов деструкции, в частности те, которые имеют высокое время удержания ВЭЖХ.
Пример 2:
Таблетки, которые были изготовлены по аналогии с пр. A1, B1, C1, D1 и E1 выше были упакованы в различные упаковочные материалы и хранились при 40°С и 75% отн. влажности. Продукты деструкции до и после хранения при ускоренных условиях хранения приведены в таблице здесь ниже:
К удивлению было обнаружено, что включение поглотителя кислорода в упаковке приводит к дополнительной стабилизации лекарственной формы, так что образование продуктов деструкции ограничено до очень низкого объема.
Пример 3:
Таблетки были произведены как описано в примере 1, упакованы в ПЭНД бутылки 75 мл объема вместе с поглотителем кислорода в сочетании с осушителем (Pharmakeep 20 KD), закрыты пластиковой крышкой с индукционным затвором.
Отдельные компоненты экструдируемых смесей, общее количество продуктов деструкции до и после хранения при ускоренных условия хранения приведены в таблице здесь ниже:
Результаты показали, что чистота продукта является очень высокой после изготовления и продукт проявляет стабильность в течение 8 недель хранения в ускоренных условиях при 40°С/75% отн. влажности.
Пример 4:
Таблетки были изготовлены как описано в примере 1, но нарезаны ломтиками 215 мг составили 5 мг или 40 мг оксиморфона HCl, после образования таблетки были покрыты 6.5 мг каждая обычным Opadry II пленочным покрытием, содержащим поливиниловый спирт в качестве пленкообразующего наполнителя, упакованы в ПЭНД бутылки объемом 75 мл вместе с поглотителем кислорода в сочетании с осушителем (Pharmakeep 20 KD), закрыты пластиковой крышкой с индукционным затвором.
Отдельные компоненты экструдируемых смесей, общее количество продуктов деструкции до и после хранения при ускоренных условиях хранения приведены в таблице здесь ниже:
Пример 5:
Наиболее предпочтительная лекарственная форма в соответствии с примером 3 является также подходящей для стабилизации оксикодона. Это могло быть продемонстрировано для состава, содержащего 80 мг оксикодона HCl произведенного по аналогии с примером 1, но экструдируемая заготовка была нарезана ломтиками по 400 мг:
Пример 6:
В одной дозе (40 мг оксиморфона HCl, таблетки из примера 4), рандомизиованные, с трехсторонним перекрестным исследованием с 1 неделей между лечением субъекты голодали всю ночь и принимали спустя 4 и 10 часов после введения доз. Воду не давали в пределах ±1 часа от введения дозы. Все таблетки были приняты с 240 мл воды (пример Т).
Образцы для фармакокинетики были взяты для оксиморфона и 6-ОН-оксиморфона перед использованием препарата и через 48 часов после введения дозы.
Биоэквивалентности были сравнены с Opana ER® (ссылка R). Результаты приведены в таблице здесь ниже:
Становится очевидным, что лекарственные формы согласно изобретению, которые имеют увеличенное сопротивление разрушению являются биоэквивалентными к обычным лекарственным формам (Opana ER®).
Пример 7:
Таблетки были приготовлены при одинаковых условиях посредством экструзии горячего расплава двух однородных составных смесей I1 и I2
при следующих идентичных условиях экструзии:
тип экструдера: Leistritz Extruder тип Micro 27 6L 40 D оборудованный средовыми срезными винтами и заготовкой диаметром 8 мм
выработка: 10 кг/ч
скорость вращательного движения: 120 оборотов в минуту
время изготовления: 30 мин
температура temperature зоны перегретой плавки: 100°С
температура заготовки: 130°С.
Экструдируемая заготовка была нарезана ломтиками 360 мг, содержащие около 40 мг гидрохлорида оксиморфона.
100 ломтиков были взвешены индивидуально и стандартное отклонение массы было рассчитано. Ломтики состава I1 (ПЭОЛЭГ=6.82:1) показали стандартное отклонение 2.3%, в то время как ломтики состава I2 (ПЭСШЭГ=4.21:1) показали только стандартное отклонение 1.6%.
Из этих сравнительных тестов становится очевидным к удивлению, что технологичность экструдированной массы может быть улучшена путем изменения соотношения ПЭО к ПЭГ.
Пример 8:
С целью исследования когда также многоосновные карбоновые кислоты помимо лимонной кислоты могли бы препятствовать образованию оксиморфон-N-оксида, таблетки, содержащие малеиновую кислоту или фумаровую кислоту были произведены как описано в примере 1. Для сравнения также были произведены таблетки содержащие неорганическую соль NaH2PO4 Образцы были сохранены в открытых блюдцах при 40°С и 75% относительной влажности в течение 4 недель.
Отдельные компоненты экструдируемых смесей, также как и общее количество продуктов деструкции до и после хранения при ускоренных условиях хранения были суммированы в таблице здесь ниже:
В случае малеиновой и фумаровой кислоты эти соединения и для малеиновой кислоты другое связанное соединение были исследованы в течение тестов на исследование чистоты в качестве примесей (примерно до 40%). Их значения были вычтены из суммы примесей.
Становится очевидным из сравнения примеров J1 и J2-A1 и B1, что присутствие малеиновой и фумаровой кислоты защищает оксиморфон полностью от окисления N-оксидом и в значительной степени по отношению к другим деградациям несмотря на то, что образцы были сохранены в открытых емкостях, а не в закрытых бутылках. Эти результаты сопоставимы с полученными с лимонной кислотой (пример 1, D4 и Е2-E4). Образцы, содержащие NaH2PO4 (J3) проявляли защиту от образования N-оксида и другой деструкции по сравнению с составами без какого-либо кислого соединения (A1 и B1), но в меньшей степени, чем многоосновные карбоновые кислоты типа лимонной, малеиновой и фумаровой кислоты.
Пример 9:
С целью исследования, когда присутствие лимонной кислоты также защищает от окисления чувствительные опиоиды кроме оксиморфона от N-окисления, таблетки содержащие гидрохлорид оксикодона были изготовлены как описано в примере 1.
Для сравнения, также таблетки содержащие меньшее количество α-токоферола были произведены. Образцы были сохранены в открытых емкостях при 40°С и 75% относительной влажности в течение 4 недель.
Отдельные компоненты экструдируемых смесей так же как и общее количество продуктов деструкции до и после хранения при ускоренных условиях хранения были суммированы в таблице здесь ниже:
Эти результаты показывают, что лимонная кислота защищает оксикодон полностью от окисления N-оксидом и в большей степени от другой деструкции, несмотря на то, что образцы были сохранены в открытых емкостях, а не в закрытых бутылках. Уменьшение количества α-токоферола привело в результате к снижению деструкции, когда были использованы составы, не содержащие лимонную кислоту. Эти результаты сопоставимы с теми, что получены с оксиморфоном.
Пример 10:
В соответствии с Примером 1, таблетки, содержащие трамадол HCL были произведены из следующих составов:
Профиль растворения таблеток был исследован при следующих условиях: прибор с лопастью для проведения теста «Растворение» оборудованный грузилом, 75 оборотов в минуту, 37°С, 600 мл моделируемый рН 6.8 интестинальной среды (фосфатный буфер). Кривая высвобождения трамадола была определена спектрометрически при 271 нм.
Результаты отображены на Фигуре 1.
Таблетки в соответствии с примером L2 показывает ускоренное растворение, которое составляет приблизительно на 20% бестрее, чем медленное высвобождение таблеток в соответствии с примерами L1 и L4 после 480 минут. Высвобождение из таблеток в соответствиии с L3 является быстрее, чем те две партии, но все еще примерно на 6% медленнее, чем из таблеток в соответствии с L2 после 480 минут.
Это удивительно, так как наблюдается большое влияние присутствия α-.токоферола на профиль растворения. Это в особенности удивительно, учитывая, что роль α-токоферола в составе должна представлять собой действие в качестве антиоксиданта для предотвращения деструкции полимера.
Интересно, что присутствие лимонной кислоты компенсирует небольшую часть этого эффекта.
Пример 11:
Посредством разбухания таблетки в соответствии с примерами L1 (Пример 10) в соответствующем количестве воды, был получен однородный гель. Соответственным образом, таблетки в соответствии с примерами L2-L4 были подвергнуты разбуханию в таком же количестве воды, то есть при идентичных условиях, для получения соответствующих гелей. Вязкость каждого геля была измеряна как косвенный показатель для длины цепи полимера этиленоксида, содержащегося в нем. Измерения вязкости были проведены при помощи ротационного вискозиметра при скорости сдвига 40 с-1.
В сравнении с профилем растворения по примеру 10, была получена та же очередность: состав в соответствии с примером L2 проявляет низкую вязкость, в то время как составы в соответствии с примерами L1 и L4 проявляют высокую вязкость. Состав в соответствии с примером L3 проявляет значительно более низкую вязкость, чем два высоковязких состава, но все еще выше, чем состав L2.
Высокая вязкость составов L1 и L4 является показателем к более высокой средней длине цепи полимера полиэтиленоксида, содержащегося в них. Судя по всему, полиэтиленоксид, содержащийся в составах L1 и L4 имеет меньшую подверженность повреждению посредством деструкции окислением в процессе производства лекарственной формы, чем составы L2 и L3.
Суммируя результаты измерений профиля растворения (Пример 10) и измерений вязкости, можно сделать вывод, что увеличение скорости растворения является основанным на более выраженной деструкции полимера во время производства для партий без а -токоферола (примеры L2 и L3).
Эти результаты показали, что кислота (В), к примеру лимонная кислота, также имеет защитный эффект на полимере во время производства. Состав L3 который не содержит какой-либо α-токоферол, но лимонная кислота показывает более высокую вязкость и более низкое ускорение растворения по сравнению с составом L2 который не содержит ни α-токоферола, ни лимонной кислоты.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАЩИЩЕННАЯ ОТ ПРИМЕНЕНИЯ НЕ ПО НАЗНАЧЕНИЮ ЛЕКАРСТВЕННАЯ ФОРМА ДЛЯ ЧУВСТВИТЕЛЬНЫХ К ОКИСЛЕНИЮ ОПИОИДОВ | 2010 |
|
RU2555531C2 |
| УСТОЙЧИВАЯ К РАЗРУШЕНИЮ ЛЕКАРСТВЕННАЯ ФОРМА, СОДЕРЖАЩАЯ НЕОРГАНИЧЕСКУЮ СОЛЬ | 2011 |
|
RU2604676C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТВЕРДОЙ ЛЕКАРСТВЕННОЙ ФОРМЫ, В ЧАСТНОСТИ ТАБЛЕТКИ ДЛЯ ФАРМАЦЕВТИЧЕСКОГО ПРИМЕНЕНИЯ, И СПОСОБ ПОЛУЧЕНИЯ ПРЕКУРСОРА ТВЕРДОЙ ЛЕКАРСТВЕННОЙ ФОРМЫ, В ЧАСТНОСТИ ТАБЛЕТКИ | 2009 |
|
RU2508092C2 |
| ЛЕКАРСТВЕННАЯ ФОРМА | 2009 |
|
RU2493830C2 |
| УСТОЙЧИВАЯ К РАЗРУШЕНИЮ ЛЕКАРСТВЕННАЯ ФОРМА, КОТОРАЯ СОДЕРЖИТ АНИОННЫЙ ПОЛИМЕР | 2011 |
|
RU2607499C2 |
| СПОСОБ ПРИГОТОВЛЕНИЯ АНАЛЬГЕТИКОВ | 2007 |
|
RU2422445C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ОПИОИДНЫЙ АНТАГОНИСТ, ДЛЯ ЛЕЧЕНИЯ ЗАДЕРЖКИ МОЧИ | 2009 |
|
RU2478388C2 |
| ЭКСТРУДИРОВАННАЯ ИЗ ГОРЯЧЕГО РАСПЛАВА ФАРМАЦЕВТИЧЕСКАЯ ЛЕКАРСТВЕННАЯ ФОРМА | 2010 |
|
RU2547555C2 |
| КОМБИНАЦИИ АГОНИСТ/АНТАГОНИСТ ОПИОИДА | 1998 |
|
RU2241458C2 |
| ФАРМАЦЕВТИЧЕСКИЕ СИСТЕМЫ ДОСТАВКИ ДЛЯ ГИДРОФОБНЫХ ЛЕКАРСТВЕННЫХ СРЕДСТВ И КОМПОЗИЦИЙ, ИХ СОДЕРЖАЩИХ | 2006 |
|
RU2429850C2 |
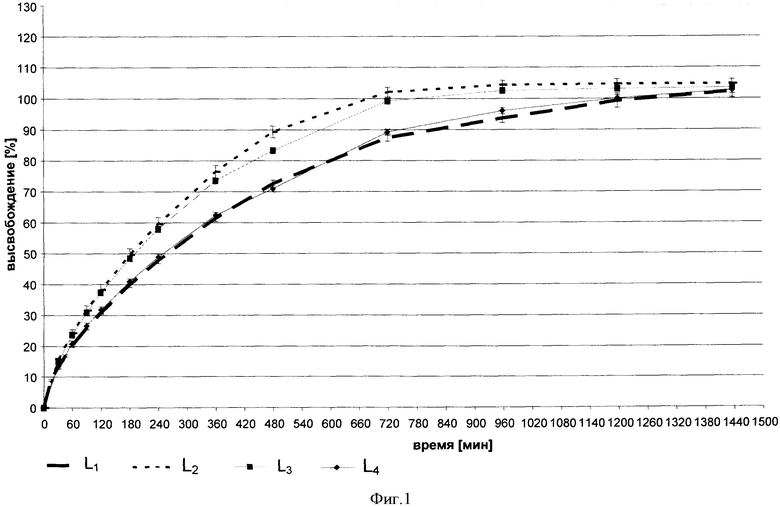
Группа изобретений относится к термоформируемой фармацевтической лекарственной форме, которая имеет сопротивление разрушению по крайней мере 300 Н, и к способу её получения. Указанная лекарственная форма содержит фармакологически активный ингредиент (А), выбранный из морфина, гидроморфона, оксикодона, гидрокодона, оксиморфона, (1R,2R-3-(3-диметиламино-1-этил-2-метил-пропил)фенола и их физиологически приемлемых солей, свободную физиологически приемлемую кислоту (В) в количестве 0,3±0,18 мас.% в пересчете на общую массу фармацевтической лекарственной формы, антиоксидант в количестве от 0,001 мас.% до 5,0 мас.% в пересчете на общую массу фармацевтической лекарственной формы и полиалкиленоксид (С), который имеет среднемассовую молекулярную массу Mw по крайней мере 200,000 г/моль. Способ получения данной лекарственной формы включает смешивание всех компонентов, нагревание до точки размягчения полиэтиленоксида (С), выдавливание через выходное отверстие экструдера, отделение пластичного экструдата и формирование фармацевтической лекарственной формы или охлаждение. Технический результат: повышение стабильности фармацевтической лекарственной формы при хранении. 2 н. и 11 з.п. ф-лы, 1 ил., 9 пр.
1. Прочная на излом фармацевтическая лекарственная форма в форме таблетки, которая имеет сопротивление разрушению по крайней мере 300 Н, термоформируемая путем экструзии горячего расплава смеси, которая включает
- фармакологически активный ингредиент (А), выбранный из группы, включающей морфин, гидроморфон, оксикодон, гидрокодон, оксиморфон, (1R,2R)-3-(3-диметиламино-1-этил-2-метилпропил)фенол и их физиологически приемлемые соли,
- свободную физиологически приемлемую многоосновную карбоновую кислоту (В) в количестве 0,3±0,18 мас.% в пересчете на общую массу фармацевтической лекарственной формы и
- антиоксидант, выбранный из группы, включающей аскорбиновую кислоту или ее соли, аскорбилпальмитат, α-токоферол, витамин Е-сукцинат, витамин Е-пальмитат, бутилгидроксианизол, бутилгидрокситолуол, монотиоглицерин, конифериловый бензоат, нордигидрогваяретовую кислоту, сложные эфиры галловой кислоты, фосфорную кислоту и бисульфит натрия в количестве от 0.001 мас.% до 5.0 мас.% в пересчете на общую массу фармацевтической лекарственной формы; и
- полиалкиленоксид (С), который имеет среднемассовую молекулярную массу Mw по крайней мере 200,000 г/моль.
2. Фармацевтическая лекарственная форма по п.1, в которой многоосновная карбоновая кислота выбрана из группы, включающей малеиновую кислоту, фумаровую кислоту, пентандиовую кислоту, малоновую кислоту и лимонную кислоту.
3. Фармацевтическая лекарственная форма по п.1, в которой антиоксидант представляет собой α-токоферол.
4. Фармацевтическая лекарственная форма по п.1, в которой после хранения на протяжении 4 недель при 40°С и 75% отн. влажности содержание фармакологически активного ингредиента (А) составляет по крайней мере 98.0% его первоначального содержания перед хранением.
5. Фармацевтическая лекарственная форма по п.1, в которой после хранения на протяжении 4 недель при 40°С и 75% отн. влажности содержание полиэтиленоксида (С) составляет по крайней мере 98.0% его первоначального содержания перед хранением.
6. Фармацевтическая лекарственная форма по п.1, в которой фармакологически активный ингредиент (А) внедрен в матрицу, включающую полиалкиленоксид (С), где указанная матрица регулирует высвобождение фармакологически активного ингредиента (А) из фармацевтической лекарственной формы.
7. Фармацевтическая лекарственная форма по п.1, в которой фармакологически активный ингредиент (А) выбран из группы, включающей оксиморфон, оксикодон, гидроморфон и их физиологически приемлемые соли.
8. Фармацевтическая лекарственная форма по п.1, в которой относительное соотношение массы полиалкиленоксида (С) к фармакологически активному ингредиенту (А) составляет по крайней мере 1:1.
9. Фармацевтическая лекарственная форма по п.1, которая является адаптированной для введения один раз в сутки или два раза в сутки.
10. Фармацевтическая лекарственная форма по п.1, которая имеет сопротивление разрушению по крайней мере 500 Н.
11. Фармацевтическая лекарственная форма по п.1, которая помещена в упаковку, содержащую поглотитель кислорода.
12. Способ получения фармацевтической лекарственной формы по любому из пп.1-10, который включает этапы:
a) смешивание всех компонентов;
b) нагревание получившейся в результате смеси в экструдере по крайней мере до точки размягчения полиалкиленоксида (С) и выдавливание через выходное отверстие экструдера с применением силы,
c) отделение еще пластичного экструдата и формирование в фармацевтическую лекарственную форму или
d) охлаждение.
13. Способ получения фармацевтической лекарственной формы по п.12, который дополнительно включает повторный нагрев отделенного экструдата и формирование его в фармацевтическую лекарственную форму.
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Биохимия М., Мир 1974 с.68 глава Денатурация | |||
Авторы
Даты
2015-11-10—Публикация
2010-07-21—Подача