Изобретение касается фотополимерной композиции, включающей полимеры матрицы, записывающие мономеры и фотоинициаторы. Другими предметами изобретения являются применения этой фотополимерной композиции для изготовления голографических сред.
Фотополимерные композиции указанного в начале типа являются известными в вопросах уровня техники. Так, например, в международной заявке WO 2008/125229 A1 описана фотополимерная композиция, которая содержит полимеры матрицы на основе полиуретанов, записывающий мономер на основе акрилата, а также фотоинициаторы. В отвержденном состоянии записывающий мономер и фотоинициаторы включены в полиуретановую матрицу с однородным распределением по объему.
Из патента США 2005/031986 A1 также известна фотополимеризующаяся композиция, которая включает полимеры матрицы, записывающие мономеры на основе сложных эфиров и фотоинициаторы. Трехмерно же сшитые полиуретановые полимеры матрицы в этом документе не предлагаются.
Для применения фотополимерных композиций решающую роль играет вызываемая в фотополимере голографическим освещением амплитуда изменения показателя преломления Δn. В случае голографического освещения интерференционное поле из предметного луча и луча сравнения (в простейшем случае двух плоских волн) в результате локальной фотополимеризации, например, акрилатов с высоким показателем преломления, в точках высокой интенсивности интерференционного поля преобразуется в решетку с различными показателями преломления. Эта решетка с различными показателями преломления в фотополимере (голограмма) содержит всю информацию предметного луча. Тогда путем освещения этой голограммы только лучом сравнения сигнал снова может быть восстановлен. Отношение мощности восстановленного таким образом сигнала к мощности падающего луча сравнения называется дифракционной эффективностью, в дальнейшем обозначаемой DE, сокр. от англ. Diffraction Efficiency.
В простейшем случае для голограммы, которая возникает при наложении двух плоских волн, DE получается из отношения интенсивности волны, дифрагированной при восстановлении, и суммы интенсивностей проникающего луча сравнения и дифрагированной волны. Чем больше эта DE, тем эффективней голограмма по отношению к необходимому количеству световой энергии луча сравнения, которое необходимо, чтобы сделать видимым сигнал стабильной яркости.
Акрилаты, имеющие высокий показатель преломления, могут давать решетку с различными показателями преломления с большой амплитудой между областями с низким показателем преломления и областями с высоким показателем преломления и тем самым делать возможным образование в фотополимерных композициях голограмм с высокой DE и высокой Δn. При этом следует принимать во внимание, что DE полученного изделия зависит от Δn и толщины фотополимерного слоя d. Чем больше полученное изделие, тем больше возможная DE (для отражательной голограммы). Ширина углового диапазона, при котором эта голограмма становится видимой (восстанавливается), например, при монохроматическом освещении, зависит только от толщины слоя d.
При освещении голограммы, например, белым светом, ширина спектральной области, которая может содействовать восстановлению голограммы, также зависит только от толщины слоя d. При этом справедливо то, что чем меньше d, тем больше соответствующие диапазоны применимости. Следовательно, если хотят получить яркие и легко визуально различимые голограммы, то нужно добиваться высокой Δn и незначительной толщины d, а именно таким образом, чтобы DE становилась максимально большой. То есть, чем выше становится Δn, тем больше свободы достигают в отношении конструирования толщины слоя d для яркой голограммы без потери для DE. Таким образом, оптимизирование Δn при оптимизировании фотополимерных композиций имеет выдающееся значение (P.Hariharan, Optical Holography, 2nd Edition, Cambridge University Press, 1996).
Для того чтобы иметь возможность реализовать для голограмм как можно более высокие значения Δn и DE, полимеры матрицы и записывающие мономеры фотополимерной композиции в основном должны выбираться таким образом, чтобы они как можно сильнее различались по своим показателям преломления. В одном варианте исполнения это означает, что применяются полимеры матрицы с как можно более низким, а записывающие мономеры с как можно более высоким показателем преломления. Правда, при этом подходе существуют отдельные сложности: так, это большое различие в показателях преломления между полимерами матрицы и записывающими мономерами приводит к тому, что оба компонента не могут смешиваться в любой степени, что может объясняться структурными различиями компонентов, выраженными в различии показателей преломления. Это, в частности, означает, что количество записывающего мономера, которое можно использовать в фотополимерной композиции, является ограниченным, поскольку в случае его превышения доходит до расслоения компонентов, чего, безусловно, следует избегать. В противном случае, среда из соответствующей композиции может утратить свою функциональность, или даже голограмма, записанная в среде такого типа, впоследствии может повреждаться или разрушаться.
Тем не менее, представляет интерес также иметь в распоряжении фотополимерные композиции с высоким содержанием записывающих мономеров, поскольку тем самым, с одной стороны, могут быть изготовлены более яркие голограммы, а, с другой стороны, также благоприятным образом устанавливаются механические характеристики, чтобы содействовать хорошей интеграции голограммы в других материалах.
Следовательно, задачей данного изобретения было предоставить фотополимерную композицию, которая может содержать более высокую концентрацию записывающих мономеров в сравнении с известными композициями, без того, чтобы возникали описанные выше отрицательные эффекты, и одновременно с помощью которой могут получаться яркие голограммы.
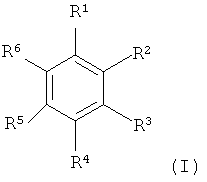
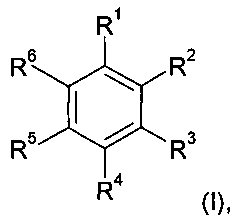
Эта задача в случае фотополимерной композиции согласно изобретению решается благодаря тому, что записывающие мономеры содержат ароматические соединения формулы (I)
 ,
,
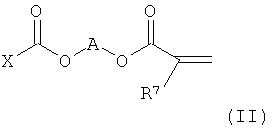
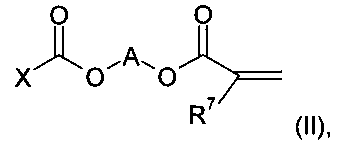
в которой по меньшей мере один из остатков R1, R2, R3, R4, R5, R6 представляет собой соединенный через X с ароматическим кольцом остаток формулы (II)
 ,
,
причем в формуле (II) A является линейной или разветвленной, при необходимости содержащей кислород или азот углеводородной цепью, остальные остатки R1, R2, R3, R4, R5, R6 соответственно независимо друг от друга представляют собой атом водорода или органический остаток, a R7 является атомом водорода или метилом.
Таким образом, X не является группой, а исключительно характеризует положение остатка формулы (II), через которое этот остаток связан с ароматическим кольцом.
Голограммы, которые записываются, например, в пленках из фотополимерной композиции согласно изобретению, отличаются своей высокой яркостью. Кроме того, возможно увеличить концентрацию записывающих мономеров в сравнении с известными фотополимерными композициями без того, чтобы возникало расслоение компонентов композиции.
Соединения формулы (I) могут получаться, например, в результате взаимодействия активированных производных ароматических карбоновых кислот, таких как хлорангидриды, с функционализированными спиртами формулы (IIa)
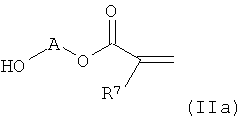
или в результате катализируемого кислотой взаимодействия ароматических карбоновых кислот с функционализированными спиртами формулы (IIa).
Получение соединений такого типа описывается, например, в японских патентах JP 61012925, JP 48008744 и патенте США US 1987-77715.
Предпочтительно два или три из остатков R1, R2, R3, R4, R5, R6 могут быть остатками формулы (II), через X присоединенными к ароматическому кольцу. В этом случае записывающий мономер формулы (I) имеет более высокую плотность двойных связей. Результатом этого является более высокая реакционная способность, более высокая степень превращения и более сильная химическая сшивка компонентов записывающего мономера. Полученный таким образом химически сшитый компонент записывающего мономера имеет более высокую среднюю молекулярную массу, чем линейный полимер на основе монофункционального записывающего мономера, и является тем самым значительно более устойчивым к диффузии и лишенным подвижности. Функциональность по двойным связям >1,0 также может устанавливаться любой при помощи смешиваний моно- и имеющих более высокую функциональность по двойным связям записывающих мономеров.
Особенно предпочтительным является, когда присутствуют два остатка формулы (II), при условии, что эти остатки присоединены в мета- или пара-положении ароматического кольца, и когда присутствуют три остатка формулы (II), при условии, что эти остатки присоединены соответственно в мета-положениях.
Согласно предпочтительному варианту исполнения предусматривается, что этот органический остаток содержит радиационно-отверждаемую группу. Под радиационно-отверждаемой группой согласно данному изобретению понимают функциональную группу, которая при действии актиничного излучения реагирует с образованием полимеров. Особенно предпочтительно, если радиационно-отверждаемая группа представляет собой акрилатную или метакрилатную группу. В этом случае записывающий мономер формулы (I) также имеет повышенную или гораздо более повышенную плотность двойных связей, что влечет за собой уже указанные выше преимущества.
Особенно яркие голограммы могут получаться с помощью фотополимерных композиций, которые содержат записывающие мономеры, у которых А представляет собой этил (-CH2-СН2-), пропил (-СН2-CH 2-СН2-) или бутил (-CH2-CH2-CH2-CH2-), (-СН2-СН(CH)3-СН2).
Полимеры матрицы могут представлять собой, прежде всего, полиуретаны.
Предпочтительно эти полиуретаны могут получаться в результате взаимодействия изоцианатного компонента a) с компонентом b), реакционноспособным в отношении изоцианатов.
Изоцианатный компонент a) предпочтительно включает полиизоцианаты. В качестве полиизоцианатов могут использоваться все хорошо известные специалисту соединения или их смеси, которые в среднем содержат две или больше NCO-функциональных групп в молекуле. Они могут иметь ароматическую, арилалифатическую, алифатическую или циклоалифатическую основу. Также во вспомогательных количествах совместно могут использоваться моноизоцианаты и/или полиизоцианаты, содержащие ненасыщенные группы.
Например, подходящими являются бутилендиизоцианат, гексаметилендиизоцианат (ГМДИ), изофорондиизоцианат (ИФДИ), 1,8-диизоцианато-4-(изоцианатометил)октан, 2,2,4- и/или 2,4,4-триметилгексаметилендиизоцианат, изомерные бис-(4,4′-изоцианотоциклогексил)метаны и их смеси с любым содержанием изомеров, изоцианатометил-1,8-октандиизоцианат, 1,4-циклогексилендиизоцианат, изомерные циклогександиметилендиизоцианаты, 1,4-фенилендиизоцианат, 2,4- и/или 2,6-толуилендиизоцианаты, 1,5-нафтилендиизоцианат, 2,4′- или 4,4′-дифенилметандиизоцианаты и/или трифенилметан-4,4′,4″-триизоцианат.
Также возможно использование производных мономерных ди- или триизоцианатов с уретановыми, карбамидными, карбодиимидными, ацилкарбамидными, изоциануратными, аллофанатными, биуретовыми, оксадиазинтрионовыми, уретдионовыми и/или иминооксадиазиндионовыми структурами.
Предпочтительным является использование полиизоцианатов на основе алифатических и/или циклоалифатических ди- или триизоцианатов.
Особенно предпочтительно полиизоцианатами компонента a) являются ди- или олигомеризованные алифатические и/или циклоалифатические ди- или триизоцианаты.
В высшей степени предпочтительными являются изоцианураты, уретдионы и/или иминооксадиазиндионы на основе ГМДИ, 1,8-диизоцианато-4-(изоцианатометил)октана или их смеси.
Также в качестве компонента a) могут использоваться NCO-функциональные форполимеры с уретановыми, аллофанатными, биуретовыми и/или амидными группами. Форполимеры компонента а) получаются по способу хорошо известному специалисту, путем взаимодействия мономерных, олигомерных или полимерных изоцианатов a1) с соединениями a2), реакционноспособными по отношению к изоцианатам, в походящем стехиометрическом соотношении, при желании с использованием катализаторов и растворителей.
В качестве полиизоцианатов a1) подходят все известные специалисту алифатические, циклоалифатические, ароматические или арилалифатические ди- и триизоцианаты, причем не существенно, были ли они получены фосгенированием или по способам без использования фосгена. Наряду с этим, также могут использоваться хорошо известные специалисту более высокомолекулярные продукты превращения этих мономерных ди- и/или триизоцианатов, содержащие уретановые, карбамидные, карбодиимидные, ацилкарбамидные, изоциануратные, аллофанатные, биуретовые, оксадиазинтрионовые, уретдионовые, иминооксадиазиндионовые структуры, соответственно или по-отдельности или в любых смесях друг с другом.
Примерами подходящих мономерных ди- или триизоцианатов, которые могут использоваться в качестве компонента a1), являются бутилендиизоцианат, гексаметилендиизоцианат (ГМДИ), изофорондиизоцианат (ИФДИ), триметилгексаметилендиизоцианат (TMDI), 1,8-диизоцианато-4-(изоцианатометил)октан, изоцианатометил-1,8-октандиизоцианат (TIN), 2,4- и/или 2,6-толуолдиизоцианаты.
В качестве соединений a2), реакционноспособных в отношении изоцианатов, для образования форполимеров предпочтительно используются соединения с OH-функциональными группами. Эти соединения аналогичны соединениям с ОН-функциональными группами, таким как те, что описаны далее для компонента b).
Также для получения форполимера возможно использование аминов. Подходящими являются, например, этилендиамин, диэтилентриамин, триэтилентетрамин, пропилендиамин, диаминоциклогексан,
диаминобензол, диаминобисфенил, дифункциональные полиамины, такие как, например, Jeffamine®, полимеры с терминальными аминогруппами со среднечисленными молекулярными массами до 10000 г/моль или их любые смеси друг с другом.
Для получения форполимеров с биуретовыми группами изоцианат в избытке взаимодействует с амином, причем образуется биуретовая группа. В качестве аминов в этом случае для взаимодействия с вышеназванными ди-, три- или полиизоцианатами подходят все олигомерные или полимерные, первичные или вторичные дифункциональные амины приведенного выше типа.
Предпочтительными форполимерами являются уретаны, аллофанаты или биуреты из алифатических соединений с изоцианатными функциональными группами и олигомерных или полимерных соединений, реакционноспособных по отношению к изоцианатам, со среднечисленными молекулярными массами от 200 до 10000 г/моль, особенно предпочтительными являются уретаны, аллофанаты или биуреты из алифатических соединений с изоцианатными функциональными группами и олигомерных или полимерных полиолов или полиаминов со среднечисленными молекулярными массами от 500 до 8500 г/моль и наиболее предпочтительными являются аллофанаты из ГМДИ или TMDI и дифункциональных простых полиэфирполиолов со среднечисленными молекулярными массами от 1000 до 8200 г/моль.
Предпочтительно описанные выше форполимеры имеют остаточное содержание свободного мономерного изоцианата менее чем 1% масс., особенно предпочтительно менее чем 0,5% масс. и в высшей степени предпочтительно менее чем 0,2% масс.
Разумеется, изоцианатный компонент, наряду с описанными форполимерами, может содержать пропорциональное доле участия количество других изоцианатных компонентов. С этой целью рассматривают ароматические, арилалифатические, алифатические и циклоалифатические ди-, три- или полиизоцианаты. Также могут использоваться смеси таких ди-, три- или полиизоцианатов. Примерами подходящих ди-, три- или полиизоцианатов являются бутилендиизоцианат, гексаметилендиизоцианат (ГМДИ), изофорондиизоцианат (ИФДИ), 1,8-диизоцианато-4-(изоцианатометил)октан, 2,2,4- и/или 2,4,4-триметилгексаметилендиизоцианаты (TMDI), изомерные бис(4,4′-изоцианатоциклогексил)метаны и их смеси с любым содержанием изомеров, изоцианатометил-1,8-октандиизоцианат, 1,4-циклогексилендиизоцианат, изомерные циклогександиметилендиизоцианаты, 1,4-фенилендиизоцианат, 2,4- и/или 2,6-толуилендиизоцианаты, 1,5-нафтилендиизоцианат, 2,4′- или 4,4′-дифенилметандиизоцианаты, трифенилметан-4,4′,4″-триизоцианат или их производные с уретановыми, карбамидными, карбодиимидными, ацилкарбамидными, изоциануратными, аллофанатными, биуретовыми, оксадиазинтрионовыми, уретдионовыми, иминооксадиазиндионовыми структурами и их смеси. Предпочтительными являются полиизоцианаты на основе олигомеризованных и/или превращенных в производные диизоцианатов, которые подходящим способом были освобождены от избыточного диизоцианата, в частности, такие производные гексаметилендиизоцианата. Особенно предпочтительными являются олигомерные изоцианураты, уретдионы и иминоокадиазиндионы из ГМДИ, а также их смеси.
При необходимости также возможно, чтобы изоцианатный компонент a) пропорционально доле участия содержал изоцианаты, которые частично подверглись взаимодействию с реакционноспособными в отношении изоцианатов этиленовыми ненасыщенными соединениями. Предпочтительно при этом в качестве реакционноспособных в отношении изоцианатов этиленовых ненасыщенных соединений используются производные α,β-ненасыщенных карбоновых кислот, такие как акрилаты, метакрилаты, малеинаты, фумараты, малеинимиды, акриламиды, а также соединения, содержащие структурные единицы простых виниловых, пропениловых и аллиловых эфиров и дициклопентадиенила, которые содержат по меньшей мере одну группу, реакционноспособную по отношению к изоцианатам. Особенно предпочтительными являются эти акрилаты или метакрилаты по меньшей мере с одной реакционноспособной в отношении изоцианатов группой. В качестве акрилатов или метакрилатов с гидроксильными функциональными группами рассматриваются такие соединения, как например, 2-гидроксиэтил(мет)акрилат, полиэтиленоксидмоно(мет)акрилаты, полипропиленоксидмоно(мет)акрилаты, полиалкиленоксидмоно(мет)акрилаты, поли(ε-капролактон)моно-(мет)акрилаты, такие как, например, Tone® М100 (Dow, США), 2-гидроксипропил(мет)акрилат, 4-гидроксибутил(мет)акрилат, 3-гидрокси-2,2-диметилпропил(мет)акрилат, гидроксифункциональные моно-, ди- или тетра(мет)акрилаты из многоатомных спиртов, таких как триметилолпропан, глицерин, пентаэритрит, дипентаэритрит, этоксилированного, пропоксилированного или алкоксилированного триметилолпропана, глицерина, пентаэритрита, дипентаэритрита или их технические смеси. Кроме того, подходящими являются олигомерные или полимерные, реакционноспособные в отношении изоцианатов соединения, содержащие ненасыщенные акрилатные и/или метакрилатные группы, как самостоятельно, так и в комбинации с вышеназванными мономерными соединениями. Доля изоцианатов, которые частично прореагировали с этиленовыми ненасыщенными соединениями, реакционноспособными в отношении изоцианатов, в изоцианатном компоненте a) составляет от О до 99%, предпочтительно от 0 до 50%, особенно предпочтительно от 0 до 25% и в высшей степени предпочтительно от 0 до 15%.
При необходимости также возможно, чтобы вышеназванный изоцианатный компонент a) полностью представлял собой или содержал пропорционально доле участия изоцианаты, которые полностью или частично подверглись взаимодействию с блокирующими агентами, известными специалисту из технологии нанесения покрытий. В качестве примеров блокирующих агентов следует упомянуть: спирты, лактамы, оксимы, сложные малоновые эфиры, алкилацетоацетаты, триазолы, фенолы, имидазолы, пиразолы, а также амины, такие как, например, бутаноноксим, диизопропиламин, 1,2,4-триазол, диметил-1,2,4-триазол, имидазол, сложный диэтиловый эфир малоновой кислоты, ацетоуксусный эфир, ацетоноксим, 3,5-диметилпиразол, ежапролактам, N-третбутилбензиламин, сложный циклопентанонкарбоксиэтиловый эфир или любые смеси этих блокирующих агентов.
В качестве компонента b) могут использоваться все полифункциональные, реакционноспособные в отношении изоцианатов соединения, которые в среднем содержат по меньшей мере 1,5 групп, реакционноспособных в отношении изоцианатов, в расчете на одну молекулу.
Группами, реакционноспособными в отношении изоцианатов, в рамках данного изобретения являются предпочтительно гидрокси-, амино- или тиогруппы, особенно предпочтительными являются гидроксисоединения.
Подходящими полифункциональными, реакционноспособными по отношению к изоцианатам соединениями являются, например, сложные полиэфир-, простые полиэфир-, поликарбонат-, поли(мет)акрилат- и/или полиуретанполиолы.
В качестве сложных полиэфирполиолов подходят, например, линейные сложные полиэфирдиолы или разветвленные сложные полиэфирполиолы, как те, которые получаются по известному способу из алифатических, циклоалифатических или ароматических ди- или поликарбоновых кислот или соответственно их ангидридов и многоатомных спиртов, у которых OH-функциональность ≥2.
Примерами таких ди- или поликарбоновых кислот или соответственно ангидридов являются янтарная, глутаровая, адипиновая, пимелиновая, пробковая, азелаиновая, себациновая, нонандикарбоновая, декандикарбоновая, терефталевая, изофталевая, o-фталевая, тетрагидрофталевая, гексагидрофталевая или тримеллитовая кислоты, а также ангидриды кислот, такие как o-фталевый, тримеллитовый или янтарный ангидрид или их любые смеси друг с другом.
Примерами подходящих спиртов являются этандиол, ди-, три-, тетраэтиленгликоли, 1,2-пропандиол, ди-, три-, тетрапропиленгликоли, 1,3-пропандиол, бутандиол-1,4, бутандиол-1,3, бутандиол-2,3, пентандиол-1,5, гександиол-1,6, 2,2-диметил-1,3-пропандиол, 1,4-дигидроксициклогексан, 1,4-диметилолциклогексан, октандиол-1,8, декандиол-1,10, додекандиол-1,12, триметилолпропан, глицерин или их любые смеси друг с другом.
Сложные полиэфирполиолы могут также иметь в качестве основы натуральное сырье, такое как касторовое масло. Также возможно, чтобы сложные полиэфирполиолы имели в качестве основы гомо- или сополимеризаты лактонов, такие как те, которые предпочтительно могут быть получены присоединением лактонов или смесей лактонов, таких как бутиролактон, ε-капролактон и/или метил-ε-капролактон, к соединениям с гидроксильными функциональными группами, таким как многоатомные спирты, например, вышеназванного типа, у которых функциональность по OH-группам ≥2.
Такие сложные полиэфирполиолы предпочтительно имеют среднечисленные молекулярные массы от 400 до 4000 г/моль, особенно предпочтительно от 500 до 2000 г/моль. Их OH-функциональность составляет предпочтительно от 1,5 до 3,5, особенно предпочтительно от 1,8 до 3,0.
Подходящие поликарбонатполиолы являются доступными по известному способу путем взаимодействия органических карбонатов или фосгена с диолами или смесями диолов.
Подходящими органическими карбонатами являются диметил-, диэтил- и дифенил карбонат.
Подходящие диолы или соответственно смеси включают многоатомные спирты, имеющие OH-функциональность ≥2, перечисленные в рамках описания сложных полиэфиров, предпочтительно 1,4-бутандиол, 1,6-гександиол и/или 3-метилпентандиол, или в поликарбонатполиолы могут также перерабатываться сложные полиэфирполиолы.
Такие поликарбонатполиолы предпочтительно имеют среднечисленные молекулярные массы от 400 до 4000 г/моль, особенно предпочтительно от 500 до 2000 г/моль. OH-функциональность этих полиолов составляет предпочтительно от 1,8 до 3,2, особенно предпочтительно от 1,9 до 3,0.
Подходящие простые полиэфирполиолы представляют собой полученные при необходимости полимеризацией в блоке продукты полиприсоединения простых циклических эфиров к исходным молекулам с ОН- или NH-функциональными группами.
Подходящими простыми циклическими эфирами являются, например, стиролоксиды, этиленоксид, пропиленоксид, тетрагидрофуран, бутиленоксид, эпихлоргидрин, а также любые их смеси.
В качестве исходных соединений могут применяться названные в рамках описания получения сложных полиэфирполиолов многоатомные спирты, имеющие ОН-функциональность ≥2, а также первичные или вторичные амины и аминоспирты.
Предпочтительными простыми полиэфирполиолами являются такие простые полиэфирполиолы указанного выше вида, основанные исключительно на пропиленоксиде или на статистических или блок-сополимерах на основе пропиленоксида с другими 1-алкиленоксидами, причем доля этих 1-алкиленоксидов составляет не более 80% масс.
Наряду с этим предпочтительными являются поли(триметиленоксид)ы, соответствующие формуле (III), а также смеси полиолов, указанных в качестве предпочтительных. Особенно предпочтительными являются гомополимеры пропиленоксида, а также статистические или блоксополимеры, которые содержат оксиэтиленовые, оксипропиленовые и/или оксибутиленовые структурные единицы, причем доля этих оксипропиленовых структурных единиц по отношению к общему количеству всех оксиэтиленовых, оксипропиленовых и/или оксибутиленовых структурных единиц составляет по меньшей мере 20% масс, предпочтитетльно по меньшей мере 45% масс. При этом оксипропилен и оксибутилен включают все соответствующие линейные и разветвленные изомеры с числом атомов углерода 3 и 4.
Такие простые полиэфирполиолы предпочтительно имеют среднечисленные молекулярные массы от 250 до 10000 г/моль, особенно предпочтительно от 500 до 8500 г/моль и в высшей степени предпочтительно от 600 до 4500 г/моль. Их OH-функциональность составляет предпочтительно от 1,5 до 4,0, особенно предпочтительно от 1,8 до 3,1.
Наряду с этим, в качестве составного элемента компонента b), как полифункциональные, реакционноспособные в отношении изоцианатов соединения, также подходят низкомолекулярные, то есть, с молекулярными массами меньше 500 г/моль, короткоцепные, то есть, содержащие от 2 до 20 атомов углерода, алифатические, арилалифатические или циклоалифатические ди-, три- или полифункциональные спирты.
Это могут быть, например, этиленгликоль, диэтиленгликоль, триэтиленгликоль, тетраэтиленгликоль, дипропиленгликоль, трипропиленгликоль, 1,2-пропандиол, 1,3-пропандиол, 1,4-бутандиол, неопентилгликоль, 2-этил-2-бутилпропандиол, триметилпентандиол, изомеры положения диэтилоктандиола, 1,3-бутиленгликоль, циклогександиол, 1,4-циклогександиметанол, 1,6-гександиол, 1,2- и 1,4-циклогександиолы, гидрированный бисфенол A (2,2-бис-(4-гидроксициклогексил)пропан), сложный 2,2-диметил-3-гидроксипропиловый эфир 2,2-диметил-3-гидроксипропионовой кислоты. Примерами подходящих триолов являются триметилолэтан, триметилолпропан или глицерин. Подходящими спиртами более высокой функциональности являются дитриметилолпропан, пентаэритрит, дипентаэритрит или сорбит.
Используемые фотоинициаторы обычно представляют собой инициаторы, которые могут активироваться под действием актиничного излучения, вызывающие полимеризацию соответствующих полимеризующихся групп. Фотоинициаторы представляют собой известные, коммерчески доступные соединения, причем, среди них выделяют инициаторы мономолекулярные (типа I) и бимолекулярные (типа II). Кроме того, эти инициаторы, в зависимости от химической природы, используются для радикальной, анионной (или), катионной (или смешанной) форм вышеупомянутой полимеризации.
Эти фотоинициаторы могут включать, в частности, анионный, катионный или нейтральный краситель и со-инициатор.
Системами (типа I) для радикальной фотополимеризации являются, к примеру, ароматические кетосоединения, например, бензофеноны в комбинации с третичными аминами, алкилбензофеноны, 4,4′-бис-(диметиламино)бензофенон (кетон Михлера), антрон и галогенированные бензофеноны или смеси указанного вида. Кроме того, подходящими являются инициаторы (типа II), такие как бензоин и его производные, бензилкетали, ацилфосфиноксиды, например, 2,4,6-триметилбензоилдифенилфосфиноксид, бисацилофосфиноксид, сложный эфир фенилглиоксиловой кислоты, камфорхинон, альфа-аминоалкилфенон, альфа.альфа-диалкоксиацетофенон, 1-[4-(фенилтио)фенил]октан-1,2-дион-2-(O-бензоилоксим) и альфа-гидроксиалкилфенон.
Также в качестве фотоинициаторов могут использоваться фотоинициирующие системы, состоящие из смеси арилбората аммония с одним или несколькими красителями, описанные в европейской заявке на патент EP-A 0223587. В качестве арилборатов аммония пригодны, например, трифенилгексиборат тетрабутиламмония, трифенилбутилборат тетрабутиламмония, тринафтилгексилборат тетрабутиламмония, трис-(4-третбутил)фенилбутилборат тетрабутиламмония, трис-(3-фторфенил)гексилборат тетрабутиламмония, трифенилбензилборат тетраметиламмония, вторбутилтрифенилборат тетра(н-гексил)аммония, дипентилдифенилборат 1-метил-3-октилимидазолия и трис-(3-хлор-4-метилфенил)гексилборат тетрабутиламмония. В качестве красителей подходят, например, New-Methylenblau, тионин, основный желтый, пинацианол хлорид, родамин 6Ж, галлоцианин, этилфиолет, Victoria Blue R, Celestine Blue, хинальдиновый красный, кристаллический фиолетовый, бриллиантовый зеленый, Astrazon Orange G, Darrow Red, пиронин Y, Basic Red 29, Pyrillium I, цианин и метиленовый синий, азур A (Cunningham с соавт., RadTech'98 North America UV/EB Conference Proceedings, Chicago, Apr. 19-22, 1998).
Фотоинициаторами, использующимися для анионной полимеризации, являются, как правило, системы (типа I), в первую очередь, ведущие начало от комплексов переходных металлов. Среди них известны соли хрома, как например, 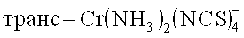
Фотоинициаторы, применяемые для катионной полимеризации, в основном представлены тремя классами: солями арилдиазония, ониевыми солями (в частности, йодониевыми, сульфониевыми и селенониевыми солями), а также, металлорганическими соединениями. Соли фенилдиазония при облучении могут, как в присутствии, так и в отсутствие донора водорода, давать катион, который инициирует полимеризацию. Эффективность совокупной системы определяется природой использованного в диазониевом соединении противоиона. При этом предпочтительными являются мало реакционноспособные, но достаточно дорогостоящие 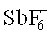
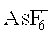
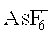
Очень широко распространены и коммерчески доступны в различных формах ониевые соли, особенно сульфониевые и йодониевые соли. Фотохимия этих соединений была подробно исследована. Йодониевые соли после инициирования распадаются в первую очередь гомолитически и, следовательно, дают радикал и анион-радикал, который стабилизируется путем отщепления протона, протон высвобождается, и затем начинается катионная полимеризация (Dektar с соавт. J. Org. Chem. 1990, 55, 639; J. Org. Chem. 1991, 56, 1838). Этот механизм делает возможным использование йодониевых солей также и для радикальной фотополимеризации. При этом снова большое значение приобретает выбор противоиона, предпочитают также 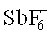
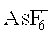
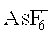
В случае сульфониевых солей речь идет о соединениях, которые распадаются по Норришу (II) (Crivello с соавт. Macromolecules, 2000, 33, 825). В случае с сульфониевыми солями выбор противоиона также имеет критическое значение, которое выражается преимущественно в скорости отверждения полимера. Наилучшие результаты, как правило, достигаются с солями 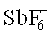
Поскольку самопоглощение йодониевых и сульфониевых солей лежит в области <300 нм, то эти соединения соответственно должны сенсибилизироваться к фотополимеризации излучением в ближней УФ-области или коротковолновой видимой области. Это удается при использовании ароматических соединений с высоким поглощением, таких как, например, антрацена и его производных (Gu с соавт., Am. Chem. Soc. Polymer Preprints, 2000, 41 (2), 1266) или фенотиазина или его производных (Hua с соавт., Macromolecules, 2001, 34, 2488-2494).
Также может быть предпочтительным использовать смеси этих соединений. В зависимости от применяемого для отверждения источника излучения тип и концентрация фотоинициатора должны подбираться известным специалисту способом. Подробности описываются, например, в издании Р.К.Т. Oldring (Ed.), Chemistry & Technology of UV & EB Formulations For Coatings, Inks & Paints, Vol.3, 1991, SITA Technology, London, стр.61-328.
Предпочтительными фотоинициаторами являются смеси из тетрагексилбората тетрабутиламмония, трифенилгексилбората тетрабутиламмония, трис-(3-фторфенил)гексилбората тетрабутиламмония ([191726-69-9], CGI 7460, продукт фирмы Ciba Inc. Базель) и трис-(3-хлор-4-метилфенил)гексилбората тетрабутиламмония ([1147315-11-4], CGI 909, продукт фирмы Ciba Inc, Базель) с красителями, такими как, например, Astrazon Orange G, метиленовый синий, New Methylenblau, азур A, Pyrillium I, сафранин O, цианин, галлоцианин, бриллиантовый зеленый, кристаллический фиолетовый, этилфиолет и тионин.
Согласно другому предпочтительному варианту исполнения предусматривается, что фотополимерная композиция дополнительно содержит в качестве пластификаторов уретаны, причем эти уретаны, в частности, могут быть замещены по меньшей мере одним атомом фтора.
Предпочтительно эти уретаны могут иметь общую формулу (III)
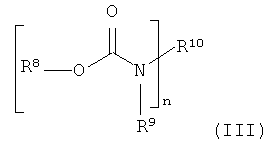 ,
,
в которой n≥1 и n≤8, a R8, R9, R10 независимо друг от друга являются атомами водорода, линейными, разветвленными, циклическими или гетероциклическими незамещенными или при необходимости также замещенными гетероатомами органическими остатками, причем предпочтительно по меньшей мере один из остатков R8, R9, R10 является замещенным по меньшей мере одним атомом фтора, и особенно предпочтительно R4 является органическим остатком по меньшей мере с одним атомом фтора. Особенно предпочтительно R10 представляет собой линейный, разветвленный, циклический или гетероциклический незамещенный или также при необходимости замещенный гетероатомами, такими как, например, фтор, органический остаток.
В случае другого предпочтительного варианта исполнения предусматривается, что записывающие мономеры дополнительно включают другой моно- или мультифункциональный записывающий мономер, причем речь может идти особенно о моно- или полифункциональном акрилате.
Этот акрилат может, в частности, иметь общую формулу (IV)
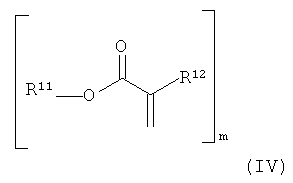 ,
,
в которой m≥1 и m≤4, a R11, R12 независимо друг от друга являются атомами водорода, линейными, разветвленными, циклическими или гетероциклическими незамещенными или при необходимости также замещенными гетероатомами органическими остатками. Особенно предпочтительно R12 представляет собой атом водорода или метил, и/или R11 является линейным, разветвленным, циклическим или гетероциклическим незамещенным или также при необходимости замещенным гетероатомами органическим остатком.
Также возможно, чтобы добавлялись другие ненасыщенные соединения, такие как производные α,β-ненасыщенных карбоновых кислот, такие как акрилаты, метакрилаты, малеинаты, фумараты, малеинимиды, акриламиды, а также соединения, содержащие структурные единицы простых виниловых, пропениловых и аллиловых эфиров и дициклопентадиенила, а также олефиновые ненасыщенные соединения, такие как, например, стирол, α-метил стирол, винилтолуол, олефины, такие как, например, 1-октен и/или 1-децен, сложные виниловые эфиры, (мет)акрилонитрил, (мет)акриламид, метакриловые кислоты, акриловые кислоты. Предпочтительными являются акрилаты и метакрилаты.
Акрилатами или метакрилатами в общем обозначаются сложные эфиры акриловой или соответственно метакриловой кислот. Примерами пригодных к использованию акрилатов и метакрилатов являются метилакрилат, метилметакрилат, этилакрилат, этилметакрилат, этоксиэтилакрилат, этоксиэтилметакрилат, н-бутилакрилат, н-бутилметакрилат, третбутилакрилат, третбутилметакрилат, гексилакрилат, гексилметакрилат, 2-этилгексилакрилат, 2-этилгексилметакрилат, бутоксиэтилакрилат, бутоксиэтилметакрилат, лаурилакрилат, лаурилметакрилат, изоборнилакрилат, изоборнилметакрилат, фенилакрилат, фенилметакрилат, п-хлорфенилакрилат, п-хлорфенилметакрилат, п-бромфенилакрилат, п-бромфенилметакрилат, 2,4,6-трихлорфенилакрилат, 2,4,6-трихлорфенилметакрилат, 2,4,6-трибромфенилакрилат, 2,4,6-трибромфенилметакрилат, пентахлорфенилакрилат, пентахлорфенилметакрилат, пентабромфенилакрилат, пентабромфенилметакрилат, пентабромбензилакрилат, пентабромбензилметакрилат, феноксиэтилакрилат, феноксизтилметакрилат, феноксиэтоксиэтилакрилат, феноксиэтоксиэтилметакрилат, фенилтиоэтилакрилат, фенилтиоэтилметакрилат, 2-нафтилакрилат, 2-нафтилметакрилат, 1,4-бис(2-тионафтил)-2-бутилакрилат, 1,4-бис(2-тионафтил)-2-бутилметакрилат, пропан-2,2-диилбис[(2,6-дибром-4,1-фенилен)окси-(2-{[3,3,3-трис(4-хлорфенил)пропаноил]окси}пропан-3,1-диил)оксиэтан-2,1-диил]диакрилат, бисфенола A диакрилат, бисфенола A диметакрилат, тетрабромобисфенола A диакрилат, тетрабромобисфенола A диметакрилат, а также их этоксилированные аналоги, N-карбазоилакрилаты, приведенные только для того, чтобы перечислить выбор пригодных для использования акрилатов и метакрилатов.
Разумеется, могут также применяться дополнительные уретанакрилаты. Под уретанакрилатами понимают соединения, которые имеют по меньшей мере одну сложноэфирную акрилатную группу и дополнительно содержат по меньшей мере одну уретановую связь. Известно, что такие соединения могут получаться взаимодействием гидрокси-функционализированных сложных эфиров акриловой кислоты с соединениями, содержащими изоцианатные функциональные группы.
Примерами применяемых для этого соединений с изоцианатными функциональными группами являются ароматические, арилалифатические, алифатические и циклоалифатические ди-, три- или полиизоцианаты. Можно также использовать смеси таких ди-, три- или полиизоцианатов. Примерами подходящих ди-, три- или полиизоцианатов являются бутилендиизоцианат, гексаметилендиизоцианат (ГМДИ), изофорондиизоцианат (ИФДИ), 1,8-диизоцианато-4-(изоцианатометил)октан, 2,2,4- и/или 2,4,4-триметилгексаметилендиизоцианаты, изомерные бис-(4,4′-изоцианатоциклогексил)метаны и их смеси с любым содержанием изомеров, изоцианатометил-1,8-октандиизоцианат, 1,4-циклогексилендиизоцианат, изомерные циклогександиметилендиизоцианаты, 1,4-фенилендиизоцианат, 2,4- и/или 2,6-толуилендиизоцианаты, 1,5-нафтилендиизоцианат, 2,4′- или 4,4′-дифенилметандиизоцианаты, 1,5-нафтилендиизоцианат, м-метилтиофенилизоцианат, трифенилметан-4,4′,4″-триизоцианат и трис(п-изоцианатофенил)тиофосфат или их производные с уретановыми, карбамидными, карбодиимидными, ацилкарбамидными, изоциануратными, аллофанатными, биуретовыми, оксадиазинтрионовыми, уретдионовыми, иминооксадиазиндионовыми структурами и их смеси. При этом предпочтительными являются ароматические или арилалифатические ди-, три- или полиизоцианаты.
В качестве акрилатов или метакрилатов с гидроксильными функциональными группами для получения уретанакрилатов рассматриваются такие соединения, как например, 2-гидроксиэтил(мет)акрилат, полиэтиленоксидмоно(мет)акрилаты, полипропиленоксидмоно(мет)акрилаты, полиалкиленоксидмоно(мет)акрилаты, поли(ε-капролактон)моно(мет)акрилаты, как, например, Tone® М100 (Dow, Швальбах, Германия), 2-гидроксипропил(мет)акрилат, 4-гидроксибутил(мет)акрилат, 3-гидрокси-2,2-диметилпропил(мет)акрилат, гидроксипропил(мет)акрилат, сложный 2-гидрокси-3-феноксипропиловый эфир акриловой кислоты, гидроксифункциональные моно-, ди- или тетраакрилаты из многоатомных спиртов, таких как триметилолпропан, глицерин, пентаэритрит, дипентаэритрит, этоксилированного, пропоксилированного или алкоксилированного триметилолпропана, глицерина, пентаэритрита, дипентаэритрита или их технические смеси. Предпочтительными являются 2-гидроксиэтилакрилат, гидроксипропилакрилат, 4-гидроксибутилакрилат и поли(ε-капролактон)моно(мет)акрилаты. Кроме того, в качестве олигомеров или полимеров, реакционноспособных в отношении изоцианатов, подходят соединения, содержащие ненасыщенные акрилатные и/или метакрилатные группы, как самостоятельно, так и в комбинации с вышеназванными мономерными соединениями. Также могут применяться известные, содержащие гидроксильные группы эпокси(мет)акрилаты с содержанием ОН-групп от 20 до 300 мг КОН/г, или содержащие гидроксильные группы полиуретан(мет)акрилаты с содержанием ОН-групп от 20 до 300 мг КОН/г, или акрилированные полиакрилаты с содержанием ОН-групп от 20 до 300 мг КОН/г, а также их смеси друг с другом и смеси с содержащими гидроксильные группы ненасыщенными сложными полиэфирами, а также смеси со сложными полиэфир(мет)акрилатами или смеси содержащих гидроксильные группы ненасыщенных сложных полиэфиров со сложными полиэфир(мет)акрилатами.
Предпочтительными являются, прежде всего, уретанакрилаты, которые могут получаться из взаимодействия трис(п-изоцианатофенил)тиофосфата и м-метилтиофенилизоцианата с акрилатами со спиртовыми функциональными группами, такими как гидроксиэтил(мет)акрилат, гидроксипропил(мет)акрилат и гидроксибутил(мет)акрилат.
Другим предметом изобретения является применение фотополимерной композиции согласно изобретению для изготовления голографических сред, которые в результате соответствующего процесса освещения могут быть переработаны с получением голограмм для оптического применения во всей видимой и ближней УФ-областях (300-800 нм). Визуальные голограммы включают все голограммы, которые могут быть записаны известными специалисту способами. К ним, среди прочих, относятся осевые голограммы (голограммы Габора), внеосевые голограммы, голограммы сфокусированного изображения, голограммы, восстанавливаемые в белом свете («радужные голограммы»), голограммы Денисюка, внеосевые отражательные голограммы, голограммы краевого освещения, а также голографические стереограммы. Предпочтительными являются отражательные голограммы, голограммы Денисюка, голограммы в проходящем свете.
Возможные оптические функции голограмм, которые могут быть получены из фотополимерных композиций согласно изобретению, соответствуют оптическим функциям фотоэлементов, таких как линзы, зеркала, отклоняющие зеркала, фильтры, рассеиватели, дифракционные элементы, световоды, устройства, изменяющие направление светового пучка (волноводы), проекционные стекла и/или пластинки фотомасок. Часто эти оптические элементы проявляют частотную избирательность в зависимости от того, как облучали голограмму, и сколько измерений она имеет.
Наряду с этим, с помощью фотополимерных композиций согласно изобретению также могут быть изготовлены голографические картинки или изображения, как например, для персональных портретов, биометрических изображений в защищаемых документах, или вообще для изображений или объектов с изображениями для рекламы, маркировок подлинности, защиты товарных знаков, товарных маркировок, этикеток, элементов дизайна, декорирования, иллюстраций, карточек для коллекционеров, картинок и тому подобного, а также изображений, которые могут представлять цифровые данные, среди прочего, также в комбинации с представленными ранее продуктами. Голографические изображения могут содержать отпечаток трехмерной картинки, но они также могут представлять покадровые изображения, короткие фильмы или ряд различных объектов, в зависимости от того, под каким углом, каким источником света (также подвижным) и т.д. они облучаются. Благодаря этим многочисленным возможностям оформления, голограммы, особенно объемные голограммы, представляют собой привлекательное техническое решение для вышеназванных областей использования.
Фотополимерные композиции, прежде всего, могут применяться как голографическая среда в форме пленки. При этом в качестве носителя с одной или с обеих сторон покрывается слой материала, проницаемого для света в видимой области спектра (пропускание более чем 85% в области длин волн от 400 до 780 нм) или композитного материала, а также при необходимости на один или на все слои фотополимера накладывается покрывающий слой.
Предпочтительные материалы или композитные материалы носителя содержат в качестве основы поликарбонат (ПК), полиэтилентерефталат (ПЭТ), полибутилентерефталат, полиэтилен, полипропилен, ацетат целлюлозы, гидрат целлюлозы, нитрат целлюлозы, полимеры циклоолефинов, полистирол, полиэпоксид, полисульфон, триацетат целлюлозы (СТА), полиамид, полиметилметакрилат, поливинилхлорид, поливинилбутираль или полидициклопентадиен или их смеси. Особенно предпочтительно в качестве основы они содержат ПК, ПЭТ и СТА. Композитные материалы могут представлять собой ламинированные пленки или соэкструдаты. Предпочтительными композитными материалами являются двойные или тройные пленки, образованные по одной из следующих схем: A/B, A/B/A или A/B/C. Особенно предпочтительными являются ПК/ПЭТ, ПЭТ/ПК/ПЭТ и ПК/ТПУ (ТПУ-термопластичный полиуретан).
В качестве альтернативы вышеназванным синтетическим носителям могут также применяться плоские стеклянные пластинки, которые находят применение, в частности, при широкопольном экспонировании точного изображения, например, для голографических литографий (Ng, Willie W.; Hong, Chi-Shain; Yariv, Amnon. Holographic interference lithography for integrated optics. IEEE Transactions on Electron Devices (1978), ED-25(10), 1193-1200. ISSN: 0018-9383).
Эти материалы или композитные материалы носителя могут быть с одной или с двух сторон подвергнуты антисклеивающей, антистатической, гидрофобной или гидрофильной обработке. Перечисленные модификации стороны носителя, направленной к фотополимерному слою, служат для той цели, чтобы фотополимерный слой мог отделяться от носителя без повреждений. Модификация стороны носителя, направленной в противоположную от фотополимерного слоя сторону, служит для того, чтобы среды, согласно данному изобретению, удовлетворяли специальным механическим требованиям, которые предъявляются, например, при обработке в рулонных ламинаторах, в частности, при способе печати с рулона на рулон.
Другим предметом изобретения является применение соединения формулы (I) в качестве записывающего мономера в фотополимерной композиции.
Примеры
Изобретение далее поясняется более подробно на основании примеров. При этом в случае, если не отмечается иное, все процентные величины понимают как массовые проценты.
Методы:
Показатели содержания твердого вещества определяли путем того, что, руководствуясь инструкцией по эксплуатации инфракрасного влагомера, на специальную одноразовую алюминиевую кювету помещали примерно 1 г вещества и нагревали при 140°C до тех пор, пока в течение 30 секунд не сохранялась постоянная масса, или на специальную одноразовую алюминиевую кювету (подходящую для системы с максимальным содержанием растворителя 10% масс.) помещают примерно 1 г вещества и нагревают в сушильном шкафу при 125°C в течение 60 минут. При этом вещество, которое следует проанализировать, с помощью изогнутой подходящим образом канцелярской скрепки распределяют таким образом, что обеспечивается равномерное высушивание пленки. Эта канцелярская скрепка для измерения остается в образце и должна учитываться уже при взвешивании.
Приведенные величины содержания NCO-групп (содержание изоцианатов) определялись в соответствии со стандартом DIN EN ISO 11909.
Определение содержания 2-гидроксиэтилакрилата (ГЭА) проводится по образцу стандарта DIN/ISO 10283 (2007). 1,41 г антрацена (калибровочного вещества) в качестве внутреннего вещества-стандарта отвешивают в мерную колбу объемом 1 л и доливают этилацетатом. Примерно 1 г образца отвешивают и смешивают с 10 мл раствора внутреннего стандарта, приготовленного, как описано выше, и 10 мл этилацетата, из этого 2,0 мкл разделяют с помощью газовой хроматографии и рассчитывают содержание ГЭА в % масс. с корректировкой по площади поверхности.
Плотность двойных связей DD рассчитывают путем того, что делят функциональность молекулы на молекулярную массу и умножают на 1000 и указывают в единицах гэкв/кг.
Измерение показателя преломления осуществлялось в зависимости от состояния соединения из примера в соответствии с одним из двух следующих методов:
Измерения показателя преломления n при длине волны 405 нм (Метод A): Зависимости показателя преломления n от длины волны для образца определяли из спектров пропускания и отражения. Для этого на носителе из кварцевого стекла осаждали из разбавленного раствора в бутилацетате пленки образца толщиной примерно 100-300 нм. Спектры пропускания и отражения этой стопки пластов регистрировались на спектрометре фирмы STEAG ETA-Optik, система анализа оптических носителей CD, тесты ЕТА-RT, и сообразно с этим определяли толщину слоя и спектральные изменения n по регистрируемым спектрам пропускания и отражения. Это осуществлялось с помощью встроенного программного обеспечения спектрометра и дополнительно требовало информации о показателе преломления n материала из кварцевого стекла, который определяли предварительно в холостом опыте.
Измерение показателя преломления 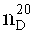
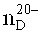
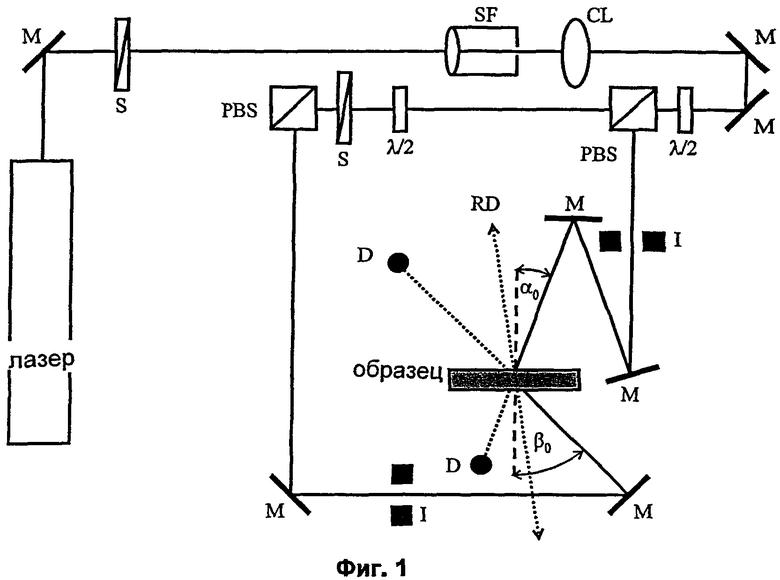
Значения дифракционной эффективности сред (DE) были измерены с помощью голографической испытательной установки, как представлено на Фигуре 1.
Луч гелий-неонового лазера (длина волны излучения 633 нм) был преобразован в параллельный гомогенный луч при помощи объемного фильтра (SF) совместно с коллимационной линзой (CL). Конечное сечение сигнального луча и луча сравнения устанавливается при помощи ирисовых диафрагм (I). Диаметр отверстия в ирисовой диафрагме составляет 0,4 см. Поляризационно-зависимые разделители луча (PBS) делят лазерный луч на два когерентных, одинаково поляризованных луча. На пластинках в половину длины волны λ/2 устанавливается мощность луча сравнения на 0,5 мВт, а мощность предметного луча на 0,65 мВт. Мощности определялись полупроводниковыми детекторами (D) около установленного образца. Угол падения луча сравнения (α0) составляет - 21,8°, угол падения предметного луча (β0) составляет 41,8°. Углы измеряются, начиная от перпендикуляра к образцу, до направления луча. Таким образом, в соответствии с Фигурой 1 α0 имеет отрицательный знак, а β0 положительный знак. В точке образца (среды) интерференционное поле двух накладывающихся лучей создавало решетку из более светлых и более темных полос, которые расположены перпендикулярно биссектрисам углов двух падающих на образец лучей (отражательная голограмма). Расстояние между серединами полос Λ, также называемое периодом решетки, в среде составляет ~225 нм (показатель преломления среды принимается за величину ~1,504).
Фигура 1 демонстрирует геометрию прибора для испытания голографических сред (англ. Holographic Media Tester - НМТ) при λ=633 нм (гелий-неоновый лазер (He-Ne Laser): М=зеркало, S=затвор, SF=объемный фильтр, CL=коллимационная линза, λ/2=пластинка в половину длины волны λ/2, PBS=поляризационно-зависимый разделитель луча, D=детектор, I=ирисовая диафрагма, α0=-21,8°, β0=41,8° представляют собой углы падения когерентных лучей, измеренные за пределами образца (среды). RD=направление поворотного столика при восстановлении лучом сравнения.
Голограммы в среде были записаны следующим образом:
- Оба затвора (S) открыты в течение времени облучения t.
- Затем при закрытых затворах (S) среду оставляли в течение 5 минут для диффузии еще не заполимеризовавшегося записывающего мономера.
Записанные голограммы затем считывались следующим образом. Затвор предметного луча оставался закрытым. Затвор луча сравнения был открыт. Ирисовая диафрагма луча сравнения была закрыта до величины диаметра отверстия <1 мм. Тем самым достигали того, что для всех углов поворота среды (Ω), луч всегда полностью попадал на ранее записанную голограмму. Затем управляемый компьютером поворотный столик поворачивали в угловом диапазоне от Ωmin до Ωmax с величиной шага угла равной 0,05°. Ω измеряется от перпендикуляра к образцу до направления поворотного столика при восстановлении лучом сравнения. Тогда направление поворотного столика при восстановлении лучом сравнения получается, если при записи голограммы углы падения луча сравнения и предметного луча являются равными по абсолютной величине, значит, имеет место α0=-31,8° и β0=31,8°. Тогда имеет место равенство Ωrecording=0°. Для α0=-21,8° и β0=41,8°, таким образом, Ωrecording составляет 10°. В общем, для интерференционного поля при записи (англ. обозн. «recording») голограммы справедливо следующее:
α0=θ0+Ωrecording.
θ0 представляет собой половинный угол в лабораторной системе за пределами среды, и при записи голограммы справедливо следующее:
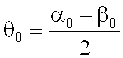
Следовательно, в этом случае имеет место θ0=-31,8°. При каждом достигнутом значении угла поворота Ω были измерены мощности проходящего луча при нулевом порядке дифракции при помощи соответствующего детектора D, а также мощности дифрагированного луча для дифракции первого порядка при помощи детектора D. Эффективность дифракции для каждого достигнутого угла Ω получалась как следующее соотношение:
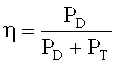
Где PD - это мощность дифрагированного луча, измеренная в детекторе, а PT - это мощность проходящего луча, измеренная в детекторе.
По вышеописанному способу для записанных голограмм были измерены и зафиксированы в компьютере кривые Брэгга, которые описывают дифракционную эффективность n в зависимости от угла поворота Ω. Дополнительно также измерили и занесли в компьютер интенсивности проходящих лучей для дифракции нулевого порядка в зависимости от угла поворота Ω.
Максимальная дифракционная эффективность голограммы (DE=ηmax), также являющаяся ее пиковой величиной, была определена при Ωreconstruction. При необходимости для этого положение детектора дифрагированного луча должны были изменять с тем, чтобы определить эту максимальную величину.
Амплитуда изменения показателя преломления Δn и толщина фотополимерного слоя d теперь были определены на основе теории двухволнового взаимодействия (смотрите Н.Kogelnik, The Bell System Technical Journal, Volume 48, November 1969, Number 9, стр.2909-стр.2947) по измеренным кривым Брэгга и угловому изменению интенсивности проходящего потока. При этом следует обращать внимание, что из-за возникающей в результате фотополимеризации усадки толщины расстояние между серединами полос Λ′ голограммы и ориентация этих полос (уклон) могут не совпадать с расстоянием между серединами полос Λ интерференционной картины и ее ориентации. Следовательно, угол 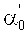
Все геометрические величины, которые относятся к описанной голограмме, а не к интерференционной картине, представляются в виде величин со штрихом.
Для кривой Брэгга η(Ω) отражательной голограммы согласно теории Когельника считается, что:
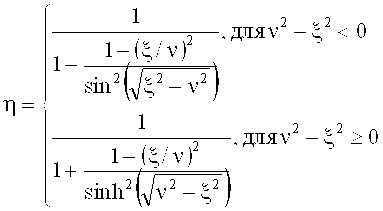
где
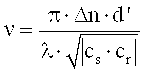
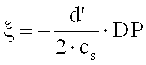
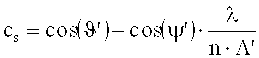
cr=cos(ϑ')
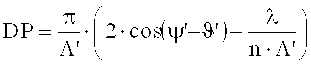
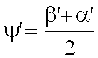
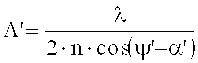
При считывании голограммы («восстановлении» - англ. «reconstruction») справедливо, как аналогично представлено выше:
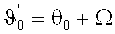
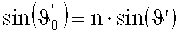
При условии Брэгга «дефазирование» DP=0. И соответственно из этого следует:
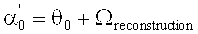
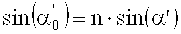
Еще неизвестный угол β′ может определяться из сравнения условия Брэгга для интерференционного поля при записи голограммы и условия Брэгга при считывании этой голограммы при допущении, что имеет место только усадка толщины. В таком случае следует, что:
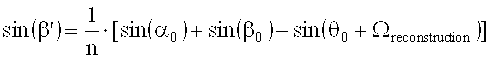
ν представляет собой разрешающую способность решетки, ξ - параметр рассогласования, а ψ′ - ориентация (уклон) решетки с различными показателями преломления, которая была записана, α′ и β′ соответствуют углам α0 и β0 интерференционного поля при записи голограммы, но измерены в среде и являются действительными для решетки голограммы (после усадки толщины), n - средний показатель преломления фотополимера и был принят за 1,504. λ - длина волны лазерного излучения в вакууме.
Тогда максимальная дифракционная эффективность (DE=ηmax) для ξ=0 получается равной:
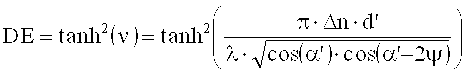
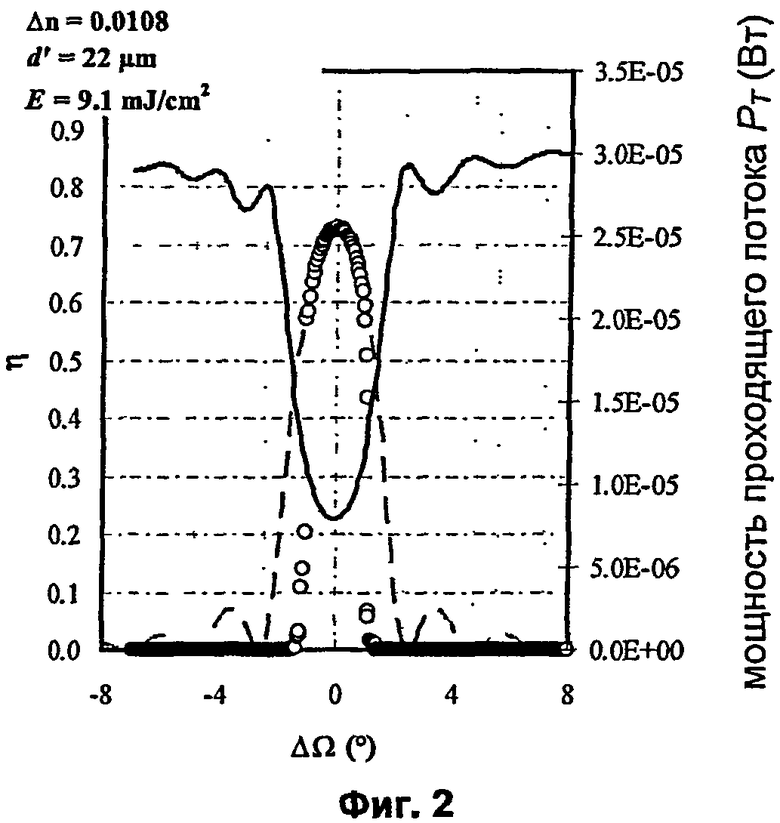
Фигура 2 показывает измеренную мощность проходящего луча PT (по правой оси y), нанесенную в виде сплошной линии, в зависимости от углового рассогласования ΔΩ, измеренную дифракционную эффективность η (по левой оси y), нанесенную в виде закрашенных кружочков, в зависимости от углового рассогласования ΔΩ (насколько это позволила конечная величина детектора) и согласование с теорией Когельника в виде пунктирной линии (по левой оси y).
Результаты измерений дифракционной эффективности, теоретическая кривая Брэгга и кривая мощности проходящего потока наносятся, как показано на Фигуре 2, как зависимости от центрированного угла поворота 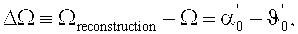
Поскольку DE является известной величиной, то форма теоретической кривой Брэгга согласно Когельнику определяется еще только толщиной фотополимерного слоя d′. Через величину DE для данной толщины d′ таким образом корректируют Δn, чтобы измеренное и теоретическое значение для DE всегда совпадали. Величину d′ подбирают до тех пор, пока угловое положение первого вторичного минимума теоретической кривой Брэгга не совпадет с угловым положением первого вторичного максимума кривой интенсивности проходящего потока и, кроме того, значения полной ширины на полувысоте (англ. FWHM-Full-width at half-maximum) для теоретической кривой Брэгга и кривой интенсивности проходящего потока не совпадут.
Поскольку положение отражательной голограммы изменяется синхронно при восстановлении путем Ω-сканирования, а детектор для дифрагированного света может охватывать только ограниченный угловой диапазон, то кривая Брэгга для плоских голограмм (малые значения d′) при одном Ω-сканировании захватывает ее не полностью, а только центральную область при подходящем расположении детектора. Поэтому для подбора толщины слоя d′ дополнительно к кривой Брэгга привлекают форму кривой интенсивности проходящего потока.
Фигура 2 показывает изображение кривой Брэгга η согласно теории двухволнового взаимодействия (пунктирная линия), измеренную величину дифракционной эффективности (закрашенные кружочки) и кривую мощности проходящего потока (черная непрерывная линия) в зависимости от углового рассогласования ΔΩ.
Для получения результата эта процедура была повторена по возможности несколько раз для различных значений времени облучения t в различных средах, чтобы установить при каких средних величинах энергии падающего лазерного излучения при записи голограммы DE достигает значения насыщения. Средняя величина энергии E получается из величин мощности двух относящихся к углам α0 и β0 частичным лучам (луч сравнения Рг=0,50 мВт и предметный луч Ps=0,63 мВт), времени облучения t и величины диаметра отверстия в ирисовой диафрагме (0,4 см) следующим образом:
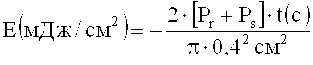
Мощности частичных лучей подбирали таким образом, чтобы в среде при применявшихся углах α0 и β0 достигалась равная плотность мощности.
Вещества:
Использованные спирты и хлорангидриды карбоновых кислот, а также растворители и реагенты приобретались в химической промышленности.
Пример 1: бис[2-(акрилоилокси)этил]изофталат
В круглодонную колбу объемом 500 мл при 0°C помещали 64,1 г гидроксиэтилакрилата в 100 мл смеси пиридин/толуол (1:1, об.:об.) с 0,1 г 2,6-дитретбутил-4-метилфенола и медленно прикапывали 56,1 г дихлорангидрида изофталевой кислоты. Дополнительно перемешивали при комнатной температуре, пока содержание гидроксиэтилакрилата не опускалось ниже 0,1%. После этого смесь выливали в 0,5 л воды со льдом и доводили до кислой среды с помощью 1 N водного раствора соляной кислоты. Водную фазу трижды экстрагировали порциями по 0,5 л простого метилтретбутилового эфира. Органическую фазу промывали 10%-ным раствором гидрокарбоната натрия, сушили над сульфатом натрия и фильтровали. Снова добавляли 0,1 г 2,6-дитретбутил-4-метилфенола и отгоняли органический растворитель. Получали продукт в виде бесцветного масла.
Пример 2: бис[2-(акрилоилокси)этил]терефталат
В круглодонную колбу объемом 500 мл при 0°C помещали 64,1 г гидроксиэтилакрилата в 100 мл смеси пиридин/толуол (1:1, об.: об.) с 0,1 г 2,6-дитретбутил-4-метилфенола и медленно прикапывали 56,1 г дихлорангидрида терефталевой кислоты. Дополнительно перемешивали при комнатной температуре, пока содержание гидроксиэтилакрилата не опускалось ниже 0,1%. После этого смесь выливали в 0,5 л воды со льдом и доводили до кислой среды с помощью 1 N водного раствора соляной кислоты. Водную фазу трижды экстрагировали порциями по 0,5 л простого метилтретбутилового эфира. Органическую фазу промывали 10%-ным раствором гидрокарбоната натрия, сушили над сульфатом натрия и фильтровали. Снова добавляли 0,1 г 2,6-дитретбутил-4-метилфенола и отгоняли органический растворитель. Получали продукт в виде бесцветного твердого вещества.
Пример 3: трис[2-(акрилоилокси)этил]бензол-1.3.5-трикарбоксилат
В круглодонную колбу объемом 250 мл при 0°C помещали 27,6 г гидроксиэтилакрилата в 50 мл смеси пиридин/толуол (1:1, об.: об.) с 0,05 г 2,6-дитретбутил-4-метилфенола и медленно прикапывали 21,1 г трихлорангидрида бензолтрикарбоновой кислоты. Дополнительно перемешивали при комнатной температуре, пока содержание гидроксиэтилакрилата не опускалось ниже 0,1%. После этого смесь выливали в 0,25 л воды со льдом и доводили до кислой среды с помощью 1 N водного раствора соляной кислоты. Водную фазу трижды экстрагировали порциями по 0,25 л простого метилтретбутилового эфира. Органическую фазу промывали 10%-ным раствором гидрокарбоната натрия, сушили над сульфатом натрия и фильтровали. Снова добавляли 0,05 г 2,6-дитретбутил-4-метилфенола и отгоняли органический растворитель. Получали продукт в виде бесцветного масла.
Пример 4: 2-(акрилоилокси)этилбензоат
В круглодонную колбу объемом 500 мл при 0°C помещали 51,1 г гидроксиэтилакрилата в 100 мл смеси пиридин/толуол (1:1, об.: об.) с 0,05 г 2,6-дитретбутил-4-метилфенола и медленно прикапывали 65,0 г бензоилхлорида. Дополнительно перемешивали при комнатной температуре, пока содержание гидроксиэтилакрилата не опускалось ниже 0,1%. После этого смесь выливали в 0,5 л воды со льдом и доводили до кислой среды с помощью 1 N водного раствора соляной кислоты. Водную фазу трижды экстрагировали порциями по 0,5 л простого метилтретбутилового эфира. Органическую фазу промывали 10%-нь раствором гидрокарбоната натрия, сушили над сульфатом натрия фильтровали. Снова добавляли 0,05 г 2,6-дитретбутил-4-метилфенола отгоняли органический растворитель. Получали продукт в виде бесцветного масла.
Пример для сравнения 1:2-[(фенилкарбамоил)окси]этилпроп-2-еноат
В круглодонную колбу объемом 500 мл помещали 0,25 г 2,6-дитретбутил-4-метилфенола, 0,12 г Desmorapid Z, 126,4 г фенилизоцианата и нагревал до 60°C. Затем прикапывали 123,3 г 2-гидроксиэтилакрилата и смесь дополнительно выдерживали при 60°С, пока содержание изоцианата и опускалось ниже 0,1%. Затем охлаждали. Продукт получался в вид кристаллического твердого вещества (получение описано в немецком патенте DE 2329142).
Таблица 1: Сводная таблица для Примеров 1-4 и Примера для сравнения 1
Для испытаний оптических характеристик были получены среды и измерены их оптические показатели, как описано далее:
Получение полиолового компонента:
В колбу объемом 1 л помещали 0,18 г октоата олова, 374,8 г ε-капролактона и 374,8 г дифункционального простого политетрагидрофуранполиэфирполиола (эквивалентная масса 500 г/моль OH) и нагревали до 120°C, а затем выдерживали при этой температуре до тех пор, пока содержание твердого вещества (доля нелетучих компонентов) не достигало 99,5% или выше. Затем охлаждали и получали продукт в виде воскоподобного твердого вещества.
Изготовление сред
Среда 1:
При температуре 60°C 5,927 г полиолового компонента, полученного как описано выше, смешивали с 2,50 г бис[2-(акрилоилокси)этил]изофталата (Пример 1), 0,10 г CGI 909 и 0,010 г Neu Methylenblau, а также 0,35 г N-этилпирролидона таким образом, что получался прозрачный раствор. Затем его охлаждали до 30°C, добавляли 1,098 г Desmodur® N 3900 и снова перемешивали. В заключение добавляли 0,006 г Fomrez UL 28 и вновь перемешивали непродолжительное время. Полученную жидкую массу затем помещали на стеклянную пластинку и там накрывали второй стеклянной пластинкой, которая удерживалась фиксатором на расстоянии 20 мкм. Этот образец для испытаний оставляли лежать в течение 12 часов при комнатной температуре и отверждали.
Среда 2:
При температуре 60°C 5,927 г полиолового компонента, полученного как описано выше, смешивали с 2,50 г трис[2-(акрилоилокси)этил]бензол-1,3,5-трикарбоксилата (Пример 3), 0,10 г CGI 909 и 0,010 г Neu Methylenblau, а также 0,35 г N-этилпирролидона таким образом, что получался прозрачный раствор. Затем его охлаждали до 30°C, добавляли 1,098 г Desmodur® N 3900 и снова перемешивали. В заключение добавляли 0,006 г Fomrez UL 28 и вновь перемешивали непродолжительное время. Полученную жидкую массу затем помещали на стеклянную пластинку и там накрывали второй стеклянной пластинкой, которая удерживалась фиксатором на расстоянии 20 мкм. Этот образец для испытаний оставляли лежать в течение 12 часов при комнатной температуре и отверждали.
Среда 3:
При температуре 60°C 5,927 г полиолового компонента, полученного как описано выше, смешивали с 1,25 г бис[2-(акрилоилокси)этил]изофталата (Пример 1), 1,25 г 2-(акрилоилокси)этилбензоата (Пример 4), 0,10 г CGI 909 и 0,010 г Neu Methylenblau, а также 0,35 г N-этилпирролидона таким образом, что получался прозрачный раствор. Затем его охлаждали до 30°C, добавляли 1,098 г Desmodur® N 3900 и снова перемешивали. В заключение добавляли 0,006 г Fomrez UL 28 и вновь перемешивали непродолжительное время. Полученную жидкую массу затем помещали на стеклянную пластинку и там накрывали второй стеклянной пластинкой, которая удерживалась фиксатором на расстоянии 20 мкм. Этот образец для испытаний оставляли лежать в течение 12 часов при комнатной температуре и отверждали.
Среда для сравнения 1:
При температуре 60°C 5,927 г полиолового компонента, полученного как описано выше, смешивали с 2,50 г 2-[(фенилкарбамоил)оксил]этилпроп-2-еноата (Пример для сравнения 1), 0,10 г CGI 909 и 0,010 г Neu Methylenblau, а также 0,35 г N-этилпирролидона таким образом, что получался прозрачный раствор. Затем его охлаждали до 30°C, добавляли 1,098 г Desmodur® N 3900 и снова перемешивали. В заключение добавляли 0,006 г Fomrez UL 28 и вновь перемешивали непродолжительное время. Полученную жидкую массу затем помещали на стеклянную пластинку и там накрывали второй стеклянной пластинкой, которая удерживалась фиксатором на расстоянии 20 мкм. Этот образец для испытаний оставляли лежать в течение 12 часов при комнатной температуре и отверждали.
Испытания топографических свойств:
Среды, полученные как описано, были затем протестированы на их голографические характеристики при помощи измерительного оборудования в соответствии с Фигурой 1 по способу, описанному выше. При этом получились следующие величины измерений для значений насыщения Δnsat при величине энергии E [мДж/см2]:
Таблица 2: Оценка голографических характеристик выбранных Примеров
Обнаруженные значения для динамической области показывают, что уретанакрилат, использованный в среде для сравнения, является менее подходящим для применения в голографических средах, в то время как акрилаты, использованные в средах с 1 по 3, с более высокой плотностью двойных связей (DD>4,50 гэкв/кг) очень хорошо подходят для изготовления голографических сред для визуальных голограмм благодаря более высокой величине Δnsat, а также имеет место лучшая совместимость и смешиваемость отдельных компонентов.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФОТОПОЛИМЕРНАЯ КОМПОЗИЦИЯ И ЕЕ ПРИМЕНЕНИЕ ДЛЯ ИЗГОТОВЛЕНИЯ ГОЛОГРАФИЧЕСКИХ СРЕД | 2009 |
|
RU2515991C9 |
| ФОТОПОЛИМЕРНЫЕ КОМПОЗИЦИИ С РЕГУЛИРУЕМЫМ МЕХАНИЧЕСКИМ МОДУЛЕМ GUV | 2010 |
|
RU2542975C9 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ГОЛОГРАФИЧЕСКИХ СРЕД | 2010 |
|
RU2542981C9 |
| ФТОРУРЕТАНЫ В КАЧЕСТВЕ ДОБАВКИ В ФОТОПОЛИМЕРНОЙ КОМПОЗИЦИИ | 2010 |
|
RU2570662C9 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ГОЛОГРАФИЧЕСКОЙ ПЛЕНКИ | 2010 |
|
RU2542984C2 |
| ПОЛИУРЕТАНОВЫЕ КОМПОЗИЦИИ НА ОСНОВЕ ФОРПОЛИМЕРА ДЛЯ ИЗГОТОВЛЕНИЯ ГОЛОГРАФИЧЕСКИХ СРЕД | 2009 |
|
RU2515549C9 |
| ПОЛИУРЕТАНОВЫЙ СОСТАВ И ЕГО ПРИМЕНЕНИЕ ДЛЯ ПОЛУЧЕНИЯ ГОЛОГРАФИЧЕСКИХ СРЕД | 2009 |
|
RU2510666C2 |
| ПОЛИУРЕТАНОВЫЙ СОСТАВ И ЕГО ПРИМЕНЕНИЕ ДЛЯ ПОЛУЧЕНИЯ ГОЛОГРАФИЧЕСКИХ СРЕД | 2009 |
|
RU2518125C9 |
| ПОЛИУРЕТАНОВЫЙ СОСТАВ И ЕГО ПРИМЕНЕНИЕ ДЛЯ ПОЛУЧЕНИЯ ГОЛОГРАФИЧЕСКИХ СРЕД | 2010 |
|
RU2531625C9 |
| ПОЛИУРЕТАНОВАЯ КОМПОЗИЦИЯ ДЛЯ ИЗГОТОВЛЕНИЯ ГОЛОГРАФИЧЕСКИХ СРЕД, ЕЕ ПРИМЕНЕНИЕ, СПОСОБ ЗАПИСИ ГОЛОГРАММ И НЕНАСЫЩЕННЫЕ УРЕТАНЫ | 2009 |
|
RU2515977C2 |
Изобретения касаются фотополимерной композиции, включающей полимеры матрицы, записывающие мономеры и фотоинициаторы, и применения этой фотополимерной композиции для изготовления голографических сред. Описана фотополимерная композиция для изготовления голографических сред, включающая полимеры матрицы, записывающие мономеры и фотоинициаторы, причем полимеры матрицы представляют собой полиуретаны, которые получаются в результате взаимодействия изоцианатного компонента а) с компонентом b), реакционноспособным по отношению к изоцианатам, который в среднем содержит в молекуле по меньшей мере 1,5 групп, реакционноспособных по отношению к изоцианатам, причем записывающие мономеры содержат ароматические соединения формулы (I), в которой по меньшей мере один из остатков R1, R2, R3, R4, R5, R6 представляет собой соединенный через X с ароматическим кольцом остаток формулы (II), причем в формуле (II) А является линейной или разветвленной, при необходимости содержащей кислород углеводородной цепью, остальные остатки R1, R2, R3, R4, R5, R6 соответственно независимо друг от друга представляют собой атом водорода или органический остаток, a R7 является атомом водорода или метилом. Также описано применение указанной фотополимерной композиции для изготовления голографических сред, особенно для изготовления осевых голограмм, внеосевых голограмм, голограмм сфокусированного изображения, голограмм, восстанавливаемых в белом свете, голограмм Денисюка, внеосевых отражательных голограмм, голограмм краевого освещения, а также голографических стереограмм.
Технический результат - получение фотополимерной композиции, которая может содержать более высокую концентрацию записывающих мономеров в сравнении с известными композициями, без того, чтобы возникали какие-либо отрицательные эффекты, и одновременно с помощью которой могут получаться яркие голограммы. 2 н. и 8 з.п. ф-лы, 6 пр., 1 табл., 2 ил.
1. Фотополимерная композиция для изготовления голографических сред, включающая полимеры матрицы, записывающие мономеры и фотоинициаторы, причем полимеры матрицы представляют собой полиуретаны, которые получаются в результате взаимодействия изоцианатного компонента а) с компонентом b), реакционноспособным по отношению к изоцианатам, который в среднем содержит в молекуле по меньшей мере 1,5 групп, реакционноспособных по отношению к изоцианатам, отличающаяся тем, что записывающие мономеры содержат ароматические соединения формулы (I)

в которой по меньшей мере один из остатков R1, R2, R3, R4, R5, R6 представляет собой соединенный через X с ароматическим кольцом остаток формулы (II)

причем в формуле (II) А является линейной или разветвленной, при необходимости содержащей кислород углеводородной цепью, остальные остатки R1, R2, R3, R4, R5, R6 соответственно независимо друг от друга представляют собой атом водорода или органический остаток, a R7 является атомом водорода или метилом.
2. Фотополимерная композиция по п. 1, отличающаяся тем, что два или три из остатков R1, R2, R3, R4, R5, R6 являются остатками формулы (II), через X присоединенными к ароматическому кольцу.
3. Фотополимерная композиция по п. 2, отличающаяся тем, что если присутствуют два остатка формулы (II), остатки присоединены в мета- или пара-положении ароматического кольца, а если присутствуют три остатка формулы (II), остатки присоединены соответственно в мета-положениях.
4. Фотополимерная композиция по п. 1, отличающаяся тем, что органический остаток содержит радиационно-отверждаемую группу.
5. Фотополимерная композиция по п. 4, отличающаяся тем, что радиационно-отверждаемая группа представляет собой акрилатную или метакрилатную группу.
6. Фотополимерная композиция по п. 1, отличающаяся тем, что А представляет собой -СН2-СН2-, -СН2-СН2-СН2-, -СН2-СН(СН)3-СН2- или -СН2-СН2-СН2-СН2-.
7. Фотополимерная композиция по п. 1, отличающаяся тем, что фотоинициаторы включают анионный, катионный или нейтральный краситель и со-инициатор.
8. Фотополимерная композиция по п. 1, отличающаяся тем, что она дополнительно содержит в качестве пластификаторов уретаны.
9. Фотополимерная композиция по п. 8, отличающаяся тем, что уретаны имеют общую формулу (III) 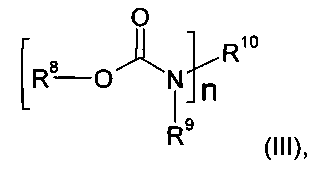
в которой n≥1 и n≤8, a R8, R9, R10 независимо друг от друга являются атомами водорода, линейными, разветвленными, циклическими или гетероциклическими незамещенными или при необходимости также замещенными гетероатомами органическими остатками.
10. Применение фотополимерной композиции по одному из пп. 1-9 для изготовления голографических сред, особенно для изготовления осевых голограмм, внеосевых голограмм, голограмм сфокусированного изображения, голограмм, восстанавливаемых в белом свете, голограмм Денисюка, внеосевых отражательных голограмм, голограмм краевого освещения, а также голографических стереограмм.
| US 2005031986 A1, 10.02.2005 | |||
| АППАРАТ ДЛЯ ПРОВЕДЕНИЯ ХИМИЧЕСКИХ ПРОЦЕССОВ | 0 |
|
SU300203A1 |
| US 3832176 A, 27.08.1974 | |||
| US 4339527 A, 13.07.1982 | |||
| US 2003044690 A1, 06.03.2003 | |||
| WO 2008125200 A1, 23.10.2008 | |||
| ОПТИЧЕСКОЕ ВОЛОКНО С ОТВЕРЖДЕННЫМ ПОЛИМЕРНЫМ ПОКРЫТИЕМ | 2002 |
|
RU2320590C2 |
Авторы
Даты
2015-11-10—Публикация
2011-01-28—Подача