Изобретение относится к области фармацевтики и может быть использовано для лечения болезней бактериальной этиологии у сельскохозяйственных животных и птиц.
Болезни бактериальной этиологии существенно повышают падеж животных при остром или подостром течении (пастереллез, колибактериоз, стафилококкоз и др.). При хронических же, вялотекущих болезнях бактериальной этиологии отмечают неравномерный или низкий прирост массы животных, повышенную чувствительность к стрессам, ухудшение продуктивности и биологических качеств эмбрионов, поствакцинального противовирусного иммунитета, плохую конверсию корма, особенно это проявляется при наличии в стаде микоплазм.
Изучение видового состава и патогенных свойств микрофлоры, выделенной от здоровых, заболевших или павших животных, указывает на ее полимикробный состав в самых разнообразных ассоциациях. Следовательно, причиной респираторных и желудочно-кишечных заболеваний в последнее время зачастую является смешанный характер микрофлоры, что осложняет как течение данных заболеваний, так и выбор эффективного лекарственного средства. Затрудняет борьбу с данными инфекциями и растущей резистентностью микрофлоры.
Таким образом, широкое распространение заболеваний микробной этиологии не только служит одной из причин снижения продуктивности и племенных качеств животных, вынужденного их убоя и падежа, требует больших затрат на лечение и профилактику, но и негативно сказывается как на эпизоотической ситуации, так и на экономике предприятия.
Так как бактериальные болезни наносят огромный ущерб сельскохозяйственному производству и сдерживают развитие животноводства и птицеводства, разработка новых эффективных средств борьбы с желудочно-кишечными и респираторными заболеваниями сельскохозяйственных животных и птиц является актуальной задачей.
Наиболее целесообразный метод, повышающий эффективность лечения бактериальных инфекций и замедляющий развитие резистентности у микроорганизмов - рациональное применение в составе препаратов сочетаний различных антибиотиков, обладающих широким спектром антимикробного действия.
Известно комплексное лекарственное средство для лечения бактериальных болезней крупного рогатого скота на основе антибиотиков последних поколений, обладающих широким спектром бактериостатического действия - доксициклина и флорфеникола. Препарат вводят внутримышечно (см., например, Жукова Н.Н. и др. Применение нового препарата на основе доксициклина и флорфеникола при болезнях молодняка крупного рогатого скота. Материалы международного научно-практического симпозиума, Саратов, 23 марта 2011 г.).
Известный препарат имеет высокую терапевтическую эффективность при трахеитах и диспепсии молодняка крупного рогатого скота, в применяемых дозах не обладает гепато- и нефротоксичностью.
Однако в указанном источнике информации отсутствуют сведения о возможности использования известного препарата для других видов сельскохозяйственных животных и птиц, а внутримышечный способ введения препарата повышает трудоемкость способа лечения.
Также известен комплексный препарат для лечения болезней бактериальной и микоплазменной этиологии у свиней и сельскохозяйственных птиц, включающий комбинацию антибиотиков с широким спектром бактериостатического действия - ципрофлоксацина, относящегося к группе фторхинолонов, и гентамицина.
Препарат вводят в форме раствора для перорального применения (см., например, Ципроген, адрес в Интернете: http://belfarma.com/index.php?option=com-content&view…, 21.05.2013).
Данный препарат является наиболее близким заявленному.
Недостатком известного препарата является то, что в его состав входит гентамицин. Гентамицин давно и широко применяется в медицинской и ветеринарной практике, что привело к возникновению и распространению устойчивых к нему штаммов микроорганизмов. По литературным данным в России уровень резистентности к гентамицину превышает таковой в большинстве других стран. Данные по антибиотикорезистентности в России свидетельствуют о том, что уже за период 2002-2004 гг. наблюдалась чрезвычайно высокая резистентность нозокомиальных штаммов H. aeruginosa и Klebsiella pneumonia к гентамицину, составляя 74,9% и 76,5% соответственно (см., например, Решедько Г.К. и др. Современные аспекты эпидемиологии, диагностики и лечения нозокомиальной пневмонии - Ж.: Клиническая микробиология и антимикробная химиотерапия, 2008, 10 (2), с. 143-153 или Зайцев А.А. и др. Аминогликозиды с позиций современной практики лечения инфекций дыхательных путей, ж.: Лечащий врач, 2009, №9).
Задачей настоящего изобретения является разработка эффективного и безвредного комплексного лекарственного средства на основе антибиотиков для лечения болезней бактериальной этиологии у сельскохозяйственных животных и птиц.
Поставленная задача решается тем, что антибактериальная фармацевтическая композиция для лечения сельскохозяйственных животных и птиц, содержащая соединение из группы фторхинолонов и вспомогательные вещества, согласно изобретению, дополнительно содержит апрамицина сульфат в эффективном количестве.
Поставленная задача решается также тем, что антибактериальная фармацевтическая композиция для лечения сельскохозяйственных животных и птиц содержит соединение из группы фторхинолонов и апрамицина сульфат при следующем соотношении (в масс. ч.): соединение из группы фторхинолонов: апрамицина сульфат 1:2-1:10.
Поставленная задача решается также тем, что антибактериальная фармацевтическая композиция для лечения сельскохозяйственных животных и птиц в качестве вспомогательных веществ содержит сахара.
Кроме того, поставленная задача решается тем, что антибактериальная фармацевтическая композиция в качестве соединения из группы фторхинолонов содержит энрофлоксацин, или ципрофлоксацин, или норфлоксацин, или пефлоксацин, или офлоксацин, или левофлоксацин, или моксифлоксацин.
Целесообразно в качестве сахаров в составе антибактериальной композиции использовать лактозу, или глюкозу, или фруктозу, или декстрозу, или сахарную пудру, или лактулозу.
Техническим результатом заявленного изобретения является то, что полученная антибактериальная фармацевтическая композиция для лечения сельскохозяйственных животных и птиц обладает повышенной эффективностью лечения при снижении дозы активных веществ, позволяет не только проводить лечение смешанных инфекций до выделения этиотропного возбудителя и изучения его чувствительности к антибиотикам, но и сократить сроки и снизить трудоемкость лечения, и при этом является безвредной и положительно влияет на морфологические показатели крови животных и птиц.
Заявленное изобретение характеризуется следующими примерами выполнения, которые, однако, не ограничивают объем притязаний заявителя.
Пример 1. Получение препарата.
В качестве соединения из группы фторхинолонов использовали ципрофлоксацин, а в качестве вспомогательного вещества - лактозу. Получают препарат смешиванием всех ингредиентов в миксере-грануляторе.
По внешнему виду препарат представляет собой порошок желтого цвета и содержит (в мг/1 г порошка): ципрофлоксацин 100, апрамицина сульфат 500, лактоза до 1 г.
Соотношение ципрофлоксацина и апрамицина сульфата 1:5.
Заявленная антибактериальная фармацевтическая композиция для лечения сельскохозяйственных животных и птиц является комплексным антибактериальным препаратом.
Входящие в состав композиции соединения из группы фторхинолонов обладают широким спектром антибактериального и антимикоплазменного действия. Активны в отношении грамположительных и грамотрицательных бактерий, в том числе Echerichia coli, Salmonella spp., Shigella spp., Klebsiella spp., Enterobacter spp., Proteus spp., Yersinia spp., Haemophilus spp., Pseudomonas aeruginosa, Pasteurella multocida, Plesiomonas shigelloides, Campilobacter jejuni, Brucella spp., Chlamydia trachomatis, Listeria monocytogenes, Mycobacterium spp., Corynebacterium diphtheriase, Staphylococcus aureus, Streptococcus spp., а также Mycoplasma spp.
Апрамицина сульфат оказывает бактерицидное действие преимущественно в отношении грамотрицательных, а также некоторых грамположительных бактерий, в том числе Echerichia coli, Salmonella spp., Pseudomonas spp., Staphylococcus spp., Streptococcus spp., Proteus spp., Bordetella bronchiseptica, Klebsiella spp., Shigella spp., Campilobacter spp., Brachyspira hyodysenteriae и некоторых видов микоплазм (Mycoplasma hyopneumonae). He активен в отношении анаэробных микроорганизмов. Механизм действия соединений из группы фторхинолонов основан на способности ингибировать активность фермента гиразы, обеспечивающего репликацию ДНК в бактериальной клетке.
Механизм антибактериального действия апрамицина сульфата обусловлен подавлением синтеза белка микроорганизмов путем необратимого связывания с 3OS-субъединицей рибосом.
Пример 2. Изучение острой токсичности.
Использовали фармацевтическую композицию, полученную по примеру 1.
Экспериментальные исследования по изучению острой токсичности были проведены на белых крысах и белых мышах. Исходный вес животных колебался в пределах 190-200 г для крыс и 20-21 г для мышей. В опыт брали клинически здоровых животных, которых предварительно выдерживали на 15-дневном карантине. Всех животных содержали в одинаковых условиях и на стандартном рационе.
Препарат в виде суспензии насильно вводили в желудок с помощью металлического зонда. Были испытаны 4 дозы: 3, 6, 8 и 10 г/кг массы тела. Каждую дозу вводили 6 животным. Контрольные животные получали воду в тех же объемах. За животными вели наблюдение в течение 2-х недель после введения, отмечая сроки гибели или выздоровления животных. Учитывали общее состояние животных, сохранение двигательных функций, аппетита, состояние шерстного покрова, дыхания, реакцию на внешние раздражители.
В результате введения препарата в диапазоне доз 3-10 г/кг гибели животных не выявлено. Максимально-переносимой дозой препарата в однократном опыте следует считать дозу - 10 г/кг. Клиническая картина интоксикации животных не выражена. Все опытные животные были активны, подвижны, хорошо принимали корм и практически не отличались от контрольных животных. При проведении патологоанатомического вскрытия животных была отмечена незначительная гиперемия слизистой желудка у крыс после введения дозы 10 г/кг. Макроанатомических изменений печени, почек, сердца и селезенки выявлено не было.
Таким образом, заявленный препарат согласно классификации ГОСТ 12.1.007-76 относится к 4-му классу токсичности (малотоксичное соединение).
Пример 3. Изучение кумулятивных свойств препарата в подостром эксперименте.
Препарат вводили в желудок белых крыс в постоянной дозе, составляющей 1/5 от максимально-введенной дозы (10 г/кг), т.е. ежедневно вводимая доза составляла 2,0 г/кг. Длительность эксперимента - 19 дней. Учитывали как материальную (гибель животных), так и функциональную кумуляцию.
Графический анализ зависимости «доза-эффект» позволил определить смертельные дозы ЛД16 и ЛД84, которые составили 25,1 г/кг и 36,5 г/кг соответственно. С учетом стандартной ошибки, которую определяли по формуле Гаддама, ЛД50п препарата в условиях повторного введения составила 30,6±0,96 г/кг массы тела. Коэффициент кумуляции (Kcum) рассчитывали по отношению эффективных доз подострого и острого опытов.
Kcum составил 3,1, что, согласно классификации Ю.С. Кагана, позволяет отнести заявленный препарат к 3 классу опасности (умеренная кумуляция).
При изучении функциональной кумуляции проводили оценку ряда показателей, а именно регистрировали массу тела, определяли суммационно-пороговый показатель (СПП), проводили анализ периферической крови (гемоглобин, лейкоциты, эритроциты), осуществляли оценку функционального состояния печени и почек, регистрировали некоторые поведенческие реакции животных.
По величине суммационно-порогового показателя оценивали функциональное состояние центральной нервной системы. Нервно-мышечную возбудимость животных определяли с помощью электродов по сокращению межпальцевых мышц с увеличением подачи тока.
Для выявления функциональной кумуляции животных обследовали на 5, 10 и 15 дни опыта (при этом животные получили суммарные дозы - 10, 20 и 30 г/кг соответственно). Следует сказать, что эти дозы в несколько раз больше доз, рекомендуемых производителем в Инструкции по применению.
Как следует из полученных результатов, у опытных животных уже с 10 дня эксперимента намечается тенденция к уменьшению массы тела, а на 15 день, после получения суммарной дозы 30 г/кг, отмечалось достоверное его снижение.
На том же сроке достоверно повышался суммационно-пороговый показатель (СПП), что свидетельствует о заторможенности животных.
Состояние периферической крови оценивали на гематологическом анализаторе Cell-dyn. Определяли количество гемоглобина, лейкоцитов и эритроцитов. Кроме того, использовали различные расчетные величины, отражающие физико-химические свойства эритроцитов, позволяющие количественно характеризовать показатели их состояния.
Результаты исследований свидетельствуют о том, что из показателей, характеризующих функциональное состояние периферической крови, было отмечено снижение количества гемоглобина (P<0,05) на 15 день. Все остальные показатели крови у опытных животных не отличались от контроля и не выходили за границу физиологической нормы для данных показателей.
Результаты измерения ректальной температуры и некоторых поведенческих реакций животных свидетельствуют о том, что на 15 день было отмечено и достоверное снижение ректальной температуры. Остальные показатели опытных животных достоверно не отличались от контроля и не выходили за границу физиологической нормы.
При изучении функционального состояния почек определяли диурез, удельный вес мочи, общий белок в моче и хлориды. Результаты исследований показали, что у опытных животных все показатели, характеризующие функциональное состояние почек, достоверно не отличаются от тех же показателей контрольных животных на всем протяжении опыта.
Функциональное состояние печени оценивали по способности органа синтезировать гиппуровую кислоту (обезвреживающая функция) и по содержанию в сыворотке крови общего белка (белковообразовательная функция).
Не менее важными для жизнедеятельности организма животных в целом, а также для оценки печени, является определение в сыворотке крови общих сульфгидрильных групп (SH-групп).
SH-группы - это функциональные группы в молекулах органических соединений, в т.ч. белков, определяющие их функциональные специфические свойства. SH-группы играют важную роль в образовании внутримолекулярных связей; в том числе -S-s-связи, которая, в свою очередь, обеспечивает жесткое скрепление отдельных полипептидных цепей, например, в иммуноглобулинах.
Как показали результаты исследований, у опытных животных на данном сроке выявлено достоверное уменьшение содержания в моче гиппуровой кислоты, что свидетельствует о снижении обезвреживающей функции печени. Все остальные показатели, характеризующие функцию печени, у животных, подвергавшихся повторному воздействию препарата в суммарной дозе, составляющей 30,0 г/кг, достоверно не отличались от контрольных величин.
При регистрации поведенческих реакций учитывали показатели динамической активности и статической работоспособности животных.
Динамическую активность определяли с помощью «вертикального» двигательного компонента, который основан на подсчете количества вставаний животных на задние лапы за 3 минуты. Имеются данные о высокой чувствительности данной реакции для крыс. Указанный метод может служить объективным показателем общего состояния животных.
Для оценки статической мышечной работоспособности применяли метод удерживания животных на горизонтальном стержне. Учитывали длительность пребывания животного на стержне. Этот метод является наиболее простым и доступным для токсикологических исследований. Он не требует дорогостоящих приборов, и длительность его выполнения может быть учтена с достаточной точностью.
Анализ результатов опыта показывает, что количество вставаний животных на задние лапы за 3 мин снижается с 10-го по 15-й дни эксперимента, также в данный период времени становится короче и длительность пребывания животного на стержне.
После окончания опыта животных убивали и определяли массовые коэффициенты внутренних органов. Массовые коэффициенты органов у животных опытной группы находились на одном уровне с контролем и достоверно от него не отличались, что свидетельствует о том, что этот показатель не является определяющим при воздействии заявленного препарата.
Таким образом, в условиях субхронического воздействия заявленный препарат вызывал достоверные изменения со стороны нервной системы, массы животных, крови (снижение гемоглобина) и тенденцию к снижению поведенческих показателей. Это показывает, что препарат обладает незначительной как материальной, так и функциональной кумуляцией. Однако все изменения проявлялись только на уровне доз, в несколько раз больших, чем практические, и в условиях многократного введения. В связи со сказанным препарат не представляет реальной опасности в условиях лечения сельскохозяйственных животных и птицы.
Необходимо отметить, что были проведены аналогичные испытания препаратов, содержащих в качестве соединения из группы фторхинолонов энрофлоксацин, норфлоксацин, пефлоксацин, офлоксацин, левофлоксацин, моксифлоксацин. Испытывались композиции с различным соотношением соединений из группы фторхинолонов к апрамицину сульфату. На основании данных статистической обработки полученных результатов, возможно сделать вывод о том, что достоверных отличий при использовании в составе комозиции указанных выше соединений из группы фторхинолонов при соотношении их с апрамицином сульфатом в пределах 1:2-1:8 мас.ч. не выявлено, и поэтому результаты данных испытаний в настоящем описании не приведены.
Пример 4. Изучение антимикробной активности.
Композиция получена по примеру 1.
Основной целью исследования стало сравнительное определение величин МПК (минимально подавляющей концентрации) препарата и его компонентов для обоснования эффективности заявленной композиции.
В работе в качестве тест-штаммов использованы следующие тест-штаммы: S. aureus АТСС 6538Р (FDA 209Р), Е. coli АТСС 25922, Ps. aeruginosa АТСС 9027, Вас. subtilis АТСС 6633 и Salmonella abony №103/39.
Для инокуляции использовали свежие 24-часовые культуры возбудителей, выращенные в среде №8, с определением инокулирующей дозы титрованием на среде №1 поверхностным методом.
Исследования проведены на средах производства ФБУН «ГНЦ прикладной микробиологии и биотехнологии» №8 ГРМ, рег. уд. № ФСР 2007/00839 от 27.12.2011 г. и №1 ГРМ, per. уд. № ФСР 2011/11415 от 27.12.2011 г.
Навески препаратов массой 50 мг растворяли в 5 мл стерильной воды с последующим приготовлением серийных разведений на жидкой питательной среде №8 ГРМ.
Титрование обогащенных культур тест-штаммов показало, что биологическая активность суточных культур (концентрация живых бактериальных клеток) составила от 4,5·107 до 9·109 КОЕ/мл.
Усредненные результаты оценки антимикробной активности препарата и его компонентов представлены в таблицах 1-11.
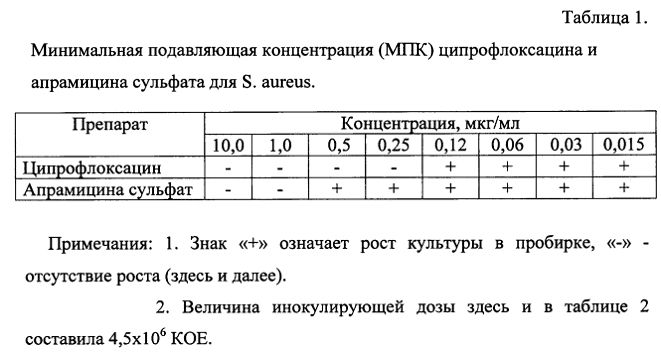
Как видно из результатов, представленных в таблице 1, МПК ципрофлоксацина в отношении S. aureus составила 0,25 мкг/мл, апрамицина сульфата 1,0 мкг/мл. Результаты определения МПК комбинации ципрофлоксацина и апрамицина сульфата для S. aureus в различных соотношениях представлены в таблице 2.
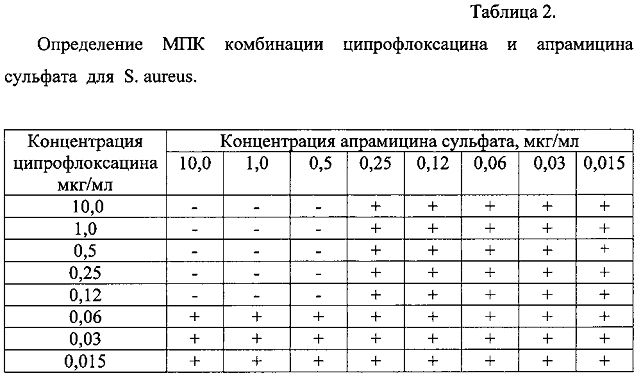
Сочетание ципрофлоксацина и апрамицина сульфата приводит к снижению МПК анализируемых компонентов: минимальная концентрация ципрофлоксацина в комбинации, подавляющая рост тест-микроба, составила 0,12 мкг/мл, апрамицина сульфата 0,5 мкг/мл (соотношение Ц:А составило 1:4).
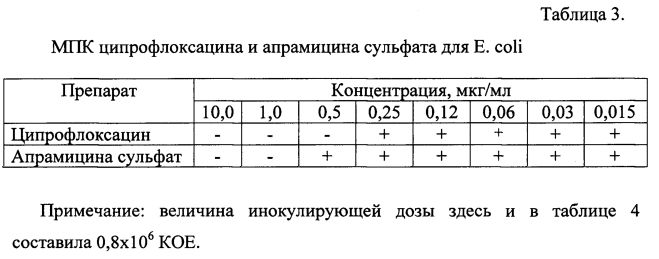
Изучение эффективности препаратов на модели Е. coli показало (таблица 3), что МПК ципрофлоксацина составила 0,5 мкг/мл, апрамицина сульфата 1,0 мкг/мл. Результаты определения МПК комбинации ципрофлоксацина и апрамицина сульфата для Е. coli в различных соотношениях представлены в таблице 4.
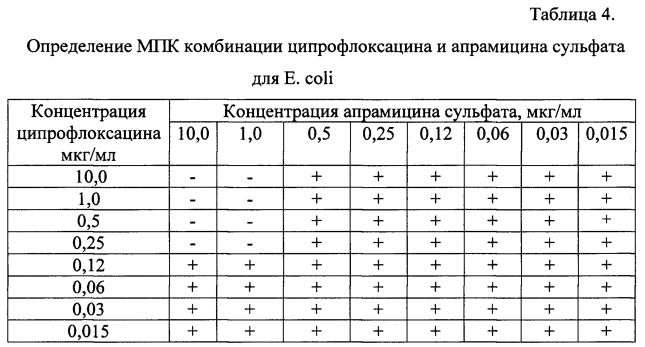
Минимальная концентрация ципрофлоксацина в комбинации, подавляющая рост тест-микроба, составила 0,25 мкг/мл, апрамицина сульфата 1,0 мкг/мл (соотношение Ц:А составило 1:4).

МПК ципрофлоксацина для Ps. aeruginosa (таблица 5) составила 0,06 мкг/мл, апрамицина сульфата 1,0 мкг/мл.
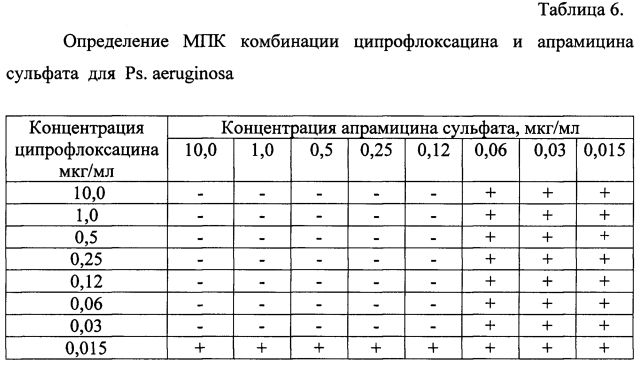
Определение МПК комбинации ципрофлоксацина и апрамицина сульфата в различных соотношениях на модели Ps. aeruginosa (таблица 6) показало, что МПК ципрофлоксацина в комбинации, подавляющая рост тест-микроба, составила 0,03 мкг/мл, апрамицина сульфата - 0,12 мкг/мл (соотношение Ц:А - 1:4).
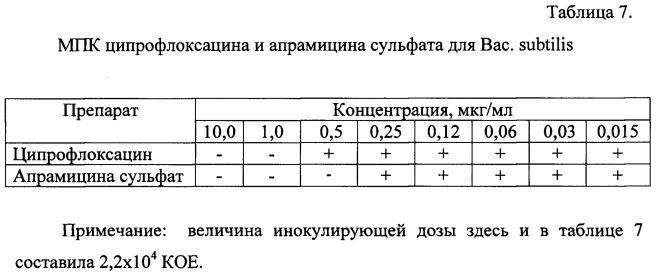
МПК ципрофлоксацина в отношении Вас.subtilis составила 1,0 мкг/мл (таблица 7), апрамицина сульфата 0,5 мкг/мл.
Результаты определения МПК комбинации ципрофлоксацина и апрамицина сульфата в различных соотношениях представлены в таблице 8.
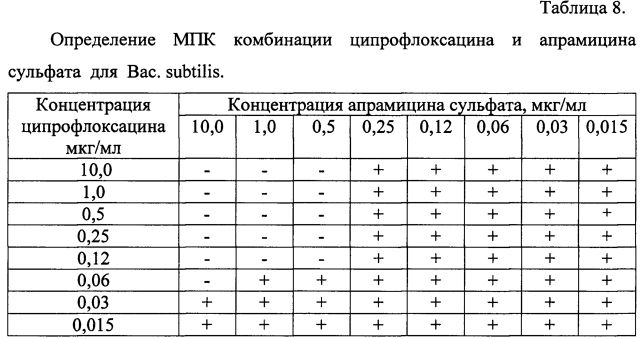
МПК ципрофлоксацина в комбинации, подавляющая рост тест-микроба, составила 0,12 мкг/мл, апрамицина сульфата - 0,5 мкг/мл (соотношение Ц:А составило 1:4).
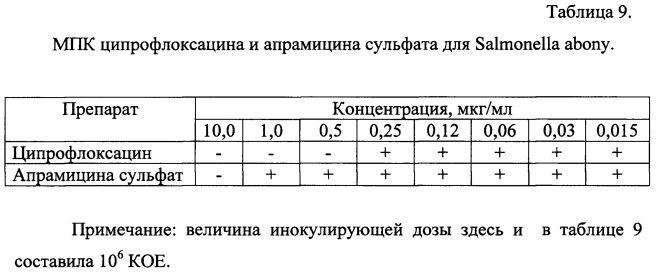
МПК ципрофлоксацина в отношении S. abony составила 0,5 мкг/мл, апрамицина сульфата - 10,0 мкг/мл (таблица 9).
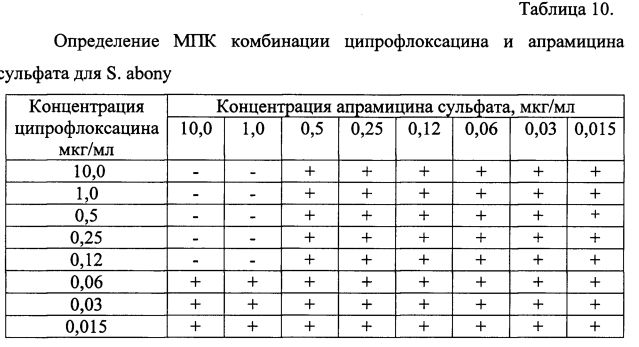
Результаты определения МПК комбинации ципрофлоксацина и апрамицина сульфата в различных соотношениях, представленные в таблице 10, показали, что МПК ципрофлоксацина в комбинации, подавляющая рост тест-микроба, составила 0,12 мкг/мл, апрамицина сульфата 1,0 мкг/мл (соотношение Ц:А - 1:8).
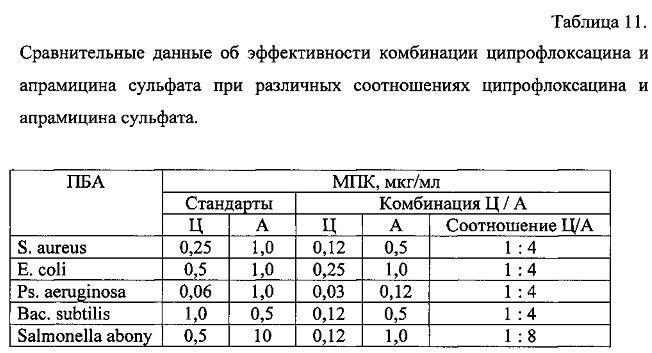
Обобщенная оценка эффективности различных комбинаций ципрофлоксацина и апрамицина сульфата, представленная в таблице 11, показала, что сочетание этих антибиотиков в среднем соотношении 1:6 приводит к уменьшению величин их МПК по сравнению с МПК стандартов ципрофлоксацина и апрамицина сульфата.
Схожие результаты были получены и при использовании в составе композиции таких соединений из группы фторхинолонов, как энрофлоксацин, норфлоксацин, пефлоксацин, офлоксацин, левофлоксацин, моксифлоксацин при их соотношении с апрамицином сульфатом в пределах 1:2-1:10, что позволяет сделать вывод о том, что комбинация - соединение из группы фторхинолонов + апрамицин - обладает синергидным эффектом.
Пример 5.
Эффективность лечения бактериальных болезней с помощью заявленной фармацевтической композиции.
Препарат был исследован с лечебной целью на поросятах, телятах, жеребятах, ягнятах и сельскохозяйственной птице при респираторных и желудочно-кишечных заболеваниях бактериальной этиологии, в том числе сальмонеллезе, пастереллезе, микоплазмозе, колибактериозе.
Применяли препарат перорально с водой для поения. В период лечения животные с ярко выраженными клиническими признаками респираторных заболеваний (сухой кашель, истечения из носа, пониженный аппетит, затрудненное дыхание и малоподвижность), а также с диареей, получали только воду, содержащую лекарственный препарат. В результате проведения экспериментов установлено, что препарат обладает выраженной антимикробной активностью. После введения препарата физиологические и биохимические показатели крови нормализовались на 3-5 сутки. Например, у телят, которые получали предложенную композицию в дозе 0,5-0,6 г на 10 кг массы тела, общее состояние улучшилось, и клиническая картина нормализовалась на 3-4 день после дачи препарата. В результате испытаний установлено, что эффективными суточными дозами препарата являются следующие (г/10 кг массы животного): поросята - 0,25; телята, жеребята - 0,60, ягнята - 0,25.
Эффективная суточная доза для сельскохозяйственных птиц - 0,6 кг заявленной композиции на тонну воды.
Исследование морфобиохимических показателей крови животных и птиц опытных групп после применения заявленной композиции свидетельствует о ее хорошей переносимости и выраженном биологическом действии на организм животных. Так, в результате применения заявленного препарата в течение 5 дней увеличилось содержание эритроцитов, лейкоцитов и гемоглобина, нормализовались показатели кислотно-щелочного равновесия и общего белка в крови. Увеличение в крови подопытных животных и птиц количества эритроцитов указывает на активизацию окислительно-восстановительных процессов и на снижение токсических и воспалительных процессов, а также на улучшение дыхательной и токсико-выделительной функций организма на клеточном уровне.
Результаты по изменению содержания в крови лейкоцитов свидетельствуют об усилении фагоцитарной активности, активизации защитных реакций организма. Увеличение общего белка в крови у подопытных животных и птиц указывает на нормализацию физиологического состояния, активизацию внутриклеточного метаболизма.
По-видимому, повышается уровень неспецифической резистентности, что свидетельствует о положительном влиянии препарата на морфологические показатели крови. Увеличение щелочного резерва крови свидетельствует о снижении процессов ацидоза и более высоком уровне окислительно-восстановительных процессов в организме. Указанные позитивные изменения, происходящие в организме, обеспечивают сокращение продолжительности лечения до 4-5 дней, а также более интенсивный рост подопытных животных и птиц.
Таким образом, получена безвредная антибактериальная фармацевтическая композиция для лечения сельскохозяйственных животных и птиц, которая:
- обладает повышенной эффективностью лечения при снижении дозы активных веществ;
- положительно влияет на морфологические показатели крови;
- позволяет не только проводить лечение смешанных инфекций до выделения этиотропного возбудителя и изучения его чувствительности к антибиотикам, но и сократить сроки и снизить трудоемкость лечения.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПЛЕКСНЫЙ АНТИБАКТЕРИАЛЬНЫЙ ПРЕПАРАТ ДЛЯ ЖИВОТНЫХ | 2014 |
|
RU2554797C1 |
| Комплексная антибактериально-противогельминтозная композиция для лечения сельскохозяйственных животных и птиц | 2017 |
|
RU2676326C1 |
| КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ИНФЕКЦИЙ БАКТЕРИАЛЬНОЙ ЭТИОЛОГИИ У ЖИВОТНЫХ | 2013 |
|
RU2514647C1 |
| Способ лечения болезней бактериальной этиологии у сельскохозяйственных животных и птиц | 2016 |
|
RU2611351C1 |
| ИНЪЕКЦИОННАЯ АНТИБАКТЕРИАЛЬНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2014 |
|
RU2563826C1 |
| АНТИБАКТЕРИАЛЬНОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО В ФОРМЕ КАПЕЛЬ ДЛЯ ЛЕЧЕНИЯ ГЛАЗНЫХ БОЛЕЗНЕЙ У ЖИВОТНЫХ | 2015 |
|
RU2580630C1 |
| Способ лечения больных сальмонеллёзом телят | 2019 |
|
RU2691139C1 |
| АНТИБАКТЕРИАЛЬНОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО В ФОРМЕ МАЗИ ДЛЯ ЛЕЧЕНИЯ ГЛАЗНЫХ БОЛЕЗНЕЙ У ЖИВОТНЫХ | 2015 |
|
RU2580631C1 |
| ЖЕЛАТИНОВЫЕ КАПСУЛЫ НА ОСНОВЕ 3,3-ДИИНДОЛИЛМЕТАНА И ЭПИКАТЕХИН-3-ГАЛЛАТА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2011 |
|
RU2448700C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ ДИСБИОЗОВ КИШЕЧНИКА В ПРОЦЕССЕ ПРОВЕДЕНИЯ АНТИБАКТЕРИАЛЬНОЙ ТЕРАПИИ У ТЕПЛОКРОВНЫХ ЖИВОТНЫХ: КРУПНОГО РОГАТОГО СКОТА, СВИНЕЙ, ДОМАШНИХ ЖИВОТНЫХ, В ЧАСТНОСТИ СОБАК, КОШЕК, И СЕЛЬСКОХОЗЯЙСТВЕННЫХ ПТИЦ И СПОСОБ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ ДИСБИОЗОВ КИШЕЧНИКА В ПРОЦЕССЕ ПРОВЕДЕНИЯ АНТИБАКТЕРИАЛЬНОЙ ТЕРАПИИ У ТЕПЛОКРОВНЫХ ЖИВОТНЫХ: КРУПНОГО РОГАТОГО СКОТА, СВИНЕЙ, ДОМАШНИХ ЖИВОТНЫХ, В ЧАСТНОСТИ СОБАК, КОШЕК, И СЕЛЬСКОХОЗЯЙСТВЕННЫХ ПТИЦ | 2008 |
|
RU2415684C2 |
Изобретение относится к области ветеринарии и предназначено для лечения болезней бактериальной этиологии у сельскохозяйственных животных и птиц. Заявленная композиция содержит соединение из группы фторхинолонов, апрамицина сульфат и вспомогательные вещества. Композиция обладает повышенной эффективностью лечения при снижении дозы активных веществ. Позволяет не только проводить лечение смешанных инфекций до выделения этиотропного возбудителя и изучения его чувствительности к антибиотикам, но и сократить сроки и снизить трудоемкость лечения. При этом композиция является безвредной и положительно влияет на морфологические показатели крови животных и птиц. 4 з.п. ф-лы, 11 табл., 5 пр.
1. Антибактериальная фармацевтическая композиция для лечения сельскохозяйственных животных и птиц, содержащая соединение из группы фторхинолонов и вспомогательные вещества, отличающаяся тем, что дополнительно содержит апрамицина сульфат в эффективном количестве.
2. Антибактериальная фармацевтическая композиция по п. 1, отличающаяся тем, что содержит соединение из группы фторхинолонов и апрамицина сульфат при соотношении (мас. ч.): соединение из группы фторхинолонов:апрамицина сульфат 1:2-1:10.
3. Антибактериальная фармацевтическая композиция по п. 1, отличающаяся тем, что в качестве соединения из группы фторхинолонов содержит энрофлоксацин, или ципрофлоксацин, или норфлоксацин, или пефлоксацин, или офлоксацин, или левофлоксацин, или моксифлоксацин.
4. Антибактериальная фармацевтическая композиция по п. 1, отличающаяся тем, что в качестве вспомогательных веществ содержит сахара.
5. Антибактериальная фармацевтическая композиция по п. 1, отличающаяся тем, что в качестве сахаров содержит лактозу, или глюкозу, или фруктозу, или декстрозу, или сахарную пудру, или лактулозу.
| WO 2005072644 A1, 11.08.2005 | |||
| ПРЕПАРАТ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ ЖИВОТНЫХ И ПТИЦ БАКТЕРИАЛЬНОЙ ЭТИОЛОГИИ | 2002 |
|
RU2227741C2 |
| ХМЕЛЕВСКАЯ Ю.В | |||
| Применение макролидов и фторхинолонов для коррекции нарушений иммунитета при экспериментальном панкреатите// Успехи современного естествознания, 2003, 12, с.71. | |||
Авторы
Даты
2015-12-10—Публикация
2015-02-19—Подача