Изобретение относится к области ветеринарии и может быть использовано для лечения и профилактики болезней смешанной бактериальной и гельминтозной этиологии у сельскохозяйственных животных.
Болезни смешанной бактериальной и гельминтозной этиологии при остром или подостром течении существенно повышают отход животных, обуславливают низкий прирост массы, повышенную чувствительность к стрессам, ухудшают продуктивность и биологические качества мяса и молока, снижение срока поствакцинного иммунитета, плохую биоконверсию корма (гельминтозы + пастереллез, гельминтозы + колибактериоз, гельминтозы + стафилококкоз, гельминтозы + стрептококкозы, гельминтозы + микоплазмозы, гельминтозы + лямблиозы и другие сочетания).
Изучение видового состава микрофлоры и фауны гельминтов и их патогенных свойств, выделенных от здоровых, заболевших или павших животных, указывает на ее полимикробный состав и многообразие видов гельминтофауны в самых разнообразных ассоциациях и сочетаниях.
Причиной желудочно-кишечных заболеваний сельскохозяйственных животных в последнее время является смешанный характер микрофлоры и гельминтофауны, что осложняет течение болезней и выбор эффективного лекарственного средства, а также возрастающая резистентность патогенов.
Таким образом, широкое распространение болезней смешанной бактериальной и гельминтозной этиологии наносят огромный ущерб сельскохозяйственному производству и сдерживают развитие животноводства, служит одной из причин ухудшения эпизоотической ситуации, снижения продуктивности и племенных качеств животных, вынужденного их убоя и падежа и требует больших затрат на лечение и профилактику, на разработку новых эффективных средств борьбы с ассоциативными заболеваниями сельскохозяйственных животных.
Наиболее целесообразный метод, повышающий эффективность лечения заболеваний смешанной бактериальной и гельминтозной этиологии и замедляющий развитие резистентности у патогенов - рациональное применение в составе препаратов сочетаний различных антибиотиков и антигельминтиков, обладающих широким спектром антимикробного и противопаразитарного действия методами орального назначения.
Среди известных комплексных лекарственных средств для лечения ассоциативных заболеваний сельскохозяйственных животных смешанной бактериальной и гельминтозной этиологии порошковых препаратов, предназначенных для индивидуальной и групповой терапии и профилактики методами орального назначения не разработано.
Известно комплексное лекарственное средство для лечения бактериальных болезней крупного рогатого скота на основе антибиотиков последних поколений, обладающих широким спектром бактериостатического действия - доксициклина и флорфеникола. Препарат вводят внутримышечно. Применение нового препарата на основе доксициклина и флорфеникола при болезнях молодняка крупного рогатого скота имеет высокую эффективность при трахеитах и диспепсии молодняка крупного рогатого скота, в применяемых дозах не обладает гепато- и нефротоксичностью [1, 2].
Однако в указанном источнике информации отсутствуют сведения о возможности использования известного препарата для других видов сельскохозяйственных животных и птиц, а внутримышечный способ введения препарата повышает трудоемкость способа лечения.
Известно антибактериальная композиция для лечения сельскохозяйственных животных и птиц, содержащая соединение из группы фторхинолонов и апрамицина сульфат при следующем соотношении (в масс. ч.): соединение из группы фторхинолонов: апрамицина сульфат 1:2-1:10 [2, 3, 6].
Антибактериальная фармацевтическая композиция в качестве соединения из группы фторхинолонов содержит энрофлоксацин, или ципрофлоксацин, или норфлоксацин, или пефлоксацин, или офлоксацин, или левофлоксацин, или моксифлоксацин. Антибактериальная фармацевтическая композиция для лечения сельскохозяйственных животных и птиц является только комплексным антибактериальным препаратом, но не эффективен против гельминтов. Входящие в состав композиции соединения из группы фторхинолонов обладают широким спектром антибактериального и антимикоплазменного действия. Активны в отношении грамположительных и грамотрицательных бактерий, не активна в отношении анаэробных микроорганизмов. Механизм действия соединений из группы фторхинолонов основан на способности ингибировать активность фермента гиразы, обеспечивающего репликацию ДНК в бактериальной клетке [1, 2, 3, 6].
Известны препараты, содержащие в качестве действующего вещества (ДВ) авермектиновый комплекс, и препараты, являющиеся химически модифицированными членами семейства авермектинов, получаемых на основе почвенного гриба Streptomyces avermitilis (абиктин, авертин, аверсект-2, баймек, бимектин, дектомакс, дуотин, ивермаг, ивермек, иверсект, ивертин, новомек), которые всесторонне изучены и широко используются в борьбе с гельминтами [1, 2, 3].
Однако недостатками препаратов, содержащих в качестве ДВ авермектины или ивермектин, является высокое содержание ДВ (1%) в готовой форме и, соответственно, в лечебной дозе - 20-30 мг на 100 кг массы тела животного [4], а также то, что они неудобны для применения мелким домашним животным, например небольшим собакам и кошкам, из-за трудности дозирования. При применении ивермектина необходимо соблюдать осторожность, так как он обладает гепатотоксическим действием. Установлено, что собаки породы Колли, Бордер-Колли, Бобтейл, Шелти особенно чувствительны к действию ивермектина. Отмечено влияние ивермектина на центральную нервную систему собак, у брахеоцефалов (короткомордых) препарат проходит через гематоэнцефалитический барьер.
Препарат ДИРОНЕТ для профилактики и лечения гельминтозов животных, содержащий соединение из группы авермектинов, пирантел или его соль и целевую добавку, содержит празиквантель при следующем соотношении ингредиентов, мас. ч.: соединение из группы авермектинов: пирантел или его соль: празиквантель: целевая добавка = 1,2:3,0:1,0:6,0 [4].
В качестве соединения из группы авермектинов препарат может содержать ивермектин, или абамектин, или дорамектин, или моксидектин.
Препарат в качестве соли пирантела может содержать пирантел памоат, или пирантел тартрат, или пирантел эмбонат, или пирантел гидрохлорид.
В качестве целевой добавки препарат содержит смесь, состоящую из аскорбиновой кислоты, бикарбоната натрия, крахмала, сахара, аэросила, талька, лаурил сульфата натрия и поливинилпирролидона.
Технический результат, обеспечиваемый изобретением, заключается в повышении устойчивости животных к повторному заражению.
Препарат получают путем смешивания или растворения компонентов, а затем делают гранулы, таблетки, суспензию, spot on или pur on [4].
Изобретение дирофен включает албендазола сульфоксид (n-[6-(пропан-1-сульфинил)-1Н-1,3-бензодиазол-2-ил]метоксикарбоксимидовая кислота) 5,0-10,0% массовой доли соотношения компонентов, бутафосфан (1-бутиламино-1-метил) этилфосфоновая кислота) 10,0-20,0% массовой доли, воду для инъекций - остальное и имеет следующие преимущества: 1. Комплексная терапия побочных эффектов гельминтозной инвазии за счет использования в составе препарата бутафосфана. 2. Низкая токсичность. 3. Удобный способ дозирования и введения. Препарат для лечения гельминтозов у животных, содержащий албендазола сульфоксид, сопутствующие вещества дополнительно содержит бутафосфан. Однако недостатком препарата является его негативное влияние на биохимические показатели крови при передозировке. Изучение основных биохимических показателей сыворотки крови выявило изменения при действии препарата па функцию печени, почек, обмен белка и активность ферментов [5].
Задачей настоящего изобретения является разработка эффективного и безвредного комплексного лекарственного средства на основе антибиотиков и антгельминтиков для лечения болезней смешанной бактериальной и гельминтозной этиологии у сельскохозяйственных животных и птиц.
Поставленная задача решается тем, что комплексная антибактериальная фармацевтическая композиция для лечения сельскохозяйственных животных и птиц, содержащая азитромицин, празиквантель, фенбендазол, характеризуется тем, что дополнительно содержит вспомогательные вещества: бентонит (Герпегежского месторождения (влажность 10%), йодированную поваренную соль, патоку, хелатную медь, медный купорос при соотношении в мг/г порошка: азитромицин - 100 мг, празиквантель - 100 мг, фенбендазол - 100 мг, бентонит-(Герпегежского месторождения (влажность 10%) - 200 мг, йодированная поваренная соль - 100 мг, патока - 200 мг, хелатная медь - 100 мг и медный купорос - 100 мг.
Техническим результатом заявленного изобретения является то, что полученная антибактериально-противогельминтозная фармацевтическая композиция для лечения сельскохозяйственных животных и птиц обладает повышенной эффективностью лечения при снижении дозы активных веществ, позволяет не только проводить лечение смешанных инфекто-инвазий до выделения этиотропных возбудителей и изучения их чувствительности к антибиотикам и антгельминтикам, но и сократить сроки и снизить трудоемкость лечения, и при этом является безвредной и положительно влияет на морфологию крови животных и птиц.
Заявленное изобретение характеризуется следующими примерами.
Пример 1. Получение антибактериально-противогельминтозной фармацевтической композиции.
В качестве бактерицидного соединения из группы макролидов использовали азитромицин, в качестве антигельминтиков - субстанции празиквантела и фенбендазола. а в качестве вспомогательных веществ - бентонит (Герпегежского месторождения (влажность 10%), йодированную поваренную соль, патоку, хелатную медь и медный купорос.Получают антибактериально-противогельминтозную фармацевтическую композицию смешиванием всех ингредиентов в миксере-грануляторе при 300 оборотах в минуту в течение 30 минут.
По внешнему виду антибактериально-противогельминтозная фармацевтическая композиция представляет собой порошок серого цвета и содержит (в мг/1 г порошка): азитромицин 100 мг, празиквантель 100 мг, фенбендазол 100 мг, бентонит Герпегежского месторождения (влажность 10%) 200 мг, йодированная поваренная соль 100 мг, патока 200 мг, хелатная медь 100 мг и медный купорос 100 мг.Заявленная антибактериально-противогельминтозная фармацевтическая композиция для лечения сельскохозяйственных животных и птиц является комплексным антибактериально-противогельминтозным препаратом для индивидуального и группового назначения. Входящий в его состав азитромицин обладает широким спектром антибактериального и антимикоплазменного действия. Активен в отношении грамположительных бактерий, в т ч: Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococcus aureus; аэробных грамотрицательных бактерий: Pasteurella multocida, Haemophilus influenzae, Haemophilus parainfluenzae, Moraxella catarrhalis, Neisseria gonorrhoeae, Legionella pneumophila; некоторых анаэробных микроорганизмов: Fusobacterium spp., Clostridium perfringens, Prevotella spp., Porphyriomonas spp.; а также против Chlamydia psittaci, Chlamydia pneumoniae, Chlamydia trachomatis, Mycoplasma hominis, Mycoplasma pneumoniae, Borrelia burgdorferi.
Механизм действия азитромицина связан с подавлением синтеза белка микробной клетки. Связываясь с 50S субъединицей рибосом, угнетает пептидтранслоказу на стадии трансляции, подавляет синтез белка, замедляет рост и размножение бактерий, т.е. действует бактериостатически. В высоких концентрациях оказывает бактерицидное действие.
Входящий в его состав празиквантель обладает широким спектром антигельминтного действия в отношении био - и геогельминтов: Fasciola hepatica L., 1758; Dicrocoelium lanceatum Stilles et Hassall, 1896; Moniezia expansa Rud., 1810; Moniezia benedeni Moniez, 1879; Avitellina centripunctata Rivolta, 1874; Thysaniezia giardi Moniez, 1879; Echinococcus granulosus Batsch, 1789; Cysticercus tenuicollis Pallas, 1766 larvae; Ostertagia ostertagi Stilles, 1892; Ostertagia circumcincta; Ostertagia occidentalis; Ostertagia trifurcata; Ostertagia orloffi; Ostertagia trifida; Bunostomum trigonocephalum Rud., 1808; Bunostomum phlebotomum Railliet, 1900; Oesophagostomum radiatum Rud., 1803; Trichostrongylus axei Cob., 1879; Trichostrongylus capricola Ransom, 1907; Trichostrongylus columbriformis Giles, 1829; Trichostrongylus skrjabini Kalant., 1928; Trichostrongylus vitrinus Looss, 1905; Haemonchus contortus Rud., 1803; Chabertia ovina Fabricius, 1788; C. oncophora Railliet, 1898; Nematodirus filicollis Rud., 1802; Nematodirus helvetianus May, 1920; Nematodirus oiratianus; Nematodirus spathiger; Nematodirus abnormalis; Dictyocaulus filaria; Protostrongylus hobmaeri; Protostrongylus skrjabini; Protostrongylus raillieti; Mulleria capillaris; Cystocaulus nigrescens; Trichocephalus ovis; Trichocephalus skrjabini.
Входящий в его состав фенбендазол обладает также широким спектром антигельминтного действия преимущественно в отношении геогельминтов: Ostertagia ostertagi Stilles, 1892; Ostertagia circumcincta; Ostertagia occidentalis; Ostertagia trifurcata; Ostertagia orloffi; Ostertagia trifida; Chabertia ovina Fabricius, 1788; Bunostomum trigonocephalum Rud., 1808; Trichostrongylus axei Cob., 1879; Trichostrongylus capricola Ransom, 1907; Trichostrongylus columbriformis Giles, 1829; Trichostrongylus skrjabini Kalant., 1928; Trichostrongylus vitrinus Looss, 1905; Bunostomum phlebotomum Railliet, 1900; Oesophagostomum radiatum; Haemonchus contortus Rud., 1803; Nematodirus helvetianus May, 1920; Nematodirus filicollis; Nematodirus oiratianus; Nematodirus spathiger; Nematodirus abnormalis; Nematodirus schulzi; Dictyocaulus filaria; Trichocephalus ovis; Trichocephalus skrjabini
Входящий в его состав вспомогательные вещества бентонит (Герпегежского месторождения (влажность 10%), йодированная поваренная соль, патока, хелатная медь и медный купорос пролонгируют эффект азитромицина, празиквантела и фенбендазола, улучшают вкусовые свойства композиции, активизируют все виды обмена веществ.
Пример 2. Изучение острой токсичности композиции.
Использовали фармацевтическую композицию, полученную по примеру 1.
Экспериментальное изучение острой токсичности композиции проводили на 45 самцах мышах линии Balb/c, живой массой в пределах 22,0-25,0 грамм. В опыт брали клинически здоровых животных, которых разделили на 5 групп (по 9 гол в каждой) и выдерживали на 10-дневном карантине и содержали в одинаковых условиях. Мышам 1-4 опытных групп композицию вводили в желудок в форме водной суспензии в дозах 1, 3, 5 и 6 г/кг массы тела с помощью резинового зонда. Контрольные мыши получали воду в тех же объемах. За животными вели клинические наблюдения в течение 2-х недель после введения. Учитывали общее состояние животных, сохранение двигательных функций, аппетита, состояние шерстного покрова, дыхания, реакцию на внешние раздражители. В крови мышей указанных групп определяли некоторые метаболические параметры. Полученные результаты суммированы в таблице 1. Из этой таблицы видно, что композиция способствует повышению содержания общего белка в сыворотке крови мышей на 14-27%. Под влиянием композиции в крови у мышей увеличилась концентрация мочевины, вновь наиболее значительно в третьей группе. В среднем, в сыворотке крови подопытных животных активность ACT была ниже нормы на 2-8%, а АЛТ, напротив, выше на 6-14%, что отражает возможное некоторое органостабилизирующее действие ее на ACT, а также нормализацию переанимирующей функции печени. Об этом и свидетельствует коэффициент де Ритиса (ACT/АЛТ), который колебался в пределах нормы. В то же время, после введения композиции в сыворотке крови самцов мышей линии Balb/c всех подопытных групп увеличилось содержание глюкозы, в среднем нВ 8,5%. Положительным моментом следует считать снижение уровня холестерина на 5,2-7,4% при всех дозах введения композиции.
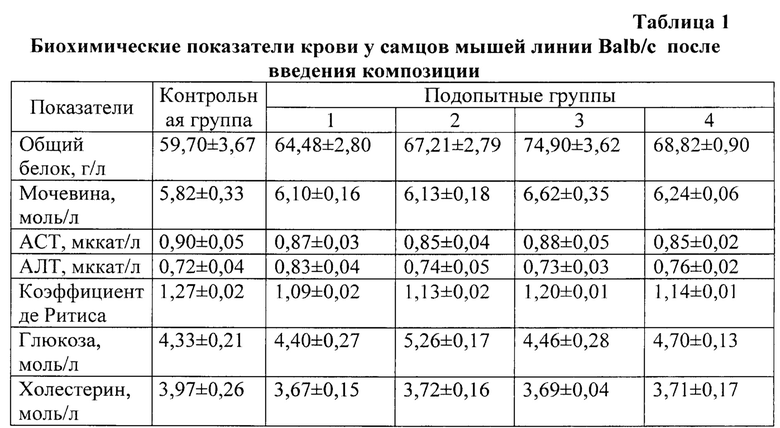
Таким образом, заявленная композиция оказывает благоприятное действие на мышей. У них после введения препарата прослеживается тенденция к улучшению морфологической картины и биохимического спектра крови, происходит уменьшение проявлений воспаления, повышается общая резистентность, улучшается обмен веществ и функциональное состояние печени. У самцов мышей линии Balb/c показатели гематологии и гемостаза за исключением 4-ой группы наблюдались на уровне нормы (таблица 2).
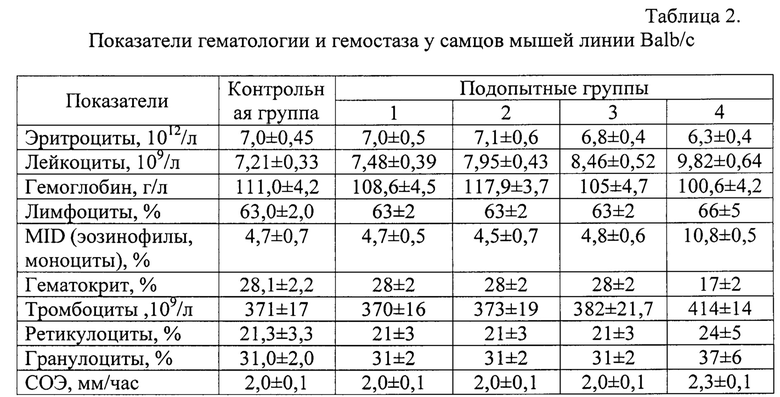
Вместе с тем в периферической крови подопытных животных статистически достоверно незначительно увеличилось число лейкоцитов, составляя для 1-, 2-, 3-, 4-й подопытных групп, соответственно, (7,48±0,39)⋅109 л, (7,95±0,43)⋅109 л, (8,46±0,52)⋅109 л, (9,82±0,64)⋅109 л, при норме (7,21±0,33)⋅109 л.
В результате введения заявленной композиции в диапазоне доз 3-6 г/кг гибели животных не выявлено. Максимально-переносимой дозой препарата в однократном опыте следует считать дозу - 6 г/кг массы тела. Клиническая картина интоксикации самцов мышей линии Balb/c не выражена. Все опытные животные были активны, подвижны, хорошо принимали корм и практически не отличались от контрольных животных. При проведении патологоанатомического вскрытия была отмечена незначительная гиперемия слизистой желудка у самцов мышей Balb/c после введения дозы 6 г/кг. Патанатомические изменения в печени, почках, сердце и селезенке не были выявлены.
Как видно, заявленная антибактериально-противогельминтозная фармацевтическая композиция для лечения сельскохозяйственных животных и птиц согласно классификации ГОСТ 12.1.007-76 относится к 4-му классу токсичности (малотоксичное соединение).
Пример 3. Изучение кумулятивных свойств композиции в подостром эксперименте.
С этой целью, композицию вводили 1/5 от максимально-введенной дозы (6 г/кг) в желудок самцов мышей линии Balb/c, т.е. ежедневно вводимая доза составляла 1,2 г/кг массы тела. Длительность опыта - 15 дней. Учитывали как материальную (гибель животных), так и функциональную кумуляцию.
График зависимости «доза-эффект» позволил определить смертельные дозы ЛД16 и ЛД84, которые составили 21,6 г/кг и 29,3 г/кг массы тела, соответственно.
Стандартную ошибку ЛД50п композиции «Азитропразифен» в условиях повторного введения определяли по формуле Гаддама, которая составила 25,47±1,62 г/кг массы тела.
Коэффициент кумуляции (Kcum) рассчитывали по отношению эффективных доз подострого и острого опытов.
Kcum составил 3,3, что, согласно классификации Ю.С. Кагана, позволяет отнести заявленный препарат к 3 классу опасности (умеренная кумуляция).
При изучении функциональной кумуляции проводили оценку массы тела, определяли суммационно-пороговый показатель (СПП), проводили анализ периферической крови (эритроциты, гемоглобин, лейкоциты), осуществляли оценку функционального состояния печени и почек, регистры некоторых поведенческих реакций у опытных животных.
Функциональное состояние центральной нервной системы оценивали по величине суммационно-порогового показателя. Нервно-мышечную возбудимость животных определяли с помощью электродов по сокращению межпальцевых мышц с увеличением подачи тока.
Для выявления функциональной кумуляции животных обследовали на 5, 10 и 15 дни опыта (при этом животные получили суммарные дозы - 8, 16 и 24 г/кг, соответственно). Как следует из результатов, у опытных животных с 10 дня эксперимента намечается тенденция к уменьшению массы тела, а на 15 день, после получения суммарной дозы 24 г/кг, отмечалось его снижение.
На том же сроке достоверно повышался суммационно-пороговый показатель (СПП), что свидетельствует о заторможенности животных.
На гематологическом анализаторе Celldyn определяли состояние периферической крови и оценивали количество эритроцитов, гемоглобина и лейкоцитов. Кроме того, использовали различные расчетные величины, отражающие физико-химические свойства эритроцитов, позволяющие количественно характеризовать показатели их состояния.
Результаты исследований свидетельствуют о том, что из показателей, характеризующих функциональное состояние периферической крови, было отмечено снижение количества гемоглобина (Р<0,05) на 15 - й день. Все остальные показатели крови у опытных животных не отличались от контроля и не выходили за границу физиологической нормы для данных показателей.
Результаты измерения ректальной температуры и некоторых поведенческих реакций самцов мышей линии Balb/c свидетельствуют о том, что на 1.5 - й день было отмечено и их достоверное снижение. Остальные показатели опытных животных не отличались от контрольных и не выходили за границу физионормы.
При изучении функционального состояния почек определяли удельный вес мочи, частоту диуреза, общий белок в моче и хлориды.
Результаты исследований показали, что у опытных самцов мышей линии Balb/c все показатели, характеризующие функциональное состояние почек, не отличаются от показателей контрольных животных на всем протяжении опыта.
Функциональное состояние печени оценивали по способности органа. синтезировать гиппуровую кислоту (обезвреживающая функция) и по содержанию в сыворотке крови общего белка.
Не менее важными для жизнедеятельности организма животных в целом, а также для оценки печени, является определение в сыворотке крови SH-групп, которые играют важную роль в образовании внутримолекулярных связей; в том числе -S-s-связи, которые, в первую очередь обеспечивают жесткое скрепление отдельных полипептидных цепей в иммуноглобулинах.
Как показали результаты, у опытных самцов мышей линии Balb/c на данном сроке выявлено достоверное уменьшение содержания в моче гиппуровой кислоты, что свидетельствует о снижении обезвреживающей функции печени. Все остальные показатели, характеризующие функцию печени, у животных, подвергавшихся повторному воздействию препарата в суммарной дозе, составляющей 24,0 г/кг, достоверно не отличались от контрольных величин.
При регистрации поведенческих реакций учитывали показатели динамической активности и статической работоспособности животных.
Динамическую активность определяли с помощью «вертикального» двигательного компонента, который основан на подсчете количества вставаний животных на задние лапы за 3 минуты. Имеются данные о высокой чувствительности данной реакции для самцов мышей линии Balb/c. Указанный метод может служить объективным показателем общего состояния животных.
Для оценки статической мышечной работоспособности применяли метод удерживания самцов мышей линии Balb/c на горизонтальном стержне. Учитывали длительность пребывания животного на стержне. Этот метод является наиболее простым и доступным для токсикологических исследований. Он не требует дорогостоящих приборов, и длительность его выполнения может быть учтена с достаточной точностью.
Анализ результатов опыта показывает, что количество вставаний животных на задние лапы за 3 мин снижается с 10-го по 15-й дни эксперимента, также в данный период времени становится короче и длительность пребывания животного на стержне.
После окончания опыта самцов мышей линии Balb/c убивали и определяли массовые коэффициенты внутренних органов. Массовые коэффициенты органов у животных опытной группы находились на одном уровне с контролем и достоверно от него не отличались, что свидетельствует о том, что этот показатель не является определяющим при воздействии композиции.
Таким образом, в условиях субхронического воздействия заявленная композиция вызывала достоверные изменения со стороны нервной системы, массы самцов мышей линии Balb/c, крови (снижение гемоглобина) и тенденцию к снижению поведенческих показателей. Это показывает, что препарат обладает незначительной как материальной, так и функциональной кумуляцией. Однако все изменения проявлялись только на уровне доз, в несколько раз больших, чем практические, и в условиях многократного введения. В связи со сказанным препарат не представляет реальной опасности в условиях лечения сельскохозяйственных животных и птицы.
Пример 4.
Эффективность лечения ассоциативных бактериально-гельминтозных болезней с помощью заявленной композиции.
Заявленная антибактериально-противогельминтозная фармацевтическая композиция была исследована с лечебной целью на телятах, жеребятах и ягнятах при желудочно-кишечных заболеваниях бактериально-гельминтозной этиологии, в том числе при ассоциациях био - и геогельминтозов с пастереллезом, колибактериозом, сальмонеллезом и микоплазмозом. Применяли композицию в смеси с комбикормом в соотношении 1:100, однократно. В результате проведения экспериментов установлено, что антибактериально-противогельминтозная фармацевтическая композиция обладает выраженной антимикробной и антигельминтной активностью. После назначения композиции физиологические и биохимические показатели крови нормализовались на 4-6 сутки. Например, у телят, которые получали заявленную композицию в дозе 0,5-0,6 г/ 10 кг массы тела, общее состояние улучшилось, и клиническая картина нормализовалась на 3-4 день после ее дачи. В результате испытаний установлено, что эффективными терапевтическими дозами композиции являются следующие (г/10 кг массы животного): телята и жеребята - 0,50, ягнята - 0,30.
Исследование морфобиохимических показателей крови животных опытных групп после применения заявленной композиции свидетельствует о ее хорошей переносимости и выраженном биологическом действии на организм животных. Так, в результате применения заявленного препарата в течение 5 дней увеличилось содержание эритроцитов, лейкоцитов и гемоглобина, нормализовались показатели кислотно-щелочного равновесия и общего белка в крови. Увеличение в крови подопытных животных количества эритроцитов указывает на активизацию окислительно-восстановительных процессов и на снижение токсических и воспалительных процессов, а также на улучшение дыхательной и токсико-выделительной функций организма на клеточном уровне. Результаты по изменению содержания в крови лейкоцитов свидетельствуют об усилении фагоцитарной активности, активизации защитных реакций организма. Увеличение общего белка в крови у подопытных животных указывает на нормализацию физиологического состояния, активизацию внутриклеточного метаболизма, на повышение уровня неспецифической иммунной резистентности, что свидетельствует о положительном влиянии фармацевтической композиции на морфологические показатели крови. Увеличение щелочного резерва крови свидетельствует о снижении процессов ацидоза и более высоком уровне окислительно-восстановительных процессов в организме. Указанные позитивные изменения, происходящие в организме, обеспечивают сокращение продолжительности лечения до 4-6 дней, а также способствуют более интенсивному росту подопытных животных.
Таким образом, получена безвредная и биобезопасная антибактериально-противогельминтозная фармацевтическая композиция для комплексного лечения и профилактики ассоциативных болезней сельскохозяйственных животных и птиц, которая:
- обладает повышенным лечебным и профилактическим эффектом при смешанных инфекто-инвазиях бактериальной и гельминтозной этиологии при снижении дозы АДВ (азитромицин, празиквантель и фенбендазол);
- положительно влияет на морфологические показатели крови;
- позволяет проводить лечение смешанных инфекто-инвазий до выделения этиотропных возбудителей и изучения их чувствительности к антибиотикам и антигельминтикам, но и сократить сроки и снизить трудоемкость лечения.
Получают антибактериально-противогельминтозную фармацевтическую композицию смешиванием всех ингредиентов в миксере-грануляторе при 300 об./мин. в течение 30 минут.
Входящие в состав композиции вспомогательные вещества бентонит (Герпегежского месторождения (влажность 10%), йодированная поваренная соль, патока, хелатная медь и медный купорос пролонгируют эффект азитромицина, празиквантела и фенбендазола, улучшают вкусовые свойства, активизируют обмен веществ. Эффективными терапевтическими дозами композиции являются следующие (г/10 кг массы животного): телята и жеребята - 0,50, ягнята - 0,30.
Источники информации
1. Государственный Реестр лекарственных средств 2005. 8 изд., Т. 2, М.: «Медицина», 2005, с. 1662-1663.
2. Машковский М.Д. Лекарственные средства / М.Д. Машковский. Изд. 15-е М.: "Новая волна", 2005 г. с. 803-804, 807-808, 847-848.
3. Энциклопедия лекарств, 12-е изд., М.: ООО «РЛС-2005», 2004 г., с. 154-155.
4. Кленова И.Ф., Мальцев К.Л., Яременко Н.А., Архипов И.А. Ветеринарные препараты в России. М.: Сельхозиздат, 2004. Т. 1. С. 367-384.
5. Patent №2571543 US "Препарат для лечения гельминтозов животных".
6. Patent №2570389 US "Антибактериальная фармацевтическая композиция для лечения сельскохозяйственных животных и птиц".
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЙ АНТГЕЛЬМИНТНЫЙ ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ОСТЕРТАГИОЗА КРУПНОГО И МЕЛКОГО РОГАТОГО СКОТА | 2016 |
|
RU2608132C1 |
| СПОСОБ ГРУППОВОЙ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ АССОЦИИРОВАННЫХ ТРЕМАТОДОЗОВ, ЦЕСТОДОЗОВ И НЕМАТОДОЗОВ КРУПНОГО РОГАТОГО СКОТА | 2021 |
|
RU2778233C1 |
| Универсальное средство в виде мази для комплексного лечения глазных болезней животных и способ его получения | 2017 |
|
RU2667118C1 |
| ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ ГЕЛЬМИНТОЗОВ ЖИВОТНЫХ | 2014 |
|
RU2571543C1 |
| КОМПЛЕКСНЫЙ ПРОТИВОПАРАЗИТАРНЫЙ СОСТАВ "АЗИНАЛ ПЛЮС" - 3 ДЛЯ ХИМИОТЕРАПИИ И ПРОФИЛАКТИКИ ТРИХОЦЕФАЛЕЗА, АНКИЛОСТОМОЗА И ЭХИНОКОККОЗА СОБАК | 2015 |
|
RU2614711C2 |
| АНТИГЕЛЬМИНТНОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ДЕЛАФОНДИОЗА, АЛЬФОРТИОЗА, ОКСИУРОЗА, СТРОНГИЛЕЗА И ТРИХОНЕМАТИДОЗОВ ЛОШАДЕЙ | 2016 |
|
RU2629203C2 |
| Композиция на основе R(-)-празиквантела для лечения и профилактики гельминтозов у теплокровных | 2015 |
|
RU2613490C2 |
| КОМПЛЕКСНЫЙ АНТИГЕЛЬМИНТНЫЙ ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ СТРОНГИЛЯТОЗОВ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА ЛОШАДЕЙ | 2016 |
|
RU2629318C2 |
| СПОСОБ ПРОИЗВОДСТВА КОМБИНИРОВАННОЙ АНТИГЕЛЬМИНТНОЙ ТАБЛЕТКИ С СИМБИОТИКОМ ДЛЯ ЛЕЧЕНИЯ МЕЛКОГО РОГАТОГО СКОТА | 2016 |
|
RU2627893C1 |
| АНТГЕЛЬМИНТНОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ФАСЦИОЛЕЗА, ДИКРОЦЕЛИОЗА И ПАРАМФИСТОМАТОЗА КРУПНОГО РОГАТОГО СКОТА | 2016 |
|
RU2612013C1 |
Изобретение относится к области медицины, а именно к ветеринарии, и предназначено для лечения заболеваний смешанной бактериальной и гельминтозной этиологии у сельскохозяйственных животных и птиц. Комплексная антибактериально-противогельминтозная композиция содержит азитромицин, празиквантел, фенбендазол, бентонит, йодированную поваренную соль, патоку, хелатную медь и медный купорос. Компоненты применяют в заявленных количествах. Использование изобретения позволяет повысить эффективность лечения заболеваний смешанной бактериальной и гельминтозной этиологии до выделения этиотропного возбудителя и изучения его чувствительности к антибиотикам, сократить сроки и снизить трудоемкость лечения. 2 табл., 4 пр.
Комплексная антибактериально-противогельминтозная композиция для лечения сельскохозяйственных животных и птиц, содержащая азитромицин, празиквантель, фенбендазол, характеризующаяся тем, что дополнительно содержит вспомогательные вещества: бентонит, йодированную поваренную соль, патоку, хелатную медь, медный купорос при соотношении в мг/г порошка:
| ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ ГЕЛЬМИНТОЗОВ ЖИВОТНЫХ | 2014 |
|
RU2571543C1 |
| АНТИБАКТЕРИАЛЬНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ И ПТИЦ | 2015 |
|
RU2570389C1 |
| ПРЕПАРАТ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ГЕЛЬМИНТОЗОВ ЛОШАДЕЙ | 2005 |
|
RU2279874C1 |
| АНТИГЕЛЬМИНТНОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ДЕЛАФОНДИОЗА, АЛЬФОРТИОЗА, ОКСИУРОЗА, СТРОНГИЛЕЗА И ТРИХОНЕМАТИДОЗОВ ЛОШАДЕЙ | 2016 |
|
RU2629203C2 |
| Способ вязки веретенных шнурков на ватерах | 1930 |
|
SU26947A1 |
Авторы
Даты
2018-12-28—Публикация
2017-12-26—Подача