Область техники
Изобретение относится к специфическим связывающим агентам против белка B7-H1 и к применению таких агентов. В некоторых вариантах воплощения изобретение относится к полностью человеческим моноклональным антителам, направленным на B7-H1, и к применению таких антител. Аспекты изобретения также относятся к клеточным линиям, экспрессирующим такие специфические связывающие агенты или антитела. Описанные специфические связывающие агенты пригодны для использования в качестве диагностических средств и для лечения болезней, ассоциированных с активностью и/или экспрессией B7-H1.
Уровень техники
Адаптивный иммунный ответ включает активацию, селекцию и клональную пролиферацию двух основных классов лимфоцитов, названных T-клетками и B-клетками. После встречи с антигеном T-клетки пролиферируют и дифференцируют в антигенспецифические эффекторные клетки, в то время как B-клетки пролиферируют и дифференцируют в антителосекретирующие клетки. Активация T-клетки представляет собой многостадийный процесс, требующий нескольких сигнальных событий между T-клеткой и антигенпрезентирующей клеткой (APC) (АГК). Для активации T-клетки к покоящейся T-клетке должны быть доставлены два типа сигналов. Первый тип медиируется рецептором антигенспецифической T-клетки (TcR) (ТкР), и придает иммунному ответу специфичность. Второй, костимулирующий, тип регулирует величину ответа и доставляется через вспомогательные рецепторы на T-клетке.
Первичный костимулирующий сигнал доставляется путем активации рецептора CD28 при связывании его лигандов B7-1 или B7-2. В отличие от этого, связывание ингибирующего рецептора CTLA-4 этими же лигандами B7-1 или B7-2 приводит к ослаблению T-клеточного ответа. Таким образом, сигналы CTLA-4 антагонизируют костимуляцию, медиируемую CD28. При высоких концентрациях антигена костимуляция CD28 преобладает над ингибирующим эффектом CTLA-4. Временная регуляция экспрессии CD28 и CTLA-4 поддерживает баланс между активирующими и ингибирующими сигналами и обеспечивает развитие эффективного иммунного ответа, предотвращая в то же время развитие аутоиммунитета.
В последнее время были идентифицированы молекулярные гомологи CD28 и CTLA-4 и их B-7-подобные лиганды. ICOS представляет собой CD28-подобный костимулирующий рецептор. Рецептор PD-1 (запрограммированной смерти 1) является ингибирующим рецептором и партнером CTLA-4. Данное изобретение относится к модуляции иммунных ответов, медиируемых B7-H1.
B7-H1, также известный как PD-L1, представляет собой трансмембранный белок типа I размером приблизительно 53 кДа. У людей B7-H1 экспрессируется на ряде типов иммунных клеток, включая активированные и анергичные/истощенные T-клетки, на наивных и активированных B-клетках, а также на миелоидных дендритных клетках (DC), моноцитах и мастоцитах. Он также экспрессируется на неиммунных клетках, включая панкреатические островки, клетки Купфера в печени, сосудистый эндотелий и избранный эпителий, например, эпителий дыхательных путей и эпителий почечных канальцев, где его экспрессия усиливается во время воспалительных эпизодов. Повышенные уровни экспрессии B7-H1 были также обнаружены на ряде опухолей, включая, без ограничений, опухоли молочной железы, ободочной кишки, колоректальные, легкого, почки, включая почечно-клеточную карциному, желудка, мочевого пузыря, немелкоклеточный рак легкого (NSCLC), гепатоцеллюлярную карциному (HCC) и рак поджелудочной железы, а также меланому.
B7-H1 является членом семейства белков B7, которые включают два внеклеточных Ig-домена, один N-концевой домен V-типа, за которым следует домен C-типа. Внутриклеточный домен длиной 30 аминокислот не содержит явных сигнальных мотивов, но несет потенциальный сайт фосфорилирования протеинкиназы C. Мышиная форма B7-H1 имеет 69% идентичности аминокислотных последовательностей с человеческой формой B7-H1, а также общую с ней консервативную структуру.
Известно, что B7-H1 связывает два альтернативных лиганда, первый из которых, PD-1, представляет собой 50-55 кДа трансмембранный рецептор типа I, который был первоначально идентифицирован в T-клеточной линии, подвергнутой индуцируемому активацией апоптозу. PD-1 экспрессируется на активированных T-клетках, B-клетках и моноцитах, а также других клетках иммунной системы, и связывает как B7-H1 (PD-L1), так и родственный B7-DC (PD-L2). Вторым является B7-1, член семейства B7, который экспрессируется на активированных T-клетках, B-клетках, моноцитах и антигенпрезентирующих клетках.
PD-1 является членом суперсемейства иммуноглобулинов (Ig), содержащим один V-подобный домен Ig в своей внеклеточной области. Цитоплазматический домен PD-1 содержит два тирозина, причем проксимальный по отношению к мембране тирозин (VAYEEL в мышином PD-1) расположен в ITIM (иммунорецепторный тирозиновый ингибирующий мотив). Присутствие ITIM на PD-1 указывает, что эта молекула функционирует, ослабляя сигналы антигенного рецептора путем рекрутмента цитоплазматических фосфатаз. Человеческие и мышиные белки PD-1 имеют примерно 60% идентичности аминокислотных последовательностей, с сохранением четырех потенциальных сайтов N-гликозилирования и остатков, образующих домен Ig-V. ITIM в цитоплазматической области и ITIM-подобный мотив, окружающие карбоксиконцевой тирозин (TEYATI у человека и мыши), также остаются консервативными в человеческих и мышиных ортологах.
Считается, что сигнализация по оси PD-1/B7-H1 выполняет в иммунной системе критические, незарезервированные функции, негативно регулируя T-клеточные ответы. Эта регуляция участвует в развитии T-клеток в тимусе, в регуляции хронических воспалительных ответов и в поддержании как периферической толерантности, так и иммунной привилегии. Критический характер этих функций продемонстрирован на примере PD-1-дефицитных мышей, которые проявляют аутоиммунный фенотип. Дефицит PD-1 у C57BL/6 мышей приводит к хроническому прогрессирующему волчаночному гломерулонефриту и артриту. У мышей Balb/c дефицит PD-1 приводит к тяжелой кардиомиопатии вследствие присутствия специфических к сердечным тканям аутореактивных антител. Функция сигнализации B7-H1/B7-1 менее понятна, но считается, что она также принимает участие в передаче негативных регуляторных сигналов как к T-клеткам, так и к антигенпрезентирующим клеткам.
Считается, что экспрессия B7-H1 на опухолевых клетках помогает опухолям избегать обнаружения и уничтожения иммунной системой. B7-H1 функционирует в этом отношении по нескольким альтернативным механизмам, включая стимуляцию истощения и анергии инфильтрующих опухоль T-лимфоцитов, стимуляцию секреции иммуннорепрессивных цитокинов в микроокружение опухоли, стимуляцию репрессорной функции регуляторных T-клеток и защиту экспрессирующих B7-H1 опухолевых клеток от лизиса специфическими к опухолевым клеткам цитотоксическими T-клетками.
В общем, существует потребность в создании безопасных и эффективных терапевтических способов лечения расстройств, ассоциированных с репрессией иммунного ответа, таких как, например, рак и хронические вирусные инфекции. Модуляция иммунных ответов, задействованных в этих расстройствах, может быть осуществлена путем проведения манипуляций с проводящим путем B7-H1/PD-1.
Сущность изобретения
Настоящее изобретение относится к специфическим связывающим агентам, которые специфически связываются с B7-H1 и ингибируют биологическую активность B7-H1. В одном варианте воплощения изобретение относится к специфическим связывающим агентам, которые специфически связываются с B7-H1 и тем самым ингибируют активность B7-H1. В другом варианте воплощения изобретения оно относится к специфическим связывающим агентам, которые специфически связываются с B7-H1 и тем самым ингибируют связывание B7-H1 с PD-1. В еще одном варианте воплощения изобретение относится к специфическим связывающим агентам, которые блокируют индуцируемую B7-H1 супрессию T-клеток и тем самым усиливают противоопухолевый иммунитет. В еще одном варианте воплощения изобретения оно дополнительно относится к специфическим связывающим агентам, которые могут дополнительно стимулировать одну или несколько из следующих активностей, включая пролиферацию T-клеток, секрецию IFN-γ и/или IL-2 в смешанных лимфоцитарных реакциях. Варианты воплощения изобретения относятся к специфическим связывающим агентам, которые специфически связываются с B7-H1 и ингибируют биологическую активность B7-H1. В одном варианте воплощения изобретения специфический связывающий агент ингибирует по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 15%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 35%, по меньшей мере 40%, по меньшей мере 45%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% биологической активности, которая наблюдалась бы в отсутствие специфического связывающего агента.
Варианты воплощения изобретения относятся к специфическим связывающим агентам, которые специфически связываются с B7-H1 и тем самым ингибируют активность B7-H1. В одном варианте воплощения изобретения специфический связывающий агент ингибирует по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 15%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 35%, по меньшей мере 40%, по меньшей мере 45%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% активности B7-H1, которая наблюдалась бы в отсутствие специфического связывающего агента.
Варианты воплощения изобретения относятся к специфическим связывающим агентам, которые специфически связываются с B7-H1 и тем самым ингибируют связывание с PD-1. В одном варианте воплощения изобретения специфический связывающий агент ингибирует по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 15%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 35%, по меньшей мере 40%, по меньшей мере 45%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% связывания лиганда рецептором B7-H1/PD-1 по сравнению с тем, которое наблюдалось бы в отсутствие специфического связывающего агента.
В другом варианте воплощения специфические связывающие агенты по изобретению могут ингибировать связывание PD-1/Fc с человеческим B7-H1, экспрессируемым на клетках ES-2. В одном варианте воплощения специфический связывающий агент ингибирует связывание с IC50 менее 1 нМ, 0,5 нМ, 0,4, 0,3, 0,2, 0,1, 0,09, 0,08, 0,07 или 0,06 нМ. Дополнительно, в другом варианте воплощения, антитела по изобретению имеют IC50, равный от примерно 1 нМ до примерно 0,06 нМ; или от примерно 0,5 нМ до примерно 0,06 нМ; или от примерно 0,1 нМ до примерно 0,06 нМ; или от примерно 1 нМ до примерно 0,1 нМ; или от примерно 1 нМ до примерно 0,5 нМ.
Варианты воплощения изобретения относятся к специфическим связывающим агентам, которые специфически связываются с B7-H1 и тем самым ингибируют связывание с его лигандом B7-1. В одном варианте воплощения специфический связывающий агент ингибирует, по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 15%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 35%, по меньшей мере 40%, по меньшей мере 45%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, 95%, 96%, 97%, 98%, 99% или 100% связывания лиганда рецептором B7-H1/B7-1 по сравнению с тем, которое наблюдалось бы в отсутствие специфического связывающего агента.
Варианты воплощения изобретения относятся к специфическим связывающим агентам, которые специфически связываются с B7-H1 и ингибируют индуцируемую B7-H1 пролиферацию опухоли. В одном варианте воплощения специфический связывающий агент ингибирует по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 15%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 35%, по меньшей мере 40%, по меньшей мере 45%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% от индуцируемой B7-H1 пролиферации опухоли, которая наблюдалась бы в отсутствие специфического связывающего агента.
Дополнительные варианты воплощения изобретения относятся к специфическим связывающим агентам, которые специфически связываются с B7-H1 и тем самым ингибируют индуцируемое B7-H1 выживание опухолевых клеток. В одном варианте воплощения специфический связывающий агент ингибирует по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 15%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 35%, по меньшей мере 40%, по меньшей мере 45%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% индуцируемого B7-H1 выживания опухолевых клеток, которое наблюдалась бы в отсутствие специфического связывающего агента.
Дополнительные варианты воплощения изобретения относятся к специфическим связывающим агентам, которые специфически связываются с B7-H1 и тем самым ингибируют рост опухоли раковых клеточных линий A375 или HPAC. В одном варианте воплощения специфический связывающий агент ингибирует по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 15%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 35%, по меньшей мере 40%, по меньшей мере 45%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% роста раковых клеток в день 30 по сравнению с изотипическим контролем.
Дополнительные варианты воплощения изобретения относятся к специфическим связывающим агентам, которые специфически связываются с B7-H1 и тем самым ингибируют медиируемую B7-H1 супрессию опухолевореактивных T-клеток, тем самым усиливая противоопухолевую цитолитическую активность T-клеток. В одном варианте воплощения специфический связывающий агент ингибирует по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 15%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 35%, по меньшей мере 40%, по меньшей мере 45%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% медиируемой B7-H1 супрессии опухолевореактивной T-клеточной активности, которая наблюдалась бы в отсутствие специфического связывающего агента.
Дополнительные варианты воплощения изобретения относятся к специфическим связывающим агентам, которые специфически связываются с B7-H1 и тем самым усиливают противоопухолевый иммунитет. В одном варианте воплощения специфический связывающий агент повышает на по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 15%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 35%, по меньшей мере 40%, по меньшей мере 45%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% противоопухолевый иммунитет, который наблюдался бы в отсутствие специфического связывающего агента.
Дополнительные варианты воплощения изобретения относятся к специфическим связывающим агентам, которые специфически связываются с B7-H1 и тем самым ингибируют пролиферацию клеток. В одном варианте воплощения специфический связывающий агент ингибирует по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 15%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 35%, по меньшей мере 40%, по меньшей мере 45%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% пролиферации клеток, которая наблюдалась бы в отсутствие специфического связывающего агента.
Дополнительные варианты воплощения изобретения относятся к специфическим связывающим агентам, которые специфически связываются с B7-H1 и усиливают специфическую цитолитическую (CTL) активность против опухолевых клеток, экспрессирующих B7-H1. В одном варианте воплощения антитела по изобретению имеют величину EC50, меньшую или равную 100 нМ, 50 нМ или 1 нМ. Дополнительно, в другом варианте воплощения, антитела по изобретению имеют величину EC50, составляющую от примерно 100 нМ до примерно 1 нМ; или от примерно 50 нМ до примерно 1 нМ; или от примерно 20 нМ до примерно 1 нМ; или от примерно 100 нМ до примерно 50 нМ; или от примерно 100 нМ до примерно 70 нМ.
Дополнительные варианты воплощения изобретения относятся к специфическим связывающим агентам, которые специфически связываются с B7-H1 и ингибируют медиируемую B7-H1 супрессию пролиферации T-клеток при величине EC50, меньшей или равной 100 нМ. В одном варианте воплощения антитела по изобретению имеют величину EC50, меньшую или равную 100 нМ, например, 90, 80, 70, 60, 50, 40, 30, 20 или 10 нМ. Дополнительно, в другом варианте воплощения, антитела по изобретению имеют величину EC50, составляющую от примерно 100 нМ до примерно 10 нМ; или от примерно 50 нМ до примерно 10 нМ; или от примерно 20 нМ до примерно 10 нМ; или от примерно 100 нМ до примерно 50 нМ; или от примерно 100 нМ до примерно 70 нМ; или от примерно 100 нМ до примерно 80 нМ.
Специфические связывающие агенты также ингибируют адгезию, подвижность, инвазию опухолевых клеток и клеточные метастазы, и, в дополнение к этому, специфические связывающие агенты пригодны для уменьшения роста опухоли. Механизмы, по которым это может быть достигнуто, могут включать, без ограничений, ингибирование активности B7-H1.
В одном варианте воплощения изобретения специфический связывающий агент представляет собой антитело. В одном варианте воплощения изобретения специфический связывающий агент представляет собой моноклональное антитело. В одном варианте воплощения изобретения специфический связывающий агент представляет собой полностью человеческое моноклональное антитело или его фрагмент. Такие моноклональные антитела могут быть названы здесь анти-B7-H1 антителами или антителами по изобретению.
Антитела, моноклональные антитела и человеческие моноклональные антитела включают антитела изотипов IgG1, IgG2, IgG3 и IgG4, например, IgG2. В одном варианте воплощения изобретения специфический связывающий агент представляет собой полностью человеческое моноклональное антитело изотипа IgG2. Этот изотип обладает пониженным потенциалом возбуждения эффекторной функции по сравнению с другими изотипами, что может приводить к пониженной токсичности. В другом варианте воплощения изобретения специфический связывающий агент представляет собой полностью человеческое моноклональное антитело изотипа IgG1. Изотип IgG1 обладает повышенным потенциалом возбуждения опосредованной антителами клеточной цитотоксичности (ADCC) по сравнению с другими изотипами, что может приводить к повышенной эффективности. Изотип IgG1 обладает повышенной стабильностью по сравнению с другими изотипами, например, IgG4, что может приводить к улучшенной биодоступности/простоте производства/большего периода полувыведения. В одном варианте воплощения полностью человеческое моноклональное антитело изотипа IgG1 принадлежит к аллотипу z, za или f. В одном варианте воплощения изобретения специфический связывающий агент обладает желательными терапевтическими свойствами, выбранными из одного или нескольких из следующего: высокая аффинность связывания с B7-H1, способность ингибировать активность B7-H1 in vitro и in vivo, способность ингибировать медиируемое B7-H1 выживание опухолевых клеток, и способность ингибировать медиируемую B7-H1 супрессию опухолевореактивных T-клеток, что может, в свою очередь, уменьшить пролиферацию, подвижность, инвазивность, метастазирование опухолевых клеток и рост опухоли.
В одном варианте воплощения изобретение включает антитела, которые специфически связываются с B7-H1 с очень высокими аффинностями (Kd). В некоторых вариантах воплощения изобретения специфический связывающий агент связывает B7-H1 с аффинностью связывания (Kd) менее 5 наномоль (нМ). В других вариантах воплощения специфический связывающий агент связывается с величиной Kd менее 4 нМ, 3 нМ, 2,5 нМ, 2 нМ или 1 нМ. Дополнительно, в некоторых других вариантах воплощения антитела по изобретению связывают B7-H1 с величиной Kd, равной от примерно 5 нМ до примерно 1 нМ; или от примерно 5 нМ до примерно 2 нМ; или от примерно 5 нМ до примерно 3 нМ; или от примерно 5 нМ до примерно 4 нМ; или от примерно 3 нМ до примерно 1 нМ; или от примерно 2 нМ до примерно 1 нМ. В некоторых вариантах воплощения изобретения специфический связывающий агент связывает B7-H1 с величиной Kd менее 950 пикомоль (пМ). В некоторых вариантах воплощения изобретения специфический связывающий агент связывает B7-H1 с величиной Kd менее 900 пМ. В других вариантах воплощения специфический связывающий агент связывает B7-H1 с величиной Kd менее 800 пМ, 700 пМ или 600 пМ. В некоторых вариантах воплощения изобретения специфический связывающий агент связывает B7-H1 с величиной Kd менее 500 пМ. В других вариантах воплощения специфический связывающий агент связывает B7-H1 с величиной Kd менее 400 пМ. В еще одних вариантах воплощения специфический связывающий агент связывает B7-H1 с величиной Kd менее 300 пМ. В некоторых других вариантах воплощения специфический связывающий агент связывает B7-H1 с величиной Kd менее 200 пМ. В некоторых других вариантах воплощения специфический связывающий агент связывает B7-H1 с величиной Kd менее 100 пМ. Дополнительно, в некоторых других вариантах воплощения антитела по изобретению связывает B7-H1 с величиной Kd, равной от примерно 900 пМ до примерно 100 пМ; или от примерно 900 пМ до примерно 200 пМ; или от примерно 900 пМ до примерно 300 пМ; или от примерно 900 пМ до примерно 400 пМ; или от примерно 900 пМ до примерно 500 пМ; или от примерно 900 пМ до примерно 600 пМ; или от примерно 900 пМ до примерно 700 пМ; или от примерно 200 пМ до примерно 100 пМ; или от примерно 300 пМ до примерно 200 пМ; или от примерно 400 пМ до примерно 300 пМ. В некоторых других вариантах воплощения специфический связывающий агент связывает B7-H1 с величиной Kd менее 90 пМ, 80 пМ, 70 пМ, 60 пМ, 55 пМ или 50 пМ. В некоторых других вариантах воплощения специфический связывающий агент связывает B7-H1 с величиной Kd менее 60 пМ. В некоторых других вариантах воплощения специфический связывающий агент связывает B7-H1 с величиной Kd менее 55 пМ. Дополнительно, в некоторых других вариантах воплощения антитела по изобретению связывает B7-H1 с величиной Kd, равной от примерно 100 пМ до примерно 50 пМ; или от примерно 100 пМ до примерно 70 пМ; или от примерно 100 пМ до примерно 80 пМ; или от примерно 100 пМ до примерно 90 пМ; или от примерно 70 пМ до примерно 50 пМ; или от примерно 60 пМ до примерно 50 пМ; или от примерно 55 пМ до примерно 50 пМ. Величину Kd можно оценить с помощью метода, описанного здесь или известного квалифицированному специалисту (например, анализ BIAcore, ELISA) (Biacore International AB, Uppsala, Sweden). Специфические связывающие агенты по изобретению имеют значительно улучшенные аффинности связывания B7-H1 по сравнению с антителами, описанными в предшествующем уровне техники.
Связывающие свойства специфического связывающего агента или антитела по изобретению также могут быть измерены путем сопоставления со скоростями диссоциации или ассоциации (koff и kon, соответственно).
В одном варианте воплощения изобретения специфический связывающий агент или антитело по изобретению может иметь константу скорости kon (антитело (Ab) + антиген (Ag)kon→Ab-Ag), равную по меньшей мере 104 М-1с-1, по меньшей мере 5×104 М-1с-1, по меньшей мере 105 М-1с-1, по меньшей мере 2×105 М-1с-1, по меньшей мере 5×105 М-1с-1, по меньшей мере 106 М-1с-1, по меньшей мере 5×106 М-1с-1, по меньшей мере 107 М-1с-1, по меньшей мере 5×107 М-1с-1 или по меньшей мере 108 М-1с-1 при измерении методом анализа BIAcore. Дополнительно, в некоторых других вариантах воплощения, антитела по изобретению имеют константу скорости kon, равную от примерно 5×104 М-1с-1 до примерно 5×108 М-1с-1; или от примерно 5×105 М-1с-1 до примерно 5×108 М-1с-1; или от примерно 5×106 М-1с-1 до примерно 5×108 М-1с-1; или от примерно 5×107 М-1с-1 до примерно 5×108 М-1с-1, при измерении методом анализа BIAcore.
В другом варианте воплощения изобретения специфический связывающий агент или антитело может иметь константу скорости koff ((Ab-Ag)koff(→антитело (Ab) + антиген (Ag)) менее 5×10-1 с-1, менее 10-1 с-1, менее 5×10-2 с-1, менее 10-2 с-1, менее 5×10-3 с-1, менее 10-3 с-1, менее 5×10-4 с-1, менее 10-4 с-1, менее 5×10-5 с-1, менее 10-5 с-1, менее 5×10-6 с-1, менее 10-6 с-1, менее 5×10-7 с-1, менее 10-7 с-1, менее 5×10-8 с-1, менее 10-8 с-1, менее 5×10-9 с-1, менее 10-9 с-1 или менее 10-10 с-1 при измерении методом анализа BIAcore. Дополнительно, в некоторых других вариантах воплощения, антитела по изобретению имеют константу скорости koff, равную от примерно 1×10-4 с-1 до примерно 1×10-5 с-1; или от примерно 1×10-4 с-1 до примерно 5×10-4 с-1, при измерении методом анализа BIAcore.
Специфический связывающий агент по изобретению специфически связывает человеческий B7-H1. В некоторых примерах специфический связывающий агент по изобретению не связывает другие иммунные комодулирующие белки, например, человеческий PD-L2, человеческий B7-H2, человеческий B7-H3, человеческий CD28, человеческий CTLA-4 и человеческий PD1.
В другом варианте воплощения специфический связывающий агент по изобретению является кросс-реактивным с другими белками B7-H1 от других видов. В одном варианте воплощения специфический связывающий агент по изобретению является кросс-реактивным с B7-H1 яванского макака (cynomolgus monkey). В другом варианте воплощения специфический связывающий агент по изобретению является кросс-реактивным с мышиным B7-H1, например, 2.7A4. В другом варианте воплощения специфический связывающий агент по изобретению является кросс-реактивным с B7-H1 яванского макака и с мышиным B7-H1, например, 2.7A4. В другом варианте воплощения специфический связывающий агент по изобретению является кросс-реактивным с B7-H1 яванского макака, но не с мышиным B7-H1, например, 2.9D10 и 2.14H9.
В одном варианте воплощения специфический связывающий агент или антитело включает последовательность, содержащую любую из последовательностей тяжелых цепей (VH), приведенных в Таблице 8. В другом варианте воплощения специфический связывающий агент или антитело включает последовательность, содержащую любую из последовательностей тяжелых цепей антител 2.9D10, 2.7A4, 2.14H9, 3.15G8, 2.20A8, 3.18G1, 2.7A4OPT или 2.14H9OPT. Способность легкой цепи к образованию случайных связей (promiscuity) хорошо известна специалистам, и, таким образом, специфический связывающий агент или антитело, включающие последовательность, содержащую любую из последовательностей тяжелых цепей антител 2.9D10, 2.7A4, 2.14H9, 3.15G8, 2.20A8, 3.18G1, 2.7A4OPT или 2.14H9OPT или другого антитела, раскрытого здесь, может дополнительно включать любую из последовательностей легких цепей (VL), приведенных в Таблице 9, или антител 2.9D10, 2.7A4, 2.14H9, 3.15G8, 2.20A8, 3.18G1, 2.7A4OPT или 2.14H9OPT или другого антитела, раскрытого здесь. В другом варианте воплощения специфический связывающий агент или антитело включает последовательность, содержащую любую из последовательностей тяжелых цепей антител 2.9D10, 2.7A4, 2.14H9, 3.15G8, 2.20A8, 3.18G1, 2.7A4OPT или 2.14H9OPT, и дополнительно включает соответствующую последовательность легкой цепи антитела 2.9D10, 2.7A4, 2.14H9, 3.15G8, 2.20A8, 3.18G1, 2.7A4OPT или 2.14H9OPT. В некоторых вариантах воплощения антитело представляет собой полностью человеческое моноклональное антитело.
В одном варианте воплощения специфический связывающий агент или антитело включает последовательность, содержащую любую из последовательностей легких цепей, приведенных в Таблице 9. В другом варианте воплощения специфический связывающий агент или антитело включает последовательность, содержащую любую из последовательностей легких цепей антител 2.9D10, 2.7A4, 2.14H9, 3.15G8, 2.20A8, 3.18G1, 2.7A4OPT или 2.14H9OPT. В некоторых вариантах воплощения антитело представляет собой полностью человеческое моноклональное антитело.
В другом варианте воплощения специфический связывающий агент или антитело включает последовательность, содержащую любую из последовательностей тяжелых цепей антитела 2.7A4, и дополнительно включает последовательность легкой цепи антитела 2.7A4. В другом варианте воплощения специфический связывающий агент или антитело включает последовательность, содержащую любую из последовательностей тяжелых цепей антитела 2.14H9, и дополнительно включает последовательность легкой цепи антитела 2.14H9. В другом варианте воплощения специфический связывающий агент или антитело включает последовательность, содержащую любую из последовательностей тяжелых цепей антитела 2.9D10, и дополнительно включает последовательность легкой цепи антитела 2.9D10. В другом варианте воплощения специфический связывающий агент или антитело включает последовательность, содержащую любую из последовательностей тяжелых цепей антитела 2.7A.4OPT, и дополнительно включает последовательность легкой цепи антитела 2.7A.4OPT. В другом варианте воплощения специфический связывающий агент или антитело включает последовательность, содержащую любую из последовательностей тяжелых цепей антитела 2.14H9OPT, и дополнительно включает последовательность легкой цепи антитела 2.14H9OPT.
В некоторых вариантах воплощения специфический связывающий агент представляет собой любое из моноклональных антител, приведенных в Таблице 1. В некоторых вариантах воплощения специфический связывающий агент представляет собой моноклональное антитело, выбранное из группы, состоящей из 2.7A4, 2.14H9, 2.9D10, 2.7A4OPT или 2.14H9OPT. В одном варианте воплощения специфический связывающий агент включает однл или несколько полностью человеческих моноклональных антител 2.7A4, 2.14H9, 2.9D10, 2.7A4OPT или 2.14H9OPT. В определенных вариантах воплощения специфический связывающий агент представляет собой моноклональное антитело 2.7A4. В определенных других вариантах воплощения специфический связывающий агент представляет собой моноклональное антитело 2.14H9. В еще одних вариантах воплощения специфический связывающий агент представляет собой моноклональное антитело 2.9D10. В определенных вариантах воплощения специфический связывающий агент представляет собой моноклональное антитело 2.7A4OPT. В определенных других вариантах воплощения специфический связывающий агент представляет собой моноклональное антитело 2.14H9OPT. В дополнительных вариантах воплощения специфический связывающий агент является производным от любого из вышеописанных моноклональных антител.
В другом варианте воплощения специфический связывающий агент может включать последовательность, содержащую любой из CDR1, CDR2 или CDR3 вариабельных последовательностей тяжелой цепи, кодируемых полинуклеотидом в плазмиде, обозначенной 2.7A4_G, 2.14H9_G, и 2.9D10_NG, которые были депонированы в NCIMB под номером 41598 19 ноября 2008 года, под номером 41597 19 ноября 2008 года и под номером 41599 19 ноября 2008 года, соответственно.
В другом варианте воплощения специфический связывающий агент может включать последовательность, содержащую любой из CDR1, CDR2 или CDR3 последовательностей вариабельного домена легкой цепи, кодируемых полинуклеотидом в плазмиде, обозначенной 2.7A4_G, 2.14H9_G и 2.9D10_NG, которые были депонированы под номером 41598 19 ноября 2008 года, под номером 41597 19 ноября 2008 года, или под номером 41599 19 ноября 2008 года, соответственно.
В одном варианте воплощения специфический связывающий агент или антитело по изобретению включают аминокислотную последовательность вариабельного домена тяжелой цепи, содержащую CDR3, кодируемый полинуклеотидом в плазмиде, обозначенной 2.7A4_G, которая была депонирована в NCIMB под депозитарным номером 41598 19 ноября 2008 года, и аминокислотную последовательность вариабельного домена легкой цепи, содержащую CDR3, кодируемый полинуклеотидом в плазмиде, обозначенной 2.7A4_G, которая была депонирована в NCIMB под депозитарным номером 41598 19 ноября 2008 года.
В другом варианте воплощения специфический связывающий агент или антитело по изобретению включают аминокислотную последовательность вариабельного домена тяжелой цепи, содержащую, по меньшей мере, один, по меньшей мере, два или, по меньшей мере, три CDR антитела, кодируемых полинуклеотидом в плазмиде, обозначенной 2.7A4_G, которая была депонирована в NCIMB под депозитарным номером 41598 19 ноября 2008 года.
В другом варианте воплощения специфический связывающий агент или антитело по изобретению включают аминокислотную последовательность вариабельного домена легкой цепи, содержащую, по меньшей мере, один, по меньшей мере, два или, по меньшей мере, три CDR антитела, кодируемых полинуклеотидом в плазмиде, обозначенной 2.7A4_G, которая была депонирована в NCIMB под депозитарным номером 41598 19 ноября 2008 года.
В другом варианте воплощения специфический связывающий агент или антитело по изобретению включают аминокислотную последовательность вариабельного домена тяжелой цепи, содержащую, по меньшей мере один, по меньшей мере, два или, по меньшей мере, три CDR антитела, кодируемых полинуклеотидом в плазмиде, обозначенной 2.7A4_G, которая была депонирована в NCIMB под депозитарным номером 41598 19 ноября 2008 года, и аминокислотную последовательность вариабельного домена легкой цепи, содержащую, по меньшей мере один, по меньшей мере, два или, по меньшей мере, три CDR антитела, кодируемых полинуклеотидом в плазмиде, обозначенной 2.7A4_G, которая была депонирована в NCIMB под депозитарным номером 41598 19 ноября 2008 года.
В одном варианте воплощения специфический связывающий агент или антитело по изобретению включают аминокислотную последовательность вариабельного домена тяжелой цепи, содержащую CDR3, кодируемый полинуклеотидом в плазмиде, обозначенной 2.14H9_G, которая была депонирована в NCIMB под номером 41597 19 ноября 2008 года.
В одном варианте воплощения специфический связывающий агент или антитело по изобретению включают аминокислотную последовательность вариабельного домена тяжелой цепи, содержащую CDR3, кодируемый полинуклеотидом в плазмиде, обозначенной 2.14H9_G, которая была депонирована в NCIMB под номером 41597 19 ноября 2008 года, и аминокислотную последовательность вариабельного домена легкой цепи, содержащую CDR3, кодируемый полинуклеотидом в плазмиде, обозначенной 2.14H9_G, которая была депонирована в NCIMB под номером 41597 19 ноября 2008 года.
В другом варианте воплощения специфический связывающий агент или антитело по изобретению включают аминокислотную последовательность вариабельного домена тяжелой цепи, содержащую, по меньшей мере, один, по меньшей мере, два или, по меньшей мере, три CDR антитела, кодируемых полинуклеотидом в плазмиде, обозначенной 2.14H9_G, которая была депонирована в NCIMB под номером 41597 19 ноября 2008 года.
В другом варианте воплощения специфический связывающий агент или антитело по изобретению включают аминокислотную последовательность вариабельного домена легкой цепи, содержащую, по меньшей мере, один, по меньшей мере, два или, по меньшей мере, три CDR антитела, кодируемых полинуклеотидом в плазмиде, обозначенной 2.14H9_G, которая была депонирована в NCIMB под номером 41597 19 ноября 2008 года.
В другом варианте воплощения специфический связывающий агент или антитело по изобретению включают аминокислотную последовательность вариабельного домена тяжелой цепи, содержащую, по меньшей мере, один, по меньшей мере, два или, по меньшей мере, три CDR антитела, кодируемых полинуклеотидом в плазмиде, обозначенной 2.14H9_G, которая была депонирована в NCIMB под номером 41597 19 ноября 2008 года, и аминокислотную последовательность вариабельного домена легкой цепи, содержащую, по меньшей мере, один, по меньшей мере, два или, по меньшей мере, три CDR антитела, кодируемых полинуклеотидом в плазмиде, обозначенной 2.14H9_G, которая была депонирована в NCIMB под номером 41597 19 ноября 2008 года.
В одном варианте воплощения специфический связывающий агент или антитело по изобретению включают аминокислотную последовательность вариабельного домена тяжелой цепи, содержащую CDR3, кодируемый полинуклеотидом в плазмиде, обозначенной 2.9D10_NG, которая была депонирована в NCIMB под номером 41599 19 ноября 2008 года.
В одном варианте воплощения специфический связывающий агент или антитело по изобретению включают аминокислотную последовательность вариабельного домена тяжелой цепи, содержащую CDR3, кодируемый полинуклеотидом в плазмиде, обозначенной 2.9D10_NG, которая была депонирована в NCIMB под номером 41599 19 ноября 2008 года, и аминокислотную последовательность вариабельного домена легкой цепи, содержащую CDR3, кодируемый полинуклеотидом в плазмиде, обозначенной 2.9D10_NG, которая была депонирована в NCIMB под номером 41599 19 ноября 2008 года.
В другом варианте воплощения специфический связывающий агент или антитело по изобретению включают аминокислотную последовательность вариабельного домена тяжелой цепи, содержащую, по меньшей мере, один, по меньшей мере, два или, по меньшей мере, три CDR антитела, кодируемых полинуклеотидом в плазмиде, обозначенной 2.9D10_NG, которая была депонирована в NCIMB под номером 41599 19 ноября 2008 года.
В другом варианте воплощения специфический связывающий агент или антитело по изобретению включают аминокислотную последовательность вариабельного домена легкой цепи, содержащую, по меньшей мере, один, по меньшей мере, два или, по меньшей мере, три CDR антитела, кодируемых полинуклеотидом в плазмиде, обозначенной 2.9D10_NG, которая была депонирована в NCIMB под номером 41599 19 ноября 2008 года.
В другом варианте воплощения специфический связывающий агент или антитело по изобретению включают аминокислотную последовательность вариабельного домена тяжелой цепи, содержащую, по меньшей мере, один, по меньшей мере, два или, по меньшей мере, три CDR антитела, кодируемых полинуклеотидом в плазмиде, обозначенной 2.9D10_NG, которая была депонирована в NCIMB под номером 41599 19 ноября 2008 года, и аминокислотную последовательность вариабельного домена легкой цепи, содержащую, по меньшей мере, один, по меньшей мере, два или, по меньшей мере, три CDR антитела, кодируемых полинуклеотидом в плазмиде, обозначенной 2.9D10_NG, которая была депонирована в NCIMB под номером 41599 19 ноября 2008 года.
В другом варианте воплощения специфический связывающий агент или антитело по изобретению включают вариабельную последовательность тяжелой цепи антитела, кодируемого полинуклеотидом в плазмиде, обозначенной 2.7A4_G, которая была депонирована в NCIMB номер 41598 19 ноября 2008 года.
В другом варианте воплощения специфический связывающий агент или антитело по изобретению включают вариабельную последовательность тяжелой цепи антитела, кодируемого полинуклеотидом в плазмиде, обозначенной 2.14H9_G, которая была депонирована в NCIMB под номером 41597 19 ноября 2008 года.
В другом варианте воплощения специфический связывающий агент или антитело по изобретению включают последовательность вариабельного домена тяжелой цепи антитела, кодируемого полинуклеотидом в плазмиде, обозначенной 2.9D10_NG, которая была депонирована в NCIMB под номером 41599 19 ноября 2008 года.
В другом варианте воплощения специфический связывающий агент или антитело по изобретению включают вариабельный домен легкой цепи антитела, кодируемого полинуклеотидом в плазмиде, обозначенной 2.7A4_G, которая была депонирована в NCIMB под номером 41598 19 ноября 2008 года.
В другом варианте воплощения специфический связывающий агент или антитело по изобретению включают вариабельный домен легкой цепи антитела, кодируемого полинуклеотидом в плазмиде, обозначенной 2.14H9_G, которая была депонирована в NCIMB под номером 41597 19 ноября 2008 года.
В другом варианте воплощения специфический связывающий агент или антитело по изобретению включают вариабельный домен легкой цепи антитела, кодируемого полинуклеотидом в плазмиде, обозначенной 2.9D10_NG, которая была депонирована в NCIMB под номером 41599 19 ноября 2008 года.
В другом варианте воплощения специфический связывающий агент или антитело по изобретению включают последовательность вариабельного домена тяжелой цепи антитела, кодируемого полинуклеотидом в плазмиде, обозначенной 2.7A4_G, которая была депонирована в NCIMB под номером 41598 19 ноября 2008 года, и последовательность вариабельного домена легкой цепи антитела, кодируемого полинуклеотидом в плазмиде, обозначенной 2.7A4_G, которая была депонирована в NCIMB под номером 41598 19 ноября 2008 года.
В другом варианте воплощения специфический связывающий агент или антитело по изобретению включают последовательность вариабельного домена легкой цепи антитела, кодируемого полинуклеотидом в плазмиде, обозначенной 2.14H9_G, которая была депонирована в NCIMB под номером 41597 19 ноября 2008 года, и последовательность вариабельного домена тяжелой цепи антитела, кодируемого полинуклеотидом в плазмиде, обозначенной 2.14H9_G, которая была депонирована в NCIMB под номером 41597 19 ноября 2008 года.
В другом варианте воплощения специфический связывающий агент или антитело по изобретению включают последовательность вариабельного домена тяжелой цепи антитела, кодируемого полинуклеотидом в плазмиде, обозначенной 2.9D10_NG, которая была депонирована в NCIMB под номером 41599 19 ноября 2008 года, и последовательность вариабельного домена легкой цепи антитела, кодируемого полинуклеотидом в плазмиде, обозначенной 2.9D10_NG, которая была депонирована в NCIMB под номером 41599 19 ноября 2008 года.
В одном варианте воплощения специфический связывающий агент или антитело могут включать последовательность, содержащую CDR1 тяжелой цепи (HCDR1), CDR2 тяжелой цепи (HCDR2) и CDR3 тяжелой цепи (HCDR3), выбранные из любой из последовательностей, приведенных в Таблице 8. В одном варианте воплощения специфический связывающий агент или антитело могут включать последовательность, содержащую CDR1 легкой цепи (LCDR1), CDR2 легкой цепи (LCDR2) и CDR3 легкой цепи (LCDR3), выбранные из любой из последовательностей, приведенных в Таблице 9. В одном варианте воплощения специфический связывающий агент или антитело могут включать последовательность, содержащую HCDR1, HCDR2 и HCDR3, выбранные из любого из CDR антител 2.9D10, 2.7A4, 2.14H9, 3.15G8, 2.20A8 или 3.18G1. В одном варианте воплощения специфический связывающий агент или антитело могут включать последовательность, содержащую LCDR1, LCDR2 и LCDR3, выбранные из любого из CDR антител 2.9D10, 2.7A4, 2.14H9, 3.15G8, 2.20A8 или 3.18G1.
Дополнительный вариант воплощения представляет собой специфический связывающий агент или антитело, которые специфически связываются с B7-H1 и включают последовательность, содержащую одну из последовательностей CDR2 и одну - из CDR3, приведенных в Таблице 9. В дополнительном варианте воплощения специфический связывающий агент или антитело дополнительно включают последовательность, содержащую последовательность CDR3, приведенную в Таблице 8. В дополнительном варианте воплощения специфический связывающий агент или антитело дополнительно включают последовательность, содержащую: последовательность CDR2 и CDR3, приведенную в Таблице 8 и/или Таблице 9. В дополнительном варианте воплощения специфический связывающий агент или антитело дополнительно включают последовательность, содержащую последовательность CDR1, CDR2 и CDR3, приведенную в Таблице 8 и/или Таблице 9.
В другом варианте воплощения специфический связывающий агент или антитело могут включать последовательность, содержащую любой один из CDR1, CDR2 или CDR3 любого из полностью человеческих моноклональных антител 2.7A4, 2.14H9 или 2.9D10, приведенных в Таблице 8. В другом варианте воплощения специфический связывающий агент или антитело могут включать последовательность, содержащую любой один из CDR1, CDR2 или CDR3 любого из полностью человеческих моноклональных антител 2.7A4, 2.14H9 или 2.9D10, приведенных в Таблице 9. В одном варианте воплощения специфический связывающий агент или антитело могут включать последовательность, содержащую CDR1, CDR2 и CDR3 любого из полностью человеческих моноклональных антител 2.7A4, 2.14H9, 2.9D10, 2.7A4OPT или 2.14H9OPT, приведенных в Таблице 8. В другом варианте воплощения специфический связывающий агент или антитело могут включать последовательность, содержащую CDR1, CDR2 и CDR3 любого из полностью человеческих моноклональных антител 2.7A4, 2.14H9, 2.9D10, 2.7A4OPT или 2.14H9OPT, приведенных в Таблице 9.
В другом варианте воплощения специфический связывающий агент или антитело включают последовательность, содержащую последовательность CDR1, CDR2 и CDR3 полностью человеческого моноклонального антитела 2.7A4, приведенную в Таблице 8, и последовательность CDR1, CDR2 и CDR3 полностью человеческого моноклонального антитела 2.7A4, приведенную в Таблице 9. В другом варианте воплощения специфический связывающий агент или антитело включают последовательность, содержащую последовательность CDR1, CDR2 и CDR3 полностью человеческого моноклонального антитела 2.14H9, приведенную в Таблице 8, и последовательность CDR1, CDR2 и CDR3 полностью человеческого моноклонального антитела 2.14H9, приведенную в Таблице 9. В другом варианте воплощения специфический связывающий агент или антитело включают последовательность, содержащую последовательность CDR1, CDR2 и CDR3 полностью человеческого моноклонального антитела 2.9D10, приведенную в Таблице 8, и последовательность CDR1, CDR2 и CDR3 полностью человеческого моноклонального антитела 2.9D10, приведенную в Таблице 9. В некоторых вариантах воплощения антитело представляет собой полностью человеческое моноклональное антитело.
Отметим, что рядовые специалисты в данной области техники могут легко осуществить определения CDR. См., например, Kabat et al., Sequences of Proteins of Immunological Interest, Fifth Edition, NIH Publication 91-3242, Bethesda MD (1991), vols. 1-3. Kabat приводит многочисленные выравнивания последовательностей иммуноглобулиновых цепей из изотипов антител различных видов. Выровненные последовательности нумеруют в соответствии с единой системой нумерации - системой нумерации Кабат (Kabat). Последовательности Kabat обновлялись после публикации в 1991 г. и доступны в виде электронной базы данных последовательностей (в настоящее время размещена на веб-сайте базы данных Kabat; см. также Nucleic Acids Research, 2000, 28(1), 214-218). Любая иммуноглобулиновая последовательность может быть пронумерована в соответствии с Кабат путем проведения выравнивания с эталонной последовательностью Кабат. Соответственно, система нумерации Кабат обеспечивает унифицированную систему нумерации иммуноглобулиновых цепей.
Дополнительный вариант воплощения изобретения представляет собой специфический связывающий агент или антитело, включающие последовательность, содержащую непрерывную последовательность, охватывающую каркасные участки и CDR, конкретнее, FR1-FR4 или CDR1-CDR3, любой из последовательностей 2.9D10, 2.7A4, 2.14H9, 3.15G8, 2.20A8, 3.18G1, 2.7A4OPT или 2.14H9OPT или приведенных в Таблице 8 или Таблице 9. Дополнительный вариант воплощения изобретения представляет собой специфический связывающий агент или антитело, включающие последовательность, содержащую непрерывную последовательность, охватывающую каркасные участки и CDR, конкретнее, FR1-FR4 или CDR1-CDR3, любой из последовательностей 2.9D10, 2.7A4, 2.14H9, 3.15G8, 2.20A8, 3.18G1, 2.7A4OPT или 2.14H9OPT или приведенных в Таблице 8 и Таблице 9. В одном варианте воплощения специфический связывающий агент или антитело включает последовательность, содержащую непрерывные последовательности, охватывающие каркасные участки и CDR, конкретнее, FR1-FR4 или CDR1-CDR3, любой из последовательностей моноклональных антител 2.9D10, 2.7A4, 2.14H9, 3.15G8, 2.20A8, 3.18G1, 2.7A4OPT или 2.14H9OPT или приведенных в Таблице 8 или Таблице 9. Дополнительный вариант воплощения изобретения представляет собой специфический связывающий агент или антитело, включающие последовательность, содержащую непрерывную последовательность, охватывающую каркасные участки и CDR, конкретнее, FR1-FR4 или CDR1-CDR3, любой из последовательностей моноклональных антител 2.9D10, 2.7A4, 2.14H9, 3.15G8, 2.20A8, 3.18G1, 2.7A4OPT или 2.14H9OPT или приведенных в Таблице 8 и Таблице 9. В некоторых вариантах воплощения антитело представляет собой полностью человеческое моноклональное антитело.
В другом варианте воплощения специфический связывающий агент или антитело по изобретению включают последовательность CDR3, приведенную в Таблице 8 или 9; или любую одну из последовательностей CDR1, CDR2 или CDR3, приведенных в Таблице 8 или 9; или последовательность CDR1, CDR2 и CDR3 последовательности вариабельного домена легкой цепи, как приведено в Таблице 8; или последовательность CDR1, CDR2 и CDR3 последовательности вариабельного домена тяжелой цепи, как приведено в Таблице 9.
Один вариант воплощения предусматривает специфический связывающий агент или антитело, или его антигенсвязывающий участок, где агент или антитело, или его антигенсвязывающий участок включает последовательность, содержащую SEQ ID NO:2, SEQ ID NO:7, SEQ ID NO:12, SEQ ID NO:17, SEQ ID NO:22, SEQ ID NO:27, SEQ ID NO:32, SEQ ID NO:37, SEQ ID NO:42, SEQ ID NO:47, SEQ ID NO:52, SEQ ID NO:57, SEQ ID NO:62, SEQ ID NO:67, SEQ ID NO:72 или SEQ ID NO:77.
Один вариант воплощения предусматривает специфический связывающий агент или антитело, или его антигенсвязывающий участок, где агент или антитело, или его антигенсвязывающий участок включает последовательность тяжелой цепи, содержащую последовательность SEQ ID NO:2. В одном варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок, дополнительно включает последовательность легкой цепи, содержащую последовательность SEQ ID NO:7. В некоторых вариантах воплощения антитело представляет собой полностью человеческое моноклональное антитело.
В другом варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок включает вариабельный домен тяжелой цепи, имеющий, по меньшей мере, 90% идентичности с аминокислотной последовательностью SEQ ID NO:2, и включает вариабельный домен легкой цепи, имеющий, по меньшей мере, 90% идентичности с аминокислотной последовательностью SEQ ID NO:7.
В другом варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок включает последовательность тяжелой цепи, содержащую последовательность SEQ ID NO:12. В одном варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок, дополнительно включает последовательность легкой цепи, содержащую последовательность SEQ ID NO:17. В некоторых вариантах воплощения антитело представляет собой полностью человеческое моноклональное антитело.
В одном варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок включает вариабельный домен тяжелой цепи, имеющий, по меньшей мере, 90% идентичности с аминокислотной последовательностью SEQ ID NO:12, и включает вариабельный домен легкой цепи, имеющий, по меньшей мере, 90% идентичности с аминокислотной последовательностью SEQ ID NO:17.
В другом варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок включает последовательность тяжелой цепи, содержащую последовательность SEQ ID NO:22. В другом варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок дополнительно включает последовательность легкой цепи, содержащую последовательность SEQ ID NO:27. В некоторых вариантах воплощения антитело представляет собой полностью человеческое моноклональное антитело.
В другом варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок включает вариабельный домен тяжелой цепи, имеющий, по меньшей мере, 90% идентичности с аминокислотной последовательностью SEQ ID NO:22, и включает вариабельный домен легкой цепи, имеющий, по меньшей мере, 90% идентичности с аминокислотной последовательностью SEQ ID NO:27.
В другом варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок включает последовательность тяжелой цепи, содержащую последовательность SEQ ID NO:32. В другом варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок дополнительно включает последовательность легкой цепи, содержащую последовательность SEQ ID NO:37. В некоторых вариантах воплощения антитело представляет собой полностью человеческое моноклональное антитело.
В другом варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок включает вариабельный домен тяжелой цепи, имеющий, по меньшей мере, 90% идентичности с аминокислотной последовательностью SEQ ID NO:32, и включает вариабельный домен легкой цепи, имеющий, по меньшей мере, 90% идентичности с аминокислотной последовательностью SEQ ID NO:37.
В другом варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок включает последовательность тяжелой цепи, содержащую последовательность SEQ ID NO:42. В другом варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок дополнительно включает последовательность легкой цепи, содержащую последовательность SEQ ID NO:47. В некоторых вариантах воплощения антитело представляет собой полностью человеческое моноклональное антитело.
В другом варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок включает вариабельный домен тяжелой цепи, имеющий, по меньшей мере, 90% идентичности с аминокислотной последовательностью SEQ ID NO:42, и включает вариабельный домен легкой цепи, имеющий, по меньшей мере, 90% идентичности с аминокислотной последовательностью SEQ ID NO:47.
В другом варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок включает последовательность тяжелой цепи, содержащую последовательность SEQ ID NO:52. В другом варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок дополнительно включает последовательность легкой цепи, содержащую последовательность SEQ ID NO:57. В некоторых вариантах воплощения антитело представляет собой полностью человеческое моноклональное антитело.
В другом варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок включает вариабельный домен тяжелой цепи, имеющий, по меньшей мере, 90% идентичности с аминокислотной последовательностью SEQ ID NO:52, и включает вариабельный домен легкой цепи, имеющий, по меньшей мере, 90% идентичности с аминокислотной последовательностью SEQ ID NO:57.
В другом варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок включает последовательность тяжелой цепи, содержащую последовательность SEQ ID NO:62. В другом варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок дополнительно включает последовательность легкой цепи, содержащую последовательность SEQ ID NO:67. В некоторых вариантах воплощения антитело представляет собой полностью человеческое моноклональное антитело.
В другом варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок включает вариабельный домен тяжелой цепи, имеющий, по меньшей мере, 90% идентичности с аминокислотной последовательностью SEQ ID NO:62, и включает вариабельный домен легкой цепи, имеющий, по меньшей мере, 90% идентичности с аминокислотной последовательностью SEQ ID NO:67.
В другом варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок включает последовательность тяжелой цепи, содержащую последовательность SEQ ID NO:72. В другом варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок дополнительно включает последовательность легкой цепи, содержащую последовательность SEQ ID NO:77. В некоторых вариантах воплощения антитело представляет собой полностью человеческое моноклональное антитело.
В другом варианте воплощения специфический связывающий агент или антитело, или его антигенсвязывающий участок включает вариабельный домен тяжелой цепи, имеющий, по меньшей мере, 90% идентичности с аминокислотной последовательностью SEQ ID NO:72, и включает вариабельный домен легкой цепи, имеющий, по меньшей мере, 90% идентичности с аминокислотной последовательностью SEQ ID NO:77.
В одном варианте воплощения специфический связывающий агент или антитело включает варианты или производные CDR, раскрытых здесь, непрерывные последовательности, охватывающие каркасные участки и CDR (конкретнее, FR1-FR4 или CDR1-CDR3), последовательности легкой или тяжелой цепей, раскрытые здесь, или антитела, раскрытые здесь. Варианты включают специфические связывающие агенты или антитела, включающие последовательности, имеющие до двадцати, шестнадцати, десяти, девяти или меньше, например, одну, две, три, четыре, пять или шесть вставок, замещений, делеций и/или инсерций аминокислот в любом из CDR1, CDR2 или CDR3, как приведено в Таблице 8 или Таблице 9, непрерывные последовательности, охватывающие каркасные участки и CDR (конкретнее, FR1-FR4 или CDR1-CDR3), приведенные в Таблице 8 или Таблице 9, последовательности легкой или тяжелой цепей, раскрытые здесь, или с моноклональными антителами, раскрытыми здесь. Варианты включают специфические связывающие агенты или антитела, включающие последовательности, имеющие одну, две или три аминокислотных вставок, замещений, делеций и/или инсерций в любом из CDR1, CDR2 или CDR3, приведенных в Таблице 8 или Таблице 9, непрерывных последовательностях, охватывающих каркасные участки и CDR (конкретнее, FR1-FR4 или CDR1-CDR3), приведенных в Таблице 8 или Таблице 9, последовательностях легкой или тяжелой цепей, раскрытых здесь, или с моноклональными антителами, раскрытыми здесь. Варианты включают специфические связывающие агенты или антитела, включающие последовательности, имеющие, по меньшей мере, примерно 60, 70, 80, 85, 90, 95, 98 или примерно 99% идентичности аминокислотной последовательности с любым из CDR1, CDR2 или CDR3, приведенных в Таблице 8 или Таблице 9, непрерывными последовательностями, охватывающими каркасные участки и CDR (конкретнее, FR1-FR4 или CDR1-CDR3), приведенные в Таблице 8 или Таблице 9, последовательностями легкой или тяжелой цепей, раскрытыми здесь, или с моноклональными антителами, раскрытыми здесь. Процент идентичности двух аминокислотных последовательностей может быть определен любым способом, известным квалифицированному специалисту в данной области техники, включая, без ограничений, попарное сравнение первичной структуры белков. В одном варианте воплощения варианты содержат изменения в последовательностях CDR или последовательностях легкой или тяжелой цепей, раскрытые здесь, имеющие природное происхождение или введенные in vitro методами генной инженерии нативных последовательностей с использованием методик рекомбинантной ДНК или методик мутагенеза. Варианты природного происхождения включают образующиеся in vivo в соответствующих нуклеотидных последовательностях первичных клеток при получении антител к чужеродному антигену.
В одном варианте воплощения варианты включают специфические связывающие агенты или антитела, включающие последовательности, содержащие (a) VH CDR1 (вариабельного участка тяжелой цепи), имеющий аминокислотную последовательность, идентичную с или включающую 1, 2 или 3 замещения аминокислотных остатков по сравнению с SEQ ID NO:3;
(b) VH CDR2, имеющий аминокислотную последовательность, идентичную с или включающую 1, 2 или 3 замещения аминокислотных остатков по сравнению с SEQ ID NO:4;
(c) VH CDR3, имеющий аминокислотную последовательность, идентичную с или включающую 1, 2 или 3 замещения аминокислотных остатков по сравнению с SEQ ID NO:5;
(d) VL CDR1 (вариабельного участка легкой цепи), имеющий аминокислотную последовательность, идентичную с или включающую 1, 2 или 3 замещения аминокислотных остатков по сравнению с VL CDR1 SEQ ID NO:8;
(e) VL CDR2, имеющий аминокислотную последовательность, идентичную с или включающую 1, 2 или 3 замещения аминокислотных остатков по сравнению с SEQ ID NO:9; и
(f) VL CDR3, имеющий аминокислотную последовательность, идентичную с или включающую 1, 2 или 3 замещения аминокислотных остатков по сравнению с SEQ ID NO:10.
В другом варианте воплощения варианты включают специфические связывающие агенты или антитела, включающие последовательности, содержащие (a) VH CDR1, имеющий аминокислотную последовательность, идентичную с или включающую 1, 2 или 3 замещения аминокислотных остатков по сравнению с SEQ ID NO:23;
(b) VH CDR2, имеющий аминокислотную последовательность, идентичную с или включающую 1, 2 или 3 замещения аминокислотных остатков по сравнению с SEQ ID NO:24;
(c) VH CDR3, имеющий аминокислотную последовательность, идентичную с или включающую 1, 2 или 3 замещения аминокислотных остатков по сравнению с SEQ ID NO:25;
(d) VL CDR1, имеющий аминокислотную последовательность, идентичную с или включающую 1, 2 или 3 замещения аминокислотных остатков по сравнению с VL CDR1 SEQ ID NO:28;
(e) VL CDR2, имеющий аминокислотную последовательность, идентичную с или включающую 1, 2 или 3 замещения аминокислотных остатков по сравнению с SEQ ID NO:29; и
(f) VL CDR3, имеющий аминокислотную последовательность, идентичную с или включающую 1, 2 или 3 замещения аминокислотных остатков по сравнению с SEQ ID NO:30.
В одном варианте воплощения производное может быть гетероантителом, т.е. антителом, в котором два или несколько антител соединены вместе. Производные включают антитела, которые были химически модифицированы. Примеры включают ковалентное присоединение одного или нескольких полимеров, таких как водорастворимые полимеры, N-связанные или O-связанные углеводы, сахара, фосфаты и/или другие подобные молекулы. Производные модифицированы таким образом, чтобы они отличались от антитела природного происхождения или исходного антитела по типу или местоположению присоединенной молекулы. Производные дополнительно включают удаление одной или нескольких химических групп, присутствующих в природных условиях в антителе.
В некоторых вариантах воплощения изобретения специфический связывающий агент или антитело включает последовательность, содержащую SEQ ID NO:2. В некоторых вариантах воплощения изобретения специфический связывающий агент или антитело включает последовательность, содержащую SEQ ID NO:2, где SEQ ID NO:2 включает любую из уникальных комбинаций остатков, принадлежащих и не принадлежащих зародышевой линии, приведенных в каждом ряду Таблицы 10. В некоторых вариантах воплощения изобретения специфический связывающий агент или антитело включает последовательность, содержащую SEQ ID NO:2, где SEQ ID NO:2 включает любой один, любые два, любые три, любые четыре или все пять остатков зародышевой линии, указанных в Таблице 10. В некоторых вариантах воплощения изобретения специфический связывающий агент или антитело включает последовательность, содержащую SEQ ID NO:2, где SEQ ID NO:2 включает любую из уникальных комбинаций остатков, принадлежащих и не принадлежащих зародышевой линии, указанных в каждом ряду Таблицы 10. В некоторых вариантах воплощения изобретения специфический связывающий агент или антитело включает последовательность, содержащую SEQ ID NO:2, где SEQ ID NO:2 включает любой один, любые два, любые три, любые четыре, любые пять или все пять остатков зародышевой линии, указанных в Таблице 10.
В некоторых вариантах воплощения изобретения специфический связывающий агент или антитело включает последовательность, содержащую SEQ ID NO:7, где SEQ ID NO:7 включает любую из уникальных комбинаций остатков, принадлежащих и не принадлежащих зародышевой линии, указанных в каждом ряду Таблицы 11, и любую из уникальных комбинаций остатков, принадлежащих и не принадлежащих зародышевой линии, указанных в каждом ряду Таблицы 11. В некоторых вариантах воплощения изобретения специфический связывающий агент или антитело включает последовательность, содержащую SEQ ID NO:7, где SEQ ID NO:7 включает любой один, любые два, любые три, любые четыре, любые пять или все пять остатков зародышевой линии, указанных в Таблице 11.
В некоторых вариантах воплощения изобретения специфический связывающий агент или антитело включает последовательность, содержащую SEQ ID NO:12. В некоторых вариантах воплощения изобретения специфический связывающий агент или антитело включает последовательность, содержащую SEQ ID NO:12, где SEQ ID NO:12 включает любую из уникальных комбинаций остатков, принадлежащих и не принадлежащих зародышевой линии, указанных в каждом ряду Таблицы 12. В некоторых вариантах воплощения изобретения специфический связывающий агент или антитело включает последовательность, содержащую SEQ ID NO:12, где SEQ ID NO:12 включает любой один, любые два или оба остатка зародышевой линии, указанных в Таблице 12.
В некоторых вариантах воплощения изобретения специфический связывающий агент или антитело включает последовательность, содержащую SEQ ID NO:17. В некоторых вариантах воплощения изобретения специфический связывающий агент или антитело включает последовательность, содержащую SEQ ID NO:17, где SEQ ID NO:17 включает любую из уникальных комбинаций остатков, принадлежащих и не принадлежащих зародышевой линии, указанных в каждом ряду Таблицы 13. В некоторых вариантах воплощения изобретения специфический связывающий агент или антитело включает последовательность, содержащую SEQ ID NO:17, где SEQ ID NO:17 включает любой один, любые два, любые три, любые четыре или все четыре остатка зародышевой линии, указанных в Таблице 13.
В некоторых вариантах воплощения изобретения специфический связывающий агент или антитело включает последовательность, содержащую SEQ ID NO:27. В некоторых вариантах воплощения изобретения специфический связывающий агент или антитело включает последовательность, содержащую SEQ ID NO:27, где SEQ ID NO:27 включает любую из уникальных комбинаций остатков, принадлежащих и не принадлежащих зародышевой линии, указанных в каждом ряду Таблицы 14. В некоторых вариантах воплощения изобретения специфический связывающий агент или антитело включает последовательность, содержащую SEQ ID NO:27, где SEQ ID NO:27 включает любой один, любые два, любые три или все три остатка зародышевой линии, указанных в Таблице 14.
Дополнительный вариант воплощения изобретения представляет собой специфический связывающий агент или антитело, конкурирующие за связывание с B7-H1 со специфическим связывающим агентом или антителами по изобретению. В другом варианте воплощения изобретения предусматривается антитело, конкурирующее за связывание с B7-H1 со специфическим связывающим агентом или антителами по изобретению. В другом варианте воплощения специфический связывающий агент или антитело конкурирует за связывание с B7-H1 с любым из полностью человеческих моноклональных антител 2.7A4, 2.14H9 или 2.9D10, 2.7A4OPT или 2.14H9OPT. «Конкурирует» указывает, что специфический связывающий агент или антитело конкурирует за связывание с B7-H1 с любым из полностью человеческих моноклональных антител 2.7A4, 2.14H9 или 2.9D10, 2.7A4OPT или 2.14H9OPT, т.е. конкуренция является однонаправленной.
Варианты воплощения изобретения включают специфический связывающий агент или антитело, которые перекрестно конкурируют с любым из полностью человеческих моноклональных антител 2.7A4, 2.14H9 или 2.9D10, 2.7A4OPT или 2.14H9OPT за связывание с B7-H1. «Перекрестно конкурирует» указывает, что специфический связывающий агент или антитело конкурирует за связывание с B7-H1 с любым из полностью человеческих моноклональных антител 2.7A4, 2.14H9 или 2.9D10, 2.7A4OPT или 2.14H9OPT, и наоборот, т.е. конкуренция является двунаправленной.
Дополнительный вариант воплощения изобретения представляет собой специфический связывающий агент или антитело, которые связываются с тем же эпитопом или эпитопами на внеклеточном домене человеческого B7-H1, что и специфический связывающий агент или антитела по изобретению. Варианты воплощения изобретения также включают специфический связывающий агент или антитело, которые связываются тем же эпитопом или эпитопами на внеклеточном домене человеческого B7-H1, что и любое из полностью человеческих моноклональных антител 2.7A4, 2.14H9 или 2.9D10, 2.7A4OPT или 2.14H9OPT.
В одном варианте воплощения специфический связывающий агент или антитело связывает эпитоп на человеческом B7-H1, включающий, по меньшей мере, одну или несколько из следующих аминокислот, выбранных из группы, состоящей из Asp в положении 122 и Arg в положении 125. В другом варианте воплощения антитело по изобретению связывает эпитоп на человеческом B7-H1, содержащий, по меньшей мере, два из следующих трех аминокислотных остатков - Asp в положении 122, Arg в положении 125 и Arg в положении 113. В другом варианте воплощения антитело связывает эпитоп на человеческом B7-H1, где антитело не связывается с Ile в положении 54, Ser в положении 117 и Ala в положении 121 на человеческом B7-H1. В еще одном варианте воплощения антитело по изобретению теряет свою способность связываться с человеческим B7-H1, если Arg в положении 113 мутирует на Ala, или на Tyr, или на Leu, при определении методом конкурентного анализа по сравнению со связыванием с B7-H1 дикого типа. В еще одном варианте воплощения антитело по изобретению теряет свою способность связываться с человеческим B7-H1, если Arg в положении 125 мутирует на Ala, или на Gln, или на Ser, при определении методом конкурентного анализа по сравнению со связыванием с B7-H1 дикого типа. В еще одном варианте воплощения антитело по изобретению сохраняет свою способность связываться с человеческим B7-H1, если Arg в положении 123 мутирует на Ala, или на Phe, или на Thr, при определении методом конкурентного анализа по сравнению со связыванием с B7-H1 дикого типа. В данном примере антитело представляет собой 2.14H9. В другом примере антитело представляет собой 2.14H9OPT.
В одном варианте воплощения специфический связывающий агент или антитело связывает эпитоп на внеклеточном домене человеческого B7-H1, содержащий, по меньшей мере, одну или несколько из следующих аминокислот - Asp в положении 122 и Thr в положении 20. В одном варианте воплощения антитело связывает, по меньшей мере, два из следующих трех аминокислотных остатков - Phe в положении 19, Thr в положении 20 и Asp в положении 122 на человеческом B7-H1. В другом варианте воплощения антитело не проявляет связывания, по меньшей мере, одного из следующих трех аминокислотных остатков - Ile в положении 54, Met в положении 115, Ser в положении 117 и Ala в положении 121 на человеческом B7-H1. В еще одном варианте воплощения антитело по изобретению теряет свою способность связываться с человеческим B7-H1, если Phe в положении 19 мутирует на Ala, или на Gly, или на Ser, при определении методом конкурентного анализа по сравнению со связыванием с B7-H1 дикого типа. В еще одном варианте воплощения антитело по изобретению теряет свою способность связываться с человеческим B7-H1, если Thr в положении 20 мутирует на Ala, или на Val, или на Asp, при определении методом конкурентного анализа по сравнению со связыванием с B7-H1 дикого типа. В еще одном варианте воплощения антитело по изобретению теряет свою способность связываться с человеческим B7-H1, если Asp в положении 122 мутирует на Asn или на Glu, при определении методом конкурентного анализа по сравнению со связыванием с B7-H1 дикого типа. В еще одном варианте воплощения антитело по изобретению сохраняет свою способность связываться с человеческим B7-H1, если Arg в положении 123 мутирует на Ala, или на Phe, или на Thr, при определении методом конкурентного анализа по сравнению со связыванием с B7-H1 дикого типа. В одном примере антитело представляет собой 2.7A4. В другом примере антитело представляет собой 2.7A4OPT.
В одном варианте воплощения специфический связывающий агент представляет собой биспецифическое антитело. Биспецифическое антитело представляет собой антитело, обладающее специфичностью связывания, по меньшей мере, двух разных эпитопов одного и того же или разных белков. Способы получения биспецифических антител известны специалистам (см., например, Millstein et al., Nature, 305:537-539 (1983); Traunecker et al., EMBO J., 10:3655-3659 (1991); Suresh et al., Methods in Enzymology, 121:210 (1986); Kostelny et al., J. Immunol., 148(5):1547-1553 (1992); Hollinger et al., Proc. Natl Acad. Sci. USA, 90:6444-6448 (1993); Gruber et al., J. Immunol., 152:5368 (1994); патенты США №№ 4474893; 4714681; 4925648; 5573920; 560181; 95731168; 4676980 и 4676980 WO 94/04690; WO 91/00360; WO 92/200373; WO 93/17715; WO 92/08802; и EP 03089).
Варианты воплощения изобретения, описанные здесь, относятся к моноклональным антителам, которые специфически связывают B7-H1 и влияют на функцию B7-H1. Другие варианты воплощения относятся к полностью человеческим антителам, которые специфически связывают B7-H1, и их препаратам с желательными свойствами с терапевтической точки зрения, включая высокую аффинность связывания с B7-H1, высокую селективность ингибирования сигналов B7-H1, низкую токсичность, способность блокировать активность рецептора PD-1, способность ингибировать B7-H1-индуцируемое выживание опухолевых клеток путем иммунной супрессии, способность ингибировать B7-H1-медиируемую репрессию противоопухолевого иммунитета, что может, в свою очередь, ингибировать болезни, связанные с пролиферацией или инвазией, включая неопластические болезни, и/или способность опухолевых клеток к росту in vitro и in vivo. Еще одни варианты воплощения относятся к способу репрессии B7-H1-медиируемого ингибирования T-клеток у животного путем введения животному, нуждающемуся в этом, эффективного количества композиции, содержащей антитела по изобретению. Еще одни варианты воплощения относятся к полностью человеческим антителам, которые специфически связывают B7-H1, и их препаратам, не вызывающим значительной реакции человеческих антихимерных антител (HACA), тем самым обеспечивая возможность повторного введения.
В одном варианте воплощения изобретения предусматривается молекула нуклеиновой кислоты, кодирующая любые специфические связывающие агенты или антитела по изобретению. В одном варианте воплощения предусматривается молекула нуклеиновой кислоты, кодирующая легкую цепь или тяжелую цепь антитела по изобретению. В одном варианте воплощения молекула нуклеиновой кислоты кодирует легкую цепь или тяжелую цепь полностью человеческого моноклонального антитела любого из описанных здесь антител. В одном варианте воплощения молекула нуклеиновой кислоты кодирует легкую цепь или тяжелую цепь любого из полностью человеческих моноклональных антител 2.7A4, 2.14H9, 2.9D10, 2.7A4OPT и 2.14H9OPT. В другом варианте воплощения молекула нуклеиновой кислоты кодирует легкую цепь и тяжелую цепь любого из полностью человеческих моноклональных антител 2.7A4, 2.14H9, 2.9D10, 2.7A4OPT и 2.14H9OPT. Изобретение также охватывает полинуклеотиды, которые гибридизуются в суровых или менее суровых условиях гибридизации, как определено здесь, с полинуклеотидами, кодирующими любые специфические связывающие агенты или антитела, описанные тут.
В другом варианте воплощения изобретения предусматривается вектор, включающий молекулу или молекулы нуклеиновой кислоты, как описано выше, где вектор кодирует специфический связывающий агент, как описано выше. В одном варианте воплощения изобретения предусматривается вектор, включающий молекулу или молекулы нуклеиновой кислоты, как описано выше, где вектор кодирует легкую цепь и/или тяжелую цепь антитела, как определено выше. В одном варианте воплощения вектор включает молекулу нуклеиновой кислоты, кодирующую легкую цепь и/или тяжелую цепь полностью человеческого моноклонального антитела. В одном варианте воплощения вектор включает молекулу нуклеиновой кислоты, кодирующую легкую цепь или тяжелую цепь любого из полностью человеческих моноклональных антител 2.7A4, 2.14H9, 2.9D10, 2.7A4OPT и 2.14H9OPT. В другом варианте воплощения вектор включает молекулу нуклеиновой кислоты, кодирующую легкую цепь и тяжелую цепь любого из полностью человеческих моноклональных антител 2.7A4, 2.14H9, 2.9D10, 2.7A4OPT и 2.14H9OPT.
В дополнительном варианте воплощения предусматривается клетка-хозяин, трансформированная любой из молекул нуклеиновой кислоты, как описано выше. В другом варианте воплощения изобретения предусматривается клетка-хозяин, включающая вектор, включающий молекулу нуклеиновой кислоты, как описано выше. В одном варианте воплощения клетка-хозяин может включать несколько векторов.
Как известно специалистам, антитела могут эффективно быть, например, поликлональными, олигоклональными, моноклональными, химерными, гуманизированными и/или полностью человеческими антителами.
Следует понимать, что варианты воплощения изобретения не ограничены какой-либо конкретной формой антитела или способом получения или производства. В некоторых вариантах воплощения изобретения специфический связывающий агент представляет собой связывающий фрагмент полностью человеческого моноклонального антитела. Например, специфический связывающий агент может быть полноразмерным антителом (например, имеющим интактный человеческий Fc-участок) или антителосвязывающим фрагментом (например, Fab, Fab' или F(ab')2, Fv, dAb или другим хорошо известным фрагментом антитела, как детальнее описано ниже). Кроме того, антитела могут быть однодоменными антителами, такими как отдельные VH или VL домены семейства верблюжьих или человека, которые связываются с B7-H1, такие как фрагмент dAb.
Варианты воплощения изобретения, описанные здесь, также предусматривают клетки для продуцирования таких антител. Примеры клеток включают гибридомы, или рекомбинантно созданные клетки, такие как клетки яичника китайского хомячка (CHO), варианты клеток CHO (например, DG44) и клетки NS0, продуцирующие антитела против B7-H1. Дополнительная информация о вариантах клеток CHO приведена в Andersen and Reilly (2004) Current Opinion in Biotechnology 15, 456-462, которая целиком включена сюда в качестве ссылки. Антитело может быть получено от гибридомы, которая секретирует антитело, или от рекомбинантно модифицированной клетки, которая была трансформирована или трансфицирована геном или генами, кодирующими антитело.
Кроме того, один вариант воплощения изобретения представляет собой способ получения специфического связывающего агента или антитела по изобретению путем культивации клеток-хозяев в условиях, при которых экспрессируется молекула нуклеиновой кислоты для получения специфического связывающего агента или антитела с последующим выделением специфического связывающего агента или антитела. В одном варианте воплощения предусматривается способ получения антитела по изобретению путем культивации клеток-хозяев в условиях, при которых экспрессируется молекула нуклеиновой кислоты для получения антитела, с последующим выделением антитела. Еще одни варианты воплощения включают антитело по изобретению, полученное способом культивации клетки-хозяина, которая экспрессирует антитело, кодируемое молекулой нуклеиновой кислоты, кодирующей антитело по изобретению, и выделения указанного антитела из указанной культуры.
Следует понимать, что варианты воплощения изобретения также включают любую молекулу нуклеиновой кислоты, кодирующую антитело или фрагмент антитела по изобретению, включая последовательности нуклеиновой кислоты, оптимизированные для увеличения выхода антител или их фрагментов при трансфекции в клетки-хозяева для продуцирования антитела.
Дополнительный вариант воплощения данного изобретения включает способ получения антител, которые специфически связываются с B7-H1 и ингибируют биологическую активность B7-H1, путем иммунизации млекопитающего клетками, экспрессирующими B7-H1, выделенными клеточными мембранами, содержащими B7-H1, очищенным B7-H1 или его фрагментом, и/или одной или несколькими ортологичными последовательностями или их фрагментами.
Дополнительный вариант воплощения данного изобретения включает способ получения высокоаффинных антител, которые специфически связываются с B7-H1 и ингибируют биологическую активность B7-H1, путем иммунизации млекопитающего клетками, экспрессирующими B7-H1, выделенными клеточными мембранами, содержащими B7-H1, очищенным B7-H1 или его фрагментом, и/или одной или несколькими ортологичными последовательностями или их фрагментами.
Другие варианты воплощения основаны на получении и идентификации выделенных антител, которые специфически связываются с B7-H1 и ингибируют биологическую активность B7-H1. B7-H1 экспрессируется на ряде типов опухолей. Антитела, которые специфически связываются с B7-H1, могут предотвращать B7-H1-медиируемое выживание опухолевых клеток и ингибировать B7-H1-медиируемую репрессию противоопухолевых иммунных ответов путем иммунной супрессии, что, в свою очередь, снижает инвазивность опухолевых клеток, метастазирование, рост опухоли, и другие свойства.
Кроме того, антитело может быть получено от гибридомы, которая секретирует антитело, или от рекомбинантно модифицированной клетки, которая была трансформирована или трансфицирована геном или генами, кодирующими антитело.
В одном варианте воплощения предусматривается гибридома, которая продуцирует специфический связывающий агент или антитело по изобретению. В одном варианте воплощения предусматривается гибридома, продуцирующая легкую цепь и/или тяжелую цепь антитела по изобретению. В одном варианте воплощения гибридома может продуцировать легкую цепь и/или тяжелую цепь полностью человеческого моноклонального антитела. В другом варианте воплощения гибридома продуцирует легкую цепь и/или тяжелую цепь полностью человеческого моноклонального антитела 2.7A4, 2.14H9, 2.9D10, 2.7A4OPT и 2.14H9OPT. Альтернативно, гибридома может продуцировать антитело, которое связывается с тем же эпитопом или эпитопами, что и полностью человеческое моноклональное антитело 2.7A4, 2.14H9, 2.9D10, 2.7A4OPT и 2.14H9OPT. Альтернативно, гибридома может продуцировать антитело, конкурирующее за связывание с B7-H1 с полностью человеческим моноклональным антителом 2.7A4, 2.14H9, 2.9D10, 2.7A4OPT и 2.14H9OPT. Альтернативно, гибридома может продуцировать антитело, перекрестно конкурирующее за связывание с B7-H1 с полностью человеческим моноклональным антителом 2.7A4, 2.14H9, 2.9D10, 2.7A4OPT и 2.14H9OPT.
В других вариантах воплощения изобретение предусматривает композиции, включающие специфический связывающий агент или антитело по изобретению или его связывающий фрагмент и фармацевтически приемлемый носитель.
Другие дополнительные варианты воплощения изобретения включают способы лечения пролиферативной или ассоциированной с инвазией болезни у животного путем введения животному терапевтически эффективной дозы специфического связывающего агента по изобретению. В определенных вариантах воплощения способ дополнительно включает выбор животного, нуждающегося в лечении пролиферативной или ассоциированной с инвазией болезни, и введение животному терапевтически эффективной дозы специфического связывающего агента по изобретению. В определенных вариантах воплощения животное является человеком. В определенных вариантах воплощения специфический связывающий агент представляет собой полностью человеческое моноклональное антитело. В определенных вариантах воплощения специфический связывающий агент представляет собой антитело по изобретению и может быть выбран из группы, состоящей из 2.7A4, 2.14H9 или 2.9D10, 2.7A4OPT или 2.14H9OPT.
Другие дополнительные варианты воплощения изобретения включают способы ингибирования у животного ассоциированной с пролиферацией клеток или инвазией болезни с B7-H1-медиируемой компонентой, путем введения животному терапевтически эффективной дозы специфического связывающего агента по изобретению. В определенных вариантах воплощения способ дополнительно включает выбор животного, нуждающегося в лечении ассоциированной с пролиферацией или инвазией болезни с B7-H1-медиируемой компонентой, и введение указанному животному терапевтически эффективной дозы специфического связывающего агента по изобретению. В определенных вариантах воплощения животное является человеком. В определенных вариантах воплощения специфический связывающий агент представляет собой полностью человеческое моноклональное антитело. В определенных вариантах воплощения специфический связывающий агент представляет собой антитело по изобретению и может быть выбран из группы, состоящей из 2.7A4, 2.14H9 или 2.9D10, 2.7A4OPT или 2.14H9OPT.
Другие дополнительные варианты воплощения изобретения включают способы ингибирования инвазии опухолевых клеток, метастазирование клеток или рост опухоли у животного путем введения животному терапевтически эффективной дозы специфического связывающего агента по изобретению. В определенных вариантах воплощения способ дополнительно включает выбор животного, нуждающегося в лечении опухолевых клеток, инвазии, метастазирования клеток или роста опухоли, и введение животному терапевтически эффективной дозы специфического связывающего агента по изобретению. В определенных вариантах воплощения животное является человеком. В определенных вариантах воплощения специфический связывающий агент представляет собой полностью человеческое моноклональное антитело. В определенных вариантах воплощения специфический связывающий агент представляет собой антитело по изобретению и может быть выбран из группы, состоящей из 2.7A4, 2.14H9 или 2.9D10, 2.7A4OPT или 2.14H9OPT.
Другие дополнительные варианты воплощения изобретения включают способы лечения животного, страдающего от неопластической болезни, путем введения животному терапевтически эффективной дозы специфического связывающего агента по изобретению. В определенных вариантах воплощения способ дополнительно включает выбор животного, нуждающегося в лечении неопластической болезни, и введение животному терапевтически эффективной дозы специфического связывающего агента по изобретению.
Другие дополнительные варианты воплощения изобретения включают способы лечения животного, страдающего от не-неопластической болезни, путем введения животному терапевтически эффективной дозы специфического связывающего агента по изобретению. В определенных вариантах воплощения способ дополнительно включает выбор животного, нуждающегося в лечении не-неопластической болезни, и введение животному терапевтически эффективной дозы специфического связывающего агента по изобретению.
Другие дополнительные варианты воплощения изобретения включают способы лечения животного, страдающего от хронической вирусной инфекции, путем введения животному терапевтически эффективной дозы специфического связывающего агента по изобретению. В определенных вариантах воплощения способ дополнительно включает выбор животного, нуждающегося в лечении хронической вирусной инфекции, и введение животному терапевтически эффективной дозы специфического связывающего агента по изобретению.
Другие дополнительные варианты воплощения изобретения включают способы лечения животного, страдающего от злокачественной опухоли, путем введения животному терапевтически эффективной дозы специфического связывающего агента по изобретению. В определенных вариантах воплощения способ дополнительно включает выбор животного, нуждающегося в лечении злокачественной опухоли, и введение животному терапевтически эффективной дозы специфического связывающего агента по изобретению.
Другие дополнительные варианты воплощения изобретения включают способы лечения животного, страдающего от болезни или состояния, ассоциированного с экспрессией B7-H1, путем введения животному терапевтически эффективной дозы специфического связывающего агента по изобретению. В определенных вариантах воплощения способ дополнительно включает выбор животного, нуждающегося в лечении болезни или состояния, ассоциированного с экспрессией B7-H1, и введение животному терапевтически эффективной дозы специфического связывающего агента по изобретению.
Злокачественная опухоль может быть выбрана из группы, состоящей из солидных опухолей, таких как меланома, раки кожи, мелкоклеточный рак легкого, немелкоклеточный рак легкого, глиома, гепатоцеллюлярная (печеночная) карцинома, рак желчного пузыря, опухоль щитовидной железы, рак кости, желудочный рак (рак желудка), рак простаты, рак молочной железы, рак яичника, рак шейки матки, рак матки, вульварный рак, эндометриальный рак, тестикулярный рак, рак мочевого пузыря, рак легкого, глиобластома, эндометриальный рак, рак почки, почечно-клеточная карцинома, рак ободочной кишки, колоректальный рак, рак поджелудочной железы, карцинома пищевода, раки головного мозга/ЦНС, раки головы и шеи, нейрональные раки, мезотелиома, саркомы, билиарный (холангиокарцинома), аденокарцинома тонкой кишки, педиатрические злокачественности, эпидермоидная карцинома, саркомы, рак плевры/перитонеальной мембраны и лейкоз, включая острый миелоидный лейкоз, острый лимфобластный лейкоз, и множественная миелома.
Поддающиеся лечению ассоциированные с пролиферацией или инвазией болезни включают неопластические болезни, такие как меланома, рак кожи, мелкоклеточный рак легкого, немелкоклеточный рак легкого, слюнной железы, глиома, гепатоцеллюлярная (печеночная) карцинома, рак желчного пузыря, опухоль щитовидной железы, рак кости, желудочный рак (рак желудка), рак простаты, рак молочной железы, рак яичника, рак шейки матки, рак матки, вульварный рак, эндометриальный рак, тестикулярный рак, рак мочевого пузыря, рак легкого, глиобластома, рак щитовидной железы, эндометриальный рак, рак почки, рак ободочной кишки, колоректальный рак, рак поджелудочной железы, карцинома пищевода, раки головного мозга/ЦНС, нейрональные раки, головы и шеи, мезотелиома, саркомы, билиарный (холангиокарцинома), аденокарцинома тонкой кишки, педиатрические злокачественности, эпидермоидная карцинома, саркомы, рак плевры/перитонеальной мембраны и лейкоз, включая острый миелоидный лейкоз, острый лимфобластный лейкоз, и множественная миелома. Поддающиеся лечению хронические вирусные инфекции включают ВИЧ, вирус гепатита B (HBV) и вирус гепатита C (HCV) у людей, вирус иммунодефицита (SIV) у обезьян и вирус лимфоцитарного хориоменингита (LCMV) у мышей.
Ассоциированная с болезнью клеточная инвазия и/или пролиферация может быть любой аномальной, нежелательной или патологической клеточной инвазией и/или пролиферацией, например, ассоциированной с опухолью, клеточной инвазией и/или пролиферацией.
В одном варианте воплощения неопластическая болезнь представляет собой солидную опухоль, выбранную из любой из следующих карцином: молочной железы, ободочной кишки, колоректальной, простаты, желудка, желудочной, яичника, пищевода, поджелудочной железы, желчного пузыря, немелкоклеточного рака легкого, щитовидной железы, эндометрия, головы и шеи, почки, почечно-клеточной карциномы, мочевого пузыря и глиом.
В одном варианте воплощения настоящее изобретение пригодно для использования при ингибировании B7-H1 у пациентов с опухолью, зависимой единственно, или частично, от B7-H1.
Другие дополнительные варианты воплощения изобретения включают использование специфического связывающего агента или антитела по изобретению при изготовлении лекарственного средства для лечения животного, страдающего от пролиферативной или ассоциированной с инвазией болезнью. В определенных вариантах воплощения использование дополнительно включает выбор животного, нуждающегося в лечении пролиферативной или ассоциированной с инвазией болезни.
Другие дополнительные варианты воплощения изобретения включают использование специфического связывающего агента или антитела по изобретению при изготовлении лекарственного средства для лечения ассоциированной с пролиферацией или инвазией болезни с B7-H1-медиируемой компонентой у животного. В определенных вариантах воплощения использование дополнительно включает выбор животного, нуждающегося в лечении ассоциированной с пролиферацией или инвазией болезни с B7-H1-медиируемой компонентой.
Другие дополнительные варианты воплощения изобретения включают использование специфического связывающего агента или антитела по изобретению при изготовлении лекарственного средства для лечения инвазии опухолевых клеток, метастазирования клеток или роста опухоли у животного. В определенных вариантах воплощения использование дополнительно включает выбор животного, нуждающегося в лечении инвазии опухолевых клеток, метастазирования клеток или опухоли.
Другие дополнительные варианты воплощения изобретения включают использование специфического связывающего агента или антитела по изобретению при изготовлении лекарственного средства для лечения животного, страдающего от неопластической болезни. В определенных вариантах воплощения использование дополнительно включает выбор животного, нуждающегося в лечении неопластической болезни.
Другие дополнительные варианты воплощения изобретения включают использование специфического связывающего агента или антитела по изобретению при изготовлении лекарственного средства для лечения животного, страдающего от болезни, этиология которой ассоциирована с инфекционным агентом, такой как, например, гепатоцеллюлярная карцинома, желудочный рак или рак шейки матки. В определенных вариантах воплощения использование дополнительно включает выбор животного, нуждающегося в лечении неопластической болезни.
Другие дополнительные варианты воплощения изобретения включают использование специфического связывающего агента или антитела по изобретению при изготовлении лекарственного средства для лечения животного, страдающего от не-неопластической болезни. В определенных вариантах воплощения использование дополнительно включает выбор животного, нуждающегося в лечении не-неопластической болезни.
Другие дополнительные варианты воплощения изобретения включают использование специфического связывающего агента или антитела по изобретению при изготовлении лекарственного средства для лечения животного, страдающего от хронической вирусной инфекции. В определенных вариантах воплощения использование дополнительно включает выбор животного, нуждающегося в лечении не-неопластической болезни. В еще одних вариантах воплощения использование дополнительно включает болезнь глаз, воспалительную болезнь, сердечно-сосудистую болезнь и сепсис.
Другие дополнительные варианты воплощения изобретения включают использование специфического связывающего агента или антитела по изобретению при изготовлении лекарственного средства для лечения животного, страдающего от злокачественной опухоли. В определенных вариантах воплощения использование дополнительно включает выбор животного, нуждающегося в лечении злокачественной опухоли.
Другие дополнительные варианты воплощения изобретения включают использование специфического связывающего агента или антитела по изобретению при изготовлении лекарственного средства для лечения животного, страдающего от болезни или состояния, ассоциированного с экспрессией B7-H1. В определенных вариантах воплощения использование дополнительно включает выбор животного, нуждающегося в лечении болезни или состояния, ассоциированных с экспрессией B7-H1.
Другие дополнительные варианты воплощения изобретения включают специфический связывающий агент или антитело по изобретению для использования в качестве лекарственного средства для лечения животного, страдающего от пролиферативной или ассоциированной с инвазией болезни.
Другие дополнительные варианты воплощения изобретения включают специфический связывающий агент или антитело по изобретению для использования в качестве лекарственного средства для лечения животного, страдающего от инвазии опухолевых клеток, метастазирования клеток или роста опухоли у животного.
Другие дополнительные варианты воплощения изобретения включают специфический связывающий агент или антитело по изобретению для использования в качестве лекарственного средства для лечения животного, страдающего от болезни или состояния, ассоциированных с экспрессией B7-H1.
В одном варианте воплощения лечение
ассоциированной с пролиферацией или инвазией болезни;
неопластической болезни;
не-неопластической болезни;
злокачественной опухоли; или
хронической вирусной инфекции; или
болезни или состояния, ассоциированных с экспрессией B7-H1,
включает ведение, улучшение состояния, предотвращение любой из вышеупомянутых болезней или условий.
В одном варианте воплощения лечение неопластической болезни включает ингибирование роста опухоли, замедление роста опухоли, регрессию опухоли, уменьшение опухоли, увеличение времени повторного роста опухоли после прекращения лечения, увеличение времени до рецидивирования опухоли, замедление прогрессирования болезни.
В одном варианте воплощения лечение болезни или состояния, ассоциированных с экспрессией B7-H1, включает ингибирование роста клеток, экспрессирующих B7-H1.
В некоторых вариантах воплощения после введения специфического связывающего агента или антитела по изобретению вводится выводящий (clearing) агент для удаления избытка циркулирующего антитела из крови.
В некоторых вариантах воплощения изобретения животное, лечение которого должно проводиться, является человеком.
В некоторых вариантах воплощения изобретения специфический связывающий агент представляет собой полностью человеческое моноклональное антитело.
В некоторых вариантах воплощения изобретения специфический связывающий агент выбирают из группы, состоящей из полностью человеческих моноклональных антител 2.7A4, 2.14H9 и 2.9D10.
Варианты воплощения изобретения включают конъюгат, включающий специфический связывающий агент, описанный здесь, и терапевтический агент. В некоторых вариантах воплощения изобретения терапевтический агент представляет собой токсин. В других вариантах воплощения терапевтически агент представляет собой радиоизотоп. В еще одних вариантах воплощения терапевтически агент представляет собой фармацевтическую композицию.
В другом аспекте предусматривается способ селективного уничтожения раковых клеток у пациента. Способ включает введение конъюгата полностью человеческого антитела пациенту. Конъюгат полностью человеческого антитела включает антитело, которое может связываться с B7-H1 и агентом. Агент представляет собой токсин, радиоизотоп или другое вещество, которое будет убивать раковые клетки. Тем самым конъюгат антитела селективно убивает раковые клетки.
В одном аспекте предусматривается конъюгированное полностью человеческое антитело, которое специфически связывается с B7-H1. К антителу присоединен агент, и связывание антитела с клеткой приводит к доставке агента в клетку. В одном варианте воплощения вышеупомянутое конъюгированное полностью человеческое антитело связывается с внеклеточным доменом B7-H1. В другом варианте воплощения антитело и конъюгированный токсин интернализуются клеткой, экспрессирующей B7-H1. В другом варианте воплощения агент представляет собой цитотоксический агент. В другом варианте воплощения агент представляет собой, например, сапорин или иммуноконъюгаты на основе ауристатина, экзотоксина Pseudomonas, гелонина, рицина, калихеамицина или майтансина и т.п. В еще одном варианте воплощения агент представляет собой радиоизотоп.
Специфический связывающий агент или антитело по изобретению могут быть введены сами или могут быть введены в комбинации с дополнительными антителами или химиотерапевтическими лекарственными препаратами, или лучевой терапией, или терапевтическими вакцинами. Например, моноклональная, олигоклональная или поликлональная смесь антител B7-H1, которые блокируют B7-H1-медиируемую репрессию противоопухолевого иммунитета, может быть введена в комбинации с лекарственным препаратом, для которого было показано, что он ингибирует пролиферацию опухолевых клеток.
В соответствии с другим аспектом изобретения, предусматривается фармацевтическая композиция, включающая специфический связывающий агент антитела по изобретению и фармацевтически приемлемый носитель.
Другой вариант воплощения изобретения включает способ диагностики болезни или состояния, в котором раскрытое здесь антитело используется для детектирования присутствия и/или уровня B7-H1 у пациента или во взятом у пациента образце. В одном варианте воплощения взятый у пациента образец представляет собой кровь или сыворотку крови или мочу. В дополнительных вариантах воплощения представлены способы идентификации факторов риска, установления диагноза болезни и определения стадии болезни, предусматривающие идентификацию экспрессии и/или сверхэкспрессии B7-H1 с использованием анти-B7-H1 антител. В некоторых вариантах воплощения способы включают введение пациенту конъюгата полностью человеческого антитела, который селективно связывается с B7-H1 на клетке. Конъюгат антитела включает антитело, которое специфически связывается с B7-H1, и метку. Способы дополнительно включают выявление присутствия метки у пациента. Относительно высокое количество метки будет указывать на относительно высокий риск болезни, а относительно низкое количество метки будет указывать на относительно низкий риск болезни. В одном варианте воплощения метка представляет собой зеленый флуоресцентный белок.
Изобретение дополнительно предусматривает способы оценки присутствия и/или уровня B7-H1 во взятом у пациента образце, включающие введение в контакт антитела, раскрытого здесь, с биологическим образцом, взятым у пациента, и детектирование уровня связывания между указанным антителом и B7-H1 в указанном образце. В более конкретных вариантах воплощения биологический образец представляет собой кровь, плазму или сыворотку.
Другой вариант воплощения изобретения включает способ диагностики состояния, ассоциированного с экспрессией B7-H1 в клетке, путем введения в контакт сыворотки или клетки с антителом, раскрытым здесь, и затем детектирования присутствия B7-H1. В одном варианте воплощения состояние может быть пролиферативной или ассоциированной с инвазией болезнью, включая, без ограничений, неопластическую болезнь.
В другом варианте воплощения изобретение включает набор для анализа, предназначенный для детектирования B7-H1 в тканях, клетках или жидкостях организма млекопитающего. Такой набор будет пригодным для скрининга ассоциированных с B7-H1 болезней. Набор включает специфический связывающий агент или антитело по изобретению и средства, указывающие на протекание реакции специфического связывающего агента или антитела с B7-H1, в случае его присутствия. В одном варианте воплощения антитело представляет собой моноклональное антитело. В одном варианте воплощения антитело, связывающее B7-H1, является меченым. В другом варианте воплощения антитело представляет собой немеченое первичное антитело, и набор дополнительно включает средства детектирования первичного антитела. В одном варианте воплощения средства детектирования включают меченое второе антитело, представляющее собой анти-иммуноглобулин. Антитело может быть меченым с помощью маркера, выбранного из группы, состоящей из флуорохрома, фермента, радионуклида и радионепрозрачного материала.
В некоторых вариантах воплощения специфические связывающие агенты или антитела, раскрытые здесь, могут быть модифицированы для усиления их способности к фиксации комплемента и участию в комплементзависимой цитотоксичности (CDC). В других вариантах воплощения специфические связывающие агенты или антитела могут быть модифицированы для усиления их способности активировать эффекторные клетки и участвовать в антителозависимой цитотоксичности (ADCC). В еще одних вариантах воплощения специфические связывающие агенты или антитела могут быть модифицированы как для усиления их способности активировать эффекторные клетки и участвовать в антителозависимой цитотоксичности (ADCC), так и для усиления их способности к фиксации комплемента и участию в комплементзависимой цитотоксичности (CDC).
В некоторых вариантах воплощения специфические связывающие агенты или антитела, раскрытые здесь, могут быть модифицированы для уменьшения их способности к фиксации комплемента и участию в комплементзависимой цитотоксичности (CDC). В других вариантах воплощения специфические связывающие агенты или антитела могут быть модифицированы для уменьшения их способности активировать эффекторные клетки и участвовать в антителозависимой цитотоксичности (ADCC). В еще одних вариантах воплощения специфические связывающие агенты или антитела, раскрытые здесь, могут быть модифицированы как для уменьшения их способности активировать эффекторные клетки и участвовать в антителозависимой цитотоксичности (ADCC), так и для уменьшения их способности к фиксации комплемента и участию в комплементзависимой цитотоксичности (CDC).
В определенных вариантах воплощения период полувыведения специфического связывающего агента или антитела, раскрытого здесь, и композиций по изобретению составляет, по меньшей мере, от примерно 4 до 7 дней. В определенных вариантах воплощения средний период полувыведения специфического связывающего агента или антитела, раскрытого здесь, и композиций по изобретению составляет, по меньшей мере, от примерно 2 до 5 дней, от 3 до 6 дней, от 4 до 7 дней, от 5 до 8 дней, от 6 до 9 дней, от 7 до 10 дней, от 8 до 11 дней, от 8 до 12, от 9 до 13, от 10 до 14, от 11 до 15, от 12 до 16, от 13 до 17, от 14 до 18, от 15 до 19 или от 16 до 20 дней. В других вариантах воплощения средний период полувыведения специфического связывающего агента или антитела, раскрытого здесь, и композиций по изобретению, составляет, по меньшей мере, примерно от 17 до 21 дней, от 18 до 22 дней, от 19 до 23 дней, от 20 до 24 дней, от 21 до 25, дней, от 22 до 26 дней, от 23 до 27 дней, от 24 до 28 дней, от 25 до 29 дней или от 26 до 30 дней. В других дополнительных вариантах воплощения период полувыведения специфического связывающего агента или антитела, раскрытого здесь, и композиций по изобретению может составлять до примерно 50 дней. В определенных вариантах воплощения периоды полувыведения антител и композиций по изобретению могут быть увеличены способами, известными специалистам. Такое увеличение продолжительности может, в свою очередь, уменьшить количество и/или частоту введения доз композиций антител. Антитела с улучшенными периодами полувыведения in vivo и способы их получения раскрыты в патенте США № 6277375 и международных публикациях №№ WO 98/23289 и WO 97/3461.
В другом варианте воплощения изобретение предусматривает изделие, включающее контейнер. Контейнер содержит композицию, включающую специфический связывающий агент или антитело, раскрытые здесь, и вкладыш в упаковку или метку, указывающие, что композиция может быть использована для лечения болезней, ассоциированных с клеточной адгезией, инвазией, ангиогенезом и/или пролиферацией, включая, без ограничений, болезни, характеризующиеся экспрессией или сверхэкспрессией B7-H1.
В других вариантах воплощения изобретение предусматривает набор для лечения болезни, связанной с экспрессией B7-H1, включающий специфический связывающий агент или антитело, раскрытые здесь, и инструкции по введению моноклональных антител субъекту, нуждающемуся в лечении.
Настоящее изобретение предусматривает составление композиции белков, включающих вариант Fc-участка. Под этим подразумевается Fc-участок неприродного происхождения, например, Fc-участок, включающий один или несколько неприродных аминокислотных остатков. Варианты Fc-участков по настоящему изобретению также охватывают Fc-участки, включающие делеции, вставки и/или модификации аминокислот.
Период полувыведения из сыворотки белков, содержащих Fc-участки, может быть увеличен путем повышения аффинности связывания Fc-участка с FcRn. В одном варианте воплощения вариант Fc-белка имеет увеличенный период полувыведения из сыворотки по сравнению с молекулой сравнения.
В другом варианте воплощения настоящее изобретение предусматривает вариант Fc, в котором Fc-участок включает, по меньшей мере, одну неприродную аминокислоту в одной или нескольких позициях, выбранных из группы, состоящей из 239, 330 и 332, пронумерованных в соответствии с индексом EU, как описано в Кабат (Kabat). В конкретном варианте воплощения настоящее изобретение предусматривает вариант Fc, в котором Fc-участок включает, по меньшей мере, одну неприродную аминокислоту, выбранную из группы, состоящей из 239D, 330L и 332E, пронумерованных в соответствии с индексом EU, как описано в Кабат. Необязательно, Fc-участок может дополнительно включать дополнительную неприродную аминокислоту в одной или нескольких позициях, выбранных из группы, состоящей из 252, 254 и 256, пронумерованных в соответствии с индексом EU, как описано в Кабат. В конкретном варианте воплощения настоящее изобретение предусматривает вариант Fc, в котором Fc-участок включает, по меньшей мере, одну неприродную аминокислоту, выбранную из группы, состоящей из 239D, 330L и 332E, пронумерованных в соответствии с индексом EU, как описано в Кабат, и по меньшей мере одна неприродная аминокислота в одной или нескольких позициях выбрана из группы, состоящей из 252Y, 254T и 256E, пронумерованных в соответствии с индексом EU, как описано в Кабат.
В другом варианте воплощения настоящее изобретение предусматривает вариант Fc, в котором Fc-участок включает, по меньшей мере, одну неприродную аминокислоту в одной или нескольких позициях, выбранных из группы, состоящей из 234, 235 и 331, пронумерованных в соответствии с индексом EU, как описано в Кабат. В конкретном варианте воплощения настоящее изобретение предусматривает вариант Fc, в котором Fc-участок включает, по меньшей мере, одну неприродную аминокислоту, выбранную из группы, состоящей из 234F, 235F, 235Y, 235E и 331S, пронумерованных в соответствии с индексом EU, как описано в Кабат. В еще одном конкретном варианте воплощения вариант Fc по изобретению включает неприродные аминокислотные остатки 234F, 235F и 331S, пронумерованные в соответствии с индексом EU, как описано в Кабат. В другом конкретном варианте воплощения вариант Fc по изобретению включает неприродные аминокислотные остатки 234F, 235Y и 331S, пронумерованные в соответствии с индексом EU, как описано Кабат. В другом конкретном варианте воплощения вариант Fc по изобретению включает неприродные аминокислотные остатки 234F, 235E и 331S, пронумерованные в соответствии с индексом EU, как описано в Кабат. Необязательно, Fc-участок может дополнительно включать дополнительную неприродную аминокислоту в одной или нескольких позициях, выбранных из группы, состоящей из 252, 254 и 256, пронумерованных в соответствии с индексом EU, как описано в Кабат. В конкретном варианте воплощения настоящее изобретение предусматривает вариант Fc, в котором Fc-участок включает, по меньшей мере, одну неприродную аминокислоту, выбранную из группы, состоящей из 234F, 235F, 235Y, 235E и 331S, пронумерованных в соответствии с индексом EU, как описано в Кабат; по меньшей мере, одну неприродную аминокислоту, выбранную из группы, состоящей из 234F, 235F и 331S, пронумерованных в соответствии с индексом EU, как описано в Кабат, и, по меньшей мере, одна неприродная аминокислота в одной или нескольких позициях выбрана из группы, состоящей из 252Y, 254T и 256E, пронумерованных в соответствии с индексом EU, как описано в Кабат. В используемом здесь значении, обозначения «OPT» и «TM» являются синонимами и используются для описания антител по изобретению, сконструированных с целью введения трех мутаций; L234F и L235E в шарнирной области и P331S в CH2-домене молекулы IgG для удаления его способности инициировать антителозависимую клеточно-опосредованную цитотоксичность и комплементзависимую цитотоксичность (Oganesyan V. et al. (2008), Acta Cryst., D64: 700-704).
В другом варианте воплощения настоящее изобретение предусматривает композицию варианта белка Fc, в котором Fc-участок включает, по меньшей мере, неприродную аминокислоту в одной или нескольких позициях, выбранных из группы, состоящей из 239, 330 и 332, пронумерованных в соответствии с индексом EU, как описано в Кабат. В конкретном варианте воплощения настоящее изобретение предусматривает композицию варианта белка Fc, в котором Fc-участок включает, по меньшей мере, одну неприродную аминокислоту, выбранную из группы, состоящей из 239D, 330L и 332E, пронумерованных в соответствии с индексом EU, как описано в Кабат. Необязательно, Fc-участок может дополнительно содержать дополнительную неприродную аминокислоту в одной или нескольких позициях, выбранных из группы, состоящей из 252, 254 и 256, пронумерованных в соответствии с индексом EU, как описано в Кабат. В конкретном варианте воплощения настоящее изобретение предусматривает композицию варианта белка Fc, в котором Fc-участок включает, по меньшей мере, одну неприродную аминокислоту, выбранную из группы, состоящей из 239D, 330L и 332E, пронумерованных в соответствии с индексом EU, как описано в Кабат, и, по меньшей мере, одна неприродная аминокислота в одной или нескольких позициях выбрана из группы, состоящей из 252Y, 254T и 256E, пронумерованных в соответствии с индексом EU, как описано в Кабат.
В другом варианте воплощения настоящее изобретение предусматривает композицию варианта белка Fc, в котором Fc-участок включает, по меньшей мере, одну неприродную аминокислоту в одной или нескольких позициях, выбранных из группы, состоящей из 234, 235 и 331, пронумерованных в соответствии с индексом EU, как описано в Кабат. В конкретном варианте воплощения настоящее изобретение предусматривает композицию варианта белка Fc, в котором Fc-участок включает, по меньшей мере, одну неприродную аминокислоту, выбранную из группы, состоящей из 234F, 235F, 235Y, 235E и 331S, пронумерованных в соответствии с индексом EU, как описано в Кабат. Необязательно, Fc-участок может дополнительно включать дополнительную неприродную аминокислоту в одной или нескольких позициях, выбранных из группы, состоящей из 252, 254 и 256, пронумерованных в соответствии с индексом EU, как описано в Кабат. В конкретном варианте воплощения настоящее изобретение предусматривает композицию варианта белка Fc, в котором Fc-участок включает, по меньшей мере, одну неприродную аминокислоту, выбранную из группы, состоящей из 234F, 235F, 235Y, 235E и 331S, пронумерованных в соответствии с индексом EU, как описано в Кабат; и, по меньшей мере, одна неприродная аминокислота в одной или нескольких позициях выбрана из группы, состоящей из 252Y, 254T и 256E, пронумерованных в соответствии с индексом EU, как описано в Кабат.
Способы получения неприродных Fc-участков известны специалистам. Например, аминокислотные замещения и/или делеции могут быть созданы методами мутагенеза, включая, без ограничений, сайт-направленный мутагенез (Kunkel, Proc. Natl. Acad. Sci. USA 82:488-492 (1985)), ПЦР (PCR) мутагенез (Higuchi, в "PCR Protocols: A Guide to Methods and Applications", Academic Press, San Diego, pp. 177-183 (1990)) и кассетный мутагенез (Wells et al., Gene 34:315-323 (1985)). Предпочтительно, сайт-направленный мутагенез осуществляют методом ПЦР-удлинения с перекрытием (Higuchi, в "PCR Technology: Principles and Applications for DNA Amplification", Stockton Press, New York, pp. 61-70 (1989)). Методика ПЦР-удлинения с перекрытием (Higuchi, ibid.) также может быть использована для введения любой желательной мутации (мутаций) в последовательность-мишень (исходную ДНК). Например, первый раунд ПЦР в методе удлинения с перекрытием включает амплификацию последовательности-мишени с внешним праймером (праймер 1) и внутренним праймером мутагенеза (праймер 3), и отдельно со вторым внешним праймером (праймер 4) и внутренним праймером (праймер 2), с образованием двух сегментов ПЦР (сегменты A и B). Внутренний праймер мутагенеза (праймер 3) сконструирован так, чтобы он содержал несовпадения с последовательностью-мишенью, определяющие желательную мутацию (мутации). Во втором раунде ПЦР продукты первого раунда ПЦР (сегменты A и B) амплифицируют методом ПЦР с использованием двух внешних праймеров (праймеры 1 и 4). Полученный полноразмерный сегмент ПЦР (сегмент C) гидролизуют рестрикцирующими ферментами, и полученный фрагмент рестрикции клонируют в пригодный вектор. На первой стадии мутагенеза исходную ДНК (например, кодирующую слитый белок Fc, антитело или просто Fc-участок) функционально клонируют в вектор мутагенеза. Праймеры сконструированы так, чтобы они отображали желательное аминокислотное замещение. Другие способы получения вариантов Fc-участков известны специалистам (см., например, патенты США №№ 5624821; 5885573; 5677425; 6165745; 6277375; 5869046; 6121022; 5624821; 5648260; 6528624; 6194551; 6737056; 6821505; 6277375; патентные публикации США №№ 2004/0002587 и публикации PCT WO 94/29351; WO 99/58572; WO 00/42072; WO 02/060919; WO 04/029207; WO 04/099249; WO 04/063351).
В некоторых вариантах воплощения изобретения приведенные здесь схемы (patterns) гликозилирования антител модифицированы с целью усиления эффекторной функции ADCC и CDC. См. Shields RL et al., (2002) JBC. 277:26733; Shinkawa T et al., (2003) JBC. 278:3466, и Okazaki A et al., (2004) J. Mol. Biol., 336:1239. В некоторых вариантах воплощения вариант белка Fc включает одну или несколько сконструированных гликоформ, т.е. углеводных композиций, ковалентно присоединенных к молекуле, содержащей участок Fc. Сконструированные гликоформы могут быть пригодными для различных целей, включая, без ограничений, усиление или ослабление эффекторной функции. Сконструированные гликоформы могут быть получены любым способом, известным квалифицированному специалисту в данной области техники, например, путем использования генно-модифицированных или вариантных экспрессионных штаммов, путем коэкспрессии с одним или несколькими ферментами, например, DI N-ацетилглюкозаминилтрансферазы III (GnTI11), путем экспрессирования молекулы, включающей Fc-участок, в различных организмах или клеточных линиях от различных организмов, или путем модификации углевода (углеводов) после экспрессии молекулы, включающей Fc-участок. Способы получения генно-модифицированных гликоформ известны специалистам и включают, без ограничений, описанные Umana et al., 1999, Nat. Biotechnol 17:176-180; Davies et al., 20017 Biotechnol Bioeng 74:288-294; Shields et al., 2002, J Biol Chem 277:26733-26740; Shinkawa et al., 2003, J Biol Chem 278:3466-3473; патент США № 6602684; заявку США № 10/277370; заявку США № 10/113929; PCT WO 00/61739A1; PCT WO 01/292246A1; PCT WO 02/311140A1; PCT WO 02/30954A1; технологию Potillegent™ (Biowa, Inc. Princeton, N.J.); технологию генно-модифицированного гликозилирования GlycoMAb™ (GLYCART biotechnology AG, Zurich, Switzerland). См., например, WO 00061739; EA01229125; US 20030115614; Okazaki et al., 2004, JMB, 336:1239-49.
Специалистам также известно, что гликозилирование Fc-участка может быть модифицировано с целью усиления или ослабления эффекторной функции (см., например, Umana et al., 1999, Nat. Biotechnol 17:176-180; Davies et al., 2001, Biotechnol Bioeng 74:288-294; Shields et al., 2002, J Biol Chem 277:26733-26740; Shinkawa et al., 2003, J Biol Chem 278:3466-3473), патент США № 6602684; заявка США № 10/277370; заявка США № 10/113929; PCT WO 00/61739A1; PCT WO 01/292246A1; PCT WO 02/311140A1; PCT WO 02/30954A1; технология Potillegent™ (Biowa, Inc. Princeton, N.J.); технология генно-модифицированного гликозилирования GlycoMAb™ (GLYCART biotechnology AG, Zurich, Switzerland). Соответственно, в одном варианте воплощения Fc-участки антител по изобретению включают видоизмененное гликозилирование аминокислотных остатков. В другом варианте воплощения видоизмененное гликозилирование аминокислотных остатков приводит к пониженной эффекторной функции. В другом варианте воплощения видоизмененное гликозилирование аминокислотных остатков приводит к повышенной эффекторной функции. В конкретном варианте воплощения Fc-участок имеет пониженное фукозилирование. В другом варианте воплощения Fc-участок является афукозилированным (см., например, публикацию патентной заявки США № 2005/0226867).
Краткое описание чертежей
Фиг. 1 представляет собой столбчатую диаграмму, демонстрирующую влияние анти-B7-H1 антител по изобретению на пролиферацию T-клеток при проведении анализа на бусинах.
Фиг. 2 представляет собой столбчатую диаграмму, демонстрирующую усиление пролиферации T-клеток анти-B7-H1 антителами по изобретению при проведении анализа методом DCMLR.
Фиг. 3 представляет собой столбчатую диаграмму, демонстрирующую высвобождение IFN-γ анти-B7-H1 антителами по изобретению при проведении анализа методом DCMLR.
Фиг. 4 представляет собой график, демонстрирующий 95% доверительный интервал для величины IC50 анти-B7-H1 анти-B7-H1 антител по изобретению при проведении анализа методом ингибирования лиганда человеческого PD1/человеческого B7-H1 для оценки влияния переключения класса IgG и гуманизирования (germlining) на активность антитела.
Фиг. 5 представляет собой линейный график, демонстрирующий результаты анализа методом ELISA, проведенного для оценки перекрестной реактивности анти-B7-H1 антитела по изобретению по отношению к комодулирующим антигенам.
Фиг. 6 представляет собой столбчатую диаграмму, демонстрирующую эффекты анти-B7-H1 антител по изобретению при проведении анализа in vitro методом Tet-recall.
Фиг. 7 представляет собой столбчатую диаграмму, демонстрирующую результаты тестирования агонистической активности анти-B7-H1 антител по изобретению с использованием анализа методом Tet-recall.
Фиг. 8A/B/C представляют собой линейные графики, демонстрирующие эффект анти-B7-H1 антител по изобретению на клетки HPAC в мышиной модели ксенотрансплантата.
Фиг. 9A/B/C представляют собой линейные графики, демонстрирующие эффект анти-B7-H1 антител по изобретению на клетки A375 в мышиной модели ксенотрансплантата.
Фиг. 10A/B представляют собой линейные графики, демонстрирующие эффект анти-B7-H1 антител по изобретению на клетки HPAC в мышиной модели ксенотрансплантата.
Фиг. 11 представляет собой линейный график, демонстрирующий эффект анти-B7-H1 антител по изобретению на клетки HPAC в мышиной модели ксенотрансплантата.
Фиг. 12A/B/C/D представляют собой линейные графики, демонстрирующие эффект анти-B7-H1 антител по изобретению на клетки A375 в мышиной модели ксенотрансплантата.
Фиг. 13A/B представляют собой линейные графики, демонстрирующие эффект анти-B7-H1 антител по изобретению на клетки A375 в мышиной модели ксенотрансплантата в присутствии T-клеток и без них.
Фиг. 14A/B представляют собой линейные графики, демонстрирующие эффект анти-B7-H1 антител по изобретению на клетки A375 в мышиной модели ксенотрансплантата в присутствии T-клеток и без них.
Фиг. 15 представляет собой линейный график, демонстрирующий эффект анти-B7-H1 антител по изобретению на клетки A375 в мышиной модели ксенотрансплантата.
Определения
Если не будет указано иное, то научные и технические термины, используемые в данном описании, должны иметь значения, являющиеся общепринятыми для рядовых специалистов в данной области техники. Дополнительно, если иное не следует из контекста, термины в единственном числе включают множественное число, и термины во множественном числе включают единственное число. В общем, номенклатуры, используемые в связи с и методики клеточных и тканевых культур, молекулярной биологии и химии белка и олиго- или полинуклеотидов и гибридизации, описанные здесь, являются хорошо известными и общепринятыми в данной области техники.
Стандартные методики используются для получения рекомбинантных ДНК, синтеза олигонуклеотидов и культур тканей и трансформации (например, электропорация, липофекция). Ферментативные реакции и методики очистки выполняются в соответствии с указаниями производителей или общепринятыми в данной области методами или как описано здесь. Вышеупомянутые методики и процедуры обычно осуществляются в соответствии с обычными методами, хорошо известными специалистам, и как описано в различных общих и более специализированных источниках, упомянутых и обсуждаемых в данном описании. См., например, Sambrook et al. Molecular Cloning: A Laboratory Manual (3rd ed., Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y. (2001)), который включен сюда в качестве ссылки. Номенклатуры и лабораторные процедуры и методики, используемые в связи с аналитической химией, химией органического синтеза и медицинской и фармацевтической химией, описанные здесь, являются хорошо известными и общепринятыми в данной области. Стандартные методики используются для химических синтезов, химических анализов, изготовления фармацевтических препаратов, составления рецептур и доставки, и лечения пациентов.
При использовании в соответствии с данным описанием, следующие термины, если не будет указано иное, должны пониматься как имеющие такие значения:
Антагонист или ингибитор может быть полипептидом, нуклеиновой кислотой, углеводом, липидом, низкомолекулярным соединением, олигонуклеотидом, олигопептидом, интерферирующей РНК (RNAi), антисмысловым, рекомбинантным белком, антителом или их фрагментами или конъюгатами или их слитыми белками. Обзор RNAi сделан http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Retrieve&db=pubmed&dopt=Abstract&list_uids=14657420&query_hl=2 (Pharmacol Rev. 2003 Dec; 55(4):629-48. Review), а антисмысловых соединений - http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Retrieve&db=pubmed&dopt=Abstract&list_uids=14583589&query_hl=2 (Sci STKE. 2003 Oct 28; 2003 (206):pe47).
Соединение относится к любому низкомолекулярному соединению с молекулярным весом менее примерно 2000 дальтон.
Термин «B7-H1» относится к человеческим B7-H, B7H1, B7-H1, B7 гомологу 1, CD274 антигену, PDCD1L1, PDCD1LG1, PDCD1 лиганду 1, PDL1, PD-L1, прекурсору лиганда 1 запрограммированной клеточной смерти 1 или лиганду 1 запрограммированной смерти.
Термин «нейтрализующий» или «ингибирующий» при упоминании специфического связывающего агента, такого как антитело, относится к способности указанного агента устранять, ослаблять или значительно ослаблять активность антигена-мишени. Соответственно, «нейтрализующее» анти-B7-H1 антитело по изобретению способно устранять или значительно ослаблять активность B7-H1. Нейтрализующее, антагонизирующее или ингибирующее антитело, которое специфически связывает B7-H1, может, например, действовать путем блокирования связывания B7-H1 с его родственными лигандами. Идеально, нейтрализующее антитело против B7-H1 ингибирует B7-H1-медиируемую репрессию T-клеточного иммунитета. Нейтрализующее, антагонизирующее или ингибирующее антитело, которое специфически связывает B7-H1, может, например, действовать путем ингибирования связывания B7-H1 с PD-1 и/или с B7-1.
«Ингибирование биологической активности B7-H1» охватывает ингибирование активности B7-H1 на по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 15%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 35%, по меньшей мере 40%, по меньшей мере 45%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95%, по сравнению с биологической активностью в отсутствие специфического связывающего агента или антитела по изобретению.
Термин «полипептид» используется здесь как родовой термин для описания нативного белка, фрагментов или аналогов полипептидной последовательности. Таким образом, нативный белок, фрагменты и аналоги рассматриваются как виды рода полипептидов. Предпочтительные полипептиды в соответствии с изобретением включают человеческую тяжелую цепь молекул иммуноглобулина и человеческую каппа-легкую цепь молекул иммуноглобулина, а также молекулы антитела, образованные комбинациями, включающими тяжелую цепь молекулы иммуноглобулина с легкой цепью молекул иммуноглобулина, такой как каппа- или лямбда-легкой цепью молекул иммуноглобулина, и наоборот, а также их фрагменты и аналоги. Предпочтительные полипептиды в соответствии с изобретением могут также включать только человеческую тяжелую цепь молекул иммуноглобулина или ее фрагменты.
Термин «природный» в используемом здесь значении по отношению к объекту указывает на тот факт, что объект может быть найден в природе. Например, полипептидная или полинуклеотидная последовательность, присутствующая в организме (включая вирусы), которая может быть выделена из природного источника и не была целенаправленно модифицирована человеком в лаборатории или иначе, имеет природное происхождение.
Термин «контрольная последовательность» в используемом здесь значении относится к полинуклеотидной последовательности, которая является необходимой для того, чтобы вызвать или повлиять на экспрессию и процессинг кодирующих последовательностей, с которыми она связана. Природа таких контрольных последовательностей меняется в зависимости от организма-хозяина; у прокариотов такие контрольные последовательности обычно включают промотор, рибосомальный сайт связывания и последовательность терминации транскрипции; у эукариотов, обычно, такие контрольные последовательности могут включать промоторы, энхансеры, интроны, последовательности терминации транскрипции, последовательности сигнала полиаденилирования и 5'- и 3'-нетранслированные участки. Предполагается, что термин «контрольные последовательности» включает, как минимум, все компоненты, присутствие которых является существенным для экспрессии и процессинга, и может также включать дополнительные компоненты, присутствие которых является предпочтительным, например, лидерные последовательности и последовательности партнеров слияния.
Термин «полинуклеотид», упоминаемый здесь, обозначает полимерную форму нуклеотидов длиной, по меньшей мере, 10 оснований, которые могут быть рибонуклеотидами или дезоксинуклеотидами или модифицированной формой любого из этих типов нуклеотидов, или гетеродуплексы РНК-ДНК. Термин включает одно- и двухцепочечные формы ДНК.
Термин «олигонуклеотид», упоминаемый здесь, включает природные и модифицированные нуклеотиды, соединенные природными и неприродными связями. Олигонуклеотиды являются подгруппой полинуклеотидов, обычно включающей длину 200 оснований или меньше. Предпочтительно, олигонуклеотиды имеют в длину от 10 до 60 оснований, наиболее предпочтительно - 12, 13, 14, 15, 16, 17, 18, 19, или от 20 до 40 оснований в длину. Олигонуклеотиды обычно являются одноцепочечными, например, для зондов; хотя олигонуклеотиды могут быть двухцепочечными, например, для использования при сооружении генного мутанта. Олигонуклеотиды могут быть смысловыми или антисмысловыми олигонуклеотидами.
Термин «природные нуклеотиды», упоминаемый здесь, включает дезоксирибонуклеотиды и рибонуклеотиды. Термин «модифицированные нуклеотиды», упоминаемый здесь, включает нуклеотиды с модифицированными или замещенными группами сахаров и т.п. Термин «олигонуклеотидные связи», упоминаемый здесь, включает олигонуклеотидные связи, такие как фосфоротиоатные, фосфородитиоатные, фосфороселеноатные, фосфородиселеноатные, фосфороанилотиоатные, фосфораниладатные, фосфороамидатные и т.п. См., например, LaPlanche et al. Nucl. Acids Res. 14:9081 (1986); Stec et al. J. Am. Chem. Soc. 106:6077 (1984); Stein et al. Nucl. Acids Res. 16:3209 (1988); Zon et al. Anti-Cancer Drug Design 6:539 (1991); Zon et al. Oligonucleotides and Analogues: A Practical Approach, pp. 87-108 (F. Eckstein, Ed., Oxford University Press, Oxford England (1991)); Stec et al. патент США № 5151510; Uhlmann and Peyman Chemical Reviews 90:543 (1990), описания которых настоящим включены сюда в качестве ссылок. Олигонуклеотид, при необходимости, может включать метку для детектирования.
Термин «селективно гибридизоваться», упоминаемый здесь, означает детектируемое и специфическое связывание. Полинуклеотиды, олигонуклеотиды и их фрагменты селективно гибридизуются с цепями нуклеиновой кислоты в условиях гибридизации и отмывки, минимизирующих значительную величину детектируемого связывания с неспецифическими нуклеиновыми кислотами. Условия высокой жесткости могут быть использованы для достижения условий селективной гибридизации, как известно специалистам и описано здесь. Обычно гомология последовательностей нуклеиновой кислоты между полинуклеотидами, олигонуклеотидами или фрагментами антител и последовательностью нуклеиновой кислоты, представляющей интерес, будет составлять, по меньшей мере, 80%, и более типично с возрастающими в порядке предпочтительности величинами гомологиями, составляющими, по меньшей мере, 85%, 90%, 95%, 99% и 100%.
Жесткие условия гибридизации включают, без ограничения, гибридизацию со связанной с фильтром ДНК в 6× хлориде натрия/цитрате натрия (SSC) (0,9 М NaCl/90 мМ цитрата Na, pH 7,0) при примерно 45°C с последующими одним или несколькими промываниями в 0,2× SSC/0,1% ДСН (SDS) при примерно 50-65°C, очень жесткие условия, такие как гибридизация со связанной с фильтром ДНК в 6× SSC при примерно 45°C с последующими одним или несколькими промываниями в 0,1× SSC/0,2% ДСН при примерно 60°C, или любые другие жесткие условия гибридизации, известные квалифицированным специалистам (см., например, Ausubel, F.M. et al., eds. 1989 Current Protocols in Molecular Biology, vol. 1, Green Publishing Associates, Inc. и John Wiley and Sons, Inc., NY, на страницах 6.3.1-6.3.6 и 2.10.3).
Две аминокислотные последовательности являются «гомологичными», если существует частичная или полная идентичность между их последовательностями. Например, 85% гомологии означает, что 85% аминокислот являются идентичными при выравнивании двух последовательностей с максимальным совпадением. Пробелы (в любой из двух сравниваемых последовательностей) разрешаются для максимизации совпадений; длина пробелов 5 или меньше является предпочтительной, 2 или меньше - более предпочтительной. Альтернативно и предпочтительно, две белковые последовательности (или производные от них полипептидные последовательности длиной, по меньшей мере, примерно 30 аминокислот) являются гомологичными, в используемом здесь значении этого термина, если они имеют оценку выравнивания не более 5 (в стандартных единицах отклонения) с использованием программы ALIGN с матрицей данных мутации и штрафом за открытие пробела 6 или больше. См. Dayhoff, M.O., в: Atlas of Protein Sequence and Structure, pp. 101-110 (Volume 5, National Biomedical Research Foundation (1972)) и Приложение (Supplement) 2 к этому тому, страницы 1-10. Две последовательности или их части, более предпочтительно, являются гомологичными, если аминокислоты являются не менее чем на 50% идентичными при оптимальном выравнивании с использованием программы ALIGN. Следует понимать, что могут существовать разные участки гомологии в двух ортологичных последовательностях. Например, функциональные сайты мышиных и человеческих ортологов могут иметь более высокую степень гомологии, чем нефункциональные области.
Термин «соответствует» используется здесь для обозначения того, что полинуклеотидная последовательность является гомологичной (т.е. является идентичной, не будучи строго эволюционно родственной) всей или части эталонной полинуклеотидной последовательности, или что полипептидная последовательность является идентичной эталонной полипептидной последовательности.
В отличие от этого, термин «комплементарный по отношению к» используется здесь для обозначения того, что комплементарная последовательность является гомологичной ко всей или части эталонной полинуклеотидной последовательности. Для иллюстрации, нуклеотидная последовательность «TATAC» соответствует эталонной последовательности «TATAC» и является комплементарной к эталонной последовательности «GTATA».
Термин «идентичность последовательности» означает, что две полинуклеотидные или аминокислотные последовательности являются идентичными (т.е. на основании попарного сравнения нуклеотидов или остатков) в окне сравнения. Термин «процент идентичности последовательности» рассчитывают путем сравнения двух оптимально выровненных последовательностей в окне сравнения, определения числа позиций, в которых находятся идентичные основания нуклеиновой кислоты (например, A, T, C, G, U или I) или аминокислотного остатка в обеих последовательностях, с получением числа совпадающих позиций, деления числа совпадающих позиций на общее число позиций в окне сравнения (т.е. размер окна) и умножения результата на 100 с получением процента идентичности последовательностей. Термины «существенная идентичность» в используемом здесь значении подразумевает характеристику полинуклеотидной или аминокислотной последовательности, в которой полинуклеотид или аминокислота включает последовательность, имеющую, по меньшей мере, 85 процентов идентичности последовательности, предпочтительно, по меньшей мере, 90-95 процентов идентичности последовательности, более предпочтительно, по меньшей мере, 99 процентов идентичности последовательности, по сравнению с эталонной последовательностью в окне сравнения, состоящем из, по меньшей мере, 18 нуклеотидных (6 аминокислотных) позиций, часто, в окне, состоящем из, по меньшей мере, 24-48 нуклеотидных (8-16 аминокислотных) позиций, где процент идентичности последовательности рассчитывают путем сравнения эталонной последовательности с последовательностью, которая может включать делеции или вставки, составляющие в общем 20 процентов или меньше от эталонной последовательности в окне сравнения. Эталонная последовательность может быть подмножеством большей по размеру последовательности. В используемом здесь значении, двадцать обычных аминокислот и их сокращенные обозначения соответствуют общепринятой практике. См. Immunology - A Synthesis (2nd Edition, E.S. Golub and D.R. Gren, Eds., Sinauer Associates, Sunderland, Mass. (1991)), которая включена сюда в качестве ссылки. Стереоизомеры (например, D-аминокислоты) двадцати обычных аминокислот, неприродные аминокислоты, такие как α-,α-дизамещенные аминокислоты, N-алкиламинокислоты, молочная кислота и другие нестандартные аминокислоты также могут быть пригодными компонентами полипептидов по настоящему изобретению. Примеры нестандартных аминокислот включают: 4-гидроксипролин, γ-карбоксиглутамат, ε-N,N,N-триметиллизин, ε-N-ацетиллизин, O-фосфосерин, N-ацетилсерин, N-формилметионин, 3-метилгистидин, 5-гидроксилизин, σ-N-метиларгинин и другие подобные аминокислоты и иминокислоты (например, 4-гидроксипролин). В используемой здесь системе обозначений полипептидов, направление влево соответствует направлению к аминоконцу, и направление вправо соответствует направлению к карбоксильному концу, в соответствии со стандартным использованием и принятыми правилами. Аналогично, если не указано иное, левый конец одноцепочечных полинуклеотидных последовательностей является 5'-концом; направление влево для двухцепочечных полинуклеотидных последовательностей называется направлением к 5'-концу. Направление удлинения образующихся транскриптов РНК от 5'- к 3'-концу называется направлением транскрипции; участки последовательности ДНК цепи, имеющие такую же последовательность, как и РНК, и ориентированные 5'-концом к 5'-концу РНК-транскрипта, называются «предшествующими последовательностями»; участки последовательности ДНК-цепи, имеющие такую же последовательность, как и РНК, и ориентированные 3'-концом к 3'-концу РНК-транскрипта, называются «последующими последовательностями». По отношению к полипептидам, термин «существенная идентичность» означает, что две пептидные последовательности, при оптимальном выравнивании, таком как с помощью программ GAP или BESTFIT с использованием веса пробелов по умолчанию, имеют, по меньшей мере, 80 процентов идентичности последовательностей, предпочтительно, по меньшей мере, 90 процентов идентичности последовательностей, более предпочтительно, по меньшей мере, 95 процентов идентичности последовательностей и наиболее предпочтительно, по меньшей мере, 99 процентов идентичности последовательностей. Предпочтительно, позиции остатков, не являющихся идентичными, различаются консервативными аминокислотными замещениями. Консервативные аминокислотные замещения относятся к взаимозаменяемости остатков, имеющих схожие боковые цепи. Например, группа аминокислот, имеющих алифатические боковые цепи, состоит из глицина, аланина, валина, лейцина и изолейцина; группа аминокислот, имеющих алифатические гидроксилсодержащие боковые цепи, состоит из серина и треонина; группа аминокислот, имеющих амидсодержащие боковые цепи, состоит из аспарагина и глутамина; группа аминокислот, имеющих ароматические боковые цепи, состоит из фенилаланина, тирозина и триптофана; группа аминокислот, имеющих основные боковые цепи, состоит из лизина, аргинина и гистидина; и группа аминокислот, имеющих серосодержащие боковые цепи, состоит из цистеина и метионина. Предпочтительными группами консервативных аминокислотных замещений являются: валин-лейцин-изолейцин, фенилаланин-тирозин, лизин-аргинин, аланин-валин, глутаминовая-аспарагиновая кислоты и аспарагин-глутамин. Как описано здесь, незначительные вариации аминокислотных последовательностей антител или молекул иммуноглобулина рассматриваются как входящие в настоящее изобретение, при условии, что варианты аминокислотных последовательностей сохраняют, по меньшей мере, 75%, более предпочтительно, по меньшей мере, 80%, 90%, 95%, и наиболее предпочтительно, 99% идентичности последовательностей с антителами или молекулами иммуноглобулина, описанными здесь. В частности, предусматриваются консервативные аминокислотные замещения. Консервативными являются замещения, происходящие в пределах семейства аминокислот, имеющих родственные боковые цепи. Генетически кодируемые аминокислоты в общем делятся на семейства: (1) кислотные = аспартат, глутамат; (2) основные = лизин, аргинин, гистидин; (3) неполярные = аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин, триптофан; и (4) незаряженные полярные = глицин, аспарагин, глутамин, цистеин, серин, треонин, тирозин. Более предпочтительными семействами являются: серин и треонин, составляющие алифатическое гидроксилсодержащее семейство; аспарагин и глутамин - амидсодержащее семейство; аланин, валин, лейцин и изолейцин - алифатическое семейство; и фенилаланин, триптофан и тирозин - ароматическое семейство. Например, разумно ожидать, что отдельное замещение лейцина на изолейцин или валин, аспартата на глутамат, треонина на серин или подобное замещение аминокислоты на структурно родственную аминокислоту не будет иметь значительного влияния на функцию связывания или свойства полученной молекулы, особенно, если замещение не затрагивает аминокислоту в каркасном сайте. Приводит ли замена аминокислоты к получению функционального пептида, можно легко определить путем оценки специфической активности полипептидного производного. Анализы описаны подробнее в данном описании. Фрагменты или аналоги антител или молекулы иммуноглобулина могут быть легко получены рядовыми специалистами в данной области техники. Предпочтительные амино- и карбоксильные концы фрагментов или аналогов находятся вблизи границ функциональных доменов. Структурные и функциональные домены могут быть идентифицированы путем сравнения данных о нуклеотидной и/или аминокислотной последовательности с публичными или частными базами данных последовательностей. Предпочтительно, компьютеризованные методы сравнения используются для идентификации мотивов последовательностей или предсказанных доменов конформации белка, присутствующих в других белках известной структуры и/или функции. Известны способы идентификации белковых последовательностей, укладывающихся в известные трехмерные структуры (Bowie et al. Science 253:164 (1991)). Таким образом, вышеупомянутые примеры демонстрируют, что квалифицированные специалисты могут распознавать мотивы последовательностей и структурные конформации, которые могут быть использованы для определения структурных и функциональных доменов в соответствии с антителами, описанными здесь. Глутаминильные и аспарагинильные остатки часто деамидируются до соответствующих глутамильных и аспартильных остатков, соответственно. Эти остатки деамидируются в нейтральных или основных условиях. Деамидированная форма этих остатков входит в объем данного изобретения.
В общем, цистеиновые остатки в белках или участвуют в цистеин-цистеиновых дисульфидных связях, или стерически защищены от образования дисульфидной связи, когда они входят в состав складчатого участка белка. Образование дисульфидной связи в белках представляет собой сложный процесс, который определяется окислительно-восстановительным потенциалом окружающей среды и специализированными ферментами тиол-дисульфидного обмена (Creighton, Methods Enzymol. 107, 305-329, 1984; Houee-Levin, Methods Enzymol. 353, 35-44, 2002). Если цистеиновый остаток не имеет пары в структуре белка и не защищен стерически образованием складчатой структуры, он может образовывать дисульфидную связь со свободным цистеином из раствора в результате процесса, известного как дисульфидное перемешивание (shuffling). В другом процессе, известном как дисульфидная перестановка (scrambling), свободные цистеины могут также взаимодействовать с природными дисульфидными связями (такими как присутствующие в структурах антитела) и приводить к низкому связыванию, низкой биологической активности и/или низкой стабильности.
Предпочтительными аминокислотными замещениями являются такие, которые: (1) снижают восприимчивость к протеолизу, (2) снижают восприимчивость к окислению, (3) изменяют аффинность связывания при образовании белковых комплексов, (4) изменяют аффинности связывания, и (4) придают или модифицируют другие физико-химические или функциональные свойства таких аналогов. Аналоги могут включать различные мутеины с последовательностями, отличными от природной пептидной последовательности. Например, единичные или множественные аминокислотные замещения (предпочтительно, замещения консервативных аминокислот) могут быть выполнены в природной последовательности (предпочтительно, в частях полипептида, не входящих в домен(ы), образующие межмолекулярные контакты). Консервативное аминокислотное замещение не должно существенно изменять структурные характеристики родительской последовательности (например, замещающая аминокислота не должна приводить к разрушению спирали, присутствующей в родительской последовательности, или разрушать другие типы вторичной структуры, характеризующие родительскую последовательность). Примеры известных специалистам вторичных и третичных структур полипептидов описаны в Proteins, Structures and Molecular Principles (Creighton, Ed., W. H. Freeman and Company, New York (1984)); Introduction to Protein Structure (C. Branden and J. Tooze, eds., Garland Publishing, New York, N.Y. (1991)); и Thornton et at. Nature 354:105 (1991), которые все включены сюда в качестве ссылок. Дополнительно, такие способы могут быть использованы для осуществления аминокислотных замещений или делеций одного или нескольких цистеиных остатков вариабельной области, участвующих в внутрицепьевой дисульфидной связи, для получения молекул антитела с отсутствующими одной или несколькими внутрицепьевыми дисульфидными связями.
Термин «участок CDR» или «CDR» (комплемент-определяющий участок) используется для обозначения гипервариабельных участков тяжелых и легких цепей антитела, которые придают антителу антигенсвязывающую специфичность. CDR могут быть определены в соответствии с системой Кабат (Kabat, E.A. et al. (1991) Sequences of Proteins of Immunological Interest, 5th Edition. US Department of Health and Human Services, Public Service, NIH, Washington), и последующие издания. Антитело типично содержит 3 CDR тяжелой цепи и 3 CDR легкой цепи. Термин CDR используется в данном описании для обозначения, в зависимости от конкретного случая, одного или нескольких из этих участков, или даже всех этих участков, содержащих большую часть аминокислотных остатков, отвечающих за связывание посредством аффинности антитела с антигеном или эпитопом, которые оно распознает.
Третий CDR тяжелой цепи (HCDR3) имеет большую вариабельность размера (большее разнообразие по существу вследствие механизмов размещения генов, которые его образуют). Он может иметь в длину всего 2 аминокислоты, хотя наибольший известный размер равен 26. Длина CDR может также меняться в зависимости от длины, которая может быть размещена на конкретном нижележащем каркасном участке. Функционально, HCDR3 участвует частично в определении специфичности антитела (Segal et al., PNAS, 71:4298-4302, 1974, Amit et al., Science, 233:747-753, 1986, Chothia et al., J. Mol. Biol., 196:901-917, 1987, Chothia et al., Nature, 342:877-883, 1989, Caton et al., J. Immunol., 144:1965-1968, 1990, Sharon et al., PNAS, 87:4814-4817, 1990, Sharon et al., J. Immunol., 144:4863-4869, 1990, Kabat et al., J. Immunol., 147:1709-1719, 1991).
Термин «набор CDR», используемый здесь, включает CDR1, CDR2 и CDR3. Таким образом, набор HCDR относится к HCDR1, HCDR2 и HCDR3, а набор LCDR относится к LCDR1, LCDR2 и LCDR3.
Варианты доменов VH и VL и CDR по настоящему изобретению, включая те, для которых аминокислотные последовательности приведены здесь, и которые могут быть использованы в специфических связывающих агентах и антителах к B7-H1, могут быть получены с помощью способов изменения последовательностей или мутации и скрининга для нацеливания на антиген с желательными характеристиками. Примеры желательных характеристик включают, без ограничений: повышенную аффинность связывания с антигеном по сравнению с известными антителами, специфическими по отношению к антигену; повышенную нейтрализацию активности антигена по сравнению с известными антителами, специфическими по отношению к антигену, если активность известна; определенную конкурентную способность с известным антителом или лигандом к антигену при определенном молярном соотношении; способность к иммунопреципитации комплекса лиганд-рецептор; способность связываться с определенным эпитопом; линейным эпитопом, например, пептидной последовательностью, идентифицированной путем сканирования пептидного связывания, например, с использованием пептидов, подвергнутых скринингу в линейной и/или стесненной конформации; конформационный эпитоп, образованный прерывистыми (non-continuous) остатками; способность модулировать новую биологическую активность B7-H1 или последующей молекулы; способность связывать и/или нейтрализовать B7-H1 и/или любое другое желательное свойство. Методики, необходимые для выполнения замещений в аминокислотных последовательностях CDR, доменах VH или VL антитела и антигенсвязывающих сайтах, являются доступными для специалистов. Варианты молекул антител, раскрытые здесь, могут быть получены и использованы в настоящем изобретении. Используя подходы вычислительной химии по применению методов анализа многомерных данных к соотношениям структура/свойство-активность (Wold, et al. Multivariate data analysis in chemistry. Chemometrics - Mathematics and Statistics in Chemistry (Ed.: B. Kowalski), D. Reidel Publishing Company, Dordrecht, Holland, 1984), можно определить количественные соотношения активность-свойство антител с использованием хорошо известных математических методов, таких как статистическая регрессия, распознавание и классификация образов (Norman et al. Applied Regression Analysis. Wiley-Interscience; 3rd edition (April 1998); Kandel, Abraham & Backer, Eric. Computer-Assisted Reasoning in Cluster Analysis. Prentice Hall PTR, (May 11, 1995); Krzanowski, Wojtek. Principles of Multivariate Analysis: A User's Perspective (Oxford Statistical Science Series, No 22 (Paper)). Oxford University Press; (December 2000); Witten, Ian H. & Frank, Eibe. Data Mining: Practical Machine Learning Tools and Techniques with Java Implementations. Morgan Kaufmann; (October 11, 1999); Denison David G. T. (Editor), Christopher C. Holmes, Bani K. Mallick, Adrian F. M. Smith. Bayesian Methods for Nonlinear Classification and Regression (Wiley Series in Probability and Statistics). John Wiley & Sons; (July 2002); Ghose, Arup K. & Viswanadhan, Vellarkad N. Combinatorial Library Design and Evaluation Principles, Software, Tools, and Applications in Drug Discovery). В некоторых случаях свойства антител могут быть получены из эмпирических и теоретических моделей (например, анализ вероятно контактирующих остатков или расчетного физико-химического свойства) последовательности антитела, функциональных и трехмерных структур, и эти свойства могут быть рассмотрены по отдельности и в комбинации. Антигенсвязывающий сайт антитела, состоящий из домена VH и домена VL, типично образован шестью петлями полипептида: тремя из вариабельного домена легкой цепи (VL) и тремя из вариабельного домена тяжелой цепи (VH). Анализ антител с известной атомной структурой выявил соотношения между последовательностью и трехмерной структурой антитела, образующего сайты. Эти соотношения позволяют предположить, что, за исключением третьего участка (петли) доменов VH, петли связывающего сайта имеют одну из небольшого числа конформаций основной цепи: канонические структуры. Было продемонстрировано, что каноническая структура, формирующаяся в конкретной петле, определяется ее размером и присутствием определенных остатков в ключевых положениях как петли, так и каркасных участков.
Такое исследование соотношения последовательность-структура может быть использовано для прогнозирования остатков в антителе, имеющем известную последовательность, но неизвестную трехмерную структуру, которые являются важными для сохранения трехмерной структуры его петель CDR и, таким образом, сохранения специфичности связывания. Эти прогнозы могут быть подтверждены путем сравнения прогнозов с результатами экспериментов по оптимизации исходной структуры (lead optimisation). При структурном подходе, может быть создана модель молекулы антитела с использованием любого бесплатно распространяемого или коммерческого программного пакета, такого как WAM. Затем может быть использован пакет прикладных программ для визуализации и анализа белка, такой как Insight II (Accelrys, Inc.) или Deep View, для оценки возможных замещений в каждой позиции CDR. Эта информация затем может быть использована для получения замещений, которые вероятно имеют минимальный или благоприятный эффект на активность или придают другие желательные свойства.
Термин «полипептидный фрагмент», в используемом здесь значении, относится к полипептиду, имеющему аминоконцевую и/или карбоксиконцевую делецию, но в котором остальная аминокислотная последовательность идентична соответствующим позициям в природной последовательности, выделенной, например, из полноразмерной последовательности кДНК. Фрагменты типично имеют в длину, по меньшей мере, 5, 6, 8 или 10 аминокислот, предпочтительно, по меньшей мере, 14 аминокислот в длину, более предпочтительно, по меньшей мере, 20 аминокислот в длину, обычно, по меньшей мере, 50 аминокислот в длину, и еще более предпочтительно, по меньшей мере, 70 аминокислот в длину. Термин «аналог», в используемом здесь значении, относится к полипептидам, которые состоят из сегмента, содержащего, по меньшей мере, 25 аминокислот, имеющего существенную идентичность с частью выделенной аминокислотной последовательности и имеющего, по меньшей мере, одно из следующих свойств: (1) специфическое связывание с B7-H1, в пригодных условиях связывания, (2) способность блокировать соответствующее связывание B7-H1-белок, или (3) способность ингибировать активность B7-H1. Обычно полипептидные аналоги включают консервативное аминокислотное замещение (или вставку, или делецию) по сравнению с природной последовательностью. Аналоги типично содержат, по меньшей мере, 20 аминокислот в длину, предпочтительно, по меньшей мере, 50 аминокислот в длину или больше, и часто могут достигать длины полноразмерного природного полипептида.
Пептидные аналоги широко используются в фармацевтической промышленности в качестве непептидных лекарственных препаратов со свойствами, аналогичными матричному пептиду. Эти типы непептидных соединений называются «пептидными миметиками» или «пептидомиметиками». Fauchere, J. Adv. Drug Res. 15:29 (1986); Veber and Freidinger TINS p.392 (1985); и Evans et al. J. Med. Chem. 30:1229 (1987), которые включены сюда в качестве ссылок. Такие соединения часто разрабатывают с использованием компьютерного молекулярного моделирования. Пептидомиметики, структурно схожие с терапевтически пригодными пептидами, могут быть использованы для создания эквивалентного терапевтического или профилактического эффекта. Обычно пептидомиметики структурно схожи с используемым в качестве образца полипептидом (т.е. полипептидом, проявляющим биохимическое свойство или фармакологическую активность), таким как человеческое антитело, но имеют одну или несколько пептидных связей, необязательно замещенных на связь, выбранную из группы, состоящей из: -CH2NH-, -CH2S-, -CH2-CH2-, -CH=CH- (цис и транс), -COCH2-, -CH(OH)CH2- и -CH2SO-, способами, хорошо известными специалистам. Систематическое замещение одной или нескольких аминокислот консенсусной последовательности на D-аминокислоту такого же типа (например, D-лизин вместо L-лизина) может быть использовано для получения более стабильных пептидов. Кроме того, конформационно ограниченные пептиды, содержащие консенсусную последовательность или по существу идентичный вариант консенсусной последовательности, могут быть получены способами, известными специалистам (Rizo and Gierasch Ann. Rev. Biochem. 61:387 (1992), включена я сюда в качестве ссылки); например, путем вставки внутренних цистеиновых остатков, способных образовывать внутримолекулярные дисульфидные мостики, циклизующие пептид.
В используемом здесь значении «антитело» и «антитела» (иммуноглобулины) могут быть олигоклональным антителом, поликлональным антителом, моноклональным антителом (включая полноразмерные моноклональные антитела), камелизированным (camelised) антителом, химерным антителом, CDR-привитым антителом, мультиспецифическим антителом, биспецифическим антителом, каталитическим антителом, химерным антителом, гуманизированным антителом, полностью человеческим антителом, анти-идиотипическим антителом и антителами, которые могут быть мечеными в растворимой или связанной форме, а также их фрагментами, вариантами или производными, самими или в комбинации с другими аминокислотными последовательностями, приготовленными по известным методикам. Антитело может быть получено от любого вида. Антитело включает полипептид или группу полипептидов, которые состоят из, по меньшей мере, одного связывающего домена, образованного в результате укладки полипептидных цепей, имеющего трехмерные пространственные области связывания с формами внутренних поверхностей и распределениями заряда, комплементарными к характеристикам антигенной детерминанты антигена. Антитело типично имеет тетрамерную форму и включает две идентичных пары полипептидных цепей, причем каждая пара имеет одну «легкую» и одну «тяжелую» цепь. Вариабельные участки каждой пары легкой/тяжелой цепей образуют связывающий сайт антитела. Нативные антитела обычно представляют собой гетеротетрамерные гликопротеины размером примерно 150000 дальтон, состоящие из двух идентичных легких (L) цепей и двух идентичных тяжелых (H) цепей. Каждая легкая цепь связана с тяжелой цепью одной ковалентной дисульфидной связью, тогда как разные изотипы иммуноглобулина отличаются по числу дисульфидных связей в тяжелых цепях. Каждая тяжелая и легкая цепь также имеет регулярно расположенные внутрицепьевые дисульфидные мостики. Каждая тяжелая цепь имеет на одном конце вариабельный домен (VH), за которым следует ряд константных доменов. Каждая легкая цепь имеет вариабельный домен на одном конце (VL) и константный домен на другом его конце; константный домен легкой цепи соответствует первому константному домену тяжелой цепи, и вариабельный домен легкой цепи соответствует вариабельному домену тяжелой цепи. Легкие цепи делятся на лямбда-цепи или каппа-цепи, основанные на аминокислотной последовательности константного участка легкой цепи. Вариабельный домен каппа-легкой цепи также может обозначаться в данном описании как VK. Термин «вариабельный участок» также может быть использован для описания вариабельного домена тяжелой цепи или легкой цепи. Считается, что определенные аминокислотные остатки образуют поверхность раздела между вариабельными доменами легкой и тяжелой цепей. Вариабельные участки каждой пары легкая/тяжелая цепи образуют связывающий сайт антитела. Такие антитела могут быть получены от любого млекопитающего, включая, без ограничений, человека, обезьян, свиней, лошадей, кроликов, собак, кошек, мышей и т.д.
Термин «антитело» или «антитела» включает связывающие фрагменты антител по изобретению, типичные примеры фрагментов включают одноцепочечные Fv (scFv), одноцепочечные антитела, однодоменные антитела, доменные антитела, фрагменты Fv, фрагменты Fab, фрагменты F(ab'), фрагменты F(ab')2, фрагменты антител, проявляющие желательную биологическую активность, стабилизированный дисульфидной связью вариабельный участок (dsFv), димерный вариабельный участок (диатело), анти-идиотипические (анти-Id) антитела (включая, например, анти-Id антитела к антителам по изобретению), интратела, линейные антитела, молекулы одноцепочечных антител и мультиспецифические антитела, образованные из фрагментов антител и эпитопсвязывающих фрагментов любых вышеупомянутых материалов. В частности, антитела включают молекулы иммуноглобулина и иммунологически активные фрагменты молекул иммуноглобулина, т.е. молекулы, содержащие антигенсвязывающий сайт. Молекулы иммуноглобулина могут принадлежать к любому типу (например, IgG, IgE, IgM, IgD, IgA и IgY), классу (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2) или подклассу.
Расщепление антител ферментом папаином приводит к образованию двух идентичных антигенсвязывающих фрагментов, известных также как фрагменты «Fab», и фрагмента «Fc», не обладающего антигенсвязывающей активностью, но способного кристаллизоваться. Расщепление антител ферментом пепсином приводит к образованию фрагмента F(ab')2, в котором две ветви молекулы антитела остаются связанными, и который включает два антигенсвязывающих сайта. Фрагмент F(ab')2 обладает способностью к образованию поперечных связей с антигеном.
«Fv», при использовании в данном описании, относится к минимальному фрагменту антитела, сохраняющему как антигенраспознающий, так и антигенсвязывающий сайты. Этот участок состоит из димера вариабельных доменов одной тяжелой и одной легкой цепи в тесной, нековалентной или ковалентной, связи. Именно в такой конфигурации три CDR каждого вариабельного домена взаимодействуют с образованием антигенсвязывающего сайта на поверхности димера VH-VL. Коллективно, шесть CDR обеспечивают специфичность связывания антигена с антителом. Однако даже отдельно взятый вариабельный домен (или половинка Fv, включающая только три CDR, специфических по отношению к антигену) обладает способностью распознавать и связывать антиген, хотя с меньшей аффинностью, чем целый связывающий сайт.
«Fab», при использовании в данном описании, относится к фрагменту антитела, включающему константный домен легкой цепи и CH1 домен тяжелой цепи.
«dAb», при использовании в данном описании, относится к фрагменту антитела, представляющему собой наименьшую функциональную связывающую единицу человеческих антител. «dAb» представляет собой однодоменное антитело и включает вариабельный домен тяжелой цепи антитела (VH домен) или вариабельный домен легкой цепи антитела (VL домен). Каждый dAb включает три из шести природных CDR (Ward et al., Binding activities of a repertoire of single immunoglobulin variable domains secreted from Escherichia coli. Nature 341, 544-546 (1989); Holt, et al., Domain antibodies: protein for therapy, Trends Biotechnol. 21, 484-49 (2003)). Имея молекулярные веса в интервале значений от 11 до 15 кДа, они в четыре раза меньше антигенсвязывающего фрагмента (Fab)http://www.sciencedirect.com/" \l "fn2 и соответствуют половине размера одноцепочечной молекулы Fv (scFv).
«Верблюжий» (camelid), при использовании в данном описании, относится к молекулам антитела, состоящим из димеров тяжелых цепей, лишенных легких цепей, которые, тем не менее, имеют обширный антигенсвязывающий репертуар (Hamers-Casterman C, Atarhouch T, Muyldermans S, Robinson G, Hamers C, Songa EB, Bendahman N, Hamers R (1993) Naturally occurring antibodies devoid of light chains. Nature 363:446-448).
Термин «диатела» относится к малым фрагментам антител с двумя антигенсвязывающими сайтами, причем фрагменты включают вариабельный домен тяжелой цепи (VH), соединенный с вариабельным доменом легкой цепи (VL) в одну полипептидную цепь (VH-VL). При использовании линкера, слишком короткого для того, чтобы обеспечить возможность спаривания между двумя доменами одной цепи, домены вынуждены будут спариваться с комплементарными доменами другой цепи и создавать два антигенсвязывающих сайта. Диатела описаны более подробно, например, в EP 404097; WO 93/11161; и Hollinger et al., Proc. Natl. Acad. Sci. USA, 90:6444-6448 (1993).
Было продемонстрировано, что фрагменты цельного антитела могут выполнять функцию связывания антигенов. Примерами связывающих фрагментов являются (Ward, E.S. et al., (1989) Nature 341, 544-546) фрагмент Fab, состоящий из доменов VL, VH, CL и CH1; (McCafferty et al. (1990) Nature, 348, 552-554) фрагмент Fd, состоящий из доменов VH и CH1; (Holt et al. (2003) Trends in Biotechnology 21, 484-490) фрагмент Fv, состоящий из доменов VL и VH одного антитела; (iv) фрагмент dAb (Ward, E.S. et al., Nature 341, 544-546 (1989), McCafferty et al. (1990) Nature, 348, 552-554, Holt et al. (2003) Trends in Biotechnology 21, 484-490], который состоит из домена VH или VL; (v) изолированные участки CDR; (vi) фрагменты F(ab')2, представляющие собой бивалентный фрагмент, включающий два связанных фрагмента Fab; (vii) одноцепочечные молекулы Fv (scFv), в которых домен VH и домен VL соединены пептидным линкером, позволяющим двум доменам объединяться с образованием антигенсвязывающего сайта (Bird et al., (1988) Science, 242, 423-426,, Huston et al., (1988) PNAS USA, 85, 5879-5883); (viii) биспецифические одноцепочечные димеры Fv (PCT/US92/09965); и (ix) «диатела», мультивалентные или мультиспецифические фрагменты, сконструированные методом слияния генов (WO94/13804; Holliger, P. (1993) et al., Proc. Natl. Acad. Sci. USA 90:6444-6448,). Молекулы Fv, scFv или диатела могут быть стабилизированы путем включения дисульфидных мостиков, соединяющих домены VH и VL (Reiter, Y. et al., Nature Biotech, 14, 1239-1245, 1996). Также могут быть получены мини-тела, включающие scFv, соединенный с доменом CH3 (Hu, S. et al., (1996) Cancer Res., 56, 3055-3061). Другими примерами связывающих фрагментов являются Fab', которые отличаются от фрагментов Fab несколькими добавленными остатками на карбоксильном конце домена CH1 тяжелой цепи, включая один или несколько цистеинов из шарнирного участка антитела, и Fab'-SH, представляющий собой фрагмент Fab', в котором цистеиновый остаток (остатки) константных доменов несут свободную тиольную группу.
Термин «вариабельный» относится к тому факту, что последовательности определенных участков вариабельных доменов значительно различаются у разных антител и отвечают за специфичность связывания каждого конкретного антитела с его конкретным антигеном. Однако вариабельность не распределена равномерно по вариабельным доменам антител. Она сконцентрирована в сегментах, называемых участками, определяющими комплементарность (CDR), вариабельных доменов как легких, так и тяжелых цепей. Более консервативные участки вариабельных доменов называются каркасными участками (FR). Вариабельные домены нативных тяжелой и легкой цепей содержат каждый по четыре участка FR, преимущественно принимающих конфигурацию β-листа, соединенных тремя CDR, которые образуют петли, соединяющие и, в некоторых случаях, образующие часть структуры β-листа. CDR в каждой цепи удерживаются вместе на близком расстоянии участками FR и, вместе с CDR другой цепи, участвуют в образовании антигенсвязывающего сайта антител (см., Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD (1991)). Константные домены обычно не принимают непосредственного участия в связывании антигена, но могут влиять на аффинность связывания антигена и могут проявлять различные эффекторные функции, такие как участие антитела в ADCC, CDC и/или апоптозе.
Термин «гипервариабельный участок», при использовании в данном описании, относится к аминокислотным остаткам антитела, которые ассоциированы с его связыванием с антигеном. Гипервариабельные участки охватывают аминокислотные остатки «участков, определяющих комплементарность» или «CDR» (например, остатки 24-34 (L1), 50-56 (L2) и 89-97 (L3) вариабельного домена легкой цепи и остатки 31-35 (H1), 50-65 (H2) и 95-102 (H3) вариабельного домена тяжелой цепи; Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD (1991)) и/или остатки из «гипервариабельной петли» (например, остатки 26-32 (L1), 50-52 (L2) и 91-96 (L3) в вариабельном домене легкой цепи и 26-32 (H1), 53-55 (H2) и 96-101 (H3) в вариабельном домене тяжелой цепи; Chothia and Lesk, J. Mol. Biol., 196:901-917 (1987)). «Каркасными» или «FR»-остатками являются остатки вариабельного домена, фланкирующие CDR. FR-остатки присутствуют в химерных, гуманизированных, человеческих, доменных антителах, диателах, вакцителах (vaccibodies), линейных антителах и биспецифических антителах.
В используемом здесь значении «специфический связывающий агент», «целевой связывающий белок», «специфический связывающий белок» и т.п. термины относятся к агенту, например, антителу, или его связывающему фрагменту, которые предпочтительно связываются с сайтом-мишенью. В одном варианте воплощения специфический связывающий агент является специфическим по отношению только к одному сайту-мишени. В других вариантах воплощения специфический связывающий агент является специфическим к нескольким сайтам-мишеням. В одном варианте воплощения специфический связывающий агент может быть моноклональным антителом, и сайт-мишень может быть эпитопом. Специфический связывающий агент может включать, по меньшей мере, один антигенсвязывающий домен (например, CDR) антитела, причем указанный домен является слитым с или содержится внутри гетерологического белкового каркаса (protein scaffold), например, не относящегося к антителу белкового каркаса.
«Связывающие фрагменты» антитела получают методами рекомбинантных ДНК, или ферментативным или химическим расщеплением интактных антител. Связывающие фрагменты включают Fab, Fab', F(ab')2, Fv, dAb и одноцепочечные антитела. Подразумевается, что у антитела, отличного от «биспецифического» или «бифункционального» антитела, все его связывающие сайты идентичны. Антитело существенно ингибирует адгезию рецептора с контррецептором, когда избыток антитела уменьшает количество рецептора, связанного с контррецептором, на, по меньшей мере, примерно 20%, 40%, 60% или 80%, и чаще всего на более чем примерно 85% (при измерении методом in vitro анализа конкурентного связывания).
Термин «эпитоп» включает любую белковую детерминанту, способную специфически связываться с иммуноглобулином или T-клеточным рецептором. Эпитопные детерминанты обычно состоят из химически активных поверхностных группировок молекул, таких как боковые цепи аминокислот или сахаров, и могут, но не всегда, обладать специфическими трехмерными структурными характеристиками, а также специфическими характеристиками заряда. Говорят, что антитело специфически связывает антиген, когда константа диссоциации имеет значение ≤1 мкМ, предпочтительно ≤100 нМ, и наиболее предпочтительно ≤10 нМ.
Термин «агент» используется здесь для обозначения химического соединения, смеси химических соединений, биологической макромолекулы, или экстракта, изготовленного из биологических материалов.
«Активный» или «активность» по отношению к полипептиду B7-H1 относится к части полипептида B7-H1, обладающей биологической или иммунологической активностью нативного полипептида B7-H1. «Биологический», при использовании в данном описании, относится к биологической функции, которая является результатом активности нативного полипептида B7-H1. Предпочтительная биологическая активность B7-H1 включает, например, индуцируемую B7-H1 пролиферацию клеток, клеточную адгезию и инвазию.
«Млекопитающее», при использовании в данном описании, относится к любому животному, которое считается млекопитающим. Предпочтительно, млекопитающее является человеком.
«Животное», при использовании в данном описании, охватывает животных, которые считаются млекопитающими. Предпочтительно, животное является человеком.
Термин «пациент» включает людей и субъектов ветеринарии.
Термин «mAb» относится к моноклональному антителу.
«Липосома», при использовании в данном описании, относится к малой везикуле, которая может быть пригодной для доставки млекопитающему лекарственных препаратов, которые могут включать полипептид B7-H1 по изобретению или антитела к такому полипептиду B7-H1.
«Метка» или «меченый», в используемом здесь значении, относится к введению детектируемого фрагмента в полипептид, например, радиоактивная метка, флуоресцентная метка, ферментативная метка, хемолюминесцентно меченая или биотинильная группа. Радиоизотопы или радионуклиды могут включать 3H, 14C, 15N, 35S, 90Y, 99Tc, 111In, 125I, 131I, флуоресцентные метки могут включать родамин, лантанидные фосфоры или FITC, и ферментативные метки могут включать пероксидазу хрена, β-галактозидазу, люциферазу, щелочную фосфатазу.
Дополнительные метки включают, в качестве иллюстраций и без ограничений: ферменты, такие как глюкоза-6-фосфатдегидрогеназа («G6PDH»), альфа-D-галактозидаза, глюкозооксидаза, глюкозоамилаза, карбоангидраза, ацетилхолинэстераза, лизоцим, малатдегидрогеназа и пероксидаза; красители; дополнительные флуоресцентные метки или люминофоры, такие как, например, флуоресцеин и его производные, флуорохром, GFP (GFP обозначает «зеленый флуоресцентный белок»), дансил, умбеллиферон, фикоэритрин, фикоцианин, аллофикоцианин, о-фталевый альдегид и флуорескамин; флуорофоры, такие как криптаты и хелаты лантанидов, например, европия и т.д. (анализы Perkin Elmer и Cisbio); хемолюминесцентные метки или хемолюминофоры, такие как изолюминол, люминол и диоксетаны; сенсибилизаторы; коферменты; субстраты ферментов; частицы, такие как латексные или углеродные частицы; металлический золь; кристаллит; липосомы; клетки и т.д., которые могут быть дополнительно мечены красителем, катализатором или другими детектируемыми группами; молекулы, такие как биотин, дигоксигенин или 5-бромдезоксиуридин; фрагменты токсинов, такие как, например, фрагмент токсина, выбранного из группы экзотоксина Pseudomonas (PE или его цитотоксический фрагмент или мутант), дифтерийный токсин или его цитотоксический фрагмент или мутант, ботулотоксин A, B, C, D, E или F, рицин или его цитотоксический фрагмент, например, рицин A, абрин или его цитотоксический фрагмент, сапорин или его цитотоксический фрагмент, антивирусный токсин фитолакки американской (pokeweed) или его цитотоксический фрагмент и бриодин 1 или его цитотоксический фрагмент.
Термин «фармацевтический агент или лекарственное средство», в используемом здесь значении, относится к химическому соединению или композиции, способной индуцировать желательный терапевтический эффект при надлежащем введении пациенту. Другие химические термины в данном описании используются в соответствии с общепринятыми значениями, приведенными, например, в The McGraw-Hill Dictionary of Chemical Terms (Parker, S., Ed., McGraw-Hill, San Francisco (1985)) (включен сюда в качестве ссылки).
В используемом здесь значении, «по существу чистый» означает, что объекты указанного типа (object species) являются преобладающим присутствующим типом (т.е. на молярной основе являются более распространенными, чем любые другие индивидуальные типы объектов в композиции), и, предпочтительно, в существенной степени очищенная фракция представляет собой композицию, в которой объекты указанного типа включают, по меньшей мере, примерно 50 процентов (на молярной основе) от всех присутствующих типов макромолекулярных объектов. Обычно по существу чистая композиция будет содержать более примерно 80 процентов от всех типов макромолекулярных объектов, присутствующих в композиции, более предпочтительно, более примерно 85%, 90%, 95% и 99%. Наиболее предпочтительно, объекты указанного типа являются очищенными до по существу гомогенного состояния (примесные материалы не детектируются в композиции обычными способами детектирования), причем композиция состоит по существу из одного типа макромолекулярных объектов.
«Антителозависимая клеточно опосредованная цитотоксичность» и «ADCC» относятся к клеточно-медиируемой реакции, в которой неспецифические цитотоксические клетки, экспрессирующие Fc рецепторы Ig (FcR) (например, природные клетки-убийцы (NK), моноциты, нейтрофилы и макрофаги) распознают связанное антитело на клетке-мишени и затем вызывают лизис клетки-мишени. Первичные клетки, медиирующие ADCC - природные клетки-убийцы (NK) - экспрессируют только FcγRIII, в то время как моноциты экспрессируют FcγRI, FcγRII и FcγRIII. Экспрессия FcR на гематопоэтических клетках приведена в Таблице 9 на странице 464 работы Ravetch and Kinet, Annu. Rev. Immunol 9:457-92 (1991). Для оценки ADCC-активности молекулы, представляющей интерес, может быть проведен in vitro анализ ADCC, такой как описанный в патенте США № 5500362 или 5821337. Пригодные эффекторные клетки для таких анализов включают мононуклеарные клетки периферической крови (PBMC) и природные клетки-убийцы (NK). Альтернативно, или дополнительно, ADCC-активность молекулы, представляющей интерес, можно оценить in vivo, например, в животной модели, такой как раскрытая в Clynes et al. PNAS (USA) 95:652-656 (1988).
«Комплементзависимая цитотоксичность» и «CDC» относятся к механизму, по которому антитела осуществляют свою функцию уничтожения клеток. Она инициируется связыванием C1q, составной части первого компонента комплемента, с Fc-доменом иммуноглобулина - IgG или IgM, - образующего комплекс с антигеном (Hughs-Jones, N.C., and B. Gardner. 1979. Mol. Immunol. 16:697). C1q представляет собой большой, структурно сложный гликопротеин размером около 410 кДа, присутствующий в человеческой сыворотке в концентрации 70 мкг/мл (Cooper, N.R. 1985. Adv. Immunol. 37:151). Вместе с двумя сериновыми протеазами, C1r и C1s, C1q образует комплекс C1, первый компонент комплемента. По меньшей мере, две N-концевые глобулярные головки C1q должны быть связаны с Fc иммуноглобулина (Ig) для активации C1 и, таким образом, для инициирования каскада комплемента (Cooper, N.R. 1985. Adv. Immunol. 37:151).
Термин «период полувыведения антитела», в используемом здесь значении, означает фармакокинетическое свойство антитела, представляющее собой меру среднего времени жизни молекул антитела после их введения. Период полувыведения антитела может быть выражен как время, необходимое для элиминирования 50 процентов известного количества иммуноглобулина из организма пациента или его определенного компартмента, например, при измерении в сыворотке или плазме, т.е. период полувыведения из циркуляции, или в других тканях. Период полувыведения может различаться для разных иммуноглобулинов или классов иммуноглобулинов. В общем, увеличение периода полувыведения антитела приводит к увеличению среднего времени пребывания (MRT) в циркуляции для введенного антитела.
Термин «изотип» относится к классификации константного участка тяжелой или легкой цепи антитела. Константные домены антител не участвуют в связывании с антигеном, но проявляют различные эффекторные функции. В зависимости от аминокислотной последовательности константного участка тяжелой цепи, данное человеческое антитело или иммуноглобулин могут быть отнесены к одному из пяти основных классов иммуноглобулинов: IgA, IgD, IgE, IgG и IgM. Некоторые из этих классов могут быть дополнительно разделены на подклассы (изотипы), например, IgG1 (гамма 1), IgG2 (гамма 2), IgG3 (гамма 3) и IgG4 (гамма 4), и IgA1 и IgA2. Константные участки тяжелой цепи, соответствующие разным классам иммуноглобулинов, обозначаются α, δ, ε, γ и μ, соответственно. Структуры и трехмерные конфигурации разных классов иммуноглобулинов хорошо известны. Известно, что из различных классов человеческих иммуноглобулинов только человеческие IgG1, IgG2, IgG3, IgG4 и IgM активируют комплемент. Известно, что человеческие IgG1, IgG2, IgG3 и IgG4 связывают гамма-рецепторы Fc, которые медиируют различные эффекторные функции, включая ADCC. Константные участки человеческой легкой цепи могут быть разделены на два основных класса - каппа и лямбда.
При необходимости, изотип антитела, которое специфически связывает B7-H1, может быть переключен, например, для того, чтобы использовать биологическое свойство другого изотипа. Например, в некоторых обстоятельствах может быть желательным в связи с получением антител в качестве терапевтических антител против B7-H1, чтобы антитела были способны к фиксации комплемента и участию в комплементзависимой цитотоксичности (CDC). Существует ряд изотипов антител, обладающих такой способностью, включая, без ограничений, следующие: мышиный IgM, мышиный IgG2a, мышиный IgG2b, мышиный IgG3, человеческий IgM, человеческий IgA, человеческий IgG1 и человеческий IgG3. В других вариантах воплощения может быть желательным в связи с получением антител в качестве терапевтических антител против B7-H1, чтобы антитела были способны связывать Fc-рецепторы на эффекторных клетках и участвовать в антителозависимой цитотоксичности (ADCC). Существует ряд изотипов антител, обладающих такой способностью, включая, без ограничений, следующие: мышиный IgG2a, мышиный IgG2b, мышиный IgG3, человеческий IgG1 и человеческий IgG3. Следует понимать, что получаемые антитела не обязательно должны сразу обладать таким изотипом, скорее, полученное антитело может обладать любым изотипом и может быть подвергнуто переключению изотипа после этого с использованием обычных методик, хорошо известных специалистам. Такие методики включают, в числе прочего, использование прямых рекомбинантных методик (см., например, патент США № 4816397), методики межклеточного слияния (см., например, патенты США №№ 5916771 и 6207418).
В качестве примера, анти-B7-H1 антитела, описанные здесь, являются полностью человеческими антителами. Если антитело обладает желательным связыванием с B7-H1, его изотип можно легко переключить для получения изотипа человеческого IgM, человеческого IgG1 или человеческого IgG3, при сохранении того же вариабельного участка (определяющего специфичность антитела и некоторую часть его аффинности). Такая молекула будет затем способна к фиксации комплемента и участию в CDC и/или будет способна к связыванию с Fc-рецепторами на эффекторных клетках и участию в ADCC.
«Анализы цельной крови» используют нефракционированную кровь в качестве источника природных эффекторов. Кровь содержит комплемент в плазме, вместе с FcR-экспрессирующими клеточными эффекторами, такими как полиморфонуклеарные клетки (PMN) и мононуклеарные клетки (MNC). Таким образом, анализы цельной крови позволяют одновременно оценивать синергию обоих эффекторных механизмов ADCC и CDC in vitro.
«Терапевтически эффективное» количество, в используемом здесь значении, представляет собой количество, обеспечивающее некоторое улучшение или полезный эффект для субъекта. Другими словами, «терапевтически эффективное» количество представляет собой количество, обеспечивающее некоторое облегчение, смягчение и/или ослабление, по меньшей мере, одного клинического симптома. Клинические симптомы, ассоциированные с расстройствами, лечение которых может проводиться способами по изобретению, хорошо известны квалифицированным специалистам. Дополнительно, квалифицированным специалистам будет понятно, что терапевтические эффекты не должны обязательно быть полными или исцеляющими, при условии, что обеспечивается некоторый полезный эффект для субъекта.
Типичные примеры раков у людей включают опухоль мочевого пузыря, опухоль молочной железы, опухоль простаты, базально-клеточную карциному, рак желчных путей, рак мочевого пузыря, рак кости, рак головного мозга и ЦНС (например, глиомную опухоль), рак шейки матки, хориокарциному, рак ободочной и прямой кишки, рак соединительной ткани, рак пищеварительной системы; эндометриальный рак, рак пищевода; рак глаза; рак головы и шеи; желудочный рак; интраэпителиальную неоплазму; рак почки; рак гортани; лейкоз; рак печени; рак легкого (например, мелкоклеточный и немелкоклеточный); лимфому, включая лимфому Ходжкина и неходжкинскую лимфому; меланому; миелому, нейробластому, рак полости рта (например, губ, языка, ротовой полости и глотки); рак яичника; рак поджелудочной железы, ретинобластому; рабдомиосаркому; ректальный рак, почечный рак, рак респираторной системы; саркому, рак кожи; рак желудка, тестикулярный рак, рак щитовидной железы; рак матки, рак мочевой системы, а также другие карциномы и саркомы.
Типичные примеры хронической инфекции у людей включают ВИЧ, вирус гепатита B (HBV) и вирус гепатита C (HCV).
Термин «и/или» в используемом здесь значении следует понимать как конкретное указание на каждый из двух указанных признаков или компонентов вместе с другим или без него. Например, «A и/или B» следует понимать как конкретное указание на каждый вариант из (i) A, (ii) B и (iii) A и B, как если бы они были перечислены здесь индивидуально.
Структура антитела
Известно, что основная структурная единица антитела включает тетрамер. Каждый тетрамер состоит из двух идентичных пар полипептидных цепей, каждая пара содержит одну «легкую» (примерно 25 кДа) и одну «тяжелую» цепь (примерно 50-70 кДа). Аминоконцевой участок каждой цепи включает вариабельный участок, содержащий от примерно 100 до 110 или больше аминокислот, ответственных в первую очередь за распознавание антигена. Карбоксиконцевой участок каждой цепи образует константный участок, ответственный в первую очередь за эффекторную функцию. Человеческие легкие цепи делятся на каппа- и лямбда-легкие цепи. Тяжелые цепи делятся на мю, дельта, гамма, альфа или эпсилон, и определяют изотип антитела IgM, IgD, IgA и IgE, соответственно. В легких и тяжелых цепях вариабельные и константные участки соединены «J»-цепью, содержащей примерно 12 или больше аминокислот, а тяжелая цепь также включает «D»-сегмент, содержащий примерно 10 или больше аминокислот. См. общее описание в Fundamental Immunology Ch. 7 (Paul, W., ed., 2nd ed. Raven Press, N.Y. (1989)) (целиком включена в качестве ссылки). Вариабельные участки каждой пары легкой/тяжелой цепей образуют антителосвязывающий сайт.
Таким образом, интактное антитело имеет два связывающих сайта. За исключением бифункциональных или биспецифических антител, два связывающих сайта являются одинаковыми.
Все цепи обладают одинаковой общей структурой, состоящей из относительно консервативных каркасных участков (FR), соединенных тремя гипервариабельными участками, также называемыми CDR. CDR из двух цепей каждой пары ориентируются каркасными участками, что позволяет связываться со специфическим эпитопом. В направлении от N-конца к C-концу, как легкие, так и тяжелые цепи включают домены FR1, CDR1, FR2, CDR2, FR3, CDR3 и FR4. Отнесение аминокислот к каждому домену производится в соответствии с определениями Kabat в Sequences of Proteins of Immunological Interest (National Institutes of Health, Bethesda, Md. (1987 и 1991)) или Chothia & Lesk J. Mol. Biol. 196:901-917 (1987); Chothia et al. Nature 342:878-883 (1989).
Биспецифическое или бифункциональное антитело представляет собой искусственное гибридное антитело, имеющее две разных пары тяжелая/легкая цепь и два разных связывающих сайта. Биспецифические антитела могут быть получены различными способами, включая слияние гибридом или сцепление Fab'-фрагментов. См., например, Songsivilai & Lachmann Clin. Exp. Immunol. 79:315-321 (1990), Kostelny et al. J. Immunol. 148:1547-1553 (1992). Биспецифические антитела не существуют в форме фрагментов с одним связывающим сайтом (например, Fab, Fab' и Fv).
Типично домен VH спаривается с доменом VL, образуя антигенсвязывающий сайт антитела, хотя для связывания антигена может быть использован один домен VH или VL. VH-домен (см. Таблицу 9) может спариваться с VL-доменом (см. Таблицу 13) для образования антигенсвязывающего сайта антитела, включающего оба домена VH и VL.
Человеческие антитела и гуманизация антител
Человеческие антитела позволяют избежать некоторых проблем, ассоциированных с антителами, содержащими мышиные или крысиные вариабельные и/или константные участки. Присутствие таких белков мышиного или крысиного происхождения может приводить к быстрому клиренсу антител или может приводить к возникновению у пациента иммунного ответа против антитела. Для того чтобы избежать использования антител мышиного или крысиного происхождения, могут быть получены полностью человеческие антитела путем введения функциональных локусов человеческого антитела грызуну, другому млекопитающему или животному, так чтобы грызун, другое млекопитающее или животное продуцировали полностью человеческие антитела.
Один из способов получения полностью человеческих антител заключается в использовании мышей линии XenoMouse®, генетически сконструированных так, чтобы они содержали фрагменты человеческих локуса тяжелой цепи и локуса легкой цепи каппа размером до, но не больше 1000 т.п.н. (kb) в конфигурации зародышевой линии. См. Mendez et al. Nature Genetics 15:146-156 (1997) и Green and Jakobovits J. Exp. Med. 188:483-495 (1998). Мышей линии XenoMouse® можно приобрести у фирмы Amgen, Inc. (Fremont, California, U.S.A).
Такие мыши способны продуцировать молекулы человеческих иммуноглобулина и антител и дефицитны по продуцированию мышиных молекул иммуноглобулина и антител. Используемые для этого технологии раскрыты в патентной заявке США № 08/759620, поданной 3 декабря 1996 года, и международных патентных заявках №№ WO 98/24893, опубликованной 11 июня 1998 г., и WO 00/76310, опубликованной 21 декабря 2000 г., описания которых настоящим включены сюда в качестве ссылок. См. также Mendez et al. Nature Genetics 15:146-156 (1997), описание которой настоящим включено сюда в качестве ссылки.
Продуцирование мышей линий XenoMouse® дополнительно обсуждается и описывается в патентных заявках США №№ 07/466008, поданной 12 января 1990 года, 07/610515, поданной 8 ноября 1990 года, 07/919297, поданной 24 июля 1992 года, 07/922649, поданной 30 июля 1992 года, 08/031801, поданной 15 марта 1993 года, 08/112848, поданной 27 августа 1993 года, 08/234145, поданной 28 апреля 1994 года, 08/376279, поданной 20 января 1995 года, 08/430938, поданной 27 апреля 1995 года, 08/464584, поданной 5 июня 1995 года, 08/464582, поданной 5 июня 1995 года, 08/463191, поданной 5 июня 1995 года, 08/462837, поданной 5 июня 1995 года, 08/486853, поданной 5 июня 1995 года, 08/486857, поданной 5 июня 1995 года, 08/486859, поданной 5 июня 1995 года, 08/462513, поданной 5 июня 1995 года, 08/724752, поданной 2 октября 1996 года, 08/759620, поданной 3 декабря 1996 года, публикации США 2003/0093820, поданной 30 ноября 2001 года, и патентах США №№ 6162963, 6150584, 6114598, 6075181 и 5939598 и патентах Японии №№ 3068180 B2, 3068506 B2 и 3068507 B2. См. также европейский патент № EP 0463151 B1, решение о выдаче опубликовано 12 июня 1996 года, международную патентную заявку № WO 94/02602, опубликованную 3 февраля 1994 года, международную патентную заявку № WO 96/34096, опубликованную 31 октября 1996 года, WO 98/24893, опубликованный 11 июня 1998 года, WO 00/76310, опубликованный 21 декабря 2000 года. Описания всех вышеупомянутых патентов, заявок и публикаций настоящим целиком включены сюда в качестве ссылок.
В альтернативном подходе, другие, включая GenPharm International, Inc., использовали подход «мини-локуса». В подходе мини-локуса, экзогенный Ig-локус имитируется путем включения кусочков (индивидуальных генов) из локуса Ig. Таким образом, из одного или нескольких генов VH, одного или нескольких генов DH, одного или нескольких генов JH, константного участка мю и обычно второго константного участка (предпочтительно, константного участка гамма) формируют конструкт для введения животному. Этот подход описан в патенте США № 5545807 на имя Surani et al. и патентах США №№ 5545806, 5625825, 5625126, 5633425, 5661016, 5770429, 5789650, 5814318, 5877397, 5874299 и 6255458, все на имя Lonberg and Kay, патентах США №№ 5591669 и 6023010 на имя Krimpenfort and Berns, патентах США №№ 5612205, 5721367 и 5789215 на имя Berns et al., и патенте США № 5643763 на имя Choi and Dunn, и в принадлежащих фирме GenPharm International патентных заявках США №№ 07/574748, поданной 29 августа 1990 года, 07/575962, поданной 31 августа 1990 года, 07/810279, поданной 17 декабря 1991 года, 07/853408, поданной 18 марта 1992 года, 07/904068, поданной 23 июня 1992 года, 07/990860, поданной 16 декабря 1992 года, 08/053131, поданной 26 апреля 1993 года, 08/096762, поданной 22 июля 1993 года, 08/155301, поданной 18 ноября 1993 года, 08/161739, поданной 3 декабря 1993 года, 08/165699, поданной 10 декабря 1993 года, 08/209741, поданной 9 марта 1994 года, описания которых настоящим включены сюда в качестве ссылок. См. также европейский патент № 0546073 B1, международные патентные заявки №№ WO 92/03918, WO 92/22645, WO 92/22647, WO 92/22670, WO 93/12227, WO 94/00569, WO 94/25585, WO 96/14436, WO 97/13852 и WO 98/24884, и патент США № 5981175, описания которых настоящим целиком включены сюда в качестве ссылок. См. дополнительно Taylor et al., 1992, Chen et al., 1993, Tuaillon et al., 1993, Choi et al., 1993, Lonberg et al., (1994), Taylor et al., (1994), и Tuaillon et al., (1995), Fishwild et al., (1996), описания которых настоящим целиком включены сюда в качестве ссылок.
Kirin также продемонстрировал получение человеческих антител из мышей, которым были введены, путем слияния микроклеток, большие фрагменты хромосом или целые хромосомы. См. европейские патентные заявки №№ 773288 и 843961, описания которых настоящим включены сюда в качестве ссылок. Дополнительно, были получены KMTM-мыши, являющиеся результатом кроссбридинга Tc-мышей Kirin с мышами с мини-локусом Medarex (Humab). Эти мыши обладают человеческой IgH трансхромосомой мышей Kirin и трансген цепи каппа мышей Genpharm (Ishida et al., Cloning Stem Cells, (2002) 4:91-102).
Человеческие антитела также могут быть получены in vitro способами. Пригодные примеры включают, без ограничений, фаговый дисплей (CAT, Morphosys, Dyax, Biosite/Medarex, Xoma, Symphogen, Alexion (бывшая Proliferon), Affimed), рибосомальный дисплей (CAT), дрожжевой дисплей и т.п.
Приготовление антител
Антитела, описанные здесь, были приготовлены с использованием технологии XenoMouse®, как описано ниже. Такие мыши способны продуцировать человеческие молекулы иммуноглобулина и антитела и дефицитны по продуцированию мышиных молекул иммуноглобулина и антител. Технологии, используемые для достижения этого, раскрыты в патентах, заявках и публикациях, раскрытых в разделе Известный уровень техники данной заявки. В частности, однако, предпочтительный вариант воплощения трансгенного продуцирования мышей и антител от них раскрыт в патентной заявке США № 08/759620, поданной 3 декабря 1996 года, и международных патентных заявках №№ WO 98/24893, опубликованной 11 июня 1998 г., и WO 00/76310, опубликованной 21 декабря 2000 года, описания которых настоящим включены сюда в качестве ссылок. См. также Mendez et al. Nature Genetics 15:146-156 (1997), описание которой настоящим включено сюда в качестве ссылки.
Благодаря использованию такой технологии были получены полностью человеческие моноклональные антитела к различным антигенам. По существу, мышей линий XenoMouse® иммунизируют антигеном, представляющим интерес (например, B7-H1), выделяют лимфатические клетки (такие как B-клетки) из гипериммунизированных мышей, и выделенные лимфоциты сливают с клеточной линией миелоидного типа для получения бессмертных гибридомных клеточных линий. Такие гибридомные клеточные линии подвергают скринингу и селектированию для идентификации гибридомных клеточных линий, которые продуцируют антитела, специфические по отношению к антигену, представляющему интерес. Настоящее изобретение предусматривает способы получения множества гибридомных клеточных линий, продуцирующих антитела, специфические по отношению к B7-H1. Дополнительно, настоящее изобретение предусматривает характеризацию антител, продуцируемых такими клеточными линиями, включая анализы нуклеотидных и аминокислотных последовательностей тяжелых и легких цепей таких антител.
Альтернативно, вместо слияния с клетками миеломы для получения гибридом, может осуществляться анализ непосредственно B-клеток. Например, CD19+ B-клетки могут быть выделены из гипериммунных мышей XenoMouse® и помещены в условия, обеспечивающие возможность пролиферации и дифференцировки в антителосекретирующие клетки плазмы. Антитела из клеточных супернатантов затем подвергают скринингу методом ELISA на реактивность против иммуногена B7-H1. Супернатанты также могут быть подвергнуты скринингу на иммунореактивность против фрагментов B7-H1 для последующего картирования разных антител по связыванию с доменами B7-H1, представляющими функциональный интерес. Антитела также могут быть подвергнуты скринингу с другими родственными человеческими белками и против крысиных, мышиных и принадлежащих нечеловекообразным приматам, таким как яванский макак, ортологов B7-H1, в последнем случае - для определения видовой перекрестной реактивности. B-клетки из лунок, содержащих антитела, представляющие интерес, могут быть иммортализованы различными способами, включая слияние для получения гибридом из индивидуальных или из пулов лунок, или путем инфицирования EBV (вирус Эпштейна-Барр) или трансфекции известными иммортализующими генами и затем высевания в пригодную среду. Альтернативно, отдельные клетки плазмы, секретирующие антитела с желательными специфичностями, затем выделяют с использованием метода B7-H1-специфического локального гемолиза в геле (см., например, Babcook et al., Proc. Natl. Acad. Sci. USA 93:7843-48 (1996)). Клетками-мишенями для лизиса являются предпочтительно красные кровяные клетки овцы (SRBC), покрытые B7-H1 антигеном.
В присутствии культуры B-клеток, содержащей клетки плазмы, секретирующие иммуноглобулин, представляющий интерес, и комплемент, образование бляшек указывает на специфический B7-H1-медиируемый лизис красных кровяных клеток овцы, окружающих клетку плазмы, представляющую интерес. Может быть выделена отдельная антигенспецифическая клетка плазмы, находящаяся в центре бляшки, и генетическую информацию, кодирующую специфичность антитела, выделяют из отдельной клетки плазмы. ДНК, кодирующие вариабельные участки тяжелой и легкой цепей антитела, могут быть клонированы с использованием обратной транскрипции с последующей ПЦР (ОТ-ПЦР). Такие клонированные ДНК могут быть затем вставлены в пригодный экспрессионный вектор, предпочтительно, векторную кассету, такую как пкДНК (pcDNA), более предпочтительно, вектор пкДНК, содержащий константные домены тяжелой и легкой цепей иммуноглобулина. Полученный вектор может быть затем трансфицирован в клетки-хозяева, например, клетки HEK293, клетки CHO, и культивироваться в обычных питательных средах, соответствующим образом модифицированных для индуцирования транскрипции, селектирования трансформантов или амплификации генов, кодирующих желательные последовательности.
Следует понимать, что антитела, описанные здесь, могут экспрессироваться в клеточных линиях, отличных от гибридомных клеточных линий. Последовательности, кодирующие конкретные антитела, могут быть использованы для трансформации пригодной клетки-хозяина млекопитающего. Трансформация может быть проведена любым известным способом введения полинуклеотидов в клетку-хозяина, включая, например, упаковку полинуклеотид в вирус (или в вирусный вектор) и трансдукцию клетки-хозяина вирусом (или вектором), или с помощью процедур трансфекции, известных специалистам, примеры которых описаны в патентах США №№ 4399216, 4912040, 4740461 и 4959455 (указанные патенты настоящим включены сюда в качестве ссылок). Используемая процедура трансформации зависит от хозяина, которого требуется трансформировать. Способы введения гетерологических полинуклеотидов в клетки млекопитающего хорошо известны специалистам и включают декстран-медиируемую трансфекцию, преципитацию фосфатом кальция, полибрен-медиируемую трансфекцию, слияние протопластов, электропорацию, инкапсулирование полинуклеотида (полинуклеотидов) в липосомы и прямую микроинъекцию ДНК в ядро.
Клеточные линии млекопитающих, доступные для использования в качестве хозяев для экспрессии, хорошо известны специалистам и включают многие иммортализованные клеточные линии, доступные от NCIMB (Национальная коллекция промышленных и морских бактерий), включая, без ограничений, клетки яичника китайского хомячка (CHO), клетки HeLa, клетки почки детенышей хомячка (BHK), клетки почки обезьяны (COS), клетки человеческой гепатоцеллюлярной карциномы (например, Hep G2), эпителиальные клетки человеческой почки 293 (Hek293) и ряд других клеточных линий. Особенно предпочтительные клеточные линии выбирают путем определения клеточных линий, имеющих высокие уровни экспрессии и продуцирующих антитела с конститутивной способностью связывания B7-H1.
По методике межклеточного слияния получают миелому, клетку CHO или другую клеточную линию, имеющую тяжелую цепь с любым желательным изотипом, и другую миелому, клетку CHO или другую клеточную линию, содержащую легкую цепь. Такие клетки могут быть затем подвергнуты слиянию, и может быть выделена клеточная линия, экспрессирующая интактное антитело.
Соответственно, при получении антител-кандидатов, обладающих желательными «структурными» признаками, как описано выше, они обычно могут быть снабжены, по меньшей мере, некоторыми из желательных «функциональных» признаков путем переключения изотипа.
По методике межклеточного слияния получают миелому, клетку CHO или другую клеточную линию, имеющую тяжелую цепь с любым желательным изотипом, и другую миелому, клетку CHO или другую клеточную линию, содержащую легкую цепь. Такие клетки могут быть затем подвергнуты слиянию, и может быть выделена клеточная линия, экспрессирующая интактное антитело.
Соответственно, при получении антител-кандидатов, обладающих желательными “структурными” признаками, как описано выше, они обычно могут быть снабжены, по меньшей мере, некоторыми из желательных “функциональных” признаков путем переключения изотипа.
Последовательности антитела
Варианты воплощения изобретения включают антитела, перечисленные ниже в Таблице 1. В этой таблице указаны идентификационный номер каждого антитела, вместе с SEQ ID номером генов и полипептидов вариабельного домена соответствующей тяжелой цепи и легкой цепи, соответственно. Каждой последовательности антитела был присвоен идентификационный номер.
Терапевтическое введение и рецептуры композиций
Варианты воплощения изобретения включают стерильные фармацевтические композиции анти-B7-H1 антител, пригодные для использования в качестве средств для лечения болезней. Такие композиции будут ингибировать связывание B7-H1 с одним или несколькими его когнатными лигандами, тем самым обеспечивая лечение патологических состояний, при которых, например, B7-H1 в сыворотке или ткани аномально повышен. Антитела по изобретению предпочтительно обладают достаточной аффинностью для сильного ингибирования активности B7-H1, или ингибируют связывание B7-H1 с одним или несколькими его когнатными лигандами, и предпочтительно имеют достаточную продолжительность действия для того, чтобы обеспечить редко повторяющееся введение доз людям. Увеличенная продолжительность действия позволит использовать схемы лечения с менее частым и более удобным введением доз альтернативными парентеральными путями, такими как подкожная или внутримышечная инъекция.
Стерильные композиции могут быть созданы, например, путем фильтрации через стерильные фильтровальные мембраны перед или после лиофилизации и восстановления антитела. Антитело обычно будет храниться в лиофилизированной форме или в растворе. Терапевтические композиции антитела обычно помещают в контейнер, имеющий стерильный входной канал, например, пакетик с раствором для внутривенного введения или флакон, имеющий переходное приспособление, позволяющее отбирать композицию, такое как пробка, которую можно проткнуть иглой для подкожных инъекций.
Путь введения антитела соответствует известным способам, например, инъекции или инфузии внутривенным, интраперитонеальным, интрацеребральным, внутримышечным, внутриглазным, интраартериальным, интратекальным путями, ингаляцией или в очаг поражения, прямой инъекции в место локализации опухоли, или с помощью систем замедленного высвобождения, как описано ниже. Антитело, предпочтительно, вводят непрерывно путем инфузии или болюсной инъекции.
Эффективное количество антитела для терапевтического применения будет зависеть, например, от терапевтических целей, пути введения и состояния пациента. Соответственно, предпочтительно, чтобы терапевт титровал дозу и модифицировал путь введения, необходимый для достижения оптимального терапевтического эффекта. Типично, практикующий врач будет вводить антитело до достижения дозы, обеспечивающей желательный эффект. Ход такой терапии легко контролируется обычными методами анализа или с помощью анализов, описанных здесь.
Антитела, описанные здесь, могут быть приготовлены в виде смеси с фармацевтически приемлемым носителем. Такая терапевтическая композиция может быть введена внутривенно или через нос или легкие, предпочтительно в виде жидкого или порошкообразного аэрозоля (лиофилизированного). Композиция также может быть введена парентерально или подкожно, по желанию. При системном введении терапевтическая композиция должна быть стерильной, апирогенной и иметь вид парентерально приемлемого раствора, с учетом требований к pH, изотоничности и стабильности. Такие условия известны квалифицированным специалистам. Вкратце, дозированные композиции соединений, описанных здесь, готовят для хранения или введения путем смешивания соединения, имеющего желательную степень чистоты, с фармацевтически приемлемыми носителями, эксципиентами или стабилизаторами. Такие материалы являются нетоксичными для реципиентов в используемых дозах и концентрациях, и включают буферы, такие как TRIS HCl, фосфат, цитрат, ацетат и другие соли органических кислот; антиоксиданты, такие как аскорбиновая кислота; низкомолекулярные (менее примерно десяти остатков) пептиды, такие как полиаргинин, белки, такие как сывороточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутаминовая кислота, аспарагиновая кислота или аргинин; моносахариды, дисахариды и другие углеводы, включая целлюлозу или ее производные, глюкозу, маннозу или декстрины; хелатирующие агенты, такие как EDTA; сахароспирты, такие как маннит или сорбит; противоионы, такие как натрий, и/или неионные поверхностно-активные вещества, такие как TWEEN, PLURONICS или полиэтиленгликоль.
Стерильные композиции для инъекций могут быть составлены в соответствии с обычной фармацевтической практикой, как описано в Remington: The Science and Practice of Pharmacy (20th ed, Lippincott Williams & Wilkens Publishers (2003)). Например, может быть желательным растворение или суспендирование активного соединения в носителе, таком как вода или природное растительное масло, такое как кунжутное, арахисовое или хлопковое, или синтетическом жирном носителе, таком как этилолеат и т.п. Буферы, консерванты, антиоксиданты и т.п. могут быть включены в соответствии с принятой фармацевтической практикой.
Пригодные примеры препаратов с замедленным высвобождением включают полупроницаемые матрицы из твердых гидрофобных полимеров, содержащие полипептид, где матрицы имеют вид формованных изделий, пленок или микрокапсул. Примеры матриц с замедленным высвобождением включают сложные полиэфиры, гидрогели (например, поли-(2-гидроксиэтилметакрилат), как описано Langer et al., J. Biomed Mater. Res., (1981) 15:167-277 и Langer, Chem. Tech., (1982) 12:98-105, или поли(виниловый спирт)), полилактиды (патент США № 3773919, EP 58481), сополимеры L-глутаминовой кислоты и гамма-этил-L-глутамата (Sidman et al., Biopolymers, (1983) 22:547-556), неразлагающийся этилен-винилацетат (Langer et al., выше), разлагающиеся сополимеры молочной кислоты-гликолевой кислоты, такие как LUPRON Depot™ (микросферы для инъекций, состоящие из сополимера молочной кислоты-гликолевой кислоты и лейпролида ацетата), и поли-D-(-)-3-оксимасляной кислоты (EP 133988).
Если полимеры, такие как этилен-винилацетат и молочная кислота-гликолевая кислота, обеспечивают высвобождение молекул на протяжении более 100 дней, определенные гидрогели высвобождают белки в течение более коротких периодов времени. Когда инкапсулированные белки остаются в организме в течение длительного времени, они могут денатурировать или агрегировать в результате воздействия влаги при 37°C, приводя к потере биологической активности и возможным изменениям иммуногенности. Могут быть разработаны рациональные стратегии стабилизации белка в зависимости от задействованного механизма. Например, если было обнаружено, что образование межмолекулярной S-S связи протекает по механизму агрегации путем дисульфидного обмена, то стабилизацию можно обеспечить путем модификации сульфгидрильных остатков, лиофилизации из кислотных растворов, контроля влагосодержания, использования пригодных добавок и разработки специальных композиций полимерной матрицы.
Композиции с замедленным высвобождением также включают препараты кристаллов антитела, суспендированных в пригодных композициях, способных обеспечивать сохранность кристаллов в суспензии. Такие препараты, при введении подкожной или интраперитонеальной инъекцией, могут создавать эффект замедленного высвобождения. Другие композиции также включают липосомально захваченные антитела. Липосомы, содержащие такие антитела, получают способами, по известному патенту США № DE 3218121; Epstein et al., Proc. Natl. Acad. Sci. USA, (1985) 82:3688-3692; Hwang et al., Proc. Natl. Acad. Sci. USA, (1980) 77:4030-4034; EP 52322; EP 36676; EP 88046; EP 143949; 142641; патентной заявке Японии 83-118008; патентам США №№ 4485045 и 4544545; и EP 102324.
Дозировка композиции антитела для конкретного пациента будет определяться лечащим врачом с учетом различных факторов, как известно, модифицирующих действие лекарственных препаратов, включая тяжесть и тип болезни, вес тела, пол, диету, время и путь введения, другие лекарственные средства и другие релевантные клинические факторы. Терапевтически эффективные дозы могут быть определены in vitro или in vivo способами.
Эффективное для терапевтического применения количество антител, описанное здесь, будет зависеть, например, от терапевтических целей, пути введения и состояния пациента. Соответственно, терапевт предпочтительно будет титровать дозу и модифицировать путь введения, необходимый для достижения оптимального терапевтического эффекта. Типичная суточная доза может составлять от примерно 0,0001 мг/кг, 0,001 мг/кг, 0,01 мг/кг, 0,1 мг/кг, 1 мг/кг, 10 мг/кг и до 100 мг/кг, 1000 мг/кг, 10000 мг/кг или больше, в пересчете на вес тела пациента, в зависимости от вышеперечисленных факторов. Доза может составлять от 0,0001 мг/кг до 20 мг/кг, от 0,0001 мг/кг до 10 мг/кг, от 0,0001 мг/кг до 5 мг/кг, от 0,0001 до 2 мг/кг, от 0,0001 до 1 мг/кг, от 0,0001 мг/кг до 0,75 мг/кг, от 0,0001 мг/кг до 0,5 мг/кг, от 0,0001 мг/кг до 0,25 мг/кг, от 0,0001 до 0,15 мг/кг, от 0,0001 до 0,10 мг/кг, от 0,001 до 0,5 мг/кг, от 0,01 до 0,25 мг/кг или от 0,01 до 0,10 мг/кг веса тела пациента в зависимости от вышеперечисленных факторов. Типично, практикующий врач будет вводить терапевтическое антитело до достижения дозы, обеспечивающей желательный эффект. Ход такой терапии легко контролируется обычными или описанными здесь методами анализа.
Дозы антител по изобретению могут повторяться и введение может производиться с интервалом в, по меньшей мере, 1 день, 2 дня, 3 дня, 5 дней, 10 дней, 15 дней, 30 дней, 45 дней, 2 месяца, 75 дней, 3 месяца или, по меньшей мере, 6 месяцев.
Следует понимать, что введение терапевтических веществ в соответствии с композициями и способами по настоящему изобретению будет осуществляться с пригодными носителями, эксципиентами и другими агентами, включаемыми в рецептуры композиций для обеспечения улучшенного переноса, доставки, толерантности и т.п. Такие композиции включают, например, порошки, пасты, жидкие мази, желе, воска, масла, липиды, липид (катионный или анионный)-содержащие везикулы (такие как LipofectinTM), конъюгаты ДНК, обезвоженные (anhydrous absorption) пасты, эмульсии масло-в-воде и вода-в-масле, эмульсии материала carbowax (полиэтиленгликоли с различными молекулярными весами), полутвердые гели и полутвердые смеси, содержащие материал carbowax. Любые из вышеупомянутых смесей могут быть пригодны для лечения и терапии в соответствии с настоящим изобретением, при условии, что активный ингредиент композиции не инактивируется композицией и композиция является физиологически совместимой и переносимой для пути введения. См. также Baldrick P. “Pharmaceutical excipient development: the need for preclinical guidance.” Regul. Toxicol. Pharmacol. 32(2):210-8 (2000), Wang W. “Lyophilisation and development of solid protein pharmaceuticals.” Int. J. Pharm. 203(1-2):1-60 (2000), Charman WN “Lipids, lipophilic drugs, and oral drug delivery - some emerging concepts.” J Pharm Sci. 89(8):967-78 (2000), Powell et al. “Compendium of excipients for parenteral formulations” PDA J Pharm Sci Technol. 52:238-311 (1998) и приведенные в них ссылки для получения дополнительной информации, относящейся к рецептурам композиций, эксципиентам и носителям, хорошо известным химикам-фармацевтам.
Разработка и создание других терапевтических средств
В соответствии с настоящим изобретением и на основании активности антител, продуцируемых и охарактеризованных здесь в связи с B7-H1, становится возможной и раскрытой для квалифицированного специалиста в данной области техники разработка других терапевтических модальностей кроме фрагментов антител. Такие модальности включают, без ограничений, усовершенствованные терапевтические средства на основе антител, такие как биспецифические антитела, иммунотоксины, меченые радиоактивными изотопами терапевтические средства, и V-домены отдельного антитела, антителоподобный связывающий агент на основании каркасных участков, отличных от V-области, однодоменные антитела, создание пептидных терапевтических средств, B7-H1 связывающие домены в новых каркасных структурах, генные терапии, в частности, интратела, антисмысловые терапевтические средства и малые молекулы.
Антигенсвязывающий сайт может быть получен путем размещения CDR на не принадлежащих антителу белковых каркасах, таких как фибронектин или цитохром B и т.д. (Haan & Maggos (2004) BioCentury, 12(5): A1-A6; Koide et al. (1998) Journal of Molecular Biology, 284:1141-1151; Nygren et al. (1997) Current Opinion in Structural Biology, 7:463-469), или путем рандомизации или мутирования аминокислотных остатков петли белкового каркаса для придания специфичности связывания с желательной мишенью. Подробный обзор каркасных структур для конструирования новых связывающих сайтов в белках приведен Nygren et al. (Nygren et al. (1997) Current Opinion in Structural Biology, 7:463-469). Белковые каркасы для миметиков антител раскрыты в WO/0034784, целиком включенном сюда в качестве ссылки, в котором авторы изобретения описывают белки (миметики антитела), включающие домен фибронектина типа III, имеющий, по меньшей мере, одну рандомизированную петлю. Пригодным каркасом для прививки в него одного или нескольких CDR, например, набора HCDR, может быть любой домен, являющийся членом суперсемейства гена иммуноглобулина. Структурный каркас может быть человеческим или нечеловеческим белком. Преимущество не связанного с антителом белкового каркаса заключается в том, что он может обеспечивать антигенсвязывающий сайт в каркасной молекуле, имеющей меньшие размеры, и/или более простой в производстве, чем, по меньшей мере, некоторые молекулы антитела. Малый размер связывающего элемента может обеспечивать полезные физиологические свойства, такие как способность проникать в клетки, глубоко проникать в ткани или достигать мишеней в других структурах, или связываться с белковыми карманами антигена-мишени. Обзор использования антигенсвязывающих сайтов в не принадлежащих антителу белковых каркасах приведен Wess, 2004 (Wess, L. in: BioCentury, The Bernstein Report on BioBusiness, 12(42), A1-A7, 2004). Типичными являются белки, имеющие стабильную основную цепь и одну или несколько вариабельных петель, в которых аминокислотная последовательность петли или петель специфически или случайным образом мутирована для создания антигенсвязывающего сайта, связывающего антиген-мишень. Такие белки включают IgG-связывающие домены белка A из областей S, трансферрин, альбумин, тетранектин, фибронектин (например, 10-й домен фибронектина типа III), липокалины, а также гамма-кристаллические и другие каркасные структуры Affilin™ (Scil Proteins). Примеры других подходов включают синтетические «микротела» (Microbodies) на основе циклотидов - малых белков, имеющих внутримолекулярные дисульфидные связи, микробелки (Microproteins) (Versabodies™, Amunix) и белки с анкириновыми повторами (DARPins, Molecular Partners).
Кроме последовательностей антитела и/или антигенсвязывающего сайта, специфический связывающий агент в соответствии с настоящим изобретением может включать другие аминокислоты, например, образующие пептид или полипептид, такой как складчатый домен, или для придания молекуле другой функциональной характеристики помимо способности связывать антиген. Специфические связывающие агенты по изобретению могут нести детектируемую метку, или могут быть конъюгированы с токсином или нацеливающим фрагментом или ферментом (например, с помощью пептидильной связи или линкера). Например, специфический связывающий агент может включать каталитический сайт (например, в ферментном домене), а также антигенсвязывающий сайт, причем антигенсвязывающий сайт связывается с антигеном и, таким образом, нацеливает каталитический сайт на антиген. Каталитический сайт может ингибировать биологическую функцию антигена, например, путем расщепления.
В связи с созданием усовершенствованных терапевтических средств на основе антител, для которых фиксация комплемента является желательной характеристикой, может возникнуть возможность обойти зависимость от комплемента для уничтожения клеток путем использования, например, биспецифических антител, иммунотоксинов или радиоактивных меток.
Например, могут быть созданы биспецифические антитела, включающие (i) два конъюгированных вместе антитела - одно со специфичностью к B7-H1 и другое - ко второй молекуле, (ii) единое антитело, имеющее одну цепь, специфическую по отношению к B7-H1, и вторую цепь, специфическую по отношению ко второй молекуле, или (iii) одноцепочечное антитело, обладающее специфичностью по отношению к B7-H1 и другой молекуле. Такие биспецифические антитела могут быть созданы с использованием хорошо известных методик; например, в связи с (i) и (ii) см., например, Fanger et al. Immunol Methods 4:72-81 (1994), и Wright and Harris, supra, и в связи с (iii) см., например, Traunecker et al. Int. J. Cancer (Suppl.) 7:51-52 (1992). В любом случае, вторая специфичность может быть выбрана по желанию. Например, вторая специфичность может относиться к рецепторам активации тяжелой цепи, включая, без ограничений, CD16 или CD64 (см., например, Deo et al. Immunol. Today 18:127 (1997)) или CD89 (см., например, Valerius et al. Blood 90:4485-4492 (1997)).
Антитела также могут быть модифицированы таким образом, чтобы они действовали как иммунотоксины, с использованием методик, хорошо известных специалистам. См., например, Vitetta, Immunol Today 14:252 (1993). См. также патент США № 5194594. В связи с приготовлением радиоактивно меченых антител, такие модифицированные антитела также могут быть легко приготовлены с использованием методик, хорошо известных специалистам. См., например, Junghans et al., Cancer Chemotherapy and Biotherapy 655-686 (2d edition, Chafner and Longo, eds., Lippincott Raven (1996)). См. также патенты США №№ 4681581, 4735210, 5101827, 5102990 (RE 35500), 5648471 и 5697902. Каждый из иммунотоксинов или радиоактивно меченой молекулы будет, вероятно, уничтожать клетки, экспрессирующие желательный домен олигомеризации субъединиц мультимерного фермента.
Если антитело связано с агентом (например, радиоизотопом, фармацевтической композицией или токсином), то предусматривается, что агент обладает фармацевтической способностью, выбранной из группы антимитотических, алкилирующих, антиметаболитных, антиангиогенных, апоптических, алкалоидных, COX-2 и антибиотических агентов и их комбинаций. Агент может быть выбран из группы азотистых аналогов горчичного газа, производных этиленимина, алкилсульфонатов, нитрозомочевин, триазенов, аналогов фолиевой кислоты, антрациклинов, таксанов, ингибиторов COX-2, аналогов пиримидина, аналогов пурина, антиметаболитных веществ, антибиотических веществ, ферментов, эпиподофиллотоксинов, координационных комплексов платины, алкалоидов барвинка (vinca), замещенных мочевин, метилгидразиновых производных, адренокортикальных супрессантов, антагонистов, эндостатина, таксолов, камптотецинов, оксалиплатина, доксорубицинов и их аналогов, и их комбинаций. Примеры токсинов дополнительно включают гелонин, экзотоксин Pseudomonas (PE), PE40, PE38, дифтерийный токсин, рицин, абрин, альфа-токсин, сапорин, рибонуклеазу (РНКазу), ДНКазу I, стафилококковый энтеротоксин-A, антивирусный белок фитолакки американской, гелонин, эндотоксин Pseudomonas, члены энедиинового семейства молекул, такие как калихеамицин и эсперамицин, а также их производные, комбинации и модификации. Химические токсины также могут быть взяты из группы, состоящей из дуокармицина (см., например, патент США № 5703080 и патент США № 4923990), метотрексата, доксорубицина, мелфалана, хлорамбуцила, ARA-C, виндезина, митомицина C, цисплатина (cis-platinum), этопозида, блеомицина и 5-фторурацила. Примеры химиотерапевтических агентов также включают адриамицин, доксорубицин, 5-фторурацил, цитозинарабинозид (Ara-C), циклофосфамид, тиотепа, таксотер (доцетаксел), бусульфан, цитоксин, таксол, метотрексат, цисплатин, мелфалан, винбластин, блеомицин, этопозид, ифосфамид, митомицин C, митоксантрон, винкристин (vincreistine), винорелбин, карбоплатин, тенипозид, дауномицин, карминомицин, аминоптерин, дактиномицин, митомицины, эсперамицины (см., патент США № 4675187), мелфалан и другие родственные азотистые аналоги горчичного газа. Пригодные токсины и химиотерапевтические агенты описаны в Remington's Pharmaceutical Sciences, 19th Ed. (Mack Publishing Co. 1995), и в Goodman and Gilman's Pharmacological Basis of Therapeutics, 7th Ed. (MacMillan Publishing Co. 1985). Другие пригодные токсины и/или химиотерапевтические агенты известны квалифицированным специалистам.
Примеры радиоизотопов включают гамма-излучатели, излучатели позитронов и рентгеновские излучатели, которые могут быть использованы для локализаци и/или терапии, и бета-излучатели и альфа-излучатели, которые могут быть использованы для терапии. Радиоизотопы, описанные ранее как пригодные для диагностики, прогнозирования и определения стадии, также являются пригодными для использования в терапевтических средствах.
Неограничивающие примеры противораковых или антилейкемических агентов включают антрациклины, такие как доксорубицин (адриамицин), даунорубицин (дауномицин), идарубицин, деторубицин, карминомицин, эпирубицин, эзорубицин, и их морфолино и замещенные производные, комбинации и модификации. Типичные примеры фармацевтических агентов включают цисплатин, таксол, калихеамицин, винкристин, цитарабин (Ara-C), циклофосфамид, преднизон, даунорубицин, идарубицин, флударабин, хлорамбуцил, интерферон-альфа, гидроксимочевину, темозоломид, талидомид и блеомицин, и их производные, комбинации и модификации. Предпочтительно, противораковое или антилейкемическое средство представляет собой доксорубицин, морфолинодоксорубицин или морфолинодаунорубицин.
Антитела по изобретению также охватывают антитела, имеющие периоды полувыведения (например, периоды полувыведения из сыворотки) у млекопитающего, предпочтительно, человека, большие, чем у немодифицированного антитела. В одном варианте воплощения указанный период полувыведения антитела составляет более примерно 15 дней, более примерно 20 дней, более примерно 25 дней, более примерно 30 дней, более примерно 35 дней, более примерно 40 дней, более примерно 45 дней, более примерно 2 месяцев, более примерно 3 месяцев, более примерно 4 месяцев или более примерно 5 месяцев. Увеличенные периоды полувыведения антител по настоящему изобретению или их фрагментов у млекопитающего, предпочтительно человека, приводят к более высокому титру указанных антител или фрагментов антител в сыворотке млекопитающего и, таким образом, уменьшают частоту введения указанных антител или фрагментов антител и/или снижают концентрацию указанных антител или фрагментов антител при введении. Антитела или их фрагменты, имеющие увеличенные периоды полувыведения in vivo, могут быть получены методами, известными квалифицированным специалистам. Например, антитела или их фрагменты с увеличенными периодами полувыведения in vivo могут быть получены путем модификации (например, замещения, делеции или введения) аминокислотных остатков, идентифицированных как принимающие участие во взаимодействии между Fc-доменом и FcRn-рецептором (см., например, международные публикации №№ WO 97/34631 и WO 02/060919, которые целиком включены сюда в качестве ссылок). Антитела или их фрагменты с увеличенными периодами полувыведения in vivo могут быть получены путем присоединения к указанным антителам или фрагментам антител полимерных молекул, таких как высокомолекулярный полиэтиленгликоль (ПЭГ). ПЭГ может быть присоединен к указанным антителам или фрагментам антител с использованием мультифункционального линкера или без него путем сайт-специфической конъюгации ПЭГ с N- или C-концом указанных антител или фрагментов антител или через эпсилон-аминогруппы, присутствующие на лизиновых остатках. Будет использоваться линейная или разветвленная дериватизация полимера, приводящая к минимальной потере биологической активности. Степень конъюгации будет точно контролироваться методами SDS-PAGE (электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия) и масс-спектрометрии для обеспечения требуемой конъюгации молекул ПЭГ с антителами. Непрореагировавший ПЭГ может быть отделен от конъюгатов антитело-ПЭГ, например, с помощью эксклюзионной или ионообменной хроматографии.
Квалифицированному специалисту будет понятно, что хотя в вышеупомянутых вариантах воплощения величины аффинности могут быть важны, другие факторы могут иметь такую же или большую важность, в зависимости от конкретной функции антитела. Например, для иммунотоксина (токсина, ассоциированного с антителом) событие связывания антитела с мишенью может быть полезным; однако в некоторых вариантах воплощения желательным конечным результатом будет интернализация токсина в клетку. По существу, антитела с высоким процентом интернализации могут быть желательными в таких ситуациях. Таким образом, в одном варианте воплощения предусматриваются антитела с высокой эффективностью интернализации. Высокая эффективность интернализации может быть измерена как процент интернализованного антитела и может иметь значения от низких величин до 100%. Например, в различных вариантах воплощения высокая эффективность может составлять 0, 1-5, 5-10, 10-20, 20-30, 30-40, 40-45, 45-50, 50-60, 60-70, 70-80, 80-90, 90-99 и 99-100%. Квалифицированному специалисту будет понятно, что желательная эффективность может быть разной в различных вариантах воплощения, в зависимости от, например, ассоциированного агента, количества антитела, которое может быть введено в область поражения, побочных эффектов комплекса антитело-агент, типа (например, типа рака) и тяжести проблемы, требующей лечения.
В других вариантах воплощения раскрытых здесь антител предусматривается аналитический набор для детектирования экспрессии B7-H1 в тканях или клетках млекопитающего с целью проведения обследования на предмет болезни или расстройства, ассоциированных с изменениями экспрессии B7-H1. Набор включает антитело, связывающее B7-H1, и средства, указывающие на протекание реакции антитела с антигеном, в случае его присутствия.
В некоторых вариантах воплощения предусматривается изделие, включающее контейнер, включающий композицию с антителом, специфически связывающим B7-H1, и вкладыш в упаковку или метку, указывающие, что композиция может быть использована для лечения болезни, медиируемой экспрессией B7-H1. Предпочтительно, млекопитающее, более предпочтительно, человек, получает антитело, специфически связывающее B7-H1.
Комбинации
Противоопухолевое лечение, описанное здесь, может быть применено как монотерапия или может включать, в дополнение к соединениям по изобретению, обычную хирургию, трансплантации костного мозга и периферических стволовых клеток или лучевую терапию или химиотерапию. Такая химиотерапия может включать одну или несколько из следующих категорий противоопухолевых агентов:
(i) другие антипролиферативные/антинеопластические лекарственные препараты и их комбинации, используемые в медицинской онкологии, такие как алкилирующие агенты (например, цисплатин, оксалиплатин, карбоплатин, циклофосфамид, азотистый иприт, мелфалан, хлорамбуцил, бусульфан, темозоламид и нитрозомочевины); антиметаболитные средства (например, гемцитабин и антифолаты, такие как фторпиримидины, например, 5-фторурацил и тегафур, ралтитрексед, метотрексат, цитозинарабинозид и гидроксимочевина); противоопухолевые антибиотические средства (например, антрациклины, такие как адриамицин, блеомицин, доксорубицин, дауномицин, эпирубицин, идарубицин, митомицин-C, дактиномицин и митрамицин); антимитотические агенты (например, алкалоиды барвинка, такие как винкристин, винбластин, виндезин и винорелбин, и таксоиды, такие как таксол и таксотер, и ингибиторы полокиназы); и ингибиторы топоизомеразы (например, эпиподофиллотоксины, такие как этопозид и тенипозид, амсакрин, топотекан и камптотецин);
(ii) цитостатические агенты, такие как антиэстрогены (например, тамоксифен, фулвестрант, торемифен, ралоксифен, дролоксифен и йодоксифен), антиандрогены (например, бикалутамид, флутамид, нилутамид и ципротерон ацетат), антагонисты LHRH или агонисты LHRH (например, госерелин, лейпрорелин и бусерелин), прогестогены (например, мегестрол ацетат), ингибиторы ароматазы (например, анастрозол, летрозол, воразол и экземестан) и ингибиторы 5α-редуктазы, такие как финастерид;
(iii) антиинвазивные агенты (например, ингибиторы семейства киназ c-Src, такие как 4-(6-хлор-2,3-метилендиоксианилино)-7-[2-(4-метилпиперазин-1-ил)этокси]-5-тетрагидропиран-4-илоксихиназолин (AZD0530; международная патентная заявка WO 01/94341) и N-(2-хлор-6-метилфенил)-2-{6-[4-(2-гидроксиэтил)пиперазин-1-ил]-2-метилпиримидин-4-иламино}тиазол-5-карбоксамид (дасатиниб, BMS-354825; J. Med. Chem., 2004, 47, 6658-6661), и ингибиторы металлопротеиназы, такие как маримастат, ингибиторы рецепторной функции активатора плазминогена урокиназы или ингибиторы катепсиновой активности, ингибиторы серинпротеаз, например, матриптаза, гепсин, урокиназа и ингибиторы функции интегрина αvβ6;
(iv) цитотоксические агенты, такие как флударабин, 2-хлордезоксиаденозин, хлорамбуцил или доксорубицин и их комбинации, такие как флударабин + циклофосфамид, CVP: циклофосфамид + винкристин + преднизон, ACVBP: доксорубицин + циклофосфамид + виндезин + блеомицин + преднизон, CHOP: циклофосфамид + доксорубицин + винкристин + преднизон, CNOP: циклофосфамид + митоксантрон + винкристин + преднизон, m-BACOD: метотрексат + блеомицин + доксорубицин + циклофосфамид + винкристин + дексаметазон + лейковорин, MACOP-B: метотрексат + доксорубицин + циклофосфамид + винкристин + преднизон фиксированная доза + блеомицин + лейковорин, или ProMACE CytaBOM: преднизон + доксорубицин + циклофосфамид + этопозид + цитарабин + блеомицин + винкристин + метотрексат + лейковорин;
(v) ингибиторы функции фактора роста: например, такие ингибиторы включают антитела фактора роста и антитела рецептора фактора роста (например, анти-erbB2 антитело трастузумаб [Herceptin™], анти-EGFR антитело панитумумаб, анти-erbB1 антитело цетуксимаб [Erbitux, C225] и любые антитела факторов роста или рецепторов фактора роста, раскрытые Stern et al. Critical reviews in oncology/haematology, 2005, Vol. 54, pp11-29); такие ингибиторы также включают ингибиторы тирозинкиназы, например, ингибиторы семейства эпидермального фактора роста (например, ингибиторы EGFR семейства тирозинкиназы, такие как N-(3-хлор-4-фторфенил)-7-метокси-6-(3-морфолино-пропокси)хиназолин-4-амин (гефитиниб, ZD1839), N-(3-этинилфенил)-6,7-бис(2-метоксиэтокси)хиназолин-4-амин (эрлотиниб, OSI-774) и 6-акриламидо-N-(3-хлор-4-фторфенил)-7-(3-морфолинопропокси)хиназолин-4-амин (CI 1033), ингибиторы erbB2 тирозинкиназы, такие как лапатиниб, ингибиторы семейства фактора роста гепатоцитов, ингибиторы семейства тромбоцитарного фактора роста, такие как матиниб, ингибиторы серин/треонинкиназ (например, ингибиторы сигнальных путей Ras/Raf, такие как ингибиторы фарнезилтрансферазы, например, сорафениб (BAY 43-9006)), ингибиторы клеточной сигнализации посредством MEK и/или AKT-киназ, ингибиторы семейства факторов роста гепатоцитов, ингибиторы c-kit, ингибиторы abl киназы, ингибиторы киназы IGF рецептора (инсулиноподобный фактор роста); ингибиторы ауроракиназы (например, AZD1152, PH739358, VX-680, MLN8054, R763, MP235, MP529, VX-528 и AX39459) и ингибиторы циклинзависимой киназы, такие как ингибиторы CDK2 и/или CDK4, и ингибиторы выживания сигнальных белков, такие как Bcl-2, Bcl-XL например, ABT-737;
(vi) антиангиогенные агенты, такие как ингибирующие эффекты сосудистого эндотелиального фактора роста, [например, антитело против фактора роста сосудистых эндотелиальных клеток бевацизумаб (Avastin™)] и ингибиторы рецептора тирозинкиназы VEGF, такие как 4-(4-бром-2-фторанилино)-6-метокси-7-(1-метилпиперидин-4-илметокси)хиназолин (ZD6474; Пример 2 WO 01/32651), 4-(4-фтор-2-метилиндол-5-илокси)-6-метокси-7-(3-пирролидин-1-илпропокси)хиназолин (AZD2171; Пример 240 WO 00/47212), ваталаниб (PTK787; WO 98/35985) и SU11248 (сунитиниб; WO 01/60814), соединения, такие как раскрытые в международных патентных заявках WO97/22596, WO 97/30035, WO 97/32856, WO 98/13354, WO00/47212 и WO01/32651, антитела против рецепторов сосудистого эндотелиального фактора роста, такие как анти-KDR антитела и анти-flt1 антитела), и соединения, действующие по другим механизмам (например, линомид, ингибиторы функции интегрина αvβ3 и ангиостатин)] или колониестимулирующий фактор 1 (CSF1) или рецептор CSF1; дополнительную информацию о AZD2171 можно найти в Wedge et al. (2005) Cancer Research. 65(10):4389-400; дополнительную информацию о AZD6474 можно найти в Ryan & Wedge (2005) British Journal of Cancer. 92 Suppl 1:S6-13; обе публикации целиком включены сюда в качестве ссылок;
(vii) агенты, поражающие сосуды, такие как Комбретастатин A4 и соединения, раскрытые в международных патентных заявках WO 99/02166, WO 00/40529, WO 00/41669, WO 01/92224, WO 02/04434 и WO 02/08213;
(viii) антисмысловые терапии, например, направленные на вышеперечисленные мишени, такие как ISIS 2503, анти-ras антисмысловые средства или G3139 (Genasense), анти-bcl2 антисмысловые средства;
(ix) подходы генной терапии, включая, например, подходы с заменой аберрантных генов, таких как аберрантный p53 или аберрантный BRCA1 или BRCA2, GDEPT (ген-направленная ферментная пролекарственная терапия) подходы с использованием цитозиндеаминазы, тимидинкиназы или фермента бактериальной нитроредуктазы, и подходы, направленные на повышение толерантности пациента к химиотерапии или лучевой терапии, такие как генная терапия мультилекарственной резистентности;
(x) иммунотерапевтические подходы, включая, например, лечение Алемтузумабом (campath-1H™), моноклональным антителом, направленным на CD52, или лечение антителами, направленными на CD22, ex vivo и in vivo подходы по повышению иммуногенности опухолевых клеток пациента, трансфекцию цитокинами, такими как интерлейкин 2, интерлейкин 4 или гранулоцит-макрофаг колониестимулирующий фактор, подходы, направленные на снижение анергии T-клеток, такие как лечение моноклональными антителами, ингибирующими функцию CTLA-4, подходы с использованием трансфицированных иммунных клеток, таких как цитокин-трансфицированные дендритные клетки, подходы с использованием цитокин-трансфицированных опухолевых клеточных линий и подходы, использующие анти-идиотипические антитела, адаптивный перенос T-клеток с использованием T-клеток, подвергнутых неспецифической активации или нацеленных на конкретный антиген, представляющий интерес, ex vivo;
(xi) подходы с вакцинацией, включая, например, лечение вакциной, направленной против определенной вирусной инфекции, такой как ВИЧ или вирус гепатита B (HBV), или лечение вакциной, направленной против определенного опухолевого антигена;
(xii) ингибиторы деградации белка, такие как ингибитор протеасом, такой как Велкаде (бортезомид); и
(xiii) биотерапевтические терапевтические подходы, например, использующие пептиды или белки (такие как антитела или растворимые конструкты внешних рецепторных доменов), которые секвестируют рецепторы лигандов, блокируют связывание лиганда с рецептором или ослабляют сигнализацию рецептора (например, вследствие повышенной деградации рецептора или сниженных уровней экспрессии).
В одном варианте воплощения противоопухолевое лечение, описанное здесь, может предусматривать, в дополнение к соединениям по изобретению, лечение другими антипролиферативными/антинеопластическими лекарственными препаратами и их комбинациями, используемыми в медицинской онкологии, такими как алкилирующие агенты (например, цисплатин, оксалиплатин, карбоплатин, циклофосфамид, азотистый иприт, мелфалан, хлорамбуцил, бусульфан, темозоламид и нитрозомочевины); антиметаболитные средства (например, гемцитабин и антифолаты, такие как фторпиримидины, например, 5-фторурацил и тегафур, ралтитрексед, метотрексат, цитозинарабинозид и гидроксимочевина); противоопухолевые антибиотические средства (например, антрациклины, такие как адриамицин, блеомицин, доксорубицин, дауномицин, эпирубицин, идарубицин, митомицин-C, дактиномицин и митрамицин); антимитотические агенты (например, алкалоиды барвинка, такие как винкристин, винбластин, виндезин и винорелбин, и таксоиды, такие как таксол и таксотер, и ингибиторы полокиназы); и ингибиторы топоизомеразы (например, эпиподофиллотоксины, такие как этопозид и тенипозид, амсакрин, топотекан и камптотецин).
Такое совместное лечение может осуществляться путем одновременного, последовательного или раздельного дозирования индивидуальных компонентов лечения. Такие комбинированные продукты используют соединения по настоящему изобретению, или их фармацевтически приемлемые соли, в диапазонах значений доз, описанных выше, и другой фармацевтически активный агент в его дозволенном диапазоне значений доз.
ПРИМЕРЫ
Следующие примеры, включая проведенные эксперименты и полученные результаты, приводятся только в иллюстративных целях и не должны истолковываться как ограничивающие данное описание.
ПРИМЕР 1: ЭКСПРЕССИЯ РЕКОМБИНАНТНОГО ЧЕЛОВЕЧЕСКОГО B7-H1
кДНК человеческого B7-H1 (Dong, H. et al., 1999, Nat. Med. 5:1365-1369) амплифицируют из клона Image 7262208 (ATCC), используя полимеразную цепную реакцию (ПЦР), и затем клонируют в сайты Nhe 1 и EcoR1 вектора pcr3.1Bid. Этот конструкт вводят путем липофекции в клетки CHO (American Type Tissue Collection, № по каталогу CCL-61), и экспрессию на клеточной поверхности подтверждают с помощью анализа методом флуоресцентно активируемой сортировки клеток (FACS).
Внеклеточный домен человеческого B7-H1 (аминокислотные остатки 1-239), слитый с Fc-участком человеческого IgG1, был приобретен у фирмы R&D Systems Inc., № по каталогу 156-B7-100.
ПРИМЕР 2: ИММУНИЗАЦИЯ И ТИТРОВАНИЕ
Иммунизация
Моноклональные антитела против человеческого B7-H1 были созданы путем последовательной иммунизации мышей XenoMouse® (линии XenoMouse: XMG2 (IgG2 каппа/лямбда) и XMG4 (IgG4 каппа/лямбда) Amgen, Inc. Vancouver, British Columbia, Canada) с использованием 5-10 мкг химерного белка B7-H1/Fc или 1-2×106 клеток CHO, экспрессирующих рекомбинантный человеческий B7-H1, как описано в Примере 1.
Иммунизации проводили в соответствии со способами, раскрытыми в патентной заявке США № 08/759620, поданной 3 декабря 1996 года, и международных патентных заявках №№ WO 98/24893, опубликованной 11 июня 1998 года, и WO 00/76310, опубликованной 21 декабря 2000 года, описания которых настоящим включены сюда в качестве ссылок. Программы иммунизации приведены в Таблице 2.
Селекция животных для получения клеток по титру
Титры антител в сыворотке иммунизированных мышей определяют с помощью анализа методом ELISA. Планшеты (Corning Costar, № по каталогу 3368) покрывают человеческим белком B7-H1/Fc (R&D Systems Inc., № по каталогу 156-B7-100). B7-H1-специфические антитела детектируют с помощью мышиного антитела против человеческого IgG и козьего антитела против мышиного IgG Fc, конъюгированного с пероксидазой хрена. Типично отбирают пять животных с наивысшими титрами из каждой когорты иммунизации для выделения лимфоцитов и получения гибридом.
Описание программ иммунизации
ПРИМЕР 3: ВЫДЕЛЕНИЕ ЛИМФОЦИТОВ, ИЗОЛЯЦИЯ B-КЛЕТОК, СЛИЯНИЕ И ПОЛУЧЕНИЕ ГИБРИДОМ
Иммунизированных мышей умерщвляют цервикальной дислокацией, и дренирующие лимфатические узлы собирают и объединяют в пул для каждой когорты. Лимфоидные клетки диссоциируют путем измельчения в DMEM для высвобождения клеток из тканей и клетки суспендируют в DMEM. Клетки подсчитывают и прибавляют к клеточному осадку 0,9 мл DMEM на 100 миллионов лимфоцитов для осторожного, но полного ресуспендирования клеток. Клетки метят с помощью 100 мкл CD90+ магнитных бусин на 100 миллионов клеток, путем инкубации клеток с магнитными бусинами при 4°C в течение 15 минут. Суспензию магнитно меченых клеток, содержащую до 108 позитивных клеток (или до общего числа клеток 2×109) загружают на LS+ колонку и колонку промывают DMEM. Весь эффлюент собирают в качестве CD90-отрицательной фракции (ожидается, что большинство этих клеток будет B-клетками).
Слияние проводят путем смешения промытых обогащенных B-клеток, полученных выше, и несекреторных клеток миеломы P3X63Ag8.653, приобретенных у ATCC, № по каталогу CRL 1580 (Kearney et al, J. Immunol. 123, 1979, 1548-1550) в соотношении 1:1. Смесь клеток осторожно осаждают центрифугированием при 800×g. После полного удаления супернатанта клетки обрабатывают 2-4 мл раствора проназы (Pronase) (CalBiochem, № по каталогу 53702; 0,5 мг/мл в PBS (фосфатно-солевой буфер)) в течение не более 2 минут. Затем прибавляют 3-5 мл FBS (сыворотка плода коровы) для остановки активности фермента, и суспензию доводят до полного объема 40 мл с помощью раствора для электрослияния клеток (ECFS, 0,3M сахарозы, Sigma, № по каталогу S7903, 0,1 мМ ацетата магния, Sigma, № по каталогу M2545, 0,1 мМ ацетата кальция, Sigma, № по каталогу C4705). Супернатант удаляют после центрифугирования и клетки ресуспендируют в 40 мл ECFS. Эту стадию промывки повторяют и клетки снова ресуспендируют в ECFS до концентрации 2×106 клеток/мл.
Электрослияние клеток осуществляют с помощью генератора слияния (модель ECM2001, Genetronic, Inc., San Diego, CA). Размер используемой камеры слияния составляет 2,0 мл, при таких настройках прибора:
Состояние синхронизации (Alignment condition): напряжение: 50 В, время: 50 с;
Разрыв мембраны при: напряжение: 3000 В, время: 30 мкс;
Время выдерживания после слияния: 3 с.
После ECF, суспензии клеток осторожно извлекали из камеры слияния в стерильных условиях и переносили в стерильную пробирку, содержащую такой же объем культуральной среды для гибридом (DMEM, JRH Biosciences), 15% FBS (Hyclone), с добавкой L-глутамина, пенициллина/стрептомицина (pen/strep), OPI (оксалоацетат, пируват, бычий инсулин) (все - Sigma) и IL-6 (Boehringer Mannheim). Клетки инкубируют в течение 15-30 минут при 37°C и затем центрифугируют при 400×g (1000 об/мин) в течение пяти минут. Клетки осторожно ресуспендируют в небольшом объеме селективной среды для гибридом (культуральная среда для гибридом с добавкой 0,5× HA (Sigma, № по каталогу A9666)), и объем доводят до требуемого значения дополнительным количеством селективной среды для гибридом, чтобы обеспечить конечное высевание общего количества 5×106 B-клеток на 96-луночный планшет и 200 мкл на лунку. Клетки осторожно перемешивают и пипеткой переносят на 96-луночные планшеты и оставляют для выращивания. В день 7 или 10 половину среды удаляют и клетки подпитывают селективной средой для гибридом.
Гибридомы выращивают как обычно в селективной среде. Истощенные супернатанты, собранные из гибридом, подвергают различным анализам, как описано в Примерах 4-5. Отметим только, что антитела, обозначение которых начинается с цифры 3, например, 3.15G8, представляют собой IgG4, и антитела, обозначение которых начинается с цифры 2, например, 2.9D10, представляют собой IgG2.
ПРИМЕР 4: СВЯЗЫВАНИЕ С ЗАКРЕПЛЕННЫМ НА КЛЕТКАХ B7-H1 ЧЕЛОВЕКА И ЯВАНСКОГО МАКАКА
Супернатанты, собранные от клеток гибридомы, анализируют для оценки способности секретируемых антител связываться с 293T-клетками, транзиентно экспрессирующими полноразмерный B7-H1 человека или яванского макака. В качестве отрицательного контроля используют псевдотрансфицированную клеточную линию 293T. Клетки, разведенные в PBS, содержащем 2% FBS, высевают с плотностью 2500-3000 экспрессирующих и 15000-17500 псевдотрансфицированных клеток в 40 мкл/лунку на 384-луночные планшеты (Corning Costar, № по каталогу 3712). Немедленно после высевания прибавляют 10 мкл/лунку супернатантов гибридом и планшеты инкубируют в течение 1,5 ч при комнатной температуре. Затем прибавляют 10 мкл/лунку Cy5-конъюгированного козьего античеловеческого IgG Fc (700 нг/мл, Jackson Immunoresearch, № по каталогу 109-175-098) и планшеты инкубируют в течение 3 ч при комнатной температуре перед считыванием флуоресцентного сигнала с помощью прибора FMAT 8200 (Applied Biosystems). Результаты для 6 супернатантов гибридом приведены в Таблице 3.
Связывание супернатантов гибридом с закрепленным на клетках B7-H1 человека или яванского макака
яванского макака
ПРИМЕР 5: ИНГИБИРОВАНИЕ СВЯЗЫВАНИЯ РЕЦЕПТОР-ЛИГАНД
B7-H1/PD-1
Для определения относительной активности супернатантов, содержащих антитела, оценивают их способность ингибировать связывание человеческого белка PD-1/Fc с человеческим B7-H1, экспрессируемым на поверхности клеток CHO. Высевают 25000 клеток/лунку в 50 мкл среды в лунки 384-луночного планшета для тканевых культур (Corning Costar, № по каталогу 3712). На следующий день прибавляют 50 мкл/лунку разбавленного (1:5) супернатанта гибридомы и планшеты инкубируют при 4°C в течение 1 часа на встряхивателе. Прибавляют биотинилированный человеческий белок PD-1/Fc (R&D Systems, № по каталогу 1086-PD) до конечной концентрации 1,25 мкг/мл и планшеты инкубируют при 4°C в течение 1 часа на встряхивателе. Клетки промывают и фиксируют в 100 мкл PBS, содержащего 3,7% формальдегида и 3% бычьего сывороточного альбумина в течение 20 мин при комнатной температуре. Клетки промывают и инкубируют в 100 мкл PBS, содержащего 0,6% H2O2 и 3% бычьего сывороточного альбумина в течение 10 мин при комнатной температуре. Клетки промывают и инкубируют в 50 мкл конъюгированного с пероксидазой хрена стрептавидина, разбавленного в соотношении 1:4000 в течение 30 мин при 4°C. Клетки промывают до детектирования сигнала. Данные представлены как процентная доля (ODmax-ODmin), где ODmax представляет собой среднее значение, полученное для клеток, инкубируемых с иррелевантными супернатантами гибридом в присутствии конъюгированного с биотином человеческого белка PD-1/Fc, и ODmin представляет собой среднее значение, полученное для клеток, инкубируемых с иррелевантными супернатантами гибридом в отсутствие конъюгированного с биотином человеческого белка PD-1/Fc. 0% от максимального ответа указывает на 100% ингибирования связывания B7-H1/PD-1 супернатантом гибридомы (Таблица 4).
Ингибирование супернатантами гибридом связывания человеческого PD1 с клетками, экспрессирующими человеческий B7-H1
(% от максимума)
ПРИМЕР 6: СВЯЗЫВАНИЕ ОЧИЩЕННЫХ АНТИ-B7-H1 АНТИТЕЛ С ЧЕЛОВЕЧЕСКИМ B7-H1, ЧЕЛОВЕЧЕСКИМ B7-DC, МЫШИНЫМ B7-H1
Способность очищенных антител связываться с человеческими B7-H1, B7-DC, мышиным B7H1 и B7-H1 яванского макака определяют с помощью анализа методом FACS. Вкратце, клетки 293T псевдотрансфицируют или транзиентно трансфицируют с человеческим B7-H1 или человеческим B7-DC с использованием Lipofectamine 2000 (Invitrogen, № по каталогу 11668). Мышиные клетки J558, экспрессирующие мышиный B7-H1, были получены от ATCC (№ по каталогу TIB-6). Клетки ресуспендируют в PBS, содержащем 2% FBS (буфер для FACS), и высевают в количестве 50000 клеток/лунку в планшеты с V-образным дном. Прибавляют анти-B7-H1 антитела и антитела изотипического контроля, разбавленные буфером для FACS в конечной концентрации 5 мкг/мл, и планшеты инкубируют в течение 1 ч при 4°C. После промывания буфером для FACS, прибавляют козий античеловеческий Fc Cy5 (5 мкг/мл, Jackson Immunoresearch, № по каталогу 109-175-098) и 7-AAD (5 мкг/мл) и планшеты инкубируют в течение 15 мин при 4°C перед промыванием снова буфером для FACS и считыванием с помощью прибора FACSCalibur. Таблица 5 демонстрирует способность очищенных антител (5 мкг/мл) связываться с 293T-клетками, трансфицированными человеческим B7-H1. Ни одно из выбранных антител, связанных с 293T-клетками, не были трансфицированы с человеческим B7-DC или с клетками J558, экспрессирующими мышиный B7-H1. Мышиное античеловеческое антитело B7-DC (PD-L2) (R&D Systems, № по каталогу MAB1224, детектируемое козьим антимышиным Fc Cy5, Jackson Immunoresearch) используют в качестве положительного контроля экспрессии B7-DC. PE-конъюгированное крысиное антимышиное B7-H1 антитело (eBioscience, клон M1H5, детектируемое козьим антикрысиным Fc Cy5, Jackson Immunoresearch) используют в качестве положительного контроля экспрессии мышиного B7-H1.
Связывание очищенного анти-B7-H1 антитела с
закрепленными на клетках человеческим B7-H1, мышиным B7-H1 или
человеческим B7-DC
(h)B7-H1/293T
(геом. среднее)
(геом. среднее)
(геом. среднее)
(геом. среднее)
ПРИМЕР 7: СВЯЗЫВАНИЕ ОЧИЩЕННОГО ЧЕЛОВЕЧЕСКОГО АНТИ-B7-H1 АНТИТЕЛА СО СТИМУЛИРОВАННЫМИ T-КЛЕТКАМИ ЧЕЛОВЕКА И ЯВАНСКОГО МАКАКА
Инкубируют 96-луночные планшеты для сильного связывания (high binding) со 100 мкл/лунку анти-CD3 антитела, разбавленного до 1 мкг/мл в PBS (клон OKT3, eBioscience, № по каталогу 160037) при 4°C в течение ночи. Человеческие T-клетки выделяют из замороженной упаковки leukopack с использованием набора для обогащения T-клеток (StemCell Technologies, № по каталогу 19051). Планшеты, покрытые анти-CD3 mAb, промывают PBS и прибавляют очищенные T-клетки в 200 мкл среды ICM в количестве 360000 клеток/лунку и культивируют в течение 72 часов. T-клетки затем собирают, промывают в буфере для FACS и смешивают с разбавленными очищенными анти-B7-H1 антителами или иррелевантными человеческими IgG2 или IgG4 антителами в конечной концентрации 1 мкг/мл в 96-луночном планшете для анализов с V-образным дном (50 мкл/лунку). После 2 часов инкубации при 4°C, T-клетки промывают дважды в буфере для FACS и затем окрашивают Cy5-конъюгированным козьим античеловеческим IgG Fc антителом (5 мкг/мл, Jackson Immunoresearch, № по каталогу 109-175-098) и 7-AAD (10 мкг/мл). Клетки инкубируют в течение 30 мин при 4°C перед промыванием снова буфером для FACS и считыванием с помощью прибора FACSCalibur. Выбирают для анализа популяцию живых лимфоцитов на основании данных прямого и бокового рассеяния, а также отрицательного окрашивания 7-AAD.
Для активации T-клеток яванского макака инкубируют 96-луночные планшеты для сильного связывания со 100 мкл/лунку козьего антимышиного IgG Fc антитела, разбавленного до 1 мкг/мл в PBS при 4°C в течение ночи. Планшеты промывают PBS и инкубируют анти-CD3 антителом, разбавленным до 1 мкг/мл в среде ICM (клон SP-34, BD № по каталогу 556610) при 37°C в течение 2 часов. PBMC яванского макака выделяют из периферической крови (Bioreclamation, № по каталогу CYNWBCPT). Планшеты, покрытые анти-CD3 mAb, промывают PBS, и выделенные PBMC прибавляют в 200 мкл среды ICM в количестве около 200000 клеток/лунку и культивируют в течение 72 часов. Клетки затем собирают, промывают в буфере для FACS и смешивают с разбавленными очищенными анти-B7-H1 антителами или иррелевантными человеческими IgG2 или IgG4 антителами в конечной концентрации 1 мкг/мл в 96-луночном планшете для анализов с V-образным дном (50 мкл/лунку). После 2 часов инкубации при 4°C, клетки промывают дважды в буфере для FACS и затем окрашивают Cy5-конъюгированным козьим античеловеческим IgG Fc антителом (5 мкг/мл, Jackson Immunoresearch, № по каталогу 109-175-098), FITC-конъюгированным анти-CD3 антителом (разбавленным 1:25, Biospecialty) и 7-AAD (10 мкг/мл). Клетки инкубируют в течение 1 часа при 4°C перед промыванием снова буфером для FACS и считыванием с помощью прибора FACSCalibur. Выбирают для анализа популяцию обезьяньих T-лимфоцитов на основании данных прямого и бокового рассеяния, а также позитивного окрашивания CD3 маркером и негативного окрашивания 7-AAD. В Таблице 6 приведена способность очищенных анти-B7-H1 антител (1 мкг/мл) связываться с активированными человеческими T-клетками, а также с активированными T-клетками яванского макака.
Связывание очищенных анти-B7-H1 антител со стимулированными T-клетками человека или яванского макака
(геом. среднее)
(геом. среднее)
ПРИМЕР 8: ИНГИБИРОВАНИЕ СВЯЗЫВАНИЯ РЕЦЕПТОР-ЛИГАНД
B7-H1/PD-1
Оценивают способность очищенных человеческих анти-B7-H1 антител ингибировать связывание человеческого белка PD-1/Fc с человеческим B7-H1, экспрессируемым на поверхности клеток ES-2 (ATCC, № по каталогу CRL-1978). Вкратце, высевают 50000 клеток/лунку в 50 мкл PBS в лунки 384-луночного планшета для тканевых культур (Corning Costar, № по каталогу 3712). Затем прибавляют 50 мкл/лунку разбавленного моноклонального антитела в конечной концентрации 2,5, 0,5, 0,1, 0,02, 0,004, 0,008, 0,00016 нМ и планшеты инкубируют при 4°C в течение 1 часа. Клетки дважды промывают и прибавляют 100 мкл/лунку биотинилированного человеческого белка PD-1/Fc (10 мкг/мл, R&D Systems, № по каталогу 1086-PD) и планшеты инкубируют при 4°C в течение 1 часа. Клетки промывают один раз и прибавляют 100 мкл/лунку Cy5-конъюгированного стрептавидина и планшеты инкубируют при 4°C в течение 15 мин перед промыванием снова PBS, содержащим 2% FCS, и считыванием с помощью прибора FACSCalibur. Некоторые лунки инкубируют с иррелевантными человеческими IgG2 и IgG4 моноклональными антителами с или без биотин-конъюгированного человеческого PD-1/Fc для установления минимального (0%) и максимального (100%) уровней ингибирования связывания B7-H1/PD-1. Процентную долю ингибирования в зависимости от концентрации антитела анализируют с помощью средств аппроксимации кривых (прикладная программа GraphPad Prism) для расчета значений IC50 для каждого антитела, приведенных в Таблице 7.
Ингибирование связывания человеческого PD1 с клетками ES-2, экспрессирующими человеческий B7-H1, очищенными анти-B7-H1 антителами
ПРИМЕР 9: ОПРЕДЕЛЕНИЕ ЭФФЕКТОВ АНТИ-B7-H1 АНТИТЕЛ НА ПРОЛИФЕРАЦИЮ CD4 T-КЛЕТОК
Было продемонстрировано, что белок B7-H1, копрезентируемый с анти-CD3 антителом на бусинах, ингибирует CD3-медиируемую активацию T-клеток (Freeman et al., J. Exp. Med., 2000, 192 (7):1027-1034; Bennet et al., The Journal of Immunology, 2003, 170:711-718). Способность очищенного человеческого моноклонального анти-B7-H1 антитела препятствовать B7-H1-медиируемой супрессии активации T-клеток определяют следующим образом.
Вкратце, 5×108 бусин/мл промытых тозил-активированных Dynabeads M-450 (Invitrogen, № по каталогу 140,13) покрывают 50 мкг/мл мышиного античеловеческого CD3 антитела (BD Bioscience, № по каталогу 555329) в 0,1M натрийфосфатном буфере (pH 7,4-8,0) при 37°C в течение 24 часов при встряхивании. 4×108 CD3-покрытых бусин/мл затем связывают с рекомбинантным человеческим IgG1Fc (R&D Systems, № по каталогу 110-HG-100) в количестве 160 мкг/мл или с рекомбинантным человеческим белком B7-H1/Fc (R&D Systems, № по каталогу 156-B7-100) в количестве 80 мкг/мл в комбинации с человеческим белком IgG1Fc в количестве 80 мкг/мл (общая концентрация 160 мкг/мл) и инкубируют при 37°C в течение 24 часов при встряхивании. Бусины затем инкубируют в PBS, содержащем 0,05% бычьего сывороточного альбумина, при комнатной температуре в течение 1 часа, промывают четыре раза в 0,1% BSA и 2 мМ EDTA в PBS (pH 7,4) и, наконец, ресуспендируют в среде RPMI1640, содержащей 10% FBS, при концентрации 5×107 бусин/мл.
Моноциты периферической крови выделяют из упаковки для лейкафереза с помощью Ficoll-Paque Plus (GE Healthcare 17-1440-03) путем центрифугирования в градиенте плотности, ресуспендируют в бессывороточной RPMI 1640 (Gibco 22400-089), и CD4+ T-клетки выделяют из PBMC с помощью набора Dynal CD4 Negative Isolation Kit (Invitrogen, № по каталогу 113-37D) в соответствии с инструкциями производителя. Перемешивают 10 мкл покрытых бусин с 10 мкл разбавленного анти-B7-H1 или контрольного IgG2/4 антитела в лабораторной пробирке и инкубируют при комнатной температуре (RT) в течение 3-4 часов на встряхивателе. Очищенные CD4+ T-клетки высевают в количестве 105 клеток/80 мкл/лунку на 96-луночный планшет (Corning, № по каталогу 3603), и смесь бусины-антитело прибавляют в количестве 20 мкл/лунку до общего объема 100 мкл/лунку. Активацию T-клеток в отсутствие ингибирующего эффекта B7-H1 определяют с использованием бусин, покрытых анти-CD3 антителом и человеческим белком IgG1Fc. Клетки культивируют в течение 5 дней, и супернатанты собирают и анализируют на высвобождение IFN-γ с использованием набора BD Human IFN-γ ELISA Kit II (BD, № по каталогу 550612) в соответствии с инструкциями производителя. Пролиферацию клеток измеряют в день 5 путем прибавления 10 мкл/лунку реагента AlamarBlue (Invitrogen DAL 1025). Клетки инкубируют в течение 5 часов и флуоресценцию количественно измеряют спектрофотометром SpectraMax Gemini EM при длине волны возбуждения 545 нм и длине волны излучения 600 нм. Данные представлены как процентная доля ODmax, где ODmax представляет собой среднее значение, полученное для T-клеток, активированных анти-CD3/IgG1Fc бусинами. См. фигуру 1.
ПРИМЕР 10: ОПРЕДЕЛЕНИЕ ЭФФЕКТОВ АНТИ-B7-H1 АНТИТЕЛ НА АКТИВАЦИЮ CD4 T-КЛЕТОК С ПОМОЩЬЮ АНАЛИЗА ЛИМФОЦИТОВ В СМЕСИ ДЕНДРИТНЫХ КЛЕТОК-T-КЛЕТОК
Усиление активации T-клеток антителами, направленными против B7-H1, определяют с помощью анализа лимфоцитов в смеси дендритных клеток-T-клеток (DCMLR). Дендритные клетки получают из моноцитарных прекурсоров, как описано ранее (Curr Protoc Immunol. 2001 May; Chapter 7: Unit 7.32). Моноциты периферической крови выделяют из упаковки для лейкафереза с помощью Ficoll-Paque Plus (GE Healthcare 17-1440-03) центрифугирования в градиенте плотности, ресуспендируют в бессывороточной RPMI 1640 (Gibco 22400-089) и оставляют для прилипания к флаконам для клеточных культур T150 (Corning 430825). После 1 часа при 37°C неприлипшие T-клетки удаляют и клетки культивируют в RPMI с добавкой 5% человеческой сыворотки (Invitrogen 34005100). Прибавляют цитокины в конечной концентрации 2 нг/мл GM-CSF (BD Biosciences 550068) и 10 нг/мл IL-4 (BD Biosciences 554605). Свежую среду с цитокинами прибавляют каждые 2-3 дня. В день 6 культивации клетки были зрелыми с 20 нг/мл TNF-α (BD Biosciences 554618) и их оставляли для инкубации на 24 часа. Зрелые дендритные клетки собирают, фенотипируют и замораживают для последующего использования.
CD4+ T-клетки выделяют из PBMC с помощью набора для магнитного выделения (Dynal 113.17) в соответствии с инструкциями производителя и культивируют в первичном MLR, как описано ранее (J. Immunol. 2003 Apr 1; 170(7):3637-44). 1.5E5 аллогенные CD4+ отвечающие T-клетки культивируют на 96-луночных плоскодонных микротитровальных планшетах (Costar 3595) с дендритными клетками при соотношении T-клетки:дендритные клетки, равном 1:2,5. Препараты дендритных клеток обрабатывают 100 мкг/мл митомицина C (Sigma M4287) перед прибавлением к сокультуре для предотвращения возможной пролиферации загрязняющих лимфоцитов. Антитела прибавляют в различных концентрациях в конечном объеме 200 мкл RPMI + 10% человеческой сыворотки. Включение тимидина измеряют в день 5 путем 16-часовой импульсной обработки (pulse) [3H]-тимидином (1 мкКи/лунку, Perkin-Elmer NET027001MC). Супернатанты собирают перед введением радиоактивной метки и анализируют на высвобождение IFN-γ с помощью анализа Luminex (BioRad 171-B11921) в соответствии с инструкциями производителя. Усиление пролиферации T-клеток анти-B7-H1 антителами в повторных экспериментах показано на фигуре 2. Соответствующее высвобождение IFN-γ показано на фигуре 3.
ПРИМЕР 11: СТРУКТУРНЫЙ АНАЛИЗ B7-H1 АНТИТЕЛА
Были секвенированы последовательности вариабельного домена тяжелой цепи и последовательность вариабельного домена легкой цепи антител для определения их ДНК-последовательностей. Полная информация о последовательности анти-B7-H1 антител представлена в перечне последовательностей с указанием нуклеотидной и аминокислотной последовательностей для каждой комбинации гамма и каппа или лямбда цепей. Вариабельные тяжелые последовательности были проанализированы для определения семейства VH и последовательности J-области. Последовательности затем транслировали для определения первичной аминокислотной последовательности и сравнивали с последовательностями VH и J-области зародышевой линии для оценки соматических гипермутаций.
В Таблицах 8 и 9 сравниваются участки тяжелой цепи антитела с их когнатным участком тяжелой цепи зародышевой линии и участки легкой цепи антитела с их когнатным участком легкой цепи зародышевой линии. Приведена цифровая нумерация аминокислот.
Гены иммуноглобулина подвергаются различным модификациям во время созревания иммунного ответа, включая рекомбинацию между сегментами генов V, D и J, переключение изотипа и гипермутацию вариабельных участков. Рекомбинация и соматическая гипермутация являются основой возникновения многообразия антител и созревания аффинности, но они могут также вызывать подверженность последовательности влиянию внешних воздействий (liabilities), которая может затруднять промышленное производство таких иммуноглобулинов в качестве терапевтических агентов, или увеличить риск иммуногенности антитела. В общем, мутации в CDR-участках, вероятно, будут способствовать улучшению аффинности и функциональности, а мутации в каркасных участках могут увеличивать риск иммуногенности. Этот риск может быть уменьшен путем реверсирования каркасных мутаций к зародышевой линии при одновременном обеспечении отсутствия негативного влияния на активность антитела. Некоторые структурные компоненты подверженности могут быть созданы в процессе диверсификации, или они могут существовать в последовательностях зародышевой линии, влияя на вариабельные домены тяжелой и легкой цепей. Независимо от источника, может быть желательным устранить потенциальные структурные компоненты подверженности, которые могут приводить к нестабильности, агрегации, гетерогенности продукта или увеличению иммуногенности. Примеры нежелательных компонентов подверженности включают неспаренные цистеины (что может приводить к перестановкам дисульфидной связи или образованию вариабельного сульфгидрильного аддукта), N-связанные сайты гликозилирования (приводящие к гетерогенности структуры и активности), а также сайты деамидирования (например, NG, NS), изомеризации (DG), окисления (незащищенный метионин) и гидролиза (DP).
Для снижения риска иммуногенности и улучшения фармацевтических свойств исходного антитела, может быть желательно уменьшить число мутаций в зародышевой линии и/или удалить структурные компоненты подверженности.
Таким образом, в одном варианте воплощения, когда определенное антитело отличается от его соответствующей последовательности зародышевой линии на аминокислотном уровне, последовательность антитела может быть мутирована назад к последовательности зародышевой линии. Такие корректирующие мутации могут проводиться в одном, двух, трех или больше положений, или в комбинации любых мутированных позиций, с использованием стандартных методик молекулярной биологии. В Таблицах 10-14 ниже указаны позиции таких вариаций возврата к зародышевой линии для mAb 2.9D10, 2.7A4 и 2.14H9. Каждый ряд содержит уникальную комбинацию остатков, принадлежащих и не принадлежащих к зародышевой линии, в положении, выделенном жирным шрифтом. Приведена цифровая нумерация позиций аминокислот.
В другом варианте воплощения изобретение включает замену любых структурных компонентов подверженности в последовательности, которые могут повлиять на гетерогенность антител по изобретению. Такие компоненты подверженности включают сайты гликозилирования, неспаренные цистеины, незащищенные поверхностные метионины (methinones) и т.д. Для снижения риска таких гетерогенностей предлагается вносить изменения с целью удаления одного или нескольких таких структурных компонентов подверженности.
В одном варианте воплощения может быть желательным удаление одного или нескольких консенсусных N-связанных сайтов гликозилирования из зародышевой линии антитела или последовательности антитела. Квалифицированный специалист сможет легко идентифицировать такой сайт гликозилирования. Типично последовательность N-связанного консенсусного сайта гликозилирования имеет последовательность Asn-любая аминокислота (AA)-Ser или Thr, где средняя аминокислота не может быть пролином (Pro). В другом примере могут быть замещены неспаренные цистеины сами по себе или в сочетании с другими структурными изменениями. Неспаренный цистеин может быть мутирован на соответствующую аминокислоту, имеющую сопоставимые свойства боковой цепи, такую как серин.
В используемом здесь значении, оптимизированная последовательность представляет собой последовательность, которая была мутирована в одной или нескольких позициях назад до ее последовательности зародышевой линии, или может быть модифицирована для удаления одного или нескольких других компонентов подверженности, таких как структурные компоненты подверженности. Оптимизированная последовательность может также включать последовательность, которая была мутирована в одной или нескольких позициях назад до ее последовательности зародышевой линии, и которая также была дополнительно модифицирована для удаления одного или нескольких структурных компонентов подверженности.
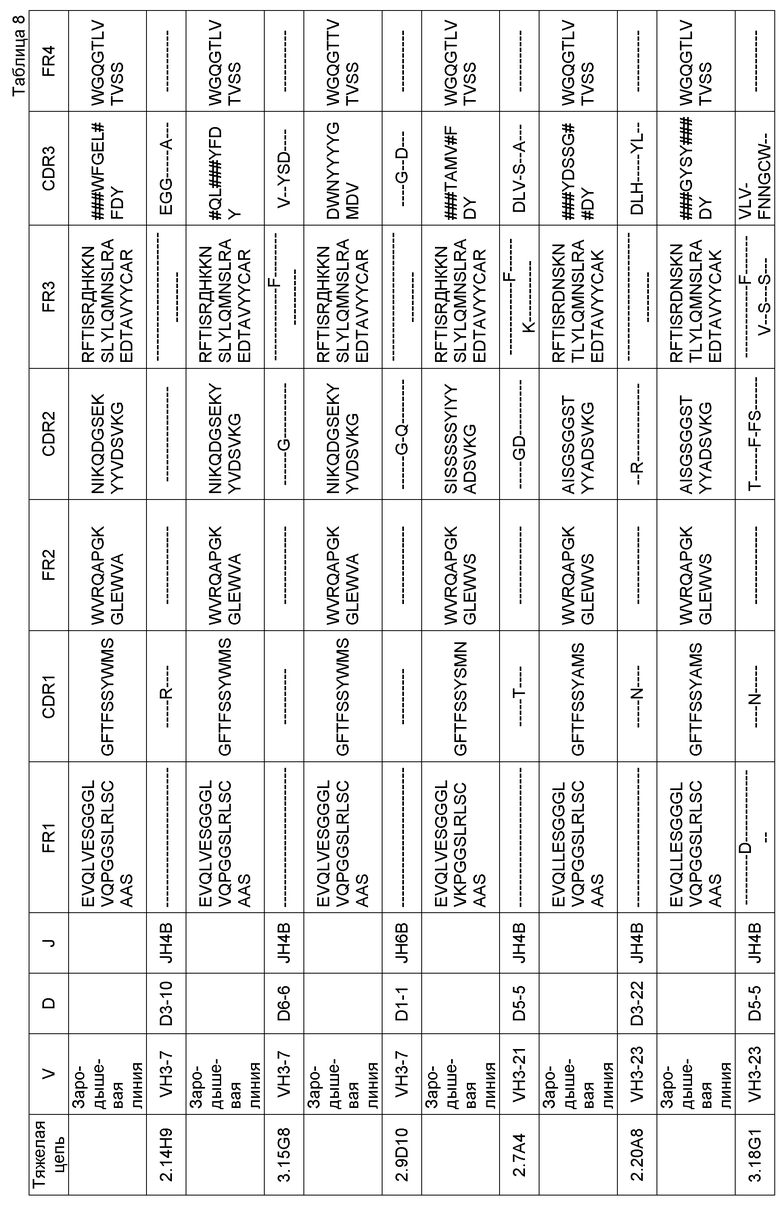
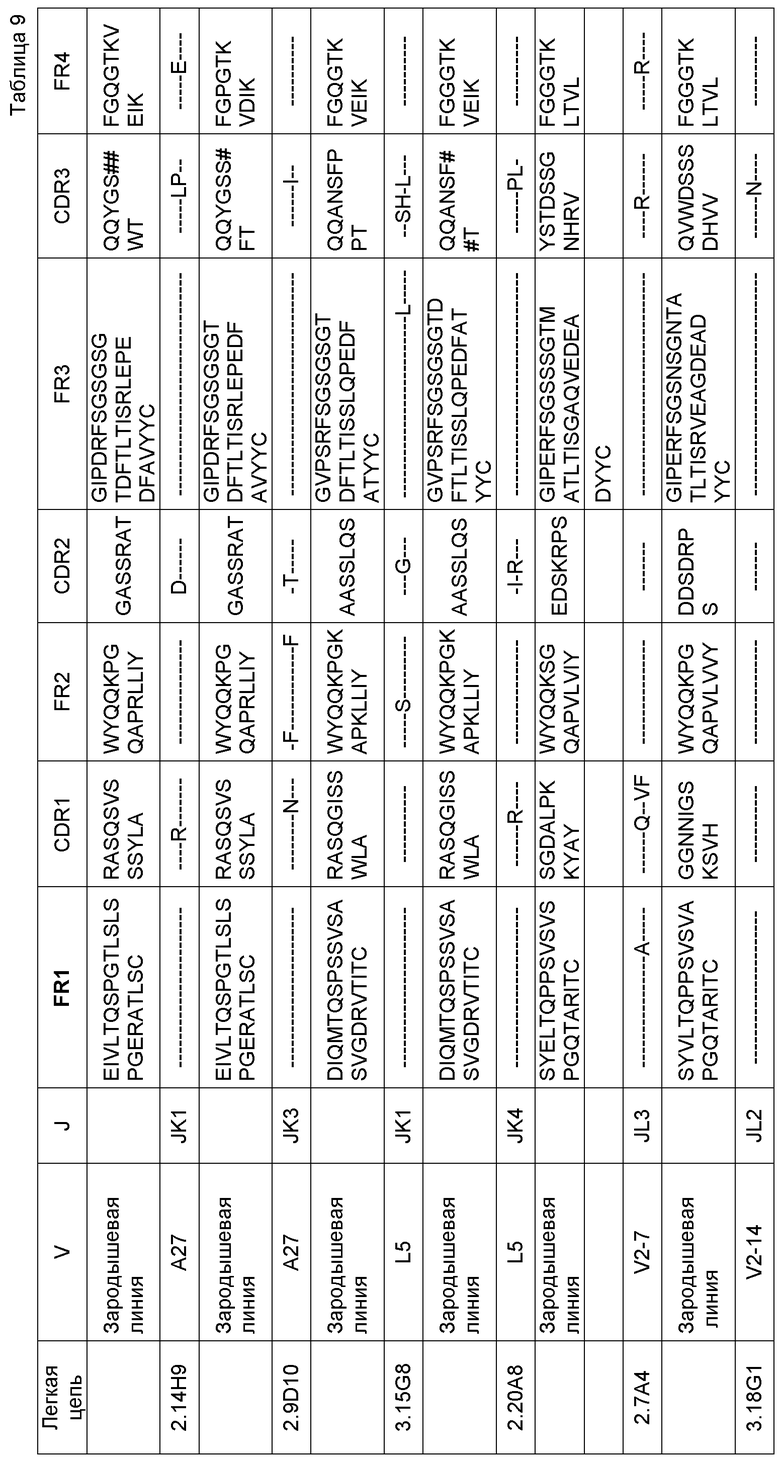
Типичные примеры мутаций тяжелой цепи 2.7A4 (SEQ ID NO:2) до зародышевой линии по указанным номерам остатков
В некоторых вариантах воплощения изобретения специфический связывающий агент или антитело включает последовательность, содержащую SEQ ID NO:2. В определенных вариантах воплощения SEQ ID NO:2 включает любую из комбинаций остатков, принадлежащих и не принадлежащих зародышевой линии, указанных в каждом ряду Таблицы 10. В некоторых вариантах воплощения SEQ ID NO:2 включает любой один, любые два, любые три, любые четыре, любые пять или все пять остатков зародышевой линии, указанных в Таблице 10. В определенных вариантах воплощения SEQ ID NO:2 включает любую из уникальных комбинаций остатков, принадлежащих и не принадлежащих зародышевой линии, указанных в каждом ряду Таблицы 10. В одном конкретном примере последовательность, не соответствующая зародышевой линии, мутирует назад до зародышевой линии в положении 80, где F заменяют на Y, и в положении 87, где K заменяют на R. Конкретным примером такой последовательности является 2.7A4VHOPT, приведенная в Таблице 15.
Типичные примеры мутаций легкой цепи 2.7A4 (SEQ ID NO:7) до зародышевой линии по указанным номерам остатков
В некоторых вариантах воплощения изобретения специфический связывающий агент или антитело включает последовательность, содержащую SEQ ID NO:7. В определенных вариантах воплощения SEQ ID NO:7 включает любую из комбинаций остатков, принадлежащих и не принадлежащих зародышевой линии, указанных в каждом ряду Таблицы 11. В некоторых вариантах воплощения SEQ ID NO:7 включает любой один, любые два, любые три, любые четыре, любые пять или все пять остатков зародышевой линии, указанных в Таблице 11. В определенных вариантах воплощения SEQ ID NO:7 включает любую из уникальных комбинаций остатков, принадлежащих и не принадлежащих зародышевой линии, указанных в каждом ряду Таблицы 11. Конкретные примеры вариабельного легкого домена 2.7A4, мутированного до конкретной последовательности зародышевой линии, включают 2.7A4 VLOPT (оптимизированный, в котором последовательность, не отвечающая зародышевой линии, была мутирована от A до T в положении 17 и от R до K в положении 104), приведенную в Таблице 15.
Типичные примеры мутаций тяжелой цепи 2.9D10 (SEQ ID NO:12) до зародышевой линии по указанным номерам остатков
В некоторых вариантах воплощения изобретения специфический связывающий агент или антитело включает последовательность, содержащую SEQ ID NO:12. В определенных вариантах воплощения SEQ ID NO:12 включает любую из комбинаций остатков, принадлежащих и не принадлежащих зародышевой линии, указанных в каждом ряду Таблицы 12. В некоторых вариантах воплощения SEQ ID NO:12 включает любой один, любые два или оба остатка зародышевой линии, указанные в Таблице 12. В определенных вариантах воплощения SEQ ID NO:12 включает любую из уникальных комбинаций остатков, принадлежащих и не принадлежащих зародышевой линии, указанных в каждом ряду Таблицы 12.
Типичные примеры мутаций легкой цепи 2.9D10 (SEQ ID NO:17) до зародышевой линии по указанным номерам остатков
В некоторых вариантах воплощения изобретения специфический связывающий агент или антитело включает последовательность, содержащую SEQ ID NO:17. В определенных вариантах воплощения, SEQ ID NO:17 включает любую из комбинаций остатков, принадлежащих и не принадлежащих зародышевой линии, указанных в каждом ряду Таблицы 13. В некоторых вариантах воплощения SEQ ID NO:17 включает любой один, любые два, любые три, любые четыре или все четыре остатка зародышевой линии, указанных в Таблице 7. В определенных вариантах воплощения SEQ ID NO:17 включает любую из уникальных комбинаций остатков, принадлежащих и не принадлежащих зародышевой линии, указанных в каждом ряду Таблицы 13. SEQ ID NO:17 может быть изменена или дополнительно изменена путем внесения не соответствующих зародышевой линии (nongermlining) изменений в SEQ ID NO:17. В одном примере SEQ ID NO:17 может быть изменена с заменой F на Y в положении 37 и F на Y в положении 50.
Типичные примеры мутаций легкой цепи 2.14H9 (SEQ ID NO:27) до зародышевой линии по указанным номерам остатков
В некоторых вариантах воплощения изобретения специфический связывающий агент или антитело включает последовательность, содержащую SEQ ID NO:27. В определенных вариантах воплощения SEQ ID NO:27 включает любую из комбинаций остатков, принадлежащих и не принадлежащих зародышевой линии, указанных в каждом ряду Таблицы 14. В некоторых вариантах воплощения SEQ ID NO:27 включает любой один, любые два, любые три или все три остатка зародышевой линии, указанных в Таблице 14. В определенных вариантах воплощения SEQ ID NO:27 включает любую из уникальных комбинаций остатков, принадлежащих и не принадлежащих зародышевой линии, указанных в каждом ряду Таблицы 14. Конкретные примеры вариабельного легкого домена 2.7A4, мутированного до конкретной последовательности зародышевой линии, включают 2.14H9OPT (оптимизированная, в которой не соответствующая зародышевой линии последовательность была мутирована с заменой E на K в положении 104), приведенную в Таблице 15.
Тяжелая цепь 2.14H9 может быть изменена в положении аминокислоты 31 SEQ ID NO:22 с заменой R на S.
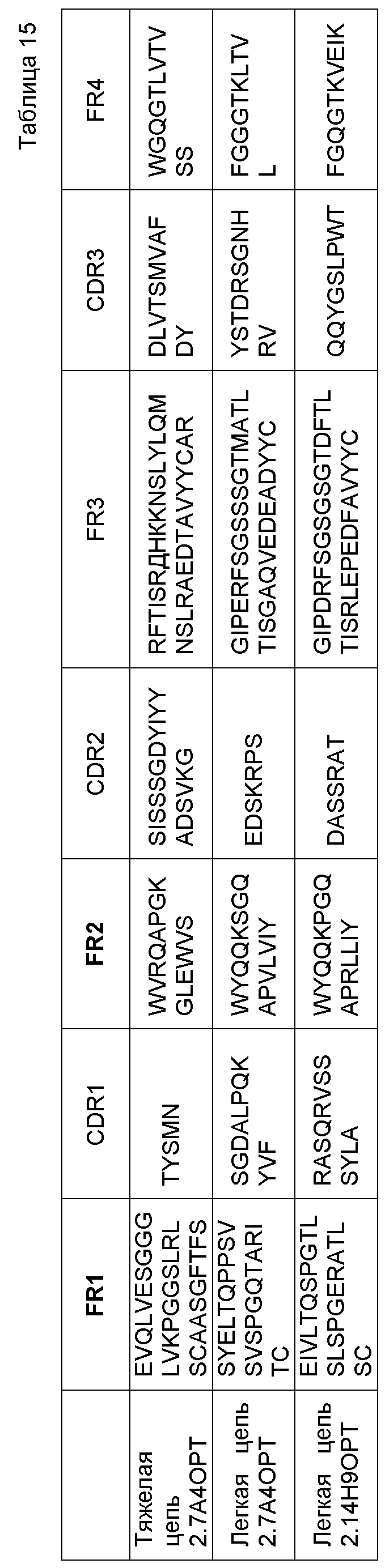
Конкретные примеры гуманизирования
Аминокислотные последовательности доменов VH и VL не соответствующих зародышевой линии (NG) анти-B7-H1 антител 2.7A4, 2.14H9 и 2.9D10 были подвергнуты выравниванию с известными последовательностями человеческой зародышевой линии в базе данных VBASE (Tomlinson, 1997; http://vbase.mrc-cpe.cam.ac.uk/), и ближайшая зародышевая линия была идентифицирована по сходству последовательностей. Ближайшие совпадения с зародышевой линией для анти-B7-H1 антител приведены в Таблицах 16 и 17. Требующие изменения позиции указаны в Таблице 18, без учета остатков Вернье (Vernier) (Foote & Winter, J Mol Biol. Mar20:224(2):487-99, 1992), которые оставались неизменными.
Ближайшие совпадения тяжелой цепи анти-B7-H1 с V и J
зародышевой линии
Ближайшие совпадения легкой цепи анти-B7-H1 с V и J
зародышевой линии
В случае антитела 2.7A4 имеем 2 изменения в каркасной части VH-домена и 2 изменения в каркасной части VL-домена. Эти остатки, расположенные в положениях с номерами по Кабат 79 и 83 (или остатки 80 и 87 при использовании цифровой нумерации) для VH-домена и номерами по Кабат 18 и 103 (или остатки 17 и 104 при использовании цифровой нумерации) для VL-домена, были реверсированы к человеческой зародышевой линии. См. Таблицу 18. В случае антитела 2.14H9 изменения отсутствуют в каркасной части VH-домена и имеется 1 изменение в каркасной части VL-домена. Этот остаток, расположенный в положении с номером по Кабат 103 в VL-домене (или 104 при определении остатка по цифровой нумерации), был реверсирован к человеческой зародышевой линии. См. Таблицу 18. В антителе 2.9D10 отсутствуют изменения в каркасной части VH-домена и имеются 2 изменения в VL домене, расположенные в положениях с номерами по Кабат 36 и 49 (или остатки 37 и 50 по цифровой нумерации). Однако эти 2 остатка расположены в положении Вернье (Vernier) и не подвергались мутированию, чтобы не менять строение CDR-петли.
Пример остатков, мутированных при гуманизации V-доменов анти-B7-H1. Остатки пронумерованы в соответствии с
номенклатурой Кабат
Гуманизирование этих аминокислотных остатков осуществляют с использованием стандартных методик сайт-направленного мутагенеза с пригодными мутагенными праймерами. Последовательности зародышевой линии имеют приставку «OPT» после названия антитела, например, 2.7A4VHOPT, 2.7VLOPT и 2.14H9VLOPT. Гуманизированные IgG затем повторно анализируют с помощью анализа ингибирования лиганда человеческого B7-H1/hPD1 для подтверждения того, что активность антитела in vitro не снизилась.
Примеры активностей гуманизированных анти-B7-H1 антител по сравнению с негуманизированными приведены на фигуре 4.
Пример синтеза гена и переформатирования на IgG1 и IgG1-TM
Клоны переводили из scFv в формат IgG путем субклонирования VH- и VL-доменов в векторы, экспрессирующие целые тяжелые и легкие цепи антитела, соответственно. VH-домены клонируют в вектор pEU15.1 для экспрессии IgG1 или в вектор pEU15.1-TM для экспрессии IgG1-TM антитела. Оба вектора содержат константные домены человеческой тяжелой цепи и регуляторные элементы для экспрессии цельной тяжелой цепи IgG в клетках млекопитающего. Вектор pEU15.1-TM представляет собой модифицированный вектор pEU15.1 человеческого IgG1. Он был сконструирован для введения трех мутаций; L234F и L235E в шарнирной области и P331S в CH2-домене молекулы IgG для устранения его способности инициировать антителозависимую клеточно-опосредованную цитотоксичность и комплементзависимую цитотоксичность (Oganesyan V. et al. (2008), Acta Cryst., D64: 700-704). Конструирование вектора проводилось с использованием стандартных методик сайт-направленного мутагенеза с пригодными мутагенными праймерами.
VL-домены клонируют в векторы pEU4.4 и pEU3.4 для экспрессии константных доменов человеческих легких цепей лямбда и каппа, соответственно, с регуляторными элементами для экспрессии цельной легкой цепи IgG в клетках млекопитающего. Векторы для экспрессии тяжелых цепей и легких цепей первоначально были описаны Vaughan et al. (Nature Biotechnology 14(3):309-314, 1996). Эти векторы были сконструированы путем простого введения элемента OriP.
Для получения IgG экспрессирующие векторы тяжелой и легкой цепей IgG трансфицируют в клетки млекопитающего EBNA-HEK293 (Invitrogen R620-07). IgG экспрессируются и секретируются в среду. Урожаи объединяют в пулы и центрифугируют перед очисткой. IgG очищают методом хроматографии с белком A с использованием системы очистки AKTA Express (GE Healthcare), предварительно дезинфицированной (sanitised) во избежание возможного загрязнения образца эндотоксинами. Супернатанты культуры загружают на колонки 1mL HiTrap™ MabSelectSure™ (GE Healthcare, 11-0034-93) и промывают 50 мМ Tris-HCl, pH 8,0, 250 мМ NaCl. Связанный IgG элюируют из колонки с помощью 0,1M цитрата натрия (pH 3,0) и нейтрализуют добавлением 1M Tris-HCl (pH 9,0). Заменяют буфер элюированного материала на PBS с помощью колонок Nap10 (Amersham, 17-0854-02) и фильтруют перед определением концентрации белка и уровней содержания эндотоксинов. Концентрацию IgG определяют спектрофотометрически, используя коэффициент экстинкции, определенный для аминокислотной последовательности IgG (Vaughan et al., выше). Уровень содержания эндотоксинов определяют с помощью портативной системы для проведения испытаний Endosafe PTS (Charles River Laboratories), оснащенной LAL-картриджами 1-0,1 EU (эндотоксиновых единиц)/мл и 10-0,1 EU/мл (Charles River Laboratories, PT520). Очищенный IgG анализируют на деградацию методом SDS-PAGE (электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия).
Анти-B7-H1 антитела в формате IgG1-TM оценивают и сравнивают с теми же антителами, но в формате IgG1, методом анализа ингибирования лиганда человеческого B7-H1/hPD1 для подтверждения того, что активность антитела in vitro не снизилась в результате переключения изотипа IgG (фигура 4).
ПРИМЕР 12: АНАЛИЗ СВЯЗЫВАНИЯ ЧЕЛОВЕЧЕСКИЙ B7H1/FC - ЧЕЛОВЕЧЕСКИЙ PD1/FC - HTRF®
Описанный метод анализа представляет собой анализ гомогенного TR-FRET (резонансный перенос энергии флуоресценции с временным разрешением) с использованием технологии анализа HTRF®, не требующей стадий промывки. В микротитровальный планшет Costar 3676 прибавляют 5 мкл/лунку биотинилированного PD1/Fc в концентрации 1 нМ, разбавленного PBS. После этого прибавляют 5 мкл/лунку стрептавидина XLent (CisBio) с концентрацией 4 нМ, разбавленного буфером для анализа (PBS+0,1% BSA+0,8M KF). Прибавляют в соответствующие лунки 5 мкл/лунку материала для титрования образца, разбавленного в PBS. Для определения общего связывания прибавляют 5 мкл PBS или соответствующего буфера образца на лунку. Для определения неспецифического связывания используют избыток (600 нМ) немеченого B7H1/Fc или PD1/Fc. Наконец, прибавляют 5 мкл/лунку меченого криптатом B7H1/Fc (криптатная метка - CisBio, B7H1/Fc - RnD Systems), разбавленного 1:100 буфером для анализа. Аналитический планшет оставляют на 3 часа при комнатной температуре, после чего считывают с помощью HTRF®-совместимого планшет-ридера.
Пример определения IC50 методом анализа ингибирования лиганда человеческий PD1/человеческий B7-H1 для анти-B7-H1 антител приведен в Таблице 19. Все античеловеческие B7-H1 антитела были в формате IgG1-TM.
Пример определения IC50 (n=2) по результатам анализа ингибирования лиганда человеческий PD1/человеческий B7-H1 для анти-B7-H1 IgG
ПРИМЕР 13: АНАЛИЗ СВЯЗЫВАНИЯ ЧЕЛОВЕЧЕСКИЙ B7H1/FC - ЧЕЛОВЕЧЕСКИЙ B7-1/FC - HTRF®
Описанный анализ представляет собой анализ гомогенного TR-FRET с использованием технологии анализа HTRF®, не требующей стадий промывки. В микротитровальный планшет Costar 3676 прибавляют 5 мкл/лунку биотинилированного B7-1/Fc с концентрацией 8 нМ, разбавленного PBS. После этого прибавляют 5 мкл/лунку стрептавидина XLent (CisBio) с концентрацией 20 нМ, разбавленного буфером для анализа (PBS+0,1% BSA+0,8M KF). Прибавляют в соответствующие лунки 5 мкл/лунку материала образца для титрования, разбавленного PBS. Для определения общего связывания прибавляют 5 мкл PBS или соответствующего буфера образца на лунку. Для определения неспецифического связывания используют избыток (200 нМ) немеченого B7H1/Fc или B7-1/Fc. Наконец, прибавляют 5 мкл/лунку меченного криптатом B7H1/Fc (криптатная метка - CisBio, B7H1/Fc - RnD Systems), разбавленного 1:100 буфером для анализа. Аналитический планшет оставляют на ночь при 4°C, после чего позволяют ему нагреться до комнатной температуры и считывают с помощью HTRF®-совместимого планшет-ридера.
Пример определения IC50 методом анализа ингибирования лиганда человеческий B7-1/человеческий B7-H1 для анти-B7-H1 антител приведен в Таблице 20. Все античеловеческие B7-H1 антитела имели формат IgG1-TM.
Пример определения IC50 (n=2) методом анализа ингибирования лиганда человеческий B7-1/человеческий B7-H1 для
анти-B7-H1 IgG
ПРИМЕР 14: ПЕРЕКРЕСТНАЯ РЕАКТИВНОСТЬ АНТИ-B7-H1 АНТИТЕЛ С ДРУГИМИ ИММУННЫМИ КОМОДУЛИРУЮЩИМИ БЕЛКАМИ
Проводят анализ методом ELISA для определения перекрестной реактивности анти-B7-H1 IgG1-TM антител по отношению к другим иммунным комодулирующим молекулам. Анализы методом ELISA заключаются в нанесении покрытий на планшеты MaxiSorp (NUNC) при 4°C в течение ночи 250 нг на лунку внеклеточного домена (ECD) человеческого B7-H1 (R&D Systems, 156-B7), человеческого PD-L2 (R&D Systems, 1224-PL), человеческого B7-H2 (R&D Systems, 165-B7), человеческого B7-H3 (R&D Systems, 1027-B3), человеческого CD28 (R&D Systems, 342-CD), человеческого CTLA-4 (R&D Systems, 325-CT) и человеческого PD1 (R&D Systems, 1086-PD) с последующим блокированием планшетов с помощью PBS, содержащего 3% сухого молока, при комнатной температуре в течение 1 ч. Также определяют перекрестную реактивность с мышами путем нанесения покрытия ECD мышиного B7-H1 (R&D Systems, 1019-B7). Биотинилированный анти-B7-H1 IgG1-TM, разбавленный до 100 нМ в PBS, содержащем 3% сухого молока, инкубируют при комнатной температуре в течение 2 ч для обеспечения связывания. Связанные биотинилированные IgG детектируют с помощью европий N1-меченного стрептавидина (Perkin Elmer, 1244-360) в концентрации 0,2 мкг/мл. Проводят контрольный эксперимент, демонстрирующий наличие покрытия антигена на планшете NUNC, с использованием коммерческих антител мышиного IgG2a античеловеческого B7-H1 (R&D Systems, MAB156), мышиного IgG2b античеловеческого PD-L2 (R&D Systems, MAB1224), мышиного IgG2b античеловеческого B7-H2 (R&D Systems, MAB165), мышиного IgG1 античеловеческого B7-H3 (R&D Systems, MAB1027), мышиного IgG1 античеловеческого CD28 (R&D Systems, MAB342), мышиного IgG2a античеловеческого CTLA-4 (Abcam, ab33320), мышиного IgG2b античеловеческого PD1 (R&D Systems, MAB1086) и крысиного IgG2a антимышиного B7-H1 (R&D Systems, MAB1019). Первичные антитела инкубируют при 5 мкг/мл в PBS, содержащем 3% сухого молока в течение 2 ч при комнатной температуре. Детектирование осуществляют путем инкубирования вторичного антитела пероксидазного конъюгата антимышиного IgG (Sigma, A2554) или пероксидазного конъюгата антикрысиного IgG (Sigma, A5795), разбавленного 1:5000 в PBS, содержащем 3% сухого молока, в течение 1 ч при комнатной температуре и последующего прибавления TMB (Sigma, T0440). Все восемь антигенов детектировались на планшете Maxisorp NUNC. Неспецифическое связывание определяют, используя лунки, покрытые изотипическим контролем IgG1 в концентрации 5 мкг/мл. Кросс-реактивности рассчитывают как процент специфического связывания с антигеном по сравнению с человеческим B7-H1.
Перекрестную реактивность 3 анти-B7-H1 IgG1-TM антител 2.7A4OPT, 2.9D10 и 2.14H9OPT к панели из восьми иммунных комодулирующих антигенов определяют с тремя параллельными измерениями. При концентрации антитела 100 нМ все три анти-B7-H1 антитела не проявляют перекрестной реактивности к любому из семи человеческих иммунных комодулирующих молекул, исследованных нами (фигура 5). IgG1-TM анти-B7-H1 антитело 2.7A4OPT демонстрирует измеримую перекрестную реактивность к мышиному B7-H1 со средним уровнем сигнала 5,3 по сравнению со 100% связывания с человеческим B7-H1. Другие два исследованные анти-B7-H1 антитела, 2,9D10 и 2,14H9OPT не проявляют какой-либо перекрестной реактивности к мышиному B7-H1 (фигура 5).
ПРИМЕР 15: АФФИННОСТЬ АНТИ-B7-H1 АНТИТЕЛ К B7-H1 ЧЕЛОВЕКА И ЯВАНСКОГО МАКАКА
Аффинность связывания и кинетические параметры анти-B7-H1 антител в формате IgG1-TM с мономерным B7-H1 человека и яванского макака определяют методом поверхностного плазмонного резонанса с использованием инструмента BIAcore T100 (BIAcore, Uppsala, Sweden). Вкратце, эксперименты проводят при 25°C с использованием буфера HBS-EP (10 мМ HEPES, 150 мМ NaCl, 3 мМ EDTA, 0,05% об./об. поверхностно-активного вещества P20) в качестве подвижного буфера. Связывают IgG за счет аффинности на поверхности сенсорного чипа CM5 (BIAcore) с помощью белка G, присоединенного через аминогруппу к поверхности CM5 для достижения плотности около 500 единиц ответа (Response Units, RU), в соответствии с инструкциями производителя (BIAapplications Handbook, BIAcore). В качестве аналитов используют рекомбинантные мономерные внеклеточные домены (ECD) B7-H1 FlagHis10 человека или японского макака. Разбавления B7-H1 ECD (200-3,12 нМ) в подвижном буфере вводят с постоянным объемным расходом 100 мкл/мин в течение 60 секунд. Во все измерения вносят поправку на базовую линию путем вычитания сенсограммы, полученной для контрольной (активируемой-дезактивируемой) проточной кюветы, а также устанавливают на ноль по двум холостым образцам (double referenced) (нулевая концентрация аналита). Данные анализируют с помощью программного пакета T-100 BIAevaluation и аппроксимируют по простой 1:1 ленгмюровской модели связывания с локальным Rmax и объемным показателем преломления, принятым равным 0. Данные обсчитывают по меньшей мере двум независимым экспериментам. Эффекты массопереноса ограничивают путем поддержания уровня аффинно-связанных IgG ниже 250 RU. Сенсограммы, полученные для всех исследованных антител, можно было легко аппроксимировать моноэкспоненциальной 1:1 моделью связывания, дающей прекрасное совпадение с величинами хи-квадрат (Chi2) устойчиво ≤0,3.
Аффинность анти-B7-H1 антител 2,7A4OPT и 2,14H9OPT к мономерному человеческому B7-H1 составляет 1 нМ и 175 пМ, соответственно (Таблица 21).
Анализ аффинности и кинетических параметров анти-B7-H1 антител при связывании с человеческим B7-H1
Аффинность анти-B7-H1 антител 2.7A4OPT и 2.14H9OPT к мономерному B7-H1 яванского макака составляет 835 пМ и 367 пМ, соответственно (Таблица 22). Эти два антитела проявляют сильную кросс-реактивность к B7-H1 яванского макака, поскольку аффинности очень близки к значениям для человеческого B7-H1.
Анализ аффинности и кинетических параметров анти-B7-H1 антител при связывании с B7-H1 яванского макака
ПРИМЕР 16: КАРТИРОВАНИЕ ЭПИТОПА АНТИ-B7-H1 АНТИТЕЛ
Картирование эпитопа проводят для идентификации остатков человеческого B7-H1, принимающих участие в связывании анти-B7-H1 антител. Структура внеклеточного домена человеческого B7H1 в комплексе с мышиным PD1 была ранее описана в литературе (Lin, D et al., 2008, Proc. Natl. Acad. Sci. USA, Vol. 105, p3011-3016) и показывает, что четырнадцать остатков B7-H1 принимают участие в связывании с PD1 (Таблица 23).
Человеческие B7-H1 остатки введены в связывание к мышиному PD1
Анти-B7-H1 антитела конкурируют за связывание человеческого B7-H1 с человеческим PD1 (Примеры 5, 8 и 12), так что они должны взаимодействовать с некоторыми из этих 14 остатков, если мы предположим, что существуют несущественные различия между поверхностями связывания B7H1 с человеческим и мышиным PD1 (62% идентичности аминокислотных последовательностей между последовательностями внеклеточного домена двух видов). Одноаминокислотные B7-H1 мутанты будут получены для всех 14 позиций, описанных в Таблице 23. Мутанты будут испытаны на связывание с анти-B7-H1 антителами методом фаговой ELISA и способность конкурировать за связывание анти-B7-H1 антител с человеческим B7-H1 методами HTRF® конкурентных анализов. Все описанные анти-B7-H1 антитела имеют формат IgG1-TM.
Клонирование гена внеклеточного домена человеческого B7-H1 при слиянии с геном III бактериофага для экспрессии методом фагового дисплея
Ген, кодирующий внеклеточный домен человеческого белка B7-H1 (Uniprot, номер доступа Q9NZQ7, аминокислоты [19-238]), был синтезирован на заказ фирмой DNA2.0 Inc. и амплифицирован методом ПЦР с использованием праймеров B7H1_FOR (5'-AATAATGGCCCAGCCGGCCATGGCCTTTACCGTGACGGTACCG-3') и B7H1_REV (5'-AATAATGCGGCCGCCCTTTCGTTTGGGGGATGC-3') для введения сайтов рестрикции Sfi I и Not I на 5'- и 3'-концах, соответственно. Продукт ПЦР затем направленно клонируют в вектор pCANTAB6 (McCafferty J. et al., 1994, Appl. Biochem. Biotechnol., Vol. 47, p157-173), используя сайты рестрикции Sfi I и Not I. Штамм TG1 E. coli трансформируют лигированием, и индивидуальные колонии подвергают скринингу путем секвенирования для идентификации трансформанта B7-H1, названного B7-H1_pCANTA6.
Получение и идентификация мутантов B7-H1
Мутанты B7-H1 были получены методом насыщающего мутагенеза всех 14 остатков поверхности раздела PD1 с использованием полностью рандомизированных NNS праймеров (Таблица 24) и плазмиды B7-H1_pCANTA6 в качестве ДНК-матрицы. Мутагенез проводят с использованием набора для мультисайт-направленного мутагенеза Stratagene's QuickChange (№ по каталогу 200513) в соответствии с инструкциями производителя. Мутагенные реакции используют для трансформации E. coli штамма TG1 и индивидуальные колонии подвергают скринингу путем секвенирования для идентификации вариантов B7-H1. Были идентифицированы в общей сложности 252 варианта из 280 возможных (20 аминокислот в 14 положениях) и избирательно перенесены на 3 96-луночных культуральных планшета.
Мутагенные праймеры, используемые для получения вариантов B7-H1
Фаговый ELISA мутантов B7-H1 для связывания с анти-B7-H1 антителами
Связывание мутантов B7-H1 с анти-B7-H1 антителами 2.14H9OPT, 2.7A4OPT или Эталонным антителом №1 оценивают методом фаговой ELISA после проверки того, что внеклеточный домен B7-H1 при слиянии с белком гена III может быть экспонирован на поверхности фага. Индивидуально отобранные культуры TG1 выращивают и суперинфицируют фагом-помощником M13K07 для получения фаговых частиц, экспонирующих мутанты B7-H1 на своей поверхности. Фаговые супернатанты блокируют в PBS+3% обезжиренного молока и инкубируют в планшетах NUNC MaxiSorb, предварительно покрытых в течение ночи 1 мкг/мл 2.14H9OPT, 2.7A4OPT или Эталонного антитела №1 в PBS и блокированных PBS+3% обезжиренного молока. Связанные фаги детектируют с использованием стрептавидина, сопряженного с европием (Perkin Elmer) после инкубации с биотинилированным анти-M13 вторичным антителом (Progen).
Из 14 остатков человеческого B7-H1, расположенных на поверхности раздела PD1, четыре не принимают участия в связывании с каким-либо из трех исследованных анти-B7-H1 антител (Asp26, Tyr56, Glu66 и Lys124). Их замещение на аланин или глицин существенно не влияет на сигнал связывания. На основании данных фагового ELISA, в общей сложности 28 мутантов, представляющих по 2-3 ключевых изменения для каждой из 10 других позиций, были выбраны для подтверждения их профиля связывания, но с использованием очищенных белков.
Биохимические конкурентные анализы
Внеклеточный домен человеческого B7-H1 дикого типа и мутантов экспрессируют в бактериях и очищают методом аффинной хроматографии, как описано ранее (Bannister D. et al., 2006, Biotechnology and bioengineering, 94, 931-937).
Конкурентные анализы HTRF® измеряют связывание анти-B7-H1 антитело с B7-H1, меченным HIS FLAG. Титрование немеченых образцов B7-H1, полученных, как описано выше, будет конкурировать с B7-H1, меченным HIS FLAG, за связывание с анти-B7-H1 антителом, приводя к ослаблению сигнала анализа. Антитела 2.14H9OPT, 2.7A4OPT и Эталонное антитело №1 используют для проведения конкурентных анализов для характеризации относительного связывания очищенных B7-H1 дикого типа или мутантов. Это позволит убедиться в том, какие именно остатки B7-H1 необходимы для связывания антитела. Прибавляют 10 мкл образца B7-H1 в 384-луночный аналитический планшет малого объема (Corning 3673). После этого прибавляют 5 мкл 0,29 нМ 2.14H9OPT или 1,15 нМ 2.7A4OPT или 1,15 нМ Эталонного антитела №1, конъюгированных с DyLight649 в соответствии с инструкциями производителя (ThermoFisher, 53051), и 5 мкл смешанного раствора 0,43 нМ анти-FLAG криптата (Cisbio International, 61FG2KLB) и 1,25 нМ меченного HIS FLAG человеческого B7-H1. Аналитические планшеты инкубируют в течение 4 часов при комнатной температуре перед считыванием разрешенной времени флуоресценции на длинах волн излучения 620 нм и 665 нм с помощью планшет-ридера EnVision (Perkin Elmer).
Три дополнительные остатка B7-H1 (Ile54, Ser117 и Ala121) не принимают участия в связывании с 2.14H9OPT и 2.7A4OPT, поскольку IC50 мутантов B7-H1 для этих остатков являются сходными или несущественно модифицированными по сравнению с B7-H1 дикого типа. Данные по конкуренции с 3 анти-B7-H1 антителами дикого типа и всех других мутантов B7-H1 приведены в Таблице 25.
IC50 (нМ) человеческого B7-H1, определенные путем конкурентного анализа связывания с анти-B7-H1 антителами
в нМ
антитело №1
Arg113 и Arg125 принимают активное участие в связывании с 2.14H9OPT. Замещение на Ala или другие аминокислоты (Tyr или Leu в положении 113 и Gln или Ser в положении 125) приводит к полной утрате связывания с этим антителом. Профиль связывания этих мутантов B7-H1 с 2.7A4OPT или Эталонным антителом №1 схож с B7-H1 дикого типа. Это показывает, что утрата связывания вызвана не общей структурной модификацией B7-H1, например, в виде нескладчатого белка, а прямым участием этих остатков в связывании 2.14H9OPT. Эти данные также демонстрируют, что эпитоп связывания 2.14H9OPT отличается от эпитопов 2.7A4OPT и Эталонного антитела №1. Met115, Asp122 и Tyr123 также принимают участие в связывании с 2.14H9OPT, но в меньшей степени. Замещение Met115 на Ala не влияет на связывание с 2.14H9OPT или 2.7A4OPT, но замещение на Asn приводит к полной утрате активности связывания с 2.14H9OPT, но не с 2.7A4OPT. Аналогично, замещение Asp122 на Asn влияет на связывание с 2.14H9OPT, но не с Эталонным антителом №1. Мутирование Tyr123 на Ala или Thr существенно модифицирует профиль связывания с 2.14H9OPT, но не с 2.7A4OPT. Интересно, что замещение на Phe не изменяет связывание с 2.14H9OPT, что позволяет предположить, что гидроксильная группа тирозина 123 не принимает участия в связывающем взаимодействии.
Phe19, Thr20 и Asp122 принимают сильное участие в связывании с 2.7A4OPT. Все мутанты B7-H1 в этих положениях не связываются с этим антителом, но связываются с 2.14H9OPT или Эталонным антителом №1 аналогично B7-H1 дикого типа, за исключением мутанта B7H1_D122E, который связывает эти 2 антитела с меньшей эффективностью. Эти три остатка являются специфическими по отношению к связывающему mAb (моноклональное антитело) эпитопу 2.7A4OPT и отсутствуют в эпитопах 2.14H9OPT или Эталонном антителе №1. Arg113 также участвует в эпитопе 2.7A4OPT, но в меньшей степени. Замещение на Ala не влияет на связывание с этим антителом, но мутации Tyr или Leu приводят к полной потере связывания. Эти мутации в положении 113 не влияют на связывание с Эталонным антителом №1, указывая на то, что мутанты B7-H1 все еще находятся в правильной конформации. Возможно, замещение на объемистую аминокислоту, такую как Tyr, может вносить определенные стерические затруднения. Эти результаты позволяют предположить, что Arg113 непосредственно не принимает участия в контакте с антителом 2.7A4OPT, но очень близок к фактическому связыванию эпитопа.
Этот пример демонстрирует, что три анти-B7-H1 антитела 2.14H9OPT, 2.7A4OPT и Эталонное антитело №1 обладают отличными связывающими эпитопами на поверхности раздела B7-H1 с PD1. Кроме того, возможно, что эти антитела могут также связываться с другими остатками человеческого B7-H1, но не расположенными на поверхности раздела с PD1.
ПРИМЕР 17. ОПРЕДЕЛЕНИЕ ЭФФЕКТОВ АНТИ-B7-H1 АНТИТЕЛ НА ОТВЕТ T-КЛЕТОК ПАМЯТИ НА СУБОПТИМАЛЬНЫЕ КОНЦЕНТРАЦИИ «ВОСКРЕСШЕГО» АНТИГЕНА
Было продемонстрировано, что взаимодействие B7-H1 с PD-1 ингибирует антигенспецифический T-клеточный ответ. Для оценки эффекта анти-B7-H1 антител на такое ингибирование были проведены анализы c субоптимальными количествами сенсибилизирующего антигена.
Моноциты периферической крови (PBMC) выделяют из лейкоцитных пленок человеческой крови, используя Ficoll-Paque Plus (GE Healthcare 17-1440-03) центрифугирование в градиенте плотности в соответствии с инструкциями производителя. После выделения клетки ресуспендируют в среде RPMI 1640 Glutamax I (GIBCO, 61870) с добавкой 1% пенициллина/стрептомицина (pen/strep) (GIBCO, 15140) и 4% человеческой сыворотки AB (Invitrogen 34005), и затем культивируют в 96-луночных круглодонных планшетах для тканевых культур (Corning, 3799) при 37°C, 5% CO2, в присутствии 0,1 мкг/мл столбнячного анатоксина или без него (Calbiochem 582231) при плотности 1×105 клеток на лунку. Через три дня культивации прибавляют анти-B7-H1 антитела в формате IgG1-TM или изотипический контроль в указанных концентрациях и культуры возвращают в условия 37°C еще на 2 дня, после чего супернатанты собирают и анализируют с помощью DELFIA на уровни интерферона-γ. Усиление высвобождения интерферона-γ анти-B7-H1 антителами показано на фигуре 6.
Анти-B7-H1 антитела 2.9D10, 2.7A4OPT и 2.14H9OPT были способны усиливать высвобождение интерферона-γ. Эти данные подтверждают способность 2.9D10, 2.7A4OPT и 2.14H9OPT усиливать антигенспецифические T-клеточные ответы.
ПРИМЕР 18. ОПРЕДЕЛЕНИЕ ЭФФЕКТОВ АНТИ-B7-H1 АНТИТЕЛ НА ОТВЕТ T-КЛЕТОК ПАМЯТИ НА ОПТИМАЛЬНЫЕ КОНЦЕНТРАЦИИ «ВОСКРЕСШЕГО» АНТИГЕНА
Было предположено, что B7-H1 обладает потенциальной ингибирующей сигнальной способностью. Потенциал анти-B7-H1 антител выступать в качестве агониста, способного осуществлять такую ингибирующую сигнализацию, проверяли путем исследования их способности ингибировать ответ на сенсибилизирующий антиген.
Моноциты периферической крови (PBMC) выделяют из лейкоцитных пленок человеческой крови, используя Ficoll-Paque Plus (GE Healthcare 17-1440-03) центрифугирование в градиенте плотности в соответствии с инструкциями производителя. После выделения клетки ресуспендируют в среде RPMI 1640 Glutamax I (GIBCO, 61870) с добавкой 1% пенициллина/стрептомицина (pen/strep) (GIBCO, 15140) и 4% человеческой сыворотки AB (Invitrogen 34005), и затем культивируют при плотности 1×105 клеток на лунку в 96-луночных круглодонных планшетах для тканевых культур (Corning, 3799) при 37°C, 5% CO2, с 5 мкг/мл столбнячного анатоксина (Calbiochem 582231) и в присутствии различных концентраций анти-B7-H1 антител в формате IgG1-TM или изотипического контроля или без них. Антитело против корецептора T-клеток было использовано в качестве положительного контроля. После 5 дней культивации клетки обрабатывают 0,5 мкКи/лунку меченного тритием тимидина в течение приблизительно 16 часов для оценки пролиферативной активности.
Ингибирующие эффекты не наблюдались для 2.9D10, 2.7A4 и 2.14H9 анти-B7-H1 антител в отличие от положительного контроля, как показано на фигуре 7. Это позволяет предположить, что антитела 2.9D10, 2.7A4 и 2.14H9 являются чистыми антагонистами, без какой-либо агонистической активности.
ПРИМЕР 19. АКТИВНОСТЬ ИНГИБИРОВАНИЯ РОСТА ОПУХОЛИ АНТИ-B7-H1 АНТИТЕЛ
Была исследована in vivo активность античеловеческих B7-H1 антител на мышиных моделях ксенотрансплантатов с использованием мышей NOD/SCID (диабет без ожирения/тяжелый комбинированный иммунодефицит) с ослабленным иммунитетом. Мышам вводили подкожно (SC) человеческие раковые клеточные линии, экспрессирующие человеческий B7-H1, и человеческие CD4+ и CD8+ T-клетки, выделенные из мононуклеарных клеток периферической крови здоровых доноров и культивировавшиеся для обогащения аллореактивных эффекторных T-клеток. Интраперитонеально (IP) вводили мышам, инокулированным клеточной линией человеческого рака поджелудочной железы (HPAC) или клеточной линией человеческой меланомы A375, дозы античеловеческих B7-H1 антител. Наблюдали эффект антител на рост опухоли до объема опухоли 2000 мм3 или выраженного некроза опухоли.
Для получения CD4+ и CD8+ T-клеточных линий человеческие PBMC от здоровых доноров обогащают CD4+ или CD8+ T-клетками путем прибавления 1 мл продукта для обогащения T-клеток RosetteSep на 20 мл цельной крови. После этого проводят 20-минутную инкубацию с последующим выделением центрифугированием в градиенте плотности с использованием среды RosetteSep DM-L density. После центрифугирования клетки промывают PBS и ресуспендируют в среде RPMI 1640 с добавкой 10% FBS. Обогащенные CD4+ и CD8+ T-клетки культивируют отдельно в течение 7-10 дней в среде с добавкой rhIL-2 и объединяют каждые с обработанными митомиозином C клетками A375 или HPAC. T-клетки собирают и отдельно культивируют снова в течение 7-10 дней в среде с добавкой rhIL-2 и объединяют с обработанными митомиозином C клетками A375 или HPAC. CD4+ и CD8+ T-клетки собирают и объединяют в соотношении 1:1.
Клеточные линии рака A375 и HPAC и PBMC, обогащенные CD4+ и CD8+ T-клетками, перемешивают непосредственно перед подкожным (SC) введением в указанных соотношениях эффектор-мишень (E:T). Число используемых для инокуляции клеток предварительно определяют для каждой раковой клеточной линии с помощью эмпирических исследований дозы, необходимой для образования опухоли; в общем, каждому животному прививают 2,5×106 клеток в общем объеме 0,2 мл.
Включают по шесть животных в каждую экспериментальную группу. Животные получают изотипический контроль человеческого IgG2a или IgG1OPT (также названного здесь «IgG1TM») антитела или анти-B7-H1 антитела 2.14H9 IgG2a, 2.14H9OPT, 2.7A4OPT или Эталонного антитела №1 в формате IgG1OPT. Проводят в общем восемь независимых экспериментов, и планы для каждого эксперимента приведены в Таблицах 26-33. Описанные анти-B7-H1 антитела имеют формат IgG1OPT, за исключением указанных случаев.
Первую дозу (200 мкл) исследуемого препарата вводят интраперитонеально (IP) через 1 час после пересадки раковых/эффекторных T-клеток; животные получают до 4 дополнительных доз исследуемого препарата в дни исследования 3, 5, 8 и/или 10. В качестве положительного контроля для усиления аллореактивности в некоторых исследованиях вводят интраперитонеально (IP) rhIL-2 через 1 час после пересадки раковых/эффекторных T-клеток; животные получают 4 дополнительные ежедневные дозы rhIL-2 на протяжении 4 последовательных дней. Образование опухоли наблюдают у каждого животного один или два раза в неделю. Опухоли измеряют штангенциркулем; объемы опухолей (V) рассчитывают по следующей формуле:
V (мм3)=0,5 (длина (мм)×ширина (мм)×ширина (мм)/2).
Для каждой группы результаты приводятся как среднее арифметическое. Противораковый эффект, выраженный как процент ингибирования роста опухоли (TGI), рассчитывают таким образом:
% TGI = [1-(средний V опухоли в группе лечения)÷(средний V опухоли в контрольной группе)]×100.
В эксперименте 1 анти-B7-H1 антитела 2.14H9 IgG2a и 2.7A4OPT значительно ингибируют рост раковых клеток HPAC (поджелудочной железы) в день 30 - до 61% и 50%, соответственно, по сравнению с группой изотипического контроля (фигура 8 и Таблица 26).
Эксперимент 1 - Группы воздействия и процент ингибирования роста опухоли у мышей с пересаженными раковыми клетками HPAC после внутривенного введения анти-B7-H1 антител
в день 30
В эксперименте 2 анти-B7-H1 антитела 2.14H9OPT и 2.7A4OPT ингибируют рост раковых клеток HPAC (поджелудочной железы) в день 39 до 70% и 68%, соответственно, по сравнению с группой изотипического контроля (фигура 9 и Таблица 27).
Эксперимент 2 - Группы воздействия и процент ингибирования роста опухоли у мышей с пересаженными раковыми клетками HPAC после внутривенного введения анти-B7-H1 антител
в день 39
В эксперименте 3 анти-B7-H1 антитело 2.14H9OPT значительно ингибирует рост раковых клеток HPAC (поджелудочной железы) в день 30 - до 60% по сравнению с группой изотипического контроля (фигура 10 и Таблица 28).
Эксперимент 3 - Группы воздействия и процент ингибирования роста опухоли у мышей с пересаженными раковыми клетками HPAC после внутривенного введения анти-B7-H1 антител
в день 30
В эксперименте 4 анти-B7-H1 антитело 2.14H9OPT значительно ингибирует рост раковых клеток HPAC (поджелудочной железы) в день 22 - до 74% по сравнению с группой изотипического контроля (фигура 11 и Таблица 29).
Эксперимент 4 - Группы воздействия и процент ингибирования роста опухоли у мышей с пересаженными раковыми клетками HPAC после внутривенного введения анти-B7-H1 антител
В эксперименте 5 интраперитонеальное (IP) введение 2.14H9 IgG2a или 2.7OPT анти-B7-H1 антител в модели ксенотрансплантата A375 (меланома) также значительно ингибируют рост опухоли в день 29 - до 64% и 61%, соответственно, по сравнению с группой изотипического контроля (фигура 12 и Таблица 30).
Эксперимент 5. Группы воздействия и процент ингибирования роста опухоли у мышей с пересаженными раковыми клетками A375 после внутривенного введения анти-B7-H1 антител
(мг/кг/мышь)
в день 29
В эксперименте 6 анти-B7-H1 антитело 2.14H9OPT значительно ингибирует рост раковых клеток A375 (меланома) в комбинации с T-клетками в день 25 - до 77% по сравнению с группой изотипического контроля (фигура 13 и Таблица 31).
Эксперимент 6. Группы воздействия и процент ингибирования роста опухоли у мышей с пересаженными раковыми клетками A375 после внутривенного введения анти-B7-H1 антител
в день 25
В эксперименте 7 анти-B7-H1 антитело 2.14H9OPT значительно ингибирует рост раковых клеток A375 (меланома) в комбинации с T-клетками в день 25 - до 82% по сравнению с группой изотипического контроля (фигура 14 и Таблица 32).
Эксперимент 7. Группы воздействия и процент ингибирования роста опухоли у мышей с пересаженными раковыми клетками A375 после внутривенного введения анти-B7-H1 антител
(мг/кг/мышь)
T-клеток
В эксперименте 8 анти-B7-H1 антитело 2.14H9OPT значительно ингибирует рост раковых клеток A375 (меланома) в комбинации с T-клетками в день 25 - до 93% по сравнению с группой изотипического контроля (фигура 15 и Таблица 33).
Эксперимент 8. Группы воздействия и процент ингибирования роста опухоли у мышей с пересаженными раковыми клетками A375 после внутривенного введения анти-B7-H1 антител
Эти результаты демонстрируют, что античеловеческие B7-H1 антитела 2.14H9 IgG2a, 2.14H9OPT и 2.7A4OPT обладают сильной in vivo противораковой активностью в мышиных моделях ксенотрансплантатов человеческих раков и свидетельствуют, что такие античеловеческие B7-H1 антитела могут проявлять активность в качестве лекарственной монотерапии при лечении пациентов с раками, экспрессирующими B7-H1.
ВКЛЮЧЕНИЕ В КАЧЕСТВЕ ССЫЛОК
Все упоминаемые здесь источники, включая патенты, патентные заявки, статьи, пособия и т.п., и приведенные в них ссылки, настоящим целиком включаются сюда в качестве ссылок в той степени, в которой они не были уже включены ранее. Временная патентная заявка США № 61/264061, поданная 24 ноября 2009 года, приведенные в ней фигуры и последовательности настоящим целиком включены сюда в качестве ссылок.
ЭКВИВАЛЕНТЫ
Приведенное выше письменное описание считается достаточным для того, чтобы позволить квалифицированным специалистам практиковать изобретение. Приведенное выше описание и примеры детализируют определенные предпочтительные варианты воплощения изобретения и описывают наилучшие решения, предусматриваемые авторами изобретения. Следует понимать, однако, что независимо от обстоятельности вышеприведенного текста, данное изобретение может практиковаться многими способами и должно истолковываться в соответствии с приложенной формулой изобретения и любыми ее эквивалентами.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ АГЕНТЫ ПРОТИВ В7-Н1 | 2010 |
|
RU2706200C2 |
| АНТИТЕЛА ПРОТИВ 5-БРОМ-2'-ДЕЗОКСИУРИДИНА И СПОСОБЫ ПРИМЕНЕНИЯ | 2015 |
|
RU2705299C2 |
| АНТИ-PD-1 АНТИТЕЛА | 2017 |
|
RU2752832C2 |
| АНТИТЕЛА К NKG2A И ИХ ПРИМЕНЕНИЯ | 2007 |
|
RU2499001C2 |
| АНТИТЕЛА К ТЕОФИЛЛИНУ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2013 |
|
RU2630664C2 |
| ОДНОВАЛЕНТНЫЕ МОДУЛИ-ПЕРЕНОСЧИКИ ЧЕРЕЗ ГЕМАТОЭНЦЕФАЛИЧЕСКИЙ БАРЬЕР | 2014 |
|
RU2694659C2 |
| АНТИТЕЛО ПРОТИВ IGF-1R И ЕГО ПРИМЕНЕНИЕ В КАЧЕСТВЕ АДРЕСУЮЩЕГО ПЕРЕНОСЧИКА ДЛЯ ЛЕЧЕНИЯ РАКА | 2015 |
|
RU2698977C2 |
| ОДНОВАЛЕНТНЫЕ МОДУЛИ-ПЕРЕНОСЧИКИ ЧЕРЕЗ ГЕМАТОЭНЦЕФАЛИТИЧЕСКИЙ БАРЬЕР | 2014 |
|
RU2799436C1 |
| АНТИИДИОТИПИЧЕСКИЕ АНТИТЕЛА И СВЯЗАННЫЕ С НИМИ СПОСОБЫ | 2017 |
|
RU2773355C2 |
| АНТИТЕЛА К HER3 И ИХ ПРИМЕНЕНИЯ | 2010 |
|
RU2560583C2 |

























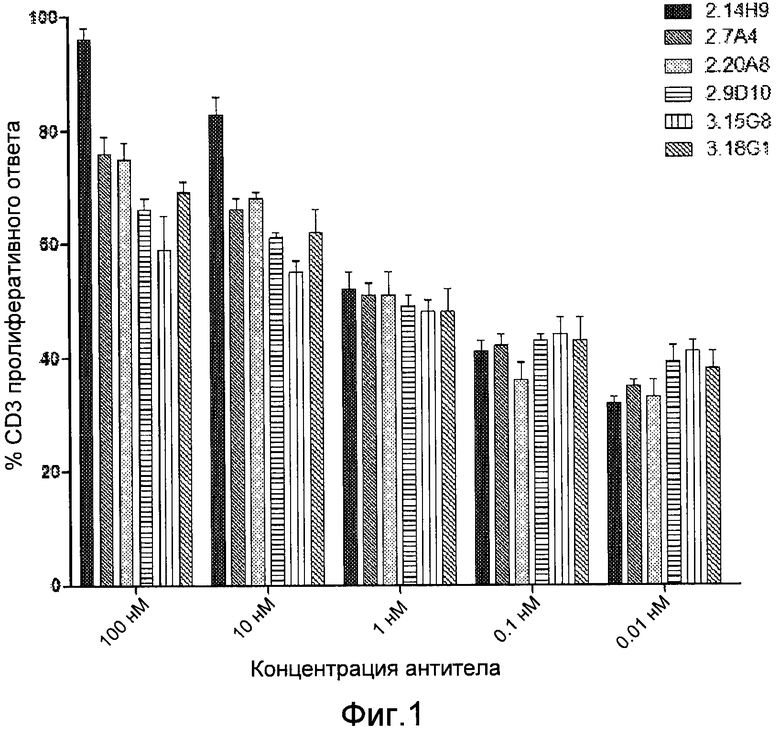
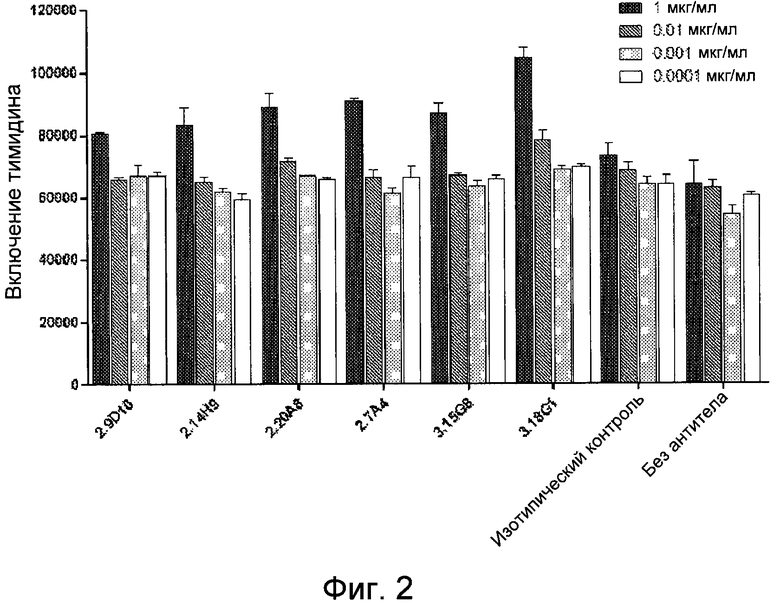
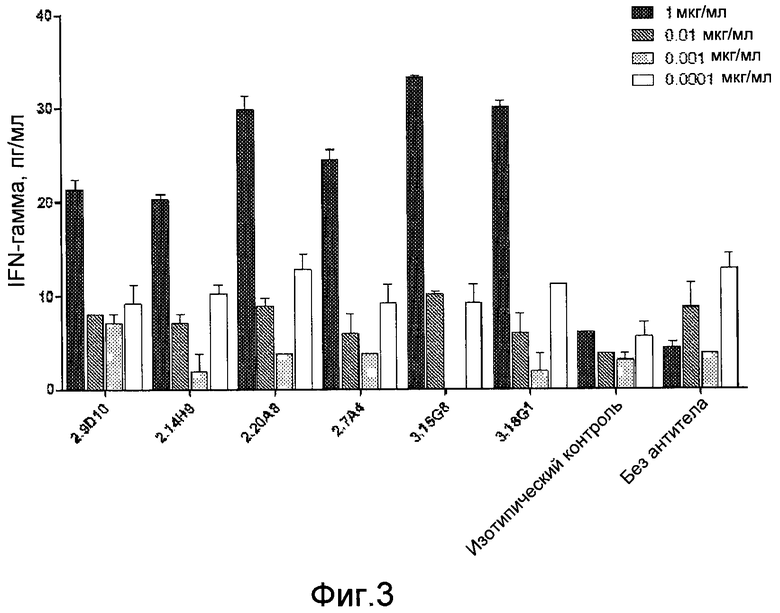
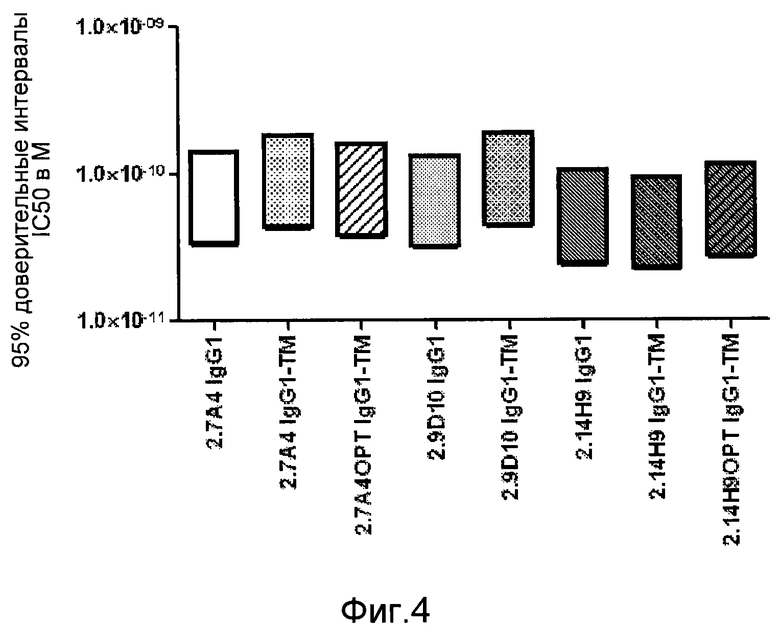
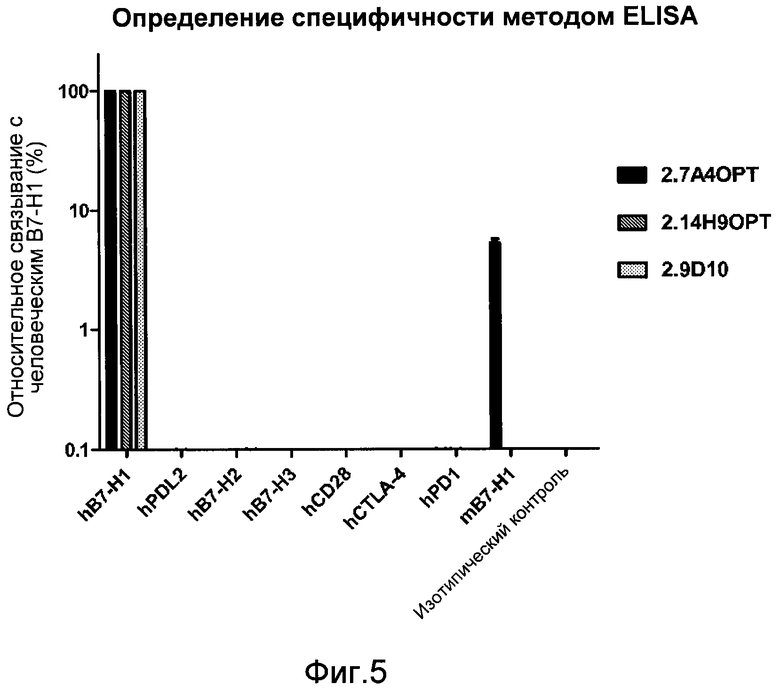
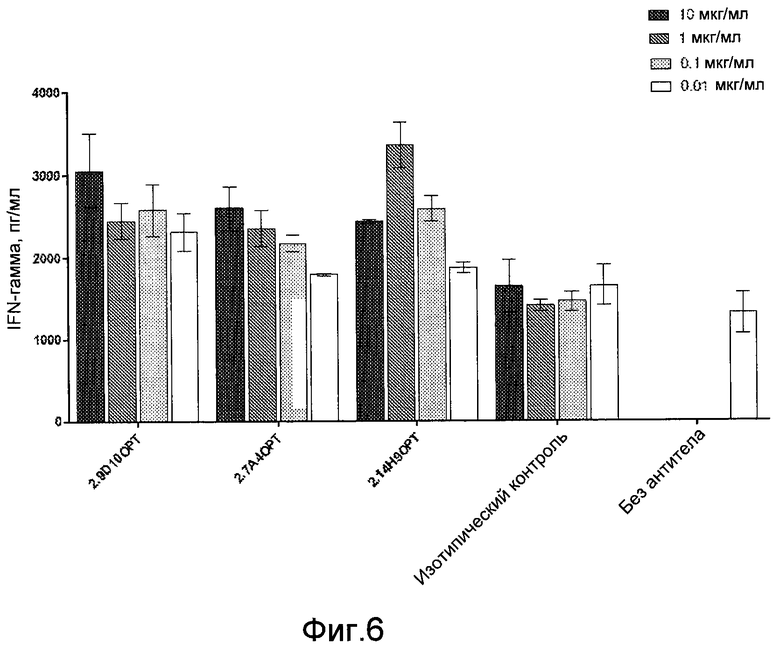
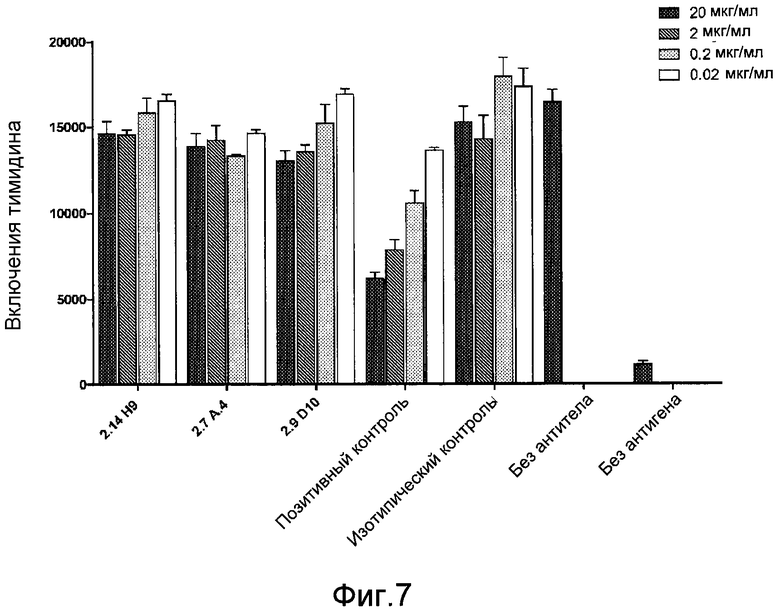
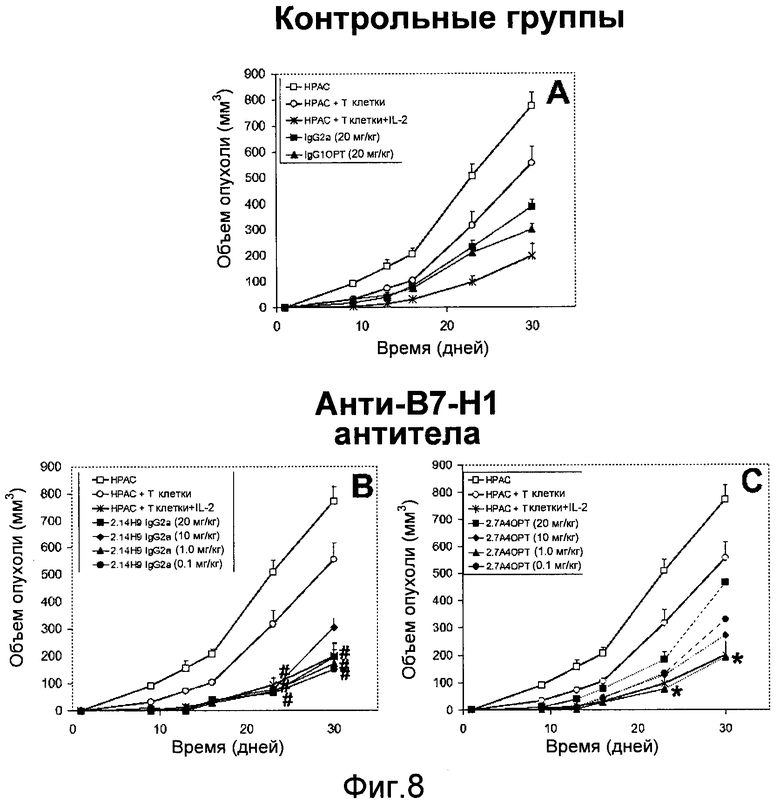
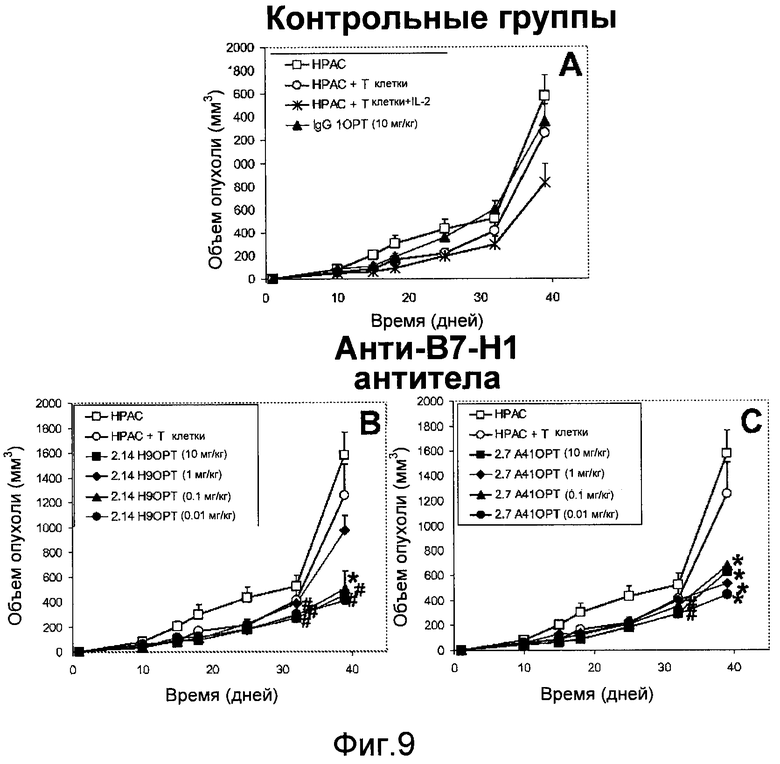
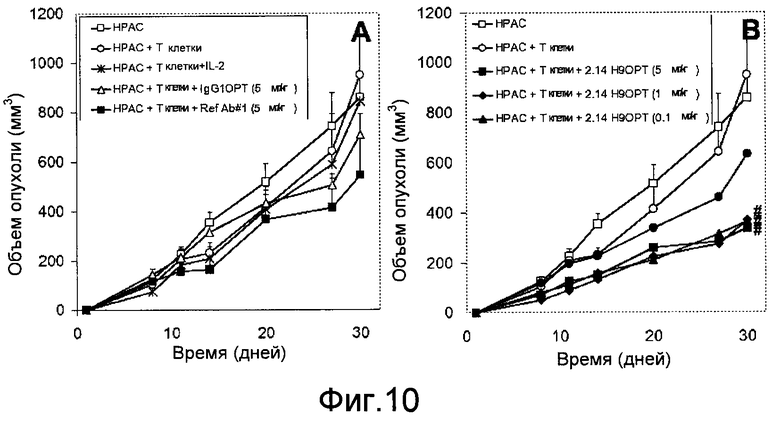

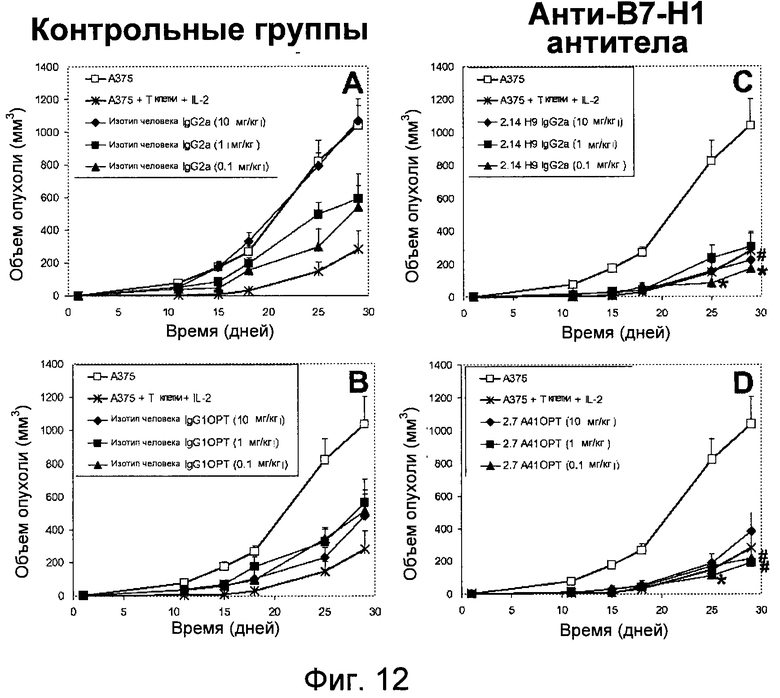
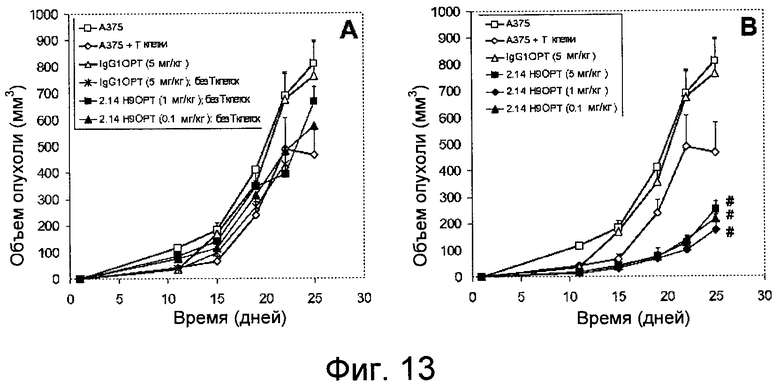
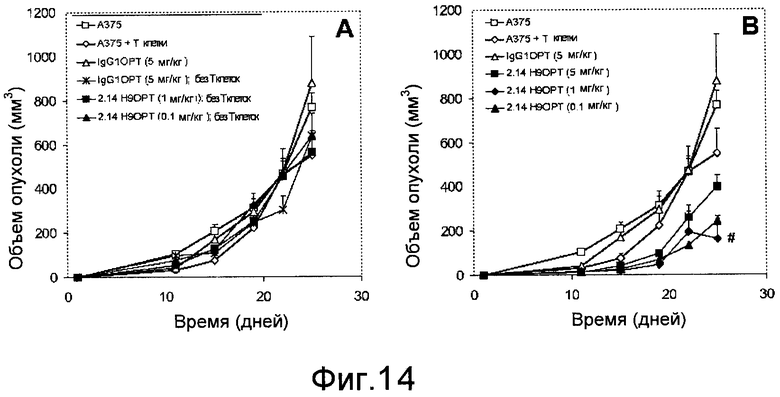
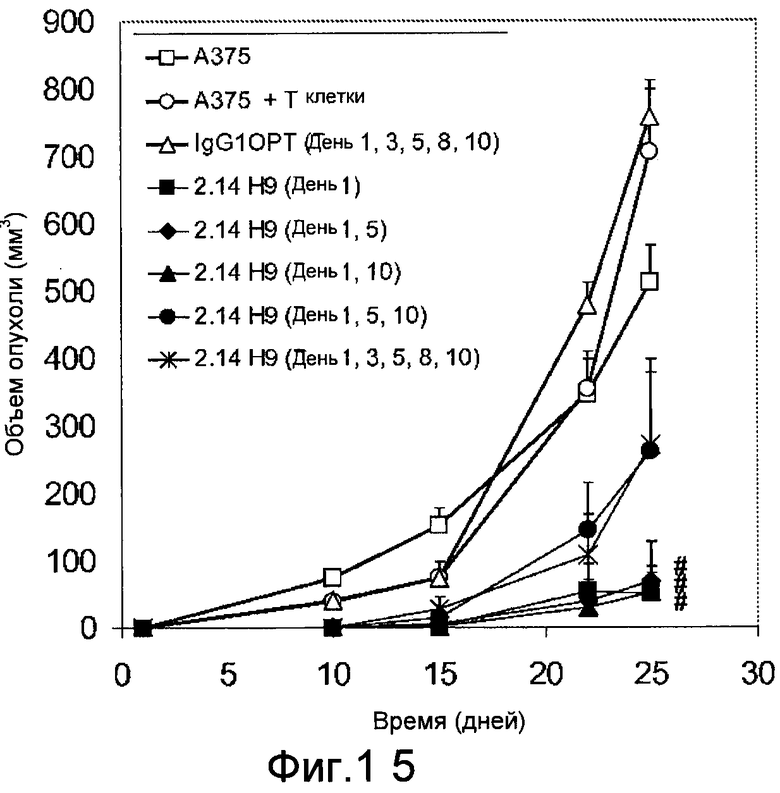
Изобретение относится к области иммунологии. Представлены вариантные выделенные антитела 2.9D10, 2.7A4, 2.14H9 и 2.14H9-opti и их антигенсвязывающие фрагменты, которые специфически связывается с В7-Н1, где каждое антитело или его антигенсвязывающий фрагмент содержит набор из 6 CDR, последовательности которых представлены в описании. Описаны: нуклеиновая кислота, кодирующая указанное антитело, и клетка-хозяин, продуцирующая указанное антитело против В7-Н1, трансфицированная вектором, содержащим указанную нуклеиновую кислоту. Раскрыты композиции, содержащие эффективное количество антитела по настоящему изобретению и фармацевтически приемлемый носитель, для использования в репрессии В7-H1-медиируемого ингибирования Т-клеток у животного. Предложены: способ репрессии В7-H1-медиируемого ингибирования Т-клеток у животного и способ лечения злокачественной опухоли у животного, связанной с В7-Н1, включающие введение животному, нуждающемуся в этом, эффективного количества указанной композиции. Изобретение позволяет расширить арсенал средств против В7-Н1. 12 н. и 10 з.п. ф-лы, 15 ил., 33 табл., 19 пр.
1. Выделенное антитело или его антигенсвязывающий фрагмент, которое специфически связывается с В7-Н1, где антитело или его антигенсвязывающий фрагмент обладает аминокислотной последовательностью, содержащей:
VH CDR1, с аминокислотной последовательностью SEQ ID NO: 13;
и
VH CDR2, с аминокислотной последовательностью SEQ ID NO: 14;
и
VH CDR3, с аминокислотной последовательностью SEQ ID NO: 15;
и
VL CDR1, с аминокислотной последовательностью SEQ ID NO: 18;
и
VL CDR2, с аминокислотной последовательностью SEQ ID NO: 19;
и
VL CDR3, с аминокислотной последовательностью SEQ ID NO: 20;
или
VH CDR1, с аминокислотной последовательностью SEQ ID NO: 63;
и
VH CDR2, с аминокислотной последовательностью SEQ ID NO: 64;
и
VH CDR3, с аминокислотной последовательностью SEQ ID NO: 65;
и
VL CDR1, с аминокислотной последовательностью SEQ ID NO: 68;
и
VL CDR2, с аминокислотной последовательностью SEQ ID NO: 69;
и
VL CDR3, с аминокислотной последовательностью SEQ ID NO: 70;
или
VH CDR1, с аминокислотной последовательностью SEQ ID NO: 73;
и
VH CDR2, с аминокислотной последовательностью SEQ ID NO: 74;
и
VH CDR3, с аминокислотной последовательностью SEQ ID NO: 75;
и
VL CDR1, с аминокислотной последовательностью SEQ ID NO: 78;
и
VL CDR2, с аминокислотной последовательностью SEQ ID NO: 79;
и
VL CDR3, с аминокислотной последовательностью SEQ ID NO: 80.
2. Антитело или его антигенсвязывающий фрагмент по п. 1, отличающееся тем, что ингибирует рост опухоли клеточной линии человеческого рака поджелудочной железы (НРАС) в модели ксенотрансплантата в день 30 более чем на 40% по сравнению с изотипическим контролем, при определении методом измерения объема опухолей.
3. Антитело или его антигенсвязывающий фрагмент по п. 1, отличающееся тем, что ингибирует рост опухоли клеточной линии А375 (меланома) в модели ксенотрансплантата в день 30 более чем на 50% по сравнению с изотипическим контролем, при определении методом измерения объема опухолей.
4. Антитело или его антигенсвязывающий фрагмент по п. 1, отличающееся тем, что представляет собой моноклональное антитело.
5. Антитело или его антигенсвязывающий фрагмент по п. 4, отличающееся тем, что представляет собой полностью человеческое моноклональное антитело.
6. Антитело или его антигенсвязывающий фрагмент по п. 1, где указанный антигенсвязывающий фрагмент выбран из группы, состоящей из Fab, Fab′, F(ab′)2 и Fv фрагмента.
7. Антитело или его антигенсвязывающий фрагмент по п. 1, отличающееся тем, что дополнительно включает вариант Fc, в котором Fc-участок содержит, по меньшей мере, одну неприродную аминокислоту, выбранную из группы, состоящей из 234F, 235F и 331S, пронумерованных в соответствии с индексом EU, как описано Кабат.
8. Молекула нуклеиновой кислоты, кодирующая антитело по п. 7.
9. Клетка-хозяин, трансфицированная вектором, содержащим молекулу нуклеиновой кислоты по п. 8 для получения антитела по п. 7.
10. Композиция, содержащая эффективное количество антитела по п. 7, для использования в репрессии В7-H1-медиируемого ингибирования Т-клеток у животного.
11. Фармацевтическая композиция, содержащая эффективное количество антитела по п. 7 и фармацевтически приемлемый носитель, для использования в репрессии В7-H1-медиируемого ингибирования Т-клеток у животного.
12. Способ репрессии В7-H1-медиируемого ингибирования Т-клеток у животного, включающий введение животному, нуждающемуся в этом, эффективного количества композиции по п. 10.
13. Способ лечения злокачественной опухоли у животного, включающий: выбор животного, нуждающегося в лечении злокачественной опухоли; и введение указанному животному терапевтически эффективного количества композиции по п. 11, где опухоль связана с В7-Н1.
14. Способ по п. 13, отличающийся тем, что указанную злокачественную опухоль выбирают из группы, состоящей из: меланомы, немелкоклеточного рака легкого, гепатоцеллюлярной карциномы, желудочного рака, рака мочевого пузыря, рака легкого, почечно-клеточной карциномы, рака шейки матки, рака ободочной кишки, колоректального рака и рака поджелудочной железы.
15. Способ по п. 12, отличающийся тем, что указанное животное является человеком.
16. Способ по п. 13, отличающийся тем, что указанное животное является человеком.
17. Очищенное антитело или его антигенсвязывающий фрагмент, где антитело или фрагмент иммуноспецифически связывается с В7-Н1 и содержит вариабельный домен тяжелой цепи с аминокислотной последовательностью SEQ ID NO: 72, и содержит вариабельный домен легкой цепи с аминокислотной последовательностью SEQ ID NO: 77, причем указанное антитело обладает активностью связывания с В7-Н1.
18. Композиция, содержащая эффективное количество антитела по п. 17, для использования в репрессии В7-H1-медиируемого ингибирования Т-клеток у животного.
19. Фармацевтическая композиция, содержащая эффективное количество антитела по п. 17 и фармацевтически приемлемый носитель, для использования в репрессии В7-H1-медиируемого ингибирования Т-клеток у животного.
20. Способ репрессии В7-Н1-медиируемого ингибирования Т-клеток у животного, включающий введение животному, нуждающемуся в этом, эффективного количества композиции по п. 18.
21. Способ лечения злокачественной опухоли у животного, включающий: выбор животного, нуждающегося в лечении злокачественной опухоли; и введение указанному животному терапевтически эффективного количества композиции по п. 19, где опухоль связана с В7-Н1.
22. Способ по п. 21, отличающийся тем, что указанную злокачественную опухоль выбирают из группы, состоящей из меланомы, немелкоклеточного рака легкого, гепатоцеллюлярной карциномы, желудочного рака, рака мочевого пузыря, рака легкого, почечно-клеточной карциномы, рака шейки матки, рака ободочной кишки, колоректального рака и рака поджелудочной железы.
| WO 2007005874 А2, 11.01.2007 | |||
| SCOTT E | |||
| STROME, et al "B7-H1 Blockade Augments Adoptive T-Cell Immunotherapy for Squamous Cell Carcinoma", CANCER RESEARCH 63, October 1, 2003, pp | |||
| ПРИСПОСОБЛЕНИЕ ДЛЯ РЕГУЛИРОВАНИЯ МОМЕНТА ЗАЖИГАНИЯ В ДВИГАТЕЛЯХ ВНУТРЕННЕГО ГОРЕНИЯ | 1926 |
|
SU6501A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| ARTERIOSCLEROSIS THROMBOSIS | |||
Авторы
Даты
2015-12-20—Публикация
2010-11-24—Подача