Область изобретения
Настоящее изобретение относится к лечению субъектов, страдающих сепсисом. Более конкретно, оно относится к определенному лечению субпопуляций субъектов, которые страдают от данного состояния.
Уровень техники
По оценкам, в год отмечается более 18 миллионов случаев сепсиса, которые в тяжелых случаях могут приводить к смерти, что делает сепсис второй по значимости причиной смерти в некоронарных отделениях интенсивной терапии. Смотри, например, Dellinger, et al., Crit. Care Med, 37(11): 2929-2938 (2009), включено посредством ссылки; Dellinger. et al., Crit. Care Med, 36(1): 296-327 (2008), также включено посредством ссылки; Marshall, et al. J Infect. Diseases, 190: 527-534 (2004), также включено посредством ссылки.
В широком смысле, "сепсис" относится к наличию системного воспалительного ответа в результате бактериальной инфекции. В свою очередь, системный воспалительный ответ определен как наличие отклонений от нормы двух или более из таких характеристик, как температура тела, частота сердечных сокращений, частота дыхания или содержание газа в крови, а также аномальное количество белых клеток крови. "Тяжелый сепсис" является результатом дисфункции одного или нескольких органов в результате ответа на вышеупомянутые инфекции, в то время как "септический шок" происходит с развитием сердечно-сосудистой нестабильности, в том числе гипотонии, также в результате ответа на вышеупомянутые инфекции. Термин "тяжелый септический шок" включает в себя как тяжелый сепсис, так и септический шок.
Когда в данном описании используется термин "сепсис", им охватываются все из перечисленных выше условий.
Подходы к лечению сепсиса включают, в частности, введение внутривенных жидкостей, антибиотиков, вазопрессоров и стероидов. Ни один из этих подходов не показал себя очень успешным, причем, в случае стероидов, терапевтические подходы являются спорными. Несмотря на данные подходы, как сообщается у Dellinger et al. (2009), выше, смертность остается высокой, и большая потребность медицины остается неудовлетворенной.
Патент США №5674855 на Levine, et al., раскрытие которого включено сюда посредством ссылки, описывает эмульсии из различных материалов, которые показали эффективность в лечении эндотоксемии. Вкратце, данные эмульсии содержат фосфолипид (фосфатидилхолин), нейтральный липид (триглицерид) и соль холата (холат натрия). Для данных материалов приводятся различные диапазоны в соотношении друг к другу. Патент раскрывает способ получения эмульсии, а также способы внутривенного введения ее.
Продукт на основе данных композиций, названный "GR270773," испытывали на эффективность у диализных субъектов с эндотоксемией (see www.clinicaltrials.gov, идентификатор NCT00506454) и в очень расширенном клиническом испытании, описанном у Dellinger et al. (2009), выше. Диализное испытание не показало какой бы то ни было эффективности, в то время как на основании клинического испытания, описанного у Dellinger et al. (2009), см. выше, был сделан вывод, что эмульсия не показала эффективности большей, чем применение плацебо.
В настоящее время было обнаружено, однако, что эмульсии типа, описанного в патенте ′855, на самом деле показывают удивительную эффективность в подгруппе субъектов, как определено здесь. Такой результат нельзя было ожидать на основе литературных источников, в которых было сделано заключение о неэффективности таких эмульсий.
Детали данного изобретения изложены в подробном описании предпочтительных вариантов, которые приведены ниже.
Подробное описание изобретения
Настоящее изобретение относится к способу лечения сепсиса, содержащему внутривенное введение количества эмульсии, которая содержит (i) фосфолипид, (ii) нейтральный липид и (iii) соль холата, субъекту, характеризующемуся уровнем сывороточного альбумина ("Alb" далее) в по меньшей мере 1,5 г/дл, а также одним или обоими из уровня общего холестерина (total cholesterol, "ТС" далее), составляющего по меньшей мере 40 мг/дл, и уровня липопротеина высокой плотности (high density lipoprotein, "HDL" далее), составляющего по меньшей мере 20 мг/дл. Субъекты, у которых обнаруживаются данные уровни биомаркеров, обладают достаточным количеством липопротеинов и имеют достаточную функцию печени, чтобы реагировать на эмульсию и удалить токсины, вызывающие сепсис.
Хотя и не желая быть связанными какой-либо теорией, используемые параметры были выбраны потому, что они служат в качестве маркеров для функций, являющихся ключом к клиренсу токсинов, вызывающих сепсис. Альбумин вырабатывается печенью, и на его концентрацию в сыворотке крови влияет множество факторов. Например, низкий уровень альбумина при критических болезненных состояниях, как полагают, связан с уменьшением уровня синтеза в печени, увеличением уровня катаболизма и капиллярной утечкой. Следовательно, уровни альбумина служат способом измерения клиренса фосфолипидов в печени.
Что касается холестерина и HDL, исследование терапевтической эмульсии показало, что она функционировала через доставку фосфолипида для HDL и к другим липопротеинам. Теоретически, в данном случае должен существовать некоторый уровень эндогенного липопротеина, который настолько мал, что фосфолипид из эмульсии не может в достаточной степени включаться в такие липопротеины, что делает эмульсию неэффективной.
Субъекты, у которых обнаруживаются уровни Alb и ТС или Alb и HDL, достаточные для удовлетворения критериям, указанным выше, получают положительный эффект от введения эмульсий согласно настоящему изобретению в гораздо большей степени, чем субъекты, у которых данные уровни недостаточны.
Эмульсии содержат, по отношению друг к другу, от около 5% до около 10% по массе соли холата, от около 5% до около 10% по массе нейтрального липида и от около 80% до около 90% по массе фосфолипидов. Могут быть добавлены другие ингредиенты, например носители или другие инертные ингредиенты, но соотношение 3-х ингредиентов по отношению друг к другу должно оставаться, как указано. Предпочтительно, соль холата представляет собой холат натрия, нейтральный липид представляет собой триглицерид, и фосфолипид представляет собой фосфатидилхолин. См. патент США номер 5674855, включенный посредством ссылки выше, для получения информации о различных составах.
Эмульсии должны вводиться субъектам внутривенно, в количестве, составляющем от около 500 мг/кг массы тела до около 1500 мг/кг массы тела, наиболее предпочтительно в дозе от около 750 мг/кг массы тела до около 1000 мг/кг массы тела, предпочтительнее, в течение трех дней. Также могут быть использованы другие схемы дозирования.
Подобные дозировки могут обеспечиваться с помощью первоначальной дозы высокой нагрузки с последующей более низкой поддерживающей дозой. Например, болюс в 75 мг/кг/ч в течение 2 часов, а затем болюс в 10 мг/кг/ч в течение 70 часов обеспечивает дозу в 850 мг/кг в течение 72-часового периода.
В примерах, которые следуют, готовили эмульсию, которая содержала 7,0 мас.% триглицерида, 7,2 мас.% холата натрия и 85,8 мас.% фосфатидилхолина. Субъекты получали внутривенную дозу в 850 мг эмульсии на кг массы тела в течение 72-часового периода.
Примеры
Пример 1
Считается, что успешное лекарственное средство для субъектов, страдающих сепсисом, должно уменьшить общую смертность по меньшей мере на 5% и предпочтительно по меньшей мере на 7% (см "Р-Е" в столбце "Положительный эффект" ниже). Тем не менее, чтобы непосредственно нормировать количество субъектов, спасенных с помощью успешного лекарственного средства, относительный положительный эффект в интервале от 15% до 20% является часто лучшим индикатором (см. "Относительный" в столбце " Положительный эффект" ниже).
Анализ выполняли с использованием образцов, взятых у пациентов, как описано у Dellinger et al. (2009) выше. Данное исследование "Dellinger" известно как испытание "LIPOS", и наименование "LIPOS" используется далее.
Образцы крови анализировали в отношении уровней Alb, ТС и HDL, используя способы, хорошо известные в данной области. Dellinger et al. (2009) не измеряли уровень Alb, и не удалось получить измерения ТС и HDL у субъектов с такими значениями, отсутствующими в исходных данных LIPOS.
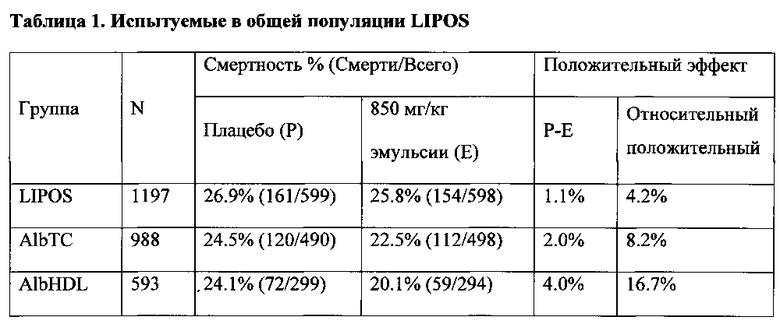
В таблице 1, выше, LIPOS относится к испытуемым, которые изучались в ходе испытания, описанного у Dellinger et al. (2009V. AlbTC" относится к субпопуляции, где, как отмечено выше, Alb≥1,5 г/дл и ТС≥40 мг/дл. "AlbHDL" представляет собой группу с уровнями Alb, как описано выше, и HDL≥20 мг/дл).
Что касается столбца "Положительный эффект", то "Р-Е" означает снижение смертности, разницу в выживаемости между теми, кто получил эмульсию, и теми, кто получил плацебо. "Относительный" положительный эффект соответствует 1 - RR, где RR, относительный риск (relative risk), представляет собой отношение вероятности смерти, произошедшей в получавшей эмульсию группе, по сравнению с группой, получавшей плацебо.
Несмотря на то, что значение относительного положительного эффекта составляло только 4,2% для всей популяции LIPOS, данное значение составляло 8,2% и 16,7%, соответственно, в группах AlbTC и AlbHDL, что, очевидно, соответствует желаемому диапазону значений.
Пример 2
В дополнительном анализе рассматривается субпопуляция испытуемых LIPOS, которые не получили вазопрессор кортизол внутривенно, для того, чтобы определить, как они будут отвечать критериям AlbTC и AlbHDL.
Таблица 2 показывает, как критерии AlbTC и AlbHDL позволяют отобрать реагирующих особей среди тех, которые не получали кортизол. Применение критериев AlbTC или Alb HDL в данной подгруппе дает преимущество Р-Е равное 6,2% и 10,8%, соответственно, по сравнению с 4,8% без применения критериев.


Данная субпопуляция испытуемых превзошла 5%-ный критерий преимущества Р-Е для обоих критериев AlbTC и AlbHDL, со значительными значениями относительного положительного эффекта в 24,3% и 40,0%, соответственно.
Пример 3
Для другого анализа взяли субпопуляцию испытуемых LIPOS, которые не имели внутрибрюшной инфекции. Данные испытуемые имели грамотрицательные бактериемии, внутрибольничную пневмонию или пиелонефрит.
Таблица 3 показывает, что данная подгруппа получалась исключением испытуемых с внутрибрюшной инфекцией и содержала только испытуемых с грамотрицательной бактериемией, внутрибольничной пневмонией или пиелонефритом. Здесь критерии AlbTC и AlbHDL дают значения положительного эффекта Р-Е лечения равные 6.2% и 8,9% по сравнению с 4,2% без использования данных критериев.
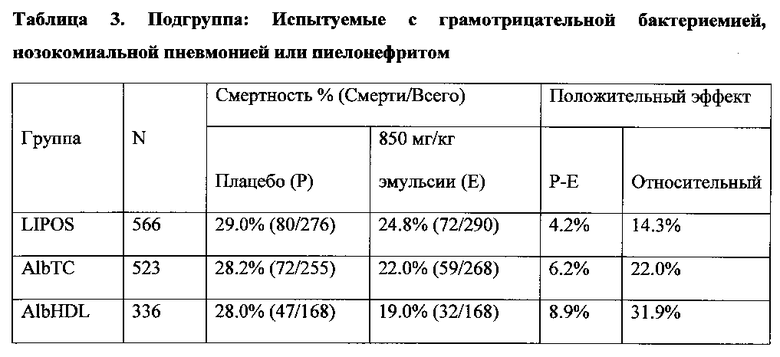
Данная субпопуляция испытуемых также превзошла 5%-ный критерий преимущества Р-Е для обоих критериев AlbTC и AlbHDL, со значительными значениями относительного положительного эффекта в 22,0% и 31,9%, соответственно.
В описании выше устанавливаются детали изобретения, которое относится к способу лечения сепсиса у субъекта, который (i) характеризуется уровнем сывороточного альбумина, составляющим по меньшей мере 1,5 г/дл, а также (ii) одним или обоими из уровня общего холестерина, составляющего по меньшей мере 40 мг/дл, и уровня липопротеина высокой плотности, составляющего по меньшей мере 20 мг/дл, внутривенным введением, в количестве, достаточном для лечения упомянутого сепсиса, эмульсии, которая содержит (i) фосфолипид, (ii) нейтральный липид и (iii) соль холата, в соотношении, при котором фосфолипид присутствует в количестве от около 80% до около 90% по массе, нейтральный липид присутствует в количестве от около 5% до около 10% по массе, и соль холата присутствует в количестве около 5% до около 10% по массе, Предпочтительно эмульсию вводят в течение трех дней, в количестве, варьирующем от около 500 мг/кг до около 1500 мг/кг массы тела, более предпочтительно от около 750 мг/кг массы тела до около 1000 мг/кг массы тела. Наиболее предпочтительно, чтобы доза была установлена в 850 мг/кг массы тела.
Способ введения может варьироваться, т.е. он может быть полностью непрерывным в течение заданного периода времени, или может принимать форму больших, "up front" болюсных доз с последующим меньшим, непрерывным дозированием, как показано выше.
Субъекты, которые должны лечиться в соответствии с изобретением, могут получать или могут не получать вазопрессор, такой как кортизол, и могут быть субъектами, у которых не проявляются внутрибрюшные инфекции, но проявляются одно или более из внутрибольничной пневмонии, пиелонефрита или бактериемии. Бактериемии, как и в общем случае сепсис, могут быть вызваны грамотрицательными и/или грамположительными бактериями.
Другие признаки изобретения будут ясны специалисту в данной области техники, и нет необходимости повторять их здесь.
Термины и выражения, которые были использованы, используются в качестве терминов описания, а не ограничения, и нет никакого намерения в использовании таких терминов и выражения исключения любых эквивалентов показанных и описанных признаков или их частей, с признанием того, что возможны различные модификации в пределах объема настоящего изобретения.
Изобретение относится к медицине и может быть использовано для лечения субъекта, страдающего сепсисом. Для этого у субъекта определяют уровни сывороточного альбумина, общего холестерина и липопротеина высокой плотности (HDL). При уровне сывороточного альбумина, составляющем по меньшей мере 1,5 г/дл, и уровне общего холестерина, составляющем по меньшей мере 40 мг/дл, и/или уровне липопротеина высокой плотности, составляющем по меньшей мере 20 мг/дл, внутривенно вводят эмульсию. Эмульсия содержит (i) фосфолипид, (ii) нейтральный липид и (iii) соль холата. Изобретение обеспечивает лечение сепсиса у субъектов, которые характеризуются превышающими минимальные пороговые значения уровнями сывороточного альбумина, а также общего холестерина и/или HDL. 15 з.п. ф-лы, 3 табл., 3 пр.
1. Способ лечения субъекта, страдающего сепсисом, включающий
(i) обнаружение у субъекта уровней сывороточного альбумина, общего холестерина и липопротеина высокой плотности, и
(ii) внутривенное введение эмульсии, которая содержит (i) фосфолипид, (ii) нейтральный липид и (iii) соль холата, субъекту, который характеризуется а) уровнем сывороточного альбумина, составляющим по меньшей мере 1,5 г/дл, и b) одним или обоими из уровня общего холестерина, составляющего по меньшей мере 40 мг/дл, и уровня липопротеина высокой плотности, составляющего по меньшей мере 20 мг/дл, в достаточном количестве, чтобы облегчить указанный сепсис, но не субъекту, у которого не обнаруживается (а) и по меньшей мере один из (b).
2. Способ по п. 1, в котором указанная эмульсия содержит:
(i) от около 80% до около 90% по массе фосфолипида,
(ii) от около 5% до около 10% по массе нейтрального липида, и
(iii) от около 5% до около 10% по массе соли холата.
3. Способ по п. 1, в котором фосфолипид представляет собой фосфатидилхолин.
4. Способ по п. 1, в котором нейтральный липид представляет собой триглицерид.
5. Способ по п. 1, в котором соль холата представляет собой холат натрия.
6. Способ по п. 1, включающий введение указанной эмульсии в количестве, варьирующем от около 500 мг/кг массы тела до около 1500 мг/кг массы тела указанного субъекта.
7. Способ по п. 6, включающий введение эмульсии в течение 72-часового периода.
8. Способ по п. 6, содержащий введение указанной эмульсии в количестве, варьирующем от около 750 мг/кг массы тела до около 1000 мг/кг массы тела.
9. Способ по п. 1, в котором указанный субъект получал или получает вазопрессор.
10. Способ по п. 1, в котором указанный субъект не получал вазопрессор.
11. Способ по п. 1, в котором сепсис вызван грамотрицательными бактериями.
12. Способ по п. 1, в котором сепсис вызван грамположительными бактериями.
13. Способ по п. 1, в котором указанный субъект страдает бактериемией.
14. Способ по п. 1, в котором указанный субъект страдает нозокомиальной пневмонией.
15. Способ по п. 1, в котором указанный субъект страдает пиелонефритом.
16. Способ по п. 1, в котором указанный субъект не страдает внутрибрюшной инфекцией.
| WO 2011050126 A1, 28.04.2011 | |||
| US 5674855 A, 07.10.1997 | |||
| DANNER RL | |||
| et al., Endotoxemia in human septic shock, Chest | |||
| Циркуль-угломер | 1920 |
|
SU1991A1 |
| DELLINGER RP et al., Efficacy and safety of a phospholipid emulsion (GR270773) in Gram-negative severe sepsis: results of a phase II multicenter, randomized, placebo-controlled, dose-finding clinical trial, Crit Care Med | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
Авторы
Даты
2015-12-20—Публикация
2013-09-30—Подача