Успех соединения в качестве лекарства зависит не только от его активности, но также от оптимального баланса между силой лекарства, лекарственных взаимодействий, безопасности, фармакокинетики и производственных затрат.
Перед тем как соединение может стать эффективным на рецепторе, значительное влияние могут оказывать его высвобождение, абсорбция и распределение. Только свободное лекарство (не связанное) может быть эффективным на рецепторе. Если лекарство слишком сильно связывается с белками, интенсивность его фармакологического ответа может быть уменьшена, и это также может влиять на объем распределения, метаболизм и выведение лекарства.
Для максимизации создания in vitro необходимо задать данные через High Throughput-ADME-скрининг (А=поглощение, D=распределение, М=обмен веществ, Е=выделение), чтобы химики получили обратную связь для нахождения вещества с лучшими физико-химическими свойствами и для понимания взаимосвязи между химической структурой и физико-химическими показателями.
Известным способом определения белкового связывания является, например, равновесный диализ. Начальной точкой этого способа являются две камеры, камера для образца и камера для белка, которые разделены полупроницаемой мембраной. MWCO мембраны (граница отсечки по молекулярному весу задерживаемых компонентов) выбрана так, что исследуемое вещество способно проникать, но макромолекула (например, белок) удерживается. В камеру для образца помещают исследуемое вещество с известной концентрацией и в известном объеме. Затем в камеру для белка помещают белок с известной концентрацией и в известном объеме, которые эквивалентны таковым у вещества в камере для образца. Поскольку исследуемое вещество диффундирует через мембрану, какая-то часть его будет связываться с белком, а какая-то часть будет оставаться свободной в растворе. Чем меньше аффинность взаимодействия, тем выше концентрация исследуемого вещества, которое останется несвязанным в какой-либо момент времени. Диффузия исследуемого вещества через мембрану и связывание исследуемого вещества продолжается до установления равновесия. При равновесии концентрация исследуемого соединения в растворе в свободном виде одинаковая в обеих камерах. Тем не менее, в камере для белка общая концентрация исследуемого вещества выше за счет связанного исследуемого вещества (если исследуемое соединение связывается с белком). Концентрация свободного исследуемого вещества в камере для образца может быть использована для определения характеристик связывания исследуемого соединения.
Другой способ заключается в использовании технологии BIAcore, при которой один из связывающих партнеров иммобилизован на сенсорном чипе. Другой связывающий партнер проходит через чип, который находится в микролунке. Обнаружение связывания основано на явлении «поверхностного плазменного резонанса» (SPR), небольших изменений в отражении монохроматического света от металлического чипа, которое возникает, когда поверхность чипа связывается с белком или другой молекулой.
Тем не менее, все эти способы не подходят для определения возможности белкового связывания высокоаффинных веществ в качестве высокопроизводительного анализа, так как невозможно провести различие между связыванием на 99% и 99,99% у веществ с высокой пропускной способностью. Причина в том, что концентрация свободного исследуемого вещества, которое анализируется в конце, является низкой, чтобы оценить ее количественно.
С высокоаффинными лекарствами небольшие изменения в количестве связанных веществ могут оказывать глубокое влияние на свободную фракцию в организме (см. таблицу ниже) и, тем самым, влиять на действие и побочные эффекты. Таким образом, очень важно делать измерения в этом самом диапазоне.
Пример с разницей 4%:
свободного
свободного
свободного
свободного
Таким образом, данное изобретение предусматривает способ определения константы связывания высокоаффинного соединения, представляющего интерес, с белками, включающий следующие этапы:
а) добавление высокоаффинного соединения в двухкамерную систему, в которой две камеры разделены мембраной, проницаемой для соединения, представляющего интерес, и определение количества высокоаффинного соединения, представляющего интерес, в одной из камер после того, как было достигнуто равновесное распределение,
б) добавление понижающего соединения в одну из камер (камеру для понижающего соединения), где понижающее соединение не может проникать через мембрану, и
определение коэффициента распределения соединения, представляющего интерес, на понижающем соединении после того, как было достигнуто равновесное распределение,
в) добавление неспецифического белка в другую камеру (камеру для белка), где неспецифический белок не может проникать через мембрану, и
определения коэффициента распределения соединения, представляющего интерес, на неспецифическом белке в присутствии понижающего соединения после того, как было достигнуто равновесное распределение, и
г) определение константы связывания исследуемого соединения с коэффициентом распределения из этапов б) и в).
Этапы а), б) и в) могут быть выполнены последовательно, или же они могут быть выполнены параллельно (см. фиг.3).
Таким образом, данное изобретение также предусматривает способ определения константы связывания высокоаффинного соединения, представляющего интерес, с белками, включающий следующие этапы:
а) обеспечение двухкамерных систем для параллельного выполнения, в которых две камеры каждой системы отделены друг от друга мембраной, которая проницаема для соединения, представляющего интерес, и добавление высокоаффинного соединения в двухкамерную систему, и
определение количества высокоаффинного соединения, представляющего интерес, в одной из камер после того, как было достигнуто равновесное распределение,
б) добавление высокоаффинного соединения и понижающего соединения в одну из камер второй системы камеры (в камеру для понижающего соединения), где понижающее соединение не может проникать через мембрану, и
определение коэффициента распределения соединения, представляющего интерес, на понижающем соединении после того, как было достигнуто равновесное распределение,
в) добавление высокоаффинного соединения и понижающего соединения в одну из камер третьей системы камеры (в камеру для понижающего соединения) и добавление неспецифического белка в другую камеру (камеру для белка), где неспецифический белок не может проникать через мембрану, и
определение коэффициента распределения соединения, представляющего интерес, на неспецифическом белке в присутствии понижающего соединения после того, как было достигнуто равновесное распределение, и
г) определение константы связывания исследуемого соединения с коэффициентом распределением из этапов б) и в),
где этапы а), б) и в) выполняются параллельно.
Кроме того, данная заявка предусматривает применение понижающего соединения для определения константы связывания высокоаффинного исследуемого соединения.
Понижающее соединение представляет собой вещество, которое значительно снижает аффинность высокоаффинных исследуемых веществ к неспецифическому белку. Значительно сниженная аффинность означает, что разница между количеством исследуемого вещества, связанного с неспецифическим белком, в присутствии и в отсутствие понижающего соединения является статистически значимой (р≤0,05, предпочтительно р≤0,01). Чтобы избежать прохождения понижающего соединения через мембрану, но позволить исследуемому соединению ее пересекать, размер понижающего соединения предпочтительно больше на коэффициент 2, чем размер исследуемого соединения. Предпочтительно, понижающее соединение является комплексообразующим агентом. Более предпочтительно понижающее соединение является поливинилпирролидоном (PVP), наиболее предпочтительно понижающее соединение является поливинилпирролидоном К-25 (PVP25, PVP К-25). Для указанного выше способа может быть использовано сочетание понижающих соединений, например, PVP и циклодекстрина.
Термин «высокоаффинное соединение», используемый в данном документе, относится к соединению, которое в физиологических условиях и в присутствии избытка белка плазмы (например, альбумина) по меньшей мере на 95% от общего количества связано с указанным белком плазмы (или не более 5% от общего количества указанного соединения находится в свободной форме). Предпочтительно, по меньшей мере 97% находятся в связанной форме, более предпочтительно по меньшей мере 98% и, наиболее предпочтительно, по меньшей мере 99% находятся в связанной форме. Физиологические условия определяются как рН 7,0 и 37°С. С точки зрения данного изобретения высокоаффинное соединение или исследуемое соединение предпочтительно представляет собой лекарство.
Термин «исследуемое вещество» или «исследуемое соединение», используемый в данном документе, относится к высокоаффинному соединению.
Термин «константа связывания» относится к постоянной, которая описывает аффинность связывания между двумя молекулами в равновесии. Она описывает состояние равновесия между свободным и связанным исследуемым веществом.
Термин «связанное вещество» или «связанное соединение», используемый в данном документе, относится к веществу или соединению, которое связано с белком (в частности, с неспецифическим белком) или с понижающим соединением. Термин «частичное заполнение» относится к доле исследуемого соединения, которая является связанной. Другими словами, это соотношение между количеством исследуемого соединения, связанным в равновесии с понижающим соединением (ссвязанного исследуемого вещества), и общим количеством исследуемого соединения (собщего исследуемого вещества).




Неспецифический белок в отличие от специфического белка связывается с широким кругом соединений (неселективное связывание). Неспецифические белки, в частности, представляют собой белки плазмы, такие как, например, сывороточный альбумин и а1-кислый гликопротеин. Предпочтительно, неспецифический белок представляет собой человеческий сывороточный альбумин (HSA).
Мембрана, используемая в способе данного изобретения, является полупроницаемой мембраной. Полупроницаемая мембрана представляет собой мембрану, которая позволяет отдельным видам молекул проходить через нее путем диффузии. Полупроницаемые мембраны для упомянутого выше анализа могут быть проходимыми для высокоаффинного соединения (и буфера), но не проходимыми для понижающего соединения или неспецифического белка. Предпочтительно, полупроницаемая мембрана является мембраной, селективной по размеру.
Полупроницаемые мембраны можно охарактеризовать с помощью показателя MWCO (граница отсечки по молекулярному весу задерживаемых компонентов). Предпочтительно, MWCO составляет примерно половину от молекулярной массы понижающего соединения или неспецифического белка, в зависимости от того, который из них меньше. Также предпочтительным является соотношение от 22 до 27 между молекулярными массами исследуемого вещества и понижающего соединения или неспецифического белка, в зависимости от того, который из них меньше. Более предпочтительно, этот показатель составляет примерно 25. Подходящие мембраны для способов данного изобретения являются коммерчески доступными, например диализные мембраны.
Предпочтительно, концентрация неспецифического белка, используемого в анализе, соответствует концентрации белка in vivo. Для HSA физиологическая концентрация составляет примерно 60 мМ.
Концентрация понижающего соединения для оптимальной производительности способа изобретения может быть определена с выполнением способа изобретения с различными концентрациями понижающего соединения (т.е. с последовательным разведением).
Анализ выполняется в двухкамерной системе, в которой две камеры разделены полупроницаемой мембраной. Проницаемость мембраны выбрана так, что исследуемое вещество может проходить через мембрану, но ни понижающее соединение, ни неспецифический белок не могут.
Измерения способа изобретения (этапы а), б) и в)) могут быть выполнены параллельно (см. фиг.3) или последовательно. Предпочтительно, чтобы измерения проводились параллельно. Далее описано предпочтительное воплощение: для референсного эксперимента (этап а) описанного выше способа соединение, представляющее интерес, добавляют в одну из камер (см. фиг.2,В) и определяют распределение соединения в этой системе после того, как достигается равновесное распределение, где масса соединения по меньшей мере в одной из камер определяется после того, как достигается равновесное распределение.
Для эксперимента по связыванию 1 (этап б) описанным выше способом соединение, представляющее интерес, и понижающее соединение добавляют в камеру двухкамерной системы, отличной от той, которая используется для выполнения референсного эксперимента (см. также фиг.2,В). После того как достигается равновесие системы связывания, измеряют количество высокоаффинного соединения в камере без понижающего соединения (камера для белка) и определяют коэффициент распределения соединения, представляющего интерес, на понижающем соединении.
Для эксперимента по связыванию 2 (этап г)) описанным выше способом соединение, представляющее интерес, и понижающее соединение добавляют в камеру (камеру для понижающего соединения) двухкамерной системы, отличной от той, которая используется для выполнения референсного эксперимента или эксперимента по связыванию (см. фиг.2,С)), и в камеру без понижающего соединения (камеру для белка) добавляют неспецифический белок. После того как достигается равновесие, измеряют количество свободного исследуемого вещества (не связанного с понижающим соединением) в камере для понижающего соединения и определяют коэффициент распределения соединения, представляющего интерес, на неспецифическом белке в присутствии понижающего соединения.
Константа связывания высокоаффинного соединения определяется следующим образом:
Связывание исследуемого соединения с неспецифическим белком является обратимым процессом, который может быть описан следующим равновесием ((Lindup, W.E., Plasma protein binding of drugs - some basic and clinical aspects, in Progress in Drug Metabolism, L.F.C. J.W. Bridges, G.G. Gibson, Editor. 1987. p.141-185):
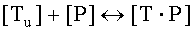
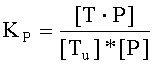
[P]=концентрация неспецифического белка,
[Tu]=концентрация исследуемого соединения, не связанного с неспецифическим белком,
KP=константа связывания исследуемого соединения с неспецифическим белком,
[T·P]=концентрация исследуемого соединения, связанного с неспецифическим белком, когда достигается равновесие.
Константа связывания KP может быть переведена в долю несвязанного fu по следующей формуле, выведенной из закона масс:
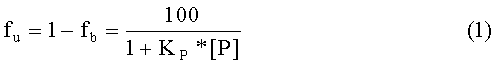
fb = фракция исследуемого соединения, связанного с неспецифическим белком.
Константа связывания с неспецифическим белком (KP) (2) может быть рассчитана из комбинации коэффициентов распределения на понижающем соединении (DСпонижающего) (3) и неспецифическом белке в присутствии понижающего соединения (DCP') (3).
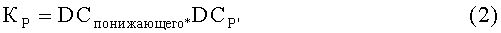
Из анализа связывания 1 (с понижающим соединением, фиг.2,В):
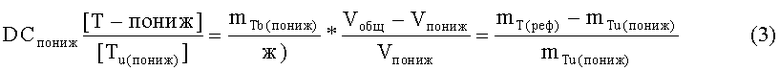
mT(реф)= масса исследуемого соединения в равновесии, в отсутствие понижающего соединения и неспецифического белка (измеряется в одной из камер),
mTu(пониж)= масса несвязанного исследуемого соединения в равновесии, в присутствии понижающего соединения.
Из анализа связывания II (система с понижающим соединением и высокоаффинным соединением, фиг.2,С):
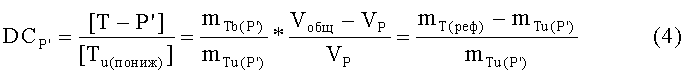
[Т-Р']=концентрация исследуемого соединения, связанного с неспецифическим белком, в присутствии понижающего соединения,
[Т-пониж]=концентрация исследуемого соединения, связанного с понижающим соединением,
mTb(P')=масса исследуемого соединения, связанного с неспецифическим белком, в равновесии, в системе с понижающим соединением и неспецифическим белком,
mTu(P')=масса исследуемого соединения, не связанного с неспецифическим белком, в равновесии, в системе с понижающим соединением и неспецифическим белком,
Vобщ является общим объемом в диализной камере (например, 200 мкл),
VP является объемом неспецифического белка,
Vпониж является объемом понижающего соединения.
Объемы могут быть рассчитаны по плотности и массе применяемого материала.
V=масса/плотность (например, плотность человеческого сывороточного альбумина: ρHSA=1.4g/cm3, плотность PVP25: ρPVP=1.2g/cm3).
Количество свободного и/или связанного исследуемого вещества может быть определено спектрофотометрически непосредственно в спектрофотометре или после разделения в системе ВЭЖХ.
Для всех контрольных экспериментов и экспериментов по связыванию камерные системы предпочтительно инкубируют при комнатной температуре и нормальном давлении (например, в течение ночи (примерно 12 часов)). Для ускорения достижения равновесия камеру можно встряхивать (предпочтительно в течение 1-3 часов, более предпочтительно в течение 1-2 часов, наиболее предпочтительно примерно в течение 1 часа).
В предпочтительном воплощении способ данного изобретения осуществляется в параллелях в планшете, содержащем множество двухкамерных систем. Эти параллельно выполненные анализы будут одинаковыми или могут отличаться, например, по идентичности или концентрации высокоаффинного соединения.
С наличием здесь общего описания изобретения также для лучшего понимания приведены ссылки на конкретные примеры, которые включены в данный документ с целью иллюстрации и не предназначены для ограничения, если иное не указано, в связи со следующими графическими материалами.
Графические материалы
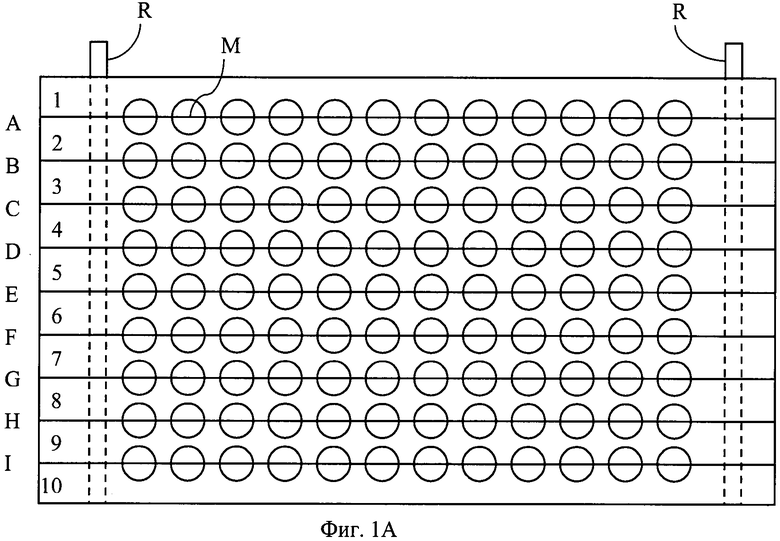
На фиг.1 показана система диализной камеры, состоящей из 10 тефлоновых брусков Teflon™, где 8 брусков Teflon™ имеют 12 отверстий на каждой стороне и два имеют 12 отверстий на одной стороне (фиг.1А). Указанные отверстия имеют форму полуцилиндра (см. фиг.1В), так что два бруска вместе образуют ряд из 12 цилиндрических лунок (строки от А до I). Между брусками Teflon™ так вставлена полупроницаемая мембрана (М), что каждая цилиндрическая лунка также разделена на две полуцилиндрические камеры. 10 брусков Teflon™ с мембранами собраны с помощью двух стержней (R) из нержавеющей стали.
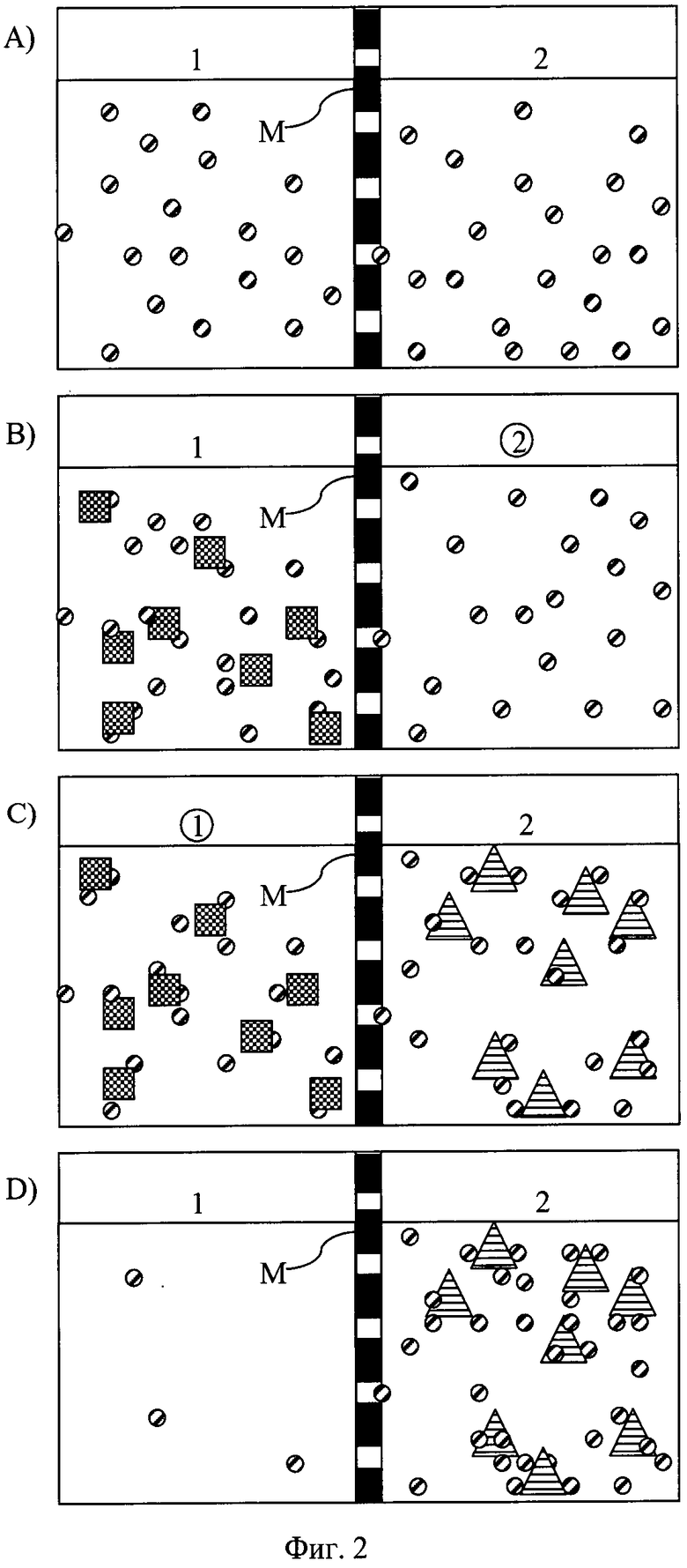
На фиг.2 показана система диализной камеры во время анализа. Камера состоит из двух камер (камера 1, камера 2), которые разделены мембраной М. Селективная по размеру мембрана М разделяет две камеры и проницаема для исследуемого соединения, но не для понижающего соединения или неспецифического белка. Исследуемое соединение:  ; неспецифический белок:
; неспецифический белок:  ; понижающее соединение:
; понижающее соединение:  . Обведенный номер камеры указывает на камеру, из которой отбирается образец для измерения. На фиг.2,А) показано схематическое представление ситуации в системе камер в референсных условиях, когда исследуемое соединение распределяется равномерно в системе камер. На фиг.2,В) показано схематическое представление ситуации в системе камер с исследуемым соединением и понижающим соединением. Исследуемое соединение и понижающее соединение добавляют в камеру 1, и они влияют на распределение исследуемого соединения, так как только несвязанное исследуемое соединение может пересечь мембрану. На фиг.2,С) показано схематическое представление ситуации в системе камер с исследуемым соединением, понижающим соединением и неспецифическим белком. Исследуемое соединение и понижающее соединение добавляют в камеру 1, а неспецифический белок добавляют в камеру 2. Понижающее соединение уменьшает количество несвязанного исследуемого соединения, доступного для неспецифического белка. На фиг.2,D) показано схематическое представление ситуации в системе камер с анализом известного уровня техники. Высокий процент исследуемого соединения связан с неспецифическим белком.
. Обведенный номер камеры указывает на камеру, из которой отбирается образец для измерения. На фиг.2,А) показано схематическое представление ситуации в системе камер в референсных условиях, когда исследуемое соединение распределяется равномерно в системе камер. На фиг.2,В) показано схематическое представление ситуации в системе камер с исследуемым соединением и понижающим соединением. Исследуемое соединение и понижающее соединение добавляют в камеру 1, и они влияют на распределение исследуемого соединения, так как только несвязанное исследуемое соединение может пересечь мембрану. На фиг.2,С) показано схематическое представление ситуации в системе камер с исследуемым соединением, понижающим соединением и неспецифическим белком. Исследуемое соединение и понижающее соединение добавляют в камеру 1, а неспецифический белок добавляют в камеру 2. Понижающее соединение уменьшает количество несвязанного исследуемого соединения, доступного для неспецифического белка. На фиг.2,D) показано схематическое представление ситуации в системе камер с анализом известного уровня техники. Высокий процент исследуемого соединения связан с неспецифическим белком.
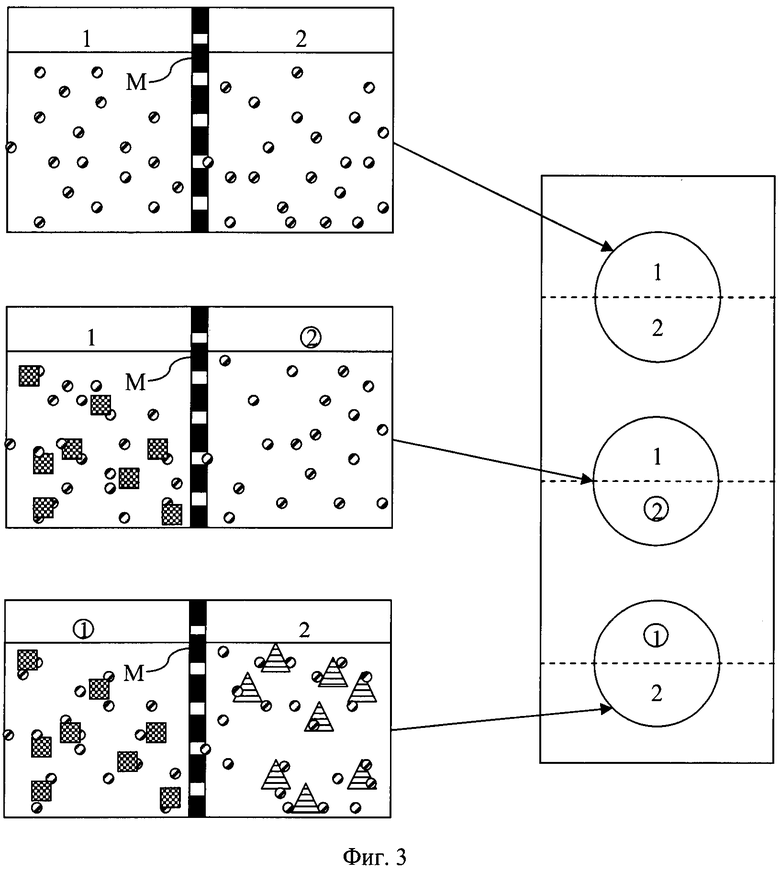
На фиг.3 показано схематическое представление способа данной заявки, выполненного параллельно в трех двухкамерных системах.
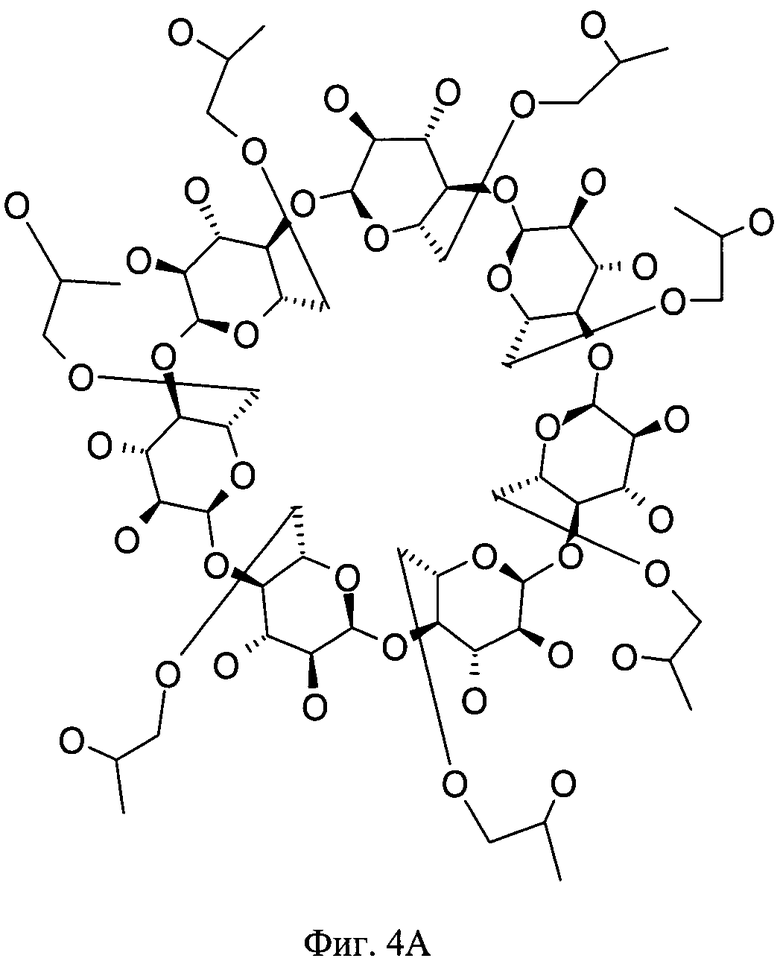
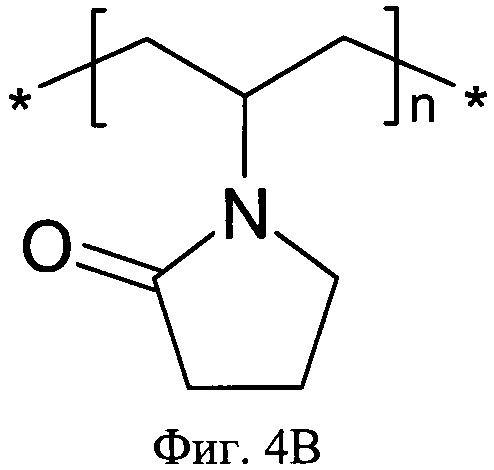
На фиг.4 показана химическая структура бета-гидроксипропил-циклодекстрина (А) и мономера поливинилпирролидона (В).
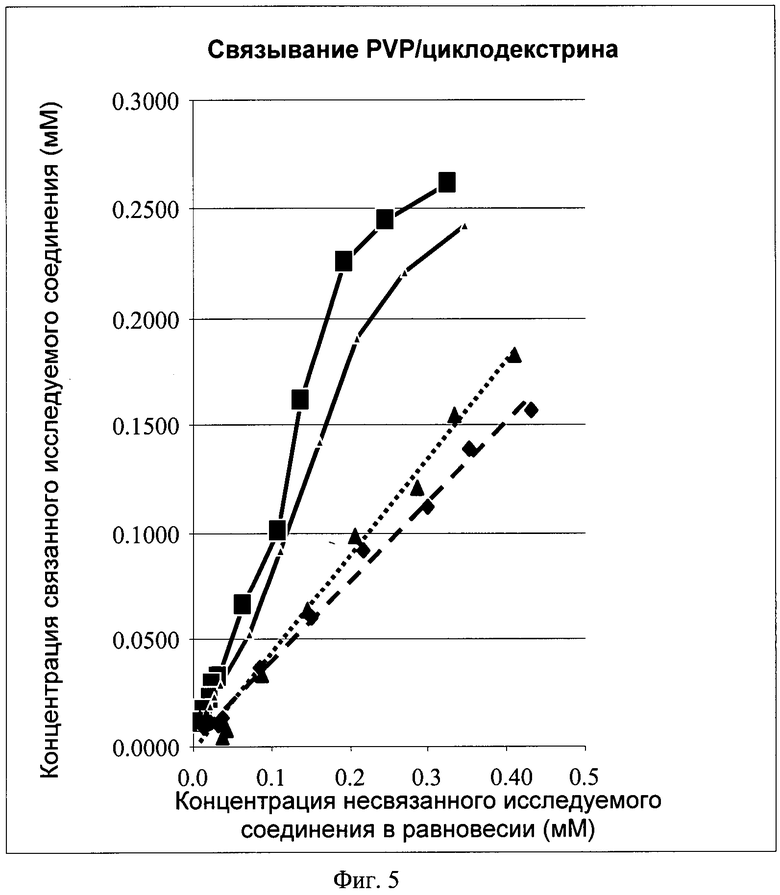
На фиг.5 показано сравнение частичного заполнения исследуемого соединения (варфарин, диклофенак) понижающим соединением PVP25 и частичного заполнения исследуемых соединений комбинацией понижающих соединений (бета-гидроксипропилциклодекстрин, PVP25). Х-ось: концентрация несвязанного исследуемого соединения в равновесии в мМ, Y-ось: концентрация связанного исследуемого соединения.  Варфарин с PVP25;
Варфарин с PVP25;  диклофенак с PVP25;
диклофенак с PVP25;  варфарин с PVP25 и β-гидроксипропилциклодекстрином (
варфарин с PVP25 и β-гидроксипропилциклодекстрином ( линеаризация);
линеаризация);  диклофенак с PVP25 и (3-гидроксипропилциклодекстрином (
диклофенак с PVP25 и (3-гидроксипропилциклодекстрином ( линеаризация).
линеаризация).
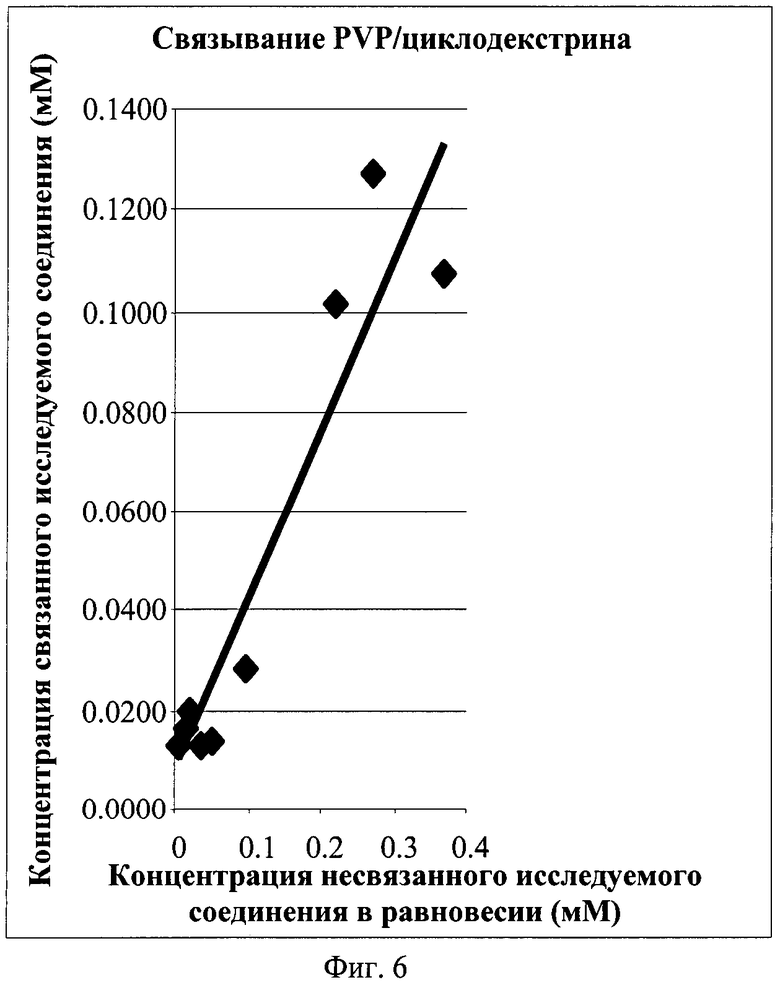
На фиг.6 показано графическое представление частичного заполнения карведилола комбинацией понижающих соединений (бета-гидроксипропилциклодекстрина, PVP25). Х-ось: концентрация несвязанного карведилола в равновесии в мМ, Y-ось: концентрация связанного исследуемого соединения.  Карведилол PVP25 с β-гидроксипропилцклодекстрином.
Карведилол PVP25 с β-гидроксипропилцклодекстрином.
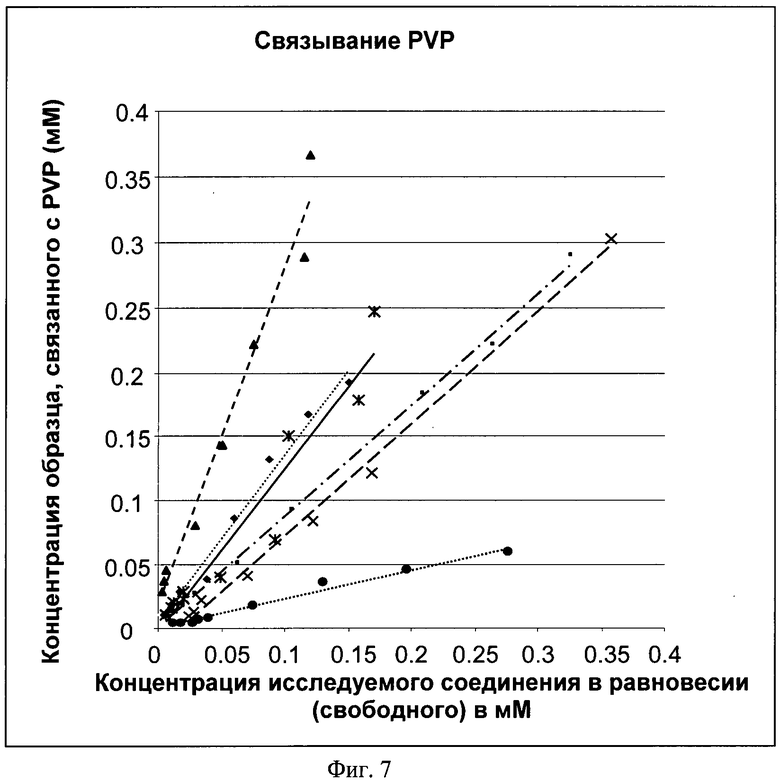
На фиг.7 показано графическое представление частичного заполнения исследуемых соединений (диклофенак, варфарин, карведилол, напроксен, пироксикам и глибенкламид) понижающим соединением PVP25. Х-ось: общая концентрация карведилола в мМ, Y-ось: частичное заполнение карведилола в % (количество исследуемого соединения, связанного с понижающим соединением).  Диклофенак с PVP25 (
Диклофенак с PVP25 ( линеаризация);
линеаризация);  варфарин с PVP (
варфарин с PVP ( линеаризация);
линеаризация);  карведилол с PVP25 (
карведилол с PVP25 ( линеаризация), × напроксен с PVP25 (
линеаризация), × напроксен с PVP25 ( линеаризация); * пироксикам с PVP25 (-линеаризация); • глибенкламид с PVP25 (
линеаризация); * пироксикам с PVP25 (-линеаризация); • глибенкламид с PVP25 ( линеаризация).
линеаризация).
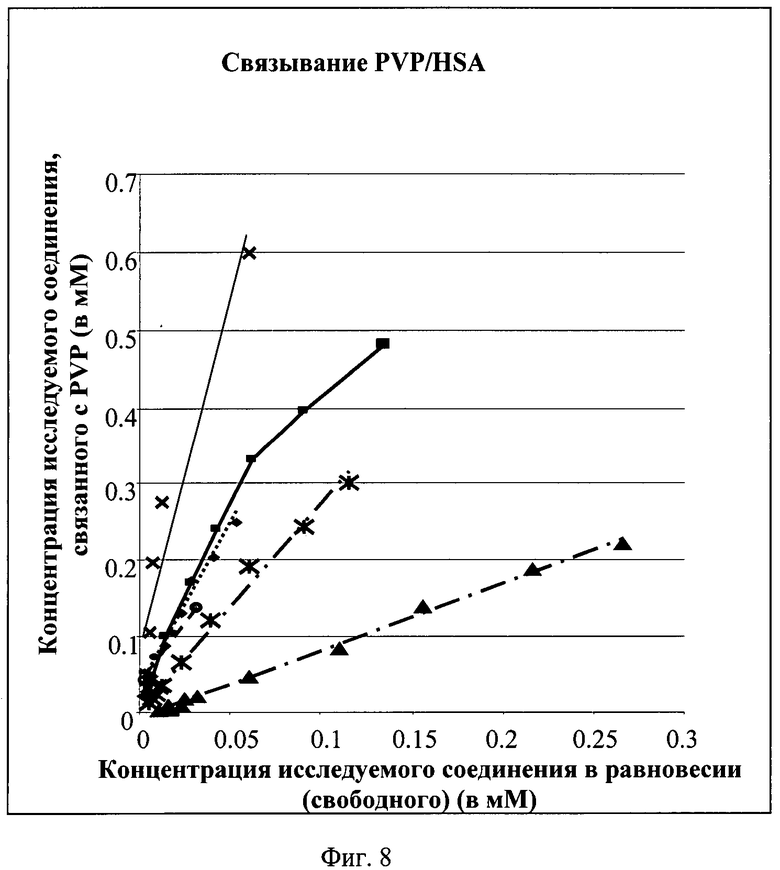
На фиг.8 показано графическое представление частичного заполнения исследуемых соединений (диклофенак, варфарин, карведилол, напроксен, пироксикам и глибенкламид) понижающим соединением PVP25 в присутствии человеческого сывороточного альбумина (HSA). Х-ось: общая концентрация карведилола в мМ, Y-ось: частичное заполнение карведилола в % (количество исследуемого соединения, связанного с понижающим соединением). • Диклофенак с PVP25 ( линеаризация);
линеаризация);  варфарин с PVP (линеаризация);
варфарин с PVP (линеаризация);  карведилол с PVP25 (
карведилол с PVP25 ( линеаризация), × напроксен с PVP25 (-линеаризация); * пироксикам с PVP25 (
линеаризация), × напроксен с PVP25 (-линеаризация); * пироксикам с PVP25 ( линеаризация);
линеаризация);  глибенкламид с PVP25 (
глибенкламид с PVP25 ( -линеаризация).
-линеаризация).
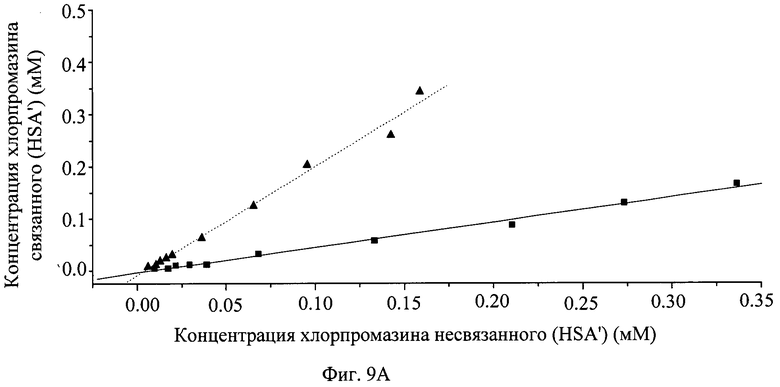
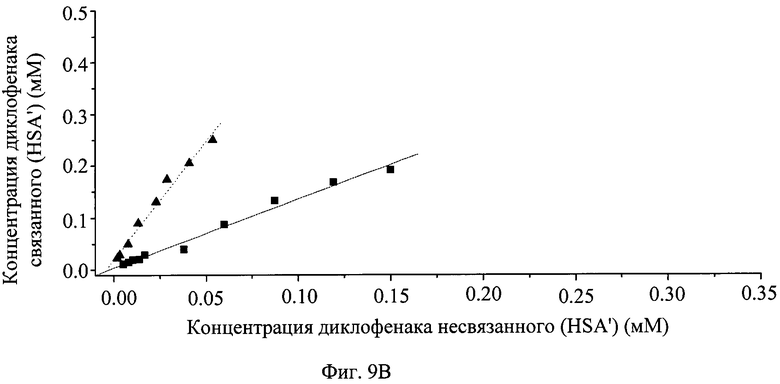
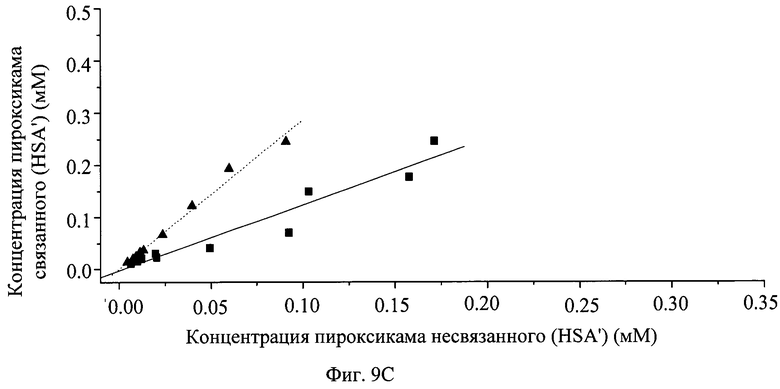
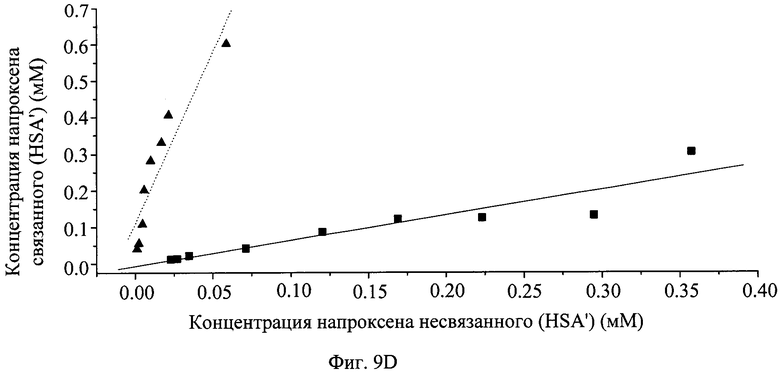
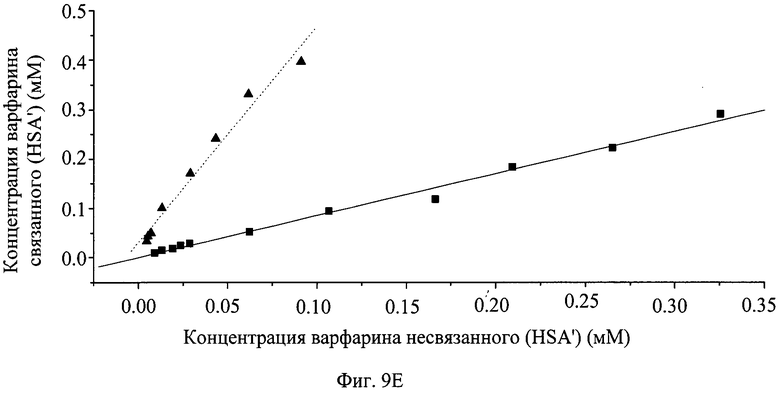
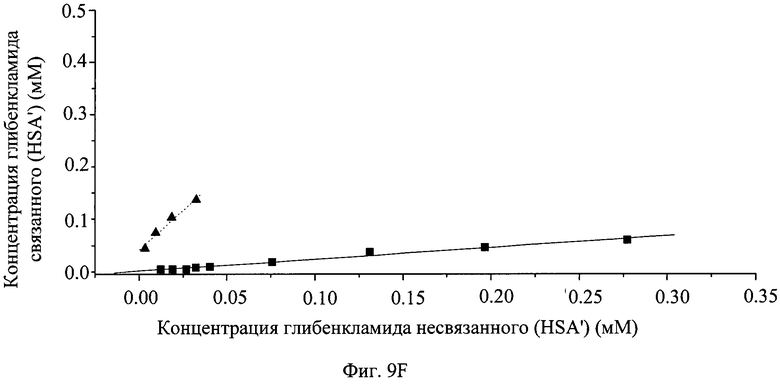
На фиг.9 показано графическое представление распределения хлорпромазина (А), диклофенака (В), пироксикама (С), напроксена (D), варфарина (Е) и глибенкламида (F) с HSA в присутствии PVP25 ( ) и с PVP25 (
) и с PVP25 ( ).
).
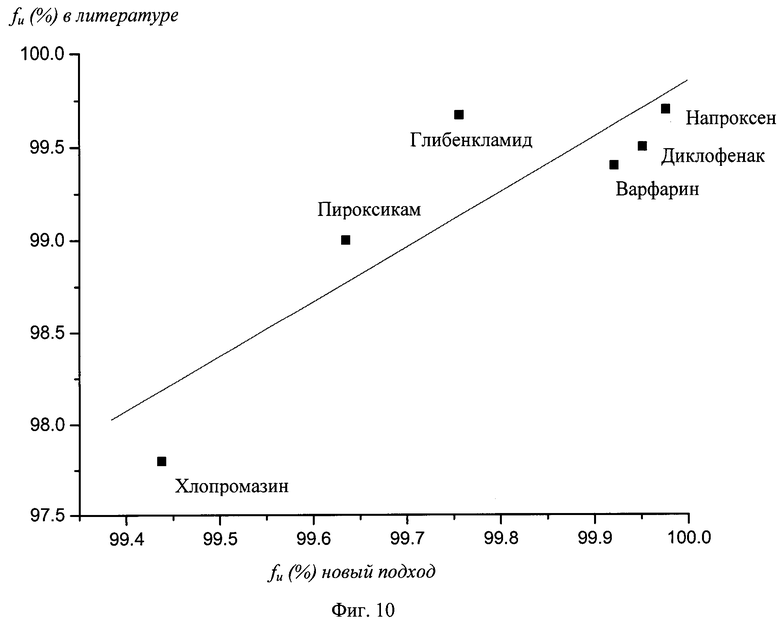
На фиг.10 показано графическое представление определения константы связывания способом данного изобретения по сравнению с литературными данными.
Примеры:
Коммерчески доступные реагенты, упомянутые в примерах, использовали в соответствии с инструкциями изготовителя, если не указано иное.
Пример 1: Материалы и методы
1.1. Диализные камеры
Для следующих экспериментов использовали многоразовую 96-луночную диализную камеру Micro-Equilibrium dialysis Device HTD. Камерная система состоит из 10 брусков Teflon™, где между каждыми двумя брусками Teflon™ помещена полупроницаемая мембрана (см. п.1.2. Мембраны), формирующая два отсека в каждой лунке.
Собранный блок Teflon™ вставлен в стальную раму. Для обеспечения плотности между отдельными лунками бруски прижимают друг к другу с помощью стальной пластины. Указанная стальная пластина зафиксирована за счет противодавления 8-ю дисковыми пружинами на брусках Teflon™.
Перед каждым экспериментом бруски Teflon™ очищали путем промывки в этаноле четыре раза.
1.2. Мембраны
•MWCO
Следующие MWCO были испытаны в зависимости от вспомогательного вещества:
* Материал для мембраны
A) НТО 96 Dialysis Мембрана Strips (регенерированная целлюлоза) с MWCO 6-8 кДа (HTDialysis, LLC, кат.№1103) и MWCO 12-14 кДа (HTDialysis, LLC, кат.№1101).
Упомянутые выше мембраны гидратировали деионизированной водой в течение 60 минут. Затем их обрабатывали в течение 20 минут 20% этанолом, а затем дважды промывали деионизированной водой.
B) Spektra/Por 6 (регенерированная целлюлоза) с MWCO 1 кДа (Spectrum Laboratories, кат.№132640, 45 мм ширина/длина 10 м) и MWCO 3,5 кДа (Spectrum Laboratories, кат.№132592, ширина 45 мм/длина 10 м).
Удаление тяжелых металлов:
Раствор для очистки от тяжелых металлов Heavy Metal Cleaning, содержащий EDTA (Spektrum, кат.№132908); 1 часть промывочного раствора+9 частей дистиллированной Н2О.
Промывание 1 час, затем 5 минут в дистиллированной Н2О.
Удаление 0.1% сульфидов:
Очищающий сернистый раствор А (=Na-сульфит) и
В (=0,4% серная кислота) (Spektrum, кат.№132906).
При 80°С мембраны промывали раствором, содержащим 2 части дистиллированной Н2О+1 часть раствора А. Затем мембраны промывали в 60°С горячей H2O в течение 2 минут. Затем мембраны промывали в растворе, содержащем 100 частей воды и 4 части раствора В, а затем их промывали в дистиллированной воде в течение нескольких минут.
Альтернативно, использовали предварительно промытые мембраны.
С) Spektra/Por 7 (регенерированная целлюлоза) MWCO 3,5 кДа (Spectrum Laboratories, кат.№132111, ширина 45 мм/длина 5 м). Мембрану промывали в дистиллированной воде.
1.3. Понижающие соединения
A) Циклодекстрин (фиг.3)
Условие для применения циклодекстрина заключается в том, что молекулярная масса больше, чем MWCO используемой мембраны, для того, чтобы понижающее соединение было отделено от камеры для понижающего соединения.
Использовали следующие циклодекстрины:
- бета-гидроксипропилциклодекстрин
- гамма-циклодекстрин.
B) Поливинилпирролидон РVР (фиг.4)
PVP (поливидон, повидон, Povidonum), гомополимер М-винилпирролидона
Молекулярная масса обычно выражается как значение К.
Молекулярная масса зависит от степени полимеризации (примерно 2500-3000000 Да).
Эксперименты проводили с PVP25 (PVP K-25) с молекулярной массой
примерно 24000 и с PVP15 (PVP K-15) с молекулярной массой примерно 10000.
1.4. Исследуемые соединения
- варфарин ((RS)-4-гидрокси-3-(3-оксо-1-фенилбутил)-2Н-хромен-2-он)
- фуросемид (4-хлор-2-(фуран-2-илметиламино)-5-сульфамоилбензойная кислота)
- диклофенак (2-(2-(2,6-дихлорфениламино)фенил)уксусная кислота)
- верапамил (2-(3,4-диметоксифенил)-5-[2-(3,4-диметоксифенил)этилметиламино]-2-(1-метилэтил)пентанонитрил)
- хлорпромазин (3-(2-хлор-10Н-фенотиазин-10-ил)-N,N-диметилпропан-1-амин)
- карведилол (3-(9Н-карбазол-4-илокси)-2-гидроксипропил][2-(2-метоксифенокси)этил]амин)
- напроксен ((+)-(S)-2-(6-метоксинафтален-2-ил)пропановая кислота)
- пироксикам ((8Е)-8-[гидрокси(пиридин-2-иламино)метилиден]-9-метил-10,10-диоксо-10λ6-тиа-9-азабицикло[4.4.0]дека-1,3,5-триен-7-он)
- глибенкламид (5-xnop-N-(4-[N-(циклогексилкарбамоил)сульфамоил]фенэтил)-2-метоксибензамид)
1.5: Процедура эксперимента
1) Подготовка мембран (см. пример 2) и сборка диализной камеры в примере 1.
2) Белковую камеру (камера 2) заполняли буфером и другими эксципиентами до конечного объема примерно 100-150 мкл. Важно, чтобы с каждой стороны объем был строго одинаковый.
Объем на одну камеру:
с чистыми циклодекстринами в качестве понижающего соединения объем в каждой камере составлял 147 мкл (γ-циклодекстрин 2,5% (масса/объем));
с PVP и PVP в сочетании с циклодекстринами в качестве понижающего соединения объем в камере составлял 100 мкл (PVP15 4% (масса/объем), PVP25 4% (масса/объем), PVP25 4% (масса/объем)+гидроксипропилциклодекстрин 4% (масса/объем)).
Буфер: 50 мМ TAPSO, рН 7,4, доведенный до изотоничности с помощью NaCl до общей концентрации 154 мМ, дополнительный эксципиент отличается в зависимости от эксципиента.
Конечная концентрация исследуемого соединения: от 0,02 мМ до 0,6 мМ.
Конечная концентрации HSA: 60 мМ.
Конечная концентрация DMSO: 6% (объем/объем).
Стоковый раствор DMSO добавляют в конце, потому что это занимает много времени, а камеры должны быть заполнены довольно быстро из-за риска, что высохнет мембрана.
3) Все этапы пипетирования были автоматизированы (Tecan).
4) Для предотвращения испарения сборку Teflon™ покрывали клейкой пленкой (кат.№1102; HT-Dialysis).
5) Камерную систему встряхивали в течение 1 часа, затем инкубировали в течение ночи (примерно 12 часов). Длительного встряхивания следует избегать из-за риска большего испарения, вызванного образованным теплом.
6) После достижения равновесия образец из камеры для понижающего соединения (референс, исследование связывания II с понижающим соединением и HSA) или из белковой камеры (референс, исследование связывания I только с понижающим соединением) переносили в половину - УФ-область - планшета и анализировали спектрометрически (планшетный ридер SpectraMax 190; 250-500 нм) или путем ВЭЖХ.
1.6. Анализ измеренных данных
Коэффициент распределения и константы связывания могут быть рассчитаны из исследований по связыванию.
Связывание лекарств с HSA является обратимым процессом, который может быть описан следующим равновесием [4]
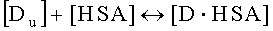
где квадратные скобки используются для обозначения концентраций, и [Du], [HAS] и [D·HSA] являются концентрациями не связанного с HSA лекарства, HSA и связанного с HSA лекарства соответственно.
Константа связывания KHSA может быть преобразована в долю несвязанного fu с помощью следующей формулы, выведенной из закона масс:
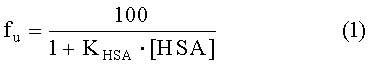
Константа связывания с HSA (KHSA) (2) может быть рассчитана из сочетания коэффициентов распределения на PVP (DCPVP) (3) и на HSA в присутствии PVP (DCHSA') (3).
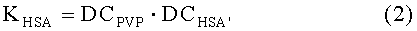
Из исследования по связыванию I:
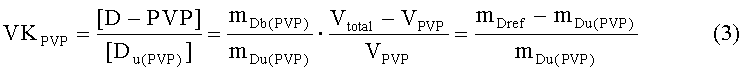
Из исследования по связыванию II:
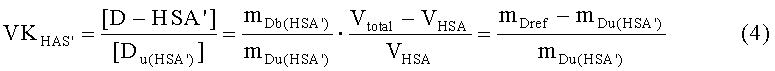
Где [D-HAS'] и [D-PVP] являются концентрациями HSA-связанного лекарства в присутствии PVP и PVP-связанного лекарства соответственно.
Vtotal представляет собой общий объем в диализной камере (200 мкл), a VHSA и VPVP представляют собой объемы HSA и PVP25, которые могут быть рассчитаны по плотности и весу образца
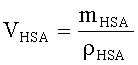
ρHAS=1.4g/cm3 и ρPVP=1.2g/cm3. Для определения плотности PVP должен быть расплавлен, и существуют вариации за счет включения воздуха. Таким образом, реальная плотность основана на информации от BASF (производителя).
Приведенное выше уравнение аналогично может быть применено для определения концентрации несвязанного/связанного исследуемого соединения в равновесии с другим понижающим соединением.
Пример 2: Сравнение бета-гидроксипропилциклодекстрина с гамма-циклодекстрином
Результаты представлены в таб. 1. С 10% раствором бета-гидроксипропилциклодекстрина может быть связано более 30% анализируемого соединения. Аффинность к гамма-циклодекстрину значительно ниже, чем у бета-гидроксипропилциклодекстрина (для достижения такого же частичного заполнения необходима в 2,5 раза более высокая концентрация гамма-циклодекстрина).
Таблица 1: Уровни связывания эксципиента, измеренные для варфарина
Пример 3: Анализ бета-гидроксипропилциклодекстрина в качестве понижающего соединения
Условия анализа являются такими же, как описано выше, если специально не указано.
Таблица 2: Среднее связывание исследуемых соединений с бета-гидроксипропилциклодекстрином
Вывод: чем ниже молекулярный вес исследуемого соединения, тем выше аффинность к бета-гидроксипропилциклодекстрину.
Пример 4: Сравнение PVP15 с PVP25
Условия анализа являются такими же, как описано выше, если специально не указано.
Концентрации лекарств: 0,02-0,6 мМ.
Количества PVP15 и PVP25: каждый 40 г/л.
Таблица 3: Среднее связывание анализируемых соединений с PVP15 и PVP25 (н.о. = не определено).
Анализируемые вещества имеют более высокую аффинность к PVP25, чем к PVP15. Таким образом, эксперименты следующих примеров проводили с PVP25.
Пример 5: Анализ с сочетанием PVP25 и циклодекстрина в качестве понижающего соединения
Результаты показаны на фиг.5 и 6. Применение бета-гидроксипропилциклодекстрина и PVP25 меньше сдвигает равновесие в сторону комплекса лекарства и понижающего соединения, чем применение только PVP25 (см. фиг.6).
Таблица 4: Данные уровней связывания эксципиента, измеренные для варфарина (в том числе результаты из Примеров 2 и 4).
Пример 6: Анализ с PVP25 и человеческим сывороточным альбумином (HSA)
Использовали такие условия анализа, которые описаны в Примере 5, за исключением случая, когда использовали анализируемое соединение карведилол. Результаты показаны на фиг.8 и 9.
Условия ВЭЖХ:
Анализ проводили на системе ВЭЖХ (Agilent 1100). Разделение проводили на колонке RP (Chromolith flash, RP18e, 4,6 x 25 мм). Образцы элюировали градиентом воды с 0,05% муравьиной кислоты (А) и ацетонитрила (В). Условия градиента: начальный 5% В, 0,4 мин 95% В; 1 мин 95% В; 1,1 мин 5% В.
Результаты с анализируемым соединением и PVP показаны на фиг.7, а результаты с анализируемым соединением, PVP25 и HSA показаны на фиг.8 и 9.
Пример 7: Сравнение с литературными данными
Определенные уровни связывания анализируемого соединения в примере 6 («новый подход») сравнивали со значениями, определенными традиционными способами (литературные значения). Результаты приведены в таблице 2 и на фиг.10.
Таблица 5. Уровни связывания анализируемых соединений из литературы и полученные в примере 6.
| название | год | авторы | номер документа |
|---|---|---|---|
| РЕКОМБИНАНТНЫЙ ПОЛИПЕПТИД А2, СЕЛЕКТИВНО СВЯЗЫВАЮЩИЙ HSA, РЕКОМБИНАНТНАЯ ДНК pa2, КОДИРУЮЩАЯ HSA-СВЯЗЫВАЮЩУЮ ЧАСТЬ ПОЛИПЕПТИДА A2, ЕГО ПРОДУЦЕНТ - РЕКОМБИНАНТНЫЙ ШТАММ Escherichia coli M15-A2, СОДЕРЖАЩИЙ РЕКОМБИНАНТНУЮ ПЛАЗМИДНУЮ ДНК pQE 32-pa2, ОБЕСПЕЧИВАЮЩУЮ ПОЛУЧЕНИЕ ПОЛИПЕПТИДА A2 И ПРИМЕНЕНИЕ ПОЛИПЕПТИДА А2 ДЛЯ ДИАГНОСТИКИ МИКРОАЛЬБУМИНУРИИ И ВЫДЕЛЕНИЯ HSA ИЗ СЫВОРОТКИ КРОВИ | 2011 |
|
RU2506271C2 |
| ГИБРИДНЫЕ ВОЙЛОКИ ИЗ НАНОВОЛОКОН, ПОЛУЧЕННЫХ ЭЛЕКТРОПРЯДЕНИЕМ | 2013 |
|
RU2658909C2 |
| Комплексы на основе микропузырьков и способы применения | 2012 |
|
RU2613321C2 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ КОМПЛЕКСЫ ВКЛЮЧЕНИЯ | 2001 |
|
RU2288921C2 |
| СРЕДСТВА И СПОСОБЫ ПОЛУЧЕНИЯ ВЫСОКОАФФИННЫХ АНТИТЕЛ | 2011 |
|
RU2585153C2 |
| МОДИФИЦИРОВАННЫЕ ЦИАНИНОВЫЕ КРАСИТЕЛИ И ИХ КОНЪЮГАТЫ | 2020 |
|
RU2833355C2 |
| Вводимый местным путем фармацевтический агент, способ визуализации посредством его введения и содержащий его набор | 2017 |
|
RU2699571C2 |
| СПОСОБЫ КУЛЬТИВИРОВАНИЯ КЛЕТОК, РАЗМНОЖЕНИЯ И ОЧИСТКИ ВИРУСОВ | 2009 |
|
RU2547587C2 |
| ДИСПЛЕЙ НА ПОВЕРХНОСТИ КЛЕТОК ПОЛИПЕПТИДНЫХ ИЗОФОРМ НА ОСНОВЕ ПРОЧИТЫВАНИЯ ТЕРМИНИРУЮЩЕГО КОДОНА | 2009 |
|
RU2528858C2 |
| ВАРИАНТЫ АЛЬБУМИНА | 2010 |
|
RU2607374C2 |

Изобретение относится к способу определения константы связывания высокоаффинного соединения с белками, включающему следующие этапы: а) добавление высокоаффинного соединения в двухкамерную систему и определение количества высокоаффинного соединения в одной из камер после того, как было достигнуто равновесное распределение, б) добавление понижающего аффинность соединения в одну из камер и определение коэффициента распределения высокоаффинного соединения на понижающем аффинность соединении после того, как было достигнуто равновесное распределение, в) добавление неспецифического белка в другую камеру и определение коэффициента распределения высокоаффинного соединения на неспецифическом белке в присутствии понижающего аффинность соединения после того, как было достигнуто равновесное распределение, и г) определение константы связывания высокоаффинного соединения с коэффициентом распределения из этапов б) и в). Изобретение эффективно в поиске вещества с лучшими физико-химическими свойствами и для понимания взаимосвязи между химической структурой и физико-химическими показателями. 6 з.п. ф-лы, 10 ил., 5 табл., 7 пр.
1. Способ определения константы связывания высокоаффинного соединения, представляющего интерес, с белками, включающий следующие этапы:
а) добавление высокоаффинного соединения, представляющего интерес, в двухкамерную систему, в которой две камеры разделены полупроницаемой мембраной, которая проницаема для высокоаффинного соединения, представляющего интерес, и
определение количества высокоаффинного соединения, представляющего интерес, в одной из камер после того, как было достигнуто равновесное распределение,
б) добавление понижающего аффинность соединения в одну из камер, где понижающее аффинность соединение не может проникать через мембрану, и
определение коэффициента распределения высокоаффинного соединения, представляющего интерес, на понижающем аффинность соединении после того, как было достигнуто равновесное распределение,
в) добавление неспецифического белка (белка, обладающего неселективным связыванием) в другую камеру, где неспецифический белок не может проникать через мембрану, и
определение коэффициента распределения высокоаффинного соединения, представляющего интерес, на неспецифическом белке в присутствии понижающего аффинность соединения после того, как было достигнуто равновесное распределение, и
г) определение константы связывания высокоаффинного соединения, представляющего интерес, с коэффициентом распределения из этапов б) и в).
2. Способ по п. 1, где фильтр является селективной по размеру мембраной.
3. Способ по п. 1, где понижающее аффинность соединение представляет собой PVP или циклодекстрин.
4. Способ по п. 1, где понижающее аффинность соединение представляет собой PVP 25.
5. Способ по п. 1, где неспецифический белок является белком плазмы.
6. Способ по п. 5, где белок плазмы представляет собой сывороточный альбумин.
7. Способ по любому из пп. 1-6, где этапы а), б) и в) выполняются параллельно.
| KRATOCHWIL N | |||
| A | |||
| et al: Predicting plasma protein binding of drugs: a new approach | |||
| Biochemical pharmacology, Pergamon, Oxford, GB, vol | |||
| Нефтяной конвертер | 1922 |
|
SU64A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| КОМБИНИРОВАННЫЙ С ВОЗДУШНЫМ КЛАПАНОМ НАСОС ДЛЯ ГОРЮЧЕЙ ЖИДКОСТИ | 1923 |
|
SU1355A1 |
| US2007215538 A1, 20.09.2007 | |||
| US2003213740 A1, 20.11.2003 | |||
| THORSTEINN LOFTSSON et al: Role of cyclodextrins in improving oral drug delivery | |||
| American Journal of Drug | |||
Авторы
Даты
2016-01-20—Публикация
2011-02-22—Подача