Изобретение относится к технологии переработки облученного ядерного топлива.
Щавелевая кислота используется для осаждения плутония в виде оксалата Pu (IV) из реэкстракта аффинажного отделения с целью последующего прокаливания и получения товарного продукта - диоксида плутония. Осаждение оксалата Pu (IV) проводят из 3 моль/л азотнокислого раствора введением стехиометрического к плутонию IV) количества щавелевой кислоты, плюс избыток ~0,2 моль/л H2C2O4. Маточные растворы после отделения оксалата плутония не являются сбросными. Они могут содержать до 100 мг/л и более Pu (IV) и направляются в «голову» экстракционного процесса для доизвлечения плутония. Однако присутствие в оборотном растворе избытка щавелевой кислоты препятствует полному извлечению плутония в органическую фазу из-за резкого снижения коэффициента распределения Pu (IV) вследствие комплексообразования с оксалат-ионами. В связи с этим появляется необходимость удаления избыточной щавелевой кислоты из маточного раствора перед его направлением в аппарат экстракции.
Известен способ разложения щавелевой кислоты действием сильных окислителей, таких как К2МnO4 [К.М. Harmon et al. // Reactor handbook/. V. 11, 2nd ed. New York: Intersci. Publ., 1961, p. 455], K2Cr2O7, O3 [J.L. Jenkins, N.J. Keen, A.G. Wain // Extractive and physical metallurgy of plutonium and its alloys / New York: Intersci. Publ., 1960, p. 25].
[Г.Н. Фрейдлин, Л.А. Голубков, Л.Г. Романова // ЖПХ. 1972, т. 45, №9, с. 219].
К недостаткам способа относятся - загрязнение перерабатываемых растворов посторонними примесями; при использовании озона требуется специальное оборудование для его генерирования.
Известен способ разложения щавелевой кислоты в растворах HNO3, включающий упаривание растворов до высоких концентраций азотной кислоты, при этом происходит постепенное разложение Н2С2О4 [J.L. Jenkins, N.J. Keen, A.G. Wain // Extractive and physical metallurgy of plutonium and its alloys/ New York: Intersci. Publ., 1960, p. 25].
К недостаткам способа относится то, что процесс прямого окисления Н2С2О4 нитрат-ионами протекает слишком медленно [[Г.Н. Фрейдлин, Л.А. Голубков, Л.Г. Романова // ЖПХ. 1972, т. 45, №9, с. 219] и его использование в технологии не целесообразно.
Известен способ взаимодействия H2C2O4 и ΗΝO3 при нагревании растворов в присутствии солей ванадия(II) [Г.Н. Фрейдлин, Л.А. Голубков, Л.Г. Романова // ЖПХ. 1972, т. 45, №9, с. 219], марганца(II) [K.М. Harmon et al. // Reactor handbook . V. 11, 2nd ed. New York: Intersci. Publ., 1961, p. 455], или палладия (II) [В.С. Колтунов // Кинетика и катализ. 1968, т. 9, №5, с. 1034], которые выступают в качестве гомогенных катализаторов реакции окисления Н2С2О4 азотной кислотой. При этом достигается полное разложение щавелевой кислоты. К недостаткам способа относятся - загрязнение перерабатываемых растворов каталитическими примесями.
Известен способ разложения H2C2O4 из азотнокислых растворов на твердофазных катализаторах. В качестве таковых были изучены различные марки активных углей, платина на силикагеле и на анионитах АВ-17 и ВП-3Ап [Н.Н. Крот, В.П. Шилов, В.И. Дзюбенко, В.А. Матюха, Н.Н. Малкова. Разложение Н2С2О4 на твердофазных катализаторах в растворах HNO3. // Радиохимия, 1994, т. 36, №1, с. 19-24],
[Н.Н. Крот, В.П. Шилов, В.И. Дзюбенко, В.А. Матюха, В.П. Стародумов, Н.Н. Малкова. Разложение H2C2O4 на твердофазных катализаторах в азотнокислых растворах в присутствии гидразина. // Радиохимия, 1995, т. 37, №1, с. 23-28], [Н.Н. Крот, В.П. Шилов, В.И. Дзюбенко, В.А. Матюха, В.П. Стародумов, Н.Н. Малкова. Стехиометрия и механизм разложения H2C2O4 на твердофазных катализаторах в растворах ΗΝO3. // Радиохимия, 1994, т. 36, №5, с. 426-428].
Если процесс осуществляют в статических условиях при перемешивании растворов с катализатором в реакционной ячейке, то происходит истирание и дробление основы (силикагеля, угля и сорбента), что является недостатком способа [Н.Н. Крот, В.П. Шилов, В.И. Дзюбенко, В.А. Матюха, Н.Н. Малкова. Разложение H2C2O4 на твердофазных катализаторах в растворах ΗΝO3. // Радиохимия, 1994, т. 36, №1, с 19-24].
Известен способ разложения H2C2O4 из азотнокислых растворов на рутениевом катализаторе 5% Ru/SiO2 [М.С. Тюменцев. Окислительно-восстановительные реакции актиноидов, гидразина и щавелевой кислоты в водных средах в присутствии рутениевых и платино-рутениевых катализаторов. Автореферат диссертации на соискание ученой степени кандидата химических наук. Москва, 2013]. При этом скорость процесса в сопоставимых экспериментальных условиях оказывается почти в 50 раз ниже, чем скорость разложения H2C2O4 в присутствии катализатора 1% Pt/SiO2.
Наиболее близким является способ разложения H2C2O4 из азотнокислых растворов на биметаллическом платино-рутениевом катализаторе в статических условиях [М.С. Тюменцев. Окислительно-восстановительные реакции актиноидов, гидразина и щавелевой кислоты в водных средах в присутствии рутениевых и платино-рутениевых катализаторов. Автореферат диссертации на соискание ученой степени кандидата химических наук. Москва, 2013].
Техническим результатом предлагаемого способа разложения щавелевой кислоты из азотнокислых растворов на биметаллическом платино-рутениевом катализаторе в динамических условиях является следующее:
- ускорение скорости реакции разложения щавелевой кислоты;
- увеличение степени разложения щавелевой кислоты в динамических условиях по сравнению со статическими условиями;
- снижение в 2 раза расхода платины на приготовление катализатора без потери его каталитической активности.
Технический результат достигается тем, что разложение Н2С2О4 в азотной кислоте на биметаллических Pt-Ru катализаторах ведут в динамических условиях при соотношении платины к рутению (0,4-0,5):(0,6-0,5). Исходный раствор подают в сорбционную колонку, заполненную биметаллическим платино-рутениевым катализатором, снизу вверх. Разложение щавелевой кислоты проходит в колонке на катализаторе с выделением газообразных продуктов, а очищенный раствор свободно перетекает в приемную емкость.
Процесс разложения щавелевой кислоты ведут при температуре исходного раствора 60-80°С. При этом степень превращения достигает 100%.
В присутствии наиболее активного для данной реакции катализатора, содержащего в металлической фазе 40% ат. Pt, константа скорости разложения Н2С2О4 в динамических условиях превышает константу скорости этой реакции на том же катализаторе в статических условиях более чем в два раза. Был обнаружен мощный синергетический эффект между Pt и Ru, состоящий в резком увеличении активности данных катализаторов относительно монометаллических при достижении определенного соотношения Pt/Ru.
Пример 1.
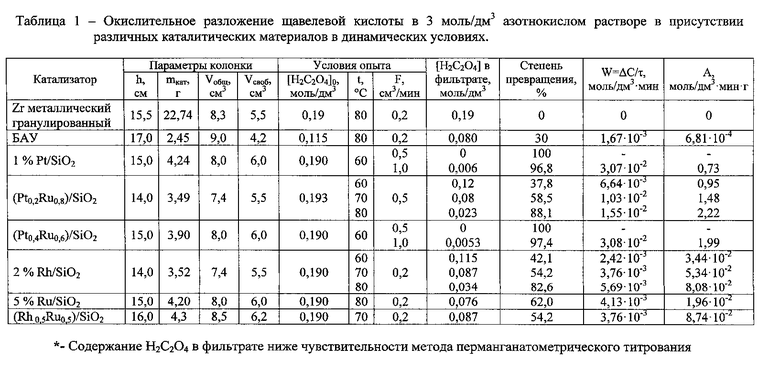
Проведены исследования по сравнительному изучению каталитической активности различных материалов (катализатор 1% Pt/SiO2, свойства которого известны, был выбран в качестве эталона) по отношению к реакции окислительной деструкции щавелевой кислоты в 3 моль/дм3 HNO3 в динамических условиях. Результаты представлены в таблице 1.
Анализ результатов, представленных в таблице 1, показывает, что металлический цирконий в виде «крупки» не катализирует реакцию разложения щавелевой кислоты в азотнокислом растворе. Каталитическое действие активированного угля БАУ становится заметным только при высокой температуре (80°С) и большом времени контакта жидкой фазы с материалом катализатора. При этом удельная массовая активность БАУ более чем на три порядка ниже, чем активность 1% Pt/SiO2.
Наиболее эффективным каталитическими материалами для разложения щавелевой кислоты в азотнокислом растворе оказались биметаллические платино-рутениевые катализаторы. Максимальную эффективность разложения щавелевой кислоты в динамических условиях показал катализатор (Pt0,4Ru0,6)/SiO2. Его удельная активность, в пересчете на 1 г платины, более чем в 2 раза превышает удельную каталитическую активность монометаллического платинового катализатора при одинаковых условиях эксперимента.
Пример 2.
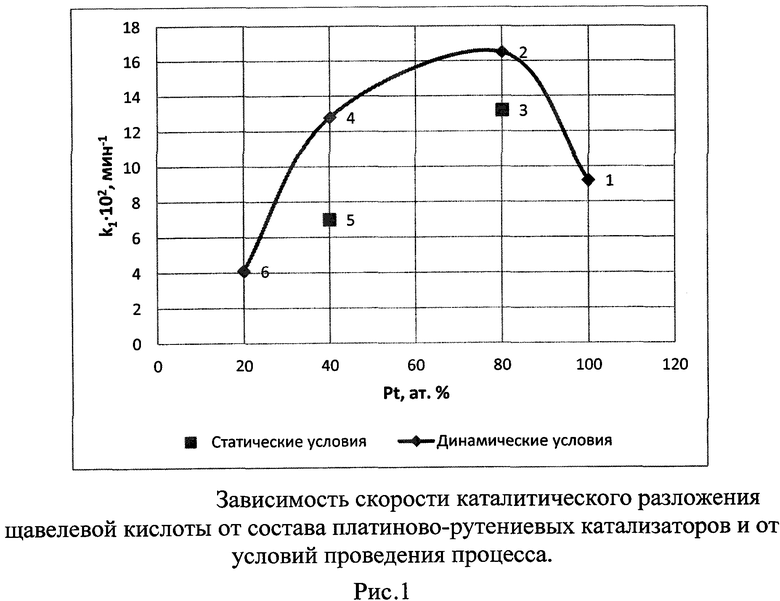
Проведены исследования в статических и в динамических условиях в присутствии биметаллических Pt-Ru катализаторов с различным атомным отношением Pt/Ru по определению константы скорости реакции первого порядка, как функции процентного содержания (атомные %) платины в биметаллическом композите. Результаты опыта представлены на рисунке 1. Рисунок 1 - Зависимость скорости каталитического разложения щавелевой кислоты от состава платиново-рутениевых катализаторов и от условий проведения процесса
[H2C2O4]=0,32 моль/дм3; [ΗΝO3]=2,5 моль/дм3; t=60°С
1 - Pt/SiO2; 2 - (Pt0,8Ru0,2)/SiO2; 3 - (Pt0,4Ru0,6)/SiO2;
4 - (Pt0,4Ru0,6)/SiO2; 5 - (Pt0,4Ru0,6)/SiO2; 6 - (Pt0,2Ru0,8)/SiO2.
Из данных, редставленных на рисунке 1, идно, что при содержании платины в биметаллическом катализаторе 40 атомных процентов, скорость реакции разложения щавелевой кислоты в динамических условиях выше в два раза, чем при осуществлении процесса в статических условиях. Применение катализатора (Pt0,4Ru0,6)/SiO2 позволяет более чем в 2 раза сократить расход платины на приготовление катализатора для разложения щавелевой кислоты без потери его каталитической активности.
Пример 3
Проведены исследования по изучению влияния температуры и скорости подачи исходного раствора на разложение щавелевой кислоты для катализатора (Pt0,4Ru0,6)/SiO2 в динамических условиях. Результаты представлены в таблице 2.
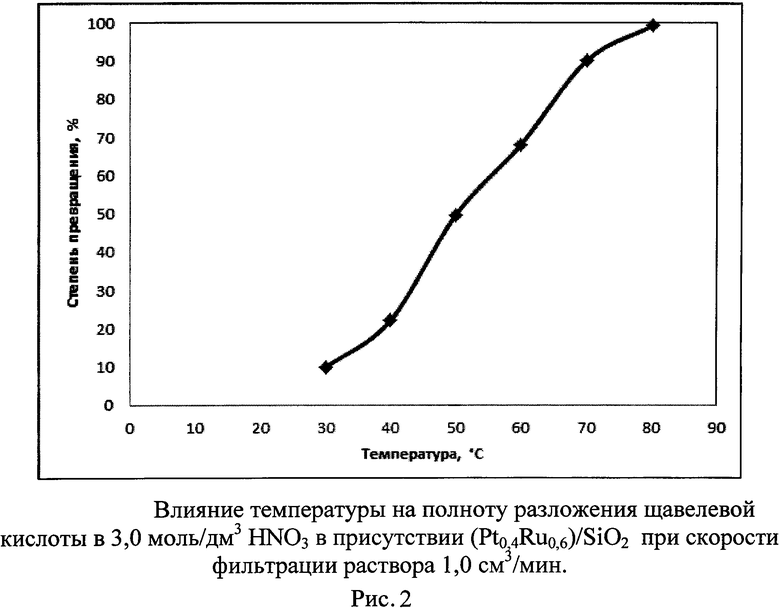
На рисунке 2 показано влияние температуры на полноту разложения щавелевой кислоты в 3,0 моль/дм3 ΗΝO3 в присутствии (Pt0,4Ru0,6)/SiO2 при скорости фильтрации раствора 1,0 см /мин.
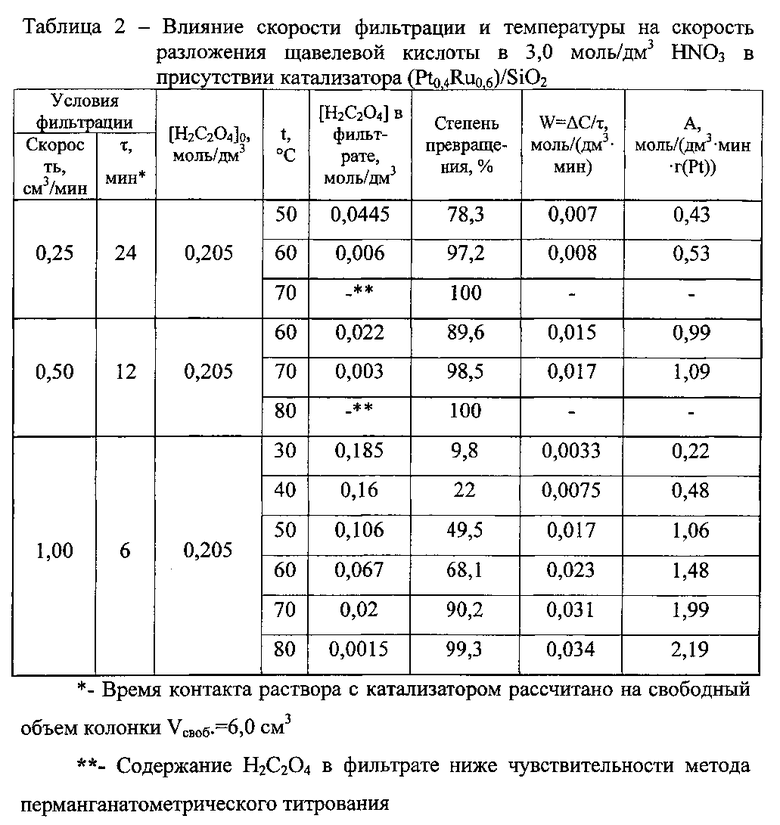
Как видно из полученных данных повышение температуры приводит к увеличению скорости разложения щавелевой кислоты, в то время как повышение скорости подачи исходного раствора в колонку не оказывает значительного влияния на степень разложения.
Пример 4
Проведены исследования по изучению влияния концентрации азотной кислоты в исходном растворе на разложение щавелевой кислоты для катализатора (Pt0,4Ru0,6)/SiO2 в динамических условиях. Результаты представлены в таблице 3.
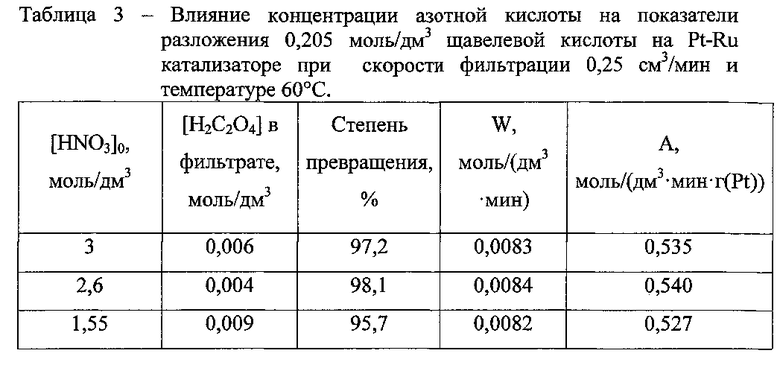
Изменение концентрации азотной кислоты в интервале 2,5-3 моль/дм3 практически не сказывается на скорости каталитического разложения Н2С2О4 (таблица 3).
В процессе работы через колонку с катализатором было пропущено около литра рабочего раствора, что составляет более 150 свободных колоночных объемов. При этом снижения каталитической активности в отношении реакции разложения щавелевой кислоты не отмечено. Механической деградации катализатора также визуально не наблюдалось.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ СМЕШАННЫХ ОКСИДОВ УРАНА И ПЛУТОНИЯ | 2015 |
|
RU2626854C2 |
| СПОСОБ РАЗЛОЖЕНИЯ НИТРАТА АММОНИЯ В ТЕХНОЛОГИЧЕСКИХ РАСТВОРАХ РАДИОХИМИЧЕСКОГО ПРОИЗВОДСТВА | 2016 |
|
RU2607646C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ БИМЕТАЛЛИЧЕСКОГО КАТАЛИЗАТОРА ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ ПРОЦЕССОВ В АЗОТНОКИСЛЫХ СРЕДАХ | 2015 |
|
RU2598944C1 |
| СПОСОБ УТИЛИЗАЦИИ ОКСАЛАТНЫХ МАТОЧНЫХ РАСТВОРОВ ТРАНСУРАНОВЫХ ЭЛЕМЕНТОВ | 1996 |
|
RU2111562C1 |
| СПОСОБ ПОДГОТОВКИ РАСТВОРОВ ПЕРЕРАБОТКИ ОЯТ, СОДЕРЖАЩИХ КОМПЛЕКСООБРАЗУЮЩИЕ ВЕЩЕСТВА, ДЛЯ ЭКСТРАКЦИОННОГО ИЗВЛЕЧЕНИЯ МНОГОВАЛЕНТНЫХ АКТИНИДОВ | 2011 |
|
RU2490735C2 |
| СПОСОБ КАТАЛИТИЧЕСКОЙ ДЕНИТРАЦИИ ЖИДКИХ РАДИОАКТИВНЫХ ОТХОДОВ | 2015 |
|
RU2593163C1 |
| СПОСОБ ГЕТЕРОГЕННОГО КАТАЛИТИЧЕСКОГО РАЗЛОЖЕНИЯ КОМПЛЕКСОНОВ И ПОВЕРХНОСТНО-АКТИВНЫХ ВЕЩЕСТВ В ТЕХНОЛОГИЧЕСКИХ РАСТВОРАХ РАДИОХИМИЧЕСКИХ ПРОИЗВОДСТВ НА НИКЕЛЬ-ФЕРРИЦИАНИДНОМ КАТАЛИЗАТОРЕ | 2014 |
|
RU2569374C1 |
| СПОСОБ ГЕТЕРОГЕННОГО КАТАЛИТИЧЕСКОГО РАЗЛОЖЕНИЯ ОКСАЛАТ-ИОНОВ, КОМПЛЕКСОНОВ И ПОВЕРХНОСТНО-АКТИВНЫХ ВЕЩЕСТВ В ТЕХНОЛОГИЧЕСКИХ РАСТВОРАХ РАДИОХИМИЧЕСКИХ ПРОИЗВОДСТВ | 2014 |
|
RU2553266C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ МЕТАЛЛОВ ПЛАТИНОВОЙ ГРУППЫ ИЗ ОСАДКОВ ПОСЛЕ ОСВЕТЛЕНИЯ ПРОДУКТА КИСЛОТНОГО РАСТВОРЕНИЯ ВОЛОКСИДИРОВАННОГО ОТРАБОТАВШЕГО ЯДЕРНОГО ТОПЛИВА | 2016 |
|
RU2632498C2 |
| СПОСОБ ЭЛЕКТРОХИМИЧЕСКОГО ВЫДЕЛЕНИЯ ПАЛЛАДИЯ ИЗ АЗОТНОКИСЛЫХ РАСТВОРОВ | 2002 |
|
RU2235374C2 |
Изобретение относится к способу разложения щавелевой кислоты из азотнокислых маточных растворов на биметаллическом платино-рутениевом катализаторе. Процесс ведут в динамических условиях в сорбционной колонке, заполненной биметаллическим платино-рутениевым катализатором при соотношении платины к рутению (0,4-0,5):(0,6-0,5). При этом исходный раствор подают в колонку снизу вверх, разложение щавелевой кислоты проходит в колонке с выделением газообразных продуктов, а очищенный раствор свободно перетекает в приемную емкость. Предлагаемый способ позволяет повысить скорость разложения щавелевой кислоты и увеличить степень ее разложения в динамических условиях по сравнению со статическими условиями. 1 з.п. ф-лы, 2 ил., 3 табл., 4 пр.
1. Способ разложения щавелевой кислоты из азотнокислых маточных растворов на биметаллическом платино-рутениевом катализаторе, отличающийся тем, что процесс ведут в динамических условиях в сорбционной колонке, заполненной биметаллическим платино-рутениевым катализатором при соотношении платины к рутению (0,4-0,5):(0,6-0,5), при этом исходный раствор подают в колонку снизу вверх, разложение щавелевой кислоты проходит в колонке с выделением газообразных продуктов, а очищенный раствор свободно перетекает в приемную емкость.
2. Способ по п.1, отличающийся тем, что в динамических условиях процесс разложения щавелевой кислоты ведут при температуре исходного раствора 60-80°C.
| ТЮМЕНЦЕВ М.С., Окислительно-восстановительные реакции актинидов, гидразина и щавелевой кислоты в водных средах в присутствии рутениевых и платино-рутениевых катализаторов, Автореферат диссертации на соискание ученой степени кандидата наук, Москва, 2013 | |||
| КРОТ Н.Н | |||
| И ДР., Разложение HCOв азотнокислых растворах в |
Авторы
Даты
2016-02-10—Публикация
2014-10-28—Подача