Настоящее изобретение касается способа получения этиленово-ненасыщенного гликозида путем реакции этиленово-ненасыщенного спирта с сахаридом в присутствии гликозидазы.
Полимеры, содержащие остатки сахаров (сахаридные сополимеры), могут обладать типичными свойствами сахаридов, такими как хорошая растворимость в воде, высокая устойчивость к электролитам, коллоидная стабильность в горячей воде, сильные взаимодействия с такими субстратами, как хлопок, и отсутствие токсичности. Перечисленные специфические свойства открывают широкие возможности для применения таких полимеров. Поэтому вызывает большой интерес возможность разработки экономически эффективных методов получения определенных сахаридных сополимеров и соответствующих мономеров. Такие мономеры могут представлять собой полимеризуемые, этиленово-ненасыщенные гликозиды, получаемые при гликозидном сочетании сахарида и этиленово-ненасыщенного спирта. Синтез таких гликозидов сталкивается с рядом трудностей. Возможно образование множества изомеров положения, в которых разные гидроксильные группы сахарида участвуют в образовании связи. Кроме того, потенциально возможно образование различных аномерных форм. Поэтому химический синтез большинства мономеров, содержащих остатки сахаров, в целом неосуществим и дает низкие выходы целевого мономера.
Применение ферментов рассматривалось как альтернативный подход к получению гликозидных мономеров. В отличие от химического синтеза, катализируемые ферментами реакции незащищенных сахаров обычно дают намного более гомогенный по структуре продукт, благодаря их высокой стереоселективности.
В целом, применяются два подхода к ферментативному синтезу гликозидов: термодинамически контролируемый обратный гидролиз и кинетически контролируемое трансгликозилирование. Перенос гликозильных фрагментов на несахарные соединения с первичными гидроксильными группами посредством трансгликозилирования, катализируемого ферментами, был показан, например, в публикации S. Matsumura et al. (Makromol. Chem., Rapid Commun. 14: 55-58, 1993). Также применялись подходы с применением гликозидаз, которые катализируют гидролиз гликозидов in vivo, для синтеза гликозидов путем обратного гидролиза (см., например, I. Gill and R. Valivety, Angew. Chem. Int. Ed. 39(21): 3804-3808, 2000).
При разработке методов синтеза гликозидов, катализируемого гликозидазами, возникли трудности с подбором оптимального растворителя. С одной стороны, для способствования термодинамически контролируемому обратному гидролизу необходимо минимизировать содержание воды, или точнее даже термодинамическую активность воды aw. С другой стороны, сахариды, которые обычно легко растворимы в воде, часто плохо растворяются в органических средах. Была предложена замена воды на безводные растворители средней полярности как способ удовлетворения обеих потребностей. Однако было показано, что обычно применяемым гликозидазам требуется хотя бы небольшое количество воды для сохранения активности. (F. van Rantwijk et al., J. Mol. Catalysis В: Enzymatic 6: 511-532, 1999). Такие противоречивые требования к растворителю сложно удовлетворить. Это выражается в повышенных температурах и большом времени реакций, которые обычно требуются для известных методов ферментативного синтеза гликозидов.
Поэтому целью настоящего изобретения была разработка более эффективного способа ферментативного получения этиленово-ненасыщенных гликозидов. Ее можно достичь путем увеличения скорости реакции и/или путем смещения равновесия реакции в сторону синтеза гликозида. Таким образом, образуется большее количество продукта после определенного времени протекания реакции и/или при установлении равновесия.
Авторы настоящего изобретения неожиданно обнаружили, что добавление смешивающегося с водой растворителя, не вступающего в реакцию, в реакционную смесь, содержащую сахарид, этиленово-ненасыщенный спирт, гликозидазу и воду, может значительно увеличить количество этиленово-ненасыщенного гликозида, образующегося по истечении определенного времени реакции.
Таким образом, в настоящем изобретении описан способ получения этиленово-ненасыщенного гликозида формулы I
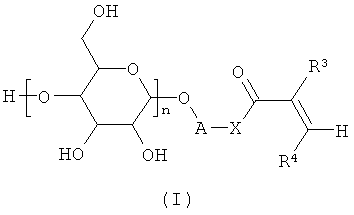
где
n равно 1, 2 или 3;
А представляет собой C2-20 алкилен или -R6-O-[-R6-O-]x-C2-20 алкилен;
Х выбран из группы, состоящей из -O-, -NH- и -NR5-;
BR3 выбран из группы, состоящей из -Н и C1-10 алкила;
R4 выбран из группы, состоящей из -H, -COOH и -COO- M+;
R5 представляет собой C1-10 алкил;
R6 представляет собой Н или -CH3;
M+ выбран из группы, состоящей из Li+, Na+, K+ и 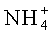
x представляет собой целое число от 0 до 200;
включающий реакцию этиленово-ненасыщенного спирта формулы II
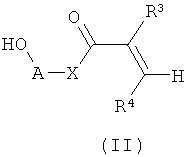
с сахаридом формулы III
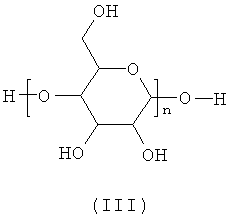 ,
,
в присутствии гликозидазы
(i) при начальном молярном соотношении этиленово-ненасыщенного спирта формулы II к сахариду формулы III от 2:1 до 30:1, например от 15:1 до 25:1;
(ii) в присутствии смеси растворителей, состоящей из воды и смешивающегося с водой органического растворителя, который не является первичным или вторичным спиртом, при весовом соотношении воды и органического растворителя от 0,1:1 до 9:1, например от 1:1 до 3:1; и
(iii) при начальном весовом соотношении смеси растворителей к сахариду от 3:1 до 30:1, например от 10:1 до 20:1.
Определения
Термин "моносахарид" при использовании в настоящем тексте относится к отдельному фрагменту полигидроксиальдегида, формирующему внутримолекулярный полуацеталь, структура которого включает шестичленный цикл из пяти атомов углерода и одного атома кислорода. Моносахариды могут присутствовать в разных диастереомерных формах, таких как α или β аномеры, и D или L изомеры. "Олигосахарид" состоит из коротких цепочек ковалентно связанных моносахаридных фрагментов. Олигосахариды включают дисахариды, которые содержат два моносахаридных фрагмента, а также трисахариды, которые содержат три моносахаридных фрагмента. «Полисахарид» состоит из длинных цепочек ковалентно связанных моносахаридных фрагментов.
Термин «гликозидная связь» или «гликозидный мостик» означает тип химической связи или мостика, образующегося между аномерной гидроксильной группой сахарида или производного сахарида (гликона) и гидроксильной группой другого сахарида или несахаридного органического соединения (агликона), такого как спирт.Восстанавливающий конец ди- или полисахарида направлен в сторону последнего аномерного атома углерода в структуре, а терминальный конец находится в противоположном направлении.
«Ферментативно катализируемый» или «биокаталитический» метод при использовании в настоящем тексте означает, что указанный метод осуществляется в условиях каталитического действия фермента, в частности гликозидазы. Данный метод может осуществляться в присутствии указанной гликозидазы в выделенной (очищенной, обогащенной) или неочищенной форме. Термин «гликозидаза» также включает варианты, мутанты и ферментативно активные фрагменты гликозидаз.
Каталитические количества фермента выражаются в "U" («единицах»), где 1 U равняется количеству фермента, который катализирует реакцию 1 мкмоль субстрата в минуту в специфических условиях (обычно 37°C и рН 7,5). Так, 10 U гликозидазы равняется каталитическому количеству фермента, необходимому для реакции 10 мкмоль сахаридного субстрата в минуту. Каталитические количества мальтогенной амилазы можно выражать в "MANU" (Maltogenic Amylase Novo Unit), где 1 MANU равно каталитическому количеству фермента, необходимому для реакции 1 мкмоль мальтотриозы в минуту в стандартных условиях (10 мг/мл мальтотриозы, 37°C, рН 5,0, время реакции 30 мин). Каталитическое количество фермента можно определить хорошо известными способами.
Термин «алкил» охватывает C1-10 алкильные радикалы, линейные или разветвленные, которые содержат от 1 до 10 атомов углерода. Их примерами являются метил, этил, н-пропил, изопропил, н-бутил, 2-бутил, изобутил или трет-бутил, пентил, 1-метилбутил, 2-метилбутил, 3-метилбутил, 2,2-диметилпропил, 1-этилпропил, гексил, 1,1-диметилпропил, 1,2-диметилпропил, 1-метилпентил, 2-метилпентил, 3-метилпентил, 4-метилпентил, 1,1-диметилбутил, 1,2-диметилбутил, 1,3-диметилбутил, 2,2-диметилбутил, 2,3-диметилбутил, 3,3-диметилбутил, 1-этилбутил, 2-этилбутил, 1,1,2-триметилпропил, 1,2,2-триметилпропил, 1-этил-1-метилпропил, 1-этил-2-метилпропил, гептил, октил, нонил и децил, а также их изомеры положения, такие как 2-этилгексил.
Термин "алкилен" охватывает C2-20 алкиленовые дирадикалы, которые являются линейными или разветвленными дирадикалами, содержащими от 1 до 20 атомов углерода.
Термин "этиленово-ненасыщенный" относится к соединению, содержащему неароматическую двойную связь C=C. В частности, термин "этиленово-ненасыщенный гликозид" при использовании в настоящем тексте означает гликозид, состоящий из сахарида, гликозидно связанного с этиленово-ненасыщенным спиртом.
Под термином "смешивающийся с водой органический растворитель" понимается органический растворитель, формирующий гомогенную смесь с водой при используемом весовом соотношении воды к органическому растворителю.
Органический растворитель не является первичным или вторичным спиртом и, соответственно, не реагирует с сахаридом. В целом, органический растворитель выбран из группы, состоящей из алканонов, алкилнитрилов, третичных спиртов и циклических простых эфиров, и их смесей.
Предпочтительные растворители выбраны из группы, состоящей из ацетона, ацетонитрила, трет-пентанола, трет-бутанола, 1,4-диоксана и тетрагидрофурана, и их смесей. 1,4-Диоксан является особенно предпочтительным.
Этиленово-ненасыщенный спирт формулы II выбран из
гидроксиалкил (мет)акрилатов;
N-гидроксиалкил (мет)акриламидов; или
моно(гидроксиалкиловых) эфиров малеиновой кислоты или их солей.
В других вариантах осуществления изобретения этиленово-ненасыщенный спирт формулы II представляет собой этоксилированное, пропоксилированное или этоксилированное и пропоксилированное производное указанных выше этиленово-ненасыщенных спиртов.
Предпочтительные этиленово-ненасыщенные спирты формулы II выбраны из 2-гидроксиэтил акрилата, 2-гидроксиэтил метакрилата, 3-гидроксипропил акрилата, 3-гидроксипропил метакрилата, N-(2-гидроксиэтил)акриламида, N-(2-гидроксиэтил)метакриламида, N-(3-гидроксипропил)акриламида, N-(3-гидроксипропил)метакриламида, (2-гидроксиэтил)гидромалеата.
В некоторых вариантах осуществления изобретения n равен 1; А представляет собой алкилен с 2-6 атомами углерода; Х представляет собой -O-; и R3 представляет собой -H или -CH3.
Сахарид может представлять собой моносахарид, такой как глюкоза, галактоза или манноза; дисахарид, такой как мальтоза, лактоза или целлобиоза; трисахарид, такой как мальтотриоза; или их смесь. Способ по настоящему изобретению не требует того, чтобы сахарид был активирован, например присутствием алкильной или о-нитрофенильной группы, связанной простоэфирной связью с атомом углерода в положении 1 (C-1) сахарида. Подходящим является сахарид, выбранный из группы, состоящей из D-глюкозы, D-галактозы, D-маннозы и их смесей.
В способе по настоящему изобретению реакция сахарида и этиленово-ненасыщенного спирта катализируется гликозидазой, ферментом, известным также как гликозид гидролаза. В типичном случае, ферменты обладают высокой специфичностью в отношении реакций, которые они катализируют, и к субстратам, которые вступают в данные реакции. Гликозидазы представляют собой ферменты, способные катализировать гидролиз О- и S-гликозидных соединений. Кроме того, гликозидазы могут применяться для катализа образования гликозидных связей посредством обратного гидролиза, в котором положение равновесия в реакции обращено, или трансгликозилирования, при котором гликозидный фрагмент переносится с одного гликозида, т.е. донорного гликозида, к другому гликозиду, т.е. акцепторному гликозиду, с образованием нового гликозида. Гликозидазам присвоен классификационный номер фермента EC 3.2.1.x.
Гликозидазу можно применять в очищенном виде, в виде обогащенного концентрата или в виде неочищенного ферментного препарата.
Таким образом, гликозидаза для способа по настоящему изобретению выбрана из группы, состоящей из амилаз, целлюлаз, глюкозидаз и галактозидаз.
α-Амилаза представляет собой фермент, имеющий классификационный номер фермента ЕС 3.2.1.1, и также известна как гликогеназа, эндоамилаза, така-амилаза А или 1,4-α-D-глюкан глюканогидролаза. α-Амилазы способны катализировать эндогидролиз (1→4)-α-D-глюкозидных связок в полисахаридах, содержащих три или более (1→4)-α-связанных фрагментов D-глюкозы, таких как крахмал и гликоген, таким образом высвобождая восстанавливающие группы в α-конфигурации.
β-Амилаза представляет собой фермент, имеющий классификационный номер фермента ЕС 3.2.1.2, и известна также как сахароген амилаза, гликогеназа или 1,4-α-D-глюкан мальтогидролаза. β-Амилазы способны катализировать гидролиз (1→4)-α-D-глюкозидных связок в полисахаридах, таких как крахмал и гликоген, таким образом высвобождая последовательные фрагменты β-мальтозы с не восстанавливающих концов полисахаридных цепочек.
Целлюлаза представляет собой фермент, имеющий классификационный номер фермента ЕС 3.2.1.4, и известна также как эндо-1,4-β-D-глюканаза, β-1,4-глюканаза, β-1,4-эндоглюкан гидролаза, целлюлаза А, целлюлозин АР, эндоглюканаза D, щелочная целлюлаза, целлюлаза А 3, целлудекстриназа, 9,5 целлюлаза, авицелаза, панцеллаза SS или 1,4-(1,3;1,4)-β-D-глюкан 4-глюканогидролаза. Целлюлазы способны катализировать эндогидролиз (1→4)-β-D-глюкозидных связок в целлюлозе, лихенине и β-D-глюканах зерновых, а также 1,4-связок в β-D-глюканах, содержащих также 1,3-связки.
α-Глюкозидаза представляет собой фермент, имеющий классификационный номер фермента ЕС 3.2.1.20, и известна также как мальтаза, глюкоинвертаза, глюкозидосахараза, мальтаза-глюкоамилаза, α-глюкопиранозидаза, глюкозидоинвертаза, α-D-глюкозидаза, α-глюкозид гидролаза или α-1,4-глюкозидаза. α-Глюкозидазы способны катализировать гидролиз терминальных невосстанавливающих (1→4)-связанных остатков α-D-глюкозы, высвобождая тем самым α-D-глюкозу.
β-Глюкозидаза представляет собой фермент, имеющий классификационный номер фермента ЕС 3.2.1.21, и известна также как гентиобиаза, целлобиаза, эмульсин, элатераза, арил-β-глюкозидаза, β-D-глюкозидаза, β-глюкозид глюкогидролаза, арбутиназа, амигдалиназа, п-нитрофенил β-глюкозидаза, примаверозидаза, амигдалаза, лимараза, салицилиназа или β-1,6-глюкозидаза. β-Глюкозидазы способны катализировать гидролиз терминальных невосстанавливающих β-D-глюкозильных фрагментов, высвобождая тем самым β-D-глюкозу.
α-Галактозидаза представляет собой фермент, имеющий классификационный номер фермента ЕС 3.2.1.22, и известна также как мелибиаза, α-D-галактозидаза, α-галактозидаза А или α-галактозид галактогидролаза. α-Галактозидазы способны катализировать гидролиз терминальных невосстанавливающих фрагментов α-D-галактозы в α-D-галактозидах, включая олигосахариды галактозы и галактоманнаны.
β-Галактозидаза представляет собой фермент, имеющий классификационный номер фермента ЕС 3.2.1.23, и известна также как лактаза, β-лактозидаза, максилакт, гидролакт, β-D-лактозидаза, S 2107, лактозим, трилактаза, β-D-галактаназа, оризатим или сумиклат. β-Галактозидазы способны катализировать гидролиз терминальных невосстанавливающих остатков β-D-галактозы в β-D-галактозидах.
Неочищенной формой глюкозидазы, которая может применяться в способе по настоящему изобретению, является фруктовая жмыховая мука. Фруктовая жмыховая мука представляет собой устойчивый и пригодный для повторного использования катализатор, который можно получать легким и экономически эффективным способом. Получение и специфическая ферментативная активность фруктовой жмыховой муки были описаны в статьях Lu et al. (Practical methods for Biocatalysts, Whittall and Satton (eds.), Wiley, 2010, chapter 7,3, pages 236-239). Фруктовая жмыховая мука, которая может применяться в способе по настоящему изобретению, включает муку косточек Prunus dulcis (миндаль), муку косточек Prunus persica (персик), муку косточек Prunus armeniaca (абрикос), муку семян Malus pumila (яблоко) и муку семян Eriobotrya japonica (японская мушмула). Предпочтительно, применяемая фруктовая жмыховая мука выбрана из группы, состоящей из муки косточек Prunus dulcis, муки косточек Prunus persica и муки семян Malus pumila.
Фермент может быть растворен в реакционной смеси или иммобилизован на твердой подложке, контактирующей с реакционной смесью. Если фермент иммобилизован, это означает, что он закреплен на инертном носителе. Подходящие материалы носителя известны в данной области техники. Примеры подходящих материалов носителя представляют собой глины, глинистые минералы, такие как каолинит, диатомовая земля, перлит, оксид кремния, оксид алюминия, карбонат натрия, карбонат кальция, порошок целлюлозы, анионообменные материалы, синтетические полимеры, такие как полистирол, акриловые смолы, фенолформальдегидные смолы, полиуретаны и полиолефины, такие как полиэтилен и полипропилен. При приготовлении ферментов, связанных с носителем, материал носителя обычно применяется в виде тонко измельченного порошка, где предпочтительной является пористая форма. Размер частиц материала носителя обычно не превышает 5 мм, в частности 2 мм. Кроме того, подходящими материалами носителя являются альгинат кальция и каррагинан. Ферменты могут быть связаны напрямую глутаровым альдегидом. В данной области техники известен широкий набор методов иммобилизации (например, J. Lalonde and A. Margolin "Immobilization of Enzymes" в K. Drauz und H. Waldmann, Enzyme Catalysis in Organic Synthesis 2002, Vol.III, 991-1032, Wiley-VCH, Weinheim).
Реакцию, катализируемую ферментами, можно проводить партиями, полунепрерывным методом или непрерывным методом. Реагенты можно загружать в начале реакции или можно добавлять последовательно, полунепрерывно или непрерывно. Каталитическое количество гликозидазы, необходимое для способа по настоящему изобретению, зависит от условий реакции, таких как температура, растворители и количество субстрата.
Реакцию проводят в смеси растворителей, состоящей из воды и смешивающегося с водой органического растворителя, как описано выше. Реакционная смесь может (необязательно) дополнительно содержать подходящий буферный раствор, для доведения значения рН до значения в интервале от 6,0 до 9,0, например в интервале от 6,5 до 8,0, например в интервале от 7,0 до 7,8. Подходящие буферные системы включают (но не ограничены только ими) ацетат натрия, трис(гидроксиметил)аминометан ("TRIS") и фосфатные буферы.
Концентрацию реагентов, т.е. сахарида и этиленово-ненасыщенного спирта, можно изменять для достижения оптимальных условий реакции. Например, начальная концентрация сахарида может находиться в интервале от 100 мМ до 3000 мМ, например от 200 мМ до 500 мМ. Один реагент, например этиленово-ненасыщенный спирт, используется в молярном избытке для сдвига равновесия реакции в сторону продукта.
Температуру реакции можно регулировать для достижения оптимальных условий реакции, которые могут зависеть от конкретного применяемого фермента. Реакцию рационально проводить при температурах между температурой замерзания реакционной смеси и температурой денатурирования фермента. После достижения температуры денатурирования, каталитическая активность фермента теряется. Например, реакцию можно проводить при температуре в интервале от 0°C до 80°C, например от 40°C до 60°C, или при температуре около 50°C.
Процесс можно проводить до тех пор, пока не установится равновесие между реагентами и продуктами, но можно остановить раньше. Обычное время реакции составляет от 6 ч до 96 ч, например около 24 ч.
Методология настоящего изобретения может дополнительно включать стадию выделения получаемого этиленово-ненасыщенного гликозида. Термин «выделение» включает экстракцию, сбор, извлечение или очистку соединения из реакционной смеси. Выделение соединения можно проводить по любой обычной методике выделения или очистки, известной в данной области техники, включая (но не ограничиваясь только ими) обработку с помощью общеприменимых смол (например, анионо- или катионообменных смол, неионогенных адсорбирующих смол и т.д.), обработку общеприменимыми адсорбентами (например, активированным углем, кремниевой кислотой, силикагелем, целлюлозой, оксидом алюминия и т.д.), изменение рН, экстракцию растворителем (например, общеизвестным растворителем, таким как спирт, этилацетат, гексан и т.п.), перегонку, диализ, фильтрование, концентрирование, кристаллизацию, перекристаллизацию, корректировку значения рН, лиофилизацию и т.п.
Подлинность и чистоту полученного продукта можно определить известными методами, такими как тонкослойная хроматография (ТСХ), высокоэффективная жидкостная хроматография (ВЭЖХ), газовая хроматография (ГХ), спектроскопия (например, ИК, УФ, ЯМР спектроскопия), методы окрашивания, спектроскопия в ближней ИК-области или ферментативные исследования.
Представленные ниже примеры имеют своей целью проиллюстрировать настоящее изобретение, без ограничения его каким-либо образом.
Пример 1. Катализируемый β-глюкозидазой синтез 2-(β-глюкозилокси)-этилакрилата из D-глюкозы.
1,0 г D(+)-глюкозы растворяли в 2 мл воды. В полученный раствор глюкозы добавляли 12 мл 2-гидроксиэтилакрилата (содержащего 200 част./млн пара-метоксифенола) и 1 мл 1,4-диоксана. Реакцию начинали добавлением 0,070 г (364 U) β-глюкозидазы из миндаля. Реакционную смесь перемешивали в течение 24 часов при 50°C. Продукт детектировали методом тонкослойной хроматографии (ТСХ) (хлороформ/метанол 4/1 (об./об.), Rf 0,55) и очищали методом колоночной хроматографии (силикагель, элюент: хлороформ/метанол 7/1 (об./об.)). Фракции, содержащие целевой продукт, объединяли и удаляли растворитель на роторном испарителе. Выход: 0,459 г (46%). Чистота: 99%.
1H-ЯМР δ (м.д.): 3,2-4,2 GlucOCH2CH2R (8H); 4,39 GlucOCH2CH2R (2H, т, J 4,38 и 4,38 Гц); 4,50 GlucHα, (1H, д, J 7,91 Гц); 5,99 HтрансCH=CHR (1H, д, J 10,46 Гц); 6,22 CH2=CHR (1H, дд, J 17,29 и 10,46 Гц); 6,46 HцисCH=CHR (1H, A,J 17,30 Гц).
13C-ЯМР δ (м.д.): 60,9 GlucC6; 64,4 OCH2CH2; 68,1 OCH2CH2; 69,8 GlucC5; 73,3 GlucC2; 75,9 GlucC3; 76,1 GlucC4; 102,7 GlucC1β; 127,6 H2C=CHR; 132,9 H2C=CHR; 168,6 O(O)CR.
ESI-MS (полож.): вычислено: 301,0894 (C11H18O8Na); найдено: 301,2500.
Пример 2: Катализируемый β-глюкозидазой синтез 2-(β-глюкозилокси)-этилметакрилата из D-глюкозы.
1,0 г D(+)-глюкозы растворяли в 2 мл воды. В полученный раствор глюкозы добавляли 12 мл 2-гидроксиэтилметакрилата (содержащего 200 м.д. пара-метоксифенола) и 1 мл 1,4-диоксана. Реакцию начинали добавлением 0,070 г (364 U) β-глюкозидазы из миндаля. Реакционную смесь перемешивали в течение 24 часов при 50°C. Продукт детектировали методом ТСХ (хлороформ/метанол 4/1 (об./об.), Rf 0,59) и очищали методом колоночной хроматографии (силикагель, элюент: хлороформ/метанол 7/1 (об./об.)). Фракции, содержащие целевой продукт, объединяли и удаляли растворитель на роторном испарителе. Выход: 0,514 г (51%). Чистота: 97%.
1H-ЯМР δ (м.д.): 1,91 CH2=C(CH3)R (3H, с); 3,2-4,2 GlucOCH2CH2R (8H); 4,35 GlucOCH2CH2R (2H, т, J 4,37 и 4,37 Гц); 4,48 GlucHα (1H, д, J 7,92 Гц); 5,70 HтрансCH=CCH3R (1H, с); 6,14 HцисCH=CHCH3R (1H, с).
13C-ЯМР δ (м.д.): 17,5 H2C=C(CH3)R; 60,8 GlucC6; 64,5 OCH2CH2; 68,1 OCH2CH2; 69,7 GlucC5; 73,2 GlucC2; 75,8 GlucC3; 76,1 GlucC4; 102,7 GlucC1β; 127,1 H2C=C(CH3)R; 135,9 H2C=C(CH3)R; 169,8 O(O)CR.
Пример 3: Катализируемый β-глюкозидазой синтез 4-(β-глюкозилокси)-бутилакриалата из D-глюкозы.
1,0 г D(+)-глюкозы растворяли в 2 мл воды. В полученный раствор глюкозы добавляли 12 мл 4-гидроксибутилакрилата (содержащего 200 м.д. пара-метоксифенола) и 1 мл 1,4-диоксана. Реакцию начинали добавлением 0,070 г (364 U) β-глюкозидазы из миндаля. Реакционную смесь перемешивали в течение 24 часов при 50°C. Продукт детектировали методом ТСХ (хлороформ/метанол 4/1 (об/об), Rf 0,69) и очищали методом колоночной хроматографии (силикагель, элюент: хлороформ/метанол 7/1 (об/об)). Фракции, содержащие целевой продукт, объединяли, и удаляли растворитель на роторном испарителе. Выход: 0,310 г (31%). Чистота >85%.
1H-ЯМР δ (м.д.): 1,75 OCH2CH2CH2CH2O (4H); 3,2-4,2 GlucOCH2CH2R (8H); 4,21 (O)COCH2R (2H, т, J 5,90 и 5,90 Гц); 4,43 GlucHα (1H, д, J 7,96 Гц); 5,95 HтрансCH=CHR (1H, д, J 10,43 Гц); 6,22 CH2=CHR (1H, дд, J 17,36 и 10,35 Гц); 6,41 HцисCH=CHR (1H, д, J 17,32 Гц).
13C-ЯМР δ (м.д.): 24,7 OCH2CH2CH2CH2O; 25,6 OCH2CH2CH2CH2O; 61,0 GlucC6; 61,7 OCH2R; 65,4 (O)COCH2R; 69,9 GlucC5; 73,3 GlucC2; 76,0 GlucC3; 76,1 GlucC4; 102,4 GlucC1β; 127,9 H2C=CHR; 132,4 H2C=CHR; 168,9 RO(O)CR.
ESI-MS (полож.): вычислено: 329,1207 (C13H22O8Na); найдено: 329,1188.
Изобретение относится к области биотехнологии. Предложен способ получения этиленово-ненасыщенного гликозида формулы I

где n, A, X, R3 и R4 имеют значения, приведенные в формуле. Гликозид формулы I получают реакцией этиленово-ненасыщенного спирта формулы II
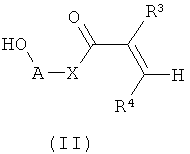
с сахаридом формулы III

в присутствии β-глюкозидазы. При этом молярное соотношение этиленово-ненасыщенного спирта формулы II к сахариду формулы III составляет от 2:1 до 30:1. Реакцию проводят в присутствии смеси растворителей, состоящей из воды и 1,4-диоксана. Весовое соотношение воды и 1,4-диоксана составляет от 0,1:1 до 9:1. Весовое соотношение смеси растворителей к сахариду составляет от 3:1 до 30:1. Изобретение позволяет увеличить выход этиленово-ненасыщенного гликозида после определенного времени протекания реакции и/или при установлении равновесия. 2 з.п. ф-лы, 3 пр.
1. Способ получения этиленово-ненасыщенного гликозида формулы I
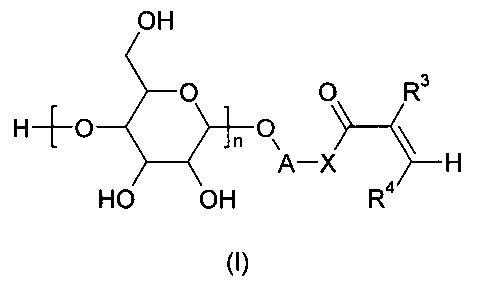
где
n равно 1, 2 или 3;
А представляет собой С2-20 алкилен или R6-O-[R6-O-]х-С2-20 алкилен;
X выбран из группы, состоящей из -О-, -NH- и -NR5-;
R3 выбран из группы, состоящей из -Н и С1-10 алкила;
R4 выбран из группы, состоящей из -Н, -СООН и -СОО- М+;
R5 представляет собой С1-10 алкил;
R6 представляет собой -С2Н4- или -С3Н6-;
М+ выбран из группы, состоящей из Li+, Na+, К+ и NH4 +; и
x представляет собой целое число от 0 до 200;
включающий реакцию этиленово-ненасыщенного спирта формулы II
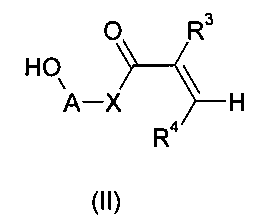
с сахаридом формулы III
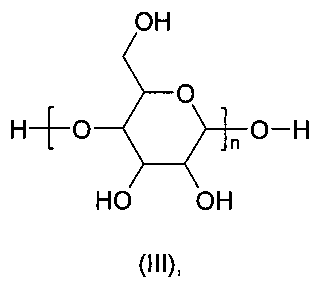
в присутствии β-глюкозидазы
(i) при молярном соотношении этиленово-ненасыщенного спирта формулы II к сахариду формулы III от 2:1 до 30:1;
(ii) в присутствии смеси растворителей, состоящей из воды и 1,4-диоксана, при весовом соотношении воды и 1,4-диоксана от 0,1:1 до 9:1; и
(iii) при весовом соотношении смеси растворителей к сахариду от 3:1 до 30:1.
2. Способ по п.1, в котором
А представляет собой С2-6 алкилен;
X представляет собой -О-; и
R3 представляет собой -Н или -СН3.
3. Способ по п.1, в котором сахарид выбран из группы, состоящей из D-глюкозы, D-галактозы, D-маннозы и их смесей.
| СУДОПОДЪЕМНИК | 0 |
|
SU394496A1 |
| EP 226563 A, 24.06.1987 | |||
| GILL I., VALIVETY R | |||
| "Enzymatic Glycosylation in Plasticized Glass Phases: A Novel and Efficient Route to O-Glycosides", Angewandte chemie | |||
| international edition, vol | |||
| Машина для изготовления проволочных гвоздей | 1922 |
|
SU39A1 |
| Выбрасывающий ячеистый аппарат для рядовых сеялок | 1922 |
|
SU21A1 |
| VAN RANTWIJK F | |||
| ET AL | |||
| "Glycosidase-catalysed synthesis of alkyl glycosides", Journal of molecular | |||
Авторы
Даты
2016-02-20—Публикация
2011-07-26—Подача