ПЕРЕКРЕСТНАЯ ССЫЛКА НА СВЯЗАННЫЕ ЗАЯВКИ
[1] По данной заявке испрашивают приоритет заявки США с серийным № 62/434,033, поданной 14 декабря 2016 года, которая включена в настоящее описание посредством ссылки.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
[2] Изобретение относится к получению сахара D-аллюлозы. Более конкретно, изобретение относится к способам получения D-аллюлозы посредством ферментативного превращения сахаридов (например, полисахаридов, олигосахаридов, дисахаридов, сахарозы, D-глюкозы и D-фруктозы) в D-аллюлозу.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[3] D-аллюлоза (также известная как D-псикоза) (далее аллюлоза) представляет собой низкокалорийный, природный подсластитель, который имеет 70% сладости сахарозы, но только 10% калорий. Она представляет встречаемый в природе моносахарид гексозу, который присутствует только в малых количествах в пшенице и других растениях. Аллюлоза одобрена в качестве пищевой добавки в Food and Drug Administration (FDA) в 2012 году, которая отнесена к общепризнанным в качестве безопасных (GRAS). Однако из-за высоких продажных цен аллюлозы, ее использование в качестве подсластителя ограничено. Аллюлоза славится множеством аспектов пользы для здоровья: она низкокалорийна (10% от сахарозы); она имеет очень низкий гликемический индекс 1; она полностью абсорбируется в тонкой кишке, но не метаболизируется и вместо этого секретируеся в мочу и фекалии; она помогает регулировать сахар крови посредством ингибирования α-амилазы, сукразы и мальтазы; и в продуктах питания и напитках она обладает функциональностью, схожей с сахарозой. По существу, аллюлоза явно имеет различные применения в индустрии продуктов питания и напитков.
[4] В настоящее время аллюлозу получают в основном через ферментативную изомеризацию фруктозы (WO 2014049373). В целом, способ страдает повышенными расходами на исходное сырье, дорогостоящим отделением аллюлозы от фруктозы и относительно низким выходом продукта.
[5] Существует необходимость разработать экономически-эффективный путь синтеза для получения аллюлозы с высоким выходом, где по меньшей мере одна стадия способа включает энергетически благоприятную химическую реакцию. Кроме того, существует потребность в способе получения, в котором стадии способа можно проводить в одном резервуаре или биореактор. Также существует потребность в способе получения аллюлозы, который можно проводить при относительно низкой концентрации фосфата, где фосфат можно использовать повторно, и/или в способе, который не требует использования аденозинтрифосфата (АТФ) в качестве источника фосфата. Также существует потребность в пути получения аллюлозы, для которого не нужно использовать дорогостоящий кофермент никотинамидаденозиндинуклеотид (NAD(H)) на любой из стадий реакции.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[6] Изобретения, описанные в настоящем описании, относятся к способу получения аллюлозы. В различных аспектах способа включают превращение фруктозо-6-фосфата (F6P) в аллюлозо-6-фосфат (A6P), катализируемое с помощью аллюлозо-6-фосфат-3-эпимеразы (A6PE); и превращение A6P в аллюлозу, катализируемое с помощью аллюлозо-6-фосфатфосфатазы (A6PP). Изобретения также относятся к аллюлозе, получаемой с помощью любого из способов, описанных в настоящем описании.
[7] В некоторых аспектах изобретения, способ получения аллюлозы также включает стадия превращения глюкозо-6-фосфата (G6P) в F6P, где стадию катализируют с помощью фосфоглюкоизомеразы (PGI). В других аспектах способа синтеза аллюлозы также включает стадию превращения глюкозо-1-фосфата (G1P) в G6P, и эту стадию превращения катализируют с помощью фосфоглюкомутазы (PGM).
[8] В различных аспектах способ получения аллюлозы может включать превращение сахарида в G1P, катализируемое с помощью по меньшей мере одного фермента; превращение G1P в G6P, катализируемое с помощью фосфоглюкомутазы (PGM); превращение G6P в F6P, катализируемое с помощью фосфоглюкоизомеразы (PGI); превращение F6P в аллюлозо-6-фосфат (A6P), катализируемое с помощью A6PE; и превращение получаемого A6P в аллюлозу, катализируемое с помощью A6PP.
[9] Сахариды, используемые в любом из способов, можно выбирать из группы, состоящей из крахмала или его производного, целлюлозы или ее производного и сахарозы. Крахмал или его производное может представлять собой амилозу, амилопектин, растворимый крахмал, амилодекстрин, мальтодекстрин, мальтозу или глюкозу. В некоторых аспектах изобретения способ получения аллюлозы включает превращение крахмала в производное крахмала с помощью ферментативного гидролиза или посредством кислотного гидролиза крахмала. В других аспектах, производное крахмала можно получать с помощью ферментативного гидролиза крахмала, катализируемого с помощью изоамилазы, пуллуланазы, α-амилазы или комбинации из двух или больше из этих ферментов. Способ получения аллюлозы, в определенных аспектах, также может включать добавление 4-глюкантрансферазы (4GT).
[10] В различных аспектах способ получения аллюлозы может включать превращение фруктозы в F6P, катализируемое с помощью по меньшей мере одного фермента; превращение F6P в аллюлозо-6-фосфат (A6P), катализируемое с помощью A6PE; и превращение получаемого A6P в аллюлозу, катализируемое с помощью A6PP. В других вариантах осуществления способ получения аллюлозы включает превращение сахарозы во фруктозу, катализируемое с помощью по меньшей мере одного фермента; превращение фруктозы в F6P, катализируемое с помощью по меньшей мере одного фермента; превращение F6P в аллюлозо-6-фосфат (A6P), катализируемое с помощью A6PE; и превращение получаемого A6P в аллюлозу, катализируемое с помощью A6PP.
[11] В других аспектах изобретения, G6P, подлежащий использованию в способе получения аллюлозы, можно создавать посредством превращения глюкозы в G6P, катализируемое с помощью по меньшей мере одного фермента. Глюкозу можно в свою очередь получать посредством превращения сахарозы в глюкозу, катализируемое с помощью по меньшей мере одного фермента.
[12] В других аспектах изобретения, стадии способа получения аллюлозы проводят без АТФ, без NAD(H), при концентрации фосфата приблизительно от 0 мМ приблизительно до 150 мМ, фосфат используют повторно и/или по меньшей мере одна стадия способа включает энергетически благоприятную химическую реакцию.
КРАТКОЕ ОПИСАНИЕ ФИГУР
[13] Эти рисунки иллюстрируют определенные аспекты некоторых из вариантов осуществления изобретения, и их не следует использовать в качестве ограничения или определения изобретения.
[14] На фиг. 1 представлено схематическое изображение, иллюстрирующее ферментативный путь превращения фруктозо-6-фосфата в аллюлозо-6-фосфат и затем в аллюлозу.
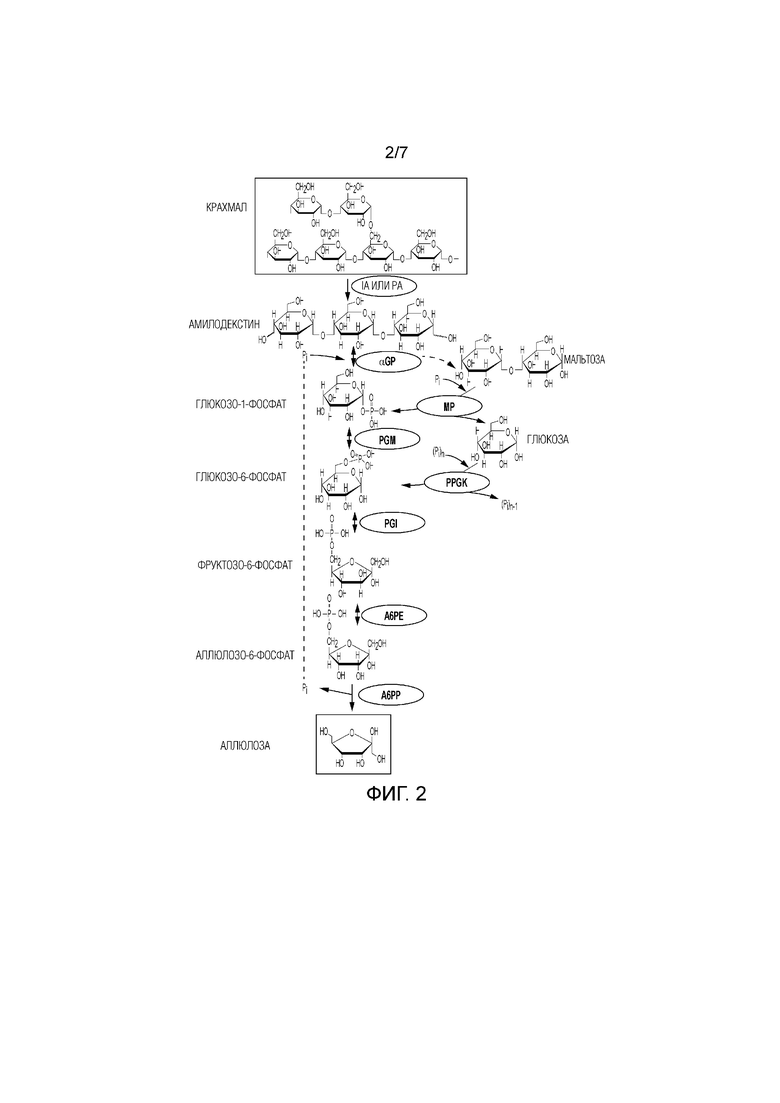
[15] На фиг. 2 представлено схематическое изображение, иллюстрирующее ферментативный путь превращения крахмал или его производных продуктов в аллюлозу. Используют следующие сокращения: αGP, α-глюканфосфорилаза или крахмалфосфорилаза; PGM, фосфоглюкомутаза; PGI, фосфоглюкоизомераза; IA, изоамилаза; PA, пуллуланаза; MP, мальтозофосфорилаза; PPGK, полифосфатглюкокиназа.
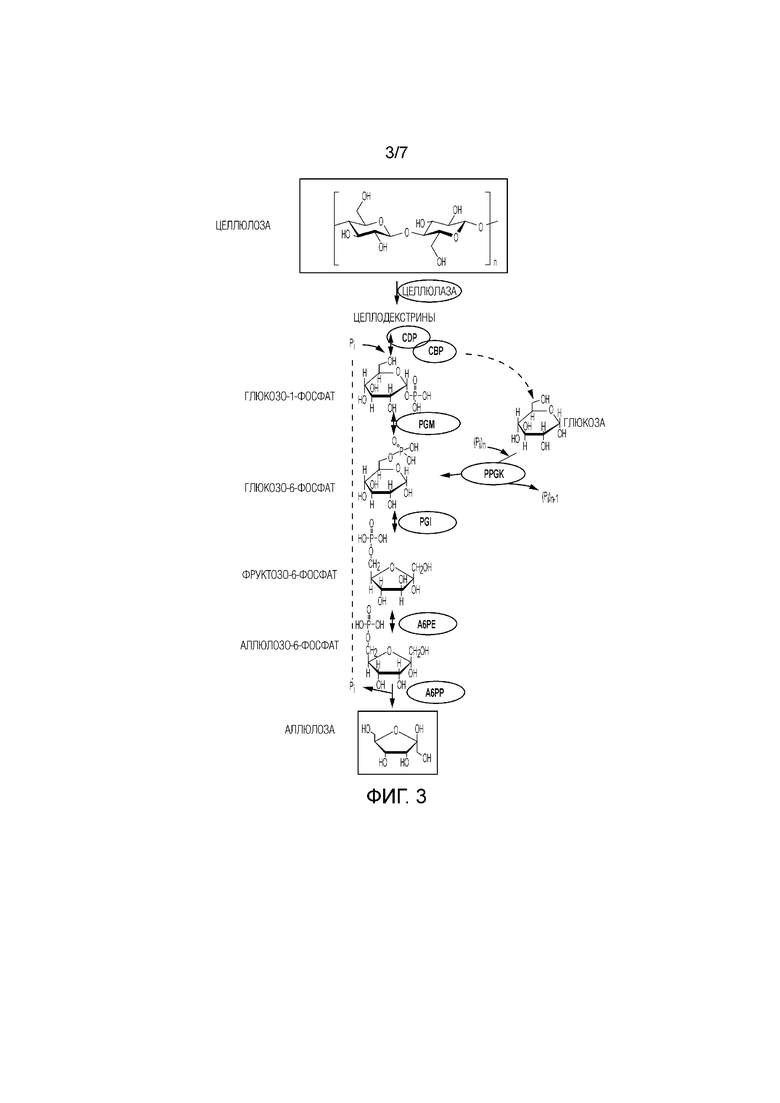
[16] На фиг. 3 представлен ферментативный путь превращения целлюлозы или ее производных продуктрв в аллюлозу. CDP, целлодекстринфосфорилаза; CBP, целлобиозофосфорилаза; PPGK, полифосфатглюкокиназа; PGM, фосфоглюкомутаза; PGI, фосфоглюкоизомераза.
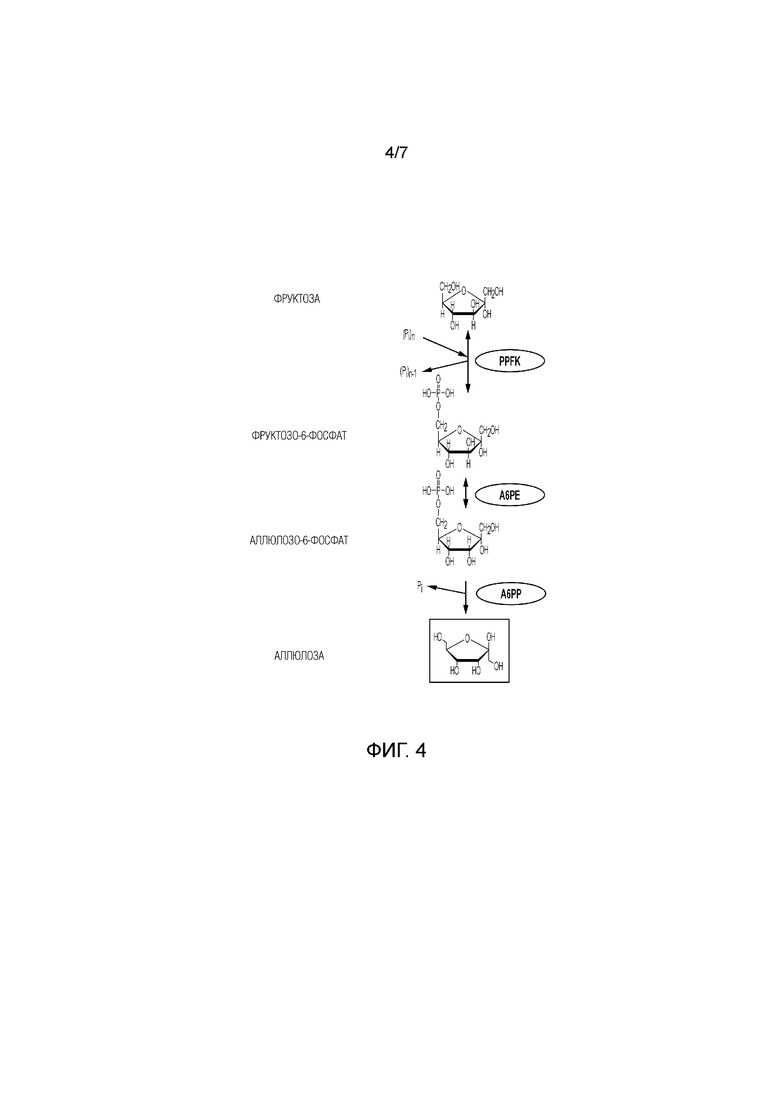
[17] На фиг. 4 представлено схематическое изображение, иллюстрирующее ферментативный путь превращения фруктозы в аллюлозу. PPFK, полифосфатфруктокиназа.
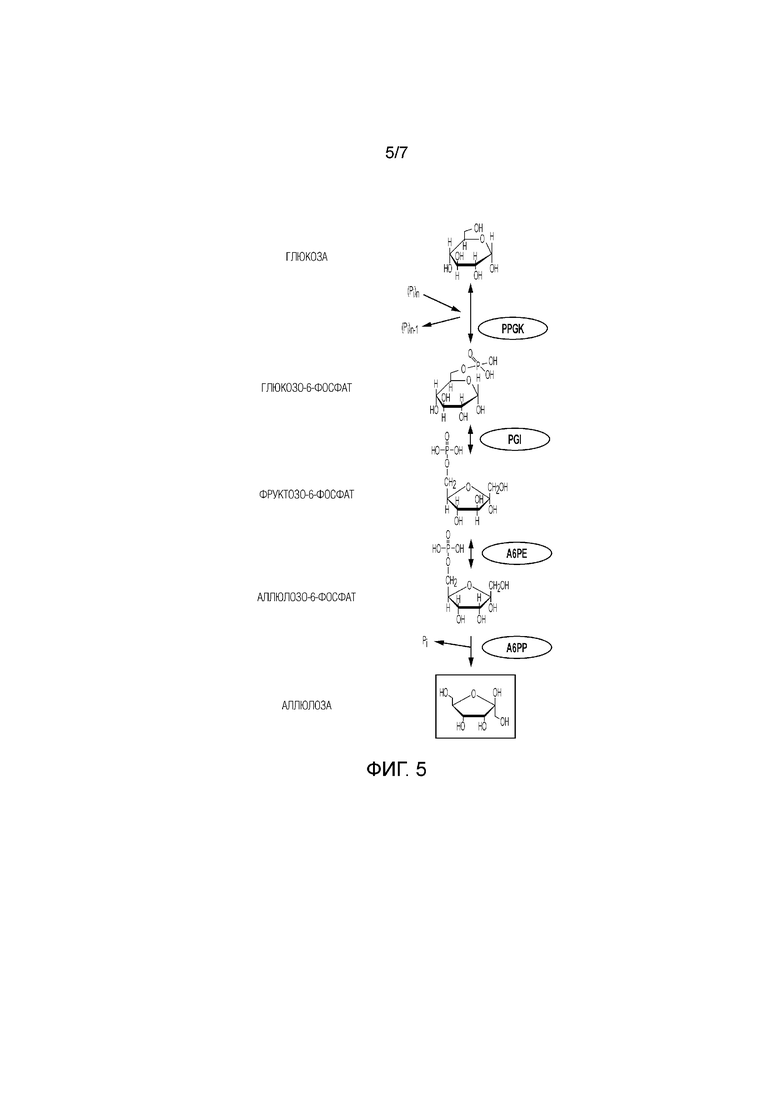
[18] На фиг. 5 представлено схематическое изображение, иллюстрирующее ферментативный путь превращения глюкозы в аллюлозу. PPGK, полифосфатглюкокиназа; PGI, фосфоглюкоизомераза.
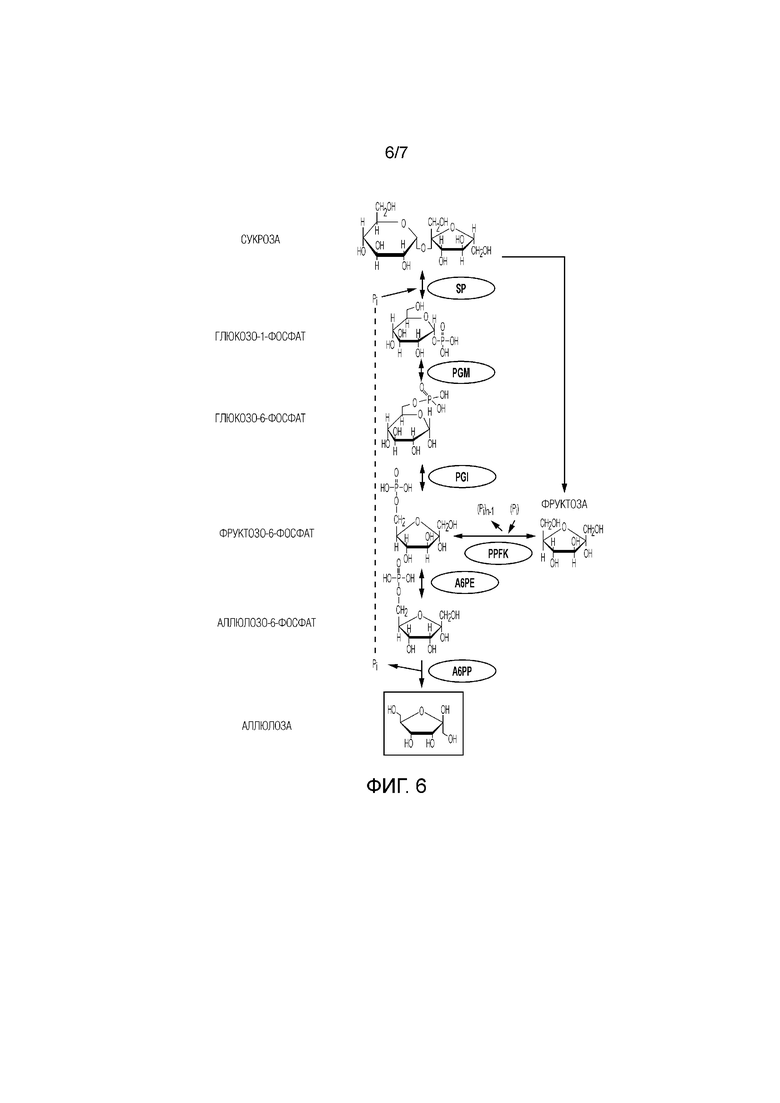
[19] На фиг. 6 представлен ферментативный путь превращения сахарозы или ее производных продуктов в аллюлозу. SP, сахарозофосфорилаза; PPFK, полифосфатфруктокиназа; PGM, фосфоглюкомутаза; PGI, фосфоглюкоизомераза.
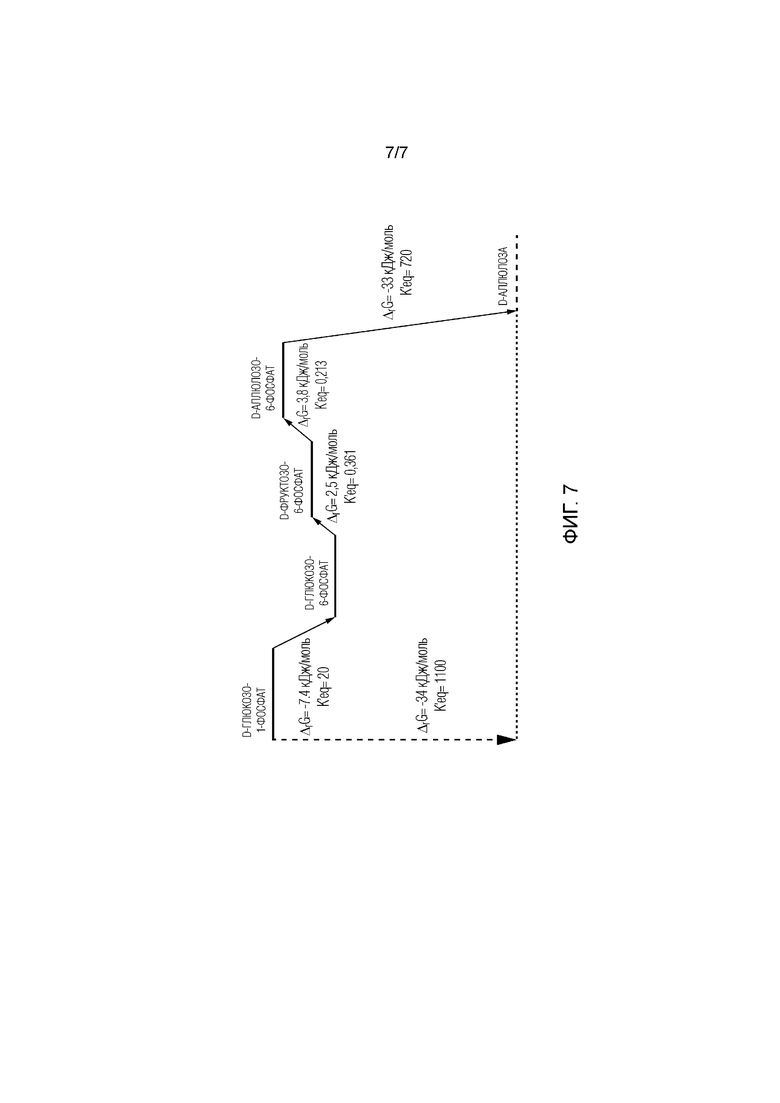
[20] На фиг. 7 представлен энергия Гиббса для реакции между промежуточными продуктами на основе энергии Гиббса для образования при превращении глюкозо-1-фосфата в аллюлозу.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[21] Изобретение относится к ферментативным путям или способам для синтеза аллюлозы с высоким выходом продукта при значительном снижении расходов на выделение продукта и стоимости получения аллюлозы.
[22] Изобретение относится к способу получения аллюлозы, где способ включает превращение фруктозо-6-фосфата (F6P) в аллюлозо-6-фосфат (A6P), катализируемое с помощью эпимеразы, и превращение получаемого A6P в аллюлозу, катализируемое с помощью фосфатазы (например, аллюлозо-6-фосфатфосфатазы, A6PP). Этот способ в целом показан на фиг. 1. В определенных вариантах осуществления эпимераза, которая катализирует превращение F6P в A6P, представляет собой аллюлозо-6-фосфат-3-эпимеразу (A6PE).
[23] Эпимеразы, которые превращают F6P в A6P, можно использовать в способе по изобретению. Эпимеразы также способны превращать A6P в F6P. В некоторых аспектах изобретения эпимеразы, пригодные для использования в способах для того, чтобы превращать F6P в A6P, содержат аминокислотную последовательность, которая обладает степенью идентичности с аминокислотной последовательностью из SEQ ID №№ 3 или 6 по меньшей мере 45%, более предпочтительно по меньшей мере 50%, более предпочтительно по меньшей мере 55%, более предпочтительно по меньшей мере 60%, более предпочтительно по меньшей мере 65%, более предпочтительно по меньшей мере 70%, более предпочтительно по меньшей мере 75%, более предпочтительно по меньшей мере 80%, более предпочтительно по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93% или по меньшей мере 94%, наиболее предпочтительно по меньшей мере 95% и даже наиболее предпочтительно по меньшей мере 96, 97, 98, 99 или 100%. Подходящие эпимеразы кодирует полинуклеотид, содержащий нуклеотидную последовательность, которая обладает степенью идентичности с нуклеотидной последовательностью из SEQ ID №№ 1, 2, 4 и 5 по меньшей мере 30%, предпочтительно по меньшей мере 35%, более предпочтительно по меньшей мере 40%, более предпочтительно по меньшей мере 45%, более предпочтительно по меньшей мере 50%, более предпочтительно по меньшей мере 55%, более предпочтительно по меньшей мере 60%, более предпочтительно по меньшей мере 65%, более предпочтительно по меньшей мере 70%, более предпочтительно по меньшей мере 75%, более предпочтительно по меньшей мере 80%, более предпочтительно по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, наиболее предпочтительно по меньшей мере 95% и даже наиболее предпочтительно по меньшей мере 96, 97, 98, 99 или 100%.
[24] Примеры A6PE включают, но не ограничиваясь этим, следующие белки, идентифицируемые номерами UNIPROT ID: D9TQJ4, A0A090IXZ8 и P32719. Среди них, D9TQJ4 и A0A090IXZ8 получают из термофильных организмов. P32719 получают из мезофильного организма. P32719 на 53% идентичен A0A090IXZ8 и на 55% идентичен D9TQJ4, и каждый белок катализирует эпимеризацию F6P в A6P. Кроме того, A0A090IXZ8 на 45% идентичен D9TQJ4. Наоборот, другие эпимеразные белки, идентифицируемее по номерам UNIPROT ID: A0A101D823, R1AXD6, A0A150LBU8, A0A023CQG9 и H1XWY2, которые обладают определенной степенью идентичности с D9TQJ4 в 45% или меньше, не катализируют эпимеризацию F6P в A6P.
[25] В некоторых аспектах изобретения эпимеразы, пригодные для использования в способах для того, чтобы превращать F6P в A6P, используют кофактор двухвалентный металл: предпочтительно, но не ограничиваясь этим, кобальт. В дополнительных аспектах по изобретению эпимераза содержит, но не ограничиваясь этим, домен (α/β)8-бочонка для катализа; дополнительно, но не ограничиваясь этим, содержит фосфатсвязывающий домен, содержащий Ser на конце 7-го β-тяжа бочонка, Ser на конце 8-го β-тяжа бочонка и Gly в петле активного центра; дополнительно, но не ограничиваясь этим, содержит металлсвязывающий домен, содержащий His во 2-м и 3-м β-тяжах бочонка; дополнительно, но не ограничиваясь этим, содержит Asp во 2-м и 7-м β-тяже бочонка, чтобы действовать в качестве кислотного/основного катализатора для переноса 1,1 протона, и дополнительно, но не ограничиваясь этим, содержит сигнатуру His-гидрофобный остаток-Asp во 2-м β-тяже бочонка, где His участвует в связывании металла и Asp для кислотного/основного катализа. Эти признаки известны в данной области и упомянуты, например, в Chan et al., Structural Basis for Substrate Specificity in Phosphate Binding (beta/alpha)8-Barrels: D-Allulose 6-Phosphate 3-Epimerase from Escherichia coli K-12. Biochemistry. 2008; 47 (36); 9608-9617. Предпочтительно, эпимераза для использования в способах по изобретению содержит домен (α/β)8-бочонка для катализа, Ser на конце 7-го β-тяжа бочонка, Ser на конце 8-го β-тяжа бочонка, Gly в петле активного центра, His во 2-м и 3-м β-тяжах бочонка, Asp во 2-м и 7-м β-тяже бочонка и сигнатуру His-гидрофобный остаток-Asp во 2-м β-тяже бочонка.
[26] Способы по изобретению используют фосфатазы, которые превращают A6P в аллюлозу (D-аллюлозу). В некоторых аспектах изобретения, фосфатазы, подходящие для способа для того, чтобы превращать A6P в аллюлозу, содержат аминокислотную последовательность, которая обладает степенью идентичности с аминокислотной последовательностью SEQ ID № 9 по меньшей мере 45%, более предпочтительно по меньшей мере 50%, более предпочтительно по меньшей мере 55%, более предпочтительно по меньшей мере 60%, более предпочтительно по меньшей мере 65%, более предпочтительно по меньшей мере 70%, более предпочтительно по меньшей мере 75%, более предпочтительно по меньшей мере 80%, более предпочтительно по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, наиболее предпочтительно по меньшей мере 95%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93% или по меньшей мере 94% и даже наиболее предпочтительно по меньшей мере 96, 97, 98, 99 или 100%. Подходящие эпимеразы кодирует полинуклеотид, содержащий нуклеотидную последовательность, которая обладает степенью идентичности с нуклеотидной последовательностью из SEQ ID №№ 7 и 8 по меньшей мере 30%, предпочтительно по меньшей мере 35%, более предпочтительно по меньшей мере 40%, более предпочтительно по меньшей мере 45%, более предпочтительно по меньшей мере 50%, более предпочтительно по меньшей мере 55%, более предпочтительно по меньшей мере 60%, более предпочтительно по меньшей мере 65%, более предпочтительно по меньшей мере 70%, более предпочтительно по меньшей мере 75%, более предпочтительно по меньшей мере 80%, более предпочтительно по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, наиболее предпочтительно по меньшей мере 95% и даже наиболее предпочтительно по меньшей мере 96, 97, 98, 99 или 100%.
[27] Примеры A6PP включают, но не ограничиваясь этим, следующие белки, идентифицируемы по номерам UNIPROT ID: A3DC21, Q5LGR4 и Q89ZR1. A3DC21 на 46% идентичен Q5LGR4 и на 45% идентичен Q89ZR1, и каждый белок катализирует специфическое дефосфорилирование A6P до аллюлозы. Наоборот, другие фосфатазы из суперсемейства дегидрогеназ галогенокислот, белки, идентифицируемые по номерам UNIPROT ID: H0UQ29, Q67LU4, A0A0K6IPM3, C8WSJ0, A0A151YX61 и другие, которые меньше чем на 45% идентичны A3DC21, не катализируют специфическое дефосфорилирование A6P до аллюлозы.
[28] Фосфатазы для превращения A6P в аллюлозу, пригодные для использования в способах по изобретению, обладают специфичностью к аллюлозо-6-фосфату. Как используют в настоящем описании, специфичность аллюлозо-6-фосфату относится к наличию более высокой специфической активности в отношении аллюлозо-6-фосфата по сравнению с глюкозо-1-фосфатом, глюкозо-6-фосфатом или фруктозо-6-фосфатом.
[29] Фосфатазы для превращения A6P в аллюлозу используют кофактор двухвалентный металл: предпочтительно магний. В дополнительных аспектах по изобретению фосфатаза содержит, но не ограничиваясь этим, домен с Россман-подобной укладкой для катализа; дополнительно, но не ограничиваясь этим, содержит домен кэппирования C1 для субстратной специфичности; дополнительно, но не ограничиваясь этим, содержит сигнатуру DxD в 1-м β-тяже Россман-подобной укладки для координации магния, где второй Asp является основным кислотным/основным катализатором; дополнительно, но не ограничиваясь этим, содержит Thr или Ser на конце 2-го β-тяжа Россман-подобной укладки, что способствует стабильности промежуточных продуктов реакции; дополнительно, но не ограничиваясь этим, содержит Lys на N-конце α-спирали ближе к C-концу относительно 3-го β-тяжа Россман-подобной укладки, что способствует стабильности промежуточных продуктов реакции; и дополнительно, но не ограничиваясь этим, содержит сигнатуру GDxxxD на конце 4-го β-тяжа Россман-подобной укладки для координации магния. Эти признаки известны в данной области и упомянуты, например, в Burroughs et al., Evolutionary Genomics of the HAD Superfamily: Understanding the Structural Adaptations and Catalytic Diversity in a Superfamily of Phosphoesterases and Allied Enzymes. J. Mol. Biol. 2006; 361; 1003-1034. Предпочтительно, фосфатаза для превращения A6P в аллюлозу, используемая в способах по изобретению, содержит домен с Россман-подобной укладкой для катализа, домен кэппирования C1, сигнатуру DxD в 1-м β-тяже Россман-подобной укладки, Thr или Ser на конце 2-го β-тяжа Россман-подобной укладки, Lys на N-конце α-спирали ближе к C-концу относительно 3-го β-тяжа Россман-подобной укладки и сигнатуру GDxxxD на конце 4-го β-тяжа Россман-подобной укладки.
[30] В некоторых вариантах осуществления способ получения аллюлозы в соответствии с изобретением также включает стадию ферментативного превращения глюкозо-6-фосфата (G6P) в F6P, и эту стадию катализируют с помощью фосфоглюкоизомеразы (PGI). В других вариантах осуществления способ получения аллюлозы дополнительно включает стадию превращения глюкозо-1-фосфата (G1P) в G6P, где стадию катализируют с помощью фосфоглюкомутазы (PGM). В других вариантах осуществления способ получения аллюлозы также включает стадию превращения сахарида в G1P, которую катализирует по меньшей мере один фермент.
[31] Следовательно, способ получения аллюлозы в соответствии с изобретением может включать, например, следующие стадии: (i) превращение сахарида в глюкозо-1-фосфат (G1P) с использованием одного или нескольких ферментов; (ii) превращение G1P в G6P с использованием фосфоглюкомутазы (PGM, EC 5.4.2.2); (iii) превращение G6P в F6P с использованием фосфоглюкоизомеразы (PGI, EC 5.3.1.9); (iv) превращение F6P в A6P через A6PE и (v) превращение A6P в аллюлозу через A6PP. Пример способа, где сахаридом является крахмал, показан на фиг. 2.
[32] Обычно, соотношения единиц фермента, используемого в раскрытом способе, составляют 1:1:1:1:1 (αGP:PGM:PGI:A6PE:A6PP). Для того чтобы оптимизировать выход продукта, эти соотношения можно корректировать в любом числе комбинаций. Например, соотношение 3:1:1:1:1 можно использовать для того, чтобы максимизировать концентрацию фосфорилированных промежуточных продуктов, что приведет к увеличенной активности последующих реакций. Наоборот, соотношение 1:1:1:1:3 можно использовать для того, чтобы поддерживать устойчивое снабжение фосфатом для αGP, что приведет к более эффективному фосфоролитическому расщеплению α-1,4-гликозидных связей. Соотношение ферментов, например, 3:1:1:1:3 можно использовать для того, чтобы дополнительно увеличивать скорость реакции. Следовательно, соотношения ферментов, включая другие необязательные ферменты, рассмотренные далее, можно варьировать для увеличения эффективности получения аллюлозы. Например, конкретный фермент может присутствовать в количестве приблизительно 2×, 3×, 4×, 5× и т. д. относительно количества других ферментов.
[33] Одним из важных преимуществ способов является то, что стадии способа можно проводить в одном биореакторе или реакционном сосуде. Альтернативно, стадии также можно проводить во множестве биореакторов или реакционных сосудов, которые расположены последовательно.
[34] Затем ионы фосфата, образуемые при дефосфорилировании A6P, можно использовать повторно в способе на стадии превращения сахарида в G1P, в частности, когда все стадии способа проводят в одном биореакторе или реакционном сосуде. Способность повторно использовать фосфат в раскрытых способах делает возможными нестехиометрические количества фосфата, подлежащего использованию, что сохраняет низкие концентрации фосфата в реакции. Это нарушает общий путь и общую скорость способов, но не ограничивает активность индивидуальных ферментов и допускает общую эффективность способов получения аллюлозы.
[35] Например, концентрации фосфата в реакции могут находиться в диапазоне приблизительно от 0 мМ приблизительно до 300 мМ, приблизительно от 0 мМ приблизительно до 150 мМ, приблизительно от 1 мМ приблизительно до 50 мМ, предпочтительно приблизительно от 5 мМ приблизительно до 50 мМ или более предпочтительно приблизительно от 10 мМ приблизительно до 50 мМ. Например, концентрация фосфата в реакции может составлять приблизительно 0,1 мМ, приблизительно 0,5 мМ, приблизительно 1 мМ, приблизительно 1,5 мМ, приблизительно 2 мМ, приблизительно 2,5 мМ, приблизительно 5 мМ, приблизительно 6 мМ, приблизительно 7 мМ, приблизительно 8 мМ, приблизительно 9 мМ, приблизительно 10 мМ, приблизительно 15 мМ, приблизительно 20 мМ, приблизительно 25 мМ, приблизительно 30 мМ, приблизительно 35 мМ, приблизительно 40 мМ, приблизительно 45 мМ, приблизительно 50 мМ или приблизительно 55 мМ.
[36] Следовательно, низкая концентрация фосфата ведет к сниженной стоимости производства из-за низкого общего фосфата и, таким образом, сниженной стоимости удаления фосфата. Также это препятствует ингибированию A6PP высокими концентрациями свободного фосфата и снижает потенциал загрязнения фосфатами.
[37] Кроме того, способы, раскрытые в настоящем описании, можно проводить без добавления АТФ в качестве источника фосфата, т. е. без АТФ. Способы также можно проводить без необходимости добавлять NAD(H), т. е. без NAD(H). Другие преимущества также включают тот факт, что по меньшей мере одна стадия раскрытых способов получения аллюлозы включает энергетически благоприятную химическую реакцию (фиг. 7).
[38] Примеры ферментов, используемых для того, чтобы превращать сахарид в G1P, включают α-глюканфосфорилазу (αGP, EC 2.4.1.1, которая также включает мальтодекстринфосфорилазу, крахмалфосфорилазу, гликогенфосфорилазу и другие фосфорилазы, разрушающие α-1,4 гликозидные связи), мальтозофосфорилазу (MP, EC 2.4.1.8), целлодекстринфосфорилазу (CDP, EC 2.4.1.49), целлобиозофосфорилазу (CBP, EC 2.4.1.20), целлюлозофосфорилазу, сахарозофосфорилазу (SP, EC 2.4.1.7) и их сочетание. Выбор фермента или комбинации ферментов зависит от сахарида, используемого в способе.
[39] Сахариды, используемые для получения G1P, могут представлять собой полисахариды, олигосахариды и/или дисахариды. Например, сахаридом может быть крахмал, одно или несколько производных крахмала, целлюлоза, одно или несколько производных целлюлозы, сахароза, одно или несколько производных сахарозы или их сочетание.
[40] Крахмал является наиболее широко используемым соединением накопления энергии в природе и главным образом хранится в семенах растений. Природный крахмал содержит линейную амилозу и разветвленный амилопектин. Примеры производных крахмала включают амилозу, амилопектин, растворимый крахмал, амилодекстрин, мальтодекстрин, мальтозу, фруктозу и глюкозу. Примеры производных целлюлозы включают предварительно обработанную биомассу, регенерированную аморфную целлюлозу, целлодекстрин, целлобиозу, фруктозу и глюкозу. Производные сахарозы включают фруктозу и глюкозу.
[41] Производные крахмала можно получать с помощью ферментативного гидролиза крахмала или посредством кислотного гидролиза крахмала. В частности, ферментативный гидролиз крахмала можно катализировать или усиливать с помощью изоамилазы (IA, EC. 3.2.1.68), которая гидролизует α-1,6-глюкозидные связи; пуллуланазы (PA, EC. 3.2.1.41), которая гидролизует α-1,6-глюкозидные связи; 4-α-глюканoтрансферазы (4GT, EC 2.4.1.25), которая катализирует трансгликозилирование коротких мальтоолигосахаридов, давая более длинные мальтоолигосахариды; или α-амилазы (EC 3.2.1.1), которая расщепляет α-1,4-глюкозидные связи.
[42] Кроме того, производные целлюлозы можно получать с помощью ферментативного гидролиза целлюлозы, катализируемого с помощью смесей целлюлаз, с помощью кислот или с помощью предварительной обработки биомассы.
[43] В определенных вариантах осуществления ферменты, используемые для того, чтобы превращать сахарид в G1P, содержат αGP. На этой стадии, когда сахариды включают крахмал, G1P создают из крахмала с помощью αGP; когда сахариды содержат растворимый крахмал, амилодекстрин или мальтодекстрин, G1P получают из растворимого крахмала, амилодекстрина или мальтодекстрина с помощью αGP.
[44] Когда сахариды включают мальтозу и ферменты содержат мальтозофосфорилазу, G1P создают из мальтозы посредством мальтозофосфорилазы. Если сахариды включают сахарозу и ферменты содержат сахарозофосфорилазу, G1P создают из сахарозы с помощью сахарозофосфорилазы.
[45] В еще одном другом варианте осуществления, когда сахариды содержат целлобиозу и ферменты содержат целлобиозофосфорилазу, G1P создают из целлобиозы с помощью целлобиозофосфорилазы.
[46] В дополнительном варианте осуществления, когда сахариды содержат целлодекстрины и ферменты содержат целлодекстринфосфорилазу, G1P создают из целлодекстринов с помощью целлодекстринфосфорилазы.
[47] В альтернативном варианте осуществления превращения сахарида в G1P, когда сахариды содержат целлюлозу и ферменты содержат целлюлозофосфорилазу, G1P создают из целлюлозы с помощью целлюлозофосфорилазы.
[48] В соответствии с изобретением, аллюлозу также можно получать из фруктозы. Пример способа показан на фиг. 4. Например, способ включает создание F6P из фруктозы и полифосфата, катализируемое с помощью полифосфатфруктокиназы (PPFK); превращение F6P в A6P, катализируемое с помощью A6PE; и превращение A6P в аллюлозу, катализируемое с помощью A6PP. Фруктозу можно получать, например, посредством ферментативного превращения сахарозы.
[49] В других вариантах осуществления аллюлозу можно получать из сахарозы. Пример такого способа показан на фиг. 6. Способ предусматривает путь синтеза in vitro, который включает следующие ферментативные стадии: создание G1P из сахарозы и свободного фосфата, катализируемое с помощью сахарозофосфорилазы (SP); превращение G1P в G6P, катализируемое с помощью PGM; превращение G6P в F6P, катализируемое с помощью PGI; превращение F6P в A6P, катализируемое с помощью A6PE; и превращение A6P в аллюлозу, катализируемое с помощью A6PP.
[50] Ионы фосфата, образуемые при превращении A6P в аллюлозу, затем можно использовать повторно на стадии превращения сахарозы в G1P. Дополнительно, как показано на фиг. 6, PPFK и полифосфат можно использовать для увеличения выхода аллюлозы посредством получения F6P из фруктозы, образуемой посредством фосфоролитического расщепления сахарозы с помощью SP.
[51] В некоторых вариантах осуществления способ получения аллюлозы включает следующие стадии: создания глюкозы из полисахаридов и олигосахаридов с помощью ферментативного гидролиза или кислотного гидролиза, превращения глюкозы в G6P, катализируемое с помощью по меньшей мере одного фермента, создание фруктозы из полисахаридов и олигосахаридов с помощью ферментативного гидролиза или кислотного гидролиза, и превращения фруктозы в G6P, катализируемое с помощью по меньшей мере одного фермента. Примеры полисахаридов и олигосахаридов перечислены выше.
[52] В других вариантах осуществления G6P получают из глюкозы и полифосфата натрия с помощью полифосфатглюкокиназы.
[53] Настоящее раскрытие предусматривает способы превращения сахаридов, таких как полисахариды и олигосахариды в крахмале, целлюлозе, сахарозе и их производных продуктах, в аллюлозу. В определенных вариантах осуществления искусственные (не природные) ферментативные пути без АТФ предусмотрены для того, чтобы превращать крахмал, целлюлозу, сахарозу и их производные продукты в аллюлозу, используя бесклеточные ферментативные коктейли.
[54] Как показано выше, несколько ферментов можно использовать для того, чтобы гидролизовать крахмал для увеличения выхода G1P. Такие ферменты включают изоамилазу, пуллуланазу и α-амилазу. Кукурузный крахмал содержит множество ветвей, которые затрудняют действие αGP. Изоамилазу можно использовать для деветвления крахмала, дающего линейный амилодекстрин. Предварительно обработанный изоамилазой крахмал может вести к более высокой концентрации F6P в конечном продукте. Изоамилаза и пуллуланаза расщепляют α-1,6-гликозидные связи, что делает возможным более полное разрушение крахмала с помощью α-глюканфосфорилазы. α-амилаза расщепляет α-1,4-гликозидные связи, следовательно α-амилазу используют для того, чтобы разрушать крахмал на фрагменты для более быстрого превращения в аллюлозу.
[55] Как показано на фиг. 2, мальтозофосфорилазу (MP) можно использовать для увеличения выхода аллюлозы посредством фосфоролитического расщепления продукта разложения мальтозы на G1P и глюкозу. Альтернативно, 4-глюкантрансферазу (4GT) можно использовать для увеличения выхода аллюлозы посредством повторного использования продуктов разложения глюкозы, мальтозы и мальтотриозы на более длинные мальтоолигосахариды; которые можно фосфоролитически расщеплять с помощью αGP с получением G1P.
[56] Дополнительно, целлюлоза является наиболее распространенным биоресурсом и представляет собой основной компонент клеточной стенки растений. Непищевая лигноцеллюлозная биомасса содержит целлюлозу, гемицеллюлозу и лигнин, а также другие минорные компоненты. Чистую целлюлозу, включая Avicel (микрокристаллическая целлюлоза), регенерированную аморфную целлюлозу, бактериальную целлюлозу, фильтровальную бумагу и так далее, можно получать через ряд обработок. Частично гидролизованные целлюлозные субстраты включают водонерастворимые целлодекстрины, степень полимеризации которых больше 7, водорастворимые целлодекстрины со степенью полимеризации 3-6, целлобиозу, глюкозу и фруктозу.
[57] В определенных вариантах осуществления целлюлозу и ее производные продукты можно превращать в аллюлозу через серию стадий. Пример такого способа представлен на фиг. 3. Способ предусматривает путь синтеза in vitro, который включает следующие стадии: создание G1P из целлодекстрина и целлобиозы и без фосфата, катализируемое с помощью целлодекстринфосфорилазы (CDP) и целлобиозофосфорилазы (CBP), соответственно; превращение G1P в G6P, катализируемое с помощью PGM; превращение G6P в F6P, катализируемое с помощью PGI; превращение F6P в A6P, катализируемое с помощью A6PE; и превращение A6P в аллюлозу, катализируемое с помощью A6PP. В этом способы, ионы фосфата можно использовать повторно на стадии превращения целлодекстрина и целлобиозы в G1P.
[58] Несколько ферментов можно использовать для того, чтобы гидролизовать твердую целлюлозу до водорастворимых целлодекстринов и целлобиозы. Такие ферменты включают эндоглюканазу и целлобиогидролазу, но не включают β-глюкозидазу (целлобиазу).
[59] Перед гидролизом целлюлозы и получением G1P, целлюлозу и биомассу можно предварительно обрабатывать для увеличения их реакционной способности и снижения степени полимеризации цепей целлюлозы. Способы предварительной обработки целлюлозы и биомассы включают предварительную обработку разбавленной кислотой, фракционирование лигноцеллюлозы на основе растворителей целлюлозы, аммиачное расширение волокон, пропитывание аммиачной водой, обработку ионной жидкостью и частичный гидролиз с использованием концентрированных кислот, включая соляную кислоту, серную кислоту, фосфорную кислоту и их комбинации.
[60] В некоторых вариантах осуществления полифосфат и полифосфатглюкокиназу (PPGK) можно добавлять в способ, таким образом увеличивая выход аллюлозы посредством фосфорилирования продукта разложения глюкозы до G6P, как показано на фиг. 3.
[61] В других вариантах осуществления аллюлозу можно создавать из глюкозы. Пример такого способа представлен на фиг. 5. Способ включает стадии создания G6P из глюкозы и полифосфата, катализируемой с помощью полифосфатглюкокиназы (PPGK); превращения G6P в F6P, катализируемого с помощью PGI; превращения F6P в A6P, катализируемого с помощью фермента; и превращения A6P в аллюлозу, катализируемого с помощью A6PP.
[62] Любой подходящий биологический буфер, известный в данной области, можно использовать в способе по изобретению, таком как HEPES, PBS, BIS-TRIS, MOPS, DIPSO, Trizma и т. д. Реакционный буфер для всех вариантов осуществления может иметь pH в диапазоне 5,0-8,0. Более предпочтительно pH реакционного буфера может находиться в диапазоне приблизительно от 6,0 приблизительно до 7,3. Например, pH реакционного буфера может составлять 6,0, 6,2, 6,4, 6,6, 6,8, 7,0, 7,2 или 7,3.
[63] Реакционный буфер также может содержать ключевые катионы металла. Примеры ионов металлов включают Mg2+, Co2+ и Zn2+.
[64] Температура реакции, при которой проводят стадии способа, может находиться в диапазоне 37-85°C. Более предпочтительно, стадии можно проводить при температуре в диапазоне от приблизительно 40°C приблизительно до 70°C. Температура может составлять, например, приблизительно 40°C, приблизительно 45°C, приблизительно 50°C, приблизительно 55°C или приблизительно 60°C. Предпочтительно, температура реакции составляет приблизительно 50°C.
[65] Время реакции в раскрытых способах можно корректировать по мере необходимости, и оно может находиться в диапазоне приблизительно от 8 часов приблизительно до 48 часов. Например, время реакции может составлять приблизительно 16 часов, приблизительно 18 часов, приблизительно 20 часов, приблизительно 22 часа, приблизительно 24 часа, приблизительно 26 часов, приблизительно 28 часов, приблизительно 30 часов, приблизительно 32 часа, приблизительно 34 часа, приблизительно 36 часов, приблизительно 38 часов, приблизительно 40 часов, приблизительно 42 часа, приблизительно 44 часа, приблизительно 46 часов или приблизительно 48 часов. Более предпочтительно, время реакции составляет приблизительно 24 часа.
[66] Способы в соответствии с изобретением могут достигать высокого выхода вследствие очень благоприятной константы равновесия для общей реакции. Теоретически, можно достичь выхода вплоть до 99%, если исходный материал полностью превращают в промежуточный продукт.
[67] В способах по изобретению используют недорогие исходные материалы и снижена стоимость производства за счет снижения расходов, ассоциированных с исходным сырьем и выделением продукта. Крахмал, целлюлоза, сахароза и некоторые их производные являются менее дорогостоящим исходным сырьем, чем, например, фруктоза. Когда аллюлозу получают из фруктозы, выходы ниже, чем в настоящем изобретении, и аллюлозу нужно отделять от фруктозы через хроматографию, что ведет к более высокой стоимости производства.
[68] Также стадия превращения A6P в аллюлозу в соответствии с изобретением представляет собой необратимую фосфатазную реакцию, независимо от исходного сырья. Следовательно, аллюлозу получают с очень высоким выходом, при этом эффективно минимизируя последующие расходы на выделение продукта.
[69] В отличие от клеточных способов производства, изобретение включает бесклеточное получение аллюлозы, имеет относительно высокую скорость реакции из-за устранения клеточной мембраны, которая часто замедляет транспорт субстрата/продукта в клетку и из нее. Также оно имеет конечный продукт, свободный от ферментационных сред, богатых питательными веществами/клеточных метаболитов.
ПРИМЕРЫ
Материалы и способы
[70] Химические соединения
[71] Все химические соединения, включая кукурузный крахмал, растворимый крахмал, мальтодекстрины, мальтозу, глюкозу, фильтровальную бумагу, имели марку реактивов или выше и были приобретены в Sigma-Aldrich (St. Louis, MO, USA) или Fisher Scientific (Pittsburgh, PA, USA), если не указано иное. Рестрикционные ферменты, T4 лигазу и ДНК полимеразу Phusion приобретали в New England Biolabs (Ipswich, MA, USA). Олигонуклеотиды синтезировали или с помощью Integrated DNA Technologies (Coralville, IA, USA) или Eurofins MWG Operon (Huntsville, AL, USA). Нуклеотидная последовательность, SEQ ID № 1, кодирует термофильную A6PE из Thermoanaerobacterium thermosaccharolyticum (UNIPROT ID D9TQJ4). SEQ ID № 2 представляет собой версию этой нуклеотидной последовательности с оптимизированными кодонами. SEQ ID № 3 представляет собой аминокислотную последовательность для фермента. Нуклеотидная последовательность SEQ ID № 4 кодирует термофильную A6PE из Bacillus thermoamylovorans (UNIPROT ID A0A090IXZ8). SEQ ID № 5 представляет собой версию с оптимизированными кодонами этой нуклеотидной последовательности. SEQ ID № 6 представляет собой аминокислотную последовательность для фермента. Нуклеотидная последовательность SEQ ID № 7 кодирует термофильную A6PP из Clostridium thermocellum (UNIPROT ID A3DC21). SEQ ID № 8 представляет собой версию нуклеотидной последовательности с оптимизированными кодонами. SEQ ID № 9 представляет собой аминокислотную последовательность, соответствующую ферменту. Регенерированную аморфную целлюлозу, используемую при ферментативной очистке, получали из Avicel PH105 (FMC BioPolymer, Philadelphia, PA, USA), через ее растворение и регенерацию, как описано в: Ye et al., Fusion of a family 9 cellulose-binding module improves catalytic potential of Clostridium thermocellum cellodextrin phosphorylase on insoluble cellulose. Appl. Microbiol. Biotechnol. 2011; 92:551-560. Escherichia coli Sig10 (Sigma-Aldrich, St. Louis, MO, USA) использовали в качестве клетки-хозяина для манипуляций с ДНК, а E. coli BL21 (DE3) (Sigma-Aldrich, St. Louis, MO, USA) использовали в качестве клетки-хозяина для экспрессии рекомбинантного белка. Среды ZYM-5052, содержащие 100 мг л-1 ампициллина или 50 мг л-1 канамицина, использовали для клеточного роста E. coli и экспрессии рекомбинантного белка. Целлюлазу из Trichoderma reesei (номер по каталогу: C2730) и пуллуланазу (номер по каталогу: P1067) приобретали в Sigma-Aldrich (St. Louis, MO, USA) и получали с помощью Novozymes (Franklinton, NC, USA). Мальтозофосфорилазу (номер по каталогу: M8284) приобретали в Sigma-Aldrich.
[72] Получение и очистка рекомбинантных ферментов
[73] Штамм E. coli BL21 (DE3), несущий экспрессирующую белок плазмиду, инкубировали в 1 л колбе Эрленмейера со 100 мл сред ZYM-5052, содержащих 100 мг л-1 ампициллина или 50 мг л-1 канамицина. Клетки выращивали при 30°C при вращательном встряхивании на 220 об./мин в течение 16-24 часов. Клетки собирали посредством центрифугирования при 12°C и промывали один раз с использованием 20 мМ HEPES (pH 7,5), содержащего 50 мМ NaCl и 5 мМ MgCl2 (термопреципитация и целлюлозусвязывающий модуль), или 20 мМ HEPES (pH 7,5), содержащего 300 мМ NaCl и 5 мМ имидазола (Ni очистка). Клеточные пеллеты ресуспендировали в том же буфере и лизировали посредством обработки ультразвуком (Fisher Scientific Sonic Dismembrator Model 500; вкл. импульс 5 с и выкл. 10 с, всего 21 мин при 50% амплитуде). После центрифугирования очищали целевые белки в супернатантах.
[74] Три подхода использовали для того, чтобы очищать различные рекомбинантные белки. Белки с гистидиновыми метками очищали с помощью Profinity IMAC Ni-Charged Resin (Bio-Rad, Hercules, CA, USA). Слитые белки, содержащие целлюлозусвязывающий модуль (CBM) и самовырезающийся интеин, очищали через высокоаффинную адсорбцию на поверхности регенерированной аморфной целлюлозы большой площади. Термопреципитацию при 70-95°C в течение 5-30 мин использовали для того, чтобы очищать гипертермостабильные ферменты. Чистоту рекомбинантных белков исследовали посредством электрофореза в полиакриламидном геле с додецилсульфатом натрия (SDS-PAGE). A6PE очищали с использованием 80 мкМ CoCl2, присутствующего в средах для выращивания, элюирующих буферах, диализном буфере и буфере для хранения белка.
[75] Используемые ферменты и анализ их активности
[76] Использовали α-глюканфосфорилазу (αGP) из Thermotoga maritima (UNIPROT ID G4FEH8). Активность анализировали в 50 мМ натрий-фосфатном буфере (pH 7,2), содержащем 1 мМ MgCl2, 5 мМ DTT и 30 мМ мальтодекстрина при 50°C. Реакцию останавливали через фильтрование фермента с использованием концентратора Vivaspin 2 (10000 MWCO) (Vivaproducts, Inc., Littleton, MA, USA). Глюкозо-1-фосфат (G1P) измеряли с использованием набора для анализа с глюкозогексокиназой/G6PDH (Sigma Aldrich, № по каталогу GAHK20-1KT) с добавлением 25 Ед./мл фосфоглюкомутазы. Единица (Ед.) описана как мкмоль/мин.
[77] Использовали фосфоглюкомутазу (PGM) из Thermococcus kodakaraensis (UNIPROT ID Q68BJ6). Активность измеряли в 50 мМ буфере HEPES (pH 7,2), содержащем 5 мМ MgCl2 и 5 мМ G1P, при 50°C. Реакцию останавливали через фильтрование фермента с использованием концентратора Vivaspin 2 (10000 MWCO). Продукт глюкозо-6-фосфат (G6P) определяли с использованием набора для анализа с гексокиназой/G6PDH (Sigma Aldrich, № по каталогу GAHK20-1KT).
[78] Использовали два различных источника фосфоглюкоизомеразы (PGI) из Clostridium thermocellum (UNIPROT ID A3DBX9) и Thermus thermophilus (UNIPROT ID Q5SLL6). Активность измеряли в 50 мМ буфера HEPES (pH 7,2), содержащего 5 мМ MgCl2 и 10 мМ G6P, при 50°C. Реакцию останавливали через фильтрование фермента с использованием концентратора Vivaspin 2 (10000 MWCO). Продукт, фруктозо-6-фосфат (F6P), определяли с использованием сопряженного ферментативного анализа с фруктозо-6-фосфаткиназой (F6PK)/пируватдегидрогеназой (PK)/лактатдегидрогеназой (LD), где снижение поглощения на 340 нм указывает на получение F6P. Эта 200 мкл реакция содержала 50 мМ HEPES (pH 7,2), 5 мМ MgCl2, 10 мМ G6P, 1,5 мМ АТФ, 1,5 мМ фосфоенолпирувата, 200 мкМ NADH, 0,1 Ед. PGI, 5 Ед. PK и 5 Ед. LD.
[79] Использовали аллюлозо-6-фосфат-3-эпимеразу (A6PE) из Thermoanaerobacterium thermosaccharolyticum (UNIPROT ID D9TQJ4), SEQ ID № 3. Активность измеряли в 50 мМ буфере HEPES (pH 7,2), содержащем 5 мМ MgCl2, 80 мкМ CoCl2, 1 Ед./мл A6PP и 10 мМ F6P, при 50°C. Реакцию останавливали через фильтрование фермента с использованием концентратора Vivaspin 2 (10000 MWCO). Продукт, аллюлозо-6-фосфат (A6P), определяли с использованием аллюлозо-6-фосфатфосфатазы и обнаруживая высвобождение свободного фосфата. Для того чтобы обнаруживать высвобождение свободного фосфата, 500 мкл раствора, содержащего 0,1 M ацетата цинка и 2 мМ молибдата аммония (pH 5), добавляли к 50 мкл реакции. Их смешивали, после чего следовало 125 мкл 5% аскорбиновой кислоты (pH 5). Этот раствор смешивали, затем инкубировали при 30°C в течение 20 мин. Поглощение на 850 нм считывали для того, чтобы определять высвобождение свободного фосфата.
[80] Использовали аллюлозо-6-фосфатфосфатазу (A6PP) из Clostridium thermocellum (UNIPROT ID A3DC21), SEQ ID № 9. Активность измеряли в 50 мМ буфере HEPES (pH 7,2), содержащем 5 мМ MgCl2, 80 мкМ CoCl2, 1 Ед./мл A6PE и 10 мМ F6P, при 50°C. Реакцию останавливали через фильтрование фермента с использованием концентратора Vivaspin 2 (10000 MWCO). Продукт, аллюлозу, определяли через обнаружение высвобождения свободного фосфата, как описано для A6PE.
[81] Рекомбинантная целлодекстринфосфорилазая и целлобиозофосфорилаза из C. thermocellum описаны в Ye et al. Spontaneous high-yield production of hydrogen from cellulosic materials and water catalyzed by enzyme cocktails. ChemSusChem 2009; 2:149-152. Их активности анализировали, как описано.
[82] Рекомбинантная полифосфатглюкокиназа из Thermobifida fusca YX описана в Liao et al., One-step purification and immobilization of thermophilic polyphosphate glucokinase from Thermobifida fusca YX: glucose-6-phosphate generation without ATP. Appl. Microbiol. Biotechnol. 2012; 93:1109-1117. Ее активности анализировали, как описано.
[83] Рекомбинантная изоамилаза из Sulfolobus tokodaii описана in Cheng et al., Doubling power output of starch biobattery treated by the most thermostable isoamylase from an archaeon Sulfolobus tokodaii. Scientific Reports 2015; 5:13184. Ее активности анализировали, как описано.
[84] Рекомбинантная 4-α-глюканолтрансфераза из Thermococcus litoralis описана в Jeon et al. 4-α-Glucanotransferase from the Hyperthermophilic Archaeon Thermococcus Litoralis. Eur. J. Biochem. 1997; 248:171-178. Ее активность измеряли, как описано.
[85] Использовали сахарозофосфорилазу из Caldithrix abyssi (UNIPROT H1XT50). Ее активность измеряли в 50 мМ буфере HEPES (pH 7,5), содержащем 10 мМ сахарозы и 12 мМ органического фосфата. Глюкозо-1-фосфат (G1P) измеряли с использованием набора для анализа с глюкозогексокиназой/G6PDH с добавлением 25 Ед./мл фосфоглюкомутазы, как и в случае α-глюканфосфорилазы.
[86] Единицы фермента, используемого в каждом примере далее, можно увеличивать или уменьшать, чтобы корректировать время реакции по желанию. Например, если хотят осуществлять пример 9 за 8 ч вместо 24 ч, единицы фермента следует увеличивать приблизительно в 3 раза. Наоборот, если желают выполнять пример 9 за 48 ч вместо 24 ч, единицы фермента следует уменьшать приблизительно в 2 раз. Эти примеры иллюстрируют, как количество единиц фермента можно использовать для увеличения или уменьшения времени реакции при сохранении постоянной производительности.
[87] Пример 1
[88] Для того чтобы валидировать техническую осуществимость ферментативного биосинтеза фруктозо-6-фосфата из крахмала, рекомбинантно экспрессировали три фермента: α-глюканфосфорилазу из T. maritima (UNIPROT ID G4FEH8), фосфоглюкомутазу из Thermococcus kodakaraensis (UNIPROT ID Q68BJ6) и фосфоглюкоизомеразу из Clostridium thermocellum (UNIPROT ID A3DBX9). Рекомбинантные белки сверхэкспрессировали в E. coli BL21 (DE3) и очищали, как описано выше.
[89] 0,20 мл реакционной смеси, содержащей 10 г/л растворимого крахмала, 50 мМ фосфатно-солевого буфера pH 7,2, 5 мМ MgCl2, 0,5 мМ ZnCl2, 0,01 Ед. αGP, 0,01 Ед. PGM и 0,01 Ед. PGI, инкубировали при 50°C в течение 24 часов. Реакцию останавливали через фильтрование фермента с использованием концентратора Vivaspin 2 (10000 MWCO). Продукт, фруктозо-6-фосфат (F6P), определяли с использованием сопряженного ферментативного анализа с фруктозо-6-фосфаткиназой (F6PK)/пируватдегидрогеназой (PK)/лактатдегидрогеназой (LD), где снижение поглощения на 340 нм указывает на получение F6P, как описано выше. Конечная концентрация F6P после 24 часов составляла 3,6 г/л.
[90] Пример 2
[91] Те же тесты, как в примере 1 (кроме температуры реакции) осуществляли при 40-80°C. Обнаружено, что 10 г/л растворимого крахмала давало 0,9 г/л F6P при 40°C и 3,6 г/л F6P при 80°C после 40-часовых реакций. Эти результаты подсказывают, что увеличение температуры реакции для этого набора ферментов увеличивало выход F6P, но слишком высокая температура может снижать активность некоторых ферментов.
[92] Пример 3
[93] Обнаружено, при 80°C соотношение единиц ферментов αGP:PGM:PGI приблизительно 1:1:1 вело к быстрому образованию F6P. Отмечали, что соотношение ферментов не влияет на конечную концентрацию F6P значительно, если время реакции достаточно велико. Однако соотношение ферментов влияет на скорости реакций и общую стоимость ферментов, используемых в системе.
[94] Пример 4
[95] 0,20 мл реакционную смесь, содержащую 10 г/л мальтодекстрина, 50 мМ фосфатно-солевого буфера pH 7,2, 5 мМ MgCl2, 0,5 мМ ZnCl2, 0,01 Ед. αGP, 0,01 Ед. PGM и 0,01 Ед. PGI, инкубировали при 50°C в течение 24 часов. Реакцию останавливали через фильтрование фермента с использованием концентратора Vivaspin 2 (10000 MWCO). Продукт, фруктозо-6-фосфат (F6P), определяли с использованием сопряженного ферментативного анализа с фруктозо-6-фосфаткиназой (F6PK)/пируватдегидрогеназой (PK)/лактатдегидрогеназой (LD), где снижение поглощения на 340 нм указывает на получение F6P, как описано выше. Конечная концентрация F6P после 24 часов составляла 3,6 г/л.
[96] Пример 5
[97] Для того чтобы тестировать получение F6P из Avicel, Sigma, использовали целлюлазу, чтобы гидролизовать целлюлозу при 50°C. Для того чтобы удалять β-глюкозидазу из коммерческой целлюлазы, 10 единиц фильтровальной бумаги/мл целлюлазы смешивали с 10 г/л Avicel на водно-ледяной бане в течение 10 мин. После центрифугирования при 4°C, декантировали супернатант, содержащий β-глюкозидазу. Avicel, который был связывали с целлюлазусодержащей эндоглюканазой и целлобиогидролазой, ресуспендировали в цитратном буфере (pH 4,8) для гидролиза при 50°C в течение 3 суток. Гидролизат целлюлозы смешивали с 5 Ед./мл целлодекстринфосфорилазы, 5 Ед./л целлобиозофосфорилазы, 5 Ед./мл αGP, 5 Ед./мл PGM и 5 Ед./мл PGI в 100 мМ буфере HEPES (pH 7,2), содержащем 10 мМ фосфата, 5 мМ MgCl2 и 0,5 мМ ZnCl2. Реакцию проводили при 60°C в течение 72 часов и обнаруживали высокие концентрации F6P (небольшие количества глюкозы и без целлобиозы). F6P обнаруживали с использованием сопряженного ферментативного анализа, описанного выше. Глюкозу обнаруживали с использованием набора для анализа с гексокиназой/G6PDH как описано выше.
[98] Пример 6
[99] Для увеличения выход F6Pа из Avicel, Avicel предварительно обрабатывали концентрированной фосфорной кислотой для получения аморфной целлюлозы (RAC), как описано в Zhang et al. A transition from cellulose swelling to cellulose dissolution by o-phosphoric acid: evidence from enzymatic hydrolysis and supramolecular structure. Biomacromolecules 2006; 7:644-648. Для того чтобы удалять β-глюкозидазу из коммерческой целлюлазы, 10 единиц фильтровальной бумаги/мл целлюлазы смешивали с 10 г/л RAC на водно-ледяной бане в течение 5 мин. После центрифугирования при 4°C, декантировали супернатант, содержащий β-глюкозидазу. RAC, которую связывали с целлюлазусодержащей эндоглюканазой и целлобиогидролазой, ресуспендировали в цитратном буфере (pH 4,8) для гидролиза при 50°C в течение 12 часов. Гидролизат RAC смешивали с 5 Ед./мл целлодекстринфосфорилазы, 5 Ед./л целлобиозофосфорилазы, 5 Ед./мл αGP, 5 Ед./мл PGM и 5 Ед./мл PGI в 100 мМ буфере HEPES (pH 7,2), содержащем 10 мМ фосфата, 5 мМ MgCl2 и 0,5 мМ ZnCl2. Реакцию проводили при 60°C в течение 72 часов. Извлекали высокие концентрации F6P и глюкозы, поскольку не добавляли ферменты для того, чтобы превращать глюкозу в F6P. F6P обнаруживали с использованием сопряженного ферментативного анализа, описанного выше. Глюкозу обнаруживали с использованием набора для анализа с гексокиназой/G6PDH, как описано выше.
[100] Пример 7
[101] Для того чтобы дополнительно увеличивать выход F6P из RAC, добавляли полифосфатглюкокиназу и полифосфат. Для того чтобы удалять β-глюкозидазу из коммерческой целлюлазы, 10 единиц фильтровальной бумаги/мл целлюлазы смешивали с 10 г/л RAC на водно-ледяной бане в течение 5 мин. После центрифугирования при 4°C, декантировали супернатант, содержащий β-глюкозидазу. RAC, которую связывали с целлюлазусодержащей эндоглюканазой и целлобиогидролазой, ресуспендировали в цитратном буфере (pH 4,8) для гидролиза при 50°C инкубировали в цитратном буфере (pH 4,8) для гидролиза при 50°C в течение 12 часов. Гидролизат RAC смешивали с 5 Ед./мл полифосфатглюкокиназы, 5 Ед./мл целлодекстринфосфорилазы, 5 Ед./мл целлобиозофосфорилазы, 5 Ед./мл αGP, 5 Ед./мл PGM и 5 Ед./мл PGI в 100 мМ буфере HEPES (pH 7,2), содержащем 50 мМ полифосфата, 10 мМ фосфата, 5 мМ MgCl2 и 0,5 мМ ZnCl2. Реакцию проводили при 50°C в течение 72 часов. F6P обнаруживали в высоких концентрациях при лишь небольших количествах глюкозы, который присутствовали теперь. F6P обнаруживали с использованием сопряженного ферментативного анализа, описанного выше. Глюкозу обнаруживали с использованием набора для анализа с гексокиназой/G6PDH, как описано выше.
[102] Пример 8
[103] Для того чтобы валидировать получение аллюлозы из F6P, 2 г/л F6P смешивали с 1 Ед./мл A6PE и 1 Ед./мл A6PP в 50 мМ буфере HEPES (pH 7,2), содержащем 5 мМ MgCl2 и 80 мкМ CoCl2. Реакцию инкубировали в течение 6 часов при 50°C. 99% превращение F6P в аллюлозу наблюдали через HPLC (Agilent серии 1100) с использованием колонки Agilent Hi-Plex H и детектора показателя преломления. Образец прогоняли в 5 мМ H2SO4 при 0,6 мл/мин.
[104] Пример 9
[105] Для того чтобы валидировать получение аллюлозы из мальтодекстрина, 0,20 мл реакционную смесь, содержащую 20 г/л мальтодекстрина, 50 мМ фосфатно-солевого буфера pH 7,2, 5 мМ MgCl2, 80 мкМ CoCl2, 0,05 Ед. αGP, 0,05 Ед. PGM, 0,05 Ед. PGI, 0,05 Ед. A6PE и 0,05 Ед A6PP, инкубируют при 50°C в течение 24 часов. Реакцию останавливают через фильтрование фермента с использованием концентратора Vivaspin 2 (10000 MWCO). Аллюлозу обнаруживают и количественно определяют с использованием HPLC Agilent серии 1100 с детектором показателя преломления и колонкой Agilent Hi-Plex H. Подвижная фаза представляет собой 5 мМ H2SO4, которая идет 0,6 мл/мин. Стандарты различных концентраций аллюлозы используют для того, чтобы количественно определять выход по изобретению.
[106] Пример 10
Реакционную смесь, содержащую 200 г/л мальтодекстрина, 10 мМ ацетатного буфера (pH 5,5), 5 мМ MgCl2, 80 мкМ CoCl2 и 0,1 г/л изоамилазы, инкубируют при 80°C в течение 24 часов. Это используют для того, чтобы создавать другую реакционную смесь, содержащую 20 г/л обработанного изоамилазой мальтодекстрина, 50 мМ фосфатно-солевого буфера pH 7,2, 5 мМ MgCl2, 0,05 Ед. αGP, 0,05 Ед. PGM, 0,05 Ед. PGI, 0,05 Ед. A6PE и 0,05 Ед. A6PP, инкубируют при 50°C в течение 24 часов. Получение аллюлозы количественно определяют как в примере 9.
[107] Пример 11
Реакционную смесь, содержащую 200 г/л мальтодекстрина, 10 мМ ацетатного буфера (pH 4,5), 5 мМ MgCl2 и разведение пуллуланазы Novozymes D6 1:200 инкубируют при 50°C в течение 4 часов. Это используют для того, чтобы создавать другую реакционную смесь, содержащую 20 г/л обработанного пуллуланазой мальтодекстрина, 50 мМ фосфатно-солевого буфера pH 7,2, 5 мМ MgCl2, 80 мкМ CoCl2, 0,05 Ед. αGP, 0,05 Ед. PGM, 0,05 Ед. PGI, 0,05 Ед. A6PE и 0,05 Ед A6PP, инкубируют при 50°C в течение 24 часов. Получение аллюлозы количественно определяют как в примере 9.
[108] Пример 12
[109] Для того чтобы дополнительно увеличивать выход аллюлозы из мальтодекстрина, 0,05 Ед. 4-глюкантрансферазы (4GT) добавляют в реакцию, описанную в примере 9.
[110] 0,2 мл реакционной смеси, содержащей 20 г/л обработанного изоамилазой мальтодекстрина (см. пример 9), 50 мМ фосфатно-солевого буфера pH 7,2, 5 мМ MgCl2, 80 мкМ CoCl2, 0,05 Ед. αGP, 0,05 Ед. PGM, 0,05 Ед. PGI, 0,05 Ед. A6PE, 0,05 Ед. A6PP и 0,05 Ед. 4GT, инкубируют при 50°C в течение 24 часов. Получение аллюлозы количественно определяют как в примере 9.
[111] Пример 13
[112] Для того чтобы определять диапазон концентраций фосфатно-солевого буфера (PBS), 0,20 мл реакционной смеси, содержащей 50 г/л мальтодекстрина; 6,25 мМ, 12,5 мМ, 25 мМ, 37,5 мМ или 50 мМ фосфатно-солевого буфера pH 7,2; 5 мМ MgCl2; 0,1 Ед. aGP; 0,1 Ед. PGM; и 0,1 Ед. PGI, инкубируют при 50°C в течение 6 часов. Малая длительность гарантирует, что завершения не достигают, и, следовательно, можно ясно видеть различия в эффективности. Получение F6P количественно определяют с использованием сопряженного ферментативного анализа с фруктозо-6-фосфаткиназой (F6PK)/пируватдегидрогеназой (PK)/лактатдегидрогеназой (LD), где снижение поглощения на 340 нм указывает на получение F6P. Соответственно, выход 4,5 г/л, 5,1 г/л, 5,6 г/л, 4,8 г/л или 4,9 г/л F6P получают для реакций, содержащих 6,25 мМ, 12,5 мМ, 25 мМ, 37,5 мМ или 50 мМ фосфатно-солевого буфера pH 7,2 (таблица 1). Эти результаты показывают, что концентрация 25 мМ PBS pH 7,2 идеальна для этих конкретных условий реакции. Важно отметить, что даже использование 6,25 мМ PBS при pH 7,2 ведет к значительному обороту из-за повторного использования фосфата. Это показывает, что раскрытые способы повторного использования фосфата позволяют сохранять низкие уровни фосфата даже при промышленных уровнях производительности по объему (например, 200-300 г/л мальтодекстрина).
Таблица 1
[113] Пример 14
[114] Для того чтобы определять диапазон pH каскадной реакции, 0,20 мл реакционной смеси, содержащей 50 г/л мальтодекстрина; 50 мМ фосфатно-солевого буфера pH 6,0, 6,2, 6,4, 6,6, 6,8, 7,0 7,2 или 7,3; 5 мМ MgCl2; 0,02 Ед. αGP; 0,02 Ед. PGM; и 0,02 Ед. PGI, инкубируют при 50°C в течение 16 часов. Единицы снижают, чтобы гарантировать, что не завершения достигают, и, следовательно, можно ясно видеть различия в эффективности. Получение F6P количественно определяют как в примере 12. Соответственно, выход 4,0 г/л, 4,1 г/л 4,2 г/л, 4,1 г/л, 4,4 г/л, 4,1 г/л, 3,8 г/л или 4,0 г/л F6P получали для реакций, содержащих 50 мМ фосфатно-солевого буфера при pH 6,0, 6,2, 6,4, 6,6, 6,8, 7,0, 7,2 или 7,3 (таблица 2). Эти результаты показывают, что pH 6,8 идеален для этих конкретных условий реакции, несмотря на то, что система работает в широком диапазоне pH.
Таблица 2
[115] Пример 15
[116] Чтобы исследовать масштабирование, 20 мл реакционной смеси, содержащей 50 г/л обработанного изоамилазой мальтодекстрина (см. пример 10), 50 мМ фосфатно-солевого буфера pH 7,2, 5 мМ MgCl2, 80 мкМ CoCl2, 10 Ед. αGP, 10 Ед. PGM, 10 Ед. PGI, 10 Ед. A6PE и 10 Ед. A6PP, инкубируют при 50°C в течение 24 часов. Получение аллюлозы количественно определяли, как в примере 9.
[117] Пример 16
[118] Для того чтобы дополнительно увеличивать выход аллюлозы из мальтодекстрина, 0,05 Ед. мальтозофосфорилазы добавляют в реакцию, описанную в примере 9.
[119] Пример 17
[120] Для того чтобы дополнительно увеличивать выход аллюлозы из мальтодекстрина, 0,05 Ед. полифосфатглюкокиназа и 75 мМ полифосфата добавляют в реакцию, описанную в примере 9.
[121] Пример 18
[122] Для получения аллюлозы из фруктозы, реакционную смесь, содержащую 10 г/л фруктозы, 50 мМ буфера Tris pH 7,0, 75 мМ полифосфата, 5 мМ MgCl2, 80 мкМ CoCl2, 0,05 Ед. фруктозополифосфаткиназы, 0,05 Ед. A6PE и 0,05 Ед. A6PP, инкубируют при 50°C в течение 24 часов. Получение аллюлозы количественно определяют как в примере 9.
[123] Пример 19
[124] Для получения аллюлозы из глюкозы, реакционную смесь, содержащую 10 г/л глюкозы, 50 мМ буфера Tris pH 7,0, 75 мМ полифосфата, 5 мМ MgCl2, 80 мкМ CoCl2, 0,05 Ед. глюкозополифосфаткиназы, 0,05 Ед. PGI, 0,05 Ед. A6PE и 0,05 Ед. A6PP, инкубируют при 50°C в течение 24 часов. Получение аллюлозы количественно определяют как в примере 9.
[125] Пример 20
[126] Для получения аллюлозы из сахарозы, реакционную смесь, содержащую 10 г/л сахарозы, 50 мМ фосфатно-солевого буфера pH 7,0, 5 мМ MgCl2, 80 мкМ CoCl2, 0,05 Ед. сахарозофосфорилазы, 0,05 PGM, 0,05 Ед. PGI, 0,05 Ед. A6PE и 0,05 Ед. A6PP, инкубируют при 50°C в течение 24 часов. Получение аллюлозы количественно определяют как в примере 9.
[127] Пример 21
[128] Для того чтобы дополнительно увеличивать выход аллюлозы из сахарозы, 75 мМ полифосфата и 0,05 полифосфатфруктокиназы добавляют в реакционную смесь в примере 20. Получение аллюлозы количественно определяют как в примере 9.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> BONUMOSE LLC
<120> ФЕРМЕНТАТИВНОЕ ПОЛУЧЕНИЕ D-АЛЛЮЛОЗЫ
<130> 146.0003-WO00
<140> PCT/US17/66298
<141> 2017-12-14
<150> 62/434,033
<151> 2016-12-14
<160> 9
<170> PatentIn версии 3.5
<210> 1
<211> 663
<212> ДНК
<213> Thermoanaerobacterium thermosaccharolyticum
<400> 1
atgaaatatt tattttcgcc atctttaatg tgtatgaatt taatcaagct aaatgaacaa 60
atatctgttc ttaatagcaa ggcggatttt ttgcatgttg acatcatgga tggccatttt 120
gttaaaaata ttactttatc accgtttttt atagagcaga ttaaatcata tgtcaatatt 180
cctattgatg cacaccttat ggtagaaaat ccaggtgatt atattgaaat atgcgaaaaa 240
tcgggagcaa gttttataac tatacatgca gaaacaatta atagagaagc atttagaata 300
atagatagaa ttaaaagtca tggactcatg gttggcatag cattgaatcc agcaacacct 360
atttcggaaa ttaaacatta tattaataaa atagataaga taacaataat gactgtcgat 420
cccggcttcg ctggtcaacc atttattccg gaggtattgg aaaagatccg agatctaaag 480
agactgaaag atgataataa ttataattat ttaattgaag cagatggttc ctgcaataaa 540
aatacgtttc aagtgctaaa agatgccgga tgtaaagttt tcgtattagg ttcatcaggg 600
ctttttaatc ttagcgatga tttgggaaaa gcgtgggaaa taatgattgg caattttaat 660
gga 663
<210> 2
<211> 663
<212> ДНК
<213> Искусственная последовательность
<220>
<223> A6PE из Thermoanaerobacterium thermosaccharolyticum
с оптимизацией кодонов
<400> 2
atgaagtacc tgtttagccc gagcctgatg tgcatgaatc tgattaagct gaatgaacag 60
attagcgttc tgaatagcaa agccgatttt ctgcatgttg atattatgga tggtcatttt 120
gttaagaaca tcaccctgag cccgtttttc attgaacaga ttaagagcta tgtgaatatc 180
ccgattgatg cccatctgat ggtggaaaat ccgggtgact atattgaaat ttgtgaaaaa 240
agcggcgcaa gttttattac cattcatgcc gaaaccatta atcgtgaagc atttcgtatt 300
attgaccgta ttaagagtca tggtctgatg gtgggcattg cactgaatcc ggccaccccg 360
attagcgaaa ttaagcatta tattaacaag atcgacaaga tcaccattat gaccgttgat 420
ccgggctttg caggccagcc gtttattccg gaagtgctgg aaaaaattcg cgatctgaaa 480
cgtctgaaag atgataataa ttacaactac ctgatcgaag ccgatggtag ttgcaataag 540
aatacctttc aggttctgaa agatgcaggc tgcaaagttt ttgtgctggg cagtagcggt 600
ctgtttaatc tgagtgatga tctgggcaaa gcatgggaaa ttatgattgg caattttaat 660
ggc 663
<210> 3
<211> 221
<212> Белок
<213> Thermoanaerobacterium thermosaccharolyticum
<400> 3
Met Lys Tyr Leu Phe Ser Pro Ser Leu Met Cys Met Asn Leu Ile Lys
1 5 10 15
Leu Asn Glu Gln Ile Ser Val Leu Asn Ser Lys Ala Asp Phe Leu His
20 25 30
Val Asp Ile Met Asp Gly His Phe Val Lys Asn Ile Thr Leu Ser Pro
35 40 45
Phe Phe Ile Glu Gln Ile Lys Ser Tyr Val Asn Ile Pro Ile Asp Ala
50 55 60
His Leu Met Val Glu Asn Pro Gly Asp Tyr Ile Glu Ile Cys Glu Lys
65 70 75 80
Ser Gly Ala Ser Phe Ile Thr Ile His Ala Glu Thr Ile Asn Arg Glu
85 90 95
Ala Phe Arg Ile Ile Asp Arg Ile Lys Ser His Gly Leu Met Val Gly
100 105 110
Ile Ala Leu Asn Pro Ala Thr Pro Ile Ser Glu Ile Lys His Tyr Ile
115 120 125
Asn Lys Ile Asp Lys Ile Thr Ile Met Thr Val Asp Pro Gly Phe Ala
130 135 140
Gly Gln Pro Phe Ile Pro Glu Val Leu Glu Lys Ile Arg Asp Leu Lys
145 150 155 160
Arg Leu Lys Asp Asp Asn Asn Tyr Asn Tyr Leu Ile Glu Ala Asp Gly
165 170 175
Ser Cys Asn Lys Asn Thr Phe Gln Val Leu Lys Asp Ala Gly Cys Lys
180 185 190
Val Phe Val Leu Gly Ser Ser Gly Leu Phe Asn Leu Ser Asp Asp Leu
195 200 205
Gly Lys Ala Trp Glu Ile Met Ile Gly Asn Phe Asn Gly
210 215 220
<210> 4
<211> 690
<212> ДНК
<213> Bacillus thermoamylovorans
<400> 4
atgagcaaca aaattgaatt ttcaccgtct ttaatgacaa tggatttaga caagtttaaa 60
gaacagatta cttttttaaa taatcatgtc ggttcttacc atatcgatat tatggacgga 120
cattatgtac ctaatataac tctatcccct tggtttgtcc aagaggtacg gaaaattagt 180
gatgttccga tgtctgccca cttgatggtc acaaacccaa gtttttgggt acaacaactc 240
attgatatta agtgtgaatg gatttgcatg cacgtagaaa cccttgatgg gttagctttc 300
cgcttaattg atcaaatcca cgatgcggga ttaaaagcag gggtcgtatt aaatcctgaa 360
acaagtgttg atgcgattcg cccgtacatt gatttagtgg ataaagtcac cattatgact 420
gtcgacccag gttttgcagg tcaacgcttt attgatagta cattggagaa aatcgtggaa 480
ttaagaaaat tacgggaaga acacggttat aaatatgtga ttgaaatgga tggatcttcg 540
aatcggaaat ccttcaagaa aatttatgaa gccggtcctg acatttatat tataggtcgc 600
agcggtttgt ttggattaca cgaagatatc gaaaaagcat gggaaatcat gtgcaaagat 660
tttgaggaaa tgactggcga aaaagtatta 690
<210> 5
<211> 690
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Термофильная A6PE из Bacillus thermoamylovorans
с оптимизацией кодонов
<400> 5
atgagtaaca agatcgaatt cagcccgagc ctgatgacca tggatctgga taaatttaaa 60
gaacagatca cctttctgaa caatcatgtt ggcagttatc atattgatat catggatggt 120
cattacgtgc cgaatattac cctgagcccg tggtttgttc aggaagtgcg caaaattagc 180
gatgttccga tgagcgcaca tctgatggtt accaatccga gtttttgggt tcagcagctg 240
attgatatta aatgtgaatg gatttgcatg catgttgaaa ccctggatgg cctggccttt 300
cgtctgattg atcagattca tgatgccggc ctgaaagcag gtgtggttct gaatccggaa 360
accagtgtgg atgccattcg tccgtatatt gatctggttg ataaagttac catcatgacc 420
gtggatccgg gctttgccgg ccagcgcttt attgatagca ccctggaaaa aattgtggaa 480
ctgcgtaaac tgcgtgaaga acatggttat aaatatgtga ttgagatgga tggcagcagc 540
aatcgcaaaa gctttaaaaa aatttacgag gcaggtccgg atatttatat tattggccgt 600
agtggcctgt ttggcctgca tgaagatatt gaaaaagcat gggaaattat gtgtaaggat 660
tttgaagaaa tgaccggtga aaaagtgctg 690
<210> 6
<211> 230
<212> Белок
<213> Bacillus thermoamylovorans
<400> 6
Met Ser Asn Lys Ile Glu Phe Ser Pro Ser Leu Met Thr Met Asp Leu
1 5 10 15
Asp Lys Phe Lys Glu Gln Ile Thr Phe Leu Asn Asn His Val Gly Ser
20 25 30
Tyr His Ile Asp Ile Met Asp Gly His Tyr Val Pro Asn Ile Thr Leu
35 40 45
Ser Pro Trp Phe Val Gln Glu Val Arg Lys Ile Ser Asp Val Pro Met
50 55 60
Ser Ala His Leu Met Val Thr Asn Pro Ser Phe Trp Val Gln Gln Leu
65 70 75 80
Ile Asp Ile Lys Cys Glu Trp Ile Cys Met His Val Glu Thr Leu Asp
85 90 95
Gly Leu Ala Phe Arg Leu Ile Asp Gln Ile His Asp Ala Gly Leu Lys
100 105 110
Ala Gly Val Val Leu Asn Pro Glu Thr Ser Val Asp Ala Ile Arg Pro
115 120 125
Tyr Ile Asp Leu Val Asp Lys Val Thr Ile Met Thr Val Asp Pro Gly
130 135 140
Phe Ala Gly Gln Arg Phe Ile Asp Ser Thr Leu Glu Lys Ile Val Glu
145 150 155 160
Leu Arg Lys Leu Arg Glu Glu His Gly Tyr Lys Tyr Val Ile Glu Met
165 170 175
Asp Gly Ser Ser Asn Arg Lys Ser Phe Lys Lys Ile Tyr Glu Ala Gly
180 185 190
Pro Asp Ile Tyr Ile Ile Gly Arg Ser Gly Leu Phe Gly Leu His Glu
195 200 205
Asp Ile Glu Lys Ala Trp Glu Ile Met Cys Lys Asp Phe Glu Glu Met
210 215 220
Thr Gly Glu Lys Val Leu
225 230
<210> 7
<211> 651
<212> ДНК
<213> Clostridium thermocellum
<400> 7
atgattaaat acaaagcggt attctttgat tttgactata cgctggcaga ttcatctaaa 60
gctgttatag aatgtattaa ctatgcactg caaaaaatgg gttatcccga atcttctccg 120
gaaagtattt gcagaacaat aggacttacg ttggccgagg cttttaaaat acttagcggg 180
gatacttctg attccaatgc ggaccttttc cgccaatact ttaaagaaag agcagatctg 240
gttatgtgtg accggactgt aatgtacagc actgttgaat gtgttttgaa gaagctgaaa 300
aaggcggatg taaaaacagg aattgtttca acgaagtaca gatacaggat agaggatata 360
ttaaaaaggg acaaactttt acagtatttt gatgtaattg tcggcgggga agatgttgcg 420
gcccataaac cggatccgga agggcttcta aaggccatat cgatggttgg ctgccaaaag 480
gaagaagtcc tttttgtcgg agacagtacg gtggatgcaa ggactgcaaa aaatgcggga 540
gtggattttg tggcggttct tacggggaca accggggcaa atgagttttc agagtataat 600
cctggtgctg tgattgaaga tttgagtggt ttattggata tgtttatgtt a 651
<210> 8
<211> 651
<212> ДНК
<213> Искусственная последовательность
<220>
<223> A6PP из Clostridium thermocellum с оптимизацией кодонов
<400> 8
atgatcaagt acaaggccgt tttttttgat tttgattaca ccctggcaga tagcagcaaa 60
gccgttattg aatgtattaa ttacgccctg cagaaaatgg gctatccgga aagcagtccg 120
gaaagcattt gtcgtaccat tggcctgacc ctggcagaag catttaaaat tctgagcggt 180
gataccagcg atagcaatgc cgatctgttt cgccagtatt ttaaagaacg cgcagatctg 240
gttatgtgtg atcgcaccgt gatgtatagc accgtggaat gcgtgctgaa aaaactgaaa 300
aaagcagatg ttaagaccgg tattgtgagc accaaatatc gctatcgtat tgaagatatt 360
ctgaaacgtg ataaactgct gcagtatttt gatgttattg ttggtggcga agatgttgcc 420
gcccataaac cggatccgga aggcctgctg aaagcaatta gcatggtggg ctgccagaaa 480
gaagaagttc tgtttgttgg tgatagcacc gttgatgcac gtaccgccaa aaatgcaggc 540
gtggattttg tggccgttct gaccggcacc accggcgcaa atgaatttag cgaatataat 600
ccgggcgccg tgattgaaga tctgagcggt ctgctggata tgtttatgct g 651
<210> 9
<211> 217
<212> Белок
<213> Clostridium thermocellum
<400> 9
Met Ile Lys Tyr Lys Ala Val Phe Phe Asp Phe Asp Tyr Thr Leu Ala
1 5 10 15
Asp Ser Ser Lys Ala Val Ile Glu Cys Ile Asn Tyr Ala Leu Gln Lys
20 25 30
Met Gly Tyr Pro Glu Ser Ser Pro Glu Ser Ile Cys Arg Thr Ile Gly
35 40 45
Leu Thr Leu Ala Glu Ala Phe Lys Ile Leu Ser Gly Asp Thr Ser Asp
50 55 60
Ser Asn Ala Asp Leu Phe Arg Gln Tyr Phe Lys Glu Arg Ala Asp Leu
65 70 75 80
Val Met Cys Asp Arg Thr Val Met Tyr Ser Thr Val Glu Cys Val Leu
85 90 95
Lys Lys Leu Lys Lys Ala Asp Val Lys Thr Gly Ile Val Ser Thr Lys
100 105 110
Tyr Arg Tyr Arg Ile Glu Asp Ile Leu Lys Arg Asp Lys Leu Leu Gln
115 120 125
Tyr Phe Asp Val Ile Val Gly Gly Glu Asp Val Ala Ala His Lys Pro
130 135 140
Asp Pro Glu Gly Leu Leu Lys Ala Ile Ser Met Val Gly Cys Gln Lys
145 150 155 160
Glu Glu Val Leu Phe Val Gly Asp Ser Thr Val Asp Ala Arg Thr Ala
165 170 175
Lys Asn Ala Gly Val Asp Phe Val Ala Val Leu Thr Gly Thr Thr Gly
180 185 190
Ala Asn Glu Phe Ser Glu Tyr Asn Pro Gly Ala Val Ile Glu Asp Leu
195 200 205
Ser Gly Leu Leu Asp Met Phe Met Leu
210 215
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ФЕРМЕНТАТИВНОЕ ПОЛУЧЕНИЕ ГЕКСОЗ | 2018 |
|
RU2766710C2 |
| ФЕРМЕНТАТИВНОЕ ПОЛУЧЕНИЕ ТАГАТОЗЫ | 2019 |
|
RU2820606C2 |
| ФЕРМЕНТАТИВНОЕ ПОЛУЧЕНИЕ D-ТАГАТОЗЫ | 2016 |
|
RU2749811C1 |
| НОВАЯ ПОЛИФОСФАТ-ЗАВИСИМАЯ ГЛЮКОКИНАЗА И СПОСОБ ПОЛУЧЕНИЯ ГЛЮКОЗО-6-ФОСФАТА С ЕЕ ИСПОЛЬЗОВАНИЕМ | 2017 |
|
RU2730602C2 |
| МУЛЬТИФУНКЦИОНАЛЬНЫЙ МУЛЬТИСПЕЦИФИЧЕСКИЙ МУЛЬТИМЕРНЫЙ БИОМОЛЕКУЛЯРНЫЙ ПОЛИМЕР, ИМЕЮЩИЙ ПРОЛОНГИРОВАННУЮ ЭФФЕКТИВНОСТЬ IN VIVO | 2020 |
|
RU2805307C1 |
| ФЕРМЕНТАТИВНЫЙ СПОСОБ ПОЛУЧЕНИЯ МОДИФИЦИРОВАННЫХ ХМЕЛЕПРОДУКТОВ | 2019 |
|
RU2816511C2 |
| НОВАЯ ПСИКОЗО-6-ФОСФАТ ФОСФАТАЗА, КОМПОЗИЦИЯ ДЛЯ ПОЛУЧЕНИЯ ПСИКОЗЫ, СОДЕРЖАЩАЯ УКАЗАННЫЙ ФЕРМЕНТ, СПОСОБ ПОЛУЧЕНИЯ ПСИКОЗЫ С ИСПОЛЬЗОВАНИЕМ УКАЗАННОГО ФЕРМЕНТА | 2018 |
|
RU2757229C2 |
| РЕКОМБИНАНТНОЕ ПОЛУЧЕНИЕ СТЕВИОЛ-ГЛИКОЗИДОВ | 2014 |
|
RU2741103C2 |
| Композиции для получения глюкозных сиропов | 2015 |
|
RU2706297C2 |
| МОДИФИЦИРОВАННЫЕ МИТОХОНДРИИ И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2811467C2 |

Изобретение относится к биотехнологии. Предложен способ получения аллюлозы, включающий превращение фруктозо-6-фосфата (F6P) в аллюлозо-6-фосфат (A6P), катализируемое с помощью аллюлозо-6-фосфат-3-эпимеразы(A6PE); и превращение получаемого A6P в аллюлозу, катализируемое с помощью аллюлозо-6-фосфат-фосфатазы(A6PP). При этом А6РЕ содержит аминокислотную последовательность, имеющую по меньшей мере 55% идентичность последовательности SEQ ID NO: 3 или 6, и А6РР содержит аминокислотную последовательность, имеющую по меньшей мере 55% идентичность последовательности SEQ ID NO: 9. Изобретение обеспечивает эффективное получение аллюлозы. 16 з.п. ф-лы, 7 ил., 2 табл., 21 пр.
1. Способ получения аллюлозы, где способ включает:
превращение фруктозо-6-фосфата (F6P) в аллюлозо-6-фосфат (A6P), катализируемое с помощью аллюлозо-6-фосфат-3-эпимеразы(A6PE); и
превращение получаемого A6P в аллюлозу, катализируемое с помощью аллюлозо-6-фосфат-фосфатазы(A6PP), где А6РЕ содержит аминокислотную последовательность, имеющую по меньшей мере 55% идентичность последовательности SEQ ID NO: 3 или 6, и А6РР содержит аминокислотную последовательность, имеющую по меньшей мере 55% идентичность последовательности SEQ ID NO: 9.
2. Способ по п. 1, который дополнительно включает стадию превращения глюкозо-6-фосфата (G6P) в F6P, где стадию катализируют с помощью фосфоглюкоизомеразы (PGI).
3. Способ по п. 2, который дополнительно включает стадию превращения глюкозо-1-фосфата (G1P) в G6P, где стадию катализируют с помощью фосфоглюкомутазы (PGM).
4. Способ по п. 3, который дополнительно включает стадию превращения сахарида в G1P, где стадию катализируют с помощью по меньшей мере одного фермента, выбранного из группы, состоящей из α-глюканфосфорилазы (αGP), мальтозофосфорилазы, сахарозофосфорилазы, целлодекстринфосфорилазы, целлобиозофосфорилазы и целлюлозофосфорилазы, где сахарид выбирают из группы, состоящей из крахмала или его производного, целлюлозы или его производного и сахарозы.
5. Способ по п. 4, в котором сахарид представляет собой крахмал или его производное, выбранные из группы, состоящей из амилозы, амилопектина, растворимого крахмала, амилодекстрина, мальтодекстрина, мальтозы и глюкозы.
6. Способ по п. 5, который дополнительно включает стадию превращения крахмала в производное крахмала, где производное крахмала получают с помощью ферментативного гидролиза крахмала или посредством кислотного гидролиза крахмала.
7. Способ по п. 5, который включает добавление 4-глюкантрансферазу (4GT).
8. Способ по п. 6, в котором производное крахмала получают с помощью ферментативного гидролиза крахмала, катализируемого с помощью изоамилазы, пуллуланазы, α-амилазы или их сочетания.
9. Способ по п. 1, который дополнительно включает:
стадию превращения фруктозы в F6P, где стадию катализируют с помощью полифосфатфруктокиназы (PPFK); и необязательно стадию превращения сахарозы во фруктозу, где стадию катализируют с помощью сахарозофосфорилазы (SP).
10. Способ по п. 2, который дополнительно включает:
стадию превращения глюкозы в G6P, где стадию катализируют с помощью полифосфатфруктокиназы (PPFK), и необязательно стадию превращения сахарозы в глюкозу, где стадию катализируют с помощью сахарозофосфорилазы (SP).
11. Способ по п. 1, в котором A6PE содержит аминокислотную последовательность, обладающую по меньшей мере 90%, по меньшей мере 95%, или по меньшей мере 100% идентичностью последовательностей с SEQ ID №№ 3 или 6.
12. Способ по п. 1, в котором A6PE содержит домен (α/β)8-бочонка для катализа, Ser на конце 7-го β-тяжа бочонка, Ser на конце 8-го β-тяжа бочонка, Gly в петле активного центра, His во 2-м и 3-м β-тяжах бочонка, Asp во 2-м и 7-м β-тяже бочонка и сигнатуру His-гидрофобный остаток-Asp во 2-м β-тяже бочонка.
13. Способ по п. 1, в котором A6PP содержит аминокислотную последовательность, обладающую по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 100% идентичностью последовательностей с SEQ ID № 9.
14. Способ по п. 1, в котором A6PP содержит домен с Россман-подобной укладкой для катализа, домен кэппирования C1, сигнатуру DxD в 1-м β-тяже Россман-подобной укладки, Thr или Ser на конце 2-го β-тяжа Россман-подобной укладки, Lys на N-α-спирали ближе к C-концу относительно 3-го β-тяжа Россман-подобной укладки и сигнатуру GDxxxD на конце 4-го β-тяжа Россман-подобной укладки.
15. Способ по любому одному из пп. 1-14, в котором стадии способа проводят при температуре в диапазоне от приблизительно 37 °C приблизительно до 85°C, при pH в диапазоне от приблизительно 5,0 приблизительно до 8,0 и/или в течение от приблизительно 8 часов приблизительно до 48 часов.
16. Способ по любому одному из пп. 1-14, в котором стадии способа проводят в одном биореакторе или во множестве биореакторов, расположенных последовательно.
17. Способ по любому одному из пп. 1-14, в котором стадии способа проводят без АТФ, без NAD(H), при концентрации фосфата приблизительно от 0 мМ приблизительно до 150 мМ, и/или фосфат используют повторно.
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| CHAN K.K | |||
| et al | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Biochemistry | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| LONDON N | |||
| et al | |||
| Covalent docking predicts substrates for haloalkanoate dehalogenase superfamily | |||
Авторы
Даты
2024-05-23—Публикация
2017-12-14—Подача