Изобретение относится к способу синтеза аминофеноксибензойных кислот, в частности к получению 4-(3-амино-4-нитрофенокси)бензойной кислоты под действием ультразвука,
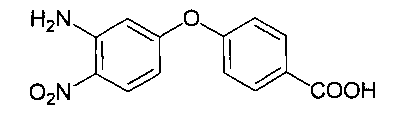
которая используется в качестве полупродукта в синтезе мономера АБ-типа для термостабильных полимерных материалов (US 4414383, 8.11.1983; US 4483977, 20.11.1984; US 5374706, 20.12.1994; А.Ю. Лейкин, А.Л. Русанов, Р.С. Бегунов, А.И. Фоменков. Синтез и свойства поли-2-(4′-оксифенилен)-5-бензимидазола и протонпроводящей мембраны на его основе // Высокомолек. соед. С. 2009. Т. 51. №7. С. 1264-1268).
Известен трехстадийный способ получения 4-(3-амино-4-нитрофенокси)бензойной кислоты (Патент 2409554 РФ, Бегунов Р.С., Зубишина А.А.), включающий следующие стадии: ацилирование 2-нитро-5-хлоранилина уксусным ангидридом при температуре 90°С в течение 1 ч, нуклеофильное замещение атома хлора, при взаимодействии с 4-гидроксибензойной кислотой в ДМСО в присутствии K2CO3 при температуре 105°С в течении 8 ч, снятие ацильной защиты аминогруппы в результате щелочного гидролиза при температуре 60°С в течении 0.5 ч.
Недостатками известного способа синтеза 4-(3-амино-4-нитрофенокси)бензойной кислоты являются: продолжительное время протекания реакции ароматического нуклеофильного замещения, а также необходимость дополнительных стадий ацилирования 2-нитро-5-хлоранилина и гидролиза ацетамидной связи в 4-(3-ацетамидо-4-нитрофенокси)бензойной кислоте, что увеличивает операционное время процесса, а также приводит к снижению суммарного выхода целевого продукта и его степени чистоты.
Цель изобретения - сокращение количества стадий, уменьшение времени и температуры реакции ароматического нуклеофильного замещения, повышение выхода 4-(3-амино-4-нитрофенокси)бензойной кислоты.
Поставленная цель достигается тем, что процесс замещения галогена в 2-нитро-5-хлоранилине осуществляют при ультразвуковой активации. Причем ароматическое нуклеофильное замещение атома хлора проводят в ДМСО в присутствии K2CO3 при частоте ультразвука, равной 37 кГц, при температуре 80°С в течении 2 ч и мольном соотношении 2-нитро-5-хлоранилин : 4-гидроксибензойная кислота = 1:1.05.
Реализация предложенной схемы синтеза 4-(3-амино-4-нитрофенокси)бензойной кислоты позволяет сократить количество стадий с трех до одной, уменьшить время с 8 ч до 2 ч и температуру с 105°С до 80°С процесса ароматического нуклеофильного замещения и получить целевой продукт с выходом 95%.
Строение и чистоту промежуточных соединений и целевых продуктов анализировали методами ЯМР 1Н - и масс-спектрометрии, определением температуры плавления и элементного состава.
Изобретение иллюстрируется следующим примером.
Пример. 4-(3-амино-4-нитрофенокси)бензойная кислота
17.3 г (0.100 моль) 5-хлор-2-нитроанилина, 14.5 г (0.105 моль) 4-гидроксибензойной кислоты и 43.5 г (0.315 моль) K2CO3 в 200 мл ДМСО подвергается воздействию ультразвука при температуре 80°С в течение 2 ч. После охлаждения реакционная смесь выливается в воду и обрабатывается уксусной кислотой до рН=6, выпавший осадок отфильтровывается. Выход 26.0 г (95%), Тпл=243-245°С.
Найдено %: С 57.06; Н 3.61; N 10.19. C13H10N2O5.
Вычислено %: С 56.93; Н 3.65; N 10.22.
Спектр ЯМР 1Н, δ, м.д.: 6.30 (дц) (1Н, Н6′, J=10.0 Гц, J=1.0 Гц), 6.35 (д) (1H, Н2′, J=1.5 Гц), 7.00 (д) (2Н, Н3,5, J=9.5 Гц), 7.55 (с) (2Н, NH2), 7.90 (д) (2Н, Н2,6, J=10.0 Гц), 8.00 (д) (1Н, Н5′, J=10.0 Гц), 13.00 (с) (1H, СООН). Масс-спектр, m/z (Iотн, %): 274 (84) [М]+, 227 (37), 123 (100), 90 (89), 76 (92).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 4-(3,4-ДИАМИНОФЕНОКСИ)БЕНЗОЙНОЙ КИСЛОТЫ | 2009 |
|
RU2409554C1 |
| СПОСОБ ПОЛУЧЕНИЯ СЛОЖНЫХ ЭФИРОВ 4-(3,4-ДИАМИНОФЕНОКСИ)БЕНЗОЙНОЙ КИСЛОТЫ | 2009 |
|
RU2409555C1 |
| СПОСОБ ПОЛУЧЕНИЯ 4-{4-АМИНО-2-ХЛОРО-5-[(5-ХЛОРО-2-МЕТИЛ-1Н-БЕНЗИМИДАЗОЛ-6-ИЛ)АМИНО]ФЕНОКСИ}БЕНЗОЙНОЙ КИСЛОТЫ | 2012 |
|
RU2506259C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРГИДРАТА 1,3-БИС(3,4-ДИАМИНОФЕНОКСИ)БЕНЗОЛА | 2010 |
|
RU2439052C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,3- И 1,4-БИС(2-АМИНО-4-(ТРИФТОРМЕТИЛ)ФЕНОКСИ)БЕНЗОЛА | 2011 |
|
RU2453533C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,2-БИС[4-(4-НИТРОФЕНОКСИ)ФЕНИЛ]ГЕКСАФТОРПРОПАНА ПОД ДЕЙСТВИЕМ УЛЬТРАЗВУКА | 2015 |
|
RU2577544C1 |
| Способ получения N-[2-амино-4-(трифторметил)фенил]-N-фенил-4-(трифторметил)бензол-1,2-диамина и его производных | 2016 |
|
RU2645922C2 |
| Способ получения полиядерных тетрааминов, содержащих мостиковые атомы | 2018 |
|
RU2691737C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,4-БИС(2-АМИНО-4-(ТРИФТОРМЕТИЛ)ФЕНИЛ)ПИПЕРАЗИНА | 2011 |
|
RU2448962C1 |
| Способ совместного получения 1-(2-амино-4-R-фенил)- и 2-(2-амино-4-R-фенил)бензотриазолов | 2023 |
|
RU2825731C1 |
Изобретение относится к способу получения 4-(3-амино-4-нитрофенокси)бензойной кислоты указанной ниже формулы под действием ультразвука. Способ включает процесс замещения галогена в 2-нитро-5-хлоранилине при взаимодействии с 4-гидроксибензойной кислотой в ДМСО в присутствии K2CO3 при ультразвуковой активации. При этом ароматическое нуклеофильное замещение атома хлора проводят в ДМСО в присутствии K2CO3 при частоте ультразвука, равной 37 кГц, при температуре 80°С в течение 2 ч и мольном соотношении 2-нитро-5-хлоранилин:4-гидроксибензойная кислота=1:1.05. Предлагаемый способ позволяет сократить количество стадий, уменьшить продолжительность и температуру реакции ароматического нуклеофильного замещения, а также повысить выход целевого продукта. 1 пр.
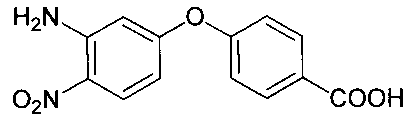
Способ получения 4-(3-амино-4-нитрофенокси)бензойной кислоты

под действием ультразвука, включающий процесс замещения галогена в 2-нитро-5-хлоранилине при взаимодействии с 4-гидроксибензойной кислотой в ДМСО в присутствии K2CO3 при ультразвуковой активации, причем ароматическое нуклеофильное замещение атома хлора проводят в ДМСО в присутствии K2CO3 при частоте ультразвука, равной 37 кГц, при температуре 80°С в течение 2 ч и мольном соотношении 2-нитро-5-хлоранилин:4-гидроксибензойная кислота=1:1.05.
| СПОСОБ ПОЛУЧЕНИЯ СЛОЖНЫХ ЭФИРОВ 4-(3,4-ДИАМИНОФЕНОКСИ)БЕНЗОЙНОЙ КИСЛОТЫ | 2009 |
|
RU2409555C1 |
| СПОСОБ ПОЛУЧЕНИЯ 4-(3,4-ДИАМИНОФЕНОКСИ)БЕНЗОЙНОЙ КИСЛОТЫ | 2009 |
|
RU2409554C1 |
| Р.С | |||
| БЕГУНОВ И ДР., Новый подход к синтезу 4-(3,4-диаминофенокси)бензойной кислоты и ее сложных эфиров, БАШКИРСКИЙ ХИМИЧЕСКИЙ ЖУРНАЛ, 2011, 18(3), 116-119. | |||
Авторы
Даты
2016-03-20—Публикация
2015-03-11—Подача