Изобретение относится к способу синтеза полиядерных opwo-фенилендиаминов, в частности к получению 4-(3,4-диаминофенокси)бензойной кислоты,
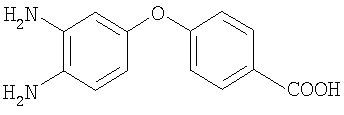
которая используется при синтезе термостабильных полимерных материалов (US 4414383, 8.11.1983; US 4431796,14.02.1984; US 4452971, 5.06.1984; US 4483977, 20.11.1984).
Цель изобретения - создание высокоэффективного способа синтеза 4-(3,4-диаминофенокси)бензойной кислоты, позволяющего минимизировать операционное время процесса и получать целевой продукт с высоким выходом и высокой степени чистоты.
Поставленная цель достигается тем, что в качестве исходного субстрата используется 2-нитро-5-хлоранилин. В результате отпадает необходимость в проведении дополнительных стадий нитрования и восстановления. Для уменьшения времени и температуры процесса нуклеофильного замещения галогена в 2-нитро-5-хлоранилине проводится снижение дезактивирующего влияния аминогруппы путем ее ацилирования. В качестве восстанавливающего агента используется SnCl2·H2O, что позволяет осуществлять процесс восстановления при невысокой температуре в течение 1 ч. Причем ацилирование 2-нитро-5-хлоранилина проводят при температуре 90°С в течение 1 ч и мольном соотношении 2-нитро-5-хлоранилин:уксусный ангидрид =1:1.5, нуклеофильное замещение атома хлора проводят в ДМСО в присутствии К2СО в течение 8 часов при температуре 105°С и мольном соотношении N-ацетил-5-хлор-2-нитроанилин:4-гидроксибензойная кислота =1:1.05, снятие ацильной защиты осуществляют в течение 0.5 часа при температуре 60°С в 20% водном растворе КОН, восстановление 4-(3-амино-4-нитрофенокси)бензойной кислоты проводят SnCl2·2H2O при температуре 90°С в течение 1 ч в концентрированной соляной кислоте и мольном соотношении 4-(3-амино-4-нитрофенокси)бензойная кислота: SnCl2·2H2O=1:3.35. Реализация предложенной схемы получения 4-(3,4-диаминофенокси)бензойной кислоты позволяет получать целевой продукт с суммарным выходом 76.25%.
Строение и чистоту промежуточных соединений и целевых продуктов анализировали методами ЯМР 1Н- и масс-спектрометрии, определением температуры плавления и элементного состава.
Изобретение иллюстрируется следующими примерами.
Пример 1. N-ацетил-5-хлор-2-нитроанилин
17.3 г (0.1 моль) 5-хлор-2-нитроанилина и 18.9 мл (0.2 моль) уксусного ангидрида нагревали при 90°С 1 ч. После охлаждения реакционной массы выпавший осадок отфильтровывали и промывали холодным изопропиловым спиртом. Выход - 19.95 г. (93%),
Тпл 117-119°С. Лит.Тпл 116-117°С.
Вычислено %: С 44.77; Н 3.29; N 16.52. C8H7CIN2O3.
Спектр ЯМР 1Н (ДМСО-d6), δ, м.д.: 2.11 (с) (3Н, СН3), 7.42 (дд) (1Н. Н4, J=8.5 Гц, J=1.0 Гц), 7.83 (д) (1Н, Н6, J 1.5 Гц), 8.00 (д) (1Н, Н3, J=10.0 Гц), 10.33 (с) (1Н, NH).
Пример 2. 4-(3-ацетамидо-4-нитрофенокси)бензойная кислота
20.7 г (0.15 моль) К2СО3 и 7.2 г (0.0525 моль) 4-гидроксибензойной кислоты в 200 мл ДМСО нагревается при 75°С 0.2 ч. После чего прибавляется 10.73 г (0.05 моль) N-ацетил-5-хлор-2-нитроанилина. Реакционная масса перемешивается 8 ч при 105°С. После охлаждения реакционная смесь выливается в воду и обрабатывается уксусной кислотой до рН 6. Выход 14.38 г (91%), Тпл=212-214°С.
Найдено %: С 56.59; Н 3.73; N 9.01; С15Н12N2О6.
Вычислено %: С 56.96; Н 3.80; N 8.86.
Спектр ЯМР 1Н, δ. м.д.: 2.1 (с) (3Н, СН3), 6.95 (дд) (1Н, Н6,, J=9.5 Гц, J=1.0 Гц), 7.25 (д) (2Н, Н3,5, J=10.0 Гц), 7.45 (д) (1Н, Н2', J=1.5 Гц), 8.05 (д) (2Н, Н2,6, J=9.0 Гц), 8.10 (д) (1Н, Н5', J=9.5 Гц), 10.30 (с) (1Н, NH), 13.05 (с) (1Н, СООН). Масс-спектр, m/z (Iотн., %): 316 (100) [М]+, 273 (85), 227 (49), 123 (91), 76 (57), 43 (100).
Пример 3. 4-(3-амино-4-нитрофенокси)бензойная кислота 12.64 г (0.04 моль) 4-(3-ацетамидо-4-нитрофенокси)бензойной кислоты перемешивается в 200 мл 20%-ном водном растворе КОН при 60°С. Выпавший осадок отфильтровывается и обрабатывается уксусной кислотой. Выход 10.8 г (99%), Тпл=243-245°С.
Найдено %: С 57.06; Н 3.61; N 10.19; С13Н10N2О5.
Вычислено %: С 56.93; Н 3.65; N 10.22.
Спектр ЯМР 1Н, δ, м.д.: 6.30 (дд) (1Н, Н6, J=10.0 Гц, J=1.0 Гц), 6.35 (д) (1Н, Н2, J=1.5 Гц), 7.00 (д) (2Н, Н3,5, J=9.5 Гц), 7.55 (с) (2Н, NH2), 7.90 (д) (2Н, Н2,6, J=10.0 Гц), 8.00 (д) (1Н, Н5, J=10.0 Гц), 13.00 (с) (1Н, СООН). Масс-спектр, m/z (Iотн., %): 274 (84) [М]+, 227 (37), 123 (100), 90 (89), 76 (92).
Пример 4. 4-(3,4-диаминофенокси)бензойная кислота
8.22 г (0.03 моль) 4-(3-амино-4-нитрофенокси)бензойной кислоты и 22.6 г (0.10 моль) SnCl2·2H2O перемешивают в 100 мл 36% НСl при 90°С 1 ч. После охлаждения реакционная смесь подщелачивается 25%-ным водным аммиаком до рН 7-8. Осадок отфильтровывается и высушивается при 60°С. Затем осадок вносится в 400 мл безводного изопропилового спирта и нагревается до кипения при перемешивании 0.5 ч. Горячий спирт отделяется фильтрованием. После охлаждения спирта выпавший осадок отфильтровывается. Выход 6,66 г (91%), Тпл=218-222°С.
Найдено %: С 63.77; Н 4.83; N 11.65; С13Н12N2О3.
Вычислено %: С63.93; Н4.92; N11.48.
Спектр ЯМР 1Н, δ, м.д.: 6.15 (дд) (1Н, Н6', J=10.0 Гц, J=1.5 Гц), 6.30 (д) (1Н, Н2', J=1.0 Гц), 6.55 (д) (1Н, Н5', J=10.0 Гц), 6.90 (д) (2Н, Н3,5, J=9.5 Гц), 7.90 (д) (2Н, Н2,6, J=10.0 Гц). Сигналы протонов NH2- и СООН-групп в спектре ЯМР 1Н отсутствуют ввиду быстрого дейтерообмена. Масс-спектр, m/z (Iотн., %): 244 (59) [М]+, 154 (9), 123 (100), 95 (96), 90 (15), 80 (37), 65 (34).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ СЛОЖНЫХ ЭФИРОВ 4-(3,4-ДИАМИНОФЕНОКСИ)БЕНЗОЙНОЙ КИСЛОТЫ | 2009 |
|
RU2409555C1 |
| СПОСОБ ПОЛУЧЕНИЯ 4-{4-АМИНО-2-ХЛОРО-5-[(5-ХЛОРО-2-МЕТИЛ-1Н-БЕНЗИМИДАЗОЛ-6-ИЛ)АМИНО]ФЕНОКСИ}БЕНЗОЙНОЙ КИСЛОТЫ | 2012 |
|
RU2506259C1 |
| СПОСОБ ПОЛУЧЕНИЯ 4-(3-АМИНО-4-НИТРОФЕНОКСИ)БЕНЗОЙНОЙ КИСЛОТЫ ПОД ДЕЙСТВИЕМ УЛЬТРАЗВУКА | 2015 |
|
RU2577545C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРГИДРАТА 1,3-БИС(3,4-ДИАМИНОФЕНОКСИ)БЕНЗОЛА | 2010 |
|
RU2439052C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,3- И 1,4-БИС(2-АМИНО-4-(ТРИФТОРМЕТИЛ)ФЕНОКСИ)БЕНЗОЛА | 2011 |
|
RU2453533C1 |
| Способ получения полиядерных тетрааминов, содержащих мостиковые атомы | 2018 |
|
RU2691737C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,4-БИС(2-АМИНО-4-(ТРИФТОРМЕТИЛ)ФЕНИЛ)ПИПЕРАЗИНА | 2011 |
|
RU2448962C1 |
| Способ получения N-арилзамещенных 3H-имидазо[4,5-b]пиридинов | 2016 |
|
RU2642456C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3,4'-ДИАМИНО-4-R-БЕНЗОФЕНОНОВ | 2006 |
|
RU2318799C1 |
| Способ получения N-[2-амино-4-(трифторметил)фенил]-N-фенил-4-(трифторметил)бензол-1,2-диамина и его производных | 2016 |
|
RU2645922C2 |
Изобретение относится к улучшенному способу получения 4-(3,4-диаминофенокси)бензойной кислоты, которая используются в качестве полупродуктов в синтезе термостабильных полимерных материалов. Целевое соединение получают путем ацилирования 2-нитро-5-хлоранилина уксусным ангидридом, нуклеофильного замещения атома хлора при взаимодействии с 4-гидроксибензойной кислотой в ДМСО в присутствии К2СО3, снятии ацильной защиты аминогруппы в результате щелочного гидролиза, одновременного восстановления и образования сложноэфирной связи 4-(3-амино-4-нитрофенокси)бензойной кислоты. Причем ацилирование 2-нитро-5-хлоранилина проводят при температуре 90°С в течение 1 ч и мольном соотношении 2-нитро-5-хлоранилин:уксусный ангидрид =1:2, нуклеофильное замещение атома хлора проводят в течение 8 часов при температуре 105°С и мольном соотношении N-ацетил-5-хлор-2-нитроанилин:4-гидроксибензойная кислота=1:1.05, снятие ацильной защиты осуществляют в течение 0.5 часа при температуре 60°С в 20% водном растворе КОН, восстановление проводят действием раствора SnCl2·2H2O в концентрированной соляной кислоте при температуре 90°С в течение 1 ч и мольном соотношении 4-(3-амино-4-нитрофенокси)бензойная кислота:SnCl2·2H2=1:3.35. Способ позволяет получать 4-(3,4-диаминофенокси)бензойную кислоту за минимальное время с высоким выходом и высокой степени чистоты.
Способ получения 4-(3,4-диаминофенокси)бензойной кислоты

включающий ацилирование 2-нитро-5-хлоранилина уксусным ангидридом, нуклеофильное замещение атома хлора, при взаимодействии с 4-гидроксибензойной кислотой в ДМСО в присутствии К2СО3, снятие ацильной защиты аминогруппы в результате щелочного гидролиза, восстановление 4-(3-амино-4-нитрофенокси)бензойной кислоты, причем ацилирование 2-нитро-5-хлоранилина проводят при температуре 90°С в течение 1 ч и мольном соотношении 2-нитро-5-хлоранилин: уксусный ангидрид =1:1.5, нуклеофильное замещение атома хлора проводят в течение 8 ч при температуре 105°С и мольном соотношении N-ацетил-5-хлор-2-нитроанилин: 4-гидроксибензойная кислота =1:1.05, снятие ацильной защиты осуществляют в течение 0,5 ч при температуре 60°С в 20% водном растворе КОН, восстановление проводят SnCl2·2H2O при температуре 90°С в течение 1 ч в концентрированной соляной кислоте и мольном соотношении 4-(3-амино-4-нитрофенокси)бензойная кислота: SnCl2·2H2O=1:3.35.
| Е.П.ФОКИН и др | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Известия Сибирского отделения АН СССР, Серия хим | |||
| наук, вып.3, №7, 1969, с.92-95 | |||
| 0 |
|
SU242906A1 | |
| 0 |
|
SU182167A1 | |
| СПОСОБ ПОЛУЧЕНИЯ АМИНОЭФИРОВ ДИФЕНИЛОВОГОРЯДА | 0 |
|
SU259077A1 |
Авторы
Даты
2011-01-20—Публикация
2009-06-23—Подача