Изобретение относится к биотехнологии и может быть использовано для элиминации бактериальных инфекций при культивировании клеточных культур растений в биотехнологической отрасли.
Одним из основных условий, определяющих успех работы с клеточными культурами растений, является отсутствие контаминации на всех этапах культивирования. В процессе работы для обеспечения стерильности осуществляется ряд мер, в том числе автоклавирование питательных сред, дезинфекция используемого растительного материала, стерилизация рабочих инструментов, а также организация стерильных зон для пересадок [Leifert С. and Waites W. Dealing with microbial contaminants in plant tissue and cell culture: hazard analysis and critical control points. Physiology, Growth and Development of Plants in Culture. 1994. Pp. 363-378; Reed В. M and Tanprasert P. Detection and control of bacterial contaminants of plant tissue cultures. A review of recent literature. Plant Tissue Culture and Biotechnology. 1995. 1:137-142]. Несмотря на соблюдение стерильных условий при работе с клеточными культурами, избежать спонтанных бактериальных заражений не удается, что приводит к гибели культуры и увеличению финансовых затрат на ее восстановление. Это происходит как в научно-исследовательских лабораториях, так и в условиях промышленного производства, когда несколько бактерий, попавших в биореактор, например объемом 4 т, способны полностью подавить рост растительных клеток за счет своего более быстрого размножения [Leifert С. & Woodward S. Laboratory contamination management: the requirement for microbiological quality assurance. Plant Cell, Tissue and Organ Culture. 1998. 52:83-88; Cassells A. Pathogen and Biological Contamination Management in Plant Tissue Culture: Phytopathogens, Vitro Pathogens, and Vitro Pests. Plant Cell Culture Protocols: Methods in Molecular Biology. 2012. 877:57-80; Hayward A. Latent infections by bacteria. Annu. Rev. Phytopathol. 1974. 12:87-97]. Кроме того, удаление потенциально опасных для человека бактерий из культур растительных клеток (E. coli и др.) также актуально [С. Leifert; А.С. Cassells. Microbial hazards in plant tissue and cell cultures. In Vitro Cellular & Developmental Biology - Plant 2090 Vol: 37(2):133-138].
В медицине, в качестве антибактериальных агентов используют наночастицы серебра, которые ингибируют внутрибольничные инфекции (hospital-acquired infection), устойчивые к антибиотикам [Rana S. And Kalaichelvan P. Antibacterial Activities of Metal Nanoparticles. Adv Bio Tech. 2011. 11(02):21-23; Mohammad J. et al. Antibacterial properties of nanoparticles. Trends in biotechnology. 2012. 30 (10):499-511; Azam A. et al. Antimicrobial activity of metal oxide nanoparticles against Gram-positive and Gram-negative bacteria: a comparative study. Int J Nanomedicine. 2012. 7:6003-9].
В этом изобретении авторы используют такой же принцип действия наночастиц серебра, какой используется для воздействия на госпитальные инфекции, но в другой области - биотехнологии растений, где он прежде не использовался. Предпосылка использования наночастиц серебра в биотехнологии - та же самая, то есть замена стандартных веществ на новый класс дезинфектантов.
Антибактериальный эффект наночастиц обусловлен их способностью к последовательному повреждению клеточной стенки и проникновению внутрь бактерии, что приводит к запуску процессов дефосфорилирования белков, необходимых для обеспечения жизнедеятельности, а это в свою очередь к гибели бактерий [Shrivastava S. et al. Characterization of enhanced antibacterial effects of novel silver nanoparticles. Nanotechnology. 2007. 18:225103]. Эффективность использования наночастиц серебра в качестве бактерицидного агента была исследована в отношении широкого спектра возбудителей инфекций [Galdiero S. et al. Silver nanoparticles as potential antiviral agents. Molecules. 2011. 16:8894-8918].
В последние годы появились публикации, свидетельствующие о возможном использовании наночастиц металлов в качестве антибактериального агента для обеззараживания растительных эксплантов, т.е. первичного материала, используемого для введения в культуру in vitro [Mahna N., Vahed S. and Khani S. Plant In vitro Culture goes Nano: Nanosilver-Mediated Decontamination of Ex vitro Explants. J Nanomed Nanotechol. 2013. 4(2):1000161; Abdi G. Evaluation the potential of Nano silver for removal of bacterial contaminants in valerian (Valeriana officinalis) tissue culture. L. J. BIOL. ENVIRON. SCI. 2012. 6(17):199-205]. Однако для обеззараживания клеточных культур растений наночастицы серебра или других металлов ранее не использовались. Важным параметром использования наночастиц металлов в качестве противомикробных агентов является их размер [Ai J. et al. Nanotoxicology and nanoparticle safety in biomedical designs. Inter. J Nanomedicine 2011.6:1117-1127]. Крупные наночастицы, размером более 100 нм, практически не используются, поскольку они не эффективны. Частицы размером до 20 нм нашли широкое техническое применение, однако с уменьшением размеров частиц повышается их токсичность для живых организмов. Чем мельче частицы, тем выше их противомикробная активность. Однако частицы серебра размером менее 15 нм способны вызывать окислительный взрыв, что приводит к деструктивным изменениям клеток [Carlson С. et al. Unique cellular interaction of silver nanoparticles: size-dependent generation of reactive oxygen species. J Phys Chem B. 2008. 112(43):13608-19; Liu W. et al. Impact of silver nanoparticles on human cells: effect of particle size. Nanotoxicology. 2010. 4(3):319-30].
В настоящее время в растительной биотехнологии нет другого способа элиминации бактериальных инфекций в живых клеточных культурах, поэтому поиск нового, более эффективного, является актуальным. Задача настоящего изобретения - создание нового способа эффективной элиминации инфекции, с использованием агента, обеспечивающего пролонгированную антибактериальную устойчивость культуры и отсутствие цитотоксическое действия. Не было очевидным то, что наночастицы серебра будут эффективны в клеточных культурах растений, поскольку ранее их действие не проверялось. Так, взаимодействие с элементами культуральной среды (22 компонента) и высокомолекулярными соединениями (белки и полисахариды, выделяемые в среду) не исследовалось, также не исследовались стабильность и активность наночастиц в этих системах. Способ использования наночастиц металлов для элиминации инфекции, описанный в данной заявке на примере наночастиц серебра, на сегодня является первым примером применения новых научных знаний в биотехнологии клеточных культур растений.
Наиболее распространенным способом элиминации возникающих бактериальных инфекций при культивировании клеток растений является внесение антибиотиков в питательные среды [Fellner et al. Identification and antibiotic sensitivity of microbial contaminants from callus cultures of garlic Allium sativum L. and Allium longicuspis Regel. Plant Science. 1996. 113:193-201]. Однако в процессе применения антибиотиков многие бактерии приобретают устойчивость к ним [Schmieder R. and Disclosures R. Insights into Antibiotic Resistance Through Metagenomic Approaches. Future Microbiol. 2012. 7(l):73-89; Dever L. and Dermody T. Mechanisms of bacterial resistance to antibiotics. Arch Intern Med. 1991. 151(5):886-95; Dessen A. et al. Molecular mechanisms of antibiotic resistance in gram-positive pathogens. Curr. Drug Targets Infect. Dis. 2001. 1:63-77]. Другим недостатком антибиотиков является цитотоксический эффект в отношении культивируемых клеток, что негативно сказывается на параметрах роста биомассы, либо вызывает гибель культуры [Catlin D. The effect of antibiotics on the inhibition of callus induction and plant regeneration from cotyledons of sugarbeet (Beta vulgaris L.). Plant Cell Reports. 1990. 9(5):285-8; Cassels A. Problems in tissue culture: Culture contamination. Micropropagation: technology and application. 1991. Pp. 31-44]. Важно также отметить низкую химическую устойчивость антибиотиков к факторам окружающей среды в процессе культивирования. Так, период распада антибиотиков составляет 2-3 суток, что иногда является недостаточным для подавления роста бактерий [Kazemi ЕМ, Jonoubi Р, Majd A and Pazhouhandeh М. 2014. Reduction of negative effects of cefotaxime in tomato transformation by using FeEDDHA. IJFAS Journal. Vol 3, p. 538-542; de Oliveira ML, Costa MG, da Silva CV and Otoni WC. 2010. Growth regulators, culture media and antibiotics in the in vitro shoot regeneration from mature tissue of citrus cultivars. Pesq. agropec. bras., Brasilia, v.45, p. 654-660].
Авторам не известны другие способы элиминации бактериальных инфекций в культивируемых клетках растений, поэтому данный способ взят как наиболее близкий, в качестве прототипа. Известен способ элиминации бактериальных инфекций при культивировании клеточных культур чеснока Allium sativum L., Allium longicuspis Regel, где в качестве антибактериального агента культуральной среды используют антибиотики - эритромицин, гентамицин и имипенем [Feltner М. et al. Identification and antibiotic sensitivity of microbial contaminants from callus cultures of garlic Allium sativum L. and Allium longicuspis Regel. Plant Science. 1996. 113:193-201], однако одним из недостатков способа является невозможность быстро и эффективно элиминировать инфекцию, обеспечить длительную антибактериальную устойчивость культуры. Причина в том, что многие представители бактериальной микрофлоры, инфицирующие клеточные культуры, выработали механизмы защиты от поражающего действия антибиотиков, использование которых становится малоэффективным или критичным по причине цитотоксического эффекта. Кроме того, неустойчивость антибиотиков к факторам окружающей среды зачастую не позволяет надежно уничтожить бактериальную контаминацию.
Каллусы Allium sativum L. и Allium longicuspis Regel культивировали в темноте при 25°C на агаризованной питательной среде [Dunstan and Short. Improved growth of tissue cultures of the onion, Allium сера. 1997. Physiologia Plantarum. 41:70-72]. При визуальном обнаружении инфекционных очагов, зараженные каллусы пересаживали на свежие питательные среды с добавлением антибиотиков. Наличие инфекции определяли по возникновению светло-желтых колоний после инкубации с антибиотиками. Проводили учет колоний. Было показано, что только совместное добавление в культуральную среду трех антибиотиков (эритромицина, гентамицина и имипенема в концентрации 10, 10 и 5 мг/л соответственно) приводило к полному ингибированию бактериальной инфекции в культурах Allium sativum и Allium longicuspis. Однако в культуре A. longicuspis были обнаружены бактерии в латентном состоянии.
Поставленная задача решена тем, что в предлагаемом способе, включающем культивирование суспензионных клеточных культур растений, согласно изобретению, элиминацию бактериальной инфекции проводят путем внесения в культуральную среду, в качестве антибактериального агента, водной суспензии наночастиц серебра диаметром 20-80 нм в конечной концентрации 50 мкг/мл и культивируют 24 часа в стандартных условиях.
Технический результат, обеспечиваемый изобретением, заключается в достижении эффекта обеззараживания культур, сопровождаемым ускорением процесса очистки культур от инфекции, пролонгированным антибактериальным действием, и отсутствием цитотоксического действия.
Эффективность способа элиминации бактериальной контаминации при культивировании суспензионных клеточных культурах растений с использованием наночастиц серебра была исследована в отношении разных видов микроорганизмов как грамположительных, так и грамотрицательных - Escherichia coli, Bacillus subtilis, Agrobacterium rhizogenes и модельных культур растений - марены сердцелистной Rubia cordifolia, винограда амурского Vitis vinifera и женьшеня настоящего Panax ginseng.
Суспензионные каллусные культуры растений Rubia cordifolia, Vitis vinifera, Panax ginseng культивируют стандартным способом на питательных средах WB/A в темноте при 20-30°C, относительной влажности воздуха 50-80% с периодичностью пассирования 14-21 суток [Mischenko N.P., Fedoreyev S.A., Glazunov V.P., Chernoded G.K., Bulgakov V.P., Zhuravlev Y.N. Anthraquinone production by callus cultures of Rubia cordifolia. Fitoterapia. 1999. V. 70. N6. P. 552-557].
Далее, полученные суспензионные культуры растений искусственно инфицируют, моделируя контаминацию в промышленных условиях. Для этого используют суточные культуры Escherichia coli, Bacillus subtilis, Agrobacterium rhizogenes. Бактерии выращивают при температуре 28°C в известной бактериальной среде LB [Feltner М. et al. Identification and antibiotic sensitivity of microbial contaminants from callus cultures of garlic Allium sativum L. and Allium longicuspis Regel. Plant Science. 1996. 113:193-201]. Заражение осуществляют путем кокультивации клеточных культур с 20 мкл бактерий в концентрации 1×106 КОЕ/мл, в темноте, при температуре 23-26°C и постоянном помешивании со скоростью 100 об/мин, в течение 30 минут.
Для удаления искусственно-индуцированного бактериального заражения, в колбы с зараженными клеточными культурами добавляют водную суспензию наночастиц серебра диаметром 20-80 нм до конечной концентрации 50 мкг/мл и культивируют 24 часа в стандартных условиях: в темноте, при перемешивании со скоростью 100 об/мин, температуре 23-26°C и относительной влажности воздуха 50-70%. Для элиминации используют любые коммерчески доступные наночастицы серебра указанного размера. По истечении суток очищенные от инфекции каллусы используют по назначению.
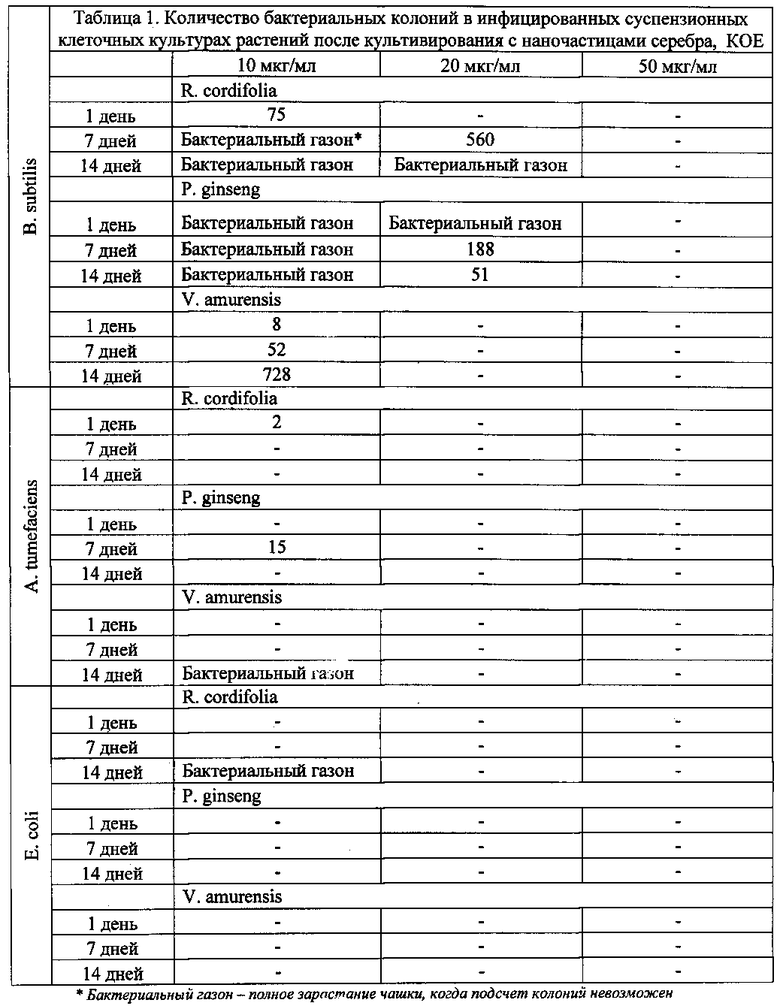
Оценку качества и скорости элиминации проводят с помощью известного метода бактериологического исследования, путем высевания сплошным газоном аликвоты культуральной жидкости на бактериальной среде LB. Бактериологические тесты проводят через сутки после добавления в культуру суспензии наночастиц и с интервалом в 7 и 14 суток. Результаты экспериментов показали, что полная элиминация инфекции происходит через сутки после введения водной суспензии наночастиц серебра в концентрации 50 мкг/мл и сохраняется в течение всего эксперимента (таблица 1).
Для подтверждения эффективности элиминации и длительности антибактериального эффекта, очищенные суспензионные культуры переносят на питательные среды WB/A, не содержащие наночастицы серебра, и выращивают в стандартных условиях в течение нескольких пассажей. Отсутствие бактериального заражения в культурах свидетельствует об эффективности использования наночастиц серебра в качестве антибактериального агента.
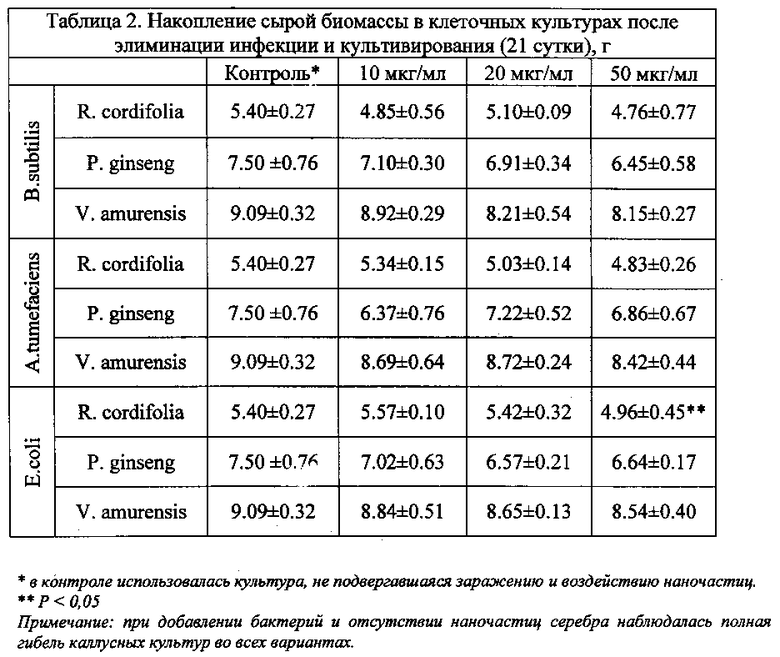
Известно, что наночастицы серебра широко применяются в различных отраслях промышленности [Shankar S.S. et al. Biological Synthesis of Triangular Gold Nanoprisms. Nature Materials. 2004. 3:482-488; Mohanpuria P. et al. Biosynthesis of nanoparticles: technological concepts and future applications. J Nanopart Res. 2008. 10:507-517], но пo причине токсичности наночастиц серебра, область их применения для человека и животных ограничена [Carlson С. et al. Unique cellular interaction of silver nanoparticles: size-dependent generation of reactive oxygen species. J Phys Chem B. 2008. 112(43):13608-19; Liu W. et al. Impact of silver nanoparticles on human cells: effect of particle size. Nanotoxicology. 2010. 4(3):319-30]. Однако авторами установлено, что наночастицы серебра проявляют низкую токсичность в отношении клеток растений. Так, результаты экспериментов показали, что внесение наночастиц серебра в культуральную среду не подавляло рост биомассы, что свидетельствовало об отсутствии цитотоксического эффекта (таблица 2).
Способ иллюстрируется следующим примером.
Пример 1. Показан способ элиминации контаминации на примере культуры марены сердцелистной Rubia cordifolia, как вариант использования любой суспензионной клеточной культуры. Суспензионную клеточную культуру R. cordifolia выращивают стандартным методом в колбах Эрленмейера объемом 250 мл, содержащих 50 мл питательной среды WB/A следующего состава, мг/л воды:
Суспензионную культуру выращивают на указанной среде при постоянном помешивании со скоростью 100 об/мин, при температуре 25°C и относительной влажности воздуха 60%, в течение 14 суток. В случае обнаружения бактериальной инфекции, либо при риске микробной контаминации, в суспензионную клеточную культуру добавляют наночастицы серебра диаметром 20-80 нм до конечной концентрации в культуральной среде 50 мкг/мл. Далее суспензионную культуру культивируют 24 часа в аналогичных условиях.
Таким образом, предлагаемый способ позволяет быстро и эффективно провести элиминацию бактериальных инфекций при культивировании клеточных культур растений. Использование наночастиц серебра в качестве нового антибактериального агента позволяет повысить устойчивость культуры к действию микробных контаминантов и обеспечить длительный антабактериальный эффект. Отсутствие цитотоксического действия наночастиц позволяет применять способ не только для элиминации уже возникшей инфекции, но и для защиты каллусов от возможной контаминации в процессе культивирования в лабораторных или промышленных условиях.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ НАНОЧАСТИЦ МЕТАЛЛОВ | 2011 |
|
RU2477172C1 |
| Модифицированная питательная среда для культивирования растений картофеля на основе агаризованной питательной среды Мурасиге-Скуга и способ выращивания растений картофеля в асептических условиях с использованием данной питательной среды | 2022 |
|
RU2794777C1 |
| СПОСОБ ПОЛУЧЕНИЯ РЕЗВЕРАТРОЛА | 2006 |
|
RU2326165C1 |
| СПОСОБ РЕГЕНЕРАЦИИ ХЛОПЧАТНИКА ИЗ СОМАТИЧЕСКИХ КЛЕТОК (ВАРИАНТЫ) | 1988 |
|
RU2128428C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОЧАСТИЦ БЛАГОРОДНЫХ МЕТАЛЛОВ С ПОМОЩЬЮ БАЗИДИАЛЬНЫХ МАКРОМИЦЕТОВ | 2017 |
|
RU2679065C1 |
| КЛЕТОЧНЫЕ КЛОНЫ КАМБИЯ, СПОСОБ ИХ ВЫДЕЛЕНИЯ И КОНСЕРВАЦИИ | 2006 |
|
RU2398874C2 |
| СПОСОБ ПОЛУЧЕНИЯ БЕЛКОВЫХ ВЕЩЕСТВ | 2000 |
|
RU2250264C2 |
| СПОСОБ СОХРАНЕНИЯ in vitro РАСТЕНИЙ ЗЕМЛЯНИКИ (Fragaria L.) | 2014 |
|
RU2564565C1 |
| Применение препарата "Зерокс®" (ВРК) в качестве стимулятора роста сахарной свеклы | 2019 |
|
RU2726251C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИГАПЛОИДНЫХ РАСТЕНИЙ ЯЧМЕНЯ ИЗ КУЛЬТИВИРУЕМЫХ МИКРОСПОР IN VITRO | 2013 |
|
RU2557389C2 |
Изобретение относится к биотехнологии. Изобретение представляет собой способ элиминации бактериальной инфекции клеточных культур растений, включающий культивирование суспензионных клеточных культур с использованием антибактериального агента, где в качестве антибактериального агента используют водную суспензию наночастиц серебра диаметром 20-80 нм, которую вносят в суспензионную клеточную культуру до конечной концентрации в культуральной среде 50 мкг/мл, при этом культивирование осуществляют 24 часа в стандартных условиях. Изобретение позволяет обеззараживать клеточные культуры растений и сопровождается ускорением процесса очистки культур от инфекции, пролонгированным антибактериальным действием, и отсутствием цитотоксического действия. 2 табл., 1 пр.
.
Способ элиминации бактериальной инфекции клеточных культур растений, включающий культивирование суспензионных клеточных культур с использованием антибактериального агента, отличающийся тем, что в качестве антибактериального агента используют водную суспензию наночастиц серебра диаметром 20-80 нм, которую вносят в суспензионную клеточную культуру до конечной концентрации в культуральной среде 50 мкг/мл, при этом культивирование осуществляют 24 часа в стандартных условиях.
| FELLNER M, et al, Identification and antibiotic sensitivity of microbial contaminats from callus cultures of garlic Allium sativum L | |||
| and Allium longicuspis Regel, Plant Science 113, 1996, p.193-201 | |||
| SARMAST M.K., Nano silver treatment is effective in reducing bacterial contaminations of Fraucaria excelsa R | |||
| BR.Var | |||
| Glauca explants, Acta Biol Hung, |
Авторы
Даты
2016-03-20—Публикация
2014-12-01—Подача