Область техники. Изобретение относится к области сельскохозяйственной биотехнологии, в частности прикладным исследованиям, связанным с созданием новых сортов и гибридов, и может быть востребовано образовательными и научными учреждениями биотехнологического и сельскохозяйственного профиля, семеноводческими компаниями и селекционными станциями.
Актуальность изобретения. Ячмень принадлежит к числу важнейших сельскохозяйственных культур, в селекции которых показана перспективность использования удвоенных гаплоидов. Использование удвоенных гаплоидов ячменя может существенно сократить время селекционного процесса, а также повысить его эффективность (Maluszynski М. et al. 2003).
Наиболее перспективным способом получения гаплоидных растений является метод индукции эмбриогенеза в культуре изолированных микроспор (Touraev A. et al. 2009). Микроспора представляет собой гаплоидную клетку высших растений, из которой в процессе нормального гаметофитного развития формируется зрелое пыльцевое зерно, готовое к опылению. Посредством специальных технологий (стрессовая обработка, особый состав питательной среды и т.п.) можно изменить путь развития микроспоры от гаметофитного к спорофитному (формирование тотипотентной клетки) и индуцировать регенерацию гаплоидного растения (Touraev А. et al. 2009). Полученное гаплоидное растение будет иметь одинарный набор хромосом, т.е. геном будет представлен одной аллелью каждого гена. При искусственном (использование антимитотических веществ) или спонтанном (самопроизвольном) удвоении генома, аллели тоже удваиваются и гаплоидное растение переходит в диплоидное (дигаплоидное) состояние, т.е. получается гомозиготное (инбредное) растение. В отличие от этого при классическом размножении в геноме растения объединяются и мужские и женские хромосомы, т.е. происходит совмещение разных аллелей, которые могут маскировать друг друга. Наличие всего одной удвоенной аллели (у дигаплоидов) позволяет признаку проявить себя в фенотипе даже в том случае, если изначально в популяции он всегда рецессивный. Генетическое расщепление при использовании дигаплоидов менее сложно, что позволяет использовать для выделения определенной комбинации генов сравнительно малочисленные популяции (Wedzony М. et al. 2009).
Уровень техники. Проблеме создания дигаплоидных растений посвящено много обзоров. Существуют публикации и патенты на изобретения, в которых предлагается использовать удаленную гибридизацию (Патент WO 2005084420 (2005-09-15), Kasha K.J. and Kao K.N., 1970, Mujeeb-Kazi A. and Riera-Lizarazu О., 1996), женский гаметофит (Патент JPH 0698648 (1994-04-12), Keller E. and Korzun L. 1996)), культуру пыльников (Патенты US 5770788 А (1995-06-06), US 6362393 B1 (1999-08-26)) и культуру микроспор (Патенты KR 100952103 (2009-07-01), WO 2002052926 A3 (2002-01-02), SUS 6764854 В2 (2004-07-20). Из-за сложности получения гаплоидных растений все работы описывают решение какой-либо частной проблемы, применимой для конкретного сорта или вида растения.
Метод получения гаплоидных растений ячменя через элиминирование хромосом
Данный метод основан на феномене элиминирования половины хромосом в клетках гибридного ячменя на ранних стадиях эмбриогенеза (Kasha K.J. and Kao K.N., 1970). Этот процесс можно наблюдать при межвидовом скрещивании ячменя (Н.vulgare) с ячменем луковичным (Н.bulbosum). Результатом подобного процесса становится элиминирование хромосом Н.bulbosum.
Метод получения гаплоидных растений через межвидовую гибридизацию совершенствовался на протяжении нескольких лет, что сделало его достаточно эффективным (Hayes P. et al. 2003, Devaux P. 2003). К настоящему времени метод элиминирования хромосом позволил получить большое число гаплоидных и дигаплоидных линий и данная технология применяется в селекционных программах ряда компаний (Devaux Р. 2003).
Однако в данном методе можно отметить ряд существенных недостатков: сложность отбора полученных гибридов по признаку гаплоидии, длительность самого экспериментального процесса и его низкая эффективность. К положительным сторонам данной методики можно отнести то, что для ее выполнения не требуется специального дорогостоящего оборудования, и она может быть проведена в обычных для селекционного процесса условиях и почти не зависит от генотипа (Maluszynski М. et al. 2003).
Метод получения гаплоидных растений из женского гаметофита (партеногенез)
В течение нескольких лет были предприняты попытки культивирования in vitro изолированных яйцеклеток, зародышевых мешков, неопыленных завязей или семяпочек с целью получения гаплоидов путем партеногенеза (Keller Е. and Korzun L. 1996). Наиболее эффективно данный метод показал себя на таких культурах, как картофель, сахарная свекла, лук и огурец (Metwally et al. 1998). Гаплоиды ячменя также были получены с помощью культуры семяпочки, однако метод оказался низкоэффективным (0,2-1,4%) и трудоемким, что не позволило найти ему широкое применение для прикладных целей (Yean-San L.H. 1987).
Метод получения гаплоидных растений ячменя культуру пыльников
Получение гаплоидных растений из изолированных пыльников может проходить двумя путями: прямая регенерация соматических зародышей (эмбриоидогенез) и через каллусогенез. Эффективность формирования эмбриоидов является генотипзависимым процессом и может существенно различаться, варьируя от 0 до 95% (Germana М.А. 2011).
Суть методики заключается в том, что из растений, выращенных в контролируемых температурных и световых условиях, выделяют пыльники. Перед выделением пыльников колосья культивируют 14-28 дней при низких температурах 4-8°C, затем выделяют пыльники и переносят их на бедные среды с маннитолом (0,3-0,7 М) на 3-4 дня. После стрессовой обработки пыльники переносят на искусственные питательные среды и культивируют в темноте при 23-28°C в течение 3-5 недель до формирования эмбриоидов, которые, в свою очередь, переносят на среду для регенерации. Состав сред варьируется в зависимости от используемого генотипа (Szarejko I., Kasha K.J. 1991, Cistué L. et al. 1994, Hoekstra S. et al. 1997, Jacquard C. 2006).
Главным и существенным недостатком помимо высокой генотипической зависимости этой методики является то, что получаемые растения могут иметь различную степень плоидности (из-за возможности регенерации растений из соматических тканей пыльника): от гаплоидных до ди-, поли- и анеуплоидных. К тому же, при использовании этой технологии происходит формирование большого количества альбиносов среди растений-регенерантов (Castillo A.M. et al. 2000, Li H, Devaux P. 2005, Jacquard C. 2006, Germana M.A. 2011).
Метод получения гаплоидных растений через культуру изолированных микроспор
Другой подход для получения гаплоидных растений основан на культивировании in vitro изолированных микроспор. Внешне этот метод схож с методом изолированных пыльников, однако в своей основе они сильно различаются, так как базируются на использовании различных типов тканей и клеток. Культура микроспор представляет собой процесс культивирования в жидкой питательной среде генеративных клеток, освобожденных от соматических тканей пыльника. Данный метод технологически отличается от культуры пыльников. Главным отличием культуры изолированных микроспор от культуры пыльников является процесс и время изоляции микроспоральных клеток. Основная схема эксперимента по изоляции микроспор следующая: изолированные пыльники или фрагменты колоса мацерируются в питательной среде. Для эффективного выделения чистой популяции микроспор полученная пульпа фильтруется и центрифугируется несколько раз. Дальнейшее культивирование микроспор осуществляется в жидких питательных средах, состав которых различается в зависимости от генотипов или целей эксперимента.
В настоящее время существует несколько патентов на данный метод получения дигаплоидных растений. Однако предлагаемые в них методы разработаны и подходят только для таких культур как перец (Capsicum annuum L.) (Патент KR 100952103 (2009-07-01)) и кукуруза (Zéa máys L.) (WO 2002052926 A3 (2002-01-02)), рис (SUS 6764854 B2 (2004-07-20)). Предлагаемый же нами метод позволяет получать гаплоидные растения ячменя (H.vulgare).
В настоящее время описано два способа получения гаплоидных растения ячменя, которые наиболее близки к нашей работе (Kasha K.J. et al. 2003, Devies P.A. 2003). Однако они значительно отличаются от предлагаемого нами по таким параметрам, как условия культивирования растений-доноров, возраст используемого растения-донора, по наличию и продолжительности стрессовой обработки растений, способу изоляции микроспор, по плотности микроспор в индукционной питательной среде и составу индукционной питательной среды и составу питательной среды для регенерации растений.
Предлагаемые методы имеют также несколько существенных минусов: необходимость определения стадии развития микроспоры цитологическими методами, высокая частота получения растений-альбиносов, высокая зависимость эффективности получения дигаплоидов от генотипа растения. Мы предлагаем эффективный малозависимый от генотипа метод получения дигаплоидных растений ячменя с высоким уровнем спонтанного удвоения хромосом и низким выходом альбиносных растений.
Удвоение хромосом у гаплоидов
Для того чтобы от гаплоидных растений можно было получить здоровое потомство, на одной из стадий развития необходимо провести удвоение хромосом в клетках растения, что в большинстве случаев индуцируется применением антимитотического агента - колхицина. Данное вещество обладает способностью связываться с особыми структурами клетки, ответственными за деление, блокировать расхождение дочерних клеток, что приводит к формированию клеток с двойным (дигаплоидным) набором хромосом. Существенным недостатком колхицина является его высокая токсичность как в отношении клеток, так и в отношении персонала (Ade R. and Rai М.K. 2010).
Метод обработки растений колхицином не претерпел значимых изменений с 1938 года, когда он впервые был описан (Levan А. 1938): колхицином обрабатывают корни, верхушечные меристемы и т.п. (Wong С.K. 1989, Swanson Е.В. 1990, Mathias R. and Robbelen G. 1991). Процедуры обработки растений в связи с необходимостью использовать высокие концентрации препарата являются потенциально опасными и дорогостоящими (De Раере R. et al. 1981, Hansen F.L. et al. 1988, Barnabas B. et al. 1991, Hassawi D.S. and Liang G.H. 1991, Zhao J.P. and Davidson D. 1984).
При этом процедура обработки растений колхицином не всегда позволяет добиться желаемого результата, так как после подобного воздействия формируется большое количество химерных растений, анеуплоидов и т.д. (Zhao J.P. and Davidson D. 1984, Barnabas B. et al. 1991, Mathias R. and Robbelen G. 1991).
Структурная формула колхицина была определена в 1955 году (Corrodi and Hardegger, 1955). Согласно определенной структуре колхицин представляет собой комплекс из триметоксифенила, семичленного кольца, несущего ацетамид в положении 7 и трополоновое кольцо.
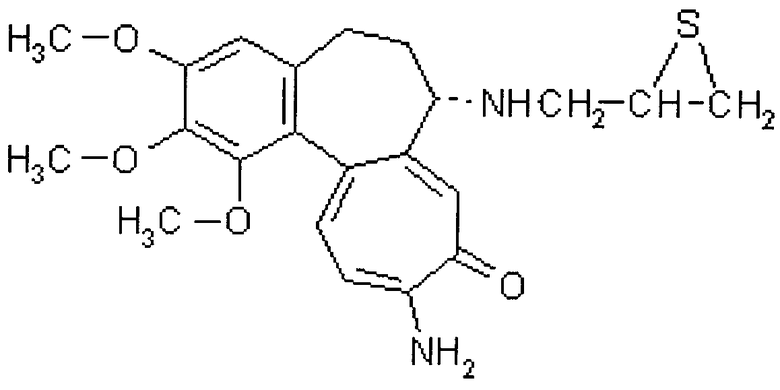
Для удвоения хромосом и перевода гаплоидных растений ячменя в дигаплоидные мы предлагаем использовать аминопроизводный аналог колхицина - N-диацетил-N-(β,γ-эпоксипропил)аминоколхицин (Рисунок). Данный аналог показал более низкую токсичность относительно растительных клеток и большую способность связывать тубулин (T. Resh and A. Touraev неопубликованные данные).
Раскрытие изобретения
Разработанная методика представляет собой способ получения гаплоидных и дигаплоидных растений ячменя из микроспор, выделенных из пыльников, и состоит из следующих ключевых этапов:
- выращивание растений-доноров при определенных условиях (яровизация семян и проростков, пониженная температура воздуха 15-20°C, световой режим: 16 ч день/8 ч ночь, влажностью воздуха 60-70%, интенсивность освещения 10000-15000 люкс, фитосанитарная обработка);
- использование растений-доноров на стадии открытия влагалища флагового листа, когда колос находится внутри флагового листа;
- низкотемпературная обработка свежесобранных колосьев растений-доноров на среде с маннитолом (при 4°C, бедная среда с 60 г/л маннитолом, 7 дней);
- наличие в среде для индукции эмбриогенеза 6% мальтозы, завязей (10 зав. на 1,5 мл культуры) и регуляторов роста растений (1 мг/л 2,4-Д, 0,2 мг/л зеатина).
Добавление всех компонентов среды перед добавлением микроспор;
- регенерация растений из эмбриоидов на среде без добавления регуляторов роста растений,
- обработка молодых гаплоидных растений для получения удвоенных гаплоидов (замачивание тепличных растений в 0,05% N-диацетил-N-(β,γ-эпоксипропил)аминоколхицин на 5 ч).
Данная методика была использована на 6 сортах отечественной селекции (3 озимых и 3 яровых). Эффективность регенерации растений оказалась высокой для всех исследуемых сортов, независимо от генотипа и составила от 16 до 20 зеленых растений на один колос. При этом спонтанное удвоение хромосом произошло у 78% полученных растений-регенерантов. В результате применения N-диацетил-N-(β,γ-эпоксипропил)аминоколхицина удвоение хромосом произошло у 80% обработанных гаплоидных растений и таким образом общая эффективность методики составила от 16-19 дигаплоидных растений на один использованный колос. Данный показатель свидетельствует о высокой эффективности предлагаемого способа.
Краткое описание чертежей
На чертеже представлена структурная формула N-диацетил-N-(β,γ-эпоксипропил)аминоколхицин
Осуществление изобретения
Пример 1. Выращивание растений-доноров
Выращивание качественных растений-доноров является необходимым условием для получения эмбриогенных микроспор для последующего эмбриогенеза и регенерации гаплоидных и дигаплоидных растений. Помимо обязательного предохранения растений от таких заболеваний как мучнистая роса, карликовая ржавчина, корневые гнили и насекомых (паутинный клещ, тля, трипсы и т.д.), должны быть созданы оптимальные условия вегетации - качественное освещение, водоснабжение, почвенные субстраты, удобрения, влажность и качество воздуха.
Подготовка и проращивание семян. Чтобы повысить всхожесть, семена выдерживали при температуре 4°C не менее 2 недель, а затем шелушили для удаления плотного семенной кожуры. Для обеззараживания семена обрабатывали 2%-ным раствором KMnO4 в течение 20 мин. Обработку семян проводили при комнатной температуре с последующей отмывкой водопроводной водой. Для приготовления 2%-ного раствора - 2 г KMnO4 растворяли в 100 мл воды. Далее семена замачивали в воде на 12-24 ч, а затем переносили на влажную фильтровальную бумагу и культивировали в темноте 2-3 дня до появления проростков, при температуре 15-20°C.
Проросшие семена ячменя по 3-5 шт. высевали в горшочки со стерильным почвенным субстратом (pH 6,5-7). Глубина посева 3-4 см. Семена проращивали в условиях искусственного климата при температуре 15/12°C (день/ночь), со световым режимом: 16 ч день/8 ч ночь, влажностью воздуха 60-70% и интенсивность освещения 10000-15000 люкс. После появления всходов температура культивирования повышалась до 15-20°C. Семена озимых сортов высевали на 1,5-2 месяца раньше яровых для проведения этапа яровизации.
Яровизация ячменя. Проросшие саженцы озимых сортов ячменя проходили этап яровизации в течение 1,5-2 месяцев при 4°C и влажности воздуха 70-80%. После яровизации проростки переносили в условия, аналогичные условиям прорастания.
Прорывка и браковка нетипичных растений. После образования 2-3 листьев, перед началом стадии кущения, проводилась прорывка и браковка нетипичных растений. В горшках оставляли по 1-му растению и проводили присыпку почвенным грунтом. Полив смесью из водорастворимых удобрений проводили раз в 8-12 дней.
Выращивание растений с целью получения микроспор.
Растения выращивали при поливе водопроводной водой по мере подсыхания почвенного субстрата при 60-70% влажности воздуха. Для улучшения аэрации корневой системы, проводилось рыхление верхнего почвенного слоя не менее 1 раза в 10 дней. Температура в помещении поддерживалась в пределах 15-20°C, освещенность 10-15 тыс. люкс при 16-часовом фотопериоде. Каждые 2 недели проводилась прикорневая подкормка растений органическими удобрениями и микроэлементами.
Фитосанитарная обработка. Очень важным при выращивании растений-доноров является предотвращение заболеваний растений и появление вредителей, т.к. эти факторы сильно снижают фертильность растений и эффективность эмбриогенеза в культуре микроспор. Перед посадкой и во время выращивания растений проводили профилактическую обработку растений смесью фунгицидов и бактерицидов, а при обнаружении пораженных растений производили немедленную их изоляцию.
Обработку растений смесью фунгицидов и бактерицидов прекращали за 2-3 недели до сбора микроспор, т.к. данные препараты снижали жизнеспособность последних. После появления у растений флагового листа проводили еженедельную подкормку водным раствором удобрений NPK (20:20:20).
Пример 2. Сбор и низкотемпературная обработка колосков
Колоски собирали с растений-доноров на стадии, когда влагалище флагового листа открывалось, но соцветие еще находится внутри флагового листа. Большая часть микроспор в таких растениях находились в поздней одноядерной фазе развития (70-80% микроспор).
Стебель отрезали на 8-10 см ниже колоса (флаговый лист удаляли), помещали в стакан с водой и переносили в лабораторию. До начала стерилизации влагалище флагового листа не удаляли.
В стерильных условиях (ламинарный бокс) с колоса снимали влагалище флагового листа и колос помещали на 1 мин в 70%-ный этиловый спирт и затем тщательно промывали в стерильной дистиллированной воде.
Затем колосья помещали в пробирки с бедной средой и маннитолом (KCl 1,5 г/л, MgSO4×7H2O 0,25 г/л, CaCl2×2H2O 0,1 г/л, маннитол 60 г/л, калий-фосфатный буфер (pH 7) 1 мл/л, pH - 7,0) таким образом, чтобы в среде находилась только нижняя часть (ость) колоса. Пробирки герметично закрывали и помещали в холодильник (4°C, темнота) на 7 дней.
Пример 3. Выделение микроспор
В стерильных условиях (ламинарный бокс) с использованием стерильного (автоклавированного) инструмента от колосьев удаляли верхние и нижние колоски (по 1-2 см). Колосья разрезали на сегменты по 2-3 см и помещали в стерильную чашу блендера (Waring Blender, USA) объемом от 50 до 200 мл (в зависимости от количества колосков), так чтобы колоски не занимали больше половины объема. К колоскам сразу добавляли охлажденную бедную среду с маннитолом (2-4°C) в таком объеме, чтобы она покрывала колоски (от 25 до 100 мл). Измельчали при низких оборотах около 5 с, затем полученную суспензию пропускали через фильтр (100 мкм) в стерильные колбы. Затем суспензию разделяли по пробиркам для центрифугирования объемом 15 мл и центрифугировали при 900 об/мин в течение 5 мин. Супернатант удаляли, а осажденные микроспоры промывали путем двукратного центрифугирования в охлажденной среде с маннитолом (по 15 мл) по 5 мин при 600 об/мин. Супернатант удаляли и к осажденным микроспорам добавляли в модифицированную среду №1 (табл. 1), до приблизительной плотности 2×104. Для подсчета количества микроспор на мл среды использовали камеру Горяева. Суспензию микроспор переносили на чашки Петри (35×10 мм) по 1,5 мл на чашку и добавляли к ним свежевыделенные завязи (10 шт. на чашку). С каждого колоса получали 3-4 чашки с культурой микроспор, которые плотно запечатывали парафильмом (Parafilm, USA) и культивировали в темноте при температуре 25°C.
Завязи выделяли в стерильных условиях под бинокулярным световым микроскопом из свежесрезанных и простерилизованных по описанной выше методике колосьев.
Пример 4. Индукция эмбриоидогенеза
Чашки с микроспорами культивировали в темноте при 25°C. Содержание живых микроспор после низкотемпературной обработки и культивирования на среде для индукции эмбриогенеза (с мальтозой, фитогормонами и завязями) в течение 5 дней составило от 69 до 91% в зависимости от генотипа (табл. 2). Эмбриоиды формировались течение 20-30 дней. Среднее количество эмбриоидов сформированных из микроспор составило от 188 до 214 шт. на использованный колос (табл. 2).
Пример 5. Регенерация и культивирование растений
После того, как эмбриоиды достигали 1,5-2 мм, их переносили на чашки Петри (100×15 мм) с твердой средой №2 для культивирования эмбриоидов (табл. 1) по 20-25 шт. на чашку и культивировали в течение 4-5 дней в темноте. Затем чашки переносили на свет при 25°C и культивировали до формирования проростков (около 2 недель). Примерно 8-10% из сформировавшихся эмбриоидов регенерировали в полноценные зеленые растения, еще около 2% из сформированных растений были альбиносами (табл. 2).
После формирования 2-3 листьев из полученных растений отбирали зеленые и переносили на среду №3 Мурасиге и Скуга (Murashige Т. and Skoog F. 1962) для культивирования растений (табл. 1). Культивирование осуществляли в пробирках или контейнерах со световым режимом: 16 ч день, 8 ч ночь при 25°C до образования хорошо развитых корней (2-4 недели). Затем растения выдерживали при 4°C в течение 4 недель в климатической камере при низкоинтенсивном световом режиме: 8 ч день, 16 ч ночь (этап яровизации). Затем увеличивали температуру и интенсивность освещения до 15°C и 12/12 ч день/ночь соответственно. При таком режиме культивировали еще 1 неделю.
После яровизации растения из пробирок переносили в горшки с почвенной смесью для выращивания в теплице. В течение первой недели после переноса растений в теплицу на них оставляли пластиковые контейнеры, которые постепенно приоткрывали, для мягкой адаптации.
Эффективность метода составила 16-20 зеленных растений на один использованный колос. При этом спонтанное удвоение хромосом происходило у 78% полученных растений, что свидетельствует о высокой эффективности, разработанного протокола. Количество полученных дигаплоидов составило от 13 до 17 шт. на один использованный колос. Плоидность растений определяли с использованием стандартных методов (Maluszynski М. et al.).
Пример 6. Обработка гаплоидных растений ячменя антимитотическим препаратом для получения удвоенных гаплоидов
Растения, прошедшие этап яровизации и адаптации к условиям теплицы, доращивали до формирования не менее двух побегов. Затем растения извлекали из почвы, промывали корни и обрезали их на 1-2 см. Опускали корни и нижнюю часть побегов на 5-8 см в 0,05%-ный раствор антимитотического агента (500 мг/л N-диацетил-N-(β,γ-эпоксипропил)аминоколхицина + 20 мл/л DMSO + 100 мг/л гиббереллиновой кислоты + 20 капель/л TWEEN 20) и оставляли на 5 ч при температуре 15-20°C и интенсивном освещении (10-15 тыс. люкс). Затем промывали корни проточной водой и помещали в почвенный грунт. Далее растения культивировали по описанной выше методике выращивания растений-доноров до получения зрелых зерновок.
В результате применения N-диацетил-N-(β,γ-эпоксипропил)аминоколхицина удвоение хромосом произошло у 80% обработанных гаплоидных растений и, таким образом, общая эффективность методики составила от 16-19 дигаплоидных растений на один использованный колос (табл. 2).
Список литературы
1. Ade R., Rai M.K. Review: Colchicine, current advances and future prospects. 2010. Nusantara Bioscience. Vol.2, No.2, P.90-96.
2. Barnabas В., Pfahler P., Kovacs G. Direct effect of colchicine on the microspore embriogenesis to produce dihaploid plants in wheat (Triticum aestivum L.) 1991. Theor Appl Genet. 81:675-678.
3. Castillo A.M., Vallés M.P., Cistué L. Comparison of anther and isolated microspore culture in barley. Effects of culture density and regeneration medium. 2000. Euphytica 113:1-8.
4. Cistué L., Ramos A., Castillo A.M., Romagosa I. Production of large numbers of doubled haploid plants from barley anthers pretreated with high concentrations of mannitol // Plant Cell. 1994. Vol.13. P.709-712.
5. Corrodi H., Hardegger E. Die configuration des colchicins und verwandter Verbindungen Helv. Acta 1955. 38, 2030-2033.
6. De Paepe R., Bleton D., Gnangbe F. Basis and extent of genetic variability among doubled haploid plants obtained by pollen culture in Nicotiana sylvestris. 1981. Theor Appl Genet. 59:177-84.
7. Devaux P. The Hordeum bulbosum (L.) method. In: Maluszynski M, Kasha KJ, Forster BP, Szarejko I (eds) Doubled haploid production in crop plants // A manual. 2003. P.15-19.
8. Devies P.A. Barley isolated microspore culture (IMC) method In: Maluszynski M, Kasha KJ, Forster BP, Szarejko I (eds) Doubled haploid production in crop plants // A manual. 2003. P 49-52.
9. Germana M.A. Anther culture for haploid and doubled haploid production // Plant Cell, Tissue Organ Cult. 2011. Vol. 104. P.283-300.
10. Hansen F.L., Andersen S.B., Due I.K., Olsen A. Nitrous oxide as a possible alternative agent for chromosome doubling of wheat haploids. Plant Sci. 1988. 54:219-222.
11. Hassawi D.S., Liang G.H. Antimitotic agents: effects of double haploid production in wheat. 1991. Crop Sci. 31:723-726.
12. Hayes P., Corey A., DeNoma J. Doubled haploid production in barley using the Hordeum bulbosum (L.) technique. In: Maluszynski M, Kasha KJ, Forster BP, Szarejko I (eds) Doubled haploid production in crop plants // A manual. 2003. P.5-14.
13. Hoekstra S., van Bergen S., van Brouwershaven I.R., Schilperoort R.A., Wang M. Androgenesis in Hordeum vulgare L: effects of mannitol, calcium and abscisic acid on anther pretreatment // Plant Sci. 1997. Vol. 126. P.211-218.
14. Jacquard C., Asakaviciute R., Hamalian A.M., Sangwan R.S., Devaux P., Clément C. Barley anther culture: effects of annual cycle and spike position on microspore embryogenesis and albinism // Plant Cell Rep. 2006. Vol. 25. P.375-381.
15. Kasha K.J., Simion E., Oro R. and Shim Y.S. Barley isolated microspore culture protocol Maluszynski M. et al. (eds.), Doubled Haploid Production in Crop Plants, 43-47.
16. Kasha K.J., Kao K.N. (1970) High frequency haploid production in barley (Hordeum vulgare L.). Nature 225:874-876.
17. Keller E.R.J., Korzun L. (1996) Ovary and ovule culture for haploid production. In: Mohan Jain S, Sopory SK, Veilleux RE (eds) In vitro Haploid Production in Higher Plants, Vol 1, Kluwer Academic Publishers, Dordrecht, P.217-236.
18. Levan A. The effect of colchicines on root mitoses in allium. 1938. Hereditas. V 24,I 4, 471-486.
19. Li H., Devaux P. Isolated microspore culture over performs anther culture for green plant regeneration in barley (Hordeum vulgare L.). Acta Physiol Plant 2005 V 27:611-619.
20. Maluszynski M., Kasha K.J., Forster B.P., Szarejko I. Doubled haploid production in crop plants: a manual // Kluwer Academic Publishers. 2003
21. Mathias R., Robbelen G. Effective diplodization of microspore-derived haploids of rape (Brassica napus L.) by in vitro colchicines treatment. 1991. Plant breed 106:82-84.
22. Metwally E.I., Moustafa S.A., El-Sawy B.I., Haroun S.A., Shalaby Т.А. (1998) Production of haploid plants from in vitro culture of unpollinated ovules of Cucurbita pepo. Plant Cell Tiss Org Cult 52:117-121.
23. Mujeeb-Kazi A., Riera-Lizarazu О. (1996) Polahaploid production in the Triticeae by sexual hybridization. In: Mohan Jain S, Sopory SK, Veilleux RE (eds) In vitro Haploid Production in Higher Plants, Vol 1, Kluwer Academic Publishers, Dordrecht, pp 275-296.
24. Murashige T. and Skoog F. 1962. A revised medium for rapid growth and bioassays with tobacco tissue cultures. Physiol Plant, 15:437-497.
25. Swanson E.B. Microspore culture in Brassica. 1990. In: J.W. Walker (Eds), Methods in molecular biology. V 6. Plant cell and tissue culture. Chap.17.
26. Szarejko I., Kasha K.J. Induction of anther culture derived doubled haploids in barley // Cereal Res Commun. 1991. Vol. 19. P.219-237.
27. Touraev A., Forster B.P., Jain, Shri Mohan Advances in Haploid Production in Higher Plants. 2009. Springer Science + Business Media B.V, ISBN 978-1-4020-8853-7.
28. Wedzony M., Forster B.P., Žur I., Golemiec E., Szechyńska-Hebda M., Dubas E., Gotębiowska G. Progress in doubled haploid technology in higher plants. In: Advances in Haploid Production in Higher Plants // Springer Science. 2009. P.1-34.
29. Wong C.K. A new approach to chromosome doubling for haploid rice plants. 1989. Theoretical and applied genetics. 149-151.
30. Yean-San L.H. Gynogenèse in vitro. Variabilité des haploides doublés issus d′androgenèse in vitro et de croisement interspécifique chez Hordeum vulgare L. 1987 Thèse Doctorat d′Etat, Université de Paris-sud, France.
31. Zhao J.P., Davidson D. Distribution of chromosomes into discrete group in colchicines-induced C-metaphases of barley. 1984. Caryologia. 37:331-42.
32. JPH 0698648 (1994-04-12) Method For Creating Haploid Plant From Female Gamete Of Seed Plant.
33. KR 100952103 (2009-07-01) Method For Plant Production From Embryos Obtained By Microspore Culture Of Hot Pepper (Capsicum Annuum L.).
34. SUS 6764854 B2 (2004-07-20) Methods For Generating Doubled Haploid Rice Plant.
35. US 6362393 B1 (1999-08-26) Methods For Generating Doubled Haploid Plants.
36. US 5770788 A (1995-06-06) Inducing Chromosome Doubling In Anther Culture In Maize.
37. WO 2002052926 A3 (2002-01-02) Methods For Generating Doubled Haploid Maize Plants.
38. WO 2005084420 (2005-09-15) A Breeding Material Which Can Induce Wheat Hybrids To Produce Genetically Pure Diploid Plants And The Practical Method Thereof.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ изоляции микроспор для получения удвоенных гаплоидов семейства Brassicaceae в культуре микроспор in vitro | 2022 |
|
RU2807444C1 |
| Способ получения дигаплоидных растений озимой пшеницы | 2023 |
|
RU2821696C1 |
| Способ получения удвоенных гаплоидов из микроспор в культуре пыльников in vitro ячменя обыкновенного (Hordeum vulgare) | 2023 |
|
RU2828837C1 |
| Способ удвоения хромосомного набора гаплоидов рапса (Brassica napus L.) | 2022 |
|
RU2808269C1 |
| Способ получения удвоенных гаплоидов моркови в культуре изолированных микроспор in vitro | 2020 |
|
RU2750959C1 |
| Способ получения растений-регенерантов Brassica oleracea L. in vitro | 2021 |
|
RU2759735C1 |
| Способ получения растений-регенерантов рода Brassica in vitro | 2020 |
|
RU2741647C1 |
| Питательные среды для способа получения дигаплоидов озимой пшеницы | 2023 |
|
RU2821590C1 |
| СПОСОБ КУЛЬТИВИРОВАНИЯ ИЗОЛИРОВАННЫХ ПЫЛЬНИКОВ РАСТЕНИЙ ЯРОВОГО РАПСА | 2006 |
|
RU2314680C2 |
| СПОСОБ ГЕНОТИПИЧЕСКОЙ ОЦЕНКИ ПРОИСХОЖДЕНИЯ РЕГЕНЕРАНТОВ КУЛЬТУРЫ ПЫЛЬНИКОВ ПРОСА (PANICUM MILIACEUM L.) | 2001 |
|
RU2199209C2 |
Изобретение относится к области сельскохозяйственной биотехнологии. Изобретение представляет собой способ получения дигаплоидных растений ячменя из культивируемых микроспор in vitro, включающий:
- выращивание растений-доноров при пониженной температуре воздуха 15-20°C, световом режиме: 16 ч день/8 ч ночь, влажности воздуха 60-70%, интенсивности освещения 10000-15000 люкс, с проведением фитосанитарной обработки, при этом выращивание растений-доноров осуществляют до стадии от открытия влагалища флагового листа, когда соцветие находится внутри флагового листа,
- стрессовую обработку колосьев при 4°C, в пробирках с бедной средой, содержащей KCl - 1,5 г/л, MgSO4×7H2O - 0,25 г/л, CaCl2×2Н2О - 0,1 г/л, маннитол - 60 г/л, калий-фосфатный буфер - 1 мл/л, pH 7,0, в течение 7 дней для переключения из гаметофитного пути развития микроспоры на спорофитный путь,
- выделение микроспор из колосков в стерильных условиях,
- культивирование выделенных микроспор на модифицированной среде для индукции эмбриогенеза, включающей 6% мальтозу, 10 завязей на 1,5 мл культуры и регуляторы роста растений в количестве 1 мг/л 2,4-Д, 0,2 мг/л зеатина, причем добавление вышеуказанных компонентов осуществляется перед добавлением микроспор,
- регенерацию растений из эмбриоидов путем культивирования на твердой питательной среде Мурашига и Скуга без добавления регуляторов роста растений,
- обработку гаплоидных растений ячменя антимитотическим препаратом N-диацетил-N-(β,γ-эпоксипропил) аминоколхицином для удвоения хромосом и получения дигаплоидых растений. Изобретение позволяет получить дигаплоидные гомозиготные линии ячменя для селекции новых сортов и гибридов с улучшенными свойствами. 1 ил., 2 табл., 6 пр.
1. Способ получения дигаплоидных растений ячменя из культивируемых микроспор in vitro, включающий:
- выращивание растений-доноров при пониженной температуре воздуха 15-20°C, световом режиме: 16 ч день/8 ч ночь, влажности воздуха 60-70%, интенсивности освещения 10000-15000 люкс, с проведением фитосанитарной обработки, при этом выращивание растений-доноров осуществляют до стадии от открытия влагалища флагового листа, когда соцветие находится внутри флагового листа,
- стрессовую обработку колосьев при 4°C, в пробирках с бедной средой, содержащей KCl - 1,5 г/л, MgSO4×7H2O - 0,25 г/л, CaCl2×2Н2О - 0,1 г/л, маннитол - 60 г/л, калий-фосфатный буфер - 1 мл/л, pH 7,0, в течение 7 дней для переключения из гаметофитного пути развития микроспоры на спорофитный путь,
- выделение микроспор из колосков в стерильных условиях,
- культивирование выделенных микроспор на модифицированной среде для индукции эмбриогенеза включающей 6% мальтозу, 10 завязей на 1,5 мл культуры и регуляторы роста растений в количестве 1 мг/л 2,4-Д, 0,2 мг/л зеатина, причем добавление вышеуказанных компонентов осуществляется перед добавлением микроспор,
- регенерацию растений из эмбриоидов путем культивирования на твердой питательной среде Мурашига и Скуга без добавления регуляторов роста растений,
- обработку гаплоидных растений ячменя антимитотическим препаратом N-диацетил-N-(β,γ-эпоксипропил) аминоколхицином для удвоения хромосом и получения дигаплоидых растений.
| БАШАБАЕВА Б.М., и др., Культура изолированных микроспор в создании генетически однородных и стабильных дигаплоидных генотипов ячменя, Биотехнология | |||
| Теория и практика, N1 (1 квартал), 2013, с | |||
| Пишущая машина для тюркско-арабского шрифта | 1922 |
|
SU24A1 |
| Приспособление для снятия бумаги с верхнего вала мокрого пресса | 1925 |
|
SU5799A1 |
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
Авторы
Даты
2015-07-20—Публикация
2013-10-04—Подача