ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА СМЕЖНЫЕ ЗАЯВКИ
В рамках настоящего изобретения испрашивается приоритет заявки с серийным номером 61/226923, поданной 20 июля 2009 года.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
В настоящем изобретении предлагается способ снижения концентрации глюкозы в крови животного путем трансплантации популяции клеток-предшественников панкреатических эндокринных клеток.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Достижения в области клеточной заместительной терапии сахарного диабета 1 типа и нехватка трансплантируемых островков Лангерганса заставили обратить внимание на разработку источников инсулинпродуцирующих клеток, или β-клеток, подходящих для трансплантации. Одним из подходов является формирование функциональных β-клеток из плюрипотентных стволовых клеток, таких как, например, эмбриональные стволовые клетки.
При эмбриональном развитии позвоночных плюрипотентные стволовые клетки дают начало группе клеток, формирующих три зародышевых листка (эктодерму, мезодерму и эндодерму) в ходе процесса, именуемого гаструляцией. Ткани, из которых состоят, например, щитовидная железа, тимус, поджелудочная железа, кишечник и печень, будут развиваться из эндодермы, через промежуточную стадию. Промежуточной стадией данного процесса является образование сформированной эндодермы. Клетки сформированной эндодермы экспрессируют ряд маркеров, таких как HNF3 бета, GATA4, MIXL1, CXCR4 и SOX17.
Формирование поджелудочной железы происходит при дифференцировке сформированной эндодермы в панкреатическую эндодерму. Клетки панкреатической эндодермы экспрессируют ген панкреатическо-дуоденального гомеобокса, PDX1. При отсутствии PDX1 развитие поджелудочной железы не идет дальше формирования вентрального и дорзального зачатков. Следовательно, экспрессия PDX1 является важным этапом органогенеза поджелудочной железы. Зрелая поджелудочная железа содержит, среди других типов клеток, экзокринную ткань и эндокринную ткань. Экзокринная и эндокринная ткани образуются при дифференцировке панкреатической эндодермы.
Клетки, обладающие свойствами островковых клеток, как сообщалось, были получены из эмбриональных клеток мыши. Например, в публикации Lumelsky et al. (Science 292:1389, 2001) сообщается о дифференцировке мышиных эмбриональных стволовых клеток в инсулин-секретирующие структуры, аналогичные островкам поджелудочной железы. Soria et al. (Diabetes 49:157, 2000) сообщают, что инсулин-секретирующие клетки, полученные из мышиных эмбриональных стволовых клеток, нормализовали гликемию у мышей с диабетом, вызванным стрептозотоцином.
В одном примере в публикации Hori et al. (PNAS 99: 16105, 2002) описывается, что обработка мышиных эмбриональных стволовых клеток ингибиторами фосфоинозитид-3-киназы (LY294002) приводила к получению клеток, подобных β-клеткам.
В другом примере в публикации Blyszczuk et al. (PNAS 100:998, 2003) сообщается о получении инсулинпродуцирующих клеток из мышиных эмбриональных стволовых клеток с конститутивной экспрессией Pax4.
В публикации Micallef et al. сообщается, что ретиноевая кислота может регулировать способность эмбриональных стволовых клеток формировать PDX1-положительную панкреатическую эндодерму. Ретиноевая кислота с наибольшей эффективностью индуцирует экспрессию PDX1 при добавлении в культуру на четвертый день дифференцировки эмбриональных стволовых клеток в течение периода, соответствующего концу гаструляции эмбриона (Diabetes 54:301, 2005).
В публикации Miyazaki et al. сообщается о линии мышиных эмбриональных стволовых клеток со сверхэкспрессией Pdx1. Результаты показывают, что экспрессия экзогенного Pdx1, очевидно, повышает экспрессию генов инсулина, соматостатина, глюкокиназы, нейрогенина3, p48, Pax6 и HNF6 в образующихся дифференцированных клетках (Diabetes 53: 1030, 2004).
В публикации Skoudy et al. сообщается, что активин A (входящий в суперсемейство TGF-β) повышает экспрессию экзокринных панкреатических генов (p48 и амилаза) и эндокринных генов (Pdx1, инсулин и глюкагон) в эмбриональных стволовых клетках мыши. Максимальный эффект наблюдался при использовании активина A в концентрации 1 нМ. Также эти авторы наблюдали, что на уровень экспрессии мРНК инсулина и Pdx1 не влияла ретиноевая кислота; однако обработка раствором FGF7 с концентрацией 3 нМ приводила к повышению уровня транскрипта Pdx1 (Biochem. J. 379: 749, 2004).
В работе Shiraki et al. изучались эффекты факторов роста, специфически ускоряющих дифференцирование эмбриональных стволовых клеток в PDX1-положительные клетки. Эти авторы наблюдали, что TGF-β2 приводил к воспроизводимому увеличению доли PDX1-положительных клеток (Genes Cells. 2005 Jun; 10(6): 503-16.).
В публикации Gordon et al. продемонстрирована индукция образования brachyury-[положительных]/HNF3 бета [положительных] эндодермальных клеток из эмбриональных стволовых клеток мыши в отсутствие сыворотки и в присутствии активина в сочетании с ингибитором сигнального пути Wnt (патент США № 2006/0003446A1).
В публикации Gordon et al. (PNAS, Vol 103, page 16806, 2006) говорится: «Для образования передней первичной полоски требовались одновременно сигнальные пути Wnt и TGF-бета/Nodal/активин».
Однако модель развития эмбриональных стволовых клеток на мышах может не имитировать в точности программу развития у высших млекопитающих, как, например, у человека.
Thomson et al. выделяли эмбриональные стволовые клетки из человеческих бластоцист (Science 282:114, 1998). Параллельно Gearhart и соавторы получили клеточные линии человеческих эмбриональных зародышевых клеток (чЭЗ) из ткани половых желез эмбриона (Shamblott et al., Proc. Natl. Acad. Sci. USA 95: 13726, 1998). В отличие от эмбриональных стволовых клеток мыши, воспрепятствовать дифференцировке которых можно путем простого культивирования с фактором торможения лейкемиии (Leukemia Inhibitory Factor, LIF), человеческие эмбриональные стволовые клетки должны культивироваться в очень специфических условиях (патент США № 6200806, WO 99/20741, WO 01/51616).
D'Amour et al. описывают производство обогащенных культур сформированной эндодермы, производной от человеческих эмбриональных стволовых клеток, в присутствии высокой концентрации активина и низкой концентрации сыворотки (Nature Biotechnology 2005). Трансплантация этих клеток под почечную капсулу мышей приводит к их дифференцировке в более зрелые клетки, обладающие характерными особенностями некоторых эндодермальных органов. Клетки сформированной эндодермы, производные от человеческих эмбриональных стволовых клеток, могут подвергаться дальнейшей дифференцировке в PDX1-положительные клетки после добавления FGF-10 (№ US2005/0266554A1).
В публикации D'Amour et al. (Nature Biotechnology - 24, 1392-1401 (2006)) говорится: «Мы разработали процесс дифференцирования, преобразующий человеческие эмбриональные стволовые клетки (чЭС) в эндокринные клетки, способные синтезировать гормоны поджелудочной железы, инсулин, глюкагон, соматостатин, панкреатический полипептид и грелин. Данный процесс имитирует органогенез поджелудочной железы in vivo, проводя клетки через стадии, напоминающие образование сформированной эндодермы, эндодермы кишечной трубки, панкреатической эндодермы и превращение предшественников эндокринных клеток в клетки, экспрессирующие эндокринные гормоны».
В другом примере Fisk et al. сообщают о системе для производства островковых клеток поджелудочной железы из человеческих эмбриональных стволовых клеток (заявка на патент № US2006/0040387A1). В данном случае процесс дифференцировки был разделен на три стадии. Сначала человеческие эмбриональные стволовые клетки были дифференцированы до эндодермы с помощью сочетания бутирата натрия и активина А. Далее клетки культивировались с антагонистами TGF-β, такими как Noggin, в сочетании с EGF или бетацеллюлином с получением PDX1-положительных клеток. Окончательная дифференцировка запускалась никотинамидом.
В одном примере Benvenistry et al. сообщают: «Мы делаем вывод, что сверхэкспрессия PDX1 увеличивала экспрессию панкреатических обогащенных генов, а для индукции экспрессии инсулина могут требоваться дополнительные сигналы, присутствующие только in vivo» (Benvenistry et al., Stem Cells 2006; 24:1923-1930).
В другом примере в заявке на патент № US2008/0241107A1 объявляется о способе получения клеток, секретирующих инсулин, включающем: a) получение клеток, не продуцирующих инсулин, и b) инкубацию клеток в среде, содержащей высокую концентрацию глюкозы, в которой клетки секретируют инсулин.
Следовательно, насущной потребностью по-прежнему остается разработка условий для создания стабильных линий плюрипотентных стволовых клеток, способных расти для решения текущих клинических задач и сохраняющих потенциал дифференцировки в панкреатические эндокринные клетки, в клетки, экспрессирующие гормоны поджелудочной железы, или в клетки, секретирующие гормоны поджелудочной железы. Мы использовали альтернативный подход к повышению эффективности дифференцирования человеческих эмбриональных стволовых клеток в панкреатические эндокринные клетки.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В одном варианте осуществления настоящего изобретения предлагается способ снижения концентрации глюкозы в крови животных путем трансплантации животному популяции клеток-предшественников панкреатических эндокринных клеток.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг. 1 показано влияние разных базальных сред на экспрессию NKX6.1 (панель a), PDX1 (панель b), PTF1 альфа (панель c) и NGN3 (панель d). Повторные образцы отбирались на стадии 4, день 3, для анализа методом ПЦР реального времени. На графиках представлена кратность индукции экспрессии каждого гена в сравнении с использованием среды DMEM/F12.
На фиг. 2 показаны иммунофлуоресцентные фотографии с окрашиванием панкреатического маркера PDX1 (панели a и b), NKX6.1 (панели c и d), CDX2 (панели e и f) и NGN3 (панели g и h) при обработке клеток средой DMEM/F12 (панели a, c, e и g) и при обработке клеток средой DMEM с высоким содержанием глюкозы (панели b, d, f и h) на стадии 4, день 3, обработка проводилась в соответствии с примером 1.
На фиг. 3 показана экспрессия PDX1 (панель a), NKX6.1 (панель b), PTF1 альфа (панель c), NGN3 (панель d), PAX4 (панель e) и NKX2.2 (панель f) в образцах клеток, обработанных способами, описанными в примере 2. Повторные образцы отбирались для анализа методом ПЦР реального времени в указанные сроки. На графиках показана кратность увеличения экспрессии каждого гена относительно экспрессии этих генов на стадии 3, день 1.
На фиг. 4 показана экспрессия инсулина (INS), глюкагона (GCG), PDX1, NKX6.1, NGN3, MAFB и NEUROD в клетках, обработанных способами, описанными в примере 2. Повторные образцы отбирались для анализа методом ПЦР реального времени. На графиках показана кратность увеличения экспрессии каждого гена относительно экспрессии этих генов на стадии 3, день 4. Светло-серыми столбцами представлены данные для образцов, полученных из клеток, собранных на стадии 3, день 4. Темно-серыми столбцами представлены данные для образцов, полученных из клеток, собранных на стадии 4, день 3. Черными столбцами представлены данные для образцов, полученных из клеток, собранных на стадии 5, день 5.
На фиг. 5, панель a, показана экспрессия PDX1, NKX6.1, NGN и PTF1-альфа в клетках, обработанных способами, описанными в примере 3. Повторные образцы отбирались на стадии 4, день 3, для анализа методом ПЦР реального времени. На графиках показана кратность индукции экспрессии каждого гена относительно первой группы обработки на стадии 4, день 3. Светло-серыми столбцами представлены данные для образцов, полученных из клеток, собранных из группы T1 (обработка 1). Белыми столбцами представлены данные для образцов, полученных из клеток, собранных из группы T2 (обработка 2). Темно-серыми столбцами представлены данные для образцов, полученных из клеток, собранных из группы T3 (обработка 3). Черными столбцами представлены данные для образцов, полученных из клеток, собранных из группы T4 (обработка 4). На панели b показана экспрессия инсулина в клетках, обработанных способами, описанными в примере 3. Повторные образцы отбирались для анализа методом ПЦР реального времени на стадии 4, день 3 (S4, D3), и на стадии 4, день 8 (S4, D8). На графиках показана кратность индукции экспрессии каждого гена относительно первой группы обработки (T1) на стадии 4, день 3.
На фиг. 6 показана кинетика секреции человеческого С-пептида при стимуляции глюкозой в трансплантированных клетках-предшественниках эндокринных клеток. В частности, показаны уровни человеческого С-пептида (ось y) через 60 минут после добавления глюкозы. На оси x показан номер животного и количество дней после трансплантации.
На фиг. 7 показана кинетика секреции человеческого С-пептида при стимуляции глюкозой в трансплантированных клетках-предшественниках эндокринных клеток. В частности, показаны уровни человеческого С-пептида (ось y) через 60 минут после добавления глюкозы (панель a) и уровни человеческого С-пептида до и после добавления глюкозы (панель b). На оси x показан номер животного и количество дней после трансплантации.
На фиг. 8 показана кинетика секреции человеческого С-пептида при стимуляции глюкозой в трансплантированных клетках-предшественниках эндокринных клеток. В частности, показаны уровни человеческого С-пептида (ось y) через 60 минут после добавления глюкозы. На оси x показан номер животного и количество дней после трансплантации.
На фиг. 9 показана кинетика секреции человеческого С-пептида при стимуляции глюкозой в трансплантированных клетках-предшественниках эндокринных клеток. В частности, показаны уровни человеческого С-пептида (ось y) через 60 минут после добавления глюкозы (панель a) и уровни человеческого С-пептида до и после добавления глюкозы (панель b). По оси x показан номер животного и количество дней после трансплантации.
На фиг. 10 показана кинетика секреции человеческого С-пептида при стимуляции глюкозой в трансплантированных клетках-предшественниках эндокринных клеток. В частности, показаны уровни человеческого С-пептида (ось y) через 60 минут после добавления глюкозы (панель a) и уровни человеческого С-пептида до и после добавления глюкозы (панель b). На оси x показан номер животного и количество дней после трансплантации.
На фиг. 11 показаны данные морфологического и иммунофлуоресцентного анализа образцов трансплантата через 3 недели после имплантации. На микрофотографиях серии срезов показаны a) окрашивание на человеческий ядерный антиген и DAPI, b) окрашивание на CK19 и PDX1.
На фиг. 12 показаны данные морфологического и иммунофлуоресцентного анализа образцов трансплантата, окрашенных на инсулин и глюкагон, через 3 недели (панель a), 10 недель (панель b) и 13 недель (панель c) после имплантации. На панели d показаны данные морфологического и иммунофлуоресцентного анализа образцов трансплантата, окрашенных на PDX1 и инсулин через 13 недель после имплантации. На панели e показаны данные морфологического и иммунофлуоресцентного анализа образцов трансплантата, окрашенных на NEUROD1 и инсулин через 13 недель после имплантации.
ПОДРОБНОЕ ОПИСАНИЕ
Для ясности описания, а не для ограничения изобретения, подробное описание изобретения разделено на следующие подразделы, описывающие или иллюстрирующие определенные особенности, варианты осуществления или области применения настоящего изобретения.
Определения
Стволовые клетки представляют собой недифференцированные клетки, определяемые по их способности на уровне единичной клетки как самообновляться, так и дифференцироваться с образованием клеток-потомков, таких как самообновляющиеся клетки-предшественники, необновляющиеся клетки-предшественники и окончательно дифференцированные клетки. Стволовые клетки также характеризуются способностью дифференцироваться in vitro в функциональные клетки различных клеточных линий дифференцирования из нескольких зародышевых листков (эндодермы, мезодермы и эктодермы), а также после трансплантации давать начало тканям, происходящим от нескольких зародышевых листков, и вносить существенный вклад в формирование большинства, если не всех, тканей после инъекции в бластоцисты.
По потенциалу развития стволовые клетки классифицируются следующим образом: (1) тотипотентные, т.е. способные давать начало всем эмбриональным и внеэмбриональным типам клеток; (2) плюрипотентные, т.е. способные давать начало всем эмбриональным типам клеток; (3) мультипотентные, т.е. способные давать начало группе клеточных линий дифференцирования в пределах конкретной ткани, органа или физиологической системы (например, гематопоэтические стволовые клетки (HSC) могут давать таких потомков, как HSC (самообновление), олигопотентные предшественники, ограниченные клетками крови, и все типы клеток и клеточных элементов (таких как тромбоциты), являющиеся нормальными компонентами крови); (4) олигопотентные, т.е. способные давать начало более ограниченному набору клеточных линий дифференцирования, чем мультипотентные стволовые клетки; и (5) унипотентные, т.е. способные давать начало единственной клеточной линии дифференцирования (например, сперматогенные стволовые клетки).
Дифференцировка представляет собой процесс, при помощи которого неспециализированная («некоммитированная») или малоспециализированная клетка приобретает свойства специализированной клетки, например нервной или мышечной. Дифференцированная клетка или клетка с индуцированной дифференцировкой представляет собой клетку, занявшую более специализированную («коммитированную») позицию в пределах клеточной линии дифференцировки. Термин «коммитированная» применительно к процессу дифференцирования обозначает клетку, дошедшую в ходе процесса дифференцирования до стадии, от которой в нормальных условиях она продолжит дифференцироваться до определенного типа клеток или набора типов клеток и не сможет в нормальных условиях дифференцироваться в иной тип клеток или вернуться обратно к менее дифференцированному типу. Дедифференцированием называется процесс, в ходе которого клетка возвращается к менее специализированному (или коммитированному) положению в линии дифференцирования. В настоящем документе линией дифференцировки клеток называется наследственность клетки, т.е. от каких клеток она происходит и каким клеткам может дать начало. В линии дифференцировки клетка помещается в наследственную схему развития и дифференцировки. Маркером, специфичным для линии дифференцировки, называется характерная особенность, специфически ассоциированная с фенотипом клеток конкретной линии дифференцировки, которая может использоваться для оценки дифференцировки некоммитированных клеток в данную линию дифференцировки.
Используемые в настоящей заявке термины «клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы», «клетки стадии 1» или «стадия 1», относятся к клеткам, экспрессирующим по меньшей мере один из следующих маркеров: SOX-17, GATA4, HNF3 бета, GSC, CER1, Nodal, FGF8, Brachyury, Mix-подобный гомеобоксовый белок, FGF4 CD48, эомезодермин (EOMES), DKK4, FGF17, GATA6, CXCR4, C-Kit, CD99 или OTX2. К клеткам, экспрессирующим маркеры, характерные для линии сформированной эндодермы, относятся клетки-предшественники первичной полоски, клетки первичной полоски, клетки мезэндодермы и клетки сформированной эндодермы.
Используемый в настоящей заявке термин «клетки с экспрессией маркеров, характерных для линии панкреатической эндодермы» относится к клеткам с экспрессией по меньшей мере одного из следующих маркеров: PDX1, HNF-1 бета, PTF1 альфа, HNF6 или HB9. К клеткам, экспрессирующим маркеры, характерные для линии панкреатической эндодермы, относятся клетки панкреатической эндодермы, клетки первичной кишечной трубки и клетки поздней передней кишки.
Используемый в настоящей заявке термин «клетки с экспрессией маркеров, характерных для линии панкреатических эндокринных клеток» относится к клеткам с экспрессией по меньшей мере одного из следующих маркеров: NEUROD, ISL1, PDX1, NKX6.1, MAFB, инсулин, глюкагон или соматостатин. Клетки с экспрессией маркеров, характерных для линии панкреатических эндокринных клеткок, включают в себя панкреатические эндокринные клетки, клетки, экспрессирующие панкреатические гормоны, клетки, секретирующие панкреатические гормоны, а также клетки β-клеточной линии.
Используемый в настоящей заявке термин «сформированная эндодерма» относится к клеткам, обладающим характерными особенностями клеток, происходящих в ходе гаструляции от эпибласта, и формирующим желудочно-кишечный тракт и его производные. Клетки дефинитивной эндодермы экспрессируют следующие маркеры: HNF3 бета, GATA4, SOX17, Cerberus, OTX2, goosecoid, C-Kit, CD99 и MIXL1.
«Маркерами» в настоящем документе называются молекулы нуклеиновых кислот или полипептидов, дифференциально экспрессируемые в конкретной клетке. В данном контексте под дифференциальной экспрессией подразумевается повышение уровня экспрессии для положительного маркера и понижение уровня экспрессии для отрицательного маркера. Поддающийся обнаружению уровень маркерной нуклеиновой кислоты или полипептида в интересующих клетках оказывается значительно выше или ниже по сравнению с другими клетками, что позволяет идентифицировать интересующую клетку и отличить ее от других клеток с помощью любого из множества известных в данной области способов.
«Панкреатической эндокринной клеткой» или «клеткой, экспрессирующей гормон поджелудочной железы» в настоящем документе называется клетка, экспрессирующая по меньшей мере один из следующих гормонов: инсулин, глюкагон, соматостатин и панкреатический полипептид.
«Клеткой-предшественником панкреатической эндокринной клетки» в настоящем документе называется мультипотентная клетка линии сформированной эндодермы, которая экспрессирует NGN3 и которая может подвергаться дальнейшей дифференцировке в клетки эндокринной системы, включая, помимо прочего, панкреатические островковые клетки, экспрессирующие гормоны. Клетки-предшественники эндокринных клеток не могут дифференцироваться в разные типы клеток, тканей и (или) органов, как и менее специфически дифференцированные клетки линии сформированной эндодермы, такие как PDX1-положительные клетки панкреатической эндодермы.
«Клеткой, продуцирующей гормон поджелудочной железы» в настоящем документе называется клетка, способная производить по меньшей мере один из следующих гормонов: инсулин, глюкагон, соматостатин и панкреатический полипептид.
«Клеткой, секретирующей гормон поджелудочной железы» в настоящем документе называется клетка, способная секретировать по меньшей мере один из следующих гормонов: инсулин, глюкагон, соматостатин и панкреатический полипептид.
Выделение, размножение и культивирование плюрипотентных стволовых клеток
Характеристика плюрипотентных стволовых клеток
Плюрипотентные стволовые клетки могут экспрессировать один или несколько стадийно-специфичных эмбриональных антигенов (SSEA) 3 и 4, а также маркеры, определяемые антителами, обозначенными Tra-1-60 и Tra-1-81 (Thomson et al., Science 282:1145, 1998). Дифференцировка плюрипотентных стволовых клеток in vitro приводит к утрате экспрессирования SSEA-4, Tra-1-60 и Tra-1-81 (если имеются) и к увеличению экспрессии SSEA-1. В недифференцированных плюрипотентных стволовых клетках, как правило, активна щелочная фосфатаза, которая может быть обнаружена путем фиксации клеток с помощью 4% параформальдегида, с последующим обнаружением с помощью Vector Red, применяемого в качестве субстрата, в соответствии с инструкциями производителя (Vector Laboratories, Burlingame Calif.). Недифференцированные плюрипотентные стволовые клетки так же, как правило, экспрессируют Oct-4 и TERT, обнаруживаемые методом ОТ-ПЦР.
Другим желательным фенотипическим свойством выращенных плюрипотентных клеток является потенциал дифференцировки в клетки всех трех зародышевых листков: в эндодермальные, мезодермальные и эктодермальные ткани. Плюрипотентность плюрипотентных стволовых клеток может быть подтверждена, например, путем инъекции клеток мышам с тяжелым комбинированным иммунодефицитом (SCID), фиксирования образующихся тератом с помощью 4% параформальдегида, и их гистологического исследования для получения доказательств наличия клеточных типов, происходящих от трех зародышевых листков. Как вариант, плюрипотентность можно определить путем создания эмбриоидных телец и анализа их на предмет присутствия маркеров, ассоциирующихся с тремя зародышевыми листками.
Выращенные линии плюрипотентных стволовых клеток могут быть кариотипированы с применением стандартного способа окрашивания с использованием красителя Гимза (G-banding) и сравнения с опубликованными кариотипами соответствующих видов приматов. Желательно получить клетки, имеющие «нормальный кариотип», т.е. эуплоидные клетки, при этом все человеческие хромосомы должны присутствовать и не иметь видимых изменений.
Источники плюрипотентных стволовых клеток
К типам плюрипотентных стволовых клеток, которые можно использовать, относятся стабильные линии плюрипотентных клеток, получаемых из ткани, формирующейся после наступления беременности, в том числе из преэмбриональной ткани (например, бластоциста), эмбриональной ткани или ткани плода, взятой в любой момент в ходе беременности, как правило, но не обязательно, до срока приблизительно 10-12 недель беременности. Примерами, не ограничивающими настоящее изобретение, являются стабильные линии человеческих эмбриональных стволовых клеток или человеческих эмбриональных зародышевых клеток, например, клеточные линии человеческих эмбриональных стволовых клеток H1, H7 и H9 (WiCell). Также возможно использование описываемых в настоящей заявке составов в ходе первоначального установления или стабилизации таких клеток; в этом случае исходными клетками являются первичные плюрипотентные клетки, взятые непосредственно из тканей-источников. Также подходящими являются клетки, взятые из популяции плюрипотентных стволовых клеток, уже культивируемых в отсутствие питающих клеток. Также соответствуют целям настоящего изобретения клетки мутантных линий эмбриональных стволовых клеток человека, таких как, например, BG01v (BresaGen, Атенс, Джорджия, США).
В одном из вариантов осуществления эмбриональные стволовые клетки человека готовят, как описано в следующих публикациях Thomson et al. (патент № 5843780; Science 282:1145, 1998; Curr. Top. Dev. Biol. 38:133 ff., 1998; Proc. Natl. Acad. Sci. U.S.A. 92:7844, 1995).
Культивирование плюрипотентных стволовых клеток
В одном из вариантов осуществления плюрипотентные стволовые клетки, как правило, культивируются на слое питающих клеток, которые оказывают разнообразную поддержку плюрипотентным клеткам. Как вариант, плюрипотентные стволовые клетки культивируются в культуральной системе, по существу не содержащей питающих клеток, но, тем не менее, поддерживающей пролиферацию плюрипотентных стволовых клеток и не допускающей существенной дифференцировки. Выращивание плюрипотентных стволовых клеток в культуре, не содержащей питающих клеток, без дифференцировки, осуществляется при помощи среды, кондиционированной путем предварительного культивирования в ней клеток другого типа. Как вариант, выращивание плюрипотентных стволовых клеток в культуре, не содержащей питающих клеток, без дифференцировки, осуществляется при помощи среды с определенным химическим составом.
Например, в работе Reubinoff et al. (Nature Biotechnology 18: 399-404 (2000)) и Thompson et al. (Science 6 November 1998: Vol. 282. no. 5391, pp. 1145-1147) описано культивирование линий плюрипотентных стволовых клеток из человеческих бластоцист с применением слоя питающих клеток из мышиных эмбриональных фибробластов.
Richards et al. (Stem Cells 21: 546-556, 2003) анализировали набор из одиннадцати слоев питающих клеток, полученных от взрослых, новорожденных и эмбрионов людей, по их способности осуществлять поддержку культуры человеческих плюрипотентных стволовых клеток. Richards et al. сообщают следующее: «Линии человеческих эмбриональных стволовых клеток, культивируемые на питающих слоях из фибробластов кожи взрослых людей, сохраняют морфологию, характерную для эмбриональных стволовых клеток, и остаются плюрипотентными».
В заявке на патент № US20020072117 описываются линии клеток, продуцирующие среду, осуществляющую поддержку плюрипотентных стволовых клеток приматов в культуре, не содержащей питающих клеток. Использованные клеточные линии представляют собой мезенхимо- и фибробласто-подобные линии, полученные из эмбриональной ткани или дифференцированные из эмбриональных стволовых клеток. В заявке на патент № US20020072117 также описывается использование этих клеточных линий в качестве первичного слоя питающих клеток.
В другом примере Wang et al. (Stem Cells 23: 1221-1227, 2005) описывают способы длительного выращивания человеческих плюрипотентных стволовых клеток на слоях питающих клеток, полученных из человеческих эмбриональных стволовых клеток.
В другом примере Stojkovic et al. (Stem Cells 2005 23: 306-314, 2005) описывают систему питающих клеток, получаемую в результате спонтанного дифференцирования человеческих эмбриональных стволовых клеток.
В еще одном примере Miyamoto et al. (Stem Cells 22: 433-440, 2004) описывают получение питающих клеток из человеческой плаценты.
Amit et al (Biol. Reprod 68: 2150-2156, 2003) описывают слой питающих клеток, полученных из человеческой крайней плоти.
В другом примере Inzunza et al. (Stem Cells 23: 544-549, 2005) описывают слой питающих клеток, полученных из человеческих фибробластов постнатальной крайней плоти.
В патенте № US6642048 описывается среда, поддерживающая рост плюрипотентных стволовых клеток приматов (пПС) в среде, не содержащей питающих клеток, и клеточные линии, которые могут использоваться для производства такой среды. В патенте № US6642048 говорится: «Настоящее изобретение включает мезенхимо- и фибробласто-подобные клеточные линии, полученные из эмбриональной ткани или дифференцированные из эмбриональных стволовых клеток. В документе описываются и иллюстрируются способ получения таких клеточных линий, обработки среды и выращивания стволовых клеток с применением кондиционированной среды».
В другом примере, заявке на патент № WO2005014799, описывается кондиционированная среда для поддержания, пролиферации и дифференцировки клеток млекопитающих. В заявке на патент № WO2005014799 говорится: «Культуральная среда, изготовленная в соответствии с настоящим изобретением, кондиционируется при помощи секреторной активности клеток мыши, в частности активности дифференцированных и иммортализованных трансгенных гепатоцитов, именуемых MMH (Met Murine Hepatocyte)».
В другом примере Xu et al. (Stem Cells 22: 972-980, 2004) описывают кондиционированную среду, полученную из производных человеческих эмбриональных стволовых клеток, генетически модифицированных для увеличения экспрессии обратной транскриптазы человеческой теломеразы.
В другом примере, заявке на патент № US20070010011, описывается культуральная среда определенного химического состава для поддержания плюрипотентных стволовых клеток.
В альтернативной культуральной системе используется не содержащая сыворотки среда, обогащенная факторами роста, способными стимулировать пролиферацию эмбриональных стволовых клеток. Например, Cheon et al. (BioReprod DOI:10.1095/biolreprod.105.046870, October 19, 2005) описывают не содержащую питающих клеток и сыворотки культуральную систему, в которой эмбриональные стволовые клетки поддерживаются в некондиционированной, заменяющей сыворотку среде (SR), обогащенной различными факторами роста, способными запустить самообновление эмбриональных стволовых клеток.
В другом примере Levenstein et al. (Stem Cells 24: 568-574, 2006) описывают способы длительного культивирования человеческих эмбриональных стволовых клеток в отсутствие фибробластов или кондиционированной среды с применением среды, обогащенной основным фактором роста фибробластов (bFGF).
В другом примере, заявке на патент № US20050148070, описывается способ культивирования человеческих эмбриональных стволовых клеток в среде с определенным составом без сыворотки и без питающих клеток-фибробластов, где данный способ включает: культивирование стволовых клеток в культуральной среде, содержащей альбумин, аминокислоты, витамины, минеральные вещества, по меньшей мере один трансферрин или заменитель трансферрина, по меньшей мере один инсулин или заместитель инсулина, культуральную среду, в основном не включающую эмбриональную сыворотку млекопитающих и содержащую по меньшей мере приблизительно 100 нг/мл фактора роста фибробластов, способного активировать сигнальный рецептор фактора роста фибробластов, при этом фактор роста фибробластов происходит из источника, иного, чем просто слой питающих клеток-фибробластов, среду, поддерживающую пролиферацию стволовых клеток в недифференцированном состоянии без слоя питающих клеток или кондиционированной среды.
В другом примере, заявке на патент № US20050233446, описывается среда с определенным составом, которая может использоваться при культивировании стволовых клеток, включая недифференцированные зародышевые стволовые клетки приматов. В растворе среда по существу является изотонической относительно культивируемых стволовых клеток. В данной культуре указанная среда содержит основную среду и количество bFGF, инсулина и аскорбиновой кислоты, достаточное для поддержки роста зародышевых стволовых клеток без значительной дифференцировки.
В другом примере, патенте № US6800480, говорится: «В одном варианте осуществления предлагается культуральная среда для выращивания клеток зародышевых стволовых клеток приматов, в значительной степени в недифференцированном состоянии, включающая основную среду с низким содержанием эндотоксина и низким осмотическим давлением, которая эффективно поддерживает рост зародышевых стволовых клеток приматов. Основная среда объединяется с питательной сывороткой, способной поддерживать рост зародышевых стволовых клеток приматов, и субстратом, выбираемым из группы, включающей питающие клетки и экстраклеточный матрикс, полученный из питающих клеток. Среда также содержит аминокислоты, не относящиеся к незаменимым, антиоксидант и первый фактор роста, выбираемый из группы, содержащей нуклеозиды и соль-пируват».
В другом примере, заявке на патент № US20050244962, говорится: «В одном аспекте, в изобретении предлагается способ культивирования эмбриональных стволовых клеток приматов. Стволовые клетки культивируются в культуре, в основном не содержащей эмбриональной сыворотки млекопитающих (предпочтительно также в основном не содержащей эмбриональной сыворотки любых животных) и в присутствии фактора роста фибробластов, полученного из источника, иного, чем просто питающие клетки-фибробласты. В предпочтительной форме слой питающих фибробластов, ранее необходимый для поддержания культуры стволовых клеток, становится необязательным вследствие добавления достаточного количества фактора роста фибробластов».
В другом примере, заявке на патент № WO2005065354, описывается изотоническая культуральная среда определенного состава, в основном не содержащая питающих клеток и сыворотки, включающая: a. базовую среду, b. количество bFGF, достаточное для поддержки роста в основном не дифференцированных стволовых клеток млекопитающих, c. количество инсулина, достаточное для поддержки роста в основном не дифференцированных стволовых клеток млекопитающих, и d. количество аскорбиновой кислоты, достаточное для поддержки роста в основном не дифференцированных стволовых клеток млекопитающих.
В другом примере в заявке на патент № WO2005086845 описывается способ поддержания недифференцированных стволовых клеток, включающий воздействие на стволовые клетки одним членом семейства белков трансформирующего ростового фактора-бета (TGF-β), одним членом семейства белков фактора роста фибробластов (FGF) или никотинамидом (NIC) в количестве, достаточном для поддержания клеток в недифференцированном состоянии в течение периода времени, достаточного для получения желаемого результата.
Плюрипотентные стволовые клетки могут быть нанесены на подходящий культуральный субстрат. В одном из вариантов осуществления подходящим культуральным субстратом является компонент экстраклеточного матрикса, например, полученный из базальной мембраны или тот, который может участвовать в образовании связи между рецептором молекул адгезии и лигандом. В одном из вариантов осуществления подходящим культуральным субстратом является MATRIGEL® (Becton Dickenson). MATRIGEL® представляет собой растворимый препарат из клеток опухоли Энгельбрета-Холма-Суорма, который при комнатной температуре превращается в гель и образует восстановленную базальную мембрану.
В альтернативном варианте, можно использовать другие компоненты экстраклеточного матрикса и смеси компонентов. В зависимости от типа пролиферирующих клеток, это может быть ламинин, фибронектин, протеогликан, энтактин, гепарансульфат и т. п., отдельно или в различных сочетаниях.
Плюрипотентные стволовые клетки могут высеваться на субстрат с соответствующим распределением по поверхности и в присутствии среды, поддерживающей выживание, размножение и сохранение требуемых характеристик клеток. На все характеристики оказывает влияние аккуратность распределения клеток при посеве, которая легко может быть определена специалистом в данной области.
Подходящая культуральная среда может быть изготовлена из следующих компонентов, таких как, например, модифицированная по способу Дульбекко среда Игла (DMEM), Gibco № 11965-092, нокаутная модифицированная по способу Дульбекко среда Игла (KO DMEM), Gibco № 10829-018, базовая среда Хэма F12/50% DMEM, 200 мМ L-глутамин, Gibco № 15039-027, раствор заменимых аминокислот, Gibco № 11140-050, β-меркаптоэтанол, Sigma № M7522, человеческий рекомбинантный основной фактор роста фибробластов (bFGF), Gibco № 13256-029.
Получение клеток-предшественников панкреатических эндокринных клеток
В одном из вариантов осуществления настоящего изобретения предлагается способ получения клеток-предшественников панкреатических эндокринных клеток, включающий следующие этапы:
a. культивирование плюрипотентных стволовых клеток;
b. дифференцировку плюрипотентных стволовых клеток в клетки, экспрессирующих маркеры, характерные для линии сформированной эндодермы;
c. дифференцировку клеток, экспрессирующих маркеры, характерные для линии сформированной эндодермы, в клетки, экспрессирующие маркеры, характерные для линии панкреатической эндодермы;
d. дифференцировку клеток, экспрессирующих маркеры, характерные для линии панкреатической эндодермы, в клетки-предшественники панкреатических эндокринных клеток.
К плюрипотентным стволовым клеткам, которые могут использоваться в настоящем изобретении, относятся, например, человеческие эмбриональные стволовые клетки линии H9 (код NIH: WA09), человеческие эмбриональные стволовые клетки линии H1 (код NIH: WA01), человеческие эмбриональные стволовые клетки линии H7 (код NIH: WA07) и человеческие эмбриональные стволовые клетки линии SA002 (Cellartis, Швеция). Также для использования в рамках настоящего изобретения подходят клетки, экспрессирующие по меньшей мере один из следующих маркеров, характерных для плюрипотентных клеток: ABCG2, CRIPTO, CD9, FOXD3, Connexin43, Connexin45, OCT4, SOX2, Nanog, hTERT, UTF1, ZFP42, SSEA-3, SSEA-4, Tra 1-60, Tra 1-81.
Маркеры, характерные для линии сформированной эндодермы, выбираются из группы, состоящей из SOX17, GATA4, HNF3 бета, GSC, CER1, Nodal, FGF8, Brachyury, Mix-подобного гомеобоксового белка, FGF4 CD48, эомезодермина (EOMES), DKK4, FGF17, GATA6, CXCR4, C-Kit, CD99 и OTX2. Подходит для использования в настоящем изобретении клетка, экспрессирующая по меньшей мере один из маркеров, характерных для линии сформированной эндодермы. В одном аспекте настоящего изобретения клетка, экспрессирующая маркеры, характерные для линии сформированной эндодермы, представляет собой клетку-предшественницу первичной полоски. В другом аспекте настоящего изобретения клетка, экспрессирующая маркеры, характерные для линии сформированной эндодермы, представляет собой мезэндодермальную клетку. В другом аспекте настоящего изобретения клетка, экспрессирующая маркеры, характерные для линии сформированной эндодермы, представляет собой клетку сформированной эндодермы.
Маркеры, характерные для линии дифференцирования панкреатической эндодермы, выбирают из группы, состоящей из следующих маркеров: PDX1, HNF1 бета, HNF6, HB9 и PROX1. Подходит для использования в настоящем изобретении клетка, экспрессирующая по меньшей мере один из маркеров, характерных для линии панкреатической эндодермы. В одном из аспектов настоящего изобретения клетка, экспрессирующая маркеры, характерные для линии панкреатической эндодермы, представляет собой клетку панкреатической эндодермы.
Маркеры, характерные для клеток-предшественников панкреатических эндокринных клеток, выбирают из группы, состоящей из следующих маркеров: NGN3, NKX6.1, NeuroD, ISL1, PDX1, PAX4, NKX2.2 или ARX. Подходит для использования в настоящем изобретении клетка, экспрессирующая по меньшей мере один из маркеров, характерных для линии клеток-предшественников панкреатических эндокринных клеток.
Образование клеток, экспрессирующих маркеры, характерные для линии сформированной эндодермы
Плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы, с использованием любого известного специалистам способа или с использованием любого способа, предложенного в настоящем изобретении.
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы, в соответствии со способами, описанными в публикации D'Amour et al., Nature Biotechnology 23, 1534-1541 (2005).
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы, способами, описанными в публикации Shinozaki et al., Development 131, 1651-1662 (2004).
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы, в соответствии со способами, описанными в публикации McLean et al., Stem Cells 25, 29-38 (2007).
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы, в соответствии со способами, описанными в публикации D'Amour et al., Nature Biotechnology 24, 1392-1401 (2006).
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы, путем культивирования плюрипотентных стволовых клеток в среде, содержащей активин A в отсутствие сыворотки, затем культивирования клеток с активином A и сывороткой, а затем культивирования клеток с активином A и сывороткой в другой концентрации. Пример данного способа описан в публикации Nature Biotechnology 23, 1534-1541 (2005).
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы, путем культивирования плюрипотентных стволовых клеток в среде, содержащей активин А в отсутствие сыворотки, затем культивирования клеток с активином A и сывороткой в другой концентрации. Пример использования данного способа приведен в публикации D'Amour et al., Nature Biotechnology, 2005.
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы, путем культивирования плюрипотентных стволовых клеток в среде, содержащей активин А и лиганд Wnt в отсутствие сыворотки, затем удаления лиганда Wnt и культивирования клеток с активином A и сывороткой. Пример использования данного способа приведен в публикации Nature Biotechnology 24, 1392-1401 (2006).
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы, путем обработки плюрипотентных стволовых клеток в соответствии со способами, изложенными в заявке на патент США № 11/736908, принадлежащей LifeScan, Inc.
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы, путем обработки плюрипотентных стволовых клеток в соответствии со способами, изложенными в заявке на патент США № 11/779311, принадлежащей LifeScan, Inc.
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы, путем обработки плюрипотентных стволовых клеток в соответствии со способами, изложенными в заявке на патент США № 60/990529.
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы, путем обработки плюрипотентных стволовых клеток в соответствии со способами, изложенными в заявке на патент США № 61/076889.
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы, путем обработки плюрипотентных стволовых клеток в соответствии со способами, изложенными в заявке на патент США № 61/076900.
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы, путем обработки плюрипотентных стволовых клеток в соответствии со способами, изложенными в заявке на патент США № 61/076908.
Например, плюрипотентные стволовые клетки могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы, путем обработки плюрипотентных стволовых клеток в соответствии со способами, изложенными в заявке на патент США № 61/076915.
Характеристика клеток, экспрессирующих маркеры, характерные для линии сформированной эндодермы
Образование клеток, экспрессирующих маркеры, характерные для линии сформированной эндодермы, может быть выявлено путем проверки на наличие маркеров до и после выполнения конкретного протокола. Плюрипотентные стволовые клетки, как правило, не экспрессируют данных маркеров. Таким образом, дифференцировка плюрипотентных клеток обнаруживается, когда клетки начинают экспрессировать эти маркеры.
Эффективность дифференцировки может быть определена путем обработки популяции клеток агентом (например, антителом), специфически распознающим белковый маркер, экспрессированный клетками, экспрессирующими маркеры, характерные для линии сформированной эндодермы.
Способы анализа экспрессии маркерных белков и нуклеиновых кислот в культивированных или изолированных клетках являются стандартными для данной области. Сюда относятся количественная ревертазная полимеразная цепная реакция (ОТ-ПЦР), Нозерн-блоттинг, гибридизация in situ (см., например, Current Protocols in Molecular Biology (Ausubel et al., eds. 2001 supplement)), а также способы иммунологического анализа, такие как иммуногистохимический анализ среза материала, Вестерн-блоттинг, а для маркеров, доступных в интактных клетках, - метод проточной цитометрии (FACS) (см., например, Harlow and Lane, Using Antibodies: A Laboratory Manual, New York: Cold Spring Harbor Laboratory Press (1998)).
Характеристики плюрипотентных стволовых клеток хорошо известны специалистам в данной области, и продолжается выявление дополнительных характеристик плюрипотентных стволовых клеток. К маркерам плюрипотентных стволовых клеток относится, например, экспрессия одного или нескольких следующих маркеров: ABCG2, CRIPTO, FOXD3, Connexin43, Connexin45, OCT4, SOX2, Nanog, hTERT, UTF1, ZFP42, SSEA-3, SSEA-4, Tra 1-60, Tra 1-81.
После обработки плюрипотентных стволовых клеток с применением способов, составляющих предмет изобретения, дифференцированные клетки могут быть выделены путем воздействия на популяцию клеток агентом (например, антителом), специфически распознающим белковый маркер, например CXCR4, экспрессируемый клетками, экспрессирующими маркеры, характерные для линии сформированной эндодермы.
Формирование клеток, экспрессирующих маркеры, характерные для линии панкреатической эндодермы, из клеток, экспрессирующих маркеры, характерные для линии сформированной эндодермы
Клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы, могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии панкреатической эндодермы, с использованием любого известного специалистам способа или с использованием любого способа, предложенного в настоящем изобретении.
Например, клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы, могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии панкреатической эндодермы, в соответствии со способами, описанными в публикации D'Amour et al., Nature Biotechnology 24, 1392-1401 (2006).
Например, клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы, дифференцируются в клетки, экспрессирующие маркеры, характерные для линии панкреатической эндодермы, путем обработки клеток, экспрессирующих маркеры, характерные для линии сформированной эндодермы, фактором роста фибробластов и ингибитором сигнального пути Hedgehog KAAD-циклопамином, затем удаления среды, содержащей фактор роста фибробластов и KAAD-циклопамин с последующим культивированием клеток в среде, содержащей ретиноевую кислоту, фактор роста фибробластов и KAAD-циклопамин. Пример использования данного способа приведен в публикации Nature Biotechnology 24, 1392-1401 (2006).
Например, клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы, дифференцируются в клетки, экспрессирующие маркеры, характерные для линии панкреатической эндодермы, путем обработки клеток, экспрессирующих маркеры, характерные для линии сформированной эндодермы, ретиноевой кислотой и по меньшей мере одним фактором роста фибробластов в течение периода времени, соответствующего способам, описанным в заявке на патент США № 11/736908, принадлежащей LifeScan, Inc.
Например, клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы, дифференцируются в клетки, экспрессирующие маркеры, характерные для линии панкреатической эндодермы, путем обработки клеток, экспрессирующих маркеры, характерные для линии сформированной эндодермы, ретиноевой кислотой и по меньшей одним фактором роста фибробластов в течение периода времени, соответствующего способам, описанным в заявке на патент США № 11/779311, принадлежащей LifeScan, Inc.
В одном из аспектов настоящего изобретения клетки, экспрессирующие маркеры, характерные для линии сформированной эндодермы, далее дифференцируются в клетки, экспрессирующие маркеры, характерные для линии панкреатической эндодермы, путем обработки клеток, экспрессирующих маркеры, характерные для линии сформированной эндодермы, в соответствии со способами, описанными в заявке на патент США № 60/990529.
Характеристика клеток, экспрессирующих маркеры, характерные для линии панкреатической эндодермы
Маркеры, характерные для линии панкреатической эндодермы, хорошо известны специалистам в данной сфере, и дополнительные маркеры, характерные для линии панкреатической эндодермы, продолжают выявляться. Данные маркеры могут использоваться для подтверждения того, что клетки, прошедшие обработку в соответствии с настоящим изобретением, дифференцировались и приобрели характерные особенности линии панкреатической эндодермы. К маркерам, характерным для линии панкреатической эндодермы, относится экспрессия одного или нескольких факторов транскрипции, таких как, например, HLXB9, PTF1 альфа, PDX1, HNF6, HNF-1 бета.
Эффективность дифференцировки может быть определена путем обработки популяции клеток агентом (например, антителом), специфически распознающим белковый маркер, экспрессированный клетками, экспрессирующими маркеры, характерные для линии панкреатической эндодермы.
Способы анализа экспрессии маркерных белков и нуклеиновых кислот в культивированных или изолированных клетках являются стандартными для данной области. Сюда относятся количественная ревертазная полимеразная цепная реакция (ОТ-ПЦР), Нозерн-блоттинг, гибридизация in situ (см., например, Current Protocols in Molecular Biology (Ausubel et al., eds. 2001 supplement)), а также способы иммунологического анализа, такие как иммуногистохимический анализ среза материала, Вестерн-блоттинг, а для маркеров, доступных в интактных клетках, - метод проточной цитометрии (FACS) (см., например, Harlow and Lane, Using Antibodies: A Laboratory Manual, New York: Cold Spring Harbor Laboratory Press (1998)).
Формирование клеток, экспрессирующих маркеры, характерные для линии клеток-предшественников панкреатических эндокринных клеток, из клеток линии панкреатической эндодермы
В одном аспекте настоящего изобретения клетки, экспрессирующие маркеры, характерные для линии панкреатической энддермы, дифференцируются в клетки-предшественники панкреатических эндокринных клеток путем культивирования клеток, экспрессирующих маркеры, характерные для линии панкреатическиой эндодермы, в среде с добавлением фактора, способного ингибировать BMP, и ингибитора киназы TGF-β рецептора I.
В одном варианте осуществления фактором, способным ингибировать BMP, является noggin. Noggin может использоваться в концентрациях от приблизительно 100 пг/мл до приблизительно 500 мкг/мл. В одном из вариантов осуществления, Noggin используется в концентрации 100 нг/мл.
В одном варианте осуществления ингибитор киназы TGF-β рецептора I представляет собой ALK5 ингибитор II (Calbiochem, Калифорния, США). ALK5 ингибитор II может использоваться в концентрациях от приблизительно 0,1 мкМ до приблизительно 10 мкМ. В одном варианте осуществления ALK5 ингибитор II используется в концентрации 1 мкМ.
В одном варианте осуществления среда представляет собой DMEM с содержанием глюкозы 4500 мг/л и 1% B27.
В одном варианте осуществления клетки культивируются в культуральной среде в течение приблизительно четырех суток.
Эффективность дифференцировки может быть определена путем обработки популяции клеток агентом (например, антителом), специфически распознающим белковый маркер, экспрессированный клетками-предшественниками панкреатических эндокринных клеток.
Способы анализа экспрессии маркерных белков и нуклеиновых кислот в культивированных или изолированных клетках являются стандартными для данной области. Сюда относятся количественная ревертазная полимеразная цепная реакция (ОТ-ПЦР), Нозерн-блоттинг, гибридизация in situ (см., например, Current Protocols in Molecular Biology (Ausubel et al., eds. 2001 supplement)), а также способы иммунологического анализа, такие как иммуногистохимический анализ среза материала, Вестерн-блоттинг, а для маркеров, доступных в интактных клетках, - метод проточной цитометрии (FACS) (см., например, Harlow and Lane, Using Antibodies: A Laboratory Manual, New York: Cold Spring Harbor Laboratory Press (1998)).
Характеристики плюрипотентных стволовых клеток хорошо известны специалистам в данной области, и продолжается выявление дополнительных характеристик плюрипотентных стволовых клеток. К маркерам плюрипотентных стволовых клеток относится, например, экспрессия одного или нескольких следующих маркеров: ABCG2, CRIPTO, FOXD3, Connexin43, Connexin45, OCT4, SOX2, Nanog, hTERT, UTF1, ZFP42, SSEA-3, SSEA-4, Tra 1-60, Tra 1-81.
После обработки плюрипотентных стволовых клеток с применением способов, составляющих предмет изобретения, дифференцированные клетки могут быть выделены путем воздействия на популяцию клеток агентом (например, антителом), специфически распознающим белковый маркер, например CXCR4, экспрессируемый клетками, экспрессирующими маркеры, характерные для линии панкреатической эндодермы.
Маркеры, характерные для линии дифференцирования панкреатической эндодермы, выбирают из группы, состоящей из следующих маркеров: PDX1, HNF-1 бета, PTF1 альфа, HNF6, HB9 и PROX1. Подходит для использования в настоящем изобретении клетка, экспрессирующая по меньшей мере один из маркеров, характерных для линии панкреатической эндодермы. В одном из аспектов настоящего изобретения клетка, экспрессирующая маркеры, характерные для линии панкреатической эндодермы, представляет собой клетку панкреатической эндодермы.
Маркеры, характерные для клеток-предшественников панкреатических эндокринных клеток, выбирают из группы, состоящей из следующих маркеров: NGN3, NKX6.1, NEUROD, ISL1, PDX1, PAX4, NKX2.2, PAX6 или ARX.
Формирование клеток, экспрессирующих маркеры, характерные для линии панкреатических эндокринных клеток, из клеток-предшественников панкреатических эндокринных клеток
В одном варианте осуществления клетки-предшественники панкреатических эндокринных клеток, получаемые с использованием способов настоящего изобретения, могут далее быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии панкреатических эндокринных клеток.
Клетки, экспрессирующие маркеры, характерные для клеток-предшественников панкреатических эндокринных клеток, могут быть дифференцированы в клетки, экспрессирующие маркеры, характерные для линии панкреатических эндокринных клеток, с использованием любого способа, известного специалистам в данной области, или с использованием любого способа, предлагаемого в настоящем изобретении.
Например, клетки-предшественники панкреатических эндокринных клеток, полученные в соответствии со способами настоящего изобретения, затем подвергаются дифференцировке в клетки, экспрессирующие маркеры, характерные для линии панкреатических эндокринных клеток, путем культивирования клеток-предшественников панкреатических эндокринных клеток в среде, содержащей экзендин 4, последующего удаления среды, содержащей экзендин 4, и дальнейшего культивирования клеток в среде, содержащей экзендин 1, IGF1 и HGF. Пример использования данного способа приведен в публикации D'Amour et al., Nature Biotechnology, 2006.
Например, клетки-предшественники панкреатических эндокринных клеток, полученные в соответствии со способами настоящего изобретения, затем подвергаются дифференцировке в клетки, экспрессирующие маркеры, характерные для линии панкреатических эндокринных клеток, путем культивирования клеток-предшественников панкреатических эндокринных клеток в среде, содержащей DAPT (Sigma-Aldrich, Миссури, США) и экзендин 4. Пример использования данного способа приведен в публикации D'Amour et al., Nature Biotechnology, 2006.
Например, клетки-предшественники панкреатических эндокринных клеток, полученные в соответствии со способами настоящего изобретения, затем подвергаются дифференцировке в клетки, экспрессирующие маркеры, характерные для линии панкреатических эндокринных клеток, путем культивирования клеток-предшественников панкреатических эндокринных клеток в среде, содержащей экзендин 4. Пример использования данного способа приведен в публикации D'Amour et al., Nature Biotechnology, 2006.
Например, клетки-предшественники панкреатических эндокринных клеток, полученные в соответствии со способами настоящего изобретения, затем подвергаются дифференцировке в клетки, экспрессирующие маркеры, характерные для линии панкреатических эндокринных клеток, путем обработки клеток-предшественников панкреатических эндокринных клеток фактором, ингибирующим сигнальный путь Notch, способами, описанными в заявке на патент США № 11/736908, принадлежащей LifeScan, Inc.
Например, клетки-предшественники панкреатических эндокринных клеток, полученные в соответствии со способами настоящего изобретения, затем подвергаются дифференцировке в клетки, экспрессирующие маркеры, характерные для линии панкреатических эндокринных клеток, путем обработки клеток-предшественников панкреатических эндокринных клеток фактором, ингибирующим сигнальный путь Notch, способами, описанными в заявке на патент США № 11/779311, принадлежащей LifeScan, Inc.
Например, клетки-предшественники панкреатических эндокринных клеток, полученные в соответствии со способами настоящего изобретения, затем подвергаются дифференцировке в клетки, экспрессирующие маркеры, характерные для линии панкреатических эндокринных клеток, путем обработки клеток-предшественников панкреатических эндокринных клеток фактором, ингибирующим сигнальный путь Notch, способами, описанными в заявке на патент США № 60/953178, принадлежащей LifeScan, Inc.
Например, клетки-предшественники панкреатических эндокринных клеток, полученные в соответствии со способами настоящего изобретения, затем подвергаются дифференцировке в клетки, экспрессирующие маркеры, характерные для линии панкреатических эндокринных клеток, путем обработки клеток-предшественников панкреатических эндокринных клеток фактором, ингибирующим сигнальный путь Notch, способами, описанными в заявке на патент США № 60/990529, принадлежащей LifeScan, Inc.
Маркеры, характерные для линии панкреатических эндокринных клеток, выбирают из группы, состоящей из NEUROD, ISL1, PDX1, NKX6.1, PAX4, PAX6, NGN3 и NKX2.2. В одном из вариантов осуществления, панкреатической эндокринной клеткой является клетка, способная экспрессировать по меньшей мере один из следующих гормонов: инсулин, глюкагон, соматостатин и панкреатический полипептид. Подходит для использования в настоящем изобретении клетка, экспрессирующая по меньшей мере один из маркеров, характерных для линии панкреатических эндокринных клеток. В одном аспекте настоящего изобретения клетка с экспрессией маркеров, характерных для линии дифференцировки панкреатических эндокринных клеток, представляет собой панкреатическую эндокринную клетку. Указанная панкреатическая эндокринная клетка может представлять собой панкреатическую клетку, экспрессирующую гормоны. В альтернативном варианте указанная панкреатическая эндокринная клетка может представлять собой панкреатическую клетку, секретирующую гормоны.
В одном аспекте настоящего изобретения панкреатическая эндокринная клетка представляет собой клетку с экспрессией маркеров, характерных для линии дифференцирования β-клеток. Клетка с экспрессией маркеров, характерных для линии β-клеток, экспрессирует PDX1 и по меньшей мере один из следующих транскрипционных факторов: NGN-3, NKX2.2, NKX6.1, NEUROD, ISL1, HNF3 бета, MAFA, PAX4 и PAX6. В одном аспекте настоящего изобретения клетка с экспрессией маркеров, характерных для линии дифференцирования β-клеток, представляет собой β-клетку.
Способы лечения
В одном аспекте настоящее изобретение предлагает способ лечения пациентов, страдающих от диабета 1 типа или подверженных риску развития этого заболевания. В одном варианте осуществления данный способ включает культивирование плюрипотентных стволовых клеток, дифференцирование плюрипотентных стволовых клеток in vitro в линию β-клеток и имплантирование клеток β-линии пациенту. В альтернативном варианте осуществления способ включает культивирование плюрипотентных стволовых клеток, дифференцирование плюрипотентных стволовых клеток in vitro в клетки-предшественники панкреатических эндокринных клеток и имплантирование клеток-предшественников панкреатических эндокринных клеток пациенту.
В еще одном аспекте настоящее изобретение предлагает способ лечения пациентов, страдающих от диабета 2 типа или подверженных риску развития этого заболевания. В одном варианте осуществления данный способ включает культивирование плюрипотентных стволовых клеток, дифференцирование плюрипотентных стволовых клеток in vitro в линию β-клеток и имплантирование клеток β-линии пациенту. В альтернативном варианте осуществления способ включает культивирование плюрипотентных стволовых клеток, дифференцирование плюрипотентных стволовых клеток in vitro в клетки-предшественники панкреатических эндокринных клеток и имплантирование клеток-предшественников панкреатических эндокринных клеток пациенту.
При необходимости пациент дополнительно может получать лечение фармакологическими агентами или биологически активными веществами, повышающими выживаемость и функционирование трансплантированных клеток. К этим агентам могут относиться, например, помимо прочего, инсулин, члены семейства TGF-β, включая TGF-β1, 2 и 3, костные морфогенетические белки (BMP-2, -3, -4, -5, -6, -7, -11, -12 и -13), факторы роста фибробластов-1 и -2, тромбоцитарный фактор роста -AA и -BB, плазма, богатая тромбоцитами, инсулин-подобный фактор роста (IGF-I, II), фактор роста и дифференцировки (GDF-5, -6, -7, -8, -10, -15), фактор роста из клеток эндотелия сосудов (VEGF), плейотропин, эндотелин. К другим фармакологическим веществам могут относиться, например, никотинамид, глюкагон-подобный пептид-I (GLP-1) и II, миметические антитела GLP-1 и 2, экзендин-4, ретиноевая кислота, паратиреоидный гормон, ингибиторы MAPK, такие, например, как описаны в опубликованной патентной заявке США № 2004/0209901 и опубликованной патентной заявке США № 2004/0132729.
Плюрипотентные стволовые клетки могут быть дифференцированы в инсулин-продуцирующие клетки до трансплантации реципиенту. В конкретном варианте осуществления плюрипотентные стволовые клетки являются полностью дифференцированными в β-клетки до трансплантации реципиенту. В альтернативном варианте плюрипотентные стволовые клетки могут быть трансплантированы реципиенту в недифференцированном или частично дифференцированном состоянии. Дальнейшая дифференцировка может происходить в организме реципиента.
Клетки сформированной эндодермы или, в альтернативном варианте, клетки панкреатической эндодермы или, в альтернативном варианте, β-клетки, могут имплантироваться в форме дисперсных клеток или клеток, образовавших кластеры, которые путем инфузии могут вводиться в воротную вену печени. В альтернативном варианте клетки могут вводиться в биологически-совместимых разрушающихся полимерных вспомогательных материалах, в пористых неразрушающихся приспособлениях или в инкапсулированном виде для защиты от иммунного ответа организма-хозяина. Клетки могут имплантироваться в подходящее место организма реципиента. К местам для имплантации относятся, например, печень, естественная поджелудочная железа, пространство под почечной капсулой, сальник, брюшная полость, субсерозное пространство, кишечник, желудок или подкожный карман.
Для облегчения дальнейшей дифференцировки, выживания и активности имплантированных клеток, предварительно, одновременно или после имплантации клеток могут вводиться дополнительные факторы, такие как факторы роста, антиоксиданты или противовоспалительные агенты. В некоторых вариантах осуществления факторы роста применяются для дифференцировки введенных клеток in vivo. Такие факторы могут секретироваться эндогенными клетками и воздействовать на введенные клетки in situ. Дифференцировку имплантированных клеток можно индуцировать любым сочетанием эндогенных или введенных экзогенно факторов роста, известных специалистам.
Количество клеток, используемое при имплантации, зависит от ряда факторов, в том числе от состояния пациента и его реакции на лечение, и оно может быть определено специалистом в данной сфере.
В одном аспекте настоящее изобретение предлагает способ лечения пациентов, страдающих от диабета или подверженных риску развития этого заболевания. Данный способ включает культивирование плюрипотентных стволовых клеток, дифференцирование культивированных стволовых клеток in vitro в линию β-клеток и заключение клеток в опорный материал с трехмерной структурой. Клетки могут поддерживаться in vitro на этом опорном материале до имплантации пациенту. В альтернативном варианте опорный материал, содержащий клетки, может напрямую имплантироваться в организм пациента без дополнительного культивирования in vitro. В опорный материал может быть заключен по меньшей мере один фармакологический агент, повышающий выживание и функционирование трансплантированных клеток.
К опорным материалам, подходящим для применения для целей настоящего изобретения, относятся тканевые шаблоны, каналы, перегородки и резервуары, применяемые для лечения тканей. В частности, для практического применения способов настоящего изобретения подходят синтетические и природные материалы в форме пеноматериалов, губок, гелей, гидрогелей, тканых и нетканных структур, применяемых in vitro и in vivo для реконструкции и регенерации биологической ткани, а также для доставки хемотаксических агентов, индуцирующих рост ткани. См., например, материалы, описанные в патенте США № 5770417, патенте США № 6022743, патенте США № 5567612, патенте США № 5759830, патенте США № 6626950, патенте США № 6534084, патенте США № 6306424, патенте США № 6365149, патенте США № 6599323, патенте США № 6656488, патентной заявке США № 2004/0062753 A1, патенте США № 4557264 и патенте США № 6333029.
Для того чтобы создать опорный материал с включенным фармакологическим агентом, фармакологический агент можно смешать с раствором полимера до изготовления опорной структуры. В альтернативном варианте фармакологический агент можно нанести в виде покрытия на изготовленную опорную структуру, предпочтительно в присутствии фармакологического носителя. Фармакологический агент может иметь форму жидкости, мелкодисперсного твердого вещества или любую другую подходящую физическую форму. В альтернативном варианте в опорный материал могут быть добавлены инертные наполнители для изменения скорости высвобождения фармакологического агента. В альтернативном варианте в опорный материал включается по меньшей мере одно фармакологическое соединение, являющееся противовоспалительным средством, как, например, описанные в патенте США № 6509369.
В опорный материал может включаться по меньшей мере одно фармакологическое соединение, являющееся антиапоптозным средством, как, например соединения, описанные в патенте США № 6793945.
В опорный материал также может включаться по меньшей мере одно фармакологическое соединение, являющееся ингибитором фиброза, как, например, соединения, описанные в патенте США № 6331298.
В опорный материал также может включаться по меньшей мере одно фармакологическое соединение, являющееся стимулятором ангиогенеза, как, например, соединения, описанные в опубликованной патентной заявке США № 2004/0220393 и в опубликованной патентной заявке США № 2004/0209901.
В опорный материал также может включаться по меньшей мере одно фармакологическое соединение, являющееся иммуносупрессором, как, например, соединения, описанные в опубликованной патентной заявке США № 2004/0171623.
В опорный материал также может включаться по меньшей мере одно фармакологическое вещество, представляющее собой фактор роста, например, члены семейства TGF-β, включая TGF-β1, 2 и 3, костные морфогенетические белки (BMP-2, -3, -4, -5, -6, -7, -11, -12 и -13), факторы роста фибробластов-1 и -2, тромбоцитарный фактор роста -AA и -BB, плазма, богатая тромбоцитами, инсулин-подобный фактор роста (IGF-I, II), фактор роста и дифференцировки (GDF-5, -6, -8, -10, -15), фактор роста из клеток эндотелия сосудов (VEGF), плейотропин, эндотелин. К другим фармакологическим соединениям могут относиться, например, никотинамид, индуцированный гипоксией фактор 1-альфа, глюкагон-подобный пептид-I (GLP-1), миметические антитела GLP-1 и GLP-2, и II, экзендин-4, Nodal, Noggin, NGF, ретиноевая кислота, паратиреоидный гормон, тенасцин-C, тропоэластин, пептиды тромбинового происхождения, кателицидины, дефензины, ламинин, биологические пептиды, содержащие связывающие клетки и гепарин домены протеинов адгезивного экстраклеточного матрикса, таких как фибронектин и витронектин, ингибиторы MAPK, такие как соединения, описанные в опубликованной патентной заявке США № 2004/0209901 и в опубликованной патентной заявке США № 2004/0132729.
Включение клеток, составляющих предмет настоящего изобретения, в опорный каркас может осуществляться путем простого нанесения клеток на опорный каркас. Клетки могут вводиться внутрь каркаса путем простой диффузии (J. Pediatr. Surg. 23 (1 Pt 2): 3-9 (1988)). Было разработано несколько иных подходов для повышения эффективности высевания клеток. Например, для нанесения хондроцитов на каркас из полигликолевой кислоты используются центрифужные пробирки. (Biotechnol. Prog. 14(2): 193-202 (1998)). Другой подход к нанесению клеток представляет собой использование центрифугирования, создающего минимальный стресс для высеваемых клеток и повышающего эффективность нанесения. Например, в публикации Yang et al. разработан способ нанесения клеток (J.Biomed. Mater. Res. 55(3): 379-86 (2001)), названный центрифужной иммобилизацией клеток (CCI).
Настоящее изобретение иллюстрируют, но не ограничивают следующие примеры.
ПРИМЕРЫ
Пример 1
Формирование популяции клеток-предшественников панкреатических эндокринных клеток
Клетки линии эмбриональных стволовых клеток H1 культивировались на покрытых материалом MATRIGEL планшетах (разведение 1:30) и дифференцировались в клетки-предшественники панкреатических эндокринных клеток с использованием следующего протокола:
a. среда RPMI (№ по каталогу 22400, Invitrogen, Калифорния, США) с добавлением 2% BSA (№ по каталогу 152401, MP Biomedical, Огайо, США) и 100 нг/мл активина A (R&D Systems, Миннесота, США), с добавлением 20 нг/мл WNT-3a (№ по каталогу 1324-WN-002, R&D Systems, Миннесота, США), с добавлением 8 нг/мл bFGF (№ по каталогу 100-18B, PeproTech, Нью-Джерси, США), в течение одного дня с последующей обработкой средой RPMI с добавлением 2% BSA и 100 нг/мл активина A, с добавлением 8 нг/мл bFGF в течение еще двух дней; затем
b. DMEM/F12 (№ по каталогу 11330, Invitrogen, Калифорния, США) + 2% BSA + 50 нг/мл FGF7 в течение трех дней (стадия 2); затем
c. использовали другую базальную среду, указанную в таблице 1, с добавлением 1% B27 (№ 17504-044, Invitrogen, Калифорния, США) + 50 нг/мл FGF7 + 0,25 мкМ Cyclopamine- KAAD (№239804, Calbiochem, Калифорния, США) + 2 мкМ ретиноевой кислоты (RA) (Sigma, Миссури, США) + 100 нг/мл Noggin (R&D Systems, Миннесота, США) в течение четырех дней (стадия 3); затем
d. использовали другую базальную среду, указанную в таблице 1, с добавлением 1% B27 (Invitrogen, Калифорния, США) + 100 нг/мл Noggin + 1 мкМ ALK5 ингибитора II (№ по каталогу 616452, Calbiochem, Калифорния, США) в течение трех дней (стадия 4).
На стадии 4 на третий день дифференцировки из культур отбирались образцы и исследовались на экспрессию панкреатических маркеров с помощью метода ПЦР реального времени. Параллельно культуры стадии 4, день 3, фиксировались и окрашивались на следующие белки: NKX6.1 (№ по каталогу F64A6B4, Developmental Studies Hybridoma Bank, Университет Айовы, США), PDX1, NGN3 и CDX2.
В образцах стадии 4, день 3, культивированных в среде DMEM (обработка 1 и обработка 2, таблица 1), наблюдалось существенное повышение уровня экспрессии NKX6.1, NGN3 и PTF1 альфа по данным ПЦР (фиг. 1) в сравнении с клетками, культивированными в DMEM/F12 (обработка 4, таблица 1) или CMRL (обработка 3, таблица 1). В исследованных культурах не наблюдалось отличий в уровне экспрессии PDX1. Однако иммуноцитохимический анализ показал, что среди клеток, культивированных в среде DMEM/F12, значительная доля клеток, экспрессировавших PDX1, также экспрессировала CDX2, маркер эндодермы кишечной трубки (фиг. 2, панели a и e). И наоборот, среди клеток, обработанных средой DMEM, наблюдалось разделение PDX1-положительных и CDX2-положительных клеток (фиг. 2, панели b и f), т.е. значительная доля клеток, экспрессирующих PDX1, не экспрессировала CDX2.
Кроме того, клетки, экспрессирующие PDX1, полученные из клеток, обработанных средой DMEM, также экспрессировали NKX6.1. Как видно на фиг. 2, от 50 до 60% PDX1-положительных клеток также экспрессировали NKX6.1 к концу стадии 4 (фиг. 2, панель d), а от 20 до 30% PDX1-положительных клеток экспрессировали NGN3 (фиг. 2, панель h). Тем не менее в клетках, культивированных в среде DMEM, не наблюдалась коэкспрессия NKX6.1 и NGN3. Коэкспрессию PDX1 и NGN3 также наблюдали в клетках, культивировавшихся в среде DMEM/F12 или CMRL (фиг. 2, панель g), однако экспрессия NKX6.1 не наблюдалась в клетках, обработанных ни средой DMEM/F12, ни средой CMRL (фиг. 2, панель c).
Эти данные указывают на то, что разные базальные среды усиливают образование разных популяций клеток панкреатической эндодермы: при использовании среды DMEM/F12 образовывалась популяция, коэкспрессирующая PDX1 и CDX2, а при использовании DMEM образовывалась популяция, экспрессирующая PDX1 и NKX6.1, но не экспрессирующая CDX2. Кроме того, данные позволяют предположить, что экспрессия панкреатических генов увеличивается при увеличении концентрации глюкозы в культуральной среде. См. фиг. 1 и фиг. 2.
Пример 2
Прямая дифференцировка человеческих эмбриональных стволовых клеток в клетки-предшественники панекреатических эндокринных клеток
Клетки линии эмбриональных стволовых клеток H1 культивировались на покрытых материалом MATRIGEL планшетах (разведение 1:30) и дифференцировались в клетки-предшественники панкреатических эндокринных клеток с использованием следующего протокола:
a. среда RPMI (№ по каталогу 22400, Invitrogen, Калифорния, США) с добавлением 2% BSA (№ по каталогу 152401, MP Biomedical, Огайо, США) и 100 нг/мл активина A (R&D Systems, Миннесота, США), с добавлением 20 нг/мл WNT-3a (№ по каталогу 1324-WN-002, R&D Systems, Миннесота, США), с добавлением 8 нг/мл bFGF (№ по каталогу 100-18B, PeproTech, Нью-Джерси, США), в течение одного дня с последующей обработкой средой RPMI с добавлением 2% BSA и 100 нг/мл активина A, с добавлением 8 нг/мл bFGF в течение еще двух дней; затем
b. DMEM/F12 (№ по каталогу 11330, Invitrogen, Калифорния, США) + 2% BSA + 50 нг/мл FGF7 в течение трех дней (стадия 2); затем
c. DMEM (с высоким содержанием глюкозы) + 1% B27 (Invitrogen, Калифорния, США) + 50 нг/мл FGF7 + 0,25 мкМ Cyclopamine- KAAD + 2 мкМ ретиноевой кислоты (RA) (Sigma, Миссури, США) + 100 нг/мл Noggin (R&D Systems, Миннесота, США) в течение четырех дней (стадия 3); затем
d. DMEM (с высоким содержанием глюкозы) + 1% B27 (Invitrogen, Калифорния, США) + 100 нг/мл Noggin + 1 мкМ ALK5 ингибитора II (№ по каталогу 616452, Calbiochem, Калифорния, США) в течение трех дней (стадия 4); затем
e. DMEM (с высоким содержанием глюкозы) + 0,5% ITS (Invitrogen, Калифорния, США) + 0,1% BSA + 1 мкМ Alk5 ингибитора II + 100 нг/мл Noggin + 20 нг/мл Betacellulin (R&D Systems, Миннесота, США) в течение пяти дней (стадия 5).
Образцы из культур отбирались в двух повторностях ежедневно от стадии 2, день 3, до стадии 4, день 3, и анализировались на экспрессию панкреатических маркеров методом ПЦР реального времени. После вступления клеток в стадию 4 наблюдалось существенное увеличение экспрессии PDX1, NKX6.1 и PTF1 альфа (фиг. 3, панели a, b и c). Кроме того, также наблюдалось существенное увеличение экспрессии NGN3, PAX4, NKX2.2 и NEUROD (фиг. 3, панели d-f). PAX4, NKX2.2 и NEUROD напрямую регулируются NGN3, а это предполагает, что панкреатическая эндодерма начала коммитироваться в панкреатическую эндокринную линию.
Дальнейшая дифференцировка клеток-предшественников панкреатических эндокринных клеток in vitro инсулин-экспрессирующие клетки проводится путем добавления ингибитора рецептора TGF-β, Noggin и Betacellulin. Как показано на фиг. 4, существенное повышение экспрессии инсулина наблюдается после добавления Alk5 ингибитора II (ингибитора рецептора TGF-β), Noggin и Betacellulin в течение 5 дней. Уровни экспрессии NGN3 и PAX4 снижаются, а уровни экспрессии PDX1, NKX6.1 MAFB и NEUROD остаются постоянными.
Пример 3
Альтернативный способ прямой дифференцировки человеческих эмбриональных стволовых клеток в клетки-предшественники панкреатических эндокринных клеток
В данном примере демонстрируется альтернативный способ дифференцировки человеческих эмбриональных стволовых клеток в клетки-предшественники панкреатических эндокринных клеток с использованием Alk5 ингибитора II (ингибитора семейства рецепторов TGF-бета) в сочетании с низкой дозой экзогенного ретиноидного соединения, например ретинола (витамина A), который может присутствовать в качестве добавки к среде, например, B27.
Клетки линии эмбриональных стволовых клеток H1, пассаж 45, культивировались на покрытых материалом MATRIGEL планшетах (разведение 1:30) и дифференцировались в клетки-предшественники панкреатических эндокринных клеток с использованием следующего протокола:
a. среда RPMI с добавлением 2% BSA и 100 нг/мл активина A, с добавлением 20 нг/мл WNT-3a, с добавлением 8 нг/мл bFGF, в течение одного дня с последующей обработкой средой RPMI с добавлением 2% BSA и 100 нг/мл активина A, с добавлением 8 нг/мл bFGF в течение еще двух дней (стадия 1); затем
b. DMEM/F12 + 2% BSA + 50 нг/мл FGF7 в течение трех дней (стадия 2); затем
c. DMEM (с высоким содержанием глюкозы) + 1% B27 (Invitrogen, Калифорния, США) + 50 нг/мл FGF7 + 0,25 мкМ Cyclopamine-KAAD + 0,1 мкМ ретиноевой кислоты (RA)+100 нг/мл Noggin в течение четырех дней (обработка 1, стадия 3); или
d. DMEM (с высоким содержанием глюкозы) + 1% B27 (Invitrogen, Калифорния, США) + 50 нг/мл FGF7 + 0,25 мкМ Cyclopamine-KAAD + 0,1 мкМ ретиноевой кислоты (RA) + 1 мкМ ингибитора Alk5 + Noggin 100 нг/мл в течение четырех дней (обработка 2, стадия 3); или
e. DMEM (с высоким содержанием глюкозы) + 1% B27 (Invitrogen, Калифорния, США) + 50 нг/мл FGF7 + 0,25 мкМ Cyclopamine-KAAD + 1 мкМ ингибитора Alk5 + 100 нг/мл Noggin в течение четырех дней (обработка 3, стадия 3); или
f. DMEM (с высоким содержанием глюкозы) + 1% B27 (Invitrogen, Калифорния, США) + 50 нг/мл FGF7 + 0,25 мкМ Cyclopamine-KAAD + 2 мкМ ретиноевой кислоты (RA) + 100 нг/мл Noggin в течение четырех дней (обработка 4, стадия 3); затем
g. DMEM (с высоким содержанием глюкозы) + 1% B27 (Invitrogen, Калифорния, США) + 100 нг/мл Noggin + 1 мкМ ALK5 ингибитор II в течение восьми дней (стадия 4).
Образцы из культур отбирались в двух повторностях, в день 3 и в день 8 стадии 4, и анализировались на экспрессию панкреатических маркеров методом ПЦР реального времени.
Обработка клеток, экспрессирующих маркеры, характерные для линии панкреатической эндодермы, средой с добавлением FGF7, Noggin и Cyclopamine-KAAD, ALK5 ингибитора II и низкой концентрации ретиноевой кислоты (0,1 мкМ) или без добавления экзогенной ретиноевой кислоты, запускала экспрессию NGN3 и продолжала усиливать экспрессию PDX1 и NKX6.1 (фиг. 5, панель a, обработка 3 и 4). Уровень экспрессии NGN3 был аналогичен уровню в клетках, обработанных высокой концентрацией (2 мкМ) ретиноевой кислоты (фиг. 5, панель a, обработка 4, соответственно). Эти данные показывают, что добавление Alk5 ингибитора II является достаточным для запуска образования клеток-предшественников панкреатических эндокринных клеток, если клетки, экспрессирующие маркеры, характерные для линии панкреатической эндодермы, обрабатываются FGF7, Noggin и Cyclopamine-KAAD. См. фиг. 5, панель a, где экспрессия NGN3 не наблюдается в клетках, обработанных низкой концентрацией ретиноевой кислоты (0,1 мкМ) в отсутствие Alk5 ингибитора II (фиг. 5, панель a, обработка 1). Панкреатические эндокринные клетки, полученные в результате описанной выше обработки, были достаточно компетентными, чтобы образовывать инсулин-экспрессирующие клетки in vitro. См. фиг. 5, панель b, где полученные клетки, экспрессирующие NGN3, экспрессировали инсулин после обработки средой DMEM (с высоким содержанием глюкозы) + 1% B27 (Invitrogen, Калифорния, США) + 100 нг/мл Noggin + 1 мкМ ALK5 ингибитора II в течение восьми дней.
Пример 4
Созревание клеток-предшественников панкреатических эндокринных клеток in vivo
Клетки линии эмбриональных стволовых клеток H1, пассаж 45, культивировались на покрытых материалом MATRIGEL планшетах (разведение 1:30) и дифференцировались в клетки-предшественники панкреатических эндокринных клеток с использованием следующего протокола:
a. среда RPMI + 2% BSA + 100 нг/мл активина A + 20 нг/мл WNT-3a + 8 нг/мл bFGF в течение одного дня с последующей обработкой средой RPMI + 2% BSA + 100 нг/мл активина A + 8 нг/мл bFGF в течение еще двух дней (стадия 1); затем
b. DMEM/F12 + 2% BSA + 50 нг/мл FGF7 в течение трех дней (стадия 2); затем
c. DMEM с высоким содержанием глюкозы + 1% B27 + 50 нг/мл FGF7 + 0,25 мкМ Cyclopamine-KAAD + 2 мкМ ретиноевой кислоты (RA) + 100 нг/мл Noggin в течение четырех дней (стадия 3); затем
d. DMEM с высоким содержанием глюкозы + 1% B27 + 100 нг/мл Noggin + 1 мкМ ALK5 ингибитора II в течение трех дней (стадия 4).
Описанный выше способ (способ 1) культивирования клеток in vitro использовался для трансплантации клеток животным с №№ 8, 11, 14, 17, 20 и 23. См. фиг. 6.
Был также протестирован альтернативный протокол дифференцировки, при котором человеческие эмбриональные стволовые клетки линии H1, пассаж 45, культивировались на покрытых материалом MATRIGEL планшетах (разведение 1:30) и дифференцировались в клетки-предшественники панкреатических эндокринных клеток с использованием следующего протокола:
a. среда RPMI + 2% BSA + 100 нг/мл активина A + 20 нг/мл WNT-3a + 8 нг/мл bFGF в течение одного дня с последующей обработкой средой RPMI + 2% BSA + 100 нг/мл активина A + 8 нг/мл bFGF в течение еще двух дней (стадия 1); затем
b. DMEM/F12 + 2% BSA + 50 нг/мл FGF7 в течение трех дней (стадия 2); затем
c. DMEM (с высоким содержанием глюкозы) + 1% B27 + 50 нг/мл FGF7 + 0,25 мкМ Cyclopamine-KAAD + 2 мкМ ретиноевой кислоты (RA) + 100 нг/мл Noggin + Alk5 ингибитора II 1 мкМ в течение четырех дней (стадия 3); затем
d. DMEM (с высоким содержанием глюкозы) + 1% B27 + 100 нг/мл Noggin + Alk5 ингибитор II 1 мкМ в течение трех дней (стадия 4).
В конце четвертой стадии клетки механически собирались стеклянной пипеткой на 1 мл и далее переносились на не допускающие прикрепления планшеты и культивировались в течение ночи. Получившиеся агрегаты собирались. Агрегаты с количеством клеток от 5 до 8 миллионов трансплантировались в почечную капсулу мышей с иммунодефицитом (SCID/Bg). Данный способ (способ 2) культивирования клеток in vitro использовался для трансплантации клеток животным с №№ 324, 326, 329, 331 и 333. См. фиг. 7, панели a и b.
Также был протестирован альтернативный протокол дифференцировки, при котором человеческие эмбриональные стволовые клетки линии H1, пассаж 45, культивировались на покрытых материалом MATRIGEL (разведение 1:30) планшетах и дифференцировались в клетки-предшественники панкреатических эндокринных клеток с использованием следующего протокола:
a. среда RPMI + 2% BSA + 100 нг/мл активина A + 20 нг/мл WNT-3a + 8 нг/мл bFGF в течение одного дня с последующей обработкой средой RPMI + 2% BSA + 100 нг/мл активина A + 8 нг/мл bFGF в течение еще двух дней (стадия 1); затем
b. DMEM/F12 + 2% BSA + 50 нг/мл FGF7 в течение трех дней (стадия 2); затем
c. культивирование клеток в течение четырех дней в среде DMEM (с высоким содержанием глюкозы) + 1% B27 + 50 нг/мл FGF7 + 0,25 мкМ Cyclopamine-KAAD + 0,1 мкМ ретиноевой кислоты (RA) + 100 нг/мл Noggin + Alk5 ингибитор II 1 мкМ (стадия 3); затем
d. DMEM (с высоким содержанием глюкозы) + 1% B27 в течение трех дней (стадия 4).
В конце четвертой стадии клетки механически собирались стеклянной пипеткой на 1 мл и затем переносились на не допускающие прикрепления планшеты и инкубировались в течение ночи. Получившиеся агрегаты собирались. Агрегаты с количеством клеток от 5 до 8 миллионов трансплантировались в почечную капсулу мышей с иммунодефицитом (SCID/Bg). Данный способ (способ 3) культивирования клеток in vitro использовался для трансплантации животным с №№ 294, 295, 296 и 297. См. фиг. 8.
Также был протестирован альтернативный протокол дифференцировки, при котором человеческие эмбриональные стволовые клетки линии H1, пассаж 45, культивировались на покрытых материалом MATRIGEL (разведение 1:30) планшетах и дифференцировались в клетки-предшественники панкреатических эндокринных клеток с использованием следующего протокола:
a. среда RPMI + 2% BSA + 100 нг/мл активина A + 20 нг/мл WNT-3a + 8 нг/мл bFGF в течение одного дня с последующей обработкой средой RPMI + 2% BSA + 100 нг/мл активина A + 8 нг/мл bFGF в течение еще двух дней (стадия 1); затем
b. DMEM/F12 + 2% BSA + 50 нг/мл FGF7 в течение трех дней (стадия 2); затем
c. культивирование клеток в течение четырех дней в DMEM (с высоким содержанием глюкозы) + 1% B27 + 50 нг/мл FGF7 + 0,25 мкМ Cyclopamine-KAAD + 0,1 мкМ ретиноевой кислоты (RA) + 100 нг/мл Noggin + Alk5 ингибитор II 1 мкМ (стадия 3); затем
d. DMEM (с высоким содержанием глюкозы) + 1% B27+ 100 нг/мл Noggin + Alk5 ингибитор II 1 мкМ в течение трех дней (стадия 4).
В конце четвертой стадии клетки механически собирались стеклянной пипеткой на 1 мл и затем переносились на не допускающие прикрепления планшеты и инкубировались в течение ночи. Получившиеся агрегаты собирались. Агрегаты с количеством клеток от 5 до 8 миллионов трансплантировались в почечную капсулу мышей с иммунодефицитом (SCID/Bg). Данный способ (способ 4) культивирования клеток in vitro использовался для трансплантации животным с №№ 336, 338, 340, 342 и 344. См. фиг. 9, панели a и b.
Также был протестирован альтернативный протокол дифференцировки, при котором человеческие эмбриональные стволовые клетки линии H1, пассаж 45, культивировались на покрытых материалом MATRIGEL (разведение 1:30) планшетах и дифференцировались в клетки-предшественники панкреатических эндокринных клеток с использованием следующего протокола:
a. среда RPMI + 2% BSA + 100 нг/мл активина A + 20 нг/мл WNT-3a + 8 нг/мл bFGF в течение одного дня с последующей обработкой средой RPMI + 2% BSA + 100 нг/мл активина A + 8 нг/мл bFGF в течение еще двух дней (стадия 1); затем
b. DMEM/F12 + 2% BSA + 50 нг/мл FGF7 в течение трех дней (стадия 2); затем
c. культивирование клеток в течение четырех дней в среде DMEM (с высоким содержанием глюкозы) + 1% B27 + 50 нг/мл FGF7 + 0,25 мкМ Cyclopamine-KAAD + 100 нг/мл Noggin + Alk5 ингибитор II 1 мкМ (стадия 3); затем
d. DMEM (с высоким содержанием глюкозы) + 1% B27 + 100 нг/мл Noggin + Alk5 ингибитор II (стадия 4).
В конце четвертой стадии клетки механически собирались стеклянной пипеткой на 1 мл и затем переносились на не допускающие прикрепления планшеты и инкубировались в течение ночи. Получившиеся агрегаты собирались. Агрегаты с количеством клеток от 5 до 8 миллионов трансплантировались в почечную капсулу мышей с иммунодефицитом (SCID/Bg). Данный способ (способ 5) культивирования клеток in vitro использовался для трансплантации животным с №№ 335, 337, 339, 341 и 343. См. фиг. 10, панели a и b.
Мыши с тяжелым комбинированным иммунодефицитом, вызванным врожденным отсутствием клеток-киллеров (C.B-Igh-1b/GbmsTac-Prkdcscid-Lystbg N7) возрастом от пяти до шести недель, были приобретены в Taconic Farms. Мышей содержали в клетках-микроизоляторах со свободным доступом к стерилизованной пище и воде. В ходе подготовки к хирургической операции мыши были помечены идентификационной меткой, нанесенной на ухо, была измерена масса тела, а также содержание глюкозы в крови с помощью ручного глюкометра (LifeScan, One Touch).
Для анестезии использовали смесь изофлурана и кислорода. Шерсть на месте операции выстригли малыми ножницами, предназначенными для животных. Перед операцией мышам подкожно ввели 0,1 мг/кг Buprenex. Место хирургической операции было подготовлено путем последовательного промывания 70% раствором изопропилового спирта и 10% повидон-йодидом.
В конце четвертой стадии клетки были кратковременно (в течение 5 минут) обработаны раствором диспазы 1 мг/мл и механически отобраны с помощью стеклянной пипетки на 1 мл, после чего перенесены на не допускающие прикрепления планшеты и культивировались в течение ночи. В ходе предоперационной подготовки мышей клетки отцентрифугировали в 1,5 мл микроцентрифужной пробирке, большую часть супернатанта удалили, оставив количество среды, достаточное лишь для отбора осажденных клеток. Клетки отобрали с помощью пипетки с объемным вытеснением Rainin Pos-D, после чего пипетку перевернули, чтобы клетки могли осесть под собственным весом. Излишки среды вытеснили, оставив компактный препарат клеток для трансплантации.
При трансплантации для проникновения в почечную капсулу использовался катетер для внутривенных введений 24G × 1,9 см (¾ дюйма), после чего игла извлекалась. Затем катетер продвинули под почечной капсулой к дистальному концу почки. Наконечник пипетки Pos-D плотно вставили во втулку катетера и выдавили 5 миллионов клеток через катетер под почечную капсулу, к дистальному концу почки. Почечную капсулу загерметизировали, используя низкотемпературное прижигание, после чего почку вернули в первоначальное анатомическое положение. Одновременно агрегаты по 5 миллионов клеток загрузили в приспособление для имплантации на 50 мкл при помощи наконечника пипетки Post-D. Приспособления на 50 мкл были приобретены в компании TheraCyte, Inc (Irvine, Калифорния, США). Приспособление после загрузки клеток загерметизировали медицинским клейким силиконом типа А (Dow Corning, № по каталогу 129109) и имплантировали под кожу мышам SICD/Bg (животные с №№ 3 и 4). Мышцы сшили непрерывным швом с помощью викриловой нити 5-0, а кожу стянули скобами для ран. После операции мышам подкожно ввели 1,0 мг/кг Metacam. Мышей вывели из наркоза и дали возможность полностью восстановиться.
После трансплантации мышей взвешивали раз в неделю, а дважды в неделю брали анализ крови для определения уровня глюкозы. На разных сроках после трансплантации мышам интраперитонеально ввели 3 г/кг глюкозы. Через 60 минут после введения глюкозы через ретроорбитальный синус отобрали кровь, поместив ее в микроцентрифужные пробирки, содержащие небольшое количество гепарина. Кровь центрифугировали, плазму собрали во вторую микроцентрифужную пробирку, заморозили на сухом льду и хранили при -80°C до проведения анализа на человеческий С-пептид. Уровни человеческого С-пептида измеряли с помощью комплекта Mercodia/ALPCO Diagnotics Ultrasensitive C-peptide ELISA (№ по каталогу 80-CPTHU-E01, Alpco Diagnostics, Нью-Гемпшир, США) в соответствии с инструкциями производителя.
Человеческий C-пептид определялся в крови животных уже через 4 недели после трансплантации, и его содержание со временем увеличивалось. По истечении трех месяцев животным не давали есть 15-20 часов, после чего проводили ретроорбитальный отбор образца крови (до введения глюкозы). Далее каждому животному интраперитонеально вводили глюкозу в дозе 3 г/кг в 30% растворе декстрозы и приблизительно через 60 минут после введения глюкозы отбирали образец крови. Сыворотку отделяли от клеток крови путем центрифугирования в микроконтейнерах. Твердофазный иммуноферментный анализ (ELISA) выполняли на повторных образцах сыворотки объемом 25 мкл с использованием планшет для сверхчувствительного специфического ELISA-анализа на человеческий C-пептид (№ по каталогу 80-CPTHU-E01, Alpco Diagnostics, Нью-Гемпшир, США). Определение человеческого C-пептида показывает, что трансплантированные клетки секретируют инсулин.
Через 60 дней после трансплантации низкий уровень человеческого C-пептида (менее 0,5 нг/мл) в ответ на стимуляцию глюкозой обнаруживался у всех животных, которым был введен трансплантат с клетками-предшественниками панкреатических эндокринных клеток. В срок от двух до трех месяцев после трансплантации уровень С-пептида в сыворотке после стимуляции глюкозой резко возрастал (фиг. 6-10). Как правило, животные, которым были трансплантированы кластеры клеток, также давали ответ на стимуляцию глюкозой (фиг. 7, панель b, фиг. 9, панель b, и фиг. 10, панель b).
Гистологическое исследование трансплантатов, отобранных в разные сроки, показало наличие человеческих клеток под почечной капсулой мыши (по данным окрашивания на человеческий ядерный антиген). См. фиг. 11, панели a и b. Наблюдалось, что клетки, трансплантированные под почечную капсулу, через три недели после трансплантации формировали структуры, напоминающие протоки. См. фиг. 11, панель a. Со временем количество таких структур увеличивалось. В большинстве протокообразных структур наблюдались высокие уровни PDX1 и CK19 (фиг. 11, панель b). Это указывает на то, что клетки-предшественники панкреатических эндокринных клеток были способны к дальнейшей дифференцировке in vivo.
Поскольку экспрессия PDX1 в протоках важна для определения популяций предшественников, которые в итоге формируют эндокринную поджелудочную железу, было проведено определение коэкспрессии PDX1 и инсулина или глюкагона в трансплантатах. Клетки, экспрессирующие инсулин и глюкагон, наблюдались в трансплантатах уже через три недели после трансплантации (фиг. 12, панель a). Большинство эндокринных клеток, экспрессирующих гормоны клеток, формировалось, когда PDX1-положительные клетки покидали структуру протока. Значительное количество инсулин-положительных клеток обнаруживалось в трансплантате приблизительно через 10 недель. Большинство инсулин-положительных клеток экспрессировало PDX1 и NKX6.1 (фиг. 12, панель b). Эти данные коррелируют с данными о сроке экспрессии С-пептида, указанными выше. К двадцатой неделе количество инсулин-положительных клеток существенно возрастало, и в трансплантате обнаруживалось большое количество одиночных клеток, экспрессирующих только инсулин. Большинство клеток, экспрессирующих инсулин, также экспрессировало PDX1 (фиг. 12, панель c), NKX6.1 (фиг. 12, панель b) и NEUROD (фиг. 12, панель e). Было продемонстрировано, что экспрессия PDX1 и NKX6.1 полезна с точки зрения поддержания секреции инсулина при стимуляции глюкозой в зрелых бета-клетках.
В отдельном контрольном эксперименте животным вводили клетки, дифференцировавшиеся до конца четвертой стадии в среде DMEM/F12, в соответствии со способами, описанными в примере 1. В сыворотке животных, которым вводились эти клетки, человеческий С-пептид в течение 3 месяцев после трансплантации не обнаруживался. Более того, ПЦР и иммуногистохимический анализ не выявили экспрессии инсулина, PDX1 или NKX6.1. Однако через три месяца после трансплантации наблюдалось значительное количество глюкагон-положительных клеток.
Пример 5
Гистологическое исследование трансплантатов
Гистологическое исследование трансплантатов, отобранных у животных, которым были имплантированы клетки, проводилось в целом, как описано в предыдущем примере.
Трансплантаты от животных, проходивших обработку, описанную в предыдущем примере, извлекались и дважды промывались раствором PBS-/- (не содержащим ионов Mg++ и Ca++, Invitrogen), а затем переносились в 4% параформальдегид/PBS и фиксировались приблизительно 2-3 часа при 4°C, при этом PBS (-) меняли через 1 час. Затем трансплантаты доводили до равновесного состояния в растворе 30% сахарозы/PBS (-) в течение ночи при температуре 4°C, помещали в соединение OCT (SAKURA, №4583) и замораживали сухим льдом. Из тканей трансплантата приготавливали срезы толщиной 10 микрон с использованием криостата и срезы хранили при -80°C.
Для анализа замороженные срезы оттаивали до комнатной температуры, оттаявшие срезы промывали дважды раствором PBS в кассетах для микроскопических препаратов Shandon. Срезы тканей пермеабилизировали раствором PBS+0,5% Triton-X в течение 20 минут с последующей промывкой 2 мл PBS. Далее срезы инкубировали в блокирующем растворе, содержащем 4% куриную сыворотку в PBS. Препараты инкубировали приблизительно 1 час при комнатной температуре. Блокирующий раствор удаляли путем трехкратной промывки 2 мл PBS. Затем срезы снова инкубировали в кассетах Shandon в течение ночи при температуре 4°C с первичными антителами, разведенными в 4% куриной сыворотке.
После инкубации с первичными антителами препараты трижды промывали 2 мл PBS. Затем срезы снова инкубировали в кассетах Shandon при комнатной температуре с подходящими вторичными антителами, разведенными в 4% куриной сыворотке. Через 0,5-1 час срезы трижды промывали 2 мл PBS, после чего извлекали из кассет Shandon и закрепляли средой Vectashield, содержащей DAPI. С помощью других антител анализировали другие маркеры, характерные для клеток, секретирующих панкреатические гормоны, в том числе транскрипционные факторы PDX1. См. таблицу 2 ниже.
Публикации, цитируемые в данном документе, полностью включаются в настоящий документ в форме ссылок. Хотя различные аспекты изобретения иллюстрируются выше ссылками на примеры и предпочтительные варианты осуществления, подразумевается, что область изобретения ограничивается не указанным выше описанием, а следующими пунктами формулы изобретения, составленными в соответствии с принципами патентного законодательства.


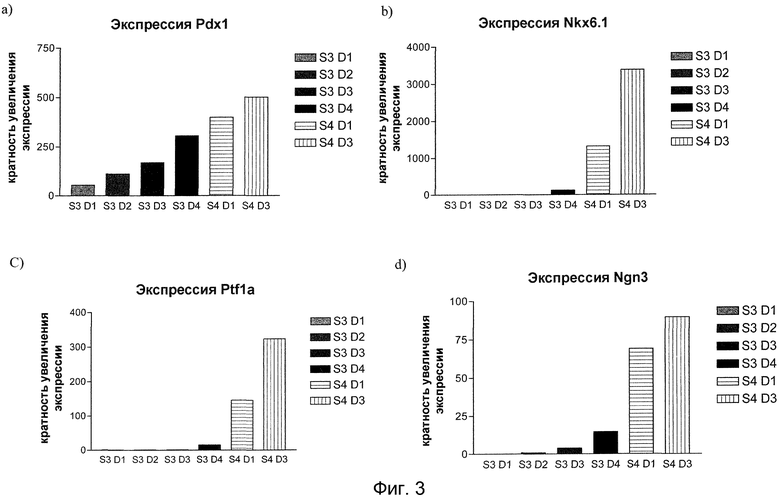
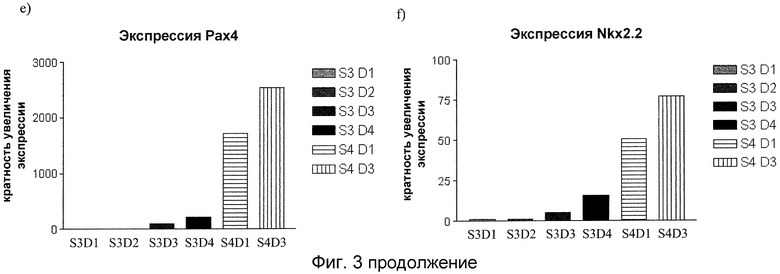
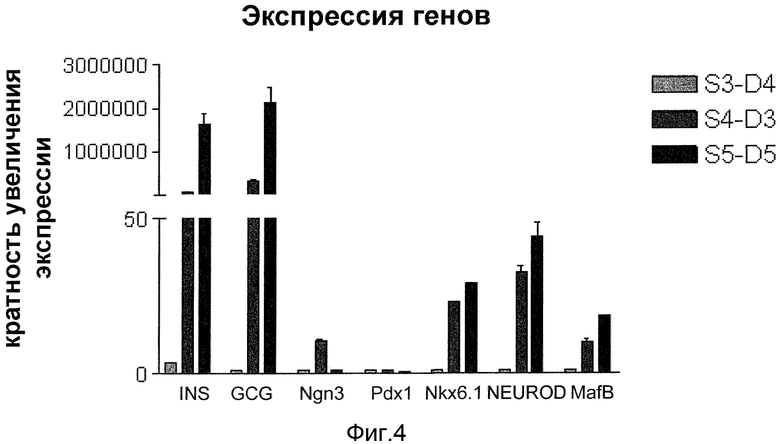
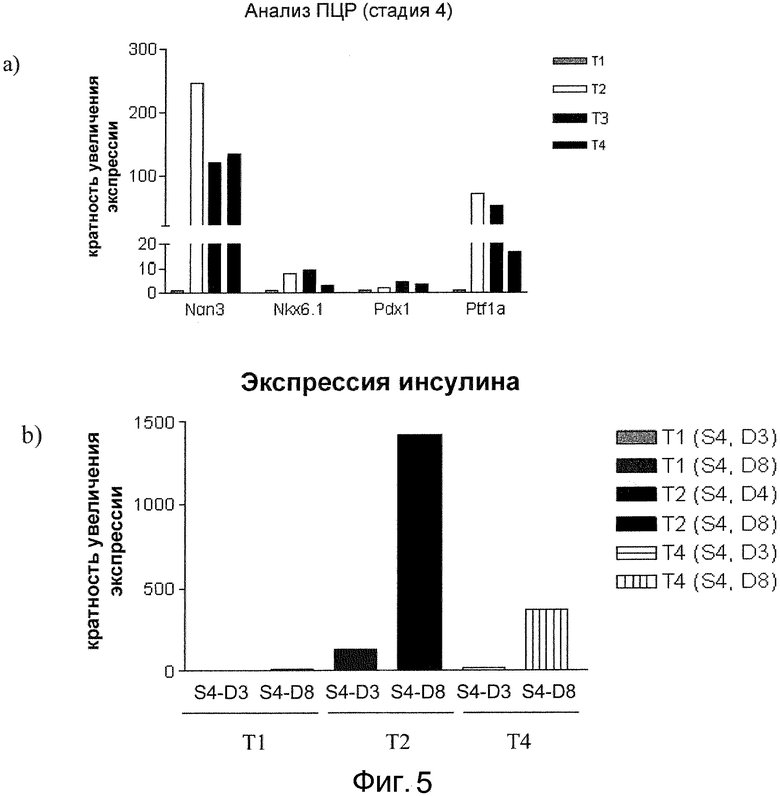
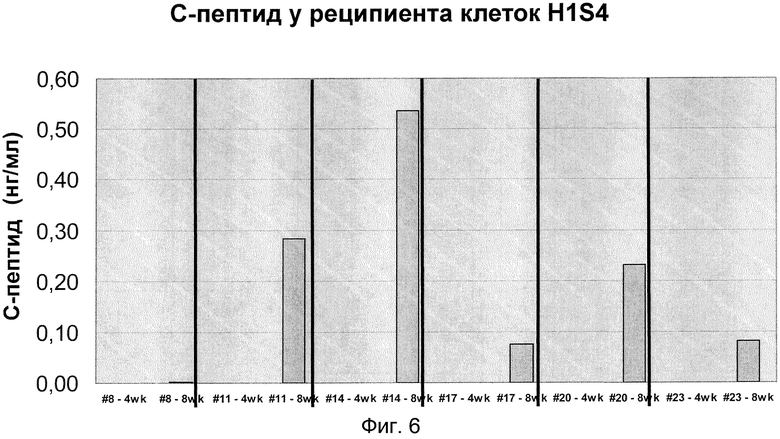
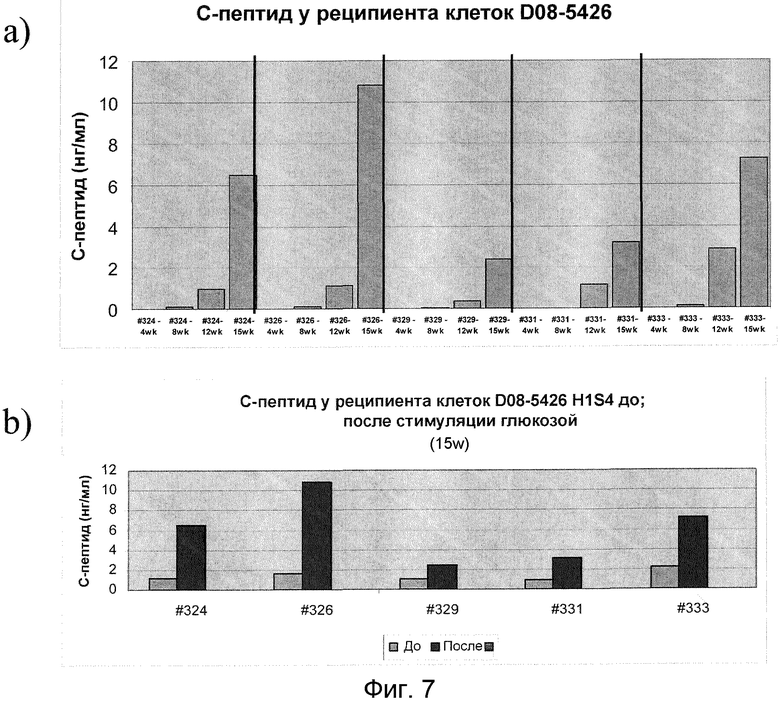
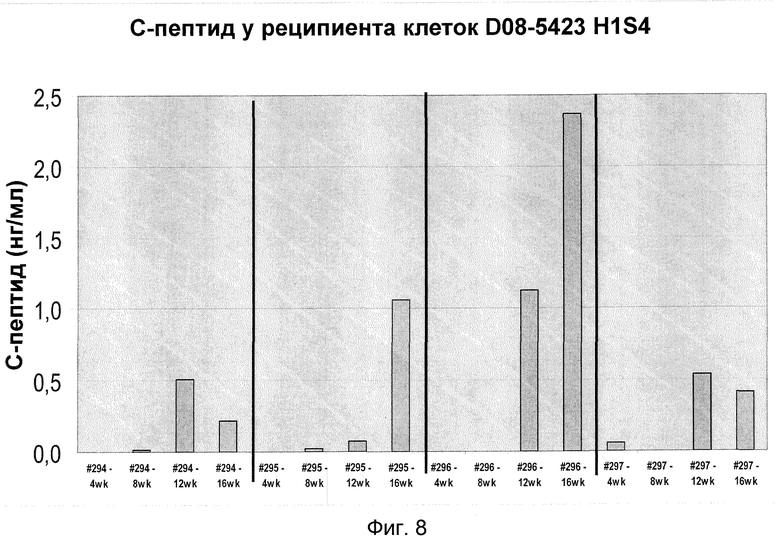
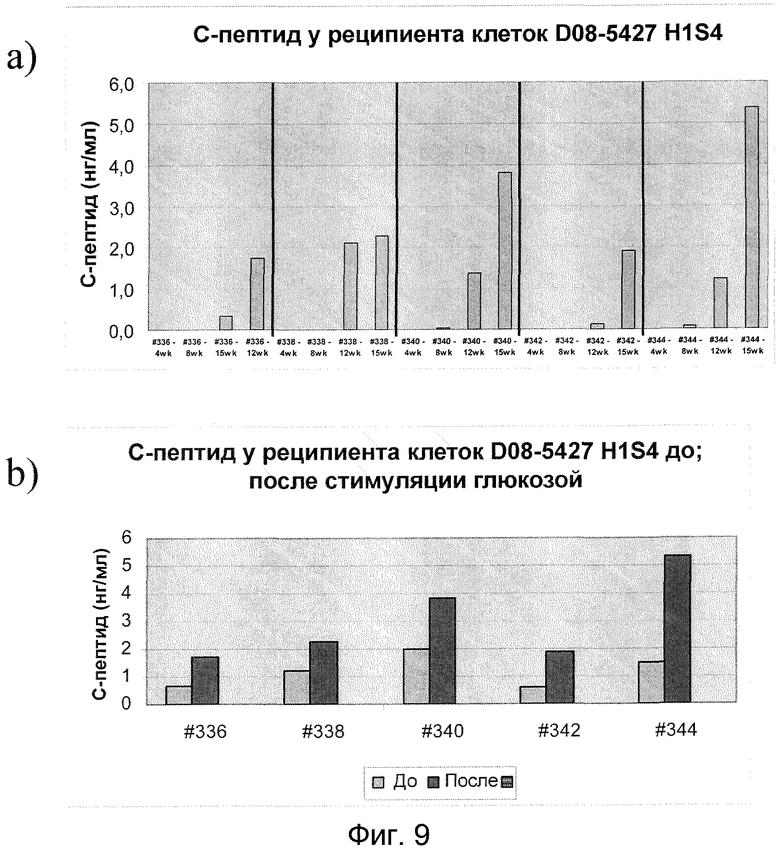
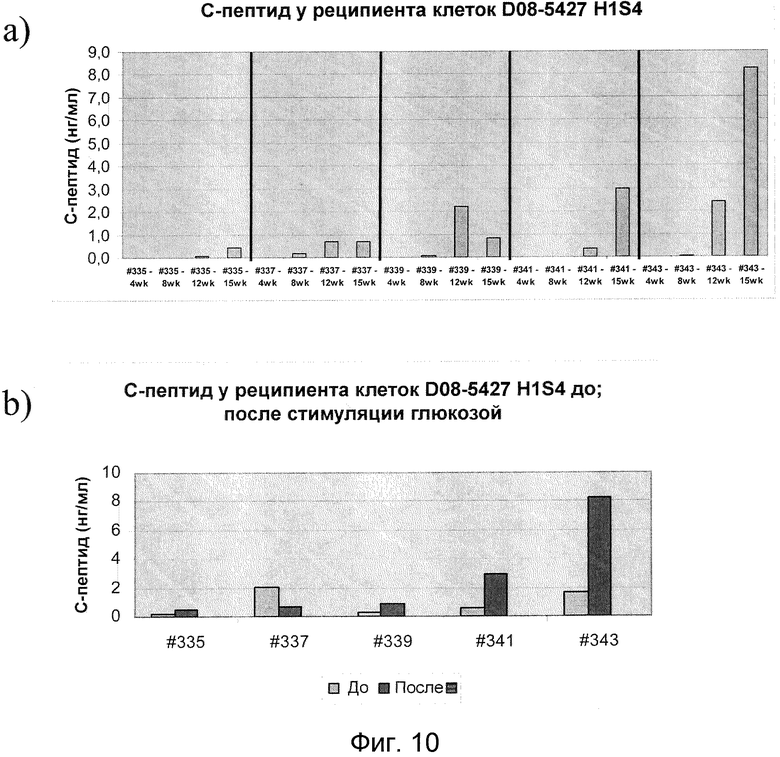
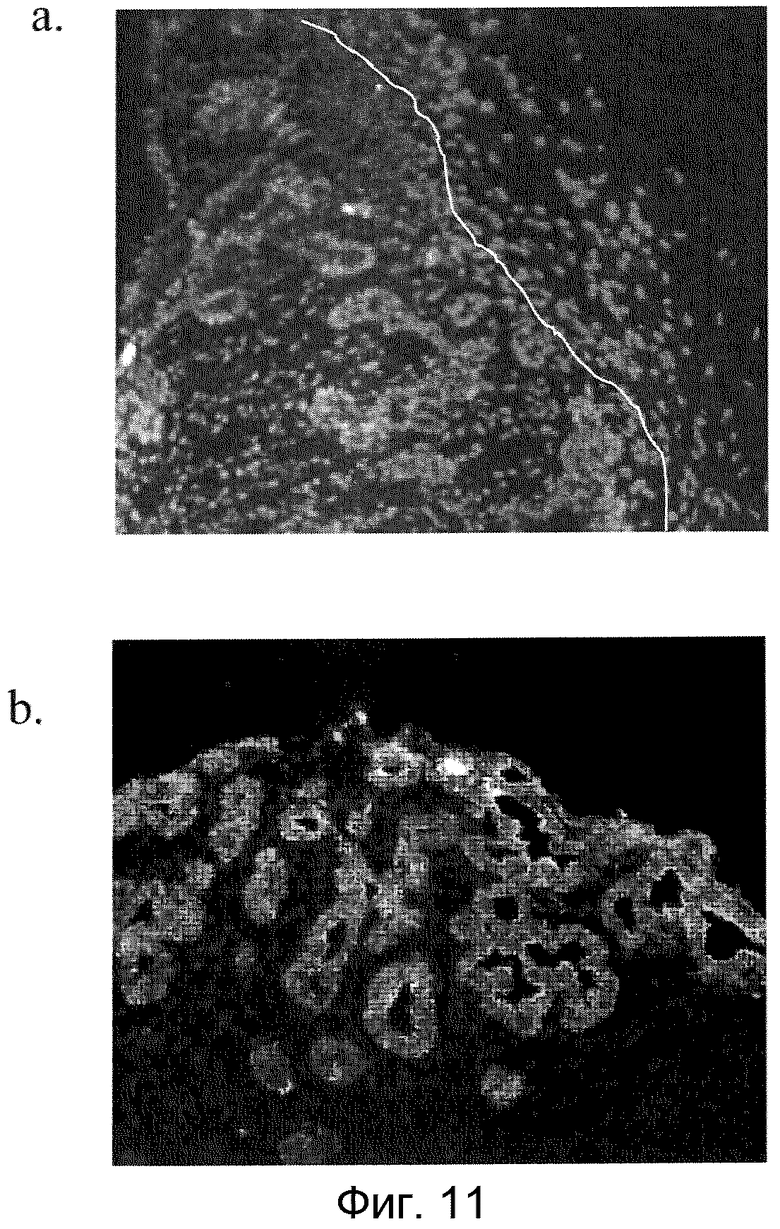
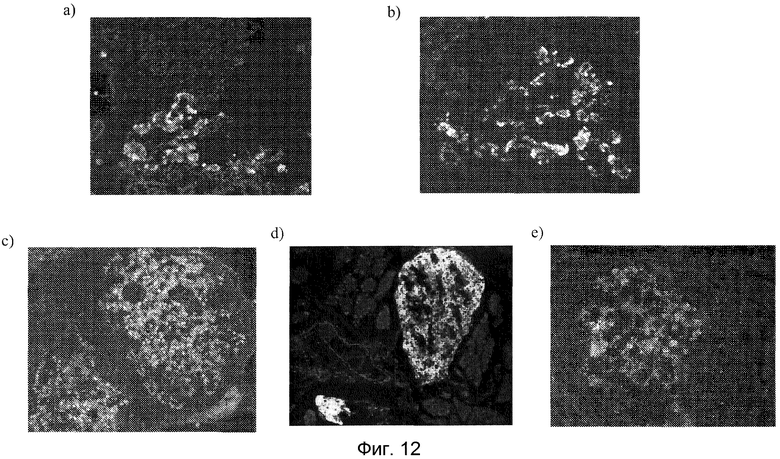
Группа изобретений относится к медицине, в частности к эндокринологии, и касается популяции панкреатических эндокринных клеток-предшественников для снижения концентрации глюкозы в крови у животного путем их трансплантации. Экспрессирующие PDX1 и NKX6.1 клетки-предшественники получают путем культивирования панкреатических эндодермальных клеток, полученных из клеток линии H1, Н7, Н9 или SA002. Культивирование проводят в среде, содержащей DMEM с высоким содержанием глюкозы, FGF7 и KAAD-циклопамин. Среда дополнена фактором, способным ингибировать BMP, и ингибитором киназы TGF-β рецептора I. Предложен также способ дифференцировки панкреатических эндодермальных клеток в клетки-предшественники, экспрессирующие PDX1 и NKX6. Для этого культивируют клетки в указанной выше среде. Группа изобретений обеспечивает эффективное снижение уровней глюкозы в крови у животного при повышении успешности трансплантации клеток. 2 н. и 16 з.п. ф-лы, 12 ил., 2 табл., 5 пр.
1. Популяция панкреатических эндокринных клеток-предшественников, экспрессирующих PDX1 и NKX6.1, для применения в способе снижения концентрации глюкозы в крови у животного путем трансплантации популяции клеток в животное, где панкреатические эндокринные клетки-предшественники получают путем культивирования панкреатических эндодермальных клеток, полученных из клеток линии H1, Н7, Н9 или SA002, в среде, содержащей DMEM с высоким содержанием глюкозы, FGF7 и KAAD-циклопамин, и где среда дополнена фактором, способным ингибировать BMP, и ингибитором киназы TGF-β рецептора I.
2. Популяция клеток для применения в соответствии с п. 1, где среда содержит DMEM (с высоким содержанием глюкозы), содержащую 4500 мг/л глюкозы и 1% В27.
3. Популяция клеток для применения в соответствии с п. 2, где фактором, способным ингибировать BMP, является noggin.
4. Популяция клеток для применения в соответствии с п. 3, где noggin применяется в концентрации от приблизительно 100 пг/мл до приблизительно 500 мкг/мл или в концентрации 100 нг/мл.
5. Популяция клеток для применения в соответствии с п. 2, где ингибитором киназы TGF-β рецептора I является ALK5 ингибитор II.
6. Популяция клеток для применения в соответствии с п. 5, где ALK5 ингибитор II применяется в концентрации от приблизительно 0,1 мкМ до приблизительно 10 мкМ или в концентрации 1 мкМ.
7. Популяция клеток для применения в соответствии с любым из пп. 1-6, где клетки культивируют в культуральной среде в течение приблизительно четырех суток.
8. Популяция клеток для применения в соответствии с п. 1, где культуральная среда содержит DMEM (с высоким содержанием глюкозы), В27 (1% Invitrogen, СА), FGF7 (50 нг/мл), KAAD-циклопамин (0,25 мкМ), Noggin (100 нг/мл), и, необязательно, ингибитор Alk5 (1 мкМ).
9. Популяция клеток для применения в соответствии с любым из пп. 1-6, где животным является пациент с диабетом 1 типа или 2 типа или с риском его развития.
10. Популяция клеток для применения в соответствии с любым из пп. 1-6, где клетки не дифференцированы, или частично дифференцированы, или полностью дифференцированы в инсулинпродуцирующие клетки до трансплантации в животное, и, необязательно, содержит дополнительную дифференциацию клеток в животном.
11. Популяция клеток для применения в соответствии с любым из пп. 1-6, где клетки дифференцированы in vtro в линию β-клеток или в панкреатические эндокринные клетки-предшественники и клетки линии β-клеток или панкреатические эндокринные клетки-предшественники имплантированы в животное.
12. Популяция клеток для применения в соответствии с любым из пп. 1-6, где клетки, трансплантированные или имплантированные в животное, представлены в биологически-совместимых разрушающихся полимерных вспомогательных материалах, в пористых неразрушающихся приспособлениях или в инкапсулированном виде для защиты от иммунного ответа организма-хозяина.
13. Популяция клеток для применения в соответствии с любым из пп. 1-6, где способ дополнительно содержит обработку животного фармацевтическими средствами или биологически активными веществами, которые повышают выживаемость и функционирование трансплантированных клеток, выбранными из списка, содержащего: инсулин, члены семейства TGF-β, включая TGF-β1, 2 и 3, костные морфогенетические белки (ВМР-2, -3, -4, -5, -6, -7, -11, -12 и -13), факторы роста фибробластов -1 и -2, тромбоцитарный фактор роста -АА и -ВВ, плазма, богатая тромбоцитами, инсулин-подобный фактор роста (IGF-I, II), фактор роста и дифференцировки (GDF-5, -6, -7, -8, -10, -15), фактор роста из клеток эндотелия сосудов (VEGF), плейотропин, эндотелии, никотинамид, глюкагон-подобный пептид-I (GLP-1) и II, миметические антитела GLP-1 и 2, экзендин-4, ретиноевая кислота, паратиреоидный гормон, ингибиторы МАРК.
14. Популяция клеток для применения в соответствии с любым из пп. 1-6, где дополнительные факторы, такие как факторы роста, антиоксиданты или противовоспалительные средства вводят до, одновременно с или после введения клеток.
15. Способ дифференцировки панкреатических эндодермальных клеток, полученных из клеток линии H1, Н7, Н9 или SA002, в панкреатические эндокринные клетки-предшественники, экспрессирующие PDX1 и NKX6.1, где способ включает культивирование панкреатических эндодермальных клеток в среде, содержащей DMEM с высоким содержанием глюкозы, FGF7 и KAAD-циклопамин, и где среда дополнена фактором, дополнена фактором, способным ингибировать BMP, и ингибитором киназы TGF-β рецептора I.
16. Способ в соответствии с п. 15, где среда представляет собой среду, как она определена в любом из пп. 2-6.
17. Способ в соответствии п. 15 или 16, где клетки культивируют, как определено в п. 7.
18. Способ в соответствии с любым из пп. 15, 16, где среда представляет собой среду, как она определена в п. 8.
Авторы
Даты
2016-04-10—Публикация
2010-07-19—Подача