Изобретение относится к химии биологически активных соединений, а именно к способу получения геометрических изомеров 2-(6′-хлорпиридин-3′ил)-7-азабицикло[2.2.1]гептана.
2-(6′-Хлорпиридин-3′-ил)-7-азабицикло[2.2.1]-гептан может существовать в виде двух диастереомеров, различающихся расположением 6-хлор-3-пиридинового фрагмента относительно бицикла: 2-эндо-(6′-хлорпиридин-3′-ил)-7-азабицикло[2.2.1]гептан (I) и 2-экзо-(6′-хлор-пиридин-3′-ил)-7-азабицикло[2.2.1]гептан (II)
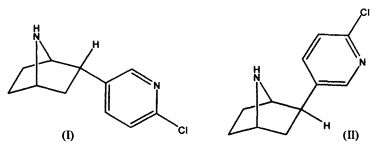
Оба изомера проявляют высокую анальгетическую активность, превышающую морфин, и могут рассматриваться как анальгетики неопиоидного действия.
Известен способ получения 2-(6′-хлорпиридин-3′-ил)-7-азабицикло[2.2.1]гептана из N-защищенного-7-азабицикло[2.2.1]гепт-2-ена восстановительной реакцией Хека
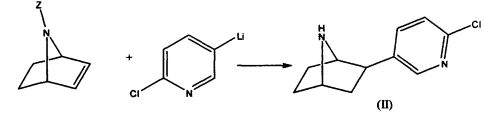
К недостаткам данного способа можно отнести образование большого количества побочных продуктов, в результате выход 2-(6′-хлорпиридин-3′-ил)-7-азабицикло[2.2.1]гептана не превышает 35% (Liang F., Navarro Н.А., Abraham P. et al., J. Med. Chem., 1997, 40 (15), 2293).
Кроме того, реакция Хека протекает как экзо-процесс и проводит только к экзо-изомеру, то есть 2-эндо-(6′-хлорпиридин-3′-ил)-7-азабицикло[2.2.1]-гептан получить по данному способу невозможно.
Известен способ получения 2-(6′-хлорпиридин-3′-ил)-7-азабицикло[2.2.1]-гептана, исходя из 7-азабицикло[2.2.1]гептан-2-она. Первоначально осуществляют классический синтез по Гриньяру: к 7-азабицикло[2.2.1]гептан-2-ону присоединяют 3-литий-6-хлорпиридин, в результате образуется соответствующий третичный спирт. Затем следует восстановительное удаление гидроксильной группы, которое осуществляется следующим образом: спирт ацилируют хлорангидридом монометилового эфира щавелевой кислоты в присутствии 4-диметиламинопиридина и полученный сложный эфир восстанавливают при повышенной температуре (100°C) смесью замещенных гидридов олова и алюминия. Дезоксигенирование третичного спирта протекает с обращением конфигурации, в результате образуется эндо-изомер (Zhang С, Trudell M.L., J. Org. Chem., 1996, 61 (20), 7189)
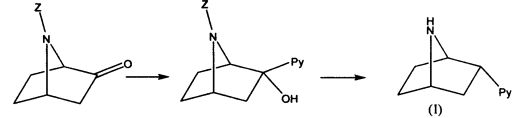
где Py - 6-хлор-3-пиридил.
К недостаткам данного способа можно отнести образование значительного количества побочных продуктов и использование на стадии восстановительного удаления сложноэфирной группы труднодоступных, дорогих восстановителей. Также по данному способу можно получить только 2-эндо-(6′-хлор-пиридин-3′-ил)-7-азабицикло[2.2.1]гептан.
Для получения 2-(6′-хлорпиридин-3′-ил)-7-азабицикло[2.2.1]гептана можно использовать циклизацию производных циклогексиламина, замещенных в 4-м положении легко уходящей группой. Причем, варьируя положение хлорпиридинового фрагмента, можно получить как экзо-, так и эндо-изомер.
Так, если хлорпиридиновый фрагмент находится в 2е положении циклогексиламина, то образуется 2-эндо-(6′-хлор-пиридин-3′-ил)-7-азабицикло[2.2.1]гептан:
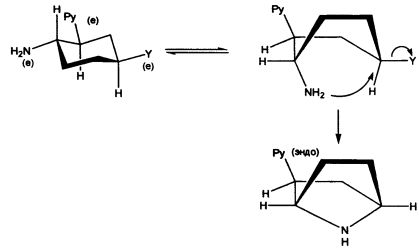
где Py - 6-хлор-3-пиридил.
Если хлорпиридиновый фрагмент находится в 3е положении циклогексиламина, то образуется 2-экзо-(6′-хлорпиридин-3′-ил)-7-азабицикло[2.2.1] гептан:
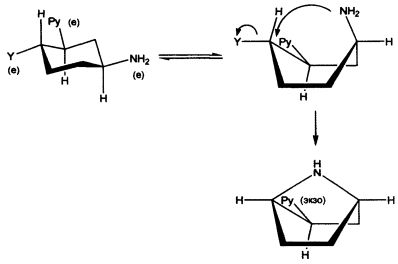
где Py - 6-хлор-3-пиридил.
Известен способ получения 2-экзо-(6′-хлорпиридин-3′-ил)-7-азабицикло-[2.2.1]гептана, заключающийся в нагревании до температуры кипения 0,01 М раствора 1α-амино-3β-[3′-(6′-хлорпиридил)]-4β-метансульфонилоксицикло-гексана в хлороформе в течение 3 суток. Затем реакционную смесь охлаждают и промывают водным раствором бикарбоната натрия, сушат прокаленным карбонатом калия, фильтруют и кипятят еще 1 сутки. Отгоняют растворитель и получают целевое соединение с выходом 84% (Szantay Cs., Kardos-Balogh Zs., Moldvai I. et al., Tetrahedron Lett., 1994, 35 (19), 3171).
Известен способ получения 2-эндо-(6′-хлорпиридин-3′-ил)-7-азабицикло-[2.2.1]гептана, заключающийся в нагревании до температуры кипения 0,01 М раствора 1α-амино-2β-[3′-(6′-хлорпиридил)]-4β-метансульфонилокси-циклогексана в толуоле 24 часа. Затем реакционную смесь охлаждают и промывают 10%-ным водным раствором гидроксида натрия, водную фазу экстрагируют хлористым метиленом, объединенный экстракт промывают насыщенным водным раствором хлорида натрия, сушат прокаленным сульфатом магния, фильтруют, растворитель отгоняют, остаток хроматографируют с использованием элюента хлороформ-метанол-аммиак в соотношении 10:1:0,1. Получают соединение с выходом 46% (Szantay Cs., Kardos-Balogh Zs., Moldvai I. et al., Tetrahedron, 1996, 52 (33), 11053).
К недостаткам известного способа следует отнести длительность процесса циклизации и необходимость в сложном выделении целевого соединения из реакционной смеси с использованием значительного количества различных растворителей и нехимических операций.
Настоящее изобретение направлено на повышение выхода целевого соединения, сокращение времени проведения процесса и упрощение выделения целевого соединения.
Сущность предлагаемого изобретения состоит в проведении циклизации соответствующего замещенного циклогексиламина (формулы III и формулы IV) в растворе низкомолекулярного спирта в присутствии стерически затрудненного третичного амина
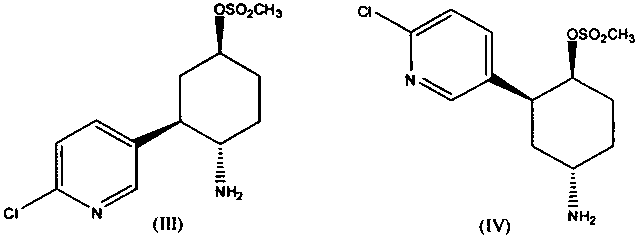
В качестве стерически затрудненного третичного амина можно использовать любые третичные амины, имеющие разветвления у двух атомов углерода, связанных с атомом азота. Предпочтительней использовать N-алкил-N,N-диизопропиламины. Природа алкильной группы в N-алкил-N,N-диизопропиламине не оказывает существенного влияния на циклизацию. Предпочтительно использовать N-метил- или N-этил-N,N-диизопропиламин, имеющие невысокие температуры кипения, что упрощает процесс выделения целевого соединения.
Для достижения высокого выхода и высокой скорости реакции предпочтительно использовать 1-25%-ный мольный избыток стерически затрудненного третичного амина. Количество третичного амина оказывает влияние на скорость циклизации. Так, в присутствии от 1 до 5% мольного избытка реакция завершается за 3-4 часа, а при увеличении мольного избытка стерически затрудненного третичного амина до 10-25% требуется 1,5-2 часа для достижения полного расходования исходного соединения. Использование мольного избытка третичного амина более 25% нецелесообразно, так как не оказывает влияния на процесс циклизации.
Циклизацию проводят в растворе низкомолекулярного спирта, природа которого не оказывает существенного влияния. Предпочтительно использовать спирты С1-С4 как нормального, так и разветвленного строения, так как данные соединения имеют невысокие температуры кипения, что позволяет упростить процесс выделения целевого соединения.
Проведение циклизации по предлагаемому способу позволяет предотвратить образование побочных продуктов, что способствует достижению высоких выходов и высокой степени чистоты получаемых целевых соединений. В результате отсутствует необходимость в дополнительной очистке, что существенно упрощает процесс получения 2-(6′-хлор-пиридин-3′-ил)-7-азабицикло[2.2.1]гептанов.
Таким образом, предлагаемый способ легко реализуется в промышленных условиях и позволяет получать эндо- и экзо-изомеры 2-(6′-хлорпиридин-3′-ил)-7-азабицикло[2.2.1]гептана с высоким выходом и высокой степенью чистоты.
Сущность данного изобретения иллюстрируется, но не ограничивается следующими примерами.
Пример 1. Получение 2-эндо-(6′-хлорпиридин-3′-ил)-7-азабицикло[2.2.1]-гептана
Раствор 315 мг (1,03 ммоль) 1α-амино-2β-[3′-(6′-хлорпиридил]-4β-метансульфонилоксициклогексана и 167 мг (1,29 ммоль) N-этил-N,N-диизопропиламина в 15 мл сухого изопропанола кипятят при перемешивании в течение 2 часов в атмосфере аргона. Охлаждают и при перемешивании добавляют 0,5 мл 10%-ного водного раствора гидроксида натрия. Смесь энергично перемешивают 15 минут. Слои разделяют, водный экстрагируют хлористым метиленом. Объединенный экстракт промывают насыщенным водным раствором хлорида натрия и сушат карбонатом калия. Фильтруют, растворитель отгоняют при пониженном давлении. Получают 192 мг 2-эндо-(6′-хлорпиридин-3′-ил)-7-азабицикло[2.2.1]гептана в виде бледно-желтой жидкости, выход 96%, содержание основного вещества 99% (ВЭЖХ).
Спектр ЯМР 1Н (400 МГц, CDCl3): 1,32-1,48 м (3Н, 5-СН2, 6-СНэкзо), 1,53 дд (1Н, 3-СНэкзо, 3J 12,4; 5,6 Гц), 1,64-1,72 м (1Н, 6-СНэндо), 2,15 дддд (1Н, 3-СНэндо, 3J 12,4; 10,4; 4,8; 3,2 Гц), 2,31 уш.с (1Н, NH), 3,34 ддд (1Н, 2-СН, 3J 10,4; 6,4; 4,8 Гц), 3,81 дд (2Н, 1- и 4-СН, 3J 9,6; 5,6 Гц), 7,29 д (1Н, 5′-СН(Py), 3J 8,4 Гц), 7,47 дд (1H, 4′-СН(Py), 3J 8,4; 2,4 Гц), 8,26 д (1Н, 2′-CH(Py), 3J 2,4 Гц).
Масс-спектр, m/z (%): 210 (М[37Cl]+, 5%), 208 (М[35Cl]+, 15%), 179 (6), 140 (25), 68 (100).
Пример 2. Получение 2-эндо-(6′-хлорпиридин-3′-ил)-7-азабицикло[2.2.1]-гептана
Раствор 861 мг (2,82 ммоль) 1α-амино-2β-[3′-(6′-хлорпиридил]-4β-метансульфонилоксициклогексана и 383 мг (2,97 ммоль) N-этил-N,N-диизопропиламина в 35 мл сухого метанола кипятят при перемешивании в течение 3 часов в атмосфере аргона. Далее аналогично примеру 1.
Получают 525 мг 2-эндо(6′-хлорпиридин-3′-ил)-7-азабицикло[2.2.1]гептана в виде бледно-желтой жидкости, выход 89%, содержание основного вещества 99% (ВЭЖХ).
Пример 3. Получение 2-эндо-(6′-хлорпиридин-3′-ил)-7-азабицикло[2.2.1]-гептана
Раствор 486 мг (1,59 ммоль) 1α-амино-2β-[3′-(6′-хлорпиридил]-4β-метансульфонилоксициклогексана и 202 мг (1,75 ммоль) N-метил-N,N-диизопропиламина в 20 мл сухого трет-бутанола кипятят при перемешивании в течение 2 часов в атмосфере аргона. Далее аналогично примеру 1.
Получают 316 мг 2-эндо-(6′-хлорпиридин-3′-ил)-7-азабицикло[2.2.1]гептана в виде бледно-желтой жидкости, выход 95%, содержание основного вещества 99% (ВЭЖХ).
Пример 4. Получение 2-экзо-(6′-хлорпиридин-3′-ил)-7-азабицикло[2.2.1]-гептана
Раствор 248 мг (0,81 ммоль) 1α-амино-3β-[3′-(6′-хлорпиридил]-4β-метансульфонилоксициклогексана и 113 мг (0,98 ммоль) N-метил-N,N-диизопропиламина в 10 мл сухого бутанола-2 кипятят при перемешивании в течение 2 часов в атмосфере аргона. Далее аналогично примеру 1.
Получают 160 мг 2-экзо-(6′-хлорпиридин-3′-ил)-7-азабицикло[2.2.1]гептана в виде бледно-желтой жидкости, кристаллизующейся при хранении, выход 95%, содержание основного вещества 99% (ВЭЖХ).
Спектр ЯМР 1Н (400 МГц, CDCl3, δ, м.д., J Гц): 1,50-1,62 м (6Н, 5-СН2, 6-СН2, 3-СНендо и NH), 1,90 дд (1Н, 3-СНэкзо, 3J 12,0; 9,0 Гц), 2,75 дд (1Н, 2-СН, 3J 9,0; 4,9 Гц), 3,54 д (1Н, 1-СН, 3J 1,1 Гц), 3,78 дд (1H, 4-СН, 3J 3,9; 3,9 Гц), 7,22 д (1Н, 5′-СН(Py), 3J 8,3 Гц), 7,76 дд (1Н, 4′-СН(Py), 3J 8,3; 2,5 Гц), 8,27 д (1Н, 2′-СН(Py), 3J 2,5 Гц).
Масс-спектр, m/z (%): 210 (М[37Cl]+, 8%), 208 (М[35Cl]+, 25%), 179 (14), 140 (30), 69 (100), 68 (75).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 2-ЭКЗО-[3'-(6'-ХЛОРПИРИДИЛ)]-7-АЗАБИЦИКЛО[2.2.1]-ГЕПТАНА | 2013 |
|
RU2537390C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕРАПЕВТИЧЕСКОГО ЭФФЕКТА ИНГИБИТОРА LSD1 НА ОСНОВЕ ЭКСПРЕССИИ INSM1 | 2018 |
|
RU2789449C2 |
| УСИЛИТЕЛЬ ПРОТИВООПУХОЛЕВОГО ЭФФЕКТА С ПРИМЕНЕНИЕМ НОВОГО СОЕДИНЕНИЯ БИФЕНИЛА | 2018 |
|
RU2765153C2 |
| НОВОЕ СОЕДИНЕНИЕ БИФЕНИЛА ИЛИ ЕГО СОЛЬ | 2018 |
|
RU2765152C2 |
| АЗАБИЦИКЛИЧЕСКИЕ АЛКАНОВЫЕ ПРОИЗВОДНЫЕ, ЗАМЕЩЕННЫЕ КОНДЕНСИРОВАННЫМ БИЦИКЛОГЕТЕРОЦИКЛОМ | 2007 |
|
RU2437884C2 |
| ИНГИБИТОР ДИПЕПТИДИЛПЕПТИДАЗЫ-4 ДЛЯ ЛЕЧЕНИЯ САХАРНОГО ДИАБЕТА 2-ГО ТИПА, СОЕДИНЕНИЯ (ВАРИАНТЫ) | 2018 |
|
RU2712097C1 |
| НОВОЕ СОЕДИНЕНИЕ БИФЕНИЛА ИЛИ ЕГО СОЛЬ | 2016 |
|
RU2726622C2 |
| O-Ациламидоксимы и 1,2,4-оксадиазолы, содержащие фрагмент бицикло[2.2.1]гептанона-2, в качестве ингибиторов репродукции филогенетически различных вирусов гриппа А: штаммы A/Puerto Rico/8/34 (H1N1), A/Anhui/1/2013 (H7N9) | 2022 |
|
RU2798171C1 |
| 2-ОКСА-5-АЗАБИЦИКЛО[2.2.1]ГЕПТАН-3-ИЛЬНЫЕ ПРОИЗВОДНЫЕ | 2015 |
|
RU2697651C2 |
| Способ получения амидов ряда 1,4,7,7-тетраметилбицикло[2.2.11]гептана | 1988 |
|
SU1631058A1 |
Изобретение относится к способу получения экзо- и эндо-изомеров 2-(6′-хлорпиридин-3′-ил)-7-азабицикло[2.2.1]гептана - анальгетиков неопиоидного действия. Предложен способ, основанный на циклизации соответствующего замещенного циклогексиламина (формулы III и формулы IV) в растворе низкомолекулярного спирта в присутствии стерически затрудненного третичного амина. Предлагаемый способ легко реализуется в промышленных условиях и позволяет получать эндо- и экзо-изомеры 2-(6′-хлорпиридин-3′-ил)-7-азабицикло[2.2.1]гептана с высоким выходом и высокой степени чистоты. 3 н. и 6 з.п. ф-лы, 4 пр.
1. Способ получения 2-(6′-хлорпиридин-3′-ил)-7-азабицикло[2.2.1]гептана циклизацией замещенного циклогексиламина, отличающийся тем, что реакцию проводят в растворе низкомолекулярного спирта в присутствии стерически затрудненного третичного амина, взятого в 1-25%-ном мольном избытке.
2. Способ по п. 1, отличающийся тем, что циклизацию проводят в среде спирта С1-С4 нормального и разветвленного строения.
3. Способ по п. 1, отличающийся тем, что циклизацию проводят в присутствии N-метил-NN-диизопропиламина или N-этил-NN-диизопропиламина.
4. Способ получения 2-эндо-(6′-хлорпиридин-3′-ил)-7-азабицикло[2.2.1]-гептана (I), отличающийся тем, что в качестве исходного реагента используется 1α-амино-2β-[3′-(6′-хлорпиридил)]-4β-метансульфонил-оксициклогексан (III)
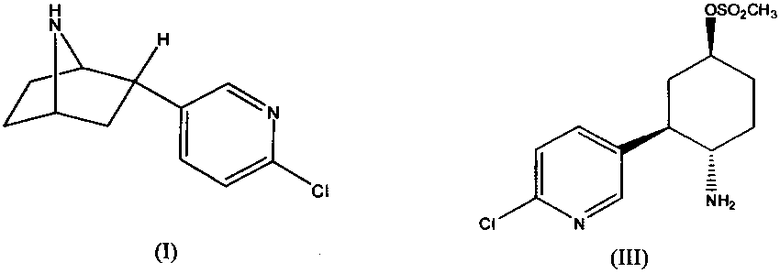
5. Способ по п. 4, отличающийся тем, что циклизацию проводят в среде спирта С1-С4 нормального и разветвленного строения.
6. Способ по п. 4, отличающийся тем, что циклизацию проводят в присутствии N-метил-NN-диизопропиламина или N-этил-NN-диизопропиламина.
7. Способ получения 2-экзо-(6′-хлорпиридин-3′-ил)-7-азабицикло[2.2.1]-гептана (II), отличающийся тем, что в качестве исходного реагента используется 1α-амино-3β-[3′-(6′-хлорпиридил)]-4β-метансульфонил-оксициклогексан (IV)
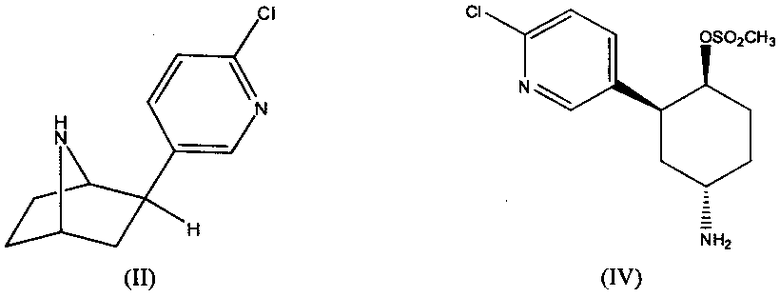
8. Способ по п. 7, отличающийся тем, что циклизацию проводят в среде спирта С1-С4 нормального и разветвленного строения.
9. Способ по п. 7, отличающийся тем, что циклизацию проводят в присутствии N-метил-NN-диизопропиламина или N-этил-NN-диизопропиламина.
| Szantay Cs., Kardos-Balogh Zs., Moldvai I., et al., Tetrahedron, 1996, 52 (33), pp.11053. | |||
| JPH06312989,A,08.11.1994 | |||
| Hodgson, David M.; Maxwell, Christopher R.; Matthews, Ian R | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Synthesis of an epibatidine analog."(Dyson Perrins Laboratory, Department Chemistry, | |||
Авторы
Даты
2016-07-10—Публикация
2015-01-23—Подача