Изобретение относится к медицине, а именно к коагулологии, и может быть использовано в лечении подострых венозных тромбозов различной локализации при резистентности к проводимой адекватной антикоагулянтной терапии.
Острые тромбозы глубоких вен и тромбофлебиты поверхностных вен нижних конечностей являются распространенными заболеваниями и встречаются у 10-20% населения [1]. При этом частота тромбозов глубоких вен (ТГВ) составляет от 50 до 160 случаев на 100 тыс. населения [2, 3]. Наиболее опасным осложнением тромбоза глубоких вен, несущим угрозу летального исхода, является тромбоэмболия легочной артерии (ТЭЛА). ТЭЛА встречается приблизительно в 10% случаев ТГВ, при этом у 20% больных в течение последующих двух лет развивается рецидив заболевания либо тяжелые формы ХВН. У 300 больных на 100 тысяч популяции ранее перенесенные венозные тромбозы служат причиной развития трофических язв нижних конечностей. Такие состояния требуют обязательного назначения антитромботической терапии. Наиболее эффективным способом лечения тромбозов глубоких вен, независимо от локализации, признана антикоагулянтная терапия. При отсутствии противопоказаний она показана всем больным ТГВ. Ее использование возможно в качестве самостоятельного метода лечения при неэмболоопасных видах флеботромбоза, предотвращая формирование флотирующих тромбов, она выступает в качестве действенной меры профилактики ТЭЛА. Исход ТГВ в плане развития рецидива и основных осложнений напрямую зависит от сроков диагностики и начала адекватной антикоагулянтной терапии, от длительности ее проведения [4, 5, 6, 7].
Известно, что при тромбозе глубоких вен в лечении применяют прямые антикоагулянты: нефракционированный гепарин (НФГ) или низкомолекулярные гепарины (НМГ) в течение периода острого тромбоза с последующим переходом на антикоагулянты непрямого действия (АНД) в лечебных дозах. Общая продолжительность лечения антикоагулянтами зависит от наличия и характера факторов, предрасполагающих к рецидиву заболевания, наличия венозных тромбоэмболических осложнений в анамнезе, распространенности поражения. Она должна составлять не менее 3-6 мес, а при наличии генетической тромбофии применяется в течение всей жизни (Российские клинические рекомендации по диагностике, лечению и профилактике венозных тромбоэмболических осложнений. - М.: Медиа Сфера, стр. 32. Источник информации - официальный сайт Ассоциации флебологов России www.phlebo-union.ru и Журнал "Флебология", том 4, выпуск 2, N1, 2010 год, стр. 32).
Наиболее близким к предлагаемому является способ лечения подострых тромбозов различной локализации, включающий проведение антикоагулянтной терапии с начальной дозой препарата, определение целевого уровня показателя эффективности антикоагулянтного действия препарата, подбор индивидуальной лечебной дозы на фоне значений целевого уровня и ее коррекцией в сторону увеличения или уменьшения в случае отклонения целевого уровня, с последующим переходом на профилактические дозы («Российские клинические рекомендации по диагностике, лечению и профилактике тромбоэмболических осложнений», журнал «Флебология», том 4, выпуск 2, №1, 2010 год, стр. 32).
В данном способе терапию проводят с помощью непрямого антикоагулянта, нарушающего синтез витамин-К-зависимых факторов свертывания - варфарина. Согласно этому способу осуществляют выбор объема антикоагулянтной терапии у больных различными формами ТГВ нижних конечностей. Индивидуальную, эффективную дозу АДН подбирают таким образом, чтобы поддерживать целевой уровень MHO в пределах от 2,0 до 3,0. При этом лечение начинают с минимальных доз, а затем продолжают лечение с использованием индивидуально установленной дозы под контролем целевого уровня, коррекцией дозы в сторону увеличения или уменьшения до достижения максимального результата с последующим переходом на профилактические дозы.
Основным недостатком как первого, так и второго способов лечения подострых венозных тромбозов различной локализации является неадекватность лечения.
Так, например, даже при соблюдении всех рекомендаций наблюдается различная реакция пациентов на антикоагулянтную терапию, вплоть до парадоксальной в виде прогрессирования тромботического процесса или отсутствия достижения реканализации вен. Это объясняется тем, что большинство антикоагулянтов как прямого действия, инактивирующих фактор Ха (НМГ, нефракционированный гепарин, фондопаринукс, ривароксабан (Ксарелто), так и непрямых антикоагулянтов, нарушающих синтез витамин-К-зависимых факторов свертывания (варфарин и др.), не воздействуют на уже сформированный тромб, а лишь предотвращают образование новых, при этом растворение тромбов осуществляется за счет собственной системы фибринолиза. Применение антикоагулянтов не гарантирует от прогрессирования тромботического процесса или формирования резистентных форм тромбозов с последующим развитием ПТФС [7]. Неадекватное лечение приводит к развитию декомпенсированных форм ХВН. Неполноценная реабилитация нарушает социальную адаптацию пациентов. Хронические заболевания вен (ХЗВ) сохраняют за собой статус важной медико-социальной проблемы, не только затрагивающей интересы врачей и организаторов здравоохранения, но и влияющей на глобальную экономику развитых стран [7].
В последнее время в мире наблюдается активная тенденция к применению в клинической практике новых пероральных антикоагулянтов: синтетического ингибитора фактора Ха - Ксарелто (ривароксабан) и прямых ингибиторов тромбина - Прадакса (дабигатран), эффективность которых доказана в ряде клинических исследований.
Известен способ лечения подострых венозных тромбозов различной локализации с использованием дабигатрана (пат. РФ №2530645, кл. A61K 31/4439, публ. 2014 г.). Однако в данном техническом решении использование препарата происходит по прямому назначению, в качестве антикоагулянта для лечения тромбозов, а не на фоне резистентности к другой антикоагулянтной терапии. Отсутствует подбор индивидуальной дозы для лечения и контроль в процессе лечения, что существенно снижает его эффективность.
Дабигатран - непептидный высокоспецифичный ингибитор тромбина. Он взаимодействует как со свободным тромбином, так и с тромбином, связанным с тромбом, обратимо связываясь с активным центром молекулы. Пик концентрации и пик антикоагулянтного действия наступают уже через 30-120 минут. Время полужизни (Т½) после однократного приема составляет 8 часов и 12-17 часов - при регулярном применении [8, 9].
В условиях эксперимента было доказано, что дабигатран значительно снижает образование и генерацию тромбина, снижает уровень TAFI (ингибитора фибринолиза, активируемого тромбином) и тем самым значительно ускоряет лизис сгустка, а также, влияя на тромбин, фиксированный в сгустках, дабигатран в клинически значимых концентрациях снижает активацию фибринстабилизирующего фактора XIII и усиливает восприимчивость плазменных сгустков к t-PA-индуцированному лизису (t-PA - тканевой активатор плазминогена). Таким образом, фибринолитическое действие дабигатрана осуществляется внутри сгустка путем трех механизмов: уменьшения ингибирующего влияния на фибринолиз (ТАФИ - зависимый механизм), ослабления стабилизации (укрепления) сгустка, снижая активность фактора XIII и активируя взаимодействие t-PA с плазминогеном (ТАФИ-независимый механизм) [9].
Дабигатран создавался как препарат, не требующий лабораторного контроля в связи с высокой предсказуемостью его антикоагулянтного эффекта и низким риском кровотечений. Тем не менее, существуют ситуации, когда такой контроль необходим. К ним относятся угрожающие жизни кровотечения, включая внутричерепные кровоизлияния, кровотечения из расширенных вен пищевода при тромбозах портальной системы при передозировке препарата. У каждого пациента существует индивидуальная чувствительность к препарату, что важно не только для профилактики кровотечений, но и для подбора достаточной лечебной (а не профилактической) дозы.
В соответствии с этим авторами поставлена задача, направленная на расширение возможностей способа за счет применения его в особо сложных ситуациях при резистентности к терапии другими антикоагулянтами. Это достигается путем использования препарата дабигатрана «Прадакса», усиливающего тромболитический эндогенный потенциал в индивидуально подобранных дозировках и контроля за адекватностью проводимой терапии.
В качестве прототипа нами выбран способ лечения подострых венозных тромбозов различной локализации, опубликованный в журнале «Флебология», том 4, выпуск 2, №1, 2010 г., стр. 32. Данное техническое решение имеет наибольшее количество сходных существенных признаков с предложенным способом.
Задача, поставленная авторами, достигается тем, что в способе лечения подострых венозных тромбозов различной локализации, включающем проведение антикоагулянтной терапии с начальной дозой препарата, определение целевого уровня показателя эффективности антикоагулянтного действия препарата, подбор индивидуальной лечебной дозы на фоне значений целевого уровня, продолжение лечения с подобранной дозой под контролем целевого уровня и ее коррекцией в сторону увеличения или уменьшения, в случае отклонения целевого уровня, с последующим переходом на профилактические дозы, предложено в качестве антикоагулянта использовать дабигатран «Прадакса», а в качестве показателя эффективности антикоагулянтного действия препарата - тромбиновое время, целевой уровень которого, определенный через 2 часа после приема начальной лечебной дозы препарата в количестве 220-3000 мг в сутки, составляет 100-200 сек, лечение с подобранной дозой осуществляют в течение 2-4 месяцев, поддерживая при этом тромбиновое время на целевом уровне 100-200 сек, а при переходе на профилактические дозы 110-220 мг, тромбиновое время поддерживают на уровне 50-100 сек.
В качестве показателя эффективности антикоагулянтного действия дабигатрана «Прадакса» выбрано тромбиновое время. Тромбиновое время является особенно чувствительным тестом для определения действия препарата. Оно прямо пропорционально концентрации дабигатрана в плазме. Но и этот тест имеет свои ограничения. Он улавливает даже минимальные концентрации дабигатрана, но при высокой концентрации препарата в крови (свыше 600 нг/мл) длительность образования сгустка в кювете коагулометра становится столь долгой, что превышает верхний предел возможности определения [10].
В процессе исследования дабигатрана было установлено, что пик концентрации и пик его антикоагулянтного действия наступают уже через 30-120 минут.
В этой связи, с целью стандартизации, предложено тромбиновое время определять через 2 часа после приема препарата. Эмпирически установлено, что при приеме лечебной дозы препарата 220-300 мг в сутки, через 2 часа показатель целевого уровня тромбинового времени составляет 100-200 сек. Именно при этом значении показателя проявляется максимальный тромболитический эффект дабигатрана, через 2-4 месяца лечения. При показателе тромбинового времени менее 100 сек, снижается тромболитический эффект дабигатрана, а при показателе выше 200 секунд повышается угроза геморрагический осложнений.
В таблице 1 представлены сравнительные данные результатов лечения с помощью известных способов и предложенного способа лечения.
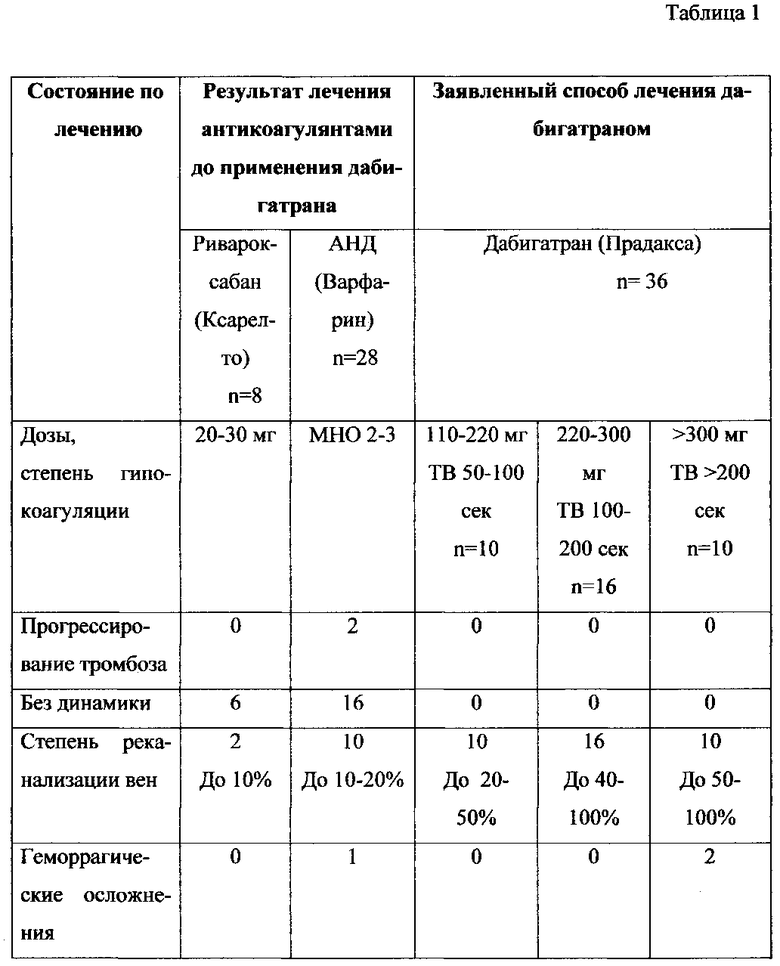
Как видно из табл. 1, лечение антикоагулянтами до назначения препарата дабигатрана (Прадакса) было неэффективно либо приводило к прогрессированию тромбоза, применения препарата «Прадакса» в профилактических дозах не достаточно для регрессии тромбозов, при применении дозы выше заявленной отмечались геморрагические осложнения. В заявляемом способе применение препарата «Прадакса» в лечебных дозах 220-300 мг не вызывает геморрагических осложнений и приводит к хорошей или полной реканализации тромбированных вен. Осуществление способа показано на конкретных примерах.
Пример 1. Пациент Я.А., 38 лет, МО
У пациента в мае 2014 г. состоялся острый тромбоз глубоких вен левой голени (суральные вены, подколенная вена, поверхностная бедренная вена). После проведенного лечения острого тромбоза низкомолекулярным гепарином - клексаном, был назначен варфарин с подбором дозы по показателю MHO, скорректированная доза составила 5 мг, MHO поддерживалось от 1,8-2,5, через 2 месяца в июле 2014 г на фоне терапии варфарином состоялся окклюзионный ЗББВ слева, при увеличении дозы варфарина до 7,5 мг увеличился показатель MHO до 4,5, возникло геморрагическое осложнение - гематурия, что потребовало возвращения на прежние дозы варфарина. Через 1 месяц в августе 2014 г. появились боли в правой нижней конечности, по данным УЗДГ вен нижних конечностей состоялся окклюзионный тромбоз ЗББВ, МБВ справа.
При обследовании у пациента была выявлена генетическая тромбофилия: мутация протромбина F II 20210 GA (het).
УЗДГ вен нижних конечностей от 15.08.2014 г. - Частичная реканализация глубоких вен левой нижней конечности, отсутствие динамики в венах правой нижней конечности.
Учитывая неэффективность терапии варфарином, пациенту был назначен препарат Ривароксабан (ксарелто) 20 мг в день.
Через 2 месяца лечения препаратом Ксарелто проведено исследование УЗДГ вен от 22.10.2014 г. - данных за ретромбоз не получено, сохранялась без динамики частичная реканализация вен левой нижней конечности, отмечалась начальная реканализация в венах правой голени. Учитывая слабую динамику по тромбозу, пациент был переведен на препарат дабигатрана (Прадакса) по 150 мг × 2 раза в день. Был проведен контроль тромбинового времени свертывания через 7 дней от начала приема препарата (анализ проводился через 2 часа после приема дабигатрана (Прадакса), тромбиновое время составило 140 сек). Через месяц приема Прадаксы по данным УЗДГ вен нижних конечностей отмечалась хорошая реканализация вен правой и левой нижних конечностей. Через 2 месяца - хорошая реканализация вен левой нижней конечности, полная реканалация вен справа.
Пациент был переведен на профилактическую дозу дабигатрана (Прадакса) - 110 мг × 2 раза в день, контрольное исследование тромбинового времени составило 80 сек.
Таким образом, у пациента на фоне адекватной терапии варфарином возник рецидив тромбоза, слабая реканализация вен, при увеличении дозы - геморрагическое осложнение, при применении препарата Ксарелто - отсутствие динамики по тромбозу. Применение препарата дабигатрана (Прадакса) в подобранной лечебной дозе через 2 месяца привело к хорошей реканализации вен нижних конечностей слева и к полной реканализации вен справа, при переводе пациента на профилактическую дозу сохранялась положительная динамика.
Пример 2
Пациентка А.Л., 26 лет, г. Москва.
У пациентки в августе 2012 г. на фоне приема комбинированного орального контрацептива состоялся окклюзионный илеофеморальный флеботромбоз справа. Был назначен низкомолекулярный гепарин клексан 80 мг × 2 раза в день, через 3 недели затем пациентка переведена на вафарин 3 таб., MHO составило 2,2-2,8.
В семье у отца и родного брата тромбозы. При исследовании на генетическую тромбофилию выявлен ген фактора V Лейден (гетерозигота). Через 2 месяца лечения варфарином у пациентки не отмечалась положительная динамика по УЗДГ век нижних конечностей. 12.10.2012 г. УЗДГ вен - реканализация подвздошной вены, поверхностной бедренной и глубокой бедренной вены - 10%, подколенной вены - 20%, сохраняется окклюзия ЗББВ и суральных вен.
Пациентка была переведена на прием дабигатрана «Прадакса» 150 мг × 2 раза в день. Проведен контроль тромбинового времени свертывания через 7 дней от начала применения препарата, через 2 часа после приема Прадаксы тромбиновое время составило 250 сек, доза препарата была снижена до 110 мг + 150 мг в день под контролем тромбинового времени, показатель составил 180 сек.
Через 2 месяца применения Прадаксы отмечена положительная динамика по УЗДГ вен нижних конечностей. Данные от 15.11.2012 г - реканализация подвздошной вены, поверхностной бедренной и глубокой бедренной вены - 60%-70%, подколенной вены - 100%, ЗББВ и суральных вен - 70-80%. Пациентке продолжена терапия прежней дозой препарата Прадаксы. Через 2 месяца при контрольном исследовании УЗДГ вен нижних конечностей существенной динамики не отмечено и пациентка переведена на поддерживающую дозу препарата 110 мг × 2 раза в день, тромбиновое время составило 90 сек.
Использование данного способа на практике обеспечит возможность лечения подострых венозных тромбозов различной локализации при резистентности к проводимой антикоагулянтной терапии, а также при лечении тромбозов с возможностью возникновения внутричерепного кровоизлияния, кровотечения из расширенных вен пищевода при тромбозах портальной системы, при передозировке препарата. При этом лечение проводят с индивидуально подобранными дозировками, под постоянным контролем адекватности проводимой терапии, что существенно повысит его эффективность.
ЛИТЕРАТУРА
1. Widmer L.K., Stahelin H.B., Nissen С. et al. Venen-, Arterienkrankheiten, koronare Herzkrankheite bei Berufstatigen: epidemiologische Untersuchung. BaslerStudiel-III 1981; 1959-1978.
2. Silverstein M.D., Heit J.A., Mohr D.N., Petterson T.M., OTallon W.M., Melton L.J. 3rd. Trends in the incidence of deep vein thrombosis and pulmonary embolism: a 25-year population-based study // Arch Intern Med. 1998; Mar 23; 158: 6: 585-93.
3. Nordstrom M., Lindblad В., Bergqvist D., Kjelstrom T. A prospective study of the incidence of deep-vein thrombosis within a defined urban population // J Intern Med. 1992; 232: 155-60.
4. Buller H.R., Agnelli G., Hull R.D., Hyers T.M., Prins M.H., Raskob G.E. Antithrombotic therapy for venous thromboembolic disease: the Seventh ACCP Conference on Antithrombotic and Thrombolytic Therapy // Chest. 2004; 126: 401S-28S.
5. Баркаган З.С. Очерки антитромботической фармакопрофилактики и терапии. - М.: Ньюдиамед, 2000. - 148 с. - стр. 49.
6. Леонтьев С.Г., Золотухин И.А., Селиверстов Е.И., Андрияшкин В.В., Петухов Е.Б. Амбулаторное лечение тромбозов глубоких вен нижних конечностей. - Флебология, 2009, №4, т. 3, стр. 41-44.
7. Савельев B.C., Кириенко А.И., Богачев В.Ю. Хронические заболевания вен в Российской Федерации. Результаты международной исследовательской программы VEIN CONSULT - Флебология, 2010; №3, т. 4, стр. 9-12.
8. W. Wienen, J.M. Stassen, H. Priepke, U.J. Ries and Hauel. Antithrombotic and anticoagulant effects of thrombin ingibitor dabigatran, and its oral prodrug, dabigatran etexilate, in a rabbit model of venous thrombosis // Journal of Thrombosis and Haemostasis, 2007, V. 5, P. 1237-1242.
9. C.T. Ammollo, F. Semeraro, F. Incampo, N. Semeraro and Collucci. Dabigatran enhances clot susceptibility to fibrinolysis by mechaninsms dependent of thrombinactivatable fibrinolysis ingibitor // Journal of Thrombosis and Haemostasis, 2010, V. 8 P. 790-798.
10. Затейщиков Д.А., Зотова И.В. Дабигатран: перспективы клинического применения // Журнал «Фарматека», 2011. №15.
11. Пат. РФ №2530645, кл. A61K 31/4439, публ. 2014 г.
12. Журнал "Флебология", том 4, выпуск 2, №1, 2010 г., стр. 32.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ОСТРЫХ ВЕНОЗНЫХ ТРОМБОЗОВ РАЗЛИЧНОЙ ЛОКАЛИЗАЦИИ НА ФОНЕ ГЕМОРРАГИЧЕСКИХ ОСЛОЖНЕНИЙ | 2012 |
|
RU2477636C1 |
| Способ антикоагулянтной терапии и профилактики тромботических осложнений у пациентов с тяжелым повреждением головного мозга в хроническом критическом состоянии | 2021 |
|
RU2762945C1 |
| СПОСОБ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ РЕЦИДИВА ВЕНОЗНОГО ТРОМБОЗА ПОСЛЕ ПЕРЕНЕСЕННОЙ НОВОЙ КОРОНАВИРУСНОЙ ИНФЕКЦИИ | 2022 |
|
RU2791373C1 |
| Антикоагулянтное лекарственное средство, представляющее собой синтетический дипептид Ac-Trp-Arg-Pip ⋅HCl, фармацевтическая композиция, включающая это антикоагулянтное лекарственное средство | 2019 |
|
RU2712194C1 |
| Способ реканализации латеральных синусов при тромбозах отогенной этиологии у детей | 2020 |
|
RU2758759C1 |
| СПОСОБ НАЗНАЧЕНИЯ ИНДИВИДУАЛЬНОЙ АНТИТРОМБОТИЧЕСКОЙ ТЕРАПИИ В ОСТРЫЙ И РАННИЙ ПЕРИОДЫ ПОЗВОНОЧНО-СПИННОМОЗГОВОЙ ТРАВМЫ ШЕЙНОГО ОТДЕЛА | 2021 |
|
RU2770633C1 |
| СПОСОБ ЛЕЧЕНИЯ ПАЦИЕНТОВ СО СТИХАЮЩИМ ИЛИ СТИХШИМ ТРОМБОФЛЕБИТОМ ПОДКОЖНЫХ ВЕН НИЖНИХ КОНЕЧНОСТЕЙ ПОСЛЕ ПЕРЕНЕСЕННОЙ КОРОНАВИРУСНОЙ ИНФЕКЦИИ COVID-19 | 2024 |
|
RU2825065C1 |
| СПОСОБ ПРОФИЛАКТИКИ КРОВОТЕЧЕНИЙ, ВЫЗВАННЫХ ПРИМЕНЕНИЕМ ДАБИГАТРАНА ЭТЕКСИЛАТА, В ЭКСПЕРИМЕНТЕ | 2013 |
|
RU2552331C1 |
| ПЕРСОНАЛИЗИРОВАННЫЙ СПОСОБ ЛЕЧЕНИЯ ТРОМБОЗА ВЕН НИЖНИХ КОНЕЧНОСТЕЙ У РАНЕНЫХ | 2023 |
|
RU2813947C1 |
| СПОСОБ ТРОМБЭКТОМИИ ИЗ НИЖНЕЙ ПОЛОЙ ВЕНЫ ПРИ ОСТРЫХ ВОСХОДЯЩИХ ФЛОТИРУЮЩИХ КАВАЛЬНЫХ ТРОМБОЗАХ | 2020 |
|
RU2746606C1 |
Изобретение относится к медицине, а именно к коагулогии, и касается лечения подострых венозных тромбозов различной локализации. Для этого вводят препарат дабигатрана «Парадакса» в индивидуально подобранной дозе, которую определяют как обеспечивающую через 2 часа после введения уровень тромбинового времени 100-200 секунд. Лечение осуществляют в течение 2-4 месяцев, поддерживая указанный уровень тромбинового времени. Затем переходят на профилактические дозы, обеспечивающие тромбиновое время 50-100 секунд. Способ обеспечивает эффективное лечение подострых венозных тромбозов различной локализации, в том числе при резистентности к антикоагулянтной терапии, проводимой другими известными способами, за счет индивидуального подбора эффективных доз препарата. 1 табл., 2 пр.
Способ лечения подострых венозных тромбозов различной локализации, включающий проведение антикоагулянтной терапии с начальной дозой препарата, определение целевого уровня показателя эффективности антикоагулянтного действия препарата, подбор индивидуальной лечебной дозы на фоне значений целевого уровня, продолжение лечения с подобранной дозой под контролем целевого уровня и ее коррекцией в сторону увеличения или уменьшения в случае отклонения целевого уровня, с последующим переходом на профилактические дозы, отличающийся тем, что в качестве антикоагулянта используют дабигатран «Прадакса», а в качестве показателя эффективности антикоагулянтного действия препарата - тромбиновое время, целевой уровень которого, определенный через 2 часа после приема начальной лечебной дозы препарата в количестве 220-300 мг в сутки, составляет 100-200 сек, лечение с подобранной терапевтической дозой осуществляют в течение 2-4 месяцев, поддерживая при этом тромбиновое временя на целевом уровне 100-200 сек, а при переходе на профилактические дозы 110-220 мг в сутки тромбиновое время поддерживают на уровне 50-100 сек.
| СПОСОБ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ ТРОМБОЗА С ИСПОЛЬЗОВАНИЕМ ЭТЕКСИЛАТА ДАБИГАТРАНА ИЛИ ЕГО СОЛИ С УЛУЧШЕННОЙ ЭФФЕКТИВНОСТЬЮ ПО СРАВНЕНИЮ СО СТАНДАРТНЫМ ЛЕЧЕНИЕМ ВАРФАРИНОМ | 2009 |
|
RU2530645C2 |
| CN 103554087 A 05.02.2014 | |||
| ЗАТЕЙЩИКОВ Д.А | |||
| и др | |||
| "Дабигатран: перпспективы клинического применения" Фарматека, 2011, найдено 11.12.2015, найдено из интернет: http://www.pharmateca.ru/ru/archive/article/8262 | |||
| ANTONIJEVIC N et al | |||
| " Contribution of novel anticoagulants fondaparinux and dabigatran to venous thromboembolism | |||
Авторы
Даты
2016-08-20—Публикация
2015-05-18—Подача