Данная заявка заявляет приоритет предварительной заявки на патент США: US provisional patent application serial no. 61/167984, поданной 9 апреля 2009 г., предварительной заявки на патент США: US provisional patent application serial no. 61/308667, поданной 26 февраля 2010 г., предварительной заявки на патент США: US provisional patent application serial no. 61/309091, поданной 1 марта 2010 г., каждая из которых, таким образом, включена путем ссылки в полном своем объеме.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
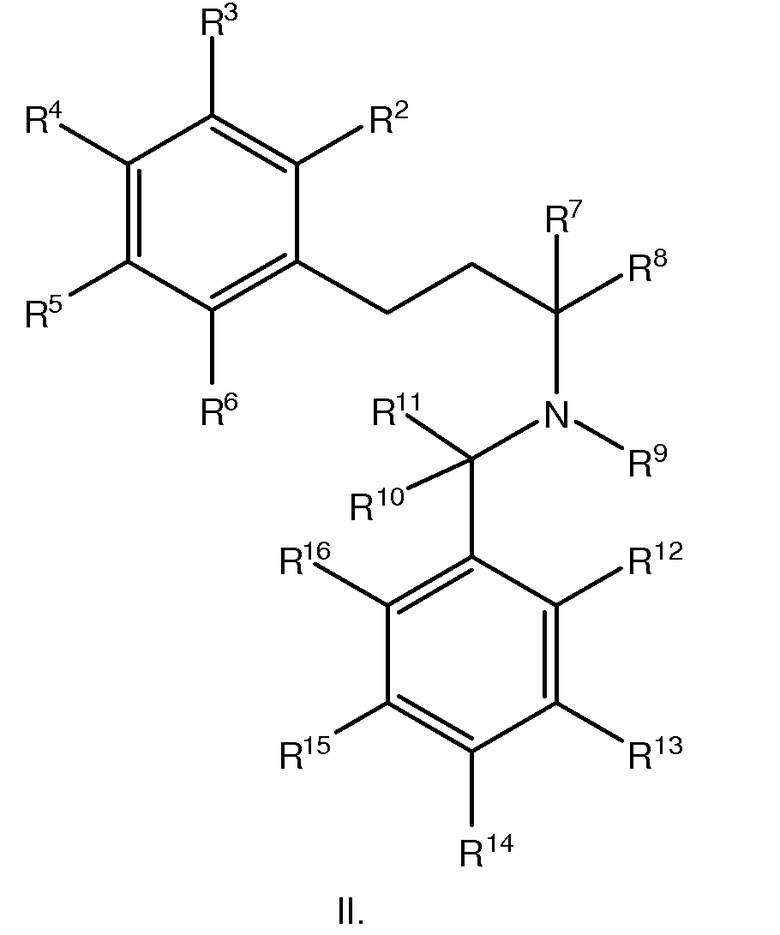
Настоящее изобретение обеспечивает, наряду с прочим, соединения формулы I, II, или III:
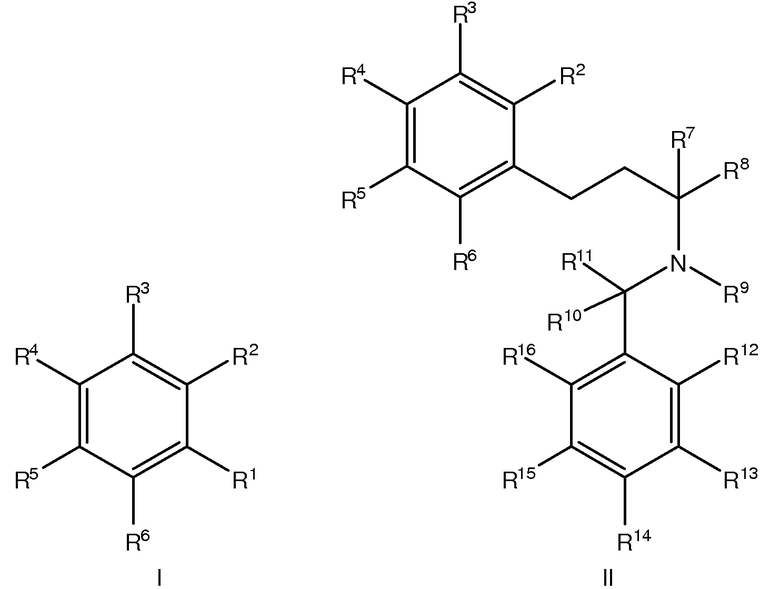
или их фармацевтически приемлемые соли, где составляющие группы этих солей представлены ниже.
Настоящее изобретение дополнительно обеспечивает фармацевтические композиции, содержащие соединение Формулы I, II, или III, или его фармацевтически приемлемую соль, и, по меньшей мере, один фармацевтически приемлемый носитель.
Настоящее изобретение дополнительно обеспечивает способы ингибирования, лечения, и/или подавления снижения когнитивных способностей и/или болезни Альцгеймера посредством соединения формулы I, II, или III, или его фармацевтически приемлемой соли.
Настоящее изобретение дополнительно обеспечивает способы ингибирования, лечения, или подавления снижения когнитивных способностей посредством соединения формулы I, II, или III, или его фармацевтически приемлемой соли.
Настоящее изобретение дополнительно обеспечивает способы ингибирования, лечения, или подавления одного или более процессов, включающих продуцирование амилоида, скопление амилоида, агрегацию амилоида, связывание амилоида (с клетками в мозге, такими как нервные клетки), активность/действие Абета-олигомеров на нейроны и отложение амилоида (на клетках в мозге, таких как нервные клетки), посредством соединения формулы I, II, или III, или его фармацевтически приемлемой соли.
Настоящее изобретение дополнительно обеспечивает соединения формулы I, II, или III, или их фармацевтически приемлемые соли, для применения в терапии.
Настоящее изобретение дополнительно обеспечивает применение соединений формулы I, II, или III, или их фармацевтически приемлемых солей, для изготовления/получения лекарственного препарата для применения в терапии.
В некоторых вариантах осуществления, обеспечивают способы получения соединений, полезных в ингибировании, лечении, или подавлении снижения когнитивных способностей. В способе «химическая обработка с сохранением действующих начал растений», некоторые соединения настоящего изобретения получают из соединений природного происхождения, таких как соединения, обнаруженные в лекарственных растениях, подобных имбирю. Процесс химической обработки с сохранением действующих начал растений, описанный в этом документе, применим к большому ряду биологических экстрактов и может быть использован для создания набора соединений для скрининга потенциальных кандидатов в новое лекарственное средство. Кроме того, как правило, соединения, полученные посредством процесса химической обработки с сохранением действующих начал растений, являются химически стабильными и структурно разнообразными, и хорошими кандидатами для применения в скринингах лекарственного средства на предмет фармацевтической активности. В некоторых вариантах осуществления, обеспечивают соединения, полученные из имбирного масла. В соответствии с некоторыми вариантами осуществления изобретения, обеспечивают соединения, полученные из имбирного масла посредством процесса химической обработки с сохранением действующих начал растений, описанного в этом документе. В другом варианте осуществления, изобретение обеспечивает способ приготовления набора химических соединений из имбирного масла.
В некоторых вариантах осуществления, соединения настоящего изобретения ингибируют, лечат, или подавляют (частично ингибируют) связывание амилоида (включая Абета-олигомеры) с нейронами (такими как нейроны в мозге) и являются полезными для ингибирования, лечения, и подавления снижения когнитивных способностей и/или болезни Альцгеймера. В некоторых вариантах осуществления, соединения настоящего изобретения ингибируют, лечат, или подавляют один или более процессов, включающих агрегацию амилоида, связывание амилоида и отложение амилоида. В некоторых вариантах осуществления, соединения настоящего изобретения ингибируют, лечат или подавляют агрегацию амилоида. В некоторых вариантах осуществления, соединения настоящего изобретения ингибируют, лечат или подавляют связывание амилоида. В некоторых вариантах осуществления, соединения настоящего изобретения ингибируют, лечат или подавляют отложение амилоида. В некоторых вариантах осуществления, соединения настоящего изобретения ингибируют, лечат или подавляют активность/действие Абета-олигомеров на нейроны. В некоторых вариантах осуществления, соединения показывают активность в анализе активности бета-секретазы и являются потенциально полезными в ингибировании, лечении, и подавлении снижения когнитивных способностей и болезни Альцгеймера. В некоторых вариантах осуществления, производное имбирного масла представляет собой соединение в очищенном и выделенном виде (например, со степенью чистоты более, чем 80%, 85%, 90%, 95%, 98%, или 99% по массе). Соединения и способы, описанные в этом документе, могут быть использованы для лечения одного или более симптомов снижения когнитивных способностей и/или болезни Альцгеймера, таких как потеря памяти, спутанность сознания (дезориентация во времени и в пространстве), помутнение сознания, изменение личности, дезориентация, и потеря языковых навыков и умений. Кроме того, соединения и способы, описанные в этом документе, могут быть полезными в ингибировании, лечении, и/или подавлении снижения когнитивных способностей и/или болезни Альцгеймера путем восстановления долговременной потенциации синаптической передачи, и/или ингибирования, лечения, или подавления одного или обоих процессов, включающих нейродегенерацию и общий амилоидоз, более конкретно, путем ингибирования, лечения, или подавления одного или более процессов, включающих продуцирование амилоида, скопление амилоида, агрегацию амилоида, связывание амилоида, и отложение амилоида.
ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг.1 показывает результаты МТТ-теста (анализ на основе 3-{4,5-диметилтиазол-2-ил}-2,5-дифенилтетразолий бромида) в присутствии и в отсутствии продукта процессинга белка-предшественника амилоида.
Фиг.2 показывает ингибирование эффекта мембранного трафика, опосредованного продуктом процессинга белка-предшественника амилоида, посредством образца соединения 2.
Фиг.3 показывает ингибирование действия продукта процессинга белка-предшественника амилоида в отношении потери памяти посредством образца соединения 2.
Фиг.4 показывает ингибирование действия Абета-скоплений, выделенных из пациентов, страдающих болезнью Альцгеймера, в отношении мембранного трафика посредством образца соединения 2.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Снижение когнитивных способностей, такое как потеря памяти, помутнение сознания, изменения личности, дезориентация, и потеря языковых навыков и умений, происходит у большинства населения по мере старения, в различной степени. Наиболее распространенной, тяжелой и необратимой формой снижения когнитивных способностей является болезнь Альцгеймера, которая, в настоящее время, всегда является летальной.
Симптомы снижения когнитивных способностей и болезни Альцгеймера, как полагают, обуславливаются образованием амилоидных бляшек и нейрофибриллярных клубков, которые, как полагают, вносят вклад в деградацию нейронов (нервных клеток) в мозге и в последующее появление симптомов. Амилоид представляет собой общий термин для фрагментов белка, которые обычно вырабатывает организм. Бета-амилоид представляет собой фрагмент белка, который отрезается от другого белка, называемого как белок-предшественник амилоида (APP). В здоровом мозге, фрагменты белка бета-амилоида разрушаются и удаляются. У субъектов, страдающих болезнью Альцгеймера и другими формами снижения когнитивных способностей, фрагменты аккумулируются с образованием твердых, нерастворимых бляшек. Нейрофибриллярные клубки представляют собой нерастворимые скрученные волокна, которые обнаружены внутри клеток мозга. Белок, содержащийся в нейрофибриллярных клубках, то есть, тау-протеин, образует микротрубочку, которая помогает транспортировать питательные вещества и другие важные вещества из одной части нервной клетки в другую часть. При наличии болезни Альцгеймера тау-протеин является аномальным, и структуры микротрубочек схлопываются/спадают.
Бета-секретаза представляет собой фермент в мозге человека, ответственный за продуцирование бета-амилоида, патогенного вещества, ответственного за образование бляшек и клубков в мозге человека, страдающего болезнью Альцгеймера. Также полагают, что Бета-амилоид и его олигомеры (олигомеры бета-амилоида или Абета-олигомеры) являются ответственными за снижение когнитивных способностей на ранней стадии заболевания мозга человека, находящегося в доклинической стадии болезни Альцгеймера. Ожидают, что ингибирование бета-секретазы могло бы снижать массу бета-амилоида в мозге и, таким образом, сбавлять снижение когнитивных способностей, блокировать образование олигомеров амилоида, образование бляшек и клубков, останавливать нейродегенерацию, и потенциально лечить умеренные когнитивные нарушения и более тяжелые формы когнитивного нарушения, такие как болезнь Альцгеймера.
Гингеролы представляют собой ряд природных небольших молекул, выделенных из имбиря, Zingiber officinale, и классифицируются в соответствии с длиной их алкильной цепи, например [6]-гингерол, [8]-гингерол. Гингеролы, как известно, являются относительно нестабильными в условиях как химической среды, так и биологической среды, и образуют неактивные вещества. Например, бета-гидроксикарбонильная функциональная группа гингеролов подвержена окислению или дегидратации с образованием неактивных продуктов, и гингеролы в особенности склонны к быстрой дегидратации в кислотных условиях, так что даже чистое вещество трудно хранить в течение длительных периодов времени. В соответствии с вышеизложенным, простое пероральное введение дозы гингеролов для лечебного действия не могло бы быть возможным вследствие кислотной среды желудка и верхнего отдела кишечного тракта. Кроме того, химическая и биологическая нестабильность, вероятно, также является серьезной проблемой для введения внутривенных доз. В связи с этим, существует сильная потребность в обнаружении ингибиторов снижения когнитивных способностей, и, в особенности, соединений, которые являются полезными в лечении и в подавлении снижения когнитивных способностей и болезни Альцгеймера, посредством способов, таких как ингибирование продуцирования амилоида (включая Абета-олигомеры), агрегации амилоида (включая Абета-олигомеры), и/или отложения амилоида (включая Абета-олигомеры) (то есть, образования бляшек), ингибирование нейродегенерации, и/или восстановление долговременной потенциации синаптической передачи, и/или ингибирование активности/действия Абета-олигомеров на нейроны. Также существует потребность в ингибиторах снижения когнитивных способностей, которые являются химически и биологически стабильными.
Растения привлекли к себе сравнительно небольшое внимание в качестве потенциально ценных источников для обнаружения лекарственного средства в области снижения когнитивных способностей и болезни Альцгеймера. Применение растительных экстрактов для получения неприродных производных соединений, представляющих интерес в качестве лекарственного препарата, как правило, не используется. В соответствии с этим, также существует потребность в способе получения соединений, представляющих интерес в качестве лекарственного препарата, из растительных экстрактов и экстрактов из других биологических источников. В частности, также существует потребность в получении и в идентифицировании соединений, извлеченных из растительных экстрактов, которые являются полезными в лечении и в подавлении снижения когнитивных способностей и болезни Альцгеймера.
Соединения, композиции, и способы, описанные в этом документе, направлены на удовлетворение этих потребностей и на достижение других целей.
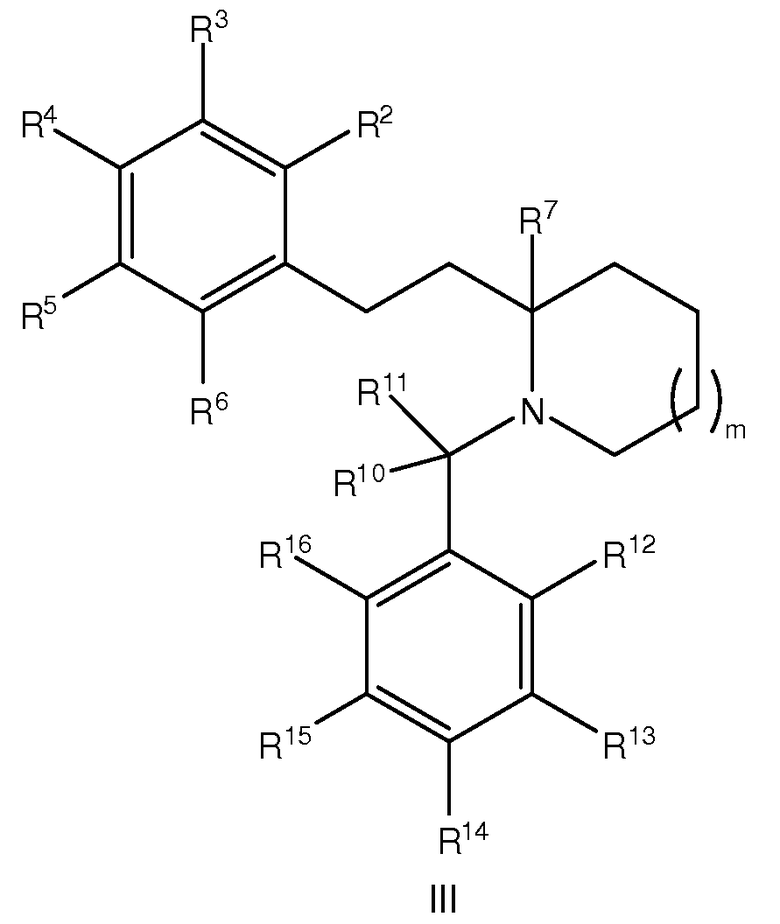
Варианты осуществления настоящего изобретения обеспечивают, в числе прочих, соединения формулы I:
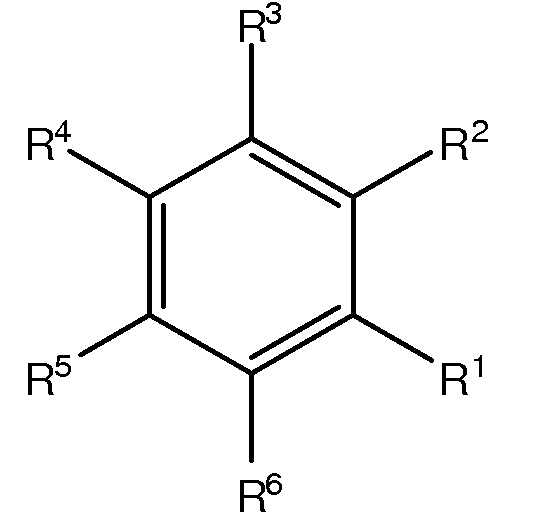
или их фармацевтически приемлемые соли, где:
R1 выбирают из (А1) и (А2):
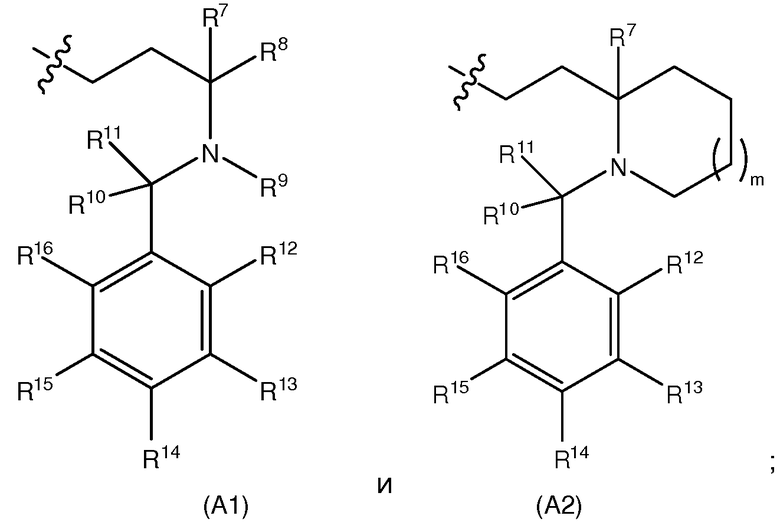
R2, R3, R4, R5, и R6, каждый, независимо, выбирают из Н, ОН, С1-6алкоксигруппы, С1-6галогеналкоксигруппы, галогена, CN, NO2, C1-6алкила, С1-6галогеналкила, С3-7циклоалкила, NH2, NH(C1-4алкил), NH(C3-7циклоалкил), N(C1-4алкил)2, NHC(O)(C1-4алкил), SH, S(C1-6алкил), C(O)ORa, C(O)Rb, C(O)NRcRd, OC(O)Rb, OC(O)NRcRd, NRcRd, NRcC(O)Rb, NRcC(O)ORa, NRcS(O)2Rb, NRcS(O)2NRcRd, S(O)Rb, S(O)2Rb, и S(O)2NRcRd;
R7 представляет собой Н, C1-6алкил, С1-6галогеналкил, или С3-7циклоалкил;
R8 представляет собой C1-6алкил, С1-6галогеналкил, или С3-7циклоалкил;
R9 представляет собой Н, C1-6алкил, С1-6галогеналкил, или С3-7циклоалкил;
R10 представляет собой Н, C1-6алкил, С1-6галогеналкил, или С3-7циклоалкил;
R11 представляет собой Н, C1-6алкил, С1-6галогеналкил, или С3-7циклоалкил;
R12, R13, R14, R15, и R16, каждый, независимо, выбирают из Н, ОН, С1-6алкоксигруппы, С1-6галогеналкоксигруппы, галогена, CN, NO2, C1-6алкила, С1-6галогеналкила, С3-7циклоалкила, NH2, NH(C1-4алкил), NH(C3-7циклоалкил), N(C1-4алкил)2, NHC(O)(C1-4алкил), SH, S(C1-6алкил), C(O)ORa1, C(O)Rb1, C(O)NRc1Rd1, OC(O)Rb1, OC(O)NRc1Rd1, NRc1Rd1, NRc1C(O)Rb1, NRc1C(O)ORa1, NRc1S(O)2Rb1, NRc1S(O)2NRc1Rd1, S(O)Rb1, S(O)2Rb1, и S(O)2NRc1Rd1;
каждый Ra независимо выбирают из Н, C1-6алкила, С1-6галогеналкила, арилалкила, гетероарилалкила, циклоалкилалкила, гетероциклоалкилалкила, C2-6алкенила, C2-6алкинила, арила, циклоалкила, гетероарила и гетероциклоалкила, где каждый заместитель из группы, включающей C1-6алкил, С1-6галогеналкил, арилалкил, гетероарилалкил, циклоалкилалкил, гетероциклоалкилалкил, C2-6алкенил, C2-6алкинил, арил, циклоалкил, гетероарил и гетероциклоалкил, необязательно замещен 1, 2, 3, 4 или 5 заместителями, независимо выбранными из ОН, CN, аминогруппы, галогена, C1-6алкила, С1-6галогеналкила, С1-6алкоксигруппы, С1-6галогеналкоксигруппы, арила, арилалкила, гетероарила, гетероарилалкила, циклоалкила и гетероциклоалкила;
каждый Rb независимо выбирают из Н, C1-6алкила, С1-6галогеналкила, арилалкила, гетероарилалкила, циклоалкилалкила, гетероциклоалкилалкила, C2-6алкенила, C2-6алкинила, арила, циклоалкила, гетероарила, гетероциклоалкила, арилалкила, гетероарилалкила, циклоалкилалкила и гетероциклоалкилалкила, где каждый заместитель из группы, включающей C1-6алкил, С1-6галогеналкил, арилалкил, гетероарилалкил, циклоалкилалкил, гетероциклоалкилалкил, C2-6алкенил, C2-6алкинил, арил, циклоалкил, гетероарил, гетероциклоалкил, арилалкил, гетероарилалкил, циклоалкилалкил и гетероциклоалкилалкил, необязательно замещен 1, 2, 3, 4 или 5 заместителями, независимо выбранными из ОН, аминогруппы, галогена, C1-6алкила, С1-6галогеналкила, С1-6алкоксигруппы, С1-6галогеналкоксигруппы, арила, арилалкила, гетероарила, гетероарилалкила, циклоалкила и гетероциклоалкила;
Rc и Rd независимо выбирают из Н, C1-6алкила, С1-6галогеналкила, арилалкила, гетероарилалкила, циклоалкилалкила, гетероциклоалкилалкила, C2-6алкенила, C2-6алкинила, арила, гетероарила, циклоалкила, гетероциклоалкила, арилалкила, гетероарилалкила, циклоалкилалкила и гетероциклоалкилалкила, где каждый заместитель из группы, включающей C1-6алкил, С1-6галогеналкил, арилалкил, гетероарилалкил, циклоалкилалкил, гетероциклоалкилалкил, C2-6алкенил, C2-6алкинил, арил, гетероарил, циклоалкил, гетероциклоалкил, арилалкил, гетероарилалкил, циклоалкилалкил и гетероциклоалкилалкил, необязательно замещен 1, 2, 3, 4 или 5 заместителями, независимо выбранными из ОН, аминогруппы, галогена, C1-6алкила, С1-6галогеналкила, С1-6алкоксигруппы, С1-6галогеналкоксигруппы, арила, арилалкила, гетероарила, гетероарилалкила, циклоалкила и гетероциклоалкила;
или Rc и Rd вместе с атомом N, к которому они присоединены, образуют 4-, 5-, 6- или 7-членную гетероциклоалкильную группу, которая необязательно замещена 1, 2, 3, 4 или 5 заместителями, независимо выбранными из ОН, аминогруппы, галогена, C1-6алкила, С1-6галогеналкила, С1-6алкоксигруппы, С1-6галогеналкоксигруппы, арила, арилалкила, гетероарила, гетероарилалкила, циклоалкила и гетероциклоалкила;
каждый Ra1 независимо выбирают из Н, С1-6алкила, С1-6галогеналкила, арилалкила, гетероарилалкила, циклоалкилалкила, гетероциклоалкилалкила, C2-6алкенила, C2-6алкинила, арила, циклоалкила, гетероарила и гетероциклоалкила, где каждый заместитель из группы, включающей С1-6алкил, С1-6галогеналкил, арилалкил, гетероарилалкил, циклоалкилалкил, гетероциклоалкилалкил, C2-6алкенил, C2-6алкинил, арил, циклоалкил, гетероарил и гетероциклоалкил, необязательно замещен 1, 2, 3, 4 или 5 заместителями, независимо выбранными из ОН, CN, аминогруппы, галогена, C1-6алкила, С1-6галогеналкила, С1-6алкоксигруппы, С1-6галогеналкоксигруппы, арила, арилалкила, гетероарила, гетероарилалкила, циклоалкила, и гетероциклоалкила;
каждый Rb1 независимо выбирают из Н, С1-6алкила, С1-6галогеналкила, арилалкила, гетероарилалкила, циклоалкилалкила, гетероциклоалкилалкила, C2-6алкенила, C2-6алкинила, арила, циклоалкила, гетероарила, гетероциклоалкила, арилалкила, гетероарилалкила, циклоалкилалкила и гетероциклоалкилалкила, где каждый заместитель из группы, включающей С1-6алкил, С1-6галогеналкил, арилалкил, гетероарилалкил, циклоалкилалкил, гетероциклоалкилалкил, C2-6алкенил, C2-6алкинил, арил, циклоалкил, гетероарил, гетероциклоалкил, арилалкил, гетероарилалкил, циклоалкилалкил и гетероциклоалкилалкил, необязательно замещен 1, 2, 3, 4 или 5 заместителями, независимо выбранными из ОН, аминогруппы, галогена, C1-6алкила, С1-6галогеналкила, С1-6алкоксигруппы, С1-6галогеналкоксигруппы, арила, арилалкила, гетероарила, гетероарилалкила, циклоалкила и гетероциклоалкила;
Rc1 и Rd2 независимо выбирают из Н, С1-6алкила, С1-6галогеналкила, арилалкила, гетероарилалкила, циклоалкилалкила, гетероциклоалкилалкила, C2-6алкенила, C2-6алкинила, арила, гетероарила, циклоалкила, гетероциклоалкила, арилалкила, гетероарилалкила, циклоалкилалкила и гетероциклоалкилалкила, где каждый заместитель из группы, включающей С1-6алкил, С1-6галогеналкил, арилалкил, гетероарилалкил, циклоалкилалкил, гетероциклоалкилалкил, C2-6алкенил, C2-6алкинил, арил, гетероарил, циклоалкил, гетероциклоалкил, арилалкил, гетероарилалкил, циклоалкилалкил и гетероциклоалкилалкил, необязательно замещен 1, 2, 3, 4 или 5 заместителями, независимо выбранными из ОН, аминогруппы, галогена, C1-6алкила, С1-6галогеналкила, С1-6алкоксигруппы, С1-6галогеналкоксигруппы, арила, арилалкила, гетероарила, гетероарилалкила, циклоалкила, и гетероциклоалкила;
или Rc1 и Rd1 вместе с атомом N, к которому они присоединены, образуют 4-, 5-, 6- или 7-членную гетероциклоалкильную группу, которая необязательно замещена 1, 2, 3, 4 или 5 заместителями, независимо выбранными из ОН, аминогруппы, галогена, C1-6алкила, С1-6галогеналкила, С1-6алкоксигруппы, С1-6галогеналкоксигруппы, арила, арилалкила, гетероарила, гетероарилалкила, циклоалкила и гетероциклоалкила; и
m имеет значение 0, 1, или 2.
В некоторых вариантах осуществления, в том случае, когда R1 представляет собой фрагмент группы (A1), тогда два заместителя из группы, включающей R2, R3, R4, R5, и R6, независимо выбирают из ОН, С1-6алкоксигруппы, и С1-6галогеналкоксигруппы.
В некоторых вариантах осуществления, в том случае, когда R1 представляет собой фрагмент группы (A1), тогда, по меньшей мере, один заместитель из группы, включающей R12, R13, R14, R15 и R16, является отличным от Н.
В некоторых вариантах осуществления, два заместителя из группы, включающей R2, R3, R4, R5, и R6, независимо выбирают из ОН, С1-6алкоксигруппы, и С1-6галогеналкоксигруппы. В некоторых дополнительных вариантах осуществления, каждый из оставшихся заместителей из группы, включающей R2, R3, R4, R5 и R6, представляет собой Н.
В некоторых вариантах осуществления, R2, R3, R4, R5 и R6, каждый, независимо выбирают из Н, ОН, С1-6алкоксигруппы, С1-6галогеналкоксигруппы, галогена, CN, NO2, C1-6алкила, С1-6галогеналкила, С3-7циклоалкила, NH2, NH(C1-4алкил), NH(C3-7циклоалкил), N(C1-4алкил)2, NHC(O)(C1-4алкил), SH, S(C1-6алкил), C(O)OH, C(O)О(С1-4алкил), C(O)(С1-4алкил) и C(O)NH(С1-4алкил).
В некоторых вариантах осуществления, один заместитель из группы, включающей R2, R3, R4, R5, и R6, представляет собой ОН; и один заместитель из группы, включающей R2, R3, R4, R5 и R6, представляет собой ОН, С1-6алкоксигруппу, или С1-6галогеналкоксигруппу. В некоторых дополнительных вариантах осуществления, каждый из оставшихся заместителей из группы, включающей R2, R3, R4, R5 и R6, представляет собой Н.
В некоторых вариантах осуществления, один заместитель из группы, включающей R2, R3, R4, R5, и R6, представляет собой ОН; и один заместитель из группы, включающей R2, R3, R4, R5, и R6, представляет собой ОН, С1-6алкоксигруппу, или С1-6галогеналкоксигруппу. В некоторых дополнительных вариантах осуществления, каждый из оставшихся заместителей из группы, включающей R2, R3, R4, R5, и R6, представляет собой Н.
В некоторых дополнительных вариантах осуществления, один заместитель из группы, включающей R2, R3, R4, R5 и R6, представляет собой ОН; и один заместитель из группы, включающей R2, R3, R4, R5 и R6, представляет собой метоксигруппу, или тригалогенметоксигруппу (в некоторых дополнительных вариантах осуществления, каждый из оставшихся заместителей из группы, включающей R2, R3, R4, R5 и R6, представляет собой H). В других дополнительных вариантах осуществления, один заместитель из группы, включающей R2, R3, R4, R5 и R6, представляет собой ОН; и один заместитель из группы, включающей R2, R3, R4, R5 и R6, представляет собой метоксигруппу (в некоторых дополнительных вариантах осуществления, каждый из оставшихся заместителей из группы, включающей R2, R3, R4, R5 и R6, представляет собой H).
В некоторых вариантах осуществления, R4 представляет собой ОН; и R5 представляет собой метоксигруппу. В некоторых дополнительных вариантах осуществления, R4 представляет собой ОН; и R5 представляет собой метоксигруппу; и R2, R3 и R6 представляют собой, каждый, Н.
В некоторых вариантах осуществления, R7 представляет собой Н или С1-6алкил. В некоторых дополнительных вариантах осуществления, R7 представляет собой Н или С1-3алкил.
В некоторых вариантах осуществления, R7 представляет собой С1-3алкил. В некоторых дополнительных вариантах осуществления, R7 представляет собой метил или этил. В других дополнительных вариантах осуществления, R7 представляет собой метил.
В некоторых дополнительных вариантах осуществления, R7 представляет собой Н.
В некоторых вариантах осуществления, R8 представляет собой С1-6алкил. В некоторых дополнительных вариантах осуществления, R8 представляет собой С1-3алкил. В других дополнительных вариантах осуществления, R8 представляет собой метил.
В некоторых вариантах осуществления, R9 представляет собой Н или С1-6алкил. В некоторых дополнительных вариантах осуществления, R9 представляет собой Н или С1-3алкил.
В некоторых вариантах осуществления, R9 представляет собой Н.
В некоторых вариантах осуществления, R9 представляет собой С1-3алкил.
В некоторых вариантах осуществления, R10 представляет собой Н или С1-6алкил. В некоторых дополнительных вариантах осуществления, R10 представляет собой Н или С1-3алкил. В других дополнительных вариантах осуществления, R10 представляет собой Н. В других вариантах осуществления, R10 представляет собой С1-3алкил.
В некоторых вариантах осуществления, R11 представляет собой Н или С1-6алкил. В некоторых дополнительных вариантах осуществления, R11 представляет собой Н или С1-3алкил. В других дополнительных вариантах осуществления, R11 представляет собой Н. В других вариантах осуществления, R11 представляет собой С1-3алкил.
В некоторых вариантах осуществления, по меньшей мере, один из заместителей из группы, включающей R12, R13, R14, R15 и R16, является отличным от Н.
В некоторых вариантах осуществления, R12, R13, R14, R15 и R16, каждый, независимо, выбирают из Н, ОН, С1-6алкоксигруппы, С1-6галогеналкоксигруппы, галогена, CN, NO2, C1-6алкила, С1-6галогеналкила, С3-7циклоалкила, NH2, NH(C1-4алкил), NH(C3-7циклоалкил), N(C1-4алкил)2, NHC(O)(C1-4алкил), SH, S(C1-6алкил), C(O)OH, C(O)О(С1-4алкил), C(O)(С1-4алкил), и C(O)NH(С1-4алкил).
В некоторых вариантах осуществления, R12, R13, R14, R15 и R16, каждый, независимо, выбирают из Н, галогена, CN, NO2, C1-6алкила, С1-6галогеналкила, С3-7циклоалкила, C(O)О(С1-4алкил), C(O)(С1-4алкил), и C(O)NH(С1-4алкил).
В некоторых вариантах осуществления, по меньшей мере, один из заместителей из группы, включающей R12, R13, R14, R15 и R16, выбирают из галогена, CN, NO2, С1-6галогеналкила, C(O)О(С1-4алкил), C(O)(С1-4алкил), и C(O)NH(С1-4алкил).
В некоторых вариантах осуществления, по меньшей мере, один из заместителей из группы, включающей R12, R13, R14, R15 и R16, выбирают из галогена и С1-6галогеналкила. В некоторых дополнительных вариантах осуществления, по меньшей мере, один из заместителей из группы, включающей R12, R13, R14, R15 и R16, выбирают из галогена и С1-6галогеналкила, и каждый из оставшихся в группе, включающей R12, R13, R14, R15 и R16, представляет собой Н. В других дополнительных вариантах осуществления, один или два заместителя из группы, включающей R12, R13, R14, R15 и R16, выбирают из галогена и С1-6галогеналкила, и каждый из оставшихся в группе, включающей R12, R13, R14, R15 и R16, представляет собой Н. В еще одних дополнительных вариантах осуществления, один заместитель из группы, включающей R12, R13, R14, R15 и R16, выбирают из галогена и С1-6галогеналкила, а каждый из оставшихся в группе, включающей R12, R13, R14, R15 и R16, представляет собой Н.
В некоторых вариантах осуществления, R14 представляет собой галоген или С1-6галогеналкил (в некоторых дополнительных вариантах осуществления, каждый из группы, включающей R12, R13, R15 и R16, представляет собой H). В некоторых дополнительных вариантах осуществления, R14 представляет собой галоген или С1-3галогеналкил (в некоторых дополнительных вариантах осуществления, каждый из группы, включающей R12, R13, R15 и R16, представляет собой H). В других дополнительных вариантах осуществления, R14 представляет собой галоген или С1галогеналкил (в некоторых дополнительных вариантах осуществления, каждый из группы, включающей R12, R13, R15 и R16, представляет собой H).
В некоторых вариантах осуществления, R14 представляет собой галоген (в некоторых дополнительных вариантах осуществления, каждый из группы, включающей R12, R13, R15 и R16, представляет собой H). В некоторых вариантах осуществления, R14 представляет собой Cl или F. В некоторых вариантах осуществления, R14 представляет собой Cl. В некоторых вариантах осуществления, R14 представляет собой F.
В некоторых вариантах осуществления, R14 представляет собой С1-6галогеналкил (в некоторых дополнительных вариантах осуществления, каждый из группы, включающей R12, R13, R15 и R16, представляет собой H). В некоторых дополнительных вариантах осуществления, R14 представляет собой С1-3галогеналкил. В других дополнительных вариантах осуществления, R14 представляет собой С1галогеналкил. В еще одних дополнительных вариантах осуществления, R14 представляет собой CF3.
В некоторых вариантах осуществления, R15 представляет собой галоген или С1-6галогеналкил (в некоторых дополнительных вариантах осуществления, каждый из группы, включающей R12, R13, R14 и R16, представляет собой H). В некоторых дополнительных вариантах осуществления, R15 представляет собой галоген или С1-3галогеналкил (в некоторых дополнительных вариантах осуществления, каждый из группы, включающей R12, R13, R14 и R16, представляет собой H). В других дополнительных вариантах осуществления, R15 представляет собой галоген или С1галогеналкил (в некоторых дополнительных вариантах осуществления, каждый из группы, включающей R12, R13, R14 и R16, представляет собой H).
В некоторых вариантах осуществления, R15 представляет собой галоген. В некоторых вариантах осуществления, R15 представляет собой Cl или F. В некоторых вариантах осуществления, R15 представляет собой Cl. В некоторых вариантах осуществления, R15 представляет собой F.
В некоторых вариантах осуществления, R15 представляет собой С1-6галогеналкил. В некоторых дополнительных вариантах осуществления, R15 представляет собой С1-3галогеналкил. В других дополнительных вариантах осуществления, R15 представляет собой С1галогеналкил. В еще одних дополнительных вариантах осуществления, R15 представляет собой CF3.
В некоторых вариантах осуществления, R14 и R15 представляют собой, каждый независимо, галоген или С1-3галогеналкил (в некоторых дополнительных вариантах осуществления, каждый заместитель из группы, включающей R12, R13 и R16, представляет собой Н). В некоторых вариантах осуществления, R14 и R15 представляют собой, каждый независимо, галоген или С1галогеналкил.
В некоторых вариантах осуществления, R14 и R15 представляют собой, каждый независимо, галоген.
В некоторых вариантах осуществления, соединение Формулы I представляет собой соединение формулы II:
В некоторых вариантах осуществления, соединение Формулы II или его фармацевтически приемлемая соль представляет собой соединение формулы IIa или IIb:
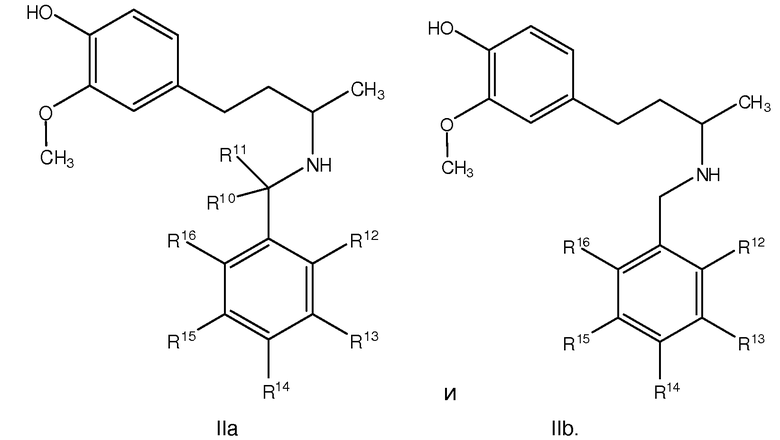
или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления, соединение формулы II представляет собой соединение формулы IIa. В некоторых дополнительных вариантах осуществления, R10 и R11, каждый, независимо, выбирают из Н и С1-3алкила. В других дополнительных вариантах осуществления, R10 и R11, каждый, независимо, выбирают из Н и метила. В других дополнительных вариантах осуществления, R10 и R11 представляют собой, каждый, Н.
В некоторых вариантах осуществления соединения формулы IIa или его фармацевтически приемлемой соли, один заместитель из группы, включающей R10 и R11, выбирают из Н и С1-3алкила, а другой представляет собой Н. В некоторых дополнительных вариантах осуществления, один заместитель из группы, включающей R10 и R11, представляет собой С1-3алкил. В других дополнительных вариантах осуществления, один заместитель из группы, включающей R10 и R11, представляет собой метил.
В некоторых вариантах осуществления соединения формулы IIa или его фармацевтически приемлемой соли, оба заместителя из группы, включающей R10 и R11, выбирают из С1-3алкила. В некоторых дополнительных вариантах осуществления, оба заместителя R10 и R11 представляет собой метил.
В некоторых вариантах осуществления соединения формулы IIa или его фармацевтически приемлемой соли, R12, R13, R14, R15 и R16, каждый, независимо, выбирают из Н, ОН, С1-6алкоксигруппы, С1-6галогеналкоксигруппы, галогена, CN, NO2, C1-6алкила, С1-6галогеналкила, С3-7циклоалкила, NH2, NH(C1-4алкил), NH(C3-7циклоалкил), N(C1-4алкил)2, NHC(O)(C1-4алкил), SH, S(C1-6алкил), C(O)OH, C(O)О(С1-4алкил), C(O)(С1-4алкил) и C(O)NH(С1-4алкил).
В некоторых вариантах осуществления соединения формулы IIa или его фармацевтически приемлемой соли, R12, R13, R14, R15 и R16, каждый, независимо, выбирают из Н, галогена, CN, NO2, C1-6алкила, С1-6галогеналкила, С3-7циклоалкила, C(O)О(С1-4алкил), C(O)(С1-4алкил) и C(O)NH(С1-4алкил).
В некоторых вариантах осуществления соединения формулы IIa или его фармацевтически приемлемой соли, R12, R13, R14, R15 и R16, каждый, независимо, выбирают из Н, галогена, CN, NO2, С1-6алкила, С1-6галогеналкила, и С3-7циклоалкила. В некоторых дополнительных вариантах осуществления, R12, R13, R14, R15 и R16, каждый, независимо, выбирают из Н, галогена, CN, С1-6алкила и С1-6галогеналкила. В других дополнительных вариантах осуществления, R12, R13, R14, R15 и R16, каждый, независимо, выбирают из Н, галогена, С1-6алкила и С1-6галогеналкила.
В некоторых вариантах осуществления соединения формулы IIa или его фармацевтически приемлемой соли, по меньшей мере, один заместитель из группы, включающей R12, R13, R14, R15 и R16, выбирают из галогена и С1-6галогеналкила, и каждый заместитель из оставшихся в группе, включающей R12, R13, R14, R15 и R16, представляет собой Н. В некоторых дополнительных вариантах осуществления, один или два заместителя из группы, включающей R12, R13, R14, R15 и R16, выбирают из галогена и С1-6галогеналкила, и каждый заместитель из оставшихся в группе, включающей R12, R13, R14, R15 и R16, представляет собой Н. В других дополнительных вариантах осуществления, один заместитель из группы, включающей R12, R13, R14, R15 и R16, выбирают из галогена и С1-6галогеналкила, и каждый заместитель из оставшихся в группе, включающей R12, R13, R14, R15 и R16, представляет собой Н.
В некоторых вариантах осуществления соединения формулы IIa или его фармацевтически приемлемой соли, по меньшей мере, один заместитель из группы, включающей R12, R13, R14, R15 и R16, выбирают из галогена, CN, NO2, С1-6галогеналкила, С(О)О(С1-4алкил), С(О)(С1-4алкил) и С(О)NH(С1-4алкил).
В некоторых вариантах осуществления соединения формулы IIa, по меньшей мере, один заместитель из группы, включающей R12, R13, R14, R15 и R16, выбирают из галогена и С1-6галогеналкила.
В некоторых вариантах осуществления соединения формулы IIa или его фармацевтически приемлемой соли, по меньшей мере, один заместитель из группы, включающей R12, R13, R14, R15 и R16, выбирают из галогена и С1-3галогеналкила. В некоторых дополнительных вариантах осуществления, по меньшей мере, один заместитель из группы, включающей R12, R13, R14, R15 и R16, выбирают из галогена и С1галогеналкила.
В некоторых вариантах осуществления соединения формулы IIa или его фармацевтически приемлемой соли, R14 представляет собой галоген или С1-6галогеналкил. В некоторых дополнительных вариантах осуществления, R14 представляет собой галоген или С1-3галогеналкил. В других дополнительных вариантах осуществления, R14 представляет собой галоген или С1галогеналкил.
В некоторых вариантах осуществления соединения формулы IIa или его фармацевтически приемлемой соли, R14 представляет собой галоген (в некоторых дополнительных вариантах осуществления, каждый заместитель из группы, включающей R12, R13, R15 и R16, представляет собой Н). В некоторых вариантах осуществления, R14 представляет собой Cl или F. В некоторых вариантах осуществления, R14 представляет собой Cl. В некоторых вариантах осуществления, R14 представляет собой F.
В некоторых вариантах осуществления соединения формулы IIa, R14 представляет собой С1-6галогеналкил (в некоторых дополнительных вариантах осуществления, каждый заместитель из группы, включающей R12, R13, R15 и R16, представляет собой Н). В некоторых дополнительных вариантах осуществления, R14 представляет собой С1-3галогеналкил. В других дополнительных вариантах осуществления, R14 представляет собой С1галогеналкил. В других дополнительных вариантах осуществления, R14 представляет собой CF3.
В некоторых вариантах осуществления соединения формулы IIa или его фармацевтически приемлемой соли, R14 представляет собой галоген или С1-6галогеналкил, и каждый заместитель из группы, включающей R12, R13, R15 и R16, представляет собой Н.
В некоторых вариантах осуществления соединения формулы IIa или его фармацевтически приемлемой соли, R15 представляет собой галоген или С1-6галогеналкил (в некоторых дополнительных вариантах осуществления, каждый заместитель из группы, включающей R12, R13, R14 и R16, представляет собой H). В некоторых дополнительных вариантах осуществления, R15 представляет собой галоген или С1-3галогеналкил. В других дополнительных вариантах осуществления, R15 представляет собой галоген или С1галогеналкил.
В некоторых вариантах осуществления соединения формулы IIa или его фармацевтически приемлемой соли, R15 представляет собой галоген. В некоторых вариантах осуществления, R15 представляет собой Cl или F. В некоторых вариантах осуществления, R15 представляет собой Cl. В некоторых вариантах осуществления, R15 представляет собой F.
В некоторых вариантах осуществления соединения формулы IIa или его фармацевтически приемлемой соли, R15 представляет собой С1-6галогеналкил. В некоторых дополнительных вариантах осуществления, R15 представляет собой С1-3галогеналкил. В других дополнительных вариантах осуществления, R15 представляет собой С1галогеналкил. В других дополнительных вариантах осуществления, R15 представляет собой CF3.
В некоторых вариантах осуществления соединения формулы IIa или его фармацевтически приемлемой соли, R14 и R15 представляют собой, каждый, независимо, галоген или С1-3галогеналкил (в некоторых дополнительных вариантах осуществления, каждый заместитель из группы, включающей R12, R13 и R16, представляет собой H). В некоторых дополнительных вариантах осуществления, R14 и R15 представляют собой, каждый, независимо, галоген или С1галогеналкил. В других дополнительных вариантах осуществления, R14 и R15 представляют собой, каждый, независимо, галоген.
В некоторых вариантах осуществления, соединение Формулы II или его фармацевтически приемлемая соль представляет собой соединение формулы IIb или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления соединения формулы IIb или его фармацевтически приемлемой соли, R12, R13, R14, R15 и R16, каждый, независимо, выбирают из Н, ОН, С1-6алкоксигруппы, С1-6галогеналкоксигруппы, галогена, CN, NO2, C1-6алкила, С1-6галогеналкила, С3-7циклоалкила, NH2, NH(C1-4алкил), NH(C3-7циклоалкил), N(C1-4алкил)2, NHC(O)(C1-4алкил), SH, S(C1-6алкил), C(O)OH, C(O)О(С1-4алкил), C(O)(С1-4алкил), и C(O)NH(С1-4алкил).
В некоторых вариантах осуществления соединения формулы IIb или его фармацевтически приемлемой соли, R12, R13, R14, R15 и R16, каждый, независимо, выбирают из Н, галогена, CN, NO2, C1-6алкила, С1-6галогеналкила, С3-7циклоалкила, C(O)О(С1-4алкил), C(O)(С1-4алкил), и C(O)NH(С1-4алкил).
В некоторых вариантах осуществления соединения формулы IIb или его фармацевтически приемлемой соли, R12, R13, R14, R15 и R16, каждый, независимо, выбирают из Н, галогена, CN, NO2, С1-6алкила, С1-6галогеналкила, и С3-7циклоалкила. В некоторых дополнительных вариантах осуществления, R12, R13, R14, R15 и R16, каждый, независимо, выбирают из Н, галогена, CN, С1-6алкила и С1-6галогеналкила. В других дополнительных вариантах осуществления, R12, R13, R14, R15 и R16, каждый, независимо, выбирают из Н, галогена, С1-6алкила, и С1-6галогеналкила.
В некоторых вариантах осуществления соединения формулы IIb или его фармацевтически приемлемой соли, по меньшей мере, один заместитель из группы, включающей R12, R13, R14, R15 и R16, выбирают из галогена и С1-6галогеналкила, и каждый заместитель из оставшихся в группе, включающей R12, R13, R14, R15 и R16, представляет собой Н. В некоторых дополнительных вариантах осуществления, один или два заместителя из группы, включающей R12, R13, R14, R15 и R16, выбирают из галогена и С1-6галогеналкила, и каждый заместитель из оставшихся в группе, включающей R12, R13, R14, R15 и R16, представляет собой Н. В других дополнительных вариантах осуществления, один заместитель из группы, включающей R12, R13, R14, R15 и R16, выбирают из галогена и С1-6галогеналкила, и каждый заместитель из оставшихся в группе, включающей R12, R13, R14, R15 и R16, представляет собой Н.
В некоторых вариантах осуществления соединения формулы IIb или его фармацевтически приемлемой соли, по меньшей мере, один заместитель из группы, включающей R12, R13, R14, R15 и R16, выбирают из галогена, CN, NO2, С1-6галогеналкила, С(О)О(С1-4алкил), С(О)(С1-4алкил), и С(О)NH(С1-4алкил).
В некоторых вариантах осуществления соединения формулы IIb, по меньшей мере, один заместитель из группы, включающей R12, R13, R14, R15 и R16, выбирают из галогена и С1-6галогеналкила.
В некоторых вариантах осуществления соединения формулы IIb или его фармацевтически приемлемой соли, по меньшей мере, один заместитель из группы, включающей R12, R13, R14, R15 и R16, выбирают из галогена и С1-3галогеналкила. В некоторых дополнительных вариантах осуществления, по меньшей мере, один заместитель из группы, включающей R12, R13, R14, R15 и R16, выбирают из галогена и С1галогеналкила.
В некоторых вариантах осуществления соединения формулы IIb или его фармацевтически приемлемой соли, R14 представляет собой галоген или С1-6галогеналкил. В некоторых дополнительных вариантах осуществления, R14 представляет собой галоген или С1-3галогеналкил. В других дополнительных вариантах осуществления, R14 представляет собой галоген или С1галогеналкил.
В некоторых вариантах осуществления соединения формулы IIb или его фармацевтически приемлемой соли, R14 представляет собой галоген (в некоторых дополнительных вариантах осуществления, каждый заместитель из группы, включающей R12, R13, R15 и R16, представляет собой Н). В некоторых вариантах осуществления, R14 представляет собой Cl или F. В некоторых вариантах осуществления, R14 представляет собой Cl. В некоторых вариантах осуществления, R14 представляет собой F.
В некоторых вариантах осуществления соединения формулы IIb, R14 представляет собой С1-6галогеналкил (в некоторых дополнительных вариантах осуществления, каждый заместитель из группы, включающей R12, R13, R15 и R16, представляет собой Н). В некоторых дополнительных вариантах осуществления, R14 представляет собой С1-3галогеналкил. В других дополнительных вариантах осуществления, R14 представляет собой С1галогеналкил. В других дополнительных вариантах осуществления, R14 представляет собой CF3.
В некоторых вариантах осуществления соединения формулы IIb или его фармацевтически приемлемой соли, R14 представляет собой галоген или С1-6галогеналкил, и каждый заместитель из группы, включающей R12, R13, R15 и R16, представляет собой Н.
В некоторых вариантах осуществления соединения формулы IIb или его фармацевтически приемлемой соли, R15 представляет собой галоген или С1-6галогеналкил (в некоторых дополнительных вариантах осуществления, каждый заместитель из группы, включающей R12, R13, R14 и R16, представляет собой H). В некоторых дополнительных вариантах осуществления, R15 представляет собой галоген или С1-3галогеналкил. В других дополнительных вариантах осуществления, R15 представляет собой галоген или С1галогеналкил.
В некоторых вариантах осуществления соединения формулы IIb или его фармацевтически приемлемой соли, R15 представляет собой галоген. В некоторых вариантах осуществления, R15 представляет собой Cl или F. В некоторых вариантах осуществления, R15 представляет собой Cl. В некоторых вариантах осуществления, R15 представляет собой F.
В некоторых вариантах осуществления соединения формулы IIb или его фармацевтически приемлемой соли, R15 представляет собой С1-6галогеналкил. В некоторых дополнительных вариантах осуществления, R15 представляет собой С1-3галогеналкил. В других дополнительных вариантах осуществления, R15 представляет собой С1галогеналкил. В других дополнительных вариантах осуществления, R15 представляет собой CF3.
В некоторых вариантах осуществления соединения формулы IIb или его фармацевтически приемлемой соли, R14 и R15 представляют собой, каждый, независимо, галоген или С1-3галогеналкил (в некоторых дополнительных вариантах осуществления, каждый заместитель из группы, включающей R12, R13 и R16, представляет собой H). В некоторых дополнительных вариантах осуществления, R14 и R15 представляют собой, каждый, независимо, галоген или С1галогеналкил. В других дополнительных вариантах осуществления, R14 и R15 представляют собой, каждый, независимо, галоген.
В некоторых вариантах осуществления, соединение формулы I представляет собой соединение формулы III:
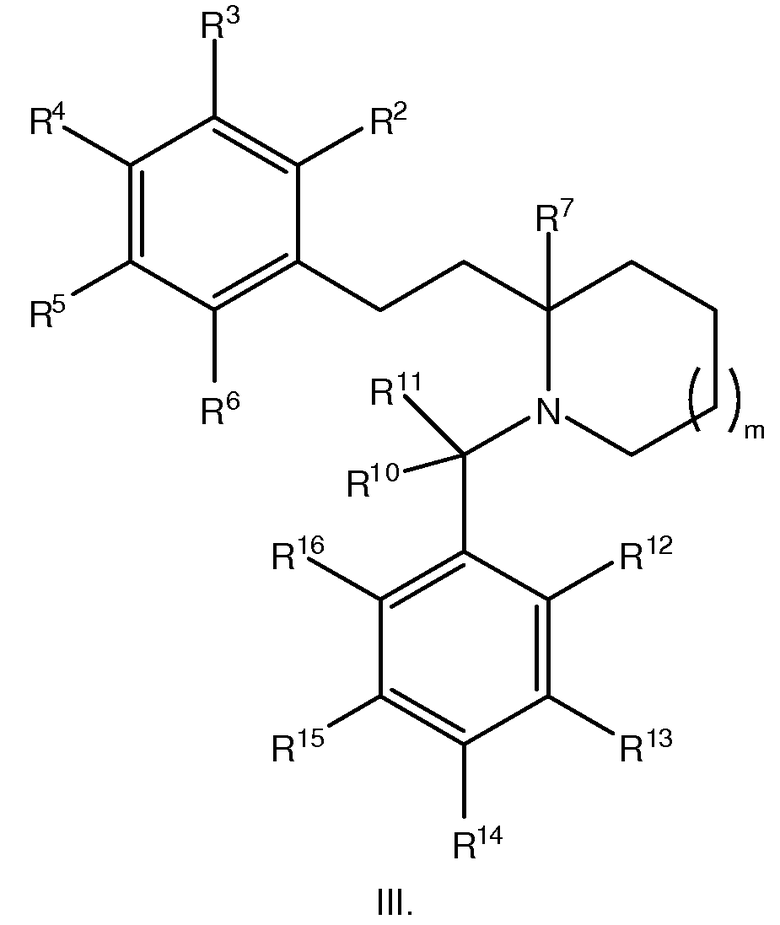
В некоторых вариантах осуществления соединений формулы III или их фармацевтически приемлемой соли, m имеет значение 1.
В некоторых вариантах осуществления соединений формулы III или их фармацевтически приемлемой соли, m имеет значение 0.
В некоторых вариантах осуществления соединений формулы III или их фармацевтически приемлемой соли, по меньшей мере, один заместитель из группы, включающей R2, R3, R4, R5 и R6, выбирают из ОН, С1-6алкоксигруппы, и С1-6галогеналкоксигруппы.
В некоторых вариантах осуществления соединений формулы III или их фармацевтически приемлемой соли, по меньшей мере, два заместителя из группы, включающей R2, R3, R4, R5 и R6, независимо выбирают из ОН, С1-6алкоксигруппы, и С1-6галогеналкоксигруппы.
В некоторых вариантах осуществления соединений формулы III или их фармацевтически приемлемой соли, по меньшей мере, один заместитель из группы, включающей R12, R13, R14, R15 и R16, является отличным от Н.
В некоторых вариантах осуществления соединения формулы III или его фармацевтически приемлемой соли, R14 и R15 представляют собой, каждый, независимо, галоген или С1-3галогеналкил. В некоторых дополнительных вариантах осуществления, R14 и R15 представляют собой, каждый, независимо, галоген или С1галогеналкил.
В различных местах описания настоящего изобретения, заместители соединений изобретения раскрыты группами или рядами. Под этим конкретно подразумевается, что варианты осуществления изобретения включают каждый элемент таких групп и рядов и каждую отдельно взятую подкомбинацию элементов таких групп и рядов. Например, термин «С1-6алкил» конкретно предназначен для индивидуального раскрытия метила (С1алкил), этила (С2алкил), С3алкила, С4алкила, С5алкила, и С6алкила.
Для соединений изобретения, в которых переменная появляется более одного раза, каждая переменная может представлять собой отличающийся фрагмент, выбранный из группы Маркуша, определяющей переменную. Например, в том случае, когда описывают структуру, имеющую две группы R, которые одновременно присутствуют в одном и том же соединении, тогда две группы R могут представлять собой различные фрагменты, выбранные из группы Маркуша, определенной для R.
Дополнительно оценивают то, что некоторые признаки изобретения, которые, для ясности, описаны в контексте отдельных вариантов осуществления, также могут быть обеспечены в комбинации в едином варианте осуществления. С другой стороны, различные признаки изобретения, которые, для краткости, описаны в контексте единого варианта осуществления, также могут быть обеспечены отдельно или в любой подходящей комбинации.
Термин «n-членный» в том случае, когда n представляет собой целое число, описывает число атомов, образующих кольцо, в фрагменте, где число атомов, образующих кольцо, составляет n. Например, пиридин представляет собой пример 6-членного гетероарильного кольца, а тиофен представляет собой пример 5-членной гетероарильной группы.
Как использовано в этом документе, термин «алкил», как подразумевается, относится к насыщенной углеводородной группе, которая является линейной или разветвленной. Примеры алкильных групп включают метил (Ме), этил (Et), пропил (например, н-пропил и изопропил), бутил (например, н-бутил, изобутил, трет-бутил), пентил (например, н-пентил, изопентил, неопентил), и тому подобное, но не ограничиваются этим. Алкильная группа может содержать от 1 до приблизительно 20, от 2 до приблизительно 20, от 1 до приблизительно 10, от 1 до приблизительно 8, от 1 до приблизительно 6, от 1 до приблизительно 4, или от 1 до приблизительно 3 атомов углерода. Термин «алкилен» относится к двухвалентной алкильной связывающей группе. Примером алкилена является метилен (СН2).
Как используется в этом документе, «алкенил» относится к алкильной группе, имеющей одну или более двойных углерод-углеродных связей. Примеры алкенильных групп включают этенил, пропенил, циклогексенил, и тому подобное, но не ограничиваются этим. Термин «алкениленил» относится к двухвалентной связывающей алкенильной группе.
Как используется в этом документе, «алкинил» относится к алкильной группе, имеющей одну или более тройных углерод-углеродных связей. Примеры алкинильных групп включают этинил, пропинил, и тому подобное, но не ограничиваются этим. Термин «алкиниленил» относится к двухвалентной связывающей алкинильной группе.
Как используется в этом документе, «галогеналкил» относится к алкильной группе, имеющей один или более галогеновых заместителей. Примеры галогеналкильных групп включают CF3, C2F5, CHF2, CCl3, CHCl2, C2Cl5, CH2CF3 и тому подобное, но не ограничиваются этим.
Как используют в этом документе, «арил» относится к моноциклическим или полициклическим (например, имеющим 2, 3 или 4 конденсированных кольца) ароматическим углеводородам, таким как, например, фенил, нафтил, антраценил, фенантренил, инданил, инденил и тому подобное. В некоторых вариантах осуществления, арильные группы имеют от 6 до приблизительно 20 атомов углерода. В некоторых вариантах осуществления, арильные группы имеют от 6 до приблизительно 10 атомов углерода.
Как используют в этом документе, «циклоалкил» относится к неароматическим циклическим углеводородам, включающим циклизованные алкильные, алкенильные, и алкинильные группы, которые содержат вплоть до 20 атомов углерода, образующих кольцо. Циклоалкильные группы могут включать моно- или поли-циклические (например, имеющие 2, 3 или 4 конденсированных кольца) кольцевые системы, а также кольцевые спиросистемы. Циклоалкильная группа может содержать от 3 до приблизительно 15, от 3 до приблизительно 10, от 3 до приблизительно 8, от 3 до приблизительно 6, от 4 до приблизительно 6, от 3 до приблизительно 5, или от 5 до приблизительно 6 атомов углерода, образующих кольцо. Атомы углерода, образующие кольцо, в циклоалкильной группе могут быть необязательно замещены оксогруппой или сульфидогруппой. Примеры циклоалкильных групп включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклопентенил, циклогексенил, циклогексадиенил, циклогептатриенил, норборнил, норпинил, норкарнил, адамантил, и тому подобное, но не ограничиваются этим. Также включенными в определение циклоалкила являются фрагменты, которые имеют один или более ароматических колец, конденсированных (то есть, имеющих связь наряду с) с циклоалкильным кольцом, например, бензо- или тиенильные производные пентана, пентена, гексана, и тому подобное (например, 2,3-дигидро-1Н-инден-1-ил, или 1Н-инден-2(3Н)-он-1-ил). Предпочтительно, «циклоалкил» относится к циклизованным алкильным группам, которые содержат вплоть до 20 атомов углерода, образующих кольцо. Примеры циклоалкила предпочтительно включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, адамантил, и тому подобное.
Как используют в этом документе, «гетероарильные» группы относятся к ароматическому гетероциклу, имеющему вплоть до 20 атомов, образующих кольцо, и имеющему, по меньшей мере, один гетероатомный кольцевой член (атом, образующий кольцо), такой как сера, кислород, или азот. В некоторых вариантах осуществления, гетероарильная группа имеет, по меньшей мере, один или более гетероатомных образующих кольцо атомов, каждый из которых независимо выбирают из серы, кислорода, и азота. Гетероарильные группы включают моноциклические и полициклические (например, имеющие 2, 3 или 4 конденсированных кольца) системы. Примеры гетероарильных групп включают без ограничения, пиридил, пиримидинил, пиразинил, пиридазинил, триазинил, фурил, хинолил, изохинолил, тиенил, имидазолил, тиазолил, индолил, пиррил, оксазолил, бензофурил, бензотиенил, бензтиазолил, изоксазолил, пиразолил, триазолил, тетразолил, индазолил, 1,2,4-тиадиазолил, изотиазолил, бензотиенил, пуринил, карбазолил, бензимидазолил, индолинил, и тому подобное. В некоторых вариантах осуществления, гетероарильная группа имеет от 1 до приблизительно 20 атомов углерода, и в дополнительных вариантах осуществления, от приблизительно 1 до приблизительно 5, от приблизительно 1 до приблизительно 4, от приблизительно 1 до приблизительно 3, от приблизительно 1 до приблизительно 2, атомов углерода в качестве образующих кольцо атомов. В некоторых вариантах осуществления, гетероарильная группа содержит 3 - приблизительно 14, 3 - приблизительно 7, или 5-6 образующих кольцо атомов. В некоторых вариантах осуществления, гетероарильная группа имеет 1 - приблизительно 4, 1 - приблизительно 3, или 1-2 гетероатома.
Как использовано в этом документе, «гетероциклоалкил» относится к неароматическим гетероциклам, имеющим вплоть до 20 образующих кольцо атомов, включающим циклизованные алкильные, алкенильные, и алкинильные группы, где один или более образующих кольцо атомов углерода заменены гетероатомом, таким как атом О, N, или S. Гетероциклоалкильные группы могут быть моно- или полициклическими (например, могут представлять собой как конденсированные, так и спиро- системы). Примеры «гетероциклоалкильных» групп включают морфолиногруппу, тиоморфолиногруппу, пиперазинил, тетрагидрофуранил, тетрагидротиенил, 2,3-дигидробензофурил, 1,3-бензодиоксол, бензо-1,4-диоксан, пиперидинил, пирролидинил, изоксазолидинил, изотиазолидинил, пиразолидинил, оксазолидинил, тиазолидинил, имидазолидинил, пирролидин-2-он-3-ил, и тому подобное. Образующие кольцо атомы углерода и гетероатомы в гетероциклоалкильной группе могут быть необязательно замещены оксогруппой или сульфидогруппой. Например, образующий кольцо атом S может быть замещен посредством 1 или 2 оксогрупп [то есть, с получением S(O) или S(O)2]. Для еще одного примера, образующий кольцо атом С может быть замещен оксогруппой (то есть, с получением карбонила). Также включенными в определение гетероциклоалкила являются фрагменты, которые имеют одно или более ароматических колец, конденсированных (то есть, имеющих связь наряду с) с неароматическим гетероциклическим кольцом, например, пиридинил, тиофенил, фталимидил, нафталимидил, и бензо-производные гетероциклов, такие как индоленовые, изоиндоленовые, изоиндолин-1-он-3-ильные, 4,5,6,7-тетрагидротиено[2,3-с]пиридин-5-ильные, 5,6-дигидротиено[2,3-с]пиридин-7(4Н)-он-5-ильные, и 3,4-дигидроизохинолин-1(2Н)-он-3-ильные группы. Образующие кольцо атомы углерода и гетероатомы в гетероциклоалкильной группе могут быть необязательно замещены оксогруппой или сульфидогруппой. В некоторых вариантах осуществления, гетероциклоалкильная группа имеет от 1 до приблизительно 20 атомов углерода, и в дополнительных вариантах осуществления, от приблизительно 3 до приблизительно 20 атомов углерода. В некоторых вариантах осуществления, гетероциклоалкильная группа содержит 3 - приблизительно 14, 3 - приблизительно 7, или 5-6 образующих кольцо атомов. В некоторых вариантах осуществления, гетероциклоалкильная группа имеет 1 - приблизительно 4, 1 - приблизительно 3, или 1-2 гетероатома. В некоторых вариантах осуществления, гетероциклоалкильная группа содержит 0-3 двойные связи. В некоторых вариантах осуществления, гетероциклоалкильная группа содержит 0-2 тройные связи.
Как используют в этом документе, «галоген» или «галогеновая группа» включает фтор, хлор, бром, или иод.
Как используют в этом документе, «алкоксигруппа» относится к -О-алкильной группе. Примеры алкоксигрупп включают метоксигруппу, этоксигруппу, пропоксигруппу (например, н-пропоксигруппу и изопропоксигруппу), трет-бутоксигруппу, и тому подобное.
Как используют в этом документе, «галогеналкоксигруппа» относится к -О-галогеналкильной группе. Примером галогеналкоксигруппы является OCF3. Как используют в этом документе, «тригалогенметоксигруппа» относится к метоксигруппе, имеющей три галогеновых заместителя. Примеры тригалогенметоксигрупп включают -OCF3, -OCClF2, -OCCl3, и тому подобное, но не ограничиваются этим.
Как используют в этом документе, «арилалкил» относится к С1-6алкилу, замещенному арилом, и «циклоалкилалкил» относится к С1-6алкилу, замещенному циклоалкилом.
Как используют в этом документе, «гетероарилалкил» относится к С1-6алкильной группе, замещенной гетероарильной группой, и «гетероциклоалкилалкил» относится к С1-6алкилу, замещенному гетероциклоалкилом.
Как используют в этом документе, «аминогруппа» относится к NH2.
Как используют в этом документе, «алкиламиногруппа» относится к аминогруппе, замещенной алкильной группой.
Как используют в этом документе, «диалкиламиногруппа» относится к аминогруппе, замещенной двумя алкильными группами.
Как используют в этом документе, С(О) относится к С(=О).
Как используют в этом документе, С(S) относится к С(=S).
Как используют в этом документе, S(О) относится к S(=О).
Как используют в этом документе, S(О)2 относится к S(=О)2.
Как используют в этом документе, термин «необязательно замещенный» означает то, что замещение является необязательным и, следовательно, включает как незамещенные, так и замещенные атомы и фрагменты. «Замещенный» атом или фрагмент указывает на то, что любой водород на обозначенном атоме или фрагменте может быть заменен группой, выбранной из упомянутой группы заместителей, при условии, что обычная валентность обозначенного атома или фрагмента не превышается, и, что замещение приводит к стабильному соединению. Например, если метильная группа (то есть, СН3) является необязательно замещенной, то 3 атома водорода на атоме углерода могут быть заменены группами-заместителями.
Как используют в этом документе, «приблизительно» в связи с численным значением обозначает то, что численное значение является приблизительным, и небольшие вариации не могли бы существенно сказаться на применении на практике раскрытых вариантов осуществления. В том случае, когда используют численное ограничение, если не указано иное в контексте, «приблизительно» означает, что численное значение может варьироваться на ±10% и оставаться в рамках объема раскрытых вариантов осуществления.
Соединения, описанные в вариантах осуществления в этом документе, могут быть асимметрическими (например, имеющими один или более стереоцентров). Все стереоизомеры, такие как энантиомеры и диастереомеры, имеются ввиду, если не указано иное. Соединения настоящего изобретения, которые содержат асимметрически замещенные атомы углерода, могут быть выделены в оптически активных или рацемических формах. Способы того, как получить оптически активные формы из оптически активных исходных веществ, известны в данной области, например, способы разделением рацемических смесей или стереоселективным синтезом. Многие геометрические изомеры олефинов, соединений с двойными связями C=N, и тому подобного, также могут иметь место в соединениях, описанных в данном документе, и все такие стабильные изомеры предусмотрены в настоящем изобретении. Описаны цис- и транс- геометрические изомеры соединений настоящего изобретения, и они могут быть выделены в виде смеси изомеров или в виде разделенных изомерных форм. В том случае, когда соединение, способное к стереоизомерии или к геометрической изомерии, обозначают в его структуре или в названии без упоминания конкретных конфигураций R/S или цис/транс, подразумевается, что все такие изомеры подлежат рассмотрению.
Разделение рацемических смесей соединений может быть выполнено посредством любых многочисленных способов, известных в данной области. Способ как образец включает фракционную перекристаллизацию с использованием кислоты для хирального разделения, которая является оптически активной, образующей соль органической кислотой. Подходящие разделяющие агенты для фракционной перекристаллизации представляют собой, например, оптически активные кислоты, такие как формы D и L винной кислоты, диацетилвинной кислоты, дибензоилвинной кислоты, миндальной кислоты, яблочной кислоты, молочной кислоты, или различные оптически активные камфорсульфокислоты, такие как β-камфорсульфокислота. Другие разделяющие агенты, подходящие для способов фракционной кристаллизации, включают стереоизомерно чистые формы α-метилбензиламина (например, формы S и R, или диастереомерно чистые формы), 2-фенилглицинола, норэфедрина, эфедрина, N-метилэфедрина, циклогексилэтиламина, 1,2-диаминоциклогексана, и тому подобное.
Разделение рацемических смесей также может быть выполнено элюированием на колонке, заполненной насадкой в виде оптически активного разделяющего агента (например, динитробензоилфенилглицина). Подходящая композиция растворителей для элюирования может быть определена специалистом в данной области.
Соединения вариантов осуществления изобретения также включают таутомерные формы. Таутомерные формы получаются в результате обмена местами одинарной связи и соседней двойной связи наряду с сопутствующей миграцией протона. Таутомерные формы включают прототропные таутомеры, которые представляют собой изомерные состояния протонирования, имеющие одни и те же эмпирическую формулу и общий заряд. Примеры прототропных таутомеров включают пары кетон - енол, пары амид - имидокислота, пары лактам - лактим, пары амид - имидокислота, пары енамин - имин, и кольцевые формы, где протон может занимать два или более положений в гетероциклической системе, например, 1Н- и 3Н-имидазол, 1Н-, 2Н- и 4Н- 1,2,4-триазол, 1Н- и 2Н-изоиндол, и 1Н- и 2Н-пиразол. Таутомерные формы могут находиться в равновесии или стерически закрыты в одной форме посредством соответствующего замещения.
Соединения вариантов осуществления изобретения дополнительно включают гидраты и сольваты, а также безводные и не-сольватированные формы.
Термин «соединение», используемый в этом документе, как полагают, включает все стереоизомеры, геометрические изомеры, таутомеры, и изотопные формы отображенных структур.
Все соединения и их фармацевтически приемлемые соли, могут быть получены или представлены вместе с другими веществами, такими как вода и растворители (например, гидраты и сольваты) или могут быть выделены.
Соединения вариантов осуществления изобретения также могут включать все изотопы атомов, встречающихся в промежуточных соединениях или в конечных соединениях. Изотопы включают те атомы, которые имеют одно и то же атомное число, но различные массовые числа. Например, изотопы водорода включают тритий и дейтерий.
В некоторых вариантах осуществления, соединения изобретения, или их соли, получают в основном выделенными. Под «в основном выделенный» понимают, что соединение, по меньшей мере, частично или в значительной степени выделяют из среды, в которой оно получено или обнаружено. Частичное разделение может включать, например, композицию, обогащенную соединением изобретения. Значительное разделение может включать композиции, содержащие, по меньшей мере, приблизительно 50%, по меньшей мере, приблизительно 60%, по меньшей мере, приблизительно 70%, по меньшей мере, приблизительно 80%, по меньшей мере, приблизительно 90%, по меньшей мере, приблизительно 95%, по меньшей мере, приблизительно 97%, или, по меньшей мере, приблизительно 99%, по массе соединения изобретения, или его соли. Способы выделения соединений и их солей являются рутинными в данной области.
Соединения вариантов осуществления изобретения, подразумевается, включают соединения со стабильными структурами. Как используют в этом документе, «стабильное соединение» и «стабильная структура» предназначены для указания соединения, которое является достаточно стойким, чтобы выдержать выделение из реакционной смеси до полезной степени чистоты, и приготовление состава эффективного терапевтического средства.
Фразу «фармацевтически приемлемый» применяют в этом документе для того, чтобы сослаться на те соединения, вещества, композиции, и/или лекарственные формы, которые, в рамках объема результатов тщательной медицинской оценки, подходят для применения в контакте с тканями человеческих существ и животных без излишней токсичности, раздражения, аллергической реакции, или другой проблемы или осложнения, соразмерно оправданному соотношению польза/риск.
Выражения, «температура окружающей среды» и «комнатная температура», используемые в этом документе, понятны в данной области, и относятся, как правило, к температуре, например, к температуре реакции, которая приблизительно равна температуре в комнате, в которой проводят реакцию, например, температуре от приблизительно 20°С до приблизительно 30°С.
Варианты осуществления настоящего изобретения также включают фармацевтически приемлемые соли соединений, описанных в этом документе. Как используют в этом документе, «фармацевтически приемлемые соли» относятся к производным раскрываемых соединений, где исходное соединение модифицируют путем превращения имеющегося в наличии кислотного или основного фрагмента в его солевую форму. Примеры фармацевтически приемлемых солей включают соли оснований, таких как амины, полученные присоединением минеральных или органических кислот; соли кислот, таких как карбоновые кислоты, полученные присоединением щелочей или органических оснований; и тому подобное, но не ограничиваются этим. Фармацевтически приемлемые соли настоящего изобретения включают традиционные нетоксичные соли исходного соединения, образованные, например, из нетоксичных неорганических или органических кислот. Фармацевтически приемлемые соли настоящего изобретения могут быть синтезированы из исходного соединения, которое содержит основный или кислотный фрагмент путем обычно применяемых химических способов. Вообще, такие соли могут быть приготовлены посредством реакционного взаимодействия этих соединений в форме свободных кислот или оснований со стехиометрическим количеством соответствующего основания или кислоты в воде или в органическом растворителе, или в смеси того и другого типа растворителей; как правило, неводные среды, подобные простому эфиру, этилацетату, этанолу, изопропанолу, или ацетонитрилу (ACN), являются предпочтительными. Перечни подходящих солей обнаружены в книге: Remington's Pharmaceutical Sciences, 17th ed., Mack Publishing Company, Easton, Pa., 1985, p. 1418, и в публикации: Journal of Pharmaceutical Science, 66, 2(1977), каждая из которых включена в этот документ путем ссылки в полном своем объеме.
Синтез
Соединения вариантов осуществления изобретения, включая их соли, могут быть получены с использованием известных методов органического синтеза и могут быть синтезированы в соответствии с любым из многочисленных возможных путей синтеза.
Реакции для получения соединений изобретения могут быть проведены в подходящих растворителях, которые могут быть легко подобраны специалистом в области органического синтеза. Подходящие растворители могут быть практически нереакционноспособными с исходными веществами (реагентами), промежуточными соединениями, или продуктами при температурах, при которых проводят реакции, например, при температурах, которые могут находиться в диапазоне от температуры замерзания растворителя до температуры кипения растворителя. Заданная реакция может быть проведена в одном растворителе или в смеси двух или более растворителей. В зависимости от конкретной реакционной стадии, подходящие растворители для конкретной реакционной стадии могут быть подобраны специалистом в данной области.
Получение соединений изобретения может включать в себя введение защиты для различных химических групп и снятие защиты с таковых. Необходимость введения защиты и снятия защиты, и выбор соответствующих защитных групп, могут быть легко определены специалистом в данной области. Химия защитных групп может быть обнаружена, например, в обзоре: T.W. Greene and P.G. M. Wuts, Protective Grups in Organic Synthesis, 3rd Ed., Wiley & Sons, Inc., New York (1999), который включен в этот документ путем ссылки в полном своем объеме.
Реакции могут быть отслежены в соответствии с любым подходящим способом, известным в данной области. Например, образование продукта может быть отслежено спектроскопическим средством, таким как спектроскопия ядерного магнитного резонанса (например, 1Н или 13С), инфракрасная спектроскопия, спектрофотометрия (например, УФ-видимая), масс-спектрометрия, или хроматографическими способами, такими как высокоэффективная жидкостная хроматография (HPLC) или тонкослойная хроматография (TLC).
Соединения вариантов осуществления изобретения могут быть получены, например, в соответствии с путями реакции, методиками синтеза, и методами, описанными ниже.
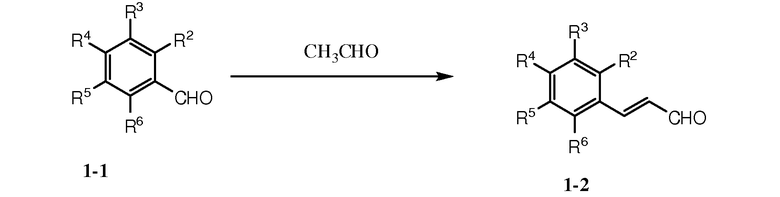
Как показано на схеме 1, бензальдегидное производное 1-1 может быть подвергнуто реакции с ацетальдегидом в присутствии либо кислотного, либо основного катализатора с предоставлением коричного альдегида 1-2. Реакция коричного альдегида 1-2 с металлоорганическим соединением, таким как реагент Гриньяра R8MgX1 [где X1 представляет собой галоген, такой как Cl или Br], с последующим окислением промежуточного спирта в кетон и восстановлением связи С=С в одинарную связь С-С в условиях гидрогенизации (например, в присутствии палладиевого катализатора на углеродном носителе Pd/C), предоставляет кетон 1-3. Реакция кетона 1-3 с амином 1-4 в условиях реактивного аминирования (например, в присутствии боргидридного восстанавливающего агента) предоставляет соединение 1-5.
Схема 1
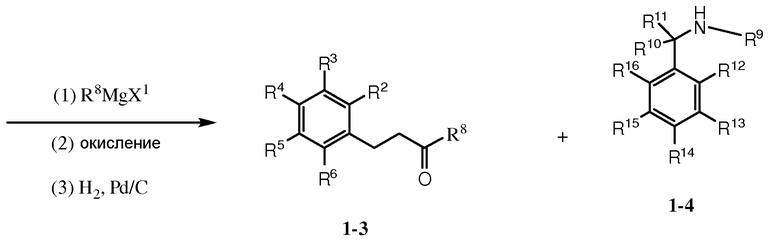
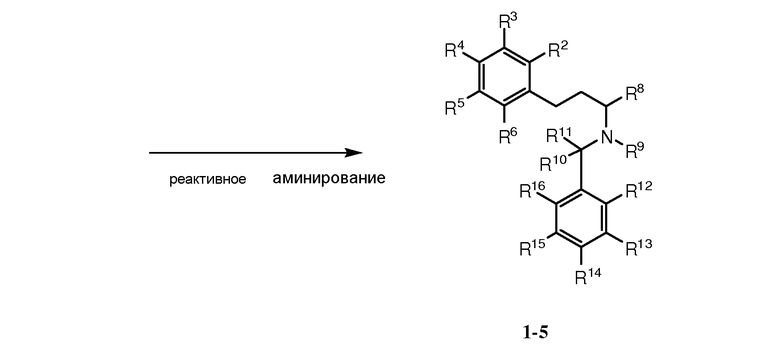
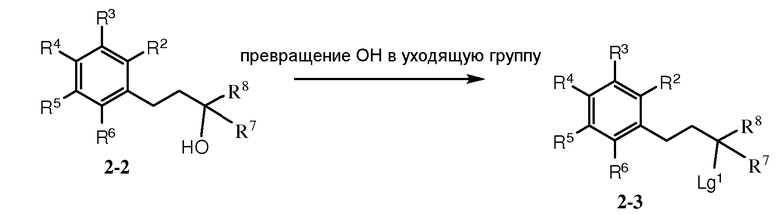
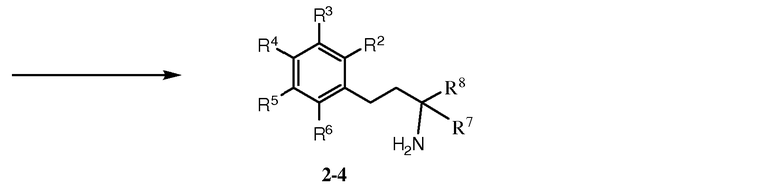
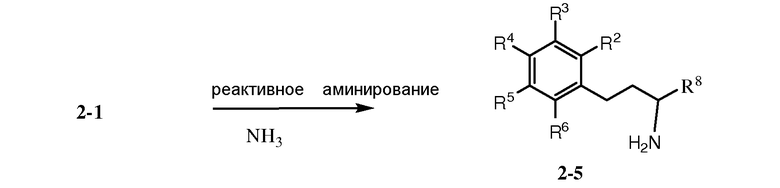
Как показано на схеме 2, кетон 2-1 может быть подвергнут реакции с металлоорганическим соединением, таким как реагент Гриньяра R7MgX2 [где R7 может представлять собой С1-6алкил или С3-7циклоалкил; и Х2 может быть галогеном, таким как Cl или Br] с предоставлением спирта 2-2а. Восстановление кетона 2-1, например, в присутствии боргидридного восстанавливающего агента, предоставляет спирт 2-2b. Группа ОН в спирте 2-2 (где R7 может представлять собой Н, С1-6алкил, или С3-7циклоалкил) может быть превращена в более хорошую уходящую группу Lg1, такую как OMs [мезилат или CH3S(O)2O-] или OTf [трифлат или CF3S(O)2O-], с последующим реакционным взаимодействием с NH3 с предоставлением амина 2-4. Кетон 2-1 также может подвергаться восстановительному аминированию посредством NH3 с предоставлением амина 2-5.
Схема 2
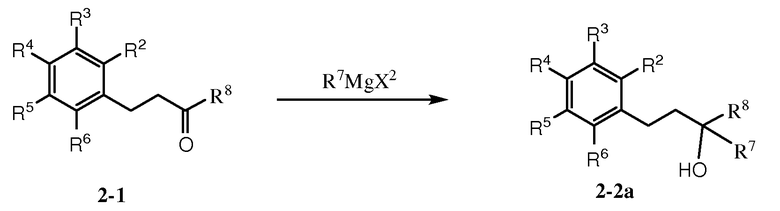
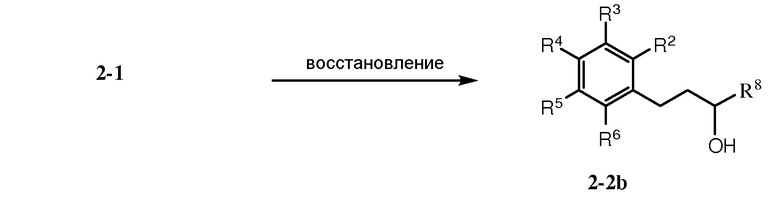
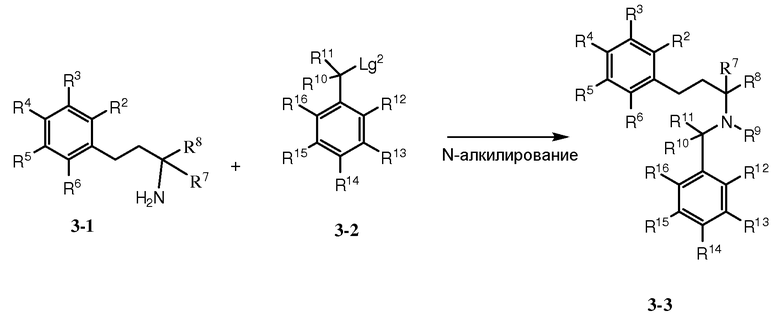
Как показано на схеме 3, амин 3-1 (где R7 может представлять собой, например, Н, С1-6алкил, или С3-7циклоалкил) может быть подвергнут реакции с соединением 3-2 [Lg2 может быть уходящей группой, такой как трифлатная группа (-OTf)] или галоген (например, Cl или Br)] с предоставлением соединения 3-3.
Схема 3
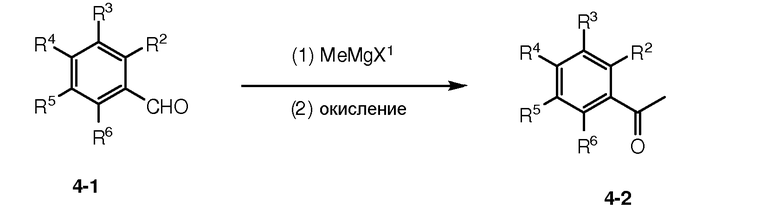
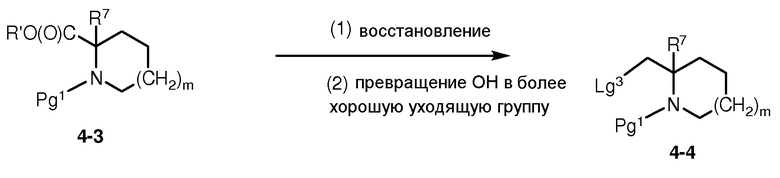
Как показано на схеме 4, бензальдегидное производное 4-1 может быть подвергнуто реакции с метилметаллсодержащим соединением, таким как реагент Гриньяра MeMgX1 [где Х1 представляет собой галоген, такой как Cl или Br], с последующим окислением промежуточного спирта в кетон с предоставлением кетона 4-2. Сложноэфирное соединение 4-3 [где R' может представлять собой алкил (например, метил или этил) или арилалкил; и Pg1 может представлять собой защитную группу для аминогруппы (такую как трет-бутилоксикарбонил или Boc; бензилоксикарбонил или Cbz; или бензил)] может быть восстановлено в спирт (в присутствии восстанавливающего агента, такого как алюмогидрид лития или LAH), с последующим превращением группы ОН в более хорошую уходящую группу Lg3, такую как OMs [мезилат или CH3S(O)2O-] или OTf [трифлат или CF3S(O)2O-], с предоставлением соединения 4-4.
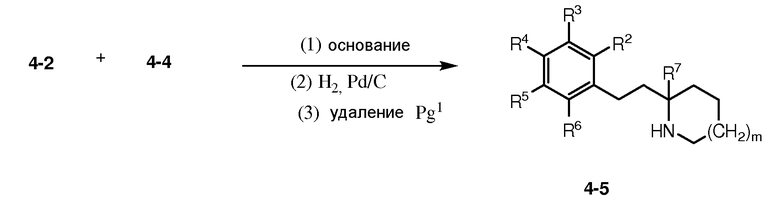
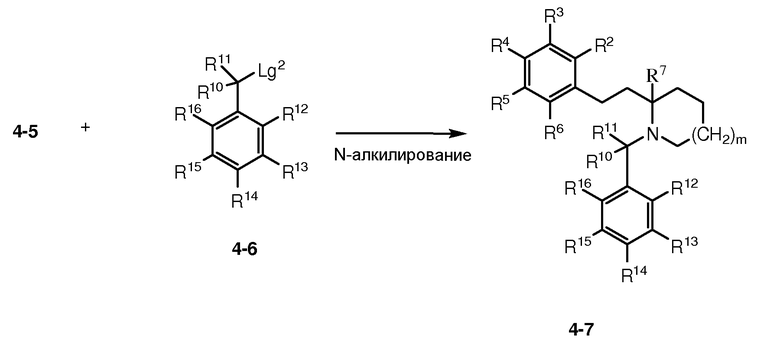
Реакция соединения 4-2 с соединением 4-4 в присутствии сильного основания (такого как диизопропиламид лития или LDA), с последующей гидрогенизацией (например, в присутствии палладиевого катализатора на углеродном носителе Pd/C) для восстановления С(О) в СН2 и путем удаления защитной группы Pg1 в подходящих условиях (например, бензильная группа может быть удалена в условиях гидрогенизации в присутствии Pd/C; или группа Boc может быть удалена в кислотных условиях), предоставляет амин 4-5. Амин 4-5 может быть подвергнут реакции с соединением 4-6 [где Lg2 может быть уходящей группой, такой как трифлатная группа (-OTf)] или галоген (например, Cl или Br)] с предоставлением соединения 4-7.
Схема 4
Специалист в данной области сможет понять, что на всех схемах, описанных в этом документе, если на группе-заместителе, такой как R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11, R12, R13, R14, R15, R16, и так далее, имеются функциональные (реакционноспособные) группы, то может быть сделана дополнительная модификация, если это приемлемо и/или желательно. Например, группа CN может быть гидролизована с предоставлением амидной группы; карбоновая кислота может быть превращена в амид; карбоновая кислота может быть превращена в сложный эфир, который в свою очередь может быть восстановлен до спирта, который в свою очередь может быть дополнительно модифицирован. В качестве еще одного примера, группа ОН может быть превращена в более хорошую уходящую группу, такую как мезилатная группа, которая в свою очередь подходит для нуклеофильного замещения, например, посредством CN. В качестве еще одного примера, -S- может быть окислена до -S(O)- и/или -S(O)2-. В качестве еще одного другого примера, ненасыщенная связь, такая как С=С или С≡С, может быть восстановлена до насыщенной связи посредством гидрогенизации. В некоторых вариантах осуществления, фрагмент первичного амина или вторичного амина (присутствующий на группе-заместителе, такой как R1 - R16, и так далее) может быть превращен в амидный, сульфонамидный, мочевинный, или тиомочевинный фрагмент посредством его реакционного взаимодействия с соответствующим реагентом, таким как хлорангидридное, сульфонилхлоридное, изоцианатное, или тиоизоцианатное соединение. Таким образом, соединение Формулы I (такое как соединение 3-3 схемы 3), имеющее заместитель, который содержит функциональную группу, может быть превращено в другое соединение формулы I, имеющее другую группу-заместитель.
Как используют в этом документе, термин «реакционное взаимодействие» относится к приведению обозначенных химических реагентов в контакт для того, чтобы произошло химическое превращение, в ходе которого образуется соединение, отличающееся от любого первоначально введенного в систему. Реакционное взаимодействие может протекать в присутствии или в отсутствии растворителя.
Химическая обработка с сохранением действующих начал растений
В некоторых вариантах осуществления, обеспечивают способ получения набора химических соединений из биологического экстракта, такого как имбирное масло.
Способ изобретения, которому дали термин «химическая обработка с сохранением действующих начал растений», как правило, применим ко всем биологическим экстрактам, в частности, к природным растительным экстрактам, универсальным или лекарственным. Смотри, например, патент: US20080193574, и международную публикацию: WO2008042755, каждый из которых включен в этот документ путем ссылки в полном своем объеме. Химическая обработка с сохранением действующих начал растений представляет собой способ, который позволяет получить новые неприродные подобные лекарству соединения из легко доступных природных материалов. В общем и целом, «химическая обработка с сохранением действующих начал растений» природных экстрактов в сочетании с предварительным фракционированием химически обработанных экстрактов облегчает успешный биохимический скрининг экстрактов путем разрушения реакционноспособных природных соединений, которые производят ложноположительные результаты в биохимических анализах. Химическая обработка с сохранением действующих начал растений дает новые подобные прототипу и подобные лекарству соединения, и протокол реактивного аминирования, описанный в этом документе, может давать структурно разнообразные азотсодержащие продукты, которые в особенности являются подобными прототипу и подобными лекарству.
В некоторых вариантах осуществления настоящего изобретения, способ получения химических соединений из биологических экстрактов приводят в качестве примера на схеме 5а ниже. Согласно способу, сначала, обеспечивают биологический экстракт, например, растительный экстракт, где биологический экстракт имеет одно или более биологических соединений, где каждое биологическое соединение имеет одну или более реакционноспособных электрофильных групп. Далее, биологические соединения в биологическом экстракте подвергают реакции с амином для внедрения амина в биологические соединения. Далее, биологические соединения, имеющие внедренный амин, подвергают реакции с восстанавливающим агентом для восстановления промежуточных иминных и енаминных соединений и получения одного или более азотсодержащих химических соединений. Таким образом, получающиеся в результате азотсодержащие химические соединения представляют собой производные биологических соединений в биологическом экстракте. В некоторых вариантах осуществления, биологические соединения в биологическом экстракте представляют собой соединения, имеющие кетоны и альдегиды, которые подвергают реакции с различными аминами. За этой реакцией следует восстановление гидридов промежуточных иминов и енаминов с обеспечением вторичных и третичных аминов. Реакция кетонов и альдегидов с аминами, с последующим восстановлением с получением иминов и енаминов, известна в данной области.
Схема 5a
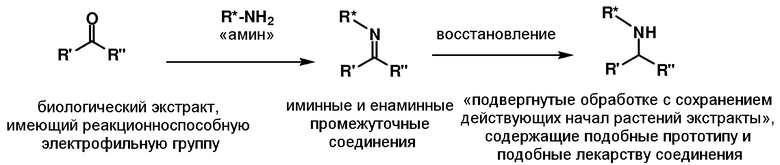
R' и R'' представляют собой ряд заместителей, которые составляют биологическое соединение; и
R* представляет собой ряд заместителей, которые, вместе с азотом, составляют аминное соединение.
В способе химической обработки с сохранением действующих начал растений, описанном в этом документе, применяют биологический экстракт, с использованием многих реагентов, для эффективного получения набора азотсодержащих химических соединений. Легкая коммерческая доступность многих аминов с низкой молекулярной массой для использования в качестве исходных реагентов в ряду реактивного аминирования дает возможность разработать много различных и структурно разнообразных подобных лекарству для центральной нервной системы смесей из одного и того же природного экстракта. Подходящие амины для применения в способе настоящего изобретения выбирают из группы, состоящей из первичных аминов, вторичных аминов, циклических аминов, пирролидина, и аминокислот. Подходящие восстанавливающие агенты для использования в способе настоящего изобретения выбирают из группы гидридных восстанавливающих агентов, включающей боргидрид натрия, триацетоксиборгидрид натрия, и алюмогидрид лития, но не ограниченной этим.
Способ может дополнительно включать прекращение реакции посредством реагента для прекращения реакции, где реагент для прекращения реакции выбирают из группы, состоящей из бикарбоната натрия, карбоната натрия, сульфата натрия, декагидрата сульфата натрия. Способ также может дополнительно включать выделение одного или более азотсодержащих химических соединений, в очищенной или в неочищенной форме. Получающееся в результате азотсодержащее химическое соединение затем может быть подвергнуто скринингу или испытанию на биологическую активность.
Процесс химической обработки с сохранением действующих начал растений посредством реактивного аминирования, описанный в этом документе, разрушает реакционноспособные электрофилы в природном экстракте, включая кетоны, как в гингеролах, и превращает их в химически стабильные соединения, такие как амины. Получающиеся в результате подвергнутые обработке экстракты содержат как природные соединения, так и новые неприродные азотсодержащие аминные продукты, которые являются потенциальными кандидатами в лекарство. В случае экстрактов гингерола, азотсодержащие аминные продукты являются потенциальными лекарственными средствами для центральной нервной системы.
Для цели этого раскрытия, следующие термины имеют следующие значения.
Термин «биологическое соединение», используемый в этом документе, относится к химическому соединению, которое встречается в природе.
Термин «биологический экстракт», используемый в этом документе, относится к экстракту из биологического образца, такому как растительный экстракт, или другой экстракт из органического материала, содержащий химические соединения, которые встречаются в природе.
Термин «реакционноспособная электрофильная группа», как используют в этом документе, относится к атому или группе атомов, который(ая) обладает способностью вступать в реакцию с нуклеофилом.
Термин «азотсодержащее производное», используемый в этом документе, представляет те производные, которые содержат атом азота, где атом азота является замещающим другой атом, такой как кислород, в исходном соединении.
В одном варианте осуществления, конкретный пример процесса химической обработки с сохранением действующих начал растений показан на схеме 5 ниже. Схема 5 показывает протокол химической обработки с сохранением действующих начал растений посредством двухстадийного реактивного аминирования, выполняемый на имбирном масле и на имбирной олеосмоле в соответствии с одним вариантом осуществления способа, где имбирное масло или гингерол, содержащие кетон 5-1, превращают в амин 5-4. В соответствии со способом, показанным на схеме 5, имбирное масло (экстракт из имбиря, содержащий кетон 5-1 и другие молекулы, имеющиеся в природном имбире) подвергают реакции с амином 5-2 с получением соединения 5-3. Затем, получающееся в результате соединение 5-3 восстанавливают, посредством восстанавливающего агента, такого как боргидрид, с получением азотсодержащего соединения 5-4 (сырой продукт реакции также включает другие химические соединения).
Схема 5
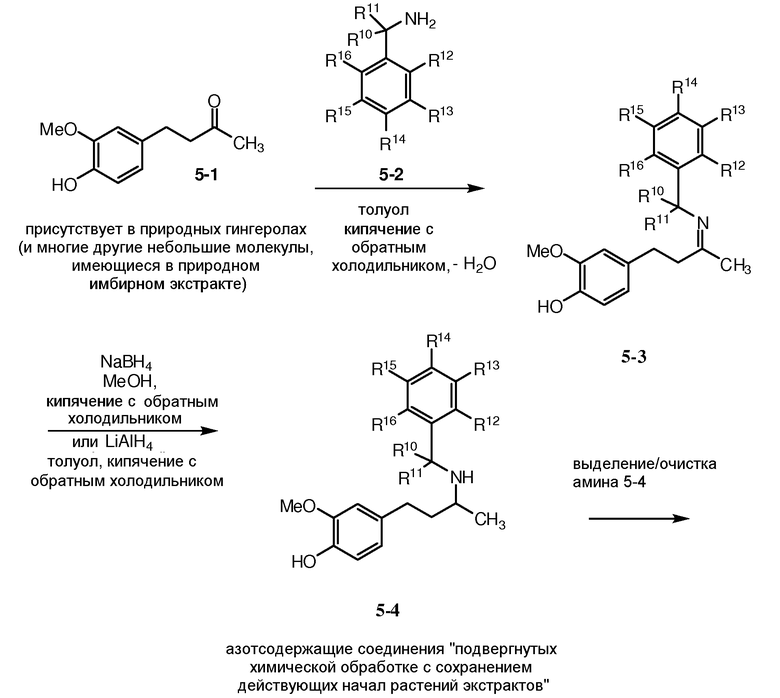
На следующей стадии способа, амин 5-4 выделяют/очищают из экстракта (сырой продукт реакции двухстадийного реактивного аминирования). Подвергнутые химической обработке с сохранением действующих начал растений экстракты могут быть подвергнуты фракционированию посредством флэш-хроматографии. Фракция, которая содержит амин 5-4, может подвергаться дополнительной(ому) очистке/выделению в соответствии со способами, известными специалистам в данной области. Далее может следовать дополнительное выделение и охарактеризовывание фракции, которая содержит амин 5-4. Выделенный амин 5-4 испытывают на его биологическую активность, например, теми способами, которые описаны в этом документе.
Некоторые примеры бензиламина 5-2, используемого в процессе химической обработки с сохранением действующих начал растений данного изобретения, который показан на схеме 5, включают:
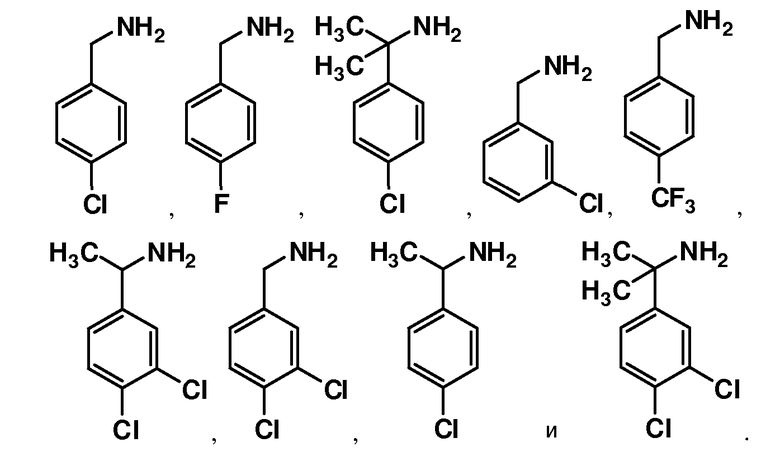
Новые соединения-прототипы, вырабатываемые посредством этого способа химической обработки с сохранением действующих начал растений, также могут быть получены синтетическими способами, описанными в этом документе.
В некоторых вариантах осуществления, производные имбирного масла, такие как амин 5-4, обладают ингибирующей активностью в отношении бета-секретазы, и/или ингибируют продуцирование амилоида, скопление амилоида, активность/действие Абета-олигомеров на нейроны (такие как нейроны в мозге), агрегацию амилоида, связывание амилоида (в том числе олигомера амилоида), или отложение амилоида. Эти соединения являются полезными терапевтическими средствами для лечения и предупреждения снижения когнитивных способностей, продуцирования амилоида, нейродегенерации, и болезни Альцгеймера.
Способы
В некоторых вариантах осуществления, соединения настоящего изобретения ингибируют, лечат, или подавляют (частично ингибируют) связывание амилоида (включая Абета-олигомеры) с нейронами (такими как нейроны в мозге) и являются полезными в ингибировании, лечении, и в подавлении снижения когнитивных способностей и/или болезни Альцгеймера. В некоторых вариантах осуществления, соединения настоящего изобретения ингибируют, лечат, или подавляют (частично ингибируют) один или более процессов, включающих агрегацию амилоида, связывание олигомера амилоида, и отложение амилоида. В некоторых вариантах осуществления, соединения настоящего изобретения ингибируют, лечат, или подавляют (частично ингибируют) отложение амилоида. В некоторых вариантах осуществления, соединения настоящего изобретения ингибируют, лечат, или подавляют (частично ингибируют) активность/воздействие Абета-олигомеров на нейроны (такие как нейроны в мозге) и являются полезными в ингибировании, лечении, и в подавлении снижения когнитивных способностей и/или болезни Альцгеймера. В некоторых вариантах осуществления, соединения настоящего изобретения ингибируют, лечат, или подавляют (частично ингибируют) активность/действие Абета-олигомеров на нейроны (такие как нейроны в мозге) посредством деструкции Абета-олигомеров, ингибирования связывания Абета-олигомеров с нейронами, и/или противодействия механизмам действия сигнальной трансдукции, инициированным связыванием Абета-олигомеров.
В некоторых вариантах осуществления, соединения показывают активность в анализе активности бета-секретазы и являются полезными в ингибировании, лечении, и в подавлении снижения когнитивных способностей и болезни Альцгеймера. В некоторых вариантах осуществления, производное имбирного масла представляет собой соединение в очищенной и в выделенной форме (например, со степенью чистоты более, чем 80%, 85%, 90%, 95%, 98%, или 99% по массе). Соединения и способы, описанные в этом документе, могут быть применены для лечения одного или более симптомов снижения когнитивных способностей и/или болезни Альцгеймера, таких как потеря памяти, спутанность сознания, помутнение сознания, изменения личности, дезориентация, и потеря языковых навыков и умений. Дополнительно, соединения и способы, описанные в этом документе, могут быть полезными в ингибировании, лечении, и/или в подавлении снижения когнитивных способностей и/или болезни Альцгеймера путем восстановления долговременной потенциации синаптической передачи, и/или путем ингибирования, лечения, или подавления одного или обоих состояний, включающих нейродегенерацию и общий амилоидоз, более конкретно, посредством ингибирования, лечения, или подавления одного или более процессов, включающих продуцирование амилоида, скопление амилоида, агрегацию амилоида, связывание амилоида (в том числе олигомера амилоида), и отложение амилоида.
В некоторых вариантах осуществления, соединения изобретения могут ингибировать, лечить, или подавлять один или более процессов, включающих продуцирование амилоида, скопление амилоида, агрегацию амилоида, связывание олигомеров амилоида, и отложение амилоида. В некоторых вариантах осуществления, соединения изобретения могут восстанавливать долговременную потенциацию синаптической передачи, ингибировать, лечить, или подавлять одно или более состояний, включающих нейродегенерацию и общий амилоидоз.
В некоторых вариантах осуществления, соединения настоящего изобретения ингибируют, лечат, или подавляют (частично ингибируют) один или более процессов, включающих агрегацию амилоида, связывание олигомеров амилоида, и отложение амилоида. В некоторых вариантах осуществления, соединения настоящего изобретения ингибируют (частично ингибируют) отложение амилоида. В некоторых вариантах осуществления, соединения настоящего изобретения ингибируют, лечат, или подавляют (частично ингибируют) связывание амилоида (включая Абета-олигомеры) с нейронами (такими как нейроны в мозге). В некоторых вариантах осуществления, соединения настоящего изобретения являются полезными в ингибировании, лечении, или в подавлении снижения когнитивных способностей и/или болезни Альцгеймера.
В некоторых вариантах осуществления, соединения настоящего изобретения ингибируют активность бета-секретазы. В некоторых вариантах осуществления, соединения изобретения могут быть применены в способах ингибирования активности бета-секретазы посредством контактирования бета-секретазы с любым одним или более соединениями или композициями, описанными в этом документе.
Другой аспект настоящего изобретения имеет отношение к способам лечения снижения когнитивных способностей и/или болезни Альцгеймера у субъекта (например, пациента) путем введения субъекту терапевтически эффективного(ой) количества или дозы соединения настоящего изобретения или его фармацевтической композиции.
Термин «лечение заболеваний/нарушений» в этом документе включает лечение одного или более симптомов, сопутствующих заболеваниям/нарушениям, например, симптомов снижения когнитивных способностей и/или болезни Альцгеймера.
Как используют в этом документе, термин «контактирование» относится к приведению в контакт упомянутых фрагментов в системе in vitro или в системе in vivo. Например, «контактирование» бета-секретазы или нервной клетки (или нервной клетки в присутствии одного или более олигомеров бета-амилоида) с соединением изобретения включает введение соединения настоящего изобретения субъекту или пациенту, такому как человек, имеющему бета-секретазу или нервную клетку, а также, например, введение соединения изобретения в образец, содержащий клеточный или очищенный препарат, содержащий бета-секретазу или нервную клетку (или нервную клетку в присутствии одного или более олигомеров бета-амилоида).
Как используют в этом документе, термин «субъект» или «пациент», используемый взаимозаменяемо, относится к любому животному, включая млекопитающих, предпочтительно мышей, крыс, других грызунов, кроликов, собак, кошек, свиней, крупный рогатый скот, овец, лошадей, или приматов, и наиболее предпочтительно людей.
Как используют в этом документе, фраза «терапевтически эффективное количество» относится к количеству активного соединения или фармацевтического средства, которое вызывает биологическую или целебную реакцию, которой добивается исследователь, ветеринар, лечащий доктор или врач-консультант в ткани, в системе, у животного, у субъекта или человека.
Как используют в этом документе, термин «процедура лечения» или «лечение» относится к одному или более вариантам воздействия на заболевание, включающим (1) предупреждение заболевания; например, предупреждение заболевания, состояния или нарушения у субъекта, который может быть предрасположен заболеванию, состоянию или нарушению, но еще не испытывает или не проявляет патологию или симптоматологию заболевания; (2) ингибирование/замедление заболевания; например, ингибирование/замедление заболевания, состояния или нарушения у субъекта, который испытывает или проявляет патологию или симптоматологию заболевания, состояния или нарушения; и (3) уменьшение интенсивности симптомов заболевания; например, уменьшение интенсивности симптомов заболевания, состояния или нарушения у субъекта, который испытывает или проявляет патологию или симптоматологию заболевания, состояния или нарушения (то есть, инициирование обратного развития патологии и/или симптоматологии), например, снижение тяжести заболевания или полное прекращение/вылечивание заболевания. Как используют в этом документе, процедура лечения заболевания дополнительно включает лечение одного или более симптомов, сопутствующих заболеванию.
Комбинированные методы терапии
В некоторых вариантах осуществления, один или более дополнительных фармацевтических средств для лечения снижения когнитивных способностей и/или болезни Альцгеймера могут быть применены в комбинации с соединениями настоящего изобретения для лечения снижения когнитивных способностей и/или болезни Альцгеймера. Один или более дополнительных фармацевтических средств могут быть введены пациенту одновременно или последовательно.
Фармацевтические составы и лекарственные формы
В некоторых вариантах осуществления, соединения изобретения могут быть введены в форме фармацевтических композиций. Эти композиции могут быть получены способом, хорошо известным в фармацевтической области, и могут быть введены разнообразными путями, в зависимости от того, желательно ли местное либо системное лечение, и от зоны, которая подлежит лечению. Введение может быть местным (топическим) (включая трансдермальное, эпидермальное, офтальмическое введение и введение в мембраны слизистой оболочки, в том числе интраназальную, вагинальную и ректальную доставку), пульмональным (например, посредством ингаляции или инсуффляции порошков или аэрозолей, в том числе с помощью небулайзера; интратрахеального или интраназального введения), пероральным или парентеральным. Парентеральное введение включает внутривенную, внутриартериальную, подкожную, интраперитонеальную внутримышечную или инъекцию или инфузию; или интракраниальное, например, интратекальное или интравентрикулярное, введение. Парентеральное введение может быть сделано в форме единой болюсной дозы, или может быть выполнено, например, с помощью перфузионного насоса с непрерывной подачей. Фармацевтические композиции и составы для местного введения могут включать трансдермальные пластыри, мази, лосьоны, крема, гели, капли, суппозитории, спреи, жидкости и порошки. Обычно применяемые фармацевтические носители, водные, порошковые или масляные основы для лекарства, загустители и тому подобное могут быть необходимы или желательны. Покрытые кондомы, перчатки и тому подобное также могут быть полезны.
Варианты осуществления этого изобретения также включают фармацевтические композиции, которые содержат, в качестве активного ингредиента, одно или более соединений вышеупомянутого изобретения в комбинации с одним или более фармацевтически приемлемыми носителями (эксципиентами). При изготовлении композиций изобретения, активный ингредиент обычно смешивают с эксципиентом, разбавляют эксципиентом или помещают в пределах такого носителя в форме, например, капсулы, саше, бумаги, или другого контейнера. В том случае, когда эксципиент служит в качестве разбавителя, он может быть твердым, полутвердым, или жидким материалом, который действует в качестве среды для лекарства, носителя или среды-основы для активного ингредиента. Так, композиции могут быть в форме таблеток, пилюль, порошков, лекарственных леденцов для рассасывания, пакетов-саше, крахмальных капсул для приема лекарств, эликсиров, суспензий, эмульсий, растворов, сиропов, аэрозолей (в форме твердого вещества или в жидкой среде), мазей, содержащих, например, вплоть до 10% по массе активного соединения, мягких и твердых желатиновых капсул, суппозиториев, стерильных инъекцируемых растворов, и стерильных расфасованных порошков.
При приготовлении состава, активное соединение может быть измельчено с обеспечением соответственного размера частиц до объединения с другими ингредиентами. Если активное соединение является практически нерастворимым, то оно может быть измельчено до размера частиц менее чем 200 меш. Если активное соединение является в значительной мере водорастворимым, размер частиц может быть скорректирован и доведен посредством измельчения до, например, 40 меш, с обеспечением в значительной мере однородного распределения в составе.
Соединения изобретения могут быть измельчены с использованием известных методик измельчения, таких как мокрое измельчение с получением размера частиц, подходящего для формования таблеток, и для приготовления других типов составов. Тонко измельченные (в форме наночастиц) препараты соединений изобретения могут быть приготовлены посредством процессов, известных в данной области, например, смотри Международную заявку на патент: International Patent Application No. WO 2002/000196.
Некоторые примеры подходящих эксципиентов включают лактозу, декстрозу, сахарозу, сорбит, маннит, крахмалы, аравийскую камедь, фосфат кальция, альгинаты, трагакантовая камедь, желатин, силикат кальция, микрокристаллическую целлюлозу, поливинилпирролидон, целлюлозу, воду, сироп, и метилцеллюлозу. Составы могут дополнительно включать: скользящие вещества, такие как тальк, стеарат магния, и минеральное масло; смачивающие вещества; эмульгирующие и суспендирующие вещества; консервирующие вещества, такие как метил- и пропилгидрокси-бензоаты; подслащивающие вещества; и ароматизирующие вещества. Композиции изобретения могут быть составлены так, чтобы обеспечить быстрое, замедленное или отсроченное высвобождение активного ингредиента после введения пациенту с применением известных в данной области методик.
Композиции могут быть составлены с приготовлением стандартной дозированной лекарственной формы, где каждая дозировка содержит от приблизительно 5 до приблизительно 1000 мг (1 г), чаще приблизительно 100 - приблизительно 500 мг, активного ингредиента. Термин «стандартные дозированные лекарственные формы» относится к физически дискретным единицам, подходящим в качестве одноразовых дозировок для человеческих субъектов и других млекопитающих, где каждая единица содержит заданное количество активного вещества, вычисленное для получения желательного терапевтического эффекта, в сочетании с подходящим фармацевтическим эксципиентом.
Активное соединение может быть эффективным в широком диапазоне дозировок и может быть, как правило, введено в фармацевтически эффективном количестве. Например, дозировка активных соединений изобретения, которая применяется для лечения пациента (например, взрослого человека), нуждающегося в таком лечении, может находиться в диапазоне от 0,1 до 3000 мг в день, в зависимости от пути и частоты введения. Такая дозировка соответствует 0,001-50 мг/кг в день. В некоторых вариантах осуществления, дозировка активных соединений изобретения, которая применяется для лечения пациента (например, взрослого человека), нуждающегося в таком лечении, может находиться в диапазоне от 1 до 2000 мг в день, от 1 до 1000 мг в день, от 10 до 1000 мг в день, или от 10 до 500 мг в день. Следует, однако, понимать, что количество фактически вводимого соединения обычно будет определяться врачом, в соответствии с релевантными обстоятельствами, включая состояние, которое подлежит лечению, выбранный путь введения, вводимое соединение как таковое, возраст, вес, и реакцию конкретного пациента, тяжесть симптомов пациента, и тому подобное.
Для приготовления твердых композиций, таких как таблетки, основной активный ингредиент может быть смешан с фармацевтическим эксципиентом с получением твердой композиции предварительного состава, содержащей гомогенную смесь соединения настоящего изобретения. В том случае, когда рассматривают эти композиции предварительного состава как гомогенные, активный ингредиент обычно является равномерно диспергированным по всему объему композиции, так что композиция может быть легко поделена на одинаково эффективные стандартные дозированные лекарственные формы, такие как таблетки, пилюли и капсулы. Этот твердый предварительный состав затем делят на стандартные дозированные лекарственные формы типа, который описан выше, содержащие, например, от приблизительно 0,1 до приблизительно 1000 мг активного ингредиента настоящего изобретения.
Таблетки или пилюли настоящего изобретения могут быть покрыты или иным образом компаундированы с обеспечением лекарственной формы, предоставляющей преимущество пролонгированного действия. Например, таблетки или пилюли могут содержать компонент с внутренней дозировкой и с внешней дозировкой, где последний находится в форме конверта, расположенного поверх предшествующего. Два компонента могут быть разделены кишечнорастворимым слоем, который служит для того, чтобы воспрепятствовать распадаемости в желудке и позволить внутреннему компоненту пройти в неизменном виде в двенадцатиперстную кишку или иметь отсроченное высвобождение. Для таких кишечнорастворимых слоев или покрытий могут быть использованы разнообразные вещества, такие как вещества, включающие ряд полимерных кислот и смеси полимерных кислот с такими веществами как шеллак, цетиловый спирт, и ацетат целлюлозы.
Жидкие формы, в которых могут быть включены соединения и композиции настоящего изобретения, для перорального введения или для введения посредством инъекции, включают водные растворы, подходяще ароматизированные сиропы, водные или масляные суспензии, и ароматизированные эмульсии с пищевыми маслами, такими как хлопковое масло, кунжутное масло, кокосовое масло, или арахисовое масло, а также эликсиры и подобные фармацевтические среды для лекарства.
Композиции для ингаляции или инсуффляции включают растворы и суспензии в фармацевтически приемлемых, водных или органических растворителях, или в смесях этих растворителей, и порошки. Жидкие или твердые композиции могут содержать подходящие фармацевтически приемлемые эксципиенты, которые описаны выше. В некоторых вариантах осуществления, композиции вводят пероральным или назальным респираторным путем для местного или системного воздействия. Композиции могут быть распылены посредством использования инертных газов. Распыленные растворы могут вдыхаться непосредственно из распыляющего устройства, или распыляющее устройство может быть присоединено к камере с дыхательными масками, или к дыхательной машине с перемежающимся положительным давлением. Растворные, суспензионные, или порошковые композиции могут быть введены перорально или назально из устройств, которые доставляют состав подходящим способом.
Количество соединения или композиции, вводимое пациенту, будет варьироваться в зависимости от того, что вводится, от цели введения, такой как профилактика или терапия, от состояния пациента, от способа введения, и тому подобного. В терапевтических применениях, композиции могут быть введены пациенту, уже имеющему заболевание, в количестве, достаточном для вылечивания или, по меньшей мере, для частичного блокирования симптомов заболевания и его осложнений. Эффективные дозы будут зависеть от стадии заболевания, подлежащей лечению, а также от заключения лечащего врача, в зависимости от факторов, таких как тяжесть заболевания, возраст, вес и общее состояние пациента, и тому подобное.
Композиции, введенные пациенту, могут быть в форме фармацевтических композиций, описанных выше. Эти композиции могут быть простерилизованы посредством обычно применяемых методов стерилизации, или могут быть подвергнуты стерильной фильтрации. Водные растворы могут быть расфасованы для применения так как есть, или подвергнуты лиофилизации, где лиофилизованный препарат соединяют со стерильным водным носителем перед введением. Значения рН препаратов соединения обычно будут находиться между 3 и 11, более предпочтительно от 5 до 9 и наиболее предпочтительно от 7 до 8. Будет ясно, что использование некоторых из вышеупомянутых эксципиентов, носителей, или стабилизаторов будет приводить к получению фармацевтических солей.
Терапевтическая дозировка соединений настоящего изобретения может варьироваться в соответствии, например, с конкретным применением, для которого выполняют лечение, со способом введения соединения, здоровья и состояния пациента, и заключения лечащего врача. Доля или концентрация соединения изобретения в фармацевтической композиции может варьироваться в зависимости от ряда факторов, включающих дозировку, химические характеристики (например, гидрофобность), и путь введения. Например, соединения изобретения могут быть обеспечены в водном физиологическом буферном растворе, содержащем приблизительно 0,1 - приблизительно 10% (масса/объем) соединения для парентерального введения. Некоторые типичные диапазоны доз составляют от приблизительно 1 г/кг до приблизительно 1 г/кг массы тела в день. В некоторых вариантах осуществления, диапазон доз составляет от приблизительно 0,01 мг/кг до приблизительно 100 мг/кг массы тела в день. Дозировка, вероятно, зависит от таких переменных, как тип и степень прогрессирования заболевания или нарушения, общий статус здоровья конкретного пациента, относительная биологическая эффективность выбранного соединения, состав эксципиента, и путь введения лекарственного препарата. Эффективные дозы могут быть экстраполированы из кривых зависимости «доза-эффект», полученных в ходе испытаний систем in vitro или экспериментальных моделей на животных.
Композиции изобретения могут дополнительно включать одно или более дополнительных фармацевтических средств, таких как химиотерапевтическое, стероидное, противовоспалительное соединение, или иммунодепрессивное средство, примеры которых приведены выше в этом документе.
Меченые соединения и методы анализа
Другой аспект настоящего изобретения относится к меченым соединениям изобретения (меченные радиоактивным изотопом, меченные флуоресцином, и так далее), которые могли бы быть полезными не только в визуализации с помощью меченных радиоактивным изотопом соединений, но также в методах анализа, как in vitro, так и in vivo, для локализации и количественной оценки фермента в образцах ткани, в том числе человека, и для идентифицирования лигандов посредством ингибирования связывания меченого соединения. В связи с вышеизложенным, настоящее изобретение включает ферментные пробы, которые содержат такие меченые соединения.
Варианты настоящего изобретения дополнительно включают изотопно-меченные соединения изобретения. «Изотопно-меченное» или «меченное радиоактивными изотопами» соединение представляет собой соединение изобретения, где один или более атомов заменены или замещены атомом, имеющим атомную массу или массовое число, отличающую(ее)ся от атомной массы или массового числа, обычно обнаруживаемой(ого) в природе (то есть, природного происхождения). Подходящие радионуклиды, которые могут быть внедрены в соединения настоящего изобретения, включают 2Н (также обозначаемый как D для дейтерия), 3Н (также обозначаемый как Т для трития), 11С, 13С, 14С, 13N, 15N, 15O, 17O, 18O, 18F, 35S, 36Cl, 82Br, 75Br, 76Br, 77Br, 123I, 124I, 125I и 131I, но не ограничиваются этим. Радионуклид, который внедряется в соединения с получением меченных радиоактивным изотопом соединений, будет зависеть от конкретного применения того меченного радиоактивным изотопом соединения. Например, для радиорецепторного анализа и анализа конкурентного связывания с рецептором in vitro, соединения, которые включают 3Н, 14С, 82Br, 125I, 131I, 35S, будут, как правило, наиболее полезными. Для применений в визуализации с использованием радиоактивных меток, наиболее полезными будут, как правило, 11С, 18F, 125I, 123I, 124I, 131I, 75Br, 76Br или 77Br.
Понятно, что «меченное радиоактивным изотопом соединение» представляет собой соединение, которое имеет включенный, по меньшей мере, один радионуклид. В некоторых вариантах осуществления, радионуклид выбирают из 3Н, 14С, 125I, 35S и 82Br.
В некоторых вариантах осуществления, меченые соединения настоящего изобретения содержат флуоресцентную метку.
Синтетические способы для введения радиоактивных изотопов и флуоресцентных меток в органические соединения хорошо известны в данной области.
Меченое соединение изобретения (меченное радиоактивным изотопом, меченное флуоресцином, и так далее) может быть использовано в скрининговом исследовании на предмет идентифицирования/оценивания соединений. Например, новосинтезированное или идентифицированное соединение (то есть, испытуемое соединение), которое является меченым, может быть оценено на его способность связывать бета-секретазу или нервную клетку (или нервную клетку в присутствии одного или более олигомеров бета-амилоида) путем мониторинга изменения его концентрации при контактировании с бета-секретазой или с нервной клеткой (или с нервной клеткой в присутствии одного или более олигомеров бета-амилоида), посредством отслеживания метки. В качестве другого примера, испытуемое соединение (меченое) может быть оценено на его способность снижать связывание другого соединения, которое, как известно, связывает бета-секретазу или нервную клетку (то есть, стандартное соединение). В связи с этим, способность испытуемого соединения конкурировать со стандартным соединением в связывании с бета-секретазой или с нервной клеткой непосредственно коррелирует с его сродством к связыванию. И наоборот, в некоторых других скрининговых исследованиях, стандартное соединение является меченым, а испытуемые соединения являются немечеными. В соответствии с этим, отслеживают концентрацию меченого стандартного соединения для того, чтобы оценить конкуренцию между стандартным соединением и испытуемым соединением, и таким образом устанавливают относительное сродство к связыванию.
Наборы
Варианты осуществления настоящего изобретения также включают фармацевтические наборы, полезные, например, в лечении или предупреждении снижения когнитивных способностей и/или болезни Альцгеймера, которые включают один или более контейнеров, содержащих фармацевтическую композицию, содержащую терапевтически эффективное количество соединения изобретения. Такие наборы могут дополнительно включать, если желательно, один или более различных традиционных компонентов фармацевтических наборов, таких как, например, контейнеры с одним или более фармацевтически приемлемыми носителями, дополнительные контейнеры, и так далее, что будет ясно со всей очевидностью специалистам в данной области. В набор также могут быть включены инструкции, либо в форме листков-вкладышей, либо в форме этикеток, указывающих количества компонентов, которые должны быть введены, предписания для введения, и/или предписания для смешения компонентов.
Изобретение будет описано более подробно с помощью конкретных примеров. Следующие примеры предложены с иллюстративными целями, и не предназначены для ограничения изобретения никаким образом. Специалистам в данной области будет легко распознать ряд некритических параметров, которые могут быть изменены или модифицированы, с предоставлением в результате по существу тех же самых результатов. Некоторые соединения Примеров, как было обнаружено, должны ингибировать, лечить, или подавлять один или более процессов, включающих продуцирование амилоида, скопление амилоида, активность/воздействие Абета-олигомеров на нейроны (такие как нейроны в мозге), агрегацию амилоида, связывание олигомеров амилоида, и отложение амилоида, в соответствии с одним или более методами анализа, обеспеченными в этом документе. В некоторых дополнительных вариантах осуществления, некоторые соединения Примеров, как было обнаружено, должны ингибировать, лечить, или подавлять один или более процессов, включающих активность/воздействие Абета-олигомеров на нейроны (такие как нейроны в мозге), агрегацию амилоида, связывание амилоида (включая олигомер амилоида), и отложение амилоида, в соответствии с одним или более методами анализа, обеспеченными в этом документе.
В некоторых вариантах осуществления, соединение изобретения имеет значение IC50 менее, чем 100 мкМ, 50 мкМ, 20 мкМ, 15 мкМ, 10 мкМ, 5 мкМ, 1 мкМ, 500 нМ, 100 нМ, 50 нМ, или 10 нМ, в отношении ингибирования одного или более процессов, включающих активность/воздействие Абета-олигомеров на нейроны (такие как нейроны в мозге), агрегацию амилоида, связывание амилоида (включая олигомер амилоида), и отложение амилоида. В некоторых вариантах осуществления, соединение изобретения имеет значение IC50 менее чем 100 мкМ, 50 мкМ, 20 мкМ, 15 мкМ, 10 мкМ, 5 мкМ, 1 мкМ, 500 нМ, 100 нМ, 50 нМ, или 10 нМ, в отношении ингибирования активности/воздействия Абета-олигомеров на нейроны (такие как нейроны в мозге.
В некоторых вариантах осуществления, ингибирование, выраженное в процентах, для соединения изобретения в отношении одного или более процессов, включающих активность/воздействие Абета-олигомеров на нейроны (такие как нейроны в мозге), агрегацию амилоида, связывание амилоида (включая олигомер амилоида), и отложение амилоида, измеряли при концентрации от 10 нМ до 10 мкМ. В некоторых вариантах осуществления, измеренное ингибирование, выраженное в процентах, составляет приблизительно 1% - приблизительно 20%, приблизительно 20% - приблизительно 50%, приблизительно 1% - приблизительно 50%, или приблизительно 1% - приблизительно 80%.
Изобретение может быть оценено по некоторым аспектам со ссылкой на следующие примеры, предложенные с целью его иллюстрации, без его ограничения. Вещества, реагенты и тому подобное, что упоминается в следующих примерах, можно получить из коммерческих источников, если не отмечено иное.
ПРИМЕРЫ
Вещества и способы
Имбирное масло
Экстракт легкого масла из корня имбиря получают по технологии суперкритической углекислой экстракции.
Имбирная олеосмола
После экстракции корня имбиря посредством суперкритической углекислой экстракции получают тяжелое остаточное масло.
Пример 1
А. Отвечающая требованиям полного сохранения действующих начал растений Экстракция Имбирного Масла: Реакция имбирного масла с 4-хлорбензиламином с последующим восстановлением боргидридом натрия в метаноле и фракционированием с использованием колоночной хроматографии
Имбирное масло (10 г) растворяют в толуоле (250 мл) и добавляют 4-хлорбензиламин (3,4 г). Смесь поддерживают в атмосфере азота и нагревают при кипячении с обратным холодильником с удалением воды перегонкой с насадкой Дина-Старка в течение 16 часов. По истечении этого периода времени насадку Дина-Старка снимают, и реакционную смесь охлаждают до 0°С на ледяной бане. Добавляют порциями в течение 30 минут при энергичном перемешивании раствор боргидрида натрия (10 г) в метаноле (100 мл). По завершении добавления смесь нагревают и кипятят с обратным холодильником в течение 16 часов. После того реакционную смесь охлаждают до комнатной температуры и выливают в насыщенный водный раствор бикарбоната натрия (300 мл). Получающуюся в результате смесь концентрируют ротационным выпариванием, и водный остаток распределяется между водой и хлороформом. Хлороформный слой сушат над безводным сульфатом натрия и затем фильтруют и концентрируют. Затем продукты подвергают фракционированию с использованием колоночной хроматографии на силикагеле с применением элюента с градиентным составом от 100% хлороформа до смеси хлороформ:метанол (5:1). Продукт обнаруживают в относительно полярных фракциях посредством тонкослойной хроматографии (TLC). Фракции, содержащие продукт, объединяют и концентрируют, затем сушат под высоким вакуумом в течение ночи с обеспечением светлого коричневого масла (0,672 г). 1Н ЯМР (500 МГц, CDCl3) δ: 7,30-7,24 (м, 4H), 6,81 (д, J=7,8 Гц, 1H), 6,66-6,62 (м, 2H), 4,25 (ушир.с, 2H), 3,82 (с, 3H), 3,82 (д, J=13,2 Гц, 1H),3,72(д, J=13,2 Гц, 1H),2,73(м, 1H), 2,66-2,51 (м,1H), 1,86-1,78 (м, 1H), 1,72-1,63 (м, 1H), 1,62-1,51 (м, 1H), 1,17 (д, J=6,3 Гц, 3H). 13С ЯМР (125 МГц, CDCl3) δ: 146,6, 143,8, 133,9, 132,8, 129,9, 129,7, 128,6, 120,8, 114,5, 110,9, 55,8, 51,9, 50,2, 38,5, 31,9, 31,6, 29,7, 26,9, 22,6, 19,9. Данные аналитической Масс-спектрометрии (М+Н+): m/z 320,2.
1Н ЯМР (500 МГц, CD3OD) δ: 7,10-7,30 (м, 4H), 6,63 (ушир.с, 1H), 6,58 (м, 1H), 6,48 (м, 1H), 3,68 (с, 3H), 3,65 (м, 1H), 3,58 (м, 1H), 2,57 (м, 1H), 2,50 (м, 1H), 2,35 (м, 1H), 1,73 (м, 1H), 1,49 (м, 1H), 1,04 (д, 3H). 13С ЯМР (125 МГц, CD3OD) δ: 147,5, 145,3, 137,2, 133,3, 132,6, 129,9, 128,1, 120,4, 114,7, 111,6, 54,9, 51,3, 49,2, 37,7, 31,5, 18,0.
Соотношение масс имбирного масла и 4-хлорбензиламина, используемое в восстановительном аминировании, составляет приблизительно 3:1 (от 2,7:1 до 3,3:1). Величина химического сдвига в 1Н ЯМР-измерениях может варьироваться, например, вплоть до 0,2 миллионных долей (ppm). Величина химического сдвига в 13Н ЯМР-измерениях может варьироваться, например, вплоть до 0,5 миллионных долей (ppm). Метод аналитической Масс-спектрометрии может давать экспериментальную ошибку, равную +/- 0,3.
Определение степени чистоты
Степень чистоты продукта измеряют методом высокоэффективной жидкостной хроматографии (HPLC). Основной пик, соответствующий времени удерживания 2,22 минуты, показывает степень чистоты, составляющую более, чем приблизительно 80%, 85%, 90%, или 95%. Используемые условия HPLC изложены ниже.
Условия HPLC
Подвижная фаза А: 13,3 мМ раствор формиата аммония/6,7 мМ раствор муравьиной кислоты в воде
Подвижная фаза В: 6 мМ раствор формиата аммония/3 мМ раствор муравьиной кислоты в воде/CH3CN (1/9, объем/объем)
Колонка: Sinergi Fusion-RP 100A Mercury, 2×20 мм, 2,5 микрон (Phenomenex Part No. 00М-4423-В0_СЕ)
Градиентная программа: время удерживания RT=2,22 минуты
Величина степени чистоты продукта, также определяемая методом 1Н ЯМР, указывает на то, что продукт представляет собой единственное соединение со степенью чистоты выше 90% или 95%.
Определяют, что структура образца соединения 1 (или соединения примера 1) является следующей.
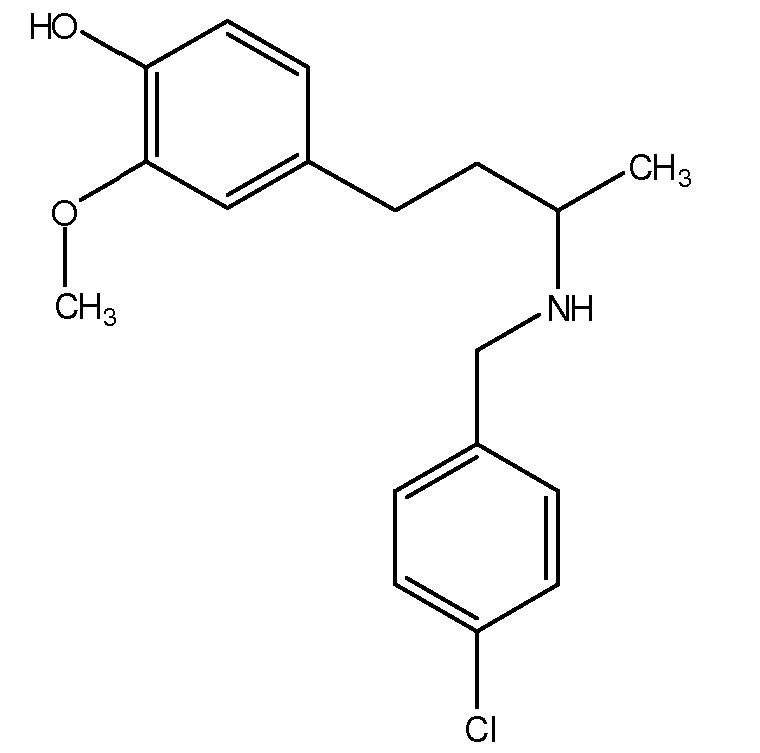
Соединение примера 1
4-(3-(4-Хлорбензиламино)бутил)-2-метоксифенол
В. Синтез по методу реактивного аминирования .
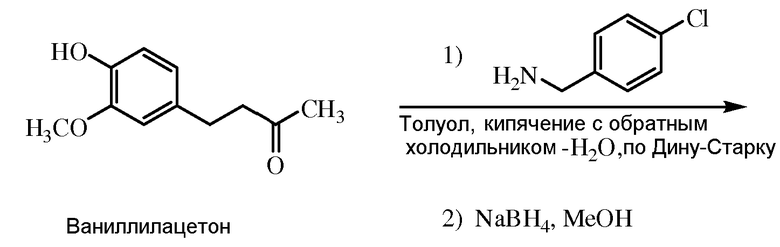
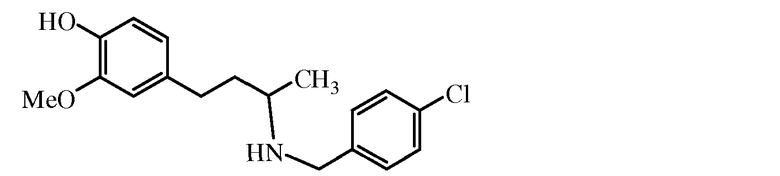
Ваниллиацетон (5,00 г, 25,7 ммоль) растворяют в толуоле (250 мл) и добавляют 4-хлорбензиламин (3,82 г, 27,0 ммоль). Смесь поддерживают в атмосфере азота и нагревают при кипячении с обратным холодильником с удалением воды перегонкой с насадкой Дина-Старка в течение 16 часов. По истечении этого периода времени насадку Дина-Старка снимают, и реакционную смесь охлаждают до 0°С на ледяной бане. Добавляют порциями в течение 30 минут при энергичном перемешивании раствор боргидрида натрия (5 г) в метаноле (100 мл). По завершении добавления смесь нагревают и кипятят с обратным холодильником в течение 16 часов. После того реакционную смесь охлаждают до комнатной температуры и выливают в насыщенный водный раствор бикарбоната натрия (300 мл). Получающуюся в результате смесь концентрируют ротационным выпариванием, и водный остаток распределяется между водой и хлороформом. Хлороформный слой сушат над безводным сульфатом натрия и затем фильтруют и концентрируют. Затем продукт очищают с использованием колоночной хроматографии на силикагеле с применением подвижной фазы, состоящей из смеси 5% аммиак-метанол в хлороформе. Фракции, содержащие продукт, объединяют и концентрируют, затем сушат под высоким вакуумом в течение ночи с обеспечением светлого коричневого масла (6,16 г, 75%). 1Н ЯМР, 13С ЯМР-данные, и масс-спектры продукта в значительной мере совпадают с 1Н ЯМР, 13С ЯМР-данными, и масс-спектрами продукта в примере 1, А (выполнено способом экстракции, отвечающим требованиям полного сохранения действующих начал растений).
Пример 2
А. Отвечающая требованиям полного сохранения действующих начал растений экстракция имбирного масла: реакция имбирного масла с 4-трифторметилбензиламином с последующим восстановлением боргидридом натрия в метаноле и фракционированием с использованием колоночной хроматографии
Имбирное масло (10 г) растворяют в толуоле (250 мл) и добавляют 4-трифторметилбензиламин (3,5 г). Смесь поддерживают в атмосфере азота и нагревают при кипячении с обратным холодильником с удалением воды перегонкой с насадкой Дина-Старка в течение 16 часов. По истечении этого периода времени насадку Дина-Старка снимают, и реакционную смесь охлаждают до 0°С на ледяной бане. Добавляют порциями в течение 30 минут при энергичном перемешивании раствор боргидрида натрия (10 г) в метаноле (100 мл). По завершении добавления смесь нагревают и кипятят с обратным холодильником в течение 16 часов. После того реакционную смесь охлаждают до комнатной температуры и выливают в насыщенный водный раствор бикарбоната натрия (300 мл). Получающуюся в результате смесь концентрируют ротационным выпариванием, и водный остаток распределяется между водой и хлороформом. Хлороформный слой сушат над безводным сульфатом натрия и затем фильтруют и концентрируют. Затем продукты подвергают фракционированию с использованием колоночной хроматографии на силикагеле с применением элюента с градиентным составом от 100% хлороформа до смеси хлороформ:метанол (5:1). Продукт обнаруживают в относительно полярных фракциях посредством тонкослойной хроматографии (TLC). Фракции, содержащие продукт, объединяют и концентрируют, затем сушат под высоким вакуумом в течение ночи с обеспечением светлого коричневого масла (0,761 г). 1Н ЯМР (500 МГц, CDCl3) δ: 7,57 (д, J=7,8 Гц, 2H), 7,43 (д, J=7,9 Гц, 2H), 6,82 (д, J=7,3 Гц, 1H), 6,65 (м, 2H), 5,16-4,42 (ушир.c, 2H), 3,90 (д, J=13,7 Гц, 1H), 3,84 (c, 3H), 3,80 (д, J=13,7 Гц, 1H), 2,76-2,70 (м, 1H), 2,67-2,55 (м,2H), 1,84-1,77 (м, 1H), 1,69-1,63 (м, 1H), 1,17 (д, J=6,3 Гц, 3H). 13С ЯМР (125 МГц, CDCl3) δ: 146,7, 144,6, 143,9, 134,0, 129,1, 128,4, 127,5, 125,4, 125,3, 123,2, 120,8, 114,6, 111,0, 55,7, 52,1, 50,6, 38,8, 32,0, 20,1. Данные масс-спектрометрии с химической ионизацией MS (CI) m/z 353 (M+).
Соотношение масс имбирного масла и 4-трифторметилбензиламина, используемое в восстановительном аминировании, составляет приблизительно 3:1 (от 2,7:1 до 3,3:1). Величина химического сдвига в 1Н ЯМР-измерениях может варьироваться, например, вплоть до 0,2 миллионных долей (ppm). Величина химического сдвига в 13Н ЯМР-измерениях может варьироваться, например, вплоть до 0,5 миллионных долей (ppm). Метод аналитической Масс-спектрометрии может давать экспериментальную ошибку, равную +/-0,3.
Определение степени чистоты
Степень чистоты продукта измеряют методом высокоэффективной жидкостной хроматографии (HPLC). Основной пик, соответствующий времени удерживания 2,22 минуты, показывает степень чистоты, составляющую более чем приблизительно 80%, 85%, 90%, или 95%. Используемые условия HPLC изложены ниже.
Условия HPLC:
Подвижная фаза А: 13,3 мМ раствор формиата аммония/6,7 мМ раствор муравьиной кислоты в воде
Подвижная фаза В: 6 мМ раствор формиата аммония/3 мМ раствор муравьиной кислоты в воде/CH3CN (1/9, объем/объем)
Колонка: Sinergi Fusion-RP 100A Mercury, 2×20 мм, 2,5 микрон (Phenomenex Part No. 00М-4423-В0_СЕ)
Градиентная программа: время удерживания RT = 2,22 минуты
Величина степени чистоты продукта, также определяемая методом 1Н ЯМР, указывает на то, что продукт представляет собой единственное соединение со степенью чистоты выше 90% или 95%.
Определяют, что структура соединения из примера 2 (или соединения 2 из примера 2) является следующей.
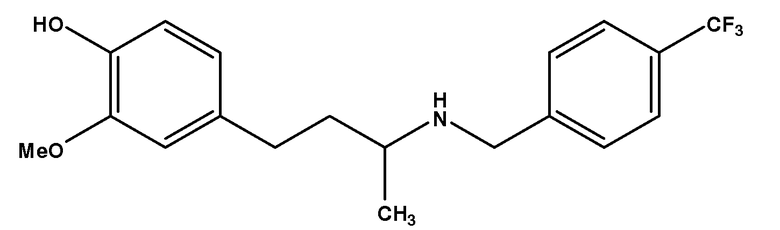
Соединение примера 2
4-(3-(4-(Трифторметил)бензиламино)бутил)-2-метоксифенол
В. Синтез по методу реактивного аминирования .

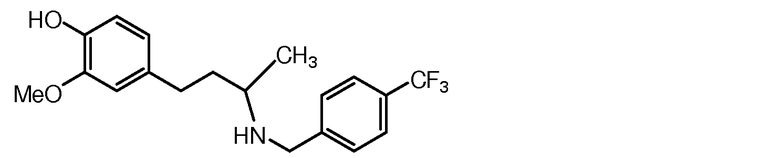
Ваниллиацетон (5,00 г, 25,7 ммоль) растворяют в толуоле (250 мл) и добавляют 4-трифторметилбензиламин (4,73 г, 27,0 ммоль). Смесь поддерживают в атмосфере азота и нагревают при кипячении с обратным холодильником с удалением воды перегонкой с насадкой Дина-Старка в течение 16 часов. По истечении этого периода времени насадку Дина-Старка снимают, и реакционную смесь охлаждают до 0°С на ледяной бане. Добавляют порциями в течение 30 минут при энергичном перемешивании раствор боргидрида натрия (5 г) в метаноле (100 мл). По завершении добавления смесь нагревают и кипятят с обратным холодильником в течение 16 часов. После того реакционную смесь охлаждают до комнатной температуры и выливают в насыщенный водный раствор бикарбоната натрия (300 мл). Получающуюся в результате смесь концентрируют ротационным выпариванием, и водный остаток распределяется между водой и хлороформом. Хлороформный слой сушат над безводным сульфатом натрия и затем фильтруют и концентрируют. Затем продукт очищают с использованием колоночной хроматографии на силикагеле с применением подвижной фазы, состоящей из смеси 5% аммиак-метанол в хлороформе. Фракции, содержащие продукт, объединяют и концентрируют, затем сушат под высоким вакуумом в течение ночи с обеспечением светлого коричневого масла (6,72 г, 74%). 1Н ЯМР, 13С ЯМР-данные, и масс-спектры продукта в значительной мере совпадают с 1Н ЯМР, 13С ЯМР-данными, и масс-спектрами продукта в примере 2, А (выполнено способом экстракции, отвечающим требованиям полного сохранения действующих начал растений).
Пример АА: Анализ экзоцитоза/анализ на основе 3-{4,5-диметилтиазол-2-ил}-2,5-дифенилтетразолий бромида (МТТ-тест)
Первичные нейроны от эмбрионов крыс Sprague-Dawley E18 высевают в оптимизированных концентрациях на 384-луночные планшеты в среде NB (Invitrogen). Нейроны поддерживают в культурах клеток в течение 3 недель, с подпитыванием среды NB дополнительным N2 (Invitrogen) дважды в неделю. В клетки вводят испытуемое соединение, после этого добавляют Среду для лекарства или препараты Абета-олигомера (1,5 мкМ), и инкубируют в течение 1-24 часов при 37°С в 5% СО2. Реагент для МТТ-теста (3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолий бромид) (Roche Molecular Biochemicals) разбавляют в забуференном фосфатом физиологическом растворе до концентрации 5 мг/мл. В каждую лунку добавляют 10 мкл МТТ-реагента для мечения, и инкубируют при 37°С в течение 1 часа, затем проводят визуализацию.
Каждый аналитический планшет обрабатывают таким образом, чтобы соединения подвергались испытанию с Абета-олигомером и без Абета-олигомера на каждом планшете. Такая схема исключает токсические или метаболически активные соединения на раннем этапе каскада скрининга (на уровне первичного подбора). Оценивают статистическую характеристику запланированной методики обработки планшетов для скрининга, и скрининг будет инициироваться, если текущая характеристика сохраняется.
Подобные методики анализа экзоцитоза/МТТ-теста могут быть обнаружены в литературе. Смотри, например, публикации: Liu Y, et. al., Detecting bioactive amyloid beta peptide species in Alzheimer's disease. J Neurochem. 2004 Nov; 91(3):648-56; Liu Y, and Schubert D. "Cytotoxic amyloid peptides inhibit cellular 3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide (MTT) reduction by enhancing MTT formazan exocytosis." J Neurochem. 1997 Dec; 69(6):2285-93; and Liu Y, and Schubert D. "Treating Alzheimer's disease by inactivating bioactive amyloid beta peptide" Curr. Alzheimer Res. 2006 Apr; 3(2): 129-35.
Экспериментальные методы контроля
Абета-олигомеры 1-42, изготовленные в соответствии с опубликованными способами [Смотри, например, Dahlgren et al., "Oligomeric and fibrillar species of amyloid-beta peptides differentially affect neuronal viability" J Biol Chem. 2002 Aug 30; 277(35): 32046-53. Epub 2002 Jun 10.; LeVine H 3rd. "Alzheimer's beta-peptide oligomer formation at physiologic concentrations" Anal Biochem. 2004 Dec 1; 335(1): 81-90; Shrestha et.al, "Amyloid beta peptide adversely affects spine number and motility in hippocampal neurons" Mol Cell Neurosci. 2006 Nov; 33(3): 274-82. Epub 2006 Sep 8; Puzzo et al., "Amyloid-beta peptide inhibits activation of the nitric oxide/cGMP/cAMP-responsive element-binding protein pathway during hippocampal synaptic plasticity" J Neurosci. 2005 Jul 20; 25(29): 6887-97; Barghorn et al., "Globular amyloid beta-peptide oligomer - a homogenous and stable neuropathological protein in Alzheimer's disease" J Neurochem. 2005 Nov; 95(3): 834-47. Epub 2005 Aug 31; Johansson et al., Physiochemical characterization of the Alzheimer's disease-related peptides A beta 1-42 Arctic and A beta 1-42wt. FEBS J. 2006 Jun; 2 73(12): 2618-30], а также Абета-олигомеры головного мозга (Смотри, например, публикации: Walsh et al., Naturally secreted oligomers of amyloid beta protein potently inhibit hippocampal long-term potentiation in vivo. Nature (2002). 416, 535-539; Lesne et al., A specific amyloid-beta protein assembly in the brain impairs memory. Nature. 2006 Mar 16; 440(7082):352-7; Shankar et al, Amyloid-beta protein dimers isolated directly from Alzheimer's brains impair synaptic plasticity and memory. Nat Med. 2008 Aug; 14(8): 837-42. Epub 2008 Jun 22) составляют позитивный контроль. Негативный контроль включает обработанные средой для лекарства нейроны, а также нейроны, обработанные раствором мемантина с концентрацией 28 мкМ. Мемантин дает 50% ингибирование действий олигомеров при этой дозе. Эти контроли, на каждом планшете, служат в качестве инструмента нормализации для калибровки выполнения анализа индивидуально для каждого планшета.
Первичные нейрональные культуры
Оптимальную плотность клетки определяют, исходя из реакции клеток на Абета-олигомеры с использованием анализа экзоцитоза в качестве считывающего средства данных, и иммуногистохимического анализа относительной доли клеток глии к нейронам в культурах клеток. Культуры клеток отслеживают еженедельно посредством иммуногистохимии и количественной оценки на основе обработки изображений для контролирования процентного содержания культур клеток, которые представляют собой нейроны и клетки глии (Глиальные клетки). Культуры клеток, содержащие более чем 20% клеток глии (позитивных к GFAP (глиальный фибриллярный кислый белок)) относительно нейронов (окрашивающиеся позитивно антителами против MAP2 (белки, ассоциированные с микротрубочками)) к периоду времени скрининга 21 день in vitro (21 DIV), отбрасываются как непригодные.
Препараты Абета-олигомеров
Пептид амилоида 1-42 человека получают в компании California Peptide, c выбором лота в зависимости от анализа контроля качества. Методы контроля качества препаратов олигомера состоят из методов Вестерн-блоттинга для определения диапазонов размера олигомера и относительных концентраций, и МТТ-теста для подтверждения ускорения экзоцитоза без токсичности. Токсичность отслеживают в каждом анализе, основанном на изображении, посредством количественной оценки морфологии ядра, визуализируемой с помощью ДНК-связывающего красителя DAPI (Invitrogen). Ядра, которые являются фрагментированными, как полагают, имеют место на поздней стадии апоптоза (Majno и Joris '95). Пептидные лоты, дающие необычные диапазоны размеров пептидов или существенную токсичность при стандартной концентрации 1,5 мкМ на нейронах, отбрасываются. Контрольные данные, основанные на планшетах - Оптимизация анализа будет завершена в том случае, когда обработанные с расширением планшеты достигают минимального значения статистически значимого двухкратного разделения данных для нейронов, обработанных средой для лекарства, и нейронов, обработанных Абета-олигомерами (р<0,01, t-критерий Стьюдента, неодинаковая дисперсия) по стандартной методике, с коэффициентом вариаций (CV) не более 10% между планшетами, эквивалентного его текущей характеристике.
Программное обеспечение для статистического анализа и анализ:
Обработку данных и анализ выполняют с помощью программного обеспечения для анализа изображений Cellomics VTI и автоматизированного программного обеспечения базы данных STORE. Из-за низкого динамического диапазона и вариабельности нейронов от лунки-к-лунке после трех недель в культуре клеток, выполняют статистические сравнения посредством парного анализа Tukey-Kramer для определения достоверности разделения результатов для соединения с Абета-олигомерами и для Абета-олигомеров как таковых, и результатов для соединения как такового и для среды для лекарства. Эти статистические данные более похожи на то, что наблюдают в испытании поведения животных, чем на z-статистические данные, которые использовали в течение прошедших двух десятилетий в высокопроизводительном скрининге. Способность зрелых первичных нейронов иметь более близкое сходство с электрофизиологически обусловленной сетью сигнальной трансдукции в мозге взрослого субъекта оправдывает стратегию скрининга. Будет установлен анализ мощности для ряда подвергающихся повторному скринингу лунок, что будет минимизировать ложноотрицательные результаты (например, N=4) и смещать сложность получения различения ложноположительных результатов от истинных результатов к скринингу подтверждения по типу «доза-реакция». Ранговый порядок соединений осуществляют на основе вторичного анализа механизма действия и физико-химических свойств, задаваемых структурами соединений. Некоторые испытуемые соединения существенно изменяют действия Абета-олигомеров, но не затрагивают нейрональный метаболизм.
Образец соединения 1 дозированно вводят в МТТ-тест и, как показано, оно блокирует инициированное Абета-олигомерами ускорение экзоцитоза со значением EC50, составляющим 10 мкМ, что указывает на то, что образец соединения 1 блокирует/подавляет активность/действие Абета-олигомера на нервные клетки.
Пример ВВ: Анализ связывания
Каждое испытуемое соединение вводят в планшет, после этого добавляют один или более Абета-олигомеров 1-42. Планшеты фиксируют посредством 3,7%-го раствора параформальдегида в забуференном фосфатом физиологическом растворе (PBS) в течение 15 минут. Затем планшет промывают три раза (×3) с помощью забуференного фосфатом физиологического раствора (PBS) в течение 5 минут каждый. Планшеты блокируют при комнатной температуре в течение 1 часа в 5%-ной сыворотке козла и 0,5%-ном растворе реагента Triton X-100 (номер CAS: 9002-93-1) в PBS. Первичные антитела (поликлональные антитела против MAP2, Millipore №AB5622, и моноклональные антитела против Бета-Амилоида Amyloid 6E10, Convance №SIG-39300) разбавляют 1:1000 5%-ным раствором сыворотки козла в PBS. Первичные антитела инкубируют либо в течение ночи при 4°С, либо в течение 1 часа при комнатной температуре. Затем планшет промывают три раза (×3) посредством PBS в течение 5 минут каждый. Вторичные антитела (поликлональные антитела Alex Flor 488, Invitrogen № А11008, и моноклональные антитела Alexa Flor 647, Invitrogen № А21235) разбавляют 1:1000 в 5%-ном растворе сыворотки козла в PBS. Вторичные антитела инкубируют при комнатной температуре в течение 1 часа. Планшеты промывают однократно забуференным фосфатом физиологическим раствором. Затем наносят краситель DAPI (4',6-диамидино-2-фенилиндол, Invitrogen) в концентрации 0,03 мкг/мкл и инкубируют при комнатной температуре в течение 5 минут, затем промывают забуференным фосфатом физиологическим раствором. Для анализа выполняют обработку изображения.
Подобные методики проведения анализа связывания могут быть обнаружены в литературе. Смотри, например, публикацию: Look GC, et. al. Discovery of ADDL - targeting small molecule drugs for Alzheimer's disease. Curr. Alzheimer Res. 2007 Dec; 4(5): 562-7. Обзор.
Препараты Абета-олигомеров
Пептид амилоида 1-42 человека получают в компании California Peptide, c выбором лота в зависимости от анализа контроля качества. Абета-олигомеры 1-42, изготовленные в соответствии с опубликованными способами [Смотри, например, "Oligomeric and fibrillar species of amyloid-beta peptides differentially affect neuronal viability" J Biol Chem. 2002 Aug 30; 277(35): 32046-53. Epub 2002 Jun 10.; LeVine H 3rd. "Alzheimer's beta-peptide oligomer formation at physiologic concentrations" Anal Biochem. 2004 Dec 1; 335(1): 81-90; Shrestha et.al, "Amyloid beta peptide adversely affects spine number and motility in hippocampal neurons" Mol Cell Neurosci. 2006 Nov; 33(3): 274-82. Epub 2006 Sep 8; Puzzo et al., "Amyloid-beta peptide inhibits activation of the nitric oxide/cGMP/cAMP-responsive element-binding protein pathway during hippocampal synaptic plasticity" J Neurosci. 2005 Jul 20; 25(29): 6887-97; Barghorn et al., "Globular amyloid beta-peptide oligomer - a homogenous and stable neuropathological protein in Alzheimer's disease" J Neurochem. 2005 Nov; 95(3): 834-47. Epub 2005 Aug 31; Johansson et al., Physiochemical characterization of the Alzheimer's disease-related peptides A beta 1-42 Arctic and A beta 1-42wt. FEBS J. 2006 Jun; 2 73(12): 2618-30], а также Абета-олигомеры головного мозга (Смотри, например, публикации: Walsh et al., Naturally secreted oligomers of amyloid beta protein potently inhibit hippocampal long-term potentiation in vivo. Nature (2002). 416, 535-539; Lesne et al., A specific amyloid-beta protein assembly in the brain impairs memory. Nature. 2006 Mar 16; 440(7082): 352-7; Shankar et al, Amyloid-beta protein dimers isolated directly from Alzheimer's brains impair synaptic plasticity and memory. Nat Med. 2008 Aug; 14(8): 837-42. Epub 2008 Jun 22) будут служить в качестве позитивного контроля. Методы контроля качества олигомерных препаратов состоят из методов Вестерн-блоттинга для определения диапазонов размера олигомеров и относительных концентраций, и МТТ-теста для подтверждения ускорения экзоцитоза без токсичности. Токсичность отслеживают в каждом анализе, основанном на изображении, посредством количественной оценки морфологии ядра, визуализируемой с помощью ДНК-связывающего красителя DAPI (Invitrogen). Ядра, которые являются фрагментированными, как полагают, имеют место на поздней стадии апоптоза (Majno и Joris Apoptosis, oncosis, and necrosis. An overview of cell death. Am. J. Pathol. 1995; 146: 3-16). Пептидные лоты, дающие необычные диапазоны размеров пептидов или значительную токсичность при стандартных концентрациях на нейронах, отбрасываются.
Обработка изображений
Изображения захватывают и анализируют с помощью платформы с автоматизированным микроскопом Cellomics VTI, с использованием алгоритма анализа профиля нейронов. Для статистического анализа, используют попарное сравнение средних по методу Tukey-Kramer'a при неравных дисперсиях выборок.
Вестерн-блоттинг
Образцы, содержащие Абета-олигомеры 1-42, разбавляют (1:5) в невосстанавливающем буферном растворе с образцом маркера для отслеживания фронта и хода разделения (Pierce №1859594). 30-Микролитровый (мкл) образец вводят в восемнадцати-луночный заранее залитый 4-15%-ный гель трис-HCl (BIORAD №345-0028). Электрофорез осуществляют в заранее залитой гелеобразной системе BIO-RAD Criterian с использованием буферного раствора трис-глицина при 125 вольтах (Вольт) в течение 90 минут. Гели блоттируют на 0,2 мкМ-ные нитроцеллюлозные мембраны в буферном растворе трис-глицина/10% метанола при 30 вольтах в течение 120 минут. Мембраны кипятят в течение 5 минут в растворе PBS (забуференный фосфатом физиологический раствор) и блокируют в течение ночи посредством раствора TBS/5% молока при 4°С. В мембрану вводят зонд с меченными пероксидазой хрена моноклональными антителами 6Е10-HRP (Covance № SIG-39345), разбавленными до 10 мкг/мл в растворе TBS/1% молока, в течение одного часа при комнатной температуре. Мембрану промывают три раза в течение 40 минут, каждый раз раствором TBS/0,05% детергента твин-20, и проявляют посредством реагента ECL (BIO-RAD №162-0112) в течение 5 минут. Получение изображения осуществляют на системе количественной визуализации и анализируют с помощью программного обеспечения AlphaView Q.
Фармакокинетические исследования
Фармакокинетические исследования проводят на приборе CEREP Inc. Of Redmond WA, в соответствии с их стандартными протоколами: пробы плазмы подвергают обработке с использованием осаждения в ацетонитриле и анализируют методом высокоэффективной жидкостной хроматографии в сочетании с масс-спектрометрией (HPLC-MS) или методом высокоэффективной жидкостной хроматографии в сочетании с тандемной масс-спектрометрией (HPLC-MS/MS). Записывают площади пиков, и определяют концентрации испытуемого соединения в неизвестных пробах плазмы с использованием соответствующей калибровочной кривой. Определяют регистрируемый линейный диапазон анализа, наряду с нижним пределом количественного анализа (LLQ).
ЯМР-спектроскопия и масс-спектрометрия
Активные фракции анализируют методом 1Н ЯМР (ЯМР-спектрометр Varian 500 МГц) и очищенные соединения охарактеризовывают с использованием комбинации одномерных и двумерных 1Н ЯМР-экспериментов и 13С ЯМР-экспериментов. Подтверждение структуры получают с использованием ЯМР-методов в комбинации с масс-спектрометрией низкого разрешения для определения молекулярной массы и в комбинации с масс-спектрометрией высокого разрешения (Ионная ловушка Thermo Finnigan LCQ) для определения композиции определенного состава.
Соединение 1 примера 1, как показано, частично блокирует связывание Абета-олигомерного лиганда с нейронами на 24% согласно анализу связывания (с использованием алгоритма обработки изображения).
Пример СС: Фармакокинетические исследования
Фармакокинетические исследования осуществляют в соответствии со следующими протоколами: пробы плазмы подвергают обработке с использованием осаждения ацетонитрилом и анализируют методом высокоэффективной жидкостной хроматографии в сочетании с масс-спектрометрией (HPLC-MS) или методом высокоэффективной жидкостной хроматографии в сочетании с тандемной масс-спектрометрией (HPLC-MS/MS). Записывают площади пиков, и определяют концентрации испытуемого соединения в неизвестных пробах плазмы с использованием соответствующей калибровочной кривой. Определяют регистрируемый линейный диапазон анализа, наряду с нижним пределом количественного анализа (LLQ). Например, определяют, что соединение 1 примера 1 имеет период полураспада 46 минут в плазме крыс при внутривенной инъекции в дозе 1 мг/кг.
Пример DD: Основанный на первичных нейронах функциональный скрининговый анализ для обнаружения блокаторов Абета-олигомеров с небольшими молекулами
Первичные нейроны крыс, выращиваемые в течение, по меньшей мере, 3 недель in vitro, выбирают в качестве основы для проведения этого скринингового анализа. Эти нейроны экспрессируют полный комплимент синаптических белков, характерных для нейронов в зрелом мозге, и показывают сложную сеть зависимой от активности передачи электрического сигнала. Нейроны и клетки глии в таких культурах клетки имеют молекулярные сети передачи сигнала, показывающие превосходное совмещение с электрической схемой здорового мозга, и по этой причине использовались в течение двух десятилетий в качестве модельной системы для обучения и запоминания (Смотри, например, публикации: Kaech S., Banker G. Culturing hippocampal neurons. Nat Protoc. 2006; 1(5): 2406-15. Epub 2007 Jan 11; Смотри также публикацию: Craig AM, Graf ER, Linhoff MW. How to build a central synapse: clues from cell culture. Trends Neurosci. 2006 Jan; 29(1): 8-20. Epub 2005 Dec 7. Обзор). Более сложные системы, такие как тонкие или органотипические срезы мозга, являются очень полезными, но не поддающимися высокопроизводительному скринингу. Иммортализованные или трансформированные линии нервных клеток поддаются высокопроизводительному скринингу, но не воспроизводят зависящую от электрофизиологического состояния передачу сигнала первичными нейрональными культурами и, маловероятно, что адекватно моделируют едва уловимые изменения такой передачи сигнала, которые вызваны олигомерами во время самых ранних проявлений болезненного состояния (Смотри, например, публикацию: Gortz P, Fleischer W, Rosenbaum C, Otto F, Siebler M. Neuronal network properties of human teratocarcinoma cell line-deribed neurons. Brain Res. 2004 Aug 20; 1018(1): 18-25). По этой причине, первичные нейрональные культуры клеток выбирают, исходя из их способности быть использованными в высокопроизводительных скринингах и точно воспроизводить то, что происходит in vivo.
Восстановленный формазан сначала является видимым во внутриклеточных визикулах (фиг.1А). Образец нейронов, наполненных мечеными везикулами после эндоцитоза красителя и восстановления до нерастворимого пурпурного продукта. (Масштабная метка = 20 микрон на фиг.1А). Возможный экзоцитоз формазана ускоряют посредством Абета-олигомеров в зрелых нейронах гиппокампа in vitro (фиг.1В). Примерная микрофотография нейронов, покрытых нерастворимым пурпурным красителем, которые были выдавлены в результате экзоцитоза. Краситель осаждается в водной среде культуры клеток и образует игольчатые кристаллы на поверхности нейрона (фиг.1В). Скорость эндоцитоза изменяется в присутствии Абета-олигомеров (фиг.1С). Скорость экзоцитоза изменяется в присутствии Абета-олигомеров (фиг.1D).
Поскольку нарушения синапсиса и памяти, и не широко распространенная гибель клетки, преобладают на самых ранних стадиях болезни Альцгеймера, методы анализа, которые позволяют измерять эти изменения, могут быть использованы для обнаружения ингибиторов олигомерной активности с небольшими молекулами. МТТ-тест может быт использован в качестве меры токсичности в культурах клеток. Соли желтого тетразолия подвергаются эндоцитозу в клетках и восстанавливаются до нерастворимого пурпурного формазана в эндосомальном пути. Уровень пурпурного формазана отражает количество активно метаболизирующих клеток в культуре, и снижение количества формазана принимают за меру гибели клеток или метаболической токсичности в культуре. В том случае, когда проводят наблюдения через микроскоп, пурпурный формазан сначала является видимым во внутриклеточных везикулах, которые наполняют клетку (фиг.1А). Со временем, визикулы подвергаются экзоцитозу, и формазан осаждается в виде игольчатых кристаллов на внешней поверхности мембраны плазмы, поскольку нерастворимый формазан подвергается воздействию водной окружающей среды (фиг.1В). Клетки реагируют на сублетальные уровни Абета-олигомеров, селективно увеличивая скорость экзоцитоза восстановленного формазана, и вместе с тем оставляя скорость эндоцитоза неизмененной, что можно наблюдать в зрелых первичных нейронах in vitro и, где можно количественно оценить эти морфологические сдвиги посредством автоматизированной микроскопии и обработки изображений. В заданный момент времени после введения соли тетразолия в лунку с культурой, клетки, обработанные средой для лекарства имеют внешний вид клеток, показанных на фиг.1А, тогда как клетки, обработанные Абета-олигомером, имеют внешний вид клеток, показанных на фиг.1В. В этих обстоятельствах, нет общего изменения всего количества восстановленного формазана, а имеется просто сдвиг его морфологии. Этот метод анализа чувствителен к низким уровням олигомеров, которые не вызывают гибель клеток.
Полученные сведения позволяют предположить, что обусловленное Абета-олигомерами снижение нейрональной экспрессии поверхностных рецепторов, опосредованной мембранным трафиком, составляет основу олигомерного ингибирования, регистрируемого посредством электрофизиологических измерений синаптической пластичности (LTP) и, соответственно, обучения и запоминания (памяти) (Смотри публикации: Kamenetz F, Tomita T, Hsieh H, Seabrook G, Borchelt D, Iwatsubo T, Sisodia S, Malinow R. APP processing and synaptic function. Neuron. 2003 Mar. 27; 37(6): 925-37; и Hsieh H, Boehm J, Sato C, Iwatsubo T, Tomita T, Sisodia S, Malinow R. AMPAR removal underlies Abeta-induced synaptic depression and dendritic spine loss. Neuron. 2006 Dec. 7; 52(5): 831-43). Измерения изменений скорости мембранного трафика, вызванных олигомерами, посредством морфологических сдвигов формазана применены на клеточных линиях для обнаружения блокирующих Абета-олигомеры лекарственных средств [Maezawa I, Hong HS, Wu HC, Battina SK, Rana S, Iwamoto T, Radke GA, Pettersson E, Martin GM, Hua DH, Jin LW. A novel tricyclic pyrone compound ameliorates cell death associated with intracellular amyloid-beta oligomeric complexes. J Neurochem. 2006 Jul; 98(1): 57-67; Liu Y, Schubert D. Cytotoxic amyloid peptides inhibit cellular 3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide (MTT) reduction by enhancing MTT formazan exocytosis. J Neurochem. 1997 Dec; 69(6): 2285-93; Liu Y, Dargusch R, Banh C, Miller CA, Schubert D. Detecting bioactive amyloid beta peptide species in Alzheimer's disease. J Neurochem. 2004 Nov; 91(3): 648-56; Liu Y, Schubert D. Treating Alzheimer's disease by inactivating bioactive amyloid beta peptide. Curr Alzheimer Res. 2006 Apr; 3(2): 129-35; Rana S, Hong HS, Barrigan L, Jin LW, Hua DH. Syntheses of tricyclic pyrones and pyridinones and protection of Abeta-peptide induced MC65 neuronal cell death. Bioorg Med Chem Lett. 2009 Feb 1; 19(3): 670-4. Epub2008 Dec 24; and Hong HS, Maezawa I, Budamagunta M, Rana S, Shi A, Vassar R, Liu R, Lam KS, Cheng RH, Hua DH, Voss JC, Jin LW. Candidate anti-Abeta fluorene compounds selected from analogs of amyloid imaging agents. Neurobiol Aging. 2008 Nov 18. (Epub ahead of print)] that lower Abeta brain levels in rodents in vivo [Hong HS, Rana S, Barrigan L, Shi A, Zhang Y, Zhou F, Jin LW, Hua DH. Inhibition of Alzheimer's amyloid toxicity with a tricyclic pyrone molecule in vitro and in vivo. J Neurochem. 2009 Feb; 108(4): 1097-1108].
Метод анализа экзоцитоза адаптируют для применения со зрелыми первичными культурами нейрональных клеток, выращиваемыми в течение 3 недель in vitro. Абета-олигомеры вызывают дозозависимое снижение внутриклеточных везикул (точка, пора), наполненных восстановленным пурпурным формазаном (фиг.2А, квадраты; доза 3 мкМ соответствует изображению на фиг.2С), что измерено посредством обработки изображения с использованием автоматизированной системы микроскопии. Увеличение количества Абета-олигомеров в конечном счете приводит к явно выраженной токсичности. Так, концентрация нейроактивных Абета-олигомеров является намного меньше концентрации, которая вызывает гибель клетки. Такое снижение может быть блокировано добавлением стехиометрических количеств моноклонального анти-Абета-антитела 6Е10 (IgG) к культурам клеток до введения олигомера (фиг.2А, круг; круг соответствует изображению на фиг.2D; антитело как таковое [нижний треугольник] не имеет воздействия на нейроны). Испытывают несколько соединений, которые, как сообщалось, блокируют действия Абета-олигомеров, включая сахарный спирт сцилло-инозитол (AZD-103), nAChR-антагонист бромид гексаметония, и NMDAR-антагонисты МК-801, и ни один из них не является активным (Fenili et al., '07, Calabrese et al., '06, LeCor et al., '07).
Метод анализа оптимизируют для работы в 384-луночных титрационных микропланшетах с автоматизированной робототехникой для осуществления манипуляций с жидкостями для дозирования, переноса, разбавления образца с соединением, и добавления внутреннего стандарта, и для маркировки аналитического планшета, с достижением согласно стандартной методике статистически значимого двухкратного разделения результатов для нейронов, обработанных средой для лекарства, и для нейронов, обработанных Абета-олигомерами (Т-критерий Стьюдента, неодинаковая дисперсия). Сначала к нейронам добавляют соединения, затем добавляют олигомеры. При выполнении манипуляций таким образом, планшет может детектировать соединения, которые действуют с расщеплением олигомеров, с ингибированием связывания олигомеров с нейронами, или с нейтрализацией механизмов действия, инициированных связыванием олигомеров, в отношении передачи сигнала.
Соединения считают активными, если они в значительной мере блокируют опосредованные Абета-олигомерами изменения мембранного трафика, но не затрагивают значительно мембранный трафик при введении доз собственно их самих. Пример показан на фиг.2В; соединение 2 примера ингибирует действие олигомера на мембранный трафик при значении EC50, равном 7 мкМ.
Фиг.2А показывает дозозависимое снижение внутриклеточных наполненных формазаном везикул (пора), вызванное ускорением экзоцитоза (квадраты) после обработки Абета-олигомером 42. Действия олигомера блокируют анти-Абета-антителами IgG (круг и верхний треугольник; круг относится к стехиометрическому количеству IgG, то есть, к 3 мкМ Аβ и 1,5 мкМ IgG; верхний треугольник относится к субстехиометрическому количеству IgG, то есть, к 3 мкМ Аβ и 0,5 мкМ IgG). IgG сам по себе (нижний треугольник) не оказывает действия. Фиг.2В показывает соединение 2 примера, которое ингибирует действия олигомера на мембранный трафик. Фиг.2С показывает репрезентативные микрофотоснимки нейронов гиппокампа на 21 день скрининга in vitro (21 DIV), показывающие действия олигомера на мембранный трафик (соответствующие экспериментальной точке 3 мкМ на фиг.2А); и фиг.2D показывает блокировку анти-Абета-антителами (что соответствует кругу на фиг.2А). Данные представляют собой среднее по 3 экспериментам. Масштабная метка = 20 микронам на фиг.2D.
Пример ЕЕ: Анализ установления состояния страха
Образец соединения 2 испытывают на экспериментальной модели на животном зависящей от памяти поведенческой задачи, известной как установление состояния страха. Протокол исследования выстраивают на основе опубликованных протоколов (смотри, например, публикацию: Puzzo D, Privitera L, Leznik E, Fa M, Staniszewski A, Palmeri A, Arancio O. Picomolar amyloid-beta positively modulates synaptic plasticity and memory in hippocampus. J. Neurosci. 2008 Dec. 31; 28(53): 14537-45.). Формирование контекстуальной памяти зависит от целостности медиальных структур височной доли, таких как гиппокамп. В этом анализе у мышей вырабатывают навыки запоминания того, что конкретный привлекающий внимание контекст (условно-рефлекторный стимул/раздражитель; CS) связан с вызывающим отвращение событием, в этом случае с легким электроболевым раздражением лап животных (безусловно-рефлекторный раздражитель, US). Животные, которые показывают хорошие навыки научения, будут показывать увеличение периода замирания при помещении обратно в тот же самый контекст. Такое замирание отсутствует в новом контексте. Увеличенный период замирания в данном контексте указывает на формирование сильно зависимой от гиппокампа памяти у животных. Память, испытываемая при установлении состояния страха, чувствительна к повышениям количества растворимых Аβ. Фиг.3 показывает результаты, заключающиеся в том, что введение Абета-олигомеров (метка, обозначенная как «а») во время выработки навыка приводит к нарушению памяти в том случае, когда животных испытывают на 24 часа позже, в сравнении с введением среды для лекарства (метка, обозначенная как «b»). Соединение 2 примера является эффективным в приостановлении опосредованного Абета-олигомерами действия на мембранный трафик (фиг.3). В том случае, когда вводят животным до введения Абета-олигомеров, соединение 2 примера блокирует действие олигомера на память дозозависимым образом. Соединение полностью блокирует опосредованное олигомером нарушение памяти в дозе 2 пмоль (фиг.3, метка, обозначенная как «d»). Такая бихевиористическая эффективность демонстрирует то, что анализ мембранного трафика может предсказывать, какие соединения будут эффективными в лечении потери бихевиористической памяти, вызванной олигомерами. Модель памяти состояния страха осуществляют так, как описано в этом документе.
Фиг.3 показывает, что Абета производит значительные нарушения в формировании памяти относительно среды для лекарства (p<0,05) в задаче формирования контекстуальной памяти установления состояния страха. Фиг.3 показывает, что доза образца соединения 2, составляющая 2 пмоль, + Абета (200 нМ) полностью блокирует действие Абета на память (р<0,05, однофакторный одномерный дисперсионный анализ «One way ANOVA», метод апостериорных множественных сравнений с введением поправки Бонферрони). Никакого действия соединения как такового не наблюдается (данные не показаны). Никаких нежелательных изменений в поведении не наблюдают ни при какой дозе.
Пример FF: Анализ мембранного трафика:
Скопления Абета выделяют из пациентов, страдающих болезнью Альцгеймера (AD), или из здоровых пациентов. Абета-скопления испытывают на их способность модулировать мембранный трафик. Скопления Абета с высокой молекулярной массой HMW (>100 килодальтон), выделенные из пациентов, страдающих болезнью Альцгеймера, не оказывают влияния на мембранный трафик (не изображено). Скопления Абета с промежуточной молекулярной массой IMW (10-100 килодальтон), выделенные из пациентов, страдающих болезнью Альцгеймера, значительно влияют на мембранный трафик (фиг.4). Скопления Абета с IMW, выделенные из здоровых пациентов соответствующего возраста, не оказывают влияния на мембранный трафик (фиг.4). Образец соединения 2 не оказывает воздействия на Абета-скопления, выделенные из здоровых субъектов соответствующего возраста. (фиг.4). Образец соединения 2 значительно блокирует действия Абета-скоплений, извлеченных из мозга пациентов, страдающих болезнью Альцгеймера, на мембранный трафик. (фиг.4).
Хотя настоящее изобретение описано в значительной мере подробно со ссылкой на некоторые предпочтительные его варианты, другие варианты являются возможными. Следовательно, сущность и объем изобретения не следует ограничивать описанием предпочтительных вариантов, описанных в этом документе.
Все признаки, раскрытые в описании изобретения, включая реферат и чертежи, и все стадии в любом раскрытом способе или процессе, могут быть объединены в любую комбинацию, за исключением комбинаций, где, по меньшей мере, некоторые из таких признаков и/или стадий являются взаимоисключающими. Каждый признак, раскрытый в описании изобретения, включая реферат и чертежи, могут быть заменены альтернативными признаками, служащими аналогичной, эквивалентной или подобной цели, если не установлено однозначно иное. Таким образом, если не установлено в явно выраженной форме иное, то каждый раскрываемый признак имеет только один пример родового ряда эквивалентных или подобных признаков. Различные модификации изобретения, в дополнение к описанным в этом документе модификациям, будут очевидны для специалистов в данной области из рассмотрения вышеприведенного описания изобретения. Также подразумевается, что такие модификации попадают в объем прилагаемых пунктов формулы изобретения.
Каждая ссылка, приведенная в настоящей заявке, включена в этот документ путем ссылки в полном своем объеме.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ФЕНЭТАНОЛАМИНА ДЛЯ ЛЕЧЕНИЯ РЕСПИРАТОРНЫХ ЗАБОЛЕВАНИЙ | 2002 |
|
RU2312854C2 |
| ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ В СИНТЕЗЕ АНАЛОГОВ ЗЕАРАЛЕНОНОВЫХ МАКРОЛИДОВ | 2008 |
|
RU2497803C2 |
| Гетероциклические соединения в качестве ингибиторов PAD | 2018 |
|
RU2764243C2 |
| ПРОИЗВОДНЫЕ ДИФЕНИЛАЗЕТИДИНОНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И КОМБИНАЦИЯ И ИХ ПРИМЕНЕНИЕ ДЛЯ ИНГИБИРОВАНИЯ ВСАСЫВАНИЯ ХОЛЕСТЕРИНА | 2003 |
|
RU2333199C2 |
| МАКРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, КОТОРЫЕ МОГУТ БЫТЬ ИСПОЛЬЗОВАНЫ В КАЧЕСТВЕ ФАРМАЦЕВТИЧЕСКИХ ПРЕПАРАТОВ | 2003 |
|
RU2334744C2 |
| ПРОИЗВОДНЫЕ НИКОТИНАМИДА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И ПРИМЕНЕНИЕ | 2003 |
|
RU2309951C2 |
| Необязательно конденсированные гетероциклилзамещенные производные пиримидина, пригодные для лечения воспалительных, метаболических, онкологических и аутоиммунных заболеваний | 2015 |
|
RU2734261C2 |
| ИНГИБИТОРЫ MAGL НА ОСНОВЕ ПИРАЗОЛА | 2018 |
|
RU2789157C2 |
| Необязательно конденсированные гетероциклил-замещенные производные пиримидина, пригодные для лечения воспалительных, метаболических, онкологических и аутоиммунных заболеваний | 2015 |
|
RU2815636C1 |
| ПИРИДО [2,3-d] ПИРИМИДИНЫ, ПОЛЕЗНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ HCV, И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2006 |
|
RU2444522C2 |
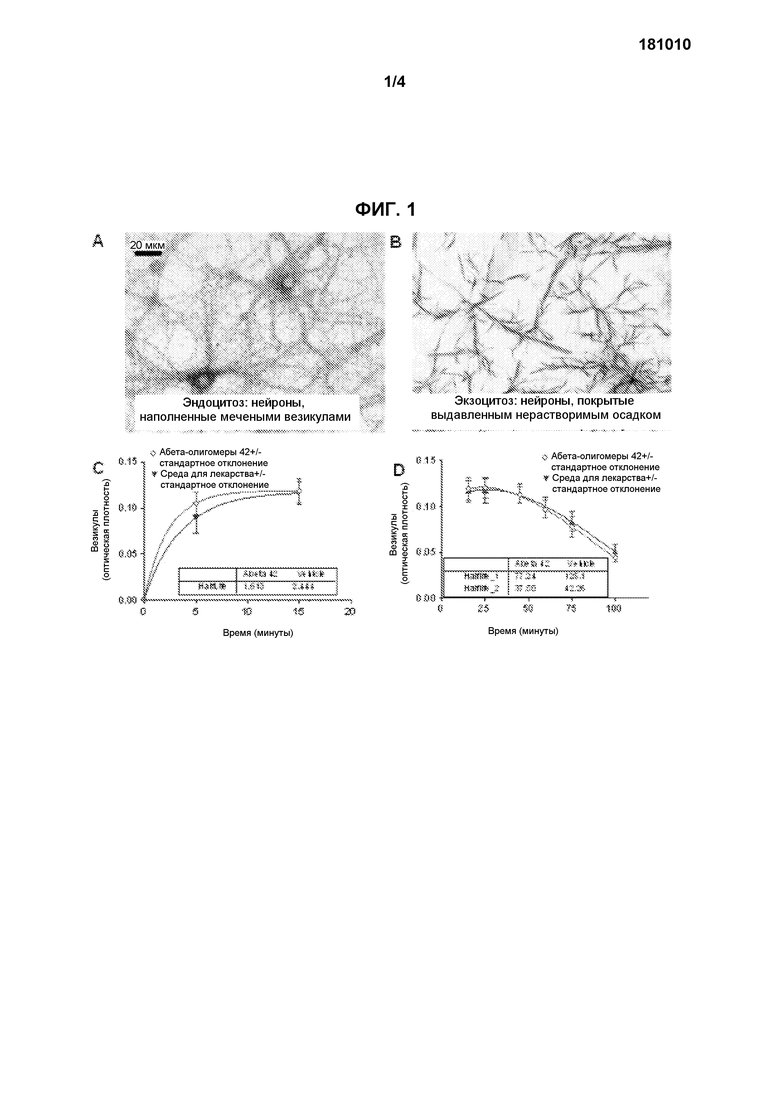
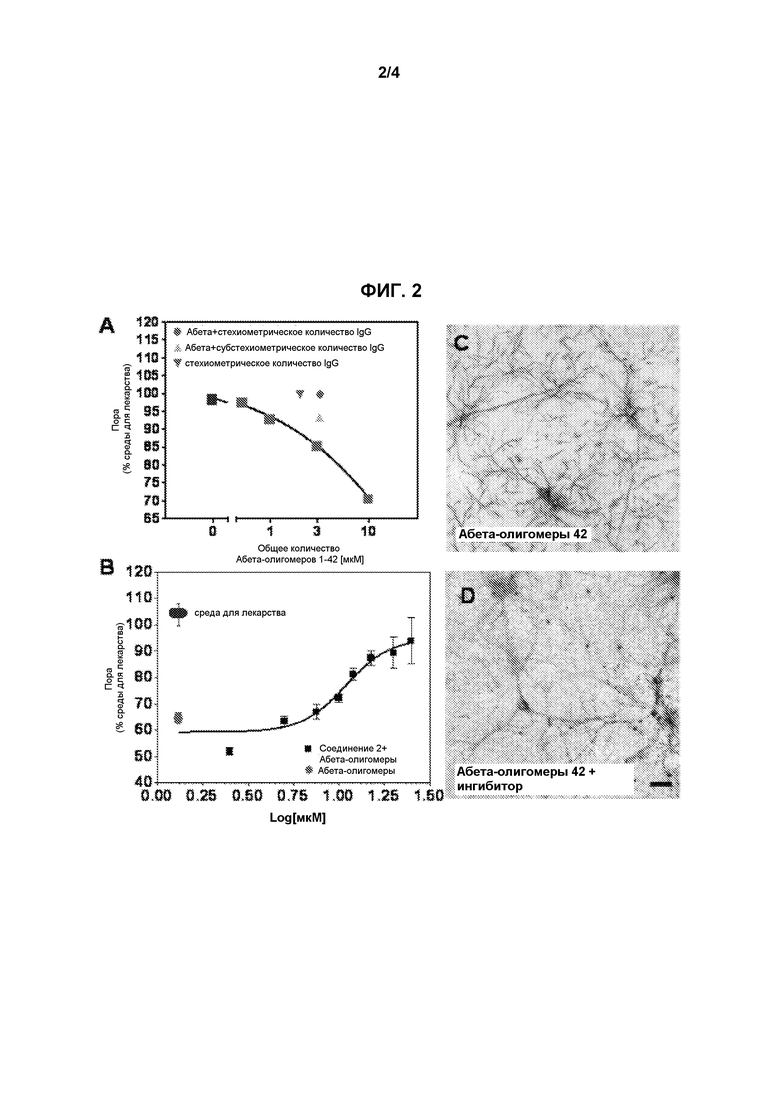
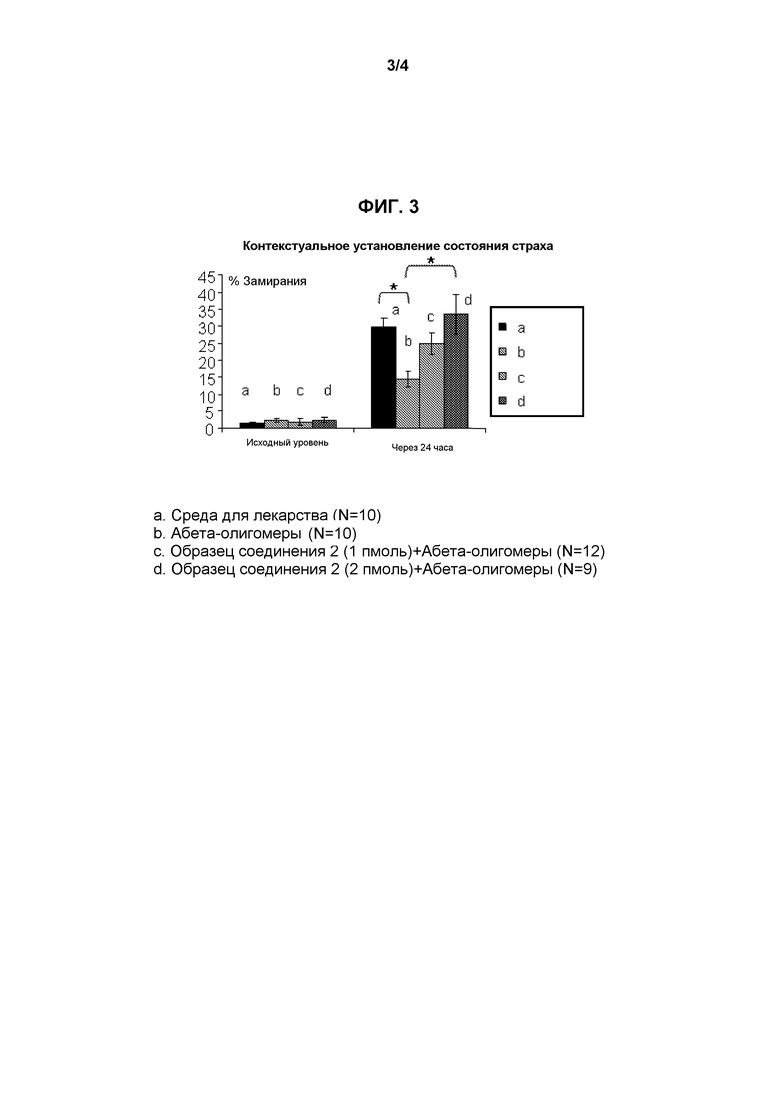
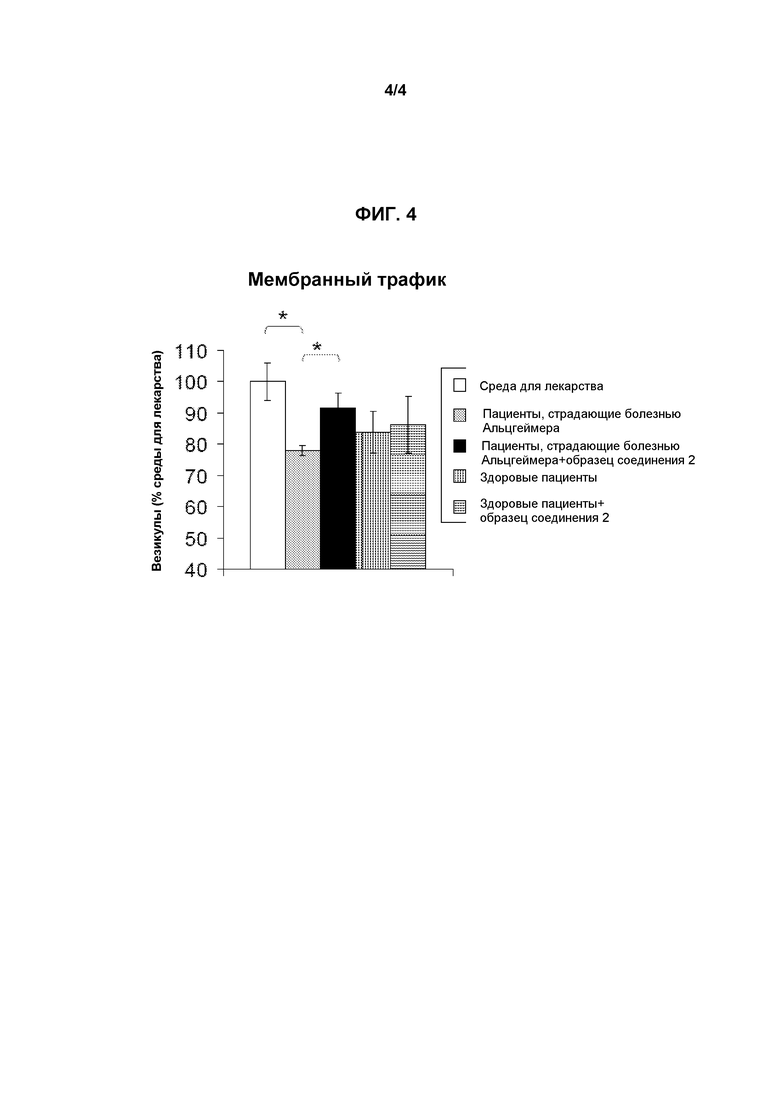
Изобретение относится к новым соединениям формулы I или его фармацевтически приемлемым солям, которые обладают свойствами ингибиторов связывания Абета-олигомеров в отношении нервной клетки у пациентов. Соединения могут быть полезными при лечении когнитивных способностей, например при болезни Альцгеймера. В формуле I
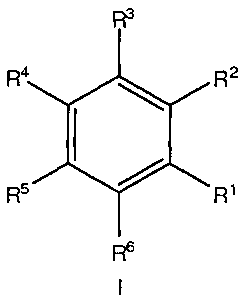

R1 представляет собой (А1); R2 и R3, каждый, представляет собой Н; R4 и R5, каждый, независимо, выбирают из ОН и С1-6алкоксигруппы; R6 представляет собой Н; R7 представляет собой Н, С1-6алкил, С1-6галогеналкил или С3-7циклоалкил; R8 представляет собой С1-6алкил, С1-6галогеналкил или С3-7циклоалкил; R9 представляет собой Н или С1-6алкил; R10 представляет собой Н, С1-6алкил, С1-6галогеналкил или С3-7циклоалкил; R11 представляет собой Н; R12 и R13, каждый, представляет собой Н; R14 выбирают из галогена и C1-6галогеналкила; R15 и R16, каждый, представляет собой Н. Предпочтительными соединениями являются 4-(3-(4-хлорбензиламино)бутил)-2-метоксифенол или 4-(3-(4-(трифторметил)бензиламино)бутил)-2-метоксифенол. Указанные соединения получают взаимодействием кетона формулы X с амином формулы XI


в условиях восстановительного аминирования с выделением соответствующего соединения. Выход продуктов 80-95% масс. При этом может быть использовано в качестве исходного соединения имбирное масло, содержащее кетон формулы X. 9 н. и 9 з.п. ф-лы, 4 ил., 8 пр.
1. Соединение формулы I:

или его фармацевтически приемлемая соль, где:
R1 представляет собой (А1)
 ;
;
R2 и R3, каждый, представляет собой Н;
R4 и R5, каждый, независимо, выбирают из ОН и С1-6алкоксигруппы;
R6 представляет собой Н;
R7 представляет собой Н, С1-6алкил, С1-6галогеналкил или С3-7циклоалкил;
R8 представляет собой С1-6алкил, С1-6галогеналкил или С3-7циклоалкил;
R9 представляет собой Н или С1-6алкил;
R10 представляет собой Н, С1-6алкил, С1-6галогеналкил или С3-7циклоалкил;
R11 представляет собой Н;
R12 и R13, каждый, представляет собой Н;
R14 выбирают из галогена и C1-6галогеналкила;
R15 и R16, каждый, представляет собой Н.
2. Соединение, которое представляет собой 4-(3-(4-хлорбензиламино)бутил)-2-метоксифенол или 4-(3-(4-(трифторметил)бензиламино)бутил)-2-метоксифенол, или его фармацевтически приемлемая соль.
3. Способ соединения формулы IIа
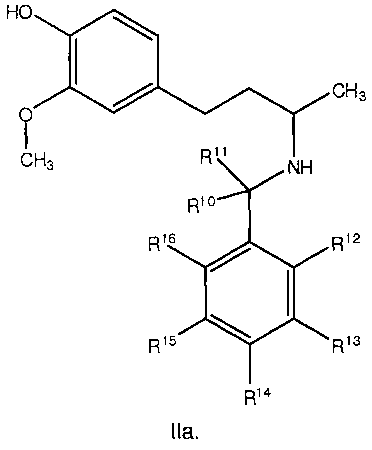
включающий
(а) взаимодействие кетона формулы X

с амином формулы XI:
в условиях восстановительного аминирования с получением соединения формулы IIa; и
(b) выделение,
где:
R10 представляет собой Н, С1-6алкил, С1-6галогеналкил или С3-7циклоалкил;
R11 представляет собой Н;
R12, R13, R15 и R16, каждый, представляет собой Н; и
R14 выбирают из галогена и C1-6галогеналкила.
4. Способ по п. 3, где в качестве исходного соединения используют имбирное масло, содержащее кетон формулы X, с получением продукта, содержащего по меньшей мере 80%, 85%, 90% или 95% по массе соединения формулы IIa.
5. Способ по п. 4, где получают продукт, полезный для лечения когнитивных способностей.
6. Способ по п. 3, где массовое соотношение имбирного масла и амина формулы XI, используемое в восстановительном аминировании, составляет от 2,7:1 до 3,3:1.
7. Соединение формулы 5 или его фармацевтически приемлемая соль 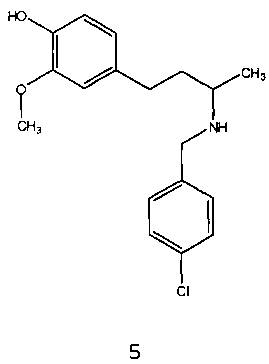 .
.
8. Способ получения соединения формулы 5 или его фармацевтически приемлемой соли по п. 7, включающий:
(a) проведение реакции между имбирным маслом и 4-хлорбензиламином в условиях восстановительного аминирования с получением сырого продукта, где соотношение имбирного масла к 4-хлорбензиламину составляет приблизительно 3:1 по массе; и
(b) выделение продукта, содержащего по меньшей мере 80%, 85%, 90% или 95% по массе соединения формулы 5, или его фармацевтически приемлемой соли,
где:
соединение имеет пик [М+Н+] на спектре, полученном методом аналитической масс-спектрометрии, на приблизительно 320,2.
9. Соединение по п. 7, где спектр 1Н ЯМР (500 МГц, CDCl3) для соединения включает следующие пики: 7,30-7,24 (м), 6,81 (д), 6,66-6,62 (м), 4,25 (шир.с), 3,82 (с), 3,82 (д), 3,72 (д), 2,73 (м), 2,66-2,51 (м), 1,86-1,78 (м), 1,72-1,63 (м), 1,62-1,51 (м) и 1,17 (д).
10. Соединение по п. 7, где спектр 13С ЯМР (125 МГц, CDC13) для соединения включает, по меньшей мере, 16 пиков, выбранных из следующих химических сдвигов: 146,6, 143,8, 133,9, 132,8, 129,9, 129,7, 128,6, 120,8, 114,5, 110,9, 55,8, 51,9, 50,2, 38,5, 31,9, 31,6, 29,7, 26,9, 22,6 и 19,9.
11. Соединение по п. 7, где спектр 1Н ЯМР (500 МГц, CD3OD) для соединения включает следующие пики: 7,10-7,30 (м, 4Н), 6,63 (шир.с, 1Н), 6,58 (м, 1Н), 6,48 (м, 1Н), 3,68 (с, 3Н), 3,65 (м, 1Н), 3,58 (м, 1Н), 2,57 (м, 1Н), 2,50 (м, 1Н), 2,35 (м, 1Н), 1,73 (м, 1Н), 1,49 (м, 1Н) и 1,04 (д, 3Н).
12. Соединение по п. 7, где спектр 13С ЯМР (125 МГц, CD3OD) для соединения включает следующие пики на: 147,5, 145,3, 137,2, 133,3, 132,6, 129,9, 128,1, 120,4, 114,7, 111,6, 54,9, 51,3, 49,2, 37,7, 31,5 и 18,0.
13. Соединение формулы 6 или его фармацевтически приемлемая соль
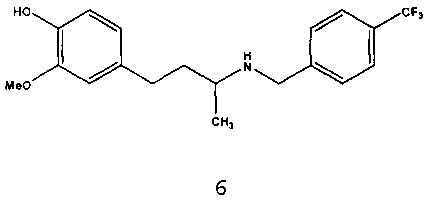 .
.
14. Способ получения соединения формулы 6 или его фармацевтически приемлемой соли по п. 13, включающий
(a) проведение реакции между имбирным маслом и 4-трифторметилбензиламином в условиях восстановительного аминирования с получением сырого продукта, где соотношение имбирного масла к 4-трифторметилбензиламину составляет приблизительно 3:1 по массе; и
(b) выделение продукта, содержащего по меньшей мере 80%, 85%, 90% или 95% по массе соединения формулы 6 или его фармацевтически приемлемой соли,
где:
соединение имеет пик [М+Н+] на спектре, полученном методом аналитической масс-спектрометрии, приблизительно на 353.
15. Соединение по п. 13, где спектр 1Н ЯМР (500 МГц, CDCl3) для соединения включает следующие пики: 7,57 (д, 2Н), 7,43 (д, 2Н), 6,82 (д, 1Н), 6,65 (м, 2Н), 5,16-4,42 (шир.с, 2Н), 3,90 (д, 1Н), 3,84 (с, 3Н), 3,80 (д, 1Н), 2,76-2,70 (м, 1Н), 2,67-2,55 (м, 2Н), 1,84-1,77 (м, 1Н), 1,69-1,63 (м, 1Н) и 1,17 (д, 3Н).
16. Соединение по п. 15, где спектр 13С ЯМР (125 МГц, CDCl3) для соединения включает, по меньшей мере, 17 пиков, выбранных из следующих химических сдвигов: 146,7, 144,6, 143,9, 134,0, 129,1, 128,4, 127,5, 125,4, 125,3, 123,2, 120,8, 114,6, 111,0, 55,7, 52,1, 50,6, 38,8, 32,0, 20,1.
17. Способ ингибирования связывания Абета-олигомеров в отношении нервной клетки у пациента, включающий введение пациенту соединения по любому из пп. 1 или 2 или их фармацевтически приемлемой соли.
18. Способ ингибирования связывания Абета-олигомеров в отношении нервной клетки, включающий введение пациенту соединения по любому из пп. 7, 9-12 или 13, 15-16 или его фармацевтически приемлемой соли.
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| . | |||
Авторы
Даты
2016-08-27—Публикация
2010-04-06—Подача