Изобретение относится к области органической химии, в частности к новому способу получения 2-аминометилстиролов.
2-Аминометилстиролы применяются для получения катализаторов на основе карбеновых комплексов рутения для полимеризации цикло- и бициклоолефинов с раскрытием цикла по реакции метатезиса. RU 2374269 C2, 20.07.2009, RU 2393171 C1, 27.08.2010, RU 2462308 C1, 27.09.2012, RU 2436801 C1, 20.12.2011.
Известен способ получения 2-аминометилстиролов кросс-сочетанием производных 2-галогензамещенных бензиламинов и 2,4,6-тривинилциклотрибороксана или винил трибутилстаннатов, катализируемым соединениями палладия. WO 2011/079799 A1, 07.07.2011 и US 2007/0027071 A1, 01.02.2007.
К недостаткам способа можно отнести сложность аппаратурного оформления синтеза, а также высокую стоимость реагентов.
Известен способ получения 2-аминометилстиролов из о-винилбензилхлорида. А. Padwa, W. Dent. On the use of N-[(trimethylsilyl)methyl]amino ethers as capped azomethine ylide equivalents. J. Org. Chem., 1987, 52, 235-244.
Недостатком способа является высокая стоимость исходного о-винилбензилхлорида.
Расщепление четвертичных солей 1,2,3,4-тетрагидроизохинолинов по Гофману является эффективным методом синтеза 2-(N,N-диалкиламинометил)стиролов.
Известен способ получения 2-аминометилстиролов из солей диалкилтетрагидроизохинолинов с использованием оксида серебра. S. Kafka, P. Trska, J. Kytner, P. Taufmann, M. Ferles. Hydroboration of unsaturated amines. Part XIX. Hydroboration of N,N-dimethyl(2-vinylbenzyl)amine. Collection of Czechoslovak Chemical Communications, 1987, 52 (8), 2047-2056, A. Rheiner, A. Brossi. Syntheses in the isoquinoline series. Hofmann degradation of 1-phenyl-substituted 1,2,3,4-tetrahydroisoquinolines. Helvetica Chimica Acta, 1962, 45, 2590-600.
К недостатком способа можно отнести необходимость использовать дорогостоящие и токсичные соли серебра.
Известен способ получения 2-(N,N-диметиламинометил)стирола из диметилтетрагидроизохинолиний иодида нагреванием в DMSO в присутствии KCN. G.A. Molander, S.K. Pack. Determining the scope of the lanthanide mediated, sequential hydroamination/C-C cyclization reaction: formation of tricyclic and tetracyclic aromatic nitrogen heterocycles, Tetrahedron, 2003, 59, 10581-10591.
Недостатком этого способа является использование высокотоксичного цианида калия.
Известен способ однореакторного получения [N-метил-N-(2-метоксиметил)]-2-винилбензиламина кипячением бензольного раствора N-(2-гидроксиэтил)-1,2,3,4-тетрагидроизохинолина, метилиодида и AliquatR 336 с гидроксидом калия. Silyl modification of biologically active compounds. 10. Lipid type organosilicon derivatives of 8-hydroxyquinoline and N-(2-hydroxyethyl)-1,2,3,4-tetrahydro(sila, iso)quinolones. Chemistry of Heterocyclic Compounds, 2005, 41 (5), 613-624.
К недостаткам данного способа можно отнести низкий (32%) выход целевого соединения.
Известен способ однореакторного получения 2-винил-N,N-диметилбензиламина из метилиодида N-метил-4-(триметилсилил)-1,2,3,4-тетрагидроизохинолина при комнатной температуре в ацетонитриле в присутствии ТБАФ и метилакрилата. Y. Ito, М. Nakatsuka, Т. Saegusa. Syntheses of Polycyclic Ring Systems Based on the New Generation of o-Quinodimethanes. J. Am. Chem. Soc, 1982, 104, 7609-7622.
Недостатком этого способа является труднодоступность исходного тетрагидроизохинолина и высокая стоимость и токсичность реагентов.
Известен способ расщепления метилсульфата производного 1,2,3,4-тетрагидроизохинолина, в котором его переводят в гидроксипроизводное на ионообменной смоле IRA-401, которое затем претерпевает расщепление по Гофману. Т. Suzuki, М. Takarnoto, Т. Okarnoto, Н. Takayarna. Acid-catalyzed double-cyclization reactions of N,N-dibenzylamino-acetaldehyde dialkyl acetals and related compounds: general synthesis of 7,12-dihydro-5H-6,12-methanodibenz[c,f]azocines and related compounds. Chemical & Pharmaceutical Bulletin, 1986, 34 (5), 1888-1900.
Недостатком этого способа можно назвать невысокий выход конечного стирола.
Наиболее близким к данному изобретению является способ получения 2-аминометилстиролов из 2-(2-бромоэтил)бензилбромида, его реакцией с вторичными аминами в диоксане под действием микроволнового облучения с последующим кипячением в системе трет-бутанол/трет-бутилат калия. Н.М. Щеглова, И.Д. Колесник, Р.В. Аширов. Общий способ получения орто-винилзамещенных аминов, эфиров и сульфидов. Журнал органической химии, 2013, 49 (9), 1344-1349.
К недостаткам данного способа можно отнести относительно низкие выходы 42-65%, необходимость применения микроволнового облучения и ограниченность рядом вторичных аминов.
Технической задачей заявленного изобретения является разработка простого способа получения 2-аминометилстиролов, содержащих гетероциклический фрагмент, позволяющего получать широкий ряд аминометилстиролов с хорошим выходом и высокой чистотой.
Технический результат от реализации заявленного изобретения заключается в упрощении процесса и повышении его технологичности за счет проведения в мягких условиях, не требующих сложного оборудования, инертной атмосферы, дорогих и токсичных реагентов, повышении выхода целевых продуктов до 79-84 масс. % на исходный изохинолин.
Технический результат достигается тем, что синтез проводят в соответствии с уравнениями реакций:
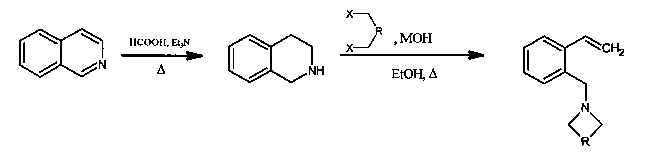
В результате получают 2-аминометилстиролы, содержащие гетероциклический фрагмент общей формулы:
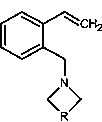 , где R=CH2NHCH2, R=о-CH2C6H4 или R=(CH2)4, предусматривая проведение реакции восстановления изохинолина до 1,2,3,4-тетрагидроизохинолина в присутствии муравьиной кислоты, триэтиламина и тристрифенилфосфинорутений дихлорида, который затем однореакторно в растворе этанола и под действием соответствующего дигалогенида и щелочи переводят в целевой продукт. При этом в качестве дигалогенида используют бис(2-хлороэтил)амин, 1-(2-бромоэтил)-2-(бромометил)бензол или 1,6-дибромгексан, а щелочь выбирают из гидроксида натрия или гидроксида калия.
, где R=CH2NHCH2, R=о-CH2C6H4 или R=(CH2)4, предусматривая проведение реакции восстановления изохинолина до 1,2,3,4-тетрагидроизохинолина в присутствии муравьиной кислоты, триэтиламина и тристрифенилфосфинорутений дихлорида, который затем однореакторно в растворе этанола и под действием соответствующего дигалогенида и щелочи переводят в целевой продукт. При этом в качестве дигалогенида используют бис(2-хлороэтил)амин, 1-(2-бромоэтил)-2-(бромометил)бензол или 1,6-дибромгексан, а щелочь выбирают из гидроксида натрия или гидроксида калия.
Ниже приведены примеры способа получения 2-аминометилстиролов, содержащих гетероциклический фрагмент общей формулы:
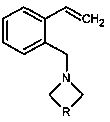 ,
,
выбранных из ряда:
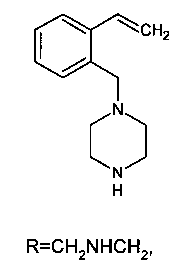
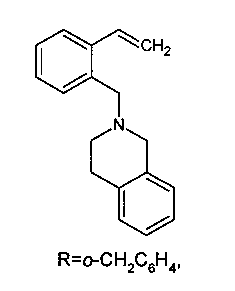
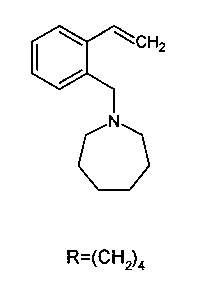
Пример 1
Получение 4-(2-винилбензил)пиперазина
В колбу объемом 500 мл, снабженную обратным холодильником, помещают 26 г (0,155 моль) изохинолина в виде гидрохлорида и через воронку прибавляют 35 мл (45 г, 0,93 моль) муравьиной кислоты, 25,3 мл (17,5 г, 0,23 моль) триэтиламина и 1,5 г (1,56 ммоль) тристрифенилфосфинорутений дихлорида. Далее перемешивают при температуре 100°C до момента прекращения выделения газа (примерно 4 ч). Затем реакционную массу охлаждают до комнатной температуры и в колбу через воронку при охлаждении и перемешивании прибавляют 100 мл изопропанола и 43,4 г (1,08 моль) NaOH, перемешивают в течение 2 ч при кипячении, затем охлаждают до комнатной температуры. Реакционную колбу переносят на ротор и упаривают растворитель досуха, к остатку прибавляют 100 мл воды и 100 мл метилтретбутилового эфира (МТБЭ), перемешивают в течение 30 мин и переносят в делительную воронку. Разделяют слои, водный еще раз экстрагируют 100 мл МТБЭ. Объединенные органические слои промывают 50 мл воды, сушат над сульфатом натрия, растворитель упаривают на роторе, остаток перегоняют под вакуумом. Получают 14,5 г (70 масс. %) 1,2,3,4-тетрагидроизохинолина. 5,0 г (0,038 моль) 1,2,3,4-тетрагидроизохинолина помещают в 50 мл круглодонную колбу, снабженную обратным холодильником, к нему прибавляют 100 мл этанола, 7,5 г (0,042 моль) бис(2-хлороэтил)амин гидрохлорид и 3,4 г (0,084 моль) гидрооксида натрия. Реакционную смесь нагревают при перемешивании в масляной бане при кипячении в течение 1 ч. Затем реакционную смесь упаривают, к остатку прибавляют 50 мл МТБЭ и перемешивают в течение 30 мин, пропускают через слой Al2O3, промывают на фильтре 50 мл МТБЭ, фильтраты упаривают, получают 6,0 г (79 масс. %) 4-(2-этенилбензил)пиперазина.
1Н NMR (400 MHz, хлороформ-d), δ, ppm: 2,52-2,65 (8Н, м, CH 2NCH 2), 3,58 (2Н, с, ArCH 2N), 5,33 (1H, дд, J=11.1, 1.6 Гц, CH=CH 2), 5,61 (1H, д, J=17,5, 1,6 Гц, CH=CH 2), 7,22-7,41 (4Н, м, СН=СН2+HAr), 7,54 (1H, д, J=6,8 Гц, HAr). GC/MS, М+: 203.
Пример 2
Осуществляют аналогично Примеру 1, но вместо бис(2-хлороэтил)амина используют 1-(2-бромоэтил)-2-(бромометил)бензол, получают 2-(2-винилбензил)-1,2,3,4-тетригидроизохинолин с выходом 82 масс. %.
1H NMR (400 MHz, хлороформ-d), δ, ppm: 2,65-2,69 (2Н, м, ArCH 2CH2N), 3,93-3,98 (4Н, м, CH 2NCH 2), 3,99 (2Н, с, CH 2N), 5,34 (1H, д, J=10,9 Гц, СН=CH 2), 5,68 (1Н, д, J=17,5 Гц, CH=CH 2), 7,21 (4Н, с, HAr), 7,28-7,32 (3Н, м, СН=СН2+HAr), 7,43 (1Н, д, J=6,8 Гц, HAr), 7,53 (1H, д, J=6,8 Гц, HAr). GC/MS, М+: 249.
Пример 3
Осуществляют аналогично Примеру 1, но вместо бис(2-хлороэтил)амина используют 1,6-дибромгексан, а вместо гидроксида натрия используют гидроксид калия, получают 1-(2-винилбензил)азепин с выходом 84 масс. %.
1Н NMR (400 MHz, хлороформ-d), δ, ppm: 1,40-1,47 (2H, м, CH2CH 2CH2), 1,52-1,60 (6H, м, CH 2CH 2CH 2), 2,29-2,46 (4Н, м, CH 2NCH 2), 3,49 (2Н, с, ArCH 2N), 5,30 (1Н, дд, J=11,0, 1.4 Гц, CH=CH 2), 5,66 (1Н, д, J=17,5 Гц, CH=CH 2), 7,22-7,33 (4Н, м, CH=CH2+HAr), 7,54 (1H, д, J=6,8 Гц, HAr). GC/MS, М+: 215.
Использование в предлагаемом способе доступных реагентов и условий (изохинолин как исходный реагент, муравьиная кислота для восстановления изохинолиниевых солей, система щелочь/этанол/дигалогенид для получения и расщепления четвертичных солей аминов) упрощает процесс и повышает его технологичность, позволяет получать различные аминометилстиролы, содержащие гетероциклический фрагмент с высокими выходами и чистотой.
Изобретение относится к способу получения 2-(N,N-диалкиламинометил)стиролов, содержащих гетероциклический фрагмент общей формулы:
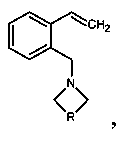 где R=CH2NHCH2, R=о-CH2C6H4 или R=(CH2)4, в котором изохинолин восстанавливают до 1,2,3,4-тетрагидроизохинолина в присутствии муравьиной кислоты, триэтиламина и тристрифенилфосфинорутений дихлорида. Затем его растворяют в растворе этанола под действием дигалогенида и щелочи, смесь упаривают, добавляют метилтретбутиловый эфир и перемешивают в течение 30-40 мин. Полученную смесь фильтруют через порошок оксида алюминия до получения целевого продукта. Изобретение обеспечивает упрощение процесса и повышение его технологичности за счет проведения его в мягких условиях, не требующих сложного оборудования, инертной атмосферы, дорогих и токсичных реагентов. Также достигается повышение выхода целевых продуктов до 79-84 масс. % на исходный изохинолин. 2 з.п. ф-лы, 3 пр.
где R=CH2NHCH2, R=о-CH2C6H4 или R=(CH2)4, в котором изохинолин восстанавливают до 1,2,3,4-тетрагидроизохинолина в присутствии муравьиной кислоты, триэтиламина и тристрифенилфосфинорутений дихлорида. Затем его растворяют в растворе этанола под действием дигалогенида и щелочи, смесь упаривают, добавляют метилтретбутиловый эфир и перемешивают в течение 30-40 мин. Полученную смесь фильтруют через порошок оксида алюминия до получения целевого продукта. Изобретение обеспечивает упрощение процесса и повышение его технологичности за счет проведения его в мягких условиях, не требующих сложного оборудования, инертной атмосферы, дорогих и токсичных реагентов. Также достигается повышение выхода целевых продуктов до 79-84 масс. % на исходный изохинолин. 2 з.п. ф-лы, 3 пр.
1. Способ получения 2-аминометилстиролов, содержащих гетероциклический фрагмент общей формулы:
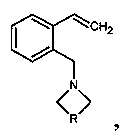
где R=CH2NHCH2, R=o-СН2С6Н4 или R=(CH2)4,
заключающийся в том, что проводят реакцию восстановления изохинолина до 1,2,3,4-тетрагидроизохинолина в присутствии муравьиной кислоты, триэтиламина и тристрифенилфосфинорутений дихлорида, который затем растворяют в растворе этанола под действием дигалогенида и щелочи, смесь упаривают, добавляют метилтретбутиловый эфир, перемешивают в течение 30-40 мин и полученную смесь фильтруют через порошок оксида алюминия до получения целевого продукта.
2. Способ по п. 1, отличающийся тем, что в качестве дигалогенида используют бис(2-хлороэтил)амин, 1-(2-бромоэтил)-2-(бромометил)бензол или 1,6-дибромгексан.
3. Способ по п. 1, отличающийся тем, что щелочь выбирают из гидроксида натрия или гидроксида калия.
| WO 2011079799 A1, 07.07.2011 | |||
| Щеглова Н | |||
| М | |||
| "Общий способ получения орто-винилбензилзамещенных аминов, эфиров и сульфидов" | |||
| Журнал органической химии | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| Способ смешанной растительной и животной проклейки бумаги | 1922 |
|
SU49A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Станок для изготовления валяной обуви | 1922 |
|
SU1344A1 |
| Погосян Г.М | |||
| "XXXI | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2016-08-27—Публикация
2015-07-23—Подача