ОБЛАСТЬ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Данное изобретение относится к применению конструкции для экспрессии ДНК, которая включает гантелеобразную кольцевую цепочку дезоксирибонуклеиновой кислоты.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Некоторые конструкции ДНК или векторы, которые являются приемлемыми для экспрессии белков, кодируемых последовательностями, содержащимися в пределах такой конструкции ДНК, являются известными в области техники. В зависимости от организма или типа клетки, в которую экспрессионная конструкция будет встроена, они конструируются как эукариотические или прокариотические экспрессионные конструкции. Термин "плазмида" обычно относится к кольцевым экспрессионным конструкциям, которые включают ковалентно замкнутую кольцевую двухцепочечную ДНК. Плазмиды обычно содержат дополнительные последовательности в дополнение к тем, которые будут экспрессироваться, подобные маркерным генам для их специфической селекции, и в некоторых случаях последовательности для их эписомальной репликации в целевой клетке.
Структурно различная экспрессионная конструкция описывается в EP 0941318. Этот документ раскрывает гантелеобразную линейную, ковалентно замкнутую конструкцию ДНК с частично одноцепочечными петлями на обоих концах. Такая конструкция после трансфекции вызывает значительное повышение уровней белковой экспрессии в зависимости от способа введения такой конструкции ДНК в клетку.
EP 0941318 также раскрывает, что применение такой гантелеобразной конструкции ДНК с помощью баллистического переноса является преимущественным в отношении белковой экспрессии. Несмотря на то, что уровень белковой экспрессии повышается, является трудоемким связывать ДНК с помощью абсорбции или ионного связывания с микрочастицами, которые используются для баллистического переноса.
Безыгольные инжекторы, которые являются приемлемыми для переноса ДНК в клетки, являются известными в области техники, например, для применения вакцин. Такой безыгольный инжектор обычно представляет собой медицинское устройство со вспрыскивающим распылителем, который использует узкую насадку высокого давления для инъекции жидкостей. Различие с используемыми обычно гиподермальными иглами для прокалывания эпидермиса заключается в том, что безыгольный инжектор снижает боль, которая ассоциируется с соответствующей инъекцией. Обычно безыгольный инжектор является оснащенным сжатым воздухом или газом, либо с помощью напорного шланга из большого цилиндра, либо из встроенного газового картриджа или маленького цилиндра. В принципе, безыгольные инжекторы используются в качестве альтернативы игольного шприца.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Задача данного изобретения заключается в обеспечении альтернативного применения гантелеподобной конструкции для экспрессии ДНК для переноса в клетки.
Данная заявка обеспечивает применение гантелеподобной линейной, ковалентно замкнутой конструкции ДНК с двухцепочечной основой и одноцепочечными петлями, расположенными на обоих концах основы, где основа комплементарных дезоксирибонуклеиновых кислот кольцевой цепочки ДНК включает промоторную последовательность, кодирующую последовательность и сигнал терминации, которая вводится путем безыгольной инъекции для лечения рака.
Она является сконструированной так, что промоторная последовательность является оперативной в эукариотических клетках и в организме человека. Может быть предпочтительным адаптировать используемый промотор к ткани или источнику соответствующей ткани, для того, чтобы оптимизировать скорость экспрессии после переноса в клетку или ядро, соответственно.
Конструкции ДНК могут использоваться для кодирования иммуномодулирующих агентов и/или маркера поверхности клеток. Термин "иммуномодулятор" включает стимуляторы и супрессоры иммунной системы. Термин "модулирование иммунного ответа" используется в качестве синонима с термином "активация иммунной системы" или в значении интенсификации или супрессии иммунного ответа.
Иммуномодулирующие агенты могут быть выбраны из группы, которая включает антитела, гормоны, цитокины или другие биологически активные вещества. Термин "биологически активный" включает все вещества, которые вызывают эффект после их применения или переноса в клетки или ткани, где не имеет значения, является ли вещество полученным синтетическим путем или оно имеет биологическое происхождение, которое включает генетические способы получения.
Применение в соответствии с данной заявкой включает конструкции ДНК, кодирующие медиатор или мессенджер иммунной системы, подобный цитокинам, который выбирают из группы, которая включает TNF-α, интерлейкин-7, колониестимулирующий фактор гранулоцитов-макрофагов, CD40L/CD154 и B7.1/CD80. Кроме упомянутых носителей. любая другая молекула, которая опосредует иммунологический сигнал, находится в рамках настоящего изобретения.
Применение в соответствии с данной заявкой охватывает также конструкцию ДНК, которую вводят одновременно или последовательно с химиотерапевтическим агентом, где одновременное введение включает ситуацию, когда одно соединение высвобождается с задержкой во времени благодаря соответствующей рецептуре или связыванию с адекватными соединениями.
Применение в соответствии с настоящей заявкой относится к химиотерапевтическим агентам, выбранным из группы, которая включает антитела, алкилирующие агенты, аналоги платины, интеркалирующие агенты, антибиотики, супрессоры митоза, таксаны, супрессоры топоизомераз, антиметаболиты и/или L-аспарагиназу, гидроксикарбамид, митотаны и/или аманитины.
Супрессор митоза виндезин демонстрирует очень хорошие результаты с гантелеподобной экспрессионной ДНК конструкцией, которая кодирует TNF-α.
Также дополнительно предусматривается, что конструкции ДНК обеспечиваются в виде фармацевтически приемлемой композиции, в частности вакцины.
Применение в соответствии с данной заявкой дополнительно предполагается для совместного введения некодирующей, иммуномодулирующей последовательности ДНК с помощью безыгольной инъекции. Опять-таки, это дополнительное соединение может вводиться одновременно или последовательно, и даже в случае одновременного введения отсроченное во времени введение также предполагается.
Также предполагается, что последовательность ДНК некодирующей последовательности ДНК включает, по крайней мере, один мотив последовательности N1N2CGN3N4, где N1N2 представляет собой элемент, взятый из группы, которая состоит из GT, GG, GA, AT или AA, N3N4 представляет собой элемент, взятый из группы, которая состоит из CT или TT, C представляет собой дезоксицитозин, G представляет собой дезоксигуанозин, A представляет собой дезоксиаденозин и T представляет собой дезокситимидин.
В случае, когда некодирующая последовательность представляет собой олигодезоксинуклеотид с открытой цепочкой, приемлемые средства защиты концов от действия нуклеаз находятся в пределах объема данного изобретения.
Некодирующая иммуномодулирующая ДНК может быть гантелеподобной и включать ковалентно замкнутую кольцевую одноцепочечную ДНК, которая частично является двухцепочечной, формируя двухцепочечный стержень и одноцепочечные петли на обоих концах стержня.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Данная заявка обеспечивает новое и изобретательское применение конструкции ДНК, которая может вводиться путем безыгольной инъекции в клетки. С одной стороны, ДНК может вводиться непосредственно в ткани, подобные опухолям, мышцы или соединительные ткани. С другой стороны, применение в соответствии с данной заявкой может осуществляться при использовании культуры клеток. Таким образом, применение является приемлемым для in vivo и in vitro использования.
Объем данной заявки охватывает не только гантелеподобные экспрессионные конструкции, а также двухцепочечные кольцевые экспрессионные конструкции ДНК. Такие экспрессионные конструкции могут кодировать TNF-α и будут применяться вместе с подобным химиотерапевтическим средствам агнетом виндезином.
Термин "рак" включает раковые заболевания или опухоли, подвергающиеся лечению или предотвращению, которые являются выбранными из группы, включающей карциномы молочной железы, меланому, кожные новообразования, опухоли желудочно-кишечного тракта, включая карциномы толстого кишечника, карциномы желудка, карциномы поджелудочной железы, рак толстого кишечника, рак тонкого кишечника, карциномы яичников, карциномы шейки матки, рак легких, рак предстательной железы, карциномы почечных клеток и/или метастазы печени.
Фармацевтический агент будет приемлемым для инъекции, в частности, безыгольной инъекции, включая стерильные водные растворы или дисперсии и стерильные порошки для непосредственного приготовления стерильных растворов или дисперсий для введения. Во всех случаях фармацевтический агент будет обеспечиваться в виде стерильной жидкости до такой степени, в которой является возможным введение с помощью шприца или путем безыгольной инъекции. Она должна быть стабильной при условиях производства и хранения, а также должна быть защищена от контаминирующего воздействия микроорганизмов, таких, как бактерии и грибы.
Носитель может представлять собой растворитель или дисперсионную среду, которая содержит, например, воду, этанол, полиол (например, глицерин, пропиленгликоль, жидкий полиэтиленгликоль и тому подобное), их приемлемые смеси и/или растительные масла. Приемлемая текучесть может поддерживаться, например, путем применения покрытия, такого, как лецитин, путем поддержания необходимого размера частиц в случае дисперсии и путем применения поверхностно-активных веществ. Предотвращение действия микроорганизмов может быть получено с помощью различных бактериальных или противогрибковых агентов, например, парабенов, хлорбутанола, фенола, сорбиновой кислоты, тиомерсала и подобных им. Во многих случаях будет желательным включать изотонические агенты, например, сахара или хлорид натрия. Длительная абсорбция введенных с помощью инъекции композиций может осуществляться путем применения композиций агентов, которые замедляют абсорбцию, например, моностеарата алюминия и желатины.
Стерильные инъецируемые растворы получают путем введения активного соединения в желаемом количестве в приемлемом растворителе с некоторыми другими ингредиентами, перечисленными выше, после чего осуществляют стерилизацию фильтрованием. В общем случае дисперсии получают путем введения различных стерилизованных ингредиентов в стерильный носитель, который содержит основную дисперсионную среду и необходимые другие ингредиенты из тех, что перечислены выше. В случае стерильных порошков для получения стерильных инъецируемых растворов предпочтительные способы получения представляют собой методики вакуумного высушивания и высушивания замораживанием, которые обеспечивают получение порошка активного ингредиента плюс любой дополнительный ингредиент из его предварительно простерилизованного фильтрованием раствора.
Композиции, раскрытые в данной заявке, могут быть рецептированы в нейтральной форме или в форме соли. Фармацевтически приемлемые соли включают соли присоединения кислоты (образованные свободными аминогруппами белка), которые получают с помощью неорганических кислот, таких, как, например, хлористоводородная или фосфорная кислота, или таких органических кислот, как, щавелевая, виннокаменная, миндальная и тому подобное. Соли, образованные с помощью свободных карбоксильных групп, могут быть получены из неорганических оснований, таких, как, например, гидроокиси натрия, калия, аммония, кальция и железа, и таких органических оснований, как изопропиламин, триметиламин, гистидин, прокаин и тому подобное. При рецептировании растворы будут вводиться путем, который является совместимым с дозированным составом, и в таком количестве, которое является терапевтически эффективным. Композиции легко вводятся в разнообразные дозированные формы, такие, как инъецируемые растворы, капсулы для высвобождения лекарственного средства и тому подобное.
Как используется в данной заявке, термин "носитель" включает любой и все растворители, дисперсионные среды, носители, покрытия, разбавители, антибактериальные и противогрибковые агенты, изотонические агенты и агенты, которые задерживают абсорбцию, буферы, растворы носителей суспензии, коллоиды и тому подобное. Применение таких сред и агентов для фармацевтически активных веществ является хорошо известным в области техники.
За исключением случаев, когда какая-либо традиционная среда или агент является несовместимым с активным ингредиентом, их применение в терапевтических композициях предусматривается. Дополнительные активные ингредиенты могут также вводиться в композиции.
Термин "фармацевтический приемлемый" относится к молекулярным частицам и композициям, которые не вызывают аллергической или подобной нежелательной реакции при введении человеку. Препараты водной композиции, которые содержат белок в качестве активного ингредиента, являются хорошо известными в области техники. Типично, такие композиции получают в виде инъецируемых растворов, либо в виде жидких растворов, либо в виде суспензий; а также твердых форм, приемлемых для получения из них раствора или суспензии, при этом жидкость может быть приготовлена перед введением. Препарат также может быть эмульгируемым.
КРАТКОЕ ОПИСАНИЕ ФИГУР
Данная заявка будет проиллюстрирована фигурами и примерами, которые не являются такими, которые ограничивают ее. Фигуры демонстрируют:
Фиг.1. Зависимость от дозы инъецируемой гантелеподобной ДНК, которая вводится в меланомы.
Фиг.2. Сравнение эффективности экспрессии in vivo в опухолях гантелеподобной ДНК и кольцевых двухцепочечных плазмид.
Фиг.3. Генный перенос при использовании гантелеподобной ДНК, взятой отдельно или в комбинации с виндезином.
ПОДРОБНОЕ ОПИСАНИЕ ФИГУР
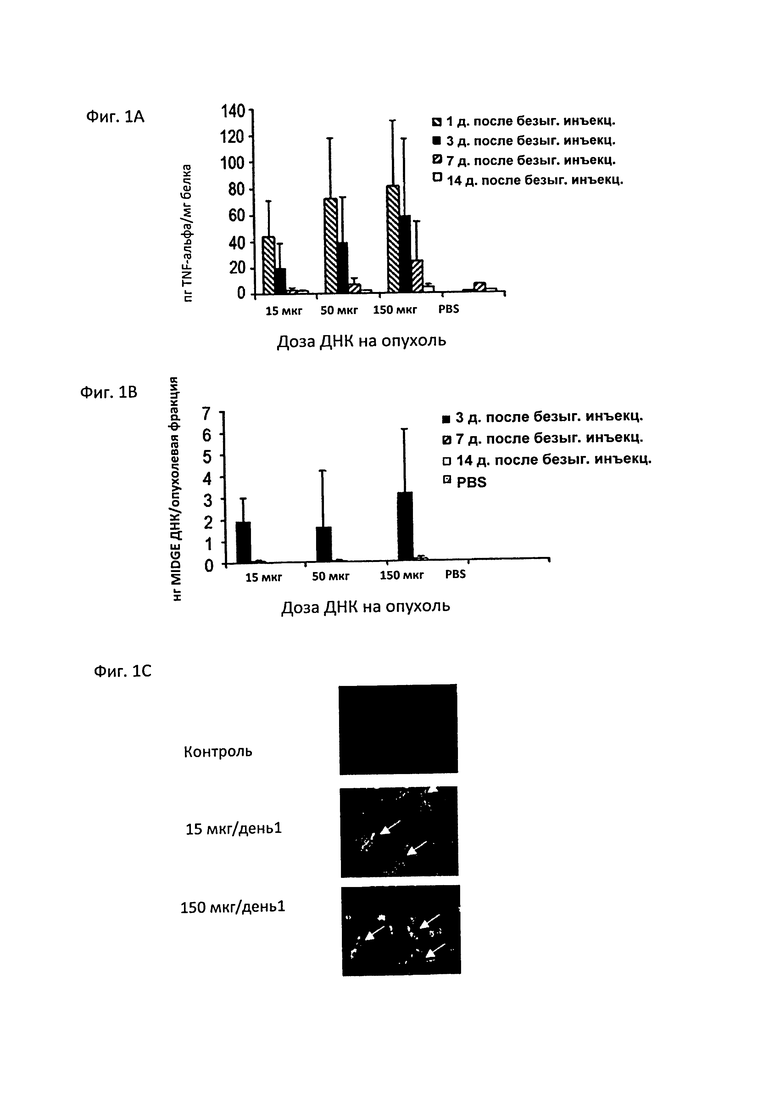
Фиг. 1 показывает зависимость от дозы экспрессии белка и присутствия перенесенной ДНК из соответствующей дозы, которая применяется к опухоли. Перенесенная гантелеподобная конструкция ДНК кодирует TNF-α. Три различных способа применяются для демонстрации экспрессии TNF-α или присутствия перенесенной ДНК в меланомах, которые представляют собой злокачественные опухоли меланоцитов.
Фиг. 1A показывает результаты TNF-ELISA с применяемой дозой ДНК, представленной на оси X (мкг) в соотношении с количеством TNF-α (пг) на количество общего белка (мг) на оси Y через один, три, семь и 14 дней после безыгольной инъекции ДНК.
Является очевидным, что уровень экспрессии белка после безыгольной инъекции зависит от дозы ДНК на опухоль. Для каждой точки времени после осуществления безыгольной инъекции экспрессия белка имела самый высокий уровень для 150 мкг ДНК. Самую сильную экспрессию ДНК наблюдали через один день после безыгольной инъекции 150 мкг ДНК, при этом она снижалась для каждой последующей временной точки проведения измерений. С правой стороны Фиг. 1A PBS, не содержащий ДНК, представлен в качестве негативного контроля.
Фигура 1B показывает количество перенесенной конструкции ДНК (нг) на опухолевую фракцию на оси Y для различных доз ДНК через три дня, семь и 14 дней после инъекции ДНК. ДНК перенесенной гантелеподобной конструкции ДНК подвергали амплификации с помощью ПЦР, и PBS использовали в качестве негативного контроля, что показано с правой стороны оси X.
Результаты амплификации ДНК совпадают с результатами определения белка на Фиг. 1A. Самый высокий уровень ДНК может быть амплифицирован через три дня после безыгольной инъекции, а минимальное количество ДНК может определяться через семь дней после инъекции.
Несмотря на то, что доза ДНК, которая составляет 50 мкг на опухоль, приводила к меньшей экспрессии ДНК, чем доза 15 мкг ДНК, величина ошибки показывает, что среднее значение экспрессии ДНК при использовании 50 мкг ДНК было выше, чем при использовании 15 мкг. В общем случае, доза ДНК 150 мкг на опухоль приводила к самому высокому количеству перенесенной ДНК, которая была способна к амплификации с помощью ПЦР.
Фиг. 1С показывает иммунофлуоресценцию для определения экспрессии TNF-α в опухолях. Стрелки на фигурах показывают клетки, экспрессирующие TNF-α. При этом видно, что перенос 15 мкг и 150 мкг через один день после безыгольной инъекции приводит к ясно определяемой экспрессии TNF-α. Картинка вверху фигуры показывает негативный контроль.
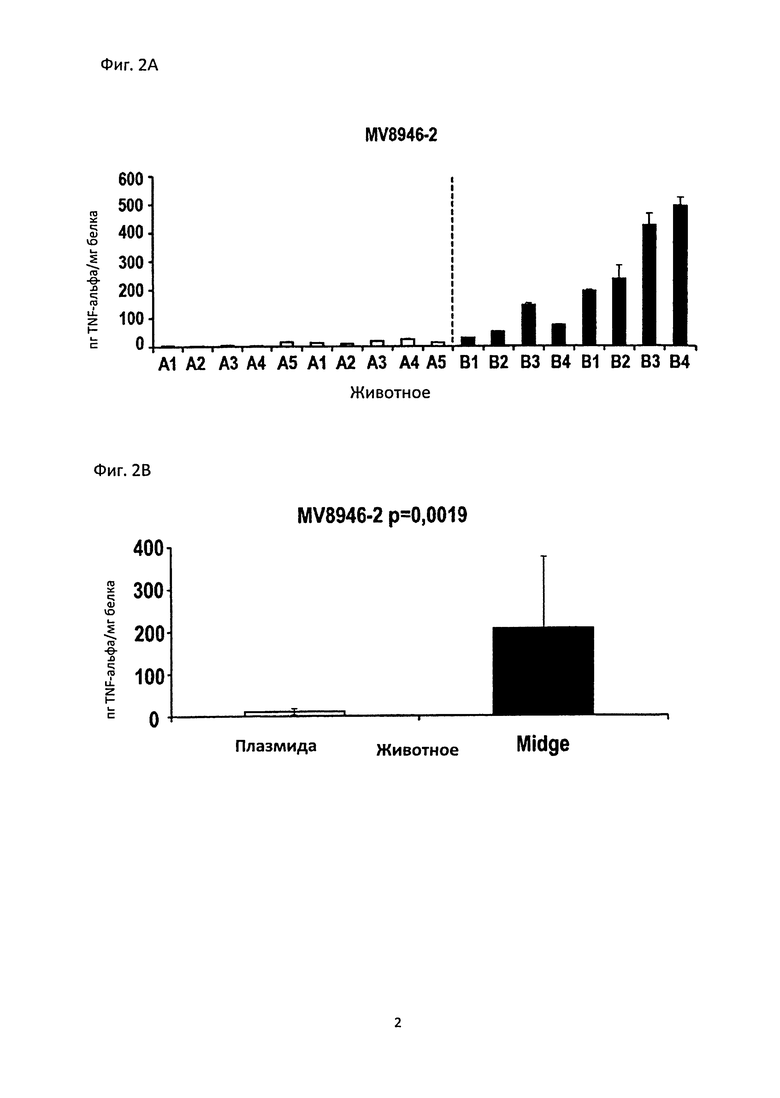
Фиг. 2 показывает эффективность in vivo экспрессии в опухолях по сравнению с гантелеподобной ДНК с замкнутой кольцевой двухцепочечной ДНК. Обе экспрессионные ДНК конструкции кодируют TNF-α. На Фиг. 2A и B результаты для плазмидной ДНК - двухцепочечной кольцевой ДНК - показаны с левой стороны (незаштрихованные столбцы) по сравнению с результатами для гантелеподобной конструкици ДНК с каждой правой стороны (заштрихованные столбцы). Применялись эквимолярные количества конструкции ДНК.
Использовали для экспериментов пять различных животных для плазмидного переноса и четырех различных животных для переноса гантелеподобной ДНК, вес опухолей вместе с массой TNF (пг) на массу опухоли (г) указывали в приведенной ниже таблице.
Фиг. 2A показывает количество TNF-α (пг) на массу общего белка (мг). Является очевидным, что применение плазмидной ДНК не приводило к получению измеряемого количества экспрессированного TNF-α (левая сторона), где применение гантелеподобной конструкции ДНК приводило к получению четко определяемого количества экспрессированного TNF-α (правая сторона).
Как можно увидеть из Фиг. 2 В, среднее количество TNF-α на общую массу белка составляет примерно более чем 200-кратное при использовании гантелеподобной конструкции вместо плазмидной ДНК. Разница между эффективностями экспрессии для плазмидной ДНК против гантелеподобной ДНК является абсолютно неожиданной и не могла быть предсказана, даже тогда, когда принимают во внимание то, что безыгольная инъекция может приводить к лучшему переносу конструкций ДНК. Несмотря на то, что плазмидная ДНК переносилась путем безыгольной инъекции, почти не существовало способной к определению экспрессии TNF-α, в то время как гантелеподобная ДНК вызывала получение значительного количества экспрессированного TNF-α.
В дополнительных экспериментах оценивали влияние экспрессии TNF-α на жизнеспособность клеток и объем опухоли. Фиг. 3 показывает результаты генного переноса при использовании гантелеподобной конструкции ДНК, которая кодирует TNF-α в комбинации с химиотерапевтическим средством виндезином (заштрихованные столбцы) по сравнению с применением только виндезина (незаштрихованные столбцы).
Фиг. 3А показывает результаты in vitro анализа химиосенсибилизации клеток A375 меланомы после переноса только виндезина, а также в комбинации с гантелеподобной конструкцией ДНК, кодирующей TNF-α. Четко видно, что применение только виндезина снижает жизнеспособность клеток. Этот эффект может быть усилен при использовании комбинации виндезина с гантелеподобной конструкцией ДНК, кодирующей TNF-α. Использование виндезина, взятого отдельно, в концентрации 12,8 мкг/мл приводило к относительной жизнеспособности клеток 0,6 по сравнению со значением 0,2, которое получали при параллельном использовании гантелеподобной конструкцией ДНК, кодирующей TNF-α. Степень усиления эффекта является неожиданной и не может приписываться аддитивному эффекту кодирующей TNF-α конструкции ДНК и виндезина, соответственно, как можно увидеть из Фиг. 3B.
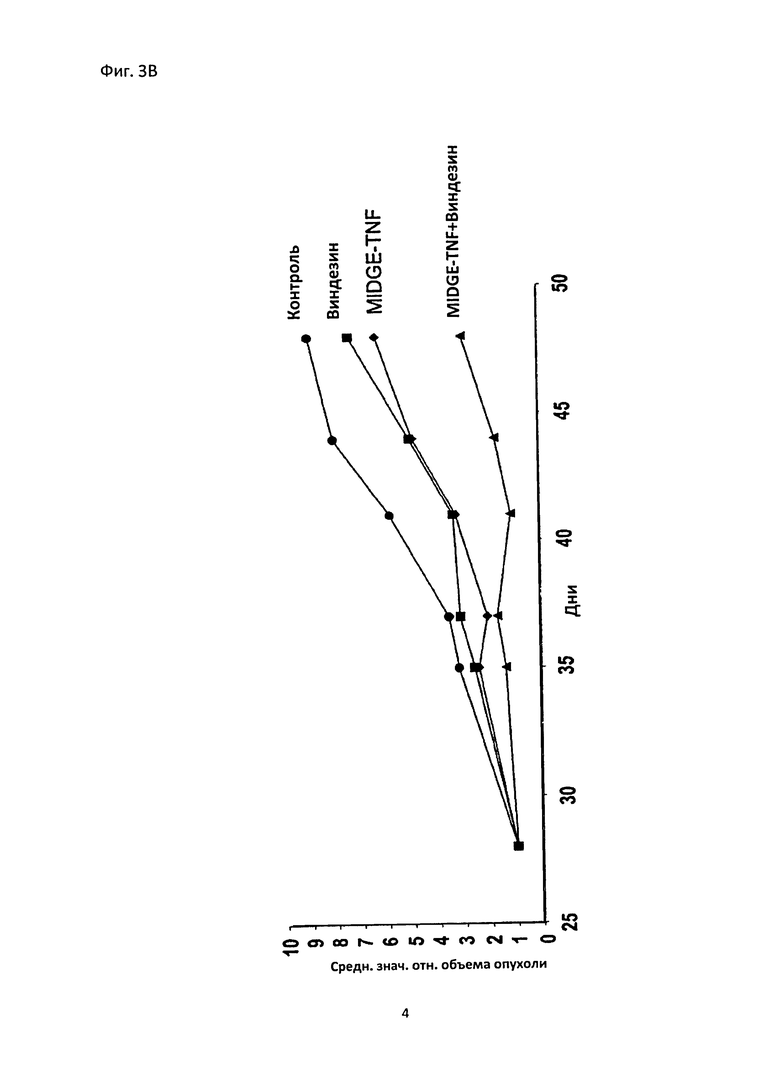
Фиг. 3B показывает химиосенсибилизацию ксенотрансплантированных опухолей A375 меланомы с помощью генного переноса гантелеподобной конструкцией ДНК, кодирующей TNF-α (MIDGE-TNF), виндезина и комбинации MIDGE-TNF с виндезином. Внутриопухолевую безыгольную инъекцию осуществляли при использовании двукратной инъекции 150 мкг гантелеподобной конструкции ДНК и где назначали дополнительно двукратную внутриопухолевую инъекцию 0,5 мг/кг виндезина.
На оси X представлено среднее значение относительного объема опухоли для указанных дней после переноса (ось X). Перенос виндезина и MIDGE-TNF, соответственно, снижал среднее значение относительного объема опухоли, но комбинация виндезина и MIDGE-TNF имела четкий синергетический эффект, который значительно выходил за пределы простого аддитивного эффекта при использовании соединений по отдельности. Такой результат не мог быть ожидаемым и подтверждает гипотезу о том, что клеточная жизнеспособность (Фиг.3А) также снижается с помощью синергетического эффекта, когда виндезин применяют с помощью безыгольной инъекции в комбинации с гантелеподобной конструкцией ДНК, кодирующей TNF-α.
Фигуры показывают, что гантелеподобная конструкция ДНК, кодирующая TNF-α, которую применяют с помощью безыгольной инъекции, приводит к множественной экспрессии кодируемого белка по сравнению с введенной с помощью безыгольной инъекции плазмидной ДНК. Применение гантелеподобной конструкции ДНК в комбинации с химиотерапевтически подобным агентом виндезином оказывает синергетический эффект на жизнеспособность опухолевой клетки и объем опухоли. Оба эффекта не могли быть ожидаемыми, поскольку они являются намного сильнее, чем аддитивные эффекты соединений, взятых по отдельности.
В общем случае эти результаты показывают, что применение гантелеподобной конструкцией ДНК, кодирующей иммуномодуляторы, в частности иммуностимуляторы или иммуносупрессоры, в комбинации с химиотерапевтическим агентом и применение ДНК путем безыгольной инъекции обладает преимуществами для лечения рака или любого другого заболевания, которое является связанным с неконтролируемым ростом.
| название | год | авторы | номер документа |
|---|---|---|---|
| АЛЛОГЕННОЕ ПРОТИВООПУХОЛЕВОЕ ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО | 2004 |
|
RU2354694C2 |
| ДНК КОНСТРУКТ ДЛЯ ЭКСПРЕССИИ | 2011 |
|
RU2604186C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ДИАГНОСТИКИ И ЛЕЧЕНИЯ РАКА | 1996 |
|
RU2174409C2 |
| SPARC-СВЯЗУЮЩИЕ ПЕПТИДЫ И ИХ ПРИМЕНЕНИЕ | 2009 |
|
RU2491085C2 |
| УНИВЕРСАЛЬНЫЕ РАКОВОСПЕЦИФИЧНЫЕ ПРОМОТОРЫ И ИХ ИСПОЛЬЗОВАНИЕ В ПРОТИВООПУХОЛЕВОЙ ТЕРАПИИ | 2013 |
|
RU2539764C2 |
| ПОЛИКОНЪЮГАТЫ ДЛЯ ВВЕДЕНИЯ IN VIVO ПОЛИНУКЛЕОТИДОВ | 2007 |
|
RU2430740C2 |
| МИКРОВЕЗИКУЛА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2014 |
|
RU2693088C2 |
| АКТИВНАЯ ИММУНОТЕРАПИЯ ПРОТИВ АНГИОГЕНЕЗА | 2003 |
|
RU2329824C2 |
| ОПОСРЕДОВАННАЯ РЕЦЕПТОРАМИ ДОСТАВКА ГЕНОВ С ИСПОЛЬЗОВАНИЕМ ВЕКТОРОВ НА ОСНОВЕ БАКТЕРИОФАГОВ | 1998 |
|
RU2209088C2 |
| ДНК, КОДИРУЮЩАЯ НОВЫЙ ПЕПТИД RG1 | 2000 |
|
RU2283130C2 |

Данное изобретение относится к области биотехнологии и медицины. Предложено применение гантелеподобной линейной, ковалентно замкнутой экспрессионной конструкции ДНК с двухцепочечной основой и одноцепочечными петлями, расположенными на обоих концах основы, где основа комплементарных дезоксирибонуклеиновых кислот кольцевой цепочки ДНК включает промоторную последовательность, кодирующую последовательность и сигнал терминации, где конструкция ДНК кодирует TNF-α, для лечения меланомы, причем указанная конструкция ДНК вводится путем безыгольной инъекции и указанная конструкция вводится одновременно или последовательно с виндесином. Применение упомянутой конструкции ДНК приводит к существенному усилению действия винденсина. 4 з.п. ф-лы, 7 ил., 1 табл.
1. Применение гантелеподобной линейной, ковалентно замкнутой экспрессионной конструкции ДНК с двухцепочечной основой и одноцепочечными петлями, расположенными на обоих концах основы, где основа комплементарных дезоксирибонуклеиновых кислот кольцевой цепочки ДНК включает промоторную последовательность, кодирующую последовательность и сигнал терминации, где конструкция ДНК кодирует TNF-α, для лечения меланомы, причем указанная конструкция ДНК вводится путем безыгольной инъекции и указанная конструкция вводится одновременно или последовательно с виндесином.
2. Применение гантелеподобной линейной, ковалентно замкнутой экспрессионной конструкции ДНК по п.1, где промоторная последовательность является функциональной в эукариотических клетках и в организме человека.
3. Применение гантелеподобной линейной, ковалентно замкнутой экспрессионной конструкции ДНК по любому из пп.1 и 2, где конструкция ДНК обеспечивается в виде фармацевтически приемлемой композиции.
4. Применение гантелеподобной линейной, ковалентно замкнутой экспрессионной конструкции ДНК по п.3, где фармацевтическая композиция является вакциной.
5. Применение гантелеподобной линейной, ковалентно замкнутой экспрессионной конструкции ДНК по п.4, где последовательность ДНК включает по крайней мере один мотив последовательности N1N2CGN3N4, где N1N2 представляет собой элемент, взятый из группы, которая состоит из GT, GG, GA, AT или АА, N3N4 представляет собой элемент, взятый из группы, которая состоит из СТ или ТТ, С представляет собой дезоксицитозин, G представляет собой дезоксигуанозин, А представляет собой дезоксиаденозин и Т представляет собой дезокситимидин.
| KOCHLING JOACHIM et al | |||
| "Anti-tumor effect of DNA-based vaccination and dSLIM immunomodulatory molecules in mice with Ph+ acute lymphoblastic leukaemia", Vaccine, 2008, 26(36): 4669-4675;US 6,451,593 B1, 17.09.2002 | |||
| SCHAKOWSKI FRANK et al | |||
| "A novel minimal-size vector (MIDGE) improves transgene expression in colon carcinoma cells and avoids |
Авторы
Даты
2016-09-27—Публикация
2011-09-08—Подача