ОБЛАСТЬ ТЕХНИКИ
[0001] Настоящее изобретение относится к соли 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина, которая пригодна в качестве противоопухолевого средства.
Предшествующий уровень техники
[0002] Известно, что 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозин (далее также обозначаемый как "соединение А") обладает превосходной противоопухолевой активностью и пригоден в качестве терапевтического средства против опухолей (патентный документ 1). Также известно, что соединение А демонстрирует сильную противоопухолевую активность у мышей даже при пероральном введении (непатентные документы 1 и 2).
Ссылки на известный уровень техники
Патентный документ
[0003] Патентный документ 1: международная патентная публикация WO 97/038001
Непатентные документы
[0004] Непатентный документ 1: Cancer Letters, Vol. 144, pp. 177-182, 1999
Непатентный документ 2: Oncology Reports, Vol. 9, pp. 1319-1322, 2002
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Цель для достижения по изобретению
[0005] Недостатком соединения А является низкая водорастворимость, и, таким образом, для применения в качестве лекарственного средства для людей необходимо улучшить растворимость. Также недостатком соединения А является плохие текучесть и свойство таблетируемости, и, таким образом, существует проблема, относящаяся к производству фармацевтических средств с его использованием.
Таким образом, крайне желательно, чтобы соединение А демонстрировало высокую водорастворимость, превосходную стабильность при хранении, текучесть и/или свойство таблетируемости.
Способы достижения цели
[0006] В таких условиях, как указано выше, авторы настоящего изобретения провели различные исследования. В результате они выявили, что соль соединения A обладает по меньшей мере одной или несколькими из таких характеристик, как то, что (1) она обладает превосходной противоопухолевой активностью, (2) она демонстрирует превосходную кристаллизуемость, (3) она обладает высокой водорастворимостью, (4) она не демонстрирует гигроскопичности (свойства растворяться за счет поглощения влаги), (5) она демонстрирует превосходную текучесть, (6) она демонстрирует превосходное свойство таблетируемости, (7) ее можно производить с меньшим воздействием на окружающую среду и (8) ее можно производить в крупном масштабе, и, таким образом, она пригодна в качестве нерасфасованного лекарственного средства для получения лекарственных средств, и, таким образом, они осуществили настоящее изобретение.
[0007] Настоящее изобретение относится к следующему:
[1] Фармацевтически приемлемая соль 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина.
[2] Соль по [1], которая представляет собой соль неорганической кислоты или сульфонат.
[3] Соль по [2], где соль неорганической кислоты представляет собой гидрохлорид, гидробромид, йодогидрат, нитрат, фосфат или сульфат; а сульфонат представляет собой метансульфонат, бензолсульфонат, п-толуолсульфонат, мезителенсульфонат или нафталинсульфонат.
[4] Соль по [2], где соль неорганической кислоты представляет собой гидрохлорид, йодогидрат, нитрат или сульфат; а сульфонат представляет собой метансульфонат.
[5] Соль по [2], где соль неорганической кислоты представляет собой гидрохлорид; а сульфонат представляет собой метансульфонат.
[6] Кристалл метансульфоната 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина, демонстрирующий характеристические пики при дифракционных углах (2θ) 19,8, 21,8, 27,5, 28,4 и 29,9 градусов при рентгеновской порошковой дифрактометрии, или кристалл гидрохлорида 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина, демонстрирующий характеристические пики при дифракционных углах (2θ) of 9,2, 14,7, 15,7, 22,9 и 27,3 градусов при рентгеновской порошковой дифрактометрии.
[7] Фармацевтическая композиция, содержащая соль по любому из [1]-[5], или кристалл по [6].
[8] Фармацевтическая композиция по [7], которая предназначена для применения при лечении опухоли.
[9] Способ получения соли по любому из [1]-[5], который включает стадию переведения 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина в его фармацевтически приемлемую соль.
[0008] Дополнительно настоящее изобретение относится к следующему.
Соль 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина с противоопухолевой активностью.
Применение соли 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина для производства противоопухолевого средства или производства лекарственного средства для применения при лечении опухоли.
Способ лечения опухоли, который включает стадию введения соли 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина индивидууму.
Соль 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина для применения в способе лечения опухоли.
Эффект изобретения
[0009] Соль по настоящему изобретению обладает по меньшей мере одной или несколькими из таких характеристик, как то, что (1) она обладает превосходной противоопухолевой активностью, (2) она демонстрирует превосходную кристаллизуемость, (3) она демонстрирует высокую водорастворимость, (4) она не демонстрирует свойства растворяться за счет поглощения влаги, (5) она демонстрирует превосходную текучесть, (6) она демонстрирует превосходное свойство таблетируемости, (7) ее можно производить с меньшим воздействием на окружающую среду и (8) ее можно производить в крупном масштабе, и, таким образом, она пригодна в качестве нерасфасованного лекарственного средства для лекарственных средств.
В частности, соль по настоящему изобретению демонстрирует превосходную водорастворимость.
Соль по настоящему изобретению не демонстрирует свойства растворяться за счет поглощения влаги и, в частности, демонстрирует превосходную стабильность при хранении.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
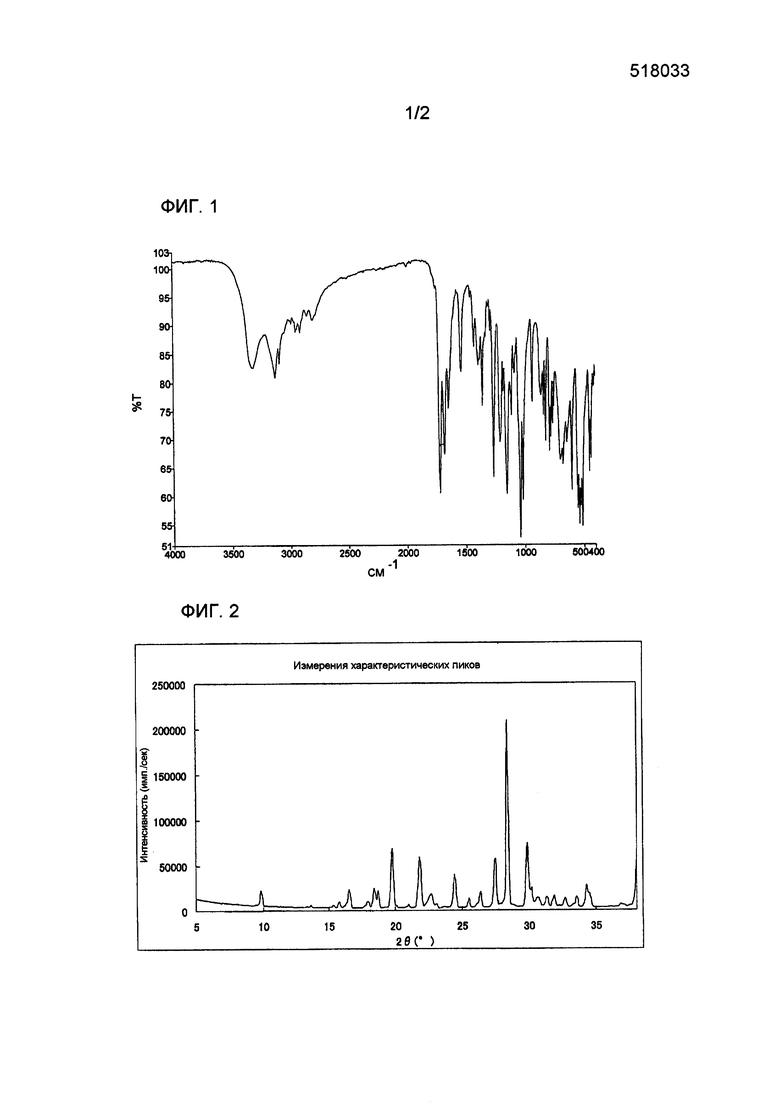
[0010] На фиг. 1 представлен результат инфракрасной абсорбционной спектрометрии метансульфоната 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина.
На фиг. 2 представлен спектр рентгеновской порошковой дифракции метансульфоната 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина.
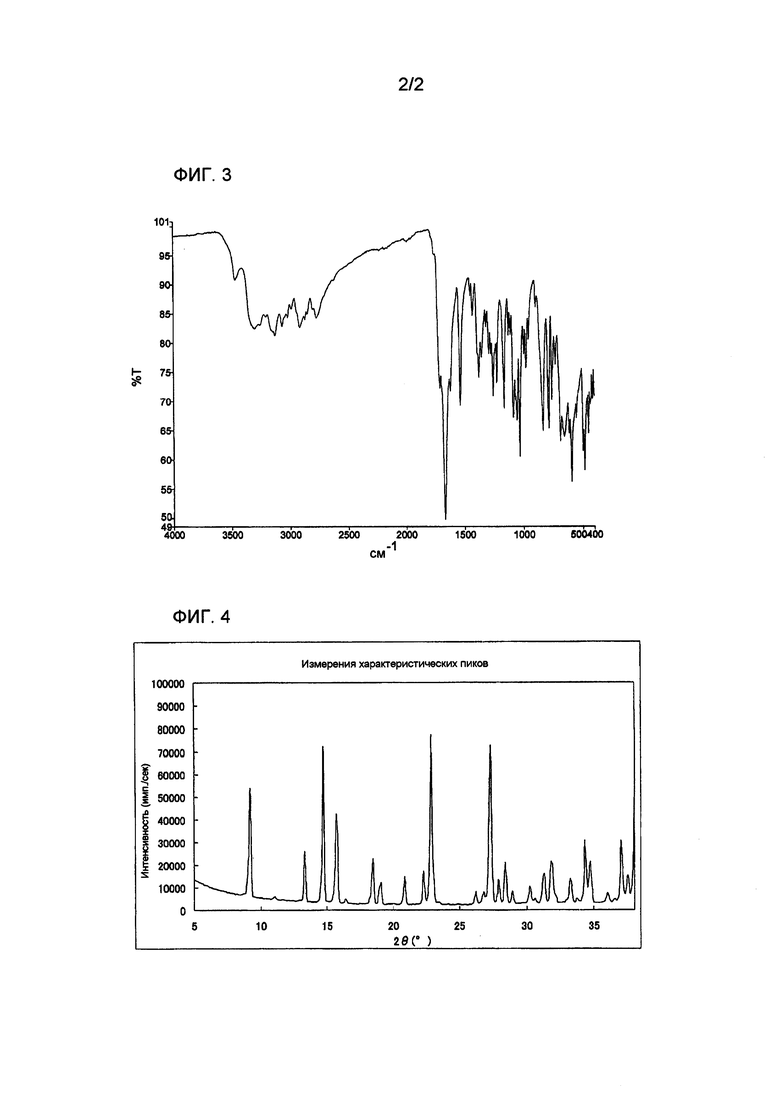
На фиг. 3 представлен результат инфракрасной абсорбционной спектрометрии гидрохлорида 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина.
На фиг. 4 представлен спектр рентгеновской порошковой дифракции гидрохлорида 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина.
Способы осуществления изобретения
[0011] Ниже подробно описано настоящее изобретение. В настоящем изобретении, если конкретно не указано, значения с последующим "%" используют по массе, и если конкретно не указано, диапазоны, указанные с использованием "-", представляют собой диапазоны, включающие значения на обеих сторонах от "-".
[0012] Настоящее изобретение относится к фармацевтически приемлемой соли соединения A. Примеры фармацевтически приемлемой соли включают соль неорганической кислоты, органический карбоксилат и сульфонат. Предпочтительные примеры соли включают соль неорганической кислоты и сульфонат.
[0013] Примеры соли неорганической кислоты включают, например, гидрохлорид, гидробромид, йодогидрат, нитрат, фосфат, а предпочтительными являются сульфат, гидрохлорид, йодогидрат, нитрат и сульфат, а наиболее предпочтительным является гидрохлорид. Примеры органического карбоксилата включают, например, формиат, ацетат, цитрат, оксалат, фумарат, малеат, сукцинат, малат, тартрат, аспартат, трихлорацетат и трифторацетат. Примеры сульфоната включают, например, метансульфонат, бензолсульфонат, п-толуолсульфонат, мезитиленсульфонат и нафталинсульфонат, а предпочтительным является метансульфонат.
[0014] Соль по настоящему изобретению может представлять собой ангидрид, гидрат или сольват. Когда термин "соль" просто используют в настоящем изобретении, она может находиться в форме ангидрида, гидрата или сольвата. В отношении термина "ангидрид", используемого в настоящем изобретении, он относится к соли в состоянии, которое не является ни гидратом, ни сольватом, и даже вещество, которое исходно не формирует гидрат или сольват, также включено в "ангидрид", указываемый в настоящем изобретении, при условии, что он не содержит воды, гидратирующей воды или взаимодействующего растворителя. Ангидрид также можно называть "ангидрат". Когда соль представляет собой гидрат, молекулярная масса гидратирующей воды конкретно не ограничена, и она может представлять собой моногидрат, дигидрат или т.п. Примеры сольвата включают, например, сольват метанола, сольват этанола, сольват пропанола и сольват 2-пропанола.
[0015] Особенно предпочтительные конкретные примеры соли по настоящему изобретению представляют собой следующее:
метансульфонат 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина;
гидрохлорид 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина;
полусульфат 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина;
нитрат 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина и
йодогидрат 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина; а также
ангидриды указанных выше солей.
[0016] Соль по настоящему изобретению может находиться в форме кристалла. Один из предпочтительных вариантов осуществления настоящего изобретения представляет собой кристалл метансульфоната 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина, демонстрирующий характеристические пики при дифракционных углах (2θ) 19,8, 21,8, 27,5, 28,4 и 29,9 градусов при рентгеновской порошковой дифрактометрии. Другим предпочтительным примером является кристалл гидрохлорида 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина, демонстрирующий характеристические пики при дифракционных углах (2θ) 9,2, 14,7, 15,7, 22,9 и 27,3 градусов при рентгеновской порошковой дифрактометрии.
[0017] Результаты рентгеновской порошковой дифрактометрии кристалла гидрохлорида и кристалла метансульфоната представлены на фиг. 1 и 2.
[0018] Дифракционные углы, при которых кристалл демонстрирует характеристические пики при рентгеновской порошковой дифрактометрии, могут варьироваться в зависимости от условий измерения. Как правило, 2θ может содержать ошибку в диапазоне ±0,2 градуса. Таким образом, если конкретно не указано, "дифракционный угол X градусов 2θ", указанный по настоящему изобретению, означает "дифракционный угол от ((X-0,2) до (X+0,2)) градусов 2θ". Таким образом, в объем настоящего изобретения входит не только кристалл, демонстрирующий характеристические пики при рентгеновской порошковой дифрактометрии при дифракционных углах, полностью соответствующих определенным углам, но также и кристалл, демонстрирующий характеристические пики при дифракционных углах, соответствующих определенным углам с ошибкой в диапазоне ±0,2 градуса.
[0019] Ниже описан способ получения соли по настоящему изобретению. Соединение A можно получать способом, описанным в патентном документе 1 или Journal of Organic Chemistry, Vol. 64, pp.7912-7920, 1999. Соль соединения A и ее гидрат или сольват можно получать комбинацией известных способов, и их можно получать, например, указанными ниже способами получения.
[0020] Соль соединения A можно получать, суспендируя соединение A в слабом растворителе, добавляя кислоту для растворения соединения A, а затем удаляя растворитель или добавляя растворитель, в котором растворенная соль соединения A является нерастворимой, для осаждения соли. Более конкретно, соль соединения A можно получать, суспендируя соединение A в воде, добавляя кислоту для растворения соединения, а затем выпаривая воду. Альтернативно, соль соединения A можно получать, суспендируя соединение A в воде, добавляя кислоту для растворения соединения, а затем добавляя ацетон для осаждения соли.
[0021] Примеры слабого растворителя включают, например, воду, ацетон, ацетонитрил, этилацетат, изопропилацетат, метанол, этанол, пропанол и 2-пропанол, и их можно использовать в качестве смеси. Количество слабого растворителя для использования составляет от 2,5- до 120-кратного количества, предпочтительно от 5- до 60-кратного количества, более предпочтительно от 10- до 30-кратного количества, относительно соединения A (об./мас.). Количество кислоты для использования составляет от 0,5 до 4,0 эквивалентов, предпочтительно от 1,0 до 2,0 эквивалентов, более предпочтительно от 1,0 до 1,5 эквивалентов, соединения A, хотя это зависит от типа кислоты.
Примеры растворителя, в котором соль нерастворима, включают, например, ацетон, изопропилацетат, этанол, пропанол и 2-пропанол, и их можно использовать в качестве смеси. Количество растворителя, в котором соль нерастворима, для использования составляет от 2,5- до 120-кратного количества, предпочтительно от 5- до 60-кратного количества, более предпочтительно от 10- до 30-кратного количества, относительно соединения A (об./мас.).
[0022] Соль, предоставляемая по настоящему изобретению, демонстрирует превосходную растворимость, физическую и химическую стабильность (свойство растворяться за счет поглощения влаги, свойство выветривания, свойства летучести, свойство испарения, свойство отверждения, свойство коагуляции, изменение на свету, изменение окраски, распад, образование нерастворимого вещества) и технологичность (простоту обработки при производстве), и, таким образом, она пригодна в качестве нерасфасованного лекарственного средства для лекарственных средств.
[0023] Соль соединения A по настоящему изобретению можно использовать в качестве противоопухолевого средства или активного ингредиента фармацевтической композиции. В настоящем изобретении термин "лечение" включает профилактическое лечение и терапевтическое лечение.
[0024] Фармацевтическую композицию по настоящему изобретению можно использовать для лечения опухоли. Фармацевтическую композицию по настоящему изобретению можно эффективно использовать для лечения опухолей различных типов, включая меланому, гепатому, нейроглиому, нейробластому, саркому, опухоли легкого, толстого кишечника, молочной железы, мочевого пузыря, яичника, семенников, предстательной железы, шеечной части, поджелудочной железы, желудка, тонкого кишечника и других органов. Среди солей соединения A различных видов для фармацевтической композиции по настоящему изобретению можно использовать только один вид или в ней может содержаться два или более видов солей. Фармацевтическую композицию по настоящему изобретению можно использовать в комбинации с другими терапевтическими лекарственными средствами, содержащими известное противоопухолевое средство, как правило, используемое в этой области.
[0025] Как правило, фармацевтическая композиция по настоящему изобретению может содержать добавки, используемые в производстве лекарственных средств, такие как эксципиент, связывающее средство, смазочное средство, дезинтегрирующее средство, краситель, корригирующее средство, эмульгатор, поверхностно-активное вещество, средство, способствующее растворению, суспендирующее средство, средство придания изотоничности, буферное средство, консервант, антиоксидант, стабилизатор и усилитель всасывания.
[0026] В отношении способа введения фармацевтической композиции по настоящему изобретению примеры способа введения включают, например, внутривенные, внутриартериальные, интраректальные, интраперитонеальные, внутримышечные, внутриопухолевые и внутрикистозные инъекции, пероральное введение, кожное введение, применение суппозиториев и т.п. В отношении дозы и частоты введения можно вводить, например, от 0,01 до 1000 мг/кг в сутки соли по настоящему изобретению перорально или парентерально (например, посредством инъекции, капельного введения, введения в прямую кишку и т.д.) взрослому раз в сутки или несколько раз в сутки с разделением указанной выше дозы. Примеры формы фармацевтической композиции в качестве фармацевтического препарата включают таблетку, капсулу, порошок, сироп, гранулу, пилюлю, суспензию, эмульсию, раствор, порошковый препарат, суппозиторий, глазные капли, назальные капли, ушные капли, пластырь, мазь и инъекцию.
ПРИМЕРЫ
[0027] Для объяснения пригодности соединения по настоящему изобретению настоящее изобретение описано на основе приводимых ниже примеров тестирования.
[0028] Пример тестирования 1: Противоопухолевая активность
В качестве тестируемых соединений выбирали соединения из примеров 1 и 2.
В качестве сравниваемого соединения выбирали соединение A.
Клетки в логарифмической фазе инокулировали в 96-луночный планшет при плотности 1000 клеток/лунку (BxPC-3, MIA PaCa-2) или 3000 клеток/лунку (Capan-1) и культивировали в течение ночи при 37°C в CO2-инкубаторе. На следующие сутки добавляли серийно разбавленные растворы каждого из тестируемых соединений и проводили культивирование в течение 3 суток в инкубаторе. После завершения культивирования измеряли испускание с использованием набора для анализа клеточной пролиферации ATPlite (Perkin Elmer) и планшетного спектрофотометра Envision (Perkin Elmer). Концентрации тестируемых соединений, обеспечивающие 50% ингибирование клеточной пролиферации (IC50), рассчитывали посредством аппроксимации с использованием сигмоидной функции. Растворы тестируемых соединений получали, разбавляя их PBS (pH 7,4) до 10 мМ и дополнительно разбавляя 10 мМ растворы PBS (pH 7,4), и использовали в тесте.
Результаты представлены в таблице 1.
[0029]
[0030] Соединения по настоящему изобретению продемонстрировали превосходную противоопухолевую активность.
[0031] Пример тестирования 2: Тест растворимости
В качестве тестируемых соединений выбирали соединения из примеров 1-5.
В качестве сравниваемого соединения выбрали соединение A.
Каждое из тестируемых соединений и сравниваемое соединение добавляли в воду и смесь перемешивали при комнатной температуре в течение 24 часов. Нерастворимое вещество удаляли посредством фильтрации с использованием мембранного фильтра (0,2 мкм). Для определения растворимости фильтрат анализировали посредством высокоэффективной жидкостной хроматографии (ВЭЖХ).
Результаты представлены в таблице 2.
[0032]
[0033] Соединения по настоящему изобретению продемонстрировали высокую растворимость в воде, т.е. превосходную растворимость.
[0034] Пример тестирования 3: Тест стабильности
В качестве тестируемых соединений выбирали соединения из примеров 1 и 2.
Соединения из примеров 1 и 2 хранили в течение 2 недели в открытом виде в условиях 60°C и 75% относительной влажности. Тестируемые соединения подвергали макроскопическому осмотру после хранения и определяли присутствие или отсутствие растворимости за счет поглощения влаги. В результате соединения из примеров 1 и 2 не растворялись за счет поглощения влаги, а были стабильными.
[0035] Соединения по настоящему изобретению не продемонстрировали свойства растворяться за счет поглощения влаги, а продемонстрировали превосходную стабильность.
[0036] Пример тестирования 4: Тест текучести
В качестве тестируемых соединений выбирали соединения из примеров 1 и 2.
В качестве сравниваемого соединения выбрали соединение A.
Каждое из тестируемых соединений и сравниваемое соединение просеивали через сито 177 мкм (80M) с получением порошкового образца. Полученным порошковым образцом приблизительно заполняли стеклянный мерный цилиндр (10 см3), верхнюю поверхность слоя порошка горизонтально выравнивали и определяли значение объема. Массу порошкового образца делили на объем с определением насыпной объемной плотности (г/см3).
Затем стеклянный мерный цилиндр заполняли порошковым образцом, который обстукивали с использованием устройства измерения основных характеристик порошков (Powdertester Type PT-E, Hosokawa Micron CORP.). Когда объем порошка переставал изменяться, определяли значение объема. Массу порошкового образца делили на объем с определением утрамбованной объемной плотности (г/см3).
Коэффициент уплотнения (%) получали в соответствии со следующим уравнением:
Коэффициент уплотнения (%) = [(уплотненная объемная плотность - насыпная объемная плотность)/уплотненная объемная плотность] × 100.
Результаты представлены в таблице 3.
[0037]
[0038] Соединения по настоящему изобретению продемонстрировали малые коэффициенты уплотнения и, таким образом, продемонстрировали превосходную текучесть. Соединения по настоящему изобретению продемонстрировали превосходные физические свойства.
[0039] Пример тестирования 5: Тестирование свойства таблетируемости
В качестве тестируемых соединений выбирали соединения из примеров 1 и 2.
В качестве сравниваемого соединения выбрали соединение A.
Каждое из тестируемых соединений и сравниваемое соединение просеивали через сито 177 мкм (80M) с получением порошкового образца. Полученный порошковый образец прессовали с использованием таблетирующей машины (Tableting Machine HT-P18A, Hata Iron Works, Ltd.; диаметр таблетирования 6,5 мм; давление таблетирования 1000 кгс; масса таблетки 100 мг) с получением таблеток. Полученные таблетки осматривали макроскопически и классифицировали по следующим критериям:
5 баллов: Поверхность глянцевая.
4 балла: Поверхность немного шероховатая.
3 балла: Поверхность шероховатая.
2 балла: Поверхность немного зазубренная.
1 балл: Поверхность зазубренная.
0 баллов: Таблетки прилипают к пестику и не могут отклеиться.
Таблетирование проводили пять раз и рассчитывали среднее пяти оценок. Результаты представлены в таблице 4.
[0040]
[0041] Соединения по настоящему изобретению продемонстрировали высокие оценки и, таким образом, продемонстрировали превосходное свойство таблетируемости. Соединения по настоящему изобретению продемонстрировали превосходные физические свойства.
[0042] Ниже настоящее изобретение описано на основе примеров. Однако настоящее изобретение не ограничено этими примерами.
Содержание влаги измеряли гигрометром Karl Fischer.
Спектр поглощения в инфракрасной части измеряли посредством спектроскопии нарушенного полного внутреннего отражения поглощения в инфракрасной части спектра (способ ATR).
Сокращения в примерах имеют следующие значения.
Соединение A: 1-(2-Дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозин
DMSO-D6: Тяжелый диметилсульфоксид
[0043] ПРИМЕР 1
Соединение A получали способом, описанным в Journal of Organic Chemistry, Vol. 64, pp.7912-7920, 1999 (то же самое применяют в приводимых ниже примерах). В суспензию соединения A (4,0 г) в воде (73 мл) добавляли метансульфоновую кислоту (0,99 мл) и смесь перемешивали при комнатной температуре в течение 35 минут. После визуального подтверждения растворения выпаривали растворитель при пониженном давлении. К полученному остатку добавляли ацетон (75 мл) и смесь перемешивали при комнатной температуре в течение 30 минут. Твердое вещество собирали посредством фильтрации, промывали ацетоном и сушили на воздухе с получением метансульфоната соединения A (5,2 г) в виде белого твердого вещества. Содержание влаги: 1,3% (массовое отношение).
[0044] 1Н ЯМР (ДМСО-d6) δ: 9,55 (1Н, с), 8,56 (1Н, с), 8,46 (1Н, д, J=7,9 Гц), 6,28 (1Н, дд, J=10,6, 5,3 Гц), 6,14 (1Н, д, J=7,9 Гц), 5,06 (1Н, дт, J=50,2, 5,9 Гц), 4,24-4,13 (1Н, м), 3,80-3,61 (2Н, м) 3,23 (1Н, кв, J=5,7 Гц), 2,35 (3Н, с).
[0045] Результат инфракрасной абсорбционной спектрометрии полученного кристалла метансульфоната соединения A представлен на фиг. 1.
[0046] Проводили рентгеновскую порошковую дифракцию полученного кристалла метансульфоната соединения A.
Условия рентгеновской порошковой дифрактометрии:
Используемые рентгеновские лучи: CuKα
Прилагаемое напряжение: 50 кВ
Прилагаемый ток: 280 мА
Ось сканирования: 2θ
[0047] Полученный спектр рентгеновской порошковой дифракции представлен на фиг. 2 и в таблице 5.
[0048]
[0049] ПРИМЕР 2
К суспензии соединения A (4,0 г) в воде (68 мл) добавляли концентрированную соляную кислоту (1,31 мл) и смесь перемешивали при комнатной температуре в течение 1 часа. После визуального подтверждения растворения выпаривали растворитель при пониженном давлении. К полученному остатку добавляли ацетон (68 мл) и смесь перемешивали при комнатной температуре в течение 1 часа. Твердое вещество собирали посредством фильтрации, промывали ацетоном и сушили на воздухе с получением гидрохлорида соединения A (4,5 г) в виде белого твердого вещества. Содержание влаги: 0,9% (массовое отношение).
[0050] 1Н ЯМР (ДМСО-d6) δ: 9,80 (1Н, с), 8,71 (1Н, с), 8,47 (1Н, д, J=7,9 Гц), 6,27 (1Н, дд, J=9,9, 5,3 Гц), 6,21 (1Н, д, J=7,9 Гц), 5,07 (1Н, дт, J=50,4, 6,1 Гц), 4,22-4,14 (1Н, м), 3,80-3,61 (2Н, м) 3,23 (1Н, кв, J=5,7 Гц).
[0051] Результат инфракрасной абсорбционной спектрометрии полученного кристалла гидрохлорида соединения A представлен на фиг. 3.
[0052] Измеряли рентгеновскую порошковую дифракцию полученного кристалла гидрохлорида соединения A. Условия измерения являлись такими же, как условия, используемые в примере 1. Полученный спектр рентгеновской порошковой дифракции представлен на фиг. 4 и в таблице 6.
[0053]
[0054] ПРИМЕР 3
К суспензии соединения A (50 мг) в воде (1,0 мл) добавляли серную кислоту (5 мкл) и смесь перемешивали при комнатной температуре в течение 10 минут. После визуального подтверждения растворения выпаривали растворитель при пониженном давлении. К полученному остатку добавляли ацетон (1,0 мл). Твердое вещество собирали посредством фильтрации и сушили на воздухе с получением полусульфата соединения A (50 мг) в виде белого твердого вещества.
[0055] 1Н ЯМР (D2O) δ: 8,56 (1Н, д, J=8,6 Гц), 6,40 (1Н, дд, J=8,9, 5,6 Гц), 6,26 (1Н, д, J=7,9 Гц), 5,19 (1Н, дт, J=50,0, 6,3 Гц), 4,42-4,34 (1Н, м), 3,94-3,84 (2Н, м) 3,44 (1Н, кв, J=5,5 Гц).
[0056] ПРИМЕР 4
К суспензии соединения A (50 мг) в воде (1,0 мл) добавляли 60% азотную кислоту (0,014 мл) и смесь перемешивали при комнатной температуре в течение 10 минут. После визуального подтверждения растворения выпаривали растворитель при пониженном давлении. К полученному остатку добавляли ацетон (1,0 мл). Твердое вещество собирали посредством фильтрации и сушили на воздухе с получением нитрата соединения A (70 мг) в виде белого твердого вещества.
[0057] 1Н ЯМР (ДМСО-d6) δ: 9,50 (1Н, с), 8,45 (1Н, д, J=7,9 Гц), 8,35 (1Н, с), 6,29 (1Н, дд, J=10,6, 5,3 Гц), 6,13 (1Н, д, J=7,9 Гц), 5,06 (1Н, дт, J=50,2, 5,9 Гц), 4,22-4,14 (1Н, м), 3,71 (2Н, м) 3,24 (1Н, кв, J=5,6 Гц).
[0058] ПРИМЕР 5
К суспензии соединения A (50 мг) в воде (1,0 мл) добавляли 57% йодистоводородную кислоту (0,025 мл) и смесь перемешивали при комнатной температуре в течение 10 минут. После визуального подтверждения растворения выпаривали растворитель при пониженном давлении. К полученному остатку добавляли ацетон (1,0 мл). Твердое вещество собирали посредством фильтрации и сушили на воздухе с получением йодогидрата соединения A (50 мг) в виде белого твердого вещества.
[0059] 1Н ЯМР (ДМСО-d6) δ: 9,51 (1Н, с), 8,45 (1Н, д, J=7,9 Гц), 8,38 (1Н, с), 6,29 (1Н, дд, J=10,6, 5,3 Гц), 6,13 (1Н, д, J=7,9 Гц), 5,06 (1Н, дт, J=50,2, 5,9 Гц), 4,22-4,14 (1Н, м), 3,71 (2Н, м) 3,24 (1Н, кв, J=5,6 Гц).
ПРИМЕНИМОСТЬ В ПРОМЫШЛЕННОСТИ
[0060] Соль по настоящему изобретению демонстрирует по меньшей мере одну или несколько из таких характеристик, как то, что (1) она обладает превосходной противоопухолевой активностью, (2) она демонстрирует превосходную кристаллизуемость, (3) она демонстрирует высокую водорастворимость, (4) она не демонстрирует свойства растворяться за счет поглощения влаги, (5) она демонстрирует превосходную текучесть, (6) она демонстрирует превосходное свойство таблетируемости, (7) ее можно производить с меньшим воздействием на окружающую среду и (8) ее можно производить в крупном масштабе, и, таким образом, она пригодна в качестве нерасфасованного лекарственного средства для лекарственных средств.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЖИДКИЙ ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ | 2017 |
|
RU2715240C1 |
| ПРОТИВООПУХОЛЕВЫЙ АГЕНТ, УСИЛИТЕЛЬ ПРОТИВООПУХОЛЕВОГО ДЕЙСТВИЯ И ПРОТИВООПУХОЛЕВЫЙ НАБОР | 2017 |
|
RU2752172C2 |
| НОВЫЕ СТАБИЛЬНЫЕ КРИСТАЛЛЫ МОНОГИДРОХЛОРИДА 1-(2-β-D-АРАБИНОФУРАНОЗИЛ)ЦИТОЗИНА | 2010 |
|
RU2538593C2 |
| СУЛЬФАТ 5-ГИДРОКСИ-1Н-ИМИДАЗОЛ-4-КАРБОКСАМИДА | 2014 |
|
RU2603137C1 |
| КРИСТАЛЛЫ ПРОИЗВОДНЫХ ДИСПИРОПИРРОЛИДИНА | 2013 |
|
RU2647840C2 |
| СОЛЬ АЗОТСОДЕРЖАЩЕГО ГЕТЕРОЦИКЛИЧЕСКОГО СОЕДИНЕНИЯ ИЛИ ЕЕ КРИСТАЛЛИЧЕСКАЯ ФОРМА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ИНГИБИТОР FLT3 | 2014 |
|
RU2641106C2 |
| КРИСТАЛЛИЧЕСКИЙ ПОЛИМОРФ 4-[5-(ПИРИДИН-4-ИЛ)-1Н-1,2,4-ТРИАЗОЛ-3-ИЛ]-ПИРИДИН-2-КАРБОНИТРИЛА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2639149C2 |
| СИНТЕЗ β-L-2'-ДЕЗОКСИНУКЛЕОЗИДОВ | 2004 |
|
RU2361875C2 |
| 2-О-Сульфонаты метил 5-О-бензил-3-фтор-3-дезокси-Д-арабинозы в качестве промежуточных продуктов в синтезе биологически активных 3 @ -фтор-3 @ -дезоксирибонуклеозидов | 1987 |
|
SU1521739A1 |
| СПОСОБ ПОЛУЧЕНИЯ 2'-ДЕЗОКСИ-2', 2'-ДИФТОРЦИТИДИНА | 2005 |
|
RU2360919C2 |
Изобретение относится к новым кристаллическим солям, пригодным в качестве противоопухолевых средств: метансульфонату 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина с характеристическими пиками рентгеновской порошковой дифрактометрии при дифракционных углах (2θ) 19,8, 21,8, 27,5, 28,4 и 29,9 градусов и гидрохлориду 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина с характеристическими пиками рентгеновской порошковой дифрактометрии при дифракционных углах (2θ) 9,2, 14,7, 15,7, 22,9 и 27,3 градусов. Предложены новые кристаллические формы с превосходной противоопухолевой активностью, водорастворимостью, текучестью, таблетируемостью, не гигроскопичные, экологичные. 5 н.п. ф-лы, 5 пр., 6 табл., 4 ил.
1. Кристалл метансульфоната 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина, демонстрирующий характеристические пики при дифракционных углах (2θ) 19,8, 21,8, 27,5, 28,4 и 29,9 градусов при рентгеновской порошковой дифрактометрии.
2. Кристалл гидрохлорида 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина, демонстрирующий характеристические пики при дифракционных углах (2θ) 9,2, 14,7, 15,7, 22,9 и 27,3 градусов при рентгеновской порошковой дифрактометрии.
3. Фармацевтическая композиция для лечения опухоли, содержащая кристалл по любому из пп. 1, 2 в качестве активного ингредиента и добавки, используемые в производстве лекарственных средств.
4. Способ получения кристаллов метансульфоната 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина по п. 1, который включает
- добавление метансульфоновой кислоты к водной суспензии 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина до его растворения,
- удаление воды и добавление растворителя, в котором полученная соль 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина нерастворима, для осаждения кристаллов метансульфоната 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина.
5. Способ получения кристаллов гидрохлорида 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина по п. 2, который включает
- добавление соляной кислоты к водной суспензии 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина до его растворения и
- удаление воды и добавление растворителя, в котором полученная соль 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина нерастворима, для осаждения кристаллов гидрохлорида 1-(2-дезокси-2-фтор-4-тио-β-D-арабинофуранозил)цитозина.
| US6147058 A, 16.10.1997;US 3116282 A1, 31.12.1963;US4211773 A, 08.07.1980 | |||
| ПРОИЗВОДНЫЕ АРАБИНОФУРАНОЗИЛ-ЦИТОЗИНА И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 1996 |
|
RU2165260C2 |
Авторы
Даты
2016-10-27—Публикация
2013-03-27—Подача