Настоящая заявка относится к новым галоген-замещенным соединениям, к способам их получения и к их применению для борьбы с животными-вредителями, в частности, членистоногими, и особенно насекомыми, паукообразными и нематодами.
Известно, что определенные галоген-замещенные соединения обладают гербицидным действием (ср. J. Org. Chem. 1997, 62(17), 5908-5919, J. Heterocycl. Chem. 1998, 35(6), 1493-1499, WO 2004/035545, WO 2004/106324, US 2006/069132, WO 2008/029084).
Кроме того, известно, что определенные галоген-замещенные соединения являются инсектицидно активными (ЕР 1911751).
Кроме того, известно, что определенные галоген-замещенные соединения обладают цитокин-ингибирующей активностью (WO 00/07980).
Современные композиции для защиты сельскохозяйственных культур должны соответствовать многим требованиям, например в отношении эффективности, устойчивости и спектра их действия и возможного применения. В данном случае играют роль вопросы токсичности, совместимости с другими активными соединениями или вспомогательными веществами составов, а также вопрос затрат, которых требует синтез активного соединения. Кроме того, может иметь место устойчивость. В силу всех этих причин, поиск новых средств защиты сельскохозяйственных культур никогда не может быть рассмотрен как завершенный, и существует постоянная потребность в новых соединениях, обладающих свойствами, которые, по сравнению с известными соединениями, улучшены по меньшей мере в отношении отдельных аспектов.
Цель настоящего изобретения заключалась в обеспечении соединений, которые расширяют спектр пестицидов в различных аспектах и/или улучшают их активность.
Неожиданно было обнаружено, что определенные галоген-замещенные соединения и их N-оксиды и соли обладают биологическими свойствами и являются особенно пригодными для борьбы с животными-вредителями, и, следовательно, могут использоваться особенно хорошо в области агрохимии и в сфере ветеринарии.
Подобные соединения уже известны из WO 2010/051926.
Галоген-замещенные соединения в соответствии с изобретением определяются общей формулой (I)
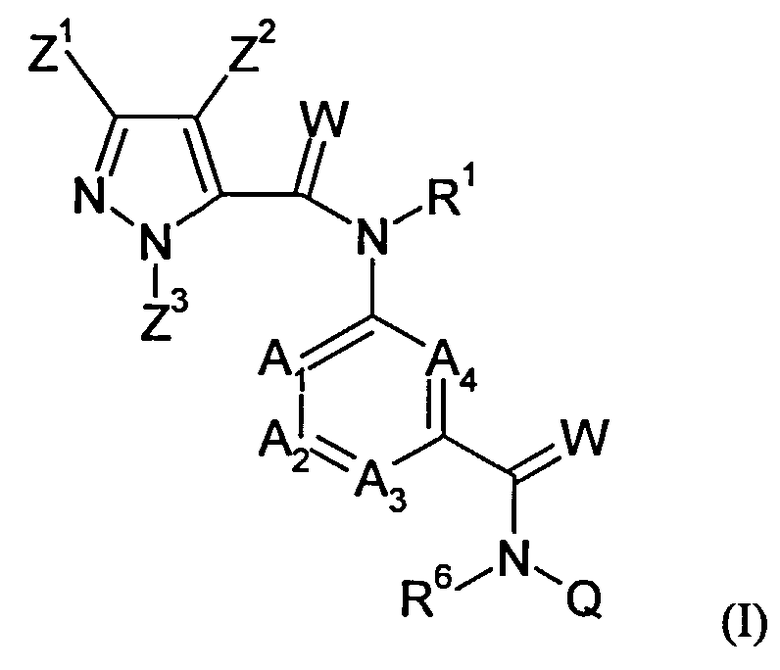
в которой
R1 означает водород, необязательно замещенный C1-С6-алкил, С2-С6-алкенил, С2-С6-алкинил, С3-С7-циклоалкил, C1-С6-алкилкарбонил, C1-С6-алкоксикарбонил, циано-C1-С2-алкил, арил-(С1-С3)-алкил, гетероарил-(С1-С3)-алкил,
химическая группа
A1 означает CR2 или азот,
А2 означает CR3 или азот,
А3 означает CR4 или азот и
А4 означает CR5 или азот,
но где азот означают одновременно не более трех химических групп A1-А4;
R2, R3, R4 и R5 независимо друг от друга означают водород, галоген, CN, NO2, необязательно замещенный C1-С6-алкил, C1-С6-галогеналкил, С3-С6-циклоалкил, С3-С6-галогенциклоалкил, C1-С6-алкокси, C1-С6-галогеналкокси, C1-С6-алкилтио, C1-С6-галогеналкилтио, C1-С6-алкилсульфинил, C1-С6-галогеналкилсульфинил, C1-С6-алкилсульфонил, C1-С6-галогеналкилсульфонил, C1-С6-алкиламино, N,N-ди-C1-С6алкиламино, N-C1-С6-алкиламинокарбонил, N-С3-С6-циклоалкиламинокарбонил или (С1-С3-алкокси)карбонил;
если ни одна из групп A2 и А3 не означает азот, R3 и R4 вместе с атомом углерода, к которому они присоединены, могут образовывать 5- или 6-членное кольцо, которое содержит 0, 1 или 2 атома азота и/или 0 или 1 атом кислорода и/или 0 или 1 атом серы, или
если ни одна из групп A1 и А2 не означает азот, R2 и R3 вместе с атомом углерода, к которому они присоединены, могут образовывать 6-членное кольцо, которое содержит 0, 1 или 2 атома азота;
W означает кислород или серу;
R6 означает водород, необязательно замещенный C1-С6-алкил, арил-(С1-С3)-алкил, гетероарил-(С1-С3)-алкил, С2-С6-алкенил, С2-С6-алкинил, С3-С6-циклоалкил, (C1-С3-алкил)-С3-С6-циклоалкил и (С3-С6-циклоалкил)-С1-С3-алкил, C1-С6-алкилкарбонил, С1-С6-алкоксикарбонил;
Q означает
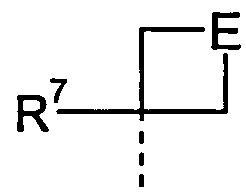 ;
;
Е означает связь, -СН2-, S, SO, SO2, -S-CH2-, -SO-CH2-, -SO2-CH2-, -CH2-S-CH2-, -CH2-SO-CH2-, -CH2-SO2-CH2-, -S-CH2-CH2-, -SO-CH2-CH2-, -SO2-CH2-CH2-, -NR6-CH2-, -CH2-NR6-CH2-;
R7 означает циано или C(=S)NH2;
Z1 означает необязательно замещенный C1-С6-галогеналкил или С3-С6-циклоалкил, С3-С6-галогенциклоалкил, и
Z2 означает галоген, циано, нитро или необязательно замещенный C1-С6-галогеналкил, C1-С6-алкилтио, C1-С6-галогеналкилтио, C1-С6-алкилсульфинил, C1-С6-галогеналкилсульфинил, C1-С6-алкилсульфонил, C1-С6-галогеналкилсульфонил, и
Z3 означает водород или необязательно замещенный C1-С6-алкил, С1-С4-алкенил, C1-С4-алкинил, C1-С6-галогеналкил.
Предпочтение отдают соединениям формулы (I)
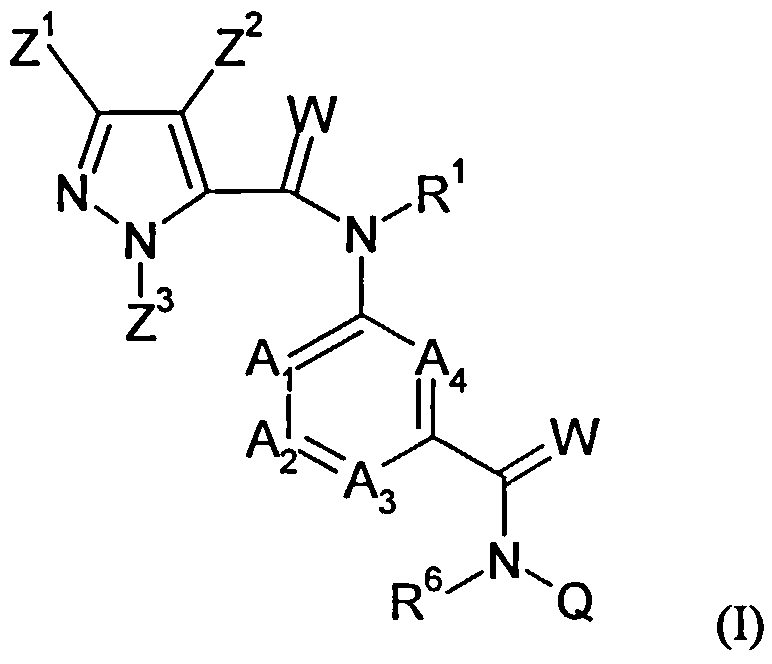
в которой
R1 означает водород, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, метоксиметил, этоксиметил, пропоксиметил, метилкарбонил, этилкарбонил, н-пропилкарбонил, изопропилкарбонил, втор-бутилкарбонил, трет-бутилкарбонил, метоксикарбонил, этоксикарбонил, н-пропоксикарбонил, изопропоксикарбонил, втор-бутоксикарбонил, трет-бутоксикарбонил, цианометил, 2-цианоэтил, бензил, 4-метоксибензил, пирид-2-илметил, пирид-3-илметил, пирид-4-илметил, 4-хлорпирид-3-илметил;
химическая группа
A1 означает CR2 или азот,
А2 означает CR3 или азот,
А3 означает CR4 или азот и
А4 означает CR5 или азот,
но где азот означают одновременно не более трех химических групп A1-А4;
R2 и R5 независимо друг от друга означают водород, метил, фтор или хлор и
R3 и R4 независимо друг от друга означают водород, фтор, хлор, бром, CN, NO2, метил, этил, фторметил, дифторметил, трифторметил, 2,2,2-трифторэтил, метокси, этокси, н-пропокси, 1-метилэтокси, фторметокси, дифторметокси, хлордифторметокси, дихлорфторметокси, трифторметокси, 2,2,2-трифторэтокси, 2-хлор-2,2-дифторэтокси, пентафторэтокси, метилсульфонил, метилсульфинил, трифторметилсульфонил, трифторметилсульфинил; где
W означает кислород,
R6 означает водород, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, метоксиметил, этоксиметил, пропоксиметил, метилкарбонил, этилкарбонил, н-пропилкарбонил, изопропилкарбонил, втор-бутилкарбонил, трет-бутилкарбонил, метоксикарбонил, этоксикарбонил, н-пропоксикарбонил, изопропоксикарбонил, втор-бутоксикарбонил, трет-бутоксикарбонил, цианометил, 2-цианоэтил, бензил, 4-метоксибензил, пирид-2-илметил, пирид-3-илметил, пирид-4-илметил, 4-хлорпирид-3-илметил;
Q означает
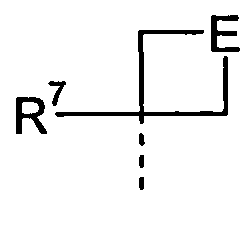 ;
;
Е означает связь или -СН2-;
R7 означает циано или C(=S)NH2;
Z1 означает дифторметил, трихлорметил, хлордифторметил, дихлорфторметил, трифторметил, бромдихлорметил, хлорметил, бромметил, 1-фторэтил, 1-фтор-1-метилэтил, 2-фторэтил, 2,2-дифторэтил, 2,2,2-трифторэтил, 1,2,2,2-тетрафторэтил, 1-хлор-1,2,2,2-тетрафторэтил, 2,2,2-трихлорэтил, 2-хлор-2,2-дифторэтил, 1,1-дифторэтил, пентафторэтил, пентафтор-трет-бутил, гептафтор-н-пропил, гептафторизопропил, нонафтор-н-бутил, циклопропил, 1-хлорциклопропил, 1-фторциклопропил, 1-бромциклопропил, 1-цианоциклопропил, 1-трифторметилциклопропил, циклобутил или 2,2-дифтор-1-метилциклопропил, и
Z2 означает галоген, циано, нитро, дифторметил, трихлорметил, хлордифторметил, дихлорфторметил, трифторметил, бромдихлорметил, хлорметил, бромметил, 1-фторэтил, 1-фтор-1-метилэтил, 2-фторэтил, 2,2-дифторэтил, 2,2,2-трифторэтил, 1,2,2,2-тетрафторэтил, 1-хлор-1,2,2,2-тетрафторэтил, 2,2,2-трихлорэтил, 2-хлор-2,2-дифторэтил, 1,1-дифторэтил, пентафторэтил, пентафтор-трет-бутил, гептафтор-н-пропил, гептафторизопропил, нонафтор-н-бутил, метилтио, метилсульфинил, метилсульфонил, этилтио, этилсульфинил, этилсульфонил, трифторметилтио, трифторметилсульфинил, трифторметилсульфонил, и
Z3 означает водород, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, этенил, 1-пропенил, 2-пропенил, этинил, 1-пропинил, 1-бутинил, дифторметил, трихлорметил, хлордифторметил, дихлорфторметил, трифторметил, хлорметил, бромметил, 1-фторэтил, 1-фтор-1-метилэтил, 2-фторэтил, 2,2-дифторэтил, 2,2,2-трифторэтил.
Дальнейшими особенно предпочтительными соединениями являются соединения общей формулы (I), в которой
Z1 означает трифторметил, 1-хлорциклопропил, 1-фторциклопропил или пентафторэтил,
Z2 означает трифторметил, нитро, метилтио, метилсульфинил, метилсульфонил, фтор, хлор, бром или йод,
Z3 означает метил, этил, н-пропил или водород,
R1 означает водород, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, метоксиметил, этоксиметил, пропоксиметил, метилкарбонил, этилкарбонил, н-пропилкарбонил, изопропилкарбонил, втор-бутилкарбонил, трет-бутилкарбонил, метоксикарбонил, этоксикарбонил, н-пропоксикарбонил, изопропоксикарбонил, втор-бутоксикарбонил, трет-бутоксикарбонил, цианометил, 2-цианоэтил, бензил, 4-метоксибензил, пирид-2-илметил, пирид-3-илметил, пирид-4-илметил, 4-хлорпирид-3-илметил,
А1, А2 и А4 означают СН,
А3 означает CR4 и
R4 означает фтор, хлор, бром или йод,
R6 означает водород, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил,
W означает кислород и
Q означает 1-цианоциклопропил.
Предпочтение, в частности, отдают дополнительным соединениям, в которых
Z1 означает трифторметил, 1-хлорциклопропил, 1-фторциклопропил или пентафторэтил,
Z2 означает трифторметил, хлор или
Z3 означает метил,
R1 означает водород, метил, этил,
А1, А2 и А4 означают СН,
А3 означает CR4 и
R4 означает хлор,
R6 означает водород, метил, этил,
W означает кислород и
Q означает 1-цианоциклопропил.
Кроме того, изобретение включает новые соединения общих формул (IVa), (IVb), (Va), (Vb) в качестве предпочтительных исходных веществ для синтеза соединений общей формулы (I).
Соединения общих формул (IVa) и (IVb) являются предпочтительными вариантами предшественников общей формулы (IV), например, в соответствии со схемами реакций 1, 2 и 3. Получение соединений общей формулы (I), среди прочего, предпочтительно проводят с применением этих соединений. Соединения общей формулы (IVb) в соединения (IVa) обычно преобразуют путем восстановления.
Соединения (IVa) и (IVb) определяются общими формулами ниже
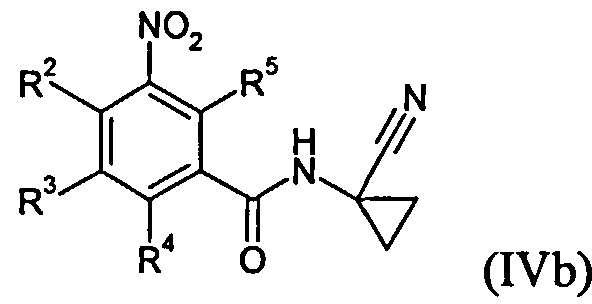
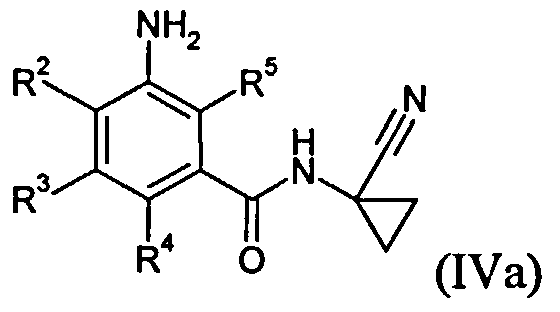
в которых
R2, R3, R4 и R5 независимо друг от друга означают водород, галоген, циано, нитро, необязательно замещенный C1-С6-алкил, C1-С6-галогеналкил, С3-С6-циклоалкил, С3-С6-галогенциклоалкил, C1-С6-алкокси, C1-С6-галогеналкокси, C1-С6-алкилтио, C1-С6-галогеналкилтио, C1-С6-алкилсульфинил, C1-С6-галогеналкилсульфинил, C1-С6-алкилсульфонил, C1-С6-галогеналкилсульфонил, C1-С6-алкиламино, N,N-ди-C1-С6-алкиламино, N-C1-С6-алкиламинокарбонил, N-С3-С6-циклоалкиламинокарбонил или (С1-С3-алкокси)карбонил.
Предпочтение отдают соединениям общих формул (IVa), (IVb), в которых
R2 и R5 означают водород или галоген, и
R3 и R4 означают водород, галоген, циано, нитро, C1-С6-алкил, C1-С6-галогеналкил, С3-С6-циклоалкил, С3-С6-галогенциклоалкил, C1-С6-алкилтио, C1-С6-галогеналкилтио, C1-С6-алкилсульфинил, C1-С6-галогеналкилсульфинил, C1-С6-алкилсульфонил, C1-С6-галогеналкилсульфонил.
Особое предпочтение отдают соединениям общих формул (IVa), (IVb), в которых
R2 означает водород или фтор, и
R3 означает водород, фтор, хлор, бром, йод, циано, нитро, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, циклопропил, 1-хлорциклопропил, 1-фторциклопропил, метилтио, трифторметилтио, метилсульфинил, трифторметилсульфинил, метилсульфонил, трифторметилсульфонил, и
R4 означает водород, фтор, хлор, бром, йод, циано, нитро, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, циклопропил, 1-хлорциклопропил, 1-фторциклопропил, метилтио, трифторметилтио, метилсульфинил, трифторметилсульфинил, метилсульфонил, трифторметилсульфонил, и
R5 означает водород.
Еще большее предпочтение отдают соединениям общих формул (IVa), (IVb), в которых
R2 и R5 означают водород, и
R3 означает водород, фтор, хлор, бром, йод, циано, метил, этил, метилтио, трифторметилтио, метилсульфинил, трифторметилсульфинил, метилсульфонил, трифторметилсульфонил, и
R4 означает фтор, хлор, бром, йод, метил, и
R5 означает водород.
Соединения общих формул (Va) и (Vb) являются предпочтительными вариантами предшественников общей формулы (V), например, в соответствии с схемами реакций 1, 2 и 8. Получение соединений общей формулы (I), среди прочего, предпочтительно проводят с применением этих соединений.
Соединения (Va) и (Vb) определяются общими формулами ниже
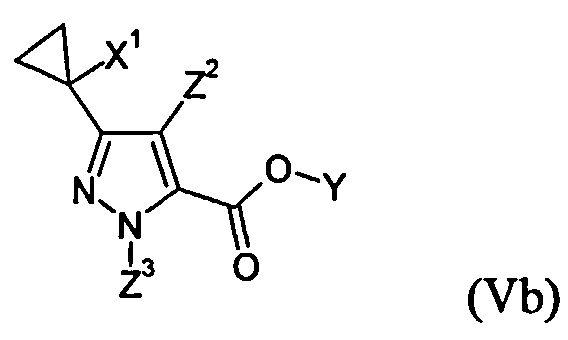
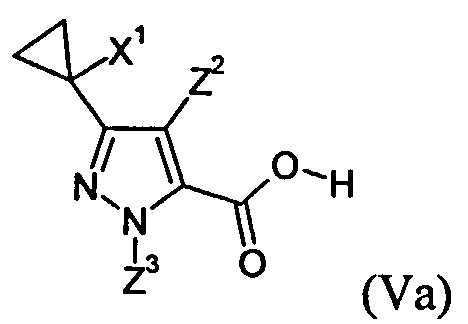
в которых
X1 означает галоген, циано и С1-С4-галогеналкил, и
Z2 означает галоген, циано, нитро или необязательно замещенный C1-С6-галогеналкил, C1-С6-алкилтио, C1-С6-галогеналкилтио, C1-С6-алкилсульфинил, C1-С6-галогеналкилсульфинил, С1-С6-алкилсульфонил, С1-С6-галогеналкилсульфонил, и
Z3 означает водород или необязательно замещенный C1-С6-алкил, С1-С4-алкенил, C1-С4-алкинил, C1-С6-галогеналкил, и
Y означает необязательно замещенный C1-С6-алкил.
Предпочтение отдают соединениям общих формул (Va) и (Vb), в которых
X1 означает фтор, хлор, бром, циано и С1-С2-галогеналкил, и
Z2 означает галоген, циано, нитро, дифторметил, трихлорметил, хлордифторметил, дихлорфторметил, трифторметил, бромдихлорметил, хлорметил, бромметил, 1-фторэтил, 1-фтор-1-метилэтил, 2-фторэтил, 2,2-дифторэтил, 2,2,2-трифторэтил, 1,2,2,2-тетрафторэтил, 1-хлор-1,2,2,2-тетрафторэтил, 2,2,2-трихлорэтил, 2-хлор-2,2-дифторэтил, 1,1-дифторэтил, пентафторэтил, пентафтор-трет-бутил, гептафтор-н-пропил, гептафторизопропил, нонафтор-н-бутил, метилтио, метилсульфинил, метилсульфонил, этилтио, этилсульфинил, этилсульфонил, трифторметилтио, трифторметилсульфинил, трифторметилсульфонил, и
Z3 означает водород, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, этенил, 1-пропенил, 2-пропенил, этинил, 1-пропинил, 1-бутинил, дифторметил, трихлорметил, хлордифторметил, дихлорфторметил, трифторметил, хлорметил, бромметил, 1-фторэтил, 1-фтор-1-метилэтил, 2-фторэтил, 2,2-дифторэтил, 2,2,2-трифторэтил, и
Y означает необязательно замещенный C1-С6-алкил.
Особое предпочтение отдают соединениям общих формул (Va) и (Vb), в которых
X1 означает фтор, хлор, трифторметил или пентафторэтил, и
Z2 означает трифторметил, нитро, метилтио, метилсульфинил, метилсульфонил, фтор, хлор, бром или йод, и
Z3 означает метил, этил, н-пропил или водород, и
Y означает метил, этил, н-пропил, изопропил, н-бутил или трет-бутил.
В соответствии с изобретением, ″алкил″ - сам по себе или в качестве части химической группы - означает углеводороды с нормальной или разветвленной цепью, предпочтительно содержащие от 1 до 6 атомов углерода, такие как, например, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, пентил, 1-метилбутил, 2-метилбутил, 3-метилбутил, 1,2-диметилпропил, 1,1-диметилпропил, 2,2-диметилпропил, 1-этилпропил, гексил, 1-метилпентил, 2-метилпентил, 3-метилпентил, 4-метилпентил, 1,2-диметилпропил, 1,3-диметилбутил, 1,4-диметилбутил, 2,3-диметилбутил, 1,1-диметилбутил, 2,2-диметилбутил, 3,3-диметилбутил, 1,1,2-триметилпропил, 1,2,2-триметилпропил, 1-этилбутил и 2-этилбутил. Предпочтение кроме того отдают алкильным группам, содержащим от 1 до 4 атомов углерода, таким как, среди прочего, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил или трет-бутил. Алкильные группы в соответствии с изобретением могут быть замещены одним или несколькими одинаковыми или разными радикалами.
В соответствии с изобретением, ″алкенил″ - сам по себе или в качестве части химической группы - означает углеводороды с нормальной или разветвленной цепью, предпочтительно содержащие от 2 до 6 атомов углерода и по меньшей мере одну двойную связь, такие как, например, винил, 2-пропенил, 2-бутенил, 3-бутенил, 1-метил-2-пропенил, 2-метил-2-пропенил, 2-пентенил, 3-пентенил, 4-пентенил, 1-метил-2-бутенил, 2-метил-2-бутенил, 3-метил-2-бутенил, 1-метил-3-бутенил, 2-метил-3-бутенил, 3-метил-3-бутенил, 1,1-диметил-2-пропенил, 1,2-диметил-2-пропенил, 1-этил-2-пропенил, 2-гексенил, 3-гексенил, 4-гексенил, 5-гексенил, 1-метил-2-пентенил, 2-метил-2-пентенил, 3-метил-2-пентенил, 4-метил-2-пентенил, 3-метил-3-пентенил, 4-метил-3-пентенил, 1-метил-4-пентенил, 2-метил-4-пентенил, 3-метил-4-пентенил, 4-метил-4-пентенил, 1,1-диметил-2-бутенил, 1,1-диметил-3-бутенил, 1,2-диметил-2-бутенил, 1,2-диметил-3-бутенил, 1,3-диметил-2-бутенил, 2,2-диметил-3-бутенил, 2,3-диметил-2-бутенил, 2,3-диметил-3-бутенил, 1-этил-2-бутенил, 1-этил-3-бутенил, 2-этил-2-бутенил, 2-этил-3-бутенил, 1,1,2-триметил-2-пропенил, 1-этил-1-метил-2-пропенил и 1-этил-2-метил-2-пропенил. Предпочтение кроме того отдают алкенильным группам, содержащим от 2 до 4 атомов углерода, таким как, среди прочего, 2-пропенил, 2-бутенил или 1-метил-2-пропенил. Алкенильные группы в соответствии с изобретением могут быть замещены одним или несколькими одинаковыми или разными радикалами.
В соответствии с изобретением, ″алкинил″ - сам по себе или в качестве части химической группы - означает углеводороды с нормальной или разветвленной цепью предпочтительно, содержащие от 2 до 6 атомов углерода и по меньшей мере одну тройную связь, такие как, например, 2-пропинил, 2-бутинил, 3-бутинил, 1-метил-2-пропинил, 2-пентинил, 3-пентинил, 4-пентинил, 1-метил-3-бутинил, 2-метил-3-бутинил, 1-метил-2-бутинил, 1,1-диметил-2-пропинил, 1-этил-2-пропинил, 2-гексинил, 3-гексинил, 4-гексинил, 5-гексинил, 1-метил-2-пентинил, 1-метил-3-пентинил, 1-метил-4-пентинил, 2-метил-3-пентинил, 2-метил-4-пентинил, 3-метил-4-пентинил, 4-метил-2-пентинил, 1,1-диметил-3-бутинил, 1,2-диметил-3-бутинил, 2,2-диметил-3-бутинил, 1-этил-3-бутинил, 2-этил-3-бутинил, 1-этил-1-метил-2-пропинил и 2,5-гексадиинил. Предпочтение кроме того отдают алкинильным группам, содержащим от 2 до 4 атомов углерода, таким как, среди прочего, этинил, 2-пропинил или 2-бутинил-2-пропенил. Алкинильные группы в соответствии с изобретением могут быть замещены одним или несколькими одинаковыми или разными радикалами.
В соответствии с изобретением, ″циклоалкил″ - сам по себе или в качестве части химической группы - означает моно-, би- или трициклические углеводороды, предпочтительно содержащие от 3 до 10 углеродов, такие как, например, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, бицикло[2.2.1]гептил, бицикло[2.2.2]октил или адамантил. Предпочтение кроме того отдают циклоалкильным группам, содержащим 3, 4, 5, 6 или 7 атомов углерода, таким как, среди прочего, циклопропил или циклобутил. Циклоалкильные группы в соответствии с изобретением могут быть замещены одним или несколькими одинаковьми или разными радикалами.
В соответствии с изобретением, ″алкилциклоалкил″ означает моно-, би- или трициклический алкилциклоалкил, предпочтительно содержащий от 4 до 10 или от 4 до 7 атомов углерода, такой как, например, этилциклопропил, изопропилциклобутил, 3-метилциклопентил и 4-метилциклогексил. Предпочтение кроме того отдают алкилциклоалкильным группам, содержащим 4, 5 или 7 атомов углерода, таким как, среди прочего, этилциклопропил или 4-метилциклогексил. Алкилциклоалкильные группы в соответствии с изобретением могут быть замещены одним или несколькими одинаковыми или разными радикалами.
В соответствии с изобретением, ″циклоалкилалкил″ означает моно-, би- или трициклический циклоалкилалкил, предпочтительно содержащий от 4 до 10 или от 4 до 7 атомов углерода, такой как, например, циклопропилметил, циклобутилметил, циклопентилметил, циклогексилметил и циклопентилэтил. Предпочтение кроме того отдают циклоалкилалкильным группам, содержащим 4, 5 или 7 атомов углерода, таким как, среди прочего, циклопропилметил или циклобутилметил. Циклоалкилалкильные группы в соответствии с изобретением могут быть замещены одним или несколькими одинаковыми или разными радикалами.
В соответствии с изобретением, ″галоген″ означает фтор, хлор, бром или йод, в частности фтор, хлор или бром.
Галоген-замещенные химические группы в соответствии с изобретением, такие как, например, галогеналкил, галогенциклоалкил, галогеналкилокси, галогеналкилтио, галогеналкилсульфинил или галогеналкилсульфонил являются моно- или полизамещенными галогеном вплоть до максимально возможного числа заместителей. В случае полизамещения галогеном, атомы галогена могут быть одинаковыми или разными, и могут быть все присоединены к одному или множеству атомов углерода. Здесь, галоген означает в частности фтор, хлор, бром или йод, предпочтительно фтор, хлор или бром, и особенно предпочтительно фтор.
В соответствии с изобретением, ″галогенциклоалкил″ означает моно-, би- или трициклический галогенциклоалкил, содержащий предпочтительно от 3 до 10 атомов углерода, такой как, среди прочего, 1-фторциклопропил, 2-фторциклопропил или 1-фторциклобутил. Предпочтение кроме того отдают галогенциклоалкилу, содержащему 3, 5 или 7 атомов углерода. Галогенциклоалкильные группы в соответствии с изобретением могут быть замещены одним или несколькими одинаковыми или разными радикалами.
В соответствии с изобретением, ″галогеналкил″, ″галогеналкенил″ или ″галогеналкинил″ означает галоген-замещенные алкильные, алкенильные или алкинильные группы, содержащие предпочтительно от 1 до 9 одинаковых или разных атомов галогена, такие как, например, моногалогеналкил, такой как CH2CH2Cl, CH2CH2F, CHClCH3, CHFCH3, CH2Cl, CH2F; пергалогеналкил, такой как CCl3 или CF3 или CF2CF3; полигалогеналкил, такой как CHF2, CH2F, CH2CHFCl, CHCl2, CF2CF2H, CH2CF3. Это, соответственно, применимо и к галогеналкенильным и другим галоген-замещенным радикалам. Галогеналкокси означает, например, OCF3, OCHF2, OCH2F, OCF2CF3, OCH2CF3 и OCH2CH2Cl.
Дополнительными примерами галогеналкильных групп являются трихлорметил, хлордифторметил, дихлорфторметил, хлорметил, бромметил, 1-фторэтил, 2фторэтил, 2,2-дифторэтил, 2,2,2-трифторэтил, 2,2,2-трихлорэтил, 2-хлор-2,2-дифторэтил, пентафторэтил и пентафтор-трет-бутил. Предпочтение отдают галогеналкильным группам, содержащим от 1 до 4 атомов углерода и от 1 до 9, предпочтительно от 1 до 5, одинаковых или разных атомов галогена, выбранных из группы, состоящей из фтора, хлора и брома. Особое предпочтение отдают галогеналкильным группам, содержащим 1 или 2 атомов углерода и от 1 до 5 одинаковых или разных атомов галогена, выбранных из группы, состоящей из фтора и хлора, таким как, среди прочего, дифторметил, трифторметил или 2,2-дифторэтил.
В соответствии с изобретением, ″гидроксиалкил″ означает спирт с нормальной или разветвленной цепью, предпочтительно содержащий от 1 до 6 атомов углерода, такой как, например, метанол, этанол, н-пропанол, изопропанол, н-бутанол, изобутанол, втор-бутанол и трет-бутанол. Предпочтение, кроме того, отдают гидроксиалкильным группам, содержащим от 1 до 4 атомов углерода. Гидроксиалкильные группы в соответствии с изобретением могут быть замещены одним или несколькими одинаковыми или разными радикалами.
В соответствии с изобретением, ″алкокси″ означает O-алкил с нормальной или разветвленной цепью, предпочтительно содержащий от 1 до 6 атомов углерода, такой как, например, метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси и трет-бутокси. Предпочтение кроме того отдают алкокси группам, содержащим от 1 до 4 атомов углерода. Алкокси группы в соответствии с изобретением могут быть замещены одним или несколькими одинаковыми или разными радикалами. В соответствии с изобретением, ″галогеналкокси″ означает галоген-замещенный O-алкил с нормальной или разветвленной цепью, предпочтительно содержащий от 1 до 6 атомов углерода, такой как, среди прочего, дифторметокси, трифторметокси, 2,2-дифторэтокси, 1,1,2,2-тетрафторэтокси, 2,2,2-трифторэтокси и 2-хлор-1,1,2-трифторэтокси. Предпочтение кроме того отдают галогеналкокси группам, содержащим от 1 до 4 атомов углерода. Галогеналкокси группы в соответствии с изобретением могут быть замещены одним или несколькими одинаковыми или разными радикалами.
В соответствии с изобретением, ″алкилтио″ означает S-алкил с нормальной или разветвленной цепью, предпочтительно содержащий от 1 до 6 атомов углерода, такой как, например, метилтио, этилтио, н-пропилтио, изопропилтио, н-бутилтио, изобутилтио, втор-бутилтио и трет-бутилтио. Предпочтение кроме того отдают алкилтио группам, содержащим от 1 до 4 атомов углерода. Алкилтио группы в соответствии с изобретением могут быть замещены одним или несколькими одинаковыми или разными радикалами.
Примерами галогеналкилтиоалкильных групп, то есть галоген-замещенных алкилтио групп, являются, среди прочего, дифторметилтио, трифторметилтио, трихлорметилтио, хлордифторметилтио, 1-фторэтилтио, 2-фторэтилтио, 2,2-дифторэтилтио, 1,1,2,2-тетрафторэтилтио, 2,2,2-трифторэтилтио или 2-хлор-1,1,2-трифторэтилтио.
В соответствии с изобретением, ″алкилсульфинил″ означает алкилсульфинил с нормальной или разветвленной цепью, предпочтительно содержащий от 1 до 6 атомов углерода, такой как, например, метилсульфинил, этилсульфинил, н-пропилсульфинил, изопропилсульфинил, н-бутилсульфинил, изобутилсульфинил, втор-бутилсульфинил и трет-бутилсульфинил. Предпочтение кроме того отдают алкилсульфинильным группам, содержащим от 1 до 4 атомов углерода. Алкилсульфинильные группы в соответствии с изобретением могут быть замещены одним или несколькими одинаковыми или разными радикалами.
Примерами галогеналкилсульфинильных групп, то есть галоген-замещенных алкилсульфинильных групп, являются, среди прочего, дифторметилсульфинил, трифторметилсульфинил, трихлорметилсульфинил, хлордифторметилсульфинил, 1-фторэтилсульфинил, 2-фторэтилсульфинил, 2,2-дифторэтилсульфинил, 1,1,2,2-тетрафторэтилсульфинил, 2,2,2-трифторэтилсульфинил и 2-хлор-1,1,2-трифторэтилсульфинил.
В соответствии с изобретением, ″алкилсульфонил″ означает алкилсульфонил с нормальной или разветвленной цепью, предпочтительно содержащий от 1 до 6 атомов углерода, такой как, например, метилсульфонил, этилсульфонил, н-пропилсульфонил, изопропилсульфонил, н-бутилсульфонил, изобутилсульфонил, втор-бутилсульфонил и трет-бутилсульфонил. Предпочтение кроме того отдают алкилсульфонильным группам, содержащим от 1 до 4 атомов углерода. Алкилсульфонильные группы в соответствии с изобретением могут быть замещены одним или несколькими одинаковыми или разными радикалами.
Примерами галогеналкилсульфонильных групп, то есть галоген-замещенных алкилсульфонильных групп, являются, среди прочего, дифторметилсульфонил, трифторметилсульфонил, трихлорметилсульфонил, хлордифторметилсульфонил, 1-фторэтилсульфонил, 2-фторэтилсульфонил, 2,2-дифторэтилсульфонил, 1,1,2,2-тетрафторэтилсульфонил, 2,2,2-трифторэтилсульфонил и 2-хлор-1,1,2-трифторэтилсульфонил.
В соответствии с изобретением, ″алкилкарбонил″ означает алкил-С(=O) с нормальной или разветвленной цепью, предпочтительно содержащий от 2 до 7 атомов углерода, такой как метилкарбонил, этилкарбонил, н-пропилкарбонил, изопропилкарбонил, втор-бутилкарбонил и трет-бутилкарбонил. Предпочтение кроме того отдают алкилкарбонильным группам, содержащим от 1 до 4 атомов углерода. Алкилкарбонильные группы в соответствии с изобретением могут быть замещены одним или несколькими одинаковыми или разными радикалами.
В соответствии с изобретением, ″циклоалкилкарбонил″ означает циклоалкилкарбонил с нормальной или разветвленной цепью, предпочтительно содержащий от 3 до 10 атомов углерода в циклоалкильном фрагменте, такой как, например, циклопропилкарбонил, циклобутилкарбонил, циклопентилкарбонил, циклогексилкарбонил, циклогептилкарбонил, циклооктилкарбонил, бицикло[2.2.1]гептил, бицикло[2.2.2]октилкарбонил и адамантилкарбонил. Предпочтение кроме того отдают циклоалкилкарбонилу, содержащему 3, 5 или 7 атомов углерода в циклоалкильном фрагменте. Циклоалкилкарбонильные группы в соответствии с изобретением могут быть замещены одним или несколькими одинаковыми или разными радикалами.
В соответствии с изобретением, ″алкоксикарбонил″ - один или в качестве составной части химической группы - означает алкоксикарбонил с нормальной или разветвленной цепью, предпочтительно содержащий от 1 до 6 атомов углерода, или содержащий от 1 до 4 атомов углерода в алкокси фрагменте, такой как, например, метоксикарбонил, этоксикарбонил, н-пропоксикарбонил, изопропоксикарбонил, втор-бутоксикарбонил и трет-бутоксикарбонил. Алкоксикарбонильныс группы в соответствии с изобретением могут быть замещены одним или несколькими одинаковыми или разными радикалами. В соответствии с изобретением, ″алкиламинокарбонил″ означает алкиламинокарбонил с нормальной или разветвленной цепью, содержащий предпочтительно от 1 до 6 атомов углерода или от 1 до 4 атомов углерода в алкильном фрагменте, такой как, например, метиламинокарбонил, этиламинокарбонил, н-пропиламинокарбонил, изопропиламинокарбонил, втор-бутиламинокарбонил и трет-бутиламинокарбонил. Алкиламинокарбонильные группы в соответствии с изобретением могут быть замещены одним или несколькими одинаковыми или разными радикалами.
В соответствии с изобретением, ″N,N-диалкиламинокарбонил″ означает N,N-диалкиламинокарбонил с нормальной или разветвленной цепью, содержащий предпочтительно от 1 до 6 атомов углерода или от 1 до 4 атомов углерода в алкильном фрагменте, такой как, например, N,N-диметиламинокарбонил, N,N-диэтиламинокарбонил, N,N-ди(н-пропиламино)карбонил, N,N-ди(изопропиламино)карбонил и N,N-ди-(втор-бутиламино)карбонил. N,N-диалкиламинокарбонильные группы в соответствии с изобретением могут быть замещены одним или несколькими одинаковьми или разными радикалами.
В соответствии с изобретением, ″арил″ означает моно-, би- или полициклическую ароматическую систему, содержащую предпочтительно от 6 до 14, в частности от 6 до 10 атомов углерода в кольце, такую как, например, фенил, нафтил, антрил, фенантренил, предпочтительно фенил. Кроме того, арил также означает полициклические системы, такие как тетрагидронафтил, инденил, инданил, флуоренил, бифенилил, где место присоединения находится на ароматической системе. Арильные группы в соответствии с изобретением могут быть замещены одним или несколькими одинаковыми или разными радикалами.
Примерами замещенных арилов являются арилалкильные группы, которые также могут быть замещены одним или несколькими одинаковыми или разными радикалами в алкильном и/или арильном фрагменте. Примерами таких арилалкильных групп являются, среди прочего, бензил и 1-фенилэтил.
В соответствии с изобретением, ″гетероцикл″, ″гетероциклическое кольцо″ или ″гетероциклическая кольцевая система″ означает карбоциклическую кольцевую систему, содержащую по меньшей мере одно кольцо, в котором по меньшей мере один атом углерода заменен на гетероатом, предпочтительно на гетероатом из группы, состоящей из N, О, S, Р, В, Si, Se, и которое является насыщенным, ненасыщенным или гетероароматическим и может быть незамещенным или замещено заместителем Z, где точка присоединения расположена на атоме кольца. Если не определено иное, гетероциклическое кольцо содержит предпочтительно от 3 до 9 атомов в кольце, особенно от 3 до 6 атомов в кольце, и один или несколько, предпочтительно от 1 до 4, в частности 1, 2 или 3, гетероатомов в гетероциклическом кольце, предпочтительно из группы, состоящей из N, О и S, однако два атома кислорода не могут располагаться непосредственно рядом. Гетероциклические кольца обычно содержат не более 4 атомов азота и/или не более 2 атомов кислорода и/или не более 2 атомов серы. Если гетероциклильный радикал или гетероциклическое кольцо необязательно замещен(-о), он(оно) может быть конденсирован(-о) с другими карбоциклическими или гетероциклическими кольцами. В случае необязательно замещенного гетероциклила, изобретение также охватывает полициклические системы, такие как, например, 8-азабицикло[3.2.1]октанил или 1-азабицикло[2.2.1]гептил. В случае необязательно замещенного гетероциклила, изобретение также охватывает спироциклические системы, такие как, например, 1-окса-5-азаспиро[2.3]гексил.
Гетероциклильные группы в соответствии с изобретением представляют собой, например, пиперидинил, пиперазинил, морфолинил, тиоморфолинил, дигидропиранил, тетрагидропиранил, диоксанил, пирролинил, пирролидинил, имидазолинил, имидазолидинил, тиазолидинил, оксазолидинил, диоксоланил, диоксолил, пиразолидинил, тетрагидрофуранил, дигидрофуранил, оксетанил, оксиранил, азетидинил, азиридинил, оксазетидинил, оксазиридинил, оксазепанил, оксазинанил, азепанил, оксопирролидинил, диоксопирролидинил, оксоморфолинил, оксопиперазинил и оксепанил.
Гетероарилены, то есть гетероароматические системы, имеют особое значение. В соответствии с изобретением, термин гетероарил означает гетероароматические соединения, то есть полностью ненасыщенные ароматические гетероциклические соединения, которые подпадают под приведенное выше определение гетероциклов. Предпочтение отдают 5-7-членным кольцам, содержащим от 1 до 3, предпочтительно 1 или 2, одинаковых или разных гетероатомов из вышеприведенной группы. Гетероарильные группы в соответствии с изобретением представляют собой, например, фурил, тиенил, пиразолил, имидазолил, 1,2,3- и 1,2,4-триазолил, изоксазолил, тиазолил, изотиазолил, 1,2,3-, 1,3,4-, 1,2,4- и 1,2,5-оксадиазолил, азепинил, пирролил, пиридил, пиридазинил, пиримидинил, пиразинил, 1,3,5-, 1,2,4- и 1,2,3-триазинил, 1,2,4-, 1,3,2-, 1,3,6- и 1,2,6-оксазинил, оксепинил, тиепинил, 1,2,4-триазолонил и 1,2,4-диазепинил. Гетероарильные группы в соответствии с изобретением также могут быть замещены одним или несколькими одинаковыми или разными радикалами.
Замещенные группы, такие как замещенные алкильные, алкенильные, алкинильные, циклоалкильные, арильные, фенильные, бензильные, гетероциклильные и Гетероарильные радикалы являются, например, замещенными радикалами, производными от незамещенной базовой структуры, где заместителями являются, например, один или несколько, предпочтительно 1, 2 или 3, радикалов из группы, включающей галоген, алкокси, алкилтио, гидроксил, амино, нитро, карбоксил или группу-эквивалент карбоксильной группы, пиано, изоциано, азидо, алкоксикарбонил, алкилкарбонил, формил, карбамоил, моно- и N,N-диалкиламинокарбонил, замещенный амино, такой как ациламино, моно- и N,N-диалкиламино, триалкилсилил и необязательно замещенный циклоалкил, необязательно замещенный арил, необязательно замещенный гетероциклил, где каждая из последних циклических групп также может быть присоединена через гетероатомы или двухвалентные функциональные группы, как, например, упомянутые алкильные радикалы, и алкилсульфинил, включая оба энантиомера алкилсульфонильной группы, алкилсульфонил, алкилфосфинил, алкилфосфонил и, в случае циклических радикалов (= ″циклический скелет″), также алкил, галогеналкил, алкилтиоалкил, алкоксиалкил, необязательно замещенный моно- и N,N-диалкиламиноалкил и гидроксиалкил.
Термин ″замещенные группы″, такой как замещенный алкил и т.д., включает в качестве заместителей, в дополнение к упомянутым насыщенным углеводородным радикалам, соответствующие ненасыщенные алифатические и ароматические радикалы, такие как необязательно замещенный алкенил, алкинил, алкенилокси, алкинилокси, алкенилтио, алкинилтио, алкенилоксикарбонил, алкинилоксикарбонил, алкенилкарбонил, алкинилкарбонил, моно- и N,N-диалкениламинокарбонил, моно- и диалкиниламинокарбонил, моно- и N,N-диалкениламино, моно- и N,N-диалкиниламино, триалкенилсилил, триалкинилсилил, необязательно замещенный циклоалкенил, необязательно замещенный циклоалкинил, фенил, фенокси и т.д. В случае замещенных циклических радикалов с алифатическими компонентами в кольце, также включены циклические системы с этими заместителями, присоединенными к кольцу с помощью двойной связи, например системы, содержащие алкилиденовую группу, такую как метилиден или этилиден, или оксогруппу, иминогруппу или замещенную иминогруппу. Когда два или большее число радикалов образуют одно или несколько колец, они могут быть карбоциклическими, гетероциклическими, насыщенными, частично насыщенными, ненасыщенными, например, также ароматическими и дополнительно замещенными.
Заместители, упомянутые в качестве примера (″первый уровень заместителей″), если они содержат углеводородсодержащие фрагменты, необязательно могут быть дополнительно замещены (″второй уровень заместителей″), например, одним из заместителей, как определено для первого уровня заместителей. Возможны соответствующие дальнейшие уровни заместителей. Термин ″замещенный радикал″ предпочтительно охватывает только один или два уровня заместителей.
Предпочтительными заместителями для уровней заместителей являются, например, амино, гидрокси, галоген, нитро, циано, изоциано, меркапто, изотиоцианато, карбоксил, карбоксамид, SF5, аминосульфонил, алкил, циклоалкил, алкенил, циклоалкенил, алкинил, N-моноалкиламино, N,N-диалкиламино, N-алканоиламино, алкокси, алкенилокси, алкинилокси, циклоалкокси, циклоалкенилокси, алкоксикарбонил, алкенилоксикарбонил, алкинилоксикарбонил, арилоксикарбонил, алканоил, алкенилкарбонил, алкинилкарбонил, арилкарбонил, алкилтио, циклоалкилтио, алкенилтио, циклоалкенилтио, алкинилтио, алкилсульфенил и алкилсульфинил, где включены оба энантиомера алкилсульфинильной группы, алкилсульфонил, N-моноалкиламиносульфонил, N,N-диалкиламиносульфонил, алкилфосфинил, алкилфосфонил, где в случае алкилфосфинила и алкилфосфонила включены оба энантиомера, N-алкиламинокарбонил, N-диалкиламинокарбонил, N-алканоиламинокарбонил, N-алканоил-N-алкиламинокарбонил, арил, арилокси, бензил, бензилокси, бензилтио, арилтио, ариламино, бензиламино, гетероциклил и триалкилсилил.
Заместители, состоящие из множества уровней заместителей, предпочтительно означают алкоксиалкил, алкилтиоалкил, алкилтиоалкокси, алкоксиалкокси, фенэтил, бензилокси, галогеналкил, галогенциклоалкил, галогеналкокси, галогеналкилтио, галогеналкилсульфинил, галогеналкилсульфонил, галогеналканоил, галогеналкилкарбонил, галогеналкоксикарбонил, галогеналкоксиалкокси, галогеналкоксиалкилтио, галогеналкоксиалканоил, галогеналкоксиалкил.
В случае радикалов, содержащих атомы углерода, предпочтение отдают радикалам, содержащим от 1 до 6 атомов углерода, предпочтительно от 1 до 4 атомов углерода, особенно 1 или 2 атома углерода. Предпочтение обычно отдают заместителям из группы, включающей галоген, например, фтор и хлор, (С1-С4)-алкил, предпочтительно метил или этил, (С1-С4)-галогеналкил, предпочтительно трифторметил, (С1-С4)-алкокси, предпочтительно метокси или этокси, (С1-С4)-галогеналкокси, нитро и циано. Особое предпочтение здесь отдают заместителям метил, метокси, фтор и хлор.
Замещенный амино, такой как моно- или дизамещенный амино, означает радикал из группы, включающей замещенный амино, который является N-замещенным, например, одним или двумя одинаковыми или разными радикалами из группы, состоящей из алкила, гидрокси, амино, алкокси, ацила и арила; предпочтительно N-моно- и N,N-диалкиламино, (например, метиламино, этиламино, N,N-диметиламино, N,N-диэтиламино, N,N-ди-н-пропиламино, N,N-диизопропиламино или N,N-дибутиламино), N-моно- или N,N-диалкоксиалкиламиногруппы (например, N-метоксиметиламино, N-метоксиэтиламино, N,N-ди(метоксиметил)амино или N,N-ди(метоксиэтил)амино), N-моно- и N,N-диариламино, такие как необязательно замещенные анилины, ациламино, N,N-диациламино, N-алкил-N-ариламино, N-алкил-N-ациламино, а также насыщенные N-гетероциклы; предпочтение здесь отдают алкильньш радикалам, содержащим от 1 до 4 атомов углерода; при этом, арил предпочтительно означает фенил или замещенный фенил; для ацила применяется определение, данное далее ниже, предпочтительно (C1-С4)-алканоил. То же самое применяется к замещенному гидроксиламино или гидразино.
В соответствии с изобретением, термин ″циклические аминогруппы″ охватывает гетероароматические или алифатические кольцевые системы, содержащие один или несколько атомов азота. Гетероциклы являются насыщенными или ненасыщенными, состоят из одной или нескольких необязательно конденсированных кольцевых систем и необязательно содержат дополнительные гетероатомы, такие как, например, один или два атома азота, кислорода и/или серы. Кроме того, термин также включает группы, содержащие спирокольцо или мостиковую кольцевую систему. Число атомов, которые образуют циклические аминогруппы, не ограничивается, в случае однокольцевой системы, например, группы могут состоять из 3-8 атомов в кольце, а в случае двухкольцевой системы - из 7-11 атомов.
Примерами, которые могут быть упомянуты, циклических аминогрупп, содержащих насыщенные и ненасыщенные моноциклические группы, содержащие атом азота в качестве гетероатома, являются 1-азетидинил, пирролидино, 2-пирролидин-1-ил, 1-пирролил, пиперидино, 1,4-дигидропиразин-1-ил, 1,2,5,6-тетрагидропиразин-1-ил, 1,4-дигидропиридин-1-ил, 1,2,5,6-тетрагидропиридин-1-ил, гомопиперидинил; примерами, которые могут быть упомянуты, циклических аминогрупп, содержащих насыщенные и ненасыщенные моноциклические группы, содержащие два или большее число атомом азота в качестве гстероатомов, являются 1-имидазолидинил, 1-имидазолил, 1-пиразолил, 1-триазолил, 1-тетразолил, 1-пиперазинил, 1-гомопиперазинил, 1,2-дигидропиперазин-1-ил, 1,2-дигидропиримидин-1-ил, пергидропиримидин-1-ил, 1,4-диазациклогептан-1-ил; примерами циклических аминогрупп, содержащих насыщенные и ненасыщенные моноциклические группы, содержащие один или два атома кислорода и от одного до трех атомов азота в качестве гетероатомов, являются, например, оксазолидин-3-ил, 2,3-дигидроизоксазол-2-ил, изоксазол-2-ил, 1,2,3-оксадиазин-2-ил, морфолино, примерами, которые могут быть упомянуты, циклических аминогрупп, содержащих насыщенные и ненасыщенные моноциклические группы, содержащие от одного до трех атомов азота и от одного до двух атомов серы в качестве гетероатомов, являются тиазолидин-3-ил, изотиазолин-2-ил, тиоморфолино, или диоксотиоморфолино; примерами, которые могут быть упомянуты, циклических аминогрупп, содержащих насыщенные и ненасыщенные конденсированные циклические группы, являются индол-1-ил, 1,2-дигидробензимидазол-1-ил, пергидропирроло[1,2-а]пиразин-2-ил; примерами, которые могут быть упомянуты, циклических аминогрупп, содержащих спироциклические группы, являются 2-азаспиро[4,5]декан-2-ил; примерами, которые могут быть упомянуты, циклических аминогрупп, содержащих мостиковые гетероциклические группы, являются 2-азабицикло[2.2.1]гептан-7-ил.
Замещенный амино также включает соединения четверичного аммония (соли) с четырьмя органическими заместителями на атоме азота.
Необязательно замещенный фенил предпочтительно представляет собой фенил, который является незамещенным или моно- или полизамещен, предпочтительно замещен вплоть до трех раз одинаковыми или разными радикалами из группы, включающей галоген, (С1-С4)-алкил, (С1-С4)-алкокси, (С1-С4)-алкокси-(С1-С4)-алкокси, (С1-С4)-алкокси-(С1-С4)-алкил, (С1-С4)-галогеналкил, (С1-С4)-галогеналкокси, (C1-C4)-алкилтио, (С1-С4)-галогеналкилтио, циано, изоциано и нитро, например о-, м- и п-толил, диметилфенилы, 2-, 3- и 4-хлорфенил, 2-, 3- и 4-фторфенил, 2-, 3- и 4-трифторметил- и -трихлорметилфенил, 2,4-, 3,5-, 2,5- и 2,3-дихлорфенил, о-, м- и п-метоксифенил.
Необязательно замещенный циклоалкил предпочтительно представляет собой циклоалкил, который является незамещенным или моно- или полизамещен, предпочтительно замещен вплоть до трех раз одинаковыми или разными радикалами из группы, включающей галоген, циано, (С1-С4)-алкил, (С1-С4)-алкокси, (С1-С4)-алкокси-(С1-С4)-алкокси, (С1-С4)-алкокси-(С1-С4)-алкил, (С1-С4)-галогеналкил и (C1-C4)-галогеналкокси, особенно одним или двумя (С1-С4)-алкильными радикалами.
Необязательно замещенный гетероциклил предпочтительно представляет собой гетероциклил, который является незамещенным или моно- или полизамещен, предпочтительно замещен вплоть до трех раз одинаковыми или разными радикалами из группы, включающей галоген, циано, (С1-С4)-алкил, (С1-С4)-алкокси, (С1-С4)-алкокси-(С1-С4)-алкокси, (С1-С4)-алкокси-(С1-С4)-алкил, (С1-С4)-галогеналкил, (C1-C4)-галогеналкокси, нитро и оксо, особенно моно- или полизамещен радикалами из группы, включающей галоген, (С1-С4)-алкил, (С1-С4)-алкокси, (С1-С4)-галогеналкил и оксо, наиболее предпочтительно замещен одним или двумя (С1-С4)-алкильными радикалами. Примерами алкил-замещенных гетероарильных групп являются фурилметил, тиенилметил, пиразолилметил, имидазолилметил, 1,2,3- и 1,2,4-триазолилметил, изоксазолилметил, тиазолилметил, изотиазолилметил, 1,2,3-, 1,3,4-, 1,2,4- и 1,2,5-оксадиазолилметил, азепинилметил, пирролилметил, пиридилметил, пиридазинилметил, пиримидинилметил, пиразинилметил, 1,3,5-, 1,2,4- и 1,2,3-триазинилметил, 1,2,4-, 1,3,2-, 1,3,6- и 1,2,6-оксазинилметил, оксепинилметил, тиепинилметил и 1,2,4-диазепинилметил.
Соли, которые являются пригодными в соответствии с изобретением, соединений в соответствии с изобретением, например соли с основаниями или кислотно-аддитивные соли, все являются обычными нетоксичными солями, предпочтительно солями, приемлемыми с точки зрения сельского хозяйства, и/или физиологически приемлемыми солями. Например, особо пригодны соли с основаниями или кислотно-аддитивные соли. Предпочтение отдают солям с неорганическими основаниями, таким как, например, соли щелочных металлов (например, соли натрия, калия или цезия), соли щелочноземельных металлов (например, соли кальция или магния), соли аммония, или солям с органическими основаниями, в частности с органическими аминами, таким как, например, соли триэтиламмония, дициклогексиламмония, N,N′-дибензилэтилендиаммония, пиридиния, пиколиния или этаноламмония, солям с неорганическими кислотами (например, гидрохлориды, гидробромиды, дигидросульфаты, тригидросульфаты или фосфаты), солям с органическими карбоновыми кислотами или органическими сульфокислотами (например, формиаты, ацетаты, трифторацетаты, малеаты, тартраты, метансульфонаты, бензолсульфонаты или 4-толуолсульфонаты). Известно, что т-амины, такие как некоторые из соединений в соответствии с изобретением, способны образовывать N-оксиды, которые также означают соли в соответствии с изобретением.
Соединения в соответствии с изобретением могут, в зависимости от природы заместителей, находиться в форме геометрических и/или оптически активных изомеров или соответствующих смесей изомеров с различными составами. Эти стереоизомеры являются, например, энантиомерами, диастереомерами, атропоизомерами или геометрическими изомерами. Соответственно, изобретение включает чистые стереоизомеры и любую смесь этих изомеров.
При необходимости, соединения в соответствии с изобретением могут присутствовать в различных полиморфных формах или в виде смесей различных полиморфных форм. Как чистые полиморфы, так и смеси полиморфов обеспечиваются настоящим изобретением и могут применяться в соответствии с изобретением.
Соединения общей формулы (I) можно смешивать или наносить совместно с другими инсектицидными, нематоцидными, акарицидными или противомикробными активными соединениями. В этих смесях или совместных нанесениях, имеет место синергетическое действие, то есть наблюдаемое действие этих смесей или совместных нанесений превышает сумму действий отдельных активных соединений при таких нанесениях. Примерами таких компонентов для смесей или комбинаций являются:
(1) Ингибиторы ацетилхолинэстеразы (AChE), например
карбаматы, например аланикарб (II-1-1), алдикарб (II-1-2), бендиокарб (II-1-3), бенфуракарб (II-1-4), бутокарбоксим (II-1-5), бутоксикарбоксим (II-1-6), карбарил (II-1-7), карбофуран (II-1-8), карбосульфан (II-1-9), этиофенкарб (II-1-10), фенобукарб (II-1-11), форметанат (II-1-12), фуратиокарб (II-1-13), изопрокарб (II-1-14), метиокарб (II-1-15), метомил (II-1-16), метолкарб (II-1-17), оксамил (II-1-18), пиримикарб (II-1-19), пропоксур (II-1-20), тиодикарб (II-1-21), тиофанокс (II-1-22), триазамат (II-1-23), триметакарб (II-1-24), XMC (II-1-25) и ксилилкарб (II-1-26); или
органофосфаты, например ацефат (II-1-27), азаметифос (II-1-28), азинфос-этил (II-1-29), азинфос-метил (II-1-30), кадусафос (II-1-31), хлорэтоксифос (II-1-32), хлорфенвинфос (II-1-33), хлормефос (II-1-34), хлорпирифос (II-1-35), хлорпирифос-метил (II-1-36), кумафос (II-1-37), цианофос (II-1-38), деметон-8-метил (II-1-39), диазинон (II-1-40), дихлорвос/DDVP (II-1-41), дикротофос (II-1-42), диметоат (II-1-43), диметилвинфос (II-1-44), дисульфотон (II-1-45), EPN (II-1-46), этион (II-1-47), этопрофос (II-1-48), фамфур (II-1-49), фенамифос (II-1-50), фенитротион (II-1-51), фентион (II-1-52), фостиазат (II-1-53), гептенофос (II-1-54), имициафос (II-1-55), изофенфос (II-1-56), изопропил O-(метоксиаминотиофосфорил) салицилат (II-1-57), изоксатион (II-1-58), малатион (II-1-59), мекарбам (II-1-60), метамидофос (II-1-61), метидатион (II-1-62), мевинфос (II-1-63), монокротофос (II-1-64), налед (II-1-65), ометоат (II-1-66), оксидеметон-метил (II-1-67), паратион (II-1-68), паратион-метил (II-1-69), фентоат (II-1-70), форат (II-1-71), фосалон (II-1-72), фосмет (II-1-73), фосфамидон (II-1-74), фоксим (II-1-75), примифос-метил (II-1-76), профенофос (II-1-77), пропетамфос (II-1-78), протиофос (II-1-79), пираклофос (II-1-80), пиридафентион (II-1-81), хиналфос (II-1-82), сульфотеп (II-1-83), тебупиримфос (II-1-84), темефос (II-1-85), тербуфос (II-1-86), тетрахлорвинфос (II-1-87), тиометон (II-1-88), триазофос (II-1-89), трихлорфон (II-1-90) и вамидотион (II-1-91).
(2) Антагонисты ГАМК-регулируемых хлоридных каналов, такие как, например, циклодиеновые хлорорганические соединения, например хлордан (II-2-1) и эндосульфан (II-2-2); или
фенилпиразолы (фипролы), например этипрол (II-2-3) и фипронил (II-2-4).
(3) Модуляторы натриевого канала/блокаторы потенциалозависимых натриевых каналов, такие как, например,
пиретроиды, например акринатрин (II-3-1), аллетрин (II-3-2), d-цис-транс аллетрин (II-3-3), d-транс аллетрин (II-3-4), бифентрин (II-3-5), биоаллетрин (II-3-6), биоаллетрин S-циклопентенил-изомер (II-3-7), биоресметрин (II-3-8), циклопротрин (II-3-9), цифлутрин (II-3-10), бета-цифлутрин (II-3-11), цигалотрин (II-3-12), лямбда-цигалотрин (II-3-13), гамма-цигалотрин (II-3-14), циперметрин (II-3-15), альфа-циперметрин (II-3-16), бета-циперметрин (II-3-17), тета-циперметрин (II-3-18), зета-циперметрин (II-3-19), цифенотрин [(1R)-транс изомеры] (II-3-20), дельтаметрин (II-3-21), эмпентрин [(EZ)-(1R) изомеры] (II-3-22), эсфенвалерат (II-3-23), этофенпрокс (II-3-24), фенпропатрин (II-3-25), фенвалерат (II-3-26), флуцитринат (II-3-27), флуметрин (II-3-28), тау-флувалинат (II-3-29), галфенпрокс (II-3-30), имипротрин (II-3-31), кадетрин (II-3-32), перметрин (II-3-33), фенотрин [(1R)-TpaHC изомер] (II-3-34), праллетрин (II-3-35), пиретрин (пиретрум) (II-3-36), ресметрин (II-3-37), силафлуофен (II-3-38), тефлутрин (II-3-39), тетраметрин (II-3-40), тетраметрин [(1R) изомеры)] (II-3-41), тралометрин (II-3-42) и трансфлутрин (II-3-43); или
DDT (II-3-44); или метоксихлор (II-3-45).
(4) Агонисты никотинового ацетилхолинового рецептора (nAChR), такие как, например,
неоникотиноиды, например ацетамиприд (II-4-1), клотианидин (II-4-2), динотефуран (II-4-3), имидаклоприд (II-4-4), нитенпирам (II-4-5), тиаклоприд (II-4-6) и тиаметоксам (II-4-7); или
никотин (II-4-8).
(5) Аллостерические активаторы никотинового ацетилхолинового рецептора (nAChR), такие как, например,
спиносины, например спинеторам (II-5-1) и спиносад (II-5-2).
(6) Активаторы хлоридных каналов, такие как, например,
авермектины/милбемицины, например абамектин (II-6-1), эмамектин бензоат (II-6-2), лепимектин (II-6-3) и милбемектин (II-6-4).
(7) Имитаторы ювенильных гормонов, такие как, например,
аналоги ювенильных гормонов, например гидропрен (II-7-1), кинопрен (II-7-2) и метопрен (II-7-3); или
феноксикарб (II-7-4); или пирипроксифен (II-7-5).
(8) Активные соединения с неизвестными или неспецифическими механизмами действия, такие как, например
алкилгалогениды, например метилбромид (II-8-1) и другие алкилгалогениды; или
хлорпикрин (II-8-2); или фтористый сульфурил (II-8-3); или боракс (II-8-4); или антимонил-тартрат калия (II-8-5).
(9) Селективные антифиданты, например пиметрозин (II-9-1); или флоникамид (II-9-2).
(10) Ингибиторы роста клещей, например клофентезин (II-10-1), гекситиазокс (II-10-2) и дифловидазин (II-10-3); или
этоксазол (II-10-4).
(11) Микробные разрушители кишечной мембраны насекомых, например Bacillus thuringiensis подвид israelensis (II-11-1), Bacillus sphaericus (II-11-2), Bacillus thuringiensis подвид aizawai (II-11-3), Bacillus thuringiensis подвид kurstaki (II-11-4), Bacillus thuringiensis подвид tenebrionis (II-11-5) и ВТ растительный белок: Cry1Ab, Cry1Ac, Cry1Fa, Cry2Ab, mCry3A, Cry3Ab, Cry3Bb, Cry34/35Ab1 (II-11-6).
(12) Ингибиторы окислительного фосфорилирования, АТФ разрыватели, такие как, например, диафентиурон (II-12-1); или
оловоорганические соединения, например азоциклотин (II-12-2), цигексатин (II-12-3) и фенбутатин оксид (II-12-4); или
пропаргит (II-12-5); или тетрадифон (II-12-6).
(13) Разобщители окислительного фосфорилирования, действующие путем прерывания Н протонного градиента, такие как, например, хлорфенапир (II-13-1), DNOC (II-13-2) и сульфурамид (II-13-3).
(14) Антагонисты никотинового ацетилхолинового рецептора, такие как, например, бенсультап (II-14-1), картап гидрохлорид (II-14-2), тиоциклам (II-14-3) и тиосультап-натрий (II-14-4).
(15) Ингибиторы биосинтеза хитина, тип 0, такие как, например, бистрифлурон (II-15-1), хлорфлуазурон (II-15-2), дифлубензурон (II-15-3), флуциклоксурон (II-15-4), флуфеноксурон (II-15-5), гексафлумурон (II-15-6), луфенурон (II-15-7), новалурон (II-15-8), новифлумурон (II-15-9), тефлубензурон (II-15-10) и трифлумурон (II-15-11).
(16) Ингибиторы биосинтеза хитина, тип 1, такие как, например, бупрофезин (II-16-1).
(17) Разрушители линьки двукрылых, такие как, например, циромазин (II-17-1).
(18) Агонисты рецептора экдизона, такие как, например, хромафенозид (II-18-1), галофенозид (II-18-2), метоксифенозид (II-18-3) и тебуфенозид (II-18-4).
(19) Октопаминергические агонисты, такие как, например, амитраз (II-19-1).
(20) Ингибиторы транспорта электронов через комплекс III, такие как, например, гидраметилнон (II-20-1); или ацеквиноцил (II-20-2); или флуакрипирим (II-20-3).
(21) Ингибиторы транспорта электронов через комплекс I, например, METI акарициды, например, феназахин (II-21-1), фенпироксимат (II-21-2), пиримидифен (II-21-3), пиридабен (II-21-4), тебуфенпирад (II-21-5) и толфенпирад (II-21-6); или
ротенон (деррис) (II-21-7).
(22) Блокаторы потенциалозависимых натриевых каналов, например индоксакарб (II-22-1); или метафлумизон (II-22-2).
(23) Ингибиторы ацетил-СоА карбоксилазы, такие как, например, производные тетроновой и тетрамовой кислоты, например спиродиклофен (II-23-1), спиромезифен (II-23-2) и спиротетрамат (II-23-3).
(24) Ингибиторы транспорта электронов через комплекс IV, такие как, например, фосфины, например, фосфид алюминия (II-24-1), фосфид кальция (II-24-2), фосфин (II-24-3) и фосфид цинка (II-24-4); или
цианид (II-24-5).
(25) Ингибиторы транспорта электронов через комплекс II, такие как, например, циенопирафен (II-25-1).
(28) Эффекторы рианодинового рецептора, такие как, например,
диамиды, например хлорантранилипрол (II-28-1) и флубендиамид (II-28-2).
Дополнительные активные соединения с неизвестным механизмом действия, такие как, например, амидофлумет (II-29-1), азадирахтин (II-29-2), бенклотиаз (II-29-3), бензоксимат (II-29-4), бифеназат (II-29-5), бромпропилат (II-29-6), хинометионат (II-29-7), криолит (II-29-8), циантранилипрол (циазипир) (II-29-9), цифлуметофен (II-29-10), дикофол (II-29-11), дифловидазин (II-29-12), флуенсульфон (II-29-13), флуфенерим (II-29-14), флуфипрол (II-29-15), флуопирам (II-29-16), фуфенозид (II-29-17), имидаклотиз (II-29-18), ипродион (II-29-19), пиридалил (II-29-20), пирифлухиназон (II-29-21) и йодметан (II-29-22); кроме того, препараты на основе Bacillus firmus (1-1582, BioNeem, Votivo) (II-29-23), а также следующие известные активные соединения: 3-бром-N-{2-бром-4-хлор-6-[(1-циклопропилэтил)карбамоил] фенил}-1-(3-хлорпиридин-2-ил)-1Н-пиразол-5-карбоксамид (II-29-24) (известный из WO 2005/077934), 4-{[(6-бромпирид-3-ил)метил](2-фторэтил)амино}фуран-2(5Н)-он (II-29-25) (известный из WO 2007/115644), 4-{[(6-фторпирид-3-ил)метил](2,2-дифторэтил)амино}фуран-2(5Н)-он (II-29-26) (известный из WO 2007/115644), 4-{[(2-хлор-1,3-тиазол-5-ил)метил](2-фторэтил)амино}фуран-2(5Н)-он (II-29-27) (известный из WO 2007/115644), 4-{[(6-хлорпирид-3-ил)метил](2-фторэтил)амино}фуран-2(5Н)-он (II-29-28) (известный из WO 2007/115644), 4-{[(6-хлорпирид-3-ил)метил](2,2-дифторэтил)амино}фуран-2(5Н)-он (II-29-29) (известный из WO 2007/115644), 4-{[(6-хлор-5-фторпирид-3-ил)метил](метил)амино}фуран-2(5Н)-он (II-29-30) (известный из WO 2007/115643), 4-{[(5,6-дихлорпирид-3-ил)метил](2-фторэтил)амино}фуран-2(5Н)-он (II-29-31) (известный из WO 2007/115646), 4-{[(6-хлор-5-фторпирид-3-ил)метил](циклопропил)амино}фуран-2(5Н)-он (II-29-32) (известный из WO 2007/115643), 4-{[(6-хлорпирид-3-ил)метил](циклопропил)амино}фуран-2(5Н)-он (II-29-33) (известный из ЕР-А-0539588), 4-{[(6-хлорпирид-3-ил)метил](метил)амино}фуран-2(5Н)-он (II-29-34) (известный из ЕР-А-0539588), {[1-(6-хлорпиридин-3-ил)этил](метил)оксидо-λ4-сульфанилиден}цианамид (II-29-35) (известный из WO 2007/149134) и его диастереомеры {[(1R)-1-(б-хлорпиридин-3-ил)этил](метил)оксидо-λ4-сульфанилиден}цианамид (А) (II-29-36) и {[(1S)-1-(6-хлорпиридин-3-ил)этил](метил)оксидо-λ4-сульфанилиден} цианамид (В) (II-29-37) (также известные из WO 2007/149134) и сульфоксафлор (II-29-38) (также известный из WO 2007/149134) и его диастереомеры [(R)-метил(оксидо){(1R)-1-[6-(трифторметил)-пиридин-3-ил]этил}-λ4-сульфанилиден]цианамид (A1) (II-29-39) и [(S)-метил(оксидо){(1S)-1-[6-(трифторметил)пиридин-3-ил]этил}-λ4-сульфанилиден]цианамид (А2) (II-29-40), обозначенные как группа диастереомеров А (известная из WO 2010/074747, WO 2010/074751), [(R)-метил(оксидо){(1S)-1-[6-(трифторметил)пиридин-3-ил]этил}-λ4-сульфанилиден] цианамид (B1) (II-29-41) и [(S)-метил(оксидо) {(1R)-1-[6-(трифторметил)пиридин-3-ил]этил}-λ4-сульфанилиден]цианамид (В2) (II-29-42), обозначенные как группа диастереомеров В (также известная из WO 2010/074747, WO 2010/074751) и 11-(4-хлор-2,6-диметилфенил)-12-гидрокси-1,4-диокса-9-азадиспиро[4.2.4.2]тетрадец-11-ен-10-он (II-29-43) (известный из WO 2006/089633), 3-(4′-фтор-2,4-диметилбифенил-3-ил)-4-гидрокси-8-окса-1-азаспиро[4.5]дец-3-ен-2-он (II-29-44) (известный из WO 2008/067911), 1-{2-фтор-4-метил-5-[(2,2,2-трифторэтил)сульфинил]фенил}-3-(трифторметил)-1Н-1,2,4-триазол-5-амин (II-29-45) (известный из WO 2006/043635), [(3S,4aR,12R,12aS,12bS)-3-[(циклопропилкарбонил)окси]-6,12-дигидрокси-4,12b-диметил-11-оксо-9-(пиридин-3-ил)-1,3,4,4а,5,6,6а, 12,12а,12b-декагидро-2Н,11Н-бензо[1]пирано[4,3-b]хромен-4-ил]метил циклопропанкарбоксилат (II-29-46) (известный из WO 2008/066153), 2-циано-3-(дифторметокси)-N,N-диметилбензолсульфонамид (II-29-47) (известный из WO 2006/056433), 2-циано-3-(дифторметокси)-Н-метилбензолсульфонамид (II-29-48) (известный из WO 2006/100288), 2-циано-3-(дифторметокси)-N-этилбензолсульфонамид (II-29-49) (известный из WO 2005/035486), 4-(дифторметокси)-N-этил-N-метил-1,2-бензотиазол-3-амин 1,1-диоксид (II-29-50) (известный из WO 2007/057407), N-[1-(2,3-диметилфенил)-2-(3,5-диметилфенил)этил]-4,5-дигидро-1,3-тиазол-2-амин (II-29-51) (известный из WO 2008/104503), {1′-[(2Е)-3-(4-хлорфенил)проп-2-ен-1-ил]-5-фторспиро[индол-3,4′-пиперидин]-1(2Н)-ил}(2-хлорпиридин-4-ил)метанон (II-29-52) (известный из WO 2003/106457), 3-(2,5-диметилфенил)-4-гидрокси-8-метокси-1,8-диазаспиро[4.5]дец-3-ен-2-он (II-29-53) (известный из WO 2009/049851), 3-(2,5-диметилфенил)-8-метокси-2-оксо-1,8-диазаспиро[4.5]дец-3-ен-4-ил этилкарбонат (II-29-54) (известный из WO 2009/049851), 4-(бут-2-ин-1-илокси)-6-(3,5-диметилпиперидин-1 -ил)-5-фторпиримидин (II-29-55) (известный из WO 2004/099160), (2,2,3,3,4,4,5,5-октафторпентил)(3,3,3-трифторпропил)малононитрил (II-29-56) (известный из WO 2005/063094), (2,2,3,3,4,4,5,5-октафторпентил)(3,3,4,4,4-пентафторбутил)малононитрил (II-29-57) (известный из WO 2005/063094), 8-[2-(никлопропилметокси)-4-(трифторметил)фенокси]-3-[6-(трифторметил)пиридазин-3-ил]-3-азабицикло[3.2.1]октан (II-29-58) (известный из WO 2007/040280), 2-этил-7-метокси-3-метил-6-[(2,2,3,3-тетрафтор-2,3-дигидро-1,4-бензодиоксин-6-ил)окси]хинолин-4-ил метилкарбонат (II-29-59) (известный из JP 2008/110953), 2-этил-7-метокси-3-метил-6-[(2,2,3,3-тетрафтор-2,3-дигидро-1,4-бензодиоксин-6-ил)окси]хинолин-4-ил ацетат (II-29-60) (известный из JP 2008/110953), PF1364 (CAS рег. №1204776-60-2) (II-29-61) (известный из JP 2010/018586), 5-[5-(3,5-дихлорфенил)-5-(трифторметил)-4,5-дигидро-1,2-оксазол-3-ил]-2-(1Н-1,2,4-триазол-1-ил)бензонитрил (II-29-62) (известный из WO 2007/075459), 5-[5-(2-хлорпиридин-4-ил)-5-(трифторметил)-4,5-дигидро-1,2-оксазол-3-ил]-2-(1Н-1,2,4-триазол-1-ил)бензонитрил (II-29-63) (известный из WO 2007/075459), 4-[5-(3,5-дихлорфенил)-5-(трифторметил)-4,5-дигидро-1,2-оксазол-3-ил]-2-метил-N-{2-оксо-2-[(2,2,2-трифторэтил)амино]этил}бензамид (II-29-64) (известный из WO 2005/085216), 4-{[(6-хлорпиридин-3-ил)метил](циклопропил)амино}-1,3-оксазол-2(5Н)-он (II-29-65), 4-{[(б-хлорпиридин-3-ил)метил](2,2-дифторэтил)амино}-1,3-оксазол-2(5Н)-он (II-29-66), 4-{[(6-хлорпиридин-3-ил)метил] (этил)амино} -1,3-оксазол-2(5Н)-он (II-29-67), 4-{[(6-хлорпиридин-3-ил)метил](метил)амино}-1,3-оксазол-2(5Н)-он (II-29-68) (все известны из WO 2010/005692), NNI-0711 (II-29-69) (известный из WO 2002/096882), 1-ацетил-N-[4-(1,1,1,3,3,3-гексафтор-2-метоксипропан-2-ил)-3-изобутилфенил]-N-изобутирил-3,5-диметил-1Н-пиразол-4-карбоксамид (II-29-70) (известный из WO 2002/096882), метил 2-[2-({[3-бром-1-(3-хлорпиридин-2-ил)-1Н-пиразол-5-ил] карбонил} амино)-5-хлор-3-метилбензоил]-2-метилгидразинкарбоксилат (II-29-71) (известный из WO 2005/085216), метил 2-[2-({[3-бром-1-(3-хлорпиридин-2-ил)-1Н-пиразол-5-ил]карбонил}амино)-5-циано-3-метилбензоил]-2-этилгидразинкарбоксилат (II-29-72) (известный из WO 2005/085216), метил 2-[2-({[3-бром-1-(3-хлорпиридин-2-ил)-1Н-пиразол-5-ил]карбонил}амино)-5-циано-3-метилбензоил]-2-метилгидразинкарбоксилат (II-29-73) (известный из WO 2005/085216), метил 2-[3,5-дибром-2-({[3-бром-1-(3-хлорпиридин-2-ил)-1Н-пиразол-5-ил]карбонил}амино)бензоил]-1,2-диэтилгидразинкарбоксилат (II-29-74) (известный из WO 2005/085216), метил 2-[3,5-дибром-2-({[3-бром-1-(3-хлорпиридин-2-ил)-1Н-пиразол-5-ил] карбонил} амино)бензоил]-2-этилгидразинкарбоксилат (II-29-75) (известный из WO 2005/085216), (5RS,7RS;5RS,7SR)-1-(6-хлор-3-пиридилметил)-1,2,3,5,6,7-гексагидро-7-метил-8-нитро-5-пропоксиимидазо[1,2-а]ииридин (II-29-76) (известный из WO 2007/101369), 2-{6-[2-(5-фторпиридин-3-ил)-1,3-тиазол-5-ил]пиридин-2-ил}пиримидин (II-29-77) (известный из WO 2010/006713), 2-{6-[2-(пиридин-3-ил)-1,3-тиазол-5-ил] пиридин-2-ил} пиримидин (II-29-78) (известный из WO 2010/006713), 1-(3-хлорпиридин-2-ил)-Н-[4-циано-2-метил-6-(метилкарбамоил)фенил]-3-{[5-(трифторметил)-1Н-тетразол-1-ил]метил}-1Н-пиразол-5-карбоксамид (II-29-79) (известный из WO 2010/069502), 1-(3-хлорпиридин-2-ил)-N-[4-циано-2-метил-6-(метилкарбамоил)фенил]-3-{[5-(трифторметил)-2Н-тетразол-2-ил]метил}-1Н-пиразол-5-карбоксамид (II-29-80) (известный из WO 2010/069502), N-[2-(трет-бутилкарбамоил)-4-циано-6-метилфенил]-1-(3-хлорпиридин-2-ил)-3-{[5-(трифторметил)-1Н-тетразол-1-ил]метил}-1Н-пиразол-5-карбоксамид (II-29-81) (известный из WO 2010/069502), N-[2-(трет-бутилкарбамоил)-4-циано-6-метилфенил]-1-(3-хлорпиридин-2-ил)-3-{[5-(трифторметил)-2Н-тетразол-2-ил]метил}-1Н-пиразол-5-карбоксамид (II-29-82) (известный из WO 2010/069502) и (1Е)-N-[(6-хлорпиридин-3-ил)метил]-N′-циано-N-(2,2-дифторэтил)этанимидамид (II-29-83) (известный из WO 2008/009360).
Антимикробные активные соединения:
(1) Ингибиторы биосинтеза эргостерола, например альдиморф, азаконазол, битертанол, бромуконазол, ципроконазол, диклобутразол, дифеноконазол, диниконазол, диниконазол-М, додеморф, додеморф ацетат, эпоксиконазол, этаконазол, фенаримол, фенбуконазол, фенгексамид, фенпропидин, фенпропиморф, флуквинконазол, флурпримидол, флусилазол, флутриафол, фурконазол, фурконазол-цис, гексаконазол, имазалил, имазалил сульфат, имибенконазол, ипконазол, метконазол, миклобутанил, нафтифин, нуаримол, окспоконазол, паклобутразол, пефуразоат, пенконазол, пипералин, прохлораз, пропиконазол, протиоконазол, пирибутикарб, пирифенокс, хинконазол, симеконазол, спироксамин, тебуконазол, тербинафин, тетраконазол, триадимефон, триадименол, тридеморф, трифлумизол, трифорин, тритиконазол, униконазол, униконазол-р, виниконазол, вориконазол, 1-(4-хлорфенил)-2-(1Н-1,2,4-триазол-1-ил)циклогептанол, метил 1 -(2,2-диметил-2,3-дигидро-1Н-инден-1-ил)-1Н-имидазол-5-карбоксилат, N′-{5-(дифторметил)-2-метил-4-[3-(триметилсилил)пропокси]фенил}-N-этил-N-метилимидоформамид, N-этил-N-метил-N′-{2-метил-5-(трифторметил)-4-[3-(триметилсилил)пропокси]фенил}имидоформамид и O-[1-(4-метоксифенокси)-3,3-диметилбутан-2-ил] 1Н-имидазол-1-карботиоат.
(2) Ингибиторы дыхания (ингибиторы дыхательной цепи), например, биксафен, боскалид, карбоксин, дифлуметорим, фенфурам, флуопирам, флутоланил, флуксапироксад, фураметпир, фурмециклокс, изопиразам - смесь син-эпимера, рацемата 1RS,4SR,9RS, и анти-эпимера, рацемата 1RS,4SR,9SR, изопиразам (анти-эпимер, рацемат), изопиразам (анти-эпимер, энантиомер 1R,4S,9S), изопиразам (анти-эпимер, энантиомер 1S,4R,9R), изопиразам (син-эпимер, рацемат 1RS,4SR,9RS), изопиразам (син-эпимер, энантиомер 1R,4S,9R), изопиразам (син-эпимер, энантиомер 1S,4R,9S), мепронил, оксикарбоксин, пенфлуфен, пентиопирад, седаксан, тифлузамид, 1-метил-N-[2-(1,1,2,2-тетрафторэтокси)фенил]-3-(трифторметил)-1Н-пиразол-4-карбоксамид, 3-(дифторметил)-1-метил-N-[2-(1,1,2,2-тетрафторэтокси)фенил]-1Н-пиразол-4-карбоксамид, 3-(дифторметил)-N-[4-фтор-2-(1,1,2,3,3,3-гексафторпропокси)фенил]-1-метил-1Н-пиразол-4-карбоксамид и N-[1-(2,4-дихлорфенил)-1-метоксипропан-2-ил]-3-(дифторметил)-1-метил-1Н-пиразол-4-карбоксамид.
(3) Ингибиторы дыхания (ингибиторы дыхательной цепи), действующие на комплекс III дыхательной цепи, например, аметоктрадин, амисулбром, азоксистробин, циазофамид, димоксистробин, энестробурин, фамоксадон, фенамидон, флуоксастробин, крезоксим-метил, метоминостробин, орисастробин, пикоксистробин, пираклостробин, пираметостробин, пираоксистробин, пирибенкарб, трифлоксистробин, (2Е)-2-(2-{[6-(3-хлор-2-метилфенокси)-5-фторпиримидин-4-ил]окси}фенил)-2-(метоксиимино)-N-метилэтанамид, (2Е)-2-(метоксиимино)-N-метил-2-(2-{[({(1Е)-1-[3-(трифторметил)фенил]этилиден}амино)окси]метил}фенил)этанамид, (2Е)-2-(метоксиимино)-N-метил-2-{2-[(Е)-({1-[3-(трифторметил)фенил]этокси} имино)метил]фенил}этанамид, (2Е)-2-{2-[({[(1Е)-1-(3-{[(Е)-1-фтор-2-фенилэтенил]окси}фенил)этилиден]амино} окси)метил]фенил}-2-(метоксиимино)-N-метилэтанамид, (2Е)-2-{2-[({[(2Е,3Е)-4-(2,6-дихлорфенил)бут-3-ен-2-илиден]амино}окси)метил]фенил}-2-(метоксиимино)-N-метилэтанамид, 2-хлор-N-(1,1,3-триметил-2,3-дигидро-1Н-инден-4-ил)пиридин-3-карбоксамид, 5-метокси-2-метил-4-(2-{[({(1Е)-1-[3-(трифторметил)фенил]этилиден}амино)окси]метил}фенил)-2,4-дигидро-3Н-1,2,4-триазол-3-он, метил (2Е)-2-{2-[({циклопропил[(4-метоксифенил)имино]метил}сульфанил)метил]фенил}-3-метоксипроп-2-еноат, N-(3-этил-3,5,5-триметилциклогексил)-3-(формиламино)-2-гидроксибензамид, 2-{2-[(2,5-диметилфенокси)метил]фенил}-2-метокси-N-метилацетамид и (2R)-2-{2-[(2,5-диметилфенокси)метил]фенил}-2-метокси-N-метилацетамид.
(4) Ингибиторы митоза и деления клеток, например, беномил, карбендазим, хлорфеназол, диэтофенкарб, этабоксам, флуопиколид, фуберидазол, пенцикурон, тиабендазол, тиофанат-метил, тиофанат, зоксамид, 5-хлор-7-(4-метилпиперидин-1-ил)-6-(2,4,6-трифторфенил)[1,2,4]триазоло[1,5-а]пиримидин и 3-хлор-5-(6-хлорпиридин-3-ил)-6-метил-4-(2,4,6-трифторфенил)пиридазин.
(5) Соединения с мультисайтовой активностью, например. Бордоская жидкость, каптафол, каптан, хлороталонил, препараты меди, такие как гидроксид меди, нафтенат меди, оксид меди, оксихлорид меди, сульфат меди, дихлофлуанид, дитианон, додин, додин в форме свободного основания, фербам, флуорофолпет, фолпет, гуазатин, гуазатин ацетат, иминоктадин, иминоктадин-албесилат, иминоктадин-триацетат, манкоппер, манкозеб, манеб, метирам, метирам-цинк, оксин-медь, пропамидин, пропинеб, сера и препараты серы, например, полисульфид кальция, тирам, толилфлуанид, зинеб и зирам.
(6) Индукторы устойчивости, например, ацибензолар-8-метил, изотианил, пробеназол и тиадинил.
(7) Ингибиторы биосинтеза аминокислот и белка, например, андоприм, бластицидин-S, ципродинил, касугамицин, гидрат гидрохлорида касугамицина, мепанипирим и пириметанил.
(8) Ингибиторы выработки АТФ, например, фентинацетат, фентинхлорид, фентингидроксид и силтиофам.
(9) Ингибиторы синтеза клеточных оболочек, например, бентиаваликарб, диметоморф, флуморф, ипроваликарб, мандипропамид, полиоксины, полиоксорим, валидамицин А и валифеналат.
(10) Ингибиторы синтеза липидов и мембран, например, бифенил, хлоронеб, диклоран, эдифенфос, этридиазол, иодокарб, ипробенфос, изопротиолан, пропамокарб, пропамокарб гидрохлорид, протиокарб, пиразофос, хинтозин, текназен и толклофос-метил.
(11) Ингибиторы биосинтеза меланина, например, карпропамид, диклоцимет, феноксанил, фталид, пироквилон и трициклазол.
(12) Ингибиторы синтеза нуклеиновых кислот, например, беналаксил, беналаксил-М (киралаксил), бупиримат, клозилакон, диметиримол, этиримол, фуралаксил, гимексазол, металаксил, металаксил-М (мефеноксам), офурас, оксадиксил, оксолиновая кислота.
(13) Ингибиторы сигнальной трансдукции, например, хлозолинат, фенпиклонил, флудиоксонил, ипродион, процимидон, хиноксифен и винклозолин.
(14) Разобщающие агенты, например, бинапакрил, динокап, феримзон, флуазинам и мептилдинокап.
(15) Дополнительные соединения, например, бентиазол, бетоксазин, капсимицин, карвон, хинометионат, хлазафенон, куфранеб, цифлуфенамид, цимоксанил, ципросульфамид, дазомет, дебакарб, дихлорофен, дикломезин, дифензокват, дифензокват метилсульфат, дифениламин, экомат, фенпиразамин, флуметовер, флуоромид, флусульфамид, флутианил, фосетил-алюминий, фосетил-кальций, фосетил-натрий, гексахлорбензол, ирумамицин, метасульфокарб, метил изотиоцианат, метрафенон, милдиомицин, натамицин, диметилдитиокарбамат никеля, нитротал-изопропил, октилинон, оксамокарб, оксифентиин, пентахлорфенол и его соли, фенотрин, фосфорная кислота и ее соли, пропамокарб-фосетилат, пропаносин-натрий, проквиназид, пирролнитрин, тебуфлоквин, теклофталам, толнифанид, триазоксид, трихламид, зариламид, 1-(4-{4-[(5R)-5-(2,6-дифторфенил)-4,5-дигидро-1,2-оксазол-3-ил]-1,3-тиазол-2-ил}пиперидин-1-ил)-2-[5-метил-3-(трифторметил)-1Н-пиразол-1-ил]этанон, 1-(4-{4-[(5S)-5-(2,6-дифторфенил)-4,5-дигидро-1,2-оксазол-3-ил]-1,3-тиазол-2-ил}пиперидин-1-ил)-2-[5-метил-3-(трифторметил)-1Н-пиразол-1-ил]этанон, 1-(4-{4-[5-(2,6-дифторфенил)-4,5-дигидро-1,2-оксазол-3-ил]-1,3-тиазол-2-ил}пиперидин-1-ил)-2-[5-метил-3-(трифторметил)-1Н-пиразол-1-ил]этанон, 1-(4-метоксифенокси)-3,3-диметилбутан-2-ил 1Н-имидазол-1-карбоксилат, 2,3,5,6-тетрахлор-4-(метилсульфонил)пиридин, 2,3-дибутил-6-хлортиено[2,3-а]пиримидин-4(3Н)-он,2-[5-метил-3-(трифторметил)-1Н-пиразол-1-ил]-1-(4-{4-[(5R)-5-фенил-4,5-дигидро-1,2-оксазол-3-ил]-1,3-тиазол-2-ил}пиперидин-1-ил)этанон, 2-[5-метил-3-(трифторметил)-1Н-пиразол-1-ил]-1-(4-{4-[(5S)-5-фенил-4,5-дигидро-1,2-оксазол-3-ил]-1,3-тиазол-2-ил}пиперидин-1-ил)этанон, 2-[5-метил-3-(трифторметил)-1Н-пиразол-1-ил]-1-{4-[4-(5-фенил-4,5-дигидро-1,2-оксазол-3-ил)-1,3-тиазол-2-ил]пиперидин-1-ил}этанон, 2-бутокси-6-йод-3-пропил-4Н-хромен-4-он, 2-хлор-5-[2-хлор-1-(2,6-дифтор-4-метоксифенил)-4-метил-1Н-имидазол-5-ил]пиридин, 2-фенилфенол и его соли, 3,4,5-трихлорпиридин-2,6-дикарбонитрил, 3-[5-(4-хлорфенил)-2,3-диметил-1,2-оксазолидин-3-ил]пиридин, 3-хлор-5-(4-хлорфенил)-4-(2,6-дифторфенил)-6-метилпиридазин, 4-(4-хлорфенил)-5-(2,6-дифторфенил)-3,6-диметилпиридазин, 5-амино-1,3,4-тиадиазол-2-тиол, 5-хлор-N′-фенил-N′-(проп-2-ин-1-ил)тиофен-2-сульфоногидразид, 5-метил-6-октил[1,2,4]триазоло[1,5-а]пиримидин-7-амин, этил (2Z)-3-амино-2-циано-3-фенилпроп-2-еноат, N-(4-хлорбензил)-3-[3-метокси-4-(проп-2-ин-1-илокси)фенил]пропанамид, N-[(4-хлорфенил)(пиано)метил]-3-[3-метокси-4-(проп-2-ин-1-илокси)фенил]пропанамид, N-[(5-бром-3-хлорпиридин-2-ил)метил]-2,4-дихлорпиридин-3-карбоксамид, N-[1-(5-бром-3-хлорпиридин-2-ил)этил]-2,4-дихлорпиридин-3-карбоксамид, N-[1-(5-бром-3-хлорпиридин-2-ил)этил]-2-фтор-4-йодпиридин-3-карбоксамид, N-{(Е)-[(циклопропилметокси)имино][6-(дифторметокси)-2,3-дифторфенил]метил}-2-фенилацетамид, N-{(Z)-[(циклопропилметокси)имино][6-(дифторметокси)-2,3-дифторфенил]метил}-2-фенилацетамид, N-метил-2-(1-{[5-метил-3-(трифторметил)-1Н-пиразол-1-ил]ацетил}пиперидин-4-ил)-N-(1,2,3,4-тетрагидронафталин-1-ил)-1,3-тиазол-4-карбоксамид, N-метил-2-(1-{[5-метил-3-(трифторметил)-1Н-пиразол-1-ил]ацетил}пиперидин-4-ил)-N-[(1R)-1,2,3,4-тетрагидронафталин-1-ил]-1,3-тиазол-4-карбоксамид, Н-метил-2-(1-{[5-метил-3-(трифторметил)-1 Н-пиразол-1-ил]ацетил} пиперидин-4-ил)-N-[(1S)-1,2,3,4-тетрагидронафталин-1-ил]-1,3-тиазол-4-карбоксамид, пентил {6-[({[(1-метил-1Н-тетразол-5-ил)(фенил)метилиден]амино}окси)метил]пиридин-2-ил}карбамат, феназин-1-карбоновая кислота, хинолин-8-ол и хинолин-8-ол сульфат (2:1),
Все компоненты смесей, упомянутые в классах (1) - (15), могут, если они способны исходя из их функциональных групп, необязательно образовывать соли с пригодными основаниями или кислотами.
(16) Дополнительные соединения, например 1-метил-3-(трифторметил)-N-[2′-(трифторметил)бифенил-2-ил]-1Н-пиразол-4-карбоксамид, N-(4′-хлорбифенил-2-ил)-3-(дифторметил)-1-метил-1Н-пиразол-4-карбоксамид, N-(2′,4′-дихлорбифенил-2-ил)-3-(дифторметил)-1-метил-1Н-пиразол-4-карбоксамид, 3-(дифторметил)-1-метил-N-[4′-(трифторметил)бифенил-2-ил]-1Н-пиразол-4-карбоксамид, N-(2′,5′-дифторбифенил-2-ил)-1-метил-3-(трифторметил)-1Н-пиразол-4-карбоксамид, 3-(дифторметил)-1-метил-N-[4′-(проп-1-ин-1-ил)бифенил-2-ил]-1Н-пиразол-4-карбоксамид, 5-фтор-1,3-диметил-N-[4′-(проп-1-ин-1-ил)бифенил-2-ил]-1Н-пиразол-4-карбоксамид, 2-хлор-N-[4′-(проп-1-ин-1-ил)бифенил-2-ил]пиридин-3-карбоксамид, 3-(дифторметил)-N-[4′-(3,3-диметилбут-1-ин-1-ил)бифенил-2-ил]-1-метил-1Н-пиразол-4-карбоксамид, N-[4′-(3,3-диметилбут-1-ин-1-ил)бифенил-2-ил]-5-фтор-1,3-диметил-1Н-пиразол-4-карбоксамид, 3-(дифторметил)-N-(4′-этинилбифенил-2-ил)-1-метил-1Н-пиразол-4-карбоксамид, N-(4′-этинилбифенил-2-ил)-5-фтор-1,3-диметил-1Н-пиразол-4-карбоксамид, 2-[хлор-N-(4′-этинилбифенил-2-ил)пиридин-3-карбоксамид, 2-хлор-N-[4′-(3,3-диметилбут-1-ин-1-ил)бифенил-2-ил] пиридин-3-карбоксамид, 4-(дифторметил)-2-метил-N-[4′-(трифторметил)бифенил-2-ил]-1,3-тиазол-5-карбоксамид, 5-фтор-N-[4′-(3-гидрокси-3-метилбут-1-ин-1-ил)бифенил-2-ил]-1,3-диметил-1Н-пиразол-4-карбоксамид, 2-хлор-N-[4′-(3-гидрокси-3-метилбут-1-ин-1-ил)бифенил-2-ил]пиридин-3-карбоксамид, 3-(дифторметил)-N-[4′-(3-метокси-3-метилбут-1-ин-1-ил)бифенил-2-ил]-1-метил-1Н-пиразол-4-карбоксамид, 5-фтор-N-[4′-(3-метокси-3-метилбут-1-ин-1-ил)бифенил-2-ил]-1,3-диметил-1Н-пиразол-4-карбоксамид, 2-хлор-N-[4′-(3-метокси-3-метилбут-1-ин-1-ил)бифенил-2-ил]пиридин-3-карбоксамид, (5-бром-2-метокси-4-метилпиридин-3-ил)(2,3,4-триметокси-6-метилфенил)метанон и N-[2-(4-{[3-(4-хлорфенил)проп-2-ин-1-ил]окси}-3-метоксифенил)этил]-N2-(метилсульфонил)валинамид.
Активные соединения, определенные здесь с помощью их общепринятых названий, известны и описываются, например, в справочнике по пестицидам (″The Pesticide Manual″ 14-е изд., British Crop Protection Council 2006), или могут быть найдены в Интернете (например, http://www.alanwood.net/pesticides).
Все компоненты смесей, упомянутые в классах (1)-(16) могут, если они способны исходя из их функциональных групп, необязательно образовывать соли с пригодными основаниями или кислотами.
В заключение, было обнаружено, что новые соединения формулы (I), при хорошей переносимости растениями, благоприятной токсичности в отношении гомеотермных животных и хорошей экологической совместимости, являются пригодными, в частности, для борьбы с животными-вредителями, особенно членистоногими, насекомыми, паукообразными, гельминтами, нематодами и моллюсками, с которыми сталкиваются в сельском хозяйстве, в лесах, при защите хранящихся продуктов и материалов, и в сфере гигиены, или в сфере ветеринарии. Соединения в соответствии с изобретением подобным образом можно применять в сфере ветеринарии, например, для борьбы с эндо- и/или эктопаразитами.
Соединения в соответствии с изобретением могут применяться в качестве средств для борьбы с животными-вредителями, предпочтительно в качестве средств для защиты сельскохозяйственных культур. Они эффективны против вредителей с нормальной чувствительностью и против устойчивых видов, на всех или некоторых стадиях развития.
Соединения в соответствии с изобретением могут быть переведены в общеизвестные составы. В общем, такие составы содержат от 0.01 до 98 мас.% активного соединения, предпочтительно от 0.5 до 90 мас.%.
Соединения в соответствии с изобретением могут присутствовать в их доступных для приобретения составах и в формах применения, полученных из таких составов, также как и в смеси с другими активными соединениями или синергистами. Синергисты представляют собой соединения, которые усиливают действие активных соединений, причем прибавляемому синергисту совершенно необязательно иметь собственную активность.
Содержание активного соединения в формах применения, полученных из доступных для приобретения составов, может варьировать в широких пределах. Концентрация активного соединения в формах нанесения может находиться в диапазоне от 0.00000001 до 95 мас.% активного соединения, предпочтительно от 0.00001 до 1 мас.%. Соединения наносят обычным способом, подходящим для формы применения.
Изобретение может применяться для обработки всех растений и частей растений. Растения в этом контексте подразумевают включающие все растения и популяции растений, такие как желательные и нежелательные дикорастущие растения или культурные растения (включая встречающиеся в природе культурные растения). Культурные растения могут представлять собой растения, доступные традиционными методами бридинга и оптимизации или с помощью биотехнологических и генно-технологических методов, или с помощью комбинаций этих методов, и включают трансгенные растения, а также культивары растений, охраняемые или неохраняемые правами растениеводов-селекционеров. Под частями растений следует понимать все надземные и подземные части и органы растений, такие как побег, лист, цветок и корень, причем примеры включают листья, иголки, стебли, стволы, цветки, плодовые тела, плоды и зерно, а также корни, клубни и корневища. Части растения также включают собранный материал и вегетативный и генеративный материал для размножения, например черенки, клубни, корневища, ростки и семена.
В соответствии с изобретением обработка растений и частей растения активными соединениями осуществляется непосредственно или путем обеспечения их действия на окружающую среду, место распространения или место хранения растений и частей растения обычными методами обработки, например путем окунания, обрызгивания, испарения, аэрозольного орошения, разбрасывания, окрашивания, впрыскивания и, в случае материала для размножения, особенно в случае зерна, также путем нанесения одного или нескольких покрытий.
Как уже упоминалось выше, в соответствии с изобретением можно обрабатывать все растения и их части. В предпочтительном варианте осуществления, обрабатывают дикорастущие виды растений и культивары растений, или те, которые получены традиционными биологическими методами бридинга, такими как скрещивание или слияние протопластов, и их части. В дополнительном предпочтительном варианте осуществления, обрабатывают трансгенные растения и культивары растений, полученные методами генной инженерии, при необходимости в комбинации с обычными методами (генетически модифицированные организмы), и их части. Термины ″части″ или ″части растений″ или ″части растения″ были объяснены выше.
Более предпочтительно, в соответствии с изобретением обрабатывают растения культиваров растений, каждый из которых является доступным для приобретения или находится в использовании. Под культиварами растений следует понимать растения, которые обладают новыми свойствами (″характерными особенностями″) и которые были получены традиционными методами бридинга, мутагенеза или рекомбинантной ДНК. Они могут представлять собой культивары, биотипы и генотипы.
В сфере ветеринарии, то есть в области ветеринарной медицины, активные соединения в соответствии с настоящим изобретением действуют против паразитов-животных, особенно эктопаразитов или эндопаразитов. Термин ″эндопаразиты″ включает, в особенности, гельминты такие как цестоды, нематоды или трематоды, и простейшие животные организмы, такие как кокцидии. Эктопаразиты типично и предпочтительно представляют собой членистоногих, в частности, насекомых, таких как мухи (жалящие и лижущие), паразитические личинки мух, вши, волосяные вши, пухоеды, блохи и т.п.; или акариды, такие как клещи, например твердые клещи или мягкие клещи, или такие как клещи, например, конские клещи, краснотелковые клещи, птичьи клещи и т.п.
Также было обнаружено, что соединения в соответствии с изобретением обладают сильным инсектицидным действием против насекомых, которые разрушают промышленные материалы. Под промышленными материалами в данном контексте подразумевают неодушевленные материалы, предпочтительно, такие как пластмассы, склеивающие вещества, клеи, бумаги и карты, кожу, древесину, продукты переработки древесины и композиции для нанесения покрытия.
Кроме того, комбинации в соответствии с изобретением могут применяться в качестве композиций, предохраняющих от биологического обрастания, отдельно или в комбинациях с другими активными соединениями.
Активные соединения также пригодны для борьбы с животными-вредителями в бытовом секторе, в сфере гигиены и при защите хранящихся продуктов, особенно с насекомыми, паукообразными и клещами, которых обнаруживают в закрытых пространствах, например, в домах, заводских помещениях, офисах, салонах транспортных средств и т.п. Они могут применяться для борьбы с этими вредителями отдельно или в комбинации с другими активными соединениями и вспомогательными веществами в инсектицидных продуктах для домашнего применения. Они эффективны против чувствительных и устойчивых видов, и на всех стадиях развития.
Под растениями следует понимать все виды растений, культивары растений и популяции растений, такие как желательные и нежелательные дикорастущие растения или культурные растения. Культурными растениями, подлежащими обработке в соответствии с изобретением, являются растения, которые встречаются в природе или растения, которые получают традиционными методами бридинга и оптимизации, или с помощью биотехнологических и рекомбинантных методов, или путем комбинирования методов, упомянутых выше. Термин культурные растения, несомненно, также включает трансгенные растения.
Под культиварами растений следует понимать растения, которые обладают новыми свойствами (характерными особенностями) и которые были получены традиционными методиками бридинга, мутагенеза или рекомбинантной ДНК, или их комбинацией. Они могут представлять собой культивары, сорта, био- или генотипы.
Под частями растения подразумевают все части и органы растений, надземные и подземные, такие как побег, лист, цветок и корень, в частности листья, иголки, цветоножки, стебли, цветки, плодовые тела, плоды, зерно, корни, клубни и корневища.
Термин части растения также включает собранный материал и вегетативный и генеративный материал для размножения, например черенки, клубни, корневища, ростки и зерно или семена.
В предпочтительном варианте осуществления, обрабатывают встречающиеся в природе виды растений и культивары растений, или таковые, полученные традиционными методами бридинга и оптимизации (например, скрещиванием или слиянием протопластов), а также их части.
В дополнительном варианте осуществления в соответствии с изобретением, обрабатывают трансгенные растения, полученные методами генной инженерии, при необходимости, в комбинации с обычными методами, и их части.
Способ обработки в соответствии с изобретением предпочтительно используют для генетически модифицированных организмов, таких как, например, растения или части растения.
Генетически модифицированные растения, так называемые трансгенные растения, представляют собой растения, в которых гетерологический ген, был стабильно интегрирован в геном.
Выражение ″гетерологический ген″ по существу означает ген, который обеспечен или собран вне растения, и когда его вводят в ядерный, хлоропластный или митохондриальный геном, это дает новые или улучшенные агрономические или другие свойства трансформированного растения путем экспрессии вызывающего интерес белка или полипептида или путем понижающего регулирования или сайленсинга другого гена(ов), которые присутствуют в растении (используя, например, антисмысловую методику, методику косупрессии или методику РНК-интерференции -РНКи). Гетерологический ген, который расположен в геноме, также называют трансгеном. Трансген, который определяют его специфическим расположением в геноме растения, называют трансформационным или трансгенным событием.
В зависимости от видов растений или культиваров растений, их месторасположения и условий роста (почва, климат, вегетационный период, питание), обработка в соответствии с изобретением также может привести к супераддитивным (″синергетическим″) действиям. Таким образом, например, возможны следующие действия, превышающие действия, которые фактически следовало бы ожидать: уменьшенные нормы внесения и/или расширение спектра активности и/или повышение активности активных соединений и композиций, которые могут применяться в соответствии с изобретением, лучший рост растения, повышенная толерантность к высоким или низким температурам, повышенная толерантность к засухе или к влажности или засоленности почвы, повышенная продуктивность цветения, более легкий сбор урожая, ускоренное созревание, повышенные выходы урожая, более крупные плоды, большая высота растения, более зеленый цвет листьев, более раннее цветение, повышенное качество и/или повышенная пищевая ценность собранных в качестве урожая продуктов, более высокая концентрация сахара в плодах, лучшая стабильность при хранении и/или способность к обработке собранных в качестве урожая продуктов.
При определенных нормах внесения, комбинации активных соединений в соответствии с изобретением также оказывают укрепляющее действие на растения. Соответственно, они также являются пригодными для мобилизации защитной системы растения против нападения нежелательных фитопатогенных грибов и/или микроорганизмов и/или вирусов. Это, при необходимости, может быть одной из причин повышенной активности комбинаций в соответствии с изобретением, например, против грибов. Под веществами, укрепляющими растения (индуцирующими устойчивость), в данном контексте следует понимать те вещества или комбинации веществ, которые способны стимулировать защитную систему растений таким образом, что, в случае инокулирования в будущем нежелательными фитопатогенными грибами и/или микроорганизмами и/или вирусами, обработанные растения демонстрируют значительную степень устойчивости к этим нежелательным фитопатогенным грибам и/или микроорганизмам и/или вирусам. В данном случае, под нежелательными фитопатогенными грибами и/или микроорганизмами и/или вирусами подразумевают фитопатогенные грибы, бактерии и вирусы. Таким образом, вещества в соответствии с изобретением можно использовать для защиты растений от нападения вышеупомянутых патогенов в пределах определенного периода времени после обработки. Период времени, на протяжении которого достигается защита, обычно длится от 1 до 10 дней, предпочтительно от 1 до 7 дней, после обработки растений активными соединениями.
Более того, растения, которые предпочтительно обрабатывают в соответствии с изобретением, являются устойчивыми к одному или нескольким биотическим стрессовым факторам, то есть указанные растения имеют лучшую защиту от животных и микробных вредителей, таких как нематоды, насекомые, клещи, фитопатогенные грибы, бактерии, вирусы и/или вироиды.
В дополнение к растениям и культиварам растений, упомянутым выше, также пригодными для обработки в соответствии с изобретением являются те растения, которые устойчивы к одному или нескольким абиотическим стрессовым факторам.
Абиотические стрессовые условия могут включать, например, засуху, воздействие низкой температуры, воздействие тепла, осмотический стресс, переувлажнение, повышенную засоленность почвы, увеличенное воздействие минералов, воздействие озона, воздействие сильного света, ограниченную доступность азотных питательных веществ, ограниченную доступность фосфорных питательных веществ или исключение тени.
Растения и сорта растений, которые также могут быть обработаны в соответствии с изобретением, представляют собой те растения, которые отличаются характеристиками повышенного урожая. Повышенный урожай этих растений может быть результатом, например, улучшенной физиологии растения, улучшенного роста и развития растения, как например, эффективность использования воды, эффективность удержания воды, улучшенное использование азота, повышенная ассимиляция углерода, улучшенный фотосинтез, повышенная эффективность прорастания и ускоренное созревание. На урожай также может влиять улучшенная структура растения (в стрессовых и нестрессовых условиях), включая раннее цветение, контроль цветения для получения гибридных семян, мощность всходов, размер растения, количество и расстояние стеблевых междоузлий, корневой рост, размер семян, размер плода, размер стручка, количество стручков или колосьев, количество семян в перерасчете на стручок или колос, масса семян, повышенное наполнение семенами, уменьшенное рассредоточение семян, уменьшенное раскрывание стручков и устойчивость к полеганию. Дополнительные характерные особенности в отношении урожая включают состав семян, такой как содержание углеводов, содержание белков, содержание масла и его состав, питательную ценность, уменьшение непитательных соединений, улучшенную способность к обработке и лучшую стабильность при хранении.
Растения, которые можно обрабатывать в соответствии с изобретением представляют собой гибридные растения, которые уже выражают характеристики гетерозиса, или гибридной силы, что приводит обычно к более высокому выходу, мощности, здоровью и устойчивость в отношении биотического и абиотического стресса. Такие растения типично получают путем скрещивания инбредной родительской линии с мужской стерильностью (материнская форма) с другой инбредной родительской линией с мужской фертильностью (отцовская форма). Гибридные семена типично собирают из растений с мужской стерильностью и продают производителям сельскохозяйственной продукции. Растения с мужской стерильностью можно иногда (например, в случае маиса) получать путем обрезания соцветия-метелки (то есть, механического удаления мужских репродуктивных органов или мужских цветков) однако, более типично, мужская стерильность является результатом генетических детерминант в геноме растения. В том случае, и особенно когда семена являются целевым продуктом, который необходимо собрать из гибридных растений, как правило, полезно удостовериться, что мужская фертильность в гибридных растениях, которые содержат генетические детерминанты, которые отвечают за мужскую стерильность, полностью восстановлена. Это можно сделать, удостоверившись, что отцовские формы имеют соответствующие гены-восстановители фертильности, которые способны восстанавливать мужскую фертильность у гибридных растениях, которые содержат генетические детерминанты, отвечающие за мужскую стерильность. Генетические детерминанты, которые отвечают за мужскую стерильность, могут находиться в цитоплазме. Примеры цитоплазматической мужской стерильности (CMS) например, были описаны для вида Brassica. Однако, генетические детерминанты, которые отвечают за мужскую стерильность, также могут находиться в ядерном геноме. Растения с мужской стерильностью также можно получить с помощью методов биотехнологии растений, таких как генная инженерия. Особенно пригодные методы получения растений с мужской стерильностью описаны в WO 89/10396, в которой, например, рибонуклеазы, такие как барназа, селективно экспрессируется в клетках тапетума в тычинках. Затем фертильность можно восстановить путем экспрессии в клетках тапетума ингибитора рибонуклеазы, такого как барстар.
Растения или культивары растений (полученные с помощью методов биотехнологии растений, таких как генная инженерия), которые могут быть обработаны в соответствии с изобретением, являются толерантными к гербицидам растениями, то есть растениями, которым придали толерантность к одному или нескольким данным гербицидам. Такие растения можно получить либо путем генетической трансформации, или путем селекции растений, содержащих мутацию, придающую такую толерантность к гербицидам.
Толерантными к гербицидам растениями являются, например, толерантные к глифосатам растения, то есть растениями, которым придали толерантность к гербициду глифосату или его соли. Например, толерантные к глифосату растения можно получить путем трансформации растения геном, который кодирует фермент 5-енолпирувилшикимат-3-фосфат синтазу (EPSPS). Примерами таких генов EPSPS являются ген AroA (мутант СТ7) бактерии Salmonella typhimurium, ген СР4 бактерии Agrobacterium sp., гены, кодирующие EPSPS петунии, EPSPS томата, или EPSPS коракана. EPSPS также может быть мутированным. Толерантные к глифосату растения также можно получить путем экспрессии гена, который кодирует фермент глифосат-оксидоредуктазу. Толерантные к глифосату растения также можно получить путем экспрессии гена, который кодирует фермент глифосат-ацетилтрансферазу. Толерантные к глифосату растения также можно получить путем селекции растений, содержащих природные мутации вышеупомянутых генов.
Другими, устойчивыми к гербицидам растениями, являются, например, растения, которым придали толерантность к гербицидам, которые ингибируют фермент глутамин-синтазу, таким как биалафос, фосфинотрицин или глуфосинат. Такие растения можно получить путем экспрессии фермента, детоксифицирующего гербицид, или мутантного фермента глутамин-синтазы, который является устойчивым к ингибированию. Одним таким эффективным детоксифицирующим ферментом является фермент, который кодирует фосфинотрицин-ацетилтрансферазу (такой как белок bar или pat из вида Streptomyces). Растения, экспрессирующие экзогенную фосфинотрицин-ацетилтрансферазу уже были описаны.
Дополнительными толерантными к гербицидам растениями также являются растения, которым придали толерантность к гербицидам, которые ингибируют фермент гидроксифенилпируватдиоксигеназу (HPPD). Гидроксифенилпируватдиоксигеназы являются ферментами, которые катализируют реакцию, в которой пара-гидроксифенилпируват (НРР) превращается в гомогентизат. Растения, толерантные к ингибиторам HPPD могут быть трансформированы геном, который кодирует природный устойчивый фермент HPPD, или геном, который кодирует мутированный фермент HPPD. Толерантность к ингибиторам HPPD также можно получить с помощью трансформации растений генами, которые кодирует определенные ферменты, позволяющие образование гомогентизата не смотря на ингибирование нативного фермента HPPD ингибитором HPPD. Толерантность растений к ингибиторам HPPD можно также улучшить путем трансформации растений геном, который кодирует фермента префенатдегидрогеназу в дополнение к гену, который кодирует HPPD-толерантный фермент.
Еще дополнительными устойчивыми к гербицидам растениями являются растения, которым придали толерантность к ингибиторам ацетолактатсинтазы (ALS). Известные ингибиторы ALS включают, например, гербициды - производные сульфонилмочевины, имидазолинона, триазолопиримидина, пиримидинилокси(тио)бензоата и/или сульфониламинокарбонилтриазолинона. Известно, что различные мутации в ферменте ALS (также известном как ацетогидроксикислотная синтаза, AHAS) придают толерантность к различным гербицидам и группам гербицидов. Получение толерантных к сульфонилмочевине растений и толерантных к имидазолинону растений описано в международной публикации WO 1996/033270. Дополнительные толерантные к сульфонилмочевине и имидазолинону растения также были описаны, например, в WO 2007/024782.
Другие растения, толерантные к имидазолинону и/или сульфонилмочевине можно получить путем индуцированного мутагенеза, селекции в культурах клеток в присутствии гербицида или мутационного бридинга.
Растения или культивары растений (полученные с помощью методов биотехнологии растений, таких как генная инженерия), которые также могут быть обработаны в соответствии с изобретением, являются устойчивыми к насекомым трансгенными растениями, то есть растениями, которым придали устойчивость к нападению определенных целевых насекомых. Такие растения можно получить путем генетической трансформации, или путем селекции растений, содержащих мутацию, которая придает такую устойчивость к насекомым.
В данном контексте ″устойчивое к насекомым трансгенное растение″, включает любое растение, содержащее по меньшей мере один трансген, содержащий кодирующую последовательность, которая кодирует:
1) инсектицидный кристаллический белок из Bacillus thuringiensis или его инсектицидную часть, такой как инсектицидные кристаллические белки, описанные онлайн на: http://www.lifesci.sussex.ac.uk/Home/Neil_Crickmore/Bt/, или их инсектицидные части, например, белки классов Cry-белков Cry1Ab, Cry1Ac, Cry1F, Cry2Ab, Cry3Ae, или Cry3Bb, или их инсектицидные части; или
2) кристаллический белок из Bacillus thuringiensis или его часть, который является инсектицидным в присутствии второго, другого кристаллического белка из Bacillus thuringiensis или его части, такой как бинарный токсин, состоящий из кристаллических белков Cry34 и Cry35; или
3) гибридный инсектицидный белок, содержащий части двух разных инсектицидных кристаллических белков из Bacillus thuringiensis, такой как гибрид белков 1), указанных выше, или гибрид белков 2), указанных выше, например, белок Cry1A.105, который продуцируется событием маиса MON89034 (WO 2007/027777); или
4) любой один из вышеуказанных белков 1)-3), в котором несколько, в частности от 1 до 10, аминокислот заменены на другую аминокислоту для получения более высокой инсектицидной активности по отношению к целевым видам насекомых, и/или для расширения диапазона поражаемых целевых видов насекомых, и/или в результате изменений, внесенных в кодирующую ДНК при клонировании или трансформации, такой как белок Cry3Bb 1 в событиях маиса MON863 или MON88017, или белок Cry3A в событии маиса MIR604; или
5) инсектицидный секретируемый белок из Bacillus thuringiensis или Bacillus cereus, или его инсектицидная часть, такой как вегетативные инсектицидные белки (VIP) перечисленные в: http://www.lifesci.sussex.ac.uk/Home/Neil_Crickmore/Bt/vip.html, например, белки из класса белков VIP3Aa; или
6) секретируемый белок из Bacillus thuringiensis или Bacillus cereus, который является инсектицидным в присутствии второго секретируемого белка из Bacillus thuringiensis или В. cereus, такой как бинарный токсин, состоящий из кристаллических белков VIP1A и VIP2A;
7) гибридный инсектицидный белок, содержащий части из различных секретируемых белков из Bacillus thuringiensis или Bacillus cereus, такой как гибрид вышеуказанных белков 1) или гибрид вышеуказанных белков 2); или
8) любой один из вышеуказанных белков 1)-3), в котором несколько, в частности от 1 до 10, аминокислот заменены на другую аминокислоту для получения более высокой инсектицидной активности по отношению к целевым видам насекомых, и/или для расширения диапазона поражаемых целевых видов насекомых, и/или в результате изменений, внесенных в кодирующую ДНК при клонировании или трансформации (несмотря на то, что она все еще кодирует инсектицидный белок), такой как белок VIP3Aa в событии хлопчатника СОТ102.
Конечно, устойчивое к насекомым трансгенное растение, в данном контексте, также включает любое растение, содержащее комбинацию генов, которые кодируют белки какого-либо из вышеуказанных классов 1-8. В одном варианте осуществления, устойчивое к насекомым растение содержит более одного трансгена, который кодирует белок какого-либо из вышеуказанных классов 1-8, для расширения диапазона поражаемых целевых видов насекомых, или для задержки развития устойчивости насекомых к растениям, используя различные белки, инсектицидные в отношении одних и тех же целевых видов насекомых, но имеющие разный способ действия, например, связывание с различными рецептор-связывающими сайтами у насекомых.
Растения или культивары растений (полученные с помощью методов биотехнологии растений, таких как генная инженерия), которые также могут быть обработаны в соответствии с изобретением, являются толерантными к абиотическому стрессу. Такие растения можно получить путем генетической трансформации, или путем селекции растений, содержащих мутацию, которая придает такую стрессоустойчивость. Особенно пригодные стрессотолерантные растения включают:
а. растения, которые содержат трансген, способный уменьшать экспрессию и/или активность гена поли(АДФ-рибозо)полимеразы (PARP) в растительных клетках или растениях;
b. растения, которые содержат усиливающий стрессотолерантность трансген, способный уменьшать экспрессию и/или активность PARG-кодирующих генов растений или растительных клеток;
с. растения, которые содержат усиливающий стрессотолерантность трансген, который кодирует функционально важный для растений фермент метаболического пути восстановительного синтеза никотинамидадениндинуклеотида, включая никотинамидазу, никотинатфосфорибозилтрансферазу, (никотиновая кислота)мононуклеотидаденилтрансферазу, никотинамидадениндинуклеотидсинтетазу или никотинамидфосфорибозилтрансферазу.
Растения или сорта растений (полученные с помощью методов биотехнологии растений, таких как генная инженерия), которые также могут быть обработаны в соответствии с изобретением, демонстрируют измененные количество, качество и/или стабильность при хранении собранных в качестве урожая продуктов и/или измененные свойства специфических ингредиентов собранных в качестве урожая продуктов, такие как, например:
1) трансгенные растения, которые синтезируют модифицированный крахмал, который по своим физико-химическим характеристикам, в частности по содержанию амилозы или по соотношению амилоза/амилопектин, по степени разветвленности, по средней величине длины цепи, по распределению боковых цепей, по характеристике вязкости, по силе гелеобразования, по размеру крахмальных зерен и/или морфологии зерен крахмала, изменен по сравнению с крахмалом, синтезированным в растительных клетках или растениях дикорастущего типа, так, что он больше подходит для специальных применений.
2) трансгенные растения, которые синтезируют некрахмальные углеводные полимеры или которые синтезируют некрахмальные углеводные полимеры с измененными свойствами по сравнению с растениями дикорастущего типа без генетической модификации. Примерами являются растения, которые продуцируют полифруктозу, особенно инулин- и леван-типа, растения, которые продуцируют альфа-1,4-глюканы, растения, которые продуцируют альфа-1,6-разветвленные альфа-1,4-глюканы, и растения, которые продуцируют альтернан.
3) трансгенные растения, которые продуцируют гиалуронан.
Растениями или культиварами растений (полученными с помощью методов биотехнологии растений, таких как генная инженерия), которые также могут быть обработаны в соответствии с изобретением, являются растения, такие как хлопчатники, с измененными характеристиками волокон. Такие растения можно получить путем генетической трансформации, или путем селекции растений, содержащих мутацию, которая придает такие измененные характеристики волокон и включают:
a) растения, такие как хлопчатник, содержащий измененную форму генов целлюлозосинтазы;
b) растения, такие как хлопчатник, содержащий измененную форму rsw2 или rsw3 гомологичных нуклеиновых кислот;
c) растения, такие как хлопчатник, с повышенной экспрессией сахарозофосфатсинтазы;
d) растения, такие как хлопчатник, с повышенной экспрессией сахарозосинтазы;
e) растения, такие как хлопчатник, у которых регулировка по времени проницаемости плазмодесмы у основания клетки волокна изменена, например посредством понижающей регуляции волокно-селективной β-1,3-глюканазы;
f) растения, такие как хлопчатник, которые имеют волокна с измененной реакционной способностью, например из-за экспрессии гена N-ацетилглюкозаминтрансферазы, включая гены nodC и хитинсинтазы.
Растениями или культиварами растений (которые могут быть получены с помощью методов биотехнологии растений, таких как генная инженерия), которые также могут быть обработаны в соответствии с изобретением, являются растения, такие как масличный рапс или родственные растения Brassica, с измененные характеристики профиля масел. Такие растения можно получить путем генетической трансформации, или путем селекции растений, содержащих мутацию, которая придает такие измененные характеристики профиля масел и включают:
a) растения, такие как растения масличного рапса, которые производят масло с высоким содержанием олеиновой кислоты;
b) растения, такие как растения масличного рапса, которые производят масло с низким содержанием линоленовой кислоты;
c) растения, такие как растения масличного рапса, производящие масло с низким уровнем насыщенных жирных кислот.
Особенно пригодными трансгенными растениями, которые могут быть обработаны в соответствии с изобретением, являются растения, которые содержат один или несколько генов, которые кодируют один или несколько токсинов, и представляют собой трансгенные растения, которые доступны под следующими торговыми наименованиями: YIELD GARD® (например, маис, хлопчатник, соя культурная), KnockOut® (например, маис), BiteGard® (например, маис), BT-Xtra® (например, маис), StarLink® (например, маис), Bollgard® (хлопчатник), Nucotn® (хлопчатник), Nucotn 33B® (хлопчатник), NatureGard® (например, маис), Protecta® и NewLeaf® (картофель). Примерами толерантных к гербицидам растений, которые следует упомянуть, являются сорта маиса, сорта хлопчатника и сорта сои культурной, которые доступны под следующими торговыми наименованиями: Roundup Ready® (толерантность к глифосату, например маис, хлопчатник, соя культурная). Liberty Link® (толерантность к фосфинотрицину, например масличный pane), IMI® (толерантность к имидазолинону) и SCS® (толерантность к сульфонилмочевине, например маис). Устойчивые к гербицидам растения (растения, выведенные обычным способом для толерантности к гербицидам), которые могут быть упомянуты, включают сорта, которые доступны под наименованием deal-field® (например, маис).
Особенно пригодными трансгенными растениями, которые могут быть обработаны в соответствии с изобретением, являются растения, содержащие трансформационные события, или комбинацию трансформационных событий, и которые перечислены, например, в базах данных различных национальных или региональных органов государственного регулирования (см., например, http://gmoinfo.jrc.it/gmp_browse.aspx и http://www.agbios.com/dbase.php).
Обработку в соответствии с изобретением растений и частей растения комбинацией активных соединений проводят непосредственно или путем обеспечения действия соединений на их окружающую среду, место произрастания или место хранения обычными методами обработки, например путем окунания, обрызгивания, испарения, аэрозольного орошения, разбрасывания, окрашивания и, в случае материала для размножения, в частности, в случае зерна, также путем нанесения одного или нескольких покрытий.
Смеси в соответствии с изобретением особенно пригодны для обработки семян. Здесь, в качестве предпочтительных или особенно предпочтительных, отдельно можно упомянуть комбинации в соответствии с изобретением, упомянутые выше. Таким образом, большая часть повреждения культурных растений, которое вызывается вредителями, возникает еще при инвазии семян во время хранения и после внесения семян в почву, а также во время и непосредственно после прорастания растений. Эта фаза является особенно важной, так как корни и побеги растущего растения являются особенно чувствительными и даже незначительное повреждение может привести к гибели всего растения. В связи с этим представляет особенно большой интерес защита семян и прорастающих растений с помощью применения пригодных композиций.
Борьба с вредителями путем обработки семян растений известна уже давно и является объектом постоянных улучшений. Однако, обработка семян влечет за собой ряд проблем, которые не всегда можно решить удовлетворительным образом. Таким образом, является желательной разработка способов защиты семян и прорастающих растений, которые обходятся без дополнительного нанесения композиций для защиты сельскохозяйственных культур после посева или после появления всходов растений. Кроме того желательно оптимизировать количества используемого активного соединения таким образом, чтобы обеспечить оптимальную защиту семян и прорастающих растений от нападения вредителей, но без повреждения самого растения используемым активным соединением. В частности, способы обработки семян должны также учитывать собственные инсектицидные свойства трансгенных растений в целях достижения оптимальной защиты семян и прорастающих растений при использовании минимального количества композиций для защиты сельскохозяйственных культур.
Следовательно, настоящее изобретение, в частности, также относится к способу защиты семян и прорастающих растений от нападения вредителей путем обработки семян композицией в соответствии с изобретением. Изобретение подобным образом относится к применению композиций в соответствии с изобретением для обработки семян для защиты семян и вырастающих из них растений от вредителей. Изобретение далее относится к семенам, которые обработаны композицией в соответствии с изобретением для защиты от вредителей.
Одним из преимуществ настоящего изобретения является то, что особые системные свойства композиций в соответствии с изобретением предполагают, что обработка семян этими композициями защищает от вредителей не только сами семена, а и получающиеся после прорастания растения. Таким путем, можно обойтись без непосредственной обработки культуры во время посева или вскоре после него.
Еще одним преимуществом является синергетически увеличенная инсектицидная активность композиций в соответствии с изобретением по сравнению с отдельным инсектицидно активным соединением, которая превышает ожидаемую активность двух активных соединений при их нанесении по отдельности. Также выгодным является синергетическое повышение фунгицидной активности композиций в соответствии с изобретением по сравнению с отдельным фунгицидно активным соединением, которая превышает ожидаемую активность активного соединения, нанесенного отдельно. Это делает возможной оптимизацию количества используемых активных соединений.
Кроме того, должно быть рассмотрено в качестве полезного то, что смеси в соответствии с изобретением, в частности, также можно использовать для обработки трансгенных семян, где растения, появляющиеся из этих семян, способны экспрессировать белок, направленный против вредителей. Путем обработки таких семян композициями в соответствии с изобретением, с определенными вредителями можно вести борьбу только с помощью экспрессии, например, инсектицидного белка, а повреждение семян может быть дополнительно предотвращено с помощью композиций в соответствии с изобретением.
Композиции в соответствии с изобретением являются пригодными для защиты семян любого сорта растений, как уже упоминалось выше, которые находят применение в сельском хозяйстве, в теплицах, в лесах или в садоводстве. В частности, такими семенами являются семена маиса, арахиса, канолы, масличного рапса, мака, сои культурной, хлопчатника, свеклы (например, сахарной свеклы и кормовой свеклы), риса, проса, пшеницы, ячменя, овса, ржи, подсолнечника, табака, картофеля или овощей (например, виды томатов, кочанной капусты). Композиции в соответствии с изобретением подобным образом пригодны для обработки семян плодовых растений и овощей, как уже упоминалось выше. Обработка семян маиса, сои культурной, хлопчатника, пшеницы и канолы или масличного рапса является особенно важной.
Как уже упоминалось выше, обработка трансгенных семян композицией в соответствии с изобретением также имеет особое значение. Такими семенами являются семена растений, которые, как правило, содержат по меньшей мере один гетерологический ген, который управляет экспрессией полипептида, в частности, с инсектицидными свойствами. В этом контексте, гетерологические гены в трансгенных семенах могут быть получены из микроорганизмов, таких как Bacillus, Rhizobium, Pseudomonas, Serratia, Trichoderma, Clavibacter, Glomus или Gliocladium. Настоящее изобретение особенно пригодно для обработки трансгенных семян, которые содержат по меньшей мере один гетерологический ген, происходящих из Bacillus sp., и чей генный продукт проявляет активность против мотылька кукурузного и/или блошки длинноусой. Вовлеченным геном более предпочтительно является гетерологический ген, который происходит из Bacillus thuringiensis.
В контексте настоящего изобретения, композиции в соответствии с изобретением наносят на семена либо сами по себе, либо в пригодном составе. Предпочтительно, семена обрабатывают в состоянии, в котором они достаточно стабильны, чтобы избежать повреждения во время обработки. В общем, семена могут быть обработаны в любой момент времени между сбором урожая и посевом. Семена обычно используются в отделенном от растения виде и свободными от початков, зерновых оболочек, цветоножек, кожуры, ворсинок или мякоти плодов.
Обычно, при обработке семян должно быть обеспечено, чтобы количество композиции в соответствии с изобретением, наносимое на семена, и/или количество дополнительных добавок было таким, которое не приводит к нарушению прорастания семян или повреждению получающихся растений. Это должно быть обеспечено особенно в случае активных соединений, которые могут проявлять фитотоксическое действие при определенных нормах внесения.
Кроме того, соединения в соответствии с изобретением могут применяться для борьбы с множеством различных вредителей, включая, например, вредных сосущих насекомых, жалящих насекомых и других вредителей, которые являются паразитами растений, вредителями хранимых материалов, вредителями, которые разрушают промышленные материалы, и вредителями в области гигиены, включая паразитов в сфере ветеринарии, например, для их уничтожения и ликвидации. Таким образом, настоящее изобретение также включает способы борьбы с вредителями.
В сфере ветеринарии, то есть в области ветеринарной медицины, активные соединения в соответствии с настоящим изобретением действуют против паразитов-животных, особенно эктопаразитов или эндопаразитов. Термин ″эндопаразиты″ включает, в частности, гельминты, такие как цестоды, нематоды или трематоды, и простейшие животные организмы, такие как кокцидии. Эктопаразиты обычно и предпочтительно представляют собой членистоногих, особенно насекомых, таких как мухи (жалящие и лижущих), паразитические личинки мух, вши, волосяные вши, пухоеды, блохи и т.п.; или акарициды, такие как клещи, например твердые клещи или мягкие клещи, или клещи, такие как клещи конские, краснотелковые клещи, птичьи клещи и т.п.
Эти паразиты включают:
Из отряда Anoplurida, например, Haematopinus spp., Linognathus spp., Pediculus spp., Phthirus spp.и Solenopotes spp.; особыми примерами являются: Linognathus setosus, Linognathus vituli, Linognathus ovillus, Linognathus oviformis, Linognathus pedalis, Linognathus stenopsis, Haematopinus asini macrocephalus, Haematopinus eurystemus, Haematopinus suis, Pediculus humanus capitis, Pediculus humanus corporis, Phylloera vastatrix, Phthirus pubis, Solenopotes capillatus;
Из отряда Mallophagida и подотрядов Amblycerina и Ischnocerina, например, Trimenopon spp., Menopon spp., Trinoton spp., Bovicola spp., Wemeckiella spp., Lepikentron spp., Damalina spp., Trichodectes spp.и Felicola spp.; особыми примерами являются: Bovicola bovis, Bovicola ovis, Bovicola limbata, Damalina bovis, Trichodectes canis, Felicola subrostratus, Bovicola caprae, Lepikentron ovis, Wemeckiella equi;
Из отряда Diptera и подотрядов Nematocerina и Brachycerina, например, Aedes spp., Anopheles spp., Culex spp., Simulium spp., Eusimulium spp., Phlebotomus spp., Lutzomyia spp., Culicoides spp., Chrysops spp., Odagmia spp., Wilhelmia spp., Hybomitra spp., Atylotus spp., Tabanus spp., Haematopota spp., Philipomyia spp., Braula spp., Musca spp., Hydrotaea spp., Stomoxys spp., Haematobia spp., Morellia spp., Fannia spp., Glossina spp., Calliphora spp., Lucilia spp., Chrysomyia spp., Wohlfahrtia spp., Sarcophaga spp.. Oestrus spp., Hypoderma spp., Gasterophilus spp., Hippobosca spp., Lipoptena spp., Melophagus spp., Rhinoestrus spp., Tipula spp.; особыми примерами являются: Aedes aegypti, Aedes albopictus, Aedes taeniorhynchus. Anopheles gambiae. Anopheles maculipennis, Calliphora erythrocephala, Chrysozona pluvialis, Culex quinquefasciatus, Culex pipiens, Culex tarsalis, Fannia canicularis, Sarcophaga camaria, Stomoxys calcitrans, Tipula paludosa, Lucilia cuprina, Lucilia sericata, Simulium reptans, Phlebotomus papatasi, Phlebotomus longipalpis, Odagmia omata, Wilhelmia equina, Boophthora erythrocephala, Tabanus bromius, Tabanus spodopterus, Tabanus atratus, Tabanus sudeticus, Hybomitra ciurea, Chrysops caecutiens, Chrysops relictus, Haematopota pluvialis, Haematopota italica, Musca autumnalis, Musca domestica, Haematobia irritans irritans, Haematobia irritans exigua, Haematobia stimulans, Hydrotaea irritans, Hydrotaea albipuncta, Chrysomya chloropyga, Chrysomya bezziana, Oestrus ovis, Hypoderma bovis, Hypoderma lineatum, Przhevalskiana silenus, Dermatobia hominis, Melophagus ovinus, Lipoptena capreoli, Lipoptena cervi, Hippobosca variegata, Hippobosca equina, Gasterophilus intestinalis, Gasterophilus haemorroidalis, Gasterophilus inermis, Gasterophilus nasalis, Gasterophilus nigricomis, Gasterophilus pecorum, Braula coeca;
Из отряда Siphonapterida, например Pulex spp., Ctenocephalides spp., Tunga spp., Xenopsylla spp., Ceratophyllus spp.; особыми примерами являются: Ctenocephalides canis, Ctenocephalides felis, Pulex irritans, Tunga penetrans, Xenopsylla cheopis;
Из отряда Heteropterida, например, Cimex spp., Triatoma spp., Rhodnius spp. и Panstrongylus spp.
Из отряда Blattarida, например Blatta orientalis, Periplaneta americana, Blattela germanica и Supella spp.(например, Suppella longipalpa);
Из подкласса Acari (Acarina) и отрядов Meta- и Mesostigmata, например, Argas spp., Omithodorus spp., Otobius spp., Ixodes spp., Amblyomma spp., Rhipicephalus (Boophilus) spp., Dermacentor spp., Haemophysalis spp., Hyalomma spp., Dermanyssus spp., Rhipicephalus spp.(исходный род клещей, паразитирующих на многих хозяевах), Omithonyssus spp., Pneumonyssus spp., Raillietia spp., Pneumonyssus spp., Stemostoma spp., Varroa spp., Acarapis spp.; особыми примерами являются: Argas persicus, Argas reflexus, Omithodorus moubata, Otobius megnini, Rhipicephalus (Boophilus) microplus, Rhipicephalus (Boophilus) decoloratus, Rhipicephalus (Boophilus) annulatus, Rhipicephalus (Boophilus) calceratus, Hyalomma anatolicum, Hyalomma aegypticum, Hyalomma marginatum, Hyalomma transiens, Rhipicephalus evertsi, Ixodes ricinus, Ixodes hexagonus, Ixodes canisuga, Ixodes pilosus, Ixodes rubicundus, Ixodes scapularis, Ixodes holocyclus, Haemaphysalis concinna, Haemaphysalis punctata, Haemaphysalis cinnabarina, Haemaphysalis otophila, Haemaphysalis leachi, Haemaphysalis longicomi, Dermacentor marginatus, Dermacentor reticulatus, Dermacentor pictus, Dermacentor albipictus, Dermacentor andersoni, Dermacentor variabilis, Hyalomma mauritanicum, Rhipicephalus sanguineus, Rhipicephalus bursa, Rhipicephalus appendiculatus, Rhipicephalus capensis, Rhipicephalus turanicus, Rhipicephalus zambeziensis, Amblyomma americanum, Amblyomma variegatum, Amblyomma maculatum, Amblyomma hebraeum, Amblyomma cajennense, Dermanyssus gallinae, Omithonyssus bursa, Omithonyssus sylviarum, Varroa jacobsoni;
Из отряда Actinedida (Prostigmata) и Acaridida (Astigmata), например, Acarapis spp., Cheyletiella spp., Omithocheyletia spp., Myobia spp., Psorergates spp., Demodex spp., Trombicula spp., Listrophorus spp., Acarus spp., Tyrophagus spp., Caloglyphus spp., Hypodectes spp., Pterolichus spp., Psoroptes spp., Chorioptes spp., Otodectes spp., Sarcoptes spp., Notoedres spp., Knemidocoptes spp., Cytodites spp.и Laminosioptes spp.; особыми примерами являются: Cheyletiella yasguri, Cheyletiella blakei, Demodex canis, Demodex bovis, Demodex ovis, Demodex caprae, Demodex equi, Demodex caballi, Demodex suis, Neotrombicula autumnalis, Neotrombicula desaleri, Neoschongastia xerothermobia, Trombicula akamushi, Otodectes cynotis, Notoedres cati, Sarcoptis canis, Sarcoptes bovis, Sarcoptes ovis, Sarcoptes rupicaprae (=S. caprae), Sarcoptes equi, Sarcoptes suis, Psoroptes ovis, Psoroptes cuniculi, Psoroptes equi, Chorioptes bovis, Psoergates ovis, Pneumonyssoidic mange, Pneumonyssoides caninum, Acarapis woodi.
Активные соединения в соответствии с изобретением также пригодны для борьбы с членистоногими, гельминтами и простейшими животными организмами, которые нападают на животных. Животные включают сельскохозяйственных животных, например крупный рогатый скот, овец, коз, лошадей, свиней, ослов, верблюдов, буйволов, кроликов, кур, индеек, уток, гусей, выращиваемую рыбу, медоносных пчел. Животные также включают домашних животных - также называемых животными-компаньонами - например, собак, кошек, птиц клеточного содержания, аквариумную рыбу, а также животных, которые известны в качестве подопытных животных, например хомяков, морских свинок, крыс и мышей.
Борьба с этими членистоногими, гельминтами и/или простейшими животными организмами должна уменьшить случаи смерти и повысить производительность (получение мяса, молока, шерсти, шкур, яиц, меда и т.д.), и улучшить здоровье животного-хозяина, и, следовательно, применение активных соединений в соответствии с изобретением дает возможность достичь более экономически обоснованного и простого животноводства.
Например, желательно предотвращать или прерывать потребление паразитами крови хозяина (при необходимости). Борьба с паразитами также может способствовать предотвращению переноса инфекционных субстанций.
Термин ″борьба″ в данном контексте в отношении ветеринарии, означает, что активные соединения действуют, уменьшая проявления рассматриваемого паразита у животного, инвазированного такими паразитами, до безопасного уровня. Более конкретно, ″борьба″ в данном контексте означает, что активное соединение уничтожает рассматриваемого паразита, замедляет его рост или подавляет его размножение.
В общем, активные соединения в соответствии с изобретением, когда их используют для лечения животных, можно использовать непосредственно. Их предпочтительно применяют в виде фармацевтических композиций, которые могут содержать фармацевтически приемлемые наполнители и/или вспомогательные вещества, известные в уровне техники.
В сфере ветеринарии и в животноводстве, активные соединения используют (вводят) известным способом путем энтерального введения в форме, например, таблеток, капсул, питья, препаратов для вливания, гранул, паст, шариков, препаратов для введения через зонд и суппозиториев, с помощью парентерального введения, например путем инъекции (среди прочего, внутримышечной, подкожной, внутривенной, внутрибрюшинной), имплантов, с помощью назального введения, накожного применения в форме, например, окунания или купания, обрызгивания, обливания и точечного нанесения, мытья и опудривание, а также с помощью формованных изделий, содержащих активное соединение, таких как ошейники, бирки на уши, бирки на хвост, повязки на конечности, недоуздки, маркировочные устройства, и т.д. Активные соединения могут быть составлены в виде шампуня или в виде пригодных составов, применяемых в аэрозолях или спреях, не находящихся под давлением, например в пульверизаторах и распыльтелях.
В случае использования для домашнего скота, домашней птицы, домашних питомецев и т.д., активные соединения в соответствии с изобретением можно использовать в виде составов (например, порошков, смачиваемых порошков [″WP″], эмульсий, эмульгируемых концентратов [″ЕС″], сыпучих композиций, гомогенных растворов и концентратов суспензий [″SC″]), которые содержат активные соединения в количестве от 1 до 80 мас.%, непосредственно или после разбавления (например, 100-10000-кратного разбавления), или они могут применяться в виде химического ванны.
В случае прменения в области ветеринарии, активные соединения в соответствии с изобретением можно применять в комбинации с пригодными синергистами или другими активными соединениями, например акарицидами, инсектицидами, антигельминтиками, противопротозойными средствами.
Соединения в соответствии с изобретением можно получить с помощью обычных методов, известных специалистам в данной области техники.
Схема реакции 1 показывает общий способ получения А соединений (I) в соответствии с изобретением.
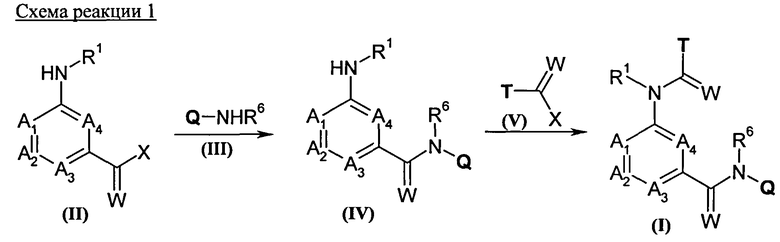
Радикалы A1-A4, Q, W, R1 и R6 имеют значения, описанные выше. Т означает группу
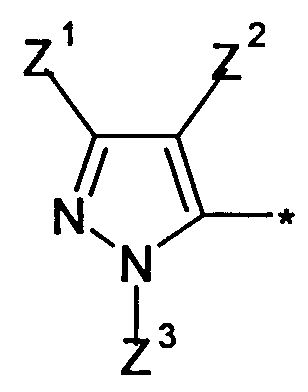
где радикалы Z1, Z2 и Z3 имеют значение, приведенное выше, и звездочка означает точку присоединения к группе C=W. X означает любую уходящую группу.
Соединения в соответствии с изобретением типа (I) могут быть получены по реакции аминов общей структуры (IV) с активированными производными карбоновой кислоты общей структуры (V). Реакцию можно проводить в присутствии или отсутствии растворителя. На этой стадии, также возможно использование пригодного основания.
В общем, целесообразно проводить первую стадию реакции способа получения А в соответствии с изобретением, при необходимости, в присутствии пригодного разбавителя и, при необходимости, в присутствии пригодного основного вещества, способствующего реакции.
Разбавители преимущественно используют в таком количестве, что реакционная смесь остается легко перемешиваемой в течение всего процесса.
Пригодными для применения в качестве растворителя являются любые растворители, которые не препятствуют реакции, такие как, например, вода. Пригодными являются ароматические углеводороды, такие как бензол или толуол; галогенированные углеводороды, такие как дихлорметан, хлороформ или четыреххлористый углерод, простые эфиры с открытой цепью или циклические, такие как диэтиловый эфир, диоксан, тетрагидрофуран или 1,2-диметоксиэтан; сложные эфиры, такие как этилацетат и бутилацетат; кетоны, такие как, например, ацетон, метилизобутилкетон и циклогексанон; амиды, такие как диметилформамид и диметилацетамид; нитрилы, такие как ацетонитрил; и другие инертные растворители, такие как 1,3-диметил-2-имидазолидинон; растворители можно использовать отдельно или в виде комбинации двух или нескольких растворителей.
Используемое основание может быть органическим основанием, таким как триэтиламин, этилдиизопропиламин, три-н-бутиламин, пиридин и 4-диметиламинопиридин; кроме того, возможно применение, например, следующих оснований: гидроксиды щелочных металлов, такие как, например, гидроксид натрия и гидроксид калия; карбонаты, такие как бикарбонат натрия и карбонат калия; фосфаты, такие как гидроортофосфат калия и ортофосфат натрия; гидриды щелочных металлов, такие как гидрид натрия; алкоголяты щелочных металлов, такие как метилат натрия и этилат натрия. Эти основания можно использовать относительно соединений (IV) и (V) при соотношениях их молярных эквивалентов от 0.01 до 5.0. Кроме того, также возможно применение цианида серебра(1) в качестве основания и активатора [Journal of Organic Chemistry. 1992, 57, 4394-4400; Journal of Medicinal Chemistry 1992, 35, 3905-3918; Journal of Organic Chemistry 2003, 68, 1843-1851].
Пригодная температура реакций находится в диапазоне от -20°С до температуры кипения рассматриваемого растворителя, а время реакций составляет от нескольких минут до 96 часов, в зависимости от выбранных реагентов, растворителей и температуры реакций.
Циклические карбонилгалогениды, представленные общей структурой (V), могут быть получены простым способом по реакции гетероциклической карбоновой кислоты с галогенирующими реагентами, такими как тионилхлорид, тионилбромид, фосфорилхлорид, оксалилхлорид, трихлорид фосфора, и т.д. [Houben-Weyl, 1952, т.VIII, с.463 и след.].
Однако, получение карбоксамидов, представленных формулой (I), также можно проводить с использованием реагентов сочетания, таких как дициклогексилкарбодиимид, и добавок, таких как 1-гидроксибензотриазол [Chem. Вег.1970, 788]. Также возможно применение реагентов сочетания, таких как 1-этил-3-(3-диметиламинопропил)карбодиимид, 1,1′-карбонил-1Н-имидазол и подобных соединений.
Реагентами сочетания, используемыми для выполнения способа получения, являются все реагенты, которые пригодны для образования сложноэфирной или амидной связи (ср., например, Bodansky и др., Peptide Synthesis, 2-е изд., Wiley & Sons, Нью-Йорк, 1976; Gross, Meienhofer, The Peptide: Analysis, Synthesis, Biology, Academic Press, Нью-Йорк, 1979).
Кроме того, для получения (1)также возможно применение смешанных ангидридов [J. Am. Chem. Soc 1967, 5012]. В этом способе, возможно применение различных сложных эфиров хлормуравьиной кислоты, например, изобутилхлороформиата, изопропилхлороформиата. Подобным образом для этой цели возможно применение диэтилацетилхлорида, триметилацетилхлорида и т.п.
Соединения общей структуры (IV) могут быть получены по реакции амина общей структуры (III) с активированными производными карбоновой кислоты общей структуры (II). Здесь, такие же условия, как и при получении (I), описанные выше, применимы в отношении выбора растворителя, условий реакции, времени реакций и реагентов.
Схема реакции 2 показывает общий способ получения В соединений (I) в соответствии с изобретением.
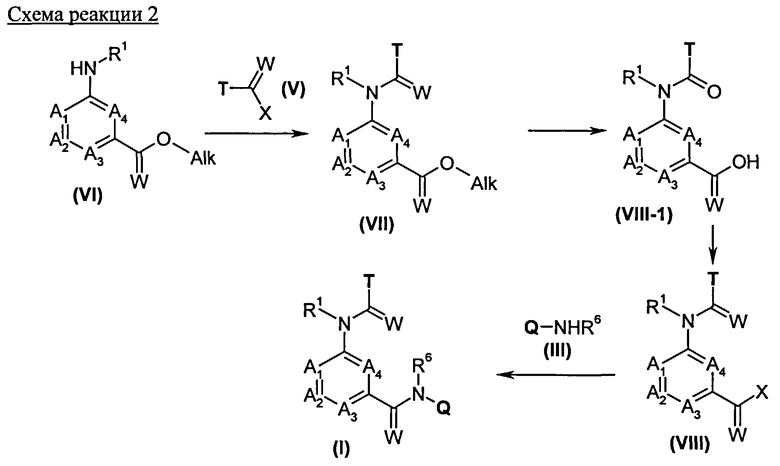
Радикалы A1-A4, Q, R1, R4 и W имеют значения, описанные выше. Х означает любую уходящую группу и Alk означает алкильный радикал, такой как, например, метил или этил. Т означает группу
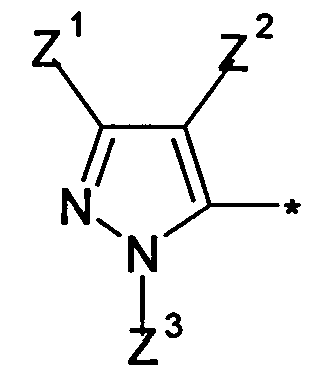
где радикалы Z1, Z2 и Z3 имеют значение, приведенное выше, и звездочка означает точку присоединения к группе C=W.
Соединения в соответствии с изобретением типа (I) могут быть получены по реакции амина общей структуры (III) с активированными производными карбоновой кислоты общей структуры (VIII). Здесь, такие же условия, как и в превращении (IV) и (V) в (I), описанные в способе получения А, применимы в отношении выбора растворителя, условий реакции, времени реакций и реагентов.
Активированные производные карбоновой кислоты общей структуры (VIII) могут быть получены путем двухстадийного синтеза из соответствующих эфиров карбоновых кислот общей структуры (VII). На первой стадии, с функции карбоновой кислоты, защищенной в форме сложного эфира (O-Alk), соединения (VII), в зависимости от используемого сложного алкилового эфира, снимают защиту пригодным реагентом [Greene′s Protective Groups in Organic Synthesis, 4-е изд., P.G.M. Wuts, T.W. Greene, John Wiley & Sons, Inc., Hoboken, Нью-Джерси], и получающуюся свободную гидроксильную группу кислотной функция (VIII-1) превращают в уходящую группу X. Здесь, можно использовать те же способы, что и уже описанные для получения (V). Соединения общей структуры (VII) могут быть получены по реакции аминов общей структуры (VI) с активированными производными карбоновой кислоты общей структуры (V). Здесь, такие же условия, как и в синтезе (I), описанные в способе получения А, применимы в отношении выбора растворителя, условий реакции, времени реакций и реагентов.
Схема реакции 3 показывает общий способ получения С соединений (I) в соответствии с изобретением.
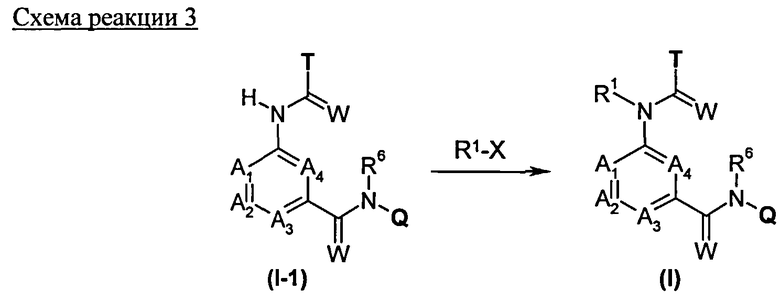
Радикалы A1-A4, Q, R6 и W имеют значения, описанные выше. Х означает любую уходящую группу, такую как, например, хлор, бром или йод. Т означает группу
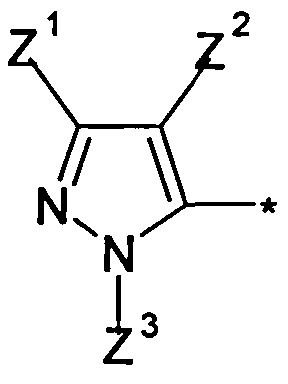
где радикалы Z1, Z2 и Z3 имеют значение, приведенное выше, и звездочка означает точку присоединения к группе C=W. R1 означает радикалы, описанные выше, за исключением водорода.
Соединения общей структуры (I), где R1≠Н, могут быть получены из соединений общей структуры (I-1). Здесь, можно использовать способы, известные из литературы [R1 = необязательно замещ. алкил & (гет)арилалкил: WO 2008/061688; Journal of Heterocyclic Chemistry 1995, 32(3), 835-839; WO 2011/029808; WO 2010/020432; US 2010/0152192; WO 2010/101949; WO 2010/043377, Medicinal Chemistry Letters 2011, 2(8), 632-637; Journal of Heterocyclic Chemistry 1977, 14(7), 1263-1265; WO 2011/020193; WO 2008/121602; WO 2006/074924; WO 2006/065794 | R1 = необязательно замещ. алкилкарбонил & (гет)арил(алкил)карбонил: WO 2010/015545; Journal of the Chemical Society, Perkin Transactions 1 2002, (2), 257-274; US 7951828 | R1 = необязательно замещ. алкоксикарбонил & (гет)арил(алкил)оксикарбонил: W02011/112731; WO 2009/027393; Journal of Organic Chemistry 2011, 76(8), 2502-2520 | R1 = необязательно замещ. алкинил: Synthesis 2007, (18), 2920-2923; Tetrahedron 2006, 62(16), 3856-3871; Journal of the American Chemical Society 2006, 128(14), 4586-4587; Chemical Communications (Кембридж, Соединенное Королевство) 2010, 46(8), 1269-1271; WO 2009/027393 | R1 = необязательно замещ. алкенил: Organic Chemistry: An Indian Journal 2010, 6(1), 52-55; European Journal of Organic Chemistry 2009, (1), 72-84; WO 2006/067444; WO 2005/049585].
Схема реакции 4 показывает общий способ получения D соединений (I) в соответствии с изобретением.
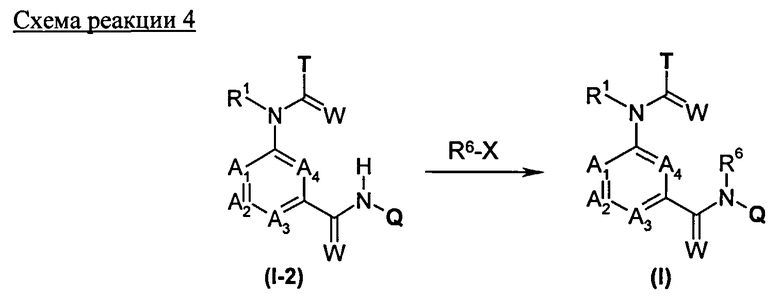
Радикалы A1-A4, Q, R1 и W имеют значения, описанные выше. Х означает любую уходящую группу, такую как, например, хлор, бром или йод. Т означает группу
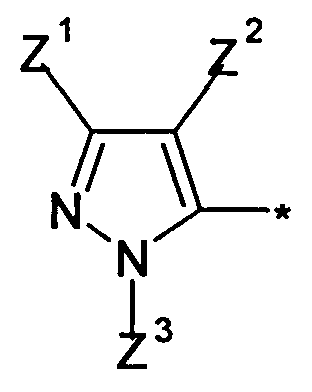
где радикалы Z1, Z2 и Z3 имеют значение, приведенное выше, и звездочка означает точку присоединения к группе C=W. R6 означает радикалы, описанные выше.
Соединения общей структуры (I) могут быть получены из соединений общей структуры (I-1). Здесь, можно использовать способы, упомянутые для способа получения С.
Соединения общих формул (II-1), (II-1-1) и (II-2) можно использовать в качестве предшественников для веществ общей формулы (II). Вещества общей формулы (II-1-1) обычно являются известными соединениями органической химии, которые могут быть получены установленными способами синтеза. Возможные пути синтеза циклических аминокарбоновых кислот общей формулы (II-1-1) показаны на схеме реакции 5.
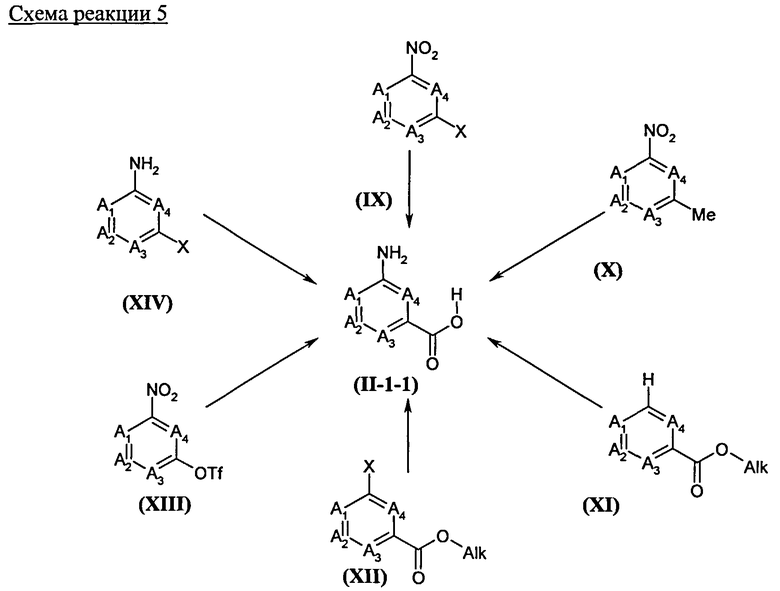
Галогенированные (гетеро)ароматические нитро- или аминосоединения, например, представленные формулами (IX) и (XIV), могут служить в качестве исходных веществ для получения аминокарбоновых кислот общей структуры (II-1-1). Здесь, уходящую группу Х заменяют цианогруппой, и последнюю затем подвергают кислотному или основному гидролизу. Обмен галоген/циано можно осуществить, например, путем нуклеофильного замещения в ароматическом кольце, используя цианидные соединения, такие как, например, цианид натрия [US 4766219], или же с помощью реакции, опосредованной медью [Journal of Antibiotics 1994, 47(12), 1456-65].
В случае нитросоединений (IX, X, и XIII), нитрофункция впоследствии может быть восстановлена до аминофункции. Пригодными способами для такого восстановления являются гидрирование и опосредованные металлами реакции, такие как, например, опосредованные хлоридом олова(П), железным порошком, цинковой пылью и им подобными соединениями.
Гидрирование можно проводить в пригодном растворителе в присутствии катализатора в атмосфере водорода (нормальное давление или повышенное давление). Пригодными для применения в качестве таких катализаторов являются палладиевые катализаторы, такие как, например, палладий на углероде, никелевые катализаторы, такие как никель Ренея, кобальтовые катализаторы, рутениевые катализаторы, родиевые катализаторы, платиновые катализаторы и соединения, подобные им. Пригодными растворителями являются вода, спирты, такие как метанол и этанол, ароматические углеводороды, такие как бензол и толуол, простые эфиры с открытой цепью или циклические, такие как диэтиловый эфир, диоксан и тетрагидрофуран, а также сложные эфиры, такие как этилацетат. Реакции восстановления можно проводить в диапазоне давлений от 1 бара до 100 бар, причем температура может изменяться между -20°С и температурой кипения используемого растворителя. В зависимости от условий реакции, время реакций находится между несколькими минутами и 96 часами.
Опосредованные металлами реакции восстановления, например с применением хлорида олова(И), можно провести в соответствии со способом, описанным в Organic Syntheses Coll. т.(III), 453.
Кроме того, (гетеро)ароматические аминокарбоновые кислоты общей структуры (II-1-1) также можно получить из соответствующих метальных предшественников типа (X) путем окисления. Окислителями, пригодными для таких реакций окисления, являются, например, перманганат калия, дихромат натрия, триоксид хрома и соединения, подобные им [Tetrahedron Letters 1995, 36(25), 4369-72; Bioorganic & Medicinal Chemistry Letters 2007, 17(4), 1043-1046]. Также возможно использование ферментативных способов для таких реакций окисления [Межд. заявка РСТ, 9502061]. Необходимое впоследствии восстановление нитрофункции можно провести аналогично способу, описанному выше.
Дополнительным способом получения (гетеро)ароматических аминокарбоновых кислот общей структуры (II-1-1) является нитрование предшественников карбоновых кислот, представленных формулой (XI) или (XII), и последующее восстановление нитрофункции. Реакции нитрования можно провести с использованием способов, известных из литературы [Justus Liebigs Annalen der Chemie 1958, 611, 194-205; Organikum, Wiley-VCH, 22. Издание, 358 и след.]. Необходимое впоследствии восстановление нитрофункции можно провести аналогично способу, описанному выше.
Кроме того, (гетеро)ароматические аминокарбоновые кислоты общей структуры (II-1-1) могут быть получены из соответствующих (гетеро)арилтрифлатов типа (XIII) с использованием палладий-катализируемого способа [Synthesis 2006, (4), 594-596]. Соединения общей формулы (II-1) могут быть получены из соединений общей формулы (II-1-1) установленными способами синтеза. Возможный путь синтеза циклических аминокарбоновых кислот общей формулы (II-1) показан на схеме реакции 6.
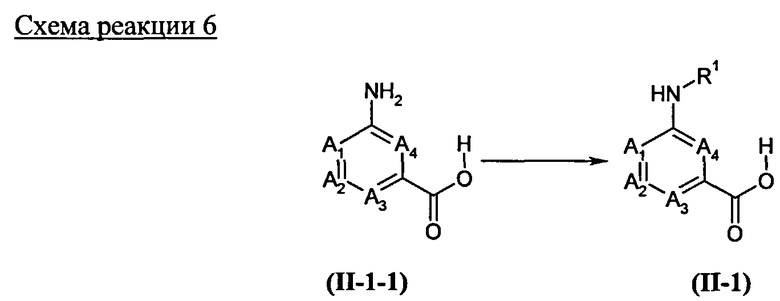
Радикалы A1-A4 имеют значения, описанные выше. Радикал R1 означает радикалы, описанные выше, за исключением водорода.
Превращение, известное из литературы, (II-1-1) в (II-1) может происходить, среди прочего, посредством восстановительного аминирования [Bioorganic & Medicinal Chemistry Letters 2005, 15(21), 4752-4756; WO 2010-142402; US2010-0324056] или прямого алкилирования [Tetrahedron Letters 1977, (9), 771-774; Journal of the American Chemical Society 1997, 119(9), 2315-2316; Journal of Combinatorial Chemistry 2006, 8(6), 834-840].
Соединения общей формулы (II-2) могут быть получены из соединений общей формулы (II-1) установленными способами синтеза. Возможный путь синтеза циклических аминокарбоновых кислот общей формулы (II-2) показан на схеме реакции 7.
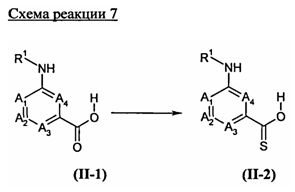
Радикалы A1-A4 и R1 имеют значения, описанные выше.
Превращение соединений общей формулы (II-1) в соединения общей формулы (II-2) можно провести аналогично реакциям, известным из литературы [US 2009-0023798; WO 2009-044200; WO 2010-085352].
Возможные пути синтеза производных гетероциклических карбоновых кислот общей формулы (V) показаны на схеме реакции 8.
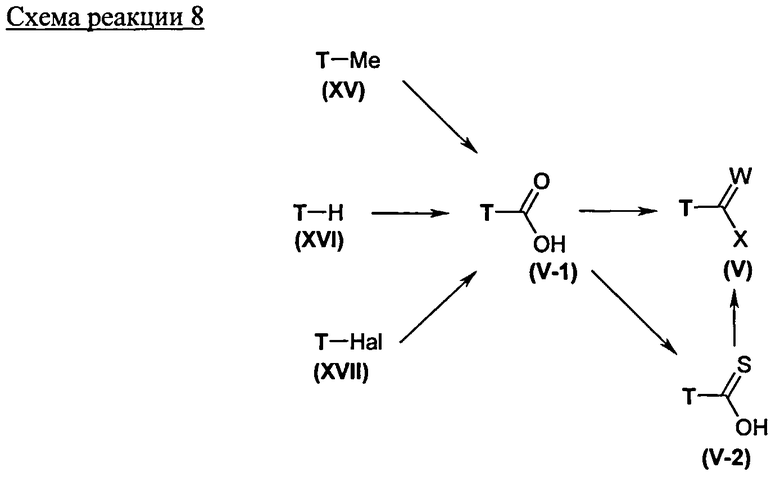
Радикал W имеет значения, описанные выше. Hal означает пригодный галоген, например бром или йод. Х означает пригодную уходящую группу, такую как, например, хлор. Т означает группу
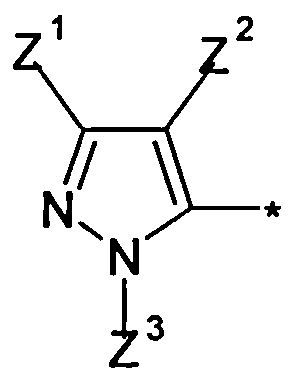
где радикалы Z1, Z2 и Z3 имеют значение, приведенное выше, и звездочка означает точку присоединения к группам Me, H, Hal, COOH, C(=S)OH или C(=W)X.
Гетероциклические карбоновые кислоты общей структуры (V-1) можно получить, среди прочего, из метальных производных общей формулы (XV) путем окисления метильной функции. С этой целью, возможно использование способов, уже упомянутых для окисления метальных групп соединений общей структуры (X).
Гетероциклические карбоновые кислоты общей структуры (V-1) могут быть получены из предшественников общей структуры (XVI) путем депротонирования с использованием пригодного основания и путем захвата соответствующего карбаниона диоксидом углерода [Journal of Medicinal Chemistry 2008, 51(4), 937-947; Bioorganic & Medicinal Chemistry Letters 2007, 17(22), 6274-6279]. Пригодными основаниями являются, например, диизопропиламид лития, н-бутиллитий, втор-бутиллитий и соединения, подобные им.
Также, для способа получения гетероциклических карбоновых кислот общей структуры (V-1), описанного выше, пригодны подходящим образом галогенированные гетероциклы (XVII). Однако, в таком случае карбанион генерируют не путем депротонирования, а с помощью реакции металлирования [Angewandte Chemie, International, Издание 2008, 47(2), 311-315]. Предпочтительными для этих реакций металлирования являются н-бутиллитий, трет-бутиллитий и хлорид изопропилмагния. Гетероциклические карбоновые кислоты общей структуры (V-1) также можно получить из галогенированных предшественников общей структуры (XVII) с помощью палладий-катализируемых реакций, известных из литературы, что приводит к соответствующим гетероциклическим эфирам карбоновых кислот [Russian Journal of Applied Chemistry 2007, 80(4), 571-575].
Гетероциклические карбоновые кислоты общей структуры (V-1), кроме того, могут быть получены из галогенированных соединений общей структуры (XVII) по реакции замещения галогенов цианидами и последующего гидролиза нитрильной функции сильной кислотой или основаниями [WO 2005079801].
Гетероциклический тиокарбоновые кислоты общей структуры (V-2) могут быть получены из (V-1) аналогично методам, известным из литературы, описанным для получения соединений общей формулы (II-2).
Активированные производные гетероциклической карбоновой кислоты, такие как, например, карбонилгалогениды, представленные общей структурой (V), могут быть получены по реакции циклической (тио)карбоновой кислоты, представленной формулами (V-1) и (V-2), с галогенирующими реагентами, такими как тионилхлорид, тионилбромид, фосфорилхлорид, оксалилхлорид, трихлорид фосфора и т.д. [Organikum, Wiley-VCH, 22. Издание, 496 и след.].
Активированные производные карбоновой кислоты общей структуры (II) могут быть получены с помощью общеизвестных, раскрытых в литературе способов из карбоновых кислот формулы (II-1) [Organikum, Wiley-VCH, 22. Издание, 496 и след.; Chem. Ber. 1970, 788; J. Am. Chem. Soc 1967, 5012]. Соединения формулы (II-1) доступны для приобретения или могут быть получены с помощью известных, раскрытых в литературе способов [Synthesis 2006, (4), 594-596; Tetrahedron Letters 1995, 36(25), 4369-72; Bioorganic & Medicinal Chemistry Letters 2007, 17(4), 1043-1046; Межд. заявка РСТ, 9502061, Journal of Organic Chemistry 1954, 19, 357-64; WO 2001083459].
Соединения общей структуры (III) доступны для приобретения и/или могут быть получены следующими способами, которые известны из литературы или аналогичны им [Journal of Organic Chemistry 1990, 55(14), 4276-81; WO 2005028429; WO 2005021485; Organic Letters 2010,12(9), 1944-1947; Tetrahedron 1999, 55(24), 7625-7644]. Соединения общей структуры (V) обычно доступны для приобретения и/или могут быть получены с помощью известных, раскрытых в литературе способов [Journal of Medicinal Chemistry 2008, 51(4), 937-947; Bioorganic & Medicinal Chemistry Letters 2007, 17(22), 6274-6279; Russian Journal of Applied Chemistry 2007, 80(4), 571-575; WO 2005079801; Journal of Organic Chemistry 2008, 73(9), 3523-3529; Bioorganic & Medicinal Chemistry Letters 2005, 15(22), 4898-4906; US 2006069270]
Соединения общей структуры (VI) могут быть получены с помощью способов, известных из литературы, из соединений общей структуры (II) [Journal of the American Chemical Society 2001, 123(34), 8177-8188; Inorganica Chimica Acta 2006, 359(6), 1912-1922].
Соединения общих структур (IX)-(XVII) доступны для приобретения и/или известны из релевантной специальной литературы.
Окислители для окисления спиртовых групп известны (ср., например, окислители в Organic Organic Synthesis by Oxidation with Metal Compounds, Mijs, de Jonge, Plenum Verlag, Нью-Йорк, 1986; Manganese Compounds as Oxidizing Agens in Organic Chemistry, Amdt, Open Court Publishing Company, Ла Саль, IL, 1981; The Oxidation of Organic Compounds by Permanganate Ion and Hexavalent Chromium, Lee, Open Court Publishing Company, Ла Саль, IL, 1980). Окисление может быть проведено, например, в присутствии перманганатов (например, перманганата калия), оксидов металлов (например, диоксида марганца, оксидов хрома, который используют, например, в виде оксида дипиридинхрома (VI) в качестве реактива Коллинза (ср. J.С. Collins и др., Tetrahedron Lett. 30, 3363-3366, 1968)). Подобным образом, окисление проводят в присутствии хлорхромата пиридиния (например, реактив Кори) (ср. также R.О. Hutchins и др., Tetrahedron Lett. 48, 4167-4170, 1977; D. Landini и др. Synthesis 134-136, 1979) или тетраоксида рутения (ср. S.-I. Murahashi, N. Komiya Ruthenium-catalyzed Oxidation of Alkenes, Alcohols, Amines, Amides, p-Lactams, Phenols and Hydrocarbons, в: Modem Oxidation Methods, Baeckvall, Jan-Erling (Ред.), Wiley-VCH-Verlag GmbH & Co. KGaA, 2004). Подобным образом, пригодными являются индуцированные ультразвуком реакции окисления и применение перманганата калия (ср. J. Yamawaki и др., Chem. Lett. 3,379-380,1983).
Все известные пригодные кислотные или основные вещества, способствующие реакции, могут применяться в соответствии со способами, описанными в литературе, для разблокирования/удаления защитной группы SG. Когда защитные группы карбаматного типа применяют для защиты аминогрупп, предпочтение отдают использованию кислотных веществ, способствующих реакции. Когда используют трет-бутилкарбаматную защитную группу (ВОС группа), например, применяют смеси минеральных кислот, таких как соляная кислота, бромисто-водородная кислота, азотная кислота, серная кислота, фосфорная кислота, или органических кислот, таких как бензойная кислота, муравьиная кислота, уксусная кислота, трифторуксусная кислота, метансульфоновая кислота, бензолсульфоновая кислота или толуолсульфоновая кислота, и пригодного разбавителя, такого как вода и/или органический растворитель, такой как тетрагидрофуран, диоксан, дихлорметан, хлороформ, этилацетат, этанол или метанол. Предпочтение отдают смесям соляной кислоты или уксусной кислоты с водой и/или органическим растворителем, таким как этилацетат.
Известно, что определенные реакции и способы получения можно провести особенно эффективно в присутствии разбавителей или растворителей и основных или кислотных веществ, способствующих реакции. Также возможно применение смесей разбавителей или растворителей. Разбавители или растворители преимущественно используют в таком количестве, что реакционная смесь остается легко перемешиваемой в течение всего процесса.
Пригодные разбавители или растворители для проведения реакций в соответствии с изобретением представляют собой, в принципе, все органический растворители, которые являются инертными в специфических условиях реакции. Примеры включают: галогенуглеводороды (например, хлоруглеводороды, такие как тетрахлорэтилен, тетрахлорэтан, дихлорпропан, метиленхлорид, дихлорбутан, хлороформ, четыреххлористый углерод, трихлорэтан, трихлорэтилен, пентахлорэтан, дифторбензол, 1,2-дихлорэтан, хлорбензол, бромбензол, дихлорбензол, хлортолуол, трихлорбензол), спирты (например, метанол, этанол, изопропанол, бутанол), эфиры (например, этилпропиловый эфир, метил-трет-бутиловый эфир, н-бутиловый эфир, анизол, фенетол, циклогексилметиловый эфир, диметиловый эфир, диэтиловый эфир, дипропиловый эфир, диизопропиловый эфир, ди-н-бутиловый эфир, диизобутиловый эфир, диизоамиловый эфир, диметиловый эфир этиленгликоля, тетрагидрофуран, диоксан, дихлордиэтиловый эфир и полиэфиры этиленоксида и/или пропиленоксида), амины (например, триметил-, триэтил-, трипропил-, трибутиламин, N-метилморфолин, пиридин и тетраметилендиамин), нитроуглеводороды (например, нитрометан, нитроэтан, нитропропан, нитробензол, хлорнитробензол, о-нитротолуол); нитрилы (например, ацетонитрил, пропионитрил, бутиронитрил, изобутиронитрил, бензонитрил, м-хлорбензонитрил), тетрагидротиофендиоксид, диметилсульфоксид, тетраметиленсульфоксид, дипропилсульфоксид, бензилметилсульфоксид, диизобутилсульфоксид, дибутилсульфоксид, диизоамилсульфоксид, сульфоны (например, диметил, диэтил, дипропил, дибутил, дифенил, дигексил, метилэтил, этилпропил, этилизобутил и пентаметиленсульфон), алифатические, циклоалифатические или ароматические углеводороды (например, пентан, гексан, гептан, октан, нонан и технические углеводороды), а также так называемые ″уайт-спириты″ с компонентами, имеющими температуру кипения в интервале от, например, 40°С до 250°С, цимен, фракции нефти с интервалом кипения от 70°С до 190°С, циклогексан, метилциклогексан, петролейный эфир, лигроин, октан, бензол, толуол, хлорбензол, бромбензол, нитробензол, ксилол, сложные эфиры (например, метил-, этил-, бутил- и изобутилацетат, диметил-, дибутил- и этиленкарбонат); амиды (например, гексаметилфосфор-триамид, формамид, N-метилформамид, N,N-диметилформамид, N,N-дипропилформамид, N,N-дибутилформамид, N-метилпирролидин, N-метилкапролактам, 1,3-диметил-3,4,5,6-тетрагидро-2(1Н)-пиримидин, октилпирролидон, октилкапролактам, 1,3-диметил-2-имидазолиндион, N-формилпиперидин, N,N′-диформилпиперазин) и кетоны (например, ацетон, ацетофенон, метилэтилкетон, метилбутилкетон).
Основными веществами, способствующими реакции, используемьми для выполнения способа в соответствии с изобретением, могут быть все пригодные связывающие кислоту вещества. Примеры включают: соединения щелочноземельных металлов или щелочных металлов (например, гидроксиды, гидриды, оксиды и карбонаты лития, натрия, калия, магния, кальция и бария), амидиновые основания или гуанидиновые основания (например, 7-метил-1,5,7-триазабицикло[4.4.0]дец-5-ен (MTBD); диазабицикло[4.3.0]нонен (DBN), диазабицикло[2.2.2]октан (DABCO), 1,8-диазабицикло[5.4.0]ундецен (DBU), циклогексилтетрабутилгуанидин (CyTBG), циклогексилтетраметилгуанидин (CyTMG), N,N,N,N-тетраметил-1,8-нафталиндиамин, пентаметилпиперидин) и амины, особенно третичные амины (например, триэтиламин, триметиламин, трибензиламин, триизопропиламин, трибутиламин, трициклогексиламин, триамиламин, тригексиламин, N,N-диметиланилин, N,N-диметилтолуидин, N,N-диметил-п-аминопиридин, N-метилпирролидин, N-метилпиперидин, N-метилимидазол, N-метилпиразол, N-метилморфолин, N-метилгексаметилендиамин, пиридин, 4-пирролидинопиридин, 4-диметиламинопиридин, хинолин, α-пиколин, β-пиколин, изохинолин, пиримидин, акридин, N,N,N′,N′-тетраметилендиамин, N,N,N′,N′-тетраэтилендиамин, хиноксалин, N-пропилдиизопропиламин, N-этилдиизопропиламин, N,N′-диметилциклогексиламин, 2,6-лутидин, 2,4-лутидин или триэтилдиамин).
Кислотные вещества, способствующие реакции, используемые для выполнения способа в соответствии с изобретением, включают все минеральные кислоты (например, галогенводородные кислоты, такие как фтористоводородная кислота, соляная кислота, бромисто-водородная кислота или йодистоводородная кислота, а также серную кислоту, фосфорную кислоту, фосфористую кислоту, азотную кислоту), кислоты Льюиса (например, хлорид алюминия(III), трифторид бора или его эфират, хлорид титана(IV), хлорид олова(IV)) и органические кислоты (например, муравьиную кислота, уксусную кислоту, пропионовую кислоту, малоновую кислоту, молочную кислоту, щавелевую кислоту, фумаровую кислоту, адипиновую кислоту, стеариновую кислоту, винную кислоту, олеиновую кислоту, метансульфоновую кислоту, бензойную кислоту, бензолсульфоновую кислоту или пара-толуолсульфоновую кислоту).
Если в схемах реакций намечены защитные группы, можно использовать все общеизвестные защитные группы. В частности, те, которые описаны Greene Т.W., Wuts P.G.W. в Protective Groups in Organic Synthesis; John Wiley & Sons, Inc. 1999, ″Protection for the hydroxyl group including 1,2- and 1,3-diols″.
Также пригодны защитные группы
типа замещенного метилового эфира (например, метоксиметиловый эфир (MOM), метилтиометиловый эфир (МТМ), (фенилдиметилсилил)метоксиметиловый эфир (SNOM-OR), бензилоксиметиловый эфир (BOM-OR) пара-метоксибензилоксиметиловый эфир (PMBM-OR), пара-нитробензилоксиметиловый эфир, орто-нитробензилоксиметиловый эфир (NBOM-OR), (4-метоксифенокси)метиловый эфир (п-AOM-OR), гваяколметиловый эфир (GUM-OR), трет-бутоксиметиловый эфир, 4-пентилоксиметиловый эфир (POM-OR), силилоксиметиловый эфир, 2-метоксиэтоксиметиловый эфир (MEM-OR), 2,2,2-трихлорэтоксиметиловый эфир, бис(2-хлорэтокси)метиловый эфир, 2-(триметилсилил)этоксиметиловый эфир (SEM-OR), метоксиметиловый эфир (ММ-OR));
типа замещенного этилового эфира (например, 1-этоксиэтиловый эфир (EE-OR), 1-(2-хлорэтокси)этиловый эфир (CEE-OR), 1-[2-(триметилсилил)этокси]этиловый эфир (SEE-OR), 1-метил-1-метоксиэтиловый эфир (MIP-OR), 1-метил-1-бензилоксиэтиловый эфир (MBE-OR), 1-метил-1-бензилокси-2-фторэтиловый эфир (MIP-OR), 1-метил-1-феноксиэтиловый эфир, 2,2,2-трихлорэтиловый эфир, 1,1-дианизил-2,2,2-трихлорэтиловый эфир (DATE-OR), 1,1,1,3,3,3-гексафтор-2-фенилизопропиловый эфир (HIP-OR), 2-триметилсилилэтиловый эфир, 2-(бензилтио)этиловый эфир, 2-(фенилселенил)этиловый эфир), эфира (например, тетрагидропираниловый эфир (ТНР-OR), 3-бромтетрагидропираниловый эфир (3-BrTHP-OR), тетрагидротиопираниловый эфир, 1-метоксициклогексиловый эфир, 2- и 4-пиколиловый эфир, N-оксид 3-метил-2-пиколиловый эфир, 2-хинолинилметиловый эфир (Qm-OR), 1-пиренилметиловый эфир, дифенилметиловый эфир (DPM-OR), пара, пара′-динитробензгидриловый эфир (DNB-OR), 5-дибензосубериловый эфир, трифенилметиловый эфир (Tr-OR), альфа-нафтилдифенилметиловый эфир, пара-метоксифенилдифенилметиловый эфир (MMTrOR), ди(пара-метоксифенил)фенилметиловый эфир (DMTr-OR), три(пара-метоксифенил)фенилметиловый эфир (TMTr-OR), 4-(4′-бромфенацилокси)фенилдифенилметиловый эфир, 4,4′,4″-трис(4,5-дихлорфталимидофенил)метиловый эфир (CPTr-OR), 4,4′,4″-трис(бензоилоксифенил)метиловый эфир (ТВТг-OR), 4,4′-диметокси-3″-[N-(имидазолилметил)]тритиловый эфир (IDTr-OR), 4,4′-диметокси-3″-[N-(имидазолил-этил)карбамоил]тритиловый эфир (IETr-OR), 1,1-бис(4-метоксифенил)-1′-пиренилметиловый эфир (Bmpm-OR), 9-антриловый эфир, 9-(9-фенил)ксантениловый эфир (Pixyl-OR), 9-(9-фенил-10-оксо)антриловый (тритилоновый эфир), 4-метокситетрагидропираниловый эфир (MTHP-OR), 4-метокситетрагидротиопираниловый эфир, 8,8-диоксид 4-метокситетрагидротиопираниловый, 1-[(2-хлор-4-метил)фенил]-4-метоксипиперидин-4-иловый эфир (CTMP-OR), 1-(2-фторфенил)-4-метоксипиперидин-4-иловый эфир (Fpmp-OR), 1,4-диоксан-2-иловый эфир, тетрагидрофураниловый эфир, тетрагидротиофураниловый эфир, 2,3,3а,4,5,6,7,7а-октагидро-7,8,8-триметил-4,7-метанбензофуран-2-иловый эфир (MBF-OR), трет-бутиловый эфир, аллиловый эфир, пропаргиловый эфир, пара-хлорфениловый эфир, пара-метоксифениловый эфир, пара-нитрофениловый эфир, пара-2,4-динитрофениловый эфир (DNP-OR), 2,3,5,6-тетрафтор-4-(трифторметил)фениловый эфир, бензиловый эфир (Bn-OR));
типа замещенного бензилового эфира (например, пара-метоксибензиловый эфир (MPM-OR), 3,4-диметоксибензиловый эфир (DMPM-OR), орто-нитробензиловый эфир, пара-нитробензиловый эфир, пара-галогенбензиловый эфир, 2,6-дихлорбензиловый эфир, пара-аминоацилбензиловый эфир (PAB-OR), пара-азидобензиловый эфир (Azb-OR), 4-азидо-3-хлорбензиловый эфир, 2-трифторметилбензиловый эфир, пара-(метилсульфинил)бензиловый эфир (Msib-OR));
типа силилового эфира (например, триметилсилиловый эфир (TMS-OR), триэтилсилиловый эфир (TES-OR), триизопропилсилиловый эфир (TIPS-OR), диметилизопропилсилиловый эфир (IPDMS-OR), диэтилизопропилсилиловый эфир (DEIPS-OR), диметилгексилсилиловый эфир (TDS-OR), трет-бутилдиметилсилиловый эфир (TBDMS-OR), трет-бутилдифенилсилиловый эфир (TBDPS-OR), трибензилсилиловый эфир, три-пара-ксилилсилиловый эфир, трифенилсилиловый эфир (TPS-OR), дифенилметилсилиловый эфир (DPMS-OR), ди-трет-бутилметилсилиловый эфир (DTBMS-OR), трис(триметилсилил)силиловый эфир (сисиловый эфир), ди-трет-бутилметилсилиловый эфир (DTBMS-OR), трис(триметилсилил)силиловый эфир (сисиловый эфир), (2-гидроксистирил)диметилсилиловый эфир (HSDMS-OR), (2-гидроксистирил)диизопропилсилиловый эфир (HSDIS-OR), трет-бутилметоксифенилсилиловый эфир (TBMPS-OR), трет-бутоксидифенилсилиловый эфир (DPTBOS-OR));
типа сложного эфира (например, такие сложные эфиры, как формиат, бензоилформиат, ацетат (ac-or), хлорацетат, дихлорацетат, трихлорацетат, трифторацетат (ТФУ-OR), метоксиацетат, трифенилметоксиацетат, феноксиацетат, пара-хлорфеноксиацетат, фенилацетат, дифенилацетат (DPA-OR), никотинат, 3-фенилпропионат, 4-пентоат, 4-оксопентоат (левулинат) (Lev-OR) 4,4-(этилендитио)пентаноат (LevS-OR), 5-[3-бис(4-метоксифенил)гидроксиметоксифенокси]левулинат, пивалоат (Pv-OR), 1-адамантаноат, кротонат, 4-метоксикротонат, бензоат (Bz-OR), пара-фенилбензоат, 2,4,6-триметилбензоат (мезитоат), 4-(метилтиометокси)бутират (MTMB-OR), 2-(метилтиометоксиметил)бензоат(МТМТ-ОР),
типа сложного эфира (например, метилкарбонат, метоксиметилкарбонат, 9-флуоренилметилкарбонат (Fmoc-OR), этилкарбонат, 2,2,2-трихлорэтилкарбонат (Fmoc-OR), 1,1-диметил-2,2,2-трихлорэтилкарбонат (TCBOC-OR), 2-(триметилсилил)этилкарбонат (TMS-OR), 2-(фенилсульфонил)этилкарбонат (Ps-OR), 2-(трифенилфосфонио)этилкарбонат (Peoc-OR), трет-бутилкарбонат (Boc-OR), изобутилкарбонат, винилкарбонат, аллилкарбонат (Alloc-OR), пара-нитрофенилкарбонат, бензилкарбонат (Z-OR), пара-метоксибензилкарбонат, 3,4-диметоксибензилкарбонат, орто-нитробензилкарбонат, пара-нитробензилкарбонат, 2-дансилэтилкарбонат (Dnseoc-OR), 2-(4-нитрофенил)этилкарбонат (Npeoc-OR), 2-(2,4-динитрофенил)этилкарбонат (Dnpeoc)), и
типа сульфата (например, аллилсульфонат (Als-OR), метансульфонат (Ms-OR), бензилсульфонат, тозилат (Ts-OR), 2-[(4-нитрофенил)этил]сульфонат (Npes-OR)).
Пригодными катализаторами для проведения каталитического гидрирования в способе в соответствии с изобретением являются все обычные катализаторы гидрирования, такие как, например, платиновые катализаторы (например, платиновая пластина, платиновая губка, платиновая чернь, коллоидная платина, оксид платины, платиновая проволока), палладиевые катализаторы (например, палладиевая губка, палладиевая чернь, оксид палладия, палладий на угле, коллоидный палладий, палладий на сульфате бария, палладий на карбонате бария, гидроксид палладия), никелевые катализаторы (например, восстановленный никель, оксид никеля, никель Ренея), рутениевые катализаторы, кобальтовые катализаторы (например, восстановленный кобальт, кобальт Ренея), медные катализаторы (например, восстановленная медь, медь Ренея, медь Ульмана). Предпочтение отдают применению катализаторов на основе благородных металлов (например, платины и палладия или рутениевых катализаторов), которые могут быть нанесены на пригодную подложку (например, уголь или кремний), родиевые катализаторы (например, хлорид трис(трифенилфосфин)родия(1) в присутствии трифенилфосфина). Кроме того, возможно применение ″хиральных катализаторов гидрирования″ (например, катализаторов, содержащих хиральные дифосфиновые лиганды, такие как (2S,3S)-(-)-2,3-бис(дифенилфосфино)бутан [(S,S)-хирафос] или (R)-(+)-2,2′- или (S)-(-)-2,2′-бис(дифенилфосфино)-1,1′-бинафталин [R(+)-BINAP или S(-)-BINAP]), посредством чего доля отдельного изомера в смеси изомеров возрастает, или образование другого изомера практически полностью подавляется.
Соли соединений в соответствии с изобретением получают стандартными методами. Типичными кислотно-аддитивными солями являются, например, соли, образованные реакцией с неорганическими кислотами, такими как, например, серная кислота, соляная кислота, бромисто-водородная кислота, фосфорная кислота, или органическими карбоновыми кислотами, такими как уксусная кислота, трифторуксусная кислота, лимонная кислота, янтарная кислота, масляная кислота, молочная кислота, муравьиная кислота, фумаровая кислота, малеиновая кислота, малоновая кислота, камфорная кислота, щавелевая кислота, фталевая кислота, пропионовая кислота, гликолевая кислота, глутаровая кислота, стеариновая кислота, салициловая кислота, сорбиновая кислота, винная кислота, коричная кислота, валериановая кислота, пикриновая кислота, бензойная кислота, или органическими сульфоновыми кислотами, такими как метансульфоновая кислота и 4-толуолсульфоновая кислота.
Также типичными являются соли соединений в соответствии с изобретением, образованные из органических оснований, таких как, например, пиридин или триэтиламин, или соли, образованные из неорганических оснований, таких как, например, гидриды, гидроксиды или карбонаты натрия, лития, кальция, магния или бария, при условии, если соединения общей формулы (I) имеют структурный элемент, пригодный для образования такой соли.
Методы синтеза для получения гетероциклических N-оксидов и т-аминов известны. Они могут быть получены с использованием пероксикислот (например, перуксусной кислоты и мета-хлорпербензойной кислоты (МСРВА), пероксида водорода), алкилгидропероксидов (например, трет-бутил гидропероксида), пербората натрия и диоксиранов (например, диметилдиоксирана). Эти методы были описаны, например, Т.L. Gilchrist, в Comprehensive Organic synthesis, т.7, сс.748-750, 1992, S.V. Ley, (ред.), Pergamon Press; M. Tisler, B. Stanovnik, в Comprehensive Heterocyclic Chemistry, т.3, cc.18-20, 1984, A.J. Boulton, A. McKillop, (Ред.), Pergamon Press; M.R. Grimmett, B.R.T. Keene в Advances in Heterocyclic Chemistry, т.43, cc.149-163, 1988, A.R. Katritzky, (ред.). Academic Press; M. Tisler, B. Stanovnik, в Advances in Heterocyclic Chemistry, т.9, cc.285-291, 1968, A.R. Katritzky, A.J. Boulton (Ред.), Academic Press; G.W.H. Cheeseman, E.S.G. Werstiuk в Advances in Heterocyclic Chemistry, т.22, cc.390-392, 1978, A.R. Katritzky, A.J. Boulton, (ред.). Academic Press.
Экспериментальная часть
Способ получения А
Пример (1) 4-Бром-N-{4-хлор-3-[(1-цианоциклопропил)карбамоил]фенил}-3-(1-фторциклопропил)-1-метил-1H-пиразол-5-карбоксамид
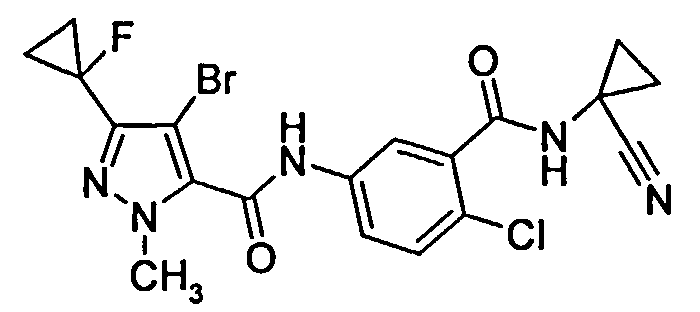
120 мг (0.45 ммоль) 4-бром-3-(1-фторциклопропил)-1-метил-1H-пиразол-5-карбоновой кислоты суспендируют в 20 мл дихлорметана ч.д.а., и добавляют 0.02 мл N,N-диметилформамида ч.д.а. К этой смеси добавляют по каплям 0.119 мл (1.36 ммоль) оксалилхлорида. Смесь затем перемешивают при комнатной температуре в течение 30 минут и затем при нагревании с обратным холодильником в течение 30 минут. После охлаждения, реакционную смесь концентрируют при пониженном давлении на роторном испарителе. Полученный таким путем сырой продукт вводят в дальнейшую реакцию без дополнительной очистки.
108 мг (0.45 ммоль) 5-амино-2-хлор-N-(1-цианоциклопропил)бензамида и 92 мг (0.68 ммоль) цианида серебра(1) изначально загружают в 10 мл дихлорметана ч.д.а. По каплям к этой суспензии добавляют раствор 129 мг (0.45 ммоль) 4-бром-3-(1-фторциклопропил)-1-метил-1H-пиразол-5-карбонилхлорида в 10 мл дихлорметана ч.д.а. Реакционную смесь перемешивают при комнатной температуре в течение 16 ч, и затем фильтруют через силикагель, и осадок на фильтре промывают этилацетатом. Растворители удаляют при пониженном давлении на роторном испарителе.
Это дает 170 мг (78%) 4-бром-N-{4-хлор-3-[(1-цианоциклопропил)карбамоил]фенил}-3-(1-фторциклопропил)-1-метил-1H-пиразол-5-карбоксамида в виде бесцветного твердого вещества.
1Н-ЯМР (400 МГц, d6-ДМСО): δ=10.96 (s, 1Н), 9.49 (s, 1H), 7.85 (d, 1H), 7.74 (dd, 1H), 7.55 (d, 1H), 3.93 (s, 3H), 1.57-1.61 (m, 2H), 1.40-1.45 (m, 2H), 1.23-1.28 (m, 2H), 1.08-1.11 (m, 2H) м.д.
ВЭЖХ-MCa): logP=2.50, масса (m/z)=482 [M+H]+.
Способ получения В
Пример (2) N-{4-Хлор-3-[(l-цианоциклопропил)карбамоил]фенил}-N,1-диметил-3,4-бис(трифторметил)-1H-пиразол-5-карбоксамид
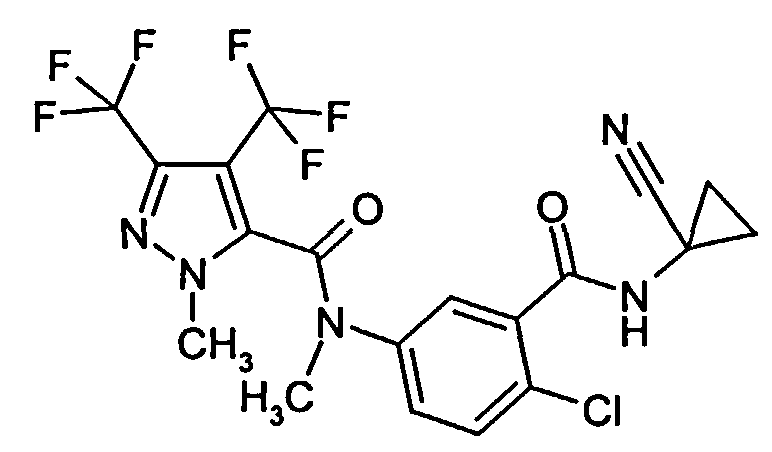
150.0 мг (0.29 ммоль) 2-хлор-5-(метил{[1-метил-3,4-бис(трифторметил)-1Я-пиразол-5-ил]карбонил}амино)бензойной кислоты суспендируют в 5.0 мл дихлорметана ч.д.а. Затем к суспензии последовательно добавляют 0.02 мл N,N-диметилформамида ч.д.а. и 0.075 мл (0.86 ммоль) оксалилхлорида. Реакционную смесь перемешивают при комнатной температуре в течение 0.5 ч и затем нагревают с обратным холодильником в течение 40 минут. Растворитель удаляют при пониженном давлении на роторном испарителе. Образованный 2-хлор-5-(метил {[1-метил-3,4-бис(трифторметил)-1Н-пиразол-5-ил]карбонил}амино)бензоилхлорид применяют для последующей стадии синтеза без дополнительной очистки.
68.3 мг (0.58 ммоль) гидрохлорида 1-аминоциклопропанкарбонитрила изначально загружают в 5.0 мл дихлорметана ч.д.а., и затем последовательно добавляют 0.148 мл (0,86 ммоль) N-этилдиизопропиламина и 156 мг 2-хлор-5-(метил {[1-метил-3,4-бис(трифторметил)-1Н-пиразол-5-ил]карбонил} амино)бензоилхлорида (0.29 ммоль), растворенного в 5.0 мл дихлорметана ч.д.а. Реакционную смесь перемешивают при комнатной температуре в течение 16 часов. Реакционный раствор разбавляют 30 мл этилацетата. Органическую фазу два раза промывают 1 н. соляной кислотой, один раз 1 н. водным раствором гидроксида натрия и один раз насыщенным раствором хлорида натрия. Органическую фазу сушат над сульфат магния и фильтруют, и растворитель удаляют на роторном испарителе при пониженном давлении.
Сырой продукт очищают с помощью препаративной ВЭЖХ. Это дает 64 мг (45%) N-{4-хлор-3 -[(1 -цианоциклопропил)карбамоил] фенил}-N,1-диметил-3,4-бис(трифторметил)-1H-пиразол-5-карбоксамида в виде бесцветного твердого вещества.
1Н-ЯМР (400 МГц, d3-ацетонитрил, смесь амидов в цис- и транс-конфигурациях): δ=7.42-7.66 (m, 2Н), 7.40 (d, 1H), 7.29 (d, 2H), 7.18 (dd, 1H), 3.83 & 3.99 (2 s, вместе 3Н), 3.46 & 3.23 (2s, вместе 3Н), 1.54-1.60 (m, 2H), 1.25-1.37 (m, 2H) м.д.
ВЭЖХ-МСа): logP=2.81, масса (m/z)=494 [M+H]+.
Способ получения С
Пример (50) N-{4-Хлор-3-[(1-цианоциклопропил)карбамоил]фенил}-N-этил-3-(пентафторэтил)-1-пропил-4-(трифторметил)-1H-пиразол-5-карбоксамид
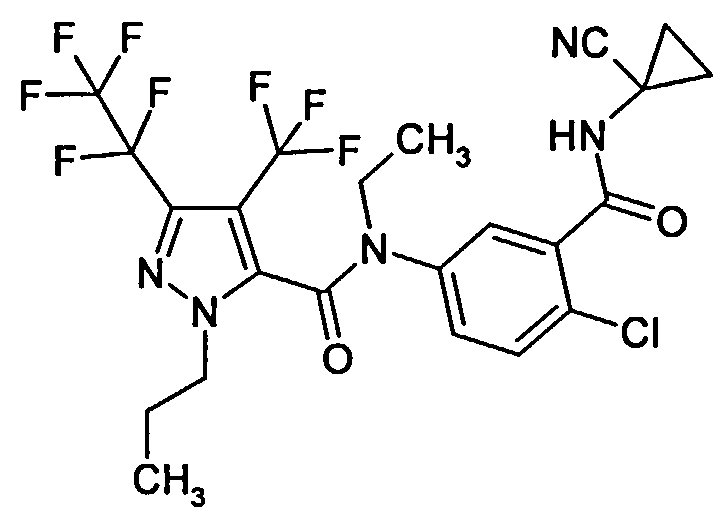
70 мг (0.13 ммоль) N-{4-хлор-3-[(1-цианоциклопропил)карбамоил]фенил}-3-(пентафторэтил)-1-пропил-4-(трифторметил)-1H-пиразол-5-карбоксамид и 35 мг (0.14 ммоль) карбоната калия суспендируют в 1.4 мл N,N-диметилформамида ч.д.а. В течение 16 ч, к смеси понемногу добавляют в сумме 29 мг (0.19 ммоль) йодэтана. После завершения добавления, реакционный раствор перемешивают при комнатной температуре в течение 20 ч. Реакционную смесь разбавляют водой, и водную фазу три раза экстрагируют этилацетатом. Объединенные органические фазы два раза промывают насыщенным раствором хлорида натрия, сушат над сульфатом натрия и фильтруют.Растворители удаляют на роторном испарителе при пониженном давлении. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле. Это дает 30 мг (41%) N-{4-хлор-3-[(1-цианоциклопропил)карбамоил]фенил}-N-этил-3-(пентафторэтил)-1-пропил-4-(трифторметил)-1H-пиразол-5-карбоксамида в виде бесцветного твердого вещества.
1Н-ЯМР (400 МГц, d6-ДМСО, смесь амидов в цис- и транс-конфигурациях): δ=9.56 & 9.42 (2s, вместе 1H), 7.69 & 7.56 (2d, вместе 1Н), 7.63 & 7.42 (2d, вместе 1Н), 7.48 & 7.28 (2dd, вместе 1Н), 3.52-4.32 (m, 4H), 0.79-1.87 (m, 12H) м.д.
ВЭЖХ-МСа): logP=4.06, масса (m/z)=586 [M+H]+.
Способ получения D
Пример (40) N-{3-[Ацетил(1-цианоциклопропил)карбамоил]-4-хлорфенил}-1-метил-3-(пентафторэтил)-4-(трифторметил)-1H-пиразол-5-карбоксамид
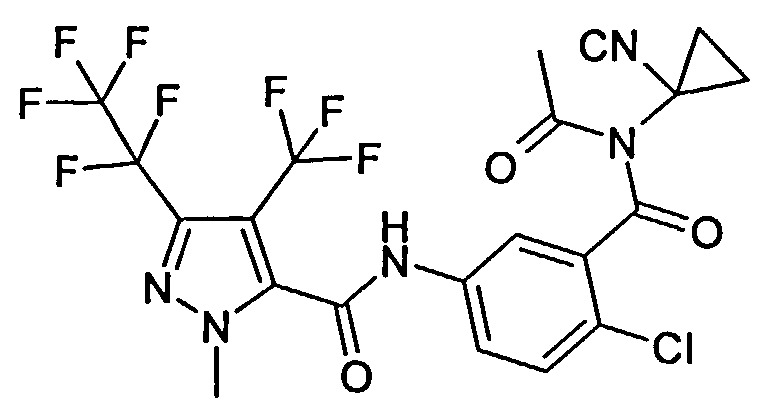
300 мг (0.57 ммоль) N-{4-хлор-3-[(1-цианоциклопропил)карбамоил]фенил}-1-метил-3-(пентафторэтил)-4-(трифторметил)-1H-пиразол-5-карбоксамида растворяют в 6.0 мл дихлорметана ч.д.а. и охлаждают на ледяной бане. К раствору последовательно добавляют 0.17 мл (0.99 ммоль) N-этилдиизопропиламина и 49 мг (0.62 ммоль) ацетилхлорида. Реакционную смесь затем нагревают до комнатной температуры и перемешивают в течение 16 ч. Реакционный раствор разбавляют дихлорметаном и затем промывают водой. Органическую фазу сушат над сульфатом натрия и фильтруют, и растворитель удаляют на роторном испарителе при пониженном давлении.
Сырой продукт очищают с помощью препаративной ВЭЖХ. Это дает 130 мг (40%) N-{3-[ацетил(1-цианоциклопропил)карбамоил]-4-хлорфенил}-1-метил-3-(пентафторэтил)-4-(трифторметил)-1H-пиразол-5-карбоксамида в виде бесцветного твердого вещества.
1Н-ЯМР (400 МГц, d6-ДМСО): δ=11.49 (s, 1Н), 7.90 (d, 1H), 7.70 (dd, 1H), 7.57 (d, 1H), 4.03 (s, 3H), 2.49 (s, 3H), 1.85-1.91 (m, 2H), 1.57-1.67 (m, 2H) м.д.
ВЭЖХ-MCa): logP=3.81, Масса (m/z)=572 [M+H]+.
a) Примечание относительно определения значений logP и масс-детектирования: Определение приведенных значений logP проводили в соответствии с директивой ЕЭС 79/831 Annex V.A8 с помощью ВЭЖХ (высокоэффективная жидкостная хроматография) на колонке с обращенной фазой (С 18). ЖХ система Agilent 1100; 50*4.6 Zorbax Eclipse Plus С 18 1.8 микрон; подвижная фаза А: ацетонитрил (0.1% муравьиная кислота); подвижная фаза В: вода (0.09% муравьиная кислота); линейный градиент от 10% ацетонитрила до 95% ацетонитрила в течение 4.25 мин., затем 95% ацетонитрил в течение дальнейших 1.25 мин; температура печи 55°С; скорость потока: 2.0 мл/мин. Масс-детектирование выполнялось с помощью системы Agilend MSD.
b) Примечание относительно определения значений logP и масс-детектирования: Указанные значения log Р определяли в соответствии с директивой ЕЭС 79/831 Annex V.A8 с помощью ВЭЖХ (высокоэффективная жидкостная хроматография), используя колонку с обращенной фазой (С18). НР1100; 50*4.6 Zorbax Eclipse Plus C18 1.8 микрон; подвижная фаза А: ацетонитрил (0.1% муравьиная кислота); подвижная фаза В: вода (0.08% муравьиная кислота); линейный градиент от 5% ацетонитрила до 95% ацетонитрила в течение 1.70 мин., затем 95% ацетонитрил в течение дальнейшей 1.00 мин; температура печи 55°С; скорость потока: 2.0 мл/мин. Масс-детектирование выполнялось с помощью масс-детектора Micromass ZQ2000 от Waters.
Соединения, перечисленные в таблицах 1 & 2 были получены с использованием способов получения А-D, описанных выше.
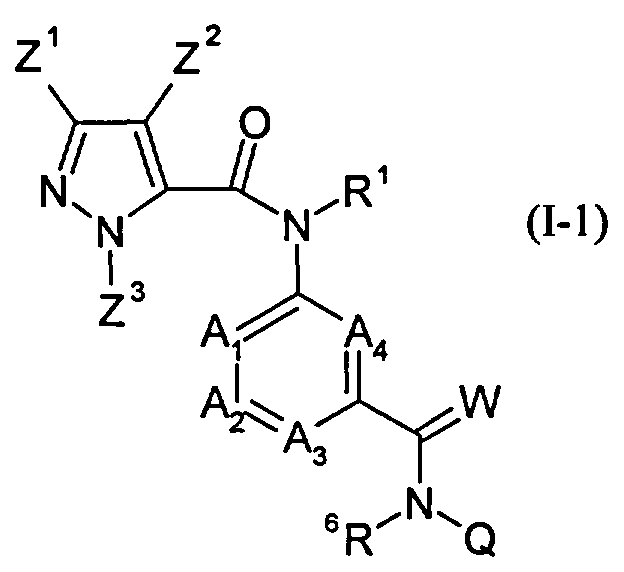
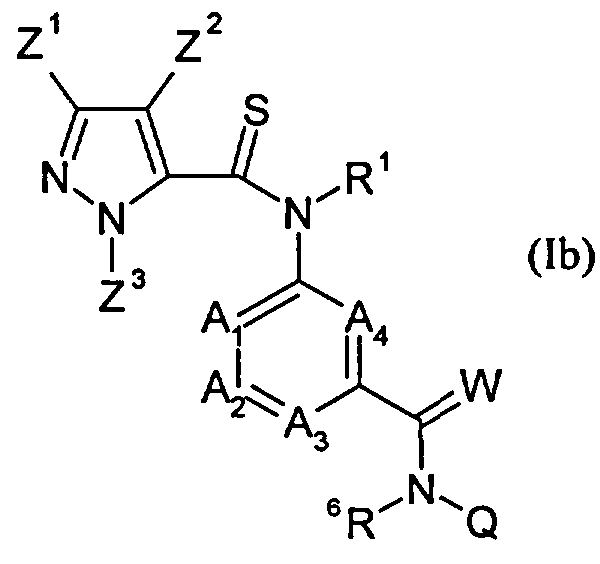
Указанная масса является пиком изотопной картины [М+Н]+ иона наибольшей интенсивности; если обнаруживали [М-Н]- ион, указанная масса отмечена2.
2Указанная масса является пиком изотопной картины [М-Н]- иона наибольшей интенсивности.
a) Примечание относительно определения значений logP и масс-детектирования: Определение приведенных значений logP проводили в соответствии с директивой ЕЭС 79/831 Annex V.A8 с помощью ВЭЖХ (высокоэффективная жидкостная хроматография) на колонке с обращенной фазой (С18). ЖХ система Agilent 1100; 50*4.6 Zorbax Eclipse Plus С18 1.8 микрон; подвижная фаза А: ацетонитрил (0.1% муравьиная кислота); подвижная фаза В: вода (0.09% муравьиная кислота); линейный градиент от 10% ацетонитрила до 95% ацетонитрила в течение 4.25 мин., затем 95% ацетонитрил в течение дальнейших 1.25 мин; температура печи 55°С; скорость потока: 2.0 мл/мин. Масс-детектирование выполнялось с помощью системы Agilend MSD.
b) Примечание относительно определения значений logP и масс-детектирования: Указанные значения logP определяли в соответствии с директивой ЕЭС 79/831 Annex V.A8 с помощью ВЭЖХ (высокоэффективная жидкостная хроматография), используя колонку с обращенной фазой (С18). НР1100; 50*4.6 Zorbax Eclipse Plus С18 1.8 микрон; подвижная фаза А: ацетонитрил (0.1% муравьиная кислота); подвижная фаза В: вода (0.08% муравьиная кислота); линейный градиент от 5% ацетонитрила до 95% ацетонитрила в течение 1.70 мин., затем 95% ацетонитрил в течение дальнейшей 1.00 мин; температура печи 55°С; скорость потока: 2.0 мл/мин. Масс-детектирование выполнялось с помощью масс-детектора Micromass ZQ2000 от Waters.
Данные ЯМР отобранных примеров
Данные 1H-ЯМР выбранных примеров указываются в виде перечней 1Н-ЯМР пиков. Для каждого пика сигнала приводится δ-значение в м.д. и интенсивность сигнала в скобках.
Интенсивность резких сигналов коррелирует с высотой сигналов в печатном примере ЯМР-спектра в см и показывает истинные соотношения интенсивностей сигналов. В случае широких сигналов, несколько пиков или середина сигнала и их относительные интенсивности могут быть показаны в сравнении с наиболее интенсивным сигналом в спектре.
Перечни 1Н ЯМР пиков подобны обычным 1Н ЯМР распечаткам, и таким образом обычно содержат все пики, перечисленные в обычных ЯМР представлениях.
Кроме того, подобно обычным 1Н ЯМР распечаткам, они могут показывать сигналы растворителя, сигналы стереоизомеров целевых соединений, которые подобным образом составляют часть объект изобретения, и/или пики загрязнений.
В сообщенных сигналах соединений в дельта диапазоне растворителей и/или воды, наши перечни 1Н ЯМР пиков показывают обычные пики растворителей, например пики ДМСО в ДМСО-d6 и пик воды, которые обычно имеют в среднем высокую интенсивность.
Пики стереоизомеров целевых соединений и/или пики загрязнений обычно имеют в среднем меньшую интенсивность, чем пики целевых соединений (например, с чистотой >90%).
Такие стереоизомеры и/или загрязнения могут быть характерными для отдельного способа получения. Их пики могут таким образом помочь идентифицировать воспроизведение нашего способа получения на основании таких ″отпечатков пальцев побочных продуктов″.
Специалист в области расчета пиков целевых соединений известными методами (MestreC, ACD моделирование, а также применение эмпирически оцененных ожидаемых значений) может, при необходимости, выделить пики целевых соединений, необязательно с использованием дополнительных фильтров интенсивности. Это выделение будет аналогичным отбору релевантных пиков в традиционной интерпретации 1Н ЯМР.
Получение исходных веществ
Этил 3-(1-хлорциклопропил)-1-метил-1H-пиразол-5-карбоксилат
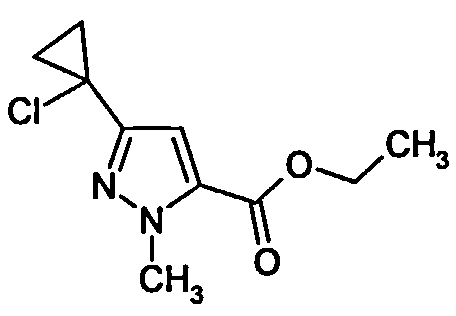
10.16 г (254.2 ммоль) гидрида натрия суспендируют в 125 мл тетрагидрофурана ч.д.а. и охлаждают до -15°С. К этой суспензии добавляют по каплям раствор 15.0 г (127.1 ммоль) 1-(1-хлорциклопропил)этанона в 25 мл тетрагидрофурана ч.д.а. Суспензию перемешивают при -15°С в течение 2 ч., и затем добавляют 37.12 г (254.2 ммоль) диэтилоксалата. Через 3 ч при комнатной температуре, реакцию гасят водой со льдом. Водную фазу многократно экстрагируют этилацетатом. Объединенные органические фазы промывают насыщенным раствором хлорида натрия, сушат над сульфатом натрия и фильтруют.Растворитель удаляют на роторном испарителе при пониженном давлении.
Остаток растворяют в 150 мл этанола ч.д.а. и кипятят с обратным холодильником. К смеси при нагревании с обратным холодильником добавляют 36.09 г (254.2 ммоль) метилгидразинсульфата, и смесь кипятят с обратным холодильником в течение дополнительных 4 ч. После охлаждения, реакционную смесь концентрируют при пониженном давлении на роторном испарителе, и полученный таким образом остаток вносят в смесь воды и этилацетата. Водную фазу многократно экстрагируют этилацетатом. Объединенные органические фазы промывают насыщенным раствором хлорида натрия, сушат над сульфатом натрия и фильтруют. Растворитель удаляют на роторном испарителе при пониженном давлении. Сырой продукт очищают с помощью колоночной хроматографии. Это дает 4.34 г (15%) этил 3-(1-хлорциклопропил)-1-метил-1Н-пиразол-5-карбоксилата.
1Н-ЯМР (300 МГц, d1-хлороформ) δ=6.89 (s, 1Н), 4.36 (q, 2H), 4.11 (s, 3H), 1.35 (t, 3H) м.д.;
Этил 4-хлор-3-(1-хлорциклопропил)-1-метил-1H-пиразол-5-карбоксилат
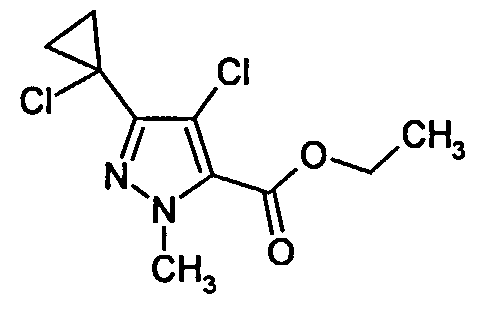
500 мг (2.19 ммоль) этил 3-(1-хлорциклопропил)-1-метил-1H-пиразол-5-карбоксилата растворяют в 10 мл N,N-диметилформамида ч.д.а., и добавляют 438 мг (3.28 ммоль) N-хлорсукцинимида. Реакционную смесь нагревают при 80°С в течение 15. Охлажденный реакционный раствор разбавляют водой и два раза экстрагируют этилацетатом. Объединенные органические фазы промывают насыщенным раствором хлорида натрия, сушат над сульфатом натрия и фильтруют. Растворитель удаляют при пониженном давлении на роторном испарителе. Сырой продукт фильтруют через силикагель и элюируют этилацетатом. Это дает 517 мг (80%) этил 4-хлор-3-(1-хлорциклопропил)-1-метил- 177-пиразол-5-карбоксилата с чистотой 89%.
1Н-ЯМР (400 МГц, d6-ДМСО): δ=4.35 (q, 2H), 4.04 (s, 3H), 1.42-1.46 (m, 2H), 1.31-1.38 (m, 5H) м.д.
ВЭЖХ-MCa): logP=3.52, масса (m/z)=263 [M+H]+.
4-Хлор-3-(1-хлорциклопропил)-1-метил-1H-пиразол-5-карбоновая кислота
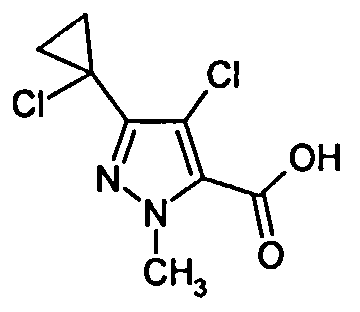
517 мг (1.76 ммоль) этил 4-хлор-3-(1-хлорциклопропил)-1-метил-1Я-пиразол-5-карбоксилата (чистота 89%) растворяют в 10 мл этанола ч.д.а. Затем к раствору добавляют 3.5 мл (3.5 ммоль) 1 н. водного раствора гидроксида натрия, и смесь перемешивают при комнатной температуре в течение 16 ч. Реакционную смесь подкисляют путем добавления 1 н. соляной кислоты. Водную фазу два раза экстрагируют этилацетатом. Объединенные органические фазы промывают насыщенным раствором хлорида натрия, сушат над сульфатом натрия и фильтруют. Растворитель удаляют при пониженном давлении на роторном испарителе. Это дает 422 мг (99%) 4-хлор-3-(1-хлорциклопропил)-1-метил-1H-пиразол-5-карбоновой кислоты.
1Н-ЯМР (400 МГц, d6-ДМСО): δ=4.02 (s, 3Н), 1.31-1.42 (m, 4H) м.д.
ВЭЖХ-MCa): logP=1.90, масса (m/z)=235 [M+H]+.
Этил 3-(1-фторциклопропил)-1-метил-1Н-пиразол-5-карбоксилат
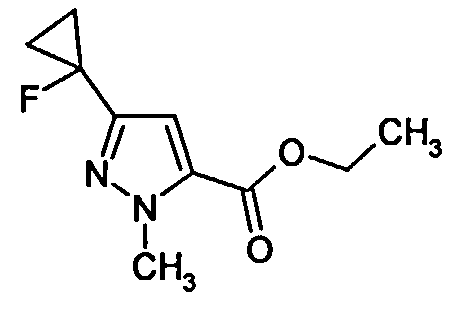
Этил 3-(1-фторциклопропил)-1-метил-1Н-пиразол-5-карбоксилат получают из 1-(1-фторциклопропил)этанона аналогично способу, описанному в синтезе этил 3-(1-хлорциклопропил)-1-метил-1H-пиразол-5-карбоксилата.
1Н-ЯМР (300 МГц, d1-хлороформ) δ=6.90 (s, 1Н), 4.34 (q, 2H), 4.13 (s, 3Н), 1.37 (t, 3Н) м.д.;
Этил 4-хлор-3-(1-фторциклопропил)-1-метил-1H-пиразол-5-карбоксилат
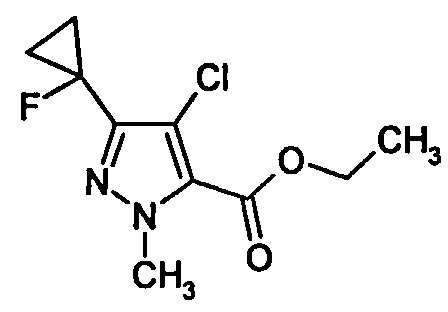
Получение проводили аналогично получению этил 4-хлор-3-(1-хлорциклопропил)-1-метил-1H-пиразол-5-карбоксилата, используя этил 3-(1-фторциклопропил)-1-метил-1Н-пиразол-5-карбоксилат и 3 экв. N-хлорсукцинимида.
1Н-ЯМР (400 МГц, d6-ДМСО): δ=4.36 (q, 2Н), 4.06 (s. 3H), 1.38-1.44 (m, 2H), 1.33 (t, 3Н), 1.04-1.09 (m, 2Н) м.д.
ВЭЖХ-MCa) logP=3.07, масса (m/z)=247 [М+Н]+.
4-Хлор-3-(1-фторциклопропил)-1-метил-1H-пиразол-5-карбоновая кислота
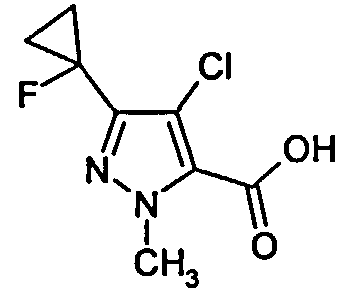
Получение проводили аналогично получению 4-хлор-3-(1-хлорциклопропил)-1-метил-1H-пиразол-5-карбоновой кислоты, используя этил 3-(1-фторциклопропил)-1-метил-1Н-пиразол-5-карбоксилат и 5.0 экв. гидроксида натрия в метаноле.
1Н-ЯМР (400 МГц, d6-ДМСО): δ=4.05 (s, 3Н), 1.37-1.43 (m, 2H), 1.05-1.09 (m, 2H) м.д.
ВЭЖХ-МСа): logP=3.07, масса (m/z)=219 [M+H]+.
Метил 2-хлор-5-({[1-метил-3-(пентафторэтил)-4-(трифторметил)-1Я-пиразол-5-ил] карбонил} амино)бензоат
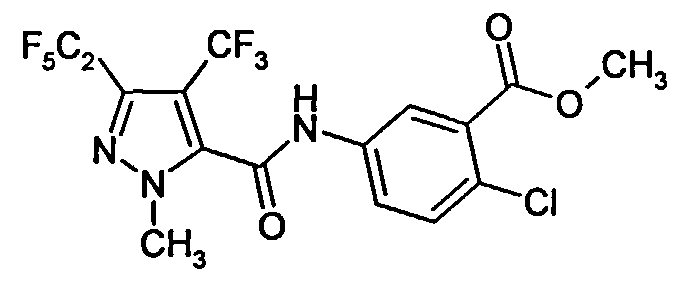
4.0 г (12.8 ммоль) 1-метил-3-(пентафторэтил)-4-(трифторметил)-17/-пиразол-5-карбоновой кислоты суспендируют в 50 мл дихлорметана. Затем последовательно добавляют 0.02 мл N,N-диметилформамида и 3.54 мл (38.4 ммоль) оксалилхлорида. Реакционную смесь затем перемешивают сначала при комнатной температуре в течение 30 минут, и затем при нагревании с обратным холодильником в течение 30 минут.Растворитель удаляют при пониженном давлении на роторном испарителе. Образованный 1-метил-3-(пентафторэтил)-4-(трифторметил)-1Н-пиразол-5-карбонилхлорид применяют для последующей стадии синтеза без дополнительной очистки.
Раствор 4.24 г (12.8 ммоль) 1-метил-3-(пентафторэтил)-4-(трифторметил)-1Я-пиразол-5-карбонилхлорида в 25 мл дихлорметана ч.д.а. добавляют к суспензии 2.38 г (12.8 ммоль) метил 5-амино-2-хлорбензоата и 2.57 г (19.2 ммоль) цианида серебра(I) в 50 мл дихлорметана ч.д.а., и смесь перемешивают при комнатной температуре в течение 16 ч. Суспензию затем фильтруют через силикагель, и продукт элюируют, используя смесь циклогексана и этилацетата (1:1). Органическую фазу промывают последовательно три раза 6 н. соляной кислотой и два раза насыщенным раствором хлорида натрия. Органическую фазу затем сушат над сульфатом натрия, фильтруют и концентрируют на роторном испарителе при пониженном давлении. Это дает 5.75 г (93%) метил 2-хлор-5-({[1-метил-3-(пентафторэтил)-4-(трифторметил)-1H-пиразол-5-ил] карбонил} амино)бензоата.
1Н-ЯМР (400 МГц, d3-ацетонитрил): δ=9.33 (s, 1Н), 8.14 (d, 1H), 7.72 (dd, 1H), 7.54 (d, 1H), 3.98 (s, 3H), 3.90 (s, 3Н) м.д.
ВЭЖХ-MCa): logP=4.05, масса (m/z)=480 [M+H]+.
2-Хлор-5-({[1-метил-3-(пентафторэтил)-4-(трифторметил)-1H-пиразол-5-ил]карбонил}амино)бензолкарбоновая кислота
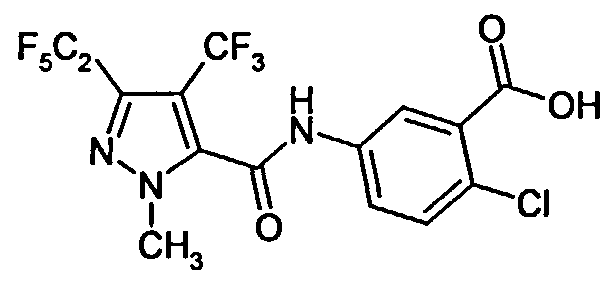
5.75 г (11.9 ммоль) метил 2-хлор-5-({[1-метил-3-(пентафторэтил)-4-(трифторметил)-1H-пиразол-5-ил]карбонил}амино)бензоата растворяют в 30 мл метанола ч.д.а., и затем добавляют 15.0 мл (30.0 ммоль) 2 н. водного раствора гидроксида натрия. Реакционную смесь перемешивают при комнатной температуре в течение 16 часов. Реакционный раствор осторожно подкисляют 6 н. соляной кислотой, и водную фазу затем три раза экстрагируют этилацетатом. Объединенные органические фазы один раз промывают насыщенным раствором хлорида натрия, сушат над сульфатом натрия и фильтруют. Растворитель удаляют при пониженном давлении на роторном испарителе. Это дает 5.57 г 2-хлор-5-({[1-метил-3-(пентафторэтил)-4-(трифторметил)-1H-пиразол-5-ил]карбонил}амино)бензолкарбоновой кислоты в виде бесцветного твердого вещества.
1Н-ЯМР (400 МГц, d3-ацетонил): δ=9.17 (s, 1H), 8.11 (d, 1H), 7.73 (dd, 1H), 7.52 (d, 1H), 3.98 (s, 3Н) м.д.
ВЭЖХ-МСа): logP=3.18, масса (m/z)=466 [M+H]+.
Этил 3.4-бис(трифторметил)-1H-пиразол-5-карбоксилат
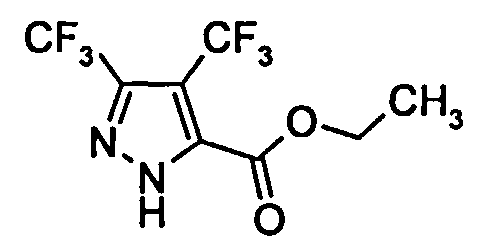
В атмосфере защитного газа, 7.57 г (63.0 ммоль) диазоэтилацетата изначально загружают в 200 мл диэтилового эфира, и температуру смеси устанавливают на -70°С. Затем в охлажденный раствор вводят 20.4 г (126 ммоль) гексафторбутина. Реакционную смесь медленно нагревают до комнатной температуры и перемешивают в течение 16 часов. Растворитель затем удаляют на роторном испарителе. Это дает 17.0 г этил 3,4-бис(трифторметил)-1H-пиразол-5-карбоксилата (98%) в виде желтого масла.
1Н-ЯМР (400 МГц, d3-ацетонитрил): δ=4.42 (q, 2Н), 1.38 (t, 3H) м.д.
ГХ-МС: время удержания 3.48 мин.; масса (m/z)=276 [M]+.
1-Метил-3,4-бис(трифторметил)-1H-пиразол-5-карбоновая кислота
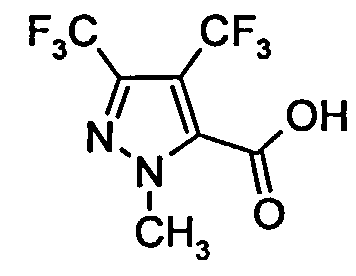
3.0 г (10.9 ммоль) этил 3,4-бис(трифторметил)-1H-пиразол-5-карбоксилата и 4.5 г (32.6 ммоль) карбоната калия суспендируют в 70 мл ацетона, и добавляют 1.35 мл йодметана (21.7 ммоль). Реакционную смесь перемешивают при комнатной температуре на протяжении ночи. К суспензии добавляют 54 мл (108 ммоль) 2 н. водного раствора гидроксида натрия. Раствор затем перемешивают при комнатной температуре на протяжении ночи. Реакционную смесь разбавляют водой, и большую часть ацетона удаляют на роторном испарителе при пониженном давлении. Значение рН остатка устанавливают на 2-3, используя 1 М соляную кислоту. Водный реакционный раствор два раза экстрагируют этилацетатом. Объединенные органические фазы сушат над сульфат магния, фильтруют и концентрируют при пониженном давлении на роторном испарителе. Это дает 2.7 г 1-метил-3,4-бис(трифторметил)-1H-пиразол-5-карбоновой кислоты (84%; чистота 88%) в виде коричневого твердого вещества.
1Н-ЯМР (400 МГц, d3-ацетонитрил): δ=4.12 (s, 3H) м.д.
ВЭЖХ-МСа): logP=1.47, масса (m/z)=263 [M+H]+.
Метил 2-хлор-5-(метиламино)бензоат
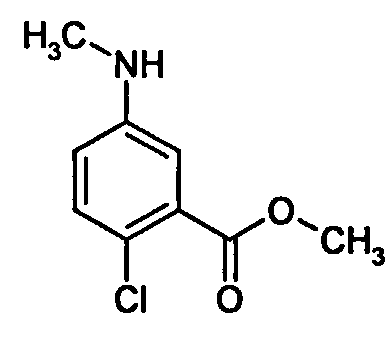
55.0 г (296 ммоль) метил 2-хлор-5-аминобензоата и 49.1 г (356 ммоль) карбоната калия суспендируют в 500 мл ацетонитрила ч.д.а. К реакционной смеси по каплям добавляют 22.1 мл (356 ммоль) метилйодида. Суспензию затем кипятят с обратным холодильником в течение 3 часов. После охлаждения, реакционную смесь фильтруют.Фильтрат разбавляют водой. Водную фазу два раза экстрагируют этилацетатом. Объединенные органические фазы сушат над сульфатом натрия и фильтруют. Растворитель удаляют при пониженном давлении на роторном испарителе. Сырой продукт очищают с помощью колоночной хроматографии. Это дает 30.0 г (51%) метил 2-хлор-5-(метиламино)бензоата.
1Н-ЯМР (300 МГц, d1-хлороформ) δ=7.21 (d, 1Н), 7.00 (d, 1H), 6.63 (d, 1H), 3.90 (s, 3H), 2.86 (s, 3H) м.д.
5-Амино-2-хлор-N-(1-цианоциклопропил)бензамид
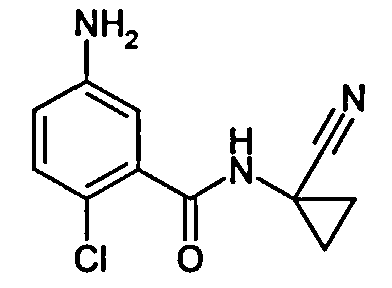
3.20 г (15.9 ммоль) 2-хлор-5-нитробензойной кислоты изначально загружают в 50 мл дихлорметана ч.д.а., и добавляют 0.06 мл N,N-диметилформамида ч.д.а. Затем к реакционной смеси добавляют 2.08 мл (23.8 ммоль) оксалилхлорида. Через 3 ч при КТ, реакционную смесь концентрируют при пониженном давлении на роторном испарителе. Сырой продукт (2-хлор-5-нитробензоилхлорид) вводят в дальнейшую реакцию без дополнительной очистки.
2.36 г (19.8 ммоль) гидрохлорида 1-аминоциклопропанкарбонитрила суспендируют в 70 мл хлороформа ч.д.а. При охлаждении льдом к суспензии добавляют 6.93 мл (39.7 ммоль) N-этилдиизопропиламина. Затем к охлажденной смеси по каплям добавляют раствор 3.50 г (15.9 ммоль) 2-хлор-5-нитробензоилхлорида в 5 мл хлороформа ч.д.а. Реакционную смесь нагревают при 50°С (температура масляной бани) в течение 4 ч. Реакционную смесь затем перемешивают при комнатной температуре в течение других 12 ч.
Реакционную смесь концентрируют при пониженном давлении на роторном испарителе, и остаток вносят в этилацетат.Органическую фазу два раза промывают 0.5 н. соляной кислотой, сушат над сульфатом натрия и фильтруют. Растворитель удаляют при пониженном давлении на роторном испарителе. Это дает 3.70 г (84%) 2-хлор-N-(1-цианоциклопропил)-5-нитробензамида.
1Н-ЯМР (400 МГц, d6-AMCO): δ=9.59 (s, 1H), 8.36 (d, 1H), 8.31 (dd, 1H), 7.85 (d, 1H), 1.55-1.61 (m, 2H), 1.32-1.37 (m, 2H) м.д.
ВЭЖХ-МСа): logP=1.52, масса (m/z)=266 [M+H]+.
3.15 г железного порошка суспендируют в 18 мл уксусной кислоты 5%-ной концентрации, и добавляют раствор 3.0 г 2-хлор-N-(1-цианоциклопропил)-5-нитробензамида в смеси 25 мл этилацетата и 22.6 мл ледяной уксусной кислоты. Во время добавления, внутреннюю температуру поддерживают ниже 45°С. Реакционную смесь перемешивают при комнатной температуре в течение 14 часов и затем фильтруют через целит. Фильтрат разбавляют водой, и водную фазу три раза экстрагируют этилацетатом. Объединенные органические фазы два раза промывают насыщенным раствором хлорида натрия, сушат над сульфат магния, фильтруют и концентрируют на роторном испарителе при пониженном давлении. Сырой продукт растирают со смесью трех частей циклогексана и одной части этилацетата, и твердое вещество отфильтровывают. Это дает 2.0 г (71%) 5-амино-2-хлор-N-(1-цианоциклопропил)бензамида.
1Н-ЯМР (400 МГц, d6-ДМСО): δ=9.20 (s, 1Н), 7.07 (d, 1H), 6.62 (dd, 1H), 6.57 (d, 1H), 1.51-1.57 (m, 2H), 1.17-1.24 (m, 2H) м.д.
ВЭЖХ-MCa): logP=0.82, масса (m/z)=236 [M+H]+.
1-Метил-4-(метилсульфанил)-3-(пентафторэтил)-1H-пиразол-5-карбоновая кислота
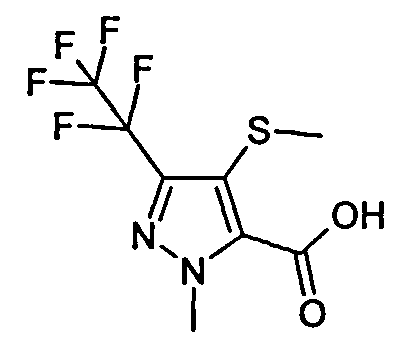
8.0 г (27.7 ммоль) 1-метил-4-нитро-3-(пентафторэтил)-1Н-пиразол-5-карбоновой кислоты [получение аналогично J. Med. Chem. 1987, 30, 91-96] растворяют в 100 мл дихлорметана. К раствору последовательно добавляют 50 мкл N,N-диметилформамида и 10.5 г (83.0 ммоль) оксалилхлорида. Через 0.5 ч при комнатной температуре, реакционную смесь нагревают с обратным холодильником в течение 0.5 ч. Реакционную смесь охлаждают до комнатной температуры. Растворители и избыток оксалилхлорида удаляют на роторном испарителе при пониженном давлении. Остаток растворяют в хлороформе ч.д.а. и медленно по каплям добавляют к суспензии 5.56 г (41.5 ммоль) цианида серебра(I), 100 мл хлороформа ч.д.а. и 56 мл метанола ч.д.а. Смесь нагревают с обратным холодильником в течение 8 ч, и затем охлаждают до комнатной температуры. Реакционную смесь фильтруют через короткую силикагелевую колонку, и колонку промывают дихлорметаном. Растворители удаляют на роторном испарителе при пониженном давлении.
Это дает 8.5 г метил 1-метил-4-нитро-3-(пентафторэтил)-1H-пиразол-5-карбоксилата.
Сырой продукт применяют для следующей реакции без дополнительной очистки.
1Н-ЯМР (600 МГц, d6-ДМСО): δ=4.16 (s, 3Н), 3.93 (s, 3H) м.д.
ВЭЖХ-МСа): logP=3.18, масса (m/z)=304 [М+Н]+.
8.5 г (28.0 ммоль) метил 1-метил-4-нитро-3-(пентафторэтил)-1H-пиразол-5-карбоксилата и 850 мг палладия на угле (10% палладий) суспендируют в 100 мл метанола. Автоклав инертизируют с помощью азота, и реакционную смесь затем перемешивают в атмосфере водорода 5 бар. Через 22 ч при КТ, смесь фильтруют через целит, и растворитель удаляют при пониженном давлении на роторном испарителе.
Сырой продукт вносят в дихлорметан и фильтруют через сульфат натрия. Дихлорметан затем удаляют при пониженном давлении на роторном испарителе.
Это дает 6.7 г (86%) метил 4-амино-1-метил-3-(пентафторэтил)-1H-пиразол-5-карбоксилата.
1Н-ЯМР (600 МГц, d6-ДМСО): δ=5.32 (s, 2H), 4.07 (s, ЗН), 3.86 (s, 3H) м.д.
ВЭЖХ-МСа): logP=2.52, масса (m/z)=274 [М+Н]+.
2.0 г (7.32 ммоль) метил 4-амино-1-метил-3-(пентафторэтил)-1H-пиразол-5-карбоксилата и 1.38 г (14.6 ммоль) диметилдисульфида растворяют в 14 мл ацетонитрила ч.д.а. К этой смеси медленно по каплям добавляют раствор 1.26 г (11.0 ммоль) трет-бутилнитрита в 5 мл ацетонитрила ч.д.а. После завершения добавления, реакционную смесь перемешивают при комнатной температуре в течение другого 1 ч. Реакционную смесь затем выливают в 1 н. соляную кислоту. Водную фазу три раза экстрагируют этилацетатом. Объединенные органические фазы два раза промывают насыщенным раствором хлорида натрия, сушат над сульфат магния и фильтруют. Растворители удаляют на роторном испарителе при пониженном давлении.
Это дает 2.0 г (72%) метил 1-метил-4-(метилсульфанил)-3-(пентафторэтил)-1Н-пиразол-5-карбоксилата в виде 8:2 смеси целевого продукта и побочного продукта, метил 1-метил-3-(пентафторэтил)-1Н-пиразол-5-карбоксилата.
1Н-ЯМР (400 МГц, d6-ДМСО): δ=4.12 (s, 3Н), 3.94 (s, 3Н), 2.34 (s, 3Н) м.д.
ВЭЖХ-МСа): logP=3.51, масса (m/z)=305 [М+Н]+.
3.0 г метил 1-метил-4-(метилсульфанил)-3-(пентафторэтил)-1Н-пиразол-5-карбоксилата растворяют в 16 мл метанола ч.д.а. К раствору затем добавляют 16.5 мл 2 н. водного раствора гидроксида натрия, и смесь перемешивают при комнатной температуре в течение 16 ч. Реакционную смесь разбавляют этилацетатом и затем промывают 100 мл 1 н. соляной кислоты. Кислую водную фазу два раза экстрагируют этилацетатом. Объединенные органические фазы промывают насыщенным раствором хлорида натрия, сушат над сульфатом натрия и фильтруют. Растворители удаляют на роторном испарителе при пониженном давлении.
Это дает 2.5 г (90%) 1-метил-4-(метилсульфанил)-3-(пентафторэтил)-1Н-пиразол-5-карбоновой кислоты в виде приблизительно 8:2 смеси целевого продукта и побочного продукта, 1-метил-3-(пентафторэтил)-1Н-пиразол-5-карбоновой кислоты.
1Н-ЯМР (400 МГц, d6-ДМСО): δ=4.12 (s, 3Н), 3.94 (s, 3H), 2.34 (s, 3H) м.д.
ВЭЖХ-MCa): logP=3.51, масса (m/z)=305 [М+Н]+.
Биологические примеры
А. Активность соединений
Испытание относительно Phaedon (PHAECO, обработка распылением)
Для получения пригодного препарата активного соединения, 1 массовую часть активного соединения смешивают с установленными количествами растворителей и эмульгатора, и концентрат разбавляют водой, содержащей эмульгатор, до желаемой концентрации. Пластинки листьев пекинской капусты (Brassica pekinensis) обрызгивают препаратом активного соединения желаемой концентрации и, после сушки, заселяют личинками листоеда хренового (Phaedon cochleariae).
Через 7 дней определяют эффективность, выраженную в %. 100% означает, что погибли все личинки жука; 0% означает, что ни одна из личинок жука не погибла.
В данном испытании, например, следующие соединения примеров получения показывают эффективность 100% при норме внесения 500 г/га: 1, 2, 3, 4, 5, 6, 7, 8, 9,10.
Испытание относительно Spodoptera frugiperda (SPODFR, обработка распылением)
Для получения пригодного препарата активного соединения, 1 массовую часть активного соединения смешивают с установленными количествами растворителей и эмульгатора, и концентрат разбавляют водой, содержащей эмульгатор, до желаемой концентрации. Пластинки листьев маиса (Zea mays) обрызгивают составом активного соединения желаемой концентрации и, после сушки, заселяют гусеницами совки (Spodopterafrugiperda).
Через 7 дней определяют эффективность, выраженную в %. 100% означает, что погибли все гусеницы; 0% означает, что ни одна из гусениц не погибла.
В данном испытании, например, следующее соединение примеров получения показывает эффективность 83% при норме внесения 500 г/га: 7.
В данном испытании, например, следующие соединения примеров получения показывают эффективность 100% при норме внесения 500 г/га: 2,4, 5, 6, 8, 9, 10.
Испытание относительно Myzus (MYZUPE, обработка распылением)
Для получения пригодного препарата активного соединения, 1 массовую часть активного соединения смешивают с установленными количествами растворителей и эмульгатора, и концентрат разбавляют водой, содержащей эмульгатор, до желаемой концентрации. Пластинки листьев пекинской капусты (Brassica pekinensis), инвазированные тлей персиковой зеленой всех стадий (Myzus persicae), обрызгивают препаратом активного соединения желаемой концентрации.
Через 6 дней определяют эффективность, выраженную в %. 100% означает, что погибли все особи тли; 0% означает, что ни одна из особей тли не погибла.
В данном испытании, например, следующие соединения примеров получения показывают эффективность 90% при норме внесения 500 г/га: 5,9.
В данном испытании, например, следующие соединения примеров получения показывают эффективность 100% при норме внесения 500 г/га: 2, 4, 6, 8, 10.
Испытание относительно Tetranychus, OP-устойчивого (TETRUR, обработка распылением)
Для получения пригодного препарата активного соединения, 1 массовую часть активного соединения смешивают с установленными количествами растворителей и эмульгатора, и концентрат разбавляют водой, содержащей эмульгатор, до желаемой концентрации. Пластинки листьев фасоли (Phaseolus vulgaris), которые инвазированы красным тепличным паутинным клещом всех стадий (Tetranychus urticae), обрызгивают препаратом активного соединения желаемой концентрации.
Через 6 дней, определяют эффективность, выраженную в %. 100% означает, что погибли все особи клеща паутинного; 0% означает, что ни одна из особей клеща паутинного не погибла.
В данном испытании, например, следующее соединение примеров получения показывает эффективность 90% при норме внесения 500 г/га: 10
В данном испытании, например, следующие соединения примеров получения показывают эффективность 100% при норме внесения 500 г/га: 1, 2, 3, 4, 5, 6, 7, 8, 9.
Испытание относительно Ctenocephalides felis при пероральной инвазии (CTECFE)
Растворитель: 1 массовая часть диметилсульфоксида
С целью получения пригодного препарата активного соединения, 10 мг активного соединения смешивают с 0.5 мл диметилсульфоксида. Часть концентрата разбавляют цитратной кровью крупного рогатого скота, и получают желаемую концентрацию.
Приблизительно 20 голодных взрослых блох (Ctenocephalides felis) помещают в камеру, которую закрывают сверху и снизу газовой тканью. Металлический цилиндр, нижний конец которого закрыт парафильмом, помещают в камеру. Цилиндр содержит кровь/препарат активного соединения, которые могут поглощаться блохами через мембрану из парафильма. Через 2 дня, определяют мертвых вредителей в %. 100% означает, что погибли все блохи; 0% означает, что ни одна из блох не погибла.
В данном испытании, например, следующее соединение примеров получения показывает при норме внесения 100 ч./млн. действие 80%: 7.
В данном испытании, например, следующие соединения примеров получения показывают, при норме внесения 100 ч./млн. действие 100%: 2, 6, 8, 9, 10.
Испытание относительно Lucilia cuprina (LUCICU)
Растворитель: диметилсульфоксид
Для получения пригодного препарата активного соединения, 10 мг активного соединения смешивают с 0.5 мл диметилсульфоксида, и концентрат разбавляют водой до желаемой концентрации. Сосуды, содержащие мясо лошадей, обработанное препаратом активного соединения желаемой концентрации, заселяют приблизительно 20 личинками Lucilia cuprina.
Через 2 дня, определяют мертвых вредителей в %. 100% означает, что погибли все личинки; 0% означает, что погибших личинок нет.
В данном испытании, например, следующие соединения примеров получения показывают эффективность 100% при норме внесения 100 ч./млн.: 6, 7, 8,9, 10.
Испытание относительно Musca domestica (MUSCDO)
Растворитель: диметилсульфоксид
Для получения пригодного препарата активного соединения, 10 мг активного соединения смешивают с 0.5 мл диметилсульфоксида, и концентрат разбавляют водой до желаемой концентрации. Сосуды, содержащие губку, обработанную препаратом активного соединения желаемой концентрации, заселяют взрослыми Musca domestica.
Через 2 дня, определяют мертвых вредителей в %. 100% означает, что погибли все мухи; 0% означает, что ни одна из мух не погибла.
В данном испытании, например, следующие соединения примеров получения показывают эффективность 100% при норме внесения 100 ч./млн.: 6, 7, 8, 10.
Испытание относительно Boophilus microplus (BOOPMI, инъекция)
Растворитель: диметилсульфоксид
Для получения пригодного препарата активного соединения, 10 мг активного соединения смешивают с 0.5 мл растворителя, и концентрат разбавляют растворителем до желаемой концентрации. Раствор активного соединения инъецируют в брюшную полость (Boophilus microplus), и животных переносят в чашки и содержат в помещении с контролируемой атмосферой. Активность оценивают по откладке оплодотворенных яиц.
Через 7 дней определяют эффективность, выраженную в %. 100% означает, что ни один из клещей не отложил какого-либо количества оплодотворенных яиц.
В данном испытании, например, следующие соединения примеров получения показывают эффективность 100% при норме внесения 20 мкг/животное: 2, 6, 7, 8, 9, 10.
Испытание относительно Boophilus microplus (DIP)
Подопытные животные: взрослые, налитые кровью Boophilus microplus женские особи SP-устойчивого штамма Parkhurst.
Растворитель: диметилсульфоксид
10 мг активного соединения растворяют в 0.5 мл диметилсульфоксида. С целью получения пригодного препарата, раствор активного соединения разбавляют водой до концентрации, желаемой в каждом случае.
Этот препарат активного соединения пипетируют в пробирки. 8-10 клещей переносят в дополнительную пробирку с отверстиями. Пробирку погружают в состав активного соединения, и всех клещей полностью смачивают. После того, как жидкость стечет, клещей переносят на диск фильтра в пластиковые чашки и выдерживают в камере искусственного климата. Активность оценивают через 7 дней по откладке оплодотворенных яиц.
Яйца, фертильность которых не видна внешне, хранят в стеклянных пробирках в шкафу с контролируемой атмосферой до тех пор, пока личинки не вылупятся. Эффективность 100% означает, что ни один из клещей не отложил какого-либо количества оплодотворенных яиц.
В данном испытании, например, следующие соединения примеров получения показывают эффективность 100% при норме внесения 100 ч./млн.: 6, 8,9, 10.
Испытание относительно Amblyomma hebaraeum (AMBYHE)
Растворитель: диметилсульфоксид
Для получения пригодного препарата активного соединения, 10 мг активного соединения смешивают с 0.5 мл диметилсульфоксида, и концентрат разбавляют водой до желаемой концентрации.
Нимф клещей (Amblyomma hebraeum) помещают в перфорированные пластиковые стаканы и погружают в желаемую концентрацию соединения на одну минуту. Клещей переносят на фильтровальную бумагу в чашку Петри и хранят в шкафу с контролируемой атмосферой.
Через 42 дня, определяют мертвых вредителей в %. 100% означает, что погибли все клещи; 0% означает, что ни один из клещей не погиб.
В данном испытании, например, следующее соединение примеров получения показывает при норме внесения 100 ч./млн. действие 100%: 10
В. Сравнительные биологические испытания
Испытание относительно Spodoptera frugiperda (SPODFR, обработка распылением)
Для получения пригодного препарата активного соединения, 1 массовую часть активного соединения смешивают с установленными количествами растворителей и эмульгатора, и концентрат разбавляют водой, содержащей эмульгатор, до желаемой концентрации (в г/га).
Пластинки листьев маиса (Zea mays) обрызгивают составом активного соединения желаемой концентрации и, после сушки, заселяют гусеницами совки (Spodoptera frugiperda).
По истечении желаемого периода времени, определяют действие в %. 100% означает, что погибли все гусеницы; 0% означает, что ни одна из гусениц не погибла.
В данном испытании, например, следующие соединения примеров получения показывают более высокую эффективность по сравнению с известным уровнем техники: см. таблицу
Испытание относительно Myzus (MYZUPE. обработка распылением)
Для получения пригодного препарата активного соединения, 1 массовую часть активного соединения смешивают с установленными количествами растворителей и эмульгатора, и концентрат разбавляют водой, содержащей эмульгатор, до желаемой концентрации (в г/га).
Пластинки листьев пекинской капусты (Brassica pekinensis), инвазированные тлей персиковой зеленой (Myzus persicae) всех стадий, обрызгивают препаратом активного соединения желаемой концентрации.
По истечении желаемого периода времени, определяют действие в %. 100% означает, что погибли все особи тли; 0% означает, что ни одна из особей тли не погибла.
В данном испытании, например, следующие соединения примеров получения показывают более высокую эффективность по сравнению с известным уровнем техники: см. таблицу.
Испытание относительно Phaedon (PHAECO. обработка распылением)
Для получения пригодного препарата активного соединения, 1 массовую часть активного соединения смешивают с установленными количествами растворителей и эмульгатора, и концентрат разбавляют водой, содержащей эмульгатор, до желаемой концентрации (в г/га).
Пластинки листьев пекинской капусты (Brassica pekinensis) обрызгивают препаратом активного соединения желаемой концентрации и, после сушки, заселяют личинками листоеда хренового (Phaedon cochleariae).
По истечении желаемого периода времени, определяют действие в %. 100% означает, что погибли все личинки жука; 0% означает, что ни одна из личинок жука не погибла.
В данном испытании, например, следующие соединения примеров получения показывают более высокую эффективность по сравнению с известным уровнем техники: см. таблицу.
Испытание относительно Tetranychus, ОР-устойчивого (TETRUR, обработка распылением)
Для получения пригодного препарата активного соединения, 1 массовую часть активного соединения смешивают с установленными количествами растворителей и эмульгатора, и концентрат разбавляют водой, содержащей эмульгатор, до желаемой концентрации (в г/га).
Пластинки листьев фасоли (Phaseolus vulgaris), которые инвазированы красным тепличным паутинным клещом всех стадий (Tetranychus urticae), обрызгивают препаратом активного соединения желаемой концентрации.
По истечении желаемого периода времени, определяют действие в %. 100% означает, что погибли все особи клеща паутинного; 0% означает, что ни одна из особей клеща паутинного не погибла.
В данном испытании, например, следующие соединения примеров получения показывают более высокую эффективность по сравнению с известным уровнем техники: см. таблицу.
Испытание относительно Phaedon cochleariae, обработка распылением (РНАЕСО)
Для получения пригодного препарата активного соединения, 1 массовую часть активного соединения смешивают с установленными количествами растворителя и эмульгатора, и концентрат разбавляют водой, содержащей эмульгатор, до желаемой концентрации (в ч./млн.). Если требуется добавление солей аммония или/и пенетрантов, их в каждом случае добавляют к раствору препарата в концентрации 1000 ч./млн.
Листья кочанной капусты (Brassica oleracea), обрызгивают препаратом активного соединения желаемой концентрации, и заселяют личинками листоеда хренового (Phaedon cochleariae).
По истечении желаемого периода времени, определяют мертвых вредителей в %. 100% означает, что погибли все личинки жука; 0% означает, что ни одна из личинок жука не погибла.
В данном испытании, например, следующее соединение примеров получения показывает более высокую эффективность по сравнению с известным уровнем техники: см. таблицу.
Испытание относительно Plutella xylostella, обработка распылением (PLUTMA)
Растворитель: 7 массовых частей диметилформамида
Эмульгатор: 2 массовых частей алкиларилполигликолевого эфира
Для получения пригодного препарата активного соединения, 1 массовую часть активного соединения смешивают с установленными количествами растворителя и эмульгатора, и концентрат разбавляют водой, содержащей эмульгатор, до желаемой концентрации (в ч./млн.). Если требуется добавление солей аммония или/и пенетрантов, их в каждом случае добавляют к раствору препарата в концентрации 1000 ч./млн.
Листья кочанной капусты (Brassica oleracea), обрызгивают препаратом активного соединения желаемой концентрации и инфицируют личинками моли капустной (Plutella xylostella).
По истечении желаемого периода времени, определяют мертвых вредителей в %. 100% означает, что погибли все гусеницы; 0% означает, что ни одна из гусениц не погибла.
В данном испытании, например, следующее соединение примеров получения показывает более высокую эффективность по сравнению с известным уровнем техники: см. таблицу.
Испытание относительно Spodoptera frugiperda, обработка распылением (SPODFR)
Для получения пригодного препарата активного соединения, 1 массовую часть активного соединения смешивают с установленными количествами растворителя и эмульгатора, и концентрат разбавляют водой, содержащей эмульгатор, до желаемой концентрации (в ч./млн.). Если требуется добавление солей аммония или/и пенетрантов, их в каждом случае добавляют к раствору препарата в концентрации 1000 ч./млн.
Листья хлопка (Gossypium hirsutuni) обрызгивают составом активного соединения желаемой концентрации, и заселяют гусеницами совки (Spodopterafrugiperdd).
По истечении желаемого периода времени, определяют мертвых вредителей в %. 100% означает, что погибли все гусеницы; 0% означает, что ни одна из гусениц не погибла.
В данном испытании, например, следующие соединения примеров получения показывают более высокую эффективность по сравнению с известным уровнем техники: см. таблицу.
Испытание относительно Heliothis armigera, обработка распылением (HELIAR)
Для получения пригодного препарата активного соединения, 1 массовую часть активного соединения смешивают с установленными количествами растворителя и эмульгатора, и концентрат разбавляют водой, содержащей эмульгатор, до желаемой концентрации (в ч./млн.). Если требуется добавление солей аммония или/и пенетрантов, их в каждом случае добавляют к раствору препарата в концентрации 1000 ч./млн.
Растения хлопка (Gossypium hirsutum) обрызгивают составом активного соединения желаемой концентрации и, после сушки, заселяют гусеницами совки хлопковой (Heliothis armigerd).
По истечении желаемого периода времени, определяют мертвых вредителей в %. 100% означает, что погибли все гусеницы; 0% означает, что ни одна из гусениц не погибла.
В данном испытании, например, следующее соединение примеров получения показывает более высокую эффективность по сравнению с известным уровнем техники: см. таблицу
Испытание относительно Tetranychus urticae. обработка распылением, ОР-устойчивого (TETRUR)
Для получения пригодного препарата активного соединения, 1 массовую часть активного соединения смешивают с установленными количествами растворителя и эмульгатора, и концентрат разбавляют водой, содержащей эмульгатор, до желаемой концентрации (в ч./млн.). Если требуется добавление солей аммония или/и пенетрантов, их в каждом случае добавляют к раствору препарата в концентрации 1000 ч./млн.
Растения фасоли (Phaseolus vulgaris), которые сильно инвазированы красным тепличным паутинным клещом всех стадий (Tetranychus urticae), обрызгивают препаратом активного соединения желаемой концентрации.
По истечении желаемого периода времени, определяют действие в %. 100% означает, что погибли все особи клеща паутинного; 0% означает, что ни одна из особей клеща паутинного не погибла.
В данном испытании, например, следующие соединения примеров получения показывают более высокую эффективность по сравнению с известным уровнем техники: см. таблицу.
Испытание относительно Nilaparvata lugens, обработка распылением (NILALU)
Для получения пригодного препарата активного соединения, 1 массовую часть активного соединения смешивают с установленными количествами растворителей и эмульгатора, и концентрат разбавляют водой, содержащей эмульгатор, до желаемой концентрации. Если требуется добавление солей аммония или/и пенетрантов, их в каждом случае добавляют к раствору препарата в концентрации 1000 ч./млн. Растения риса (Oryza sativa), обрызгивают препаратом активного соединения желаемой концентрации, и затем заселяют личинками коричневого дельфацида (Nilaparvata lugens).
По истечении желаемого периода времени, определяют действие в %. 100% означает, что погибли все особи дельфацида; 0% означает, что ни одна из особей дельфацида не погибла.
В данном испытании, например, следующие соединения примеров получения показывают более высокую эффективность по сравнению с известным уровнем техники: см. таблицу.
Испытание относительно Frankliniella occidentalis, обработка распылением (FRANOC)
7 массовых частей диметилформамида
Для получения пригодного препарата активного соединения, 1 массовую часть активного соединения смешивают с установленными количествами растворителей и эмульгатора, и концентрат разбавляют водой, содержащей эмульгатор, до желаемой концентрации. Если требуется добавление солей аммония или/и пенетрантов, их в каждом случае добавляют к раствору препарата в концентрации 1000 ч./млн. Пластинки листьев фасоли обыкновенной (Phaseolus vulgaris), обрызгивают препаратом активного соединения желаемой концентрации, и затем инфицируют смешанной популяцией трипсов (Frankliniella occidentalis).
По истечении желаемого периода времени, определяют действие в %. 100% означает, что погибли все трипсы; 0% означает, что ни одна из особей трипсов не погибла.
В данном испытании, например, следующие соединения примеров получения показывают более высокую эффективность по сравнению с известным уровнем техники: см. таблицу.
Испытание относительно Liriomyza trifolii, обработка распылением (LIRITR)
Для получения пригодного препарата активного соединения, 1 массовую часть активного соединения смешивают с установленными количествами растворителей и эмульгатора, и концентрат разбавляют водой, содержащей эмульгатор, до желаемой концентрации. Если требуется добавление солей аммония или/и пенетрантов, их в каждом случае добавляют к раствору препарата в концентрации 1000 ч./млн. Пластинки листьев фасоли (Phaseolus vulgaris), которые инвазированы личинками минирующей мухи (Liriomyza trifolii), обрызгивают препаратом активного соединения желаемой концентрации.
По истечении желаемого периода времени, определяют действие в %. 100% означает, что погибли все минирующие мухи; 0% означает, что ни одна из минирующих мух не погибла.
В данном испытании, например, следующие соединения примеров получения показывают более высокую эффективность по сравнению с известным уровнем техники: см. таблицу.
Испытание относительно Ctenocephalides felis при пероральной инвазии (CTECFE)
Растворитель: 1 массовая часть диметилсульфоксида
С целью получения подходящего препарата активного соединения, 10 мг активного соединения смешивают с 0.5 мл диметилсульфоксида. Часть концентрата разбавляют цитратной кровью крупного рогатого скота, и получают желаемую концентрацию.
Приблизительно 20 голодных взрослых блох (Ctenocephalides fells) помещают в камеру, которую закрывают сверху и снизу газовой тканью. Металлический цилиндр, нижний конец которого закрыт парафильмом, помещают в камеру. Цилиндр содержит кровь/препарат активного соединения, которые могут поглощаться блохами через мембрану из парафильма.
По истечении желаемого периода времени, определяют мертвых вредителей в %. 100% означает, что погибли все блохи; 0% означает, что ни одна из блох не погибла.
В данном испытании, например, следующие соединения примеров получения показывают более высокую эффективность по сравнению с известным уровнем техники: см. таблицу.
Испытание относительно Musca domestica (MUSCDO)
Растворитель: диметилсульфоксид
Для получения пригодного препарата активного соединения, 10 мг активного соединения смешивают с 0.5 мл диметилсульфоксида, и концентрат разбавляют водой до желаемой концентрации.
Сосуды, содержащие губку, обработанную составом активного соединения желаемой концентрации, заселяют взросльми Musca domestica.
По истечении желаемого периода времени, определяют мертвых вредителей в %. 100% означает, что погибли все мухи; 0% означает, что ни одна из мух не погибла.
В данном испытании, например, следующие соединения примеров получения показывают более высокую эффективность по сравнению с известным уровнем техники: см. таблицу.
Испытание относительно Boophilus microplus (DIP)
Подопытные животные: взрослые налитые кровью Boophilus microplus женские особи SP-устойчивого штамма Parkhurst
Растворитель: диметилсульфоксид
10 мг активного соединения растворяют в 0.5 мл диметилсульфоксида. С целью получения пригодного препарата, раствор активного соединения разбавляют водой до концентрации, желаемой в каждом случае (в ч./млн.).
Этот препарат активного соединения пипетируют в пробирки. 8-10 клещей переносят в дополнительную пробирку с отверстиями. Пробирку погружают в состав активного соединения, и всех клещей полностью смачивают.После того, как жидкость стечет, клещей переносят на диск фильтра в пластиковые чашки и содержат в помещении с контролируемой атмосферой.
Активность оценивают по истечении желаемого времени по откладке оплодотворенных яиц. Яйца, фертильность которых не видна внешне, хранят в стеклянных пробирках в шкафу с контролируемой атмосферой до тех пор, пока личинки не вылупятся. Действие 100% означает, что ни один из клещей не отложил какого-либо количества оплодотворенных яиц.
В данном испытании, например, следующие соединения примеров получения показывают более высокую эффективность по сравнению с известным уровнем техники: см. таблицу.
Испытание относительно Boophilus microplus (BOOPMI, инъекция)
Растворитель: диметилсульфоксид
Для получения пригодного препарата активного соединения, 10 мг активного соединения смешивают с 0.5 мл растворителя, и концентрат разбавляют растворителем до желаемой концентрации (в мкг/животное).
Раствор активного соединения инъецируют в брюшную полость (Boophilus microplus), и животных переносят в чашки и содержат в помещении с контролируемой атмосферой.
Через 7 дней определяют эффективность, выраженную в %. Активность оценивают по откладке оплодотворенных яиц. 100% означает, что ни один из клещей не отложил какого-либо количества оплодотворенных яиц.
В данном испытании, например, следующие соединения примеров получения показывают более высокую эффективность по сравнению с известным уровнем техники: см. таблицу.
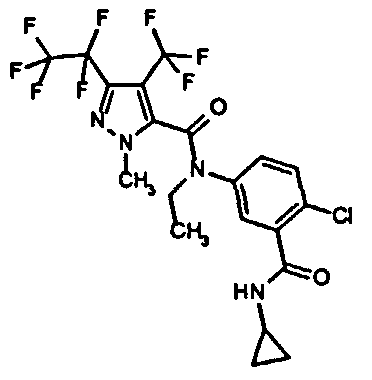
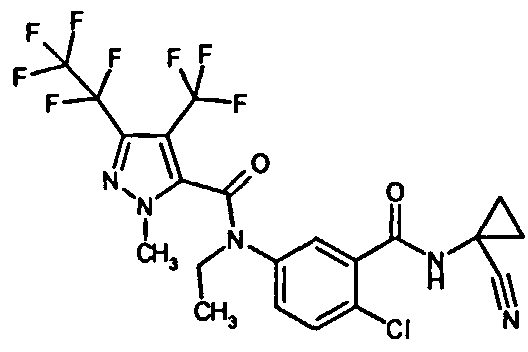
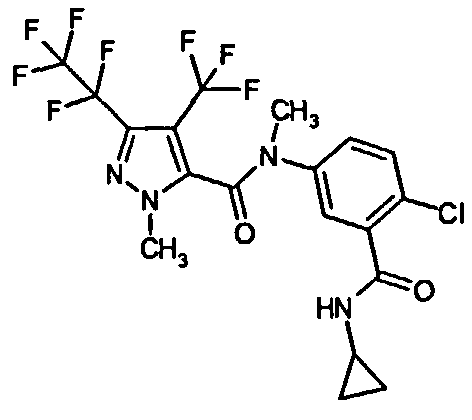
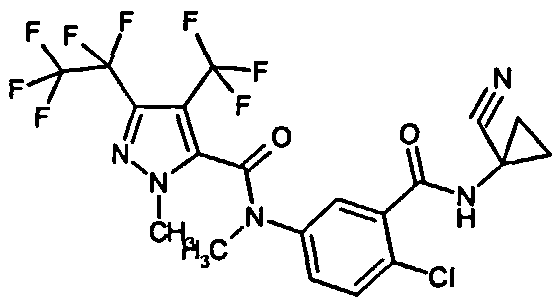
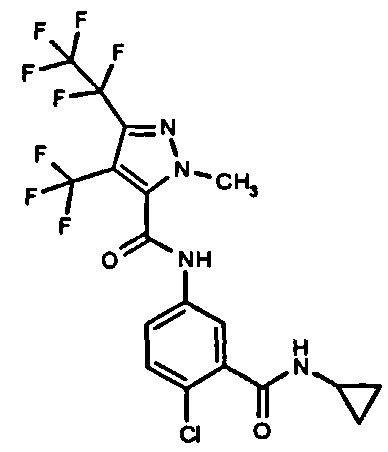
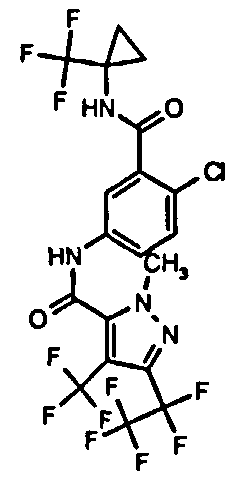
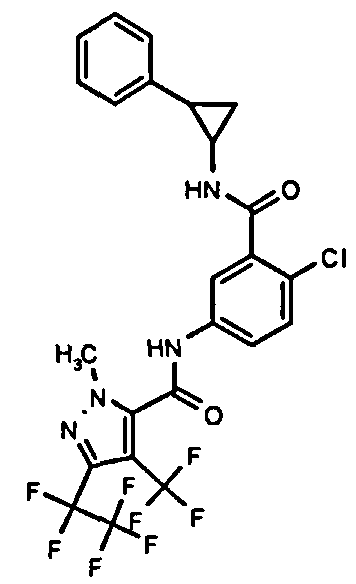
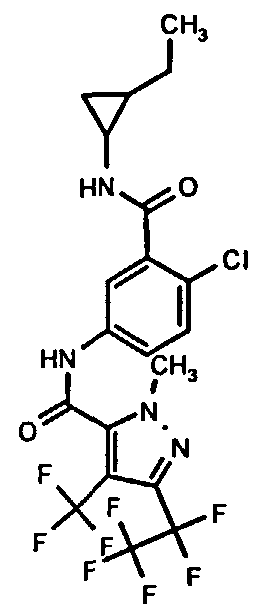
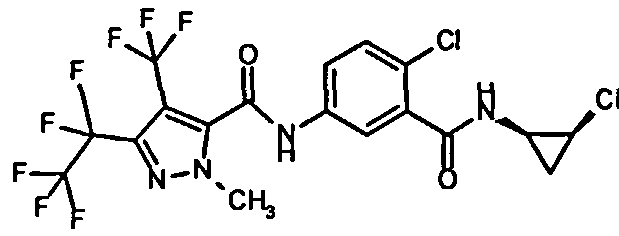
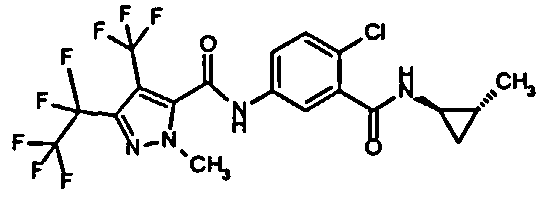
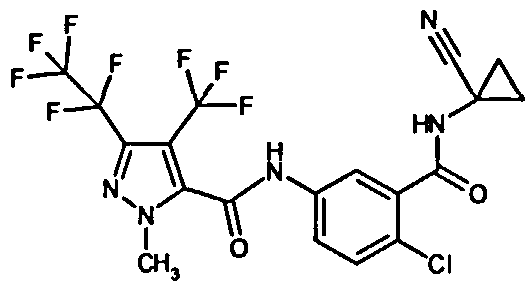
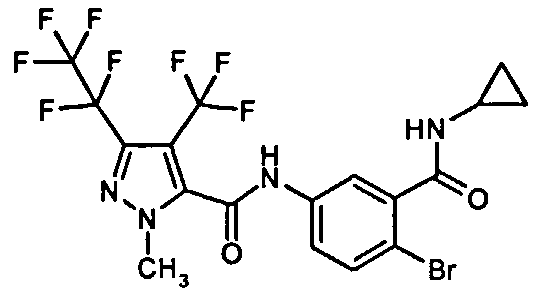
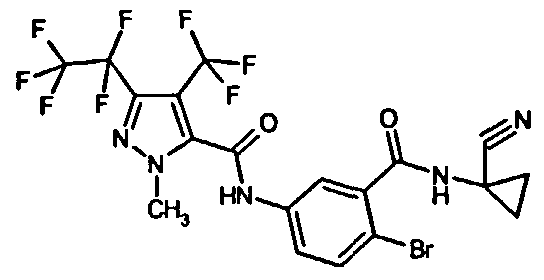
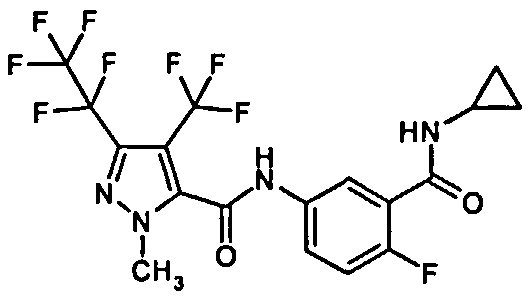
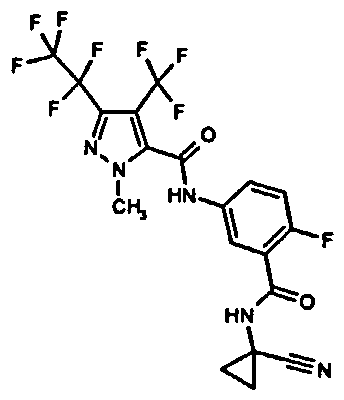
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНСЕКТИЦИДНЫЕ АРИЛПИРРОЛИДИНЫ | 2008 |
|
RU2473541C9 |
| ГЕТЕРОАРИЛ-ТРИАЗОЛЬНЫЕ И ГЕТЕРОАРИЛ-ТЕТРАЗОЛЬНЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ПЕСТИЦИДОВ | 2019 |
|
RU2807086C2 |
| СОЕДИНЕНИЕ, КОМПОЗИЦИЯ ДЛЯ БОРЬБЫ С НАСЕКОМЫМИ, СПОСОБЫ БОРЬБЫ С НАСЕКОМЫМИ | 2002 |
|
RU2298007C2 |
| НОВЫЕ ГЕТЕРОАРИЛТРИАЗОЛЬНЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ПЕСТИЦИДОВ | 2020 |
|
RU2824488C2 |
| АМИДЫ АНТРАНИЛОВОЙ КИСЛОТЫ В КОМБИНАЦИИ С ФУНГИЦИДАМИ | 2011 |
|
RU2578801C2 |
| ПРИМЕНЕНИЕ N-ФУНКЦИОНАЛИЗИРОВАННЫХ АЛКОКСИПИРАЗОЛЬНЫХ СОЕДИНЕНИЙ В КАЧЕСТВЕ ИНГИБИТОРОВ НИТРИФИКАЦИИ | 2023 |
|
RU2838138C2 |
| СОЕДИНЕНИЕ 4Н-ПИРРОЛОПИРИДИНА ИЛИ ЕГО СОЛЬ, СЕЛЬСКОХОЗЯЙСТВЕННЫЙ И САДОВОДЧЕСКИЙ ИНСЕКТИЦИД, ВКЛЮЧАЮЩИЙ УКАЗАННОЕ СОЕДИНЕНИЕ ИЛИ ЕГО СОЛЬ, И СПОСОБ ПРИМЕНЕНИЯ ИНСЕКТИЦИДА | 2017 |
|
RU2756207C2 |
| БИСАМИДНЫЕ ПРОИЗВОДНЫЕ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНСЕКТИЦИДНЫХ СОЕДИНЕНИЙ | 2008 |
|
RU2515966C2 |
| ПРИМЕНЕНИЕ N-ФУНКЦИОНАЛИЗИРОВАННЫХ АЛКОКСИПИРАЗОЛЬНЫХ СОЕДИНЕНИЙ В КАЧЕСТВЕ ИНГИБИТОРОВ НИТРИФИКАЦИИ | 2019 |
|
RU2797246C2 |
| ГЕРБИЦИДНЫЕ ЗАМЕЩЕННЫЕ ПИРИМИДИНИЛОКСИБЕНЗОЛЬНЫЕ СОЕДИНЕНИЯ | 2014 |
|
RU2703460C1 |
Изобретение относится к соединениям общей формулы (I), в которой радикалы A1, А2, А3, А4, L, Q, R1, Т и W имеют значение, приведенное в описании, и к применению соединений для борьбы с животными-вредителями. Кроме того, изобретение относится к способам и промежуточным соединениям для получения соединений формулы (I). 8 н. и 2 з.п. ф-лы, 2 табл., 256 пр.
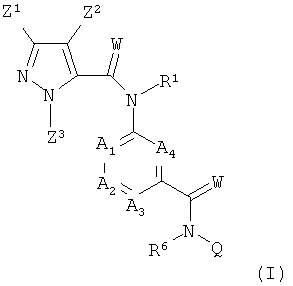
1. Соединения общей формулы (I)
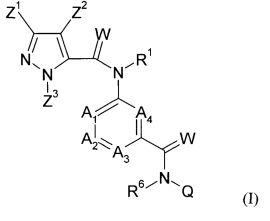
в которой
Z1 означает трифторметил, 1-хлорциклопропил, 1-фторциклопропил или пентафторэтил,
Z2 означает трифторметил, нитро, метилтио, метилсульфинил, метилсульфонил, фтор, хлор, бром или йод,
Z3 означает метил, этил, н-пропил или водород,
R1 означает водород, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, метоксиметил, этоксиметил, пропоксиметил, метилкарбонил, этилкарбонил, н-пропилкарбонил, изопропилкарбонил, втор-бутилкарбонил, трет-бутилкарбонил, метоксикарбонил, этоксикарбонил, н-пропоксикарбонил, изопропоксикарбонил, втор-бутоксикарбонил, трет-бутоксикарбонил, цианометил, 2-цианоэтил, бензил, 4-метоксибензил, пирид-2-илметил, пирид-3-илметил, пирид-4-илметил, 4-хлорпирид-3-илметил,
А1, А2 и А4 означают СН,
A3 означает CR4 и
R4 означает фтор, хлор, бром или йод,
R6 означает водород, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил,
W означает кислород и
Q означает 1-цианоциклопропил.
2. Соединения общей формулы (I) по п. 1, в которой
Z1 означает трифторметил, 1-хлорциклопропил, 1-фторциклопропил или пентафторэтил,
Z2 означает трифторметил или хлор,
Z3 означает метил,
R1 означает водород, метил, этил,
А1, А2 и А4 означают СН,
А3 означает CR4 и
R4 означает хлор,
R6 означает водород, метил, этил,
W означает кислород и
Q означает 1-цианоциклопропил.
3. Применение соединений общей формулы (I) по любому из пп. 1-2 для борьбы с насекомыми, паукообразными и нематодами для защиты растений.
4. Фармацевтические композиции для борьбы с животными-вредителями, содержащие по меньшей мере одно соединение по любому из пп. 1-2.
5. Соединения по любому из пп. 1-2 для применения в качестве лекарственных средств для борьбы с животными-вредителями.
6. Способ получения композиций для защиты сельскохозяйственных культур, включающих соединения общей формулы (I) по любому из пп. 1-2 и обычные наполнители и/или поверхностно-активные вещества.
7. Способ борьбы с вредителями на растениях или семенах, отличающийся тем, что обеспечивают действие соединения общей формулы (I) по любому из пп. 1-2 на вредителей и/или их место распространения.
8. Применение соединений общей формулы (I) по любому из пп. 1-2 для защиты материала для размножения растений, в частности семян.
9. Соединения общих формул (IVa) и (IVb),
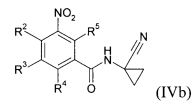
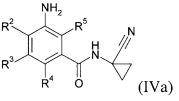
в которых
R2, R3 и R5 означают водород и
R4 означает фтор, хлор, бром или йод.
10. Соединения общих формул (Va) и (Vb),
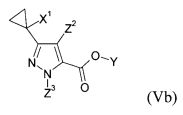
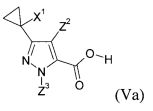
в которых
X1 означает фтор или хлор,
Z2 означает трифторметил, нитро, метилтио, метилсульфинил, метилсульфонил, фтор, хлор, бром или йод,
Z3 означает метил, этил, н-пропил или водород,
Y означает C1-С6-алкил.
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| EP 1911751 A1, 20.06.2008 | |||
| ИНСЕКТИЦИДНЫЕ АНТРАНИЛАМИДЫ | 2001 |
|
RU2278852C2 |
| УСТРОЙСТВО, СИГНАЛИЗИРУЮЩЕЕ О ВЫВИНЧИВАНИИ ЭЛЕКТРИЧЕСКОЙ ЛАМПОЧКИ | 1924 |
|
SU2278A1 |
Авторы
Даты
2016-10-27—Публикация
2012-03-12—Подача