Область техники
Изобретение относится к области медицины и химико-фармацевтической промышленности и касается способа получения новой фармацевтической композиции эритромицина в виде капсул для использования в качестве антибиотика широкого спектра действия.
Уровень техники
Известны шесть разновидностей эритромицина, которые обозначаются латинскими буквами от А до F. Из них только эритромицин А используется в клинической практике. Химическая структура препарата включает макроциклическое лактонное кольцо, содержащее 14 атомов углерода, к которому присоединены два углеводных остатка - дезозаминоза и кладиноза. Эритромицин представляет собой слабое основание, плохо растворимое в воде (ГФ XII, ч. 1, с. 92), которое быстро разрушается под действием соляной кислоты.
Эритромицин обладает широким спектром антимикробной активности, который включает многие грамположительные кокки (стрептококки, стафилококки) и палочки, некоторые грамотрицательные микроорганизмы, спирохеты, хламидии, микоплазмы, легионеллы, анаэробы.
Эритромицин высоко активен in vitro против большинства штаммов β-гемолитического стрептококка группы A (S.pyogenes), стрептококка группы В (S.agalactiae) и пневмококка. Зеленящий стрептококк (S.viridans) умеренно чувствителен к данному антибиотику.
К эритромицину чувствительны золотистый (S. aureus) и эпидермальный (S.epidermidis) стафилококки, включая штаммы, устойчивые к пенициллину.
Эритромицин действует на коринебактерии (C.diphtheriae, C.haemolyticum, C.minutissimum), листерии (L.monocytogenes) и возбудителя сибирской язвы (B.antracis).
К эритромицину чувствительны гонококки, менингококки и M.catarrhalis. Эритромицин активен против возбудителя коклюша (B.pertussis), легионелл (L.pneumophila, L.micdadei), возбудителя мягкого шанкра (H.ducreyi). К нему чувствительны более 90% штаммов кампилобактера (C.jejuni). Несколько слабее эритромицин действует на Н.influenzae. Эритромицин умеренно активен против бледной спирохеты (T.pallidum) и боррелий (B.burgdorferi). Эритромицин в 50 раз более активен против M.pneumoniae, чем тетрациклин. Среди хламидий к эритромицину наиболее чувствительны С.trachomatis и С.pneumoniae. Активность его против C.psittaci несколько ниже. Эритромицин умеренно активен против некоторых клостридий (C.perfringens) и неспорообразующих анаэробов, включая анаэробные стрептококки и бактероиды, в том числе отдельные штаммы B.fragilis. Кроме того, эритромицин действует на P.acnes. Эритромицин обладает постантибиотическим эффектом против S.pneumoniae, S.aureus и L.pneumophila. При длительном поддержании суб-МПК концентраций эритромицин оказывает бактерицидное действие на P. aeruginosa.
Первоначально эритромицин выпускался только в виде основания. Как уже было указано выше, он является кислотолабильным соединением и при приеме внутрь может в разной степени инактивироваться под влиянием соляной кислоты желудка. На всасывание эритромицина оказывают влияние скорость опорожнения желудка и пища. Поэтому биодоступность препарата при оральном приеме невысока и ее степень может изменяться у различных больных, результатом чего является вариабельность концентрации антибиотика в крови.
Для повышения стабильности в желудочно-кишечном тракте и улучшения всасывания впоследствии были разработаны и внедрены в клиническую практику особые кишечнорастворимые лекарственные формы эритромицина основания, а также его соли, эфиры и соли эфиров. Всего насчитывается более 15 различных препаратов эритромицина для приема внутрь.
Следует учитывать, что антибактериальной активностью обладает только эритромицин основание. Стеаратная соль и эфиры эритромицина микробиологически неактивны. При приеме внутрь эритромицина стеарата в двенадцатиперстной кишке происходит диссоциация соли и эритромицин всасывается в виде основания. Эритромицина эстолат и этилсукцинат всасываются в неактивном состоянии, после чего происходит гидролиз эфиров с постепенным высвобождением эритромицина основания. Эфиры эритромицина можно принимать во время и после еды, причем биодоступность эстолата под влиянием пищи даже возрастает.
Известны недавно разработанные эфиры и соли эритромицина (ацистрат, стинопрат), обладающие повышенной кислотоустойчивостью, улучшенной биодоступностью и способностью создавать более высокие концентрации в крови, однако они, как и другие эфиры, имеют ограниченное применение из-за неблагоприятных воздействий на организм.
Описано также применение эритромицина основания в виде пеллет (кишечнорастворимых шариков диаметром 0,5-1,5 мм), всасывание антибиотика более стабильное, чем при приеме кишечнорастворимых таблеток, и отмечаются более высокие концентрации эритромицина в крови. Это может быть связано с тем, что пеллеты, в отличие от таблеток, не задерживаются в пилорическом отделе желудка.
Ускоренным всасыванием и повышенной биодоступностью характеризуются кишечнорастворимые гранулы эритромицина основания - отечественный препарат "эригран", который был разработан Государственным научным центром по антибиотикам.
И хотя все диспергируемые формы эритромицина обеспечивают его быстрое высвобождение, потенциальные возможности препарата (по сравнению с активностью in vitro) в плане его эффективности используются всего на 30-50%. В связи с этим приходится использовать его в больших дозах до 4 г в день.
Описание изобретения
Задачей настоящего изобретения является создание технологичного способа получения твердой лекарственной формы фармацевтической композиции эритромицина с высокой биодоступностью, достаточной для существенного снижения дозы препарата и стабильной концентрации эритромицина в крови.
Поставленная задача решена способом получения лекарственной формы эритромицина в виде кишечнорастворимых капсул, внутри которых находится фармацевтическая композиция с инновационным качественным и количественным составом.
Технический результат достигается способом получения фармацевтической композиции для лечения бактериальных или протозойных инфекционных заболеваний в виде кишечнорастворимых капсул на основе эритромицина, в котором эритромицин смешивают с плюроником в соотношении 70:30, микронизируют полученную смесь, добавляют вспомогательные вещества, после чего проводят повторную микронизацию и наполняют полученной смесью желатиновые капсулы.
В качестве плюроника используют Колифор Р 188 (Лутрол F 68), Колифор Р 407 (Лутрол F 127) или их смесь.
При этом в качестве эритромицина предпочтительно используют основание или его фармацевтически приемлемые соли.
В качестве вспомогательных веществ используют лактозу, крахмал, стеариновую кислоту и/или ее кальциевые или магниевые соли, микрокристаллическую целлюлозу.
Желатиновая капсула 0,5 мг для лечения бактериальных или протозойных инфекционных заболеваний предпочтительно имеет следующий состав, в г/капсулу:
Предпочтительно все компоненты смеси предварительно перед гомогенизацией подвергают микронизации с просеиванием на сите 0,5 мм.
Пероральный способ применения препаратов является наиболее предпочтительным, поскольку он содержит целый ряд преимуществ перед другими способами дозирования, таких как наибольший комфорт для пациента, возможность применения гибких схем лечения, а также низкую стоимость лечения. Однако биологическая доступность многих лекарственных средств при пероральном применении сильно ограничена из-за их очень низкой растворимости и низкой степени абсорбции в тонком кишечнике. Освобождение биологически активного вещества определяется скоростью дезинтеграции лекарственной формы и временем растворения вещества в биологических жидкостях.
Оценка биодоступности является одним из важнейших этапов процесса разработки и внедрения новых лекарственных форм биологически активных соединений. Главное внимание при создании лекарственных форм сосредоточено на создании условий, обеспечивающих увеличение биодоступности препарата.
Капсулы предназначены для перорального, реже ректального, вагинального путей введения.
В зависимости от локализации оральные капсулы подразделяются на сублингвальные, желудочнорастворимые и кишечнорастворимые (устойчивые к действию желудочного сока, но легко разрушающиеся в среде тонкого кишечника).
Капсулы с модифицированным высвобождением имеют в составе содержимого или оболочки специальные вспомогательные вещества, предназначенные для изменения скорости или места высвобождения действующих веществ. Кишечнорастворимые капсулы также относятся к средствам с модифицированным высвобождением, которые должны быть устойчивы в желудочном соке и высвобождать действующие вещества в кишечнике. Они могут быть изготовлены покрытием твердых или мягких капсул кислотоустойчивой оболочкой или методом наполнения капсул гранулами или пеллетами, покрытыми кислотоустойчивыми оболочками.
В настоящее время лекарственная форма в виде желатиновых капсул стала очень популярной у производителей фармацевтических препаратов, потребителей и врачей благодаря целому ряду преимуществ и положительных характеристик. К ним, в частности, относятся:
- высокая точность дозирования помещаемых в них лекарственных веществ. Современное оборудование обеспечивает высокую точность заполнения капсул наполнителем (с допуском, не превышающим ±3%) и минимальные потери;
- высокая биологическая доступность. Исследования показали, что капсулы зачастую быстрее распадаются в организме человека, чем таблетки или драже, а их жидкое или неспресованное твердое содержимое быстрее и легче абсорбируется. Фармакологическое действие лекарственного вещества проявляется через 4-5 мин;
- высокая стабильность. Лекарственные вещества в капсулах защищены от различных неблагоприятных факторов внешней среды - воздействия света, воздуха, влаги, механических воздействий - благодаря оболочке, которая обеспечивает достаточно высокую герметичность и изоляцию компонентов. Поэтому при изготовлении капсул можно избежать необходимости применения антиоксидантов или стабилизаторов либо снизить их количество;
- корригирующая способность - исключается неприятный вкус и запах лекарственных веществ, что особенно важно в педиатрии;
- высокая эстетичность - достигается благодаря применению различных красителей при получении оболочек капсул. Сегодня ведущими фармацевтическими фирмами применяется до 1000 различных цветов и оттенков для окрашивания оболочек капсул;
- возможность задавать лекарственным веществам определенные свойства - создание кишечнорастворимых капсул, а также капсул-ретард (с пролонгированным высвобождением лекарственного средства), что может достигаться различными технологическими приемами;
- меньшее количество вспомогательных веществ при изготовлении капсул, чем, например, при производстве таблеток.
Кроме того, для изготовления капсул требуется меньшее количество машинного оборудования в связи с уменьшением этапов производства, меньшее количество применяемых аналитических методик при проведении необходимых анализов и меньшее количество разрешительных процедур и документов, чем при производстве таблеток.
В капсулы можно фасовать препараты в неизменном виде, не подвергая их влажной грануляции, тепловому воздействию, давлению, как при производстве таблеток. Кроме того, число факторов, влияющих на процессы высвобождения и всасывания ЛВ из капсул, значительно меньше, чем для других лекарственных форм.
Биополимеры (широко используются в медицине и фармацевтике и могут обеспечить внутриклеточную доставку нужных препаратов (активных фармацевтических субстанций) для лечения различных заболеваний.
Способ получения нового типа биодеградирующих материалов не представляет трудностей, а продукты разложения могут свободно транспортироваться через клеточные мембраны, что позволяет использовать полимеры в качестве средств доставки лекарств.
Блок-сополимеры оксиэтилена и оксипропилена также известны под названием «Плюроник». Гидрофобно-гидрофильные свойства плюроников и их способность солюбилизировать водонерастворимые соединения определяются размерами и соотношением полиоксиэтиленового (гидрофильного) и полиоксипропиленового (гидрфобного) блоков.
Несмотря на то, что указанные блок-сополимеры широко используются в фармацевтических и косметических композициях, в том числе, и для увеличения растворимости гидрофобных водонерастворимых соединений требуется индивидуальное решение при их использовании для каждого конкретного лекарства. Точные механизмы взаимодействия разных поверхностно-активных полимеров с различными транспортерами и их комбинациями, ограничивающими биодоступность разных лекарств, в настоящее время не установлены, и композиция, оказавшая положительный эффект на биодоступность одного активного вещества, может оказаться неэффективной для другого и наоборот.
Более высокую биодоступность обеспечивают блок-сополимеры оксиэтилена и оксипропилена, в которых содержание гидрофобного блока составляет менее 50 масс. %, а молекулярная масса гидрофильного блока составляет 2250 Да и более. Экспериментальным путем было найдено, что наилучшие результаты по увеличению растворимости эритромицина показали поверхностно-активные полимеры, так называемые плюроники или полоксамеры, а именно доступные в настоящее время продукты марок Kolliphor Р (BASF) выпускаются в гранулированном виде со средним размером частиц около 1000 мк: Kolliphor Р 407 (Колифор Р 407) и Kolliphor Р 188 (Колифор Р 188) или их старые наименования соответственно LUTROL F 68 (Лутрол F 68) и LUTROL F 127 (Лутрол F 127), которые и использовались для создания новой фармацевтической композиции эритромицина.
Используемые лактоза и крахмал являются наполнителями, обеспечивающими необходимую скорость растворения и всасывания.
Стеариновая кислота и/или ее кальциевые или магниевые соли используются по своему традиционному назначению как опудривающие и смазывающие агенты.
Существенным для улучшения технологического процесса в данном изобретении является получение гранулометрического состава с определенными размерами из микронизированных порошков субстанций как активного, так и вспомогательных веществ.
Известно, что измельчение (или микронизация) субстанций влияет на биодоступность. Однако оно также приводит к увеличению свободной энергии и соответственно может служить причиной снижения стабильности при хранении. Нами установлено, что, если использовать и активное начало и все вспомогательные вещества с заявленными средними размерами частиц, возможно значительное улучшение текучести, получение оптимальной насыпной плотности и увеличение биодоступности эритромицина.
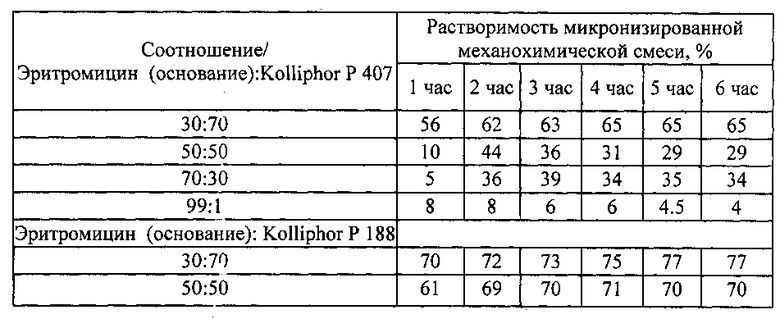
Иллюстрация процесса растворения эритромицина основания в воде с добавлением полоксамеров Kolliphor Р 407 (LUTROL F 127) и Kolliphor Р 188 (LUTROL F 68).
Примеры конкретного осуществления изобретения
Реализации заявляемого изобретения показана в примерах конкретного выполнения, но не ограничивается этими примерами.
Пример 1
Твердые желатиновые капсулы наполняют технологической смесью, полученной с использованием следующих ингредиентов, в мг на капсулу:
В загрузочный бункер мельницы засыпают эритромицин (основание) и Колифор Р 188 и измельчают до размера частиц, проходящих через сито с диаметром отверстий 0,5 мм. Затем перегружают полученную субстанцию в смеситель-гомогенизатор, добавляют лактозу и тщательно перемешивают в течение 5 минут. Далее к полученной массе добавляют крахмал кукурузный и целлюлозу микрокристаллическую и вновь перемешивают в течение 5 мин при той же скорости вращения. В конце процесса добавляют магния стеарат и вновь перемешивают в течение 3-4 мин. Полученную технологическую смесь микронизируют с использованием мельницы с одновременным просеиванием через сито с диаметром отверстий 0,5 мм, установленным на мельнице. Проверяют влажность и сыпучесть полученного порошка и заполняют им твердые желатиновые капсулы.
Твердые желатиновые капсулы наполняют технологической смесью, полученной с использованием следующих ингредиентов, в мг на капсулу:

Пример 2
Все компоненты смеси предварительно перед гомогенизацией подвергают микронизации с просеиванием на сите 0,5 мм. Далее, как в примере 1, получают механохимическую смесь нижеуказанного состава, дополнительно микронизируют и проверяют влажность и сыпучесть полученного порошка, затем заполняют им твердые желатиновые капсулы. Состав для заполнения капсул следующий, в мг/капсулу:
Пример 3
Твердые желатиновые капсулы получают, как в примере 1, используя следующие ингредиенты в количестве, мг/капсула:
| название | год | авторы | номер документа |
|---|---|---|---|
| ТВЕРДАЯ ПЕРОРАЛЬНАЯ ЛЕКАРСТВЕННАЯ ФОРМА ИНДОЛ-3-КАРБИНОЛА | 2022 |
|
RU2787538C1 |
| ТВЕРДАЯ ЛЕКАРСТВЕННАЯ ФОРМА ИНДОЛ-3-КАРБИНОЛА | 2017 |
|
RU2680967C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ АДЕМЕТИОНИНА И ЕГО ЛЕКАРСТВЕННОЙ ФОРМЫ | 2015 |
|
RU2587331C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАПСУЛ ДИКЛОФЕНАКА | 2015 |
|
RU2602681C1 |
| Пероральная фармацевтическая композиция диуретика и ингибитора АПФ в микронизированной форме, лекарственное средство и его применение | 2012 |
|
RU2618471C2 |
| ПРОТИВОГРИБКОВЫЙ СОСТАВ С ПОВЫШЕННОЙ БИОДОСТУПНОСТЬЮ | 1997 |
|
RU2207119C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТАБЛЕТОК ЭРИТРОМИЦИНА | 2009 |
|
RU2403049C1 |
| ТВЕРДАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ПРОИЗВОДНЫЕ БЕНЗОФУРАНА | 1998 |
|
RU2191578C2 |
| ПЕРОРАЛЬНЫЙ ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ НА ОСНОВЕ ГИНДАРИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2007 |
|
RU2360675C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ В ВИДЕ ТВЕРДОЙ ПЕРОРАЛЬНОЙ ЛЕКАРСТВЕННОЙ ФОРМЫ, СОДЕРЖАЩАЯ СИГЕТИН (ВАРИАНТЫ) | 2007 |
|
RU2338523C1 |
Изобретение относится к области медицины и химико-фармацевтической промышленности и касается способа получения новой фармацевтической композиции эритромицина в виде капсул для использования в качестве антибиотика широкого спектра действия. Способ получения фармацевтической композиции для лечения бактериальных или протозойных инфекционных заболеваний в виде кишечнорастворимых капсул на основе эритромицина включает смешивание эритромицина основания или его фармацевтически приемлемой соли с плюроником в соотношении 70:30, микронизацию полученной смеси, добавление вспомогательных веществ, повторную микронизацию и наполнение полученной смесью желатиновых капсул. В качестве плюроника используют Колифор Р 188, Колифор Р 407 или их смесь. Способ является высокотехнологичным, а полученная композиция и ее лекарственная форма имеет высокую биодоступность около 70%, достаточную для существенного снижения дозы препарата (до 2 г в сутки) и поддержания стабильной концентрации эритромицина в крови. 5 з.п. ф-лы, 3 пр., 2 табл.
1. Способ получения фармацевтической композиции для лечения бактериальных или протозойных инфекционных заболеваний в виде кишечнорастворимых капсул на основе эритромицина, отличающийся тем, что эритромицин смешивают с плюроником в соотношении 70:30, микронизируют полученную смесь, добавляют вспомогательные вещества, после чего проводят повторную микронизацию и наполняют полученной смесью желатиновые капсулы, а в качестве плюроника используют Колифор Р 188, Колифор Р 407 или их смесь.
2. Способ по п. 1, отличающийся тем, что в качестве эритромицина используют основание или его фармацевтически приемлемые соли.
3. Способ по п. 1, отличающийся тем, что в качестве вспомогательных веществ используют лактозу, крахмал, стеариновую кислоту и/или ее кальциевые или магниевые соли, микрокристаллическую целлюлозу.
4. Способ по п. 1, отличающийся тем, что желатиновая капсула 0,5 мг для лечения бактериальных или протозойных инфекционных заболеваний предпочтительно имеет следующий состав, в г/капсулу:
5. Способ по п. 1, отличающийся тем, что микронизацию осуществляют размолом с одновременным просеиванием на сите 0,5 мм.
6. Способ по п. 1, отличающийся тем, что предварительно все компоненты смеси подвергают микронизации с просеиванием на сите 0,5 мм.
| ГИДРАТЫ СОЛЕЙ ЭРИТРОМИЦИНА, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2009 |
|
RU2510659C2 |
| Н.А | |||
| ШАТОВА и др | |||
| Полоксамеры как инновационные вспомогательные вещества// Научно-производственный журнал: Разработка и регистрация лекарственных средств | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Способ окисления боковых цепей ароматических углеводородов и их производных в кислоты и альдегиды | 1921 |
|
SU58A1 |
| К | |||
| В | |||
| АЛЕКСЕЕВ и др | |||
| Технология повышения биологической и фармацевтической доступности лекарственных веществ//Вестник новых медицинский | |||
Авторы
Даты
2016-10-27—Публикация
2015-06-19—Подача