Предлагаемое изобретение относится к органической химии, в частности к способу получения N-(1,5,3-дитиазепан-3-ил)карбоновых кислот общей формулы (1)
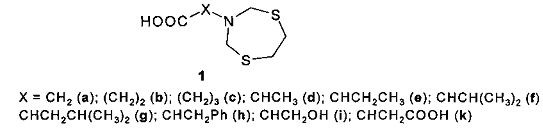
Соединения общей формулы (1) могут быть использованы в качестве биоцидов - специальных реагентов для подавления жизнедеятельности сульфатвосстанавливающих бактерий в различных технологических средах [Кунакова Р.В., Хафизова С.Р., Дальнова Ю.С. и др. Нефтехимия. 2002, 42, 5, 382 [Petroleum Chemistry, 2002, 42, 347 (Engl. Transl.)]], сорбентов палладия(II) и серебра(I) [В.Р. Ахметова, Г.Р. Анпилогова, Г.Р. Хабибуллина, Н.С. Ахмадиев, А.Г. Ибрагимов. Однореакторный синтез бис-1,5,3-дитиазепанов и их сорбционные свойства по отношению к серебру(I) и палладию(II). Журнал прикладной химии. 2014, том 87, вып. 5, с. 595-600] и линкеров фотолабильных молекулярных систем [Alexei N. Kurchan, Andrei G. Kutateladze. Amino Acid-Based Dithiazines: Synthesis and Photofragmentation of Their Benzaldehyde Adducts. Organic Letters. 2002, Vol. 4, No. 23, 4129-4131].
Известен способ [С.Р. Хафизова, В.Р. Ахметова, Г.Р. Надыргулова, И.В. Русаков, Р.В. Кунакова, У.М. Джемилев. Циклотиометилирование аминокислот и их производных с помощью формальдегида и сероводорода. Нефтехимия. 2005, том 45, №3, с. 374-378] получения дитиазинилзамещенных карбоновых кислот (3а-h) реакцией циклотиометилирования аминокислот 2a-h и их производных с помощью формальдегида и сероводорода. Реакция проходит неселективно с образованием побочных продуктов 4-6b-d
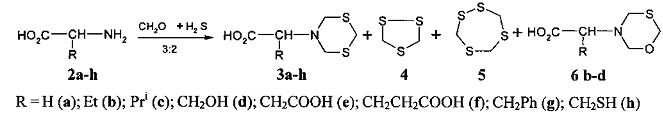
Известным способом не могут быть получены N-(1,5,3-дитиазепан-3-ил)карбоновые кислоты общей формулы (1).
Известен способ [Alexei N. Kurchan, Andrei G. Kutateladze. Amino Acid-Based Dithiazines: Synthesis and Photofragrnentation of Their Benzaldehyde Ad-ducts. Organic Letters. 2002, Vol. 4, No. 23, 4129-4131] получения дитиазинил-замещенных карбоновых кислот (8a-d) или (10) с хорошими выходами реакцией (L)-аминокислот (7a-d, 9) с формальдегидом и гидросульфидом натрия по схеме:
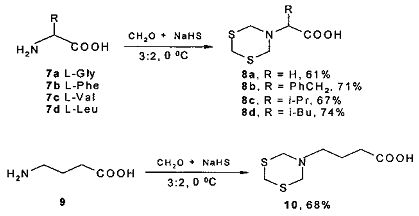
Известным способом не могут быть получены N-(1,5,3-дитиазепан-3-ил)карбоновые кислоты общей формулы (1).
Таким образом, в литературе отсутствуют сведения о селективном получении N-(1,5,3-дитиазепан-3-ил)карбоновых кислот общей формулы (1).
Предлагается новый способ получения N-(1,5,3-дитиазепан-3-ил)карбоновых кислот общей формулы (1).
Сущность способа заключается в предварительном перемешивании 1,2-этандитиола с формальдегидом (мольное соотношение 1:2) в течение 30 мин и последующем взаимодействии полученной смеси с аминокислотой общей формулы HO2C-X-NH2 [где X=CH2, (CH2)2, (CH2)3, CHCH3, CHCH2CH3, CHCH(СН3)2, CHCH2CH(CH3)2, CHCH2Ph, CHCH2OH, CHCH2COOH] при мольном соотношении 1,2-этандитиол : CH2O : аминокислота = 1:2:1 в течение 2.5-3.5 ч, предпочтительно 3 ч при температуре ~20°C и атмосферном давлении в воде в качестве растворителя. Выход N-(1,5,3-дитиазепан-3-ил)карбоновых кислот (1) составляет 85-98%. Реакция протекает по схеме:
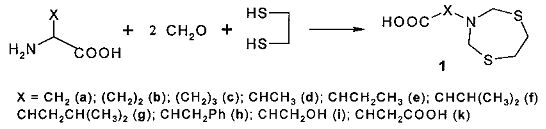
N-(1,5,3-дитиазепан-3-ил)карбоновые кислоты формулы (1) образуются только лишь с участием 1,2-этандитиола, формальдегида и аминокислот, взятых в мольном соотношении 1:2:1 (стехиометрические количества). При другом соотношении исходных реагентов снижается выход и селективность целевого продукта (1). Реакция проводится при комнатной температуре ~20°C. При более высокой температуре (например, 60°C) увеличиваются энергозатраты, при меньшей температуре (например, 0°C) снижается скорость реакции. Опыты проводятся в воде в качестве растворителя, т.к. в ней хорошо растворяются исходные реагенты.
Существенные отличия предлагаемого способа:
В известном способе в качестве исходных реагентов применяются формалин и сероводород. Известный способ не позволяет получать N-(1,5,3-дитиазепан-3-ил)карбоновые кислоты общей формулы (1). В предлагаемом способе в качестве исходных реагентов применяются коммерчески доступные 1,2-этандитиол, формалин и аминокислоты (глицин, фенилглицин, валин, лейцин, серин, глутаминовая, аспарагиновая). Предлагаемый способ позволяет получать N-(1,5,3-дитиазепан-3-ил)карбоновые кислоты общей формулы (1).
Способ поясняется следующими примерами:
Пример 1. Смесь 0.08 мл (1 ммоль) 1,2-этандитиола и 0.15 мл (2 ммоль) формалина перемешиваются в течение 30 мин. Затем к реакционной смеси добавляют 0.075 г (1 ммоль) глицина, растворенного в 3 мл воды, и перемешивают 2-3 ч. Реакционную смесь переносят в чашку Петри и оставляют до полного испарения воды. Продукт реакции - бесцветные кристаллы. Выход 2-(1,5,3-дитиазепан-3-ил)-уксусной кислоты (1а) составляет 0.19 г (98%).
Другие примеры, подтверждающие способ, приведены в табл. 1
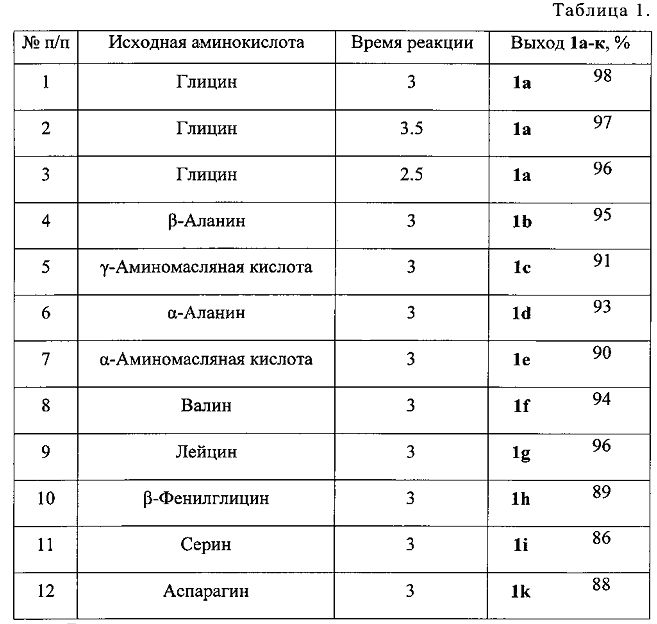
Все опыты проводятся при комнатной температуре (-20°C) в воде в качестве растворителя при мольном соотношении 1,2-этандитиол:CH2O:аминокислота = 1:2:1 (стехиометрические количества).
Физико-химические характеристики соединений.*
2-(1,5,3-Дитиазепан-3-ил)-уксусная кислота (1а).
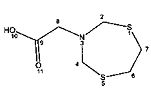
Бесцветные кристаллы, выход 0.19 г (98%), т.пл. 143-145°C. ИК-спектр, vmax; 694 (C-S), 1051 (C-N), 1620 (-C=O) см-1; Спектр ЯМР 1Н, δН (400 МГц, CDCl3, 25°C): 3.02 (4Н, с, S(CH2)2; 3.45 (2Н, с, NCH2CO2H); 4.18 (4Н, с, NCH2S). Спектр ЯМР 13C, δС (100 МГц, CDCl3): 34.9 (S(CH2)2); 51.5 (NCH2CO2H); 59.4 (NCH2S); 171.7 (CO2H). Найдено (%): С, 37.54; H, 5.65; N, 7.13; S, 33.39. C6H11NO2S2. Вычислено (%): C, 37.28; H, 5.74; N, 7.25; О, 16.55; S, 33.18.
Аналогичным способом получены N-(1,5,3-дитиазепан-3-ил)карбоновые кислоты (1b-i).
3-(1,5,3-Дитиазепан-3-ил)пропановая кислота (1b).
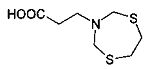
Бесцветные кристаллы, выход 0.20 г (95%), т.пл. 103-104°C. ИК-спектр, vmax; 666 (C-S), 1203 (C-N), 1461 (CH2), 1707 (-СОО-) см-1. Спектр ЯМР 1Н, δН (400 МГц, CDCl3, 25°C): 2.35 (2Н, т, J 7.2, CH2CO2H); 2.84 (2Н, т, J 7.2, NCH2CH2); 3.01 (4Н, с, S(CH2)2); 4.13 (4Н, с, NCH2S). Спектр ЯМР 13C, δС (100 МГц, CDCl3): 32.6 (CH2CO2H); 35.0 (S(CH2)2); 46.1 (NCH2CH2); 59.1 (NCH2S); 173.8 (CO2H). Найдено (%):C, 40.53; H, 6.31; N, 6.79; S, 30.95. C7H13NO2S2. Вычислено (%): C, 40.55; H, 6.32; N, 6.76; О, 15.43; S, 30.93. М 207.

4-(1,53-Дитиазепан-3-ил)бутановая кислота (1с).
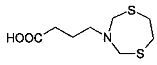
Бесцветные кристаллы, выход 0.2 г (91%), т. пл 92-93°C. ИК-спектр, vmax; 665 (C-S), 1218 (C-N), 1459 (CH2), 1697 (-СОО-) см-1; Спектр ЯМР 1Н, δН (400 МГц, ДМСО-d6, 25°C): 1.61 (2Н, кв, CH2CH2CH2); 2.21 (2Н, т, 3J 7.0, СН2СО2Н); 2.61 (2Н, т, 3J 7.0, NCH2CH2); 3.01 (4Н, с, S(CH2)2); 4.12 (4Н, с, NCH2S). Спектр ЯМР 13С, δС (100 МГц, CDCl3): δ 22.2 (СН2СН2СН2); 32.0 (CH2CH2CO2H); 35.0 (S(CH2)2); 49.3 (NCH2CH2); 59.0 (NCH2S), 174.8 (CO2H); Найдено (%): С, 43.45; H, 6.91; N, 6.37; S, 28.90. C8H15NO2S2. Вычислено (%): С, 43.41; Н, 6.83; N, 6.33; О, 14.46; S, 28.97. М 221.
2-(1,5,3-Дитиазепан-3-ил)пропановая кислота (1d).
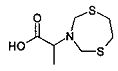
Бесцветные кристаллы, выход 0.19 г (93%), т. пл 134-136°C. ИК-спектр, vmax; 680 (C-S), 1218 (C-N), 1377 (СН3), 1703 (-СОО-) см-1; Спектр ЯМР 1Н, δН (400 МГц, ДМСО-d6, 25°C): 1.24 (3Н, д, J 7.0, CH3); 3.00 (4Н, м-АА'ВВ', S(CH2)2); 3.66 (1Н, кв, J 7.0, NCHCO2H); 4.20 (2Н, д, 2J 10.0, NCHaHeS); 4.28 (2Н, д, 2J 14.0, NCHaHeS). Спектр ЯМР 13С, δС (100 МГц, CDCl3): δ 16.1 (CH3); 35.6 (S(CH2)2); 56.7 (NCH2S), 57.3 (NCHCO2H); 174.6 (CO2H). Спектр ЯМР 15N (50.69 МГц, CDCl3), δ, м.д.: 56.8 (1N, уш. с, -N(CH2)2). Найдено (%): С, 40.59; Н, 6.41; N, 6.84; S, 30.87. C7H13NO2S2. Вычислено (%): С, 40.55; Н, 6.32; N, 6.76; О, 15.43; S, 30.93. М 207.
2-(1,5,3-Дитиазепан-3-ил)бутановая кислота (1е).
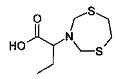
Бесцветные кристаллы, выход 0.19 г (90%), т. пл 140-141°C. ИК-спектр, vmax; 679 (C-S), 1218 (C-N), 1380 (СН3), 1458 (СН2), 1697 (-COO-) см-1; Спектр ЯМР 1Н, δН (400 МГц, ДМСО-d6, 25°C): 0.82 (3Н, т, J 7.2, CH3); 1.60-1.68 (2Н, м, CH2); 2.92-3.00 (4Н, м, S(CH2)2); 3.43 (1H, м, NCHCO2H); 4.23 (2Н, д, 2Jгем 14.0, NCH'H”S); 4.28 (2Н, д, 2Jгем 14.0, NCH'H”S). Спектр ЯМР 13С, δС (100 МГц, CDCl3): δ 10.4 (СН3); 22.7 (CHCH2); 35.9 (S(CH2)2); 56.7 (NCH2S), 64.0 (NCHCO2H); 173.4 (CO2H); Спектр ЯМР 15N (50.69 МГц, ДМСО-d6), δ, м.д.: 54.5 (1N, уш. с, -N(CH2)2). Найдено (%): С, 43.39; Н, 6.86; N, 6.25; S, 29.04. C8H15NO2S2. Вычислено (%): С, 43.41; Н, 6.83; N, 6.33; О, 14.46; S, 28.97. ESI (70 eV); m/z (%): 222 (100) [М+Н]+; 220 (~70) [М-Н]-.
2-(1,5,3-Дитиазепан-3-ил)-3-метилбутановая кислота (1f).
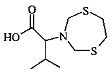
Бесцветные кристаллы, выход 0.2 г (85%), т. пл 104-105°C. ИК-спектр, vmax; 694 (C-S), 1076 (C-N), 1353 (СН3), 1463 (CH2), 1698 (-COO-) см-1; Спектр ЯМР 1Н, δН (500 МГц, ДМСО-d6, 25°C): 0.82 (3Н, д, J 6.0, CH3); 0.88 (3Н, д, J 6.0, СН3); 1.94-1.96 (1Н, м, СН(СН3)2); 2.82-2.96 (6Н, м, S(CH2) и NCHCO2H); 4.31 (4Н, с, NCH2S); 12.40 (1H, уш.с, НО). Спектр ЯМР 13С, δС (125 МГц, CDCl3): δ 19.0 (СН3); δ 19.7 (СН3); 27.5 (СН(CH3)2); 36.7 (S(CH2)2); 56.5 (NCH2S), 70.4 (NCHCO2H); 172.5 (CO2H). Найдено (%):С, 45.98; Н, 6.22; N, 6.00; S, 27.31. C9H17NO2S2. Вычислено (%): С, 45.93; Н, 6.28; N, 5.95; О, 13.60; S, 27.25. ESI (70 eV); m/z (%): 297 (30) [M+Na+K]+; 236 (100) [М+Н]+; 234(100) [М-Н]-.
2-(1,5,3-Дитиазепан-3-ил)-4-метилпентановая кислота (1g).
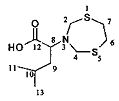
Бесцветные кристаллы, выход 0.24 г (96%), т. пл 110-112°C. ИК-спектр, vmax; 688 (C-S), 1020 (C-N), 1711 (-С=О) см-1; Спектр ЯМР 1H, δН (500.17 МГц, ДМСО-d6, 25°C): 0.87 (3Н, д, J 6.0, СН3); 0.89 (3Н, д, J 6.5, СН3); 1.50 (3Н, м, СНСН2СН(СН3)2); 2.86-3.01 (4Н, м, S(CH2)2); 3.39 (1H, уш. с, НО); 3.47 (1Н, т, J 7.0, NCHCO2H); 4.25 (2Н, д, 2J 14.0, NCHaHeS); 4.32 (2Н, д, 2J 14.0, NCHaHeS). Спектр ЯМР 13С, δС (125.78 МГц, CDCl3): δ 22.5 (СН3); 23.5 (СН3); 25.3 (СН(СН3)2); 36.3 (S(CH2)2); 38.7 (СНСН2СН), 56.6 (NCH2S), 62.0 (NCHCO2H); 173.7 (CO2H). Спектр ЯМР 15N (50.69 МГц, CDCl3), δ, м.д.: 54.4 (1N, уш. с, -N(CH2)2). Найдено (%):С, 48.10; Н, 7.63; N, 5.67; S, 25.77. C10H19NO2S2. Вычислено (%): С, 48.16; Н, 7.68; N, 5.62; О, 12.83; S, 25.71. ESI (70 eV); m/z (%): 250 (100) [М+Н]+; 248 (100) [М-Н]-.
2-(1,5,3-Дитиазепан-3-ил)-3-фенилпропановая кислота (1h).
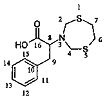
Бесцветные кристаллы, выход 0.24 г (89%), т. пл 143-145°C. ИК-спектр, vmax; 694 (C-S), 1051 (C-N), 1620 (-С=О) см-1; Спектр ЯМР 1Н, δН (500 МГц, ДМСО-d6, 25°C): 2.89-3.03 (6Н, м, CH2Ph and S(CH2)2)); 3.38 (1H, уш. с, NCHCO2H); 3.70 (1H, м, NCHCO2H); 4.36 (2H, д, 2J 14.0, NCHaHeS); 4.40 (2H, д, 2J 14.0, NCHaHeS). Спектр ЯМР 13C, δC (125 МГц, CDCl3): δ 35.9 (CHCH2Ph); 36.4 (S(CH2)2); 56.6 (NCH2S), 65.5 (NCHCO2H); 126.8 (Ph); 128.7 (Ph); 129.6 (Ph); 138.3 (Ph); 172.63 (CO2H). Спектр ЯМР 15N (50.69 МГц, CDCl3), δ, м.д.: 55.5 (1N, уш. с, -N(CH2)2). Найдено (%): С, 55.15; H, 5.98; N, 4.88; S, 22.67. C13H17NO2S2. Вычислено (%): С, 55.09; H, 6.05; N, 4.94; О, 11.29; S, 22.63.
2-(1,5,3-Дитиазепан-3-ил)-3-гидроксипропановая кислота (1i).
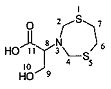
Бесцветные кристаллы, выход 0.19 г (86%), т. пл 127-128°C. ИК-спектр, vmax; 690 (C-S), 1020 (C-N), 1712 (-С=O) см-1; Спектр ЯМР 1Н, δН (500.17 МГц, ДМСО-d6, 25°C): 2.97-2.98 (4Н, м, S(CH2)2); 3.38 (1H, уш.с, CO2H); 3.55 (1Н, т, J 6.0, NCHCO2H); 3.71 (2Н, д, J 6.0, СНСН2ОН); 4.22 (2Н, д, 2J 14.0, NCHaHeS); 4.32 (2H, д, 2J 14.0, NCHaHeS); 5.74 (1H, уш. с, ОН). Спектр ЯМР 13С, δС (125.78 МГц, CDCl3): δ 35.8 (S(CH2)2); 57.2 (NCH2S); 60.5 (СНСН2ОН); 64.8 (NCHCO2H); 172.70 (CO2H). Спектр ЯМР 15N (50.69 МГц, CDCl3), δ, м.д.: 52.7 (1N, уш. с, -N(CH2)2). Найдено (%): С, 37.69; Н, 5.84; N, 6.34; S, 28.76. C7H13NO3S2. Вычислено (%): С, 37.65; Н, 5.87; N, 6.27; О, 21.49; S, 28.72. ESI (70 eV); m/z (%): 224 (100) [М+Н]+; 222 (100) [М-Н]-.
2-(1,5,3-Дитиазепан-3-ил)сукциновая кислота (1k).
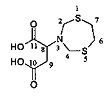
Бесцветные кристаллы, выход 0.21 г (88%), т. пл 166-167°C. ИК-спектр, vmax; 662 (C-S), 1034 (C-N), 1460 (СН2), 1736 (-COO-) см-1; Спектр ЯМР 1Н, δН (500.17 МГц, ДМСО-d6, 25°C): 2.66 (1Н, d.d., 2J 16.0, 3J 5.0, CHCHACH-BCO2H); 2.72 (1Н, d.d., 2J 16.0, 3J 10.0, CHCHACHBCO2H); 2.91 (4Н, м (АА'ВВ'), S(CH2)2); 3.36 (1H, уш. с, NCHCO2H); 3.72 (1Н, d.d., 3J 10.0, 3J 5.0, NCHCO2H); 4.28 (2H, д, 2Jгем 14.0, NCHAHBS); 4.33 (2H, д, 2Jгем 14.0, NCHAHBS); 12.27 (1Н, уш. с, CHCH2CO2H). Спектр ЯМР 13С, δС (125.78 МГц, CDCl3): δ 34.5 (CHCH2CO2H); 36.7 (S(CH2)2); 56.5 (NCH2S); 60.9 (NCHCO2H); 172.42 (NCHCO2H); 172.70 (CHCH2CO2H). Спектр ЯМР 15N (50.69 МГц, CDCl3), δ, м.д.: 52.8 (1N, уш. с, -N(CH2)2). Найдено (%): С, 38.31; Н, 5.17; N, 5.52; S, 25.58. C8H13NO4S2. Вычислено (%): С, 38.23; Н, 5.21; N, 5.57; О, 25.46; S, 25.52.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 1,2-БИС-(1, 5, 3-ДИТИАЗЕПАН-3-ИЛ)ЭТАНА, ОБЛАДАЮЩЕГО СОРБЦИОННОЙ АКТИВНОСТЬЮ ПО ОТНОШЕНИЮ К ПАЛЛАДИЮ(II) И СЕРЕБРУ(I) | 2014 |
|
RU2608730C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛ 2-(1,5,3-ДИТИАЗЕПАН-3-ИЛ)АЛКАНОАТОВ | 2015 |
|
RU2605448C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЦИКЛОАЛКИЛЗАМЕЩЕННЫХ 1,5,3-ДИТИАЗЕПАНОВ | 2017 |
|
RU2664654C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЦИКЛОПЕНТИЛЗАМЕЩЕННЫХ 1,5,3-ДИТИАЗЕПАНОВ | 2014 |
|
RU2565790C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИС-(1,5,3-ДИТИАЗЕПАН-3-ИЛ)ЦИКЛОГЕКСАНОВ | 2014 |
|
RU2574069C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-(1,5,3-ДИТИАЗЕПАН-3-ИЛ)АМИДОВ | 2011 |
|
RU2478626C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-(1,5,3-ДИТИАЗЕПАН-3-ИЛ)АМИДОВ | 2011 |
|
RU2482114C2 |
| СПОСОБ ПОЛУЧЕНИЯ (1,5,3-ДИТИАЗЕПАН-3-ИЛ)-АЛКАНДИОЛОВ | 2013 |
|
RU2559367C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЦИКЛОГЕКСИЛЗАМЕЩЕННЫХ 1,5,3-ДИТИАЗЕПАНОВ | 2014 |
|
RU2574074C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-АЛКИЛ-N,N-БИС[ω-(ПИПЕРИДИН-1-ИЛ)АЛКАДИИН-1-ИЛ]АМИНОВ, ПРОЯВЛЯЮЩИХ ФУНГИЦИДНУЮ АКТИВНОСТЬ | 2019 |
|
RU2734488C1 |
Изобретение относится к способу получения N-(1,5,3-дитиазепан-3-ил)карбоновых кислот формулы (1)

который заключается в предварительном перемешивании 1,2-этандитиола и формальдегида (мольное соотношение 1:2) в течение 30 мин, затем образующуюся смесь перемешивают с аминокислотой, взятыми в мольном соотношении 1,2-этандитиол:CH2O:аминокислота = 1:2:1 в течение 2.5-3.5 ч при температуре ~20°C и атмосферном давлении в воде в качестве растворителя. Выход N-(1,5,3-дитиазепан-3-ил)карбоновых кислот общей формулы (1) в зависимости от структуры исходной аминокислоты составляет 86-98%. 1 табл., 1 пр.
Способ получения N-(1,5,3-дитиазепан-3-ил)карбоновых кислот общей формулы (1)

отличающийся тем, что предварительно подготовленную перемешиванием в течение 30 мин смесь 1,2-этандитиола с формальдегидом (соотношение 1:2 моль) подвергают взаимодействию с аминокислотой общей формулы HO2C-X-NH2 (где X указана выше) при мольном соотношении 1,2-этандитиол:CH2O:аминокислота=1:2:1 при температуре ~20°C и атмосферном давлении в воде в качестве растворителя в течение 2.5-3.5 ч.
| СПОСОБ ПОЛУЧЕНИЯ БИС-2,4-ДИАЛКИЛ-1,5,3-ДИТИАЗЕПАН-3-ИЛОВ | 2010 |
|
RU2455303C2 |
| FR 0002966155 A1, 20.04.2012. | |||
Авторы
Даты
2016-11-10—Публикация
2014-12-31—Подача