Изобретение относится к технической микробиологии и биокоррозионным испытаниям, а именно к способам моделирования процессов биокоррозионных поражений алюминиево-магниевых сплавов, применяемых в авиа-космической технике.
Космическая станция - зона повышенного риска с экстремальными условиями для работы оборудования. Постоянный контроль всех параметров внутренней среды, в том числе и микрофлоры станции, обеспечивает повышение надежности и безопасности ее работы.
Все материалы в процессе эксплуатации неизбежно подвергаются различным воздействиям окружающей среды, которые вызывают коррозионные процессы на их поверхности. Они могут быть вызваны как воздействием химических веществ (химическая коррозия), так и действием различных микроорганизмов (биологическая коррозия). Реальные коррозионные процессы, как правило, происходят под действием обоих факторов.
Действие микроорганизмов представляет собой один из факторов, способствующих возникновению и развитию процессов коррозии металлов (Албитская О.Н., Шапошникова Н.А. «Влияние плесеней на коррозию металлов» // Микробиология. 1960. Т. 29. С. 725-730; Коваль Э.З., Касьян Д.М., Дахановский В.И. «Исследования грибной коррозии» // Биологические повреждения строительных и промышленных материалов. Киев: Наукова думка. 1978. С. 59-60; Лугаускас А.Ю.; Микульскене А.И.; Шляужене Д.Ю. Каталог микромицетов-биодеструкторов полимерных материалов. Отв. ред. М.В. Горленко. М.: Наука, 1987. 340 с.).
В основе действия микроорганизмов на металлы лежит электрохимический механизм. Микроорганизмы могут вызывать или изменять коррозию тремя основными способами:
1. Непосредственно воздействуя на кинетику электродных реакций.
2. Образованием метаболитов, обладающих коррозионными свойствами (неорганические и органические кислоты и т.п.).
3. Изменениями на поверхности раздела металл-электролит, которые могут привести к коррозии (например, образование участков с повышенным образованием оксидов) (Costello J.A., 1969. The corrosion of metals by micro-organisms. Int. Biodent. Bull., 5,101).
Плесневые грибы развиваются на поверхностях, контактирующих с металлами (ткань, лакокрасочное покрытие, топливо и т.д.), откуда споры гриба распространяются и при конденсации влаги начинают развиваться, образуя органические кислоты.
Коррозии способствует конденсация паров воды мицелием гриба, накопление им в процессе роста органических кислот. Кроме этого под мицелием грибов создаются условия, благоприятные для развития других микроорганизмов.
Алюминиевые сплавы широко используются в аэрокосмической индустрии, судостроении. При длительном использовании устойчивость и надежность деталей и узлов агрегатов в значительной мере зависит от процессов коррозии, в том числе и от коррозии, вызванной микроорганизмами - биокоррозии. Микроорганизмы могут способствовать возникновению коррозионных повреждений и усиливать их, непосредственно воздействуя на кинетику электродных реакций.
Известно воздействие органических кислот на коррозионное повреждение металлов (Д.В. Белов, А.А. Калинина, Т.Н. Соколова, В.Ф. Смирнов, М.В. Челнокова, В.Р. Карташов. Прикл. биохимия и микробиология. 2012, Т. 48, №3, с. 302-307; Белов Д.В., Соколова Т.Н., Смирнов В.Ф., Кузина О.В., Косюкова Л.В., Карташов В.Р. // Коррозия: материалы, защита. 2007. №9. С. 36-41; Смирнов В.Ф., Белов Д.В., Соколова Т.Н. // Прикл. биохимия и микробиология. 2008. Т. 44. №2. С. 213-218; Белов Д.В., Соколова Т.Н., Карташов В.Р., Смирнов В.Ф., Челнокова М.В., Ляпина М.А. // Известия Вузов. Сер. Химия и химическая технология. 2007. Т. 50. №6. С. 60-64).
В некоторых случаях под их действием металлы корродируют даже более интенсивно, чем при действии неорганических кислот. Коррозия, например, емкостей с нефтепродуктами иногда является, видимо, результатом действия на алюминиевые сплавы органических кислот, образующихся при разложении нефтепродуктов микроорганизмами.
Известен способ испытания алюминия и его сплавов по ГОСТу 9.913-90 «Единая система защиты от коррозии и старения. Алюминий, магний и их сплавы. Методы ускоренных коррозионных испытаний», издательство стандартов, 1990 г., согласно которому испытания проводят в искусственно создаваемых условиях, имитирующих воздействие климатических факторов атмосферы. Данный способ осуществляют при полном погружении образцов из алюминия и его сплавов в электролит (3%-ный раствор хлористого натрия) с добавлением пероксида водорода при температуре 18-25°C. Продолжительность испытаний - 90 суток.
Известен способ проведения испытаний и нанесения суспензии спор грибов (метод №3) по ГОСТу 9.048-89 «Единая система защиты от коррозии и старения. Изделия технические. Методы лабораторных испытаний на стойкость к воздействию плесневых грибов», издательство стандартов, 1991 г. Изготавливают испытательные и контрольные образцы, подготовленные испытательные и контрольные образцы высушивают, испытательные образцы стерилизуют, готовят суспензию спор грибов для заражения образцов, затем наносят ее на простерилизованные испытательные образцы, и помещают, по крайней мере, по два образца в чашки Петри, закрывают их, контрольные образцы, обработанные дистиллированной водой, также располагают в чашках Петри. Чашки Петри с испытательными и контрольными образцами помещают в разные эксикаторы, на дно которых наливают воду для поддержания влажности более 90%, эксикаторы закрывают и выдерживают при комнатной температуре, проводят экспозицию испытательных и контрольных образцов, затем образцы извлекают из чашек Петри, промывают их в проточной воде и осматривают.
Недостатком таких способов испытаний является то, что они не соответствуют условиям биокоррозионных повреждений, возникающих на границе раздела фаз или сред в присутствии, что чрезвычайно важно, кислорода. Развитие биокоррозионных повреждений в анаэробных условиях - один из частных случаев биокоррозии. Обычно она развивается на поверхности металлов при наличии влаги и растворенного кислорода и углекислоты, которые принимают участие в процессах, как возможных электрохимических, определяющихся именно этими факторами, так и усиливающими их биологическими процессами. Именно такие поверхностные процессы коррозии могут осуществлять повреждение аппаратуры и других конструкционных поверхностей в гермозамкнутых объектах, способствовать формированию соответствующего сообщества микроорганизмов - деструкторов.
Известно, что в органических кислотах алюминий обычно разрушается очень медленно, за исключением таких кислот как муравьиная, щавелевая и некоторых хлоридсодержащих кислот, скорость растворения алюминия в которых велика (http://metallicheckiy-portal.ru/articles/zashita_ot_korrozii_metalla/aluminii/korrozia_v_razlichnix_sredax/9).
Задачей изобретения является моделирование начальных процессов биокоррозионных поражений тонкостенных герметичных оболочек из алюминиево-магниевых сплавов АМг6 толщиной не более 2 мм с механически обработанной поверхностью в присутствии грибных метаболитов.
Техническим результатом изобретения является:
- имитация начальных процессов биокоррозии с помощью синтезируемых грибами, характерными обитателями гермозамкнутых объектов, продуктов: глюконовой, малоновой кислот;
- определение биокоррозионных эффектов (оценка начальных этапов биокоррозии и ее тип, исследование химического состава пораженной поверхности образцов);
- сокращение времени испытаний и приближение условий испытаний к натурным за счет применения глюконовой, малоновой кислот;
- упрощение метода испытаний, отсутствие необходимости создания условий для выращивания микроорганизмов и организации микробиологической лаборатории, блока для стерильных работ;
- возможность увеличения надежности и ресурса эксплуатации конструкционных материалов в присутствии технофильных микроорганизмов в эксплуатационных условиях гермозамкнутого объема.
Технический результат изобретения достигается за счет того, что в способе моделирования процессов биокоррозионных поражений тонкостенных герметичных оболочек из алюминиево-магниевых сплавов при эксплуатации космических аппаратов, характеризующемся тем, что изготавливают испытательные и контрольные образцы из алюминиево-магниевых сплавов АМг6, подготовленные испытательные и контрольные образцы высушивают, испытательные образцы стерилизуют, готовят имитационный состав на основе органической кислоты, который наносят на простерилизованные испытательные образцы, и помещают, по крайней мере, по два образца в чашки Петри, закрывают их, контрольные образцы, обработанные дистиллированной водой, также располагают в чашках Петри, чашки Петри с испытательными и контрольными образцами помещают в разные эксикаторы, на дно которых наливают воду для поддержания влажности более 90%, эксикаторы закрывают и выдерживают при комнатной температуре, проводят экспозицию испытательных и контрольных образцов, затем образцы извлекают из чашек Петри, промывают их в проточной воде. Испытательные и контрольные образцы используют с механически обработанной поверхностью. Для приготовления имитационного состава используют дистиллированную воду и одну из органических кислот, выбранную из следующих карбоновых кислот: глюконовая или малоновая, полученный состав с помощью распылителя наносят на испытательные образцы алюминиево-магниевых сплавов АМг6, после промывания образцов в проточной воде их ополаскивают дистиллированной водой и высушивают, затем с помощью растрового электронного микроскопа оценивают начальные этапы биокоррозии и ее тип, исследуют химический состав пораженной поверхности образцов, при этом экспозицию испытательных и контрольных образцов проводят в течение 30-45 суток в трехкратной - пятикратной повторности.
Технический результат достигается также и тем, что имитационный состав для моделирования процессов биокоррозионных поражений тонкостенных герметичных оболочек из алюминиево-магниевых сплавов при эксплуатации космических аппаратов включает органическую кислоту, растворитель, в качестве органической кислоты он содержит глюконовую кислоту, а в качестве растворителя - дистиллированную воду при следующем соотношении компонентов, мас.ч.:
5-10% раствор глюконовой кислоты - 0,05-0,10;
дистиллированная вода - 0,95-0,90.
Технический результат достигается также и тем, что имитационный состав для моделирования процессов биокоррозионных поражений тонкостенных герметичных оболочек из алюминиево-магниевых сплавов при эксплуатации космических аппаратов включает органическую кислоту, растворитель, в качестве органической кислоты он содержит малоновую кислоту, а в качестве растворителя - дистиллированную воду при следующем соотношении компонентов, мас.ч.:
5-10% раствор малоновой кислоты - 0,05-0,10;
дистиллированная вода - 0,95-0,90.
Сущность изобретения поясняется графическими материалами.
В таблице 1 представлен процентный состав органических карбоновых кислот (общее содержание кислот принято за 100%), выделенных из культуральной жидкости грибов, выращенных на среде Чапека-Докса в глубинных условиях.
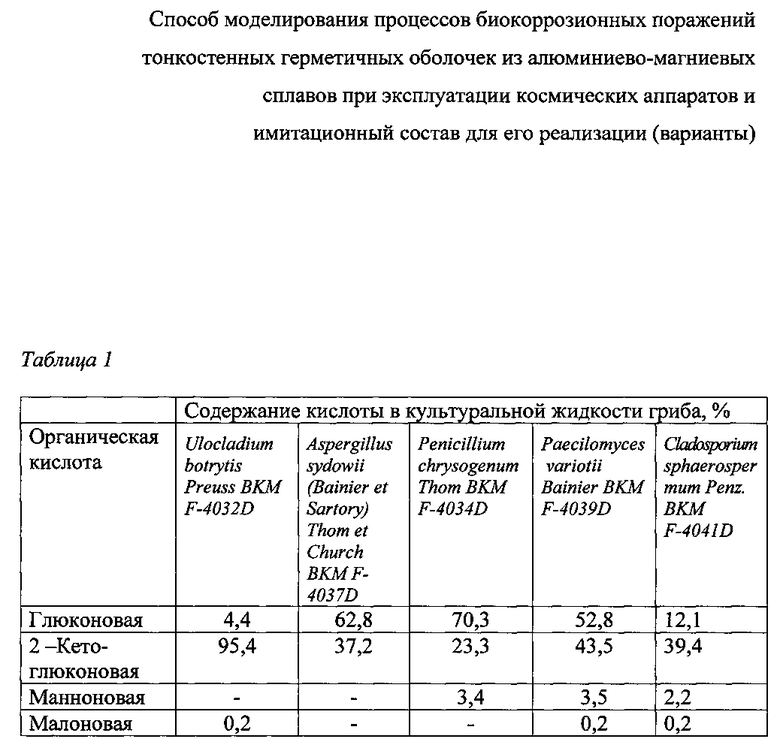
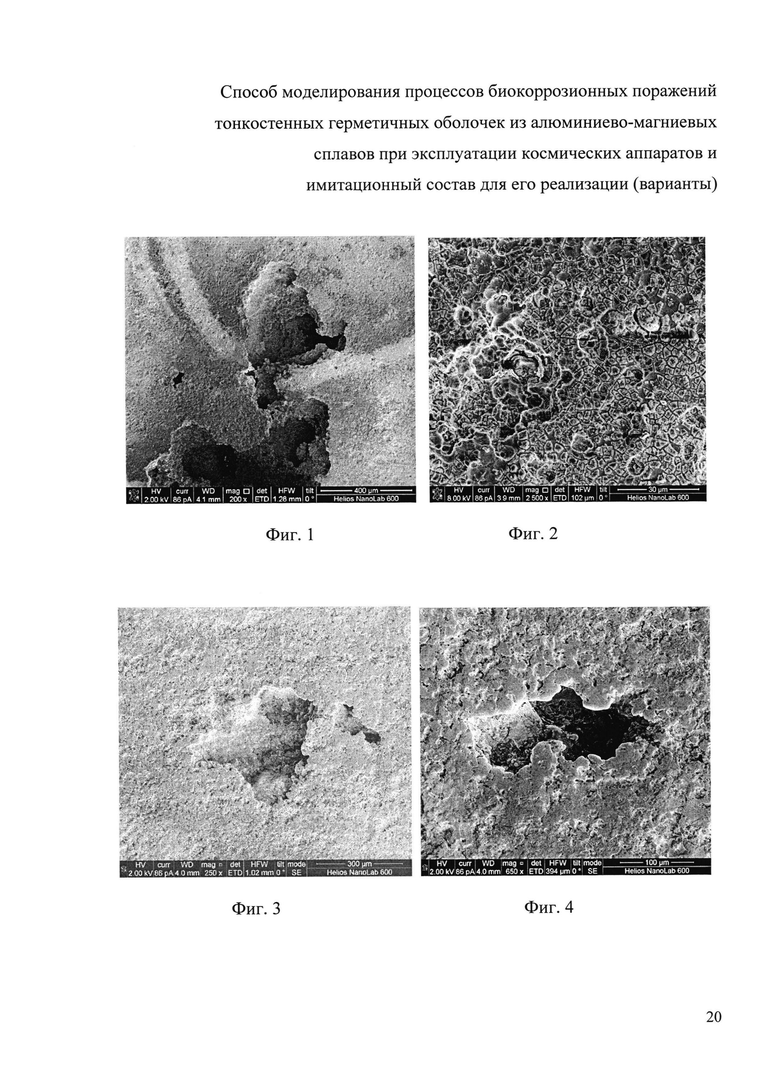
На фиг. 1, 2 представлены фотографии испытательных образцов алюминиево-магниевого сплава (Амг6), обработанные глюконовой кислотой; на фиг. 3, 4, 5 - фотографии испытательных образцов алюминиево-магниевого сплава (Амг6), обработанные малоновой кислотой; на фиг.6, 7 - фотографии контрольных образцов алюминиево-магниевого сплава (Амг6), обработанные дистиллированной водой; на фиг. 8, 9 - фотографии образцов алюминиево-магниевого сплава (Амг6), обработанные штаммом Aspergillus sidowii (Bainier et Sartory) Thom et Church BKM F-4037D.
Сущность изобретения заключается в следующем.
На углеводных субстратах различные технофильные микроорганизмы способны синтезировать и выделять в окружающую среду в зависимости от условий (температурно-влажностный режим) лимонную, янтарную, яблочную, уксусную, щавелевую, муравьиную, глюконовую, кетоглюконовую, малоновую и другие кислоты. При этом, кислоты могут взаимодействовать с оксидами алюминия, вызывая разрушение защитного оксидного слоя и способствуя контакту металла с мицелием, а также распространению мицелия по поверхности.
В проведенных опытах при выращивании в жидкой среде Чапека-Докса использовали различные штаммы по патенту RU 2486250 (27.06.2013): Paecilomyces variotii Bainier BKM F-4039D, Ulocladium botrytis Preuss BKM F-4032D, Penicillium chrysogenum Thom BKM F-4034D, Aspergillus sydowii (Bainier et Sartory) Thom et Church BKM F-4037D, Cladosporium sphaerospermum Penz. BKM F-4041D. Все эти культуры, принадлежащие к различным родам, были выделены с поверхности конструкционных материалов PC МКС и депонированы во Всероссийской коллекцией микроорганизмов (ВКМ) Института биохимии и физиологии микроорганизмов имени Г.К. Скрябина РАН (142290, г. Пущино Московской области, проспект Науки, 5).
Для изучения состава продуктов метаболизма, образуемых вышеперечисленными грибами в процессе роста, выращивание проводилось на среде Чапека-Докса. Была использована среда в соответствии ГОСТами 9.048-89 и 9.049-91 в ускоренных испытаниях образцов алюминиево-магниевого сплава АМг6. Для засева основных колб были получены 12-суточные культуры грибов в пробирках на агаризованной среде Чапека-Докса. Споровые суспензии грибов получали смывом стерильной водой с поверхности скошенной агаризованной среды. Жидкую среду Чапека-Докса готовили в качалочных колбах Эрленмейера емкостью 750 мл (по 100 мл) и после стерилизации засевали суспензией спор вышеперечисленных грибов, из расчета 5% посевного материала 5%-ной суспензией спор. Суспензию готовили следующим образом: в пробирку с культурой, растущей на скошенной среде Чапека-Докса, вносили по 10 мл жидкой среды Чапека-Докса. Затем с помощью пипетки снимали с поверхности споры гриба, закрыв пробирку пробкой, взбалтывали суспензию до получения однородного материала и быстро отбирали по 5 мл стерильной пипеткой и переносили в качалочную колбу. Культуры грибов выращивали на качалке при 29°C и 180 об/минуту в течение 4-5 суток. Затем культуральную жидкость отделяли от мицелия фильтрованием через стеклянный фильтр. В культуральной жидкости измеряли величину pH 5,5-6.0 и 1 мл культуральной жидкости лиофилизировали для получения модифицированных триметилсилильных производных и исследования состава продуктов метаболизма на газовом хроматографе с масс-селективным детектором (ГХ-МС).
Лиофильно высушенные образцы культуральной жидкости (по 1 мл культуральной среды растворяли в пиридине (99+% A.C.S. Sigma-Aldrich), добавляли силилирующий реагент BSTFA+TMCS 99:1 - N, О bis (trimethylsilyl) trifluoroacetamide)+trimethylchlorosilane (Supelco) и прогревали в герметично закупоренных флаконах при 60°C в течение 30 минут.
Хроматографический анализ проводили на газовом хроматографе SHIMADZU GS 2010 (Япония) с масс-селективным детектором QP 2010. Условия проведения анализа: температура термостата - 180°C; инжектора -200°C; интерфейса - 210°C; детектора - 200°C; газ - носитель - гелий, скорость потока 1,0 мл/минуту; деление потока 1:10; режим: 180°C 1 минута, 20°C /мин до 220°C, изотерма 5 минут, 30°C /мин до 270°C, изотерма 4 минуты. Диапазон регистрации масс 40-500. Библиотека масс спектров - NIST 05.
Таким образом, были получены хроматограммы культуральных жидкостей: Penicillium chrysogenum Thom BKM F-4034D; Aspergillus sydowii (Bainier et Sartory) Thom et Church BKM F-4037D; Ulocladium botrytis Preuss BKM F-4032D; Paecilomyces variotii Bainier BKM F-4039D; Cladosporium sphaerospermum Penz. BKM F-4041D.
Затем проводили идентификацию веществ культуральных жидкостей по соответствующим пикам на хроматограммах, используя библиотеку NIST 05, и выявили, что у большинства исследованных грибов глюконовая и ее производная - 2-кето-глюконовая кислота (при микробном окислении глюконовая кислота легко переходит в 5-кетоглюконовую и 2-кетоглюконовую кислоты), а также малоновая кислота составляют большую часть от всех идентифицированных продуктов, выделяемых грибами в культуральную жидкость (таблица 1).
Глюконовая кислота (альдоновая кислота) СН2ОН(СНОН)4СООН - одноосновная карбоновая кислота:
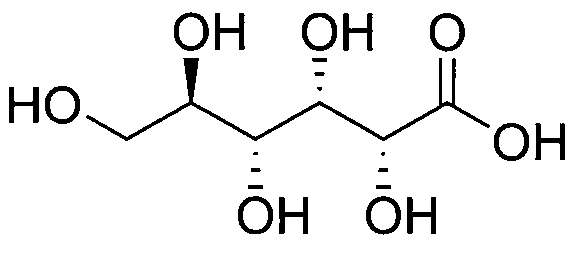
Глюконовая кислота образуется при окислении альдегидной группы глюкозы, представляет собой белый, легко плавящийся гигроскопичный кристаллический порошок без запаха со слегка кисловатым вкусом. Образует соли - глюконаты.
Малоновая кислота (пропандиовая, метандикарбоновая кислота) НООССН2СООН - двухосновная предельная карбоновая кислота:
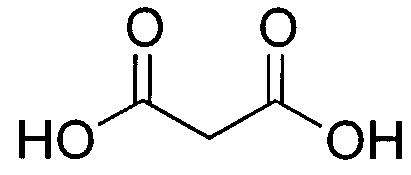
Малоновая кислота обладает всеми химическими свойствами, характерными для карбоновых кислот. Соли и сложные эфиры малоновой кислоты называются малонатами. Малонат кальция содержится в соке сахарной свеклы. Двухосновные кислоты могут давать два ряда солей, сложных эфиров амидов и других производных. В промышленности получают гидролизом циануксусной кислоты. Малоновая кислота используется в синтезе непредельных кислот, флавонов, аминокислот, витаминов B1 и В6.
За основу метода проведения испытаний и нанесения имитационного состава на основе органической карбоновой кислоты на поверхность образцов алюминиево-магниевых сплавов АМг6 взяты методы, описанные в ГОСТах 9.048-89 (метод №3) и 9.049-91. Испытания по биокоррозионным поражениям проводят при комнатной температуре и влажности более 90% в течение 30-45 суток. Испытания проводят во влажной камере (эксикаторе).
Для испытаний используют две выборки образцов: испытательную и контрольную. Испытательная выборка предназначена для определения интенсивности развития биокоррозионного поражения с помощью имитационного состава для его моделирования и определения действия на параметры изделий, контрольная выборка - для определения действия на параметры изделий повышенной влажности (более 90%) и при комнатной температуре (25±2)°С воздуха без действия имитационного состава, с целью сопоставления с результатами испытаний из испытательной выборки. Испытательные и контрольные образцы изготавливают из цилиндрических заготовок конструкционного материала - алюминиево-магниевого сплава толщиной АМг6 5 мм и диаметром 12 мм (ГОСТ/ТУ - 1-90395-91, плавка партии №89606) с механически обработанной поверхностью. Образцы промывают в дистиллированной воде, обезжиривают органическим растворителем (например, ацетоном ГОСТ 2768-84).
Подготовленные таким образом образцы стерилизуют в 70%-ном этаноле в течение 1 часа и высушивают.
Готовят имитационный состав на основе органической карбоновой кислоты. Для его приготовления используют дистиллированную воду и одну из органических кислот, выбранную из следующего ряда карбоновых кислот: глюконовая и малоновая.
Для приготовления имитационного состава по первому варианту (п. 2 формулы изобретения) взвешивают на технических весах 5 г глюконовой кислоты, используя реактив марки х.ч. (химически чистый). Затем на технических весах взвешивают пустой стеклянный стакан емкостью 200 мл. В него наливают дистиллированную воду, доводя ее массу до 95 г. Взвешенную глюконовую кислоту частями добавляют в стакан со взвешенным растворителем - дистиллированной водой, размешивая каждую новую порцию до полного растворения. Для приготовления имитационного состава по первому варианту (п. 2 формулы изобретения) взвешивают на технических весах 10 г глюконовой кислоты, используя реактив марки х.ч. Затем на технических весах взвешивают пустой стеклянный стакан, емкостью 200 мл. В него наливают дистиллированную воду, доводя ее массу до 90 г. Взвешенную глюконовую кислоту частями добавляют в стакан со взвешенным растворителем - дистиллированной водой, размешивая каждую новую порцию до полного растворения.
Для приготовления имитационного состава по второму варианту (п. 3 формулы изобретения) на технических весах взвешивают 5 г малоновой кислоты (ТУ 6-09-2608-77). Затем на технических весах взвешивают пустой стеклянный стакан, емкостью 200 мл. В него наливают дистиллированную воду, доводя ее массу до 96,4 г. Взвешенную малоновую кислоту частями добавляют в стакан со взвешенным растворителем - дистиллированной водой, размешивая каждую новую порцию до полного растворения.
Для приготовления имитационного состава по второму варианту (п. 3 формулы изобретения) на технических весах взвешивают 10 г малоновой кислоты (ТУ 6-09-2608-77). Затем на технических весах взвешивают пустой стеклянный стакан, емкостью 200 мл. В него наливают дистиллированную воду, доводя ее массу до 91,2 г. Взвешенную малоновую кислоту частями добавляют в стакан со взвешенным растворителем - дистиллированной водой, размешивая каждую новую порцию до полного растворения.
Полученные растворы (имитационные составы) используют для обработки испытательных образцов с целью моделирования начальных этапов биокоррозионных поражений герметичных оболочек из алюминиево-магниевых сплавов АМг6.
Приготовленный имитационный состав по одному из вариантов наносят на простерилизованные испытательные образцы с помощью распылителя, и помещают по 2-5 образца в чашки Петри. Затем для сохранения нанесенного состава на поверхности образцов в мелкораспыленном состоянии чашки Петри быстро закрывают крышками. Контрольные образцы, обработанные дистиллированной водой, также располагают в чашках Петри. Чашки Петри с испытательными и контрольными образцами помещают в разные эксикаторы, на дно которых наливают воду для поддержания влажности более 90%, эксикаторы закрывают и выдерживают при комнатной температуре. Экспозицию испытательных и контрольных образцов проводят в течение 30-45 суток. Затем образцы извлекают из чашек Петри, промывают в проточной воде, ополаскивают дистиллированной водой и высушивают. Контрольные образцы подвергают точно такой же обработке. Эксперименты проводят в трехкратной-пятикратной повторности для каждого имитационного состава (два варианта).
Испытательные и контрольные образцы хранят в стерильных чашках Петри до исследования в сканирующем электронном микроскопе.
Затем образцы исследуют в многофункциональном растровом электронном микроскопе (РЭМ) с интегрированной системой фокусированного ионного пучка для структурной диагностики и автоматизированных исследований в промышленных и лабораторных условиях Quanta-3D (FEI, Hillsboro, OR, США) при ускоряющем напряжении 15 кВ.
Далее проводят оценку влияния имитационного состава на процесс начальных этапов биокоррозии образцов и сравнение смоделированного биокоррозионного поражения с биокоррозионным поражением известными штаммами микроорганизмов по патенту RU 2486250 (27.06.2013). Таким образом, оценивают влияние имитационного состава на свойства алюминиево-магниевого сплава согласно ГОСТа 9.049-91 (п. 1.7.2, 1.7.3).
Электронные фотографии 8 и 9 выполнены на Quanta-3D (FEI, Hillsboro, OR, США). На фото представлены изображения поверхности образца АМг6, обработанного спорами известных грибов (фиг. 8, 9) по патенту RU 2486250 (27.06.2013) и имитационным составом по одному из вариантов (фиг. 1-5).
Исследование химического состава производилось с помощью приставки для рентгеновского энергодисперсионного микроанализа EDAX (EDAX Inc., Mahwah, NJ, США) с ультратонким окном. Рентгеновский микроанализ поверхности образцов АМг6 показал, что в составе поверхностных слоев образцов отчетливо наблюдаются пики, соответствующие линиям от Al, Mg, О и С. Судя по данным анализа, в случае происходит высвобождение магния, что указывает на разрушение зерен сплава, в которых магний локализуется по краям кристаллитов.
Таким образом, при воздействии продуктов жизнедеятельности грибов, включающих также и органические кислоты, может идти межкристаллитная коррозия, для которой характерно разрушение сплава по границам кристаллитов (зерен) (ГОСТ 9.908-85), и которая является весьма опасным видом коррозии, так как ведет к потере механической прочности сплава. Биокоррозионные спектры характеризуются появлением новых элементов - магния, кальция, серы, фосфора, натрия и др. Смоделированная коррозия характеризуется появлением кислорода: оксидов или гидрооксидов.
Можно заключить, что методы современной микроскопии позволяют успешно описывать структуру и характер различных повреждений поверхности алюминий-магниевых сплавов, что делает их использование необходимым при тестировании и контроле конструкционных поверхностей в аппаратах, которые будут длительно использоваться на околоземной орбите, а также длительных полетах.


Изобретение относится к технической микробиологии и биокоррозионным испытаниям, а именно к способам моделирования процессов биокоррозионных поражений алюминиево-магниевых сплавов, применяемых в авиа-космической технике. Описан способ моделирования процессов биокоррозионных поражений тонкостенных герметичных оболочек из алюминиево-магниевых сплавов при эксплуатации космических аппаратов, в котором изготавливают испытательные и контрольные образцы из алюминиево-магниевых сплавов АМг6, подготовленные испытательные и контрольные образцы высушивают, испытательные образцы стерилизуют, готовят имитационный состав на основе органической кислоты, который наносят на простерилизованные испытательные образцы, и помещают, по крайней мере, по два образца в чашки Петри, закрывают их, контрольные образцы, обработанные дистиллированной водой, также располагают в чашках Петри, чашки Петри с испытательными и контрольными образцами помещают в разные эксикаторы, на дно которых наливают воду для поддержания влажности более 90%, эксикаторы закрывают и выдерживают при комнатной температуре, проводят экспозицию испытательных и контрольных образцов, затем образцы извлекают из чашек Петри, промывают их в проточной воде, где испытательные и контрольные образцы используют с механически обработанной поверхностью, а для приготовления имитационного состава используют дистиллированную воду и одну из органических кислот, выбранную из следующих карбоновых кислот: глюконовая или малоновая, полученный состав с помощью распылителя наносят на испытательные образцы алюминиево-магниевых сплавов АМг6, после промывания образцов в проточной воде их ополаскивают дистиллированной водой и высушивают, затем с помощью растрового электронного микроскопа оценивают начальные этапы биокоррозии и ее тип, исследуют химический состав пораженной поверхности образцов, при этом экспозицию испытательных и контрольных образцов проводят в течение 30-45 суток. Также описан имитационный состав для моделирования процессов биокоррозионных поражений тонкостенных герметичных оболочек из алюминиево-магниевых сплавов. Технический результат: увеличенная надежность и ресурс эксплуатации конструкционных материалов в присутствии технофильных микроорганизмов в эксплуатационных условиях гермозамкнутого объема. 3 н.п. ф-лы, 9 ил., 1 табл.
1. Способ моделирования процессов биокоррозионных поражений тонкостенных герметичных оболочек из алюминиево-магниевых сплавов при эксплуатации космических аппаратов, характеризующийся тем, что изготавливают испытательные и контрольные образцы из алюминиево-магниевых сплавов АМг6, подготовленные испытательные и контрольные образцы высушивают, испытательные образцы стерилизуют, готовят имитационный состав на основе органической кислоты, который наносят на простерилизованные испытательные образцы, и помещают, по крайней мере, по два образца в чашки Петри, закрывают их, контрольные образцы, обработанные дистиллированной водой, также располагают в чашках Петри, чашки Петри с испытательными и контрольными образцами помещают в разные эксикаторы, на дно которых наливают воду для поддержания влажности более 90%, эксикаторы закрывают и выдерживают при комнатной температуре, проводят экспозицию испытательных и контрольных образцов, затем образцы извлекают из чашек Петри, промывают их в проточной воде, отличающийся тем, что испытательные и контрольные образцы используют с механически обработанной поверхностью, а для приготовления имитационного состава используют дистиллированную воду и одну из органических кислот, выбранную из следующих карбоновых кислот: глюконовая или малоновая, полученный состав с помощью распылителя наносят на испытательные образцы алюминиево-магниевых сплавов АМг6, после промывания образцов в проточной воде их ополаскивают дистиллированной водой и высушивают, затем с помощью растрового электронного микроскопа оценивают начальные этапы биокоррозии и ее тип, исследуют химический состав пораженной поверхности образцов, при этом экспозицию испытательных и контрольных образцов проводят в течение 30-45 суток.
2. Имитационный состав для моделирования процессов биокоррозионных поражений тонкостенных герметичных оболочек из алюминиево-магниевых сплавов при эксплуатации космических аппаратов, включающий органическую кислоту, растворитель, отличающийся тем, что в качестве органической кислоты он содержит глюконовую кислоту, а в качестве растворителя - дистиллированную воду при следующем соотношении компонентов, мас.ч.:
5-10% раствор глюконовой кислоты - 0,05-0,10;
дистиллированная вода - 0,95-0,90.
3. Имитационный состав для моделирования процессов биокоррозионных поражений тонкостенных герметичных оболочек из алюминиево-магниевых сплавов при эксплуатации космических аппаратов, включающий органическую кислоту, растворитель, отличающийся тем, что в качестве органической кислоты он содержит малоновую кислоту, а в качестве растворителя - дистиллированную воду при следующем соотношении компонентов, мас.ч.:
5-10% раствор малоновой кислоты - 0,05-0,10;
дистиллированная вода - 0,95-0,90.
| СПОСОБ КАЧЕСТВЕННОЙ ОЦЕНКИ БИОКОРРОЗИОННЫХ ПОРАЖЕНИЙ ТОНКОСТЕННЫХ ГЕРМЕТИЧНЫХ ОБОЛОЧЕК ИЗ АЛЮМИНИЕВО-МАГНИЕВЫХ СПЛАВОВ ПРИ ЭКСПЛУАТАЦИИ КОСМИЧЕСКИХ АППАРАТОВ И СУСПЕНЗИЯ СПОРОВЫХ МАТЕРИАЛОВ ДЛЯ ЕГО РЕАЛИЗАЦИИ | 2011 |
|
RU2486250C2 |
| СПОСОБ ЗАЩИТЫ СТАЛИ ОТ КОРРОЗИИ | 1996 |
|
RU2124579C1 |
| ГРИБОСТОЙКИЙ ЛАКОКРАСОЧНЫЙ СОСТАВ | 1995 |
|
RU2111996C1 |
| ГРИБОСТОЙКИЙ ИНГИБИРОВАННЫЙ ЛАКОКРАСОЧНЫЙ ЗАЩИТНЫЙ СОСТАВ | 1998 |
|
RU2159261C2 |
Авторы
Даты
2016-11-27—Публикация
2015-01-26—Подача