Изобретение относится к новым соединениям, а именно к комплексам лантанидов с фторпроизводными бензойной кислоты, проявляющим люминесцентные свойства.
Известно, что координационные соединения (КС) лантанидов с органическими лигандами часто проявляют люминесцентные свойства, в том числе при фото- или электровозбуждении.
При этом, как правило, изначально переходит в возбужденное состояние органический лиганд, после чего энергия передается на ион лантанида, который люминесцирует. В связи с этим за счет большего поглощения лиганда, чем лантанида, часто использование органических лигандов позволяет повысить интенсивность люминесценции КС лантанидов по сравнению с неорганическими соединениями, такими как нитраты или хлориды [1].
Фундаментальные особенности люминесценции ионов лантанидов, такие как большие времена жизни возбужденного состояния, узкие полосы люминесценции и способность ряда из них излучать в ИК диапазоне, делает координационные соединения лантанидов чрезвычайно интересными для исследования и возможного применения.
В качестве органических лигандов могут быть использованы лиганды разных классов, например ароматические карбоксилаты, бета-дикетонаты, феноляты, пиразолонаты, основания Шиффа [2, 3].
Люминесцирующие комплексные соединения лантанидов находят широкое применение в качестве различных меток, в том числе для оптической биовизуализации. Важным является также их применение в качестве люминесцентных материалов в оптических приборах, в том числе в качестве эмиссионного слоя в органических светодиодах.
Органические светодиоды - это устройства, излучающие свет под действием электрического тока. Органический светодиод состоит, по крайней мере, из эмиссионного слоя, заключенного между катодом и анодом. Эмиссионный слой - это тонкая (20-200 нм) пленка люминесцирующего соединения. При протекании тока через органический светодиод носители заряда разного знака - электроны и дырки - рекомбинируют в эмиссионном слое, что приводит к возникновению возбужденных состояний - экситонов, 75% которых являются триплетными и 25% - синглетными. Релаксация возбужденных состояний приводит к люминесценции материала эмиссионного слоя.
Поскольку 75% экситонов являются триплетными, в качестве материалов эмиссионного слоя целесообразно использовать соединения, в люминесценции которых участвует триплетный уровень. К таким относятся почти все координационные соединения (КС) лантанидов, в которых ионная люминесценция лантанидов происходит после передачи энергии с триплетного уровня органического лиганда на возбужденный уровень лантанида, кроме соединений лантана, лютеция, люминесценция которых происходит из синглетного состояния (флуоресценция), и гадолиния, у которых возможна люминесценция из триплетного состояния (фосфоресценция), но обычно только при пониженной температуре (-200°С).
С точки зрения использования особый интерес представляют ароматические карбоксилаты лантанидов, которые обладают высокой стабильностью (химической, оптической, термической). Однако большинство из них растворимы только в органических растворителях или вовсе нерастворимы [2, 4, 5], что существенно затрудняет их использование.
Получение стабильных и растворимых люминесцирующих КС является актуальной задачей.
В работах [6-9] получены комплексы Eu, Gd, Tb, Dy и Er с анионом пентафторбензойной кислоты. Показано, что комплексы Eu, Tb и Er обладают люминесценцией.
Люминесцирующие фторбензоаты лантанидов, кроме указанных пентафторбензоатов, в литературе не выявлены.
Технической задачей, на решение которой направлено представленное изобретение, является расширение арсенала комплексов лантанидов, обладающих люминесцирующими свойствами.
Поставленная задача решена тем, что получены фторзамещенные ароматические карбоксилаты лантанидов общей формулы
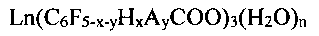
где x=0, 1, 2, 3; y=0, 1, n=0, 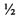 , 1, 2;
, 1, 2;
для x=0, y=0 Ln=La, Pr, Nd, Sm, Ho, Tm, Yb, Lu, Tb0.5Eu0.5;
для остальных сочетаний x и y Ln=La, Pr, Nd, Sm, Eu, Gd, Tb, Dy, Ho, Tm, Yb, Er, Lu, Tb0.5Eu0.5;
A=-Cl, -NH2, -COOCnH2n+1 (n=1, 2), -CH2R, где R=-H, -OH, -Cl, -F, -NH2, -CnH2n+1 (n=1, 2),
проявляющие люминесцентные свойства.
В качестве заместителя А (заместителя, отличного от фтора) может быть использован любой заместитель, который не гасит люминесценцию, например -Cl, -NH2, -CH2R. Причем нами показано, что введение группы-линкера (-СН2-) заметно ослабляет гасящее действие радикала, что позволяет в такой комбинации использовать в качестве радикала не только группы -Cl, -F, -NH2, -CnH2n+1, но даже такую группу, как -ОН, которая в других случаях заметно гасит люминесценцию.
Указанные комплексы могут быть получены, например, при взаимодействии гидроксида лантанида и соответствующей кислоты в органической среде или при взаимодействии растворимой соли соответствующей кислоты с нитратом или хлоридом лантанида в водном или водно-органическом растворе.
В первом случае синтез проводят при взаимодействии избытка свежеосажденного гидроксида лантанида с суспензией соответствующей кислоты в органической среде.
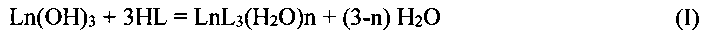
При этом происходит растворение за счет комплексообразования.
Нерастворенный избыток исходного гидроксида отфильтровывают, а прозрачный раствор быстро упаривают досуха на роторном испарителе. Полученный продукт растворяют в воде, отфильтровывают от водонерастворимых примесей и быстро упаривают досуха на роторном испарителе.
Во втором случае синтез проводят при взаимодействии водного или водно-органического раствора растворимой соли соответствующей кислоты (например, натриевой) с водным раствором нитрата или хлорида лантанида
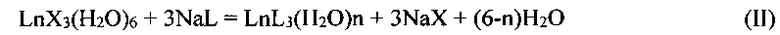
Х = Cl, NO3.
Полученный прозрачный раствор быстро упаривают досуха на роторном испарителе, сухой остаток промывают небольшим количеством воды для удаления NaX. Полученный продукт растворяют в воде, отфильтровывают от водонерастворимых примесей и быстро упаривают досуха на роторном испарителе.
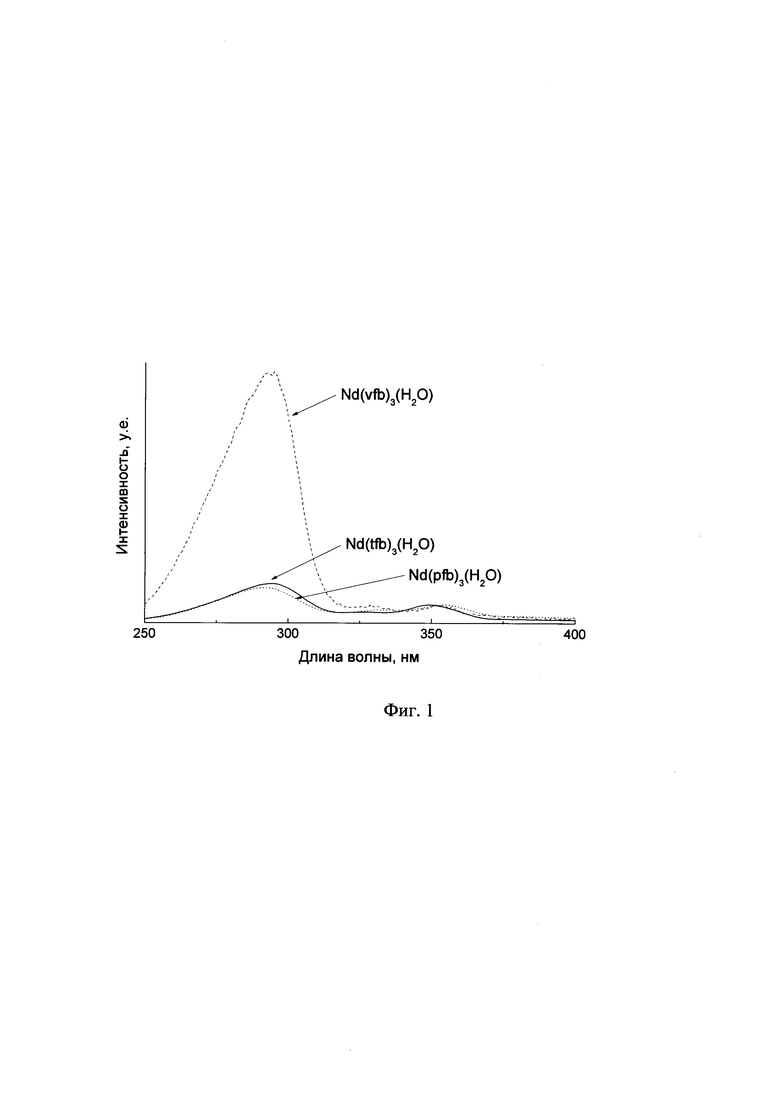
Фиг. 1 Фрагменты спектров возбуждения 2,4,5-три-, тетра- и пентафторбензоатов неодима, зарегистрированные на длине волны 1055 нм
Следующие примеры конкретного исполнения иллюстрируют заявленное изобретение, но не ограничивают его.
Примеры
Комплексы 1-41, 44-49 получают в соответствии со схемой (I) следующим образом.
К раствору 1.1 ммоль нитрата РЗЭ в 10 мл воды прикапывают стехиометрическое количество водного раствора аммиака. Выпавший гидроксид РЗЭ центрифугируют, трехкратно промывают водой и переносят в стакан с раствором 3 ммоль кислоты в 10 мл смеси ацетон:метанол (3:1). Реакционную смесь оставляют на магнитной мешалке на сутки, при этом происходит растворение за счет комплексообразования. Нерастворенный избыток исходного гидроксида РЗЭ отфильтровывают на бумажном фильтре, прозрачный раствор упаривают досуха на роторном испарителе (30 мин, водоструйный насос, 60°С). Продукт собирают и сушат на воздухе (сутки). Полученный порошок растворяют в 100 мл воды и отфильтровывают водонерастворимые примеси. Полученный прозрачный водный раствор быстро упаривают на роторном испарителе при температуре 80°С в течение 1 часа, оставшийся сухой продукт собирают.
При получении биметаллических комплексов в реакцию вводят смешанный гидроксид Tb0.5EU0.5(ОН)3, полученный взаимодействием водного раствора аммиака и раствора эквимолярной смеси хлоридов тербия и европия.
Комплексы 42-43 получают в соответствии со схемой (II).
К раствору 1 ммоль нитрата РЗЭ в 10 мл воды прикапывают 3 ммоль водно-спиртового (1:1) раствора стехиометрического количества калиевой соли 2,4,5-трифторбензойной кислоты. Выпавший белый осадок отфильтровывают на бумажном фильтре и трехкратно промывают холодной водой (по 1 мл). Полученный порошок растворяют в 100 мл воды и отфильтровывают водонерастворимые примеси. Полученный прозрачный водный раствор быстро упаривают на роторном испарителе при температуре 80° С в течение 1 часа, оставшийся сухой продукт собирают.
Состав целевого продукта устанавливают по совокупности данных элементного анализа (Vario Micro Cube, Elementar, Германия), термического анализа (термоанализатор STA 409, фирма NETZSCH, Германия, в диапазоне температур 20-1000° С в токе аргона, скорость нагрева 10°/мин, начальная масса ~5 мг), протонного магнитного резонанса (Avance-400, Bruker).
Наличие и область люминесценции устанавливают путем регистрации спектров люминесценции при возбуждении длиной волны 300 нм на люминесцентном спектрометре Perkin-Elmer LS-55 в видимой области и на люминесцентном спектрометре Edinburgh Instruments FLSP920 в ИК диапазоне.
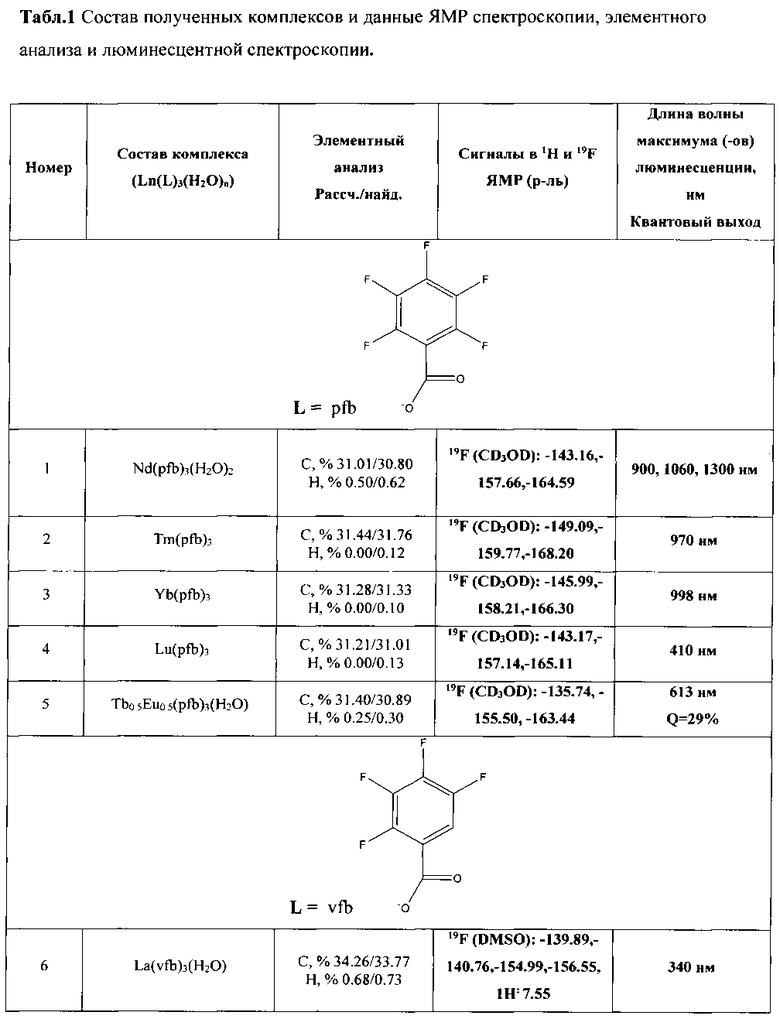
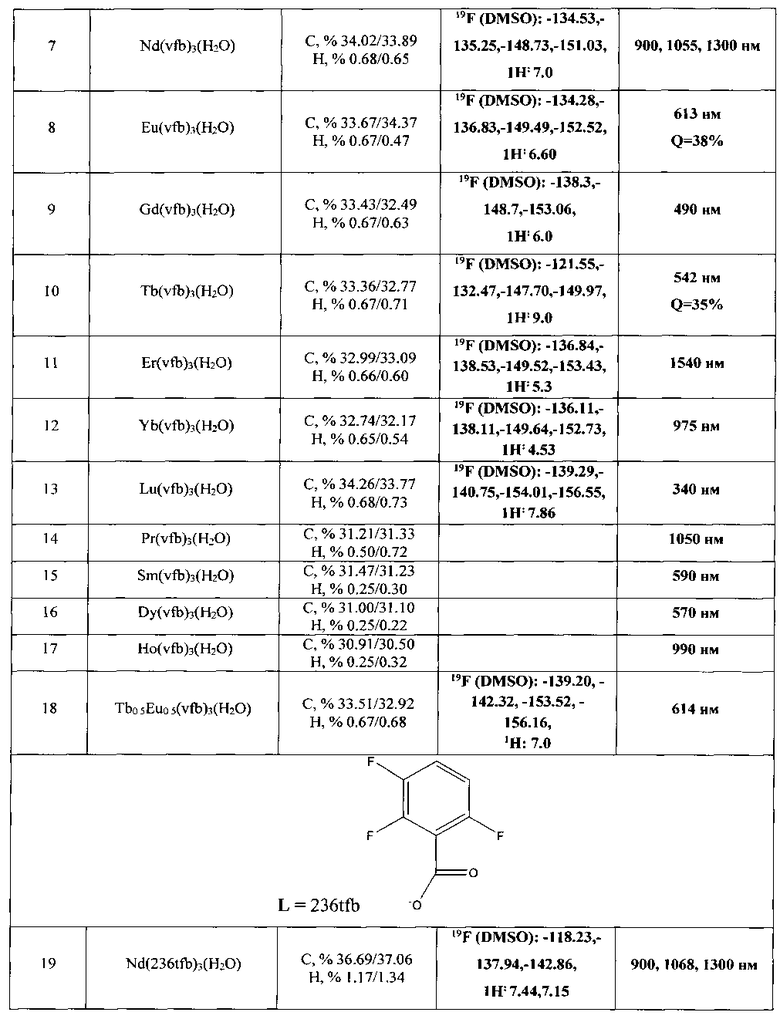
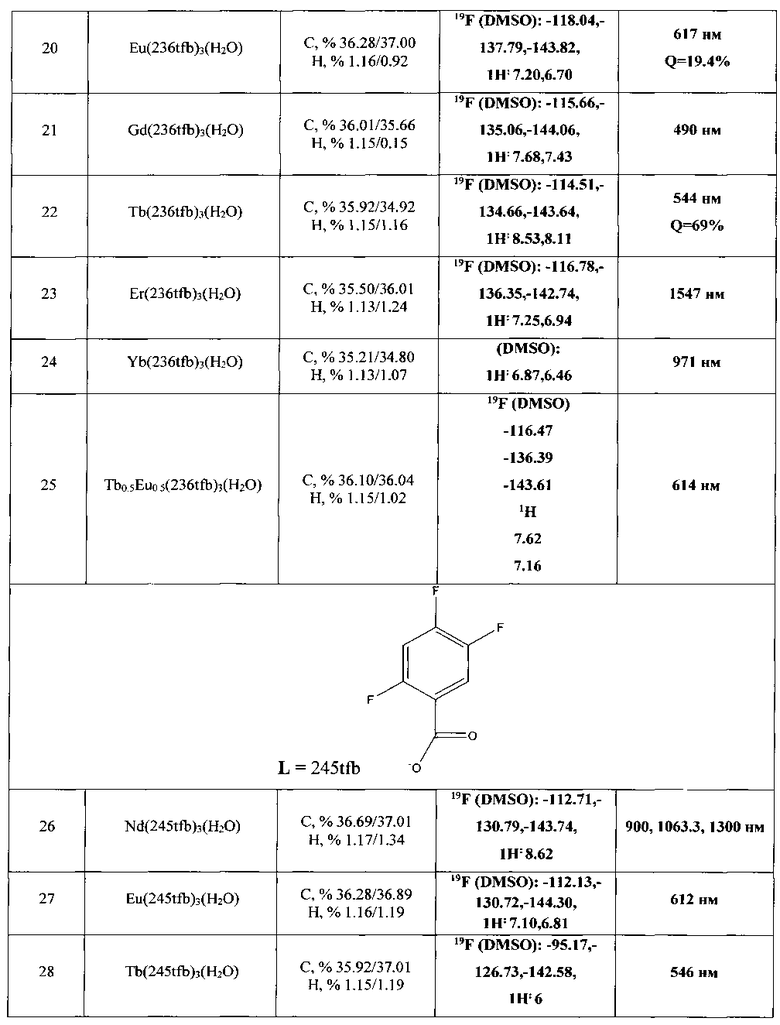
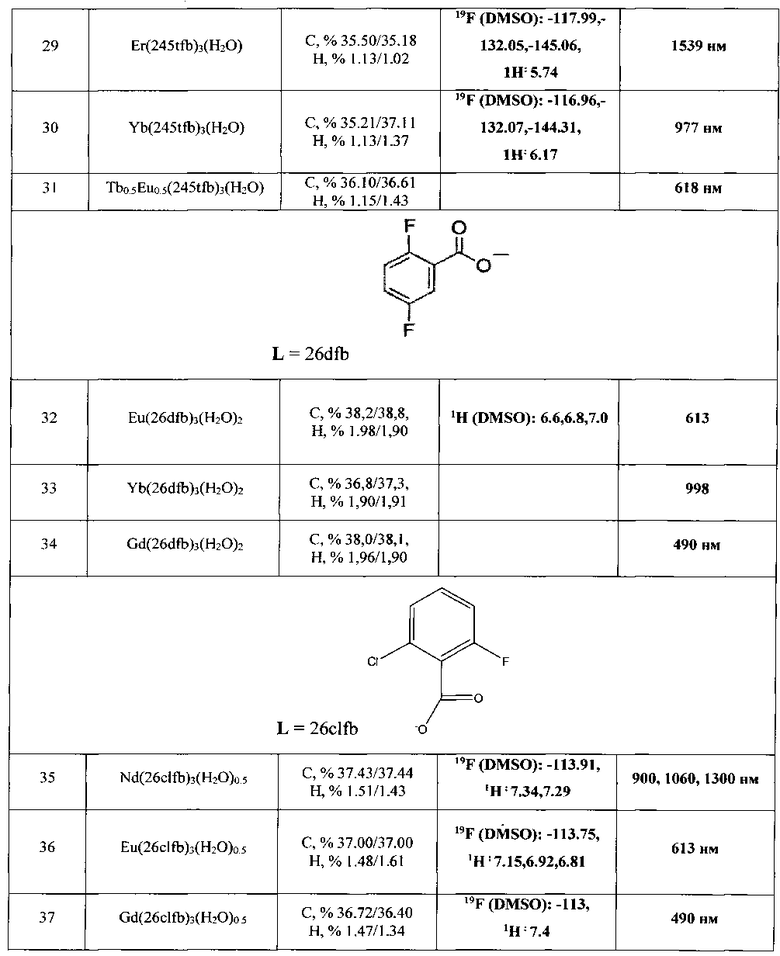
Результаты анализа приведены в табл. 1. В табл. 1 и далее по тексту использованы следующие обозначения:
pfb - пентафторбензоат
vfb - 2,3,4,5-тетрафторбензоат
236tfb - 2,3,6-трифторбензоат
245tfb - 2,4,5-трифторбензоат
26dfb - 2,6-дифторбензоат
26clfb - 2-хлор-6-фторбензоат
pam - 4-амино-2,3,5,6-тетрафторбензоат
pmc - 4-метоксикарбонил-2,3,5,6-тетрафторбензоат
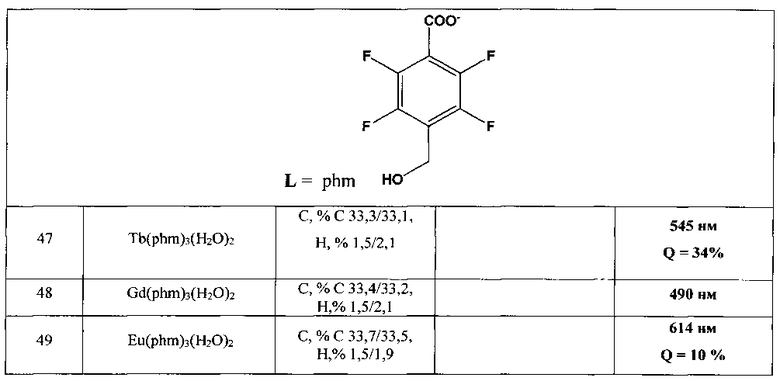
phm - 4-гидроксиметил-2,3,5,6-тетрафторбензоат
Для полученных комплексов были исследованы также растворимость в воде и ряде органических растворителях (метод [10]), стабильность на воздухе, термическая стабильность (термический анализ), оптическая стабильность (постоянное облучение азотным лазером (337 нм 50 мкВт) в течение не менее 10 часов).
Проведенные исследования показали, что полученные фторзамещенные ароматические карбоксилаты лантанидов
- люминесцируют, причем люминесценция всех полученных комплексов, кроме комплексов лантана, гадолиния и лютеция, представляет собой ионную люминесценцию соответствующего лантанида, сенсибилизированную органическим лигандом;
- растворимы в воде (растворимость составляет не менее 10 ммоль/л), что особенно важно при использовании люминофоров для оптической биовизуализации, а также хорошо растворимы в таких органических растворителях, как метанол, этанол, ацетонитрил, ДМСО, хлороформ, что позволяет получать тонкие пленки из раствора;
- стабильны:
- на воздухе,
- при нагревании до 200°С,
- оптически.
Среди полученных соединений наиболее интересными являются:
1. Комплексы Tb(pmc)3(H2O)2, Tb(236tfb)3(H2O) и Eu(vfb)3(H2O), которые, наряду с хорошей растворимостью и стабильностью, обладают большим квантовым выходом (62%, 69% и 38% соответственно), что открывает большие перспективы для их использования.
2. Комплекс неодима Nd(vfb)3(H2O), в котором наблюдается высокая эффективность сенсибилизации иона неодима через лиганд, что наглядно характеризуют приведенные на фиг. 1 фрагменты спектров возбуждения 2,4,5-три-, тетра- и пентафторбензоатов неодима, зарегистрированные на длине волны люминесценции 1055 нм. О высокой эффективности сенсибилизации свидетельствует наблюдаемое высокое соотношение интенсивности люминесценции иона лантанида в результате возбуждения через лиганд (290 нм) и в результате прямого возбуждения через металл (350 нм). Это особенно важно в связи с тем, что люминесценция данного комплекса лежит в ИК области, а создание новых люминофоров, излучающих в ИК области, является особенно сложной и актуальной задачей.
3. Все исследованные комплексы гадолиния, люминесценция которых даже при комнатной температуре представляет собой фосфоресценцию органического лиганда (длина волны 490 нм, время жизни более 1 мкс), что открывает большие перспективы для использования их в качестве эмиссионных материалов в OLED, где важны именно фосфоресцирующие соединения, как замена дорогостоящим соединениям иридия.
4. Биметаллический комплекс Tb0.5Eu0.5(pfb)3(H2O), проявляющий ионную люминесценцию иона европия с квантовым выходом 29%, что вдвое выше, чем квантовый выход монометаллического пентафторбензоата европия [9]. Ранее в литературе не были описаны примеры повышения квантового выхода комплекса европия за счет частичного замещения европия тербием.
Источники информации
1. Bunzli, J.-C.G., Eliseeva, S.V., in Lanthanide Luminescence: Photophysical, Analytical and Biological Aspects, P.H.a.H. Harma, Editor. 2010, Springer Ser Fluoresc.
2. Kotova, O.V., Utochnikova, V.V., Kuzmina, N.P., J. Mater. Chem., 2012. 22: p. 4897.
3. Utochnikova, V.V., Kovalenko, A.D., Burlov, A.D., Marciniak, L., Ananyev, I., Kalyakina, A.S., Kurchavov, N.A., Kuzmina, N.P., Dalton Trans., 2015. 44(12660-12669).
4. Hilder, M., Junk, P.C., Kynast, U.H., Lezhnina, M.M., J. of Photochem. Photobiol. A: Chemistry, 2009. 202: p.10.
5. Hilder, M., Lezhnina, M., Cole, M., Forsyth, C, Junk, P., Kynast, U.H., J. Photochem. Photobiol. A: Chemistry, 2011. 217: p. 76.
6. Larionov, S.V., Glinskaya, L.A. Leonova, T.G. et. al., Russian Journal of coordination chemistry, 2009. 35(11).
7. Глинская Л.А., Леонова Т.Г. и др. Журнал структурной химии, 2010. 51(3): р. 610-615.
8. Ron, S.-G., Oh, J.В., Nah, М.-K., Baek, N.S., Lee, Y., Kim, H.K., Bull. Korean Chem. Soc., 2004. 25: p. 1503-1507.
9. Ларионов С.В., Кириченко В.И. и др. Координационная химия, 1997. 23(6): р. 465-471.
10. Utochnikova, V., Pietraszkiewicz, О., Pietraszkiewicz, М., Kuzmina, N., J. of Photochem. and Photobiology A: Chemistry, 2013. 253: p. 72-80.

| название | год | авторы | номер документа |
|---|---|---|---|
| Разнолигандные фторзамещенные ароматические карбоксилаты лантанидов, проявляющие люминесцентные свойства, и органические светодиоды на их основе | 2017 |
|
RU2657496C1 |
| 9-антраценаты лантанидов, проявляющие люминесцентные свойства, и органические светодиоды на их основе | 2015 |
|
RU2626824C2 |
| 2-(ТОЗИЛАМИНО)БЕНЗИЛИДЕН-N-АЛКИЛ(АРИЛ, ГЕТАРИЛ)АМИНАТЫ ЛАНТАНИДОВ, ПРОЯВЛЯЮЩИЕ ЛЮМИНЕСЦЕНТНЫЕ СВОЙСТВА | 2014 |
|
RU2586096C2 |
| Пиразолкарбоксилаты лантанидов, проявляющие люминесцентные свойства в видимом диапазоне | 2017 |
|
RU2663671C2 |
| Комплексы лантанидов, проявляющие люминесцентные свойства, способ определения концентрации глюкозы на их основе | 2022 |
|
RU2813337C1 |
| Пиразоло[1,5-а]пиримидинкарбоксилаты гадолиния и органические светодиоды на их основе | 2017 |
|
RU2671964C1 |
| Способ получения эмиссионного слоя на основе соединений редкоземельных элементов и органический светоизлучающий диод | 2017 |
|
RU2657497C1 |
| ОРГАНИЧЕСКИЕ СВЕТОДИОДЫ НА ОСНОВЕ КООРДИНАЦИОННЫХ СОЕДИНЕНИЙ ЛАНТАНИДОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2022 |
|
RU2804718C1 |
| Разнолигандные комплексные соединения тербия с фенантролином, интенсивность люминесценции которых зависит от температуры | 2014 |
|
RU2620117C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЛЮМИНЕСЦИРУЮЩИХ РАСТВОРИМЫХ КОМПЛЕКСОВ ДВУХВАЛЕНТНЫХ ЛАНТАНИДОВ LnCl∙(ТГФ) (Ln=Eu, Yb, Sm) | 2014 |
|
RU2574265C2 |
Изобретение относится к фторзамещенным ароматическим карбоксилатам лантанидов общей формулы Ln(C6F5-x-yHxAyCOO)3(H2O)n, где х=0, 1, 2, 3, у=0, 1, n=0, ½, 1, 2; для х=0, у=0 Ln=La, Pr, Nd, Sm, Ho, Tm, Yb, Lu, Tb0.5Eu0.5; для остальных сочетаний x и у Ln=La, Pr, Nd, Sm, Eu, Gd, Tb, Dy, Ho, Tm, Yb, Er, Lu, Tb0.5Eu0.5; A= -Cl, -NH2, -COOCnH2n+1 (n=1, 2), -CH2R, где R=H, OH, Cl, F, NH2, CnH(2n+1) (n=1, 2). Указанные соединения проявляют люминесцентные свойства. 5 з.п. ф-лы, 1 ил., 1 табл., 2 пр.
1. Фторзамещенные ароматические карбоксилаты лантанидов общей формулы
Ln(C6F5-x-yHxAyCOO)3(H2O)n,
где х=0, 1, 2, 3; у=0, 1, n=0, 1/2, 1, 2;
для х=0, у=0 Ln=La, Pr, Nd, Sm, Ho, Tm, Yb, Lu, Tb0.5Eu0.5;
для остальных сочетаний x и у Ln=La, Pr, Nd, Sm, Eu, Gd, Tb, Dy, Ho, Tm, Yb, Er, Lu, Tb0.5Eu0.5;
A= -Cl, -NH2, -COOCnH2n+1 (n=1, 2), -CH2R, где R=H, OH, Cl, F, NH2, CnH(2n+1) (n=1, 2),
проявляющие люминесцентные свойства.
2. Фторзамещенный ароматический карбоксилат по п.1, где Ln=Eu, х=1, у=0, n=1, демонстрирующий большой квантовый выход люминесценции.
3. Фторзамещенный ароматический карбоксилат по п.1, где Ln=Tb, х=0, у=1, n=2, А= -С(O)ОСН3, демонстрирующий большой квантовый выход люминесценции.
4. Фторзамещенный ароматический карбоксилат по п.1, где Ln=Tb, х=2 (F в положении 2,3,6), у=0, n=1, демонстрирующий большой квантовый выход люминесценции.
5. Фторзамещенный ароматический карбоксилат по п.1, где Ln=Nd, х=1, у=0, n=1, в котором лиганд обладает большой сенсибилизирующей способностью.
6. Фторзамещенные ароматические карбоксилаты по п.1, где Ln=Gd, фосфоресцирующие при комнатной температуре.
| ГЛИНСКАЯ Л.А | |||
| и др., Кристаллическая и молекулярная структура соединения [Nd(HO)(CFCOO)]2HO, Журнал структурной химии, 2010, т | |||
| Способ запрессовки не выдержавших гидравлической пробы отливок | 1923 |
|
SU51A1 |
| ШАХТНАЯ ТОПКА ДЛЯ МНОГОЗОЛЬНОГО ТОРФА | 1922 |
|
SU610A1 |
| LARIONOV S.V | |||
| et al, Luminescence properties of complexes Ln(Phen)(CFCOO) (Ln | |||
Авторы
Даты
2016-12-27—Публикация
2015-09-04—Подача