Изобретение относится к области сорбционных материалов и может быть применено для концентрирования различных типов органических веществ с такими активными атомами, как кислород и фтор в химической, фармацевтической и других областях промышленности.
Существуют сорбенты для обогащения фосфорсодержащих пептидов по методу металл-аффинной хроматографии [1]. В таком случае используют хелаты производных иминодиуксусной или нитрилотриуксусной кислот с такими ионами металлов, как Fe3+, Ga3+, Ti4+, Zr4+ и др. Выбор металла обусловлен их способностью образовывать координационные связи с атомами кислорода фосфатной группы. Такое связывание позволяет достаточно селективно адсорбировать фосфорсодержащие пептиды, и в результате концентрировать их путем элюирования с сорбента. В частности, для сорбента PHOS-Select Iron Affinity Gel [2] концентрация ионов Fe3+ составляет 7-17 мкмоль/мл геля, связывающая способность - до 0.3 мкмоль/г сорбента. Недостатками таких сорбентов являются высокая степень неспецифического связывания пептидов с ними, а также весьма высокая стоимость.
Задачей изобретения является повышение селективности и степени концентрирования по методу металл-аффинной хроматографии различных типов органических веществ, содержащих активные атомы кислорода или фтора. Указанная задача решается применением регулярных мультимолекулярных структур (пленок Ленгмюра-Блоджетт) на основе стеаратов трехвалентных металлов, содержащих лабильную ковалентную связь, в качестве сорбента для металл-аффинной хроматографии водорастворимых органических и биоорганических соединений, имеющих в составе атомы кислорода или фтора [3].
Предлагаемый сорбент представляет собой соли стеариновой кислоты с различными металлами в виде регулярных мультимолекулярных слоев пленок Ленгмюра-Блоджетт, содержащих лабильную ковалентную связь. Выбор металла зависит от природы активного атома в соответствии с теорией Пирсона (теория жестких и мягких кислот и оснований), а именно: регулярные мультимолекулярные структуры (РММС), содержащие металлы, классифицируемые как жесткие кислоты Льюиса (Fe(III), La(III), Ga(III) и др.), содержат лабильную ковалентную связь и подходят для обогащения образцов водорастворимыми соединениями, в состав которых входят активные атомы кислорода или доступные атомы фтора. Структура сорбента чрезвычайно устойчива, не подвержена гидролизу.
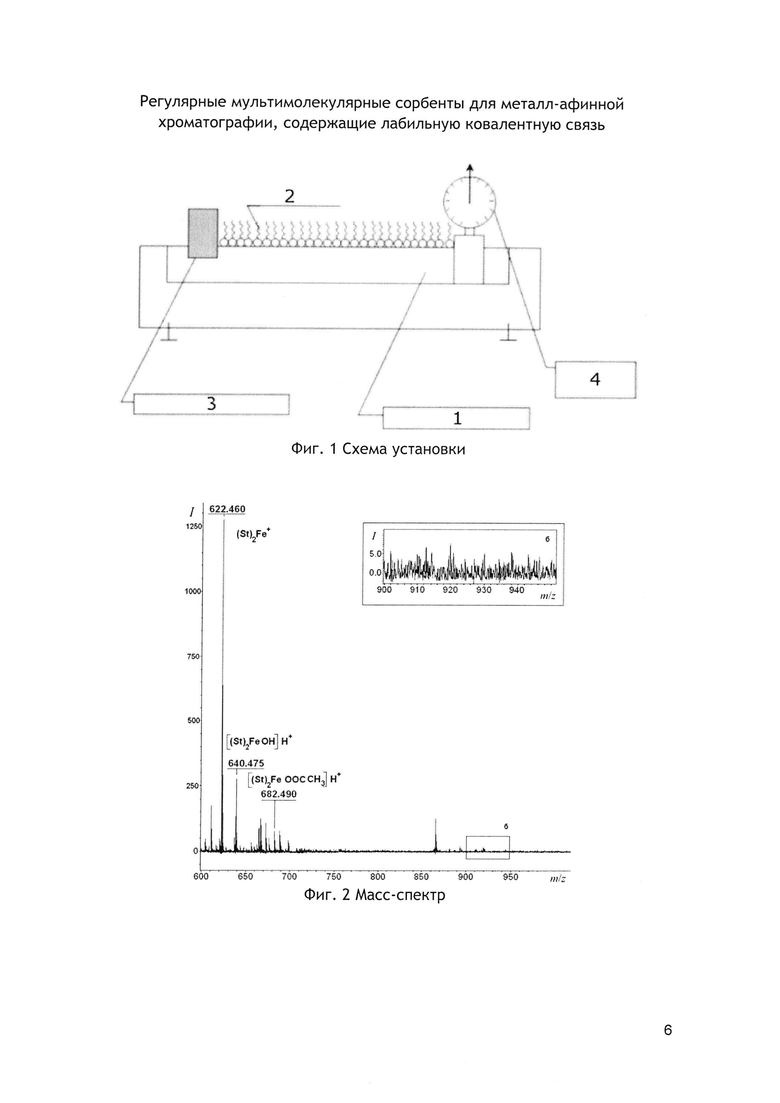
Схема процесса получения мультимолекулярных слоев пленок Ленгмюра-Блоджетт изображена на фигуре 1. РММС, нанесенные на твердую подложку, невозможно использовать в качестве сорбентов для металл-аффинной хроматографии. Нами был разработан метод получения аналогичных структур на поверхности водной субфазы, базирующийся на теории медленного коллапса (фиг. 1). В специальной ванне (1) на поверхность водной субфазы наносят по каплям раствор ПАВ (в данном случае, стеариновой кислоты) в подходящем неполярном легколетучем органическом растворителе (в данном случае, в гексане). Раствор ПАВ растекается по поверхности воды, образуя монослой (2), ограниченный бортами ванны, подвижным барьером (3) и весами Ленгмюра (4), которые могут измерять (а подвижный барьер - регулировать) поверхностное давление в образовавшемся монослое. На поверхности водной субфазы, содержащей необходимые ионы химической реакции между монослоем стеариновой кислоты и ионами металла субфазы в монослое образуются соответствующие стеараты. Далее этот монослой стеаратов очень медленно сжимается в тангенциальном направлении (0.5 см/мин). Т.к. при высоком поверхностном давлении (-25 мН/м) монослой стеаратов находится в конденсированном (кристаллическом) состоянии, то при достижении давления коллапса монослой подвергается деструкции, образуются трещины и петли. При дальнейшем увеличении поверхностного давления отдельные части монослоя начинают наползать друг на друга. Так образуются мультимолекулярные (многослойные) структуры (ММС) на поверхности водной субфазы. Далее эти структуры с поверхности собирают механически и высушивают. Преимуществом данного метода получения сорбента является то, что поверхность структуры состоит практически полностью из ионов металла, химически связанных с молекулами органической матрицы.
Охарактеризация пленок, полученных с использованием соли Fe(III), была проведена с помощью масс-спектрометрии с мягкими методами ионизации [2]. На фигуре 2 показан масс-спектр продуктов взаимодействия монослоев стериновой кислоты с ионами железа(III) субфазы (MALDI-TOF). В результате масс-спектрометрического анализа было установлено, что мономолекулярный слой пленки состоит в основном из дистеаратов железа(III), а не тристеаратов, что вызвано стерическими затруднениями. Поскольку на поверхности пленки находится большое количество ионов металла 1,5-2,2 мкмоль/мг пленки, а удельная поверхность 4 м2/г, что говорит об отсутствии пористости), такая структура может быть использована в качестве сорбента для концентрирования органических веществ по методу металл-аффинной хроматографии. В отличие от коммерческих решений, регулярные мультимолекулярные структуры, полученные с использованием соли Fe(III), имеют значительно большее количество доступных ионов металла на поверхности пленки (связывающая способность - 6.4 мкмоль белка/г сухого сорбента по результатам эксперимента с монофосфорилированным пептидом), что увеличивает емкость сорбента. Кроме того, производство РММС на основе стеариновой кислоты достаточно дешевое.
Процедура применения полученного сорбента для проведения металл-аффинной хроматографии: навеску ~10 мг сорбента нанесли на фильтр с мембраной Millex-LH, и центрифугировали 1 мин при 10000 об/мин для удаления растворителя. Полученную колонку три раза промыли 0.1% трифторуксусной кислотой (ТФУ). 30 мкл образца (например, пептида в концентрации 0.5 мг/мл) растворили в 70 мкл 0.1% ТФУ и перенесли в колонку с сорбентом. Колонку поместили в чистую микропробирку и инкубировали в течение 15 минут на качающейся платформе, после чего проскок удалили с фильтра в микропробирку. Чтобы избежать неспецифической сорбции, сорбент трижды промыли 100 мкл 0.1% ТФУ и центрифугировали 30 секунд при 5000 об/мин. Для ступенчатого элюирования на колонку, помещенную в новую микропробирку, нанесли 100 мкл элюирующего раствора (400 мМ гидроксид аммония) и смесь инкубировали в течение 10 минут на качающейся платформе, после чего центрифугировали 30 секунд при 5000 об/мин, элюат отбирали для анализа. Затем можно наносить следующий подходящий элюирующий раствор по описанной технике.
При помощи атомно-силового микроскопа Ntegra Aura (NT MDT, Россия) были проведены исследования процесса сорбции фосфорилированного белка казеина (casein Bos Taurus, молекулярная масса 18 кДа) на ПЛБ на основе стеарата лантана(III), перенесенных на твердую подложку.
На фигуре 3А представлено изображение поверхности чистой кремниевой подложки. На нее были нанесены ПЛБ на основе стеарата лантана(III) (фигура 3.Б). При сравнении рельефов видно, что ПЛБ были успешно перенесены на подложку, так как резко уменьшилась шероховатость поверхности. Затем подложка была помещена в водный раствор казеина (концентрация 100 мкг/мл) на сутки, после чего была промыта дистиллированной водой для удаления непрореагировавшего с поверхностью казеина (фигура 3.В). На поверхности ПЛБ видны участки, на которых произошла адсорбция агрегатов казеина, со средними размерами 200-500 нм. Затем для десорбции казеина подложка была помещена на 1 час в 0.4 М водный раствор аммиака (фигура 3.Г). Все ранее адсорбированные частицы, отнесенные к агрегатам казеина, были удалены с поверхности ПЛБ полностью. Успешная сорбция и десорбция фосфорилированного белка в условиях, соответствующих классическому металл-аффинному анализу, доказывает возможность использования исследуемых ПЛБ в качестве металл-аффинного сорбента.
Таким образом, полученные ПЛБ на основе стеарата лантана(III) проявляют свойства металл-аффинного сорбента, то есть проявляют специфичность к атомам кислорода, входящих в состав фосфорных групп казеина.
Смесь 8 пептидов-фрагментов тау-белка, SSNGHV(pY)EKLSSI, FGE(pS)AGAAS, FGESAGAAS, взятых в равных количествах (таблица 1). В качестве сорбента сравнения был выбран коммерческий железосодержащий Iron Affinity Gel. Все сорбенты были взяты в равных количествах по сухой массе.
Анализ, проведенный методом металл-аффинной хроматографии с последующим ВЭЖХ-МС детектированием, показал, что сорбент демонстрирует высокую селективность к фосфорилированным пептидам (1р, 1рр, 2р, 2рр, Зрр, 4р, 5р) по сравнению с нефосфорилированными (1, 2, 3, 4) (фигура 4).
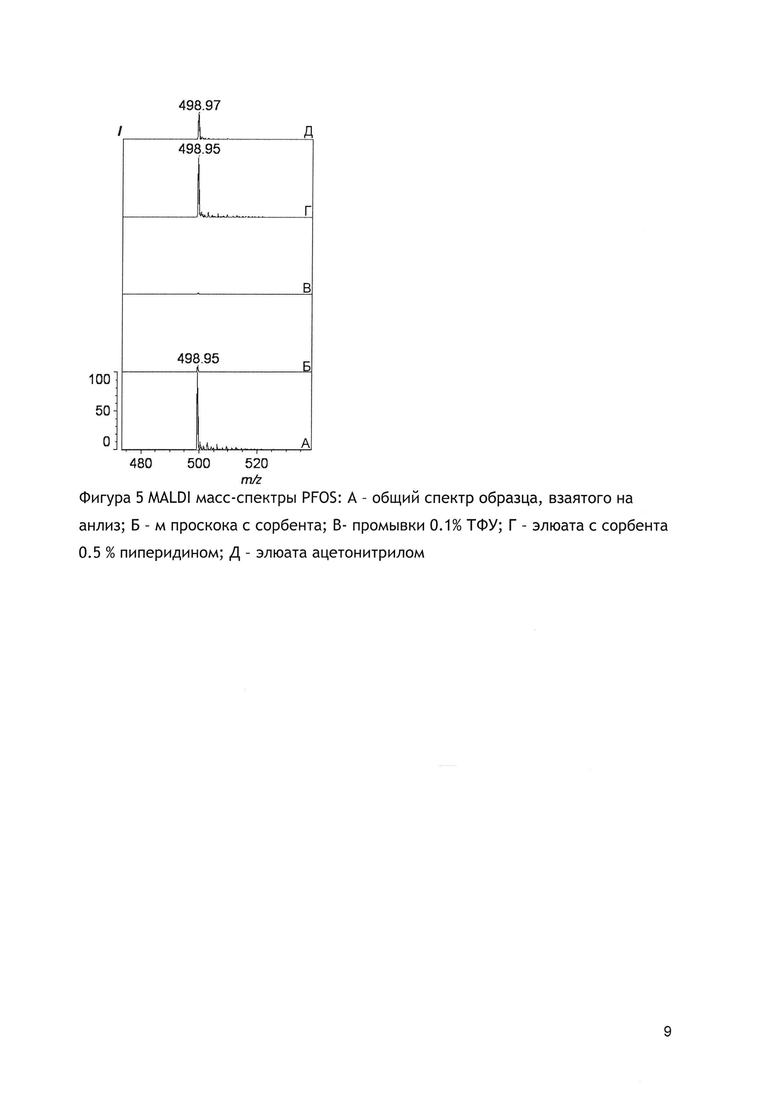
Раствор, содержащий стандарт PFOS (перфтороктановая сульфокислота), нанесли на сорбент - РММС Ga(lll), промыли и провели десорбцию раствором пиперидина и ацетонитрила по общей методике. Исходный раствор, проскок с сорбента, промывочный раствор и два элюата затем были проанализированы методом MALDI масс-спектрометрии. Несмотря на то, что MALDI масс-спектрометрия не является количественным методом, по интенсивности спектра и легкости его получения в одинаковых условиях можно сделать приблизительную оценку. Результаты представлены на фигуре 5.
Как показано на фигуре 5 в результате элюирования с сорбента 0.5% пиперидином наблюдается сигнал, соответствующий перфтороктановой сульфокислоте. Соответственно показано, что металл-аффинная хроматография на сорбенте РММС Ga(III) может быть успешно применена для экстракции фторсодержащих органических соединений из водной среды.
Применение регулярных мультимолекулярных структур на основе пленок Ленгмюра-Блоджетт, содержащих в себе ионы различных металлов, в качестве сорбента для металл-аффинной хроматографии стало возможным благодаря обнаруженной авторами способности таких структур селективно связывать органические соединения по принципу теории жестких и мягких кислот и оснований. Это позволило повысить селективность и степень концентрирования по методу металл-аффинной хроматографии различных типов органических веществ, содержащих активные атомы кислорода или фтора.
Использованная литература
1. Leonard D. Holmes, Martin R. Schiller. Immobilized Iron(III) Metal Affinity Chromatography for the Separation of Phosphorylated Macromolecules: Ligands and Applications. // Journal of Liquid Chromatography & Related Technologies. 1997. V.20(1) P.123-142.
2. Sigma Aldrich cat. number P9740.
3. Е.А. Рожкова, И.А. Краснов, Н.Г. Суходолов, Н.С.Иванов, А.И. Янклович, Е.П. Подольская, Н.В. Краснов. Исследование поверхностных свойств наноструктур (пленок Лэнгмюра-Блоджетт), содержащих ионы железа, и определение их состава с привлечением методов масс-спектрометрии // Научное приборостроение, 2008, Т.18, №4, с.54-60.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ изготовления проводящей наноячейки с квантовыми точками | 2021 |
|
RU2777199C1 |
| Устройство для нанесения наночастиц оксидов металлов на металлическую поверхность при нормальных условиях | 2019 |
|
RU2733530C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ТУННЕЛЬНОГО ПРИБОРА | 1996 |
|
RU2106041C1 |
| СИСТЕМА ПОЛУЧЕНИЯ ЧИСТОЙ И СВЕРХЧИСТОЙ ВОДЫ | 2016 |
|
RU2663172C2 |
| ОПТИЧЕСКИЕ СЕНСОРНЫЕ МАТЕРИАЛЫ НА КАТИОНЫ ТЯЖЕЛЫХ И ПЕРЕХОДНЫХ МЕТАЛЛОВ НА ОСНОВЕ ДИТИАКРАУНСОДЕРЖАЩИХ БУТАДИЕНИЛЬНЫХ КРАСИТЕЛЕЙ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2005 |
|
RU2292368C1 |
| КОМПОЗИЦИЯ, СПОСОБ И НАБОР ДЛЯ ПОЛУЧЕНИЯ ПЛАЗМИНА | 2009 |
|
RU2497948C2 |
| ТЕТРА-4-[4-(1-МЕТИЛ-1-ФЕНИЛЭТИЛ)ФЕНОКСИ]ТЕТРА-5-НИТРОФТАЛОЦИАНИНЫ КОБАЛЬТА И НИКЕЛЯ | 2016 |
|
RU2620270C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК PNDCTR1, КОДИРУЮЩАЯ ГИБРИДНЫЙ ПОЛИПЕПТИД GST-NDCTR1, ШТАММ БАКТЕРИЙ ESCHERICHIA COLI BL21(DE3)/PNDCTR1 - ПРОДУЦЕНТ ГИБРИДНОГО ПОЛИПЕПТИДА GST-NDCTR1 И ГИБРИДНЫЙ ПОЛИПЕПТИД GST-NDCTR1, ОБЛАДАЮЩИЙ СПОСОБНОСТЬЮ ХЕЛАТИРОВАТЬ ИОНЫ МЕДИ, СЕРЕБРА И ПЛАТИНЫ | 2015 |
|
RU2603092C1 |
| Способ подготовки поверхности кремния и стекла перед процессом анодного бондинга | 2024 |
|
RU2835590C1 |
| ПЕПТИД, ОБЛАДАЮЩИЙ НЕФРОПРОТЕКТОРНЫМ ДЕЙСТВИЕМ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ И СПОСОБ ЕЕ ПРИМЕНЕНИЯ | 2021 |
|
RU2778505C1 |


Изобретение относится к области сорбционных материалов. Предложено применение регулярных мультимолекулярных структур - пленок Ленгмюра-Блоджетт на основе стеаратов трехвалентных металлов, содержащих лабильную ковалентную связь, в качестве сорбентов для металл-аффинной хроматографии водорастворимых органических и биоорганических соединений. Изобретение обеспечивает повышение селективности сорбентов при хроматографии органических и биоорганических веществ, содержащих активные атомы кислорода или фтора. 5 ил.
Применение регулярных мультимолекулярных структур (пленок Ленгмюра-Блоджетт) на основе стеаратов трехвалентных металлов, содержащих лабильную ковалентную связь, в качестве сорбента для металл-аффинной хроматографии водорастворимых органических и биоорганических соединений, имеющих в составе атомы кислорода или фтора.
| Mitsuyo Mashida, Purification of phosphoproteins by immobilized metal affinity chromatography, FEBS Journal, 274, 2007, 1576-1578 | |||
| ГЛАДИЛОВИЧ В.Д | |||
| и др | |||
| Идентификация пептидов сывороточного альбумина, модифицированных фосфорорганическими соединениями, с применением методов хроматографии и масс-спектроскопии, Научное приборостроение, 2010, том 20, N4, стр | |||
| Способ приготовления сернистого красителя защитного цвета | 1921 |
|
SU84A1 |
| РОЖКОВА Е.А | |||
| и др | |||
| Исследование поверхностных свойсьв наноструктур (плёнок Лэнгмюра-Блоджетт), содержащих ионы железа, Научное приборостроение, 2008, том 18, N4, с.54-60 | |||
| СПОСОБ ПОЛУЧЕНИЯ ЧУВСТВИТЕЛЬНОГО СЛОЯ ПЬЕЗОКВАРЦЕВОГО СЕНСОРА ДЛЯ ОПРЕДЕЛЕНИЯ ПАРОВ ОРГАНИЧЕСКИХ РАСТВОРИТЕЛЕЙ | 2008 |
|
RU2371839C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НИТРОМЕТАНА В ВОЗДУХЕ | 2002 |
|
RU2236672C2 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| РУСАНОВА Т.Ю., Нано- и супрамолекулярные системы в оптических, пьезоэлектрических и тест-методах анализа, автореф | |||
| на соиск | |||
| уч.степ | |||
| доктора хим | |||
| наук, Саратов, 2009. | |||
Авторы
Даты
2017-01-19—Публикация
2012-04-18—Подача