Изобретение относится к области химии материалов и органической химии, а именно к новым полимерным мембранам, пленкам и монослоям на основе нового типа соединений - дитиакраунсодержащих бутадиенильных красителей общей формулы I:
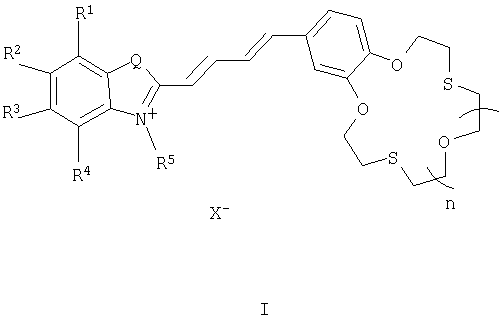
в которой R1-R4 - атом водорода, низший алкил, алкоксильная группа, арильная группа или два заместителя R1 и R2, R2 и R3, R3 и R4 вместе составляют С4Н4-бензогруппу;
R5 - алкильный радикал CmH2m+1, где m=1-18;
X=Cl, Br, I, ClO4, PF6, BF4, PhSO3, TsO, ClC6Н4SO3, СН3SO3, CF3SO3, СН3OSO3;
Q - атом серы, атом кислорода, атом селена, группа С(СН3)2, группа NH, группа NCH3; n=0-3.
Предлагаемые соединения и композитные материалы на их основе могут быть использованы в составе оптических хемосенсоров на катионы тяжелых и переходных металлов, например, в составе полимерных мембран, ультратонких пленок и молекулярных монослоев, для определения микроколичеств указанных ионов в промышленных водах и стоках, в том числе для мониторинга окружающей среды, в биологических жидкостях и др. Изобретение относится также к способам получения таких соединений и материалов.
Предлагаемые соединения и композитные материалы на их основе, их свойства и способ получения в литературе не описаны. Предлагаемые соединения представляют собой новый тип краунсодержащих непредельных красителей, так как гетероциклический остаток соединен с бензокраун-эфирным фрагментом через бутадиеновый мостик, что предопределяет их спектральные свойства. Краун-эфирный фрагмент в предлагаемых соединениях содержит атомы кислорода и серы в различных сочетаниях, что позволяет варьировать размер полости краун-эфира и повышает сродство к катионам тяжелых и переходных металлов. Композитные материалы получаются при введении предлагаемых соединений в полимерную матрицу методом полива. Структура полимерных пленочных материалов обеспечивает сочетание заданных свойств для получения нанокомпозитных материалов со свойствами оптических хемосенсоров.
Известны бутадиенильные красители (Hassner A., Birnbaum D., Loew L.M., J. Org. Chem., 1984, 49, 2546; Grinvald A., Hildesheim R., Farber I.C., Anglister L., Biophys. J., 1982, 39, 301; Frank J., Zouni A., van Hoek A., Visser A.J.W.G., Clarke R.J., Biochim. Biophys. Acta, 1996, 1280, 51; Zouni A., Clarke R.J., Visser A.J.W.G., Visser N.V., Holzwarth J.F., Biochim. Biophys. Acta, 1993, 1153, 203; Passechnik V.I., Sokolov V.S., Bioelectrochem., 2002, 55, 47; Lehmann F., Mohr G.J., Czerney P., Grummt U.-W., Dyes Pigm., 1995, 29, 85; Marder S.R., Perry J.W., Yakymyshyn C.P., Chem. Mater., 1994, 6, 1137; Matsui M., Kawamura S., Shibata K., Muramatsu H., Bull. Chem. Soc. Jpn., 1992, 65, 71; Sertova N., Nunzi J.-M., Petkov I., Deligeorgiev Т., J. Photochem. Photobiol. A: Chem., 1998, 112, 187; Alain V., Blanchard-Desce M., Ledoux-Rak I., Zyss J., Chem. Commun., 2000, 353; Brooker L.G.S., Sprague R.H., J. Am. Chem. Soc., 1941, 63, 3203; Hebert P., Baldacchino G., Gustavsson Т., Mialocq J.-C., J. Photochem. Photobiol. A: Chem., 1994, 84, 45; Quina F.H., Whitten D.G., J. Am. Chem. Soc., 1977, 99, 877; Wolfbeis O.S., Sensors & Actuators B, 1995, 29, 140), особенностью строения которых является наличие четвертичного гетероциклического остатка, связанного посредством двух сопряженных двойных углерод-углеродных связей с замещенным бензольным циклом. Эти красители интенсивно поглощают в видимой области спектра, но не способны к связыванию каких-либо катионов металлов.
В литературе описаны стириловые красители, в которых гетероциклический остаток соединен через одну двойную углерод-углеродную связь с фрагментом краун-эфира или тиакраун-эфира (Громов С.П., Алфимов M.В., Изв. АН. Сер. хим., 1997, 641; Громов С.П., Федорова О.А., Ведерников А.И., Ещеулова О.В., Федоров Ю.В., Алфимов M.В., Патент 2176256 РФ, Бюлл. изоб., 2001, №33; Громов С.П., Федорова О.А., Фомина M.В., Алфимов M.В., Патент 2012574 РФ, Бюлл. изоб., 1994, №9; Gromov S.P., Ushakov E.N., Fedorova O.A., Baskin I.I., Buevich A.V., Andryukhina E.N., Alfimov M.V., Johnels D., Ediund U.G., Whitesell J.K., Fox M.A., J. Org. Chem., 2003, 68, 6115). Для таких красителей характерна выраженная способность к комплексообразованию с катионами металлов, однако их поглощение и флуоресценция сдвинуты в коротковолновую область спектра, а интенсивность молярного поглощения и флуоресценции существенно снижены по сравнению с бутадиенильными красителями.
Известны также бутадиенильные красители, содержащие фрагменты краун-эфира или азакраун-эфира, которые обладают ярко выраженной способностью связывать катионы щелочных и щелочноземельных металлов в апротонной среде, что сопровождается существенным изменением спектральных свойств красителей (Громов С.П., Сергеев С.А., Дружинин С.И., Русалов М.В., Ужинов Б.М., Кузьмина Л.Г., Чураков А.В., Ховард Дж. А.К., Алфимов М.В., Изв. АН. Сер. хим., 1999, 530; Gromov S.P., Vedemikov A.I., Ushakov E.N., Kuz'mina L.G., Feofanov A.V., Avakyan V.G., Churakov A.V., Alaverdyan Yu. S., Malysheva E.V., Alfimov M.V., Howard J.A.K., Eliasson В., Ediund U.G., Helv. Chim. Acta, 2002, 85, 60; Ушаков E.Н., Громов С.П., Кузьмина Л.Г., Ведерников А.И., Авакян В.Г., Ховард Дж. А.К., Алфимов М.В., Изв. АН. Сер. хим., 2004, 1491). Красители данного строения не способны образовывать прочные комплексы с катионами тяжелых и переходных металлов, а также не проявляют лигандных свойств в водной среде, поэтому их использование в составе композитных материалов не приведет к созданию селективных оптических сенсоров на указанные металлы, способных работать в водных растворах.
Композитные материалы получают введением соединений, в том числе непредельных красителей, в полимерную матрицу одним из известных способов, в основном методом полива (Гуль В.E., Дьяконова В.П., Физико-химические основы производства полимерных пленок. - М.: Наука, 1978, 279 стр.; Polymer handbook, Ed. Bloch D.R., V. 2, John Wiley & Sons, 2003, 897 pp.; Composite materials handbook. Polymer matrix composites guidelines for characterization of structural materials. MIL-HDBK-17-1F, V.1, 2002, 734 pp.; Industrial Polymers Handbook, Ed. Wilks E.S., Ausgabe, 2000, Wiley-VCH, 657 pp.). Способ полива технологически прост и доступен как в лабораторной практике, так и в процессе производства и является оптимальным для целей, указанных в данном изобретении. Важным достоинством метода получения пленок из раствора является то, что отлив пленок производится при сравнительно низкой температуре, возможно введение нетермостойких добавок, например красителей, определяющих дальнейшее применение пленки. Однако краунсодержащие бутадиенильные красители ранее не вводились в полимерные пленки или композитные материалы указанным или иным способом.
Задачей настоящего изобретения является создание нового типа соединений - краунсодержащих бутадиенильных красителей, имеющих в своем составе алкильный заместитель у атома азота гетероциклического остатка и фрагмент дитиакраун-соединения с различной комбинацией атомов кислорода и серы, обладающих способностью к связыванию катионов тяжелых и переходных металлов, в том числе в водной среде, и использование их в составе новых оптических сенсорных композитных материалов. Задачей изобретения является также разработка способов получения целевых соединений с высоким выходом и получения сенсорных композитных материалов на их основе.
Решение поставленной задачи достигается структурой заявляемого нового типа бутадиенильных красителей общей формулы I и способом их получения, заключающимся в том, что четвертичную соль гетероциклического основания общей формулы II:
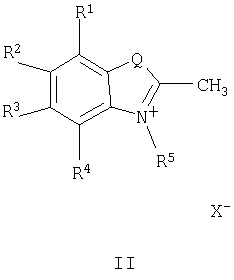
в которой R1-R5, Q и Х являются такими, как определено выше,
подвергают взаимодействию с дитиакраунсодержащим коричным альдегидом общей формулы III:

где n является таким, как определено выше, в среде органического растворителя.
Конденсация указанных четвертичных солей гетероциклических оснований II с дитиакраунсодержащими коричными альдегидами III до настоящего времени не была известна. Согласно предлагаемому способу синтез заявляемых бутадиенильных красителей общей формулы I осуществляют конденсацией активированной в четвертичных солях гетероциклических оснований II метильной группы с карбонильной группой дитиакраунсодержащих коричных альдегидов III с образованием двойной углерод-углеродной связи. Реакцию проводят в среде органического растворителя, например, спирта, при температурах 20-140°С.

Анион Х в I и II может быть одним и тем же, либо заменен в красителе I обработкой кислотой НХ или ее солями, где Х является таким, как определено выше.
Строение полученных соединений I доказано с помощью ЯМР 1H спектроскопии, электронной спектроскопии, и подтверждено данными элементного анализа (примеры 1-4).
Пример 1. Перхлорат 3-этил-2-[(1E,3E)-4-(2,3,5,6,8,9,11,12-октагидро-1,7,13,4,10-бензотриоксадитиациклопентадецен-15-ил)-1,3-бутадиенил]-1,3-бензотиазол-3-ия.
В колбе с обратным холодильником смешивают 82 мг (0.30 ммоль) перхлората 2-метил-3-этил-1,3-бензотиазол-3-ия, 115 мг (0.33 ммоль) (E)-3-(2,3,5,6,8,9,11,12-октагидро-1,7,13,4,10-бензотриоксадитиациклопентадецен-15-ил)пропен-2-аля и 10 мл абс. этанола. Реакционную смесь кипятят в течение 100 ч на масляной бане и охлаждают до 5°С. Осадок отфильтровывают, промывают холодным абс. этанолом (2×3 мл), бензолом (3 мл) и высушивают на воздухе. Получают 100 мг (55%) красителя в виде красно-коричневых кристаллов, т.пл. 201-203°С.
Спектр ЯМР 1Н (500 МГц, в ДМСО-d6, 30°С): 1.47 (т, 3Н, Me, J=7.2 Гц); 2.89 (т, 4Н, γ-CH2S, γ'-CH2S, J=6.6 Гц); 3.05 и 3.07 (2 т, 4H, β-CH2S, β'-CH2S, J=5.2 Гц, J=5.1 Гц); 3.71 и 3.72 (2 т, 4Н, δ-СН2О, δ'-CH2O, J=6.6 Гц, J=6.6 Гц); 4.27 и 4.28 (2 т, 4H, α-СН2О, α'-CH2O, J=5.1 Гц, J=5.2 Гц); 4.79 (к, 2H, CH2N, J=7.2 Гц); 7.08 (д, 1Н, Н(5'), J=8.4 Гц); 7.24 (дд, 1Н, Н(6'), J=8.4 Гц, J=1.7 Гц); 7.32 (д, 1Н, Н(2'), J=1.7 Гц); 7.37 (дд, 1Н, Н(с), 3Jтранс=15.3 Гц, J=10.3 Гц); 7.45 (д, 1Н, H(d), 3Jтранс=15.3 Гц); 7.49 (д, 1H, H(a), 3Jтранс=14.8 Гц); 7.77 (м, 1Н, Н(6)); 7.86 (м, 1Н, Н(5)); 8.04 (дд, 1Н, H(b), 3Jтранс=14.8 Гц, J=10.3 Гц); 8.27 (д, 1Н, Н(4), J=8.5 Гц); 8.40 (д, 1Н, Н(7), J=7.9 Гц).
УФ-спектр (С=1×10-5 моль·л-1, ацетонитрил), нм: 457 (ε=54000).
Найдено, %: С 52.68; Н 5.31; N 2.34.
C27H32ClNO7S3.
Вычислено, %: С 52.80; Н 5.25; N 2.28.
Пример 2. Перхлорат 2-[(1E,3E)-4-(2,3,5,6,8,9,11,12,14,15-декагидро-1,7,10,16,4,13-бензотетраоксадитиациклооктадецен-18-ил)-1,3-бутадиенил]-3-этил-1,3-бензотиазол-3-ия.
В колбе с обратным холодильником смешивают 50 мг (0.18 ммоль) перхлората 2-метил-3-этил-1,3-бензотиазол-3-ия, 79 мг (0.20 ммоль) (E)-3-(2,3,5,6,8,9,11,12,14,15-декагидро-1,7,10,16,4,13-бензотетраоксадитиациклооктадецен-18-ил)пропен-2-аля и 10 мл абс. этанола. Реакционную смесь кипятят в течение 100 ч на масляной бане и охлаждают до 5°С. Осадок отфильтровывают, промывают холодным абс. этанолом (2×3 мл), бензолом (3 мл) и высушивают на воздухе. Получают 68 мг (58%) красителя в виде красно-коричневых кристаллов, т.пл. 202-204°С.
Спектр ЯМР 1Н (500 МГц, в ДМСО-d6, 30°С): 1.47 (т, 3Н, Me, J=7.2 Гц); 2.90 и 2.92 (2 т, 4H, γ-CH2S, γ'-CH2S, J=6.3 Гц, J=6.6 Гц); 3.05 (т, 2Н, β'-CH2S, J=6.3 Гц); 3.10 (т, 2Н, β-CH2S, J=6.7 Гц); 3.54 (м, 4 Н, 2 ε-CH2O); 3.63 и 3.66 (2 т, 4H, δ-CH2O, δ'-CH2O, J=6.6 Гц, J=6.3 Гц); 4.21 (уш.т, 4Н, α-CH2O, α'-СН2O, J=6.5 Гц); 4.79 (к, 2Н, CH2N, J=7.2 Гц); 7,06 (д, 1Н, Н(5'), J=8.4 Гц); 7.21 (дд, 1Н, Н(6'), J=8.4 Гц, J=1.5 Гц); 7.30 (д, 1Н, Н(2'), J=1.5 Гц); 7.37 (дд, 1Н, Н(с), 3Jтранс=15.3 Гц, J=10.3 Гц); 7.45 (д, 1H, H(d), 3Jтранс=15.3 Гц); 7.51 (д, 1H, H(a), 3Jтранс=14.8 Гц); 7.76 (м, 1Н, Н(6)); 7.85 (м, 1Н, Н(5)); 8.04 (дд, 1Н, H(b), 3Jтранс=14.8 Гц, J=10.3 Гц); 8.26 (д, 1Н, Н(4), J=8.5 Гц); 8.39 (д, 1Н, Н(7), J=7.9 Гц).
УФ-спектр (С=1×10-5 моль·л-1, ацетонитрил), нм: 461 (ε=54000).
Найдено, %: С 52.99; Н 5.61; N 2.14.
С29Н36ClNO8S3.
Вычислено, %: С 52.91; Н 5.51; N 2.13.
Пример 3. Перхлорат 3-октадецил-2-[(1E,3E)-4-(2,3,5,6,8,9,11,12-октагидро-1,7,13,4,10-бензотриоксадитиациклопентадецен-15-ил)-1,3-бутадиенил]-1,3-бензотиазол-3-ия.
В колбе с обратным холодильником смешивают 56 мг (0.11 ммоль) перхлората 2-метил-3-октадецил-1,3-бензотиазол-3-ия, 47 мг (0.13 ммоль) (E)-3-(2,3,5,6,8,9,11,12-октагидро-1,7,13,4,10-бензотриоксадитиациклопентадецен-15-ил)пропен-2-аля и 7 мл абс. этанола. Реакционную смесь кипятят в течение 100 ч на масляной бане и охлаждают до 5°С. Осадок отфильтровывают, промывают холодным абс. этанолом (2×3 мл) и перекристаллизовывают из абс. этанола (15 мл). Получают 29 мг (31%) красителя в виде красно-коричневого порошка, т.пл. 141-143°С.
Спектр ЯМР 1Н (500 МГц, в CDCl3, 30°С): 0.89 (т, 3Н, Me, J=6.8 Гц); 1.19-1.37 (м, 28Н, 14 CH2); 1.49 (м, 2Н, CH2CH2CH2N); 1.87 (м, 2 Н, CH2CH2N); 2.98 и 3.02 (2 т, 4Н, γ- и γ'-CH2S, J=6.5 Гц, J=6.9 Гц); 3.11 (уш.т, 4 Н, β- и β'-CH2S); 3.84 и 3.86 (2 т, 4Н, δ- и δ'-CH2O, J=6.9 Гц, J=6.5 Гц); 4.12 (м, 2 Н, α-CH2О); 4.32 (м, 2 Н, α'-CH2O); 4.60 (м, 2 Н, CH2N); 6.52 (д, 1Н, Н(5'), J=8.3 Гц); 6.95 (уш.д, 1Н, Н(6'), J=8.3 Гц); 7.17 (уш.с, 1Н, Н(2')); 7.26 (д, 1Н, H(d), 3Jтранс=15.3 Гц); 7.48 (дд, 1H, H(c), 3Jтранс=15.3 Гц, J=11.1 Гц); 7.50 (д, 1Н, Н(а), 3Jтранс=14.4 Гц); 7.61 (д, 1Н, Н(4), J=8.4 Гц); 7.64 (м, 1Н, Н(6)); 7.72 (м, 1Н, Н(5)); 7.89 (дд, 1Н, H(b), 3Jтранс=14.4 Гц, J=11.1 Гц); 7.95 (д, 1H, H(7), J=8.0 Гц).
Найдено, %: С 62.13; Н 7.70; N 1.65.
С43Н64ClNO7S3.
Вычислено, %: С 61.58; Н 7.69; N 1.67.
Пример 4. Перхлорат 2-[(1E,3E)-4-(2,3,5,6,8,9,11,12,14,15-декагидро-1,7,10,16,4,13-бензотетраоксадитиациклооктадецен-18-ил)-1,3-бутадиенил]-3-октадецил-1,3-бензотиазол-3-ия.
В колбе с обратным холодильником смешивают 33 мг (0.07 ммоль) перхлората 2-метил-3-октадецил-1,3-бензотиазол-3-ия, 31 мг (0.08 ммоль) (E)-3-(2,3,5,6,8,9,11,12,14,15-декагидро-1,7,10,16,4,13-бензотетраоксадитиациклооктадецен-18-ил)пропен-2-аля и 6 мл абс. этанола. Реакционную смесь кипятят в течение 100 ч на масляной бане и охлаждают до 5°С. Осадок отфильтровывают, промывают холодным абс. этанолом (2×2 мл) и высушивают на воздухе. Получают 26 мг (45%) красителя в виде коричневато-черного порошка, т.пл. 179-181°С.
Спектр ЯМР 1Н (500 МГц, в CDCl3, 25°С): 0.88 (т, 3Н, Me, J=6.9 Гц); 1.19-1.37 (м, 28Н, 14 CH2N); 1.48 (м, 2Н, СН2CH2СН2N); 1.87 (м, 2Н, СН2СН2N); 2.91 (т, 2Н, γ-СН2S, J=5.8 Гц); 3.09 (м, 4Н, β'-CH2S, γ'-CH2S); 3.20 (т, 2Н, β-CH2S, J=7.2 Гц); 3.65 (с, 4Н, 2 ε-CH2O); 3.73 (т, 2Н, δ'-CH2O, J=7.1 Гц); 3.82 (т, 2Н, δ-СН2O, J=5.8 Гц); 4.02 (т, 2Н, α-CH2O, J=7.2 Гц); 4.30 (т, 2Н, α'-CH2O, J=5.7 Гц); 4.60 (м, 2Н, CH2N); 6.52 (д, 1Н, Н(5'), J=8.3 Гц); 6.95 (уш.д, 1Н, Н(6'), J=8.3 Гц); 7.14 (уш.с, 1Н, Н(2')); 7.23 (д, 1Н, H(d), 3Jтранс=15.3 Гц); 7.45 (дд, 1Н, Н(с), 3Jтранс=15.3 Гц, J=11.1 Гц); 7.47 (д, 1Н, Н(а), 3Jтранс=14.5 Гц); 7.60 (д, 1H, H(4), J=8.4 Гц); 7.63 (м, 1Н, Н(6)); 7.70 (м, 1Н, Н(5)); 7.89 (дд, 1Н, H(b), 3Jтранс=14.5 Гц, J=11.1 Гц); 7.95 (д, 1H, H(7), J=7.9 Гц).
Найдено, %: С 61.46; Н 7.84; N 1.58.
C45H68ClNO8S3.
Вычислено, %: С 61.23; Н 7.77; N 1.59.
Остальные соединения были получены способом аналогичным примеру 1.
Для получения соединений формулы I, в которой R1-R4 низший алкил использовались йодиды или перхлораты 2-метилполиалкилиндолениния; для получения соединений формулы I, в которой один из заместителей R1-R4 алкоксильная группа, использовались йодиды 2-метилалкоксибензотиазолия; для получения соединений формулы I, в которой один из заместителей R1-R4 арильная группа, использовались йодиды 2-метиларилбензотиазолия; для получения соединений формулы I, в которой два заместителя R1 и R2, R2 и R3, R3 и R4 вместе составляют С4Н4-бензогруппу использовались йодиды 2-метилнафтотиазолия. Для получения соединений формулы I, в которой Q=атом кислорода, атом селена, группа NH или группа NCH3 использовались йодиды или перхлораты 2-метилбензоксазолия, 2-метилбензоселенозолия, 2-метилбензимидазолия. Для перевода йодидов соединений формулы I в соли с другими противоионами использовалось добавление хлорной кислоты или соли натрия, содержащей в качестве противоионов Х=Cl, Br, I, ClO4, PF6, BF4, PhSO3, TsO, ClC6Н4SO3, СН3SO3, CF3SO3, СН3OSO3 к спиртовому раствору соединения I.
Полученные бутадиенильные красители были исследованы в качестве хромоионофорных соединений.
Соединения нового типа указанного строения I имеют глубокую и интенсивную окраску в области 460 нм, которая связана со способностью электронной пары атома кислорода фрагмента дитиакраун-соединения, находящегося в пара-положении к бутадиеновому фрагменту, участвовать в сопряжении с кватернизованным гетероциклическим остатком.
При исследовании свойств полученных соединений была обнаружена их выраженная способность к комплексообразованию с катионами тяжелых металлов за счет образования высокопрочных координационных связей с двумя атомами серы дитиакраун-эфирного фрагмента красителя. Например, было изучено комплексообразование красителя Iа, полученного в примере 1 (Q=S, R1=R2=R3=R4=Н, R5=С2Н5, Х=ClO4, n=1), и красителя Iб, полученного в примере 2 (Q=S, R1=R2=R3=R4=H, R5=C2H5, X=ClO4, n=2), (CIa,б=10-5 моль/л) с перхлоратами Hg(II), Ag(I), Pb(II), Cd(II), Zn(II), а также с перхлоратами щелочноземельных металлов в ацетонитриле, водно-ацетонитрильных смесях и воде. При образовании комплексов значительно изменяются спектральные характеристики красителей (Таблица 1). В результате координации катиона металла по фрагменту дитиакраун-соединения происходит переключение неподеленной электронной пары атома кислорода, находящегося в пора-положении к бутадиеновому фрагменту, от участия в эффективном сопряжении с хромофорным фрагментом красителя на образование координационной связи с катионом металла. При этом наблюдается гипсохромный сдвиг длинноволновой полосы поглощения красителя до 21 нм. В среде ацетонитрила сравнительно устойчивые комплексы образуются только с ионами тяжелых металлов (Hg2+, Ag+ и Pb2+). Присутствие перхлоратов Zn(II), Cd(II), Pb(II) или щелочноземельных металлов с СM=10-3 моль/л практически не влияет на спектральные характеристики красителей Iа и Iб, что подтверждает отсутствие комплексообразования с катионами этих металлов. Присутствие перхлоратов Hg(II) или Ag(I) вызывает существенные спектральные изменения также для растворов красителей Iа и Iб, в воде и водно-ацетонитрильных смесях, что свидетельствует об эффективном комплексообразовании с ионами Hg2+ и Ag+ в этих условиях.
Спектральные характеристики красителей Iа, Iб и их комплексов с ионами Ag+, Hg2+ и Pb2+ в ацетонитриле, водно-ацетонитрильном (1:1) растворе и воде.
Измеренные с помощью методов УФ- и ЯМР 1Н-титрования константы устойчивости комплексов красителей Iа, Iб с катионами тяжелых металлов указывают на их высокую прочность. Например, в водно-ацетонитрильных растворах величины констант устойчивости комплексов с Ag+ варьировались в пределах lgK=4.8-6.5, заметно увеличиваясь с ростом содержания воды в растворе. В то же время значения констант устойчивости комплексов с Pb2+ снижаются более чем на четыре порядка при увеличении содержания воды (Таблица 2). Таким образом, изменение среды приводит к изменению селективности красителей Iа,б - в водно-ацетонитрильном (1:1) растворе красители проявляет высокую селективность к Ag+ относительно Pb2+, а в безводном ацетонитриле, наоборот, предпочтительно связывают ионы Pb2+. Величины констант устойчивости комплексов с ионами Hg2+ имеют значение lgK≥11 при любом содержании воды в смеси. Таким образом, высокая селективность дитиакраунсодержащих бутадиенильных красителей к Hg2+ относительно Ag+ (а также любого другого из исследованных катионов металлов) остается высокой при любых соотношениях вода/ацетонитрил.
Константы устойчивости комплексов красителей Iа, Iб в водно-ацетонитрильных растворах с разным содержанием воды, определенные спектрофотометрическим титрованием, 22°С.
воды/объемные %
10
50
75
4.94
5.68
6.46
5.51
6.33
-
2.1
<2
-
Измеренные с помощью метода ЯМР 1Н-титрования константы устойчивости комплексов красителей Iа, Iб с перхлоратами Ag(I), Pb(II) и Hg(II) указывают на их высокую прочность в среде ацетонитрила (Таблица 3). Например, в растворе с концентрацией красителей 10-3 моль/л комплексы с ионами Hg2+ характеризуются очень высокой устойчивостью (lgK=18.3-19.0), более чем на 10 порядков превышающей устойчивость комплексов этих красителей с другими исследованными катионами тяжелых металлов. Найденные значения констант демонстрируют также высокую селективность красителей Iа, Iб к ионам Ag+ и Pb2+ относительно Cd2+.
Константы устойчивости комплексов красителей Iа, Iб с перхлоратами тяжелых металлов, определенные ЯМР 1Н-титрованием в ацетонитриле-d3, 30°С.
Заявленные дитиакраунсодержащие бутадиенильные красители были введены в полимерные пленочные материалы и исследованы их хемосенсорные свойства. Например, красители Ia, Iб вводят в состав полимерных матриц, получаемых методом полива по следующей методике. Растворы полимеров в хлороформе, дихлорэтане или ацетонитриле с концентрацией 2-8 массовых % поливают на кварцевые или предметные стекла. В раствор полимерного носителя предварительно вводят 1 массовый % красителя Iа, Iб в расчете на массу полимера. Краситель вводят в виде раствора в хлороформе, дихлорэтане или ацетонитриле (CIa,б=10 ммоль/л). Испарение растворителя приводит к образованию пленки, которую высушивают при комнатной температуре в течение 24 ч. В качестве полимеров используют поливинилбутираль Mowital B30H (Германия, содержание альдегидных звеньев около 40%) и сополимер метилметакрилата и этилакрилата (Mn=39500, Mw=101000 (ГПХ), Sigma-Aldrich Chemie GmbH). Полученные полимерные матрицы представляют собой окрашенные прозрачные пленки толщиной 10-40 мкм.
Полученные полимерные матрицы, содержащие красители Iа, Iб, были исследованы в качестве ион-селективных оптических материалов на присутствие в воде катионов тяжелых металлов. Для этого пленки в течение 1.5 ч выдерживали в водных растворах перхлоратов серебра или ртути(II) (СM=1 ммоль/л) и затем измеряли спектры поглощения композитов (Таблица 4). Наблюдаемые спектральные изменения - гипсохромные сдвиги длинноволновой полосы поглощения до 15 нм - подтверждают образование красителями Iа, Iб комплексов с ионами Ag+ и Hg2+ в полимерной матрице, что может быть использовано для оптического определения указанных ионов тяжелых металлов в водной среде.
Спектральные характеристики красителей Iа, Iб и их комплексов с ионами Ag+ и Hg2+ в полимерной матрице на основе поливинилбутираля (ПВБ) и сополимера метилметакрилата с этилакрилатом (СПММАЭА). Толщина пленок 10 мкм, СIа,б=1 массовый % в расчете на полимер.
Были исследованы спектральные и ион-селективные свойства монослоев амфифильного бутадиенильного красителя Iв, полученного в примере 3 (Q=S, R1=R2=R3=R4=Н, R5=н-C18H37, Х=ClO4, n=1) и красителя I г, полученного в примере 4 (Q=S, R1=R2=R3=R4=Н, R5=н-С18Н37, Х=ClO4, n=2). Монослои получают на установках "Film Balance" (Lauda, Германия и NIMA-NFT, Англия-Германия) следующим способом: на тщательно очищенную поверхность бидистиллированной воды (или растворов солей щелочноземельных или тяжелых металлов) между подвижным и измерительным барьерами микрошприцем наносят 10 мкл раствора Iв, Iг в хлороформе (СIв,г=1 ммоль/л). Монослой выдерживают около 5 мин до полного испарения растворителя, а затем сжимают с постоянной скоростью 1 см/мин подвижным барьером. Полученные монослои переносят методом Ленгмюра-Шеффера или Ленгмюра-Блоджетт с поверхности раздела вода/воздух на различные твердые подложки (кварц, графит, слюда) при постоянном поверхностном давлении (10-30 мН/м). Указанные монослои проявляют сильный оптический отклик на присутствие в водной фазе катионов Ag(I) и Hg(II) в результате сильного и специфического комплексообразования по краун-эфирному фрагменту красителя. Например, при регистрации спектров отражения монослоя 1 г на поверхности воды наблюдается интенсивная полоса поглощения в области 442 нм. Среди исследованных солей металлов только в случае присутствия в водной субфазе ионов Ag+ или Hg2+ (СM=1 ммоль/л) наблюдается узкая интенсивная полоса отражения монослоя 1 г с максимумом при 470-474 нм. Только в присутствии в водной субфазе ионов Hg2+ максимум отражения сдвигается при сжатии монослоя (например, при π=30 мН/м, максимум при 442 нм) и наблюдается небольшое плечо при 420 нм.
Остальные соединения обладают аналогичными соединениям, полученным в примерах 1-4, свойствами в растворах, пленках и монослоях.
Таким образом, получен новый тип бутадиенильных красителей, имеющих дитиакраун-эфирный фрагмент и содержащих алкильный N-заместитель в гетероциклическом остатке, и обнаружена их ярко выраженная способность к селективному связыванию катионов тяжелых металлов как в апротонной, так и в водной среде, в том числе в составе полимерных матриц и в монослоях, характеризующаяся существенными спектральными изменениями. Обнаруженные ионофорные эффекты позволяют использовать заявленные соединения в оптических сенсорных материалах, например, для определения ионов тяжелых металлов в промышленных водах, биологических жидкостях, для мониторинга окружающей среды. Разработан также способ получения заявленных соединений высокой степени чистоты и с хорошими выходами (до 58%) из доступных веществ.
| название | год | авторы | номер документа |
|---|---|---|---|
| N-АЛКИЛАЗАКРАУНСОДЕРЖАЩИЕ СТИРИЛОВЫЕ КРАСИТЕЛИ В КАЧЕСТВЕ ОПТИЧЕСКИХ МОЛЕКУЛЯРНЫХ СЕНСОРОВ ДЛЯ ОПРЕДЕЛЕНИЯ КАТИОНОВ ЩЕЛОЧНЫХ И ЩЕЛОЧНОЗЕМЕЛЬНЫХ МЕТАЛЛОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2008 |
|
RU2398800C2 |
| ТИАКРАУНСОДЕРЖАЩИЕ СТИРИЛОВЫЕ КРАСИТЕЛИ В КАЧЕСТВЕ СЕЛЕКТИВНЫХ СЕНСОРОВ НА КАТИОНЫ ТЯЖЕЛЫХ ИЛИ ПЕРЕХОДНЫХ МЕТАЛЛОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2000 |
|
RU2176256C1 |
| ХЕМОСЕНСОРНЫЕ ОПТОМАТЕРИАЛЫ ДЛЯ ОПРЕДЕЛЕНИЯ КАТИОНОВ МЕТАЛЛОВ БОЛЬШОГО ИОННОГО РАДИУСА И ИОНОВ ДИАММОНИЯ НА ОСНОВЕ КРАУНСОДЕРЖАЩИХ БИССТИРИЛОВЫХ КРАСИТЕЛЕЙ, ИММОБИЛИЗОВАННЫХ В ПОЛИМЕРНЫЕ ПЛЕНКИ, И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2008 |
|
RU2389745C2 |
| КРАУНСОДЕРЖАЩИЕ СТИРИЛОВЫЕ КРАСИТЕЛИ С АММОНИЙНОЙ ГРУППОЙ В N-ЗАМЕСТИТЕЛЕ ГЕТЕРОЦИКЛИЧЕСКОГО ОСТАТКА В КАЧЕСТВЕ ФОТО- И ТЕРМОЧУВСТВИТЕЛЬНЫХ СОЕДИНЕНИЙ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2005 |
|
RU2278134C1 |
| 4-ЗАМЕЩЕННЫЕ N-АРИЛ-1,8-НАФТАЛИМИДЫ, ПРОЯВЛЯЮЩИЕ СВОЙСТВА ФЛУОРЕСЦЕНТНЫХ СЕНСОРОВ НА КАТИОНЫ МЕТАЛЛОВ, И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2515195C1 |
| СТИРИЛОВЫЕ КРАСИТЕЛИ С АММОНИЙНОЙ ГРУППОЙ В N-ЗАМЕСТИТЕЛЕ ГЕТЕРОЦИКЛИЧЕСКОГО ОСТАТКА В КАЧЕСТВЕ ФОТОЧУВСТВИТЕЛЬНЫХ СОЕДИНЕНИЙ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2008 |
|
RU2383571C1 |
| АЗАКРАУНСОДЕРЖАЩИЕ N-АРИЛ-1,8-НАФТАЛИМИДЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2017 |
|
RU2656106C1 |
| 5'-АЦИЛЬНЫЕ ПРОИЗВОДНЫЕ N-АЛКИЛБЕНЗОМОНОАЗАКРАУН-СОЕДИНЕНИЙ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1999 |
|
RU2161153C1 |
| 4-(2-НАФТИЛ)ПИРИДИНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2001 |
|
RU2214401C2 |
| СИММЕТРИЧНЫЕ ЦИАНИНОВЫЕ КРАСИТЕЛИ С ТЕРМИНАЛЬНЫМИ АЗОТСОДЕРЖАЩИМИ ГРУППАМИ В N-ЗАМЕСТИТЕЛЯХ ГЕТЕРОЦИКЛИЧЕСКИХ ОСТАТКОВ В КАЧЕСТВЕ ЛЮМИНОФОРОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2011 |
|
RU2472822C1 |
Изобретение относится к области органической химии, а именно к новым полимерным материалам - мембранам, пленкам и монослоям на основе нового типа соединений - дитиакраунсодержащих бутадиенильных красителей общей формулы I:

в которой R1-R4 - атом водорода, низший алкил, алкоксильная группа, арильная группа или два заместителя R1 и R2, R2 и R3, R3 и R4 вместе составляют С4Н4-бензогруппу; R5 - алкильный радикал CmH2m+1, где m=1-18; Х=Cl, Br, I, CiO4, PF6, BF4, PhSO3, TsO, ClC6H4SO3, СН3SO3, CF3SO3, СН3OSO3; Q - атом серы, атом кислорода, атом селена, группа С(СН3)2, группа NH, группа NCH3; n=0-3. Описываются также способ получения таких соединений и композитные материалы на их основе, обладающие ион-селективными оптическими свойствами. Предлагаемые красители и композитные материалы на их основе обладают высокой селективностью к ионам тяжелых и переходных металлов и могут быть использованы в составе оптических хемосенсоров, например, в составе полимерных мембран, ультратонких пленок и молекулярных монослоев, для определения микроколичеств указанных ионов в промышленных водах и стоках, в том числе для мониторинга окружающей среды, в биологических жидкостях и др. 3 н.п. ф-лы, 4 табл.

в которой R1-R4 - атом водорода, низший алкил, алкоксильная группа, арильная группа или два заместителя R1 и R2, R2 и R3, R3 и R4 вместе составляют С4Н4-бензогруппу;
R5 - алкильный радикал CmH2m+1, где m=1-18;
Х=Cl, Br, I, ClO4, PF6, BF4, PhSO3, TsO, ClC6H4SO3, СН3SO3, CF3SO3, СН3OSO3;
Q - атом серы, атом кислорода, атом селена, группа С(СН3)2, группа NH, группа NCH3; n=0-3.
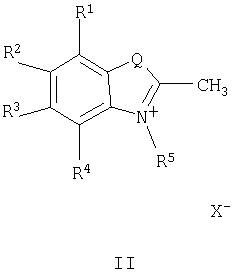
в которой R1-R5, Q и Х являются такими, как определено в п.1,
подвергают взаимодействию с дитиакраунсодержащим коричным альдегидом общей формулы III:

где n является таким, как определено в п.1,
в среде органического растворителя.
| ТИАКРАУНСОДЕРЖАЩИЕ СТИРИЛОВЫЕ КРАСИТЕЛИ В КАЧЕСТВЕ СЕЛЕКТИВНЫХ СЕНСОРОВ НА КАТИОНЫ ТЯЖЕЛЫХ ИЛИ ПЕРЕХОДНЫХ МЕТАЛЛОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2000 |
|
RU2176256C1 |
| 18(15)-КРАУН-6(5)-СОДЕРЖАЩИЕ СТИРИЛОВЫЕ КРАСИТЕЛИ В КАЧЕСТВЕ СЕЛЕКТИВНЫХ РЕАГЕНТОВ НА КАТИОНЫ АММОНИЯ, ЩЕЛОЧНЫХ ИЛИ ЩЕЛОЧНОЗЕМЕЛЬНЫХ МЕТАЛЛОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1991 |
|
RU2012574C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ИОНОВ МЕТАЛЛОВ В РАСТВОРАХ | 1992 |
|
RU2049986C1 |
Авторы
Даты
2007-01-27—Публикация
2005-12-27—Подача