Предлагаемое изобретение относится к области терапии, кардиологии и может быть использовано для контроля над состоянием пациентов с ишемической болезнью сердца после перенесенного острого коронарного синдрома.
Острый коронарный синдром (ОКС) является одной из ведущих причин госпитализаций в мире в связи с ишемической болезнью сердца (ИБС) и приносит значительный социально-экономический ущерб, включающий затраты ресурсов системы здравоохранения на экстренные госпитализации, операции реваскуляризации и непрямые потери в экономике в связи с длительной утратой трудоспособности и инвалидностью (А.В. Концевая, Р.Г. Оганов, 2011).
В течение последних лет эффективность вторичной профилактики сердечно-сосудистых заболеваний возросла (Оганов Р.Г., 2009), однако наблюдение за пациентами с ИБС и многососудистым поражением, а именно двух и более венечных сосудов, показывает, что в течение 5 лет у 51% из них развивается повторный инфаркт миокарда или коронарная смерть (Лутай М.И., 2004). Это обуславливает необходимость совершенствования имеющихся методов терапии и поиска новых подходов к лечению ИБС.
Эндотелиальная дисфункция приводит не только к развитию атеросклеротического поражения артерий, но и является пусковым моментом для активации как тромбоцитарного, так и коагуляционного механизмов свертывания и, как следствие, развитие тромбоза, являющегося основным патогенетическим механизмом развития ОКС (Ватутин Н.Т., 2006; Жданов B.C., 2006; Никитин Ю.П., 2006; Барабаш О.Л., 2007; Омельяненко М.Г., 2008; Niccoli G., Lanza G., Spaziani С. et al., 2007).
Под приверженностью к лечению, согласно определению ВОЗ, понимают «степень соответствия поведения пациента в отношении применения лекарств, выполнения рекомендаций по питанию или изменению образа жизни, следования назначениям и указаниям врача» (WHO, 2003).
Низкая приверженность к лечению связана с возникновением осложнений: нарушение режима терапии при инфаркте миокарда и гиперхолестеринемии приводит к повышению смертности у пациентов с сердечно-сосудистыми заболеваниями (Coronary Drug Project Group, 1980). Прекращение применения клопдогрела и статинов после коронарного события приводит к увеличению риска фатального повторного инфаркта и смертельного исхода (Но P.M., 2010). Нарушение приема β-адреноблокаторов приводит к увеличению смертности и сердечно-сосудистых катастроф (Mairesse S., 2012).
Поэтому представляет интерес прогнозирование эффективности терапии у пациентов с ИБС после перенесенного ОКС в ходе медикаментозного лечения в течение 12 месяцев на основании изучения факторов ангиогенеза и приверженности к терапии.
Известен способ оценки эффективности лечения ИБС путем оценки перекисного окисления липидов (ПОЛ) тромбоцитов (Л.В. Шаталина и др. "Состояние мембран и особенности ПОЛ тромбоцитов у больных с нестабильной стенокардией". Кардиология. -1989. - N 2. - с. 45-49), а также путем оценки уровня холестерола (ХС) липопротеинов (ЛП) разных классов у больных ИБС под влиянием физических тренировок (В.А. Дудаев и др. "Изменение содержания ХС ЛП разных классов у больных ИБС под влиянием физических тренировок". - Кардиология. - 1989. - N 2. - с. 49-53). Однако указанные способы не позволяют достаточно точно оценить эффективность лечения ИБС.
Из патентной литературы известен также способ оценки эффективности лечения ИБС. Сущность способа: проводят электрофорез в геле агарозы путем исследования сыворотки крови до и после лечения. Затем определяют уровень липопротеина ЛП (а) с помощью дополнительной обработки 0,3 мл 0,1% раствора Тритона Х-100 и инкубации 15 мин при 20°С, перемешивают смесь методом встряхивания 120 раз в 1 мин, последующей инкубацией сыворотки крови больного с раствором Судана Б в течение 1 ч в темном термостате при 40°С. Далее вносят пробы в лунку в геле агарозы с площадью основания 4×20 мм для электрофореза ЛП с последующей фиксацией электрофореграмм, их высушиванием, денситометрией. При снижении уровня ЛП (а) на 35% и более по сравнению с исходным уровнем и увеличении уровня ЛПВП с 13% до 28% и более оценивают лечение ишемической болезни сердца как эффективное. Использование способа обеспечивает повышение чувствительности и точности оценки эффективности лечения ишемической болезни сердца, однако оно отражает только эффективность терапии дислипидемии. (См. п. RU №2439575, кл. G01N 33/68, опубл. 10.01.2012).
Известен способ оценки эффективности лечения ишемической болезни сердца, в котором определяют концентрацию 2-ТБК активных соединений, лаг-период, ХС ЛПВП в сыворотке крови до и после лечения. При увеличении лаг-периода, ХС ЛПВП и снижении концентрации 2-ТБК соединений не менее чем на 20% от исходного уровня терапию ишемической болезни сердца считают эффективной. (См. п. RU №2122732, кл. G01N 33/49, опубл. 27.11.1998).
В доступной научно-медицинской и патентной литературе нами не выявлены работы, касающиеся прогнозирования эффективности терапии у пациентов с ИБС после перенесенного ОКС в ходе медикаментозного лечения в течение 12 месяцев и изучения количественной зависимости особенностей факторов ангиогенеза и приверженности к терапии.
Задача изобретения: спрогнозировать эффективность медикаментозной терапии у пациентов с ишемической болезнью сердца через 12 месяцев после перенесенного острого коронарного синдрома.
Технический результат, получаемый в результате использования заявляемого изобретения, состоит в повышении точности и информативности способа.
Поставленная задача решается тем, что в качестве критериев эффективности назначаемой медикаментозной терапии и маркеров прогноза заболеваемости определяют факторы ангиогенеза. При этом через 12 месяцев после ОКС у пациентов, приверженных к медикаментозной терапии, в крови исследуют уровень фактора роста сосудистого эндотелия (VEGF-A) и эндостатина. Если уровень фактора роста эндотелия составляет более 155,13 пг/мл, а уровень эндостатина превышает значение 266,39 нг/мл, прогнозируют низкую эффективность медикаментозной терапии.
Предпосылками для выбора существенных признаков изобретения и выявления причинно-следственной связи между ними и получаемым техническим результатом явились наши многочисленные научно-клинические исследования.
Универсальным механизмом, через который реализуется действие всех факторов риска развития ИБС, признана эндотелиальная дисфункция (ЭД) (Davignon J. et al., 2004; Joner M. et al., 2005; Brunner H, et al., 2005). Ряд проведенных исследований продемонстрировал, что эндотелиальная дисфункция у пациентов с ИБС связана с ухудшением прогноза и увеличением риска развития сердечно-сосудистых катастроф. Suwaidi А. и соавт. в 2000 году впервые установили, что у пациентов с ИБС и неокклюзирующим поражением коронарных артерий по данным коронарографии и выраженной дисфункцией эндотелия выше риск развития сердечно-сосудистых событий.
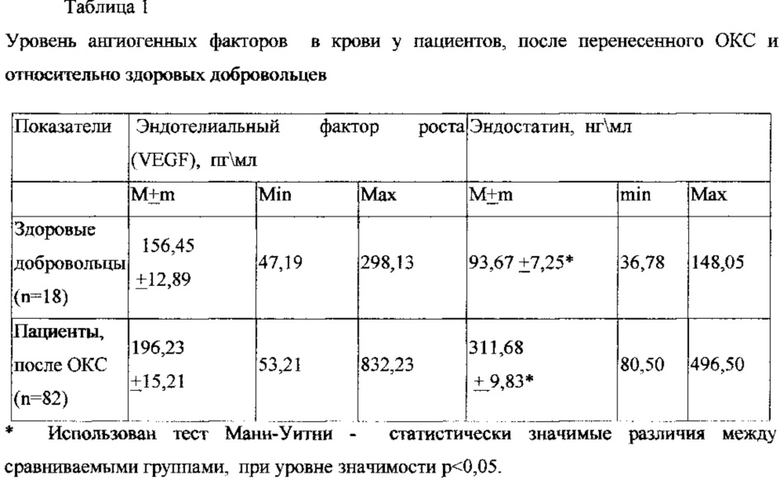
Одним из критериев эффективности назначаемой терапии является оценка ангиогенеза, который может служить маркером прогноза заболевания у пациентов с ОКС. В ходе нашего исследования произведено сравнение уровней эндотелиального фактора роста, а также эндостатина у 81 пациента, через 12 месяцев после индексного события, и у 18-ти относительно здоровых добровольцев, уровень VEGF был сопоставим среди относительно здоровых добровольцев по сравнению с пациентами, перенесшими ОКС (таблица 1).
При проведении корреляционного анализа у пациентов, перенесших ОКС, между клинико-лабораторными показателями и эндотелиальным фактором роста, а также эндостатином получена связь слабой силы, близкая к связи средней силы, статистически значимая ангиогенных факторов с величиной ПАД, для VEGF - положительная связь (r=0,29, р<0,05), для эндотстатина - отрицательная связь (r=-0,31, р<0,05). С показателями липидограммы ОХС с двумя факторами VEGF (r=-0,17, р<0,05); для эндостатина (r=0,21, р<0,05), эндостатин также коррелировал с ХС ЛПВП (r=-0,51, р<0,05) и прямая связь с ХС ЛПНП (r=0,39, р<0,05).
С учетом целей и задач исследования пациенты, которым проводилось изучение эндотелиального фактора роста и эндостатина, были разделены на две группы: первая группа - 43 человека (61,17±2,31 года), пациенты, приверженные к медикаментозной терапии, вторая группа - 38 человек (60,39±2,71 года), больные с низкой приверженностью к медикаментозной терапии.
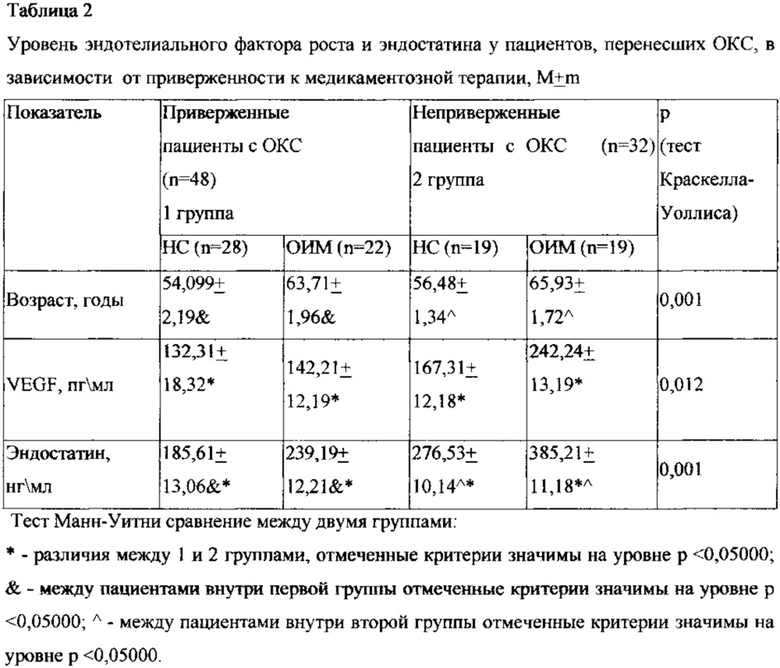
Изучение факторов ангиогенеза у пациентов, приверженных к медикаментозной терапии, показало, что VEGF был сопоставим между пациентами, перенесшими ОИМ и НС и был статистически значимо ниже по сравнению с пациентами, имеющими низкую приверженность к медикаментозной терапии (таблица 2). Во второй группе пациентов показатели эндотелиального фактора роста также не зависели от вида ОКС.
Таким образом, мы выявили, что уровень VEGF в большей степени зависит от приверженности к медикаментозной терапии, чем от вида перенесенного ОКС. А на уровень эндостатина влияют как вид ОКС, так и приверженность к лечению. Самые высокие значения как ингибитора, так и индуктора ангиогенеза регистрируются у пациентов с ОИМ в анамнезе, с низким комплайнсом к лечению, причем превалирование наблюдается за счет ингибирующего компонента ангиогенеза.
Подробное описание способа и примеры его клинического применения
У пациентов с ишемической болезнью сердца, перенесших острый коронарный синдром, через 12 месяцев медикаментозной терапии определяли уровень факторов ангиогенеза.
Для определения уровня фактор роста сосудистого эндотелия (VEGF-A) и эндостатина проводили забор крови из локтевой вены натощак в пробирки - вакутейнеры типа Monovette. При комнатной температуре образцы крови инкубировали 5-10 минут, затем центрифугировали в течение 20 минут при температуре +4°С и 1500G. Полученную сыворотку замораживали и хранили при -20°С до дня постановки реакции без размораживания.
Исследование проводили с помощью набора реактивов Quantikine производства «R&D Systems», Великобритания, методом количественного иммуноферментного сэндвич-анализа.
Произведен количественный анализ цветовой реакции с определением оптической плотности при помощи лабораторного анализатора для ИФА для VEGF-A с длиной волны 450 нм, для эндостатина с длиной волны 450 нм с коррекцией при 570 нм.
При помощи программного обеспечения Maple полученные количественные значения оптической плотности для каждого исследуемого образца пересчитаны в соответствующие величины концентрации VEGF-A и эндостатина согласно инструкции производителя реактивов.
Определяемая концентрация для VEGF-А от 0 до 1500 пг/мл, чувствительность от 5 пг/мл, для эндостатина концентрация от 0 до 10 нг/мл и чувствительность от 0,063 нг/мл.
Под приверженностью к лечению, согласно определению ВОЗ, понимали «степень соответствия поведения пациента в отношении применения лекарства, выполнения рекомендаций по питанию или изменению образа жизни назначениям и указаниям врача» (WHO, 2003).
На визит пациента просили принести пустые блистеры и упаковки препаратов, которые он принимал за период времени, прошедший после последнего визита. Подсчитывали долю оставшихся таблеток и рассчитывали процент приверженности по формуле (Osterberg L., Blaschke Т. 2005, Brown М.Т., Bussell J.K., 2011):

Приверженность к лечению считалась неудовлетворительной в том случае, когда пациент принимал ≤80% или ≥120% таблеток медикаментов, назначенных на длительный период времени.
Сравнивая количественные значения уровней эндостатина у пациентов через 12 месяцев после перенесенного ОКС с относительно здоровыми добровольцами мы выявили, что уровень эндостатина статистически значимо выше у пациентов с сердечно-сосудистой патологией, чем у здоровых. Причем разница в колебаниях уровня эндостатина у здоровых в 3 раза меньше, чем у пациентов после ОКС.
Больные с низкой приверженностью к медикаментозной терапии имели статистически значимо более высокие показатели общего холестерина, холестерина липопротеидов низкой и высокой плотности. Полученные различия в значениях липидограммы легко объясняются применением статинов, как основного класса препаратов после индексного ОКС у приверженных пациентов. Однако необходимо отметить, что целевых значений общего холестерина и холестерина липопротеидов низкой плотности для вторичной профилактики достигнуто не было.
Изучение факторов ангиогенеза у пациентов, приверженных к медикаментозной терапии, показало, что эндотелиальный фактор роста был сопоставим между пациентами, перенесшими ОИМ и нестабильную стенокардию, и был статистически значимо ниже по сравнению с пациентами, имеющими низкую приверженность к медикаментозной терапии. Во второй группе пациентов показатели эндотелиального фактора роста также не зависели от вида острого коронарного синдрома.
Анализ уровня эндостатина показал, что пациенты, перенесшие острый инфаркт миокарда, имеют статистически значимо более высокие значения данного фактора, по сравнению с пациентами, имеющими в анамнезе нестабильную стенокардию. Однако при сравнении значений уровня эндостатина среди пациентов с инфарктом миокарда видно, что значения данного показателя выше среди пациентов с низкой приверженностью к медикаментозной терапии, такая же ситуация наблюдается и для пациентов, имеющих в анамнезе нестабильную стенокардию.
Установлено, что уровень эндотелиального фактора роста в большей степени зависит от приверженности к медикаментозной терапии, чем от вида перенесенного острого коронарного синдрома. На уровень эндостатина влияют как вид острого коронарного синдрома, так и приверженность к лечению. Самые высокие значения, как ингибитора, так и индуктора ангиогенеза, регистрируются у пациентов с острым инфарктом миокарда в анамнезе, с низким комплайнсом к лечению, причем превалирование наблюдается за счет ингибирующего компонента ангиогенеза. То есть у данной когорты пациентов физиологический ангиогенез не возможен, сам патологический процесс в коронарном русле и факторы риска, такие как высокое артериальное давление и прогрессирование атеросклероза, ингибируют возможность создания новых сосудов. Длительность заболевания, пол пациентов не влияют на изученные факторы ангиогенеза.
Таким образом, пациенты с ОКС имеют повышенный уровень как ингибирующих, так и стимулирующих ангиогенез факторов, при этом пациенты, перенесшие ОИМ, имеют статистически значимо более высокие уровни изучаемых факторов, чем больные с нестабильной стенокардией. На уровень факторов ангиогенеза влияет степень приверженности пациентов к медикаментозной терапии. У пациентов с низкой приверженностью уровень факторов ангиогенеза выше, чем у пациентов с высокой приверженностью к медикаментозной терапии, главным образом за счет ингибирующего компонента. Факторы ангиогенеза у пациентов после перенесенного ОКС имеют разнонаправленную взаимосвязь с пульсовым АД и показателями липидного спектра крови, а также с приверженностью к медикаментозной терапии.
Клинический пример
Пациент Г-ко В.Н., 53 лет, диагноз: ИБС. Стенокардия напряжения ФК II. Постинфарктный кардиосклероз (2013).
Проходил медикаментозное лечение в течение 12 месяцев. Больному дополнительно назначено исследование крови. Уровень фактора роста эндотелия имеет значение 161,45 пг/мл, а уровень эндостатина равен 272,16 нг/мл, что дает основание прогнозировать низкую эффективность медикаментозной терапии. Это подтверждается низким комплайнсом пациента, равным 63%, и последующими клиническими наблюдениями за больным.
Преимущества заявляемого способа состоят в том, что способ прогнозирования низкой эффективности терапии у пациентов с ишемической болезнью сердца после перенесенного ОКС обеспечивает повышение достоверности прогноза течения заболевания, который позволяет скорректировать медикаментозное лечение, повысить комплайнс пациента и улучшить исход лечения. Применение изобретения в клинической практике позволило существенно повысить точность прогнозирования эффективности медикаментозной терапии ишемической болезни сердца, что позволило повысить качество лечебно-диагностического процесса и повлекло значительный социально-экономический эффект.
Заявляемый способ контроля над состоянием пациента после перенесенного острого коронарного синдрома в ходе медикаментозного лечения на основании изучения факторов ангиогенеза в течение 12 месяцев и изучения приверженности к терапии апробирован в клинике и может быть рекомендован к использованию в амбулаторных и стационарных условиях.
Список использованной литературы
1. Aspirin in coronary heart disease. The Coronary Drug Project Research Group. // Circulation. - 1980 Dec. - 62(6 Pt 2). - V59-62.
2. Brown M.T. Medication Adherence: WHO Cares? / M.T. Brown, J.K. Bussell // Mayo Clin. Proc. - 2011. - Vol. 86, N 4. - P. 304-314.
3. Brurmer H, Cockcroft JR, Deanfield J, Donald A, Ferrannini E, Halcox J, Kiowski W,  TF, Mancia G, Natali A, Oliver JJ, Pessina AC, Rizzoni D, Rossi GP, Salvetti A, Spieker LE, Taddei S, Webb DJ; Working Group on Endothelins and Endothelial Factors of the European Society of Hypertension. Endothelial function and dysfunction. Part II: Association with cardiovascular risk factors and diseases. A statement by the Working Group on Endothelins and Endothelial Factors of the European Society of Hypertension. // J Hypertens. - 2005 Feb; 23(2): 233-46.
TF, Mancia G, Natali A, Oliver JJ, Pessina AC, Rizzoni D, Rossi GP, Salvetti A, Spieker LE, Taddei S, Webb DJ; Working Group on Endothelins and Endothelial Factors of the European Society of Hypertension. Endothelial function and dysfunction. Part II: Association with cardiovascular risk factors and diseases. A statement by the Working Group on Endothelins and Endothelial Factors of the European Society of Hypertension. // J Hypertens. - 2005 Feb; 23(2): 233-46.
4. Davignon J. The cardioprotective effects of statins / J. Davignon // Curr. Atheroscler. Rep. - 2004. - N 6. - P. 27-35.
5. Ho PM, Tsai TT, Maddox TM, Powers JD, Carroll NM, Jackevicius C, Go AS, Margolis KL, DeFor ТА, Rumsfeld JS, Magid DJ. Delays in filling clopidogrel prescription after hospital discharge and adverse outcomes after drug-eluting stent implantation: implications for transitions of care. Circ Cardiovasc Qual Outcomes. 2010 May; 3(3):261-6. doi: 10.1161/CIRCOUTCOMES. 109.902031. Epub 2010 Apr 20.
6. Joner M. Pathology of drug-eluting stents in humans: delayed healing and late thrombotic risk / M. Joner, A. V. Finn, A. Farb [et al.] // J. Am. Coll. Cardiol. - 2006. - Vol. 48. N l.-P. 193-202.
7. Niccoli G., Lanza G., Spaziani C. et al. Baseline systemic inflammatory status and no-reflow phenomenon after percutaneous coronary angioplasty for acute myocardial infarction. // Int J Cardiol. - 117. - P. 306-311.
8. Osterberg L. Adherence to medication / L. Osterberg, T. Blaschke // N. Engl. J. Med. - 2005. - Vol. 353, N 5. - P. 487-497.
9. Sabate E. Adherence to Long-Term Therapies: Evidence for Action, World Health Organization. - Geneva, Switzerland, 2003. - URL: http://whqlibdoc.who.int/publications/2003/9241545992.pdf.
10. Suwaidi A. Long-term follow-up of patients with mild coronary artery disease and endothelial dysfunction / A. Suwaidi, S. Hamasaki, S. Higano [et al.] // Circulation. - 2000. - Vol. 101. - P. 948-954.
11. Барбараш О.Л. Клиническая значимость показателей эндотелиальной дисфункции, оксидативного стресса и гемостаза у больных инфарктом миокарда / О.Л. Барбараш, В.В. Кашталап, В.Н. Каретникова [и др.] // Патология кровообращения и кардиохирургия. - 2007. - №2. - С. 28-33.
12. Ватутин Н.Т. Эндотелины и сердечно-сосудистая патология / Н.Т. Ватутин, Н.В. Кал инки на, А.Л. Демидова // Укр. кардiол. журн. - 2006. - №1. - С. 101-106.
13. Жданов B.C. Воспалительная клеточная реакция и тучные клетки в интиме аорты и легочной артерии человека на ранних стадиях атеросклероза / B.C. Жданов, И.П. Дробкова, П.В. Чумаченко // Архив патологии. - 2006. - №2. - С. 19-24.
14. Концевая А.В. Социально-экономический ущерб от острого коронарного синдрома в Российской Федерации / АВ. Концевая, А.М. Калинина, И.Е. Колтунов, Р.Г. Оганов // РФК. - 2011. - Т. 7, №2. - С. 158-166.
15. Лутай М.И. Вторичная профилактика и медикаментозное лечение больных с ишемической болезнью сердца. Можно ли изменить прогноз? / М.И. Лутай, А.Ф. Лысенко // Укр. кардюл. журн. - 2004. - №3. - С. 9-20.
16. Никитин Ю.П. Новые фундаментальные и прикладные основы атерогенеза / Ю.П. Никитин // Бюллетень СО РАМН. - 2006. - №2 (120). - С. 6-14.
17. Оганов Р.Г. Возможности улучшения профилактики сердечно-сосудистых заболеваний в Российской Федерации / Р.Г. Оганов, С.А. Шальнова, Г.Я. Масленникова // Профилактическая медицина. - 2009. - №6. - С. 3-7.
18. Омельяненко М.Г. Эндотелиальная дисфункция и ишемическая болезнь сердца у женщин молодого и среднего возраста / М.Г. Омельяненко. - М., 2008. - 111 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ неинвазивной диагностики коронарного атеросклероза при ишемической болезни сердца | 2024 |
|
RU2830356C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИБС У ПАЦИЕНТОВ РАЗЛИЧНЫХ ВОЗРАСТНЫХ ГРУПП | 2003 |
|
RU2241226C1 |
| Способ прогнозирования приверженности к физической реабилитации пациентов после коронарного шунтирования | 2019 |
|
RU2717640C1 |
| Способ индукции экстракардиальной реваскуляризации миокарда у больных ишемической болезнью сердца | 2021 |
|
RU2758024C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ НЕБЛАГОПРИЯТНЫХ СЕРДЕЧНО-СОСУДИСТЫХ СОБЫТИЙ В ТЕЧЕНИЕ ПЯТИ ЛЕТ ПОСЛЕ ПЕРЕНЕСЕННОГО ИНФАРКТА МИОКАРДА С УЧЕТОМ ПРИВЕРЖЕННОСТИ ПАЦИЕНТОВ К ЛЕЧЕНИЮ | 2015 |
|
RU2599372C1 |
| СПОСОБ ОЦЕНКИ АНГИОГЕННОГО ПОТЕНЦИАЛА ПРОГЕНИТОРНЫХ КЛЕТОК У БОЛЬНЫХ СЕРДЕЧНО-СОСУДИСТЫМИ ЗАБОЛЕВАНИЯМИ | 2011 |
|
RU2548801C2 |
| Способ профилактики повторного инфаркта миокарда у пациентов с ишемической болезнью сердца (ИБС) после перенесенного острого коронарного синдрома и кардиоваскулярных хирургических вмешательств | 2021 |
|
RU2757965C1 |
| Способ прогнозирования кардиоваскулярных осложнений в течение 12 месяцев после плановой эндоваскулярной реваскуляризации миокарда у больных ишемической болезнью сердца | 2020 |
|
RU2749485C1 |
| Способ прогнозирования вероятности развития неблагоприятных сердечно-сосудистых событий у пациентов с ишемической болезнью сердца, перенесших плановую коронарную реваскуляризацию миокарда | 2023 |
|
RU2814112C1 |
| Способ прогнозирования неблагоприятных сердечно-сосудистых событий в течение года после операции коронарного шунтирования | 2020 |
|
RU2731305C1 |
Изобретение относится к медицине, а именно к терапии и кардиологии, и касается прогнозирования эффективности терапии у пациентов с ИБС через 12 месяцев после острого коронарного синдрома (ОКС). Для этого через 12 месяцев после ОКС у пациентов, приверженных к медикаментозной терапии, в крови исследуют уровень фактора роста сосудистого эндотелия (VEGF-A) и эндостатина. В том случае, если уровень VEGF-A превышает 155,13 пг/мл, а уровень эндостатина превышает 266,39 нг/мл, прогнозируют низкую эффективность медикаментозной терапии. Способ обеспечивает повышение точности прогнозирования, что в свою очередь позволяет своевременно скорректировать медикаментозную терапию. 2 табл., 1пр.
Способ прогнозирования эффективности терапии у пациентов с ИБС через 12 месяцев после острого коронарного синдрома (ОКС), характеризующийся тем, что в качестве критериев эффективности назначаемой медикаментозной терапии и маркеров прогноза неблагоприятного течения заболевания определяют факторы ангиогенеза, при этом через 12 месяцев после ОКС у пациентов, приверженных к медикаментозной терапии, в крови исследуют уровень фактора роста эндотелия и эндостатина, и если уровень фактора роста эндотелия составляет более 155,13 пг/мл, а уровень эндостатина превышает значение 266,39 нг/мл, прогнозируют низкую эффективность медикаментозной терапии.
| RU 2000122807 A, 27.01.2003 | |||
| RU 2011131413 A, 10.02.2013 | |||
| СПОСОБ ОЦЕНКИ АНГИОГЕННОГО ПОТЕНЦИАЛА ПРОГЕНИТОРНЫХ КЛЕТОК У БОЛЬНЫХ СЕРДЕЧНО-СОСУДИСТЫМИ ЗАБОЛЕВАНИЯМИ | 2011 |
|
RU2548801C2 |
| US 2011124714 A1, 26.05.2011 | |||
| ЛОПАТИН Ю.М | |||
| и др | |||
| "Клинико-экономические аспекты эффективности лечения больных ишемической болезнью средца с постинфарктными аневризмами левого желудочка" | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| KOSEOGLU HI et al | |||
| "Serum levels of gamma-glutamy transferase are associated with cardiovascular disease in obstructive sleep apnea syndrome" | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
Авторы
Даты
2017-03-15—Публикация
2016-04-21—Подача