Изобретение относится к медицине и может быть использовано в кардиологии, кардиохирургии.
Несмотря на значительные достижения в области разработки стентов и совершенствующиеся подходы к медикаментозному сопровождению пациентов, перенесших процедуру эндоваскулярной реваскуляризации миокарда, регистрируется частое развитие сердечно-сосудистых осложнений в течение первого года после чрескожной коронарной реваскуляризации (ЧКВ), а в дальнейшем их частота неуклонно снижается в течение последующего срока наблюдения. Поэтому прогнозирование процессов рестенозирования, развития нефатального инфаркта миокарда, нестабильной стенокардии и тромбоза стента в течение первого года после планового 4KB имеет важнейшее значение для оказания эффективной помощи данной категории больных на амбулаторном этапе.
Таким образом, поиск предикторов неблагоприятных кардиоваскулярных событий с целью индивидуализации оптимальной фармакотерапии и коррекции тактики ведения пациентов является актуальной задачей современной кардиологии.
Известен способ прогнозирования однолетнего риска развития неблагоприятных сердечно-сосудистых событий после стентирования коронарных артерий у больных ишемической болезнью сердца (ИБС) с метаболическим синдромом без инсулинорезистентности, заключающийся в том, что у пациентов выявляют факторы риска: гипергомоцистеинемию, факт курения, наличие в двух и более коронарных артериях стенозов, суживающих просвет сосуда не менее, чем на 75% [1].
Недостатком способа является его узкая направленность: способ ориентирован только на больных ИБС с метаболическим синдромом без инсулинорезистентности и подвергшихся коронарному стентированию и не распространяется на больных сахарным диабетом.
Известен способ прогнозирования риска развития неблагоприятных сердечнососудистых и цереброваскулярных событий в течение 6 лет после плановой эндоваскулярной реваскуляризации миокарда [2], заключающийся в том, что определяли следующие клинические характеристики пациента: наличие или отсутствие наследственной предрасположенности к развитию сердечно-сосудистых заболеваний; проведение 4KB на фоне приема статинов с рекомендацией их последующего постоянного приема при выписке из стационара или отсутствие приема статинов; исходный уровень постпрандиальной глюкозы в крови в ммоль/л; наличие или отсутствие высокого риска развития контраст-индуцированной нефропатии.
Способ позволяет прогнозировать наступление неблагоприятных сердечнососудистых и цереброваскулярных событий в течение 6 лет после плановой эндоваскулярной реваскуляризации миокарда. Первичной комбинированной конечной точкой исследования были только большие неблагоприятные сердечнососудистые события, включающие смерть от сердечно-сосудистых причин, острый коронарный синдром (ОКС), цереброваскулярные события. В нашем способе понятие неблагоприятные сердечно-сосудистые события включает не только эти события, но и развитие нефатального инфаркта миокарда, повторные реваскуляризации по поводу рестенозирования стентов и/или прогрессирования атеросклероза.
В проанализированной патентной и научно-медицинской литературе адекватного прототипа предлагаемого способа прогнозирования кардиоваскулярных осложнений в течение 12 месяцев после плановой эндоваскулярной реваскуляризации миокарда у больных ишемической болезнью сердца не обнаружено. Нигде в проанализированной литературе для прогнозирования отдаленных исходов после планового ЧКВ не использовались предлагаемое сочетание предикторов.
Задачей изобретения является создание способа прогнозирования кардиоваскулярных осложнений в течение 12 месяцев после плановой эндоваскулярной реваскуляризации миокарда у больных ишемической болезнью сердца.
Поставленная задача решается путем определения у пациентов следующих факторов: концентрации в сыворотке крови эндотелина-1 (ЭТ-1) и вычисления отношения объема талии (ОТ)/объему бедер (ОБ), после чего для расчета риска развития неблагоприятных сердечно-сосудистых событий осуществляют математическую обработку числовых значений по предложенной формуле:
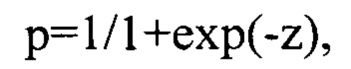
где р - вероятность развития неблагоприятных событий;
ехр - экспонента;
z - значение дискриминантной функции,
а значение дискриминантной функции определяют по формуле:
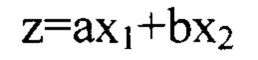
где x1-x2 - значения переменных, соответствующих рассматриваемым показателям, коэффициенты а,b - весовые коэффициенты соответствующих показателей.
x1 - концентрация ЭТ-1
x1=1 - если концентрация ЭТ-1 больше 0,751
x1=2 - если концентрация ЭТ-1 меньше или равно 0,751
а=4,591
x2 - отношение ОТ/ОБ
x2=1 - если отношение ОТ/ОБ меньше или равно 1,0495
x2=2 - если отношение ОТ/ОБ больше 1,0495
b=-2,006
Условная граница, разделяющая больных на 2 группы (развитие неблагоприятных событий и без них), по результатам анализа ROC кривой определена как 0,995. Таким образом, если вероятность развития неблагоприятных кардиоваскулярных событий, рассчитанная данным способом, менее 0,995 - предсказывается результат 1 (неблагоприятный), в случае если полученное значение больше 0,995 - предсказывается результат 0 (благоприятный).
Общий процент правильно классифицированных результатов (коэффициент конкордации) - 89,6%. Чувствительность модели - 88%, специфичность - 92%.
Статистическая значимость способа высокая: хи-квадрат=88,959, р<0,001. Качество подгонки хорошее (Критерий Хосмер-Лемешева: хи-квадрат=0,7, р=0,698). Доля совокупной дисперсии высокая - R Найджелкерка=0,695.
Новым в предлагаемом способе является выявление основных факторов, оказывающих значимое влияние на развитие кардиоваскулярных осложнений в течение 12 месяцев после плановой эндоваскулярной реваскуляризации миокарда, формула для определения вероятности развития кардиоваскулярных осложнений в течение 12 месяцев после плановой эндоваскулярной реваскуляризации миокарда, конкретное значение р меньше 0,995, позволяющее прогнозировать развитие кардиоваскулярных осложнений.
Поиск подходящих кардиометаболических биомаркеров является приоритетной задачей в области сердечно-сосудистой медицины. Это связано с тем, что традиционные факторы не всегда могут предсказать риск развития неблагоприятных кардиоваскулярных событий [3].
Предложенный способ прогнозирования риска развития неблагоприятных сердечно-сосудистых событий основан на том, что в его основе лежит учет влияния наиболее значимых и чувствительных факторов патогенеза прогрессирования атеросклероза, гиперпролиферации интимы сосудов внутри стентов и тромбоза. Учет этих факторов осуществляется путем количественной оценки в крови уровня ЭТ-1 и вычисления отношения ОТ/ОБ.
В исследовании Голикова А.П. и соавт. (2017) установлены наиболее значимые предикторы, влияющие на развитие неблагоприятных исходов в течение года наблюдения у больных СД с острым коронарным синдромом без подъема сегмента ST, которыми оказались: мультифокальный атеросклероз, снижение фракции выброса левого желудочка менее 51% и уровень ЭТ-1 более 0,87 фмоль/мл [4].
Уровень ЭТ-1 в плазме крови ранее был идентифицирован как новый маркер тяжести заболевания и клинического исхода у пациентов с ИБС [5] и ассоциирован с повышенным риском неблагоприятных событий у пациентов со стабильной ИБС [6; 7].
Отмечено, что экспрессия ЭТ-1 повышается непосредственно после имплантации стента. Наряду со способностью влиять на тонус сосудов, гиперэкспрессия ЭТ-1 может привести к вазоконстрикции и снижению коронарного кровотока, что может индуцировать или усугублять ишемию миокарда. Во-вторых, ЭТ-1 может снижать продукцию оксида азота (NO) и усиливать деградацию NO, что приводит к дисбаланс) между NO и ЭТ-1 и последующей эндотелиальной дисфункции [8]. В-третьих, ЭТ-1 может способствовать увеличению окислительного стресса и воспалительной клеточной инфильтрации, которые способствуют образованию, прогрессированию и разрыву атеросклеротических бляшек [9]. По сравнению с традиционными биомаркерами, представляющими собой повреждение миокарда (тропонин I), сердечный стресс (NT-proBNP) и воспаление (высокочувствительный С-реактивный белок), ЭТ-1 может отражать эндотелиальную функцию, что также важно для развития атеросклероза [10].
Изучение феномена висцерального ожирения как одного из наиболее значимых факторов риска СС3 и потребность в простом, доступном и достоверном методе оценки количества абдоминальной жировой ткани привели многих исследователей к использованию параметра ОТ и отношение ОТ/ОБ. Оценка ОТ представляет собой наиболее простой способ измерения, характеризующего абдоминальный тип распределения жировой ткани.
Несмотря на тесную взаимосвязь ОТ и индекса массы тела (ИМТ) измерение ОТ, в отличие от определения ИМТ, позволяет оценить не только степень отклонения массы тела от нормы, но и выраженность абдоминальной формы ожирения. Об этом свидетельствует высокая корреляционная связь между ОТ, с одной стороны, и висцеральной жировой тканью (r=0,696) и подкожной жировой тканью (r=0,828), с другой стороны, по результатам исследования с использованием компьютерной томографии абдоминальной области [11].
Однако ОТ представляет собой суррогатный параметр, не дающий информации о преобладании подкожного или интраабдоминального компонентов жировой ткани. В связи с этим более предпочтительным представляется отношение ОТ/ОБ. характеризующее распределение подкожной клетчатки на уровне бедра и талии и, тем самым, определяющее выраженность висцерального депо.
Использование ОТ и ОТ/ОБ позволяет выделить группу «метаболически толстых» пациентов из числа лиц с нормальным ИМТ.
Возможности верификации абдоминального ожирения с помощью ОТ и ОТ/ОБ обусловливают значение этих антропометрических методов для стратификации риска сердечно-сосудистых заболеваний и метаболического синдрома. В ряде исследований отмечены повышение риска развития СД в 10 раз у лиц с высоким значением ОТ. увеличение относительного риска ИБС в 1,5-2,5 раза при сравнении пациентов с высоким и низким значением ОТ, ассоциация высокого кардиометаболического риска с повышением отношения ОТ/ОБ независимо от ИМТ, в том числе у пациентов, перенесших инфаркт миокарда [12].
Технический результат достигается путем определения непосредственно перед стентированием двух показателей: уровня эндотелина-1, измерение ОТ и ОБ и вычисление отношения ОТ/ОБ и последующего расчета риска развития неблагоприятных сердечно-сосудистых событий по предложенной формуле.
Особенностью способа, полученного в настоящем исследовании, является то. что он прост в применении, в нем задействовано небольшое количество исходных факторов, что упрощает его практическое использование.
Существенные признаки, характеризующие изобретение, проявили в заявляемой совокупности новые свойства, явным образом не вытекающие из уровня техники и не являющиеся очевидными для специалиста.
Преимуществами предлагаемого способа являются:
1) малоинвазивность (однократный забор венозной крови);
2) определение всего 1 показателя дисфункции эндотелия и 1 антропометрического показателя (отношение ОТ/ОБ), который является рутинным методом и определяется у всех кардиологических пациентов;
3) патогенетическая обоснованность комбинации выделенных показателей как факторов, влияющих на развитие неблагоприятных сердечно-сосудистых событий у больных с ИБС;
4) доступность, дешевизна и простота в постановке исследования;
5) высокий уровень чувствительности - 88% и специфичности - 92%.
Метод может быть использован в кардиологических и терапевтических отделениях, на амбулаторном приеме для определения тактики ведения и диспансерного наблюдения за пациентами с ИБС после планового ЧКВ.
Значимость для врача практического здравоохранения заключается в том, что способ дает возможность:
1) получить индивидуальный профиль риска конкретного пациента с ИБС;
2) формировать сравнительно однородные по прогнозу группы риска больных;
3) осуществлять вторичную профилактику с целью предупреждения осложнений сердечно-сосудистых заболеваний, включая наиболее полную коррекцию факторов риска и применение более агрессивной тактики ведения пациентов. Основными механизмами осуществления вторичной профилактики являются: диспансерное наблюдение за больными, перенесшими коронарную реваскуляризацию в условиях первичной медицинской помощи врачами-кардиологами или врачами участковой службы, проведение медицинской реабилитации и санаторно-курортного лечения;
5) планировать индивидуальную лечебную тактику и организовывать долгосрочное адекватное лечение на этапах оказания помощи (госпитальный этап, поликлинический этап, санаторно-реабилитационный этап).
Такая поэтапная индивидуализированная оценка риска последующих неблагоприятных сердечно-сосудистых событий (ССС) у пациентов с предшествующей реваскуляризацией миокарда позволит улучшить тактику амбулаторного ведения выявленных лиц с высоким риском сердечно-сосудистых осложнений, усилить мотивацию самих пациентов и применить более интенсивные схемы вторичной профилактической терапии.
Существенные признаки, характеризующие изобретение, проявили в заявляемой совокупности новые свойства, явным образом не вытекающие из уровня техники и не являющиеся очевидными для специалиста. Идентичной совокупности признаков не обнаружено в патентной и научно-медицинской литературе.
Исходя из вышеизложенного, следует считать предлагаемый в качестве изобретения способ соответствующим условиям патентоспособности «Новизна». «Изобретательский уровень», «Промышленная применимость».
Изобретение будет понятно из следующего описания и приложенной к нему фигуры.
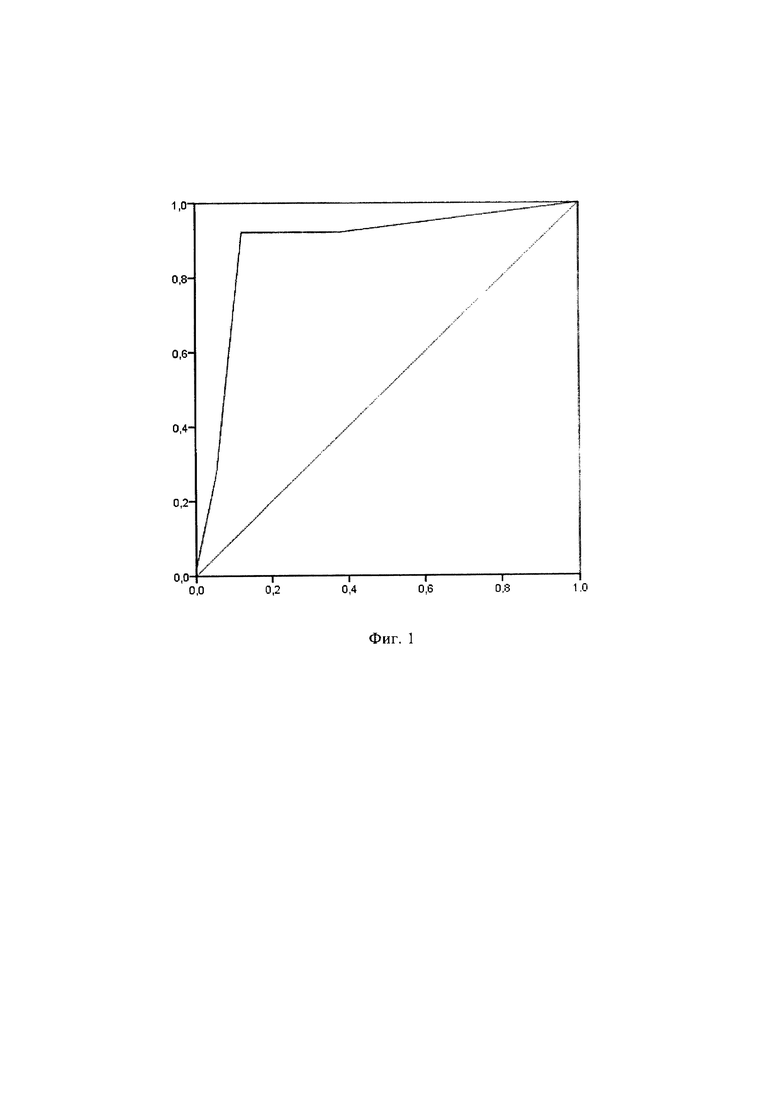
На фиг.1 представлено определение чувствительности и специфичности при различных значениях вероятности принадлежности к группе больных с неблагоприятным или благоприятным течением ИБС у обследованных пациентов (ROC-анализ): изображена характерологическая кривая (ROC-кривая) чувствительности и специфичности значений полученной модели в риске развития неблагоприятных сердечно-сосудистых событий. По оси абсцисс отложены значения специфичности (%), по оси ординат - чувствительности (%). По данным анализа следует, что «точкой отсечения» - cut off, характеризующей прогнозирование риска развития неблагоприятных сердечно-сосудистых событий с чувствительностью данного критерия 88% при специфичности 92%, является значение вероятности принадлежности к группе больных с неблагоприятным или благоприятным течением ИБС 0,995.
Способ осуществляют следующим образом:
Используемый материал для определения уровня эндотелина-1: сыворотка крови.
Сбор и хранение образцов: Свежесобранные образцы ЭДТА-плазмы или сыворотки должны быть помещены на лед немедленно после забора крови и далее их необходимо центрифугировать в течение дня. Если образцы не анализируют в течение дня взятия, то хранят при температуре -20°С, для длительного хранения - при -70°С.
Протокол анализа:
 Перед началом анализа все реагенты должны достичь комнатной температуры (18-26°С).
Перед началом анализа все реагенты должны достичь комнатной температуры (18-26°С).
 Маркируют положения стандартов, бланка, контролей и образцов на схеме анализа, поставляемой с набором.
Маркируют положения стандартов, бланка, контролей и образцов на схеме анализа, поставляемой с набором.
 Извлекают из пакета стрипы микропланшета и помечают их согласно схеме.
Извлекают из пакета стрипы микропланшета и помечают их согласно схеме.
1. Вносят по 50 мкл стандартов (белые крышки) образцов и контролей (желтые крышки) (STD/SAMPLE/CTRL) в соответствующие ячейки в дублях. Лунка для бланка должна оставаться пустой.
2. Добавляют по 200 мкл детектирующих антител (АВ, зеленая крышка флакона) в каждую ячейку, кроме бланка, тщательно перемешивают.
3. Накрывают стрипы пленкой и инкубируют в течение ночи (16-24 часа) при комнатной температуре (18-26°С). Ячейки должны быть тщательно запечатаны для предотвращения испарения.
4. Удаляют пленку с стрипов. Полностью удаляют содержимое ячеек и промывают их 5 раз по 300 мкл, разведенным буфером для промывок (WASHBUF). Удаляют остаток жидкости в ячейках после последней промывки переворачиванием стрипов на фильтровальную бумагу.
5. Добавляют по 200 мкл ферментного конъюгата (CONJ) во все ячейки.
6. Накрывают стрипы пленкой и инкубируют 1 час при комнатной температуре (18-26°С).
7. Удаляют пленку со стрипов. Полностью удаляют содержимое ячеек и промывают их 5 раз по 300 мкл, разведенным буфером для промывок (WASHBUF). Удаляют остаток жидкости в ячейках после последней промывки переворачиванием стрипов на фильтровальную бумагу.
8. Добавляют по 200 мкл субстрата (SUB) во все ячейки.
9. Инкубируют 30 минут при комнатной температуре (18-26°С) в темноте.
10. Добавляют по 50 мкл стоп-раствора (STOP) во все ячейки, перемешивают их содержимое.
11. Считают оптическую плотность при 450 нм с длинной волны сравнения 620 нм.
Калибровочная кривая строится с использованием значений оптической плотности, полученных для стандартов эндотелина-1, поставляемых с набором. Оценку результатов проводят с использованием алгоритма 4PL.
Измерение ОТ осуществляли в положении стоя по середине расстояния между вершиной гребня подвздошной кости и нижним боковым краем ребер. Измерение производили на выдохе, при упоре на обе стопы и руками, свободно висящими вдоль туловища. Окружность бедер измеряется вокруг самой широкой части ягодиц, лента удерживается параллельно полу. Используют измерительную ленту из стекловолокна. Затем вычисляют отношение путем разделения окружности талии к объему бедер.
Статистическая обработка результатов исследования проводили с помощью программ SPSS 17 и R.
Для выявления предикторов развития неблагоприятных конечных точек использовали метод логистической регрессии, а также ROC-анализ с построением характеристических кривых и расчетом AUC (площади под кривой). Значимым считали значение площади под ROC-кривой, превышающее 0,70.
Для выбора оптимального порога разделения для математических моделей, построенных с помощью пошаговой логистической регрессии (с включением и с исключением ковариат), использовали критерий «максимальной суммарной чувствительности и специфичности».
Данные представляли в виде медианы (Me) и квартального размаха (Q25-Q75 - 25-й и 75-й процентили). Критический уровень значимости р для всех используемых процедур статистического анализа принимали равным 0,05.
Для достижения поставленной цели в работе проведен анализ прогноза пациентов с ИБС, перенесших плановое ЧКВ, через год наблюдения.
В исследование включено 225 пациентов с ИБС в среднем возрасте 57 [51;63] лет, госпитализированных в стационар с целью выполнения плановой эндоваскулярной коронарной реваскуляризации миокарда посредством стентирования.
Критерии включения: документированная ИБС, показания к плановому ЧКВ.
Критерии исключения: менее 6 мес. после перенесенных острых коронарных или цереброваскулярных событий, неконтролируемая артериальная гипертензия. онкологические, гематологические и иммунные заболевания, воспалительные заболевания в стадии обострения.
Все пациенты подписывали информированное согласие на участие в исследовании и дальнейшее проспективное наблюдение, дающее право на обезличенную обработку данных. Исследование было проведено после одобрения протокола Локальным этическим комитетом НИИ кардиологии Томского НИМЦ.
Непосредственно перед стентированием коронарных артерий в сыворотке крови с помощью иммуноферментного метода определяли содержание одного из маркеров эндотелиальной дисфункции - уровень ЭТ-1 (фмоль/мл) и вычисляли отношение ОТ/ОБ.
Больные разделены на 2 группы в зависимости от наличия или отсутствия неблагоприятных сердечно-сосудистых событий (НССС).
Клинико-демографическая характеристика обследованных больных представлена в таблице 1. По основным клинико-демографическим показателям существенных различий между группами выявлено не было.
Таблица 1 - Клинико-демографическая характеристика исследуемых групп больных, Me [Q25;Q75]

Медикаментозная терапия до и после процедуры эндоваскулярной реваскуляризации миокарда статистически значимо не различалась между группами (таблица 2).
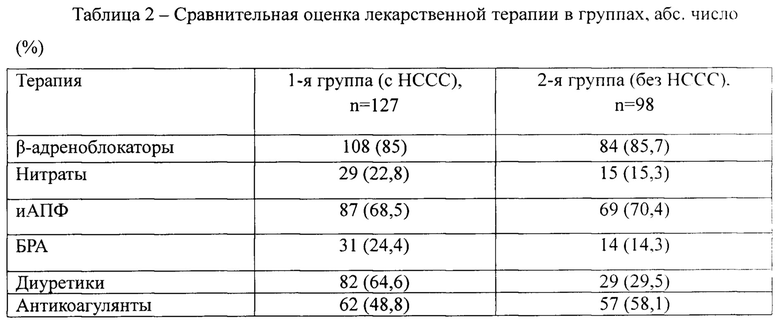

После выполнения ЧКВ все исследуемые были включены в 12-месячное проспективное наблюдение, в ходе которого регистрировались суммарные кардиоваскулярные "конечные точки", которыми в данном исследовании считали: случаи смерти, резвившиеся в результате любого сердечно-сосудистого события и декомпенсации сердечной недостаточности, а также незапланированные госпитализации в связи с развитием острого коронарного синдрома, нефатального инфаркта миокарда, острого нарушения мозгового кровообращения и в связи с возникновением или прогрессированием симптомов сердечной недостаточности на 1 функциональный класс и более (снижение толерантности к физическим нагрузкам, появление и/или усиление одышки, появление и/или нарастание отеков), возникновение нарушений ритма сердца, потребовавшее хирургической коррекции, повторная реваскуляризация (коронарное шунтирование, стентирование коронарных артерий (КА) в связи с рестенозированием первично имплантированного стента или прогрессированием атеросклероза КА. На завершающем этапе пациенты обеих групп были подвергнуты повторному комплексному обследованию (таблица 3).

Для прогнозирования кардиоваскулярных осложнений в течение 12 месяцев после плановой эндоваскулярной реваскуляризации миокарда у больных ишемической болезнью сердца была создана математическая модель. Полученная модель построена с помощью логистического регрессионного анализа с пошаговым включением предикторов. Для оценки качества построенной модели был использован ROC-анализ. Значение показателя площади под кривой AUC (Area Under Curve) составило 0,995. Для определения оптимального порога отсечения был выбран критерий «максимальной суммарной чувствительности и специфичности». В результате чувствительность модели составила - 88%, специфичность - 92%.
ПРИМЕР 1: Пациентка Ц., 60 лет поступила в клинику НИИ кардиологии 10.01.2017 г. с жалобами на давящие боли за грудиной при обычной физической нагрузке, ходьбе на 350 м, при подъеме на три лестничных пролета, купирующийся нитроглицерином (до 2 табл./сут), боли с иррадиацией в левое плечо, сопровождались одышкой смешанного характера, повышением АД до 160/90 мм рт.ст. Страдает сахарным диабетом 2 типа в течение года.
По данным коронарной ангиографии выявлен атеросклероз с поражением передней нисходящей артерии (ПНА) - 50%, огибающей артерии (OA) - 50%, 1 ветви тупого края (ВТК) - 75%, правой коронарной артерии (ПКА) - 75%.
Осуществлена реваскуляризация миокарда: стентирование стенозов ПКА 75% и 1 ВТК 75% стентами Integrity 3,5*18 и Resolute Integrity 3,0*15.
Клинический диагноз: ИБС: Стенокардия напряжения ФК III. Атеросклероз коронарных артерий (ПНА50%,ОА 50%, 1ВТК 75%, ПКА 75%). Стентирование стенозов ПКА 75% и 1 ВТК% стентами Integrity 3,5*18 мм и Resolute Integrity 3,0*15 мм. Фон: Гипертоническая болезнь III стадии. Медикаментозно достигнута нормализация АД. Сахарный диабет 2 тип, целевой гликированный гемоглобин 6,5%, достигнутый 7%. Гиперхолестеринемия. Риск 4. НК 1 стадии, ФК II (NYHA). Сопутствующие заболевания: Язвенная болезнь желудка, ремиссия. Грыжа пищеюдного отверстия диафрагмы. Хронический дуоденит, ремиссия.
Назначено лечение: клопидогрел 75 мг/сутки, аспирин 75 мг/сутки после еды. бисопролол 2,5 мг утром, фозиноприл 5 мг/сутки, розувастатин 20 мг на ночь, метформин 500 мг по 1 таблетки 2 раза в день
При оценке риска развития неблагоприятных кардиоваскулярных событий был использован разработанный способ:

Таким образом, значение р<0,995 позволяет предсказать развитие кардиоваскулярных осложнений. И действительно, через 10 месяцев на фоне рекомендованного лечения возобновились приступы стенокардии, при обследовании (проведена диагностическая коронарография): прогрессирование стеноза OA до 75%. Ранее установленные стенты проходимы. Выполнено стентирование OA стентом Cypher без остаточного стеноза. Показатели гемодинамики: АД 130/80 мм рт.ст., частота сердечных сокращений 60 уд/мин. ФК ХСН остался на прежнем уровне - II по NYHA.
ПРИМЕР 2: Пациент В., 58 лет поступил в клинику НИИ кардиологии 15.01.2018 года с жалобами на давящие боли в области сердца при ходьбе на 300 м, купирующиеся нитроглицерином (до 1-2 табл./сут.), на повышение АД до 180/100 мм рт.ст. При обследовании по данным эхокардиографии признаки постинфарктного кардиосклероза.
По данным коронарной ангиографии выявлен атеросклероз с поражением ПНА стеноз 75%. 20.01.2018 г. в ПНА имплантирован стент с лекарственным покрытием.
Клинический диагноз: ИБС: стенокардия напряжения ФК III. Атеросклероз коронарных артерий (ПНА стеноз 75%). Стентирование ПНА стентом Xience PR 3.5×23 мм (20.01.2018 г.). Постинфарктный кардиосклероз. НК I стадии. ФК II (NYHA). Фон: Гипертоническая болезнь III стадии, достигнуты целевые значения АД. Гипертрофия левого желудочка. Атеросклероз сонных (в бифуркации бляшки, слева плотная 30%. справа 35%), бедренных артерий (справа 35-40%, слева 20-25%). Ожирение I степени. Гиперхолестеринемия. Сахарный диабет 2 типа, целевой уровень гликированно] о гемоглобина 6,5%, достигнутый 6,5%. Диабетическая полинейропатия. Риск 4. Сопутствующий: Хронический атрофический гастрит, ремиссия. Хронический аутоиммунный тиреоидит, эутиреоз.
Назначено лечение: бисопролол 5 мг/сутки, кандесартан 16 мг 1 раз в день, аспирин 75 мг в обед, торасемид 5 мг утром, гликлазид MB 30 мг утром, метформин 850 мг 2 раза в день, клопидогрел 75 мг/сутки.
Для оценки риска развития неблагоприятных кардиоваскулярных событий был использован разработанный способ:
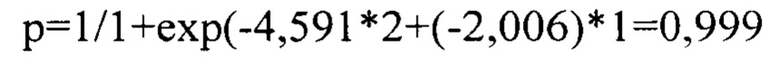
Через 12 месяцев на фоне рекомендованного лечения при контрольном обследовании (проведена диагностическая коронарография) не выявлено прогрессирования атеросклероза, признаков рестенозирования стента. Показатели гемодинамики: АД 140/80 мм рт.ст., частота сердечных сокращений 79 уд/мин. ФК ХСН остался на прежнем уровне - II по NYHA.
Литература
1. Тепляков А.Т., Гракова Е.В., Сваровская А.В., Суслова Т.Е., Лавров А.Г. Способ прогнозирования однолетнего риска развития неблагоприятных сердечно-сосудистых событий после стентирования коронарных артерий у больных ишемической болезнью сердца с метаболическим синдромом без инсулинорезистентности. Патент на изобретение RU 2663496 С1, 06.08.2018. Заявка №2017132222 от 14.09.2017.
2. Вершинина Е.О., Лавров А.Г., Репин А.Н. Способ прогнозирования риска отдаленных фатальных сердечных и цереброваскулярных событий после плановой эндоваскулярной реваскуляризации миокарда. Патент на изобретение RU 2642930 С1, 29.01.2018. Заявка №2017112673 от 12.04.2017.
3. Гарганеева А.А., Борель К.Н., Округин С.А., Кужелева Е.А. Влияние фракции выброса левого желудочка на отдаленный прогноз пациентов, перенесших коронарную катастрофу. Анализ 5-летнего мониторинга в рамках популяционной программы "Регистр острого инфаркта миокарда". Журнал сердечная недостаточность. 2014. Т. 15. №4 (85). С. 218-223
4. Голиков А.П., Берне С.А., Стрюк Р.И. и др. Факторы прогноза у пациентов с острым коронарным синдромом без подъема сегмента ST в сочетании с сахарным диабетом 2-го типа (по результатам регистра). Терапевтический архив. 2017:3:65-71 DOI: 10.17116/terarkh201789365-71 [Golikov А.Р., Burns S.A., Stryuk R.I. et al. The prognostic factors in patients with acute coronary syndrome without ST-segment elevation in combination with type 2 diabetes mellitus (register results). Therapeutic Archive. 2017; 3:65-71 (in Russ)
5. Chen J, Chen MH, Guo YL, Zhu CG, Xu RX, Dong Q, Li JJ: Plasma big endothelin-1 level and the severity of new-onset stable coronary artery disease. J Atheroscler Thromb, 2015; 22: 126-135
6. Sabatine MS, Morrow DA, de Lemos JA, Omland T, Sloan S, Jarolim P, Solomon SD, Pfeffer MA, Braunwald E: Evaluation of multiple biomarkers of cardiovascular stress for risk prediction and guiding medical therapy in patients with stable coronary disease. Circulation, 2012; 125: 233-240.
7. Zhou BY, Guo YL, Wu NQ, Zhu CG, Gao Y, Qing P, Li XL, Wang Y, Dong Q, Liu G. Xu RX. Cui CJ, Sun J, Li JJ: Plasma big endothelin-1 levels at admission and future cardiovascular outcomes: A cohort study in patients with stable coronary artery disease. Int J Cardiol, 2017; 230: 76-79.
8. Се Zhang, Jian Tian, Lin Jiang, Lianjun Xu, Junhao Liu, et al. Prognostic Value of Plasma Big Endothelin-1 Level among Patients with Three-Vessel Disease: A Cohort Study. J Atheroscler Thromb. 2019 Nov 1; 26(11): 959-969. doi: 10.555l/jat.47324.
9. Li MW, Mian MO, Barhoumi T, Rehman A, Mann K, Paradis P, Schiffrin EL: Endothelin-1 overexpression exacerbates atherosclerosis and induces aortic aneurysms in apolipoprotein E knockout mice. Arterioscler Thromb Vase Biol, 2013; 33: 2306-2315.
10. Davenport AP, Hyndman KA, Dhaun N, Southan C, Kohan DE, Pollock JS, Pollock DM. Webb DJ, Maguire JJ: Endothelin. Pharmacol Rev, 2016; 68: 357-418.
11. Kim D-W, Kim J-Y, Jeong H. Comparison of Body Mass Index, Waist Circumference, and Waist-to-Height Ratio as a Predictors of Abdominal Fat Distribution in Male Examinees from the Health Promotion Center. Korean J Fam Pract. 2017;7(4):596-599. doi: 10.21215/kjfp.2017.7.4.596.
12. Груздева О.В., Акбашева О.Е., Бородкина Д.А., и др. Взаимосвязь показателей ожирения и адипокинов с риском развития сахарного диабета 2 типа через год после перенесенного инфаркта миокарда // Российский кардиологический журнал. - 2015. - №4. - С. 59-67. [Gruzdeva OV, Akbasheva ОЕ, Borodkina DA, et al. Relationship of obesity parameters and adipokines with the risk of 2nd type diabetes development in a year after myocardial infarction. Russian Journal of Cardiology. 2015;(4):59-67. (In Russ).] doi: 10.15829/15604071-2015-4-59-67.
Изобретение относится к медицине, а именно к кардиологии, и может быть использовано при прогнозировании неблагоприятных сердечно-сосудистых событий в течение 12 месяцев после плановой эндоваскулярной реваскуляризации миокарда. Способ включает определение уровня эндотелина-1 в крови и соотношение объема талии (ОТ) к объему бедер (ОБ) до проведения плановой эндоваскулярной реваскуляризации миокарда. Затем выполняют расчет риска развития неблагоприятных сердечно-сосудистых событий р по формуле р=1/1+exp(-z), где р - вероятность развития кардиоваскулярных осложнений, ехр – экспонента, z - значение дискриминантной функции, а значение дискриминантной функции определяют по формуле z=ax1+bx2, где x1-x2 - значения переменных, соответствующих рассматриваемым показателям, коэффициенты а, b - весовые коэффициенты соответствующих показателей, x1 - концентрация эндотелина-1, x1=1 - если концентрация эндотелина-1 больше 0,75, x1=2 - если концентрация эндотелина-1 меньше или равна 0,751, а=4,591 – константа, x2 - отношение ОТ/ОБ, x2=1 - если отношение ОТ/ОБ меньше или равно 1,0495, x2=2 - если отношение ОТ/ОБ больше 1,0495, b=-2,006 - константа. При значении р менее 0,995 прогнозируют развитие кардиоваскулярных осложнений. Использование изобретения позволяет прогнозировать наступление неблагоприятных сердечно-сосудистых событий в течение 12 месяцев после плановой эндоваскулярной реваскуляризации миокарда, получить индивидуальный профиль риска конкретного пациента с ишемической болезнью сердца при малой инвазивности и высоком уровне чувствительности - 88% и специфичности - 92%. 3 табл., 1 ил., 2 пр.
Способ прогнозирования кардиоваскулярных осложнений в течение 12 месяцев после плановой эндоваскулярной реваскуляризации миокарда у больных ишемической болезнью сердца, характеризующийся тем, что у больных до процедуры реваскуляризации определяют концентрацию в сыворотке крови эндотелина-1 и вычисляют отношение объема талии (ОТ) к объему бедер (ОБ), и вероятность развития кардиоваскулярных осложнений определяют по формуле
p=1/1+exp(-z),
где р - вероятность развития кардиоваскулярных осложнений;
ехр - экспонента;
z - значение дискриминантной функции,
а значение дискриминантной функции определяют по формуле
z=ax1+bx2,
где x1-x2 - значения переменных, соответствующих рассматриваемым показателям, коэффициенты а, b - весовые коэффициенты соответствующих показателей,
x1 - концентрация эндотелина-1,
x1=1 - если концентрация эндотелина-1 больше 0,751,
x1=2 - если концентрация эндотелина-1 меньше или равна 0,751,
а=4,591 – константа,
x2 - отношение ОТ/ОБ,
x2=1 - если отношение ОТ/ОБ меньше или равно 1,0495,
x2=2 - если отношение ОТ/ОБ больше 1,0495,
b=-2,006 - константа,
и при значении р менее 0,995 прогнозируют развитие кардиоваскулярных осложнений.
| Способ прогнозирования однолетнего риска развития неблагоприятных сердечно-сосудистых событий после стентирования коронарных артерий у больных ишемической болезнью сердца с метаболическим синдромом без инсулинорезистентности | 2017 |
|
RU2663496C1 |
| Способ прогнозирования риска отдалённых фатальных сердечных и цереброваскулярных событий после плановой эндоваскулярной реваскуляризации миокарда | 2018 |
|
RU2683691C1 |
| US 20160252526 A1, 01.09.2016 | |||
| СВАРОВСКАЯ А.В | |||
| Прогнозирование кардиоваскулярных осложнений у больных ИБС, ассоциированной с сахарным диабетом 2-го типа, перенесших эндоваскулярную реваскуляризацию, роль биомаркеров/Автореф | |||
| д.м.н., Томск | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| СЕ ZHANG et al | |||
| Prognostic Value | |||
Авторы
Даты
2021-06-11—Публикация
2020-10-05—Подача