Область техники, к которой относится изобретение
Настоящее изобретение относится к области клеточной биологии, в частности клеточной трансплантологии и тканевой инженерии, и может быть использовано с целью предварительной оценки эффективности трансплантации аутологичного клеточного материала для стимуляции роста кровеносных сосудов, что необходимо для лечения целого ряда заболеваний человека, таких как сердечно-сосудистые заболевания, повреждения нервной системы, урологические заболевания, дефекты костного аппарата, заболевания суставов, пародонта, ожоги, а также для коррекции возрастных изменений и кожных дефектов в дерматокосметологии. Предлагается способ комплексной оценки ангиогенного потенциала прогениторных клеток у больных сердечно-сосудистыми заболеваниями, апробированный на мезенхимальных стромальных клетках жировой ткани (МСК-ЖТ) пациентов с ишемической болезнью сердца и включающий в себя измерение содержания мРНК и белков основных ангиогенных факторов, продуцируемых прогениторными клетками, ангиогенной активности суммарных продуктов секреции клеток, а также оценку способности прогениторных клеток стимулировать васкуляризацию подкожных имплантатов Матригеля, введенных иммунодефицитным мышам. В качестве скринингового метода может быть использован более простой и доступный, но менее точный метод экспресс-оценки ангиогенных свойств прогениторных клеток, основанный на измерении ангиогенной активности суммарных продуктов секреции. Изобретение позволяет проводить тестирование аутологичного клеточного материала, полученного от пациентов, в том числе с ишемической болезнью сердца, перед трансплантацией для выбора оптимальной тактики клеточной терапии с целью стимуляции роста кровеносных сосудов.
Уровень техники
Сердечно-сосудистые заболевания, в том числе ишемическая болезнь сердца (ИБС), занимают первое место в структуре причин смертности в большинстве стран, несмотря на значительный прогресс в развитии медикаментозных методов лечения и хирургической и эндоваскулярной реваскуляризации. Одним из перспективных подходов к их лечению является терапевтический ангиогенез, основанный на введении в ишемизированные ткани генетических конструкций с генами факторов роста или стволовых/прогениторных клеток. Многие типы прогениторных клеток взрослого организма, в том числе мультипотентные мезенхимальные стромальные клетки, выделенные из костного мозга или жировой ткани (МСК-ЖТ), могут служить перспективным инструментом для терапевтического ангиогенеза благодаря своей способности стимулировать рост кровеносных сосудов, в частности путем секреции ангиогенных факторов роста. В качестве примера для разработки данного изобретения были использованы МСК-ЖТ пациентов с ИБС, поскольку их значительно легче получить в достаточно большом количестве при малоинвазивной процедуре ограниченной липосакции или биопсии жировой ткани, однако раскрываемое изобретение может быть применимо для любых других типов прогениторных клеток со схожим механизмом действия, включающим стимуляцию ангиогенеза в поврежденных тканях.
На моделях ишемии конечностей и миокарда у животных показано, что локальное и системное введение МСК-ЖТ способствует увеличению количества сосудов в тканях с нарушенным кровоснабжением и улучшению перфузии тканей кровью (Трактуев, 2006; Парфенова, 2006; Rehman, 2004; Miyahara, 2006; Nakagami, 2006; Gimble, 2007; Cai, 2009; Kondo, 2009). Восстановление кровотока в ишемизированной ткани при трансплантации МСК-ЖТ обусловлено несколькими механизмами. Во-первых, эти клетки секретируют широкий набор ангиогенных факторов роста, которые способствуют миграции и пролиферации эндотелиальных клеток и их предшественников, а также формированию новых сосудов (Rehman, 2004; Gimble, 2007; Kondo, 2009; Rubina, 2009; Madonna, 2010). Во-вторых, МСК-ЖТ секретируют активаторы плазминогена и матриксные протеазы, что способствует локальному разрушению внеклеточного матрикса и миграции клеток, участвующих в образовании сосудистой стенки, а также высвобождению связанных с матриксом ангиогенных факторов (Kachgal, 2011). В-третьих, МСК-ЖТ могут дифференцироваться в гладкомышечные и эндотелиальные клетки, встраивающиеся в растущие сосуды, а также стабилизировать вновь образованные сосуды, выполняя функцию перицитов (Miranville, 2004; Planat-Benard, 2004; Miyahara, 2006; Sumi, 2007).
Таким образом, МСК-ЖТ являются прекрасным материалом для клеточной терапии заболеваний ишемического генеза и уже используются в ранних фазах нескольких клинических исследований (Madonna, 2009; Murohara, 2009; Bailey, 2010; Gimble, 2011). Однако подавляющее большинство результатов, касающихся ангиогенных и регенеративных свойств МСК-ЖТ человека, получено на клетках, выделенных из жировой ткани относительно здоровых молодых доноров. В то же время известно, что старение и само заболевание может оказывать негативное влияние на состояние МСК (Fehrer, 2005; Sethe, 2006; Stolzing, 2008; Katsara, 2011; Madonna, 2011; Sun, 2011). Показано, что при старении снижается пролиферативный потенциал МСК-ЖТ и их способность к дифференцировке в адипогенном и остеогенном направлениях (Zhu, 2009; Huang, 2010), а также ухудшаются их ангиогенные свойства (El-Ftesi, 2009; Huang, 2010; Efimenko, 2011). Изменения свойств МСК, в том числе их способности стимулировать рост сосудов, при старении и/или наличии хронических патологий могут снижать эффективность аутологической клеточной терапии у пожилых пациентов с ИБС или хронической ишемией нижней конечностей - наиболее вероятных кандидатов для клеточной терапии.
Это обусловливает необходимость разработки метода предтрансплантационной оценки ангиогенных свойств собственных прогениторных клеток пациентов, в частности МСК-ЖТ, для определения оптимальной тактики клеточной терапии заболеваний ишемического генеза с помощью этих клеток и выбора при необходимости методов модификации клеток. Решением этой задачи является данное изобретение.
Предлагаемое изобретение не имеет аналогов (поиск аналогичных или близких по предлагаемым решениям патентов был проведен по базам данных WIPO, USPTO, Espacenet).
Раскрытие изобретения
Поскольку способность прогениторных клеток, включая МСК-ЖТ, стимулировать рост кровеносных сосудов обусловлена в значительной степени продукцией ими широкого набора ангиогенных факторов (Rehman, 2004; Gimble, 2007; Kondo, 2009; Rubina, 2009; Madonna, 2010), в способ комплексной оценки ангиогенного потенциала МСК-ЖТ пациентов с ИБС были включены методы оценки ангиогенной активности суммарных продуктов секреции клеток (Пример 2) и измерения содержания мРНК и уровня секреции в среду культивирования белков основных ангиогенных факторов роста, таких как фактор роста эндотелия сосудов (VEGF), плацентарный фактор роста (PlGF), фактор роста гепатоцитов (HGF), ангиопоэтин-1, ангиогенин, для которых в различных исследованиях было показано проангиогенное действие (Пример 3). Поскольку все эти факторы действуют на процессы ангиогенеза не по отдельности, а в совокупности, еще одним критерием оценки ангиогенного потенциала прогениторных клеток является выраженность ангиогенной активности суммарных продуктов секреции, под которыми понимается совокупность веществ, секретируемых клетками в среду культивирования, в состав которых входят как перечисленные выше проангиогенные факторы роста, так и другие секретируемые факторы. Для учета, помимо продукции паракринных факторов, вклада межклеточных взаимодействий прогениторных клеток с другими клетками в их ангиогенный потенциал в комплексный метод оценки был включен тест на способность МСК-ЖТ стимулировать рост кровеносных сосудов in vivo на модели васкуляризации подкожных имплантатов Матригеля, введенных иммунодефицитным мышам (Пример 4).
Задачей изобретения является создание более информативного способа оценки ангиогенного потенциала прогениторных клеток больных сердечно-сосудистыми заболеваниями с целью прогноза терапевтической эффективности клеточной терапии с использованием этих клеток для лечения ишемических заболеваний.
Техническим результатом, на достижение которого направлено заявленное изобретение, является возможность получения более объективных и полных данных об ангиогенном потенциале прогениторных клеток взрослого организма посредством получения различными лабораторными способами количественных результатов продукции этими клетками ключевых факторов, стимулирующих ангиогенез, как на уровне генной экспрессии, так и секреции в среду культивирования, а также использования для оценки функциональных тестов стимуляции ангиогенеза на хорошо известных в науке моделях in vitro и in vivo. Дополнительным техническим результатом является возможность проведения более простого, быстрого и менее затратного, хотя и менее информативного экспресс-анализа ангиогенного потенциала прогениторных клеток раскрываемым в изобретении способом посредством использования одного из функциональных тестов, включенных в комплексную оценку, результаты которого достоверно коррелируют с результатами остальных тестов.
Было установлено, что:
а) ангиогенная активность суммарных продуктов секреции МСК-ЖТ пациентов с ИБС снижается с возрастом (Пример 2);
б) содержание мРНК таких проангиогенных факторов роста, как PlGF и HGF, снижается с возрастом в МСК-ЖТ пациентов с ИБС (Пример 3);
в) содержание таких проангиогенных факторов роста, как VEGF, PlGF, HGF, ангиопоэтин-1 и ангиогенин, снижается с возрастом в кондиционированной среде от МСК-ЖТ пациентов с ИБС (Пример 3);
г) способность МСК-ЖТ стимулировать васкуляризацию подкожных имплантатов Матригеля снижается с возрастом пациентов;
д) показатель ангиогенной активности суммарных продуктов секреции МСК-ЖТ достоверно коррелирует как с уровнем продукции клетками проангиогенных факторов роста (Пример 3), так и со способностью МСК-ЖТ стимулировать васкуляризацию подкожных имплантатов Матригеля (Пример 4), что позволяет предлагать этот метод в качестве экспресс-варианта данного изобретения.
Использование экспресс-метода позволяет ускорить и снизить стоимость способа оценки ангиогенного потенциала прогениторных клеток конкретного пациента, а также сохранить часть клеточного материала, который используется для осуществления методов, входящих в комплексную оценку ангиогенного потенциала этих клеток.
Однако было показано, что для реализации способности МСК-ЖТ стабилизировать формирующиеся кровеносные сосуды недостаточно только воздействия продуцируемых ими ангиогенных факторов, необходимо образование межклеточных контактов между МСК-ЖТ и другими клетками сосудистой стенки (Rubina et al., 2009). Поэтому метод экспресс-оценки ангиогенного потенциала прогениторных клеток, отражающий влияние только паракринных факторов, является более простым и доступным, но менее точным по сравнению с методом комплексной оценки.
Экспресс-метод оценки ангиогенных свойств прогениторных клеток может быть использован в качестве скринингового для выявления пациентов, клетки которых обладают сниженным ангиогенным потенциалом. В этом случае пациенту может быть рекомендован комплексный метод оценки ангиогенного потенциала прогениторных клеток для выявления мишеней для коррекции терапевтических свойств клеточного материала с помощью методов предтрансплантационной модификации клеток. В качестве последних могут быть использованы методы общей стимуляции регенеративных, в том числе ангиогенных, свойств прогениторных клеток, такие как культивирование клеток в условиях низкого содержания кислорода (1-5%) (Трактуев, 2006; Буравкова 2009; Rehman. 2004; Thangarajah, 2009; Efimenko, 2011), обработка прогениторных клеток статинами, которые активируют Akt/eNOS внутриклеточный сигнальный каскад (Dimmeler, 2001), или ингибитором протеинкиназы р38 (Seeger, 2005), что способствует усилению пролиферативной активности этих клеток, а также культивирование прогениторных клеток в присутствии гормона шишковидной железы мелатонина, что приводит к повышению жизнеспособности и пролиферативной активности клеток, увеличивает секрецию ими ангиогенных факторов и стимуляцию роста сосудов при трансплантации в ишемизированную паренхиму почки (Mias, 2008). Перспективным является использование различных методов генетической модификации клеток конструкциями, несущими гены ангиогенных факторов роста, продукция которых снижена у данного пациента. В отдельных случаях, если результат комплексной оценки ангиогенного потенциала прогениторных клеток очень низкий, пациенту может быть рекомендована клеточная терапия с использованием аллогенных клеток молодых здоровых доноров.
Вывод о конкретном уровне ангиогенного потенциала прогениторных клеток больных сердечно-сосудистыми заболеваниями делают на стадии анализа результатов всех тестов (в случае комплексной оценки) или одного теста (в случае экспресс-анализа) (Осуществление изобретения).
Краткое описание фигур
Фиг. 1. Микрофотографии, отражающие формирование тубулярных структур эндотелиальными клетками человека на Матригеле в присутствии кондиционированной среды от МСК-ЖТ пациентов с ИБС разного возраста. В качестве эндотелиальных клеток использованы: А, Б - эндотелиальные клетки пупочной вены человека (HUVEC), В, Г - эндотелиальные клетки линии EA.hy926.
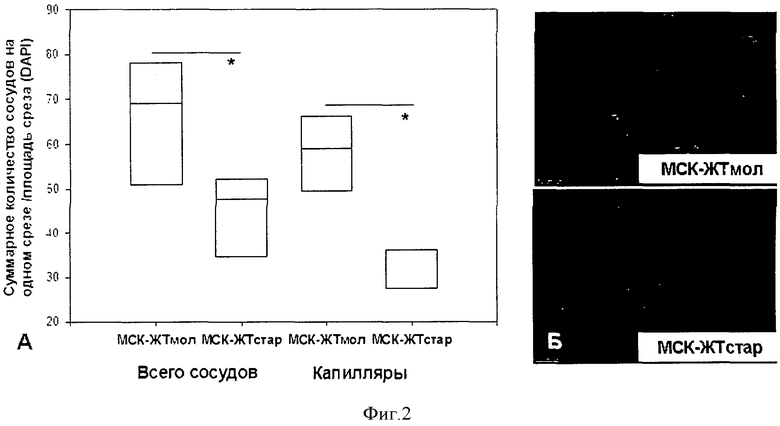
Фиг. 2. Диаграмма и микрофотографии, отражающие результаты оценки способности МСК-ЖТ пациентов с ИБС разного возраста стимулировать рост кровеносных сосудов на модели подкожной имплантации Матригеля иммунодефицитным мышам. МСК-ЖТ больных ИБС разного возраста смешивали с Матригелем, обедненным ростовыми факторами, в количестве 7×105 клеток на имплантат и вводили подкожно мышам линии NUDE. МСК-ЖТмол - тетки пациентов младше 60 лет, МСК-ЖТстар - клетки пациентов старше 60 лет. Имплантаты анализировали через 10 дней. А - Оценка количества CD31-положительных образований на срезах имплантатов Матригеля (n=16, по 5 срезов на образец). Данные представлены в виде медиана (10-й, 90-й процентили). * - 0,05<р<0,1. Б - Иммуногистохимическая окраска замороженных срезов имплантатов Матригеля, содержащих МСК-ЖТ пациентов разного возраста, на маркеры эндотелиальных клеток (CD31, зеленая флуоресценция) и перицитов (NG2, красная флуоресценция), объектив х40. Ядра клеток окрашены DAPI (синяя флуоресценция).
Осуществление изобретения
При осуществлении изобретения, помимо методов, подробно раскрытых в нижеследующих примерах, были использованы хорошо известные специалистам методики по культивированию клеток, описанные также в цитированных источниках.
Пример 1. Выделение и культивирование МСК-ЖТ больных ИБС
МСК-ЖТ выделяли из подкожного жира пациентов (n=31) с ишемической болезнью сердца, стенозирующим коронарным атеросклерозом по данным коронароангиографии. стабильной стенокардией II-IV функционального класса (по классификации Канадского общества по изучению сердечно-сосудистых заболеваний), которым проводилось аортокоронарное шунтирование. Всех пациентов с ИБС разделили на 3 группы по возрасту: больных в возрасте 44-48 лет (подгруппа А, средний возраст 46,0±1,67 лет, n=6), 52-58 лет (подгруппа Б, средний возраст 55,4±1,9 лет, n=10) и старше 60 лет (подгруппа В, средний возраст 68,9±4,2 лет, n=15). По основным клинико-анамнестическим признакам, а именно по полу, индексу массы тела, функциональному классу стенокардии, частоте инфаркта миокарда в анамнезе, наличию ожирения, артериальной гипертонии, сахарного диабета 2 типа и нарушению толерантности к глюкозе, дислипидемии, подгруппы больных ИБС разного возраста статистически значимо не различались между собой.
Выделение клеток проводили согласно ранее опубликованному протоколу (Zuk et al., 2001) с некоторыми модификациями. Подкожный жир, полученный в ходе аортокоронарного шунтирования, помещали в стерильную пробирку. Выделение клеток осуществляли в стерильных условиях ламинарного бокса. Ткань измельчали сосудистыми ножницами до консистенции суспензии мелких (размером не более нескольких кубических миллиметров) кусочков и смешивали с растворами ферментов коллагеназы I типа (200 ед/мл, Worthington Biochemical, США) и диспазы (40 ед/мл Invitrogen Corporation, Германия) при соотношении объема ткани (в мл) к объему ферментативного раствора (в мл) 1:2. Образец инкубировали при 37°C в течение 30 мин при постоянном покачивании; по окончании инкубации к нему добавляли равный объем среды AdvanceSTEM™ (HyClone) (#SH30879.01) и центрифугировали при 200 g в течение 10 мин. Белесый поверхностный слой, представленный зрелыми адипоцитами и кусочками ферментативно необработанной ткани, удаляли, а осадок, состоящий из стромальных клеток жировой ткани, а также остатков соединительной ткани и клеток крови суспендировали в лизирующем буфере для эритроцитов. Полученную смесь инкубировали 2-3 минуты в 37°C при перемешивании, после чего к образцу добавляли равный объем среды AdvanceSTEM™ (HyClone) (#SH30879.01) и фильтровали через нейлоновые мембраны (BD Falcon Cell Stainer) с размером пор 100 микрон. Для очищения популяции стромальных клеток от клеток крови и клеточного дебриса на конечном этане суспензию центрифугировали при 200 g 5 мин. Супернатант удаляли, а осадок ресуспендировали в среде AdvanceSTEM™ (HyClone) (#SH30879.01) / Antibiotic / Antimycotic Solution 100x (HyClone) (#SV30079.01). Затем высаживали клетки на чашки Петри (Corning) диаметром 60 мм в количестве 1×105 клеток на каждую чашку и культивировали в 4 ml среды AdvanceSTEM™ (HyClone) (#SH30879.01) / Antibiotic / Antimycotic Solution 100x (HyClone) (#SV30079.01) с добавлением 10% смеси факторов роста (Advance Stem Cell Growth Supplement, HyClone). На следующий день среду культивирования меняли на свежую среду этого же состава и выращивали клетки в СО2 - инкубаторе (5% CO2; 95% воздуха) при 37°C. Смену среды проводили каждые 2-3 дня; при достижении монослоя клетки пассировали с использованием HyQTase (HyClone) (#SV30030.01). Клетки, выделяемые из жировой ткани с помощью обработки ферментами, представляют собой смешанную популяцию различных клеточных типов, однако при культивировании в среде, поддерживающей рост недифференцированных МСК, ко второму пассажу в культуре остаются клетки, имеющие фибробластоподобную морфологию, причем заметных различий по морфологии клеток, полученных от пациентов разных возрастных групп, выявлено не было.
Для получения кондиционированной среды клетки второго пассажа в течение 24 часов депривировали в среде роста, не содержащей сыворотку, затем меняли среду на свежую, также не содержащую сыворотку, и культивировали клетки в течение 48 часов. После этого среду собирали, центрифугировали при 200 g 5 мин, добавляли коктейль ингибиторов протеаз (1:500, Sigma, кат. № Р1860), аликвоты по 1,5 мл замораживали в жидком азоте и хранили при -70°C.
Пример 2. Оценка ангиогенной активности суммарных продуктов секреции МСК-ЖТ пациентов с ИБС
Ангиогенную активность суммарных продуктов секреции МСК-ЖТ в среду культивирования оценивали с помощью методики образования капилляроподобных структур на Матригеле, обедненном ростовыми факторами (Growth factors reduced Matrigel, BD Biosciences) эндотелиальными клетками пупочной вены человека (HUVEC) или эндотелиальными клетками линии EA.hy926 [Aranda, Owen, 2009]. Для этого предварительно депривированные в течение 18 часов эндотелиальные клетки вены пуповины человека (HUVEC) 2-4 пассажа или эндотелиальные клетки линии EA.hy926 высаживали на 48-луночный планшет, покрытый Матригелем, в количестве 2×104 клеток на лунку. Затем в каждую лунку добавляли кондиционированную среду от МСК-ЖТ (в случае HUVEC в соотношении 1:1 со средой роста HUVEC). Каждый образец кондиционированной среды использовали не менее чем в двух лунках. В качестве отрицательного контроля использовали среду роста эндотелиальных клеток, не содержащую сыворотку, в качестве положительного контроля - среду роста HUVEC, содержащую 20% ФБС, или DMEM с низким содержанием глюкозы с добавлением 50 нг/мл VEGF человека. Планшет помещали в СО2-инкубатор при 37°C на 24 ч, после чего анализировали образование капилляроподобных структур с помощью светового микроскопа (Leica, Германия). Суммарную длину трубчатых структур в 5 случайно выбранных полях зрения в каждой лунке подсчитывали на изображениях, полученных при использовании объектива х10, с помощью программы MetaMorph 5.0 (Universal Imaging).
Было обнаружено, что способность кондиционированной среды от МСК-ЖТ пациентов с ИБС стимулировать образование тубулярных структур эндотелиальными клетками на Матригеле in vitro (Фиг. 1) снижается с возрастом, что выражалось в обратной корреляции между общей длиной тубулярных структур и возрастом пациентов (r=-0,53, р=0,03). Кондиционированная среда от клеток, выделенных из жировой ткани пациентов старшего возраста (старше 60 лет), стимулировала образование тубулярных структур достоверно менее выражено, чем среда от клеток, полученных от более молодых пациентов (Табл. 1).

Пример 3. Измерение содержания мРНК и белков основных ангиогенных факторов роста в МСК-ЖТ пациентов с ИБС
Содержание в МСК-ЖТ мРНК факторов, участвующих в регуляции ангиогенеза. проводили методом ПЦР в реальном времени. Для этого из клеток выделяли РНК при помощи набора реагентов RNeasy Miny Kit (50) (QIAGEN, США), затем на матрице РНК строили кДНК, используя набор Fermentas Reverse Transcription Reagents (Fermentas, Литва). Далее проводили ПЦР в реальном времени с использованием интеркалирующего красителя SYBR Green I («Синтол», Россия) и в амплификаторе BIO-RAD iQ5 Multicolor Real-time PCR detection system (Bio-rad, США). В качестве праймеров использовали уникальные комплементарные пары олигодезоксинуклеотидов к анализируемым генам (Табл. 2). Данные для каждого образца нормировали по экспрессии генов b-actin и gapdh.

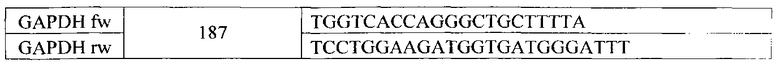
Мы проанализировали содержание мРНК генов основных регуляторов ангиогенеза в МСК-ЖТ пациентов разных возрастных групп. Результаты представлены в табл. 3.
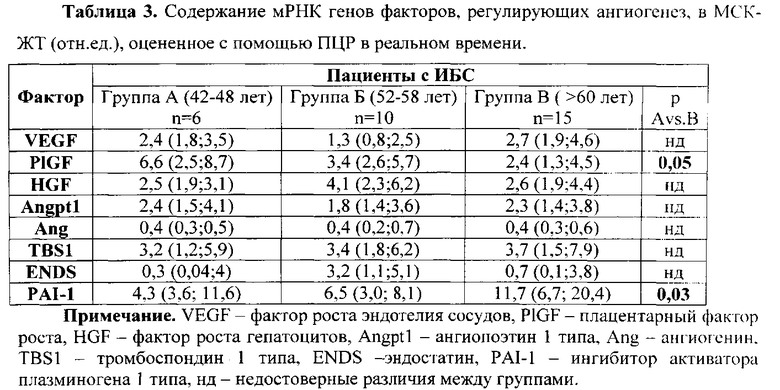
Мы наблюдали статистически значимое снижение содержания мРНК PlGF и повышение содержания мРНК PAI-1 в МСК-ЖТ пациентов старшего возраста, в то время как содержание мРНК генов других про- и антиангиогенных факторов с возрастом изменялось незначительно. Однако содержание мРНК VEGF (r=0,31, р=0,03), PlGF (r=0,54, р=0,001) и HGF (r=0,39, р=0,09) коррелировало с показателем ангиогенной активности суммарных продуктов секреции соответствующих МСК-ЖТ. Был отмечен значительный разброс среди клеток больных по содержанию мРНК антиангиогенного фактора эндостатина (ENDS), однако дальнейший анализ показал, что кондиционированная среда от МСК-ЖТ с низкими показателями содержания мРНК ENDS лучше стимулирует образование тубулярных структур эндотелиальными клетками (r=-0,46, р=0,05). Это подтверждает литературные данные об антиангиогенном действии эндостатина (O′Reilly, 1997).
Большинство ангиогенных факторов роста являются секретируемыми белками, поэтому мы оценили содержание VEGF, PlGF, HGF, ангиопоэтина-1 (Angpt1), ангиогенина, тромбоспондина-1 (TBS1) и ингибитора активатора плазминогена-1 (PAI-1) в кондиционированных средах от МСК-ЖТ пациентов разного возраста (Табл. 4).
Содержание указанных факторов оценивали с помощью наборов реагентов для иммуноферментного анализа (ELISA) компании R&D Systems (США). Для этого кондиционированную среду, полученную при культивировании в течение 48 часов предварительно депривированных МСК-ЖТ, размораживали. Измерение проводили следующим образом: 96-луночные планшеты, содержащие антитела к исследуемому белку, инкубировали с образцами кондиционированных сред или со стандартами исследуемых факторов в качестве положительного контроля в течение 2 часов. После четырехкратной промывки специальным промывочным раствором наносили биотинилированные поликлональные антитела козы в концентрации 0,2 мкг/мл на два часа, а затем повторяли процедуру отмывки. В качестве фермента, связывающегося с биотинилированными антителами, использовали стрептавидин, конъюгированный с пероксидазой хрена, в разведении 1:200, с которым инкубировали образцы в течение 20 минут. Для развития ферментативной реакции в лунки вносили субстрат на 20-30 мин, после чего реакцию останавливали добавлением стоп-раствора. Уровень поглощения раствора в лунках определяли при длине волны 450 нм с корректировкой при длине волны 620 нм. По результатам для разных разведений стандартов соответствующих белков строили калибровочную кривую, по которой определяли концентрацию исследуемого белка в образцах кондиционированных сред и пересчитывали ее на количество клеток для каждого образца. Результаты представлены в табл. 4.
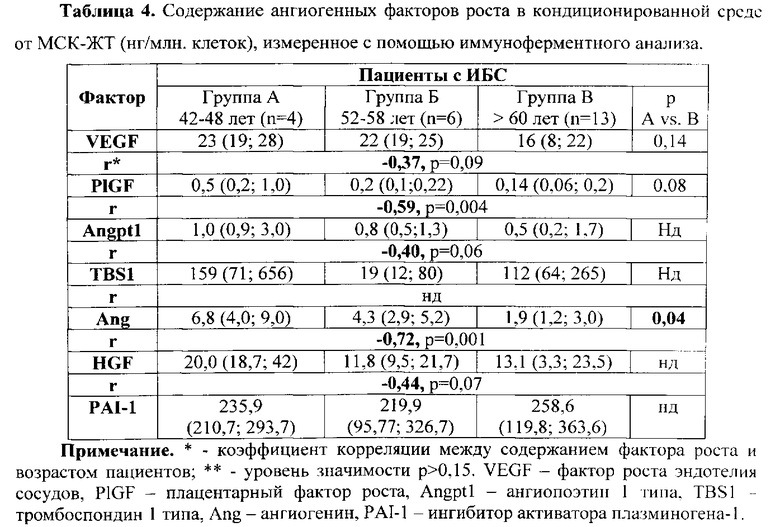
Несмотря на то, что средние значения содержания ангиогенных факторов в среде культивирования МСК-ЖТ были в несколько раз ниже в старших возрастных подгруппах, чем в более молодых подгруппах, достоверных различий для большинства факторов из-за выраженного разброса показателей не получено. Исключение составляет уровень ангиогенина, который у больных старше 60 лет был достоверно снижен более чем в три раза по сравнению с пациентами более молодой подгруппы (42-48 лет) (Табл. 4). Однако корреляционный анализ показал наличие достоверных или близких к достоверным обратных связей между содержанием проангиогенных факторов VEGF, PlGF, HGF, Angpt1 и ангиогенина в кондиционированной среде от МСК-ЖТ и возрастом пациентов с ИБС (Табл. 4).
Для того чтобы оценить, как содержание ангиогенных факторов в кондиционированной среде связано с ее способностью стимулировать образование капилляроподобных структур эндотелиальными клетками, мы сравнили для каждого образца кондиционированной среды показатели содержания разных факторов роста и ангиогенной активности суммарных продуктов секреции. Оказалось, что самая сильная положительная корреляционная связь наблюдалась для ангиопоэтина-1 (r=0,79, р=0,004), однако близкие к достоверным корреляционные связи наблюдали также между ангиогенной активностью суммарных продуктов секреции и содержанием ангиогенина (r=0,50, р=0,06), VEGF (r=0,65, р=0,04) и PlGF (r=0,56, р=0,08).
Пример 4. Оценка способности МСК-ЖТ пациентов с ИБС стимулировать васкуляризацию подкожных имплантатов Матригеля, введенных иммунодефецитным мышам
Ранее было описано несколько механизмов ангиогенного действия МСК-ЖТ, среди которых продукция ангиогенных факторов роста является основным, но не единственным механизмом, обеспечивающим способность МСК-ЖТ стимулировать рост кровеносных сосудов. Поэтому для полноценной оценки ангиогенных свойств МСК-ЖТ пациентов с ИБС мы использовали модель ангиогенеза in vivo (введение клеток в составе подкожных имплантатов Матригеля иммунодефицитным мышам).
Для этого 7×105 МСК-ЖТ второго пассажа, полученные от пациентов младше 60 лет (МСК-ЖТмол) и старше 60 лет (МСК-ЖТстар), вводили подкожно иммунодефицитным мышам линии NUDE (n=8) в виде суспензии в Матригеле, обедненном факторами роста (Growth factors reduced Matrigel, BD Biosciences), инсулиновым шприцем с иглой толщиной 23G таким образом, чтобы Матригель успевал полимеризоваться под кожей и образовывал желеобразный имплантат неправильной формы (по 2 имплантата на животное).
Через 10 дней после подкожного введения суспензии клеток в Матригеле мышей умерщвляли путем цервикальной дислокации, полностью изымали имплантаты и замораживали их в жидком азоте в среде для заморозки тканей Tissue-Tek (Sakura, Япония) для последующего приготовления срезов (6 мкм). Оценку плотности кровеносных сосудов на срезах Матригеля проводили с помощью иммунофлуоресцентного окрашивания с использованием моноклональных антител крысы против маркерного антигена эндотелия сосудов CD31 (BD Pharmigen, кат. №550274, США) и антител кролика против маркера перицитов NG2 мыши (Chemicon, кат. № ab5320, США). Ядра клеток докрашивали флуоресцентным красителем DAPI. Полученные препараты анализировали при помощи флуоресцентного микроскопа ZeissAxiovert200M. Документирование изображений производили с помощью цифровой видеокамеры Axiocam HRc (Zeiss, Германия) и обработки в программе Axiovision. Размер сосудов и их плотность оценивали с помощью программного обеспечения MetaMorph 5.0 (Universal Imaging) и ClickCounter. Подсчет сосудов проводили в 5 полях зрения на срезе (по 12 срезов на каждый имплантат) при 20-кратном увеличении, отдельно выделяя капилляры (CD31-положительные образования без просвета или длиной менее 20 мкм), сосуды среднего диаметра (CD31-положительные образования диаметром или длиной 20-50 мкм) и крупные сосуды (диаметром более 50 мкм). Полученное число сосудов нормировали на единицу площади среза.
С помощью двойного иммунофлуоресцентного окрашивания срезов Матригеля антителами против маркеров эндотелия сосудов CD31 и перицитов NG2 было установлено, что МСК-ЖТ пожилых пациентов в среднем в полтора раза слабее стимулировали васкуляризацию имплантатов, чем МСК-ЖТ более молодых пациентов (Фиг. 2), хотя различия не достигали статистической значимости (средняя плотность всех сосудов 47,7 (41,2; 49,9) vs. 69,0 (60,0; 73,6), соответственно, р=0,09; средняя плотность капилляров - 36,2 (31,9; 36,2) vs. 59,0 (54,3; 62,6), соответственно, р=0,06) (Фиг. 2).
Выявленные нами различия между ангиогенной активностью МСК-ЖТ, полученных от пациентов с ИБС разного возраста, подтверждают необходимость предварительной оценки клеточного материала для аутологической клеточной терапии заболеваний ишемического генеза.
Следует отметить, что при сравнении результатов оценки ангиогенной активности суммарных продуктов секреции МСК-ЖТ пациентов и способности соответственных образцов клеток стимулировать васкуляризацию подкожных имплантатов Матригеля (общее количество сосудов на проанализированных срезах имплантата) мы обнаружили, что эти показатели достоверно коррелируют между собой (r=0,54, р=0,03, n=16). Учитывая, что ангиогенная активность суммарных продуктов секреции также достоверно коррелирует с уровнем основных проангиогенных факторов роста, продуцируемых МСК-ЖТ, предлагается использовать в качестве экспресс-оценки ангиогенных свойств МСК-ЖТ метод образования тубулярных структур эндотелиальными клетками в присутствии кондиционированной среды от МСК-ЖТ.
Таким образом, способ комплексной оценки ангиогенного потенциала прогениторных клеток у больных сердечно-сосудистыми заболеваниями согласно настоящему изобретению включает в себя а) определение содержания мРНК и белков важнейших проангиогенных факторов роста (VEGF, PlGF, HGF, ангиопоэтина-1, ангиогенина); б) измерение ангиогенной активности суммарных продуктов секреции клеток; в) оценку способности клеток стимулировать васкуляризацию подкожных имплантатов Матригеля, введенных иммунодефицитным мышам. В качестве скринингового может быть использован более простой и доступный метод экспресс-оценки ангиогенных свойств МСК-ЖТ с помощью измерения ангиогенной активности суммарных продуктов секреции клеток, учитывая тот факт, что этот показатель достоверно коррелирует как с уровнем продуцируемых МСК-ЖТ проангиогенных факторов роста, так и со способностью МСК-ЖТ стимулировать васкуляризацию тканей in vivo. Однако он не отражает различий в способности МСК-ЖТ стабилизировать формирующиеся кровеносные сосуды и является менее точным по сравнению со способом комплексной оценки.
Стадией, на которой проводится оценка ангиогенного потенциала прогениторных клеток, является анализ количественных данных, полученных в результате проведения всех указанных тестов (в случае комплексной оценки) или одного теста (в случае экспресс-анализа). Известно, что средний возраст дебюта ИБС составляет 45-50 лет (American Heart Association, 2002), поэтому показатели пациентов с ИБС возрастной группы 42-48 лет (средний возраст 46,0±1,67 лет) рассматриваются как нормальные. Таким образом, учитывая результаты проведенных исследований, представленные в Табл. 1, результаты экспресс-анализа считаются нормальными для больных сердечно-сосудистыми заболеваниями при значениях измеряемого показателя ≥89143 отн.ед и пониженными - при значениях измеряемого показателя <89143 отн.ед. (см. Таблицу 1).
В случае комплексной оценки итоговые результаты измерений считаются для больных сердечно-сосудистыми заболеваниями нормальными при следующих значениях измеряемых показателей: VEGF ≥2,4 отн.ед. (мРНК) и ≥23 нг/млн клеток (уровень секреции), PlGF ≥6,6 отн.ед. (мРНК) и ≥0,5 нг/млн клеток (уровень секреции), HGF ≥2,5 отн.ед. (мРНК) и ≥20 нг/млн клеток (уровень секреции), ангиопоэтин-1 ≥2,4 отн.ед. (мРНК) и ≥1,0 нг/млн клеток (уровень секреции), ангиогенин ≥0,4 отн.ед. (мРНК) и ≥6,8 нг/млн клеток (уровень секреции), ангиогенная активность суммарных продуктов секреции ≥89143 отн.ед., уровень васкуляризации имплантатов Матригеля по общему количеству сосудов ≥69 отн.ед. (см. Таблицы 1, 3, 4 и текст описания на стр. 13).
Итоговые результаты измерений считаются для больных сердечно-сосудистыми заболеваниями пониженными при следующих значениях измеряемых показателей: VEGF <2,4 отн.ед. (мРНК) и <23 нг/млн клеток (уровень секреции), PlGF <6,6 отн.ед. (мРНК) и <0,5 нг/млн клеток (уровень секреции), HGF <2,5 отн.ед. (мРНК) и <20 нг/млн клеток (уровень секреции), ангиопоэтин-1 <2,4 отн.ед. (мРНК) и <1,0 нг/млн клеток (уровень секреции), ангиогенин <0,4 отн.ед. (мРНК) и <6,8 нг/млн клеток (уровень секреции), ангиогенная активность суммарных продуктов секреции <89143 отн.ед., уровень васкуляризации имплантатов Матригеля по общему количеству сосудов <69 отн.ед (см. Таблицы 1, 3, 4 и текст описания на стр. 13).
Предлагаемый способ может в дальнейшем использоваться для тестирования аутологичного клеточного материала, полученного от пациентов, в том числе с ишемической болезнью сердца, перед трансплантацией для выбора оптимальной тактики клеточной терапии с целью стимуляции роста кровеносных сосудов.
Список литературы
1. Буравкова Л.Б., Гринаковская О.С., Андреева Е.Р. и др. Характеристика мезенхимальных стромальных клеток из липоаспирата человека, культивируемых при пониженном содержании кислорода. Цитология. 2009; 51(1):5-10.
2. Ефименко А.Ю., Старостина Е.Е., Калинина Н.И., Парфенова Е.В. Влияние возраста на ангиогенные свойства мезенхимальных стволовых клеток жировой ткани. Клеточная трансплантология и тканевая инженерия. 2011; VI (3):48-57.
3. Ефименко А.Ю., Старостина Е.Е., Рубина К.А., Калинина Н.И., Парфенова Е.В. Влияние гипоксии и воспалительных факторов на жизнеспособность и ангиогенную активность мезенхимных стромальных клеток из жировой ткани и костного мозга. Цитология. 2010; 52(2):144-154.
4. Калинина Н.И., Ефименко А.Ю., Старостина Е.Е., Парфенова Е.В., Ткачук В.А. Гипоксия как основной активатор ангиогенеза и роста жировой ткани. Российский физиологический журнал им. И.М. Сеченова. 2009; 95(3):283-9.
5. Парфенова Е.В., Цоколаева З.И., Трактуев Д.О. и др. Поиск новых «инструментов» для терапевтического ангиогенеза. Молекулярная медицина. 2006; 2:10-23.
6. Рубина К.А., Калинина Н.И., Ефименко А.Ю., Лопатина Т.В., Мелихова В.А.. Цоколаева З.И., Сысоева В.Ю., Ткачук В.А., Парфенова Е.В. Механизм стимуляции ангиогенеза в ишемизированном миокарде с помощью стромальных клеток жировой ткани. Кардиология. 2010; 50(2):51-61.
7. Трактуев Д.О., Парфенова Е.В., Ткачук В.А. и др. Стромальные клетки жировой ткани - пластический тип клеток, обладающих высоким терапевтическим потенциалом. Цитология. 2006; 48:83-94.
8. Aranda Е., Owen G.I. A semi-quantitative assay to screen for angiogenic compounds and compounds with angiogenic potential using the EA.hy926 endothelial cell line. Biol Res. 2009; 42:377-389.
9. Bailey A.M., Kapur S., Katz A.J. Characterization of adipose-derived stem cells: an update. Curr Stem Cell Res Ther. 2010; 5(2):95-102.
10. Cai L., Johnstone В.H., Cook T.G., et al. IFATS collection: Human adipose tissue-derived stem cells induce angiogenesis and nerve sprouting following myocardial infarction, in conjunction with potent preservation of cardiac function. Stem Cells. 2009; 27(1):230-7.
11. Dimmeler S., Aicher A., Vasa M. et al. HMG-CoA reductase inhibitors (statins) increase endothelial progenitor cells via the PI 3-kinase / Akt pathway. J Clin Invest. 2001; 108(3):391-7.
12. Efimenko A.Yu., Starostina E.E., Rubina K.A., Kalinina N.I., Parfenova E.V. Viability and Angiogenic Activity of Mesenchymal Stromal Cells from Adipose Tissue and Bone Marrow under Hypoxia and Inflammation in vitro. Cell and Tissue Biology. 2010; 4; 2:117-127.
13. Efimenko A., Starostina E., Kalinina N, Stolzing A. Angiogenic properties of aged adipose derived mesenchymal stem cells after hypoxic conditioning. Journal of Translational Medicine. 2011; 9(1):10-22.
14. El-Ftesi S., Chang E.I., Longaker M.Т., et al. Aging and diabetes impair the neovascular potential of adipose-derived stromal cells. Plast Reconstr Surg. 2009; 123(2):475-85.
15. Gimble J.M., Bunnell B.A., Chiu E.S., Guilak F. Concise Review: Adipose derived stromal vascular fraction cells and stem cells: let′s not get lost in translation. Stem Cells. 2011; 29(5):749-54.
16. Gimble J.M., Katz A.J., Bunnell B.A. Adipose-derived stem cells for regenerative medicine. Circ Res. 2007; 100(9):1249-60.
17. Heart Disease and Stroke Statistics-2003 Update. - Dallas: American Heart Association, 2002.
18. Huang S.C., Wu T.C., Yu H.C., et al. Mechanical strain modulates age-related changes in the proliferation and differentiation of mouse adipose-derived stromal cells. BMC Cell Biol. 2010; 11-18.
19. Kachgal S., Putnam A.J. Mesenchymal stem cells from adipose and bone marrow promote angiogenesis via distinct cytokine and protease expression mechanisms. Angiogenesis. 2011; 14(1):47-59.
20. Katsara O., Mahaira L.G., Iliopoulou E.G., et al. Effects of Donor Age, Gender, and In Vitro Cellular Aging on the Phenotypic, Functional, and Molecular Characteristics of Mouse Bone Marrow-Derived Mesenchymal Stem Cells. Stem Cells Dev. 2011; in press.
21. Kondo K., Shintani S., Shibata R., et al. Implantation of adipose-derived regenerative cells enhances ischemia-induced angiogenesis. Arterioscler Thromb Vasc Biol. 2009; 29(1):61-6.
22. Madonna R., De Caterina R. Adipose tissue: a new source for cardiovascular repair. J Cardiovasc Med (Hagerstown). 2010; 11(2):71-80.
23. Madonna R., Geng Y.J., De Caterina R. Adipose tissue-derived stem cells: characterisation and potencial for cardiovascular repair. Arterioscler Thromb Vasc Biol. 2009; 29:1723-1729.
24. Madonna R., Renna F.V., Cellini C., et al. Age-dependent impairment of number and angiogenic potential of adipose tissue-derived progenitor cells. Eur J Clin Invest. 2011; 41(2):126-33.
25. Mias С., Trouche E., Seguelas M.H. et al. Ex vivo pretreatment with melatonin improves survival, proangiogenic/mitogenic activity, and efficiency of mesenchymal stem cells injected into ischemic kidney. Stem Cells. 2008; 26(7):1749-57.
26. Miranville A., Heeschen C., Sengenes C., et al. Improvement of postnatal neovascularization by human adipose tissue-derived stem cells. Circulation. 2004; 110(3):349-55.
27. Miyahara Y., Nagaya N., Kataoka M., et al. Monolayered mesenchymal stem cells repair scarred myocardium after myocardial infarction. Nat Med. 2006; 12(4):459-65.
28. Murohara Т., Shintani S., Kondo K. Autologous adipose-derived regenerative cells for therapeutic angiogenesis. Curr Pharm Des. 2009; 15(24):2784-90.
29. Nakagami H., Morishita R., Maeda K., et al. Adipose tissue-derived stromal cells as a novel option for regenerative cell therapy. J Atheroscler Thromb. 2006; 13(2):77-81.
30. O′Reilly M.S., Boehm Т., Shing Y., et al. Endostatin: an endogenous inhibitor of angiogenesis and tumor growth. Cell. 1997, 88(2):277-285.
31. Planat-Benard V., Silvestre J.S., Cousin В., et al. Plasticity of human adipose lineage cells toward endothelial cells: physiological and therapeutic perspectives. Circulation. 2004; 109(5):656-63.
32. Rehman J., Traktuev D., Li J., et al. Secretion of angiogenic and antiapoptotic factors by human adipose stromal cells. Circulation. 2004; 109(10):1292-8.
33. Rubina K.A., Kalinina N.I., Efimenko A.Y., Lopatina T.V., Melikhova V.A., Tsokolaeva Z.N., Sysoeva V.Y., Tkachuk V.A., Parfyonova Ye.V. Adipose Stromal Cells Stimulate Angiogenesis via Promoting Progenitor Cell Differentiation, Secretion of Angiogenic Factors, and Enhancing Vessel Maturation. Tissue Eng Part A. 2009; 15(8):2039-50.
34. Seeger F.H., Haendeler J., Walter D.H. et al. p38 mitogen-activated protein kinase downregulates endothelial progenitor cells. Circulation. 2005; 111(9):1184-91.
35. Sethe S., Scutt A., Stolzing A. Aging of mesenchymal stem cells. Ageing Res Rev. 2006; 5(1):91-116.
36. Stolzing A., Jones E., McGonagle D., et al. Age-related changes in human bone marrow-derived mesenchymal stem cells: consequences for cell therapies. Mech Ageing Dev. 2008; 129(3):163-73.
37. Sumi M., Sata M., Toya N., et al. Transplantation of adipose stromal cells, but not mature adipocytes, augments ischemia-induced angiogenesis. Life Sci. 2007; 80(6):559-65.
38. Sun Y., Li W., Lu Z., et al. Rescuing replication and osteogenesis of aged mesenchymal stem cells by exposure to a young extracellular matrix. FASEB J. 2011; 25(5):1474-85.
39. Thangarajah H., Vial I.N., Chang E., et al. IFATS collection: Adipose stromal cells adopt a proangiogenic phenotype under the influence of hypoxia. Stem Cells. 2009; 27(1):266-74.
40. Zhu M., Kohan E., Bradley J., et al. The effect of age on osteogenic, adipogenic and proliferative potential of female adipose-derived stem cells. J Tissue Eng Regen Med. 2009; 3(4):290-301.
41. Zuk P.A., Zhu M., Mizuno H., et al. Multilineage cells from human adipose tissue: implications for cell-based therapies. Tissue Eng. 2001; 7(2):211-28.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СТИМУЛЯЦИИ РЕГЕНЕРАТИВНЫХ ПРОЦЕССОВ В ИШЕМИЗИРОВАННЫХ ТКАНЯХ | 2011 |
|
RU2497529C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ИШЕМИЧЕСКИХ ПОРАЖЕНИЙ ТКАНЕЙ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2012 |
|
RU2522778C2 |
| Способ оценки качества клеточного материала | 2016 |
|
RU2620969C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ОЖОГОВ И РАН НА ОСНОВЕ ЦИТОКИНОВ И ФАКТОРОВ РОСТА, СЕКРЕТИРУЕМЫХ МЕЗЕНХИМНЫМИ КЛЕТКАМИ ЧЕЛОВЕКА, СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА И СПОСОБ ЛЕЧЕНИЯ ОЖОГОВ И РАН | 2014 |
|
RU2574017C1 |
| СПОСОБ ПОВЫШЕНИЯ АНГИОГЕННОЙ АКТИВНОСТИ СТРОМАЛЬНЫХ КЛЕТОК ЖИРОВОЙ ТКАНИ | 2011 |
|
RU2531502C2 |
| СПОСОБ ПОВЫШЕНИЯ АНГИОГЕННОГО ПОТЕНЦИАЛА МЕЗЕНХИМАЛЬНЫХ СТВОЛОВЫХ КЛЕТОК ЖИРОВОЙ ТКАНИ | 2010 |
|
RU2443778C1 |
| Бесклеточные терапевтические средства для регенеративной медицины и способы их получения | 2018 |
|
RU2742034C2 |
| Способ активации регенераторного потенциала стромально-васкулярной фракции жировой ткани низкоинтенсивным лазерным излучением красного диапазона | 2022 |
|
RU2796294C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА ДЛЯ СТИМУЛЯЦИИ РЕГЕНЕРАЦИИ НА ОСНОВЕ ПРОДУКТОВ СЕКРЕЦИИ МУЛЬТИПОТЕНТНЫХ МЕЗЕНХИМНЫХ СТРОМАЛЬНЫХ КЛЕТОК ЧЕЛОВЕКА | 2015 |
|
RU2620167C1 |
| Способ получения ассоциатов гемопоэтических и стромальных клеток-предшественников, способных подавлять активацию и пролиферацию аллогенных лимфоцитов | 2019 |
|
RU2722669C1 |

Настоящее изобретение относится к области биотехнологии, конкретно к предварительной оценке эффективности трансплантации аутологичного клеточного материала для стимуляции роста кровеносных сосудов, и может быть использовано в медицине. Предлагается способ комплексной оценки ангиогенного потенциала прогениторных клеток у больных сердечно-сосудистыми заболеваниями, апробированный на мезенхимальных стромальных клетках жировой ткани (МСК-ЖТ) пациентов с ишемической болезнью сердца и включающий в себя измерение содержания мРНК и белков основных ангиогенных факторов, продуцируемых прогениторными клетками, таких как фактор роста эндотелия сосудов (VEGF), плацентарный фактора роста (PlGF), фактор роста гепатоцитов (HGF), ангиопоэтин-1 и ангиогенин, ангиогенной активности суммарных продуктов секреции клеток, а также оценку способности прогениторных клеток стимулировать васкуляризацию подкожных имплантатов Матригеля, введенных иммунодефицитным мышам. В качестве скринингового метода используют более простой и доступный, но менее информативный метод экспресс-оценки ангиогенных свойств прогениторных клеток, основанный на измерении ангиогенной активности суммарных продуктов секреции. Изобретение позволяет проводить тестирование аутологичного клеточного материала, полученного от пациентов, в том числе с ишемической болезнью сердца, перед трансплантацией для выбора оптимальной тактики клеточной терапии с целью стимуляции роста кровеносных сосудов. 2 н.п. ф-лы, 2 ил., 4 табл., 4 пр.
1. Способ комплексной оценки ангиогенного потенциала прогениторных клеток у больных сердечно-сосудистыми заболеваниями, включающий количественное измерение содержания мРНК и белков ключевых проангиогенных факторов, фактора роста эндотелия сосудов (VEGF), плацентарного фактора роста (PlGF), фактора роста гепатоцитов (HGF), ангиопоэтина-1 и ангиогенина, продуцируемых клетками, ангиогенной активности суммарных продуктов секреции клеток, содержащих по крайней мере указанные факторы, на модели формирования тубулярных структур эндотелиальными клетками человека в присутствии кондиционированной среды от прогениторных клеток, а также оценку способности собственных прогениторных клеток пациента стимулировать васкуляризацию подкожных имплантатов Матригеля, введенных иммунодефицитным мышам, при этом вывод о сниженном ангиогенном потенциале делают при следующих значениях исследуемых параметров: VEGF <2,4 отн.ед. (мРНК) и <23 нг/млн клеток (уровень секреции), PlGF <6,6 отн.ед. (мРНК) и <0,5 нг/млн клеток (уровень секреции), HGF <2,5 отн.ед. (мРНК) и <20 нг/млн клеток (уровень секреции), ангиопоэтин-1 <2,4 отн.ед. (мРНК) и <1,0 нг/млн клеток (уровень секреции), ангиогенин <0,4 отн.ед. (мРНК) и <6,8 нг/млн клеток (уровень секреции), ангиогенная активность суммарных продуктов секреции <89143 отн.ед., уровень васкуляризации имплантатов Матригеля по общему количеству сосудов <69 отн.ед.
2. Способ экспресс-оценки ангиогенного потенциала прогениторных клеток у больных сердечно-сосудистыми заболеваниями с помощью измерения ангиогенной активности суммарных продуктов секреции клеток, содержащих ключевые проангиогенные факторы, включающие по крайней мере фактор роста эндотелия сосудов (VEGF), плацентарный фактор роста (PlGF), фактор роста гепатоцитов (HGF), ангиопоэтин-1 и ангиогенин, на модели формирования тубулярных структур эндотелиальными клетками пупочной вены человека или эндотелиальными клетками человека линии EA.hy926 в присутствии кондиционированной среды от прогениторных клеток, при этом вывод о сниженном ангиогенном потенциале делают при значении исследуемого параметра ниже 89143 отн.ед.
| EFIMENKO A | |||
| et al., Angiogenic properties of aged adipose derived mesenchymal stem cells after hypoxic conditioning, Journ.of Translat | |||
| Medicine, 2011, v.9, n.10, p | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| RUBINA K | |||
| et al., Adipose Stromal Cells Stimulate Angiogenesis via Promoting Progenitor Cell Differentiation, Secretion of Angiogenic Factors, and Enhancing Vessel Maturation, | |||
Авторы
Даты
2015-04-20—Публикация
2011-12-06—Подача