Изобретение относится к медицине, а именно к онкологии, и может быть использовано для раннего выявления больных с предрасположенностью к развитию послеоперационных кровотечений из шва анастомоза до панкреатодуоденальной резекции.
Наиболее частым и грозным осложнением панкреатодуоденальных резекций (ПДР) остаются осложнения панкреато-дигестивного или панкреато-кишечного анастомоза. Эти осложнения составляют до половины случаев неблагоприятных исходов ПДР (см. Алибегов Р.А. и соавт. Ранние послеоперационные осложнения панкреатодуоденальных резекций. Хирургия. Восточная Европа. 2012; 3(03): 321-327). Профилактика развития и лечение несостоятельности панкреато-дигестивного, панкреато-кишечного анастомозов являются серьезной и актуальной проблемой.
Считается, что несостоятельность панкреато-дигестивного или панкреато-энтеро-анастомозов связана с местно-деструктивным действием активированных ферментов в зоне линии шва (см. Щепотин И.Б. и др. Модификация реконструктивного этапа при панкреатодуоденальной резекции - методика физиологической реконструкции. Клиническая онкология. 2011 (1): URL http://www.clinicaloncology.com.ua/; Alghamdi A.A. et al. Use of octreotide for the prevention of pancreatic fistula after elective pancreatic surgery: a systematic review and meta-analysis. Can. J. Surg. 2007, 50(6): 459-466). Аррозивные кровотечения при разъедании стенки сосуда протеолитическими ферментами представляют особую опасность для больного в том случае, когда активированный фибринолиз не уравновешен в достаточной степени системой противосвертывания, особенно это важно в применении к реконструктивным манипуляциям на внутренних органах.
Известно, что при развитии злокачественной опухоли активизируется эндогенный протеолиз (см.  Е. Proteasen in Malignomen. DMW: Deutsche med. Wochenschr. 2004. 129(8): 391-395; см. Katarina Wolf et. al. Multi-step pericellular proteolysis controls the transition from individual to collective cancer cell invasion. Nature Cell Biol. 2007; 9(8): 893-904). Решающим звеном в начальном этапе инициации протеолиза в поджелудочной железе является активация ферментов трипсинового типа, которая обусловливает действие других протеиназ и биологически активных веществ (см. Недашковский Э.В. Острый панкреатит: руководство для врачей/под ред. проф. Э.В. Недашковского. - М.: ГЭОТАР-Медиа, 2009. (библиотека врача-специалиста). Активирующие факторы превращают трипсиноген в трипсин, который сам становится активатором панкреатических проферментов. Ферменты трипсинового типа переваривают клеточные мембраны, способствуют выходу лизосомных гидролаз и углублению клеточных деструкций. Трипсиноподобные ферменты вызывают также протеолитический некробиоз панкреоцитов, что приводит к обширным кровоизлияниям и способствует быстрому распространению ферментного аутолиза в поджелудочной железе и за ее пределами (см. Мерзликин Н.В. и др. Панкреатит: монография /под ред. профессора Н.В. Мерзликина. М.: ГЭОТАР-Медиа, 2014). Патологический процесс приобретает лавинообразный характер, скорость которого зависит от соотношения механизмов активации и ингибирования.
Е. Proteasen in Malignomen. DMW: Deutsche med. Wochenschr. 2004. 129(8): 391-395; см. Katarina Wolf et. al. Multi-step pericellular proteolysis controls the transition from individual to collective cancer cell invasion. Nature Cell Biol. 2007; 9(8): 893-904). Решающим звеном в начальном этапе инициации протеолиза в поджелудочной железе является активация ферментов трипсинового типа, которая обусловливает действие других протеиназ и биологически активных веществ (см. Недашковский Э.В. Острый панкреатит: руководство для врачей/под ред. проф. Э.В. Недашковского. - М.: ГЭОТАР-Медиа, 2009. (библиотека врача-специалиста). Активирующие факторы превращают трипсиноген в трипсин, который сам становится активатором панкреатических проферментов. Ферменты трипсинового типа переваривают клеточные мембраны, способствуют выходу лизосомных гидролаз и углублению клеточных деструкций. Трипсиноподобные ферменты вызывают также протеолитический некробиоз панкреоцитов, что приводит к обширным кровоизлияниям и способствует быстрому распространению ферментного аутолиза в поджелудочной железе и за ее пределами (см. Мерзликин Н.В. и др. Панкреатит: монография /под ред. профессора Н.В. Мерзликина. М.: ГЭОТАР-Медиа, 2014). Патологический процесс приобретает лавинообразный характер, скорость которого зависит от соотношения механизмов активации и ингибирования.
Факт активации протеиназ трипсинового типа при онкологических заболеваниях давно доказан (см. Франциянц Е.М. и др. Изучение трипсиноподобных протеиназ и ингибиторов ликвора при лечении злокачественных глиом локальной химиотерапией. Международный журнал прикладных и фундаментальных исследований (материалы конф. «Фундаментальные исследования», Израиль (Тель-авив) 16-23 октября 2012), №10 2012, с. 107; Франциянц Е.М. и др. Исследование трипсиноподобных протеиназ и их ингибиторов в плазме крови больных раком носоглотки в динамике лучевого лечения. Паллиативная медицина и реабилитация. 2013; (1): 31-36; Маслов А.А. и др. Трипсиноподобные протеиназы, кининовая система и ингибиторы в плазме крови больных при раке желудка и лимфоме селезенки.
Журнал "Международный журнал прикладных и фундаментальных исследований" №10 (часть 1), 2014 год. Биологические науки. Фундаментальные и прикладные проблемы медицины и биологии, ОАЭ (ДУБАЙ) 16-23 октября 2014 г. с.127. (дата обращения 2014-08-15); Bassi С.et al. Reconstruction by pancreaticojejunostomy versus pancreaticogastrostomy following pancreatectomy: results of a comparative study. Ann. Surg. 2005; 242(6): 767-771). Сериновые протеиназы имеют преимущество в биохимических взаимодействиях в связи с небольшими энергетическими затратами (см. Кондранина Т.Г. и др. Белки острой фазы воспаления и маркеры эндотоксемии, их прогностическая значимость в гинекологической практике. Российский вестник акушера-гинеколога. 2009; (3): 26-30; Яровая Г.А. Калликреин-кининовая система. Прошлое и настоящее. URL: http://www.myshared.ru/slide/662762/ (опубликовано 11.12.2013)).
Учитывая взаимосвязь онкологических заболеваний и нарушений многих протеолитических систем, необходимо найти критерии прогноза развития таких осложнений, как послеоперационные кровотечения в связи с несостоятельностью применяемых реконструкций - панкреато-дигестивных или панкреато-кишечных анастомозов, по возможности в ранние сроки, для своевременной медикаментозной подготовки больного и профилактики осложнений. Особенно это важно в связи с травмирующим воздействием оперативного лечения, которое непосредственно дополнительно влияет на состояние систем свертывания и фибринолиза. Белки этих систем являются трипсиноподобными протеиназами серинового ряда, большинство из них входят в число соединений, участвующих в острофазовом ответе и способных первыми дать информацию об изменениях в системе гемостаза. Протеиназы трипсинового типа серинового ряда включают большой перечень узко- и широко специализированных белков, которые содержатся в крови и тканях, освобождаются из клеток при дегрануляции.
В сообщении М.Д. Тер-Ованесова и А.В. Маджуги (см. Тер-Ованесов М.Д., Маджуга А.В. Тромботические осложнения в онкологии: опыт, реализованный на практике. Практическая онкология. 2001; 5(1): (март), 25-32) указывается, что следует проводить мониторинг послеоперационных пациентов и выявлять наступающие изменения в показателях свертывания и противосвертывания крови. Определение показателей свертывания и противосвертывания является важным моментом в обследовании онкологического больного, в частности, имеющего рак поджелудочной железы.
Однако авторы рекомендуют проводить подобные обследования для прогноза только тромботических осложнений и не касаются активации протеолитических систем, в частности трипсиноподобных протеиназ, к которым относятся все ферменты фибринолиза. Выявляя наступающие изменения в показателях свертывания и противосвертывания крови, авторы не ставили своей целью прогноз кровотечений из шва после реконструкции панкреогастродуоденальной зоны и создания панкреато-кишечного или панкреато-дигестивного анастомоза.
В диссертационном исследовании Г.А. Шатверяна (см. Шатверян Г.А. Панкреатодуоденальная резекция в лечении рака головки поджелудочной железы и периампулярной зоны. Автореф. Дисс… докт. мед. наук. М., 2006 (дата конвертации 2.04.2013)), несостоятельность панкреато-кишечного анастомоза прогнозировали после анализа следующих факторов риска: факторов патологического процесса (характер основного заболевания, состояние паренхимы поджелудочной железы, диаметр панкреатического протока и др.) и факторов, связанных с операцией (оперативная техника, хирургический опыт, интраоперационное кровотечение и др.). Для этого автор использовал корреляционный анализ по 14 параметрам (корреляционный анализ по Spearmen), после чего были выявлены наиболее значимые факторы: состояние паренхимы поджелудочной железы, уровень гиперамилаземии в 1 сутки после операции, применение октреотида и характер основного заболевания. Такой всесторонний анализ ситуации в каждом конкретном случае позволял автору с большой долей вероятности прогнозировать риск несостоятельности панкреатоеюноанастомоза, причем наибольшее значение придавалось гиперамилаземии в 1 сутки после операции. Она была обусловлена реакцией поджелудочной железы на операционную травму, что увеличивало риск несостоятельности панкреатоеюноанастомоза. С целью снижения секреции поджелудочной железы автор использовал синтетический аналог соматостатина - октреотид.
Однако автором не рассматривались другие биохимические параметры, в частности, общая активность протеолиза и не ставилась цель прогноза кровотечения из шва анастомоза. Исследования активности одной только амилазы не объясняют развивающуюся несостоятельность панкреато-дигестивного или панкреато-энтеро-анастомозов, которая связана с действием многих ферментов в зоне линии шва (см. Щепотин И.Б.и др. Модификация реконструктивного этапа при панкреатодуоденальной резекции - методика физиологической реконструкции. Клиническая онкология. 2011 (1): URL http://www.clinicaloncology.com.ua/; Alghamdi А.А. et al. Use of octreotide for the prevention of pancreatic fistula after elective pancreatic surgery: a systematic review and meta-analysis. Can. J. Surg. 2007, 50(6): 459-466). Наконец, этот способ не применялся для предоперационного выявления пациентов со скрытой (не имеющей симптомов) индивидуальной предрасположенностью к послеоперационному кровотечению из шва анастомоза.
Данные литературы подтверждают отсутствие ранних и специфических показателей такого осложнения, как послеоперационное кровотечение в первые дни после ПДР и создания панкреато-дигестивных или панкреато-кишечных анастомозов.
Ни один из используемых критериев не позволяет проводить прогноз развития послеоперационных кровотечений из шва анастомоза до панкреатодуоденальной резекции. В доступной литературе также не обнаружилось сведений о предоперационном прогнозе развития послеоперационного кровотечения.
Техническим результатом изобретения является выявление за 3 дня до панкреатодуоденальной резекции по поводу рака головки поджелудочной железы индивидуальной предрасположенности больного к развитию послеоперационного кровотечения из шва панкреато-дигестивного или панкреато-кишечного анастомоза, что, в свою очередь, позволит своевременно изменить терапевтические схемы.
Технический результат достигается тем, что за 3 суток до панкреатодуоденальной резекции в плазме крови больного определяют общую активность трипсиноподобных протеиназ и при значениях этого показателя от 2642,5 мЕ/мл до 2999,5 мЕ/мл прогнозируют наличие индивидуальной предрасположенности к послеоперационному кровотечению из швов анастомозов, а при значении от 1175,7 мЕ/мл до 1306,3 мЕ/мл прогнозируют течение послегоспитального периода без кровотечения из швов анастомозов.
Изобретение «Способ прогнозирования индивидуальной предрасположенности к послеоперационному кровотечению при раке головки поджелудочной железы» является новым, так как оно неизвестно из уровня медицины в области раннего прогнозирования развития послеоперационных кровотечений.
Новизна изобретения заключается в том, что за 3 дня до панкреатодуоденальной резекции в цитратной плазме крови больного определяют общую активность трипсиноподобных протеиназ и при значениях этого показателя от 2642,5 мЕ/мл до 2999,5 мЕ/мл прогнозируют наличие индивидуальной предрасположенности к послеоперационному кровотечению из швов анастомозов, а при значении от 1175,7 мЕ/мл до 1306,3 мЕ/мл прогнозируют течение послегоспитального периода без кровотечения из швов анастомозов.
В открытых источниках информации России, стран СНГ и зарубежья указаний на аналогичный способ прогнозирования развития тромботических осложнений в период до операции не обнаружено.
Изобретение является промышленно применимым, так как может быть воспроизведено и многократно повторено в любой клинической лаборатории лечебных учреждений системы здравоохранения.
Способ осуществляется следующим образом. За 3 дня до операции у больного производится взятие крови в пробирку с 3,8% цитратом натрия в соотношении 9:1 для получения цитратной плазмы крови. Цитратную кровь центрифугируют, получают цитратную плазму и используют ее для определения общей активности трипсиноподобных протеиназ в тот же день. Определение проводят унифицированным методом.
Метод определения общей активности трипсиноподобных протеиназ (см. Пасхина Т.С. Определение компонентов кининовой системы: методические рекомендации. М., 1987) заключается в следующем. Отбирают 30 мкл цельной плазмы крови, доводят до 2,0 мл 0,05 М трис-HCl буфером рН 8,0, туда же вносят раствор низкомолекулярного синтетического субстрата N-α-бензоил-L-аргинина этилового эфира (БАЭЭ) в том же буфере и регистрируют реакцию его гидролиза протеиназами сыворотки (плазмы) крови на спектрофотометре в течение 30 минут при длине волны 253 нанометра против контроля на реактивы, не содержащего плазмы крови. Результат рассчитывают в миллиэстеразных единицах на 1 мл исследуемой жидкости за 1 минуту реакции: мЕ/мл по системе СИ. Одна миллиэстеразная единица соответствует гидролизу 1 мкмоль субстрата БАЭЭ за 1 минуту. Статистическую обработку цифровых данных проводили при помощи пакета сертифицированных прикладных программ Statistica v. 10. Достоверность различий между количественными показателями вычисляли с помощью t-критерия Стьюдента для малых выборок.
При значениях этого показателя от 2642,5 мЕ/мл до 2999,5 мЕ/мл прогнозируют наличие индивидуальной предрасположенности к послеоперационному кровотечению из швов анастомозов, а при значении от 1175,7 мЕ/мл до 1306,3 мЕ/мл прогнозируют течение послегоспитального периода без кровотечения из швов анастомозов.
Для проведения анализа требуется 35-40 минут и обычное лабораторное оборудование.
Был составлен прогноз предрасположенности к развитию послеоперационных кровотечений из швов анастомозов до панкреатодуоденальной резекции 79 больным раком головки поджелудочной железы, находившихся на лечении в отделении абдоминальной онкологии-1 ФГБУ «РНИОИ» Минздрава России. Панкреато-дигестивный анастомоз выполнен 26 больным, панкреато-кишечный (панкреато-энтеро-анастомоз) - 49 пациентам, обходные гастроэнтероанастомоз и холецистоэнтероанастомоз - 4 пациентам.
Для оценки состояния протеолитических ферментов в организме, пораженном злокачественной опухолью, а также изменений их активности, связанных с воздействием панкреатодуоденальной резекции, общую активность трипсиноподобных протеиназ определяли до начала лечения, полученные цифры сравнивали с нормой. Нормой считали величину общей активности трипсиноподобных протеиназ в плазме крови здоровых доноров, полученную со станции переливания крови. У доноров (таблица 1) общая активность трипсиноподобных протеиназ плазмы крови колебалась в пределах от 216 мЕ/мл до 411 мЕ/мл (в среднем 279,0±18,6 мЕ/мл). Гендерных и возрастных различий у доноров не установлено.
За 3 дня до панкреатодуоденальной резекции у больных взята цитратная плазма, проведено определение общей активности протеиназ, полученные результаты статистически обработаны. Больные были разделены на 2 группы: «С кровотечениями» и «Без кровотечений», активность трипсиновых протеиназ в плазме крови каждого больного прослеживалась до выписки.
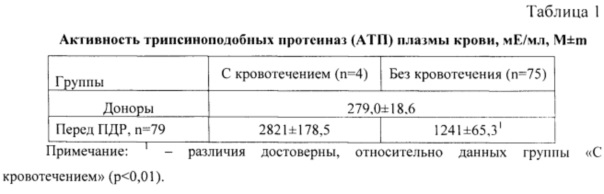
У 4 больных за 3 суток до панкреатодуоденальной резекции (ПДР) общая активность трипсиноподобных протеиназ составляла в среднем 2821±178,5 мЕ/мл. У группы больных «Без кровотечений» (75 больных) за 3 суток до ПДР активность трипсиновых протеиназ определялась в среднем 1241±65,3 мЕд/мл.
Особенности активности протеолиза проявляются в реакции на развитие в организме злокачественной опухоли, они связаны с разновидностью опухоли, скоростью ее роста, степенью злокачественности, состоянием эндогенных защитно-адаптивных систем и т.д. Активация трипсиноподобных протеиназ при раке и после оперативного лечения является закономерной и происходит в основном за счет роста калликреина, плазмина, эластазы и др. (см. А.А. Maslov et al. trypsin-like proteinases, kinin system and inhibitors in blood plasma of patients with stomach cancer or splenic lymphoma. 2015 ASCO Annual Meeting Proceedings J Clin Oncol 2015, 33, (suppl; abstr e15102) 51st Annual Meeting May 29-June 2, 2015 McCormick Place Chicago, 1L; Франциянц Е.М. и др. Метаболическое обоснование целесообразности чрескожной чреспеченочной холангиостомии при раке панкреогепатодуоденальной зоны. Журнал "Фундаментальные исследования" №1 (часть 7), 2015 год. Медицинские науки, стр. 1457-1461 (Дата обращения 2015-06-05); Франциянц Е.М. и др. Острофазовые белки плазмы крови в процессе подготовки к панкреатодуоденальной резекции при раке головки поджелудочной железы. Современные проблемы науки и образования. - 2015. - №4; URL: www.science-education.ru/127-20853 (дата обращения: 29.07.2015)).
Поздние вторичные или аррозивные кровотечения обусловлены деструкцией сосудистой стенки в результате местной активации протеолиза. Если активация протеолитических ферментов принимает лавинообразный характер еще до операции, следует принимать срочные меры для предупреждения возможных осложнений, в частности таких, как аррозивные кровотечения. Важно найти границу в активации протеолиза до или сразу после операции, которая позволит выявить группу риска для своевременной помощи, что и было сделано.
Найденные критерии предоперационного выявления предрасположенности к кровотечению позволяют предупредить такое послеоперационное осложнение, как кровотечение из швов анастомозов путем обнаружения предрасположенности больного к кровотечению.
В качестве примера приводим выписки из истории болезни. Пример №1. Больная О., 26.05.1967 г. Пол женский. Отделение абдоминальной онкологии-1 РНИОИ. Дата поступления в стационар 28.11.2014 г. Дата выписки из стационара 22.12.2014 г.
Жалобы при поступлении на боли в эпигастрии, общую слабость, похудание. Проведенное раннее лечение: нет.
Результаты обследования.
УЗИ органов брюшной полости от 19.11.2014, заключение: объемное узловое образование (D=8,0 см) тела матки (сонографически-лейомиоматозное строение). Образование в левом яичнике. Субъективно сообщалось об обильных менструациях.
МРТ органов брюшной полости от 21.11.2014, заключение: МР-картина массивного инфильтративного процесса головки поджелудочной железы с инфильтрацией парапанкреатической клетчатки и стенки двенадцатиперстной кишки.
СРКТ органов брюшной полости и малого таза от 18.11.2014, заключение: печень диффузно неоднородна, поджелудочная железа - опухоль головки 8,0×6,6×5,8 см с прорастанием 12-перстной кишки, тесно прилежит к правой доле печени, асцита нет. Матка 10,0×8,2 см неоднородной структуры, придатки слева солидно-кистозной структуры 5,4×4,1 см, справа - 2,7×2,0 см.
Предварительный диагноз при поступлении: рак головки поджелудочной железы, кл. гр. 2.
Сопутствующий диагноз: нет.
Исследование цитратной плазмы крови от 28.11.2014 за 3 суток до операции: активность трипсиновых протеиназ - 2764 мЕ/мл. Операция 01.12.2014 - панкреатодуоденальная резекция.
Гистологический анализ от 8.12.2014: ациноклеточный рак G2.
Окончательный диагноз: Рак головки поджелудочной железы T3N0M0, стадия 2, клиническая группа 2.
В послеоперационный период проводилось стандартное лечение, включающее инфузионно-трансфузионную терапию общим объемом до 3,0 литров в сутки, антибиотики широкого спектра действия, ингибиторы трансаминаз, аналоги сандостатина, блокаторы Н2-рецепторов, спазмолитики, адекватное обезболивание.
На фоне проводимой терапии на 4 сутки после операции у больной усилились боли в эпигастральной области, появилась стойкая гипотония до 60/90 мм рт.ст., отмечено повышение температуры тела до 38,0-38,5°С. Отмечено увеличение количества отделяемого по назогастральному зонду до 2,0 л. В анализе крови отмечен лейкоцитоз до 17,5×106/л со сдвигом лейкоцитарной формулы влево до миелоцитов амилаземия до 870 ммоль/л. Количество серозно-геморрагического отделяемого по дренажам из брюшной полости составило до 1000 мл/сут.
На 6 сутки отмечены признаки аррозивного кровотечения из брюшной полости: выделение по дренажам, стоящим в зоне культи поджелудочной железы, геморрагического отделяемого в объеме до 400 мл, в анализе крови признаки постгеморрагической анемии (снижение количества эритроцитов до 2,7×1012/л и гемоглобина до 73 г/л). К терапии добавлены гемостатические препараты (транексам, викасол, диценон), проводилось переливание компонентов крови - одногруппных свежезамороженной плазмы и эритроцитарной массы. Консервативная тактика была успешной, в дальнейшем признаков кровотечения не отмечалось.
В течение 10 дней больной проводилось полное парентеральное питание. На 10-й день состояние больной стабилизировалось, купировался болевой синдром, нормализовалось АД и температура тела, появилась перистальтика кишечника, стали отходить газы, был самостоятельный стул.
Лабораторно: в анализе крови отмечено уменьшение количества лейкоцитов с нормализацией лейкоцитарной формулы, амилаза в крови в пределах нормы (до 95 ммоль/л). Количество отделяемого из брюшной полости уменьшилось.
Выписка: в удовлетворительном состоянии.
Пример №2. Больная С. 02.01.1952 г. Пол женский. Отделение абдоминальной онкологии-1 РНИОИ.
Дата поступления в стационар: 21.11.2014. Дата выписки из стационара: 03.12.2014. Жалобы при поступлении на боли в эпигастрии.
Проведенное раннее лечение: чрескожная чреспеченочная холангиостомия как первый этап оперативного лечения.
Результаты обследования. МРТ органов брюшной полости от 17.11.2014, заключение: состояние после дренирующего вмешательства, МР-картина опухоли - в проекции головки поджелудочной железы с паравазальной инфильтрацией области стенки воротной вены и признаками вовлечения селезеночной вены, с признаками mts поражения лимфоузлов ворот печени.
ФГДС от 12.11.2014: перипроцесс в области постбульбарного отдела 12-перстной кишки. Гипоацидный гастрит, ассоциированный с Hp (++).
Диагноз при поступлении: рак головки поджелудочной железы, возможно прорастание в 12-перстную кишку.
Исследование цитратной плазмы крови за 3 суток до операции: активность трипсиновых протеиназ - 1235,4 мЕ/мл.
Операция 24.11.2014: панкреатодуоденальная резекция, формирование обходных гастроэнтероанастомоза и холецистоэнтероанастомоза на выключенной по Брауну петле тонкой кишки.
Гистологический анализ от 18.11.2014: аденокарцинома G2.
Окончательный диагноз: Рак головки поджелудочной железы, прорастание в 12-перстную кишку, верхнюю брыжеечную артерию.
Выписка: без осложнений, в удовлетворительном состоянии.
Последняя явка 24.03.2015 - чувствует себя удовлетворительно, проведен 6 курс полихимиотерапии.
Технико-экономическая эффективность способа заключается в его специфичности, возможности раннего выявления индивидуальной предрасположенности к кровотечению, проведения анализа в день взятия крови, что позволит своевременно изменить терапевтические схемы путем включения в них антикоагулянтов.
Специфичность способа для прогнозирования течения послегоспитального периода без развития желудочно-кишечных кровотечений из шва анастомоза - 100%, для выявления предрасположенности к развитию желудочно-кишечных кровотечений из шва анастомоза в послеоперационный период - 94,9%.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования развития тромботических осложнений после панкреатодуоденальной резекции при раке головки поджелудочной железы | 2015 |
|
RU2618402C1 |
| Способ прогнозирования развития острого послеоперационного панкреатита культи поджелудочной железы после панкреатодуоденальной резекции у онкологических больных | 2015 |
|
RU2616183C1 |
| Способ прогнозирования направленности патологического процесса при раке головки поджелудочной железы | 2015 |
|
RU2612082C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ПОСЛЕОПЕРАЦИОННЫХ ОСЛОЖНЕНИЙ ПРИ ПАНКРЕАТОДУОДЕНАЛЬНОЙ РЕЗЕКЦИИ У БОЛЬНЫХ РАКОМ ОРГАНОВ БИЛЛИОПАНКРЕАТОДУОДЕНАЛЬНОЙ ЗОНЫ | 2017 |
|
RU2650984C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ МЕСТНОРАСПРОСТРАНЕННОГО РАКА ЖЕЛУДКА | 2006 |
|
RU2330620C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ОСТРОГО ПОСЛЕОПЕРАЦИОННОГО ПАНКРЕАТИТА У ОНКОЛОГИЧЕСКИХ БОЛЬНЫХ | 2011 |
|
RU2466399C1 |
| СПОСОБ РЕКОНСТРУКЦИИ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА ПОСЛЕ ВЫПОЛНЕНИЯ ПАНКРЕАТОДУОДЕНАЛЬНОЙ РЕЗЕКЦИИ | 1995 |
|
RU2123293C1 |
| СПОСОБ ПАНКРЕАТОГАСТРОАНАСТОМОЗА ПРИ ПРИВРАТНИКОСОХРАНЯЮЩЕЙ ПАНКРЕАТОДУОДЕНАЛЬНОЙ РЕЗЕКЦИИ | 2003 |
|
RU2254816C2 |
| СПОСОБ ПАНКРЕАТОЕЮНОАНАСТОМОЗА ПРИ ПАНКРЕАТОДУОДЕНАЛЬНОЙ РЕЗЕКЦИИ | 1998 |
|
RU2197904C2 |
| Способ формирования погружного кисетного инвагинационного панкреатоеюноанастомоза | 2017 |
|
RU2665972C2 |
Изобретение относится к медицине, а именно к онкологии, и может быть использовано для раннего выявления больных с предрасположенностью к развитию послеоперационных кровотечений из шва анастомоза до панкреатодуоденальной резекции при раке головки поджелудочной железы. Для этого за 3 суток до панкреатодуоденальной резекции в плазме крови больного определяют общую активность трипсиноподобных протеиназ, и при значениях этого показателя от 2642,5 мЕ/мл до 2999,5 мЕ/мл прогнозируют наличие индивидуальной предрасположенности к послеоперационному кровотечению из швов анастомозов, а при значении от 1175,7 мЕ/мл до 1306,3 мЕ/мл прогнозируют течение послегоспитального периода без кровотечения из швов анастомозов. Способ позволяет заранее выявить индивидуальную предрасположенность к кровотечению при его специфичности и своевременном изменении терапевтических схем путем включения в них антикоагулянтов. 1 табл., 2 пр.
Способ прогнозирования предрасположенности к послеоперационному кровотечению при раке головки поджелудочной железы, включающий исследование крови, отличающийся тем, что за 3 дня до панкреатодуоденальной резекции в цитратной плазме крови больного определяют общую активность трипсиноподобных протеиназ и при значениях этого показателя от 2642,5 мЕ/мл до 2999,5 мЕ/мл прогнозируют наличие индивидуальной предрасположенности к послеоперационному кровотечению из швов анастомозов, а при значении от 1175,7 мЕ/мл до 1306,3 мЕ/мл прогнозируют течение послегоспитального периода без кровотечения из швов анастомозов.
| Шатверян Г | |||
| А | |||
| Панкреатодуоденальная резекция в лечении рака головки поджелудочной железы и периампулярной зоны: Дис | |||
| д-ра мед | |||
| наук | |||
| - М., 2006 | |||
| Приспособление для градации давления в воздухопроводе воздушных тормозов | 1921 |
|
SU193A1 |
| СПОСОБ ОДНОВРЕМЕННОЙ ОЦЕНКИ (ДИАГНОСТИКИ) ФУНКЦИИ БИЛИОДИГЕСТИВНЫХ И ГАСТРОЭНТЕРОАНАСТОМОЗОВ У БОЛЬНЫХ, ПЕРЕНЕСШИХ РАДИКАЛЬНЫЕ И ПАЛЛИАТИВНЫЕ ВМЕШАТЕЛЬСТВА ПО ПОВОДУ РАКА ГОЛОВКИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 2014 |
|
RU2536105C1 |
| EP 2933264 A2, 21.10.2015 | |||
| BASSI C | |||
| et al | |||
| Reconstruction by pancreaticojejunostomy versus pancreaticogastrostomy following pancreatectomy: results of comparative study// Ann | |||
| Surg | |||
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
Авторы
Даты
2017-03-15—Публикация
2015-11-23—Подача