Область техники
Изобретение относится к технологии получения микрокапсулированной формы живой культуральной вакцины против гриппа для интраназального применения и может быть использовано в фармацевтической промышленности для производства вакцин и лечебно-профилактических препаратов.
Как известно, наиболее эффективные вакцины - это живые аттенуированные вакцины, создающие иммунитет именно на том участке, где обычно и происходит заражение. В частности, для защиты от гриппа очень важно формирование иммунитета слизистых оболочек носа. Об актуальности такой формы вакцины могут свидетельствовать вспышки гриппа, несмотря на массовую вакцинацию субъединичной адъювантной вакциной.
Предшествующий уровень техники
Известен способ получения микрокапсулированной формы вирусной вакцины, включающий приготовление капсулируемого материала в виде субстанции, например вируса кори, диспергирование ее в водорастворимом заряженном полиэлектролите полифосфазене, получение коацервата для формирования оболочек капсул путем введения в смесь раствора соли одновалентного металла, например раствора хлористого натрия, обработку полученных микрокапсул отвердителем путем дубления их солью мультивалентного иона, например хлористым кальцием, и сушку готовых микрокапсул (US 5807757 C1, 1998).
Недостатком указанного способа является то, что в нем используют такой полиэлектролит, как полифосфазен (материал оболочки), который имеет сложный синтез и на который влияет множество факторов (температура реакции, начальное соотношение реагентов, комплекс растворителей), вследствие чего трудно контролировать степень и регулярность нуклеофильного замещения получаемого полимера. Полиэлектролит с невоспроизводимыми физико-химическими свойствами не обеспечивает получение микрокапсул с заданными характеристиками, например размер и прочность микрокапсул.
Известны способы получения микрокапсул как системы доставки антигена в Пейеровы бляшки размером от 1 до 10 мкм, например, методом получения эмульсии вода-в-масле (J.H. Eldridge, J.K. Staas, J.A. Meulbroek, J.R. McGhee, T.R. Tice and R.M. Gilley. Biodegradable microspheres as a vaccine delivery system. Molecular Immunology, Vol. 28, No. 3, p. 287-294, 1991), (US, C1, 5075109, 1991) или двойной эмульсии вода-в-масле-в-воде (Conwey, В.R., Alpar, H.О., Lewis, D.A. Studies on the optimization of loading and release kinetics of interferon-gamma from polylactide microspheres. Proc. Int. Symp.Contr. Rel. Bioact. Mater. 21: 284-285, 1994).
Недостатками этих способов является сложность технологического процесса и использование органических растворителей, которые в процессе капсулирования вирусных частиц могут инактивировать последние.
Известен метод диспергирования водного раствора анионного полимера, содержащего капсулированное вещество (ротавирусные частицы), в водный раствор связывающего реагента, например диспергирование альгината натрия (отрицательно заряженного полимера) в виде капелек размером 5 мкм в водный раствор спермина гидрохлорида - солей амина (Р.A. Offit, С.A. Khoury, С.A. Moser, H.F. Clark, J.Ε. Kim and T.J. Speaker. Enhancement of Rotavirus Immunogenicity by Microencapsulation. Virology, 203(1), 134-143, 1994). В результате формируются монодисперсные микрокапсулы вирусной вакцины размером от 1 до 10 мкм (преимущественно 2 мкм), которые вызывают у мышей выраженную индукцию гуморального ответа. К недостаткам этого метода можно отнести: а) только 1-6% от общего количества инфекционного вируса включается в матрицу альгинат-спермидиновой микрокапсулы, т.к. при микрокапсулировании в водной среде с применением водорастворимых полимеров в качестве материала оболочек микрокапсул обычно используют капсулируемые вещества, не смешивающиеся или не растворяющиеся в воде, тогда как вирусная суспензия хорошо растворима в воде и вирус легко переходит в среду диспергирования; б) сложность технологического процесса, увеличение расхода вируссодержащей жидкости и необходимость дополнительного оборудования приводит к значительному удорожанию вакцины.
Наиболее близким техническим решением (прототипом) является способ получения микрокапсулированной формы живой культуральной вакцины против гриппа для интраназального применения, включающий культивирование вакцинного штамма вируса гриппа на культуре клеток MDCK в бессывороточной питательной среде, концентрирование и очистку субстанции вируса от балластных белков, одновременное введение в субстанцию отвердителя и водорастворимого заряженного полиэлектролита до конечной концентрации полиэлектролита и отвердителя, не вызывающей разделение фаз в растворе препарата, получение микрокапсул в результате сложной коацервации заряженного полиэлектролита и отвердителя с образованием комплекса путем замораживания раствора со скоростью 0,1-3,0°С в минуту до температуры ниже температуры стеклования аморфной фазы, оставшейся после кристаллизации льда и сушку готовых микрокапсул лиофилизацией (WO 2004/035028, МПК А61К 9/50, опубл. 29.04.2004).
Недостатком указанного способа является то, что получаемые по этому способу микрокапсулы имеют плотную устойчивую оболочку, позволяющую избежать адгезии на эпителии при прохождении желудочно-кишечного тракта, обеспечивают хорошую иммуногенность при пероральном и подкожном введении, но при интраназальной иммунизации вызывают у мышей индукцию гуморального ответа почти в 100 раз меньше, чем при подкожном введении, и меньше, чем при использовании традиционной формы вакцины. Т.е. основным недостатком указанного способа является низкая эффективность при интраназальной иммунизации.
Раскрытие изобретения
Техническим результатом предлагаемого способа является получение живой культуральной гриппозной вакцины в микрокапсулированной форме, обеспечивающей более высокую иммуногенность при интраназальном применении за счет повышения адгезии микрокапсул к слизистой оболочке носа.
Указанный технический результат достигается тем, что в способе получения микрокапсулированной формы живой культуральной вакцины против гриппа для интраназального применения, включающем культивирование вакцинного штамма вируса гриппа на культуре клеток MDCK в бессывороточной питательной среде, концентрирование и очистку субстанции вакцинного вируса от балластных белков, одновременное введение в субстанцию отвердителя и водорастворимого заряженного полиэлектролита до конечной концентрации полиэлектролита и отвердителя, не вызывающей разделение фаз в растворе препарата, получение микрокапсул в результате сложной коацервации заряженного полиэлектролита и отвердителя с образованием комплекса путем замораживания раствора со скоростью 0,1-3,0°С в минуту до температуры ниже температуры стеклования аморфной фазы, оставшейся после кристаллизации льда и сушку готовых микрокапсул лиофилизацией, согласно изобретению субстанцию вакцинного штамма вируса гриппа получают со специфической активностью не менее 7,0 lg ЭИД50/0,5 мл в бессывороточной питательной среде, содержащей протеолитический фермент в количестве 0,25-50,0 мкг/мл и стабилизатор пептон из сои в концентрации (0,5-4) мас. %; в очищенную субстанцию вместе с полиэлектролитом и отвердителем вводят стабилизирующие добавки пептон из сои и сахарозу, в качестве полиэлектролита используют карбопол, а в качестве отвердителя - желатозу при следующем количественном содержании компонентов в полученной жидкой субстанции перед началом микрокапсулирования:
пептон из сои - (0,007-0,015) г/0,5 мл;
сахароза - (0,007-0,015) г/0,5 мл;
желатоза - (0,007-0,015) г/0,5 мл;
карбопол - (0,00005-0,0001) г/0,5 мл;
жидкая питательная среда, содержащая вакцинный штамм вируса гриппа титром не менее 107,0ЭИД50, остальное до 0,5 мл.
Вируссодержащую субстанцию получают путем культивирования одного из холодоадаптированных реассортантов вируса гриппа с посевной дозой, имеющей множественность заражения (0,0001-0,1) ЭИД50/кл в культуре клеток MDCK на микроносителях, имеющих концентрацию 1-20 г/л в бессывороточной питательной среде. В качестве бессывороточной среды используют питательную среду SFM4MegaVir.
Следует отметить, что соотношения между исходными компонентами полимеров выбраны исходя из оптимального выхода коацервата с размером частиц в диапазоне 1,5-2,0 мкм. При совместной коацервации водорастворимого полимера при рН, близких к физиологическому, обеспечивается сохранность живого вируса в процессе микрокапсулирования. Коацервация обусловлена понижением растворимости полимера при понижении температуры и первичной кристаллизации льда, вследствие чего концентрация полимера в маточном растворе (жидкой фазе, оставшейся после первичной кристаллизации льда) увеличивается. Полученный коацерват вместе с равновесной жидкостью подвергается дальнейшему замораживанию и лиофильному высушиванию. Концентрирование (понижение растворимости) полимера проводится за счет первичной кристаллизации льда, а не за счет выпаривания или изменения состава раствора, как правило, добавлением органических растворителей или избыточного полимера, что не вызывает инактивации живого вируса или его существенного разбавления (не более 1-50%). Весь процесс микрокапсулирования заключается в сведении раствора полимера с жидким полуфабрикатом вакцины (вируссодержащая жидкость, стабилизированная частично гидролизованным желатином, сахарозой и пептоном), замораживании полученного раствора с определенной скоростью и лиофилизации.
Ниже приведена характеристика компонентов, используемых для получения микрокапсул:
- карбопол (Carbopol 934, карбомер) для фармацевтических целей, выпускается фирмой Lubrizol, США;
- желатоза - продукт частичного гидролиза желатина;
- пептон из сои является растительным пептоном - продукт гидролиза соевой муки папаином.
Варианты осуществления изобретения
Ниже приведены примеры конкретного выполнения способа получения микрокапсулированной формы живой гриппозной вакцины.
Пример №1. Приготовление вируссодержащего материала для получения живой культуральной гриппозной вакцины
Культуральный сосуд десятилитрового ферментера заполняют бессывороточной питательной средой, например питательной средой SFM4MegaVir. Аттестованную культуру клеток MDCK берут из коллекции культур клеток ГНЦ ВБ «Вектор» и вносят ее в указанный культуральный сосуд из расчета 100-700 тыс. клеток на 1 мл питательной среды. Дополнительно в культуральный сосуд вносят микроноситель Pro-F 102-L в концентрации 1-20 г/л. Осаждение клеток на микроносителе проводят в течение 12 часов при температуре (35-37)°С (объем заполнения культурального сосуда - 25-30%). Режим посадки клеток: 5 мин перемешивание, 10 мин перерыв. Заданные параметры культивирования: частота вращения перемешивающего устройства 50-80 об/мин, аэрация поверхностная со скоростью продува от 0 до 10 л/ч. Водородный показатель рН поддерживают в пределах от 6,9 до 7,2 с помощью дозированной подачи воздуха или углекислого газа. Температура культивирования (35-37)°С. Перфузию питательной среды начинают при концентрации клеток (600-900) тыс./мл. Скорость перфузии зависит от концентрации клеток. Время культивирования клеток (96-144) часов. После наработки клеток удаляют 50% среды, в суспензию вносят вакцинный холодоадаптированный реассортант вируса гриппа, например А/17/Калифорния/2009/38(H1N1) [Ларионова Н.В., Киселева И.В., Александрова Г.И., Руденко Л.Г. Штамм вируса гриппа А/17/Калифорния/2009/38 (H1N1) для производства живой гриппозной интраназальной вакцины для взрослых и детей. Патент РФ №2413765 от 16.09.09. - Опубл. БИ 2011. - №7], с множественностью заражения (0,1-0,0001) ЭИД50/кл., и поддерживающую бессывороточную питательную среду, содержащую протеолитический фермент трипсин в количестве (2,0-20,0) мкг/мл. Далее культивируют вирус при температуре (33±2)°С. При появлении цитопатического действия вируса на клетки (2-5) суток осуществляют 2-3 сбора вируссодержащей жидкости со специфической активностью не менее 7,0 lg ЭИД50/0,5 мл, которую освобождают фильтрованием от клеточного детрита, далее освобождают от балластных примесей методом стерилизующей фильтрации через фильтры с размером пор 0,22 мкм.
Примечание: ЭИД - эмбриональная инфекционная доза.
Пример №2. Приготовление вируссодержащего материала для получения живой культуральной гриппозной вакцины
Культуральный сосуд десятилитрового ферментера заполняют бессывороточной питательной средой, например питательной средой SFM4MegaVir. Аттестованную культуру клеток MDCK берут из коллекции культур клеток ГНЦ ВБ «Вектор» и вносят ее в указанный культуральный сосуд из расчета 100-700 тыс. клеток на мл питательной среды. Дополнительно в культуральный сосуд вносят микроноситель Pro-F 102-L в концентрации (1-20) г/л. Осаждение клеток на микроносителе проводят 12 часов при температуре (35-37)°С (объем заполнения культурального сосуда - 25-30%). Режим посадки клеток: 5 мин перемешивание, 10 мин перерыв. Заданные параметры культивирования: частота вращения перемешивающего устройства 50-80 об/мин, аэрация поверхностная со скоростью продува от 0 до 10 л/ч. Водородный показатель рН поддерживают в пределах от 6,9 до 7,2 с помощью дозированной подачи 7,5%-ного раствора углекислого натрия. Температура культивирования (35-37)°С. Перфузию питательной среды начинают при концентрации клеток 600-900 тыс./мл. Скорость перфузии зависит от концентрации клеток. Время культивирования клеток - 96-144 часов. После наработки клеток удаляют 50% среды, в суспензию вносят один из вакцинных холодоадаптированных реассортантов вируса гриппа (А/17/Виктория/2011/89(H3N2) [Ларионова Н.В., Дубровина И.А., Киселева И.В., Баженова Е.А., Александрова Г.И., Руденко Л.Г. Вакцинный штамм вируса гриппа А/17/Виктория/2011/89 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и детей. Патент РФ №2532844 от 17.07.2012. Опубл. 27.01.14. Бюл. №3] или А/17/Швейцария/2013/1 (H3N2) или В/60/Висконсин/2010/125 [Баженова Е.А., Ларионова Н.В., Киселева И.В., Дубровина И.А., Руденко Л.Г., Александрова Г.И. Вакцинный штамм вируса гриппа В/60/Висконсин/2010/125. Патент РФ №2545695. Опубл. 10.04.2015. Бюл. №10] или В/60/Пхукет/2013/26 или А/17/Боливия/2013/6585 (H1N1)pdm09) с множественностью заражения (0,1-0,0001) ЭИД50/кл., поддерживающую бессывороточную питательную среду, содержащую протеолитический фермент трипсин в количестве (2,0-20,0) мкг/мл, и пептон из сои в концентрации (0,5-3) %. Далее культивируют вирус при температуре (34±1)°С. При появлении цитопатического действия вируса на клетки (2-5 суток) осуществляют 2-3 сбора вируссодержащей жидкости со специфической активностью не менее 7,0 lg ЭИД50/мл, которую освобождают фильтрованием от клеточного детрита, далее освобождают от балластных примесей методом стерилизующей фильтрации через фильтры с размером пор 0,22 мкм.
Пример №3. Получение микрокапсулированной формы живой гриппозной вакцины
К стерильному вируссодержащему материалу со специфической активностью не менее 7,0 lg ЭИД50/0,5 мл при непрерывном перемешивании добавляют стерильные водные растворы 25%-ной желатозы (мол. вес 3000), 0,3%-ного раствора карбопола, 25%-ного раствора пептона, 50%-ного раствора сахарозы в таком объеме, чтобы конечное содержание компонентов было следующим:
Вакцинный штамм вирус гриппа не менее 107,0 ЭИД50/0,5 мл;
пептон - (0,011±0,004) г/0,5 мл;
сахароза - (0,011±0,004) г/0,5 мл;
желатин - (0,011±0,004) г/0,5 мл;
карбомер - (0,00025±0,00005) г/0,5 мл;
жидкая питательная среда, содержащая вакцинный штамм вируса гриппа с титром не менее 107,0 ЭИД50, остальное до 0,5 мл.
Полученную жидкую форму вакцины разливают в ампулы по 0,5 мл в каждую и замораживают при температуре минус 60°С в течение 18 часов. Продукт лиофильно высушивают в течение 48 часов в стерильных условиях. После окончания сушки ампулы заполняют инертным газом (аргоном) и запаивают.
Пример №4. Определение специфической активности живой гриппозной культуральной вакцины
Специфическую активность живой гриппозной культуральной вакцины определяют путем титрования на куриных эмбрионах по методике, изложенной в Методических указаниях «Методы контроля медицинских иммунобиологических препаратов, вводимых людям». МУК 4.1/4.2.588-96. Специфическая активность вакцины после лиофилизации составляет не менее 7,0 lg ЭИД50/доза.
Пример №5. Определение размера микрокапсул методом атомно-силовой микроскопии
Для атомно-силовой микроскопии лиофилизированный препарат растворяют в дистиллированной воде, далее каплю препарата наносят на поверхность предметного стекла. После высушивания водорастворимые компоненты удаляют промывкой и исследуют препарат с помощью атомно-силового микроскопа Solver P47BIO (NT-MDT, Россия) в полуконтактном режиме.
На фиг. 1 представлена атомно-силовая микроскопия микрокапсулированной формы живой гриппозной культуральной вакцины, размер 10×10 мкм.
На изображении (фиг. 1) представлены овальные структуры микрокапсул размерами 1,5-2 мкм.
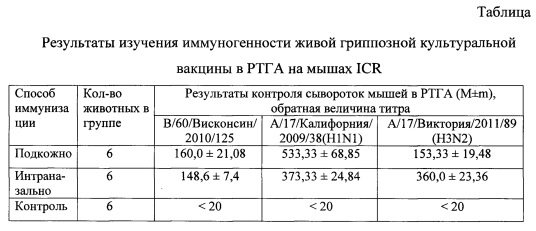
Пример №6. Исследование иммуногенности живой культуральной гриппозной вакцины на лабораторных животных
Контроль иммуногенности препаратов осуществляют на белых мышах стока ICR следующим образом: содержимое ампулы с вакциной растворяют в 0,5 мл дистиллированной воды и вводят интраназально 6-10 животным по 50 мкл в каждую ноздрю. Забор крови проводят через 21 день. Кровь исследуют на наличие антител в реакции торможения гемагглютинации (РТГА). В качестве контроля используют гриппозную вакцину для инъекционного применения. Как видно из представленных в таблице результатов, микрокапсулированная форма живой гриппозной культуральной вакцины вызывает у мышей выраженную индукцию гуморального ответа.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЖИВОЙ КУЛЬТУРАЛЬНОЙ ВАКЦИНЫ ПРОТИВ ВИРУСА ГРИППА | 2009 |
|
RU2420314C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЖИВОЙ КУЛЬТУРАЛЬНОЙ ВАКЦИНЫ ПРОТИВ ВИРУСА ГРИППА | 2003 |
|
RU2330885C2 |
| СПОСОБ ПОЛУЧЕНИЯ МИКРОКАПСУЛИРОВАННОЙ ФОРМЫ КОРЕВОЙ ВАКЦИНЫ ДЛЯ ПЕРОРАЛЬНОГО ПРИМЕНЕНИЯ | 2001 |
|
RU2210361C2 |
| СПОСОБ ПОЛУЧЕНИЯ СУБСТАНЦИИ РЕКОМБИНАНТНОГО ЭРИТРОПОЭТИНА ЧЕЛОВЕКА И НАНОКАПСУЛИРОВАННАЯ ФОРМА РЕКОМБИНАНТНОГО ЭРИТРОПОЭТИНА ЧЕЛОВЕКА С ИСПОЛЬЗОВАНИЕМ СУБСТАНЦИИ, ПОЛУЧЕННОЙ УКАЗАННЫМ СПОСОБОМ | 2012 |
|
RU2518329C1 |
| Бессывороточная питательная среда для культивирования клеток MDCK или Vero или вакцинных штаммов вирусов кори или гриппа | 2018 |
|
RU2703826C1 |
| Вакцинный штамм вируса гриппа А/17/Южная Африка/2013/01 (H1N1)pdm09 для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2016 |
|
RU2627188C1 |
| ШТАММ ВИРУСА ГРИППА В/60/Пхукет/2013/26 ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЛЯ ДЕТЕЙ | 2015 |
|
RU2605926C1 |
| Вакцинный штамм вируса гриппа А/17/Швейцария/2017/51 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2019 |
|
RU2715674C1 |
| Рекомбинантный вакцинный штамм для живой интраназальной вакцины, обеспечивающей сочетанную профилактику гриппозной и коронавирусной инфекций | 2022 |
|
RU2782531C1 |
| Вакцинный штамм вируса гриппа А/17/КАНЗАС/2017/631 (H3N2) для производства живой гриппозной интраназальной вакцины для взрослых и для детей | 2019 |
|
RU2732610C1 |

Изобретение относится к медицине, а именно к биотехнологии и иммунологии, и может быть использовано для получения микрокапсулированной формы живой гриппозной культуральной вакцины против гриппа для интраназального применения. Способ включает получение субстанции вируса гриппа, одновременное введение в вируссодержащую субстанцию отвердителя и водорастворимого заряженного полиэлектролита до конечной концентрации полиэлектролита и отвердителя, не вызывающей разделение фаз в растворе препарата. Дальнейшее получение микрокапсул проводят в результате сложной коацервации заряженного полиэлектролита и отвердителя с образованием комплекса путем замораживания раствора со скоростью 0,1-3,0°C в минуту до температуры ниже температуры стеклования аморфной фазы, оставшейся после кристаллизации льда, и сушки готовых микрокапсул лиофилизацией. Субстанцию вируса гриппа получают со специфической активностью не менее 7,0 lg ЭИД50/0,5 мл в бессывороточной питательной среде, содержащей протеолитический фермент в количестве 0,25-50,0 мкг/мл и стабилизатор пептон из сои в концентрации (0,5-4,0) мас. %. В очищенную субстанцию вместе с полиэлектролитом и отвердителем вводят стабилизирующие добавки пептон из сои и сахарозу, в качестве полиэлектролита используют карбопол, а в качестве отвердителя - желатозу, при следующем количественном содержании компонентов в полученной жидкой субстанции перед началом микрокапсулирования: пептон из сои - (0,007-0,015) г/0,5 мл; сахароза - (0,007-0,015) г/0,5 мл; желатоза - (0,007-0,015) г/0,5 мл; карбопол - (0,00005-0,0001) г/0,5 мл; жидкая питательная среда, содержащая вирус гриппа с титром не менее 107,0 ЭИД50, остальное до 0,5 мл. Использование данного способа получения живой культуральной гриппозной вакцины в микрокапсулах обеспечивает более высокую иммуногенность при интраназальном применении за счет повышения адгезии микрокапсул к слизистой оболочке носа. 2 з.п. ф-лы, 6 пр., 1 табл., 1 ил.
1. Способ получения микрокапсулированной формы живой гриппозной культуральной вакцины против гриппа для интраназального применения, включающий получение субстанции вируса гриппа, одновременное введение в вируссодержащую субстанцию отвердителя и водорастворимого заряженного полиэлектролита до конечной концентрации полиэлектролита и отвердителя, не вызывающей разделение фаз в растворе препарата, получение микрокапсул в результате сложной коацервации заряженного полиэлектролита и отвердителя с образованием комплекса путем замораживания раствора со скоростью 0,1-3,0°C в минуту до температуры ниже температуры стеклования аморфной фазы, оставшейся после кристаллизации льда, и сушку готовых микрокапсул лиофилизацией, отличающийся тем, что субстанцию вируса гриппа получают со специфической активностью не менее 7,0 lg ЭИД50/0,5 мл в бессывороточной питательной среде, содержащей протеолитический фермент в количестве 0,25-50,0 мкг/мл и стабилизатор пептон из сои в концентрации (0,5-4,0) мас. %; в очищенную субстанцию вместе с полиэлектролитом и отвердителем вводят стабилизирующие добавки пептон из сои и сахарозу, в качестве полиэлектролита используют карбопол, а в качестве отвердителя - желатозу при следующем количественном содержании компонентов в полученной жидкой субстанции перед началом микрокапсулирования:
пептон из сои - (0,007-0,015) г/0,5 мл;
сахароза - (0,007-0,015) г/0,5 мл;
желатоза - (0,007-0,015) г/0,5 мл;
карбопол - (0,00005-0,0001) г/0,5 мл;
жидкая питательная среда, содержащая вирус гриппа
с титром не менее 107,0 ЭИД50, остальное до 0,5 мл.
2. Способ по п. 1, отличающийся тем, что вируссодержащую субстанцию получают путем культивирования одного из холодоадаптированных реассортантов вируса гриппа с посевной дозой, имеющей множественность заражения (0,0001-0,1) ЭИД50/кл. в культуре клеток MDCK на микроносителях, имеющих концентрацию 1-20 г/л в бессывороточной питательной среде с последующим концентрированием и очисткой субстанции вируса от балластных белков.
3. Способ по п. 1, отличающийся тем, что в качестве бессывороточной среды используют питательную среду SFM4MegaVir.
| WO 2004035028 A1, 29.04.2004 | |||
| СПОСОБ ПОЛУЧЕНИЯ ЖИВОЙ КУЛЬТУРАЛЬНОЙ ВАКЦИНЫ ПРОТИВ ВИРУСА ГРИППА | 2009 |
|
RU2420314C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЖИВОЙ КУЛЬТУРАЛЬНОЙ ВАКЦИНЫ ПРОТИВ ВИРУСА ГРИППА | 2003 |
|
RU2330885C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЖИВОЙ ВАКЦИНЫ ДЛЯ ПРОФИЛАКТИКИ ГРИППА | 2005 |
|
RU2290205C1 |
| NECHAEVA et al | |||
| Development of live cultural pandemic influenza vaccine Vector-Flu // BMC Proceedings, 2011, 5(Suppl 8):P104. | |||
Авторы
Даты
2017-04-19—Публикация
2016-05-04—Подача