РОДСТВЕННЫЕ ЗАЯВКИ НА ПАТЕНТ
Эта заявка испрашивает приоритет на основании заявки на патент Индии № 715/MUM/2013, поданной 8 марта 2013 г., раскрытие которой включено в данный документ посредством ссылки в полном ее объеме, как если бы была полностью включена в данный документ. Все ссылочные материалы, включая патенты, заявки на патенты и литературу, приведенную в описании изобретения, явным образом полностью включены в данный документ посредством ссылок.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Изобретение относится к способу получения (2S,5R)-моно-{[(4-аминопиперидин-4-ил)карбонил]-7-оксо-1,6-диазабицикло[3.2.1]окт-6-ил}ового сложного эфира серной кислоты.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
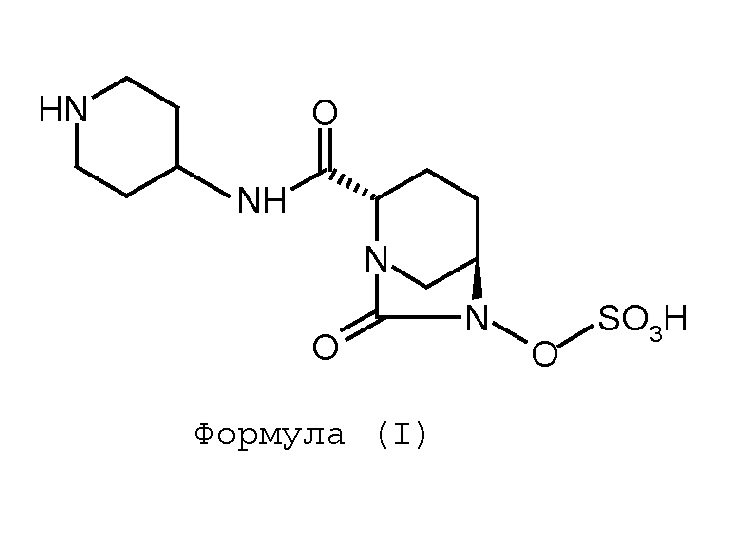
Соединение Формулы (I), имеющее химическое название (2S,5R)-моно-{[(4-аминопиперидин-4-ил)карбонил]-7-оксо-1,6-диазабицикло[3.2.1]окт-6-ил}овый сложный эфир серной кислоты, обладает антибактериальными свойствами. Соединение Формулы (I) также известно как МК-7655 и раскрыто в международной заявке на патент согласно PCT № PCT/US2009/031047.
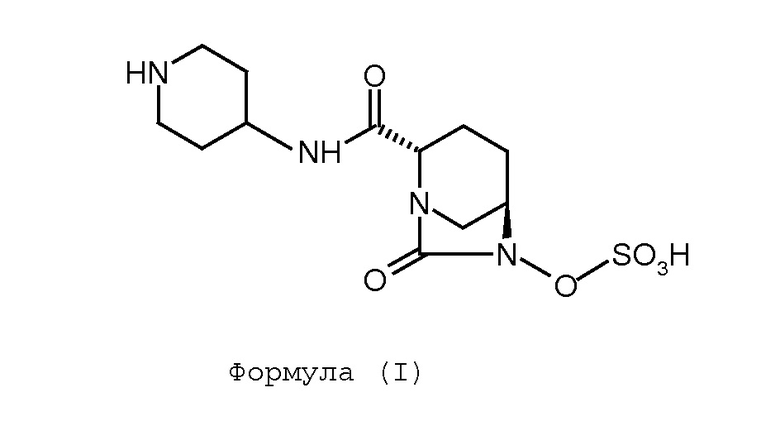
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В одном общем аспекте предоставляют способ получения соединения Формулы (I), включающий:

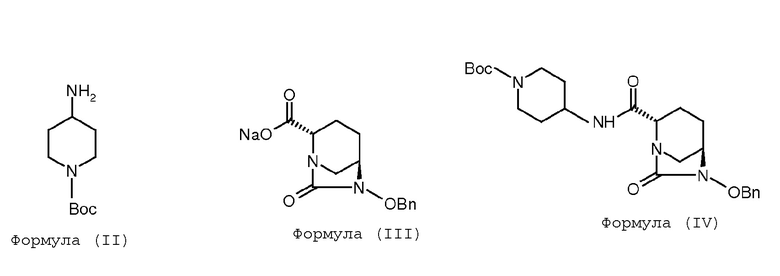
(а) проведение реакции между соединением Формулы (II) и соединением Формулы (III) с получением соединения Формулы (IV);
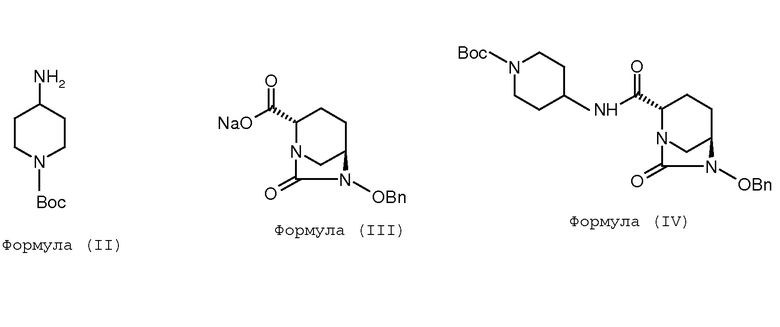
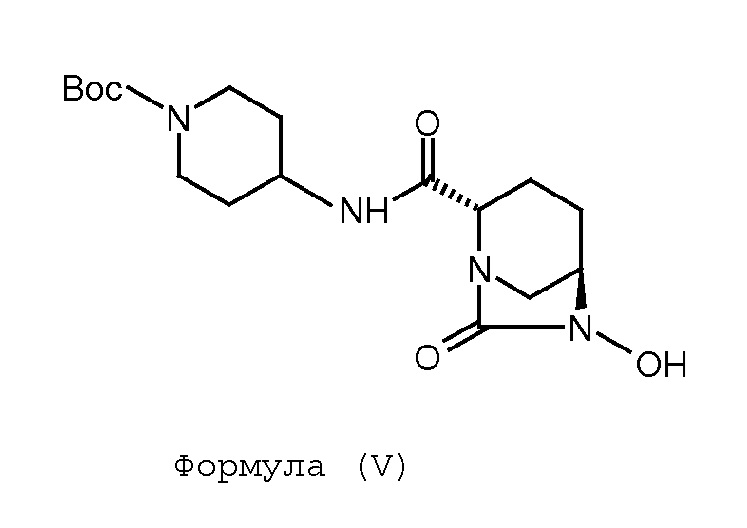
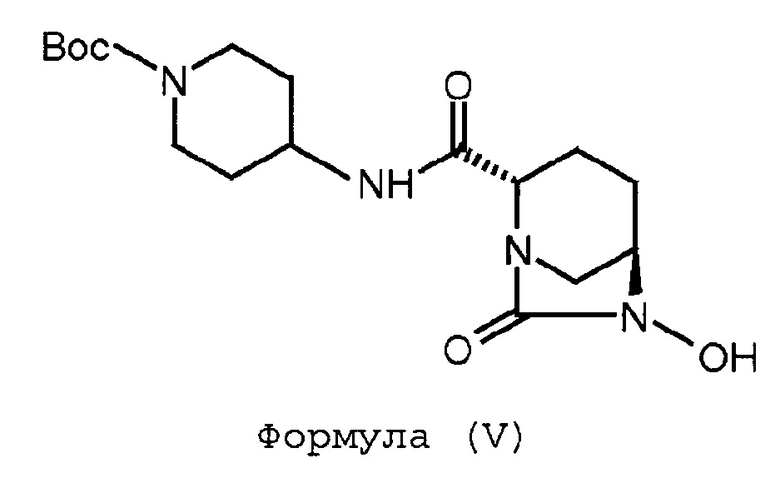
(b) гидрогенолиз соединения Формулы (IV) с получением соединения Формулы (V);

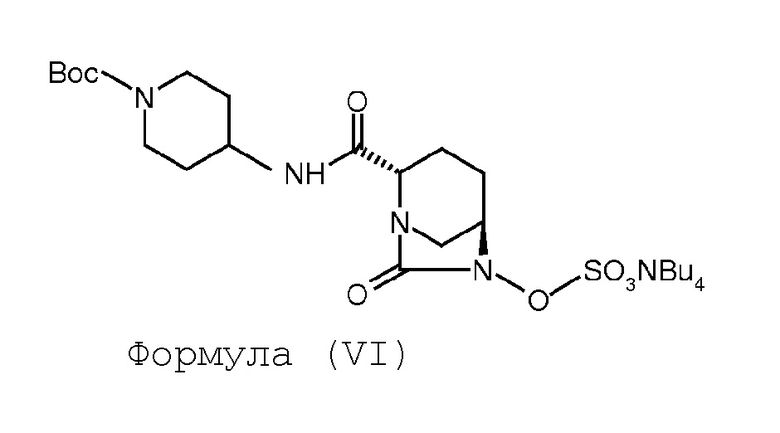
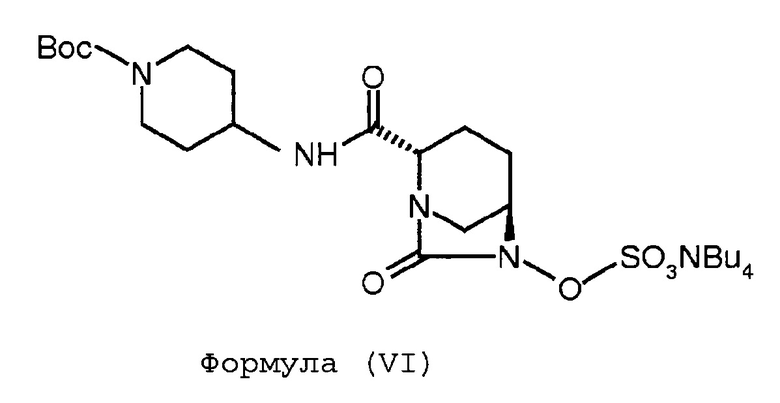
(с) сульфонирование соединения Формулы (V) с получением соединения Формулы (VI);
и

(d) превращение соединения Формулы (VI) в соединение Формулы (I).
Подробности одного или более вариантов осуществления изобретения изложены в описании изобретения ниже. Другие признаки, цели и преимущества изобретения будут очевидны из приведенного ниже описания изобретения, в том числе из формулы изобретения.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Далее будет сделана ссылка на примеры осуществления изобретения, и для описания такового в данном документе будет использован особый язык. Тем не менее, следует понимать, что ограничение объема изобретения в результате этого не предполагается. Следует полагать, что изменения и дополнительные модификации признаков изобретения, проиллюстрированных в данном документе, и дополнительные применения принципов изобретения, проиллюстрированных в данном документе, которые мог бы придумать специалист в релевантной области, обладающий таким раскрытием, попадают в рамки объема изобретения. Следует отметить, что используемые в этом описании изобретения и в прилагаемых пунктах формулы формы единственного числа включают соотносимые объекты во множественном числе, если содержание ясно не диктует иное. Все ссылки, включая патенты, заявки на патенты и литературу, приведенную в описании изобретения, явным образом включены в данный документ посредством ссылки в полном их объеме, как если бы они были полностью переписаны в данный документ.
Термин "HOBt", используемый в данном документе, относится к 1-гидроксибензотриазолу.
Термин "EDC", используемый в данном документе, относится к 1-этил-3-(3-диметиламинопропил)карбодиимиду.
В одном общем аспекте предоставляют способ получения соединения Формулы (I), включающий:
(а) проведение реакции между соединением Формулы (II) и соединением Формулы (III) с получением соединения Формулы (IV);
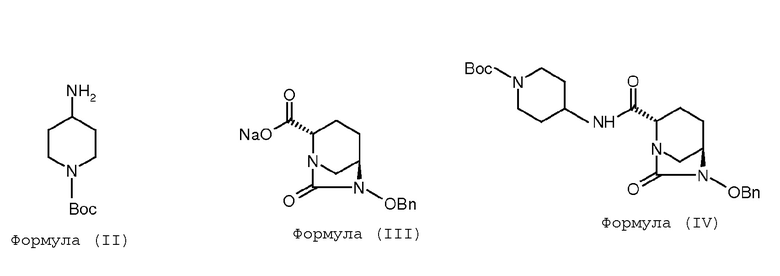
(b) гидрогенолиз соединения Формулы (IV) с получением соединения Формулы (V);
(с) сульфонирование соединения Формулы (V) с получением соединения Формулы (VI);
и
(d) превращение соединения Формулы (VI) в соединение Формулы (I).
Соединение Формулы (IV) получают путем проведения реакции между соединением Формулы (II) и соединением Формулы (III). В некоторых вариантах осуществления соединение Формулы (IV) получают в результате проведения реакции между соединением Формулы (II) и соединением Формулы (III) в присутствии подходящего связывающего агента. В некоторых других вариантах осуществления соединение Формулы (IV) получают в результате проведения реакции между соединением Формулы (II) и соединением Формулы (III) в присутствии 1-гидроксибензотриазола и гидрохлорида 1-этил-3-(3-диметиламинопропил)карбодиимида. Эта реакция может быть проведена в присутствии подходящего растворителя. В некоторых вариантах осуществления реакцию проводят в воде, взятой в качестве реакционного растворителя.
Соединение Формулы (V) получают путем гидрогенолиза соединения Формулы (IV). Реакция гидрогенолиза может быть проведена с использованием подходящего агента гидрогенолиза. В некоторых вариантах осуществления гидрогенолиз соединения Формулы (IV) с получением соединения Формулы (V) проводят в присутствии катализатора на основе переходного металла и источника водорода. В некоторых других вариантах осуществления катализатор на основе переходного металла представляет собой палладий на углеродном носителе, а источник водорода представляет собой газ водород. В некоторых других вариантах осуществления реакцию гидрогенолиза проводят в присутствии подходящего растворителя, такого как, например, метанол. В некоторых вариантах осуществления гидрогенолиз соединения Формулы (IV) с получением соединения Формулы (V) проводят с использованием катализатора на основе 10% палладия на углеродном носителе, в присутствии газа водорода, в метаноле, взятом в качестве растворителя.
Соединение Формулы (VI) получают путем сульфонирования соединения Формулы (V). Реакция сульфонирования может быть проведена в присутствии подходящего растворителя. В некоторых вариантах осуществления сульфонирование соединения Формулы (V) с получением соединения Формулы (VI) выполняют путем проведения реакции между соединением Формулы (V) и комплексом триоксид серы-пиридин, с последующей обработкой посредством гидросульфата тетрабутиламмония.
Соединение Формулы (VI) превращают в соединение Формулы (I) в присутствии подходящего реагента. В некоторых вариантах осуществления соединение Формулы (VI) превращают в соединение Формулы (I) путем проведения реакции между соединением Формулы (VI) и трифторуксусной кислотой.
В некоторых вариантах осуществления соединение Формулы (I) приготавливают с использованием способа, описанного на Схеме 1.
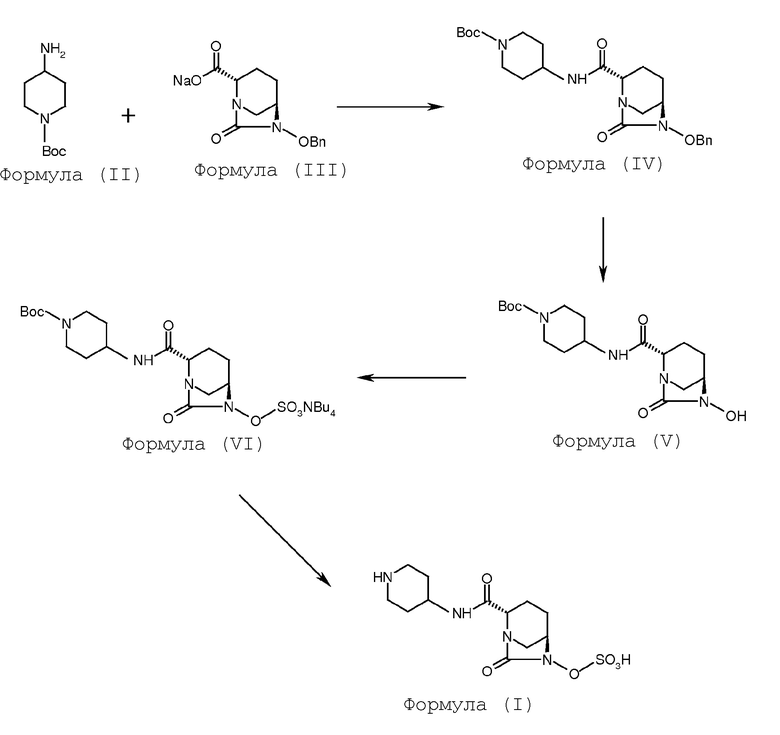
Схема-1
Для специалиста в данной области будет совершенно очевидно, что в изобретении, раскрытом в данном документе, могут быть сделаны различные замены и модификации без отступления от объема и существа изобретения. Например, специалистам в данной области будет ясно, что изобретение может быть использовано на практике с применением целого ряда различных соединений в рамках рассматриваемых общих описаний.
ПРИМЕРЫ
Следующие примеры иллюстрируют варианты осуществления изобретения, которые в настоящее время являются наиболее известными. Однако следует понимать, что следующее является только примером или иллюстрацией применения принципов настоящего изобретения. Многочисленные модификации и альтернативные композиции, способы и системы могут быть разработаны специалистами в данной области без отступления от существа и объема настоящего изобретения. Прилагаемая формула изобретения, как подразумевается, охватывает такие модификации и расстановки. Таким образом, тогда как настоящее изобретение было выше описано с использованием характерных особенностей, приведенные ниже примеры предоставляют дополнительные подробности, касающиеся, как в настоящее время считается, наиболее используемых на практике и наиболее предпочтительных вариантов осуществления изобретения.
Пример-1
Получение (2S,5R)-моно-{2-[N'-(4-аминопиперидинил)карбонил]-7-оксо-1,6-диазабицикло[3.2.1]окт-6-ил}ового сложного эфира серной кислоты (I).
Стадия-1: Получение (2S,5R)-трет-бутил{(6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]окт-2-илкарбонил)амино}пиперидин-1-карбоксилата (IV):
В 250-миллилитровую круглодонную колбу, оснащенную магнитной мешалкой, загружают раствор (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]октан-2-карбоксилата натрия (11,1 г, 0,037 моль, полученного с применением способа, раскрытого в заявке на патент Индии № 699/MUM/2013), в воде (180 мл), после этого последовательно вводят 1-трет-бутоксикарбонил-4-аминопиперидин (7,8 г, 0,039 моль), EDC гидрохлорид (11 г, 0,055 моль) и 1-гидроксибензотриазол (4,8 г, 0,037 моль) при 30°С при перемешивании. Реакционную смесь перемешивают в течение 24 часов при 30°С с получением суспензии. Полученную суспензию фильтруют при отсасывании под вакуумом и промывают водой, имеющей температуру 45°С, (40 мл) с получением (2S,5R)-трет-бутил{(6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]окт-2-илкарбонил)амино}пиперидин-1-карбоксилата в количестве 12,7 грамм с выходом 74% после проведения сушки под вакуумом.
Анализ:
ЯМР: (CDCl3) = 7,36-7,44 (м, 5Н), 6,56 (д, 1Н), 5,06 (д, 1Н), 4,91 (д, 1Н), 4,03 (шир.с, 1Н), 3,88-3,97 (м, 2Н), 3,29 (с, 1Н), 3,00 (д, 1Н), 2,86 (т, 2Н), 2,64 (д, 1Н), 2,37 (дд, 1Н), 1,85-2,01 (м, 4Н), 1,54-1,62 (м, 2Н), 1,45 (с,9Н), 1,25-1,36 (м, 2Н).
Масс-спектрометрия (ионизация электрораспылением + (ES+)) С24Н34N4O5 = 459,5 (М+1).
Стадия-2: Получение (2S,5R)-трет-бутил{(6-гидрокси-7-оксо-1,6-диазабицикло[3.2.1]окт-2-илкарбонил)амино}пиперидин-1-карбоксилата (V):
В 100-миллилитровую одногорлую круглодонную колбу, оснащенную магнитной мешалкой, загружают раствор (2S, 5R)-трет-бутил{(6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]окт-2-илкарбонил)амино}пиперидин-1-карбоксилата (9 г, 19,5 ммоль) в метаноле (90 мл), после этого добавляют 10% палладий на углеродном носителе (2,7 г) при 35°С. Реакционную смесь перемешивают при давлении водорода 1 атмосфера при 35°С в течение 2 часов. Катализатор удаляют в результате фильтрования реакционной смеси при отсасывании под вакуумом через слой целлита. Слой целлита промывают дихлорметаном (50 мл). Объединенный фильтрат упаривают под вакуумом при температуре ниже 35°С с получением (2S,5R)-трет-бутил{(6-гидрокси-7-оксо-1,6-диазабицикло[3.2.1]окт-2-илкарбонил)амино}пиперидин-1-карбоксилата в количестве 8,45 грамм; его используют без дополнительной очистки в следующей реакции.
Анализ:
ЯМР: (CDCl3) = 6,60 (д, 1Н), 3,88-4,10 (м, 4Н), 3,78 (с, 1Н), 3,20 (д, 1Н), 3,90 (т, 2Н), 2,80 (д, 1Н), 2,46 (дд, 1Н), 2,1-2,2 (м, 1Н), 2,85-2,20 (м, 4Н), 1,70-1,80 (м, 1Н), 2,47 (с, 9Н), 1,30-1,41 (м, 3Н).
Масс-спектрометрия (ионизация электрораспылением + (ES+)) С17Н28N4O5 = 369,4 (М+1).
Стадия-3: Получение Тетрабутиламмониевой соли (2S,5R)-трет-бутил{(6-сульфоокси-7-оксо-1,6-диазабицикло[3.2.1]окт-2-илкарбонил)амино}пиперидин-1-карбоксилата (VI):
В 100-миллилитровую одногорлую круглодонную колбу, оснащенную магнитной мешалкой, загружают раствор (2S,5R)-трет-бутил{(6-гидрокси-7-оксо-1,6-диазабицикло[3.2.1]окт-2-илкарбонил)амино}пиперидин-1-карбоксилата (6,40 г, 7,6 ммоль) в дихлорметане (90 мл), триэтиламин (9,3 мл), после этого добавляют комплекс пиридин-триоксид серы (5,4 г, 34,2 ммоль) при 35°С при перемешивании. Реакционную смесь перемешивают в течение дополнительных 4 часов при 35°С. Растворитель выпаривают под вакуумом при температуре ниже 40°С с предоставлением остатка. Остаток перемешивают с 0,5N-ным водным раствором дигидрофосфата калия (90 мл) в течение 1 часа. Получающийся в результате раствор экстрагируют дихлорметаном (2×100 мл) с удалением примесей. К водному слою добавляют гидросульфат тетрабутиламмония (6,9 г, 20,52 ммоль) и реакционную смесь перемешивают в течение 14 часов при 35°С. Ее экстрагируют дихлорметаном (3×30 мл). Объединенный органический слой сушат над сульфатом натрия и упаривают под вакуумом с получением тетрабутиламмониевой соли (2S,5R)-трет-бутил{(6-сульфоокси-7-оксо-1,6-диазабицикло[3.2.1]окт-2-илкарбонил)амино}пиперидин-1-карбоксилата в количестве 8,0 г с выходом 62%.
Анализ:
ЯМР: (CDCl3): 6,64 (д, 1Н), 4,36 (шир.с, 1Н), 4,05 (шир.с, 2Н), 3,90-4,00 (м, 1Н), 3,87 (д, 1Н), 2,28-3,34 (м, 10Н), 3,80-3,95 (м, 2Н), 3,74 (д, 1Н), 2,42 (дд, 1Н), 2,15-2,24 (м, 1Н), 1,82-1,97 (м, 4Н), 1,61-1,74 (м, 14Н), 1,41-1,52 (м, 10Н), 1,02 (т, 12Н).
Масс-спектрометрия (ионизация электрораспылением - (ES-)) С17Н27N4O8S.N(C4H9)4 = 447,4 (М-1) в форме свободной сульфоновой кислоты.
Стадия-4: Синтез (2S,5R)-моно-{[(4-аминопиперидин-4-ил)карбонил]-7-оксо-1,6-диазабицикло[3.2.1]окт-6-ил}ового сложного эфира серной кислоты (I):
В 100-миллилитровую круглодонную колбу, оснащенную магнитной мешалкой, загружают раствор тетрабутиламмониевой соли (2S,5R)-трет-бутил{(6-сульфоокси-7-оксо-1,6-диазабицикло[3.2.1]окт-2-илкарбонил)амино}пиперидин-1-карбоксилата (6,0 г) в дихлорметане (15 мл). Раствор охлаждают до -10°С при перемешивании и к нему добавляют по каплям трифторуксусную кислоту (15 мл). Реакционную смесь перемешивают при -10°С в течение 1 часа. Растворители выпаривают под вакуумом при температуре ниже 30°С до объема, соответствующего 1/3 его исходного объема, с предоставлением густого остатка. Густой остаток перемешивают дважды с диэтиловым эфиром (60 мл каждый раз) с получением осадка. Полученное твердое вещество отфильтровывают при отсасывании под вакуумом и суспендируют в ацетоне (90 мл). К суспензии добавляют 10%-ный раствор натрий-2-этилгексаноата в ацетоне для корректировки рН с доведением его значения до 4,5-5,5. Суспензию перемешивают в течение 10 минут и фильтруют при отсасывании под вакуумом. Влажный фильтрационный осадок промывают ацетоном и сушат под вакуумом при температуре ниже 40°С с получением 3 грамм сырого соединения. Сырое соединение перемешивают с водным изопропанолом (3 мл воды: 21 мл изопропанола) в течение ночи для дополнительной очистки. Получающуюся в результате суспензию фильтруют при отсасывании под вакуумом и промывают водным изопропанолом (IPA) (смесь 1 мл воды: 7 мл IPA). В конце фильтрационный осадок сушат под вакуумом при температуре ниже 40°С с получением указанного в заголовке соединения в виде твердого вещества грязно-белого цвета в количестве 1,8 г с выходом 65%.
Анализ:
Н1-ЯМР: (DMSO-d6, обмен с D2O) = 8,19 (д, обмен с D2O), 3,99 (с, 1Н), 3,82-3,92 (м, 1Н), 3,72 (д, 1Н), 2,24 (шир.д, 3Н), 2,90-3,04 (м, 5Н), 1,96-2,06 (м, 1Н), 1,80-1,94 (м, 3Н), 1,58-1,72 (м, 4Н).
Масс-спектрометрия (ионизация электрораспылением + (ES+)) С12Н20N4O6S = 349,2 (М+1) в форме свободной сульфоновой кислоты.
Чистота по методу высокоэффективной жидкостной хроматографии (HPLC): 99,2%.
Удельное вращение: [α]25D = -45,25° (около 0,3%, вода).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ (2S,5R)-7-ОКСО-6-СУЛЬФООКСИ-2-[((3R)-ПИПЕРИДИН-3-КАРБОНИЛ)-ГИДРАЗИНОКАРБОНИЛ]-1,6-ДИАЗАБИЦИКЛО[3.2.1]ОКТАНА | 2013 |
|
RU2627700C2 |
| СПОСОБ ПОЛУЧЕНИЯ (2S,5R)-7-ОКСО-6-СУЛЬФООКСИ-2-[((3R)-ПИРРОЛИДИН-3-КАРБОНИЛ)ГИДРАЗИНОКАРБОНИЛ]-1,6-ДИАЗАБИЦИКЛО[3.2.1]ОКТАНА | 2013 |
|
RU2625304C2 |
| СПОСОБ ПОЛУЧЕНИЯ НАТРИЕВОЙ СОЛИ (2S,5R)-2-КАРБОКСАМИДО-7-ОКСО-6-СУЛЬФООКСИ-1,6-ДИАЗАБИЦИКЛО[3.2.1]ОКТАНА | 2013 |
|
RU2632192C2 |
| НОВЫЙ ИНГИБИТОР бета-ЛАКТАМАЗЫ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2693898C2 |
| НОВЫЙ ИНГИБИТОР β-ЛАКТАМАЗЫ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2019 |
|
RU2800050C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОМЕЖУТОЧНОГО СОЕДИНЕНИЯ ДЛЯ ПОЛУЧЕНИЯ АВИБАКТАМА | 2018 |
|
RU2722625C1 |
| КРИСТАЛЛИЧЕСКИЕ ФОРМЫ ПРОИЗВОДНОГО ДИАЗАБИЦИКЛООКТАНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2014 |
|
RU2801220C2 |
| КРИСТАЛЛИЧЕСКИЕ ФОРМЫ ПРОИЗВОДНОГО ДИАЗАБИЦИКЛООКТАНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2014 |
|
RU2695219C2 |
| ИНГИБИТОРЫ БЕТА-ЛАКТАМАЗ | 2009 |
|
RU2445314C9 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ, ВКЛЮЧАЯ ТРАНС-7-ОКСО-6-(СУЛЬФОКСИ)-1,6-ДИАЗАБИЦИКЛО[3.2.1]ОКТАН-2-КАРБОКСАМИД И ЕГО СОЛИ | 2012 |
|
RU2769076C2 |
Изобретение относится к области органической химии, а именно к способу получения соединения Формулы (I), включающему: (а) проведение реакции между соединением Формулы (II) и соединением Формулы (III) в присутствии воды, взятой в качестве растворителя, с получением соединения Формулы (IV); (b) гидрогенолиз соединения Формулы (IV) с получением соединения Формулы (V); (с) сульфонирование соединения Формулы (V) с получением соединения Формулы (VI); и (d) превращение соединения Формулы (VI) в соединение Формулы (I). Технический результат: разработан простой способ получения соединения Формулы (I), полезного в качестве антибактериального агента. 5 з.п. ф-лы, 1 пр.
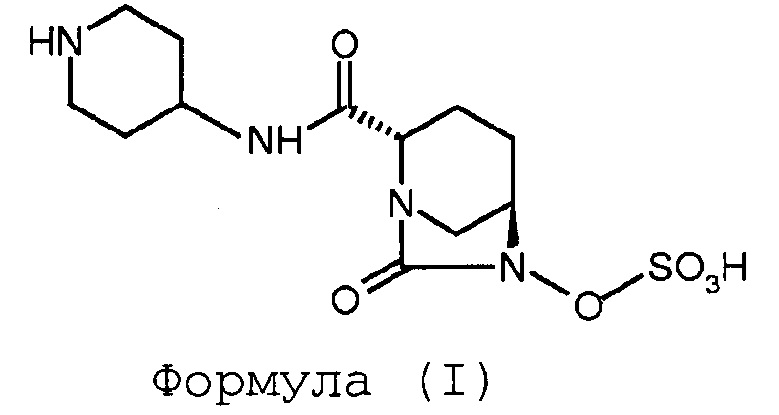

1. Способ получения соединения Формулы (I), включающий:

(а) проведение реакции между соединением Формулы (II) и соединением Формулы (III) в присутствии воды, взятой в качестве растворителя, с получением соединения Формулы (IV);

(b) гидрогенолиз соединения Формулы (IV) с получением соединения Формулы (V);

(с) сульфонирование соединения Формулы (V) с получением соединения Формулы (VI);
и
(d) превращение соединения Формулы (VI) в соединение Формулы (I).
2. Способ по п.1, где соединение Формулы (IV) получают путем проведения реакции между соединением Формулы (II) и соединением Формулы (III) в присутствии 1-этил-3-(3-диметиламинопропил)карбодиимида и 1-гидроксибензотриазола.
3. Способ по п.1, где гидрогенолиз соединения Формулы (IV) с получением соединения Формулы (V) проводят в присутствии катализатора на основе переходного металла и источника водорода.
4. Способ по п.3, где катализатор на основе переходного металла представляет собой палладий на углеродном носителе, а источник водорода представляет собой газ водород.
5. Способ по п.1, где сульфонирование соединения Формулы (V) с получением соединения Формулы (VI) выполняют путем проведения реакции между соединением Формулы (V) и комплексом триоксид серы-пиридин, с последующей обработкой водным раствором гидросульфата тетрабутиламмония.
6. Способ по п.1, где соединение Формулы (VI) превращают в соединение Формулы (I) путем проведения реакции между соединением Формулы (VI) и трифторуксусной кислотой.
| Колосоуборка | 1923 |
|
SU2009A1 |
| ДИАЗАБИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1994 |
|
RU2124014C1 |
Авторы
Даты
2017-05-31—Публикация
2013-10-12—Подача